Изобретение относится к области фармакологии и фармакодинамики, биохимической медицины, клеточной и молекулярной биологии, иммунофармакологии микроэлементов и может быть использовано в клинической медицине для лечения различных заболеваний, сопровождающихся расстройствами корригирующей функции иммунной системы, проявляющейся угнетением продукции клеток СД4-хелперов и увеличением популяции клеток СД8-супрессоров.
В настоящее время в клинической фармакологии для иммунокоррекции используют как синтетические, так и органические вещества природного происхождения. Это, как правило, препараты из экстрактов зобной железы, лимфатических узлов, соединительной ткани и селезенки. К таким лекарственным средствам относятся хорошо известные в клинической практике вещества, например, тимоген, Т-активин, миелопид, тимоптин и т.д. (Машковский М.Д. Препараты, корригирующие процессы иммунитета в кн. "Лекарственные средства", Харьков, "Торсинг", 1997, т. 2., с. 199-207).
В последнее время внимание многочисленных исследователей привлек селен и его соединения, так как доказано, что клеточные и гуморальные иммунные процессы, особенно активация и коррекция клеточных иммунных реакций, осуществляются при помощи этого микроэлемента. (Кудрин А.В., Скальный А.В., Жаворонков А.А., Скальная М.Г., Громова О.А. "Иммунофармакология микроэлементов", М.: КМК, 2000, с. 222-223, 354-357).
В связи с этим для поддержания активной функции иммунной системы селен в качестве микроэлемента вводят в комплексы витаминных препаратов, например Центрум (Справочник ВИДАЛЬ "Лекарственные препараты в России", М.: АстраФармСервис, 1997, с. Б-654). Известны также селеносодержащие препараты, полученные на основе биомассы водорослей (патент GB 2203043, 1988 или патент RU 2096037), обладающие общетонизирующим действием, реализация которого связана с непосредственным воздействием соединений селена на иммунную систему. Однако указанные лекарственные вещества имеют недостаточно высокое содержание органического селена, а технология их получения сложна и требует длительного времени.
В патенте (RU 2138271 С1, 1999) предложено иммунокорригирующее средство ПСК (протеоселеновый комплекс), технология производства которого в какой-то степени разрешала предыдущие трудности, однако идентификация структуры этого селенового органического вещества произведена не была.
Представленные данные говорят о том, что современная технология получения селеновых препаратов нового класса, осуществляющих иммунокорригирующую активность, должна основываться на структуре и топологии присутствующих в организме активных, связанных с селеном биомолекул - гликопротеинов, фосфолипидов и фосфолипопротеиновых комплексов. Новые лекарственные средства по своему строению и механизму действия должны стереохимически, т.е. биологически и химически, соответствовать тем веществам организма человека, которые непосредственно осуществляют корригирующую функцию иммунной системы.
Задачей настоящего изобретения является расширение ассортимента иммунокорригирующих средств - создание целого ряда селенопротеиновых органических веществ, введение которых в организм не сопровождается побочными последствиями, а вызывает системный лечебный эффект, основанный на нормализации энергетических и рецепторно-сенсорных процессов в самой иммунной системе. Для решения поставленной задачи предлагаются лекарственные вещества, обладающие иммунокорригирующими свойствами. Они включают низкомолекулярный компонент, полученный из протеиносодержащего сырья путем экстракции органическими растворителями с последующим высушиванием субстанции и растворением ее в 60% - 90% этиловом спирте. В молекулу протеина введен селен, образующийся при термолизе селеномочевины, и остатки углевода, фосфолипида, фосфолипида и углевода, цианид-анионы. Получение препаратов осуществлялось в электромагнитном (плотность потока мощности 5•10-3 Вт/см2) синусоидальном высокочастотном поле (20-30 МГц) в течение 5 минут.
Произведенные вещества названы нами селенопротеиновыми органическими веществами (Se-ПОВ).
Сущность изобретения поясняется прилагаемыми к описанию фиг. 1-6.
1. Вещество селенопротеин (SeП).
Молекула селенопротеина представляет собой две полипептидные цепи - альфа и бета, соединенные дисульфидным мостиком по остаткам цистеина. Альфа-цепь состоит из остатков 20 аминокислот, бета - из 29 аминокислот. Селен, полученный путем термолиза селеномочевины, входит в боковые алкильные радикалы аминокислот, соединяя некоторые звенья альфа- и/или бета-цепей одной или двух соседних молекул протеина, тем самым дополнительно "сшивая" их (фиг. 1). Молекулярная масса SeП - 6187. Молярные соотношения протеина и селена 1:4.
Пример 1. Получение селенопротеина (SeП).
В качестве исходного материала используют зеленую массу белковосодержащих растений, например злаковых, предварительно высушенных и измельченных. С помощью экстракции эфиром, этиловым спиртом или димексидом из полученного сырья извлекают растительный белок (протеин). Белковый экстракт выпаривают и производят лиофильную сушку. Изготовленный порошок растворяют в 60% - 90% этиловом спирте, после чего вводят селен, полученный термолизом селеномочевины из расчета 6-12 мкг на 1 мл раствора и помещают в электромагнитное (плотность потока мощности 5•10-3 Вт/см2) синусоидальное высокочастотное поле 20-30 МГц на 5 минут. Произведенное таким образом вещество помещают во флаконы и герметизируют.
2. Вещество селеногликопротеин (SeГП).
1. Молекула селеногликопротеина включает в себя молекулу селенопротеина (фиг. 1), к которой через остатки основных аминокислот серина и/или тирозина присоединяется сахароза посредством О-гликозидных связей (фиг. 2, 3). Молекулярная масса селеногликопротеина - 6835. Молярные соотношения протеина, селена и углевода соответственно 1:4:5.
Пример 2. Получение селеногликопротеина (SeГП).
В качестве исходных продуктов используют белковосодержащие растения, например, злаковые и бобовые, а также богатые белками листья кукурузы. Зеленую массу предварительно высушивают и измельчают. С помощью экстракции эфиром, спиртом или димексидом из полученного сырья извлекают белковоорганические комплексы. Полученный экстракт выпаривают и проводят лиофильную сушку. Изготовленный порошок растворяют в 60% - 90% этиловом спирте, вводят селен, полученный термолизом селеномочевины, из расчета 6-12 мкг на 1 мл раствора, затем добавляют сахарозу. Вещества помещают в электромагнитное (мощность 5•10-3 Вт/см2) синусоидальное высокочастотное поле 20-30 МГц на 5 минут. Указанное поле может быть создано, например, в сквидмагнитометрах, которые применяются для магнитоэнцефалографии. Произведенное таким образом вещество помещают во флаконы и герметизируют.
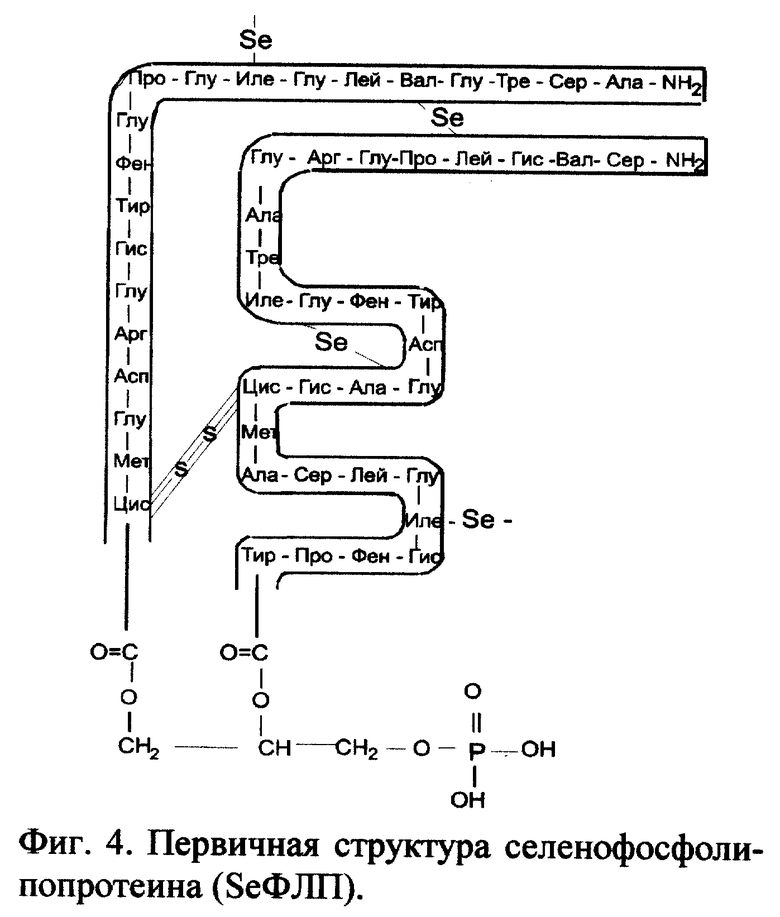
3. Вещество селенофосфолипопротеин (SeФЛП).
Молекула селенофосфолипопротеина включает молекулу селенопротеина, к которой через концевые карбоксильные группы альфа- и бета-цепей и/или боковые карбоксильные группы присоединен фосфоглицерол (фиг.4). Молекулярная масса SeФЛП - 6323. Молярные соотношения протеина, селена и фосфолипида 1:4:1.
Пример 3. Получение селенофосфолипопротеина.
Измельчили 5 г бобового высушенного растения (клевер розовый), поместили в колбу, добавили 50 г 5% димексида и оставили на 3 дня. По истечении этого времени наблюдали обесцвечивание частиц размельченного вещества. Слили жидкость в объеме 40 мл. Экстракт высушили и получили 400 мг порошка светло-зеленого цвета. Порошок высыпали в емкость объемом 50 мл, растворили в 40 мл 60% этилового спирта и ввели 240 мкг селена (из расчета 6 мкг на 1 мл). Кроме этого к раствору добавили определенное количество фосфоглицерола (молярное соотношение протеина и фосфоглицерола 1:1). Полученный раствор поместили на 5 минут в высокочастотное электромагнитное поле сквидмагнитометра, в результате чего произошло соединение фосфолипидов с протеоселеном. Произведенное вещество разлили во флаконы емкостью 14 мл и осуществили герметизацию.
4. Вещество селенофосфолипогликопротеин (SeФЛГП).
Молекула селенофосфолипогликопротеина включает молекулу селенофосфолипопротеина (фиг. 4), к которой через остатки основных аминокислот серина и/или тирозина посредством О-гликозидных связей и/или к фосфоглицеролу через фосфоэфирную связь присоединяется сахароза (фиг.5). Молекулярная масса SeФЛГП - 6953. Молярные соотношения протеин, селен, углевод и фосфолипид соответственно 1:4:5:1.
Пример 4. Получение селенофосфолипогликопротеина.
Измельчили 5 г высушенного растения (листья кукурузы), добавили 50 г 90% спирта, оставили на 3 дня. Слили жидкость и добавили 240 мкг селена. К данным веществам добавили определенное количество фосфолипида и сахарозы (молярные соотношения протеина, фосфолипида и углевода 1: 1:5), данный раствор поместили на 5 минут в высокочастотное электромагнитное поле сквидмагнитометра.
Произведенное вещество разлили во флаконы емкостью 14 мл и осуществили герметизацию.
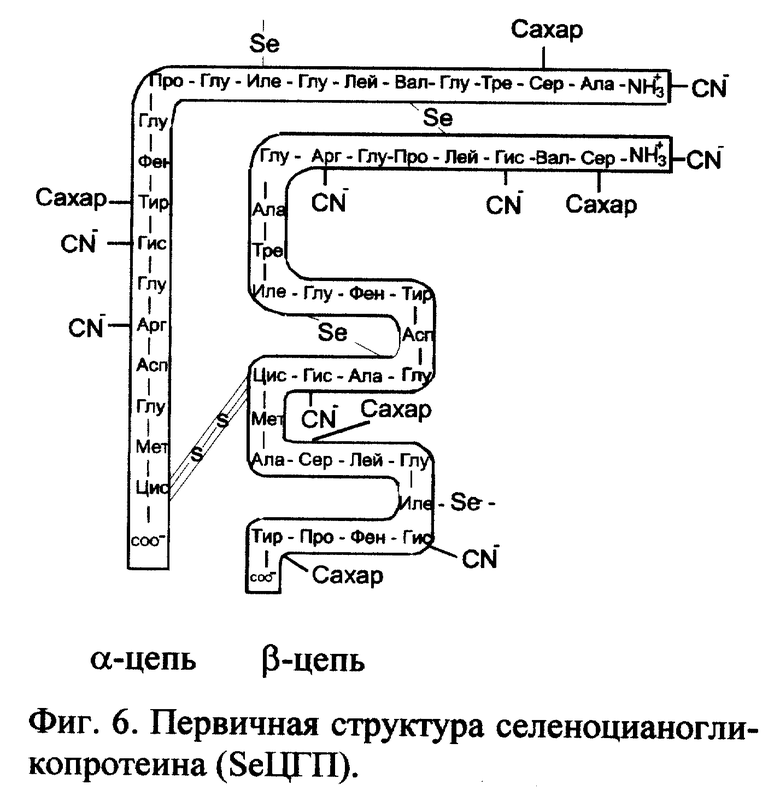
5. Вещество селеноцианогликопротеин (SeЦГП).
Молекула селеноцианогликопротеина включает молекулу ионизированного селеногликопротеина (фиг. 3), к положительно заряженным аминогруппам (-NH3 +) которой присоединяется цианид-анион (CN-) посредством ионных связей (фиг. 6). Молекулярная масса SeЦГП - 7043. Молярные соотношения протеина, селена, углевода и цианида соответственно 1:4:5:8.
Пример 5. Получение селеноцианогликопротеина.
Измельчили 10 г высушенного растения (листья кукурузы), добавили 250 г 90% спирта, оставили на 3 дня. Слили жидкость и добавили 1 мг селена и определенное количество ионов CN- (полученных путем термолиза) и сахарозы. Полученный раствор поместили на 5 минут в высокочастотное поле сквидмагнитометра. Произведенное вещество разлили во флаконы емкостью 14 мл и осуществили герметизацию.
Se-ПОВ включают в себя асимметричную белковую молекулу с альфа-спиралью и бета-структурой. Гидрофобный конец молекулы Se-ПОВ переходит в альфа-спираль, бета-структура молекулы Se-ПОВ извита соответствующим образом и на внешней стороне аминокислотной цепочки, как и на внутренней, имеются одновременно селенидные и дисульфидные связи, обеспечивающие пространственную устойчивость и в то же время гибкость данной молекулы.
В состав всей молекулы Se-ПОВ входит 15 аминокислот. Соответственно вышеизложенной технологии могут быть получены молекулы разнообразных селенопротеиновых органических веществ с различным числом аминокислот и относительно низким молекулярным весом.
Острую токсичность препарата исследовали при внутрибрюшинном введении Se-ПОВ в дозе 250 мг/кг мышам (возраст 6 недель, вес 28-30 г). Значение ЛД составило 700 мг/кг.
При исследовании общей токсичности мышам вводили Se-ПОВ в дозе 100 мг/кг в день внутрибрюшинно непрерывно в течение 10 дней. Снижение веса и каких-либо других нарушений при этом не наблюдали, в последующем при наблюдении этих мышей в течение трех месяцев отклонений от нормы не выявлено.
В результате проведенных исследований установлено, что Se-ПОВ являются органическими низкомолекулярными соединениями, обладают иммунокорригирующими свойствами, нетоксичны, полностью растворимы в воде и биологических жидкостях - крови, лимфе и ликворе. В 1 мл Se-ПОВ содержится в зависимости от количества аминокислот в лиганде от 20 до 30 мг субстанции и 6 мкг селена.
Доза вводимого препарата зависит от клинического состояния больного, его возраста, веса, а также способа введения. Эффективная терапевтическая суточная доза для больного составляет от 6 мг до 150 мг активного вещества, которое вводят одномоментно или дробно.
Способ активации и коррекции иммунной системы осуществляют следующим образом.
Полученный препарат Se-ПОВ представляет собой раствор активного вещества в 60% - 90% этиловом спирте, 1 мл которого содержит 20-30 мг лекарственной субстанции. Se-ПОВ вводят перорально, внутримышечно, внутривенно, внутриартериально, а также наружно в виде суспензии в масляном растворе или в виде мази с масляно-спиртовым наполнителем.
При пероральном введении необходимую дозу рассчитывают следующим образом:
в 20 каплях раствора содержится 20-30 мг лекарственной субстанции;
в 10 каплях (1/2 мл) содержится 10-15 мг препарата;
в 5 каплях (1/4 мл) содержится 5-7,5 мг препарата;
в 3 каплях (1/7 мл) содержится 3,3 мг препарата.
При внутримышечном, внутривенном или внутриартериальном введении препарат растворяют в физиологическом растворе для лучшей диссоциации в соотношении 1:10 при использовании 60% спирта или 1:15 при 90% спирте.
Например: детям до 6 лет при клинической патологии средней степени тяжести препарат вводят однократно в виде инъекции от 0,1 мл до 0,5 мл в день, при тяжелой степени патологии указанную дозу вводят два раза в день. При проведении интенсивной терапии препарат вводят внутримышечно или внутривенно (внутриартериально) по 1,0-2,0 мл соответственно с добавлением 10 или 20 мл физиологического раствора. В случае перорального введения в зависимости от возраста, веса и степени поражения - от 0,5 мл до 3,0 мл, причем препарат растворяют в 1/3 стакана кипяченой слегка теплой воды (36-38oC).
Длительность лечения может колебаться от 1 до 3 месяцев, в случае тяжело протекающей патологии курс лечения повторяют с интервалом 1-2 месяца до выраженного клинического эффекта. В период проведения лечения контролируют иммунологический статус больного по развернутой клинической формуле и иммунограмме.
При применении иммунокорригирующих селенопротеиновых органических веществ наблюдается активация иммунной системы, проявляющаяся улучшением клинического самочувствия больных, нормализацией иммунитета в сторону иммунокоррекции - преобладание количества СД4 Т-хелиеров над СД8 Т-супрессорами, восстановлением индекса иммунорегуляции, увеличением количества естественных киллеров в случае их снижения.



Изобретение относится к биохимической фармакологии и может быть использовано в медицине для лечения заболеваний, связанных с угнетением продукции клеток СD4-хелперов и увеличением популяции клеток СD8-супрессоров. Сущностью изобретения являются селенопротеиновые органические вещества с иммунокорригирующими свойствами. Вещества включают в себя низкомолекулярный компонент - протеин, селен, остатки углевода, фосфолипид, цианид-анионы. Техническим результатом является восстановление индекса иммунорегуляции. 5 с.п. ф-лы, 6 ил.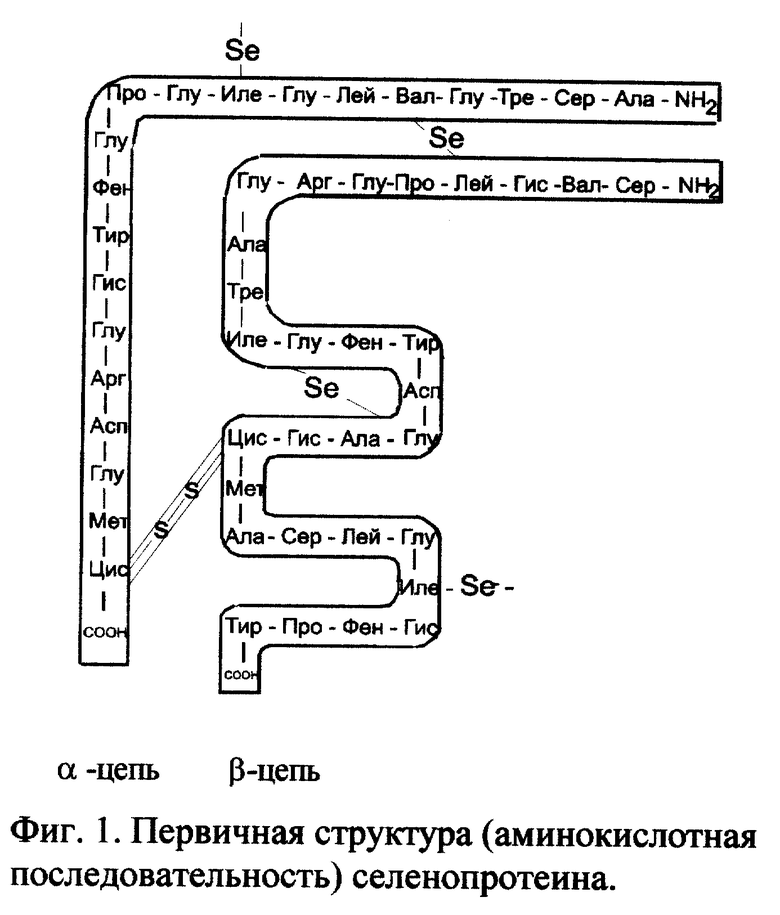
| ИММУНОКОРРЕГИРУЮЩЕЕ СРЕДСТВО И СПОСОБ ИММУНОКОРРЕКЦИИ | 1999 |
|
RU2138271C1 |
| 2000 |
|
RU2161034C1 | |
| СПОСОБ ПОЛУЧЕНИЯ СЕЛЕНСОДЕРЖАЩЕГО ПРЕПАРАТА БИОМАССЫ СПИРУЛИНЫ | 1996 |
|
RU2096037C1 |
| ПРЕПАРАТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1999 |
|
RU2157232C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ЛЕЙКОПОЭЗСТИМУЛИРУЮЩИМ, ИММУНОМОДУЛИРУЮЩИМ И АНТИБАКТЕРИАЛЬНЫМ ДЕЙСТВИЕМ | 1998 |
|
RU2157813C2 |
| WO 00/67762 A1, 16.11.2000. | |||
Авторы
Даты
2001-12-27—Публикация
2001-01-22—Подача