Область изобретения
Данное изобретение относится к способу получения катализаторов с улучшенными каталитическими свойствами, в частности с улучшенной начальной активностью, начальной селективностью и/или характеристикой активности и/или селективности с течением времени.
Предпосылки к созданию изобретения
Известно множество способов нанесения на носитель каталитически активных металлов с целью получения катализаторов. Например, в патенте США №3972829, выданном 3 августа 1976 г., описан способ распределения каталитически активных металлических компонентов на носителях с использованием раствора для пропитки, содержащего соединение предшественника катализатора и органическую тиокислоту, или меркаптокарбоновую кислоту. В патенте США №4005049, выданном 25 января 1977 г., раскрыто получение катализатора на основе серебра/переходного металла, который полезен в реакциях окисления. В международной публикации WO 96/23585, опубликованной 8 августа 1996 г., указано, что повышение количества промотора щелочного металла в растворе серебра приводит к улучшенным свойствам.
В примерах патента США №4212772, выданного 15 июля 1980 г., и патента США №4994587, выданного 19 февраля 1991 г., оба из которых относятся к катализаторам эпоксидирования этилена, отмечено, что в растворе серебра, который применяли для пропитки носителя катализатора, используют слабоосновные первичные амины, такие, как изопропиламин, вторичный бутил-амин, моноэтаноламин и этилендиамин. Их цель состоит в связывании серебра в комплекс. В литературе также предостерегают от некоторых способов. В патенте США №4908343, выданном 13 марта 1990 г., предостерегают от того, чтобы раствор серебра имел высокую кислотность или основность, поскольку раствор сильной кислоты или основания будет выщелачивать любые выщелачиваемые примеси из носителя, становясь частью серебряного катализатора в количествах, которые будут неблагоприятно влиять на эксплуатационные качества катализатора в реакции окисления.
В патенте США №4361500, выданном 30 ноября 1982 г., описан способ получения катализатора на носителе, содержащего, по меньшей мере, один металл (который может быть серебром), путем восстановительного нанесения металла(лов) на носитель с помощью раствора, содержащего ионы, или соединения металла(лов), а затем восстановления этого носителя, отличающийся тем, что металл(ы) наносят на носитель в присутствии, по меньшей мере, одного соединения четвертичного аммония, анион которого представляет собой гидроксильную группу, или остаток органической или минеральной кислоты, при этом восстановление осуществляют путем гидрирования при температуре, не превышающей 300°С, и не проводят стадию прокаливания.
Неожиданно было обнаружено, что нанесение металла и каталитические свойства катализатора можно значительно улучшить путем снижения активности водородных ионов в растворе для пропитки.
Краткое описание изобретения
В соответствии с одним из способов воплощения изобретения, предоставлен способ получения катализатора, пригодного для эпоксидирования олефинов в газовой фазе, включающий в себя стадии:
- выбора неорганического носителя;
- нанесения на носитель серебра и, необязательно, промотирующих веществ;
при этом нанесение осуществляют при помощи раствора для пропитки, активность водородных ионов в котором снижена, по меньшей мере, в 5 раз.
В частности, активность водородных ионов в растворе для пропитки снижают при добавлении основания.
Предпочтительно, чтобы активность водородных ионов в растворе для пропитки снижали в пять - тысячу раз. В водной среде эти цифры соответствуют повышению рН на величину 0,5 и 0,5-3 соответственно.
Описание предпочтительных способов воплощения
Было найдено, что снижение активности водородных ионов в растворе для пропитки, используемом для нанесения на носитель каталитически активных металлов, обеспечивает катализаторы, которые обладают улучшенными каталитическими свойствами, такими, как активность, селективность, и характеристика активности и/или селективности с течением времени. Полагают, что способ способствует улучшению свойств большинства катализаторов, в которых металл наносят на носитель при использовании раствора для пропитки.
Катализаторы обычно получают путем нанесения на носитель каталитически эффективного количества одного или более каталитически активных металлов для получения предшественника катализатора. Обычно этот носитель пропитывают металлом или соединением(ями), комплексом(сами) и/или солью(лями), достаточными для нанесения или пропитки каталитически активным веществом. Как использовано здесь, “каталитически эффективное количество” означает такое количество металла, которое обеспечит измеряемый каталитический эффект.
Пропитанный носитель, или предшественник катализатора, сушат в присутствии атмосферы, которая также восстанавливает каталитический металл. Известные в данной области техники методы сушки включают в себя паровую сушку, сушку в атмосфере с регулируемой концентрацией кислорода, сушку в восстановительной атмосфере, сушку на воздухе и постадийную сушку с использованием подходящей линейной или ступенчатой кривой температуры.
В способе изобретения улучшение в свойствах катализатора наблюдается в том случае, когда нанесение металла осуществляют при контакте носителя с раствором для пропитки, активность водородных ионов в котором снижена. “Активность ионов водорода”, как использовано здесь, представляет собой активность водородных ионов, измеренную по потенциалу водородного ион-селективного электрода. Как использовано здесь, раствор с “пониженной” активностью водородных ионов относится к раствору, активность водородных ионов в котором изменили путем добавления основания, так, что активность водородных ионов этого измененного раствора снижена по сравнению с активностью водородных ионов того же раствора в неизмененном состоянии. Основание, выбранное для изменения раствора, можно выбрать из любого основания или соединения с рКb, меньшим, чем у первоначального раствора для пропитки. Особенно желательно выбрать основание, которое не изменяет состав раствора для пропитки; то есть, которое не изменяет желательную концентрацию металлов в растворе для пропитки и нанесенных на носитель. Не меняют концентрации металлов в растворе для пропитки органические основания, примерами которых являются гидроксиды тетраалкиламмония и 1,8-бис(диметиламино)нафталин. Если изменение концентрации металлов в растворе для пропитки не важно, можно использовать гидроксиды металлов.
Если раствор для пропитки является, по меньшей мере, частично водным, показание изменения активности водородных ионов можно определить с помощью рН-метра, понимая при этом, что полученное измерение не является истинным рН водного определения. “Измеренный рН”, как использовано здесь, будет означать подобное измерение рН неводной системы с использованием стандартного рН зонда. Эффективны даже небольшие изменения в “измеренном рН” при переходе от начального раствора для пропитки к раствору с добавкой основания, и улучшения в каталитических свойствах продолжаются по мере увеличения изменения “измеренного рН” при добавлении основания. По-видимому, добавление большого количества основания не оказывает неблагоприятного воздействия на работу катализатора; однако, было замечено, что добавления больших количеств гидроксидов вызывают образование осадка в растворе для пропитки, что приводит к производственным трудностям. В том случае, когда прибавление основания слишком мало, на активность водородных ионов не будет оказано влияние.
Как описано, этот способ эффективен для улучшения, по меньшей мере, одного из каталитических свойств катализатора, в котором для нанесения или пропитки носителя каталитически активным металлом используют раствор для пропитки. “Улучшение каталитических свойств”, как использовано здесь, означает, что свойства катализатора улучшены по сравнению с катализатором, полученным при использовании того же раствора для пропитки, активность водородных ионов в котором не была снижена. Каталитические свойства означают активность катализатора, селективность, характеристику активности и/или селективности с течением времени, работоспособность (сопротивление выходу из-под контроля), конверсию и скорость работы.
Дальнейшего улучшения в свойствах можно добиться при снижении концентрации ионизуемых частиц, находящихся на поверхности носителя, перед стадией нанесения. Обычно носители являются неорганическими веществами, например, такими, как соединения на основе оксида алюминия, диоксида кремния, или диоксида титана, или их сочетаниями, такими, как носители на основе оксида алюминия-диоксида кремния. Ионизуемые частицы, обычно находящиеся на носителях неорганического типа, включают в себя натрий, калий, алюминаты, растворимый силикат, кальций, магний, алюмосиликат, цезий, литий и их сочетания. Снижение концентрации нежелательных ионизуемых частиц можно осуществить любым способом: (i), который эффективен для перевода ионизуемых частиц в ионное состояние и удаления этих частиц, или (ii), который переводит ионизуемые частицы в нерастворимое состояние, или (iii), который переводит ионизуемые частицы в стационарное состояние; однако, использование агрессивных сред, таких, как кислоты или основания, нежелательно, поскольку эти среды имеют тенденцию растворять носитель, экстрагировать слишком много вещества из массы и генерировать кислые или основные участки в порах.
Эффективные способы снижения концентрации включают в себя промывание носителя; ионный обмен; испарение, осаждение, или связывание примесей в комплекс; проведение реакции для перевода ионизуемых частиц на поверхности в нерастворимое состояние; и их сочетание. Примеры растворов для промывания и ионного обмена включают в себя водные растворы и/или растворы на основе органического растворителя, которые могут также содержать гидроксид тетраэтиламмония, ацетат аммония, карбонат лития, ацетат бария, ацетат стронция, краун-эфир, метанол, этанол, диметилформамид и их смеси. Можно обрабатывать готовый носитель, или можно обработать используемые для получения носителя вещества перед изготовлением носителя. При обработке веществ для носителя перед изготовлением носителя еще большие улучшения наблюдаются при повторной обработке поверхности готового носителя. После удаления ионизируемых частиц носитель необязательно сушат. Когда процесс удаления осуществляют промывкой водным раствором, рекомендуется сушка.
При помощи примера способ будет описан более подробно для катализатора, пригодного для производства эпоксидов в газовой фазе, известного так же, как катализатор эпоксидирования.
Прежде всего выбирают носитель. В случае катализатора эпоксидирования носитель обычно представляет собой неорганическое вещество, например такое, как носитель на основе оксида алюминия, такой, как α-оксид алюминия.
В случае носителей, содержащих α-оксид алюминия, предпочтение отдают таким, удельная поверхность которых, определенная по методу Б.Э.Т., составляет от 0,03 до 10 м2/г, предпочтительно от около 0,05 до 5 м2/г, более предпочтительно от 0,1 до 3 м2/т, а водной объем пор, определенный обычным методом абсорбции воды, составляет от 0,1 до 0,75 мл/г по объему. Метод Б.Э.Т. определения удельной поверхности подробно описан Brunauer, S., Emmett, P. Y., and Teller, E., J. Am. Chem. Soc., 60, 309-16 (1938).
Некоторые типы носителей, содержащих α-оксид алюминия, особенно предпочтительны. Эти носители из α-оксида алюминия обладают относительно однородными диаметрами пор и более полно характеризуются тем, что имеют по Б.Э.Т. удельные поверхности от 0,1 до 3 м2/г, предпочтительно от 0,1 до 2 м2/г, и водные объемы пор от 0,10 до около 0,55 мл/г. В число производителей этих носителей входит Norton Chemical Process Products Corporation and United Catalysts, Inc. (UCI).
Носитель обычно пропитывают соединением(ми), комплексом(сами) и/или солью(солями) металла, растворенными в подходящем растворителе, достаточном для того, чтобы вызвать желательное нанесение на носитель. При использовании избытка раствора для пропитки пропитанный носитель впоследствии отделяют от раствора перед восстановлением нанесенного соединения металла до состояния металла.
В способе изобретения активность водородных ионов в растворе для пропитки снижают перед началом процесса нанесения или пропитки. Обычный раствор для пропитки вначале является довольно основным, так что для дальнейшего снижения активности водородных ионов используют сильное основание. Особенно желательно выбрать основание, которое не меняет состав раствора для пропитки, такое, как органические основания; однако, если изменение концентрации металлов в растворе для пропитки не имеет значения, можно использовать основания металлов. Примеры сильных оснований включают в себя гидроксид алкиламмония, такой, как гидроксид тетраэтиламмония, гидроксид металла, такой как гидроксид лития и гидроксид цезия. Можно также использовать сочетания оснований. Для поддержания желательного состава пропиточного раствора и загрузки металла предпочитают органическое основание, такое, как гидроксид тетраэтиламмония. Эти желательные пределы добавления оснований обычно приводят к изменению “измеренного рН”, которое изменяется в интервале от около 0,5 до около 3, понимая при этом, что этот “измеренный рН” не является истинным рН, поскольку система для пропитки не водная.
При использовании избытка раствора для пропитки пропитанный носитель впоследствии отделяют от раствора перед восстановлением нанесенного соединения металла. Кроме того, на носитель либо до, либо одновременно, либо после нанесения каталитически активного металла можно также нанести промоторы, компоненты, эффективно действующие для обеспечения улучшения одного или более каталитических свойств катализатора по сравнению с катализатором, не содержащим таких компонентов.
При использовании только что описанной стадии уменьшения концентрации ионизуемых частиц концентрацию ионизуемых частиц, находящихся на поверхности носителя, снижают перед стадией нанесения или пропитки. Ионизуемые частицы, находящиеся на носителе из α-оксида алюминия, например, обычно включают в себя натрий, калий, алюминаты, растворимые силикаты, кальций, магний, алюмосиликаты и их сочетания. Было найдено, что силикаты и некоторые другие анионы являются особенно нежелательными ионизуемыми частицами в катализаторе эпоксидирования. Скорость солюбилизации силикатов можно определить методом индуктивно связанной плазмы (ИСП), а количество частиц кремния на поверхности можно определить рентгеновской фотоэлектронной спектроскопией (РФС); однако, поскольку натрий растворим в тех же растворах, в которых растворимы силикаты, скорость солюбилизации натрия становится более простым способом проверки удаления ионизуемых частиц. Другой метод определения состоит в измерении электропроводности раствора для обработки.
Концентрацию нежелательных ионизуемых частиц можно снизить любым способом, который эффективен для перевода ионизуемых частиц в ионное состояние и удаления этих частиц, или перевода ионизуемых частиц в нерастворимое состояние, или перевода ионизуемых частиц в стационарное состояние. Способы, эффективные для снижения концентрации нежелательных ионизуемых частиц на поверхности, включают в себя промывание, ионный обмен, испарение, осаждение, связывание примесей в комплекс, борьбу с примесями и их сочетание. Очистку носителя на основе оксида алюминия можно эффективно и разумно с точки зрения стоимости осуществить путем промывания или ионного обмена. Можно использовать любой раствор, который способен уменьшить концентрацию присутствующих нежелательных ионизуемых частиц, в частности анионных ионизуемых частиц и, в особенности, ионизуемых силикатов. После этого носитель необязательно сушат; однако, если способ удаления представляет собой промывание, сушка рекомендуется.
Носитель пропитывают ионами металла или соединением(ми), комплексом(ми) и/или солью(солями), растворенными в подходящем растворителе, достаточном для того, чтобы вызвать желаемое нанесение на носитель. Если наносимым веществом является серебро, обычное отложение составляет от 1 до 40 мас.%, предпочтительно от 1 до 30 мас.% серебра из расчета на массу всего катализатора. Затем пропитанный носитель отделяют от раствора, а нанесенное соединение металла(лов) восстанавливают до металлического серебра.
Можно нанести один или более промоторов либо до, либо одновременно, либо после нанесения металла. Промоторы для катализаторов эпоксидирования обычно выбирают из серы, фосфора, бора, фтора, металлов из группы с IA по группу VIII, редкоземельных металлов и их сочетаний. Промотирующее вещество, как правило, представляет собой соединение(я) и/или соль(соли) промотора, растворенные в подходящем растворителе.
Для оксидных катализаторов эпоксидирования олефинов металлы группы IA обычно выбирают из калия, рубидия, цезия, лития, натрия и их сочетаний; при этом предпочтительными являются калий и/или цезий и/или рубидий. Еще более предпочтительным является сочетание цезия и, по меньшей мере, одного дополнительного металла группы IA, такое, как цезий и калий, цезий и рубидий, или цезий и литий. Металлы группы IIA обычно выбирают из магния, кальция, стронция, бария и их сочетаний, переходные металлы группы VIII обычно выбирают из кобальта, железа, никеля, рутения, родия, палладия и их сочетаний, а редкоземельные металлы обычно выбирают из лантана, церия, неодима, самария, гадолиния, диспрозия, эрбия, иттербия и их смесей. Не ограничивающие примеры других промоторов включают в себя перренат, сульфат, молибдат, вольфрамат, хромат, фосфат, борат, сульфат-анион, фторид-анион, оксианионы групп с IIIB по VIB, оксианионы элемента, выбранного из групп с III по VIIB, соли щелочного металла с галоидными анионами, и оксианионы, выбранные из групп с IIIA по VIIA и с IIIB no VIIB. Количество промотора металла группы IA обычно находится в интервале от 10 ч. на млн. до 1500 ч. на млн., выраженное в виде металла, от массы всего катализатора, а металла группы VIIb меньше, чем 3600 ч. на млн., выраженное в виде металла, от массы всего катализатора.
Другие способы воплощения изобретения предоставляют катализаторы, полученные только что описанными способами.
Только что описанные конечные катализаторы эпоксидирования используют для получения в газовой фазе эпоксидов, в частности оксида этилена. Обычный способ эпоксидирования включает в себя загрузку катализаторов в реактор. Предназначенное для конверсии сырье, как правило, смесь этилена, кислорода, двуокиси углерода, азота и хлористого этила, пропускают над слоем катализатора при повышенных давлении и температуре. Катализатор переводит сырье в выходной поток продукта, содержащий оксид этилена. Для повышения характеристики конверсии катализатора к сырью можно также добавить оксиды азота (NOx).
Следующие примеры иллюстрируют изобретение.
ПРИМЕРЫ
Носители
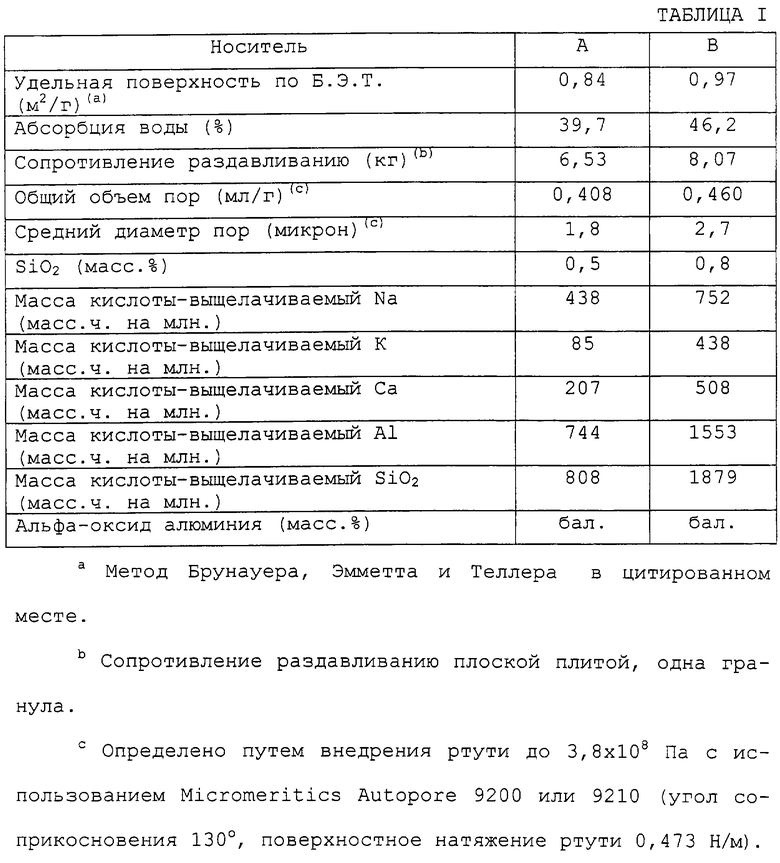
В табл.I приведены носители, использованные для примеров.
использованием Micromeritics Autopore 9200 или 9210 (угол соприкосновения 130°, поверхностное натяжение ртути 0,473 Н/м).
Методики промывания носителя водой для примеров 1, 3, 4, 5, 6, 7, 7b, 8, 9, 11
Промывание носителя осуществляли путем погружения 100 г носителя в 300 г кипящей деионизованной воды на 15 мин. Затем носитель вынимали и помещали в 300 г свежей кипящей воды еще на 15 мин. Эту процедуру повторяли еще раз, в сумме три погружения; на этой стадии носитель отделяли от воды и сушили в хорошо вентилируемой печи при 150°С в течение 18 ч. После этого высушенный носитель использовали для получения катализатора способами, основные положения которых изложены в следующих примерах.
Раствор для пропитки
Сырьевой раствор, содержащий серебро-амин-оксалат, готовили по следующей методике:
415 г химически чистого гидроксида натрия растворили в 2340 мл деионизованной воды и довели температуру до 50°С;
1699 г нитрата серебра высокой чистоты “Spectropure” растворили в 2100 мл деионизованной воды и довели температуру до 50°С.
К раствору нитрата серебра медленно, при перемешивании, прибавляли раствор гидроксида натрия, поддерживая температуру раствора при 50°С. Смесь перемешивали 15 мин, затем температуру понизили до 40°С. Из осадка, образовавшегося на стадии смешивания, удалили воду и измерили проводимость воды, содержащей ионы натрия и нитрат-ионы. К раствору серебра вновь прибавили объем свежей деионизованной воды, равный изъятому объему. Раствор перемешивали 15 мин при 40°С. Эту процедуру повторяли до тех пор, пока проводимость изъятой воды не стала меньше 90 мк·мгн·Ом/см. После этого добавили 1500 мл свежей деионизованной воды.
Прибавили 630 г дигидрата щавелевой кислоты высокой чистоты с инкрементами приблизительно 100 г. Температуру поддерживали при 40°С, а рН поддерживали выше 7,8.
Из этой смеси удалили воду, получив содержащую серебро суспензию высокой концентрации. Охладили суспензию оксалата серебра до 30°С.
Прибавили 699 г 92 мас.% этилендиамина (8% деионизованной воды), поддерживая температуру не выше 30°С. Полученный раствор содержал приблизительно 27-33 мас.% серебра.
К этому раствору прибавили достаточное количество 45 мас.% водного СsОН и воды, получив конечный катализатор, содержащий 14,5 мас.% серебра и желаемую загрузку цезия (см. примеры).
Методика измерения рН
Измерения рН раствора серебра проводили с использованием рН-метра модели Metrohm 744, используя комбинированный электрод модели 6.0220.100 и платиновый термометр сопротивления модели 6.1110.100 для компенсации температуры. Измеритель калибровали коммерчески доступными буферными растворами перед каждым употреблением. При обычном измерении аликвоту в 50 мл раствора серебра с присадкой, предназначенного для использования в качестве пропитки катализатора, фильтровали в стеклянный химический стакан на 100 мл через 2-микронный фильтр, присоединенный к пластмассовому шприцу. В раствор, перемешиваемый на магнитной мешалке, опускали рН зонд и регистрировали полученные спустя 3 минуты показания как равновесный рН. Зонд очищали перед каждым измерением деионизованной водой и проверяли калибровку. Особое внимание обращали на то, чтобы предотвратить накопление осадков АgСl на мембране электрода. Это накопление удаляли путем вымачивания зонда в растворе гидроксида аммония, что было рекомендовано производителем.
Испарение
Данный метод предназначен для удаления нежелательных ионов с поверхности носителя любыми средствами, которые приводят к перемещения этих ионов в газовую фазу. В некоторых случаях это может быть простым нагревом до требуемой температуры. В случае ионов щелочных металлов обычные температуры, при которых образуется основа из альфа-окиси алюминия, являются достаточными для удаления большинства, но не всего количества ионов щелочных металлов. Обычно к ионам металлов необходимо добавлять химический агент для того, чтобы привести к получению летучего образца. Одним общепринятым методом является введение соединений бора, таких как борная кислота, которые приводят к летучим метаборатам / Fessler, A.H. “Alkali-Free Ceramic Materials&Method for Making Same" US 2069060/. Например, в случае натрия получают Na2BО4, образуется /Kirk-Othmer Index, vol.4, р.77 (1st Edition)/. Могут использоваться и другие реагенты.
Другим хорошо известным агентом является фторид железа, который приводит к получению летучих фтористых соединений со многими металлами. Температура кипения фторидов металлов намного ниже соответствующих хлоридов, и это свойство используется при очистке металлов смеси металлов в течение многих лет. Самый известный пример использования фторидов был очень успешным при испарении редкоземельных металлов для отделения урана от других редких земель, присутствующих в руде /"Advanced Inorganic Chemistry", Cotton & Wilkinson Eds. $th Edition, copyright 1980, John Wiley & Sons,. p.1030/. Фториды также эффективны при испарении соединений кремния с образованием низкокипящего SiF4. Это находит свое применение в синтезе альфа-оксидов алюминия с очень низким содержанием кремния и может быть выполнено при относительно низких температурах /"Alumina as a Ceramic Material", Walter H.Glitzen, Ed., copyright 1970, Alumina Ceramic society, p.25/.
Часто объединяют методы нагревания и действия химического агента для повышения скорости удаления нежелательных веществ. Это часто делают в синтезе соответствующих материалов основ. Примерами являются описанные выше примеры для бора и фторида.
Осаждение
Данный метод направлен на иммобилизацию нежелательных ионов на поверхности путем химической реакции с образованием нерастворимого соединения. Основу этого метода составляет хорошо известная процедура осаждения ионов из растворов. Перечень методик осаждения и химических агентов, используемых для осаждения катионов, может быть найден в книгах по общей химии или аналитической химии в разделах по качественному анализу. В этом случае использование катионов, которые не приводят к ухудшению свойств катализаторов, является пригодным.
Не ограничивающие примеры включают литий, барий, кальций, стронций, магний, ионы переходных металлов, ионы редкоземельных элементов. Особенно используемыми являются ионы лития, которые могут вводится в различных формах (гидроксида, нитрата, бикарбоната, карбоната, хлорида, фторида и т.д.). Литий образует нерастворимый силикат Li2SiO3, а литий сам по себе является относительно безвредным на поверхности основы катализатора из серебра.
Комплексообразование (секвестрация)
Этот метод направлен на иммобилизацию нежелательных ионов на поверхности, делая их неподвижными (неспособными для перемещения). Словарь Webster's New Collegiate Dictionary, copyright 1980 G.&C.Merriam Co. описывает секвестрацию как “удерживание (в качестве металлического иона) путем включения в соответствующий координационный комплекс". Примером такого включения является захват или улавливание ионов внутри матрицы, в котором они стабилизируются. Примеры захвата катионов включают использование цеолитов, краун эфиров, алюмосиликатов, глин, гранулированных глин или другого богатого кислородом симметричного окружения.
Пример 1a (сравнительный - основной случай носителя А, промывание)
Предшественник катализатора получили из носителя А, подвергнув сначала носитель промыванию. После промывания приблизительно 30 г промытого носителя А поместили в вакуум при 3,33 кПа на 1 мин при температуре окружающей среды. Затем ввели приблизительно 50 г раствора для пропитки для погружения в него носителя и поддерживали вакуум при 3,33 кПа еще в течение 3 мин. Показатель по цезию составил 450 ч на млн./г конечного катализатора. После этого вакуум убрали и удаляли из предшественника катализатора избыток раствора для пропитки центрифугированием при 500 об/мин в течение двух минут. Затем предшественник катализатора сушили при встряхивании при 240°С в течение 4 мин в потоке воздуха, протекающего со скоростью 11,3 м3/ч.
Пример 2а (сравнительный - основной случай носителя А, нет промывания)
Носитель А пропитывали, как описано в примере 1а; однако, этот носитель не подвергали промыванию. Показатель по цезию составил 400 ч. на млн./г конечного катализатора.
Пример 3
Носитель А подвергали промыванию и пропитке, как описано в примере 1а. Показатель по цезию составил 500 ч. на млн./г конечного катализатора. Кроме того, к основному раствору для пропитки добавили 35%-ный водный гидроксид тетраэтиламмония (ТЭАГ) до показателя 117,8 микромоль ОН-/мл раствора Аg, для снижения активности водородных ионов до “измеренного рН” в 13,7.
Пример 4
Катализатор получали таким же образом, как в примере 1. Показатель по цезию составил 720 ч. на млн./г конечного катализатора. Кроме того, ТЭАГ растворили в воде и прибавили к основному раствору для пропитки до показателя 117,8 микромоль ОН-/мл Аg раствора для снижения активности водородных ионов до “измеренного рН” в 13,2 и NH4ReO4 растворили в воде и добавили в сырьевой раствор для обеспечения 1,5 микромоль Re/г конечного катализатора.
Пример 5
500 г носителя А подвергли промыванию, затем погрузили в 1500 мл кипящего 5 мас.% водного ТЭАГ на 15 мин. После этого носитель отделили от раствора и промывали последовательно кипящей водой в соответствии с процедурой промывания носителя. Затем этот носитель использовали для получения катализатора согласно процедуре, описанной в примере 2 с “измеренным рН” 13,6. Показатель по цезию составил 400 ч. на млн./г конечного катализатора.
Пример 6
Носитель А подвергали промыванию и пропитке, как описано в примере 1. Показатель по цезию составил 430 ч. на млн./г конечного катализатора. Кроме того, LiNO3 и LiOH добавили к сырьевому раствору для пропитки, снизив активность водородных ионов до “измеренного рН” 12,5.
Пример 7
Носитель А подвергали промыванию и пропитке, как описано в примере 1. Показатель по цезию составил 450 ч. на млн./г конечного катализатора. Кроме того, LiOH растворили в воде и добавили в сырьевой раствор для пропитки для того, чтобы снизить активность водородных ионов до “измеренного рН” 13,2.
Пример 8а (сравнительный)
Носитель А катализатора пропитали, как описано в примере 6, однако, носитель не подвергали промыванию. Показатель по цезию составил 400 ч. на млн./г конечного катализатора.
Пример 9а (сравнительный)
Приготовили раствор серебра, как описано в примере 6. “Измеренный рН” этого раствора составил 13,2. В раствор медленно барботировали СO2 до тех пор, пока “измеренный рН” не составил 12,0. Этот раствор использовали для получения катализатора, как описано в примере 1.
Пример 10
Катализатор получали таким же образом, как в примере 1. Показатель по цезию составил 650 ч. на млн./г конечного катализатора. Кроме того, LiOH растворили в воде и добавили в сырьевой раствор для пропитки для того, чтобы снизить активность водородных ионов до “измеренного рН” 13,2, и NH4ReO4 растворили в воде и добавили в сырьевой раствор для обеспечения 1,5 микромоль Re/г конечного катализатора.
Пример 11а (сравнительный - основной случай носителя В, промывание)
Носитель В использовали для получения катализатора, как описано в примере 1. Показатель по цезию составил 450 ч. на млн./г конечного катализатора.
Пример 12а (сравнительный - основной случай носителя В, нет промывания)
Носитель В пропитывали, как описано в примере 1, однако, этот носитель не подвергали промыванию. Показатель по цезию составил 500 ч. на млн./г конечного катализатора.
Пример 13
Носитель В использовали для получения катализатора, как описано в примере 1. Показатель по цезию составил 550 ч. на млн./г конечного катализатора. Кроме того, LiOH растворили в воде и добавили в сырьевой раствор для пропитки для того, чтобы снизить активность водородных ионов до “измеренного рН” 13,2.
Пример 14
Катализатор получали, как описано в примере 13, однако, носитель не подвергали процедуре промывания. Показатель по цезию составил 500 ч. на млн./г конечного катализатора.
Катализаторы примеров 1а-14 использовали для получения оксида этилена из этилена и кислорода. В U-образную трубку из нержавеющей стали с внутренним диаметром 6,35 мм загрузили от 3 до 5 г измельченного катализатора. Эту U-образную трубку погрузили в баню с расплавленным металлом (тепловая среда), а концы присоединили к проточной газовой системе. Массу использованного катализатора и скорость входящего газа отрегулировали таким образом, чтобы достигнуть часовой объемной скорости газа в 6800 мл газа на 1 мл катализатора в час. Входное давление газа составляло 14500 кПа.
Газовая смесь, пропускаемая через слой катализатора (в однократном режиме) во время полного опытного пробега (включая запуск), состояла из 25% этилена, 7,0% кислорода, 5% двуокиси углерода, 63% азота и от 2,0 до 6,0 об. ч. на млн. хлористого этила.
Начальная температура реактора (тепловая среда) составляла 180°С. Температуру линейно повышали со скоростью 10°С в час от 180°С до 225°С, а затем отрегулировали таким образом, чтобы достигнуть постоянного уровня оксида этилена в 1,5 об.% в выходном газовом потоке. Данные по эксплуатации при этом уровне конверсии обычно получали, когда катализатор находился в потоке в общем, по меньшей мере, 1-2 дня. Вследствие небольших различий в составе сырьевого газа, скоростях газового потока и калибровке аналитических приборов, использованных для определения составов газообразного сырья и продукта, определенные селективность и активность данного катализатора могут незначительно различаться от одного опытного пробега до другого.
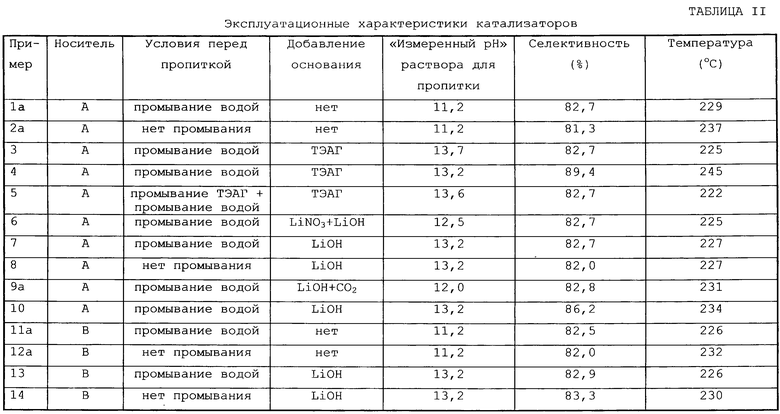
Определили начальные значения по эксплуатации для селективности при 1,5% оксида этилена, и они представлены в табл.II.
Можно видеть, что значительные улучшения в свойствах катализатора наблюдаются тогда, когда активность водородных ионов в растворе для нанесения снижена. Этот эффект не является специфичным для определенного носителя, что показано в примере, где два различных носителя проявляют улучшение при повышении “измеренного рН” раствора для пропитки. Это также остается в силе и для существенно измененного носителя, как в примере 5, где носитель А экстрагировали сильно основным раствором. Более того, показано, что обратное утверждение справедливо, когда раствор “насильно” возвращают к более кислому рН, как видно из примера 9а. В этих примерах показано, что более кислый рН (повышение активности водородных ионов) неблагоприятен для эксплуатационных качеств конечного катализатора, но эту потерю можно ликвидировать, восстановив рН системы. Еще большее улучшение наблюдают при промывании носителя перед нанесением на этот носитель каталитического металла. Кроме того, очевидно, что явление рН эффекта не ограничено особым составом катализатора, что наилучшим образом иллюстрировано в примерах 4 и 10, где к раствору для пропитки добавляют присадку, повышающую селективность, такую, как рений.
Данное изобретение относится к области получения катализаторов. Описан способ нанесения одного или более каталитически активных металлов на носитель, причем упомянутый способ включает в себя выбор носителя и нанесение на этот носитель одного или более каталитически активных металлов, при этом нанесение осуществляют путем погружения носителя в раствор для пропитки, причем активность водородных ионов в этом растворе для пропитки снижена. Кроме того, изобретение относится к катализаторам, полученным этим способом. В примерах серебро и промотор наносят на носитель из оксида алюминия в присутствии гидроксида тетраэтиламмония. Технический результат: эти катализаторы пригодны для использования при получении оксида этилена. 2 н. и 7 з.п. ф-лы, 2 табл.
при этом нанесение осуществляют с помощью раствора для пропитки, в котором при добавлении основания измеренное значение рН раствора составляет по меньшей мере 12,5.
| US 4361500 A1, 30.11.1982.GB 0568978 A1, 30.04.1945.RU 2046015 C1, 20.10.1995.US 4994587 A1, 19.02.1991. |
Авторы
Даты
2004-08-20—Публикация
1999-09-09—Подача