Предпосылки создания изобретения.
Ловастатин, правастатин, мевастатин, симвастатин, их производные и аналоги известны как ингибиторы HMG-CoA-редуктазы и применяются в качестве анти(гипер)холестеринемических агентов. Их получают ферментацией микроорганизмов различных видов, относящихся к роду Aspergillus, Monascus, Nocardia, Amycolatopsis, Mucor или Penicillium.
Чистота активного ингредиента является важным фактором для получения безопасного и эффективного фармацевтического препарата. Высочайшая возможная чистота продукта особенно важна, если фармацевтический продукт нужно применять в течение более длительного периода, как, например, в случае лечения или предотвращения высокого содержания холестерина в плазме.
Накопление примесей из фармацевтических препаратов более низкой степени чистоты может вызвать в ходе лекарственного лечения множество побочных эффектов.
Известные способы выделения и очистки антихолестеринемических агентов включают различные комбинации методов экстракции, хроматографии, лактонизации и кристаллизации. Чистота конечного продукта, получаемого в результате этих операций, ниже 99.6%. Получение продукта более высокой степени чистоты этими методами возможно, но при этом выход заданного продукта неприемлемо низок для того, чтобы можно было использовать эти методы в больших промышленных масштабах.
Способ выделения, описанный в Международной заявке WO 92/16276, решает задачу получения ингибиторов HMG-CoA-редуктазы с чистотой выше 99.5%, но требуется сложное промышленное оборудование для высокоэффективной жидкостной хроматографии (ВЭЖХ). Согласно Международной заявке WO 92/16276 сырой ингибитор HMG-CoA-редуктазы с чистотой примерно 85% или выше растворяют в органическом растворителе или в растворе органического растворителя в воде. Затем смесь забуферивают до рН между 2 и 9 и помещают на колонку для ВЭЖХ. После отбора нужной фракции (пика) с ингибитором HMG-CoA-редуктазы часть растворителя удаляют, а затем добавляют воду или же отгоняют две трети смеси растворителей, а ингибитор HMG-CoA-редуктазы кристаллизуется. Достигаемая этим методом конечная чистота продукта действительно составляет по меньшей мере 99.5% при выходе около 90%.
Сущность изобретения
Данное изобретение относится к новому промышленному способу выделения и очистки ингибиторов HMG-CoA-редуктазы с чистотой выше 99.6% и, предпочтительно, выше 99.7% из ферментационного бульона (культуральной среды). Чтобы достичь этой цели, были предприняты обширные исследования по изучению химических соединений, образующихся при брожении, с использованием различных видов микроорганизмов, принадлежащих к роду Aspergillus, Monascus, Nocardia, Mucor, Amycolatopsis или Penicillium, их химических свойств и их поведения в различных растворителях при различных рН. Т.е. вышеуказанная цель была достигнута с помощью способа по данному изобретению, который включает следующие стадии:
- осветление бульона с мицелием и концентрирование осветлённого бульона до меньшего объёма;
- подкисление концентрата до значения рН в интервале 4.5-7.5 с последующей экстракцией ингибитора HMG-CoA-редуктазы этилацетатом;
- при необходимости, лактонизация;
- кристаллизация ингибитора HMG-CoA-редуктазы из смешивающегося с водой или растворимого в воде органического растворителя, и
- кристаллизация ингибитора HMG-CoA-редуктазы из органического растворителя, ограниченно смешивающегося водой или ограниченно растворяющегося в ней.Подробное описание изобретения
Описание чертежей
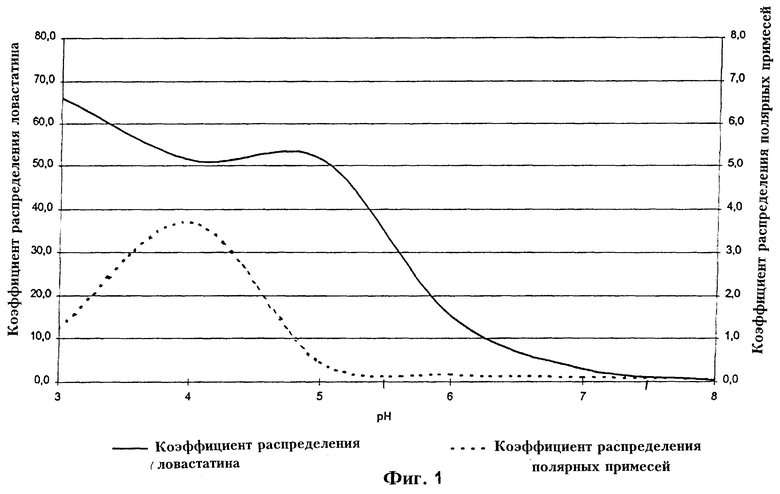
На фиг.1 показана зависимость от рН коэффициента распределения ингибитора HMG-CoA-редуктазы (ловастатин) и примесей соответственно на стадии экстракции этилацетатом, и
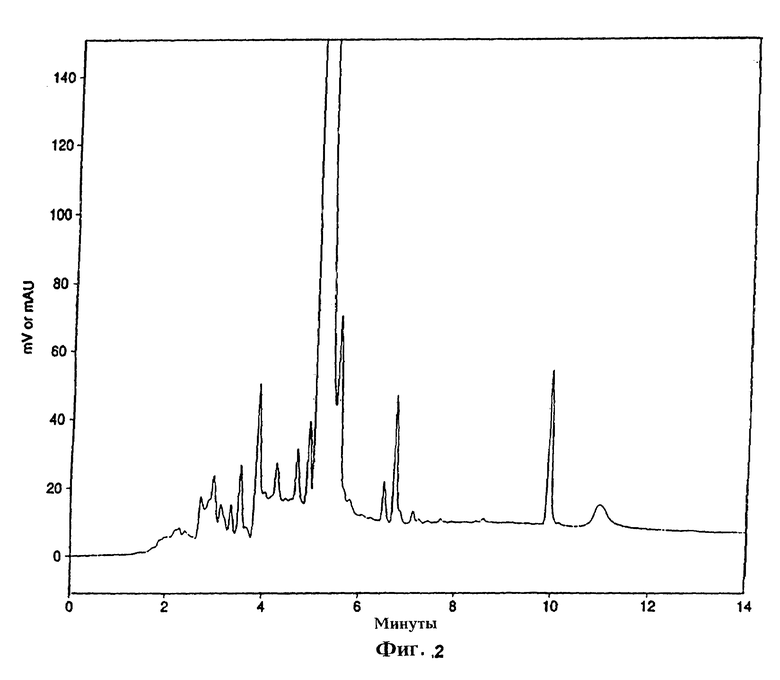
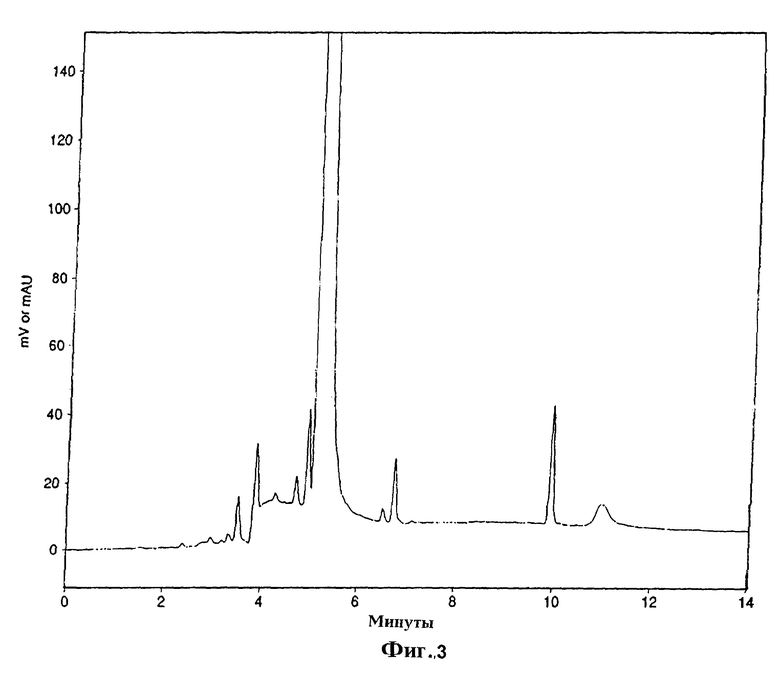
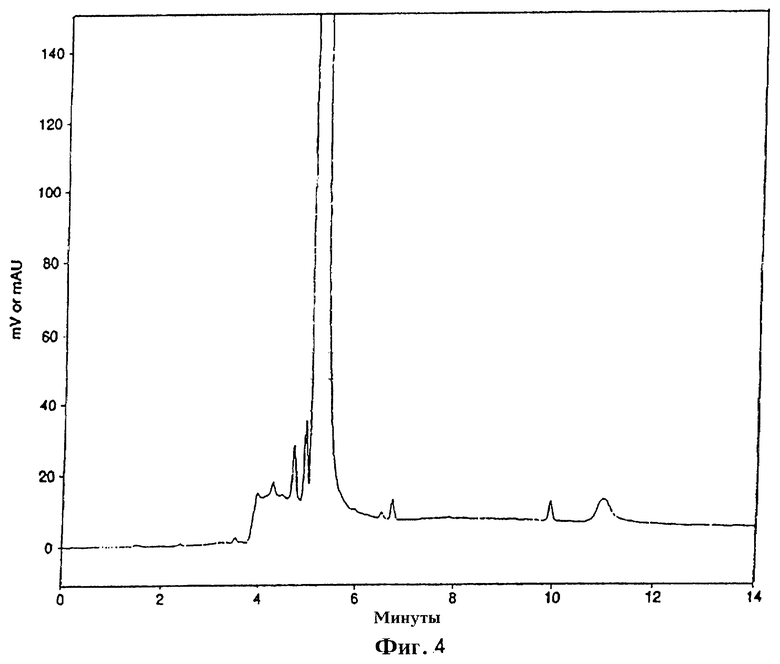
на фиг.2, 3 и 4 изображены ВЭЖХ-диаграммы (хроматограммы) образцов ингибитора HMG-CoA-редуктазы после экстракции этилацетатом в виде сырого вещества, после кристаллизации из смешивающегося с водой или растворимого в воде органического растворителя и после дополнительной кристаллизации из органического растворителя, ограниченно смешивающегося с водой или ограниченно растворяющегося в ней соответственно.
Так как ингибиторы HMG-CoA-редуктазы обычно являются как внутри-, так и внеклеточными продуктами, необязательно, но предпочтительно их энергично растворять для перехода из мицелия в ферментационную жидкость. Способ растворения, описанный в Международной заявке WO 97/20834, включает обработку ферментационного бульона щелочным основанием до рН 11.5 и перемешивание в течение трёх часов. Международная заявка WO 97/06128 показывает, что растворения можно достигнуть подщелачиванием ферментационного бульона до рН от 10-13 при температуре между 60 и 95°С. Ингибиторы HMG-CoA-редуктазы можно эффективно растворять из мицелия при рН выше 9, но слишком продолжительное воздействие столь жёстких условий вызывает разрыв сложноэфирной связи между гидроксильной группой нафталинового ядра и карбоновой кислотой. Равновесие между ингибиторами HMG-CoA-редуктазы и деацилированными ингибиторами HMG-CoA-редуктазы сдвигается в более жёстких условиях в сторону деацилированных продуктов. Неожиданно авторами настоящего изобретения было обнаружено, что эффективность процесса растворения, проводимого в температурном интервале от 10 до 40°С, предпочтительно в интервале от 18 до 40°, например, при комнатной температуре, менее чем в течение часа, предпочтительно менее чем в течение получаса, например в течение примерно 10 минут, при рН между 9.5 и 13, наиболее предпочтительно, между 9.5 и 11.5, равна эффективности, достигаемой с помощью менее экономичных и более продолжительных по времени способов, осуществляемых при более высоких температурах, описанных в более ранних приведенных выше патентных заявках. Процесс растворения можно проводить также при рН ниже 9.5 и даже ниже 6, но в этом случае требуется применение огромных количеств органических растворителей.
Если осуществляют данный предпочтительный вариант способа растворения ингибитора HMG-CoA-редуктазы, ферментационный бульон последовательно обрабатывают подкисляющим агентом, соответствующей минеральной кислотой, чтобы довести значение рН до 7.5-8.5. Соответствующие минеральные кислоты суть фосфорная, серная и соляная. Ингибиторы HMG-СоА-редуктазы устойчивы в этом интервале рН, и ферментационный бульон также может храниться некоторое время после этой стадии, если это необходимо или желательно.
Мицелий удаляют из ферментационного бульона (культуральной среды) с помощью соответствующих стадий отделения, таких, например, как фильтрование и/или центрифугирование. Фильтрование является предпочтительным, и может применяться как классическая методика фильтрования, так и микро-, ультра- и диафильтрация. Осветлённый бульон (питательная среда) затем концентрируют до меньшего объёма, наиболее предпочтительно в пять-десять раз, с помощью обратного осмоса или других способов уменьшения объёма.
Подкисление и стадия экстракции этилацетатом, описанная ниже, являются важными моментами процесса очистки.
Указанный концентрат подкисляют подкисляющим агентом, соответствующей минеральной кислотой, до рН между 4.5 и 7.5. Можно применять уже упомянутые выше в качестве примеров минеральные кислоты. Затем ингибитор HMG-CoA-редуктазы экстрагируют из указанного концентрата с корректированным рН этилацетатом. Экстракцию удобно проводить в колонне для противоточной экстракции. Соотношение между коэффициентами распределения ингибиторов HMG-CoA-редуктазы и растворимыми в этилацетате примесями является наибольшим при рН 5.5-7.5 и особенно при рН 6.0-7.0, и часть полярных примесей отделяется уже на этой стадии. Экстракция, проводимая при значениях рН ниже 5.0, особенно ниже 4.0, является более эффективной за счёт более высокого коэффициента распределения ингибиторов HMG-CoA-редуктазы, но она даёт более высокое содержание полярных примесей. Коэффициенты распределения примесей, растворимых в этилацетате, также высоки при таком значении рН, как это показано на фиг.1. Экстракция этилацетатом, проводимая при рН между 4.5 и 7.5, в частности выше 5.0 и в особенности выше 5.5, приводит к более низкому содержанию полярных примесей из-за их низких коэффициентов распределения. Более низкий коэффициент распределения ингибиторов HMG-CoA-редуктазы в процессе экстракции при таком значении рН можно компенсировать большей высотой противоточной экстракционной колонны.
Если нужно, полученные этилацетатные вытяжки затем концентрируют, и ингибитор HMG-CoA-редуктазы лактонизируют, при необходимости, на этой стадии процесса. При рН между 5.5 и 7.5 основная часть ингибитора HMG-CoA-редуктазы находится в виде свободной кислоты. Следовательно, концентрирование и лактонизацию можно опустить, если ингибитор HMG-CoA-редуктазы не используется в фармацевтическом препарате в виде лактона. Лактонизацию удобно проводить при контактировании ингибитора HMG-CoA-редуктазы с каталитическим количеством минеральной или органической кислоты, более предпочтительно трифторуксусной кислоты (TFA). Ингибитор HMG-CoA-редуктазы, который при необходимости превращают в лактон, можно затем непосредственно кристаллизовать из этилацетата, как будет описано ниже. Или же этилацетат удаляют, обычно упариванием, и получают сырой продукт-ингибитор HMG-CoA-редуктазы, который при необходимости лактонизируют.
Полученный таким образом сырой ингибитор HMG-CoA-редуктазы затем, при необходимости, подвергают адсорбционной хроматографии, предпочтительно с обращённой фазой. Соответственно, в качестве подвижной фазы для адсорбционной хроматографии можно применять ацетонитрил или низшие спирты, такие, например, как метанол, этанол или пропанол, или смесь этих растворителей с водой. Предпочтительно, сырой ингибитор HMG-CoA-редуктазы растворяют в чистом ацетонитриле или смеси ацетонитрил/вода с содержанием ацетонитрила по меньшей мере 30 объёмных % (V/V), и полученный раствор пускают на колонну для адсорбционной хроматографии. Заполнение колонны включает, но не ограничивается, неподвижной фазой на основе октилсилана, димитилсилана, октадецилсилана, цианосилана, сополимера полистирола с дивинилбензолом или полиакрилата. Можно также использовать другие типичные для неподвижной фазы материалы, например диоксид кремния, оксид алюминия и т.п. Адсорбированные соединения элюируют подходящей подвижной фазой, такой, например, как градиент ацетонитрил/вода. Нужную фракцию (пик) ингибитора HMG-CoA-редуктазы собирают и растворитель подвижной фазы отгоняют, при этом ингибитор HMG-CoA-редуктазы кристаллизуется. Чистота кристаллизованных сырых ингибиторов HMG-CoA-редуктазы составляет 80-92% и зависит от профиля (распределения) примесей в ферментационном бульоне. При необходимости адсорбционную хроматографию можно заменить также нормальной хроматографией, флеш-хроматографией, промышленной ВЭЖХ, или экстракцией, или кристаллизацией.
Общая обработка с помощью кристаллизации, которая особенно пригодна по данному изобретению, будет подробнее описана далее. Более конкретно, она включает кристаллизацию ингибитора HMG-CoA-редуктазы из органического растворителя, смешивающегося с водой или растворимого в воде, и кристаллизацию ингибитора HMG-CoA-редуктазы из органического растворителя, ограниченно смешивающегося с водой или ограниченно растворимого в воде. Порядок обеих кристаллизации может быть также обратимым. Само по себе свойство органического растворителя либо смешиваться с водой или растворяться в ней, либо ограниченно смешиваться с водой или ограниченно растворяться в ней известно специалисту в данной области и, например, описано в “Ullmann’s Encyclopedia of Industrial Chemistry”, Vol.A 24, 5th edition (1993), p.437-505. Применительно к данному изобретению термин “смешивающийся с водой или водорастворимый” относится к органическим растворителям, которые практически неограниченно, предпочтительно на 100%, смешиваются с водой или растворяются в ней, а термин “ограниченно смешиваются с водой или ограниченно растворяющийся в ней” включает также не смешивающиеся с водой или не растворимые в воде органические растворители. Кроме того, понятие “кристаллизация” по данному изобретению, в частности, также включает осаждение.
Примеры практически смешивающихся с водой или растворимых в воде органических растворителей включает: низшие алкиловые спирты, например, такие как метанол, этанол, пропанол и изопропиловый спирт, низшие алкилкетоны, например, такие как ацетон, метилэтилкетон, низшие алкиловые эфиры гликоля, такие как метилгликоль, этилгликоль, пропилгликоль и этилдигликоль, и диполярные апротонные растворители, такие как N,N-диметилформамид (ДМФА), N,N-диметилацетамид (ДМАА) и диметилсульфоксид (ДМСО), включая смеси этих растворителей. В качестве особенно предпочтительных примеров смешивающихся с водой растворителей следует упомянуть ацетон и низшие алканолы. Примеры органических растворителей с ограниченной смешиваемостью с водой или ограниченной растворимостью в ней включают: высшие алканолы, такие, например, как бутанол, изобутанол, амиловый спирт, гексанол, 2-этилгексанол, бензиловый спирт и циклогексанол, высшие алкилкетоны, такие как метилбутилкетон, метилизобутилкетон и циклогексанол, сложные эфиры, например, такие как метилацетат, этилацетат, н-пропил (и изопропил-) ацетат, н-бутил (и изобутил- или вт. -бутил-) ацетат и амилоцетат, простые эфиры, например, такие как диэтиловый эфир и диизопропиловый эфир, хлорированные углеводороды, такие, например, как хлористый метилен и хлороформ, ацетонитрил и т.п., включая смеси этих растворителей. Особенно предпочтителен в качестве растворителя, ограниченно смешивающегося с водой или ограниченно растворимого в ней, этилацетат.
Неожиданно было обнаружено, что кристаллизация ингибиторов HMG-СоА-редуктазы из смешивающегося с водой органического растворителя, такого как ацетон или низший алканол, с последующими дополнительными перекристаллизациями из того же растворителя может удалить только минорную часть неполярных и основную часть полярных примесей, а кристаллизация из органического растворителя, ограниченно смешивающегося с водой, например этилацетата, с последующими дополнительными перекристаллизациями из того же растворителя удаляет только основные неполярные примеси. Последнее четко видно из ВЭЖХ-хроматограмм сырого ингибитора HMG-CoA-редуктазы (фиг.2), ингибитора HMG-CoA-редуктазы после кристаллизации из ацетона (фиг.3) и ингибитора HMG-CoA-редуктазы, полученного кристаллизацией из ацетона и затем перекристаллизованного из этилацетона (фиг.4). В соответствии с этим неожиданным фактом последнюю стадию по данному изобретению, включающую комбинированную кристаллизацию из смешивающегося с водой или растворимого в воде органического растворителя и из органического растворителя, ограниченно смешивающегося с водой или ограниченно растворимого в ней, нельзя исключить из процесса получения ингибиторов HMG-CoA-редуктазы высокой степени чистоты.
Комбинированная кристаллизация по данному изобретению может быть осуществлена следующим образом. Сначала кристаллы сырого ингибитора HMG-CoA-редуктазы растворяют в вышеуказанном практически (предпочтительно на 100%) смешивающемся с водой или растворимом в воде органическом растворителе, в частности в ацетоне или низшем спирте, а затем добавляют воду, чтобы вызвать кристаллизацию или осаждение ингибитора HMG-CoA-редуктазы, растворённый в практически смешивающемся с водой или в практически растворимом в воде органическом растворителе, добавляют в воду для кристаллизации или осаждения. Эти операции можно повторять с тем же или другим смешивающимся с водой или растворимым в ней органическим растворителем, если необходимо, например, от одного до четырёх раз в зависимости от чистоты исходного продукта.
Полученные при этом кристаллы затем растворяют в вышеуказанном растворителе, ограниченно смешивающемся с водой или ограниченно растворимом в ней, например этилацетате, до соответствующей концентрации, предпочтительно в интервале от 10 до 35 г/л, наиболее предпочтительно в интервале от 15 до 25 г/л. После удаления от одной трети до трёх четвертей растворителя ингибитор HMG-CoA-редуктазы кристаллизуется. Кристаллизацию из этого же самого или другого органического растворителя, ограниченно смешивающегося с водой или ограниченно растворимого в ней, можно повторить, если требуется, например, от одного до трёх раз, в зависимости от чистоты продукта, полученного кристаллизацией из смешивающегося с водой или растворимого в воде органического растворителя. Перекристаллизованный ингибитор HMG-CoA-редуктазы затем фильтруют и сушат, получая продукт с чистотой по меньшей мере 99.6%.
Как уже указывалось, порядок кристаллизации может быть обратным, т.е. сначала проводят кристаллизацию из органического растворителя, ограниченно смешивающегося с водой или ограниченно растворимого в ней, а затем кристаллизуют из смешивающегося с водой или растворимого в воде ограниченного растворителя. В предпочтительном варианте изобретения осуществляемую сначала кристаллизацию из этилацетата в качестве ограниченно смешивающегося с водой или ограниченно растворимого в воде органического растворителя можно проводить непосредственно после стадии экстракции этилацетатом или, при необходимости, после описанной выше стадии лактонизации.
По способу согласно данному изобретению можно достичь чистоты продуктов по меньшей мере 99.6% и даже по меньшей мере 99.7%.
В другом альтернативном варианте изобретения можно осуществлять разные виды перекристаллизации неоднократно и попеременно.
В другом аспекте данного изобретения ранее описанное сочетание стадий кристаллизации смешивающегося с водой или растворимого в воде органического растворителя и из органического растворителя, ограниченно смешивающегося с водой или ограниченно растворимого в ней, используют в качестве стадий окончательной очистки любого процесса выделения и/или очистки ингибиторов HMG-CoA-редуктазы.
Соответственно, такую стадию окончательной очистки можно применять в случае обычно получаемого сырого ингибитора HMG-CoA-редуктазы. При этом достигается чистота ингибитора HMG-CoA-редуктазы по меньшей мере 99.6% и даже по меньшей мере 99.7%.
Способ по данному изобретению особенно пригоден, когда в качестве ингибитора HMG-CoA-редуктазы применяют ловастатин. Соответственно, в другом аспекте данного изобретения описанный выше процесс применяют для выделения и/или очистки ловастатина.
Практически чистые ингибиторы НМG-СоA-редуктазы, полученные по способу согласно данному изобретению, например, такие как ловастатин, мевастатин, правастатин и симвастатин, а также их производные и аналоги, можно использовать для получения и/или лечения заболеваний. Полученные ингибиторы и фармацевтические препараты особенно пригодны в качестве лечебных или профилактических средств, используемых для того чтобы уменьшить вероятность (риск) удара, преходящего нарушения мозгового кровообращения, атеросклероза и инфаркта миокарда.
Следующие примеры иллюстрируют способ по данному изобретению, и их не следует рассматривать как ограничивающие изобретение, сформулированное в Формуле изобретения.
Пример 1
Ферментационный бульон (160 л) с концентрацией ловастатина 1 г/л, полученный брожением Aspergillus terrus ATCC 20542, помещают в ёмкость (400 л) и доводят рН до 10 с помощью 1 М водного раствора гидроксида натрия. После 10-минутного интенсивного перемешивания при комнатной температуре рН бульона доводят до 9 с помощью 1 М серной кислоты и биомассу отфильтровывают. Затем фильтрат подкисляют 1 М серной кислоты до рН 6.5. К фильтру добавляют 160 л этилацетата и полученную смесь перемешивают 20 мин. Водную и этилацетатную фазы разделяют с помощью экстракционного центрифугирования. Этилацетатную вытяжку упаривают на роторном испарителе до объема 14 л. Концентрация ловастатина в виде свободной кислоты в этилацетатном концентрате доходит до 10 г/л.
Затем этилацетатный концентрат (14 л) помещают в реактор (40 л) и лактонизируют. Лактонизацию инициирует каталитическое количество TFA (ТФК) (0.5 мл ТФК/1л концентрата). Процесс лактонизации длится два часа при 40°С. После лактонизации концентрат промывают дважды 14 л 5% водного раствора гидрокарбоната аммония. Водную фазу отделяют, органическую фазу дополнительно упаривают (досуха) в роторном испарителе. Образующийся продукт-масло (-1.5 л)- содержит 133 г ловастатина.
Полученное масло (161 мл) растворяют в 80 мл ацетонитрила и вносят в колонку для хроматографии (80 см, 3.6 см), заполненную ХАД-16 (ХАД-16 - торговое название компании Rohm and Haas, 20-50 меш). Сначала элюируют смесью ацетонитрил/вода 40:60 (рН 3, устанавливают с помощью соляной кислоты) со скоростью 75 мл/мин. Элюирование контролируют с помощью УФ-детектора (236 нм) и после появления первой капли с таким поглощением начинают элюирование смесью ацетонитрил/вода 55/45 (рН 3, доводят соляной кислотой). Собирают основную фракцию и после исчезновения (“падения”) поглощения, колонку промывают 80:20 ацетонитрил/вода (рН 3, устанавливают соляной кислотой). Ацетонитрил отгоняют из основной фракции на роторном испарителе (50°С, 150 мбар или 15 кПа) и выпавшие кристаллы отфильтровывают. Масса кристаллов 24.5 г и содержание ловастатина 50 весовых % (вес/вес; W/W). Чистота 92.5% (ВЭЖХ).
Полученные кристаллы (24 г) растворяют в 350 мл ацетона и при постоянном перемешивании добавляют 700 мл воды. Смесь выдерживают 30 мин при 4°С. Выпавшие кристаллы отфильтровывают и сушат в вакууме при комнатной температуре. Масса кристаллов составляет 12.7 г при содержании лавастатина 90 весовых % (вес/вес). Чистота 98.8% (ВЭЖХ).
Перекристаллизацию из ацетона повторяют в тех же условиях и получают 11.3 г кристаллов с 97 вес.% содержанием ловастатина. Чистота 99.4% (ВЭЖХ).
Кристаллы (11.3 г), полученные после второй кристаллизации из ацетона, растворяют в 700 мл этилацетата и этилацетат упаривают в вакууме до концентрации ловастатина 70 г/л. Концентрат выдерживают при 8°С в течение одного часа. Выпавшие кристаллы ловастатина отфильтровывают и затем сушат в вакууме. Масса кристаллов составляет 9.4 г при содержании ловастатина 99.6% весовых. Чистота 99.7% (ВЭЖХ).
Пример 2
Кристаллы ловастатина (3 г), выделенные после ХАД-адсорбционной хроматографии, как описано в Примере 1, растворяют в 170 мл этилацетата. Этилацетат упаривают в вакууме (200 мбар, 20 кПа) при 50°С до 35 мл. Концентрат выдерживают один час при 10°С. Выпавшие кристаллы ловастатина отфильтровывают и затем сушат в вакууме. Массы кристаллов 2.1 г при содержании ловастатина 96 вес.% (вес/вес). Чистота 99.0% (ВЭЖХ).
Полученные кристаллы (2.1 г) растворяют в 50 мл ацетона и добавляют 85 мл воды. Смесь выдерживают 30 мин при 10°С и кристаллы отфильтровывают и сушат в вакууме при 40°С. Масса полученных кристаллов составляет 1.9 г с содержанием ловастатина 99 вес.% (вес/вес). ВЭЖХ-чистота 99.8%.
Пример 3
Ферментационный бульон (30 л в 50 л биореакторе), содержащий правастатин (690 г на кг ферментационного бульона; ВЭЖХ-чистота правастатина составляет 48.7%) фильтруют и полученный в результате мицелий промывают водой. Фильтрат (51 л) подкисляют до рН 5.0 10%-ным водным раствором фосфорной кислоты. Активное вещество (правастатин) затем экстрагируют на экстракционной колонне из фильтрата 70 литрами этилацетата. Водную фазу (50 л), содержащую менее 2 г правастатина и основную часть примесей, сливают. Этилацетатную фазу упаривают до 800 мл и используют далее в процессе выделения. ВЭЖХ-чистота правастатина в этилацетатном экстракте составляет 70.3%.
Для дополнительного выделения маслообразный продукт подвергают адсорбционной хроматографии и комбинированной кристаллизации в соответствии с Примером 1.
Пример 4
Сырой симвастатин (2.3 г) в лактонной форме растворяют в ацетоне (7 мл) и добавляют 15 мл воды. В результате получают маслообразный продукт, который кристаллизуется в течение 10 мин. Полученные кристаллы затем фильтруют, промывают водой и сушат при 40°С в течение 60 мин. Полученные в результате кристаллы (2.2 г) с ВЭЖХ-чистотой 99.51% растворяют в этилацетате (8 мл). Полученный раствор концентрируют до 4 мл, оставляют симвастатин кристаллизоваться на 60 мин при 8°С. Продукт отфильтровывают и промывают водой. Затем кристаллы сушат при 40°С в течение 60 мин. Чистота получающегося симвастатина (1.7 г) составляет 99.73%.
Пример 5
Сырой мевастатин (2.0 г) в лактонной форме с чистотой 98.5% (ВЭЖХ) растворяют в ацетоне (7 мл) и добавляют 20 мл воды. Получают продукт в виде масла, которое кристаллизуется в течение 10 мин. Полученные кристаллы затем фильтруют, промывают водой и сушат при 40°С в течение 60 мин. Эти кристаллы (1.8 г) с чистотой 99.33% (ВЭЖХ) затем растворяют в этилацетате (8 мл). Полученный раствор упаривают до 4 мл и мевастатин оставляют кристаллизоваться при 8°С в течение 60 мин. Продукт отфильтровывают и промывают водой. Затем кристаллы сушат при 40°С в течение 60 мин. Чистота полученного мевастатина (1.3 г) составляет 99.72%.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОЧИСТКИ ФЕРМЕНТАЦИОННОГО БУЛЬОНА | 2001 |
|
RU2265665C2 |
| СПОСОБ ОЧИСТКИ ПРАВАСТАТИНА | 2001 |
|
RU2260582C2 |
| ШТАММ ГРИБА ASPERGILLUS TERREUS № 44-62 - ПРОДУЦЕНТ ЛОВАСТАТИНА, ПРОМЫШЛЕННЫЙ СПОСОБ ВЫДЕЛЕНИЯ ЛОВАСТАТИНА И СПОСОБ ЛАКТОНИЗАЦИИ СТАТИНОВ | 2003 |
|
RU2261901C2 |
| СПОСОБ ПОЛУЧЕНИЯ НАТРИЕВЫХ СОЛЕЙ СТАТИНОВ | 2000 |
|
RU2246481C2 |
| СТАБИЛИЗИРОВАННАЯ ФАРМАЦЕВТИЧЕСКИ ЭФФЕКТИВНАЯ КОМПОЗИЦИЯ И ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ, ЕЕ СОДЕРЖАЩИЙ | 2000 |
|
RU2246943C2 |
| СПОСОБ ВЫДЕЛЕНИЯ ЛОВАСТАТИНА | 1994 |
|
RU2114912C1 |
| ПРОМЫШЛЕННЫЙ СПОСОБ ПОЛУЧЕНИЯ КОМПАКТИНА | 2013 |
|
RU2585233C2 |
| ГИДРОКСИЛИРОВАНИЕ КОМПАКТИНА ДО ПРАВАСТАТИНА С ПОМОЩЬЮ MICROMONOSPORA | 2000 |
|
RU2235780C2 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПАКТИНА | 2013 |
|
RU2585234C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИНГИБИТОРОВ HMG-COA-РЕДУКТАЗЫ С ВЫСОКОЙ СТЕПЕНЬЮ ЧИСТОТЫ | 1999 |
|
RU2235098C2 |
Изобретение относится к биотехнологии. Способ выделения и очистки ингибиторов HMG-CoA-редуктазы включает осветление питательной среды с мицелием, концентрацию осветленного бульона, подкисление концентрата до рН в интервале 4,5-7,5 с последующей экстракцией ингибитора HMG-CoA-редуктазы этилацетатом, кристаллизацию выделенного ингибитора HMG-CoA-редуктазы из смешивающегося с водой или растворимого в воде органического растворителя и кристаллизацию ингибитора HMG-CoA-редуктазы из органического растворителя, ограниченно смешивающегося с водой или ограниченно растворяющегося в воде. Последовательность стадий кристаллизации можно изменять. Сочетание конкретных стадий кристаллизации применяют для очистки сырого ингибитора HMG-CoA-редуктазы с получением ингибитора HMG-CoA-редуктазы, имеющего чистоту выше 99,6%. Изобретение обеспечивает высокую чистоту целевого продукта, составляющую выше 99,6%. 2 н. и 23 з.п. ф-лы, 4 ил.
| WO 9720834 А, 12.07.1997 | |||
| US 4319039 A, 09.03.1997 | |||
| US 4294846 А, 13.10.1981 | |||
| WO 9706128 А, 20.02.1997 | |||
| US 5202029 А, 13.04.1993. |
Авторы
Даты
2004-08-27—Публикация
1999-02-17—Подача