Область техники, к которой относится изобретение
Изобретение относится к терапевтически эффективным соединениям и к способам лечения определенных заболеваний/синдромов с помощью этих соединений.
Ссылки
В последующем описании ссылки на литературные источники, указанные в скобках или в виде верхнего индекса у соответствующей части описания, относятся к следующим публикациям:
1. Sladek F.M., Zhong W.M., Lai E., Darnell J.E., Jr. Gene Dev. 4, 2353-2365 (1990).
2. Sladek F.M. в: Liver Gene Expression (под ред. Tronche F. и Yaniv M.), стр. 207-230, R.G. Landes Co., Austin, TX (1994)
3. The Metabolic and Inherited Bases of Inherited Disease (под ред. Scriver C.R., Beaudet A.L., Sly W.S., Valle D.), том II, часть 8, 1995 (McGraw-Hill, Inc.)
4. Yamagata К. и др., Nature 384, 458-460 (1996).
5. DeFronzo R.A. и Eleaterio F., Diabetes Care 14, 173-194 (1991).
6. Leff Т., Reue К., Melian A., Culver Н. и Breslow J.L., J. Biol. Chem. 264, 16132-16137 (1989).
7. Cave W.T., FASEB J., 5, 2160-2166 (1991).
8. Chin J.P.F., Prost. Leuk. Essent. Fatty Acids 50, 211-222 (1994).
9. Grundy S.M. и Denke M.A., J. Lipid Res. 31, 1149-1172 (1990).
10. Storlien L.H. и др., Science 237, 885-888 (1987).
11. Unger R.H., Diabetes 44, 863-870 (1995).
12. Morris M.C., Saks F. и Rosner В., Circulation 88, 523-533 (1993).
13. Hultin M.B., Prog. Hemost. Thromb. 10, 215-241 (1991).
14. Bar-Tana J., Rose-Kahn G., Frenkel В., Shafer Z. и Fainaru M., J. Lipid Res. 29, 431-441 (1988).
15. Tzur R., Rose-Kahn G., Adier J. и Bar-Tana J., Diabetes 37, 1618-1624 (1988).
16. Tzur R., Smith E. и Bar-Tana J., Int. J. Obesity 13, 313-326 (1989).
17. Russel J.C., Arny P.M., Graham S.E., Dolphin P.J. и Bar-Tana J., Arterioscler. Thromb. Biol. 15, 918-923 (1995).
Вышеуказанные публикации, описания к патентам и заявкам на патенты полностью включены в настоящее описание в виде ссылок, если это и не указано конкретно для каждой отдельной публикации, соответственно для каждого отдельного описания к патенту и заявке на патент.
Предпосылки создания изобретения
Гепатоцитный ядерный фактор-4α1 (HNF-4α) (данные обобщены в ссылке 2) является орфановым представителем надсемейства ядерных рецепторов. HNF-4α экспрессируется в печени, в почках, в кишечнике и в поджелудочной железе взрослых и эмбрионов и обусловливает различные нарушения у мышей. Гомологичная рекомбинация HNF-4α приводит к смерти эмбриона. Подобно другим представителям надсемейства рецептор HNF-4α состоит из модулярной структуры, включающей высококонсервативный N-концевой ДНК-связывающий домен, который через шарнир соединен с гиброфобным С-концевым лигандсвязыващим доменом. Ранее было проведено клонирование и получены характеристики двух изоформ HNF-4α: HNF-4α1 и HNF-4α2, которая представляет собой вариант сплайсинга, имеющего вставку из 10 аминокислот в С-концевом домене.
HNF-4α является активатором экспрессии гена. Активация транскрипции с помощью HNF-4α опосредована его связыванием в виде гомодимера с реактивными последовательностями промотора DR-1 генов-мишеней, что приводит к активации комплекса инициации транскрипции. Активируемые HNF-4α гены (данные обобщены в ссылке 2), кодируют различные ферменты и протеины, участвующие в метаболизме липопротеинов, холестерина и триглицеридов (аполипопротеины AI, AII, AIV, В, CIII, микросомальный протеин переноса триглицеридов, холестерин-7α-гидроксилаза), в метаболизме липидов (митохондриальная ацил-КоА-дегидрогеназа жирных кислот со средней длиной цепи, пероксимальная ацил-КоА-оксидаза жирных кислот, изоферменты цитохрома Р450, участвующие в ω-окислении жирных ацилов и гидроксилировании стероидов, протеин, связывающий жирные кислоты, клеточный ретинолсвязывающий протеин II, трастиретин), в метаболизме глюкозы (фосфоенолпируват-карбоксикиназа, пируваткиназа, альдолаза, glut2), в метаболизме аминокислот (тирозин-аминотрансфераза, орнитин-транскарбамилаза), в свертывании крови (факторы VII, IX, X), в метаболизме железа (трансферрин, эритропоэтин) и в активации макрофагов (протеин типа гепатоцитного фактора роста/стимулирующий макрофаги протеин, протеины ядра вируса гепатита Б и Х-протеины, длинный концевой повтор человеческого ВИЧ-1, α-1-антитрипсин).
Некоторые гены, которые активируются с помощью HNF-4α, играют основную роль в возникновении и развитии атерогенеза, рака, аутоиммунных и некоторых других болезней [3]. Так, например, сверхэкспрессия аполипопротеинов В, AIV и CIII, а также протеина переноса микросомальных триглицеридов может привести к дислипопротеинемии (комбинация гипертриглицеридемии и гиперхолестеринемии) вследствие увеличения производства липопротеинов с очень низкой плотностью (ОНПЛ) и хиломикронов в сочетании с понижением их клиренса из плазмы. Аналогично этому увеличение скоростей гликолиза в поджелудочной железе, приводящее к индуцируемой HNF-4α/HNF-1 сверхэкспрессии/повышенной секреции инсулина в поджелудочной железе, может привести к гиперинсулинемии, обусловливающей устойчивость к инсулину. К настоящему времени установлено, что мутации в HNF-4α и HNF-1 ответственны за развитие юношеского сахарного диабета (MODY) [4]. Устойчивость к инсулину в сочетании с индуцированной HNF-4α сверхэкспрессией фосфоенолпируват-карбоксикиназы и с повышением производства глюкозы в печени может привести к нарушению толерантности к глюкозе (НТГ) и в итоге - к инсулиннезависимому сахарному диабету (ИНСД). Кроме того, в настоящее время гиперинсулинемия рассматривается как основной этиологический фактор, обусловливающий возникновение и развитие эссенциальной гипертензии, и, следовательно, сверхэкспрессия контролируемых HNF-4α генов может дополнительно привести к гипертензии. Индуцируемая HNF-4α сверхэкспрессия факторов свертывания крови в сочетании с возможной сверхэкспресссией ингибиторов фибринолиза крови (например, ингибитор-1 активатора плазминогена) также может привести к усиленному образованию тромбов и к понижению фибринолиза, что сопровождается увеличением предрасположенности к атеросклеротическим процессам.
Установлено также, что дислипопротеинемия, ожирение, НТГ/ИНСД, гипертензия и нарушения свертываемости/фибринолиза могут быть объединены одним синдромом (Х-синдром, метаболический синдром, синдром устойчивости к инсулину) [5]. Высокая активность HNF-4α в отношении транскрипции, приводящая к сверхэкспрессии контролируемых HNF-4α генов, вероятно может привести к возникновению этиологии, характерной для Х-синдрома. По современным данным категории Х-синдрома и сам этот синдром в целом рассматриваются в качестве основных факторов риска возникновения атеросклеротических сердечно-сосудистых заболеваний в западных странах, позволяя предположить, что HNF-4α играет определенную роль в возникновении и развитии атерогенеза. Кроме того, поскольку у людей, страдающих Х-синдромом, возникает и развивается рак молочной железы, толстой кишки и предстательной железы, можно предположить, что сверхэкспрессия контролируемых HNF-4α генов может принимать участие в возникновении и развитии этих злокачественных заболеваний.
В дополнение к той роли, которую HNF-4α играет в экспрессии генов, связанных с Х-синдромом, HNF-4α активирует экспрессию генов, которые кодируют протеины, участвующие в модуляции процесса аутоиммунных реакций. Так, например, индуцированная HNF-4α сверхэкспрессия стимулирующего макрофаги протеина может привести к сенсибилизации макрофагов по отношению к собственным антигенам или к антигенам с перекрестной реактивностью, что приводит к возникновению и развитию аутоиммуных заболеваний, например, ревматоидного артрита, рассеянного склероза и псориаза. Кроме того, поскольку транскрипция протеинов ядра вируса гепатита Б и Х-протеинов, а также длинного концевого повтора человеческого ВИЧ-1 контролируются HNF-4α, то HNF-4α может принимать участие в модуляции процесса инфекции, вызванного этими вирусными агентами.
Поскольку сверхэкспрессия индуцируемых HNF-4α генов может привести к дислипопротеинемии, НТГ/ИНСД, гипертензии, нарушениям свертываемости и фибринолиза крови, атерогенезу, раку, воспалению, иммунодефициту и к другим заболеваниям, можно ожидать, что ингибирование активности HNF-4α в отношении транскрипции приведет к уменьшению обусловленных HNF-4α патологий. Однако пока еще не обнаружены лиганды для HNP-4α, которые могли бы служить основой для создания ингибиторов активности HNF-4α в отношении транскрипции. В настоящем изобретении предложены лиганды для HNF-4α с низкой молекулярной массой, которые специально были созданы с той целью, чтобы действовать в качестве модуляторов индуцируемой HNF-4α транскрипции, которые в результате этого являются потенциальными лекарственными средствами, предназначенными для лечения патологий, вызванных контролируемыми HNF-4α генами, или в которых принимают участие контролируемые HNF-4α гены.
Краткое изложение сущности изобретения
Согласно настоящему изобретению предложены терапевтически эффективные соединения, включающие амфипатический карбоксилат формулы R-COOH или соль, эфир или амид такого соединения, где R обозначает насыщенную или ненасыщенную алкильную цепь, включающую 10-24 атома углерода, один или большее количество из которых может быть замещено гетероатомами, где один или большее количество входящих в цепь атомов углерода или гетероатомов необязательно образуют часть кольца и где указанная цепь необязательно замещена гидрокарбильным радикалом, гетероциклильным радикалом, (низш.)алкоксигруппой, замещенным гидроксилом (низш.)алкилом, гидроксилом, карбоксилом, галогеном, фенилом или замещенным гидроксигруппой, (низш.)алкилом, (низш.)алкоксигруппой, (низш.)алкенилом или (низш.)алкинилом фенилом, С3-С7циклоалкилом или замещенным гидроксигруппой, (низш.)алкилом, (низш.)алкоксигруппой, (низш.)алкенилом или (низш.)алкинилом С3-С7циклоалкилом, причем указанный амфипатический карбоксилат обладает способностью в эндогенных условиях превращаться в соответствующий тиоэфир кофермента А.
В предпочтительном варианте осуществления амфипатический карбоксилат представляет собой ксенобиотический амфипатический карбоксилат. В более предпочтительном варианте осуществления ксенобиотический амфипатический карбоксилат может представлять собой дикарбоновую кислоту с длинной цепью, ω-ОН-карбоновую кислоту, ω-В(ОН)2-карбоновую кислоту, аналог клофибриновой кислоты или нестероидного противовоспалительного лекарства. В наболее предпочтительном варианте осуществления амфипатический карбоксилат выбирают из группы, включающей стеароил(18:0)-КоА, олеоил(18:1)-КоА, линолеоил(18:2)-КоА, линоленоил(18:3)-КоА, эйкозапентаеноил(20:5)-КоА, докозагексаеноил(22:6)-КоА, 1,16-гексадекандионовую кислоту, 1,18-октадекандионовую кислоту, 2,2,15,15-тетраметилгексан-декан-1,16-дионовую кислоту, 2,2,17,17-тетраметилоктадекан-1,18-дионовую кислоту, 3,3,14,14-тетраметилгексадекан-1,16-дионовую кислоту, 3,3,16,16-тетраметилоктадекан-1,18-дионовую кислоту, 4,4,13,13-тетраметилгексадекан-1,16-дионовую кислоту, 4,4,15,15-тетраметилоктадекан-1,18-дионовую кислоту, 16-В(ОН)2-гексадекановую кислоту, 18-В(ОН)2-октадекановую кислоту, 16-В(ОН)2-2,2-диметилгексадекановую кислоту, 18-В(ОН)2-2,2-диметилоктадекановую кислоту, 16-В(ОН)2-3,3-диметилгексадекановую кислоту, 18-В(ОН)2-3,3-диметилоктадекановую кислоту, 16-В(ОН)2-4,4-диметилгексадекановую кислоту, 18-В(ОН)2-4,4-диметилоктадекановую кислоту, 16-гидроксигексадекановую кислоту, 18-гидроксиоктадекановую кислоту, 16-гидрокси-2,2-диметилгексадекановую кислоту, 18-гидрокси-2,2-диметилоктадекановую кислоту, 16-гидрокси-3,3-диметилгексадекановую кислоту, 18-гидрокси-3,3-диметилоктадекановую кислоту, 16-гидрокси-4,4-диметилгексадекановую кислоту и 18-гидрокси-4,4-диметилоктадекановую кислоту.
Другим объектом настоящего изобретения является способ лечения X-синдрома, предусматривающий введение терапевтически эффективного количества амфипатического карбоксилата. В предпочтительном варианте осуществления каждую из болезней, относящихся к категории Х-синдрома, можно лечить по отдельности.
Еще одним объектом настоящего изобретения являются способы модуляции активности HNF-4α.
И, наконец, еще одним объектом изобретения являются способы лечения заболевания или синдрома, предусматривающие введение терапевтически эффективного количества амфипатического карбоксилата. С помощью способов по изобретению можно лечить такие болезни, как, например, рак молочной железы, рак толстой кишки и рак предстательной железы.
Краткое описание чертежей
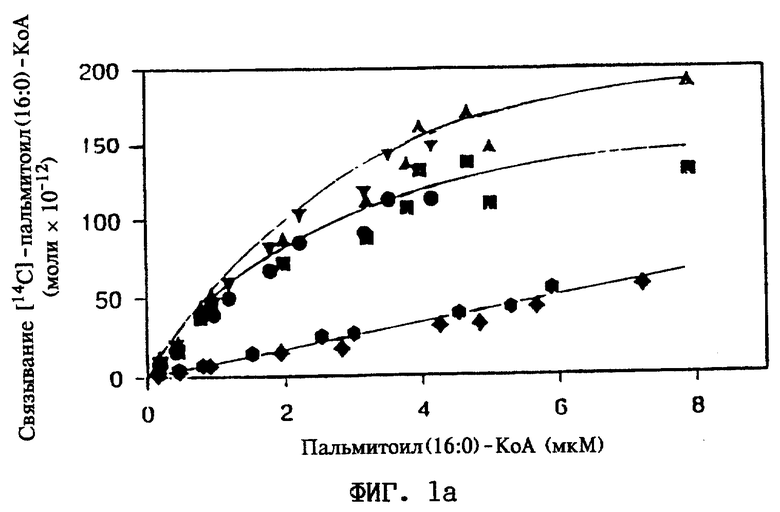
На фиг.1 показано, что тиоэфиры ацилов с длинной цепью и КоА (ацилы с длинной цепью-КоА) являются лигандами для HNF-4α. Слитый протеин GST-HNF-4α(LBD) (I) состоит из HNF-4α (LBD), слитого с глутатион-S-трансферазой (GST). His-HNF-4α (n) состоит из полноразмерного HNF-4α, меченного 6 остатками гистидина.
а. Кривая насыщения связывания для пальмитоил(16:0)-КоА
Соответствующие рекомбинантные протеины инкубируют до достижения состояния равновесия с [3H]-пальмитоил(16:0)-КоА (0,05 мкКи) и с возрастающими концентрациями немеченого пальмитоил(16:0)-КоА, как показано на чертеже. Константу диссоциации (Кd), равную 2,6 мкМ, и максимальное связывание, составляющее 1 моль пальмитоил(16:0)-КоА на 1 моль HNF-4α, определяют с помощью метода Scatchard.
б. Конкурентное связывание с миристоил (14:0)-КоА
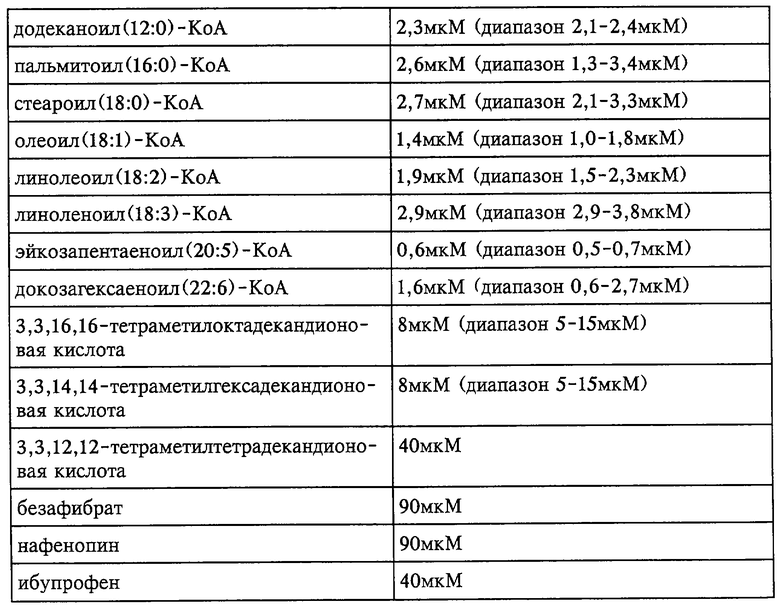
Соответствующие рекомбинантные протеины инкубируют с 8нМ [3H]-пальмитоил(16:0)-КоА (60 Ки/ммоль) и с возрастающими концентрациями немеченого миристоил(14:0)-КоА, как показано на чертеже. Процент связывания соответствует количеству радиоактивно меченного [3H]-пальмитоил(16:0)-КоА в связанной фракции. 100%-ное связывание происходит при концентрации [3H]-пальмитоил(16:0)-КоА 0,3 нмоля. Значение ЕС50 (50%-ная специфичная конкуренция) для миристоил(14:0)-КоА составляет 1,4 мкМ (диапазон 1,2-1,5 мкМ). Значения ЕС50 для других тиоэфиров жирных ацилов и КоА, а также ксенобиотических ацилов и КоА приведены в таблице.
На фиг.2 показано, что лиганды HNF-4α, представляющие собой тиоэфиры жирных ацилов и КоА, модулируют связывание HNF-4α со специфичным для него ДНК-энхансером.
а. Связывание His-HNF-4α (14 нг) с C3Р в отсутствии (полоса 1) или в присутствии либо 10 мкМ миристоил(14:0)-КоА (полоса 2), либо 10 мкМ пальмитоил(16:0)-КоА (полоса 3)
б. Связывание His-HNF-4α (20 нг) с C3Р в отсутствии (полоса 1) или в присутствии либо 10 мкМ стеароил(18:0)-КоА (полоса 2), либо 10 мкМ линоленоил(18:3, w-3)-KoA (полоса 3)
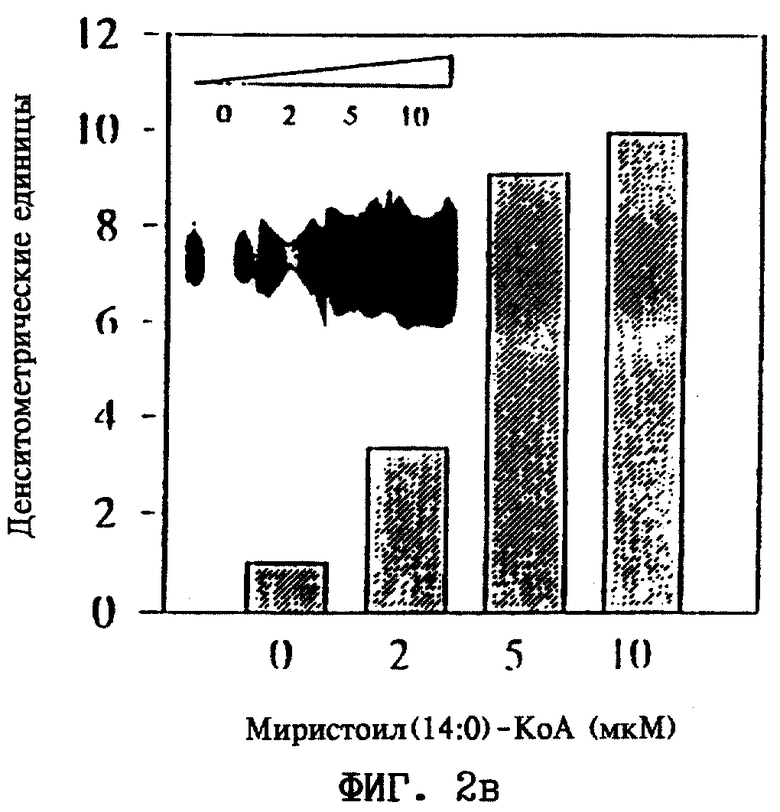
в. Активация связывания His-HNF-4α (14 нг) с СЗР при использовании возрастающих концентраций миристоил(14:0)-КоА.
Показан срез геля, содержащий радиоактивно меченный СЗР, связанный с димером His-HNF-4α.
На фиг.3 показана модуляция активности HNF-4α в отношении транскрипции in vitro с помощью тиоэфиров жирных ацилов с длинной цепью и КоА.
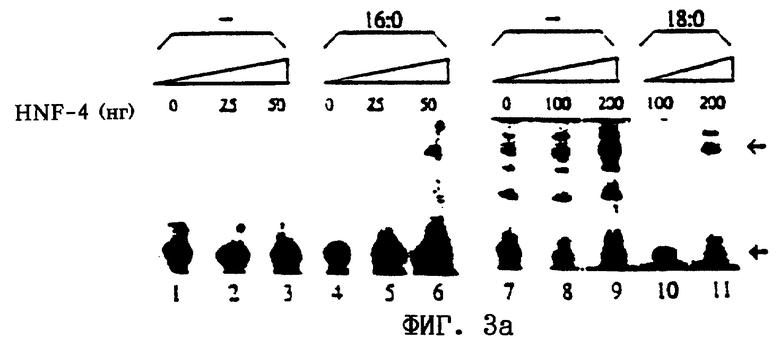
а. Приведены данные репрезентативных экспериментов, в которых оценивали транскрипцию in vitro тестируемой матрицы при добавлении указанных на чертеже возрастающих концентраций His-HNF-4α и без His-HNF-4α (полосы 1-3, 7-9) или при добавлении 10 мкМ пальмитоил(16:0)-КоА (полосы 4-6) или 10 мкМ стеароил(18:0)-КоА (полосы 10-11). Транскрипты тестируемых и контрольных матриц с правильным началом транскрипции обозначены простой стрелкой (→) и жирной стрелкой (→) соответственно.
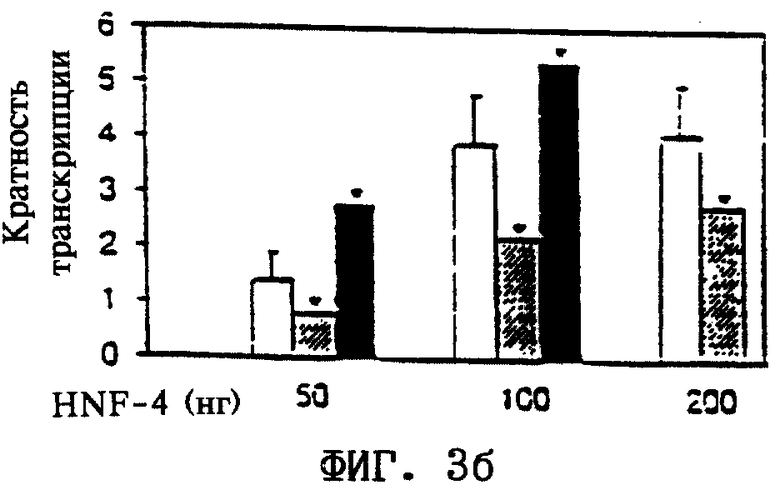
б. Индуцированная HNF-4a транскрипция в отсутствие (незакрашенные столбики) либо в присутствии 10 мкМ пальмитоил(16:0)-КоА (закрашенные столбики) или 10 мкМ стеароил(18:0)-КоА (заштрихованные столбики). Кратность транскрипции обозначает соотношение специфичных транскриптов, полученных с помощью тестируемой матрицы, и транскриптов, полученных с помощью контрольной матрицы, стандартизованное по отношению к соотношению, полученному без HNF-4α. На чертеже обобщены данные по 5 независимым экспериментам для каждого ацил-КоА. Символом * обозначены достоверные данные, полученные при сравнении с соответствующим значением в опытах без добавления лиганда.
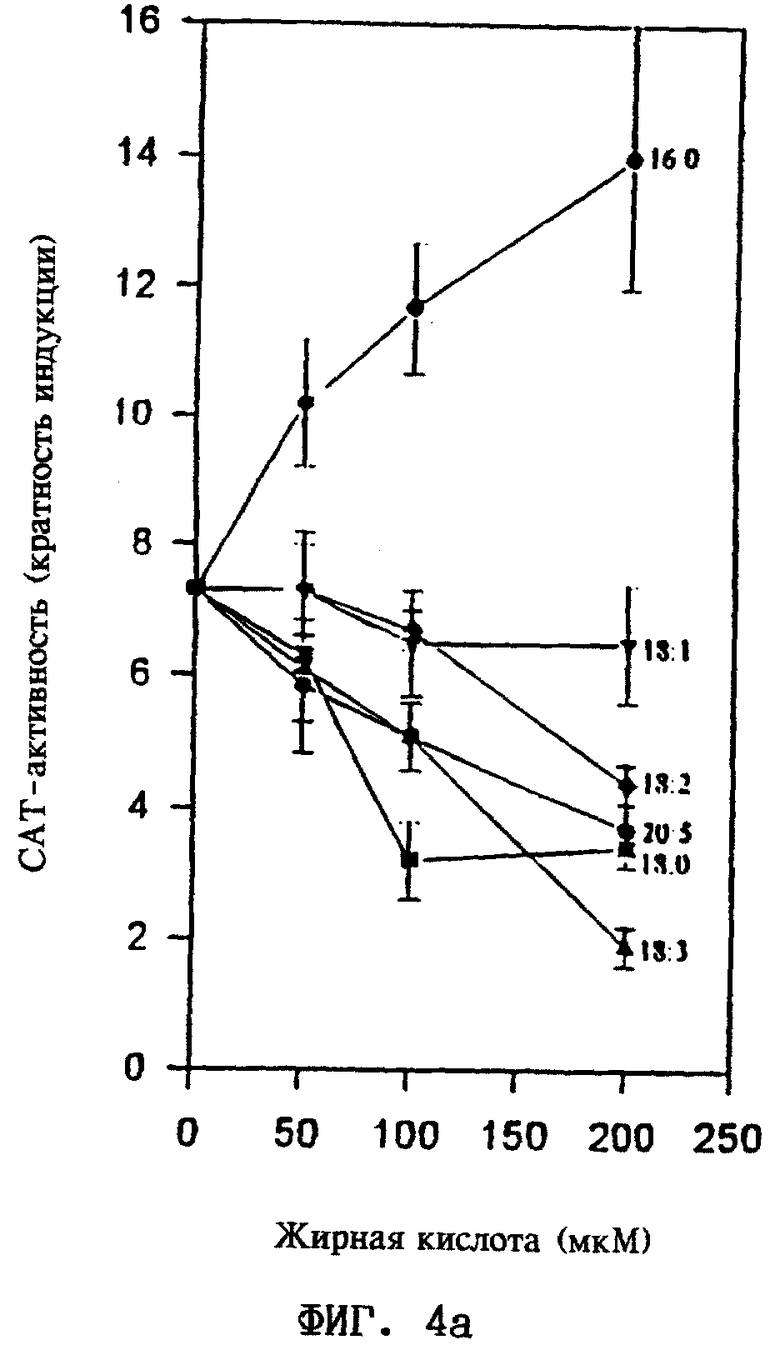
На фиг.4 показана модуляция активности HNF-4α с помощью жирных кислот с длинной цепью и с помощью ксенобиотических амфипатических карбоксилатов, обнаруженная в опытах по кратковременной трансфекции.
а. Модуляция активности HNF-4α с помощью жирных кислот с длинной цепью
Кратность индукции CAT-активности при трансфекции HNF-4α определяют, сравнивая CAT-активность при добавлении pSG5-HNF-4α и при добавлении плазмиды pSG5, а также в зависимости от соответствующих указанных на чертеже жирных кислот, добавленных в культуральную среду. На чертеже обобщены данные по 3-4-м независимым экспериментам для каждой жирной кислоты. Данные приведены в виде среднего значения ± среднеквадратичное отклонение (СКО9).
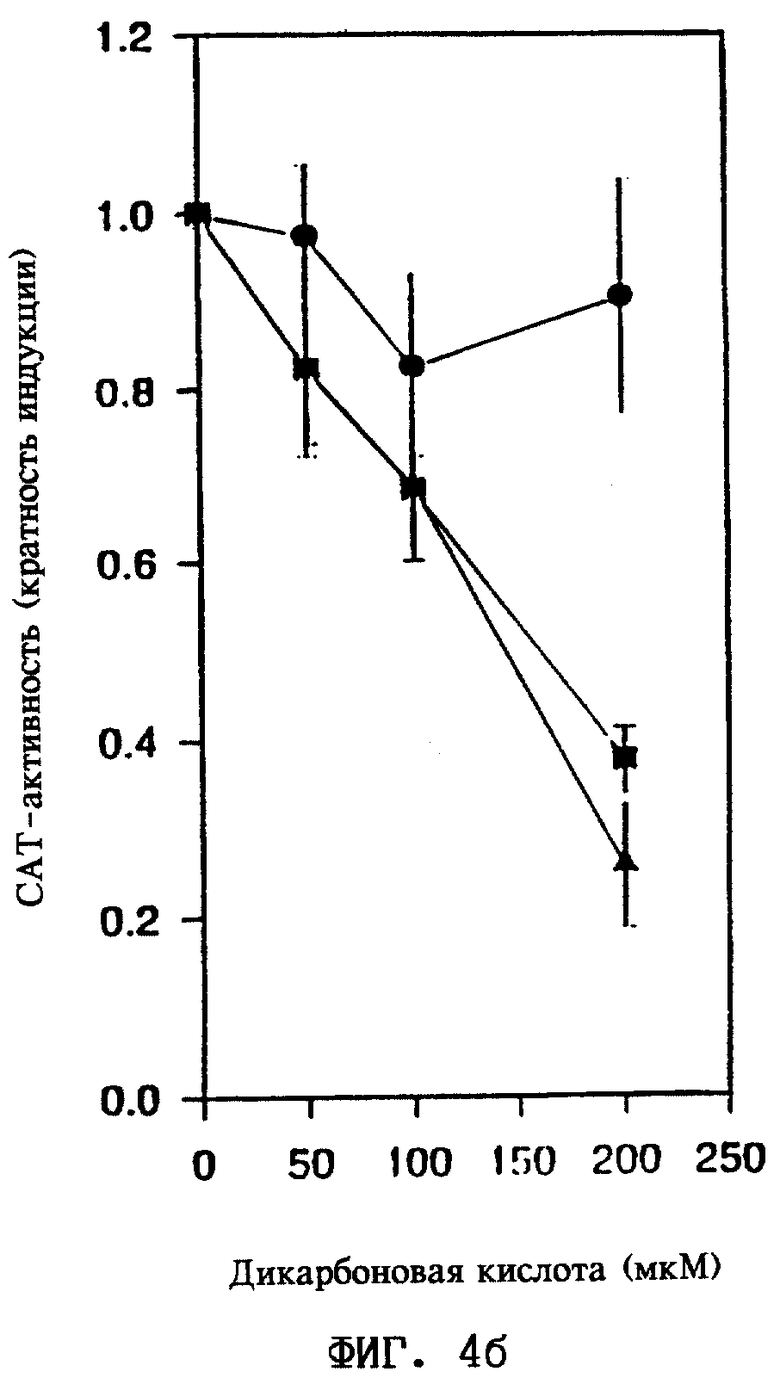
б. Суппрессия HNF-4α с помощью ксенобиотических дикарбоновых кислот
Кратность индукции определяют как CAT-активность в клетках, инкубированных с такими пролигандами, как 3,3,12,12-тетраметилтетрадеканди-оновая кислота (•), 3,3,14,14-тетраметилгексадекандионовая кислота (g) и 3,3,16,16-тетраметилоктадекандионовая кислота (5), стандартизованную по отношению к активности клеток, инкубированных без добавления пролигандов. Значения ЕС50 для вышеуказанных и для других ксенобиотических лигандов приведены ниже:
3,3,12,12-тетраметилтетрадекандионовая кислота >300 мкМ
3,3,14,14-тетраметилгексадекандионовая кислота 155 мкМ
3,3,16,16-тетраметилоктадекандионовая кислота 150 мкМ
2,2,13,13-тетраметилтетрадекандионовая кислота 230 мкМ
2,2,15,15-тетраметилгексадекандионовая кислота 150 мкМ
2,2,17,17-тетраметилоктадекандионовая кислота 150 мкМ
4,4,13,13-тетраметилгексадекандионовая кислота 150 мкМ
4,4,15,15-тетраметилоктадекандионовая кислота 150 мкМ
безафибрат 260 мкм
нафенопин 160 мкМ
индометацин 130 мкМ
Подробное описание изобретения
При создании настоящего изобретения было установлено, что жирные кислоты с длинной цепью непосредственно модулируют активность HNF-4α в отношении транскрипции путем связывания соответствующих тиоэфиров жирных ацилов и КоА с лигандсвязывающим доменом HNF-4α. Модуляция активности HNF-41 в отношении транскрипции при использовании в качестве агонистических или антагонистических лигандов тиоэфиров ацил-КоА может привести к двум совершенно независимым индуцируемым лигандами реакциям, а именно к сдвигу равновесия между олигомерной и димерной формами HNF-4α или к воздействию на присущее димерной форме HNF-4α сродство к связыванию со специфичным для нее энхансером.
В контексте настоящего описания указанные понятия имеют следующие значения.
Понятие "амфипатический карбоксилат" обозначает соединение, имеющее гидрофобный скелет и карбоксильную функцию.
Понятие "ксенобиотический" относится к соединениям, чужеродным по отношению к промежуточному метаболизму млекопитающих.
Понятие "Х-синдром" относится к синдрому, включающему некоторые или все нижеперечисленные болезни, такие как 1) дислипопротеинемия (комбинация гиперхолестеринемии и гипертриглицеридемии, низкий уровень ВПЛ-холестерина), 2) ожирение (в частности выраженное ожирение), 3) нарушение толерантности к глюкозе (НТГ), приводящее к инсулиннезависимому сахарному диабету (ИНСД), 4) эссенциальная гипертензия и 5) тромбогенные/фибринолитические дефекты.
Понятие "модуляция" относится либо к повышению, либо к понижению проявления активности HNF-4α. Модуляция HNF-4α может быть непосредственной, например, при связывании с HNF-4α, или опосредованной, например, связанной с другим механизмом, например, таким, как киназная активность. Соединения по настоящему изобретению, которые связываются с HNF-4α, в зависимости от длины цепи и/или степени насыщения могут либо активировать, либо ингибировать его связывание со специфичным для него энхансером.
Способы лечения Х-синдрома подпадают под объем настоящего изобретения. Эти способы включают введение естественных для организма или ксенобиотических амфипатических карбоксилатов. Способы ингибирования активности HNF-4α в отношении транскрипции, также подпадающие под объем изобретения, представляют собой подавление с помощью антисмыслового транскрипта, с помощью антител или с помощью любого другого метода снижения избыточной активности HNF-4α.
Методы
Рекомбинантные протеины HNF-4α
кДНК крысиного HNF-4αl (pLEN4S) [1] субклонировали в кодирующей глутатин-S-трансферазу (GST) плазмиде pGEX-2T (фирма Pharmacia) и образовавшуюся плазмиду расщепляли с помощью SmaI и АсcI и повторно лигировали, получая слитую плазмиду GST-HNF-4α(LBD). Слитую плазмиду экспрессировали в штамме Е. coll BL21(DE3) путем индукции 0,2 мМ IPTG в течение 60 мин и продукт очищали аффинной хроматографией с использованием глутатион-агарозных гранул (фирма Sigma), получая слитый протеин GST-HNF-4α(LBD), состоящий из 96-455 аминокислот последовательности HNF-4α дикого типа, слитых с GST. Полноразмерную кДНК HNF-4α1, клонированную в векторе 6His-pET11d, экспрессировали в штамме Е. coli BL21(DE3)plysS.
Анализ связывания лигандов
Рекомбинантный GST-HNF-41(LBD) (100 пмолей) или His-HNF-4α (100 пмолей) инкубировали в течение 60 мин при 22°С с [3H]-пальмитоил(16:0)-КоА (фирма American Radiolabelled Chemicals) в 100 мкл 10 мМ фосфатного буфера (рН 7,4). Добавляли в указанных концентрациях лиганды-конкуренты или только растворитель. Свободный и связанный с HNF-4α [3H]-пальмитоил(16:0)-КоА разделяли с помощью древесного угля с нанесенным на него Dowex и определяли количество связанного лиганда с помощью жидкостного сцинтилляционного счетчика. Неспецифическое связывание [3H]-пальмитоил(16:0)-КоА определяли по его связыванию с фрагментом GST или с карбонат-дегидрогеназой в качестве неспецифиченого протеина.
Анализ изменения подвижности в геле
His-HNF-4α и указанный ацил-КоА предварительно инкубировали в течение 30 мин при 22°С в ПмМ Hepes (pH 7,9), содержащем 50 мМ КСl, 1мм дитиотреитола, 2,5 мМ MgCl2, 10% глицерина, 1 мкг поли(dI-dC) в конечном объеме 20 мкл. Затем добавляли меченный с помощью 32P олигонуклеотид (0,1 нг), включающий элемент C3Р последовательности промотора аполипопротеина CIII (аро CIII) человека (-87/-66)6, и инкубацию продолжали в течение еще 15 мин. Комплексы протеин-ДНК растворяли в 5%-ном неденатурирующем полиакриламидном геле в 0,6-кратном ТВЕ и количественно оценивали путем томографии с помощью устройства Phosphor Imager.
Анализ транскрипции in vitro
Реакционная смесь содержала 20 мМ Hepes-KOH (pH 7,9), 5 мМ MgCl2, 60 мМ КСl, 8% глицерина, 2 мМ ДТТ, 1мМ 3'-О-метил-ГТФ, 10 ед. РНКазы Т1, 20 ед. RNasin, 0,5 мкг обработанной ультразвуком ДНК спермы лосося и His-HNF-4α, а также указанный тестируемый лиганд. Смесь предварительно инкубировали в течение 30 мин при 22°С, затем добавляли 10 нг контрольной матрицы pAdML200, включающей основной последний промотор аденовируса (-400/+10), связанный с не содержащей G кассетой длиной 200 пар оснований, и 200 нг тестируемой матрицы, включающей три копии элемента C3Р последовательности промотора аро CIII (-87/-66), расположенные против хода транскрипции относительно синтетического промотора бокса Хогнесса овальбумина и перед не содержащей G кассетой длиной 377 пар оснований. Смесь дополнительно предварительно инкубировали в течение 10 мин при 22°С, а затем добавляли 40 мкг ядерного экстракта HeLa и дополнительно предварительно инкубировали в течение 30 мин при 30°С. Затем добавляли 0,5 мМ АТФ, 0,5 мМ ЦТФ, 25 мкМ УТФ и 10 мкКи [α32-Р]-УТФ (т.е. 800 Ки/моль, фирма Amersham) и полную реакционную смесь инкубировали в течение 45 мин при 30°С в конечной концентрации 25 мкл. Реакцию прекращали, добавляя 175 мкл стоп-смеси (0,1 М ацетата натрия (pH 5,2), 10 мМ ЭДТК, 0,1% ДСН, 200 мкг/мл тРНК), а затем экстрагировали фенолом и осаждали этанолом. РНК ресуспендировали в образце буфера, содержащего 80% формамида и 10 мМ трис-НСl (pH 7,4), и разделяли на 5%-ном полиакриламидном геле, содержащем 7 М мочевины в ТВЕ. Путем томографии с помощью устройства Phosphor Imager количественно оценивали правильно инициированные транскрипты. Тестируемую ДНК-матрицу конструировали, встраивая в плазмиду рС2АТ19 амплифицированный с помощью ПЦР олигонуклеотид, полученный с использованием в качестве матрицы плазмиды (С3Р)3-ТК-САТ и состоящий из трех копий элемента С3Р последовательности промотора гена аро CIII (-87/-66), имеющей сайты EcoRI и SSTI на 5'- и 3'-концах соответственно. Образовавшуюся плазмиду расщепляли с помощью SphI и Sad и лигировали с синтетическим олигонуклеотидом (5'-CGAGGTCCACTTCGCTATATATTCCCCGAGCT-3'), содержащим последовательности промотора тимидинкиназы вируса герпеса простого (HSV) (-41/-29) и промотора овальбумина цыпленка (-33/-21).
Анализ с использованием трансфекции
Клетки линии COS-7, совместно трансфектированные в течение 6 ч репортерной плазмидой (С3Р)3-ТК-САТ (5 мкг) и либо экспрессирующей плазмидой pSG5-HNF-4α (0,025 мкг), либо плазмидой pSG5 (0,025 мкг), которые добавляли путем осаждения с использованием фосфата кальция, культивировали в бессывороточной среде с добавлением указанных выше жирных кислот (в виде комплексов с альбумином в молярном соотношении 6:1). К каждому осадку в качестве внутреннего контроля трансфекции добавляли экспрессирующий β-галактозидазу вектор pRSGAL (1 мкг). Конструкцию (С3Р)3-ТК-САТ получали, встраивая синтетический олигонуклеотид, включающий последовательность промотора гена аро СНГ (-87/-66) (5'-GCAGGTGACCTTTGCCCAGCGCC-3'), фланкированную сайтом рестрикции HindIII, в pBLCAT247 против хода транскрипции относительно промотора тимидинкиназы длиной 105 пар оснований. Отбирали конструкцию, содержащую три копии синтетического олигонуклеотида в прямой ориентации, и ее строение подтверждали секвенированием.
Тиоэфиры жирных ацилов и КоА
Тиоэфиры жирных ацилов и КоА получали взаимодействием свободной жирной кислоты, растворенной в безводном ацетонитриле, с 1,1’-карбонилдии-мидазолом. Реакционную смесь упаривали досуха и соответствующий конъюгат ацил-имидазол подвергали взаимодействию с одним эквивалентом восстановленного КоА, растворенного в смеси ТГФ с водой в соотношении 1:1. По завершении реакции проводили анализ методом ТСХ на пластинках из силикагеля 60Н (фирма Merck) (бутанол/уксусная кислота/вода 5:2:3). Производное в виде ацил-КоА осаждали с помощью 0,1 М НСl и осадок промывали трижды 0,1 М НСl, трижды простым эфиром, не содержащем перекиси, и трижды ацетоном. Спекторфотометрически при использовании соотношения длин волн 260/232 нм определяли содержание ацил-КоА.
Примеры
Ниже изобретение и достигаемые при его осуществлении преимущества дополнительно проиллюстрированы на примерах, которые не ограничивают его объем.
Пример 1
Тиоэфиры ацилов с длинной цепью и КоА являются лигандами для HNF-4α
Установлено, что тиоэфиры ацилов с различной длиной цепи и степенью насыщения и КоА специфично связываются с HNF-4α. Связывание оценивали либо на примере связывания с лигандсвязывающим доменом HNF-4α, слитым с глутатион-S-трансферазой (GST-HNF-4α(LBD)), либо на примере связывания с полноразмерным протеином HNF-4“, меченным шестью остатками гистидина (His-HNF-4α).
Связывание пальмитоил(16:0)-КоА с лигандсвязывающим доменом или с полноразмерными протеинами HNF-4α достигало насыщения при Кd 2,6мкМ и имело тенденцию к насыщению при соотношении 1 моль тиоэфира жирный ацил-КоА/1 моль HNF-4α (фиг.1а). Связывание с ацил-КоА оказалось специфичным, в то время как свободная жирная кислота и свободный КоА были неактивными. Связывание тиоэфиров ацилов с разной длиной цепи и с разной степенью насыщения и КоА оценивали по конкурентному связыванию радиоактивно меченного пальмитоил(16:0)-КоА с рекомбинантными GST-HNF-4α(LBD) или с His-HNF-4α (фиг.16). Связывание не было выявлено при использовании тиоэфира насыщенного жирного ацила с длиной цепи короче С12 и КоА. Однако сродство к связыванию с HNF-4α тиоэфира жирного ацила с длинной цепью и КоА не существенно зависело от длины цепи или степени насыщения соответствующих лигандов, сохраняясь в диапазоне 0,5-0,3мкМ. Специфичность связывания с HNF-4α тиоэфира жирного ацила с длинной цепью и КоА также оценивали, анализируя предполагаемое связывание пальмитоил(16:0)-КоА с рекомбинантным меченным с помощью гистидина, активированным с помощью пролифератов пероксисомы α-рецептором (His-PPARα). В отличие от результатов, полученных при использовании HNF-4α, тиоэфиры жирных ацилов с длинной цепью и КоА не связывались с PPARα или α-рецептором ретиноевой кислоты Х (RXRa). Эти результаты свидетельствуют о том, что тиоэфиры естественных для организма жирных ацилов с длинной цепью и КоА могут связываться с лигандсвязывающим доменом HNF-4α и служить в качестве специфичных для этого протеина лигандов.
Связывание тиоэфиров ацил-КоА с HNF-4α не ограничено приведенными выше в качестве примера тиоэфирами естественных для организма жирных ацилов и КоА. Так, например, связывание также обнаружено при использовании тиоэфиров ксенобиотических ацилов и КоА (RCOSKoA), где R обозначает радикал, включающий насыщенную или ненасыщенную алкильную цепь, состоящую из 10-24 атомов углерода, один или большее количество которых может быть замещено гетероатомом, где один или большее количество этих входящих в состав цепи атомов углерода или гетероатомов необязательно образуют часть кольца и где эта цепь необязательно может быть замещена (фиг.1б).
Пример 2
Модуляция активности HNF-4α с помощью тиоэфиров ацилов с длинной цепью и КоА
Влияние на активность HNF-4α связывания тиоэфиров ацилов с длинной цепью и КоА оценивали, изучая связывание HNF-4α со специфичным для него элементом C3Р последовательности промотора гена аро CIII (-87/-66)6 в присутствии тиоэфиров ацилов с различной длиной цепи, степенью насыщения и степенью замещения и КоА и без указанных тиоэфиров. Связывание определили с помощью анализа изменения подвижности в геле. Как видно на фиг.2, связывание C3Р с HNF-4ci повышалось при увеличении концентраций His-HNF-4α и активировалось при использовании тиоэфиров естественных для организма насыщенных жирных ацил с длиной цепи С12-С16 и КоА. Активация зависела от концентрации и была максимальной при добавлении миристоил(14:0)-КоА в диапазоне концентраций, необходимом для его связывания с HNF-4α. Кроме того, обнаружено, что некоторые тиоэфиры жирных ацилов и КоА, а также ксенобиотических ацилов и КоА являются истинными антагонистами HNF-4α, т.е. они ингибируют присущее ему связывание со специфичным для него энхансером. Так, в частности, инкубация HNF-4α в присутствии либо стеароил(18:0)-КоА, либо α-линоленоил(18:3)-КоА приводила к выраженному ингибированию его связывания с олигонуклеотидом С3Р (фиг.2). Аналогично этому инкубация HNF-4α в присутствии различных тиоэфиров ксенобиотических ацилов и КоА приводила к ингибированию его связывания со специфичным для него олигонуклеотидом С3Р. Таким образом, тиоэфиры естественных для организма или ксенобиотических ацилов и КоА, которые связываются с HNF-4α, в зависимости от длины цепи, степени насыщения или степени замещения могут служить агонистами, частичных агонистов или антагонистов активности HNF-4α в отношении транскрипции.
Пример 3
Модуляция индуцируемой HNF-4α активности в отношении транскрипции с помощью агонистов и антагонистов HNF-4α
Воздействие лигандов, являющихся агонистами или антагонистами для HNF-4α, также оценивали путем анализа катализируемой добавлением ядерного экстракта HeLa и индуцируемой рекомбинантным HNF-4α скорости транскрипции in vitro тестируемой матрицы, включающей не содержащую G кассету длиной 377 пар оснований под контролем промоторов, представляющих собой последовательности тимидинкиназы HSV и овальбумина цыпленка, и усиленную тремя копиями элемента C3Р промотора гена аро CIII. Способность HNF-4α активировать транскрипцию оценивали при добавлении репрезентативного тиоэфира ацила с длинной цепью и КоА и без него. Для оценки транскрипции в качестве внутренней контрольной матрицы использовали матрицу, включающую не содержащую G кассету длиной 200 пар оснований под контролем основного последнего промотора аденовируса (AdML) и лишенную энхансера HNF-4α. Как видно на фиг.3, транскрипция in vitro тестируемой матрицы возрастала в зависимости от концентрации HNF-4α, достигая насыщения при концентрации HNF-4α 200 нг. Индуцируемая HNF-4α транскрипция активировалась при добавлении пальмитоил(16:0)-КоА и ингибировалась при добавлении стеароил(18:0)-КоА, что согласуется с данными о воздействии агонистов и антагонистов HNF-4α, полученными в опытах по оценке изменения подвижности в геле. Таким образом, тиоэфиры ацилов КоА, которые связываются с HNF-4α, могут непосредственно модулировать его активность в отношении транскрипции в бесклеточной системе.
Внутриклеточное воздействие лигандов HNF-4α на опосредуемую HNF-4α транскрипцию оценивали на клетках линии COS-7, которые трансфектировали совместно вектором экспрессии HNF-4α и репортерной плазмидой CAT под контролем промотора тимидинкиназы и усиленной одной из трех копий C3Р промотора гена аро CIII. Трансфектированные клетки инкубировали в присутствии свободных жирных кислот и ксенобиотических амфипатических карбоксилатов, представляющих собой соответствующие пролиганды для HNF-4α с агонистической или антагонистической активностью. Как видно на фиг.4а, в случае, когда в культуральную среду не добавляли жирные кислоты, экспрессия усиленной C3Р репортерной плазмиды активировалась с помощью HNF-4α в 7 раз. Активация транскрипции при трансфекции HNF-4α может являться отражением активности в отношении транскрипции, присущей несвязанному с лигандом димеру HNF-4α, или может являться результатом связывания HNF-4α, активированного в эндогенных условиях ацил-КоА. Добавление в культуральную среду миристиновой(14:0) или пальмитиновой(16:0) кислоты привело к зависящей от дозы активации HNF-4α-зависимой транскрипции, в то время как стеариновая (18:0), α-линоленовая(18:3) или эйкозапентановая (20:5) кислоты подавляли транскрипцию, что согласуется с данными об агонистический или антагонистической активности соответствующих тиоэфиров жирных ацилов и КоА, полученными как в опытах по оценке изменения подвижности в геле (фиг.2), так и при анализе в бесклеточной системе транскрипции (фиг.3). Аналогично этому ингибирование активности HNF-4α в отношении транскрипции можно быть обнаружено в опытах по трансфекции (фиг.4б) при добавлении в культуральную среду ксенобиотических амфипатических карбоксилатов (RCOOH), где R обозначает радикал, представляющий собой насыщенную или ненасыщенную алкильную цепь, включающую 10-24 атома углерода, один или большее количество из которых может быть замещено гетероатомами, где один или большее количество входящих в цепь атомов углерода или гетероатомов необязательно образуют часть кольца и где указанная цепь необязательно замещена гидрокарбильным радикалом, гетероциклильным радикалом, (низш.)алкоксигруппой, (низш.)алкилом, замещенным гидроксилом, гидроксилом, карбоксилом, галогеном, фенилом, замещенным фенилом, С3-С7циклоалкилом или замещенным С3-С7циклоалкилом. Таким образом, внутриклеточная опосредуемая HNF-4α экспрессия может модулироваться с помощью естественных для организма жирных кислот, а также с помощью ксенобиотических амфипатических карбоксилатов, которые в эндогенных условиях обладают способностью превращаться в соответствующие тиоэфиры КоА (RCOSKoA). Высокоэффективными ингибиторами являются следующие соединения, в которых R замещен ω-карбоксилом: 2,2,15,15-тетраметилгексадекан-1,16-дионовая кислота, 2,2,17,17- тетраметилоктадекан-1,18-дионовая кислота, 3,3,14,14-тетраметилгексадекан-1,16-дионовая кислота, 3,3,16,16-тетраметилоктадекан-1,18-дионовая кислота, 4,4,13,13-тетраметилгексадекан-1,16-дионовая кислота, 4,4,15,15-тетраметилоктадекан-1,18-дионовая кислота. К другой группе эффективных соединений относятся следующие соединения, в которых R замещен ω-гидроксилом: 16-гидроксигексадекановая кислота, 18-гидроксиоктадекановая кислота, 16-гидрокси-2,2-диметилгексадекановая кислота, 18-гидрокси-2,2-диметилоктадекановая кислота, 16-гидрокси-3,3-диметилгексадекановая кислота, 18-гидрокси-3,3-диметилоктадекановая кислота, 16-гидрокси-4,4-диметилгексадекановая кислота, 18-гидрокси-4,4-диметилоктадекановая кислота. Еще одна группа несколько менее эффективных соединений включает аналоги клофибриновой кислоты (фибраты) или нестероидные противовоспалительные лекарства. Общее оказываемое действие может определяться главным образом композицией ядерных тиоэфиров ацил-КоА и агонистической/антагонистической активностью каждого из них при связывании с HNF-4α.
Пример 4
Физиологические механизмы действия
Ингибирование активности HNF-4α в отношении транскрипции с помощью естественных для организма или ксенобиотических амфипатических карбоксилатов, которые в эндогенных условиях обладают способностью превращаться в соответствующие тиоэфиры КоА, может служить терапевтическим целям при лечении болезней, которые вызываются и/или развиваются при сверхэкспрессии контролируемых HNF-4α генов. Действие определенного амфипатического карбоксилата в качестве ингибитора активности HNF-4α в отношении транскрипции может зависеть в первую очередь от способности, присущей соответствующему ему тиоэфиру КоА, действовать в качестве антагониста HNF-4α. В настоящее время нельзя предсказать, какие из амфипатических карбоксилатов, обладающих способностью превращаться в эндогенных условиях в соответствующие тиоэфиры КоА, могут рассматриваться как истинные антагонисты HNF-4α. Так, например, доказано, что миристоил(14:0)-КоА или пальмитоил(16:0)-КоА являются активаторами способности HNF-4α активировать транскрипцию, в то время как следующий гомолог в этой серии, т.е. стеароил(18:0)-КоА, является истинным антагонистом. Однако следует отметить, что частичные агонисты могут вызывать выраженное ингибирование активности HNF-4α при замещении в эндогенных условиях сильными агонистами HNF-4α или при конкуренции с более активными агонистами за связывание с HNF-4α.
Общая активность амфипатического карбоксилата в качестве ингибитора активности HNF-4α в отношении транскрипции in vivo может зависеть не только от присущей соответствующему ему тиоэфиру КоА способности действовать в качестве антагониста HNF-4α, но также зависеть от конкретного типа клеток и превалирующей композиции ядерных тиоэфиров жирных ацилов и КоА. Характеристики этой композиции определяются профилем питательной/фармакологической доступности соответствующих кислот, доступностью каждой из них для КоА-тиоэтерификации, а также доступностью соответствующих ацил-КоА для гидролиза ацил-КоА-гидролазами, способностью к этерификации с образованием липидов, к окислению в соответствующие продукты, к элонгации, десатурации или к связыванию с другими ацил-КоА-связывающими протеинами. Кроме того, эндогенные ацил-КоА, образовавшиеся в результате КоА-тиоэтерификации амфипатических карбоксилатов, не относящихся к жирным кислотам (например ретиноевой кислоты, простагландинов, лейкотриенов и др.), могут связываться с HNF-4α и модулировать его активность в качестве агонистов или антагонистов. Полученное действие может также зависеть от дополнительных ядерных факторов, которые могут влиять на равновесие между олигомерной и димерной формами HNF-4α, на сродство связывания HNF-4α со специфичным для него энхансером или на взаимодействие HNF-4α с протеинами комплекса инициации транскрипции. В частности, поскольку HNF-4α и активируемый пероксисомальными активаторами рецептор (PPAR) имеют сходные консенсусные последовательности DR-1, а HNF-4α так же, как и PPAR, в большей степени может активироваться свободными жирными кислотами с длинной цепью, чем их соответствующими КоА-тиоэфирами, активность, характерная для определенных ацил-КоА и опосредованно влияющая на HNF-4α, может оказаться аналогичной активности, обнаруженной при активации PPAR соответствующей свободной кислотой, либо может быть обнаружен антагонизм.
Несмотря на указанную выше гипотетичность, агонистический/антагонистический профиль лигандов для HNF-4α из группы ацил-КоА, продемонстрированный в приведенных в настоящем описании примерах, может способствовать разработке молекулярной основы воздействий, выявленных in vivo при использовании пищевых жирных кислот, которые затрагивают некоторые из регулируемых HNF-4α генов. Жирный ацил с длинной цепью состоит из пищевого жира, на долю которого приходится 30-40% калорий, поглощаемых с пищей в западных странах. Помимо их роли в качестве субстратов вследствие того, что они наиболее легко окисляются с выделением энергии или превращаются в результате этерификации в триглицериды и фосфолипиды, необходимые для образования жировой ткани и клеточных мембран соответственно, некоторые пищевые жирные кислоты уже давно признаны в качестве пищевых модуляторов возникновения и развития рака [7], атерогенза [8], дислипопротеинемии [9], устойчивости к инсулину [10,11], гипертензии [12], дефектов свертываемости крови и фибринолиза [13], воспаления, иммунодефицита и других болезней. Эти ранее необъяснимые воздействия в настоящее время могут быть расшифрованы с учетом данных о влиянии соответствующих ацил-КоА на активность HNF-4α в отношении транскрипции, что приводит к модуляции экспрессии генов, участвующих в инициации и развитии вышеуказанных патологий. Специфические воздействия пищевых жирных кислот с длинной цепью на липиды крови и на свертываемость крови следует рассматривать с свете точно доказанного воздействия HNF-4α на гены, кодирующие протеины, которые участвуют в метаболизме липопротеинов (аполипопротеины AI, АII, В, CIII, микросомальный протеин переноса триглицеридов) и в свертывании крови (факторы IV, IX, X). Фактически точно доказанное увеличение содержания в плазме ОВПЛ-, НПЛ- и ВПЛ-холестерина, вызванное пищевыми насыщенными жирными кислотами с длиной цепи С12-С16 в целом и миристиновой кислотой в частности, согласуется с активацией HNF-4α под воздействием соответствующих тиоэфиров насыщенных ацилов и КоА и с отсутствием эффекта под воздействием тиоэфиров насыщенных ацилов и КоА с длиной цепи меньше С12. Неожиданное снижение уровня липидов в крови при использовании насыщенной стеариновой (18:0) кислоты также может быть связано с антагонистическим действием стеароил(18:0)-КоА на активность HNF-4α. Аналогично этому снижение уровня липидов под воздействием моно- и полиненасыщенных жирных кислот [9], связанное с замещением ими насыщенных пищевых жирных кислот, согласуется с активностью тиоэфиров поли- или мононенысыщенных ацилов и КоА по сравнению с тиоэфирами нысыщенных жирных ацилов и КоА, что также дополняется непосредственным ингибированием HNF-4α с помощью линоленоил(18:3)-КоА, эйкозапентаеноил (20:5)-КоА или докозагексаеноил(22:6)-КоА. Кроме того, повышение свертываемости крови, индуцируемое насыщенными пищевыми жирными кислотами с длиной цепи С12-С16 и коррелирующее с соответствующим повышением фактора VII, понижение свертываемости крови, индуцируемое полиненысыщенными пищевыми жирными кислотами, а также неожиданно установленное понижение содержания фактора VII и свертываемости крови, специфично индуцируемое пищевой стеариновой(18:0) кислотой, аналогичным образом могут быть обусловлены воздействием соответствующих тиоэфиров жирных ацилов и КоА на активность HNF-4α, что приводит к модуляции экспрессии контролируемых HNF-4α генов, кодирующих зависимые от витамина К факторы свертывания крови.
Кроме того, модуляция транскрипции контролируемых HNF-4α генов ксенобиотическими амфипатическими карбоксилатами, которые в эндогенных условиях могут быть этерифицированы с образованием соответствующих им тиоэфиров КоА и которые действуют в качестве агонистов или антагонистов HNF-4α, может являться фармакологическим терапевтическим механизмом болезней, возникающих и развивающихся в результате сверхэкспрессии контролируемых HNF-4α генов. Возможность применения ксенобиотических замещенных амфипатических карбоксилатов следует рассматривать в свете обобщенной информации, полученной с помощью моделирования на животных [14-17], которая касается их фармакологической характеристики в отношении изменения течения дислипопротеинемии, ожирения, устойчивости к инсулину и атеросклероза, т.е. болезней, связанных со сверхэкспрессией некоторых контролируемых HNF-4α генов. Терапевтическая эффективность этих лекарственных средств может быть обусловлена ингибированием активности HNF-4α в отношении транскрипции, как это описано в примерах, приведенных в настоящем описании.



В заявке описаны терапевтически эффективные соединения, представляющие собой амфипатический карбоксилат формулы R -СООН либо соль, эфир или амид такого соединения, где R обозначает насыщенную или ненасыщенную алкильную цепь, включающую 10-24 атома углерода, один или большее количество из которых может быть замещено гетероатомами, где один или большее количество входящих в цепь атомов углерода или гетероатомов необязательно образуют часть кольца и где указанная цепь необязательно замещена гидрокарбильным радикалом, гетероциклильным радикалом, (низш.) алкоксигруппой, замещенным гидроксилом (низш.)алкилом, гидроксилом, карбоксилом, галогеном, фенилом или замещенным гидроксигруппой, (низш.)алкилом, (низш.)алкоксигруппой, (низш.)алкенилом или (низш.)алкинилом фенилом, С3-С7циклоалкилом или замещенным гидроксигруппой, (низш.)алкилом, (низш.)алкоксигруппой, (низш.)алкенилом или (низш.)алкинилом С3-С7циклоалкилом, причем указанный амфипатический карбоксилат обладает способностью в эндогенных условиях превращаться в соответствующий тиоэфир кофермента А. Изобретение относится также к модуляции активности HNF-4α и к способу лечения заболевания или синдрома путем введения терапевтически эффективного количества амфипатического карбоксилата. Изобретение объясняет модуляцию экспрессии генов, участвующих в инициации и развитии патологий у человека. 3 н. и 24 з.п. ф-лы, 4 ил., 1 табл.
| Способ лечения аденомы предстательной железы | 1981 |
|
SU1159578A1 |
| Прибор для охлаждения жидкостей в зимнее время | 1921 |
|
SU1994A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Способ модулирования для радиотелефонии | 1923 |
|
SU409A1 |
| J | |||
| Biol | |||
| Chem | |||
| Топка с качающимися колосниковыми элементами | 1921 |
|
SU1995A1 |
| Машина для добывания торфа и т.п. | 1922 |
|
SU22A1 |
Авторы
Даты
2004-11-10—Публикация
1998-06-23—Подача