Изобретение относится к химии гетероциклических соединений, а именно к замещенным 1-(пиридинил-3)-2-азолилэтанолам общей формулы I
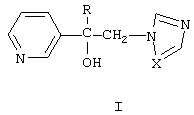
где R означает атом водорода, неразветвленный или разветвленный алкил с числом атомов углерода от одного до восьми, циклоалкил с числом атомов углерода от трех до восьми, циклоалкилалкил с общим числом атомов от четырех до десяти, алкилциклоалкил с общим числом атомов от четырех до десяти, Х означает атом азота или СН-группу, которые обладают фунгицидной активностью и могут найти применение в качестве сельскохозяйственных, промышленных, медицинских или ветеринарных фунгицидов.
Известны 1-пиридинил-2-имидазолилэтанолы общей формулы II, где R1 означает атом водорода, алкильную группу или атом галогена, R2 означает замещенный или незамещенный тиенил или замещенный или незамещенный фенил, R3 означает атом водорода или метильную группу [Заявка ФРГ №3345813 А1, кл. C 07 D 401/06, 1983], которые обладают антидепрессантной активностью и могут быть использованы в медицине

Известны 2-триазолилэтанолы общей формулы III, их соли с кислотами и комплексы с металлами, где R1 означает алкил, циклоалкил или фенил, R2 означает фенил или бензил, которые обладают фунгицидной активностью [Пат. США №4623654, кл. A 01 N 43/653, 1984]

Известна реакция присоединения к оксиранам имидазола и триазола с образованием замещенных 2-азолилэтанолов-1, которая проводится в среде высококипящего апротонного растворителя, например, N-метилпирролидона, диметилформамида или диметилсульфоксида, при 100-150°С в присутствии воды или без нее [J.M.Bentley, R.V.Jones, P.J.Wareham. A general anionic mechanism for thermodinamic control of regioselectivity in N-alkylation of heterocycles //Tetrahedron Letters. 1989. Vol. 30. No. 30. P. 4013-4016].
В зависимости от физико-химических свойств препарата, его назначения и способа использования пестициды применяют в виде различных препаративных форм (композиций), например в виде порошков, гранулированных препаратов, микрокапсулированных препаратов, растворов в воде и органических растворителях, смачивающихся порошков, концентратов эмульсий, мазей и мастик. Препаративные формы помимо основного действующего вещества содержат различные наполнители и добавки, характер которых определяется конкретными условиями применения такой формы. Так, растворы пестицидов в воде или органических растворителях, применяющиеся для опрыскивания растений, внесения в почву различными методами, пропитки материалов содержат действующее вещество и растворитель, но могут также содержать регуляторы кислотности, поверхностно-активные вещества, красители, умягчители воды, синергические добавки. Известен препарат ДНОК, который применяют в виде водного раствора для опрыскивания садов и виноградников в концентрации 0,1-0,2% [Пестициды и регуляторы роста растений /Н.Н.Мельников, К.В.Новожилов, С.Р.Белан. - М.: Химия, 1995, с.9-26, 242].
Техническая задача, решаемая настоящим изобретением, состоит в расширении ассортимента фунгицидов для более эффективной борьбы с вредоносными грибами.
Для решения этой задачи синтезируют замещенные 1-(пиридинил-3)-2-азолилэтанолы общей формулы I, обладающие фунгицидной активностью.
Согласно изобретению замещенные 1-(пиридинил-3)-2-азолилэтанолы формулы I получают взаимодействием замещенных 2-(пиридинил-3)оксиранов формулы IV с триазолом или имидазолом в присутствии твердого гидроксида щелочного металла в среде высококипящего полярного апротонного растворителя, например, N-метилпирролидона, диметилформамида или диметилсульфоксида, при 100-150°С в присутствии воды или без нее
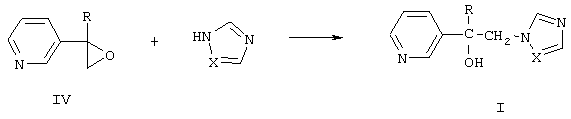
где R и Х имеют те же значения, что и в формуле I.
Замещенные 2-(пиридинил-3)оксираны формулы IV получают взаимодействием пиридинилкетонов общей формулы V с солями триметилсульфония в диметилсульфоксиде или диметилсульфиде в присутствии сильного основания, например, трет-бутилата калия, трет-амилата натрия или гидрида натрия или в межфазных условиях при температуре от -10 до +5°С
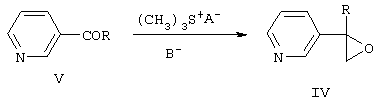
где R означает то же, что и в формуле I, А- означает анион кислоты, В-означает основание.
Для других субстратов такая реакция известна [E.J.Corey, M.Chaykovsky. Dimethyloxosulfonium methylide ((СН3)2SOСН2) and dimethylsulfonium methylide ((CH3)2SCH2). Formation and application to organic syntheses //Journal of the American Chemical Society. 1965. Vol. 87. No. 6. P. 1353-1364].
Пиридинилкетоны формулы V могут быть получены взаимодействием 3-цианопиридина с металлорганическими соединениями [P.S.Teague, A.R.Ballentine. Some pyridylhydantoins //J. Am. Chem. Soc. 1953. Vol. 75. P. 3429] или металлированного пиридина с производными карбоновых кислот:
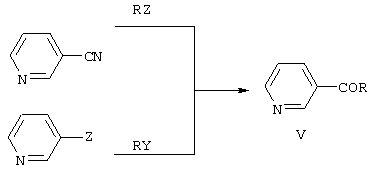
где R означает то же, что и в формуле I, Y означает группу CN, CON(CH3)2, COOAlk, COHal, Z означает Li, MgHal, CdHal.
Изобретение может быть проиллюстрировано следующими примерами.
Пример 1. (Пиридинил-3)циклогексилкетон. К охлажденному до -70°С раствору 15.8 г (0.1 моль) 3-бромпиридина в 60 мл абсолютного эфира при перемешивании приливают 65 мл 15%-ного раствора BuLi (0.1 моль), реакционную массу перемешивают 10 мин и при перемешивании прикапывают раствор 15.5 г (0,1 моль) диметиламида циклогексанкарбоновой кислоты в 100 мл абсолютного ТГФ. Охлаждение снимают и оставляют смесь на ночь. Затем смесь упаривают в вакууме, добавляют 50 мл насыщенного раствора NH4Cl и экстрагируют Et2O (3х100 мл). Эфирный экстракт промывают рассолом, сушат над MgSO4, отгоняют растворитель и перегоняют продукт в вакууме. Получают 13.7 г (72%) (пиридинил-3)циклогексилкетона, т.кип.140-155°С / 1 мм рт.ст. Спектр ЯМР 1Н (DМSO-d6, δ, м.д., J, Гц): 1,15-2.55 (м, 11Н, СН циклогекс.), 7,52 (дд, 1H, СН пирид., J1=0,4; J2=0,2), 8,25 (д, 1Н, СН пирид., J=0,4), 8,73 (д, 1Н, СН пирид., J=0,20), 9,10 (с, 1Н, СН пирид.).
Пример 2. 1-(Пиридинил-3)-3,3-диметилбутанон-1. Выход 33%, т.кип.118-123°С / 1 мм рт. ст. Спектр ЯМР 1Н (DMSO-d6, δ, м.д., J, Гц): 1,05 (с, 9Н, СН3), 2,95 (с, 2Н, СН2), 7,55 (дд, 1Н, СН пирид., J1=0,4, J2=0,2), 8,30 (д, 1Н, СН пирид., J=0,4), 8,75 (д, 1Н, СН пирид., J=0,20), 9,12 (с, 1Н, СН пирид.).
Пример 3. 2-(Пиридинил-3)-2-циклогексилоксиран. К смеси 9.45 г (0.05 моль) пиридинилцклогексилкетона, 14.28 г (0.07 моль) иодида триметил-сульфония и 31 мл ДМСО при охлаждении до 0°С добавляют по каплям в течение 30 мин раствор 4.63 г (0.063 моль) трет-бутоксида калия в 31 мл ДМСО. Смесь перемешивают 15 мин, охлаждают в смеси льда и соли и в течение 30 мин приливают по каплям 150 мл воды. Продукт извлекают СНСl3 (3х30 мл). Экстракт промывают водой (3×30 мл) и 20 мл рассола. Раствор сушат над MgSO4 и растворитель отгоняют в вакууме. Получают 8.05 г (85,2%) оксирана. Спектр ЯМР 1H (DMSO-d6, δ, м.д., J, Гц): 0,75-1,75 (м, 11 Н, СН циклогексильн.), 2,70-3,10 (АВ-система, 2 Н, CH2, J=8,0), 7,38 (дд, 1 Н, 5-СН пирид, J1=0,42, J2=0,21), 7,66 (дт, 1 Н, 4-СН пирид., J1=0,42, J2=0,1), 8,45 (дд, 1 Н, 6-СН пирид., J1=0,21, J2=0,1), 8,47 (д, 1 Н, 2-СН пирид., J=0,1).
Пример 4. 2-(Пиридинил-3)-2-(2,2-диметилпропил)оксиран. Выход 61%. Спектр ЯМР 1Н (DMSO-d6, δ, м.д., J, Гц): 0,75 (с, 9Н, СН3), 98 (с, 2Н, СН2), 2,90 (АВ-система, 2Н, СН2, J=4,8), 7,37 (дд, 1Н, СН пирид., J1=0,4, J2=0,2), 7,83 (д, 1H, СН пирид., J=0,4), 8,5 (д, 1Н, СН пирид., J=0,2), 8,67 (с, 1Н, СН пирид.).
Пример 5. 1-(3-Пиридинил)-2-(1,2,4-триазол-1-ил)-1-циклогексилэтанол (1). К раствору 1.68 г (8.3 ммоль) 2-(3-пиридинил)-2-циклогексилоксирана и 0.57 г (8.3 ммоль) триазола в 5.63 мл ДМФА прибавляют 0.033 мл воды, 0.11 г гидроксида натрия и перемешивают в течение 4 ч при температуре 120°С. Реакционную массу охлаждают и выливают в 40 мл воды. Выпавшие кристаллы отфильтровывают, промывают водой и перекристаллизовывают из толуола. Получают 1,74 г (77%) продукта, т.пл. 101-102°С. Спектр ЯМР 1Н (DMSO-d6, δ, м.д., J, Гц): 0,80-1,95 (м, 11 Н, СН циклогекс.), 4,70-5,40 (АВ-система, 2 Н, CH2, J=14,2), 4,7 (с, 1 Н, ОН), 7,26 (дд, 1 Н, СН-пирид., J1=0,38, J2=0,30), 7,69 (дт, 1 Н, СН пирид., J1=0,38, J2=0,07), 7,76 (с, 1 Н, СН триаз.), 8,21 (с, 1 Н, СН триаз.), 8,37 (дд, 1 Н, СН пирид., J1=0,2, J2=0,07), 8,54 (д, 1 Н, СН пирид., J=0,07).
Пример 6. 1-(3-Пиридинил)-2-(имидазол-1-ил)-1-циклогексилэтанол (2). Т. пл. 134-135°С. Спектр ЯМР 1H (DMSO-d6, δ, м.д., J, Гц): 0,80-1,95 (м, 11 Н, СН циклогексильн.), 4,45 (АВ-система, 2 Н, CH2, J=1,89), 5,31 (с, 1H, ОН), 6,63, 6,82 (оба с, по 1 Н, СН имид.), 7,25 (дд, 1 Н, 5-СН пирид., J1=0,42, J2=0,28), 7,32 (с, 1 Н, СН имид.), 7,72 (д, 1 Н, 4-СН пирид., J=0,42), 8,36 (д, 1 Н, 6-СН пирид., J=0,28), 8,56 (с, 1 Н, 2-СН пирид.).
Пример 7. 1-(2,2-Диметилпропил)-1-(3-пиридинил)-2-(1,2,4-триазол-1-ил)этанол (3). Выход 79%, т.пл. 92-94°С. Спектр ЯМР 1H (DMSO-d6, (м.д., J, Гц): 0,6 (с, 9Н, СН3), 1,9 (АВ-система, 2Н, СН2 алиф., J=6;43), 4,45 (АВ-система, 2Н, СН2О, J=2,14), 5,38 (с, 1Н, ОН), 7,24 (дд, СН пирид, J1=0,48, J2=0,2), 7,73 (с, 1Н, СН триаз.), 7,75 (д, 1Н, СН пирид, J=0,48), 8,18 (с, 1Н, СН триаз.), 8,35 (д, 1Н, СН пирид., J=0,2), 8,60 (с, 1Н, СН пирид.).
Пример 8. 1-(2,2-Диметилпропил)-1-(3-пиридинил)-2-(имидазол-1-ил)этанол (4). Выход 86%, т. пл. 195-196°С. Спектр ЯМР 1H (DMSO-d6, δ, м.д., J, Гц): 0,68 (с, 9Н, СН3), 1,85 (АВ-система, 2Н, СН2-неопентил, J=6,67), 4,20 (АВ-система, 2Н, СН2, J=1,48), 5,3 (с, 1Н, ОН), 6,65 (с, 1Н, СН-имидазола), 6,75 (с, 1Н, СН-имидазола), 7,23 (с, 1Н, СН-имидазола), 7,27 (дд, 1Н, СН-пиридина, J1=0,47, J2=0,26), 7,77 (д, 1Н, СН-пиридина, J=0,47), 8,32 (д, 1Н, СН-пиридина, J=0,26), 8,62 (с, 1Н, СН-пиридина)
Пример 9. Испытания на биологическую активность соединений проводили в экспериментах in vitro. В расплавленный сахарозно-картофельный агар добавляли испытуемое вещество в виде композиции, содержащей 0,377% действующего вещества, остальное - ацетон, по 1 мл на 100 мл агара. При этом получали агаровую среду, содержащую 30 мг/л испытуемого соединения. В среду для контроля добавляли чистый ацетон в том же количестве. Приготовленные таким способом среды разливали в чашки Петри, охлаждали и на поверхность затвердевшего агара высевали кусочки мицелия грибов, после чего чашки инкубировали в течение 3 суток при 25±0,5°С. Подавление роста мицелия вычисляли в процентах к необработанному контролю. В качестве эталона использовали коммерческий фунгицид триадимефон в той же концентрации. Результаты испытаний представлены в таблице.

| название | год | авторы | номер документа |
|---|---|---|---|
| ЗАМЕЩЕННЫЕ 1-(ПИРИДИНИЛ-2)-2-АЗОЛИЛЭТАНОЛЫ, ИХ СПОСОБ ПОЛУЧЕНИЯ И ФУНГИЦИДНАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2004 |
|
RU2301227C2 |
| ЗАМЕЩЕННЫЕ 1-(ПИРИДИНИЛ-3)-2-ФЕНОКСИЭТАНОЛЫ-1, ИХ СПОСОБ ПОЛУЧЕНИЯ И ФУНГИЦИДНАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2003 |
|
RU2248351C1 |
| 1-(ПИРИДИНИЛ-2)-2-АЗОЛИЛ-1-(ФТОРФЕНИЛ)ЭТАНОЛЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ФУНГИЦИДОВ | 2004 |
|
RU2267483C2 |
| НОВЫЕ 1-β-D-РИБОФУРАНОЗИЛ-3-(5-ЗАМЕЩЕННЫЕ-1,2,4-ОКСАДИАЗОЛ-3-ИЛ)-1,2,4-ТРИАЗОЛЫ, ОБЛАДАЮЩИЕ ПРОТИВОВИРУСНЫМИ СВОЙСТВАМИ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2016 |
|
RU2629360C1 |
| ПРИМЕНЕНИЕ 1-ПИРИДИНИЛ-2-АЗОЛИЛ-1-ФЕНИЛЭТАНОЛОВ В КАЧЕСТВЕ ФУНГИЦИДОВ | 2003 |
|
RU2237406C1 |
| Анелированные 9-гидрокси-1,8-диоксо-1,3,4,8-тетрагидро-2Н-пиридо[1,2-a]пиразин-7-карбоксамиды - ингибиторы интегразы ВИЧ, способы их получения и применения | 2019 |
|
RU2717101C1 |
| ДИГИДРОПИРИДОФТАЛАЗИНОНОВЫЕ ИНГИБИТОРЫ ПОЛИ(АДФ-РИБОЗА)ПОЛИМЕРАЗЫ | 2009 |
|
RU2514937C2 |
| ПРОТИВОТУБЕРКУЛЕЗНЫЕ АГЕНТЫ, ПРЕДСТАВЛЯЮЩИЕ СОБОЙ 3,7-ДИЗАМЕЩЕННЫЕ [1,2,4]ТРИАЗОЛО[1,5-b][1,2,4,5]ТЕТРАЗИНЫ | 2022 |
|
RU2802300C1 |
| ПРОТИВОВИРУСНЫЕ СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ВИЧ ИНФЕКЦИИ | 2021 |
|
RU2780103C1 |
| Способ получения 3-азолилпропанолов | 2022 |
|
RU2786670C1 |
Описываются замещенные 1-(пиридинил-3)-2-азолилэтанолы общей формулы I
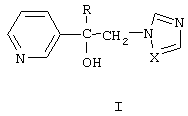
где R = алкил или циклоалкил, Х = N или СН, которые получают взаимодействием оксиранов формулы II с триазолом или имидазолом в присутствии основания при 100—150°С, и фунгицидная композиция на их основе
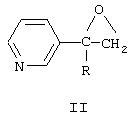
Технический результат заключается в получении соединений, активных в отношении вредоносных грибов. 3 н.п. ф-лы, 1 табл.
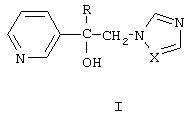
где R означает неразветвленный или разветвленный алкил с числом атомов углерода от одного до восьми, циклоалкил с числом атомов углерода от трех до восьми;
Х означает атом азота или СН-группу.
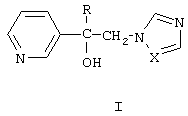
где R означает неразветвленный или разветвленный алкил с числом атомов углерода от одного до восьми, циклоалкил с числом атомов углерода от трех до восьми;
Х означает атом азота или СН-группу,
заключающийся в том, что замещенный 2-(пиридинил-3)оксиран формулы II
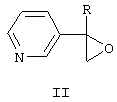
где R означает неразветвленный или разветвленный алкил с числом атомов углерода от одного до восьми, циклоалкил с числом атомов углерода от трех до восьми,
вводят в реакцию с триазолом или имидазолом в присутствии твердого гидроксида щелочного металла в среде высококипящего полярного апротонного растворителя при 100-150°С в присутствии воды или без нее.
| US 4623654, 18.11.1986.US 4657920, 14.04.1987.EP 0129186 A2, 27.12.1984.RU 2039050 C1, 09.07.1995.RU 99108250 A1, 20.02.2001. |
Авторы
Даты
2004-11-20—Публикация
2003-06-26—Подача