Настоящее изобретение относится к новым стероидным соединениям, предназначенным как для систематического, так и для несистематического применения, а также композициям на их основе, для использования в состоянии окислительного стресса и/или эндотелиальных дисфункций. Более конкретно, изобретение относится к соединениям стероидной структуры, обладающим противовоспалительной, иммунодепрессивной и ангиостатической активностью (так называемые противовоспалительные стероиды) или желудочно-кишечной активностью.
Соединения в соответствии с настоящим изобретением полезны для терапевтического лечения таких патологических состояний, при которых обычно используют стероидные продукты, но они обладают улучшенными свойствами с точки зрения переносимости и/или эффективности.
Под окислительным стрессом подразумевается возникновение свободных радикалов или радикальных соединений, которые наносят повреждения как клеткам, так и окружающим их тканям (Pathophysiology: the biological basis for disease in adults and children, McCance&Huether, 1998, pp.48-54).
Под эндотелиальными дисфункциями подразумевают дисфункции, относящиеся к сосудистому эндотелию. Известно, что повреждение сосудистого эндотелия является одной из важнейших причин, которые могут вызвать серию патологических процессов, затрагивающих различные органы и системы организма, как описано далее (Pathophysiology: the biological basis for disease in adults and children, McCance&Huether, 1998, p.1025).
Известно, что окислительный стресс и/или эндотелиальные дисфункции связаны с различными патологиями, как описано далее. Окислительный стресс также может быть обусловлен токсичностью большого числа различных лекарственных веществ, что значительно сказывается на эффективности их действия.
Указанные патологические явления имеют хронический характер, подрывающий силы организма, и очень часто являются типичными для людей пожилого возраста. Как уже было сказано, при указанных патологических состояниях применяемые лекарственные вещества обладают заметным негативным действием.
Можно привести следующие примеры патологических состояний, обусловленных окислительным стрессом и/или эндотелиальными дисфункциями или характерных для людей пожилого возраста.
- Для сердечно-сосудистой системы: миокардиальная и сосудистая ишемия в целом, гипертония, инсульт, атеросклероз и т.д.
- Для соединительной ткани: ревматоидный артрит и связанные с ним воспалительные заболевания и т.д.
- Для легочной системы: астма и связанные с ней воспалительные заболевания, и т.д.
- Для желудочно-кишечной системы: язвенные и неязвенные диспепсии, кишечные воспалительные заболевания и т.д.
- Для центральной нервной системы: болезнь Альцгеймера и т.д.
- Для мочеполовой системы: импотенция, недержание.
- Для кожных покровов: экзема, нейродерматит, угри.
- Инфекционные заболевания в целом (Schwarz, Brady "Oxidative stress during viral infection: a review". Free Radical Biol. Med. 21/5, 641-649, 1996).
Далее, сам процесс старения может рассматриваться как действительное патологическое состояние (Pathophysiology: the biological basis for disease in adults and children, pp.71-77).
Известные лекарственные вещества при введении их пациентам, имеющим патологии, связанные с окислительным стрессом и/или эндотелиальными дисфункциями, проявляют сниженную эффективность и/или повышенную токсичность.
Это происходит, например, в случае стероидов.
Исследования лекарственных веществ направлены на поиск новых молекул, имеющих улучшенный терапевтический индекс (соотношение эффективность/токсичность) или пониженное соотношение риск/полезное действие, в том числе и для указанных выше патологических состояний, при которых терапевтический индекс значительного числа лекарственных веществ оказывается низким. Фактически, при указанных выше состояниях окислительного стресса и/или эндотелиальных дисфункций многие лекарственные вещества проявляют низкую активность и/или высокую токсичность.
Хорошо известно, что при терапевтическом лечении воспалительных заболеваний для фармакологического воздействия в первую очередь выбирают стероиды. Этот класс лекарственных веществ, среди которых можно упомянуть, например, гидрокортизон, кортизон, преднизон, преднизолон, флюдрокортизон, дезоксикортикостерон, метилпреднизолон, триамцинолон, параметазон, бетаметазон, дексаметазон, триамцинолона ацетонид, флуоцинолона ацетонид, беклометазон, ацетоксипрегнелон, и т.д., оказывает заметное фармакотоксическое влияние на различные органы, и поэтому как их клиническое применение, так и перерывы в приеме приводят к ряду побочных эффектов, некоторые из которых могут быть очень серьезными. См., например, Goodman&Gilman, "The Pharmaceutical Basis of Therapeutics", 9-е изд., стр.1459-1465, 1996.
Среди указанных токсических эффектов следует отметить воздействие на костную ткань, что приводит к изменению клеточного метаболизма и повышению вероятности возникновения остеопороза; воздействие на сердечно-сосудистую систему, приводящее к гипертонии; воздействие на желудочно-кишечный аппарат, приводящее к желудочным расстройствам. См., например, Martindale "The Extrapharmacopoeia, 30-е изд., стр.712-723, 1993.
К классу стероидных лекарственных веществ также принадлежат желчные кислоты, применяемые в терапии заболеваний печени и при желчных коликах. Урсодезоксихолевая кислота также применяется при некоторых расстройствах функций печени (дирроз печени желчного происхождения и т.д.). Переносимость этих лекарственных веществ значительно ухудшается при наличии желудочно-кишечных осложнений (хронические повреждения печени, язва желудка, кишечные воспаления и т.д.). В случае желчных кислот окислительный стресс также заметно влияет на эффективность действия лекарственного вещества: как эффективность, так и переносимость хенодезоксихолевой и урсодезоксихолевой кислот значительно снижаются. Было обнаружено, что особенно усиливается нежелательное воздействие на печень. Среди стероидных соединений также можно упомянуть эстрогены, применяемые для лечения дислипидемий, гормональных заболеваний, опухолей женских органов. Упомянутые стероиды также оказывают вышеуказанное побочное воздействие, особенно на печень.
Исходя из вышеописанного уровня техники, представляется практически невозможным отделить терапевтическую активность от побочных эффектов (см. Goodman&Gilman, "The Pharmaceutical Basis of Therapeutics" 9-е изд., стр.1474, 1996).
Стероидные соединения полностью отличаются от противовоспалительных нестероидных соединений с химической, фармакологической и биохимической точек зрения, так как фармакотоксикологический механизм действия нестероидных противовоспалительных продуктов основан на ингибировании одной или более циклооксигеназ (ЦОГ), тогда как стероиды не влияют на ЦОГ и обладают более сложным фармакотоксикологическим механизмом действия, до сих пор не выясненным окончательно.
Действительно, хорошо известно, что эти две группы лекарственных веществ относятся к различным фармацевтическим классам.
Таким образом, существует необходимость разработки доступных стероидов, обладающих улучшенным терапевтическим воздействием, т.е. обеспечивающих и пониженную токсичность, и/или повышенную эффективность, чтобы их можно было вводить пациентам при патологических состояниях окислительного стресса и/или эндотелиальных дисфункций, без проявления недостатков, характерных для лекарственных веществ, известных из уровня техники.
Неожиданно было обнаружено, что вышеупомянутые технические проблемы, выявленные при введении стероидных лекарственных веществ пациентам, страдающим от окислительного стресса и/или эндотелиальных дисфункций, или пожилым пациентам в общем случае, решаются при помощи нового класса лекарственных веществ, описанных ниже.
Объектом изобретения являются стероидные соединения или их соли, соответствующие следующей общей формуле (I)
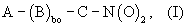
где bо=1;
А=R-, где R представляет собой радикал лекарственного стероидного вещества, определенный ниже;
В=-Тв-Х2-ТВI,
где Тв и ТBI одинаковы или различны и представляют собой СО, О, S,
Х2 представляет собой бивалентную мостиковую группу, такую как соответствующий предшественник В, имеющий формулу Z-Тв-Х2-tbi-z’, в которой Z, Z’ представляют собой независимо Н или ОН, выбраны из соответствующих соединений
С представляет собой бивалентный радикал -Tc-Y-, где Тс=(СО), когда tbi представляет собой О, S, NH, Тc представляет собой О, S, когда tbi представляет собой (СО);
или Y представляет собой Yо, выбранный из:
- алкиленокси группы R'O, где R' представляет собой линейный или, когда это возможно, разветвленный остаток C1-C20,
R-, имеющий следующую структуру:
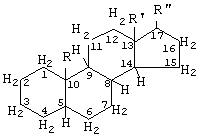
вместо атома водорода в СН группах или вместо двух атомов водорода в СН2 группах в данной общей формуле могут присутствовать следующие заместители:
в положении 1-2: может быть двойная связь;
в положении 3: может быть =O, ОН;
в положении 4-5: может быть двойная связь;
в положении 6; может быть Cl, F, СН3,
в положении 7: может быть ОН;
в положении 9: может быть Cl, F;
в положении 11: может быть ОН, =О,
в положении 16: может быть СН3, ОН,
в положении 17: может быть ОН, СН3,
в положении 16-17: могут быть следующие группы:
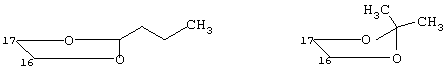
R и R’, одинаковые или разные, могут представлять собой водород,
R’’ представляет собой -СН(СН3)-СН2-СН2-СО- или -СО-СН2O-.
Предпочтительными соединениями формулы (1) являются такие соединения, в которых предшественник стероида выбран из урсодезоксихолевой кислоты, хенодезоксихолевой кислоты.
Наиболее предпочтительные соединения формулы (I) выбираются из группы, состоящей из:
-4-нитроксибутилового эфира 3-[4-[(3α,5β,7β)-3,7-дигидроксихолан-24-оилокси]-3-метоксифенил]-2-пропеновой кислоты;
-4-нитроксибутилового эфира 3-[4-[(3α,5β,7α)-3,7-дигидроксихолан-24-оилокси]-3-метоксифенил]-2-пропеновой кислоты.
Предшественник В, имеющий формулу Z-Тв-Х2-ТBI-Z’, в которой Z и Z’ представляют собой независимо Н или ОН, встречается в тесте 4 или 5,
- где тест 4 состоит в следующем: это аналитическое определение, выполняемое путем добавления порций метанольного раствора предшественника В с концентрацией 10-4 М к метанольному раствору DPPH (2,2-дифенил-1-пикрилгидразил - свободный радикал); после выдерживания этого раствора при комнатной температуре без доступа света в течение 30 минут измеряют поглощение при длине волны 517 нм тестируемого раствора, а также раствора, содержащего только DPPH в том же количестве, что и тестируемый раствор; а затем рассчитывают ингибирование образования радикалов из DPPH, вызванное соответствующим предшественником, в процентах, при помощи следующей формулы:
(1-AS/AC)×100,
где AS и АC соответственно представляют собой величины поглощения раствора, содержащего тестируемое соединение + DPPH, и раствора, содержащего только DPPH; критерий успешного прохождения теста для соединения таков: предшественники соединений В и соответствуют условиям теста 4, если процент ингибирования, рассчитанный, как указано выше, больше или равен 50%;
- где тест 5 состоит в следующем: это аналитическое определение, которое выполняют путем добавления аликвот 10-4 М метанольных растворов предшественников В к раствору путем смешивания 2 мМ водного раствора дезоксирибозы с 100 мМ фосфатным буфером и 1 мМ раствором соли FeII(NH4)2(SO4)2; после термостатирования этого раствора при 37°С в течение 1 часа добавляют аликвоты 2,8% водного раствора трихлоруксусной кислоты и 0,5 М водного раствора тиобарбитуровой кислоты в указанном порядке, нагревают раствор при 100°С в течение 15 минут, и затем измеряют поглощение тестируемых растворов при 532 нм; ингибирование образования радикалов солью FeII, вызванное предшественниками соединений В или B1, или С=-TC-Y-H, рассчитывают в процентах по следующей формуле:
(1-AS/AC)×100,
где AS и АC соответственно представляют собой величины поглощения раствора, содержащего тестируемое соединение и соль железа, и раствора, содержащего только соль железа; соединение соответствует условиям теста 5, если процент ингибирования предшественниками В со свободными валентностями, занятыми, как указано выше, определенный, как указано выше, больше или равен 50%.
Предпочтительно предшественник соединения В (соответственно предшественник X2 в формулах (I)), который соответствует условиям теста 4, выбирают из следующих классов соединений.
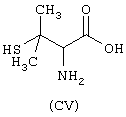
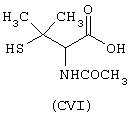
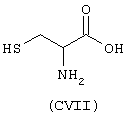
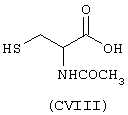
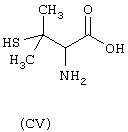
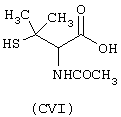
- Аминокислоты, выбранные из следующих соединений: пеницилламин (CV), N-ацетилпеницилламин (CVI), цистеин (СVII), N-ацетилцистеин (СVIII),
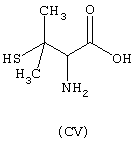
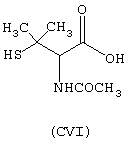
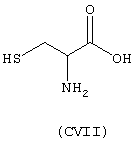
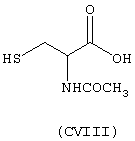
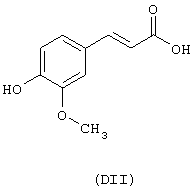
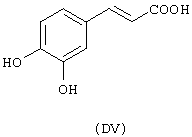
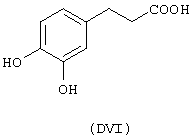
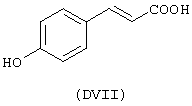
- гидроксикислоты, выбранные из следующих соединений: галловая кислота (формула DI), феруловая кислота (DII), гентизиновая кислота (DIII), лимонная кислота (DIV), кофеиновая кислота (DV), гидрокофеиновая кислота (DVI), п-кумариновая кислота (DVII), ванилиновая кислота (DVIII), сиреневая кислота (DXI):
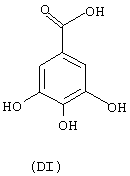
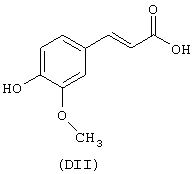
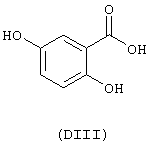
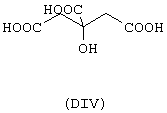
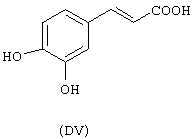
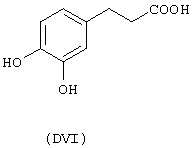
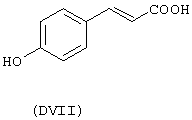
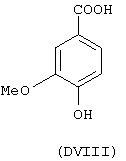
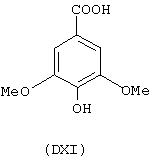
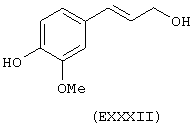
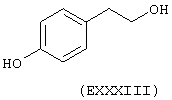
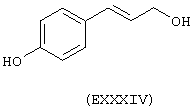
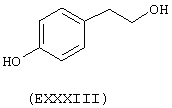
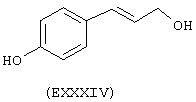
- Ароматические и гетероциклические одно- и многоатомные спирты, выбранные из следующих соединений: гидрохинон (EVIII), метоксигидрохинон (EXI), гидроксигидрохинон (ЕХII), конифериловый спирт (ЕХХХII), 4-гидроксифенетиловый спирт (ЕХХХIII), п-кумариновый спирт (EXXXIV):
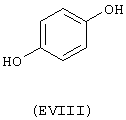
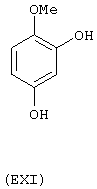
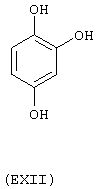
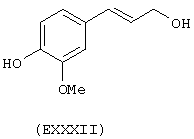
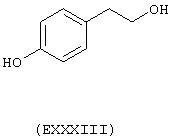
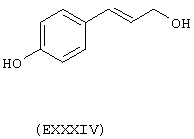
Вышеупомянутые вещества, являющиеся предшественниками В, получают в соответствии с методами, известными из уровня техники и описанными, например, в "The Merck Index, Изд. 12а, (1996), включенного сюда в качестве ссылки. Если это возможно, могут быть использованы соответствующие изомеры и оптические изомеры.
Предпочтительно предшественник соединения В (соответственно предшественник радикала Х2, в формуле (I), который соответствует условиям теста 5, выбирают из следующих соединений.
- Аминокислоты: аспарагиновая кислота (PI),
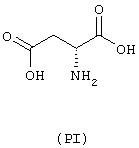
Предшественники соединений В упомянутых выше групп P, Q и R получают в соответствии с известными из уровня техники методами, описанными, например, в "The Merck Index", Изд. 12а, (1996), включенном сюда в качестве ссылки.
Y3 в формуле (III) предпочтительно выбирают из следующих групп:
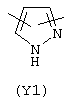
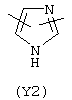
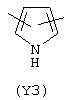
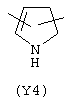
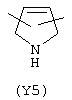
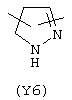
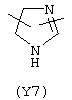
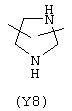
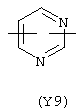
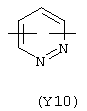
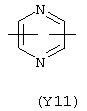
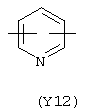
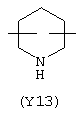
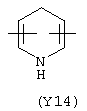
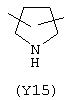
Наиболее предпочтительно Y3 представляет собой Y12 (пиридил), замещенный в положениях 2 и 6. Связи могут также находиться в асимметричных положениях, например Y12 (пиридил) может быть также замещен в положениях 2 и 3; Y1 (пиразол) может быть 3,5-дизамещенным.
Соединения по настоящему изобретению формула (I) могут быть превращены в соответствующие соли. Например, один из способов образования солей состоит в следующем: если в молекуле один из атомов азота является достаточно основным, чтобы образовать соль, то в органическом растворителе, например, таком как ацетонитрил или тетрагидрофуран, он взаимодействует с эквимолярным количеством соответствующей органической или неорганической кислоты.
Предпочтительно в формуле соединений по настоящему изобретению присутствуют Y или Y’ формулы (III).
Примеры органических кислот: щавелевая, винная, малеиновая, янтарная, лимонная кислоты.
Примеры неорганических кислот: азотная, соляная, серная, фосфорная кислоты.
В стероидных предшественниках предпочтительно
R’’=-СО-СН2О, -СН(СН3)-СН2-СН2-СО.
Среди стероидных предшественников предпочтительными являются такие, которые содержат гидроксильную функциональную группу в положении 3 или в положении 11 или имеют в составе R’’ гидроксильную или карбоксильную функциональную группу в концевом положении.
Стероидные предшественники А, которые следует упомянуть в качестве предпочтительных, перечислены ниже, их получают при помощи процессов, известных из уровня техники.
В качестве предшественников и соответствующих процессов могут быть упомянуты, например, те, которые описаны в каталоге "The Merck Index", изд. 12, 1996, включенном сюда в качестве ссылки. Эти предшественники (в соответствии с номенклатурой Merck), в которых Н2, Н, R, R’, R’’ принимают указанные выше значения, представляют собой перечисленные далее соединения: Буденозид, Гидрокортизон, Беклометазон, Бетаметазон, Хлорпреднизон, Клокортолон, Кортизон, Кортикостерон, Дезонид, Дезоксиметазон, Дексаметазон, Дифлукортолон, Флуметазон, Флунизолид, Флупреднизолон, Флурандренолид, Мепреднизон, Метилпреднизолон, Параметазон, Преднизалон, Преднизон, Триамцинолон, Урсодезоксихолевая кислота, Хенодезоксихолевая кислота.
Неожиданно выяснилось, что продукты по изобретению формулы (I) в состоянии окислительного стресса имеют улучшенный терапевтический индекс по сравнению со стероидными предшественниками. В качестве иллюстрации приведем результаты рассмотренных выше тестов для следующих соединений (см. таблицы, приложенные к описанию).
Тест 4 (тест для предшественника В, см. Таблицу III)
N-ацетилцистеин на 100% ингибирует образование радикалов из DPPH и, следовательно, соответствует условиям теста 4 и может быть использован как предшественник В или B1.
4-Тиазолидинкарбоновая кислота не ингибирует образование радикалов из DPPH, следовательно, она не соответствует условиям теста 4: эта кислота может быть использована в качестве предшественника В или B1, если она соответствует условиям теста 5.
Тест 5 (тест для предшественника В, см. Таблицу IV)
4-Тиазолидинкарбоновая кислота соответствует условиям теста 5, так как ингибирование составляет 100%. Следовательно, это соединение может быть использовано как предшественник В в формуле (I).
Соединения по изобретению могут быть использованы по тем же терапевтическим показаниям, что и лекарственные вещества-предшественники, но с указанными выше преимуществами.
Соединения формулы (I) получают с помощью синтетических методов, приведенных ниже.
Выбор реакций для каждого метода зависит от реакционноспособной группы, присутствующей в молекуле стероида, в предшественнике соединения В который может быть, как указано выше, бивалентным, и в предшественнике соединения С.
Реакции проводят при помощи методов, хорошо известных из уровня техники, которые позволяют образовывать связи между стероидом, предшественником соединения В и предшественником соединения С, как описано выше.
Когда реакционноспособные функциональные группы стероида (например, -СООН, -ОН) участвуют в образовании ковалентной связи, например типа сложноэфирной, амидной, эфирной, то указанная функциональная группа может быть регенерирована с помощью методов, хорошо известных из уровня техники.
Далее приведены некоторые схемы синтеза для получения соединений по изобретению.
А) Синтез соединений формулы (I).
1. Синтез соединения, полученного путем взаимодействия между стероидом и предшественником соединения В.
1а. Если стероид содержит карбоксильную функциональную группу (общая формула: R-COOH), а функциональная группа предшественника соединения В, которая связывается с карбоксильной функциональной группой, имеет формулу XZ, причем Х является таким, как определено выше, a Z=Н, то проводимые реакции зависят от природы второй реакционноспособной группы, присутствующей в предшественнике соединения В.
1a.1. Если вторая реакционноспособная группа, присутствующая в предшественнике соединения В, является карбоксильной группой, то общая схема синтеза предполагает первоначальное образование галогенангидрида стероида R-COHal (Hal=Сl, Вr) и последующую реакцию с НХ группой предшественника соединения В:
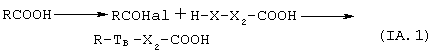
X2, ТB такие, как указано выше.
Если в двух соединениях, вступающих в реакцию, присутствуют другие функциональные группы СООН и/или НХ, они должны быть защищены перед проведением реакции в соответствии с методами, известными из уровня техники; например, как описано в публикации Th. W. Greene: "Protective groups in organic synthesis", Harward University Press, 1980.
Галогенангидрид RCOHal получают в соответствии с методами, известными из уровня техники, например при помощи тионил- или оксалилхлорида, РIII или PV галогенидов, проводя реакцию в инертных растворителях, например, таких как толуол, хлороформ, DMF и т.д.
В особых случаях, если НХ группа в предшественнике соединения В представляет собой NH2, ОН или SH, то стероид формулы R-COOH сначала превращают в соответствующий галогенангидрид RCOHal, как описано выше, и затем проводят реакцию с НХ группой предшественника соединения В, в присутствии органического основания, такого как триэтиламин, пиридин и т.д., в инертном растворителе, например, таком как толуол, тетрагидрофуран и т.д., при температуре в диапазоне от 0°С до 25°С.
В качестве альтернативы предыдущему синтезу стероид формулы R-COOH может быть обработан агентом, активирующим карбоксильную группу, выбранным из N,N’-карбонилдиимидазола (CDI), N-гидроксибензотриазола и дициклогексилкарбодиимида, в растворителе, таком как, например, DMF, THF, хлороформ и т.д., при температуре в диапазоне от -5°С до 50°С, после чего полученное соединение вводят во взаимодействие in situ (т.е. без предварительного выделения, в той же реакционной среде) с реакционноспособной функциональной группой предшественника соединения В с получением соединения формулы (IA.1).
1a.2. Если предшественник соединения В содержит две функциональные группы XZ, одинаковые или отличающиеся друг от друга, причем Х такой, как указано выше, и Z=Н, то стероид, имеющий формулу R-СООН, вначале обрабатывают агентом, активирующим карбоксильную группу, как описано выше в пункте 1а.1, а затем проводят реакцию с предшественником соединения В, у которого одна или две реакционноспособных НХ группы защищены, например, ацетильной или трет-бутилоксикарбонильной группой; удаление защит в конце синтеза позволяет регенерировать исходные функциональные группы. Схема синтеза следующая:
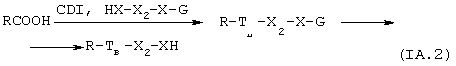
где X, ТB, X2 определены выше и G является защитной группой функциональной группы НХ.
2. Синтез нитроксипроизводных.
2а.1. Если соединение, полученное в конце предыдущей стадии la, имеет формулу (IA.1), то кислота может быть превращена в соответствующую натриевую соль, которую используют для получения конечного соединения, следуя известным из уровня техники методам, например в соответствии с одной из следующих схем синтеза:
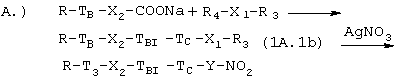
где ТB, Х2, ТBI ТC такие, как указано выше, R4 выбирают из Сl, Вr, Y такой, как указано выше, X1 является радикалом Y, свободным от атома кислорода, R3 представляет собой Сl, Вr, Йод, ОН. Если R3=ОН, то соединение формулы (1A.1b) подвергают галогенированию, например, такими агентами как РВr3, PCl5, SOCl2, РРh3+I2, и затем взаимодействию с AgNO3 в органическом растворителе, таком как ацетонитрил, тетрагидрофуран. Если R3 представляет собой Сl, Вr, Йод, то соединение формулы (1A.1b) взаимодействует непосредственно с AgNO3, как указано выше.
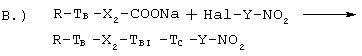
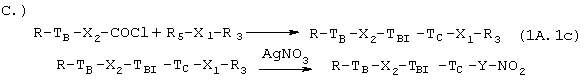
где R5=ОН или NHR1C; R1C, R3 и другие обозначения определены выше.
Если Х представляет собой линейный С4 алкил, то соответствующая кислота R-TB-X2-COOH взаимодействует с трифенилфосфином в присутствии галогенирующего агента, такого как СВr4 или N-бромсукцинимид в тетрагидрофуране, что приводит к соединению (IА.1с),где R3=Вr.
2а.2. Если соединение, полученное в конце предыдущей стадии 1a, имеет формулу (IA.2), то соответствующее нитроксипроизводное получают обработкой галогенкарбоновой кислоты, имеющей формулу Hal-X1-СООН (X1 определен выше), сначала агентом, активирующим карбоксильную группу, как описано выше в параграфе 1А.1, а затем соединением формулы (IA.2), что приводит к галогенпроизводному, которое выделяют, растворяют в органическом растворителе (см. параграф 2а.1) и затем обрабатывают нитратом серебра. Общая реакционная схема такова:
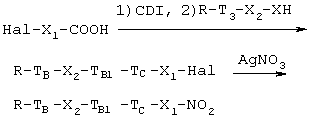
где ТB, Х2, TB1, ТC, Y такие, как указано выше.
Альтернативным методом является использование галогенида Наl-X1-COCl, где Hal предпочтительно представляет тсобой Вr, который может взаимодействовать с соединением формулы (IA.2).
1b. Если реакционноспособной функциональной группой стероида является группа -ОН (общая формула: R-OH), то две функциональные группы, присутствующие в предшественнике соединения В, могут быть следующими:
1b.1. Карбоксильная группа, которая взаимодействует с функциональной группой ОН стероида, и НХ группа, причем последняя реакционноспособная группа предшественника соединения В является такой же или иной, чем функциональная группа стероида. Формула предшественника соединения В является формулой следующего типа: Н-Х-Х2-СООН, где X и Х2 такие, как определено выше.
Функциональную группу H-X- предшественника соединения В защищают методами, известными из уровня техники, и карбоксильная группа вступает в реакцию, как указано выше, по следующей схеме:
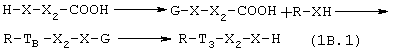
По окончании реакции функциональную группу НХ предшественника В регенерируют.
1b.2. Если предшественник соединения В содержит две карбоксильные группы, то его обрабатывают эквимолярным количеством агента, активирующего карбоксильную группу, в условиях, ранее описанных в параграфе 1а.1, и затем проводят реакцию с реакционноспособной группой ОН молекулы стероида. Другие возможные реакционноспособные функциональные группы HX типа, присутствующие в этих двух соединениях, должны быть надежно защищены, как указано выше. В итоге получают соединение формулы R-ТB-Х2-СООН (1В.2).
2b. Синтез нитроксипроизводных.
2b.1. Для получения конечного нитроксипроизводного исходя из соединения формулы R-ТB-Х2-Х-Н (1В.1), полученного в конце синтеза, описанного в параграфе 1b.1, соединение (1В.1) вводят в реакцию с галогенкислотой формулы Hal-X1-COOH, которую обрабатывают так, как описано ранее в параграфе 1а.1, или с соответствующим хлорангидридом галогенкислоты, полученное соединение растворяют в органическом растворителе, например ацетонитриле или тетрагидрофуране, и затем проводят реакцию с нитратом серебра.
2b.2. Для получения конечного нитроксипроизводного из соединения, формулы R-ТB-Х2-СООН (1В.2), полученного в конце синтеза, описанного в параграфе 1b.2, кислоту превращают в соответствующую натриевую соль, которая взаимодействует с соединением формулы R4-X1-R3, ранее определенном в схеме реакции А параграфа 2а.1, получая в соответствии с вышеупомянутым процессом конечное нитроксипроизводное. Альтернативным образом, если X1 является линейным С4 алкилом, кислота (1В.2) реагирует с трифенилфосфином в присутствии галогенирующего агента, такого как СВr4 или N-бромсукцинимид в тетрагидрофуране, и полученное в результате соединение, растворенное в органическом растворителе, например, ацетонитриле или тетрагидрофуране, взаимодействует с нитратом серебра.
2b.3. В качестве альтернативы процессу синтеза, описанному в параграфах 1b.1 и 2b.1, на первой стадии возможна реакция функциональной группы НХ- предшественника соединения В HX-Х2-СООН с хлорангидридом галогенкислоты, имеющим формулу Hal-X1-CO-Cl, где Hal предпочтительно представляет собой Вr; затем карбоксильная функция полученного таким образом соединения взаимодействует со стероидом формулы R-OH. На третьей и последней стадии Hal-группу замещают группой –ONO2 в соответствии с процессом, описанным в параграфе 2b.1. Реакционная схема является следующей:
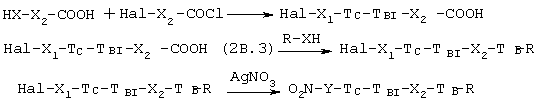
где ТC, TBI, ТB, Х2, X1, Y такие, как указано выше.
В предыдущей схеме, в качестве альтернативы, может быть проведено нитрование кислоты формулы (2B.3).
В указанных выше процессах взаимодействие стероида с предшественником В для соединений формулы (I) не проводят, если b0=0, и для реакции с предшественником соединения С напрямую используют стероид с его реакционноспособной функциональной группой.
Соединения, являющиеся объектом настоящего изобретения, были введены в состав соответствующих фармацевтических композиций для парентерального, перорального и местного применения в соответствии с хорошо известными из уровня техники методами, вместе с обычными эксципиентами; см. например "Remington’s Pharmaceutical Sciences, 15a Ed.".
Молярное количество активного действующего вещества в этих композициях является таким же или пониженным по сравнению с количеством используемого соответствующего лекарственного вещества -предшественника.
Дневные вводимые дозы являются такими же или в данном случае пониженными по сравнению с дозами лекарственных веществ-предшественников. Дневные дозы могут быть найдены в соответствующих публикациях на эту тему, например, в "Physician’s Desk Reference".
Следующие примеры приведены с целью иллюстрации настоящего изобретения и не должны рассматриваться как ограничивающие его объем.
ПРИМЕР 1
Получение 4-нитроксибутилового эфира 3-[4-[(3α,5β,7β)-3,7-дигидроксихолан-24-оилокси]-3-метоксифенил]-2-пропеновой кислоты
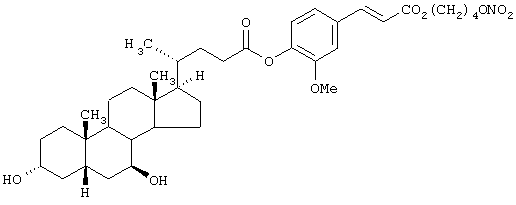
где стероидным предшественником является урсодезоксихолевая кислота формулы (XL), а предшественником В является феруловая кислота формулы (DII)
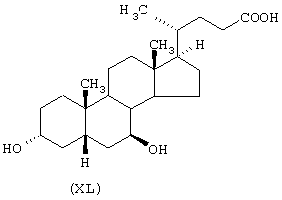
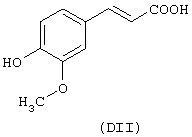
а) синтез 4-бромбутилового эфира 3-(4-гидрокси-3-метоксифенил)-2-пропеновой кислоты.
К раствору 3-(4-гидрокси-3-метоксифенил)-2-пропеновой кислоты (10 г, 51,5 ммоль) в ТГФ (400 мл) добавляют трифенилфосфин (2,7 г, 10,3 ммоль) и тетрабромметан (34,16 г, 10,3 ммоль), после чего перемешивают раствор при помощи магнитной мешалки при комнатной температуре в течение 48 часов. Раствор отфильтровывают от твердого осадка и затем упаривают при пониженном давлении. Полученный сырой продукт очищают хроматографией на силикагеле, элюируя смесью н-гексан/этилацетат 7/3. Получают 9 г 4-бромбутилового эфира 3-(4-гидрокси-3-метоксифенил)-2-пропеновой кислоты. Т.пл. 86-89°С.
b) синтез 4-бромбутилового эфира 3-[4-[(3α,5β,7β)-3,7-дигидроксихолан-24-оилокси]-3-метоксифенил]-2-пропеновой кислоты.
К раствору (3α,5β,7β)-3,7-дигидроксихолан-24-овой кислоты (2,9 г, 7,38 ммоль), растворенной в хлороформе (25 мл) и диметилацетамиде (25 мл), добавляют при перемешивании 4-бромбутиловый эфир 3-(4-гидрокси-3-метоксифенил)-2-пропеновой кислоты (2,73 г, 8,28 ммоль). К этому раствору при 0°С и перемешивании добавляют N,N’-дициклогексилкарбодиимид (2 г, 9,7 ммоль) и 4-диметиламинопиридин (100 мг, 0,81 ммоль). Через 1 час смесь нагревают до комнатной температуры и через 24 часа отфильтровывают осадок, а растворитель упаривают при пониженном давлении. Остаток обрабатывают этилацетатом (150 мл) и промывают водой (3×100 мл). После высушивания органической фазы над сульфатом натрия упаривают растворитель. Полученный сырой продукт очищают колоночной хроматографией на силикагеле, элюируя смесью н-гексан/этилацетат 1/9. Получают 2,5 г 4-бромбутилового эфира 3-[4-[(3α,5β,7β)-3,7-дигидроксихолан-24-оилокси]-3-метоксифенил]-2-пропеновой кислоты.
c) Синтез 4-нитроксибутилового эфира 3-[4-[(3α,5β,7β)-3,7-дигидроксихолан-24-оилокси]-3-метоксифенил]-2-пропеновой кислоты.
К раствору 4-бромбутилового эфира 3-[4-[(3α,5β,7β)-3,7-дигидроксихолан-24-оилокси]-3-метоксифенил]-2-пропеновой кислоты (2,3 г, 3,27 ммоль) в ацетонитриле (20 мл) и тетрагидрофуране (5 мл) добавляют при перемешивании нитрат серебра (0,84 г, 4,94 ммоль), после чего нагревают смесь до 80°С при интенсивном перемешивании на магнитной мешалке в течение 6 часов. По окончании реакции осадок отфильтровывают, а растворитель упаривают. Полученный сырой продукт очищают колоночной хроматографией на силикагеле, элюируя смесью дихлорметан/этилацетат 3/7. Получают 1,5 г 4-нитроксибутилового эфира 3-[4-[(3α,5β,7β)-3,7-дигидроксихолан-24-оилокси]-3-метоксифенил]-2-пропеновой кислоты. Суммарный выход составляет 32%.
Элементный анализ
Рассчитано, %: С 66,55; Н 8,08; N 2,04.
Найдено, %: С 66,59; Н 8,14; N 1,99.
Пример фармацевтический композиции: таблетки
Компоненты:
4-нитроксибутилового эфира 3-[4-[(3α,5β,7β)-3,7-дигидроксихолан-24-оилокси]-3-метоксифенил]-2-пропеновой кислоты, приготовленного по примеру 1: 250 мг;
микрокристаллин целлюлоза: 100 мг;
глюколат крахмала натрия: 10 мг;
стеарит магния: 20 мг.
ПРИМЕР 2
Получение 4-нитроксибутилового эфира 3-[4-[(3α,5β,7α)-3,7-дигидроксихолан-24-оилокси]-3-метоксифенил]-2-пропеновой кислоты
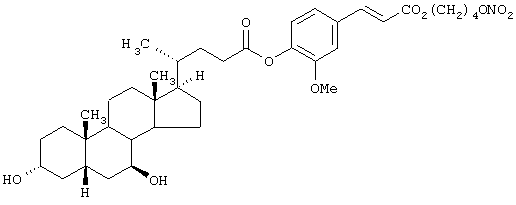
где стероидным предшественником является хенодезоксихолевая кислота формулы (XLI), а предшественником В является феруловая кислота формулы (DII)
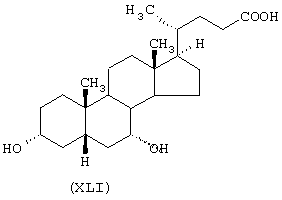
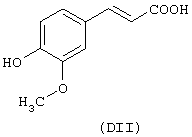
Данное соединение получено по методике, описанной в Примере 1. Суммарный выход составляет 28%.
Элементный анализ
Рассчитано, %: С 66,55; Н 8,08; N 2,04.
Найдено, %: С 66,64; Н 8,13; N 1,94.
ПРИМЕР 3
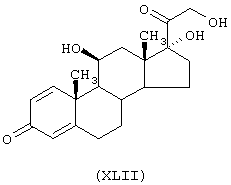
Получение (11β)-11,17-дигидрокси-21[N-ацетил-8-(4-нитроксибутироил)цистеинилокси]-прегн-1,4-диен-3,20-диона
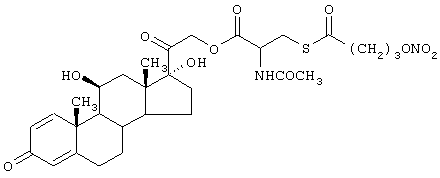
Стероидным предшественником является преднизолон формулы (ХLII), а предшественником В является N-ацетилцистеин формулы (СVIII)
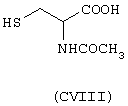
a) Синтез Н-ацетил-S-(4-бромбутироил)цистеина.
Раствор 4-бромбутановой кислоты (5,1 г, 30,6 ммоль) и 1,1’-карбонилдиимидазола (5,61 г, 34,6 ммоль) в хлороформе (50 мл) перемешивают при комнатной температуре в течение 1 часа. К реакционной смеси при перемешивании добавляют N-ацетилцистеин (5 г, 30,6 ммоль), растворенный в N,N-диметилформамиде (5 мл), и этилат натрия (50 мг). Через 24 часа раствор промывают 1% НС1 и рассолом, органическую фазу высушивают над сульфатом натрия и упаривают при пониженном давлении. Полученный сырой продукт очищают колоночной хроматографией на силикагеле, элюируя смесью этилацетат/хлороформ 7/3. Получают N-ацетил-S-(4-бромбутироил)цистеин.
b) Синтез (11β)-l1,17-дигидрокси-21[N-ацетил-S-(4-бромбутироил)цистеинилокси]-прегн-1,4-диен-3,20-диона.
К раствору N-ацетил-5-(4-бромбутироил)цистеина (2,7 г, 8,64 ммоль) и (11β)-11,17,21-тригидроксипрегн-1,4-диен-3,20-диона (3,2 г, 8,86 ммоль) в тетрагидрофуране (100 мл) при 0°С и перемешивании добавляют N,N’-дициклогексилкарбодиимид (1,9 г, 9,2 ммоль) и 4-диметиламинопиридин (100 мг, 0,8 ммоль). Через 1 час смесь нагревают до комнатной температуры и через 24 часа отфильтровывают осадок, а растворитель упаривают при пониженном давлении. Остаток обрабатывают этилацетатом (150 мл) и промывают водой (3×100 мл). После высушивания органической фазы над сульфатом натрия упаривают растворитель. Полученный сырой продукт очищают колоночной хроматографией на силикагеле, элюируя смесью хлороформ/этилацетат 3/7. Получают 0,94 г (11β)-11,17-дигидрокси-21[N-ацетил-S-(4-бромбутироил)цистеинилокси]-прегн-1,4-диен-3,20-диона.
с) Синтез (l1β)-11,17-дигидрокси-21[N-ацетил-S-(4-нитроксибутироил)цистеинилокси]-прегн-1,4-диен-3,20-диона.
К раствору (11β)-11,17-дигидрокси-21[N-ацетил-S-(4-бромбутироил)цистеинилокси]-прегн-1,4-диен-3,20-диона (0,8 г, 1,28 ммоль) в ацетонитриле (10 мл) и тетрагидрофуране (5 мл) добавляют при перемешивании нитрат серебра (0,4 г, 2,35 ммоль), после чего нагревают смесь при 80°С при перемешивании на магнитной мешалке в течение 20 часов. По окончании реакции осадок отфильтровывают, а растворитель упаривают. Полученный сырой продукт очищают колоночной хроматографией на силикагеле, элюируя смесью дихлорметан/этилацетат 3/7. Получают (11β)-11,17-дигидрокси-21[N-ацетил-S-(4-нитроксибутироил)цистеинилокси]-прегн-1,4-диен-3,20-дион. Суммарный выход составляет 12%.
Элементный анализ
Рассчитано, %: С 56,59; Н 6,33; N 4,40; S 5,04.
Найдено, %: С 56,63; Н 6,38; N 4,36; S 5,01.
ПРИМЕР 4
Получение (11β)-11,17-дигидрокси-21[N-ацетил-S-(4-нитроксибутироил)цистеинилокси]-прегн-4-ен-3,20-диона.
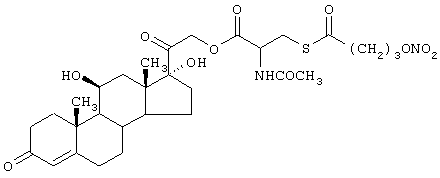
Стероидным предшественником является гидрокортизон формулы (ХLIII), а предшественником В является N-ацетилцистеин формулы (СVIII)
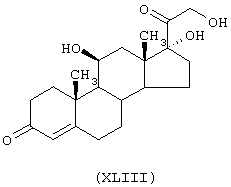
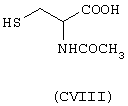
Данное соединение получено по методике, описанной в Примере 3. Суммарный выход составляет 15%.
Элементный анализ
Рассчитано, %: С 56,37; Н 6,78; N 4,39; S 5,02.
Найдено, %: С 56,39; Н 6,81; N 4,31; S 4,93.
ПРИМЕР 5
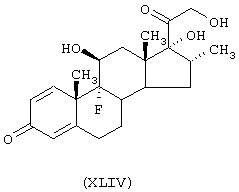
Получение (11β,16α)-9-фтор-11,17-дигидрокси-21[N-ацетил-S-(4-нитроксибутироил)цистеинилокси]-16-метилпрегн-1,4-диен-3,20-диона.
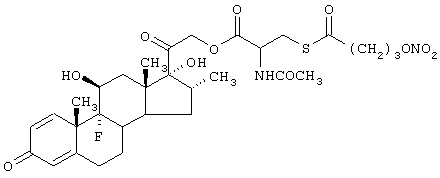
Стероидным предшественником является дезаметазон формулы (XLIV), а предшественником В является N-ацетилцистеин формулы (СVIII).
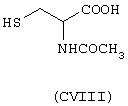
Данное соединение получено по методике, описанной в Примере 3. Суммарный выход составляет 17%.
Элементный анализ
Рассчитано, %: С 55,68; Н 6,18; N 4,19; S 4,79.
Найдено, %: С 55,72; Н 6,22; N 4,15; S 4,75.
ПРИМЕРЫ ФАРМАКОЛОГИЧЕСКИХ ТЕСТОВ
Острая токсичность
Острую токсичность оценивали путем введения группе из 10 крыс весом 20 г однократной дозы каждого из тестируемых соединений, вводя соединения в ротовое отверстие через трубку в составе водной суспензии карбоксиметилцеллюлозы (2% мас./об.). За животными вели наблюдение в течение 14 дней. Ни у одного из животных в тестируемой группе не появлялись токсические симптомы, даже после введения дозы 100 мг/кг.
ПРИМЕР F1
Экспериментальная in vivo модель с метиловым эфиром NW-нитро-L-аргинина (L-NAME): влияние стероидного предшественника и соответствующего соединения по изобретению на эндотелиальные дисфункции, вызываемые L-NAME.
Выбранная экспериментальная модель описана в J. Clin. Investigation, 90, 278-281, 1992.
Эндотелиальную дисфункцию оценивали путем определения повреждения печени (повышение уровня глутамат-пируват трансаминазы - GPT), сосудистого эндотелия и сердечно-сосудистой системы (повышение кровяного давления), вызванных введением L-NAME.
Животные (крысы Long Evans, средний вес 350-450 г) были разделены на группы, как описано ниже. Группе, получавшей L-NAME, в течение 4 недель вводили указанные соединения, растворенные до концентрации 400 мг/л в питьевой воде. Были сформированы следующие группы (по 10 животных в группе).
A) Контрольные группы:
1° группа: воздействие: только носитель (физиологический раствор),
2° группа: воздействие: носитель + L-NAME.
B) Группы, которым вводили лекарственные вещества:
3° группа: воздействие: носитель + лекарственное вещество,
4° группа: воздействие: носитель + лекарственное вещество + L-NAME.
Соединения, прошедшие данное тестирование: гидрокортизон, дезаметазон, преднизолон, хенодезоксихолевая кислота, урсодезоксихолевая кислота, а также соответствующие производные по изобретению.
В группах крыс, подвергнутых воздействию соответственно гидрокортизона, дезаметазона, преднизолона, а также соответствующих соединений по изобретению, определяли кровяное давление.
В группах крыс, подвергнутых воздействию соответственно урсодезоксихолевой кислоты и хенодезоксихолевой кислоты, а также соответствующих соединений по изобретению, определяли GPT.
Каждое лекарственное вещество вводилось внутрибрюшинно 1 раз в день в течение 4 недель.
К концу четвертой недели был прекращен доступ животных к воде, и по истечении 24 часов животные были умерщвлены.
Через 4 часа после последнего введения лекарственного вещества определяли кровяное давление.
Повреждение сосудистого эндотелия определяли, как указано выше, по влиянию L-NAME на сердечно-сосудистую систему (повышение кровяного давления). Повреждение печени определяли путем оценки содержания глутамат-пируват трансаминазы (повышение уровня GPT) после умерщвления.
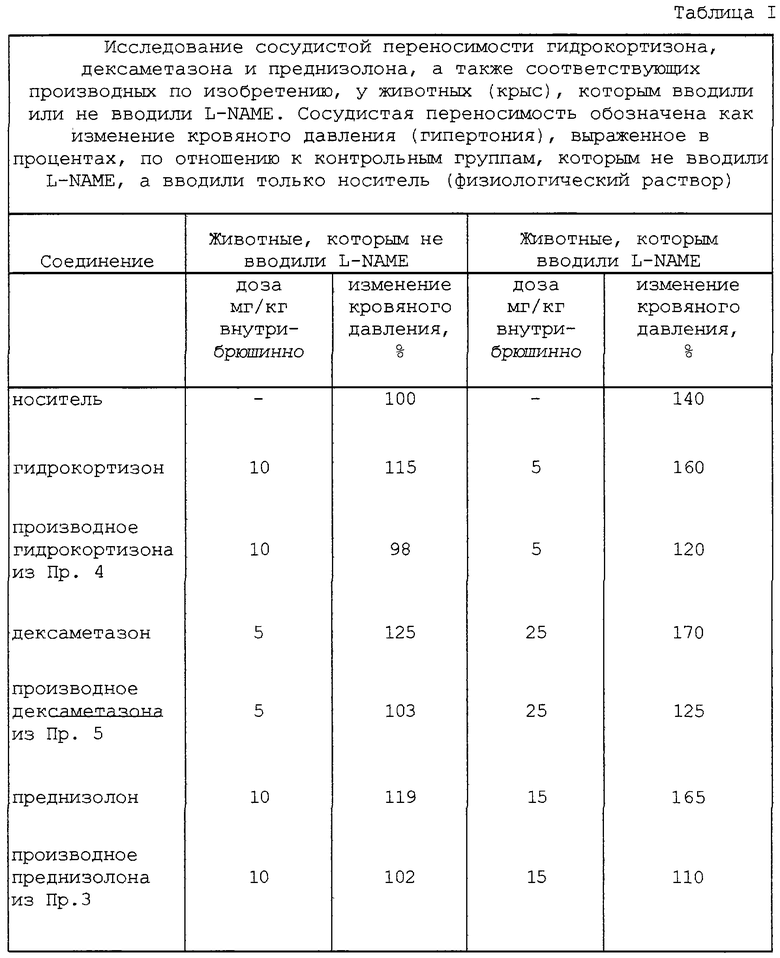
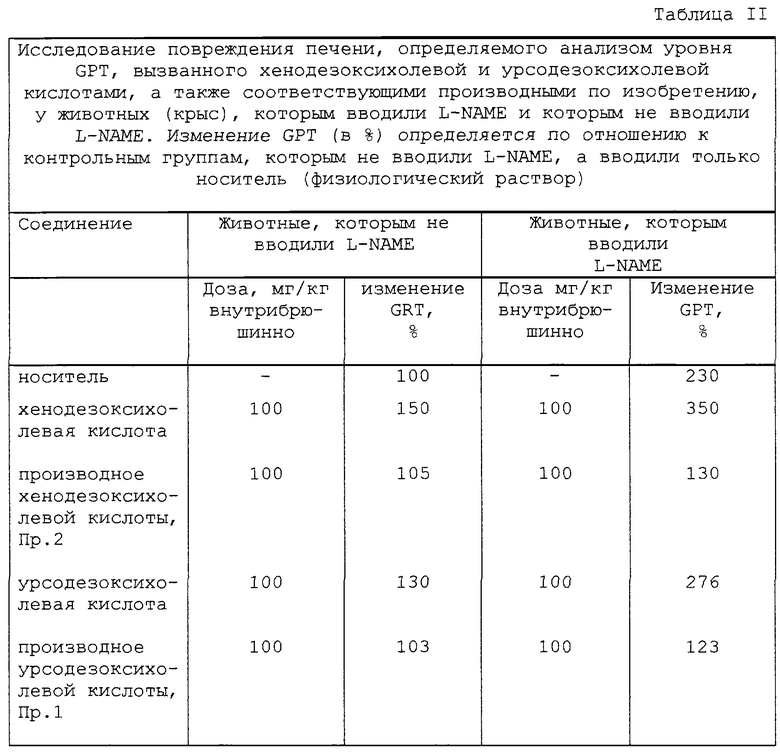
Результаты представлены в Таблицах I и II. Величины (в %) кровяного давления и GPT выражают отношение к соответствующим величинам, найденным для животных первой контрольной группы. Средняя величина кровяного давления в этой группе равна 105 мм рт.ст.
Полученные результаты свидетельствуют о том, что стероидные предшественники вызывают повреждение печени (хенодезоксихолевая кислота, урсодезоксихолевая кислота), а также артериальную гипертонию (гидрокортизон, дезаметазон, преднизолон). Уровни GPT и кровяного давления у крыс, которым вводили эти соединения, выше, чем в соответствующих группах, которым вводили лекарственные вещества без L-NAME, а также в контрольных группах, которым вводили только L-NAME. Наоборот, продукты по изобретению обладают лучшей переносимостью по сравнению с соответствующими предшественниками, даже у животных, которым не вводили L-NAME.
ПРИМЕР F2
Тест 4: Ингибирование образования радикалов из DPPH некоторыми веществами, используемыми для получения предшественников В и B1.
Метод основан на колориметрическом тесте, в котором в качестве соединения, образующего радикалы, используется DPPH (2,2-дифенил-1-пикрил-гидразил) (M.S. Nenseter et al., Atheroscler. Thromb. 15, 1338-1344, 1995).
Сначала готовят метанольные растворы тестируемых веществ в конечных концентрациях 100 мкМ. 0,1 мл каждого их этих растворов добавляют к аликвотам метанольного раствора 0,1 М DPPH объемом 1 мл, а затем объем доводят до 1,5 мл. После выдерживания раствора при комнатной температуре без доступа света в течение 30 мин измеряют поглощение при длине волны 517 нм. Определяют снижение поглощения по отношению к поглощению раствора, содержащего такую же концентрацию DPPH.
Эффективность тестируемого соединения в отношении ингибирования образования радикалов, иными словами, антирадикальная активность, выражается следующей формулой:
(1-AS/AC)×100,
где AS и АC являются, соответственно, величинами поглощения раствора, содержащего тестируемое вещество + DPPH, и раствора, содержащего только DPPH.
Соединение, предлагаемое для использования в качестве предшественника В или B1 в соответствии с настоящим изобретением, соответствует условиям теста 4, если оно ингибирует образование радикалов из DPPH с эффективностью, равной или превышающей 50%.
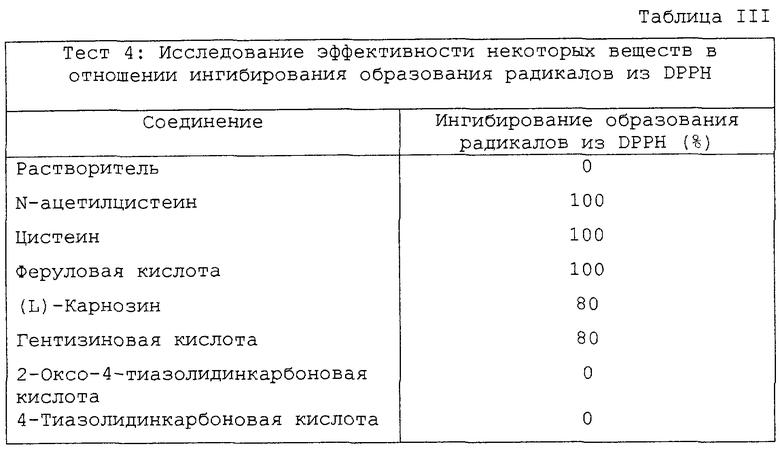
В Таблице III представлены результаты, полученные в указанном тесте со следующими соединениями: N-ацетилцистеин, цистеин, феруловая кислота, (L)-карнозин, гентизиновая кислота, 4-тиазолидинкарбоновая кислота и 2-оксо-4-тиазолидинкарбоновая кислота.
Таблица III показывает следующее:
N-ацетилцистеин, цистеин, феруловая кислота, (L)-карнозин, гентизиновая кислота соответствуют условиям теста 4, так как они ингибируют образование радикалов, вызванное DPPH, с эффективностью, превышающей 50%. Следовательно, они могут быть использованы в качестве предшественников соединения B в синтезе соединений по настоящему изобретению.
4-Тиазолидинкарбоновая кислота и 2-оксо-4-тиазолидинкарбоновая кислота не соответствуют условиям теста 4, так как они не ингибируют образование радикалов из DPPH. Следовательно, они могут быть использованы в качестве предшественников В и B1 в случае, если они соответствуют условиям теста 5.
ПРИМЕР F3
Тест 5: Ингибирование образования радикалов из FeII соединениями, используемыми в качестве предшественников В, B1 или С=-TC-Y-H.
0,1 мл аликвоты 10-4 M метанольных растворов 4-тиазолидинкарбоновой кислоты и 2-оксо-4-тиазолидинкарбоновой кислоты добавляют в пробирки, содержащие водный раствор, образованный путем смешивания 0,2 мл 2 мМ раствора дезоксирибозы, 0,4 мл 100 мМ фосфатного буфера (рН=7,4) и 0,1 мл 1 мМ раствора FeII (NH4)2(SO4)2 в 2 мМ растворе НСl. Затем пробирки выдерживают при температуре 37°С в течение одного часа. Затем в каждую пробирку добавляют 0,5 мл 2,8% водного раствора трихлоруксусной кислоты и 0,5 мл водного раствора 0,1М тиобарбитуровой кислоты в указанном порядке. Контрольный прозрачный раствор готовят путем замены указанной выше 0,1 мл аликвоты метанольного раствора тестируемого соединения на 0,1 мл метанола. Пробирки закрывают и нагревают на масляной бане при температуре 100°С в течение 15 минут. Появляется розовое окрашивание, интенсивность которого пропорциональна количеству дезоксирибозы, подвергшейся радикальному окислительному расщеплению. Растворы охлаждают до комнатной температуры и измеряют их поглощение при 532 нм относительно прозрачного контрольного раствора.
Ингибирование образования радикалов из FeII, вызываемое предшественником В или B1 или С=-TC-Y-H (где свободная валентность занята, как определяется выше), определяют в процентах по следующей формуле:
(1-AS/AS)×100,
где AS и АC являются, соответственно, величинами поглощения раствора, содержащего тестируемое вещество + соль железа, и раствора, содержащего только соль железа.
Результаты представлены в Таблице IV, которая показывает, что обе кислоты соответствуют условиям теста 5, так как они ингибируют образование радикалов из FeII с эффективностью, превышающей 50%.
Следовательно, как 4-тиазолидинкарбоновая кислота, так и 2-оксо-4-тиазолидинкарбоновая кислота могут быть использованы в качестве предшественников В, B1 или С=-TC-Y-H для получения соединений по настоящему изобретению.
ПРИМЕР F4
Пример F1 повторили с тремя группами крыс (каждая группа состояла из 10 животных), при этом одна контрольная группа не получала L-NAME, а две группы получали L-NAME; вещества вводили внутрибрюшинно в соответствии со следующей схемой:
а) контрольная группа (не получающая L-NAME): носитель (физиологический раствор),
b) 1-ой группе, получавшей L-NAME (группа сравнения b), в то же время вводили дексаметазон (25 мг/кг, 0,064 ммоль/кг) + N-ацетилцистеин (10,4 мг/кг, 0,064 ммоль/кг) с тем же самым носителем,
с) 2-ой группе, получавшей L-NAME (группа с), вводили производное дексаметазона (42,5 мг/кг, 0,064 ммоль/кг) по изобретению (см. прим. 5) в том же вышеупомянутом носителе.
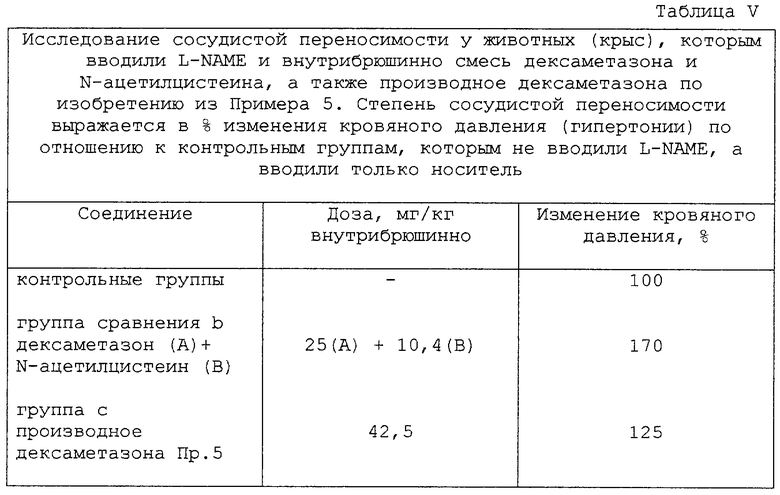
В этом эксперименте определяли сосудистую переносимость, то есть увеличение кровяного давления (повреждение сосудов), у животных групп b и с, выраженную как процентное соотношение к кровяному давлению у животных группы а, которое принимали равным 100%.
Результаты, приведенные в Таблице V, показывают, что смесь, вводимая группе b (группе сравнения), вызывала у животных большее повышение кровяного давления, чем соединение по изобретению (группа с).
ПРИМЕР F5
Пример F1 повторили с тремя группами крыс (каждая группа состояла из 10 животных), при этом одна контрольная группа не получала L-NAME, а две группы получали L-NAME; вещества вводили внутрибрюшинно в соответствии со следующей схемой:
а) контрольная группа (не получающая L-NAME): носитель (физиологический раствор),
b) 1-ой группе, получавшей L-NAME (группа сравнения d), в то же время вводили урсодезоксихолевую кислоту (100 мг/кг, 0,25 ммоль/кг) + феруловую кислоту (49,5 мг/кг, 0,064 ммоль/кг) с тем же самым носителем,
с) 2-ой группе, получавшей L-NAME (группа e), вводили производное урсодезоксихолевой кислоты (175 мг/кг, 0,25 ммоль/кг) по изобретению (см. прим.1) в том же вышеупомянутом носителе.
В этом эксперименте определяли печеночную переносимость, то есть увеличение уровня GРТ (повреждение печени), у животных групп d и e, выраженную как процентное соотношение к уровню GPT у животных группы а, которое принимали равным 100%.
Результаты, приведенные в Таблице V, показывают, что смесь, вводимая группе d (группе сравнения), вызывала у животных большее увеличение уровня GPT, чем соединение по изобретению (группа e).

| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ ЛЕКАРСТВЕННЫЕ ВЕЩЕСТВА | 2000 |
|
RU2237657C2 |
| НОВЫЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА | 2000 |
|
RU2237057C2 |
| СОЕДИНЕНИЯ, ИХ ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ НАРУШЕНИЙ ПОРТАЛЬНОЙ И ПЕЧЕНОЧНОЙ ВЕНОЗНОЙ ЦИРКУЛЯЦИИ | 2003 |
|
RU2299886C2 |
| ЛЕКАРСТВЕННЫЕ ВЕЩЕСТВА И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ ДЛЯ ИСПОЛЬЗОВАНИЯ В СЛУЧАЯХ ОКИСЛИТЕЛЬНОГО СТРЕССА | 2000 |
|
RU2264383C2 |
| АГЕНТЫ ДЛЯ КРОВЯНОГО ДЕПО ДЛЯ ДИАГНОСТИКИ С ПОМОЩЬЮ ЯДЕРНОГО МАГНИТНОГО РЕЗОНАНСА | 1999 |
|
RU2250765C2 |
| НЕЙРОАКТИВНЫЕ СТЕРОИДЫ, ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ, СПОСОБ ЛЕЧЕНИЯ ИЛИ ПРОФИЛАКТИКИ РАЗЛИЧНЫХ НАРУШЕНИЙ, СПОСОБ ИНДУКЦИИ СНА И СПОСОБ ИНДУКЦИИ АНЕСТЕЗИИ С ИХ ИСПОЛЬЗОВАНИЕМ, СПОСОБ МОДУЛИРОВАНИЯ КОМПЛЕКСА РЕЦЕПТОР ГАМКa-ХЛОРИДНЫЙ ИОНОФОР | 1996 |
|
RU2194712C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГАММА-АМИДОВ ГЛУТАМОВОЙ КИСЛОТЫ | 1999 |
|
RU2395490C2 |
| СТЕРОИДНЫЕ СОЕДИНЕНИЯ (ВАРИАНТЫ), ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ЛЕЧЕНИЯ НЕРВНЫХ РАССТРОЙСТВ (ВАРИАНТЫ) И СПОСОБ ИНДУКЦИИ АНЕСТЕЗИИ У ЖИВОТНОГО | 1995 |
|
RU2176248C2 |
| НОВЫЕ СТЕРОИДНЫЕ СОЕДИНЕНИЯ, ОБЛАДАЮЩИЕ ПОВЫШЕННОЙ РАСТВОРИМОСТЬЮ В ВОДЕ И УСТОЙЧИВОСТЬЮ К МЕТАБОЛИЗМУ, И СПОСОБЫ ИХ ПРИГОТОВЛЕНИЯ | 2007 |
|
RU2458065C2 |
| Средства для ингибирования фермента тирозил-ДНК-фосфодиэстеразы 1 на основе желчных кислот | 2018 |
|
RU2689335C1 |
Стероидные соединения или их соли, соответствующие общей формуле (I)
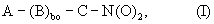
где bo=1; А=R-, где R является радикалом стероидного лекарственного вещества, C1 и С2 представляют собой бивалентные радикалы. Предшественник радикала B1 должен соответствовать условиям фармакологических тестов, содержание которых раскрыто в описании. Соединения I полезны при лечении воспалительных заболеваний, астмы и печеночных расстройств. 2 н. и 8 з.п.ф-лы, 6 табл.
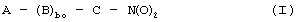
где bo=1;
А=R-, где R представляет собой радикал стероидного лекарственного вещества, определенный ниже;
В=-Тв-Х2-ТBI, где Тв и tbi одинаковы или различны и представляют собой СО или О, S;
Х2 представляет собой бивалентную мостиковую группу, такую как соответствующий предшественник В, имеющий формулу Z-Тв-Х2-tbi-Z’, в которой Z, Z’ представляют собой независимо Н или ОН, выбран из соответствующих соединений:
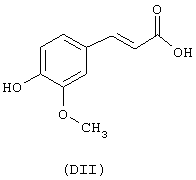
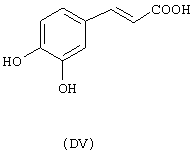
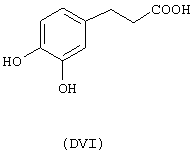
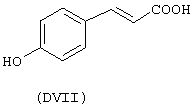
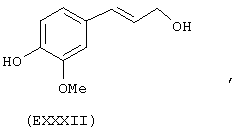
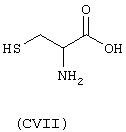
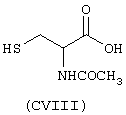
С представляет собой бивалентный радикал -Tc-Y-, где
Тс=(СО), когда tbi представляет собой О, S; Тc представляет собой O, S, когда ТBI представляет собой (СО);
Y представляет собой Y0, выбранный из - линейного или разветвленного остатка C1-C20, алкиленоксигруппы
R-, имеющий следующую структуру:
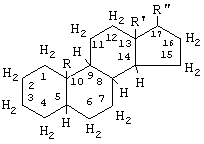
где вместо атома водорода в СН группах или вместо двух атомов водорода в СН2 группах в данной общей формуле могут присутствовать следующие заместители:
в положении 1-2 может быть двойная связь;
в положении 3 может быть =О, ОН;
в положении 4-5 может быть двойная связь;
в положении 6 может быть Cl, F, СН3,
в положении 7 может быть ОН;
в положении 9 может быть Cl, F;
в положении 11 может быть ОН, =О,
в положении 16 может быть СН3, ОН,
в положении 17 может быть ОН, СН3,
в положении 16-17 могут быть следующие группы:
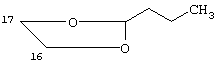
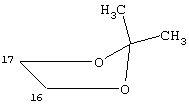
R и R’, одинаковые или разные, могут представлять собой водород;
R’’ представляет собой -СН(СН3)-СН2-СН2-СО- или -СО-СН2О-.
-4-нитроксибутилового эфира 3-[4-[(3α,5β,7β)-3,7-дигидроксихолан-24-оилокси]-3-метоксифенил]-2-пропеновой кислоты;
-4-нитроксибутилового эфира 3-[4-[(3α,5β,7α)-3,7-дигидроксихолан-24-оилокси]-3-метоксифенил]-2-пропеновой кислоты.
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
| Бесколесный шариковый ход для железнодорожных вагонов | 1917 |
|
SU97A1 |
| Ф.П.ТРИНУС | |||
| Фармако-терапевтический справочник | |||
| - Киев: Здоровья, 1989, с | |||
| Одновальный, снабженный дробителем, торфяной пресс | 1919 |
|
SU261A1 |
Авторы
Даты
2004-11-20—Публикация
2000-04-11—Подача