Изобретение относится к области медицинской и ветеринарной микробиологии, в частности, к способам приготовления иммунных сывороток и может быть использовано для приготовления на основе полученной сыворотки препаратов для иммунодиагностики туляремии, в частности - диагностикума эритроцитарного туляремийного иммуноглобулинового сухого, позволяющего идентифицировать возбудителя туляремии в культурах и обнаруживать туляремийный антиген в материалах, полученных от больных людей и животных, трупном материале и объектах внешней среды при помощи реакции непрямой гемагглютинации (РНГА).
Известен способ приготовления гипериммунной туляремийной лошадиной сыворотки (см. ФС 42-3492-98, РП №55-94 “Сыворотка диагностическая туляремийная сухая для реакции агглютинации (PA)”).
Известен способ получения туляремийной сыворотки, основанный на гипериммунизации мышей-продуцентов туляремийными микробами или извлеченными из них антигенами (Черепахина И.Я., Козловский В.Н., Ефанова Е.А. и др. Динамика образования антител к вакцинному штамму F. tularensis при различных схемах иммунизации // Микробиологический журнал. - 1990. - Т.52, №2. - С.89-93).
Общим с заявляемым способом является последовательность этапов приготовления антигенного материала, иммунизации животных-продуцентов, получения гипериммунной сыворотки.
Наиболее близким к заявляемому решению является способ, основанный на подкожной иммунизации кроликов живой культурой F. tularensis вакцинного штамма 15 НИИЭГ (см. Хлебников B.C., Головлев И.Р., Кулевацкий Д.П. и др. Изучение биохимических, антигенных и протективных свойств внешней мембраны возбудителя туляремии // Молекулярная генетика, микробиология и вирусология. - 1991. №7. - С.15-20).
Способ включает следующие этапы:
выращивание культуры F. tularensis;
приготовление корпускулярного антигена;
иммунизацию кроликов приготовленным антигенным препаратом.
Недостатком рассматриваемого способа является применение включающего в свой состав микобактерии туберкулеза полного адъюванта Фрейнда, что приводит к снижению специфичности иммунодиагностических препаратов, приготовленных на основе данной сыворотки. Кроме того, использование в качестве антигенного препарата одной живой культуры вакцинного штамма 15 НИИЭГ ставит под сомнение возможность выявления данными иммунодиагностическими препаратами вирулентных штаммов F. tularensis, обладающих более богатым антигенным спектром.
Известны способы приготовления эритроцитарных диагностикумов, предназначенных для идентификации возбудителей многих инфекционных заболеваний (см. Руководство по вакцинному и сывороточному делу / Под ред. П.Н.Бургасова. - М., 1978; Каральник М.П. Эритроцитарные белковые диагностикумы. - М., 1983).
Общим с заявляемым способом является последовательность этапов получения формалинизированных эритроцитов, выделения из гипериммунных сывороток специфических иммуноглобулинов, сенсибилизации ими эритроцитов.
Наиболее близким к заявляемому решению является способ получения диагностикума эритроцитарного туляремийного иммуноглобулинового сухого, разработанный Среднеазиатским НИПЧИ в 1990 г. (см. Регламент производства диагностикума эритроцитарного туляремийного иммуноглобулинового сухого для РНГА и РНАг / РП №230-90 - Алма-Ата, 1990) в соответствии с требованиями ФС 42-308 ВС - 90.
Способ включает следующие этапы:
получение иммуноглобулина из туляремийной агглютинирующей сыворотки;
подготовку эритроцитов барана к нагрузке иммуноглобулином;
сенсибилизацию формалинизированных эритроцитов иммуноглобулином;
лиофильное высушивание эритроцитарного диагностикума.
Основной недостаток рассматриваемого способа заключается в том, что диагностикум готовится на основе гамма-глобулиновой фракции, включающей в себя все виды сывороточных иммуноглобулинов, большая часть которых перекрестно реагирует с гетерологичными микроорганизмами, либо создает стерические препятствия взаимодействию туляремийных антигенов и антител. В результате диагностикум, полученный по этому способу, дает в РНГА положительные результаты не только с туляремийным микробом, но и с культурами возбудителей бруцеллеза, сапа, мелиоидоза, чумы, холеры и эшерихиоза. Крайне низкая специфичность сводит на нет практическую ценность диагностикума, что, по-видимому, явилось причиной невозможности переутверждения нормативно-технической документации на приготовление и применение указанного препарата. Кроме того, диагностикум-прототип отличается невысокой стабильностью, поскольку сохраняет свою активность лишь в течение 6... 8 месяцев.
Техническим результатом способа получения противотуляремийной гипериммунной кроличьей сыворотки является повышение, по сравнению с прототипом, ее специфической активности и специфичности при отсутствии у кроликов летальных исходов, а также трехкратное увеличение объема получаемой сыворотки за счет использования для иммунизации как живой культуры F. tularensis вакцинного штамма 15 НИИЭГ, так и смеси инактивированных культур вирулентных штаммов - типичных представителей трех географических рас туляремийного микроба (Schu, 503, 543), вводимых внутривенно на поздних стадиях иммунизации.
Новым в осуществлении способа получения противотуляремийной гипериммунной кроличьей сыворотки является то, что для иммунизации кроликов используют смесь инактивированных культур (корпускулярных антигенов) F. tularensis вирулентных штаммов Schu, 503, 543 и живую культуру вакцинного штамма 15 НИИЭГ, что усиливает иммунный ответ животных и обогащает спектр специфических антител в получаемых сыворотках.
Новым является использование для иммунизации кроликов неполного адъюванта Фрейнда, в составе которого отсутствуют микобактерии туберкулеза, что повышает специфичность препарата.
Новым является и то, что полученные на основе инактивированных культур туляремийного микроба корпускулярные антигены и живую культуру F. tularensis вакцинного штамма 15 НИИЭГ кроликам вводят внутривенно на поздних стадиях иммунизации, что не вызывает у них специфических поражений и гибели от анафилактического шока.
Техническим результатом предлагаемого способа приготовления диагностикума эритроцитарного туляремийного иммуноглобулинового сухого является увеличение чувствительности и специфичности препарата, сокращение времени получения окончательного результата, а также повышение сохраняемости диагностикума за счет, соответственно, использования в качестве сенситина выделенного из гипериммунной противотуляремийной сыворотки иммуноглобулинов класса G, а также - стабилизации диагностикума в оригинальной среде высушивания, содержащей 10% сахарозы, по 1% бычьего сывороточного альбумина (БСА) и натрия тетраборнокислого, 0,3% янтарной кислоты и 0,1% натрия азида.
Новым в достижении поставленного технического результата является использование в качестве сырья для приготовления препарата высокоактивной противотуляремийной гипериммунной кроличьей сыворотки с широким спектром антител ко всем расам F. tularensis, что повышает чувствительность приготовленного диагностикума.
Новым является также использование в качестве сенситина не всей гамма-глобулиновой фракции, а выделенных из нее иммуноглобулинов класса G, что повышает специфичность приготовленного диагностикума.
Новым является и способ стабилизации диагностикума в оригинальной среде высушивания, содержащей 10% сахарозы, по 1% БСА и натрия тетраборнокислого, 0,3% янтарной кислоты и 0,1% натрия азида (конечная концентрация каждого компонента подобрана опытным путем), что, по сравнению с прототипом, сокращает в 7 раз время получения окончательного результата в РНГА микрометодом и увеличивает в 3 раза сохраняемость свойств диагностикума.
Сопоставительный анализ показывает, что заявляемое техническое решение отличается тем, что для получения гипериммунной противотуляремийной кроличьей сыворотки применяется сочетанная иммунизация животных вакцинным и инактивированными вирулентными штаммами F. tularensis по оригинальной схеме, а эритроцитарный диагностикум готовят на основе выделенных из данной сыворотки иммуноглобулинов класса G и стабилизируют в специальной среде высушивания, содержащей 10% сахарозы, по 1% бычьего сывороточного альбумина и натрия тетраборнокислого, 0,3% янтарной кислоты и 0,1% натрия азида, что соответствует критерию изобретения “новизна”.
Новые существенные признаки сообщают заявленному техническому решению новые свойства, проявляющиеся в повышении чувствительности, специфичности, сохраняемости диагностикума, а также - сокращении времени получения результата анализа с использованием заявленного диагностикума, что соответствует критерию “промышленная применимость”.
Способ получения противотуляремийной гипериммунной кроличьей сыворотки осуществляют следующим образом.
1. Выращивание культур туляремийных микробов
Исходным материалом служат лиофилизированные туляремийные культуры штаммов 15 НИИЭГ, Schu, 503, 543, сохраняемые в ампулах под вакуумом и выращиваемые на FT-агаре (ВФС 42/Д-013 ВС-94, г.Оболенск) в соответствии с требованиями ФС 42-3951-00.
2. Приготовление корпускулярных антигенов
Сформировавшуюся в матрице культуру штамма 15 НИИЭГ смывают и разводят стерильным 0,9%-ным раствором натрия хлорида до концентрации 1,0 млрд клеток в 1,0 мл по ОСО 42-28-59-86П, эквивалентному 5,0 млрд клеток туляремийного микроба в 1,0 мл.
Выращенные культуры туляремийных микробов штаммов Schu, 503, 543 смывают и разводят стерильным 0,9%-ным раствором натрия хлорида до концентрации 40,0 млрд клеток в 1,0 мл, после чего инактивируют добавлением 5%-ного раствора фенола и 1%-ного раствора твина-20 до конечных концентраций 0,5% и 0,1% соответственно с последующим 5-минутным кипячением на водяной бане. Полученные взвеси смешивают в равных объемах. Для проведения 5 циклов иммунизации 10 кроликов готовят не менее 100,0 мл смеси.
Неполный адъювант Фрейнда помещают в стеклянный флакон и стерилизуют 30-минутным кипячением на водяной бане. Охлаждают до комнатной температуры и смешивают в объемном соотношении 1:1 с расчетным количеством смеси убитых культур F. tularensis. Полученную взвесь многократно (не менее 20 раз) набирают в шприц и с силой выпускают обратно до образования стабильной гомогенной эмульсии, капли которой не должны распадаться на поверхности дистиллированной воды в течение 30 мин и более.
3. Иммунизация кроликов
Используют не менее 10 животных. При внутривенных инъекциях иммуногены вводят в краевую вену уха, а при подкожных - в правую и левую паравертебральные области (вдоль позвоночника в 4 точки, удаленные друг от друга на расстояние 5 см). Препараты вводят по следующей схеме:
3.1. по 0,2 мл смеси инактивированных культур F. tularensis с неполным адъювантом Фрейнда подкожно в 4 точки правой паравертебральной области, повтор через 20 дней в левую паравертебральную область;
3.2. через 20 дней - циклическая внутривенная иммунизация смесью убитых культур F. tularensis без адъюванта по (0,8-1,6-2,4) мл с 5-дневным интервалом между инъекциями; 3. через 12 дней - циклическая внутривенная иммунизация живой культурой F. tularensis штамма 15 НИИЭГ по (0,8-1,6) мл с 2-дневным интервалом между инъекциями.
4. Получение иммунной сыворотки
Через 10 суток после последней инъекции у кроликов производят забор крови. Кровь собирают в стеклянные цилиндры и помещают в термостат для свертывания. Образовавшуюся сыворотку сливают, консервируют добавлением раствора натрия азида до конечной концентрации 0,1% и очищают центрифугированием.
Контроль активности полученной сыворотки определяют в РДП с культурами F. tularensis штаммов 15 НИИЭГ, Schu, 503, 543. Титр антител в иммунной сыворотке должен быть не ниже 1:128.
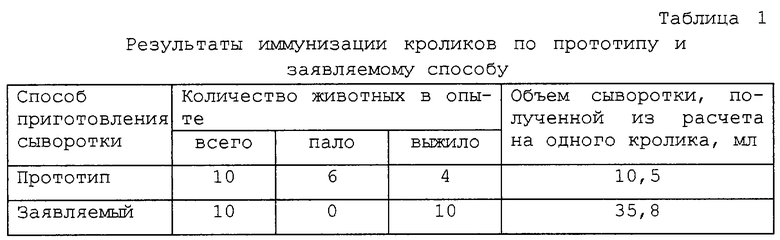
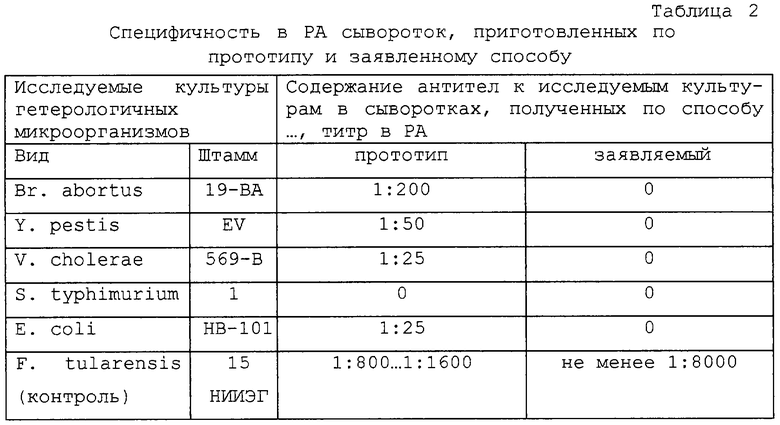
Для сравнения прототипа и заявляемого способа были проиммунизированы кролики и изучены полученные от них сыворотки (таблицы 1-3).
Наблюдения показали, что после второго цикла иммунизации по прототипу у животных нередко возникали некрозы кожи паховой области, а после третьего цикла большинство кроликов пало от анафилактического шока, что, по нашему мнению, связано с многократным использованием наиболее сенсибилизирующего организм подкожного введения иммуногенов.
Общее состояние кроликов, иммунизированных по заявляемому способу, на протяжении всего эксперимента оставалось удовлетворительным, что способствовало достаточно высокому выходу конечного продукта (сыворотки). Из расчета на одного кролика, взятого в работу, было получено в 3 раза больше сыворотки, чем в контроле (таблица 1). А сами сыворотки характеризовались отсутствием неспецифических и более высоким содержанием специфических антител, нежели сыворотки, полученные по прототипу (таблицы 2 и 3).
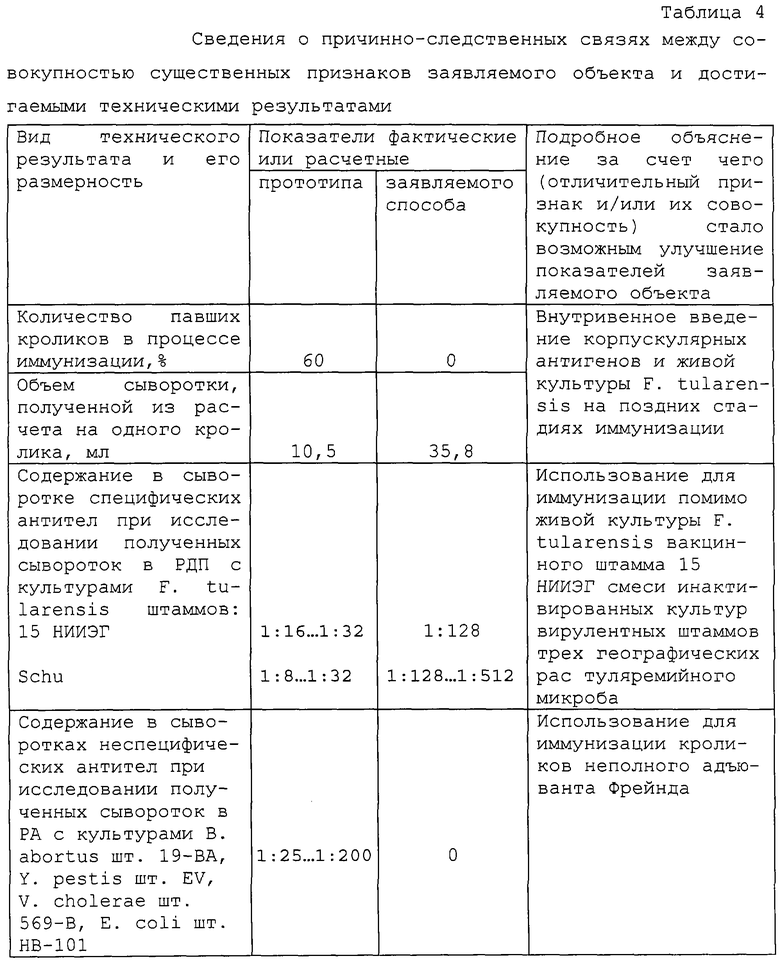
Наличие причинно-следственной связи между совокупностью существенных признаков заявляемого способа и достигаемыми техническими результатами показано в таблице 4.
Предлагаемый способ получения противотуляремийной гипериммунной кроличьей сыворотки имеет следующие преимущества:
не вызывает гибели кроликов от специфических поражений и анафилактического шока, что способствует получению в пересчете на одно животное примерно в 3 раза больше сыворотки, чем в контроле;
обеспечивает получение иммунных сывороток с более высоким титром специфических антител.
Высокое содержание специфических антител в получаемых сыворотках позволило предложить эти препараты для приготовления на их основе диагностикума эритроцитарного туляремийного иммуноглобулинового сухого, способ приготовления которого осуществляют следующим образом.
1. Приготовление иммуноглобулина
К туляремийной агглютинирующей сыворотке приливают равный объем насыщенного раствора аммония сульфата при постоянном перемешивании в течение 5 мин. После суточной инкубации при 4° С суспензию центрифугируют 15 мин при 5500 g. Удалив надосадочную жидкость, осадок иммуноглобулинов растворяют в 0,05 М растворе фосфатного буфера (ФБР) рН 7,2 в объеме, равном исходному объему взятой сыворотки.
Операцию осаждения повторяют. После центрифугирования осадок растворяют в 0,05 М ФБР рН 7,2 в объеме, равном половине исходного объема взятой сыворотки.
Раствор иммуноглобулинов диализуют двое суток против 1 л охлажденного до 4° С 0,05 М ФБР рН 7,2 со сменой буфера через 2, 8 и 24 ч. Осветляют 15-минутным центрифугированием при 5500 g. Надосадочную жидкость осторожно переливают в чистый флакон и определяют концентрацию белка спектрофотометрическим способом.
Отдиализованный раствор иммуноглобулина посредством перистальтического насоса вводят со скоростью нисходящего потока жидкости (5,0±0,5) мл· ч/см2 в хроматографическую колонку (размер 2,6× 40 см) с ДЭАЭ-сефацелем из расчета не более 10 мг белка на 1 мл геля. Пробу элюируют 0,05 М ФБР рН 7,2, контролируя выход белка по экстинкции при длине волны 280 нм посредством проточного абсорбциометра и потенциометрического самописца. Иммуноглобулин G элюируется одним широким пиком. С началом выхода белка из колонки элюат собирают в пробирки по (5,0±0,5) мл. Фракции первого пика, содержащие белок в концентрации не менее 5,0 мг/мл, объединяют. Раствор иммуноглобулина G консервируют азидом натрия, добавленным до конечной концентрации 0,1%.
2. Приготовление формалинизированных эритроцитов барана
Кровь у интактных баранов отбирают по 500 мл в стеклянные колбы, с помещенными в них стерильными бусами. После взятия крови колбы непрерывно помешивают в течение 20 мин для адгезии фибрина на бусах. Дефибринированную кровь фильтруют через капроновую ткань; от сывороточных белков эритроциты отмывают 20-минутным центрифугированием при 1100 g и 4° С 0,9%-ным раствором натрия хлорида (рН 6,8), охлажденным до той же температуры. На-досадочную жидкость удаляют; операцию отмывания эритроцитов повторяют 3-5 раз.
Для получения 8%-ной взвеси плотный осадок отмытых эритроцитов разводят в 12,5 раз 0,9%-ным раствором натрия хлорида, подогретого до 37° С. В растворе формалина (ГОСТ 1625-75) определяют процентное содержание формальдегида в соответствии с МУК 4.1/4.2.588-96, с.100-102. Необходимый для формалинизации эритроцитов объем раствора формалина вычисляют по формуле: X=3V/C, где Х - искомый объем, V - объем приготовленной 8%-ной взвеси эритроцитов, С - процент формальдегида в используемом растворе формалина.
Для получения 3%-ного раствора формальдегида к Х мл раствора формалина приливают (V-X) мл 0,9%-ного раствора натрия хлорида.
В приготовленную 8%-ную взвесь эритроцитов при постоянном перемешивании приливают 3%-ный раствор формальдегида, подогретый до 37° С. Бутыль со смесью помещают в оригинальный аппарат для формалинизации эритроцитов, автоматически поддерживающий температуру воды водяной бани и обеспечивающий непрерывное перемешивание воды в бане и эритроцитов внутри бутыли. Формалинизацию проводят при 37° С в течение 18 ч. Затем формалинизированные эритроциты четырежды отмывают в 10-кратном объеме 0,9%-ного раствора натрия хлорида путем 15-минутного центрифугирования при 1100 g. Плотный осадок разводят в 10 раз 0,9%-ным раствором натрия хлорида. 10%-ную взвесь формалинизированных эритроцитов консервируют добавлением формальдегида до конечной концентрации 0,8%. Хранят при 4° С в течение 3-5 лет. Для приготовления эритроцитарного диагностикума оптимальными являются эритроциты после хранения в течение года.
Перед использованием эритроциты контролируют на гомогенность и отсутствие склонности к спонтанному склеиванию. Для контроля гомогенности эритроциты разводят 0,9%-ным раствором натрия хлорида и одну каплю 0,5%-ной взвеси эритроцитов наносят на предметное стекло, покрывают покровным стеклом и рассматривают при малом увеличении микроскопа. Эритроциты должны лежать изолированно, допускается 2-3 скопления, содержащие не более 10 эритроцитов в 10 полях зрения. Отсутствие склонности к спонтанному склеиванию: к 0,4 мл 0,9%-ного раствора натрия хлорида в полистироловой пластине добавляют 0,05 мл 2,5%-ной взвеси эритроцитов, гомогенизируют и оставляют при комнатной температуре на 2-3 ч. Эритроциты должны выпасть в осадок в виде "пуговки" или небольшого колечка с ровным краем. В случае появления спонтанной агглютинации серия эритроцитов бракуется.
3. Приготовление диагностикума эритроцитарного туляремийного иммуноглобулинового
Необходимое количество 10%-ных формалинизированных эритроцитов отмывают от формалина 0,9%-ным раствором натрия хлорида (рН 7,2) путем 4-кратного 15-минутного центрифугирования при 1100 g. Затем эритроциты разводят подогретым до 37° С 0,9%-ным раствором натрия хлорида (рН 7,2) до концентрации 5%. К полученной взвеси при постоянном перемешивании добавляют равный объем раствора танина в разведении 1:20000. Танизацию проводят в течение 15 мин при температуре взвеси 37° С.
Взвесь отмывают 0,9%-ным раствором натрия хлорида (рН 6,4) путем 3-кратного 20-минутного центрифугирования при 1100 g. Затем эритроциты разводят 0,9%-ным раствором натрия хлорида (рН 6,4) до концентрации 5%.
Перед приготовлением основной партии диагностикума для данной серии формалинизированных эритроцитов и данной серии иммуноглобулина определяют оптимальную сенсибилизирующую дозу последнего. Для этого 16 мл полученных эритроцитов разливают по 4 мл в 4 пробирки. Аликвоту приготовленного иммуноглобулина разводят 0,9%-ным раствором натрия хлорида (рН 6,4) до 10, 20, 40, 80 мкг/мл и добавляют по 4 мл каждой концентрации в пробирки с эритроцитами (по одной концентрации иммуноглобулина на пробирку).
После 20-часовой инкубации при 4° С сенситин закрепляют в течение 2 ч добавлением формальдегида до конечной концентрации 0,4%. Пробирки с сенсибилизированными эритроцитами 4-кратно отмывают 0,9%-ным раствором натрия хлорида (рН 7,2) путем 10-минутного центрифугирования при 1100 g.
Полученные эритроциты, сенсибилизированные различными концентрациями иммуноглобулина, проверяют в РНГА с убитыми культурами F. tularensis штаммов 15 НИИЭГ, Schu, 503, 543 на чувствительность, а также с инактивированными культурами Brucella, Yersinia, Vibrio, Salmonella, Escherihia на специфичность. Постановку РНГА осуществляют согласно инструкции по применению препарата. Оптимальной сенсибилизирующей дозой иммуноглобулина считают ту, при которой получают диагностикум, обладающий наиболее высокой чувствительностью и не выявляющий культуры вышеперечисленных гетерологичных микроорганизмов в их концентрации 1· 108 м.к./мл.
Для приготовления основной партии диагностикума к 5%-ной взвеси танизированных эритроцитов при постоянном перемешивании добавляют равный объем, содержащий 1,5 оптимальные дозы иммуноглобулина в 0,9%-ном растворе натрия хлорида (рН 6,4). После 20-часовой инкубации при 4° С сенситин закрепляют в течение 2 ч добавлением формальдегида до конечной концентрации 0,4%. Препарат 4-кратно отмывают 0,9%-ным раствором натрия хлорида (рН 7,2) путем 20-минутного центрифугирования при 1100 g и тем же раствором доводят до 10%-ной концентрации. Консервант - азид натрия 1:5000.
4. Лиофильное высушивание приготовленного диагностикума
Приготовленный препарат осаждают 10-минутным центрифугированием при 1100 g, осадок ресуспендируют в 10%-ном растворе сахарозы, центрифугируют 30 мин при 1100 g.
Для приготовления среды высушивания в 650,0 мл дистиллированной воды растворяют 100,0 г сахарозы, 10,0 г БСА, 10,0 г тетраборнокислого натрия и 1,0 г натрия азида. К полученному раствору под контролем рН и при постоянном перемешивании приливают (100,0±20,0) мл 3%-ного раствора янтарной кислоты до получения значения рН (7,0±0,1). Объем доводят дистиллированной водой до 900,0 мл, раствор тщательно перемешивают и хранят при 4° С не более одного года.
Осадок отмытых 10%-ным раствором сахарозы эритроцитов разводят средой высушивания до 10%-ной концентрации и разливают в ампулы по (1,0±0,5) мл.
Установленные в кассеты ампулы с диагностикумом помещают на полки предварительно охлажденной до температуры минус (30±2)° С сублимационной камеры аппарата сублимационной сушки "МАСС-5". Камеру герметично закрывают. Диагностикум замораживают в течение (2,5±0,5) ч до достижения температуры материала не выше минус 25° С, затем создают в камере вакуум, поддерживаемый в течение всего процесса лиофильного высушивания на уровне 1,1-1 Торр (13,33 н/м2). Через (2±0,5) ч включают подогрев всех полок. Через 1 ч полки прогреваются до температуры (28±1)° С, поддерживаемой до конца лиофильного высушивания, при этом температура в ампуле с диагностикумом через (13±1) ч также достигает (28±1)° С, после чего лиофильное высушивание продолжают в течение (6±0,5) ч. Продолжительность лиофильного высушивания диагностикума - (21±1) ч. По окончании процесса ампулы запаивают и контролируют качество сухого диагностикума по следующим параметрам:
4.1. Растворимость - при добавлении в ампулу 4,0 мл 0,9%-ного раствора натрия хлорида препарат должен раствориться в течение 1 мин.
4.2. РН - должен находиться в пределах (7,0±0,2).
4.3. Потеря в массе при высушивании - не более 3%.
4.4. Гомогенность ресуспендированного препарата - под малым увеличением микроскопа - не более 3 скоплений по 10 и менее эритроцитов в 10 полях зрения.
4.5. Отсутствие спонтанной гемагглютинации - при добавлении к помещенным в лунку пластинам для постановки РНГА макрометодом 0,4 мл 0,9%-ного раствора натрия хлорида, 0,05 мл 2,5%-ной взвеси эритроцитов через 3 ч должна образоваться пуговка или узкое колечко.
4.6. Количество эритроцитов - в 1,0 мл 2,5%-ного диагностикума (5,4±0,6)· 105 м.к./мл.
4.7. Чувствительность - должен выявлять F. tularensis в концентрации 3,12· 106 м.к./мл макрометодом и 6,25· 106 м.к./мл микрометодом в РНГА.
4.8. Специфичность - не должен выявлять в РНГА культуры Brucella, Yersinia, Vibrio, Salmonella, Escherihia в концентрации 1,0· 108 м.к./мл, инактивированные 20-минутным кипячением и добавлением формалина до конечной концентрации 2%.
4.9. Качество герметизации ампул - в соответствии с МУК 4.1/4.2.588-96, с.63-65.
Гарантийный срок хранения диагностикума при температуре от 2 до 10° С составляет 2 года.
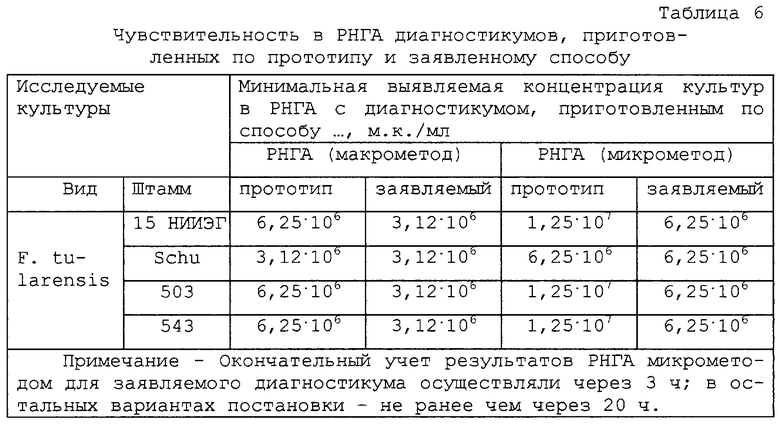
Сравнительную оценку специфичности и чувствительности в РНГА туляремийных иммуноглобулиновых эритроцитарных диагностикумов, приготовленных по предлагаемому способу и прототипу, проводили с культурами F. tularensis (штаммов 15 НИИЭГ, Schu, 503, 543), Br. abortus (штамма 19-ВА), Y. pestis (штамма EV), V. cholerae (штамма 569-B), S. typhimurium (штамма 1), E. coli (штамма НВ-101). Постановку РНГА микро- и макрометодами осуществляли согласно инструкции по применению препарата со следующими особенностями: для оценки чувствительности штаммы F. tularensis титровали с двукратным шагом с 1-й по 9-ю лунку включительно, начиная с концентрации 5,0· 107 м.к./мл, а штаммы гетерокультур для проверки специфичности использовали в концентрациях 1,0· 109, 2,0· 108 и 4,0· 107 м.к./мл каждый.
Результаты исследования специфичности, представленные в таблице 5, свидетельствуют о том, что заявляемый образец при данных условиях не давал положительных реакций в РНГА ни с одним из исследованных гетерологичных микроорганизмов. В отличие от этого, диагностикум-прототип перекрестно реагировал со всеми штаммами гетерокультур. Для S. typhimurium минимальная выявляемая концентрация составила 1,0· 109 м.к./мл, а со штаммами бруцеллезного и чумного микробов положительная реакция наблюдалась даже в их концентрации 4,0· 107 м.к./мл. Что касается чувствительности, то, как следует из данных, приведенных в таблице 6, прототип проявлял соответствующую требованиям НТД чувствительность лишь в отношении штамма Schu туляремийного микроба, тогда как заявляемый образец - в отношении всех исследуемых штаммов.
Анализ полученных данных позволяет сделать вывод, что диагностикум, приготовленный по прототипу, уступая по чувствительности заявляемому образцу, обладает значительно худшими специфическими свойствами. Столь низкая специфичность является существенным недостатком прототипа.
Диагностическая ценность полученного препарата была изучена в ходе Государственных испытаний. В соответствии с Программой испытаний диагностикума эритроцитарного туляремийного иммуноглобулинового сухого серий 1, 2, 3 материалами для исследования служили культуры F. tularensis (штаммы 15 НИИЭГ, Schu, 503, А-108 из коллекции ГИСК им. Л.А. Тарасевича; 15 НИИЭГ из коллекции НИИМ МО РФ, входящий в комплект поставки диагностикума), а также Br. abortus (штамм 19-ВА), V. cholerae (штамм 569-В), Е. coli (штамм 18), S. typhi enteritidis (штамм ВОЗ), Y. enterocolitica (штамм 237 серовар 09) из коллекции ГИСК им. Л.А.Тарасевича.
Полученные результаты показали, что испытуемый препарат имеет значительные преимущества перед прототипом по следующим показателям:
по специфичности: диагностикум, приготовленный по заявляемому способу, не реагирует РНГА с культурами гетерологичных микроорганизмов (Brucella, Yersinia, Vibrio, Salmonella, Escherihia) в концентрациях 2,0· 108 м.к./мл и 1,0· 109 м.к./мл, в то время как диагностикум-прототип перекрестно реагирует в обеих концентрациях со всеми исследуемыми гетерокультурами за исключением S. typhimurium;
по чувствительности: заявляемый образец позволяет идентифицировать в РНГА F. tularensis штаммов 15 НИИЭГ, Schu, 503, 543 в концентрации 3,12· 106 м.к./мл макрометодом и 6,25· 106 м.к./мл микрометодом, тогда как прототип выявляет в данной концентрации только F. tularensis штамма Schu;
по времени получения результатов: результаты РНГА с испытуемым препаратом учитывали через 3 ч для микрометода окончательно, для макрометода - предварительно с окончательным учетом через 20 ч (предварительный и окончательный результаты совпадали); с диагностикумом-прототипом окончательный учет результатов был возможен не ранее чем через 20 ч.
Полученные результаты подтвердили соответствие чувствительности и специфичности заявляемого диагностикума данным, приведенным в таблицах 3 и 4, а также показали, что испытуемый препарат соответствует требованиям ФС 42-308 ВС-90 и разработанному проекту НТД по следующим показателям:
по внешнему виду: аморфная пористая масса коричневого цвета;
по растворимости, прозрачности и цветности: растворим в течение 1 мин при добавлении в ампулу 4,0 мл 0,9%-ного раствора натрия хлорида, при встряхивании - гомогенная коричневая взвесь;
по концентрации эритроцитов в препарате: во всех трех сериях в пределах 5,4· 105±0,6· 105 клеток в 1 мл.
Результаты Государственных испытаний позволили рекомендовать внедрение в практику здравоохранения диагностикума эритроцитарного туляремийного иммуноглобулинового сухого, изготовленного по заявляемому способу, и оформить всю необходимую нормативно-техническую документацию ("Регламент производства диагностикума эритроцитарного туляремийного иммуноглобулинового сухого", "Фармакопейная статья", "Инструкция по применению"). Регламент производства диагностикума эритроцитарного туляремийного иммуноглобулинового сухого зарегистрирован за номером РП №1018-00. Фармакопейная статья на диагностикум эритроцитарный туляремийный иммуноглобулиновый сухой зарегистрирована за номером ФС 42-3951-00.
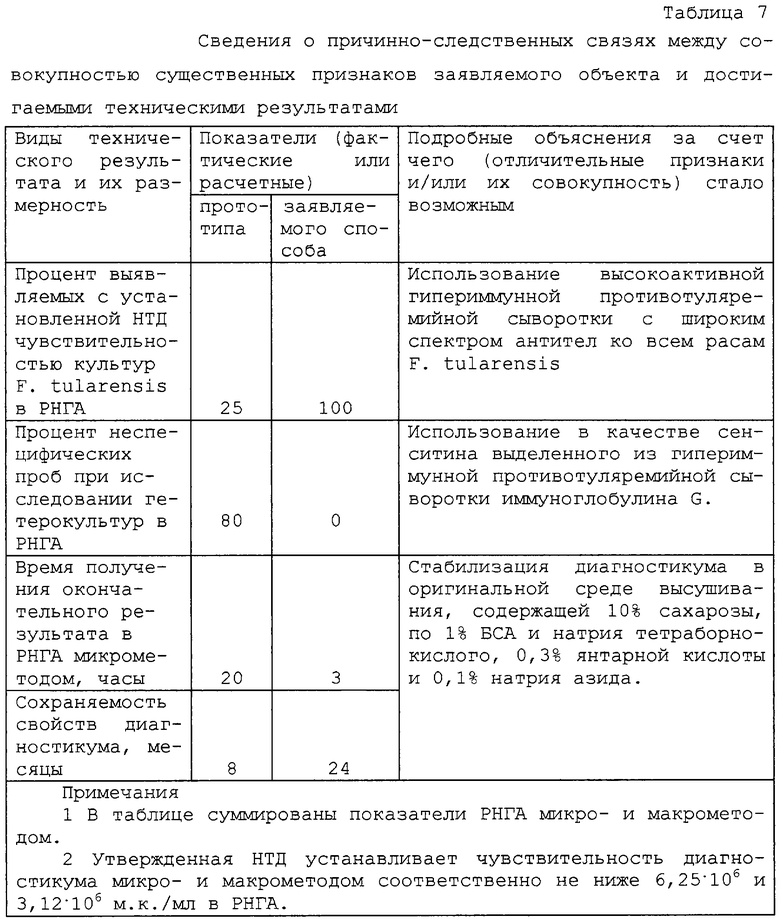
Наличие причинно-следственной связи между совокупностью существенных признаков заявляемого объекта и достигаемыми техническими результатами показано в таблице 7. Из ее анализа следует, что туляремийный эритроцитарный диагностикум, приготовленный по заявляемому способу, показывает результаты, существенно превосходящие прототип по специфичности и стабильности свойств при хранении.
Возможность осуществления предложенного способа может быть продемонстрирована следующим примером.
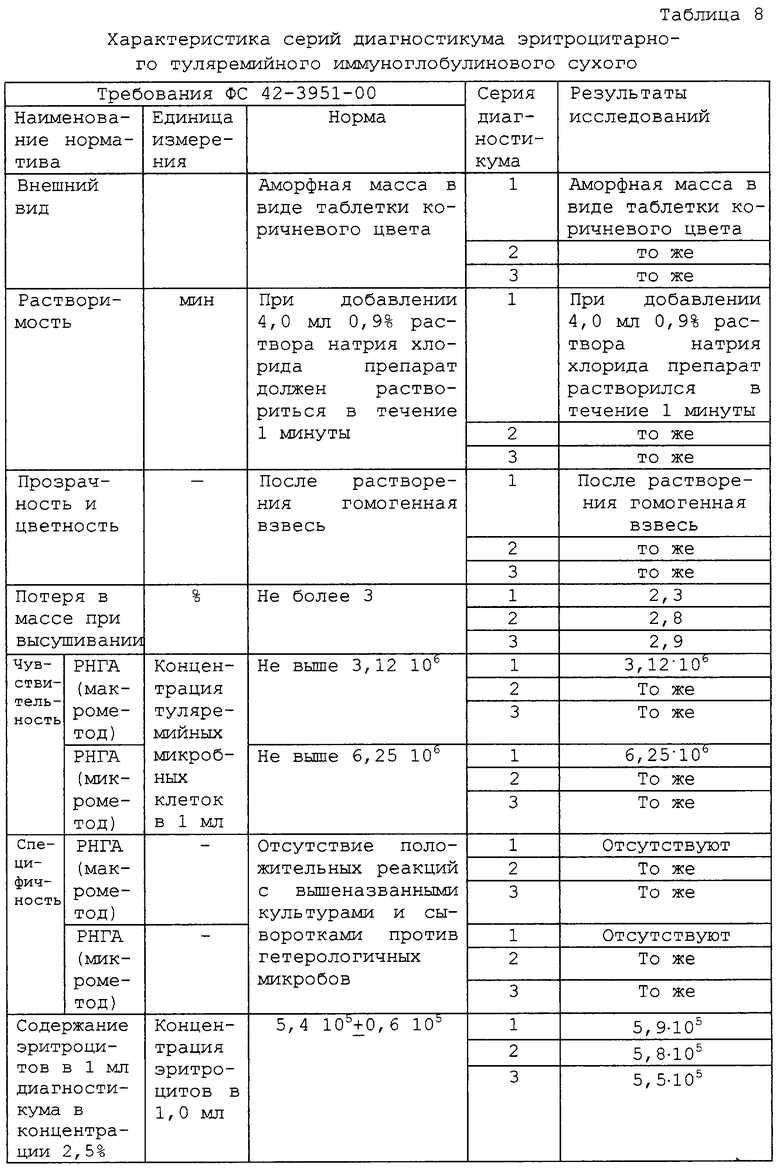
На АТЛ, созданной в НИИ микробиологии МО РФ, были приготовлены 3 серии эритроцитарного туляремийного иммуноглобулинового диагностикума в соответствии с утвержденной нормативно-технической документацией. Характеристика серий представлена в таблице 8.
Из представленных в таблице 8 данных следует, что все серии эритроцитарного туляремийного иммуноглобулинового диагностикума полностью отвечали требованиям ФС 42-3951-00.

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРИГОТОВЛЕНИЯ ЭРИТРОЦИТАРНОГО ДИАГНОСТИКУМА ИММУНОГЛОБУЛИНОВОГО ТУЛЯРЕМИЙНОГО | 2020 |
|
RU2747420C1 |
| УНИВЕРСАЛЬНАЯ СРЕДА ВЫСУШИВАНИЯ ДЛЯ СТАБИЛИЗАЦИИ ЭРИТРОЦИТАРНЫХ ДИАГНОСТИКУМОВ ТУЛЯРЕМИЙНЫХ | 2019 |
|
RU2708636C1 |
| СПОСОБ ЛИОФИЛИЗАЦИИ ЭРИТРОЦИТАРНЫХ ДИАГНОСТИКУМОВ ТУЛЯРЕМИЙНЫХ | 2020 |
|
RU2749355C1 |
| ШТАММ КУЛЬТИВИРУЕМЫХ ГИБРИДНЫХ КЛЕТОК ЖИВОТНОГО MUS MUSCULUS - ПРОДУЦЕНТ МОНОКЛОНАЛЬНОГО АНТИТЕЛА К ТЕРМОСТАБИЛЬНОМУ АНТИГЕНУ, ОБЩЕМУ ДЛЯ ВОЗБУДИТЕЛЕЙ САПА И МЕЛИОИДОЗА | 1997 |
|
RU2117043C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАГНОСТИКУМА ЭРИТРОЦИТАРНОГО АНТИГЕННОГО САПНОГО | 2001 |
|
RU2188036C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАГНОСТИКУМА ЭРИТРОЦИТАРНОГО САПНОГО ИММУНОГЛОБУЛИНОВОГО МОНОКЛОНАЛЬНОГО | 2017 |
|
RU2658434C1 |
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРА, ИСПОЛЬЗУЕМОГО В КАЧЕСТВЕ РАЗВОДЯЩЕЙ ЖИДКОСТИ И СРЕДЫ ВЫСУШИВАНИЯ ЭРИТРОЦИТАРНЫХ И ЛАТЕКСНЫХ ДИАГНОСТИКУМОВ | 2009 |
|
RU2395094C1 |
| ДИАГНОСТИКУМ ПСЕВДОТУБЕРКУЛЕЗНЫЙ ЭРИТРОЦИТАРНЫЙ МОНОКЛОНАЛЬНЫЙ | 2008 |
|
RU2377308C1 |
| НАБОР ШТАММОВ БАКТЕРИЙ ВИДА FRANCISELLA TULARENSIS ДЛЯ ПОЛУЧЕНИЯ КОМПЛЕКТА КОНТРОЛЬНЫХ ДНК ПРЕПАРАТОВ, КОМПЛЕКТ ДНК ПРЕПАРАТОВ ДЛЯ ГЕННО-ДИАГНОСТИЧЕСКИХ ИССЛЕДОВАНИЙ | 2010 |
|
RU2443772C1 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИГЕННОГО ЭРИТРОЦИТАРНОГО ДИАГНОСТИКУМА ДЛЯ ОБНАРУЖЕНИЯ АНТИТЕЛ К АНТИГЕНАМ ВОЗБУДИТЕЛЕЙ САПА И МЕЛИОИДОЗА | 2013 |
|
RU2540902C1 |
Изобретение относится к области биотехнологии. Способ получения противотуляремийной гипериммунной сыворотки включает подкожную иммунизацию кроликов живой культурой F.Tularensis вакцинного штамма 15 НИИЭГ, забор крови и отделение сыворотки. Дополнительно готовят корпускулярный антиген из смеси инактивированных культур F.Tularensis вирулентного штамма Schu, F.Tularensis вирулентного штамма 503 и F.Tularensis вирулентного штамма 543. Иммунизацию кроликов осуществляют по следующей схеме: двукратно иммунизируют путем подкожного введения смеси корпускулярного антигена с неполным адъювантом Фрейнда, затем трехкратно - путем внутривенного введения корпускулярного антигена без адъюванта, после чего кроликам двукратно внутривенно вводят живую культуру F.Tularensis вакцинного штамма 15 НИИЭГ. Способ получения диагностикума эритроцитарного туляремийного иммуноглобулинового сухого включает выделение иммуноглобулинов из противотуляремийной гипериммунной сыворотки, подготовку эритроцитов барана, сенсибилизацию эритроцитов барана выделенными иммуноглобулинами и лиофильное высушивание полученного эритроцитарного диагностикума. При этом из противотуляремийной гипериммунной сыворотки, полученной по п.1, выделяют иммуноглобулины G, которыми и сенсибилизируют эритроциты барана. Лиофильное высушивание полученного диагностикума осуществляют в среде, содержащей следующие компоненты (мас.%): сахароза 10; бычий сывороточный альбумин 1; натрий тетраборнокислый 1; янтарная кислота 0,3; натрия азид 0,1; дистиллированная вода остальное. Полученные сыворотка и диагностикум обладают высокой активностью и специфичностью, сыворотка безвредна, а диагностикум отличается высокой стабильностью. 2 н.п. ф-лы, 8 табл.
Сахароза 10
Бычий сывороточный альбумин 1
Натрий тетраборно-кислый 1
Янтарная кислота 0,3
Натрия азид 0,1
Дистиллированная вода Остальное
| ХЛЕБНИКОВ В.С | |||
| и др | |||
| Изучение биохимических, антигенных и протективных свойств внешней мембраны возбудителя туляремии | |||
| Молекулярная генетика, микробиология и вирусология | |||
| Циркуль-угломер | 1920 |
|
SU1991A1 |
| Канальная печь-сушильня | 1920 |
|
SU230A1 |
| Справочник по микробиологическим и вирусологическим методам исследования | |||
| Под ред | |||
| БИРГЕРА М.О | |||
| - М.: Медицина, 1973, с.285-289. | |||
Авторы
Даты
2004-11-27—Публикация
2002-07-17—Подача