Изобретение относится к способам определения массовой доли сернокислого и азотнокислого кальция в аммиачной селитре с доломитно-сульфатной добавкой.
Известен способ определения суммы азотнокислых кальция и магния в пересчете на СаО из водного раствора [1. ГОСТ 2-85 “Селитра аммиачная”]. Повышение прочности гранул в селитре с доломитно-сульфатной добавкой достигается за счет ввода серной кислоты в плав селитры с доломитной добавкой и переводе азотнокислого кальция в сернокислый. Одновременно с повышением прочности гранул, при этом снижаются выбросы вредных веществ в атмосферу и пылеобразование. Очень важно при этом контролировать массовую долю сернокислого кальция в аммиачной селитре повышенной прочности, она должна быть не менее 0,9 %.
Недостатком известного способа является невозможность раздельного определения CaSO4 и Ca(NO3)2 в селитре с доломитно-сульфатной добавкой.
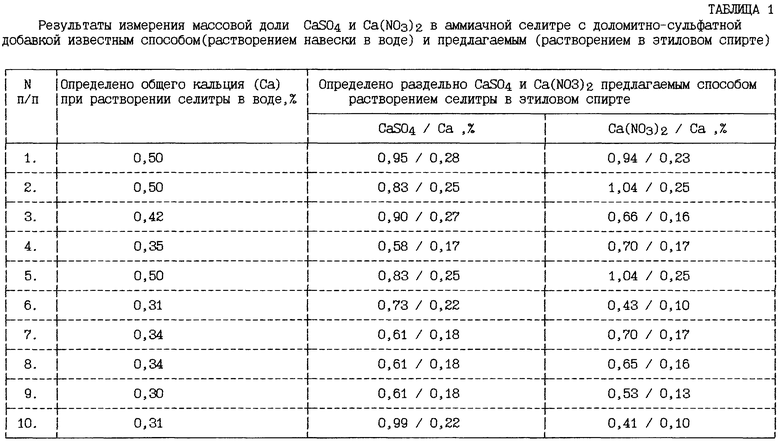
Известен способ определения массовой доли азотнокислого и сернокислого кальция, заключающийся в растворении пробы селитры с последующим комплексонометрическим титрованием ионов кальция с индикатором хромом темно-синим при рH 9,5-10,0, создаваемом буферным раствором [2. Г.Реми "Курс неорганической химии", изд-во "Мир", М., 1972 г., стр. 282 - прототип]. Хотя растворимость сернокислого кальция в воде незначительна (202 мг в 100 г воды), определение его непосредственно из водного раствора отделением осадка фильтрованием невозможно, так как в воде в присутствии солей аммония и серной кислоты растворимость сульфата кальция значительно повышается. С серной кислотой CaSO4 образует растворимые в воде продукты присоединения, например CaSO4,H2SO4 и CaSO4, 3H2SO4. Поэтому селитра, полученная добавлением серной кислоты в плав с доломитной добавкой, растворяется в воде без остатка и титрованием трилоном Б определяется весь имеющийся в пробе кальций. (Таблица 1).
Осуществить раздельное определение CaSO4 и Са(NO3)2, а следовательно, и контроль за степенью превращения азотнокислого кальция в сернокислый из водного раствора невозможно, что затрудняет управление процессом выпуска аммиачной селитры повышенной прочности.
В основу изобретения поставлена задача усовершенствования способа определения массовой доли сернокислого и азотнокислого кальция в аммиачной селитре путем разделения сернокислого и азотнокислого кальция за счет их различной растворимости в этиловом спирте, в котором Ca(NO3)2 хорошо растворяется, a CaSO4 практически нерастворим.
Поставленная задача достигается тем, что в способе определения массовой доли сернокислого и азотнокислого кальция, заключающемся в растворении пробы селитры с последующим комплексонометрическим титрованием ионов кальция с индикатором хромом темно-синим при рH 9,5-10,0, создаваемом буферным раствором, согласно изобретению при подготовке пробы к титрованию ее обрабатывают этиловым спиртом в массовом соотношении пробы к этиловому спирту 2:39,45, осадок нерастворимого в спирте сернокислого кальция отделяют фильтрованием, растворяют в соляной кислоте и определяют сернокислый кальций в соляно-кислом растворе, азотнокислый - в спиртовом фильтрате титрованием трилоном Б.
Использование этилового спирта в качестве растворителя позволяет выделить из селитры сернокислый кальций в виде осадка, азотнокислый кальций совместно с магнием, содержащимся в доломите, перевести в спиртовый раствор.
Определение массовой доли сернокислого кальция в аммиачной селитре повышенной прочности с доломитпо-сульфатной добавкой проводят следующим образом.
2 г тщательно растертой аммиачной селитры взвешивают, результат взвешивания записывают с точностью до четвертого десятичного знака, переносят в сухой стакан вместимостью 300 см3, приливают 50 см3 этилового спирта и перемешивают содержимое стакана на магнитной мешалке в течение 30-40 минут до растворения навески.
Не растворившийся в спирте осадок сернокислого кальция отфильтровывают через двойной фильтр “синяя лента”, собирая фильтрат в коническую колбу для титрования вместимостью 250 см3. Осадок промывают 20 см3 этилового спирта, присоединяя промывной раствор к основному фильтрату. Если в фильтрат перешла часть осадка, фильтрование повторяют.
Фильтрат сохраняют для определения массовой доли азотнокислых кальция и магния. Фильтр с осадком помещают в химический стакан, в котором производили растворение, приливают 10 см3 раствора соляной кислоты, 50 см3 дистиллированной воды и нагревают содержимое стакана до полного растворения осадка. Раствор в колбе охлаждают, нейтрализуют аммиаком до рН = 7,0 по индикаторной бумаге, приливают 20 см3 буферного раствора, 2-3 капли раствора хрома темно-синего и титруют раствором трилона Б молярной концентрации с (Na2H2Y·2Н2O)=0,05 моль/дм3 до перехода красно-фиолетоной окраски в синюю.
Массовую долю сернокислого кальция (X1) в % вычисляют по формуле:

где V - объем раствора трилона Б кон пен грации с (Na2H2Y·2H2O)=0,05 мoль/дм3, израсходованный на титрование кальция, см3;
К - поправочный коэффициент для приведения действительной молярной концентрации раствора трилона Б к номинальной с (Na2H2Y·2Н2O)=0,05 моль/дм3;
0,006807 - масса сернокислого кальция, соответствующая 1 см3 раствора трилона Б концентрации точно с (Na2H2Y·2Н2O)=0,05 моль/дм3, г;
m - масса навески селитры, г.
Пределы допускаемого значения относительной суммарной погрешности результата измерения +1,4% при доверительной вероятности Р=0,95 для массовой доли сернокислого кальция 0,80%.
За результат измерения массовой доли сернокислого кальция принимают среднее арифметическое результатов двух параллельных определений, абсолютное значение расхождения между которыми не превышает значения допустимого расхождения, равного +0,045% для массовой доли 0,80%.
Определение массовой доли азотнокислых кальция и магния проводят следующим образом: к спиртовому фильтрату, полученному после отделения сернокислого кальция, добавляют 20 см3 аммиачного буферного раствора. 2-3 капли хрома темно-синего и титруют раствором трилона Б молярной концентрации с (Na2H2Y·2Н2O)=0,05 моль/дм3 до перехода красно-фиолетовой окраски в синюю.
Массовую долю азотнокислых кальция и магния в пересчете на азотнокислый кальций (Х2) в % вычисляют по формуле:
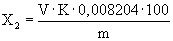
где V - объем раствора трилона Б концентрации с (Na2H2Y·2Н2О)=0,05моль/дм3, израсходованный на титрование см3;
К - поправочный коэффициент для приведения действительной молярной концентрации раствора трилона Б к номинальной с (Na2H2Y·2Н2O)=0,05 моль/дм3;
0,008204 - масса азотнокислого кальция, соответствующая 1 см3 раствора трилона Б концентрации точно с (Na2H2Y·2H2О)=0,05 моль/дм3, г;
m - масса навески селитры, г.
Пределы допускаемого значения относительной суммарной погрешности результата измерения +1,6% при доверительной вероятности Р=0,95 для массовой доли азотнокислого кальция 0,42%.
За результат измерения массовой доли азотнокислых кальция и магния принимают среднее арифметическое результатов двух параллельных определений, абсолютные значения расхождения между которыми не превышает значения допустимого расхождения, равного +0,029% для массовой доли 0,42%,
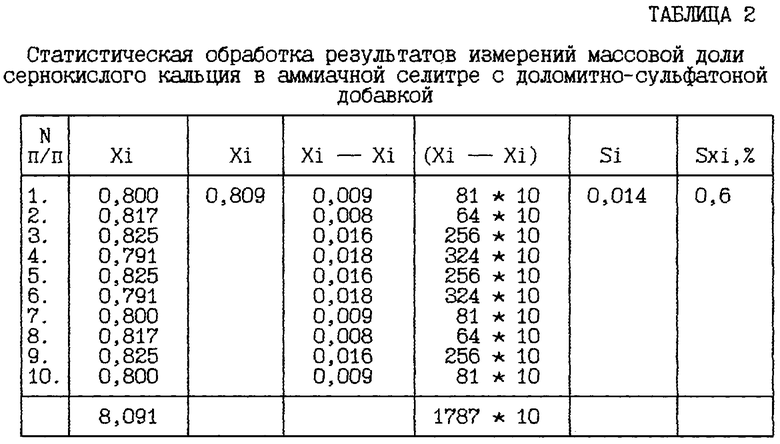
Для оценки случайной составляющей погрешности проводили десятикратные измерения одной и той же пробы аммиачной селитры по массовой доле сернокислого и азотнокислого кальция.
Статистическую обработку экспериментальных данных проводили в соответствии с ГОСТ 8,207-76 “Методы обработки результатов наблюдений и МУ 6/133-80-19-83 “Нормируемые показатели точности измерений в методиках выполнения измерений, регламентируемых в документации на химическую продукцию”. Результаты представлены в таблицах 2, 3.
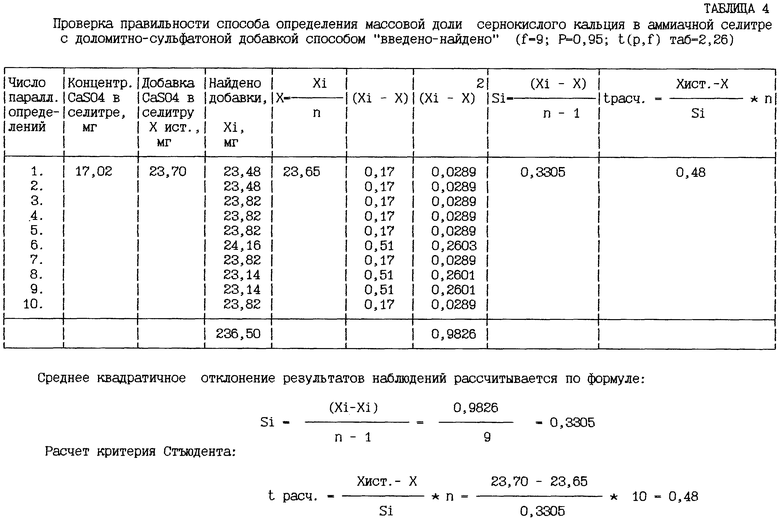
Для оценки методической систематической погрешности результата измерения (правильности методики) использовали метод “введено-найдено”, основанный на доказательстве того, что между результатами анализа (X) и истинным значением определяемого содержания (Хист.) нет статистически значимой разницы (MУ 113-03-1-84. Порядок проведения и содержание работ по метрологической аттестации методик выполнения измерений).
Сравнение значений Х и Хист. проводили с помощью критерия Стьюдента. Обработке подвергались результаты наблюдений, представленные в таблице 4.
По данным, приведенным в таблице, tрасч. меньше tтабл (0,48<2,26) и, следовательно, полученные данные не содержат методической (исключаемой) систематической погрешности.
Таким образом, предлагаемым способом можно с высокой точностью выполнить раздельное определение массовой доли сернокислого и азотнокислого кальция в аммиачной селитре повышенной прочности с доломитно-сульфатной добавкой.
Среднее квадратичное отклонение результатов наблюдений рассчитывается по формуле:
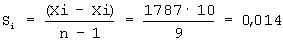
Среднее квадратичное отклонение результата измерения с учетом числа наблюдений вычисляется по формуле:

Доверительные границы случайной составляющей погрешности результата измерения рассчитываются по формуле:
Ei=t(n,p)·Sxi,
где t - коэффициент Стьюдента, зависящий от доверительной вероятности и представительности выборки.
Для n=10 p=0,95 t=2,26 Ei=2,26·0,6=1,4%
Допускаемые расхождения между результатами параллельных наблюдений рассчитываются по формуле:
d=k·Si,
где k - коэффициент, зависящий от доверительной вероятности, представительности выборки и числа параллельных наблюдении.
При P=0,95, для F=9, K=3,199
d=3,19·0,014=0,045%

Среднее квадратичное отклонение результатов наблюдений рассчитывается по формуле

Среднее квадратичное отклонение результата измерения с учетом числа наблюдений вычисляется по формуле
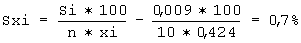
Доверительные границы случайной составляющей погрешности результата измерения рассчитывается по формуле:
Ei=t(n,p)·Sxi,
где t - коэффициент Стьюдента, зависящий от доверительной вероятности и представительности выборки.
Для n=10 p=0,95 t=2,26
Ei=2,26·0,7=1,6%
Допускаемые расхождения между результатами параллельных наблюдений рассчитываются по формуле:
d=k·Si,
где k - коэффициент, зависящий от доверительной вероятности, представительности выборки и числа параллельных наблюдении.
При P=0,95, для F=9, K=3,199
d=3,199·0,009=0,029%
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ МАССОВОЙ ДОЛИ АЗОТНОКИСЛОГО И УГЛЕКИСЛОГО КАЛЬЦИЯ В ИЗВЕСТКОВО-АММИАЧНОЙ СЕЛИТРЕ | 1999 |
|
RU2159932C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КАЛЬЦИЯ В КОРМОВЫХ ДОБАВКАХ | 2015 |
|
RU2601569C1 |
| Способ определения кальция в водных растворах | 1989 |
|
SU1691731A1 |
| РЕАГЕНТ ДЛЯ АВТОМАТИЧЕСКОГО ФОТОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ ОБЩЕЙ ЖЕСТКОСТИ ВОДЫ (ВАРИАНТЫ) | 2003 |
|
RU2233439C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОЧНЫХ ГРАНУЛ АММИАЧНОЙ СЕЛИТРЫ | 2001 |
|
RU2241691C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КАЧЕСТВА ИЗВЕСТКОВОГО МОЛОКА, СОДЕРЖАЩЕГО САХАР | 2003 |
|
RU2231556C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ МАРГАНЦА В СИККАТИВЕ | 1994 |
|
RU2069856C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ МАГНИЯ В МАСЛАХ | 2005 |
|
RU2278380C1 |
| СПОСОБ РАЗДЕЛЬНОГО ОПРЕДЕЛЕНИЯ 0-2-ЭТИЛГЕКСИЛМЕТИЛФОСФОНАТОВ ЦИНКА И КАЛЬЦИЯ В ПРЕПАРАТЕ "СТАБФОН" | 1991 |
|
RU2011197C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ МАССОВОЙ ДОЛИ ОСНОВНОГО ВЕЩЕСТВА ДИАЛКИЛОВЫХ ЭФИРОВ АЛКИЛФОСФОНОВЫХ КИСЛОТ | 2006 |
|
RU2320989C1 |
Область использования: изобретение может использоваться в химической промышленности. Сущность изобретения: заключается в растворении пробы селитры с последующим комплексонометрическим титрованием трилоном Б ионов кальция с индикатором хромом темно-синим при рН=9,5-10,0, создаваемом аммиачным буферным раствором. В качестве растворителя используется этиловый спирт в массовом соотношении пробы к этиловому спирту 2:39,45. Разделение определяемых компонентов осуществляется за счет их различной растворимости в этиловом спирте, в котором Са(NO3)2 хорошо растворяется, а CaSQ4 практически не растворим. Осадок нерастворимого в спирте сернокислого кальция отделяют фильтрованием, растворяют в соляной кислоте и определяют сернокислый кальций в солянокислом растворе, азотнокислый кальций – в спиртовом фильтрате. Технический результат: изобретение позволяет с высокой точностью выполнить раздельное определение сернокислого и азотнокислого кальция в аммиачной селитре повышенной прочности с доломитно-сульфатной добавкой. 4 табл.
Способ определения массовой доли сернокислого и азотнокислого кальция в аммиачной селитре повышенной прочности с доломитно-сульфатной добавкой, заключающийся в растворении пробы селитры с последующим комплексонометрическим титрованием ионов кальция с индикатором хромом темно-синим при рН 9,5 10,0, создаваемом буферным раствором, отличающийся тем, что при подготовке пробы к титрованию ее обрабатывают этиловым спиртом в массовом соотношении пробы к этиловому спирту 2:39,45, осадок нерастворимого в спирте сернокислого кальция отделяют фильтрованием, растворяют в соляной кислоте и определяют сернокислый кальций в солянокислом растворе, азотнокислый - в спиртовом фильтрате титрованием трилоном Б.
| РЕМИ Г | |||
| Курс неорганической химии | |||
| - М.: Мир, 1972, с | |||
| ПОРШНЕВОЙ ДВИГАТЕЛЬ | 1916 |
|
SU282A1 |
| Способ количественного определения кальция и магния | 1959 |
|
SU129060A1 |
| СПОСОБ КОМПЛЕКСОНОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ КАЛЬЦИЯ И МАГНИЯ | 0 |
|
SU237448A1 |
| Способ количественного определения кальция | 1957 |
|
SU110966A1 |
| Способ определения кальция в растворе в присутствии магния | 1949 |
|
SU80013A1 |
| Способ определения кальция в водных растворах | 1989 |
|
SU1691731A1 |
Авторы
Даты
2004-12-20—Публикация
2002-12-30—Подача