Изобретение относится к области медицины и может быть использовано для создания эффективного средства профилактики и лечения тромботических состояний (инфаркты, инсульты различной локализации).
В последнее десятилетие низкомолекулярные гепарины (НМГ) с более узким молекулярно-массовым распределением 4-6 кДа начали вытеснять нефракционированный гепарин как лекарственный препарат. Главное преимущество НМГ следует из их фармакокинетических свойств: в 2-4 раза большее время полувыведения из организма, заметно лучшая биодоступность при подкожном введении и более стабильная дозовая реакция (доза может быть рассчитана только исходя из веса пациента, без дополнительного лабораторного исследования). Меньший токсический эффект связан с вызываемой нефракционированным гепарином тромбоцитопенией, что в свою очередь обусловлено меньшим взаимодействием НМГ с тромбоцитами.
Известны разные способы получения НМГ: с низким выходом путем фракционирования природного препарата или с высоким выходом контролируемой деполимеризацией (т.е. при проверке молекулярной массы в ходе процесса возможна немедленная остановка реакции) [1]. Химическая деполимеризация в присутствии свободных радикалов позволяет получать НМГ с ММ около 5 кДа и олигогепарины около 2 кДа [2]. Окислительно-восстановительный процесс в присутствии Fe2+ при 50°С за 20 часов приводит к образованию фрагментов гепарина с ММ около 3 кДа [3]. Обработка гепарина комплексом ЭДТА с ионами железа и аскорбиновой кислотой при 37°С за 24 часа с выходом 65% дает низкомолекулярные гепарины, содержащие менее 30 сахарных звеньев. При этом авторами было продемонстрировано, что фрагменты с 20 и более сахарными остатками сохраняли существенный антикоагулянтный потенциал [4]. Эффективным методом получения НМГ с различной ММ может быть и гамма-излучение [5].
Наиболее близким по технической сущности является способ получения НМГ путем частичной деполимеризации α-гликозидных связей гепарина из слизистых оболочек свиньи с помощью гепариназы. Используемый в этом процессе фермент продуцируется Flavobacterium heparinum [6]. Получение НМГ - ферментативным путем, минимально затрагивающим структуру молекулы. На основе этого процесса получают препарат логипарин [1]. Однако в нашей стране не налажена культивация данного продукта, требующая тщательного подбора дорогостоящих импортных сред, в связи с этим использование гепариназы в нашей стране будет нерентабельно.
Цель изобретения - получение НМГ действием ферментного комплекса из Streptomyces kurssanovii, иммобилизованного на силохроме.
Культура Streptomyces kurssanovii содержит О-гликозид - гидролазы (КФ 3.2.1.), которые катализируют гидролитическое расщепление О-гликозидной связи по смешанному механизму. Культура растет на недорогих отечественных средах.
Сущность предложенного способа заключается в том, что раствор гепарина в ацетатном буфере рН 6,0 перемешивают с иммобилизованным препаратом культуральной жидкости (содержание белка 1,4 мг/г). Весовое соотношение ферментного препарата к навеске гепарина в пересчете на сухой вес сорбента 1:1. Суспензию перемешивают при 37°С в течение 3 часов. Иммобилизованный препарат отделяют центрифугированием, промывают 0,5 М NaCl и водой. Промывную жидкость присоединяют к супернатанту и обессоливают на колонке с сефадексом G-10 (размер столбика 2,5×42 см, уравновешивается водой, элюция проводится водой со скоростью 80 мл/ч, свободный объем 77 мл). Сушат лиофильно. С выходом около 70% получают гепарины с молекулярной массой на 50-75% ниже, чем у исходного гепарина.
Иммобилизацию ферментативного комплекса из Streptomyces kurssanovii осуществляли, используя реакцию азосочетания следующим образом: к 1 г аминоарильного производного силохрома (ВНИИЛ, фр. 0,1-0,16 мм, диаметр пор 1260 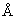 ) добавляют 20 мл 2,5 н НСl и 3 мл 14%-ного раствора NaNO2 при охлаждении (температура в бане 4°С), перемешивают в течение 30 мин. Затем промывают на стеклянном пористом фильтре водой (200 мл), 0,1 М фосфатным буфером рН 7,8 (100 мл), переносят в колбу и добавляют 15 мл культуральной жидкости Streptomyces kurssanovii (содержание белка 0,2 мг/мл). Перемешивают при охлаждении 4°С в течение 16 часов. Промывают на стеклянном пористом фильтре водой (200 мл), 1 М NaCl (200 мл) и вновь водой. Хранят в холодильнике в воде.
) добавляют 20 мл 2,5 н НСl и 3 мл 14%-ного раствора NaNO2 при охлаждении (температура в бане 4°С), перемешивают в течение 30 мин. Затем промывают на стеклянном пористом фильтре водой (200 мл), 0,1 М фосфатным буфером рН 7,8 (100 мл), переносят в колбу и добавляют 15 мл культуральной жидкости Streptomyces kurssanovii (содержание белка 0,2 мг/мл). Перемешивают при охлаждении 4°С в течение 16 часов. Промывают на стеклянном пористом фильтре водой (200 мл), 1 М NaCl (200 мл) и вновь водой. Хранят в холодильнике в воде.
Фермент из Streptomyces kurssanovii с целью деполимеризации гепарина использован нами впервые. При этом установлено, что анти-Ха-активность целевого продукта составляет 130-170 ед/мг, что соответствует удельной активности таких препаратов НМГ как фраксипарина (120-160 ед/мг) и дельтапарина (130-150 ед/мг).
Пример 1. К 10 мл 1% раствора гепарина (молекулярная масса 15 кДа) в 0,1 М ацетатном буфере рН 7,3 добавляют 340 мг иммобилизованного ферментного препарата (содержание белка 1,4 мг/г). Весовое соотношение ферментного препарата к навеске гепарина в пересчете на сухой вес сорбента 1:1. Суспензию перемешивают при 37°С в течение 3 часов. Иммобилизованный препарат отделяют центрифугированием, промывают 0,5 М NaCl и водой. Промывную жидкость присоединяют к супернатанту и обессоливают на колонке с сефадексом G-10 (2,5×42 см), элюент вода, скорость элюции 80 мл/ч, сушат лиофильно. Получают 70 мг (70% от исходного) с молекулярной массой 4,5 кДа. Анти-Ха-активность составила 160 ед/мг.
Пример 2. К 10 мл 1% раствора гепарина (с молекулярной массой 7,5 кДа) в 0,1 М ацетатном буфере рН 7,3 добавляют 680 мг иммобилизованного ферментного препарата (содержание белка 1,4 мг/г). Весовое соотношение ферментного препарата к навеске гепарина в пересчете на сухой вес сорбента 1:0,5. Суспензию перемешивают при 37°С в течение 3 часов. Иммобилизованный препарат отделяют центрифугированием, промывают 0,5 М NaCl и водой. Промывную жидкость присоединяют к супернатанту и обессоливают на колонке с сефадексом G-10 (2,5×42 см), элюент вода, скорость элюции 80 мл/ч, сушат лиофильно. Получают 66 мг (66% от исходного) с молекулярной массой 2,7 кДа. Анти-Ха-активность составила 120 ед/мг.
Литература.
1. Linhardt R., Loganathan O, Al-Hakim A., et al., J. Med. Chem., 33(6), 1639-1645, 1990.
2. Volpi N., Mascellani G., Bianchini P., Anal. Biochem., 200. 100-107, 1992.
3. Nagasawa K., Uchiyama H., Sato N., et al., Carbohydr. Res., 236, 165-180, 1992.
4. Lahiri В., Lai Р. Roiyama М., et al., Arch. Biochem. Biophys, 293, 54-60, 1992.
5. Jeske W. Lqbal O., Gonella S., et al., Semin. Tromb. Hemost, 21, 201-211, 1995.
6. Linhardt R., Grant F., Cooney С., et al., J.Biol. Chem., 257, 7310-7313, 1982.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ГЕПАРИНОВ С НИЗКОЙ МОЛЕКУЛЯРНОЙ МАССОЙ | 2005 |
|
RU2295538C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕПАРИНА С НИЗКОЙ МОЛЕКУЛЯРНОЙ МАССОЙ И АНТИКОАГУЛЯНТНОЙ АКТИВНОСТЬЮ | 2009 |
|
RU2396282C1 |
| СПОСОБ ПОЛУЧЕНИЯ НИЗКОМОЛЕКУЛЯРНОГО ГЕПАРИНА | 2007 |
|
RU2377993C2 |
| СПОСОБ ПОЛУЧЕНИЯ ФЕРМЕНТАТИВНОГО КОМПЛЕКСНОГО ПРЕПАРАТА, ОБЛАДАЮЩЕГО КОЛЛАГЕНАЗНОЙ АКТИВНОСТЬЮ | 2008 |
|
RU2412997C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА ПАПАИНА В ГЕЛЕ НА ОСНОВЕ ПИЩЕВОГО ХИТОЗАНА И СУКЦИНАТА ХИТОЗАНА | 2019 |
|
RU2712690C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИНГИБИТОРА КОЛЛАГЕНАЗ С АНТИКОАГУЛЯНТНЫМ ДЕЙСТВИЕМ ИЗ ГЕПАТОПАНКРЕАСА КАМЧАТСКОГО КРАБА | 2009 |
|
RU2403284C1 |
| СПОСОБ ПОЛУЧЕНИЯ IgAl-ПРОТЕАЗЫ ИЗ КУЛЬТУРЫ NEISSERIA MENINGITIDIS СЕРОГРУППЫ А И ИММУНОГЕННЫЙ ПРЕПАРАТ НА ЕЕ ОСНОВЕ | 2009 |
|
RU2407792C1 |
| Способ получения гетерогенного биокатализатора на основе целлюлазы, иммобилизованной на катионообменном волокне ВИОН КН-1 в Н-форме | 2024 |
|
RU2834720C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА ФИЦИНА В ГЕЛЕ НА ОСНОВЕ КАРБОКСИМЕТИЛЦЕЛЛЮЛОЗЫ | 2021 |
|
RU2771183C1 |
| СПОСОБ ПОЛУЧЕНИЯ НИЗКОМОЛЕКУЛЯРНОГО ХИТОЗАНА ДЛЯ ПРОТИВОЛУЧЕВЫХ ПРЕПАРАТОВ | 2000 |
|
RU2188829C1 |
Предложен способ получения низкомолекулярных гепаринов из высокомолекулярных путем ферментативной деполимеризации с помощью комплекса ферментов из Streptomyces kurssanovii, иммобилизованного на силохроме, при весовом соотношении гепарин: иммобилизованный фермент 1:1, суспензию перемешивают, иммобилизованный препарат отделяют центрифугированием, промывают, промывную жидкость присоединяют к супернатанту и обессоливают на колонке с сефадексом 6-10, полученный продукт лиофилизируют. Изобретение обеспечивает удешевление способа.
Способ получения низкомолекулярного гепарина из высокомолекулярного гепарина с помощью ферментативного гидролиза, отличающийся тем, что для ферментативной деполимеризации гепарина используют комплекс ферментов из Streptomyces kurssanovii, иммобилизованный на силохроме, при весовом соотношении гепарин: иммобилизованный фермент 1:1; суспензию перемешивают, иммобилизованный препарат отделяют центрифугированием, промывают, промывную жидкость присоединяют к супернатанту и обессоливают на колонке с сефадексом G -10, полученный продукт лиофилизируют.
| Linhardt R | |||
| et a | |||
| J.Med | |||
| Способ сопряжения брусьев в срубах | 1921 |
|
SU33A1 |
| ОЧИЩЕННАЯ ГЕПАРИНОВАЯ ФРАКЦИЯ, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И СОДЕРЖАЩАЯ ЕЕ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1994 |
|
RU2133253C1 |
| СТАНОК ДЛЯ НАРЕЗАНИЯ ВНУТРЕННЕЙ РЕЗЬБЫ | 0 |
|
SU244235A1 |
| US 4396762 А, 02.08.1983 | |||
| US 4826827 А, 02.05.1989. | |||
Авторы
Даты
2005-03-27—Публикация
2003-04-21—Подача