Предпосылки изобретения
1. Область изобретения
Настоящее изобретение относится к агенту для подавления заражения и пролиферации вируса иммунодефицита человека (ВИЧ-1), который заражает иммунокомпетентные клетки, такие как макрофаги или дендритные клетки, и приводит к повреждению иммунной системы. Конкретнее, настоящее изобретение относится к применению агента для подавления заражения и пролиферации вируса иммунодефицита человека, агенту, который подавляет инфицирование и пролиферацию вируса иммунодефицита человека в макрофагах типа М, производных человеческих моноцитов.
2. Описание предшествующего уровня техники
Более 40 миллионов людей заражено вирусом иммунодефицита человека (ВИЧ-1), и было установлено, что среди них у 5 миллионов людей развился синдром приобретенного иммунодефицита человека (СПИД). СПИД действительно является общемировым инфекционным заболеванием. Высокоэффективная антиретровирусная терапия (HAART) пациентов с ВИЧ-1 появилась в начале 90-х годов. В результате применения в клинике было получено значительное терапевтическое действие, такое как снижение количества вирусов в плазме крови пациентов со СПИДом и установленное выделение CD4.
Однако, с другой стороны, вызывает тревогу, что вирус, направленный к макрофагам (Мϕ), остается в ретикулоэндотелиальных тканях1),2), и у пациентов, получавших HAART, наблюдается появление резистентного штамма к HAART в течение периода времени примерно от полугода до нескольких лет после HAART. Кроме того, поскольку стоимость лечения с помощью HAART является высокой, лечение в основном назначается людям в развитых странах, и люди в развивающихся странах не могут получать подобную терапию вследствие неравенства в экономическом положении развитых стран и развивающихся стран, где как раз находится более 80% пациентов, зараженных ВИЧ в мире, и такое лечение не может способствовать прерыванию международного распространения вируса, в результате чего необходима множественная комбинированная терапия для того, чтобы подавить появление резистентных штаммов, и также сообщается о пациентах, которые не получают лечения за счет абдоминального симптома и повреждения гематопоэтической системы, следовательно, указывается на ограничения как в медицинском, так и социальном плане при применении HAART.
ВИЧ-1 представляет вирус, который заражает иммунокомпетентные клетки, такие как макрофаги и дендритные клетки, с последующим разрушением иммунной системы. В результате недавно проведенных исследований становится очевидным, что заражение и пролиферация ВИЧ-1 в макрофагах играют важную роль в поддержании инфекции и развитии патогенеза ВИЧ-13), следовательно, требуется разработка новых лекарственных препаратов, которые ингибируют заражение и пролиферацию ВИЧ-1 в макрофагах.
Несмотря на проведение многочисленных опытов по заражению макрофагов ВИЧ-1, многие исследования выполнялись с использованием клеточных штаммов макрофагов, но результаты экспериментов с использованием клеточных штаммов не всегда отражают функцию тканевых макрофагов in vivo. Akagawa et al. добились успеха в дифференциальной индукции двух типов макрофагов, способствующих пролиферации ВИЧ-1, и макрофагов, подавляющих пролиферацию ВИЧ-1, из моноцитов, кроме того, они дополнительно показали, что макрофаги, подавляющие пролиферацию, могут служить моделью человеческих альвеолярных макрофагов, в результате чего стало возможным проводить исследование заражения, пролиферации и механизма подавления пролиферации ВИЧ-1 в системе, подобной макрофагам in vivo4)-9).
Кроме того, известно, что макролиды эффективны при лечении панбронхиолита (DPB) и заболеваний в области оторинологии, и известен механизм их действия, в дополнении к антибиотическому действию, в отношении индукции противовоспалительного действия10). В частности, имеется сообщение, в результате исследования накопления макролидов в тканях, указывающее, что в макрофагах наблюдали в несколько сот-тысяч раз более высокое накопление по сравнению с периферическими лимфоцитами, следовательно, полагается, что действие макролидов на макрофаги является важным.
Основываясь на вышеуказанных предпосылках, авторы изобретения предположили, что является полезной разработка лекарственных препаратов, восполняющих недостатки HAART, подавляющих заражение и пролиферацию ВИЧ-1 в макрофагах, и нацеленных на удаление ВИЧ-1, направленного к макрофагам из лимфоидной ретикулоэндотелиальной системы, особенно разработка дешевых химиотерапевтических препаратов с точки зрения терапевтической стратегии против СПИДа во всем мире для лечения пациентов, зараженных ВИЧ-1.
Авторы изобретения исследовали, оказывают или нет известные макролидные производные действие в отношении подавления заражения и пролиферации ВИЧ-1 и неожиданно обнаружили, что они оказывают подавляющее действие на заражение и пролиферацию ВИЧ-1 в макрофагах, и показали, что подавляющее действие на пролиферацию проявляется подавлением экспрессии белка тирозинкиназы Hck в макрофагах, который является необходимым для роста вируса и подавлением активации Р38МАРК, и сделали настоящее изобретение.
Целью настоящего изобретения является обеспечение применения агента для подавления заражения и пролиферации вируса иммунодефицита человека, пригодного для лечения пациентов, зараженных ВИЧ-1, дешевым химиотерапевтическим препаратом, а также пригодного в качестве дополнительного препарата при проведении HAART.
Краткое описание изобретения
Настоящее изобретение относится к применению макролидных производных для подавления заражения и пролиферации вируса иммунодефицита человека в макрофагах, производных человеческих моноцитов. Макрофаги, производные человеческих моноцитов, являются макрофагами типа М. Подавление пролиферации вируса основано на ингибирующем действии макролидов на белок тирозинкиназа Hck и ингибировании активации Р38МАРК макрофагов, необходимых для пролиферации вируса. Известные макролидные производные, обладающие таким подавляющим действием в отношении пролиферации ВИЧ-1, включены в настоящее изобретение.
Предпочтительными примерами макролидных производных, использованных в настоящем изобретении, являются:
Оксациклотетрадекан-2,10-дион,4[(2,6-дидезокси-3-О-метил-α-L-рибо-гексопиранозил)окси]-14-этил-7,12,13-тригидрокси-3,5,7,9,11,13-гексаметил-6-[[3,4,6-тридезокси-3-(диметиламино)-β-D-ксило-гексопиранозил]окси]; 11-(1’-гидроксипропил)-3-[[2,6-дидезокси-3-С-метил-α-L-рибо-гексопиранозил]окси]-5-[(3,4,6-тридезокси-3-(диметиламино)-β-D-ксило-гексопиранозил)окси]-2,4,6,8,11,14-гексаметил-10,13,15-три-оксатрицикло[9.2.1.1.9.6]-пентадекан-1-он; 6,15,16-триоксатрицикло[10.2.1.11,4]гексадекан, производное эритромицина; 4,13-диоксабуцикло [8.2.1]тридек-12-ен-5-он,7-[(2,6-дидезокси-3-С-метил-α-L-рибо-гексопиранозил)окси]-3-(1,2-дигидрокси-1-метилбутил)-2,6,8,10,12-пентаметил-9-[[3,4,6-тридезокси-3-(диметиламино)-β-D-ксило-гексопиранозил]окси]; оксацикло-тетрадекан-2,10-дион,4-[(2,6-дидезокси-3-О-метил-α-L-рибо-гексопиранозил)окси]-14-этил-12,13-дигидрокси-7-метокси-3,5,7,9,11,13-гексаметил-6-[[3,4,6-тридезокси-3-(диметиламино)-β-D-ксило-гексопиранозил]окси]; де(3’-N-метил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль; де (3’-N-метил)-3’-N-сульфонил-8,9-ангидропсевдоэритромицина
А 6,9-гемикеталь или его соль; де(3’-N-метил)-[3’-N-(3-гидрокси-1-пропил)]-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль; де(3’-N-метил)-3’-N-(2-ацетоксиэтил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль; де(3’-N-метил)-3’-N-цианометил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль; де(3’-N-метил)-3’-N-(2-фторэтил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль; бис-де(3’-N-метил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль; бис-де(3’-N-метил)-3’-N-этил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль; бис-де(3’-N-метил)-3’,3’-N,N-диэтил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль; бис-де(3’-N-метил)-3’-N-аллил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль; бис-де (3’-N-метил)-3’,3’-N,N-диаллил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль; бис-де(3’-N-метил)-3’-N-пропаргил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль; бис-де(3’-N-метил)-3’,3’-N,N-дипропаргил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль; бис-де(3’-N-метил)-3’-N-пропил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль; бис-де(3’-N-метил)-3’,3’-N,N-дипропил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль; бис-де(3’-N-метил)-3’-N-гексил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль; бис-де(3’-N-метил)-3’,3’-N,N-дигексил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль; бис-де(3’-N-метил)-3’-N-бензил-8,9-ангидро-псевдоэритромицина А 6,9-
гемикеталь или его соль; бис-де(3’-N-метил)-3’,3’-N,N-дибензил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль; бис-де(3’-N-метил)-3’-N-(2-пропил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль; бис-де (3’-N-метил)-3’,3’-N,N-ди-(10-бром-1-деканил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль; бис-де(3’-N-метил)-3’-N-ацетил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль; де(3’-диметиламино)-3’-пиперидино-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль; де(3’-диметиламино)-3’-пирролидино-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль; де(3’-диметиламино)-3’-морфолино-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль; де(3’-диметиламино)-3’-[гексагидро-1-(1Н)-азепинил]-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль; де (12-гидрокси)-де[12-(1-гидроксипропил)]-12-гидроксиоксим-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль; де[12-(1-гидроксипропил)]-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль; де(12-гидрокси)-де[12-(1-гидроксипропил)]-12-амино-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль; де(3’-N-метил)-де[12-(1-гидроксипропил)]-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль; де(3-O-кладинозил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль и де(3-O-кладинозил)-де(3’-N-метил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль.
Для того чтобы понять настоящее изобретение, поясняется
механизм подавления пролиферации ВИЧ-1, направленного на макрофаги, в макрофагах, производных моноцитов человека.
[I] Экспериментальные материалы и методы
(1-1) Получение макрофагов, производных человеческих моноцитов и альвеолярных макрофагов
Как сообщалось ранее11), человеческие одноядерные клетки из периферической крови (РМВС) выделяли из светлого слоя кровяного сгустка от здоровых людей-добровольцев с использованием микрогранул, нагруженных антителами CD14 (Miltenyi Biotec, Германия), магнитной системы для разделения клеток (MACS) (Miltenyi Biotec, Германия) и лифопрепарата (Nycome Inc., Норвегия), затем моноциты выделяли из РМВС положительным отбором.
Макрофаги, производные моноцитов, получали культивированием выделенных моноцитов в присутствии M-CSF (колониестимулирующего фактора макрофагов) (104 Е/мл, полученного от Morinaga Milk Co.), гранулоцитов и колониестимулирующего фактора гранулоцитов, GM-CSF (500 Е/мл, полученного от Japan, Scheling Plough Co., Osaka, или полученного от R & S Genzyme-TECHNE Inc.) в среде RPMI1640 с добавлением 10% фетальной телячьей сыворотки (Nissui Seiyaku Co., Токио) в течение 7-8 дней.
Макрофаги, полученные при дифференциальной индукции с помощью M-CSF из человеческих моноцитов, обозначали, как макрофаги типа М (Мϕ типа М или М-Мϕ) и макрофаги, полученные дифференциальной индукцией с помощью GM-CSF, из человеческих моноцитов, обозначали как макрофаги типа GM (Мϕ типа GM или GM-Mϕ). Кроме того, альвеолярные макрофаги (альвеолярные Мϕ или А-Мϕ) получали следующим образом. Извлекали клетки, полученные из альвеолярной промывной жидкости, при промывании альвеол у здоровых добровольцев их суспендировали и адгезировали к пластику, затем отмывали неадгезированные клетки и оставшиеся адгезированные клетки обозначали как альвеолярные Мϕ.
(1-2) Заражение макрофагов ВИЧ-1
Заражение макрофагов ВИЧ-1 проводили следующим образом. Вирусные штаммы, направленные на макрофаги, ВИЧ-1JR-FL и ВИЧ-1BAL, использовали для заражения в течение 2 ч при контактировании с клетками М-Мϕ, GM-Мϕ и А-Мϕ (доводили до 2,5×105/лунку, Flacon №3043: Becton Dickinson Labware, Inc., США) при низкой концентрации (титр антигена р24 50 нг/мл, TCID50=3000/мл вируса до конечной концентрации 100 пг/мл), и неадсорбированный к макрофагам вирус отмывали и культивировали при добавлении свежей среды. В случае среды с М-Мϕ добавляли M-CSF (104 Е/мл) и в случае среды с GM-Mϕ добавляли GM-CSF (500 Е/мл).
В настоящих опытах количество вируса, использованное при контактном заражении, доводили до уровня вируса у пациентов, имеющегося на стадии носительства, поскольку уровень вируса в легочной ткани у пациентов на стадии носительства ВИЧ-1 составляет несколько десятков пг/мл - несколько сотен пг/мл, а уровень вируса при заражении в альвеолярных Мϕ составляет несколько копий на 104 клеток12).
(1-3) Анализ заражения и пролиферации ВИЧ-1
Пролиферацию вируса исследовали по количеству выделенных в культуральный супернатант вирусных частиц после заражения, с использованием сэндвич-ELISA с двумя типами анти-р24-антител (Nu24 и 10В513)). В качестве LTR (длинного концевого повторного)-gag генного праймера использовали следующие JAM62 и JAM65. Для групповой ПЦР использовали следующие праймеры JAM63 и JAM64 в качестве внутреннего праймера.
JAM62:
5’-GCTTCAAGTAGTGTGTGCCCGTCTG-3’
JAM65:
5’-AATCGTTCTAGCTCCCTGCTTGCCC-3’
JAM63:
5’-GTGTGACTCTGGTAACTAGAGATCC-3’
JAM64:
5’-CCGCTTAATACTGACGCTCTCGCAC-3’.
(1-4) Анализ экспрессии белка тирозинкиназы Hck и белка фактора транскрипции С/ЕВРβ
Экспрессию белка тирозинкиназы Hck и белка фактора транскрипции С/ЕВРβ в макрофагах исследовали после солюбилизации макрофагов в буфере для образца для SDC-PAGE, проведением электрофореза в 10% SDS-полиакриламидном геле, переносом белка с геля на иммобилоновую мембрану Р (Millipore Inc., США) и анализом антител против данных белков вестерн-блоттингом. Антитела против белка тирозинкиназы Hck (N-30) и антитела против С/ЕВРβ (С-19) были получены от Santacluse Inc. (США). Результаты вестерн-блоттинга детектировали реагентом Amersham ELC (Amersham International plc, Buckinghamshire, Великобритания). Интенсивность полос выражали показателем PSL (фотостимулирующей люминесценции) (А/мм2).
(1-5) Обработка макрофагов антисмысловым белком тирозинкиназой Hck и белком фактором транскрипции С/ЕВРВ
Антисмысловой олигонуклеотидный зонд белка Hck и белка С/ЕВРβ (AS), соответствующий ему смысловой олигонуклеотидный зонд (S) и несмысловой олигонуклеотидный зонд, не относящийся к транскрипции и трансляции (NS), использовали следующим образом.
Фосфортиоат-модифицированный AS-Hck;
5’-TTCATCGACCCCATCCTGGC-3’
Фосфортиоат-модифицированный S-Hck;
5’-GCCAGGATGGGGTCGATGAA-3’
Фосфортиоат-модифицированный NS-Hck;
5’-CCATATTTCCCGCTCGCGTG-3’
Фосфортиоат-модифицированный AS-C/EBPβ;
5’-CAGGCGTTGCATGAACGCGG-3’
Фосфортиоат-модифицированный S-C/ЕВРβ;
5’-CCGCGTTCATGCAACGCCTG-3’
Фосфортиоат-модифицированный NS-C/EBPβ;
5’-CCAGAGAGGGCCCGTGTGGA-3’.
Данные зонды растворяли в сыворотке, не содержащей среду RPMI1640, в которой растворяли липофектин (Life Technology
Inc., США) в концентрации 5 мкМ, при комнатной температуре в течение 30 мин, добавляли со средой RPMI1640, которая содержала 10% FCS, к макрофагам (конечная концентрация 2 мкМ) и инкубировали при 37°С в течение 24 ч. После чего клетки промывали средой, добавляли среду RPMI1640, содержащую 10% FCS, без олигонуклеотидов, дополнительно культивировали в течение 24 ч, и затем заражали ВИЧ-1.
(1-6) Анализ активации Р38МАРК и ERK1/2
Активацию Р38МАРК и ERK1/2 определяли с использованием антител против Р38МАРК, анти-ЕРК1/2-антител, анти-фосфорилирования тирозина Р38МАРК-антител и анти-фосфорилирования тирозина ERK1/2-антител (New England Biolabs, Inc., США) и реакцию фосфорилирования данных молекул определяли вестерн-блоттингом.
[2] Результаты
(2-1) Пролиферативная ответная реакция штамма ВИЧ-1, направленного на макрофаги в М-Мϕ и GM-Mϕ
(2-1-1) Количество белка р24 в ВИЧ-1 зараженных М-Мϕ и GM-Мϕ в культуральном супернатанте
Клетки М-Мϕ и GM-Mϕ заражали штаммом ВИЧ-1JR-FL и штаммом ВИЧ-1BAL и инкубировали в течение 14 суток. Количество белка р24 в культуральном супернатанте макрофагов определяли в одинаковые периоды времени. При любом из штаммов ВИЧ-1 белок р24 обнаруживали в культуральном супернатанте М-Мϕ [смотри фиг.1(А) и (В)].
(2-1-2) Цитопатия в ВИЧ-1-зараженных М-Мϕ и GM-Мϕ
Морфологические изменения клеток М-Мϕ и GM-Mϕ, зараженных штаммом ВИЧ-1JR-FL и штаммом ВИЧ-1BAL, наблюдали в зависимости от времени. Образование кластеробразующих клеток и слитых клеток наблюдали на 2-ые сутки инкубации только в продуцирующих вирус М-Мϕ и на 4-7 сутки отмечали образование многоядерных гигантских клеток в культуре [смотри фиг.2(А)]. С другой стороны, морфологические изменения не наблюдали в GM-Мϕ, в которых отсутствовало размножение вируса [смотри фиг.2(В)]. Данные результаты указывают на то, что цитопатическое действие такое, как образование кластеров, слияние клеток и образование MGC в макрофагах, при заражении ВИЧ-1, направленного на макрофаги, можно использовать в качестве показателя для определения пролиферации вируса.
(2-1-3) Анализ распределения внутриклеточного белка р24 в ВИЧ-1-зараженных М-Мϕ и GM-Mϕ
Клетки М-Мϕ и GM-Mϕ заражали штаммом ВИЧ-1JR-FL и штаммом ВИЧ-1BAL и иммунологически окрашивали антителами к р24 на 8 сутки после заражения. В М-Мϕ наблюдали экспрессию белка р24 в MGC и сходным им клетках [смотри фиг.3(А)]. В GM-Mϕ не наблюдали экспрессии белка р24 [смотри фиг.3(В)]. Исходя из данных результатов, установлено, что механизм, подавляющий продукцию вируса в GM-Mϕ, может быть подавляющим механизмом перед стадиями внутриклеточного образования и активной репликации вирусных частиц.
(2-1-4) Детектирование вирусной ДНК в ВИЧ-1-зараженных М-Мϕ и GM-Мϕ
Клетки М-Мϕ и GM-Mϕ заражали штаммом ВИЧ-1JR-FL и штаммом ВИЧ-1BAL и детектировали образование вирусной ДНК на 2 сутки после заражения групповой ПЦР с использованием праймера LTR-gаg. Образование вирусной ДНК детектировали как в М-Мϕ, в которых наблюдали пролиферацию вируса, так и GM-Мϕ, в которых не наблюдали образование вирусной ДНК [смотри фиг.4(А) и (В)]. Данные результаты указывали, что инфильтрация вируса в клетки и превращение РНК в ДНК происходило даже в GM-Мϕ без обнаружения пролиферации вируса, это показывает, что механизм подавления образования вирусов в GM-Мϕ имеет место после образования вирусной ДНК.
(2-1-5) Экспрессия белка тирозинкиназы Hck и белка С/ЕВРβ в М-Мϕ и GM-Мϕ и изменения экспрессии под действием заражения ВИЧ-1
Поскольку М-Мϕ, производные человеческих моноцитов, эффективно индуцируют пролиферацию ВИЧ-1, и GM-Mϕ ингибируют пролиферацию вируса, авторы изобретения изучали, зависят или нет различия в восприимчивости к заражению ВИЧ-1 от различий в экспрессии белка хозяина. В результате показано, что экспрессия белка тирозинкиназы Hck и фактора транскрипции С/ЕВРβ является различной в двух типах макрофагов.
Без заражения вирусом белок тирозинкиназа Hck экспрессировался в высокой степени в М-Мϕ и в меньшей степени экспрессировался в GM-Мϕ [смотри фиг.5]. Несмотря на то, что экспрессия белка тирозинкиназы Hck в М-Мϕ увеличивалась при заражении штаммом ВИЧ-1BAL на 2 сутки, напротив, экспрессия белка тирозинкиназы в GM-Mϕ была снижена [смотри фиг.5]. С другой стороны, в М-Мϕ при экспрессии белка С/ЕВРβ без заражения вирусом экспрессировался только высокомолекулярный тип (37 кД), но в GM-Mϕ была обнаружена экспрессия обоих белков высокомолекулярного типа и низкомолекулярного типа (23 кД) [смотри фиг.6]. Несмотря на то, что не было установлено изменений в экспрессии белка С/ЕВРβ в М-Мϕ на 2 сутки после заражения штаммом ВИЧ-1BAL, экспрессия низкомолекулярного белка С/ЕВРβ была значительно повышена в GM-Mϕ, и появились изменения в соотношении высокомолекулярного типа и низкомолекулярного типа (соотношение L/S) [смотри фиг.6].
(2-1-6) Изучение восприимчивости к заражению человеческих альвеолярных Мϕ к ВИЧ-1 и экспрессия белка тирозинкиназы и белка С/ЕВРβ
Было показано, что GM-Mϕ, полученные из человеческих моноцитов с помощью GM-CSF, аналогичны человеческим альвеолярным макрофагам по морфологии, экспрессии поверхностного маркера, продуктивности образования активного кислорода и экспрессии каталазы13),14). Авторы изобретения исследовали, сходна или нет восприимчивость к заражению GM-Мϕ, производных человеческих моноцитов, и человеческих альвеолярных Мϕ.
После заражения штаммом ВИЧ-1BAL альвеолярных Мϕ (А-Мϕ) определяли вирусную ДНК групповой ПЦР и анализировали пролиферацию вируса по количеству белка р24 в культуральном супернатанте с помощью ELISA. Вирусную ДНК обнаруживали во все периоды времени после заражения [смотри фиг.7(В)], но через 14 суток инкубации не был детектирован ни белок р24, ни продукция вируса [смотри фиг.7(А)].
В результате изучения экспрессии белка тирозинкиназы Hck и белка С/ЕВРβ в альвеолярных Мϕ вестерн-блоттингом было установлено снижение экспрессии белка тирозинкиназы Hck и изменение экспрессии изоформы белка С/ЕВРβ, а именно была значительно повышена экспрессия низкомолекулярного типа белка С/ЕВРβ (23 кД), и имело место снижение соотношения L/S [смотри фиг.8]. На основании данных результатов можно предположить, что механизм подавления пролиферации вируса в человеческих альвеолярных Мϕ и GM-Mϕ, производных человеческих моноцитов, может в значительной степени быть сходным.
(2-1-7) Снижение экспрессии белка тирозинкиназы Hck в обработанных антисмысловыми олигонуклеотидами М-Мϕ к белку тирозинкиназе Hck и подавление пролиферации ВИЧ-1
Клетки М-Мϕ обрабатывали антисмысловыми олигонуклеотидами (Hck-AS) к белку тирозинкиназе Hck в течение 24 ч, и М-Мϕ инкубировали еще в течение 24 ч и определяли экспрессию белка тирозинкиназы Hck. В результате было установлено, что экспрессия белка тирозинкиназы Hck была значительно снижена по сравнению с контрольной группой (L) [смотри фиг.9]. Однако в М-Мϕ, обработанных смысловым зондом (Hck-S) или не относящимся к нему зондом (Hck-NS), было установлено подавление экспрессии белка тирозинкиназы Hck [смотри фиг.9].
Данные клетки М-Мϕ, предварительно обработанные различными олигонуклеотидами, заражали штаммом ВИЧ-1BAL и оценивали экспрессию белка тирозинкиназы Hck через 2 суток после заражения, снижение экспрессии белка тирозинкиназы Hck было установлено только в группе с добавлением антисмыслового зонда (Hck-AS), и подавление экспрессии белка тирозинкиназы Hck не было детектировано в М-Мϕ, обработанных смысловым зондом (Hck-S) или не относящимся к нему зондом (Hck-NS) [смотри фиг.10]. Определяли содержание белка р24 в культуральном супернатанте через 4, 7 и 10 суток после заражения. В клетках М-Мϕ, обработанных антисмысловым зондом (Hck-AS), во все периоды времени было обнаружено значительное количество белка р24, но в М-Мϕ, обработанных смысловым зондом (Hck-S) и не относящимся к нему зондом (Hck-NS), было установлено зависимое от времени повышение уровня белка р24, сходное с контрольной группой, обработанной только липофектином (L) [смотри фиг.10]. Данные результаты указывают, что экспрессия белка тирозинкиназы в М-Мϕ необходима для пролиферации ВИЧ-1.
(2-1-8) Экспрессия С/ЕВРβ и ростовая ответная реакция ВИЧ-1 в GM-Мϕ, обработанных антисмысловыми олигонуклеотидами С/ЕВРβ
Клетки GM-Mϕ обрабатывали антисмысловым зондом к С/ЕВРβ (C/EBPβ-AS) в течение 24 ч и культивировали еще в течение 24 ч, и в GM-Мϕ через двое суток после заражения штаммом ВИЧ-1BAL в относительной степени сохранялась экспрессия высокомолекулярной изоформы (37 кД), но экспрессии низкомолекулярной изоформы (23 кД) была существенно снижена с повышением соотношения L/S [смотри фиг.11]. Кроме того, заражение ВИЧ-1 клеток GM-Мϕ, предварительно обработанных C/EBPβ-AS, индуцировало пролиферацию вируса, и в культуральном супернатанте был обнаружен белок р24 [смотри фиг.12]. Способствующее росту ВИЧ-1 действие и изменения экспрессии С/ЕВРβ не обнаруживали в группах с добавлением С/ЕВРβ-S и C/EBPβ-NS [смотри фиг.11 и фиг.12].
Вышеприведенные результаты опытов четко указывают, что клетки М-Мϕ и GM-Mϕ, производные человеческих моноцитов, обладают различной восприимчивостью к заражению ВИЧ-1, направленным к макрофагам, и в М-Мϕ значительно усиливается пролиферация вируса, в то время, как напротив, в GM-Mϕ пролиферация вируса подавляется. Кроме того, различие в характере пролиферации в М-Мϕ и GM-Mϕ совпадало с различием в экспрессии высокомолекулярной изоформы и низкомолекулярной формы белка тирозинкиназы Hck и белка фактора транскрипции С/ЕВРβ в данных клетках. В результате специфически регулируемой экспрессии изоформы белка тирозинкиназы Hck и белка С/ЕВРβ с использованием антисмысловых олигонуклеотидов, размножение вируса в клетках М-Мϕ полностью регулировалось и, напротив, размножение вируса можно было индуцировать в GM-Мϕ.
Исходя из данных результатов, четко следует, что тирозинкиназа является необходимой для пролиферации ВИЧ-1 в М-Мϕ, и низкомолекулярный тип изоформы С/ЕВРβ играет важную роль при подавлении пролиферации ВИЧ-2 в GM-Mϕ. Кроме того, поскольку результаты исследования восприимчивости к заражению ВИЧ-1 человеческих альвеолярных Мϕ и экспрессия белка тирозинкиназы Hck и С/ЕВРβ, и поскольку механизм подавления роста ВИЧ-1 в человеческих альвеолярных Мϕ и GM-Mϕ, производных человеческих моноцитов являются идентичными, анализ в GM-Mϕ может быть в высокой степени связан с анализом альвеолярных Мϕ in vivo. Результаты данных опытов указывают, что анализ механизма пролиферации ВИЧ-1 в М-Мϕ, производных человеческих моноцитов, пригоден в качестве основной экспериментальной системы для разработки лекарственных препаратов, обладающих подавляющим действием на рост ВИЧ-1.
Основываясь на вышеприведенных результатах, можно привести предпочтительные примеры макролидных производных, обладающих свойством ингибировать экспрессию белка тирозинкиназы в М-Мϕ, производных человеческих моноцитов, и ингибировать активацию Р38МАРК, который необходим для пролиферации вируса, в виде следующих соединений, и данные соединения являются промышленно доступными или их легко получить способами, описанными в литературных источниках.
Оксациклотетрадекан-2,10-дион,4[(2,6-дидезокси-3-О-метил-α-L-рибо-гексопиранозил)окси]-14-этил-7,12,13-тригидрокси-3,5,7,9,11,13-гексаметил-6-[[3,4,6-тридезокси-3-(диметиламино)-β-D-ксило-гексопиранозил]окси (Sigma Inc., США); в последующем обозначенный, как ЕМ.
11-(1’-Гидроксипропил)-3-[2,6-дидезокси-3-С-метил-α-L-рибо-гексопиранозил]окси]-5-[(3,4,6-тридезокси-3-(диметиламино)-β-D-ксило-гексопиранозил)окси]-2,4,6,8,11,14-гексаметил-10,13,15-три-оксатрицикло [9.2.1.1.9.6]-пентадекан-1-он (смотри P.Kurath et al. Exoperimentia, 27, 362, 1971); в последующем обозначенный как ЕМ201.
6,15,16-Триоксатрицикло[10.2.1.11,4]гександекан, производное эритромицина или 6,9,12-ангидроэритромицин А (смотри Р. Kurath et al. Exoperimentia, 27, 362, 1971); в последующем обозначенный как ЕМ202.
4,13-Диоксабуцикло [8.2.1] тридек-12-ен-5-он,7-[(2,6-дидезокси-3-С-метил-α-L-рибо-гексопиранозил)окси]-3-(1,2-дигидрокси-1-метилбутил)-2,6,8,10,12-пентаметил-9-[[3,4,6-тридезокси-3-(диметиламино)-β-3-D-ксило-гексопиранозил]окси] (смотри JP-A-7-247299); в последующем обозначенный как ЕМ703.
Оксациклотетрадекан-2,10-дион,4-[(2,6-дидезокси-3-О-метил-α-L-рибо-гексопиранозил)окси]-14-этил-12,13-дигидрокси-7-метокси-3,5,7,9,11,13-гексаметил-6-[[3,4,6-тридезокси-3-(диметиламино)-β-D-ксило-гексопиранозол]окси] (смотри S.Morimoto et al. J Antibiotics, 43, 286, 1990 или продукт Apin Chemicals Ltd., Великобритания и продукт Wako Pure Chemicals, Inc. Япония); в последующем обозначенный как САМ.
Примерами производных эритромицина являются:
де(3’-N-метил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ703; де(3’-N-метил)-3’-N-сульфонил-8,9-ангидро-псевдоэритромицина А G,9-гемикеталь или его соль, в последующем обозначенный как ЕМ727; де(3’-N-метил)-[3’-N-(3-гидрокси-1-пропил)]-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ744; де(3’-N-метил)-3’-N-(2-ацетоксиэтил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ745; де(3’-N-метил)-3’-N-цианометил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ742; де(3’-N-метил)-3’-N-(2-фторэтил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ740; бис-де(3’-N-метил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ721; бис-де(3’-N-метил)-3’-N-этил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ722; бис-де(3’-N-метил)-3’,3’-N,N-диэтил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ723; бис-де(3’-N-метил)-3’-N-аллил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ724; бис-де (3’-N-метил)-3’,3’-N,N-диаллил-8, 9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ725; бис-де(3’-N-метил)-3’-N-пропаргил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ728; бис-де(3’-N-метил)-3’,3’-N,N-ди-пропаргил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ729; бис-де(3’-N-метил)-3’-N-пропил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ730; бис-де(3’-N-метил)-3’,3’-N,N-дипропил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ731; бис-де (3’-N-метил)-3’-N-гексил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ738; бис-де(3’-N-метил)-3’,3’-N,N-дигексил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ739; бис-де(3’-N-метил)-3’-N-бензил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ732; бис-де (3’-N-метил)-3’,3’-N,N-дибензил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ733; бис-де(3’-N-метил)-3’-N-(2-пропил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ736; бис-де(3’-N-метил)-3’,3’-N,N-ди-(10-бром-1-деканил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ749; бис-де(3’-N-метил)-3’-N-ацетил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ726; де(3’-диметиламино)-3’-пиперидино-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ734; де(3’-диметиламино)-3’-пирролидино-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ735; де (3’-диметиламино)-3’-морфолино-8, 9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ747; де(3’-диметиламино)-3’-[гексагидро-1(1Н)-азепинил]-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ748; де(12-гидрокси)-де[12-1-(гидроксипропил)]-12-гидроксиоксим-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ743; де[12-(гидроксипропил)]-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ746; де(12-гидрокси)-де[12-(1-гидроксипропил)]-12-амино-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ750; де(3’-N-метил)-де[12-1-(гидроксипропил)]-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ751; де(3-O-кладинозил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ737 и де(3-O-кладинозил)-де(3’-N-метил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталь или его соль, в последующем обозначенный как ЕМ754.
Различные вышеуказанные производные эритромицина были установлены авторами настоящего изобретения Satoshi Omura et аl., и поданы в качестве международной патентной заявки, международная публикация WO 02/14338 А1, включая псевдоэритромицин, который, как полагается, является новым противовоспалительным агентом. В описании WO 02/14338 A1 подробно приводятся способы синтеза и химические структуры производных эритромицина, и описания способов синтеза каждого производного эритромицина поясняются ниже.
Синтез ЕМ701
Раствор эритромицина (12,4 г) в ледяной уксусной кислоте перемешивали при комнатной температуре в течение 2 ч, медленно добавляли водный раствор бикарбоната натрия и нейтрализовали. Реакционную смесь экстрагировали хлороформом, органический слой обезвоживали мирабилитом, отфильтровывали мирабилит и растворитель удаляли выпариванием с получением сырого твердого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 10:0,5:0,01→10:1:0,05) с получением ЕМ201 (7,7 г). Затем к метанольному раствору ЕМ201 (7,6 г) добавляли карбонат калия (1,4 г) и кипятили с обратным холодильником в течение 2 ч. После отгонки растворителя остаток растворяли в водном растворе бикарбоната натрия и экстрагировали хлороформом. Смесь обезвоживали мирабилитом, фильтровали и удаляли мирабилит, затем полученное сырое твердое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 10:0,5:0,01→10:1:0,5) с получением ЕМ701 (5,9 г, белый порошок).
Синтез де(3’-N-метил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ703)
Ацетат натрия (3,9 г) и йод (2,5 г) добавляли в данном порядке к раствору ЕМ701 (6,9 г) в смеси метанол (52,0 мл) - вода (13,0 мл) при комнатной температуре и перемешивали при 50°С в течение 3 ч. Во время перемешивания добавляли 1 н. водный раствор гидроокиси натрия для постоянного поддержания при рН 8-9. После подтверждения окончания реакции по ТСХ реакционную смесь разбавляли смесью водный аммиак (7,5 мл) - вода (200 мл) и экстрагировали дихлорметаном. После обезвоживания органического слоя мирабилитом мирабилит удаляли фильтрованием и растворитель отгоняли с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 10:0,5:0,01→10:1:0,05) с получением ЕМ703 (4,8 г, белый порошок).
Синтез бис-де(3’-N-метил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ721)
Натрий (4,5 г) добавляли к метанолу (15 мл) для получения метанольного раствора метилата натрия и добавляли ЕМ703 (195,4 мг) и йод (353,6 мг) в таком порядке при 0°С и перемешивали в течение 3 ч. После подтверждения окончания реакции по ТСХ добавляли тиосульфат натрия (0,8 г), водный аммиак (0,5 мл) и воду (80 мл) и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и растворитель отгоняли с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 10:0,5:0,01→10:1:0,05) с получением ЕМ721 (166,3 мг, белый порошок).
Синтез бис-де(3’-N-метил)-3’-N-этил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ722)
N,N-диизопропилэтиламин (26,6 мкл) и этилйодид (12,2 мкл) добавляли к раствору ЕМ721 (21,0 мг) в диметилформамиде (1,0 мл) и перемешивали при комнатной температуре в течение 4 ч. После подтверждения окончания реакции по ТСХ реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 10:0,5:0,01→10:1:0,05) с получением ЕМ722 (7,0 мг, белый порошок).
Синтез бис-де(3’-N-метил)-3’,3’-N,N-диэтил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ723)
N,N-диизопропилэтиламин (26,6 мкл) и этилйодид (12,2 мкл) добавляли к раствору ЕМ721 (21,0 мг) в диметилформамиде (1,0 мл) и перемешивали при комнатной температуре в течение 4 ч. После подтверждения окончания реакции по ТСХ реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 10:0,5:0,01→10:1:0,05) с -получением ЕМ723 (10,3 мг, белый порошок).
Синтез бис-де(3’-N-метил)-3’-N-аллил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ724)
Аллилбромид (148,3 мкл) добавляли к раствору ЕМ721 (117,8 мг) и N,N-диизопропилэтиламина (298,6 мкл) в дихлорметане (5,7 мл) при 0°С и перемешивали при комнатной температуре в течение 2 ч. После подтверждения окончания реакции по ТСХ реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 10:0,5:0,01→10:1:0,05) с получением ЕМ724 (21,9 мг, белый порошок).
Синтез бис-де(3’-N-метил)-3’,3’-N,N-диаллил-8,9-ангидро-псевдоэритромицина A 6,9-гемикеталя (ЕМ725)
Аллилбромид (148,3 мкл) добавляли к раствору ЕМ721 (117,8 мг) и N,N-диизопропилэтиламина (298,6 мкл) в дихлорметане (5,7 мл) при 0°С и перемешивали при комнатной температуре в течение 2 ч. После подтверждения окончания реакции по ТСХ реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол: водный аммиак = 10:0,5:0,01→10:1:0,05) с получением ЕМ725 (64,3 мг, белый порошок).
Синтез бис-де(3’-N-метил)-3’-N-ацетил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ726)
Уксусный ангидрид (8,4 мкл) добавляли к раствору ЕМ721 (34,8 мг) в дихлорметане (1,6 мл) при 0°С, перемешивали в течение 10 мин и затем перемешивали при комнатной температуре в течение 30 мин. После подтверждения окончания реакции по ТСХ реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол = 100:1,0→20:1) с получением ЕМ726 (33,4 мг, белый порошок).
Синтез де(3’-N-метил)-3’-N-сульфонил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ727)
Метансульфонилхлорид (9,3 мкл) добавляли к раствору ЕМ703 (87,6 мг) в дихлорметане (4,2 мл) при 0°С и перемешивали в течение 3 ч. После подтверждения окончания реакции по ТСХ реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол = 100:1→20:1) с получением ЕМ727 (37,2 мг, белый порошок).
Синтез бис-де(3’-N-метил)-3’-N-пропаргил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ728)
3-Бромпропин (137,8 мкл) добавляли к раствору ЕМ721 (106,3 мг) и N,N-диизопропилэтиламина (269,3 мкл) в дихлорметане (5,2 мл) и перемешивали при комнатной температуре в течение 24 ч. После подтверждения окончания реакции по ТСХ реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 10:0,5:0,01→10:1:0,05) с получением ЕМ728 (41,3 мг, белый порошок).
Синтез бис-де(3’-N-метил)-3’,3’-N,N-дипропаргил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ729)
3-Бромпропин (137,8 мкл) добавляли к раствору ЕМ721 (106,3 мг) и N,N-диизопропилэтиламина (269,3 мкл) в дихлорметане (5,2 мл) и перемешивали при комнатной температуре в течение 24 ч. После подтверждения окончания реакции по ТСХ реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 10:0,5:0,01→10:1:0,05) с получением ЕМ729 (27,9 мг, белый порошок).
Синтез бис-де(3’-N-метил)-3’-N-пропил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ730)
N,N-диизопропилэтиламин (59,6 мкл) и 1-йодпропин (33,3 мкл) добавляли в данном порядке к раствору ЕМ721 (23,5 мг) в ацетонитриле (2,3 мл) и кипятили с обратным холодильником при 80°С в течение 20 ч. После подтверждения окончания реакции по ТСХ реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 15:1:0,1) с получением ЕМ730 (5,7 мг, белый порошок).
Синтез бис-де (3’-N-метил)-3’,3’-N,N-дипропил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ731)
N,N-диизопропилэтиламин (59,6 мкл)и 1-йодпропин (33,3 мкл) добавляли в данном порядке к раствору ЕМ721 (23,5 мг) в ацетонитриле (2,3 мл) и кипятили с обратным холодильником при 80°С в течение 20 ч. После подтверждения окончания реакции по ТСХ реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 15:1:0,1) с получением ЕМ731 (12,0 мг, белый порошок).
Синтез бис-де (3’-N-метил)-3’-N-бензил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ732)
Бензилхлорид (297,3 мкл) добавляли к раствору ЕМ721 (88,8 мг) и N,N-диизопропилэтиламина (450,1 мкл) в дихлорметане (4,3 мл) при комнатной температуре и перемешивали в течение 96 ч. После подтверждения окончания реакции по ТСХ реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 15:1:0,1) с получением ЕМ732 (49,9 мг, белый порошок).
Синтез бис-де(3’-N-метил)-3’,3’-N,N-дибензил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ733)
N,N-диизопропилэтиламин (135,9 мкл) и бензилхлорид (89,7 мкл) добавляли в данном порядке к раствору ЕМ721 (26,8 мг) в ацетонитриле (1,3 мл) и кипятили с обратным холодильником при 80°С в течение 60 ч. После подтверждения окончания реакции по ТСХ реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 20:1:0,1) с получением ЕМ733 (19,6 мг, белый порошок).
Синтез де(3’-диметиламино)-3’-пиперидино-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ734)
N,N-диизопропилэтиламин (42,5 мкл) и 1,5-дибромпентан (33,2 мкл) добавляли в данном порядке к раствору ЕМ721 (16,8 мг) в ацетонитриле (4,9 мл) и кипятили с обратным холодильником при 80°С в течение 24 ч. После подтверждения окончания реакции по ТСХ реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 15:1:0,1) с получением ЕМ734 (13,3 мг, белый порошок).
Синтез де (3’-диметиламино)-3’-пирролидино-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ735)
N,N-диизопропилэтиламин (40,2 мкл) и 1,4-дибромбутан (27,6 мкл) добавляли в данном порядке к раствору ЕМ721 (15,9 мг) в ацетонитриле (4,6 мл) и кипятили с обратным холодильником при 80°С в течение 24 ч. После подтверждения окончания реакции по ТСХ реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 10:1:0,1) с получением ЕМ735 (11,9 мг, белый порошок).
Синтез бис-де(3’-N-метил)-3’-N-(2-пропил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ736)
N,N-диизопропилэтиламин (459,2 мкл) и 2-бромпропан (247,5 мкл) добавляли в данном порядке к раствору ЕМ721 (90,6 мг) в ацетонитриле (4,4 мл) и перемешивали при 80°С в течение 72 ч. После подтверждения окончания реакции по ТСХ реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 10:1:0,1) с получением ЕМ736 (25,3 мг, белый порошок). Получали 47,1 мг сырого вещества ЕМ721.
Синтез де(3-O-кладинозил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ737)
п-Толуолсульфоновую кислоту моногидрат (80,3 мг) добавляли к раствору ЕМ701 (201,6 мг) в диметилформамиде (5,6 мл) и перемешивали при 50°С в течение 8 ч. После подтверждения окончания реакции по ТСХ реакционную смесь разбавляли водой, доводили до рН 8,0 добавлением насыщенного водного раствора бикарбоната натрия и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 20:1:0,1) с получением ЕМ737 (84,7 мг, белый порошок).
Синтез бис-де(3’-N-метил)-3’-N-гексил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ738)
N,N-диизопропилэтиламин (408,5 мкл) и 1-бромгексан (328,7 мкл) добавляли в данном порядке к раствору ЕМ721 (80,6 мг) в ацетонитриле (3,9 мл) и перемешивали при 60°С в течение 24 ч. После подтверждения окончания реакции по ТСХ реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 15:1:0,1) с получением ЕМ738 (33,7 мг, белый порошок). Получали 24,6 мг сырого вещества ЕМ721.
Синтез бис-де(3’-N-метил)-3’,3’-N,N-дигексил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ739)
N,N-диизопропилэтиламин (116,0 мкл) и 1-бромгексан (93,6 мкл) добавляли в данном порядке к раствору ЕМ721 (22,9 мг) в ацетонитриле (1,1 мл) и перемешивали при 60°С в течение 72 ч. После подтверждения окончания реакции по ТСХ реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 20:1:0,1) с получением ЕМ739 (20,1 мг, белый порошок).
Синтез де (3’-N-метил)-3’-N-(2-фторэтил)-8,9-энгидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ740)
N,N-диизопропилэтиламин (347,7 мкл) и 1-бром-2-фторэтан (148,6 мкл) добавляли к раствору ЕМ703 (70,0 мг) в диметилформамиде (3,3 мл) при комнатной температуре и перемешивали в течение 48 ч. После подтверждения окончания реакции по ТСХ реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 20:1:0,1) с получением ЕМ740 (36,0 мг, белый порошок). Получали 25,5 мг сырого вещества ЕМ703.
Синтез де (3’-N-метил)-3’-N-цианометил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ742)
N,N-диизопропилэтиламин (320,9 мкл) и бромацетонитрил (128,3 мкл) добавляли к раствору ЕМ703 (64,6 мг) в диметилформамиде (3,1 мл) при комнатной температуре и перемешивали в течение 4 ч. После подтверждения окончания реакции по ТСХ реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 20:1:0,1) с получением ЕМ742 (53,1 мг, белый порошок).
Синтез де(12-гидрокси)-де[12-(1-гидроксипропил)]-12-оксо-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ705)
Тетраацетат свинца (508,0 мг) добавляли к раствору ЕМ701 (508,0 мг) в дихлорметане (24,0 мл) и перемешивали при комнатной температуре в течение 40 мин. После подтверждения окончания реакции по ТСХ реакционную смесь разбавляли смесью насыщенный раствор соли - водный насыщенный раствор бикарбоната натрия (1:1, об./об.) и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 10:0,5:0,01) с получением ЕМ705 (282,7 мг, белый порошок).
Синтез де(12-гидрокси)-де[12-(1-гидроксипропил)]-12-гидрокси-оксим-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ743)
Пиридин (0,9 мл) медленно добавляли при 0°С к раствору ЕМ705 (116,5 мг) и гидроксиламина гидрохлорида (32,0 мг) в этаноле (0,9 мл) и перемешивали в течение 3 ч. После подтверждения окончания реакции по ТСХ реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак 10:0,5:0,01→10:1:0,05) с получением ЕМ743 (114,5 мг, белый порошок).
Синтез де(3’-N-метил)-[3’-N-(3-гидрокси-1-пропил)]-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ744)
N,N-диизопропилэтиламин (338,3 мкл) и 3-бром-1-пропанол (175,6 мкл) добавляли к раствору ЕМ703 (68,1 мг) в диметилформамиде (3,3 мл) при комнатной температуре и перемешивали в течение 48 ч. После подтверждения окончания реакции по ТСХ реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 15:1:0,1) с получением ЕМ744 (27,7 мг, белый порошок). Получали 22,5 мг сырого вещества ЕМ703.
Синтез де(3’-N-метил)-3’-N-(ацетоксиэтил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ745)
N,N-диизопропилэтиламин (106,8 мкл) и 2-бромэтилацетат (67,6 мкл) добавляли к раствору ЕМ703 (21,5 мг) в диметилформамиде (1,0 мл) при комнатной температуре и перемешивали в течение 48 ч. После подтверждения окончания реакции по ТСХ реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 20:1:0,1) с получением ЕМ745 (6,0 мг, белый порошок).
Синтез де[12-(1-гидроксипропил)]-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ746)
Боргидрид натрия (21,8 мл) добавляли к раствору ЕМ705 (37,7 мг) в метаноле (2,9 мл) при -78°С и перемешивали в течение 30 мин. Температуру реакционной смеси повышали до 0°С и затем перемешивали в течение 30 мин. После подтверждения окончания реакции по ТСХ реакцию останавливали добавлением ацетона (0,5 мл). Реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 15:1:0,1) с получением ЕМ746 (35,8 мг, белый порошок).
Синтез де(3’-диметиламино)-3’-морфолино-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ747)
N,N-диизопропилэтиламин (45,8 мкл) и бис(2-бромэтил)эфир (33,1 мкл) добавляли в данном порядке к раствору ЕМ721 (18,1 мг) в ацетонитриле (2,6 мл) и перемешивали при 80°С в течение 24 ч. После подтверждения окончания реакции по ТСХ реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 20:1:0,1) с получением ЕМ747 (12,0 мг, белый порошок).
Синтез де(3’-диметиламино)-3’-[гексагидро-1-(1Н)-азепинил]-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ748)
N,N-диизопропилэтиламин (49,5 мкл) и 1,6-дибромгексан (43,6 мкл) добавляли в данном порядке к раствору ЕМ721 (19,5 мг) в ацетонитриле (2,8 мл) и перемешивали при 80°С в течение 24 ч. После подтверждения окончания реакции по ТСХ реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 20:1:0,1) с получением ЕМ748 (11,7 мг, белый порошок).
Синтез бис-де(3’-N-метил)-3’,3’-N,N-ди-(10-бром-1-деканил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ749)
N,N-диизопропилэтиламин (45,6 мкл) и 1,10-дибромдекан (58,9 мкл) добавляли в данном порядке к раствору ЕМ721 (18,0 мг) в ацетонитриле (2,6 мл) и кипятили с обратным холодильником при 80°С в течение 36 ч. После подтверждения окончания реакции по ТСХ реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 20:1:0,1) с получением ЕМ749 (14,9 мг, белый порошок).
Синтез де(12-гидрокси)-де[12-(1-гидроксипропил)]-12-амино-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ750)
Окись молибдена (IV) (10,0 мг) и боргидрид натрия (10,5 мг) добавляли к раствору ЕМ743 (15,5 мг) в этаноле (2,3 мл) при 0°С и перемешивали в течение 4 ч. После подтверждения окончания реакции по ТСХ реакцию останавливали добавлением ацетона (0,5 мл) и реакционную смесь разбавляли смесью насыщенный раствор соли - водный насыщенный раствор бикарбоната натрия (1:1, об./об.) и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 10:1:0,1) с получением ЕМ750 (13,4 мг, белый порошок).
Синтез де(3’-N-метил)-де(12-гидрокси)-де-[12-(1-гидроксипропил)]-12-оксо-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ706)
Тетраацетат свинца (508,0 мл) добавляли к раствору ЕМ701 (508,0 мг) в дихлорметане (24,0 мл) и перемешивали при комнатной температуре в течение 40 мин. После подтверждения окончания реакции по ТСХ реакцию останавливали добавлением ацетона (0,5 мл) и реакционную смесь разбавляли смесью насыщенный раствор соли - водный насыщенный раствор бикарбоната натрия (1:1, об./об.) и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ: метанол:водный аммиак = 10:0,5:0,01) с получением ЕМ706 (71,6 мг, белый порошок).
Синтез де(3’-N-метил)-де[12-(1-гидроксипропил)]-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ751)
Боргидрид натрия (22,9 мл) добавляли к раствору ЕМ706 (38,8 мг) в метаноле (3,0 мл) при 0°С и перемешивали в течение 1 ч. После подтверждения окончания реакции по ТСХ реакцию останавливали добавлением ацетона (0,5 мл) и реакционную смесь разбавляли смесью насыщенный раствор соли - водный насыщенный раствор бикарбоната натрия (1:1, об./об.) и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 15:1:0,1) с получением ЕМ751 (31,4 мг, белый порошок).
Синтез де (3-O-кладинозил)-де (3’-N-метил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя (ЕМ754)
п-Толуолсульфоновую кислоту моногидрат (53,9 мг) добавляли к раствору ЕМ703 (132,4 мг) в диметилформамиде (3,8 мл) и перемешивали при 50°С в течение 6 ч. После подтверждения окончания реакции по ТСХ реакционную смесь разбавляли водой, доводили до рН 8,0 добавлением насыщенного водного раствора бикарбоната натрия и экстрагировали дихлорметаном. Органический слой обезвоживали добавлением мирабилита, фильтровали для удаления мирабилита и удаляли растворитель с получением сырого вещества. Сырое вещество очищали колоночной хроматографией на силикагеле (смесь хлороформ:метанол:водный аммиак = 15:1:0,1) с получением ЕМ754 (50,2 мг, белый порошок).
Краткое описание фигур
На фиг.1(А) показано содержание белка р24 в культуральном супернатанте в М-Мϕ и GM-Мϕ, зараженных штаммом ВИЧ-1JR-FL, и на (В) показано содержание белка р24 в культуральном супернатанте М-Мϕ и GM-Mϕ, зараженных штаммом ВИЧ-1BAL.
На фиг.2(А) показана цитопатия М-Мϕ, зараженных штаммом ВИЧ-1JR-FL и штаммом ВИЧ-1BAL, и на (В) показана цитопатия GM-Мϕ, зараженных штаммом ВИЧ-1JR-FL и штаммом ВИЧ-1BAL.
На фиг.3(А) показано внутриклеточное распределение белка р24 в М-Мϕ, зараженных штаммом ВИЧ-1JR-FL и штаммом ВИЧ-1BAL, и на (В) показано внутриклеточное распределение белка р24 в GM-Мϕ, зараженных штаммом ВИЧ-1JR-FL и штаммом ВИЧ-1BAL.
На фиг.4(А) показано детектирование вирусной ДНК в М-Мϕ и GM-Мϕ, зараженных штаммом ВИЧ-1JR-FL, и на (В) показано детектирование вирусной ДНК в М-Мϕ и GM-Мϕ, зараженных штаммом ВИЧ-1BAL.
На фиг.5 показаны изменения экспрессии белка тирозинкиназы Hck в М-Мϕ и GM-Мϕ и экспрессии при заражении ВИЧ-1BAL.
На фиг.6 показаны изменения экспрессии белка С/ЕВРβ в М-Мϕ и GM-Мϕ и экспрессии в М-Мϕ или GM-Мϕ, зараженных штаммом ВИЧ-1BAL.
На фиг.7(А) показана ростовая ответная реакция при детектировании белка р24 в культуральном супернатанте после заражения штаммом ВИЧ-1BAL в человеческих альвеолярных Мϕ (А-Мϕ) и на (В) показано детектирование вирусной ДНК.
На фиг.8 показаны изменения экспрессии белка тирозинкиназы Hck и белка С/ЕВРβ в альвеолярных Мϕ и экспрессия при заражении штаммом ВИЧ-1BAL.
На фиг.9 показана экспрессия белка тирозинкиназы Hck в М-Мϕ, обработанных антисмысловыми олигонуклеотидами для белка тирозинкиназы Hck до и после заражения штаммом ВИЧ-1BAL.
На фиг.10 показано подавление пролиферации ВИЧ-1 в М-Мϕ, обработанных антисмысловыми олигонуклеотидами для белка тирозинкиназы Hck.
На фиг.11 показана экспрессия белка С/ЕВРβ в GM-Mϕ, обработанных антисмысловыми олигонуклеотидами для белка С/ЕВРβ до и после заражения штаммом ВИЧ-1BAL.
На фиг.12 показана пролиферация ВИЧ-1 в GM-Mϕ, обработанных антисмысловыми олигонуклеотидами для белка С/ЕВРβ.
На фиг.13 показано влияние макролидных производных на пролиферацию ВИЧ-1 в М-Мϕ при добавлении макролидных производных, таких как ЕМ, ЕМ201, ЕМ202, ЕМ703 или САМ, по сравнению с добавлением ДМСО.
На фиг.14 показано влияние макролидных производных на пролиферацию ВИЧ-1 в GM-Mϕ при добавлении макролидных производных, таких как ЕМ, ЕМ201, ЕМ202, ЕМ703 или САМ, по сравнению с добавлением ДМСО.
На фиг.15 показано влияние макролидных производных на пролиферацию ВИЧ-1 в М-Мϕ, полученных от различных людей (трех субъектов) при добавлении макролидных производных, таких как ЕМ, ЕМ201, ЕМ202, ЕМ703 или САМ, по сравнению с добавлением ДМСО.
На фиг.16 показано влияние концентрации макролидов, таких как ЕМ, ЕМ201, ЕМ202, ЕМ703 и САМ, на пролиферацию ВИЧ-1 в М-Мϕ по сравнению с добавлением ДМСО.
На фиг.17 показано влияние макролидных производных на цитопатию М-Мϕ, зараженных ВИЧ-1, при добавлении ЕМ, ЕМ201, ЕМ202, ЕМ703 или САМ по сравнению с добавлением ДМСО.
На фиг.18 показано влияние макролидных производных, таких как ЕМ, ЕМ201, ЕМ202, ЕМ703 или САМ, на экспрессию белка тирозинкиназы Hck в М-Мϕ, зараженных ВИЧ-1.
На фиг.19(А) показано влияние макролидных производных, таких как ЕМ, ЕМ201, ЕМ202, ЕМ703 или САМ, на активацию Р38МАРК в М-Мϕ, зараженных ВИЧ-1, по сравнению с ДМСО и на (В) показано влияние макролидных производных, таких как ЕМ, ЕМ201, ЕМ202, ЕМ703 или САМ, на активацию ERK1/2 в М-Мϕ, зараженных ВИЧ-1, по сравнению с ДМСО.
На фиг.20 показано влияние ингибитора р38МАРК (SB203580) и ингибитора ERK1/2 (PD98059) на пролиферацию вируса в М-Мϕ, зараженных штаммом ВИЧ-1BАL, по сравнению с контрольной группой.
На фиг.21 показано влияние различных концентраций макролидов, таких как ЕМ722, ЕМ730, ЕМ732 или ЕМ736, на пролиферацию ВИЧ-1 в М-Мϕ по сравнению с ДМСО.
На фиг.22 показано влияние различных концентраций макролидов, таких как ЕМ734, ЕМ735, ЕМ747 или ЕМ748, на пролиферацию ВИЧ-1 в М-Мϕ по сравнению с ДМСО.
На фиг.23 показано влияние различных концентраций макролида, такого как ЕМ743, на пролиферацию ВИЧ-1 в М-Мϕ по сравнению с ДМСО.
На фиг.24 показано влияние различных концентраций макролидов, таких как ЕМ746, ЕМ750 или ЕМ751, на пролиферацию ВИЧ-1 в М-Мϕ по сравнению с ДМСО.
На фиг.25 показано влияние различных концентраций макролида, такого как ЕМ754, на пролиферацию ВИЧ-1 в М-Мϕ по сравнению с ДМСО.
Подробное описание предпочтительных воплощений
Настоящее изобретение будет пояснено конкретно с помощью последующих примеров, но оно не ограничивается данными примерами.
Для того чтобы показать подавляющее действие настоящего изобретения на рост, макролидные производные, ЕМ, ЕМ201, ЕМ202, ЕМ703, САМ, ЕМ722, ЕМ730, ЕМ732, ЕМ736, ЕМ734, ЕМ735, ЕМ747, ЕМ748, ЕМ743, ЕМ746, ЕМ750 или ЕМ751 растворяли в ДМСО, каждый в концентрации 100 мМ и затем использовали при разбавлении средой. Контрольная группа представляла М-Мϕ, обработанные только ДМСО, использованного для растворения макролидных производных.
М-Мϕ и GM-Mϕ подвергали контактному заражению штаммом ВИЧ-1BAL в течение 2 ч, добавляли 30 мкМ ЕМ, ЕМ201, ЕМ202, ЕМ703, САМ, ЕМ722, ЕМ730, ЕМ732, ЕМ736, ЕМ734, ЕМ735, ЕМ747, ЕМ748, ЕМ743, ЕМ746, ЕМ750 или ЕМ751, инкубировали в течение 14 суток и определяли количество белка р24 в культуральном супернатанте в зависимости от времени.
Пример 1
Влияние ЕМ, ЕМ201, ЕМ202, ЕМ703 или САМ на пролиферацию ВИЧ-1 в М-Мϕ и GM-Mϕ.
По сравнению с контрольной группой (ДМСО) при добавлении ЕМ201 или ЕМ703 белок р24 в М-Мϕ почти не обнаруживали, и размножение вируса было в значительной степени подавлено на 14 день культивирования (смотри фиг.13). В М-Мϕ при добавлении САМ было установлено почти половинное подавление, и в группе с добавлением ЕМ или ЕМ202 также было обнаружено подавление размножения, хотя и не такое сильное по сравнению с ЕМ201 и ЕМ703 (смотри фиг.13). В GM-Mϕ в группе с добавлением ЕМ, ЕМ201, ЕМ202, ЕМ703 или САМ почти не было установлено наличия репродукции вируса во все периоды исследования, аналогичные контрольной группе (ДМСО) (смотри фиг.14). В опыте с использованием М-Мϕ, производных человеческих моноцитов, взятых от трех взрослых добровольцев, получали такие же результаты, как представлены на фиг.13 (смотри фиг.15).
Подавляющее действие ЕМ201 и ЕМ703 в отношении ВИЧ-1BAL в М-Мϕ зависело от концентрации, и размножение вируса полностью подавлялось в концентрации 3 мкМ или выше (смотри фиг.16). Несмотря на то, что пролиферацию вируса наблюдали при концентрации 300 мкМ не только для ЕМ201 и ЕМ703, но также и для ЕМ, ЕМ202 и САМ, и поскольку ее наблюдали также и в контрольной группе (ДМСО), возможно, за счет цитотоксичности ДМСО, используемого в качестве растворителя, дальнейшие опыты проводили при концентрации 30 мкМ.
Пример 2
Влияние ЕМ, ЕМ201, ЕМ202, ЕМ703 и САМ на цитопатию М-Мϕ, зараженных ВИЧ-1.
М-Мϕ подвергали контактному заражению штаммом ВИЧ-1BAL в течение 2 ч, добавляли 30 мкМ ЕМ, ЕМ201, ЕМ202, ЕМ703 или САМ, инкубировали и исследовали морфологию клеток. В контрольной группе (ДМСО) и группе с добавлением ЕМ, ЕМ201 или САМ обнаруживали незначительное образование MGC, совпадающее с повышением количества белка р24, как показано в примере 1, но в группе с добавлением ЕМ201 и ЕМ703 не наблюдали проявления цитопатического действия, такого как образование MGC (смотри фиг.17).
Пример 3
Влияние ЕМ, ЕМ201, ЕМ202, ЕМ703 и САМ на белок тиразинкиназу Hck в М-Мϕ, зараженных ВИЧ-1.
Как описано ранее, М-Мϕ эффективно экспрессировали белок тирозинканазу Hck, и регуляция экспрессии белка тирозинкиназы Hck с использованием антисмысловых олигонуклеотидов могла подавлять пролиферацию ВИЧ-1 в М-Мϕ. Данный результат указывал на то, что экспрессия белка тирозинкиназы Hck является необходимой для пролиферации ВИЧ-1 в М-Мϕ. Поскольку ЕМ201 и ЕМ203 подавляли пролиферацию ВИЧ-1 в М-Мϕ, было выдвинуто предположение, что экспрессия белка тирозинкиназы Hck была подавлена в М-Мϕ, обработанных данными агентами.
Следовательно, М-Мϕ подвергали контактному заражению штаммом ВИЧ-1BAL в течение 2 ч, добавляли 30 мкМ ЕМ, ЕМ201, ЕМ202, ЕМ703 или САМ, инкубировали и на 2 сутки после заражения оценивали экспрессию белка тирозинкиназы Hck вестерн-блоттингом. В группе с внесением ЕМ, ЕМ202 и САМ, которые проявляли не очень сильное подавляющее воздействие на пролиферацию вируса, наблюдали снижение уровня белка тирозинкиназы Hck, хотя и не такое сильное по сравнению с контрольной группой (обработанной только ДМСО) (смотри фиг.18). В опытах с ЕМ201 и ЕМ703, которые показывали сильное подавляющее действие на пролиферацию вируса, экспрессия белка тирозинкиназы Hck была в значительной степени подавлена (смотри фиг.18).
Пример 4
Влияние ЕМ, ЕМ201, ЕМ202, ЕМ703 или САМ на активацию р38МАРК и ERK1/2 в М-Мϕ, зараженных ВИЧ-1.
р38МАРК и ERK1/2 (р42/44МАРК) участвуют в различных ответных реакциях на механизм внутриклеточной сигнальной трансдукции. Фосфорилирование тирозина р38МАРК и ERK1/2 в М-Мϕ, зараженных штаммом ВИЧ-1BAL, оценивали вестерн-блоттингом. В результате было установлено, что фосфорилирование тирозина р38МАРК было значительно усилено под воздействием заражения вирусом, но фосфорилирование тирозина ERK1/2 было слабым. Данные результаты указывают, что активация р38МАРК является важной для пролиферации вируса в М-Мϕ.
Следовательно, изучали влияние ЕМ, ЕМ201, ЕМ202, ЕМ703 и САМ, которые обладают подавляющим действием на пролиферацию вируса в М-Мϕ, на активацию р38МАРК и ERK1/2.
30 мкл ЕМ, ЕМ201, ЕМ202, ЕМ703 или САМ добавляли к М-Мϕ, зараженным штаммом ВИЧ-1BAL, фосфорилирование тирозина р38МАРК определяли на 2 сутки культивирования вестерн-блоттингом. В группе с ЕМ, ЕМ202 и САМ, которые проявляли не очень сильное подавляющее воздействие на пролиферацию вируса, наблюдали снижение фосфорилирования тирозина р38МАРК, хотя и не такое сильное по сравнению с контрольной группой (ДМСО). В группе с добавлением ЕМ201 и ЕМ703, которые показывали сильное подавляющее действие на пролиферацию вируса, фосфорилирование тирозина р38МАРК было в значительной степени снижено [смотри фиг.19(А)]. Во всех группах общее количество р38МАРК (общая сумма фосфорилированного и нефосфорилированного р38МАРК) было равным. На основании данных результатов можно предположить, что подавление пролиферации вируса под воздействием ЕМ, ЕМ201, ЕМ202, ЕМ703 и САМ в М-Мϕ связано со снижением уровня р38МАРК.
С другой стороны, в группе с добавлением ЕМ, ЕМ202 и САМ, которые проявляли не очень сильное подавляющее воздействие на пролиферацию вируса, фосфорилирование тирозина ERK1/2 слабо детектировалось, как и в контрольной группе (ДМСО), но в группе с добавлением ЕМ201 и ЕМ703, которые показывают сильное подавляющее воздействие на пролиферацию вируса, установили усиление фосфорилирования тирозина ERK1/2. Во всех группах общее количество ERK1/2 (общая сумма фосфорилированного и нефосфорилированного р38МАРК) было равным [смотри фиг.19(В)].
Пример 5
Влияние ингибитора р38МАРК на пролиферацию вируса в М-Мϕ, зараженных ВИЧ-1, при подавлении добавлением ЕМ, ЕМ201, ЕМ202, ЕМ703 и САМ, использованных в настоящем изобретении.
На основании результатов примера 4 было выдвинуто предположение, что активация р38МАРК является важной для пролиферации ВИЧ-1 в М-Мϕ, и подавляющее воздействие ЕМ, ЕМ201, ЕМ202, ЕМ703 и САМ на пролиферацию вируса является результатом ингибирующего действия данных соединений на активацию р38МАРК.
Следовательно, ингибитор р38МАРК, SB203580, (4-[4-фторфенил]-2-[4-метилсульфинилфенил]-5-[4-пиридил]-1Н-имидазол) и ингибитор ERK1/2, PD98059, (2-[2-амино-3-метоксифенил]-4Н-1-бензопиран-4-он), в концентрации 10 мкМ, добавляли к М-Мϕ, зараженным штаммом ВИЧ-1BAL, и исследовали воздействие на вирус.
Когда 10 мкМ SB203580 добавляли к М-Мϕ, зараженным штаммом ВИЧ-1BAL, и инкубировали, белок р24 почти не обнаруживали даже на 14 сутки, и пролиферация вируса была подавлена (смотри фиг.20). С другой стороны, когда добавляли 10 мкМ ингибитора ERK1/2, PD98059, количество белка р24 не отличалось от контрольной группы, и была обнаружена пролиферация вируса (смотри фиг.20). Из результатов данных опытов следует, что для пролиферации штамма ВИЧ-1-, направленного к макрофагам, в основном необходима активация белка р38МАРК, и полагается, что участие ERK1/2 незначительно.
Пример 6
Влияние ЕМ722, ЕМ730, ЕМ732 и ЕМ736, использованных в настоящем изобретении, на пролиферацию ВИЧ-1 в М-Мϕ.
М-Мϕ подвергали контактному заражению штаммом ВИЧ-1BAL в течение 2 ч, добавляли ЕМ722, ЕМ730, ЕМ732 или ЕМ736 в различных концентрациях, инкубировали в течение 10 суток и определяли содержание белка р24 в культуральном супернатанте в зависимости от времени. Группа, обработанная только ДМСО, используемого для растворения макролидных производных, служила в качестве контрольной группы.
Увеличение количества белка р24 наблюдали в культуральном супернатанте в контрольной группе при добавлении только ДМСО в зависимости от продолжительности культивирования в сутках, и была обнаружена пролиферация ВИЧ-1. Однако по сравнению с контрольной группой в группе с добавлением ЕМ722, ЕМ730, ЕМ732 или ЕМ736, образование белка р24 было снижено в зависимости от концентрации агента, и было установлено наличие подавления пролиферации вируса. В частности, было установлено, что в концентрации 30 мкМ любые агенты ЕМ722, ЕМ730, ЕМ732 и ЕМ736 почти полностью подавляли пролиферацию вируса (смотри фиг.21). С агентами ЕМ703, ЕМ727, ЕМ744, ЕМ745, ЕМ742, ЕМ740, ЕМ721, ЕМ723, ЕМ724, ЕМ725, ЕМ728, ЕМ729, ЕМ731, ЕМ738, ЕМ739, ЕМ733, ЕМ749 и ЕМ726 получали аналогичные результаты, как на фиг.21. Кроме того, в опыте с использованием М-Мϕ, производных человеческих моноцитов, взятых от трех взрослых здоровых добровольцев, получали такие же результаты, как на фиг.21.
Пример 7
Влияние ЕМ734, ЕМ735, ЕМ747 и ЕМ748, использованных в настоящем изобретении, на пролиферацию ВИЧ-1 в М-Мϕ.
М-Мϕ подвергали контактному заражению штаммом ВИЧ-1BAL в течение 2 ч, добавляли ЕМ734, ЕМ735, ЕМ747 и ЕМ748 в различных концентрациях, инкубировали в течение 10 суток и определяли содержание белка р24 в культуральном супернатанте в зависимости от времени. Группа, обработанная только ДМСО, используемого для растворения макролидных производных, служила в качестве контрольной группы.
Увеличение количества белка р24 наблюдали в культуральном супернатанте в контрольной группе при добавлении только ДМСО в зависимости от продолжительности культивирования в сутках, и была обнаружена пролиферация ВИЧ-1. Однако по сравнению с контрольной группой в группе с добавлением ЕМ734, ЕМ735, ЕМ747 и ЕМ748, образование белка р24 было снижено в зависимости от концентрации агента, и было установлено наличие подавления пролиферации вируса. В частности, было установлено, что в концентрации 30 мкМ любые агенты ЕМ734, ЕМ735, ЕМ747 и ЕМ748 почти полностью подавляли пролиферацию вируса (смотри фиг.22). Кроме того, в опыте с использованием М-Мϕ, производных человеческих моноцитов, взятых от трех взрослых здоровых добровольцев, получали такие же результаты, как на фиг.22.
Пример 8
Влияние ЕМ743, использованного в настоящем изобретении, на пролиферацию ВИЧ-1 в М-Мϕ.
М-Мϕ подвергали контактному заражению штаммом ВИЧ-1BAL в течение 2 ч, добавляли ЕМ743 в различных концентрациях, инкубировали в течение 10 суток, и определяли содержание белка р24 в культуральном супернатанте в зависимости от времени. Группа, обработанная только ДМСО, используемого для растворения макролидных производных, служила в качестве контрольной группы.
Увеличение количества белка р24 наблюдали в культуральном супернатанте в контрольной группе при добавлении только ДМСО в зависимости от продолжительности культивирования в сутках, и была обнаружена пролиферация ВИЧ-1. Однако по сравнению с контрольной группой в группе с добавлением ЕМ743 образование белка р24 было снижено в зависимости от концентрации агента, и было установлено наличие подавления пролиферации вируса. В частности, было установлено, что в концентрации 30 мкМ ЕМ743 почти полностью подавлял пролиферацию вируса (смотри фиг.23). Кроме того, в опыте с использованием М-Мϕ, производных человеческих моноцитов, взятых от трех взрослых здоровых добровольцев, получали такие же результаты, как на фиг.23.
Пример 9
Влияние ЕМ746, ЕМ750 и ЕМ751, использованных в настоящем изобретении, на пролиферацию ВИЧ-1 в М-Мϕ.
М-Мϕ подвергали контактному заражению штаммом ВИЧ-1BAL в течение 2 ч, добавляли ЕМ746, ЕМ750 и ЕМ751 в различных концентрациях, инкубировали в течение 10 суток и определяли содержание белка р24 в культуральном супернатанте в зависимости от времени. Группа, обработанная только ДМСО, используемого для растворения макролидных производных, служила в качестве контрольной группы.
Увеличение количества белка р24 наблюдали в культуральном супернатанте в контрольной группе при добавлении только ДМСО в зависимости от продолжительности культивирования в сутках, и была обнаружена пролиферация ВИЧ-1. Однако по сравнению с контрольной группой в группе с добавлением ЕМ746, ЕМ750 и ЕМ751 образование белка р24 было снижено в зависимости от концентрации агента, и было установлено наличие подавления пролиферации вируса. В частности, было установлено, что в концентрации 30 мкМ агенты ЕМ746, ЕМ750 и ЕМ751 почти полностью подавляли пролиферацию вируса (смотри фиг.24). Кроме того, в опыте с использованием М-Мϕ, производных человеческих моноцитов, взятых от трех взрослых здоровых добровольцев, получали такие же результаты, как на фиг.24.
Пример 10
Влияние ЕМ754, использованного в настоящем изобретении, на пролиферацию ВИЧ-1 в М-Мϕ.
М-Мϕ подвергали контактному заражению штаммом ВИЧ-1BAL в течение 2 ч, добавляли ЕМ754 в различных концентрациях, инкубировали в течение 10 суток и определяли содержание белка р24 в культуральном супернатанте в зависимости от времени. Группа, обработанная только ДМСО, используемого для растворения макролидных производных, служила в качестве контрольной группы.
Увеличение количества белка р24 наблюдали в культуральном супернатанте в контрольной группе при добавлении только ДМСО в зависимости от продолжительности культивирования в сутках, и была обнаружена пролиферация ВИЧ-1. Однако по сравнению с контрольной группой в группе с добавлением ЕМ754 образование белка р24 было снижено в зависимости от концентрации агента, и было установлено наличие подавления пролиферации вируса. В частности, было установлено, что в концентрации 30 мкМ ЕМ754 почти полностью подавлял пролиферацию вируса (смотри фиг.25). Кроме того, в опыте с использованием М-Мϕ, производных человеческих моноцитов, взятых от трех взрослых здоровых добровольцев, получали такие же результаты, как на фиг.25.
Как описано выше, было установлено, что макролидные производные, использованные в настоящем изобретении, обладают подавляющим воздействием на пролиферацию ВИЧ-1, направленного к макрофагам, в М-Мϕ, производных человеческих моноцитов. В частности, ЕМ201 и ЕМ703, которые, как было обнаружено, обладают активностью эффективно подавлять пролиферацию ВИЧ-1, направленного к макрофагам, в М-Мϕ, почти полностью подавляли пролиферацию вируса даже в концентрации 3 мкМ. Было установлено подавляющее воздействие ЕМ201 и ЕМ703 на пролиферацию вируса с проявлением высокой подавляющей эффективности, равной 95% или более, даже на 14 сутки после инкубации только при внесении ЕМ201 или ЕМ703 в первичную культуральную среду после контактного заражения вирусом.
Кроме того, ЕМ, ЕМ202 и САМ также проявляли подавляющее воздействие на пролиферацию вируса в зависимости от концентрации лекарственного препарата, и было установлено одинаковое подавляющее действие ЕМ722, ЕМ730, ЕМ732, ЕМ736, ЕМ734, ЕМ735, ЕМ747, ЕМ748, ЕМ743, ЕМ746, ЕМ750, ЕМ751 и ЕМ754 в концентрации 30 мкМ почти с полным ингибированием. Исходя из данного факта, было установлено, что подавляющее действие входит в фармакологические свойства макролидов, накапливающихся в ткани макрофагов с длительным периодом действия.
Как описано ранее, экспрессия белка тирозинкиназы Hck важна для пролиферации ВИЧ-1 в М-Мϕ, и поскольку различные макролидные производные по настоящему изобретению ингибировали экспрессию белка тирозинкиназы в М-Мϕ, было высказано предположение, что данное ингибирующее действие является одним из механизмов подавляющего действия данных соединений на пролиферацию ВИЧ-1. Кроме того, поскольку различные макролидные производные по настоящему изобретению, которые проявляют подавляющее действие на пролиферацию вируса, ингибировали фосфорилирование тирозина р38МАРК, было высказано предположение, что подавление пролиферации ВИЧ-1 основано на подавлении активации р38МАРК данными соединениями.
Промышленная применимость
Как описано выше, настоящее изобретение относится к применению макролидных производных для подавления заражения и пролиферации вируса иммунодефицита человека в макрофагах, производных человеческих моноцитов. Настоящее изобретение не только пригодно в качестве препаратов для подавления заражения и пролиферации вируса иммунодефицита человека, но также возможно их применение в клинике в качестве дополнительного препарата при HAART.
Список литературы
1. Tae-Wook Chun, Richard T. Davey Jr., Mario Ostrowski, J. Shawn Justement, Delphine Engel, James I. Mullins & Anthony S. Fauci: Relationship between pre-existing viral reservoires and the re-emergence of plasma viremia after discontinuation of highly active anti-retroviral therapy, Nat Med 6: 757-761, 2000.
2. Lewis К. Schrager, M. Patricia D’Souza; Cellular and Anatomical Reservoirs of HIV-1 in Patients Receiving Potent Antiretroviral Combination Therapy, Jama 280: 67-71, 1998.
3. Swingler S, Mann A, Jacque J, Brichacek В, Sasseville VG, Williams K, Lackner AA, Janoff EN, Wang R, Fisher D, Stevenson M.: HIV-1 Nef mediates lymphocyte chemotaxis and activation By infected macrophages. Nat Med 5: 997-1003, 1999.
4. Kiyoko Akagawa, Iwao Komuro and Keiko Mochida: Diversity of macrophage derived from monocytes, Inflammation and Immunity, Vol. 8, 360-366, 2000.
5. Komuro, I., Keicho, N., Iwamoto, I., and Akagawa, K. S.: Human alvelolar macrophages and GM-CSF-induced monocyte-derived macrophages are resistant to H2O2 via their high basal-and inducible-levels of catalase activity, J. Biol. Chem. 276: 24360-24364, 2001.
6. Hashimoto, S., Komuro, I., Yamada, M. Akagawa, K.S.: IL-10 inhibits GM-CSF-dependent human monocyte survival at the early stage of the culture and inhibits the generation of macrophages, J. Immunol. 167: 3619-3625, 2001.
7. Hashimoto, S., Yamada, M., Motoyoshi, K. and Akagawa, K. S.: Enhancement of macrophage-colony-stimulating factor-induced growth and differentiation of human monocytes by interleukin-10, BLOOD 89: 315-321, 1997.
8. Akagawa, К. S., Takasuka, N., Nozaki, Y., Komuro, I., Miyuki. A., Ueda, M., Naito, M. and Takahashi, K.: Generation of CD1+ RelB+ Dendritic Cells and TRAP-positive Osteoclast-like Multi- nucleated Giant Cells from Human Monocytes, BLOOD 88: 4029-4039, 1996.
9. Matsuda, S., Akagawa, K., Honda, M., Yokota, Y., Takabe, Y. and Takemori, Т.: Suppression of HIV replication in human monocyte-derived macrophages induced by granulocyte/macrophage colony- stimulating factor, AIDS Research and Human Retroviruses, 11: 1031-1038, 1995.
10. Inflammation and Immunity and Macrolides Up to Date,. Ed. Sup. Kihachiro Shimizu and Satoshi Omura, Ed. Shoji Kudo: lyaku Journal, Inc. Osaka, 1996.
11. Hashimoto, S., Komuro, I., Yamada, M., Akagawa. K. S.: IL-10 inhibits GM-CSF-dependent human monocyte survival at.the early stage of the culture and inhibits the generation of macrophages, J. Immunol. 167: 3619-3625, 2001.
12. Nakata, К., Weiden, M., Harkin, Т., Но, D. and Rom, W.N. (1995). Low copy number and limited variability of proviral DNA in alvelolar macrophages from HIV-1-infected patients: evidence for genetic differences in HIV-1 between lung and blood macrophage populations. Mol Med 1, 744-757.
13. Kiyoko Akagawa, Iwao Komuro and Keiko Mochida: Diversity of macrophage derived from monocytes, Inflammation and Immunity, Vol.8, 360-366, 2000. Akagawa, К.S., Takasuka, N., Nozaki, Y., Komuro, I., Miyuki, A., Ueda, M., Naito, M. and Takahashi. K: Generation of CD1 + Re1B + Dendritic Cells and TRAP-positive Osteoclast-like Multi-nucleated Giant Cells from Human Monocytes, BLOOD 88: 4029-4039, 1996.
14. Komuro, I., Keicho, N., Iwamoto, I., and Akagawa, K. S.: Human alvelolar macrophages and GM-CSF-induced monocyte-derived macrophages are resistant to H2O2 via their high basal-and inducible-levels of catalase activity, J. Biol. Chem. 276: 24360-24364, 2001.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ идентификации функционального М1 и М2 фенотипа макрофагов человека, генерированных in vitro из моноцитов крови | 2019 |
|
RU2717024C1 |
| Способ моделирования ВИЧ-инфекции | 1991 |
|
SU1837355A1 |
| ПРОИЗВОДНЫЕ ХИНОЛИНА ДЛЯ ПРИМЕНЕНИЯ В ЛЕЧЕНИИ ИЛИ ПРОФИЛАКТИКЕ ВИРУСНОЙ ИНФЕКЦИИ | 2016 |
|
RU2723016C2 |
| СПОСОБЫ ЛЕЧЕНИЯ ИНФЕКЦИИ ВИЧ-1 | 2020 |
|
RU2827716C1 |
| ДВОЙНОЙ ВЕКТОР ДЛЯ ПОДАВЛЕНИЯ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА | 2010 |
|
RU2562868C2 |
| КОМПЛЕКСНОЕ АНТИ-ВИЧ СОЕДИНЕНИЕ | 2004 |
|
RU2270690C1 |
| КОМПЛЕКСНАЯ АУТОЛОГИЧНАЯ ВАКЦИНА ПРОТИВ ВИЧ-ИНФЕКЦИИ И СПИД | 2005 |
|
RU2306950C2 |
| СРЕДСТВО ДЛЯ ИНГИБИРОВАНИЯ ВИЧ И ЦМВ-ИНФЕКЦИЙ И СПОСОБ ИХ ИНГИБИРОВАНИЯ | 2002 |
|
RU2196602C1 |
| НОВОЕ ПРОИЗВОДНОЕ ХИНОЛИНА ДЛЯ ПРИМЕНЕНИЯ В ЛЕЧЕНИИ И ПРОФИЛАКТИКЕ ВИРУСНЫХ ИНФЕКЦИЙ | 2016 |
|
RU2723013C2 |
| КОМПОЗИЦИИ ДЛЯ СУПРЕССИИ ЭКСПРЕССИИ CCR5 И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2004 |
|
RU2353357C2 |
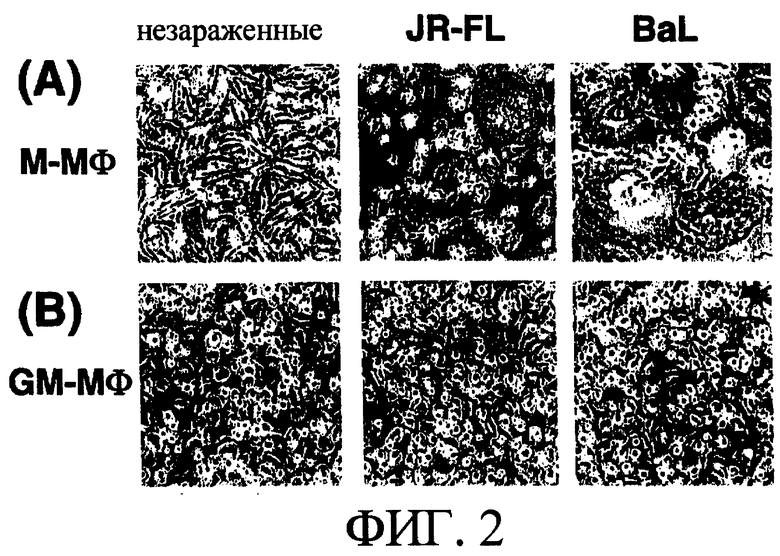
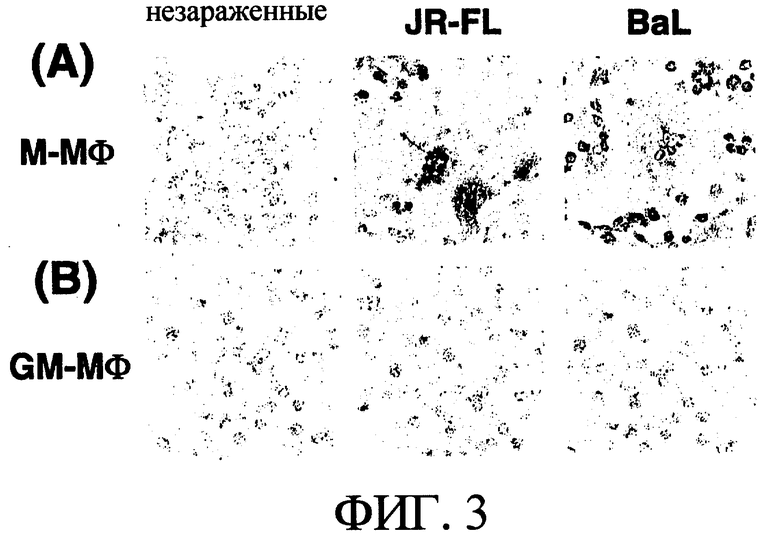
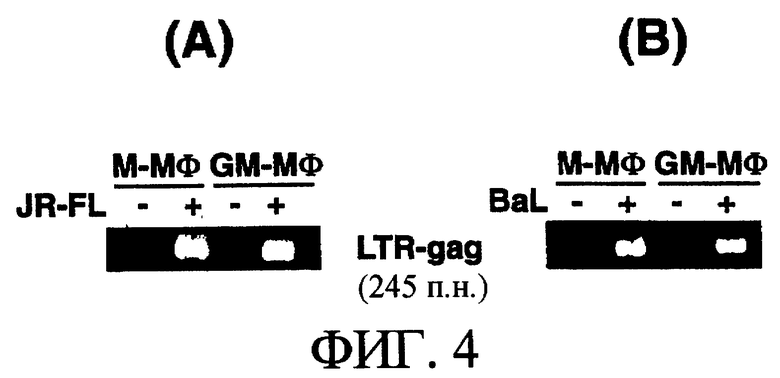
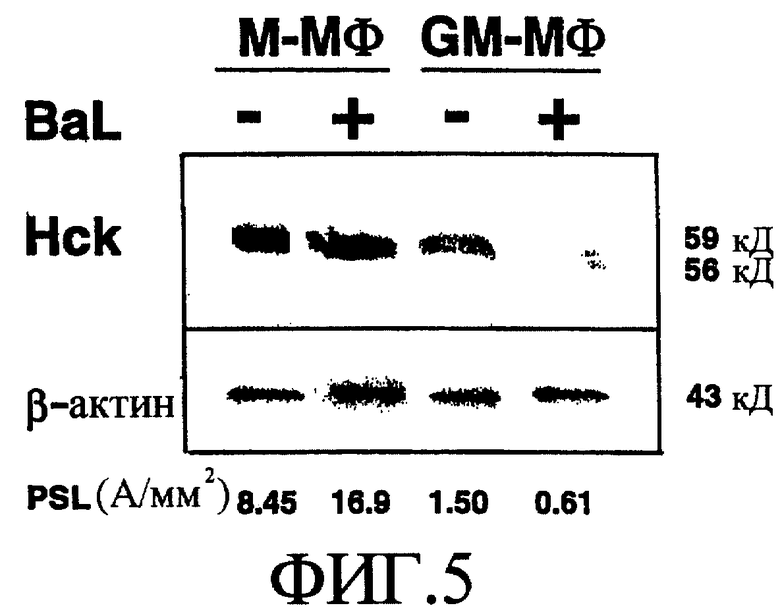
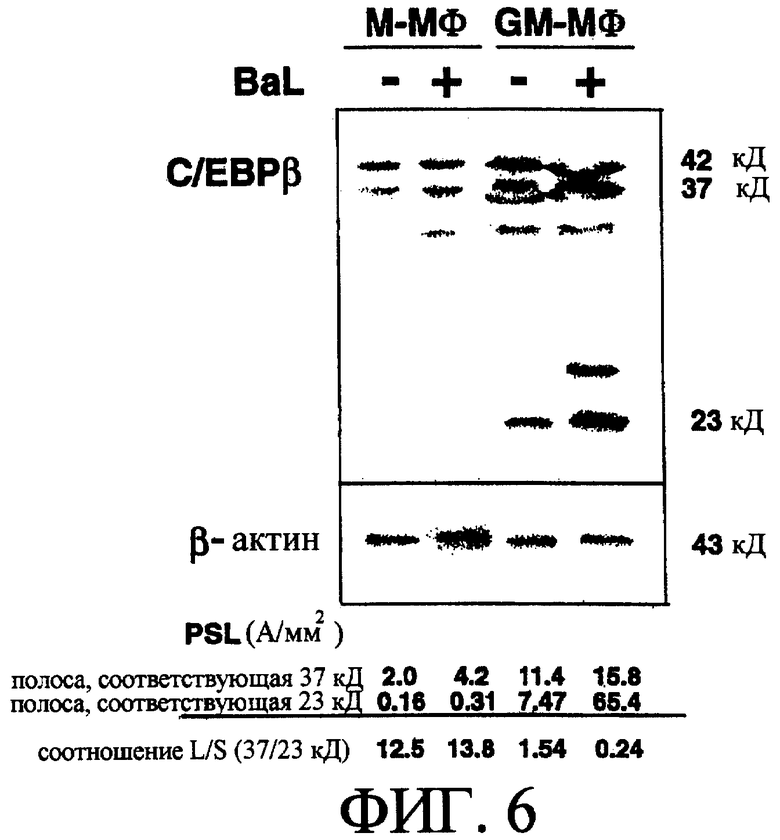
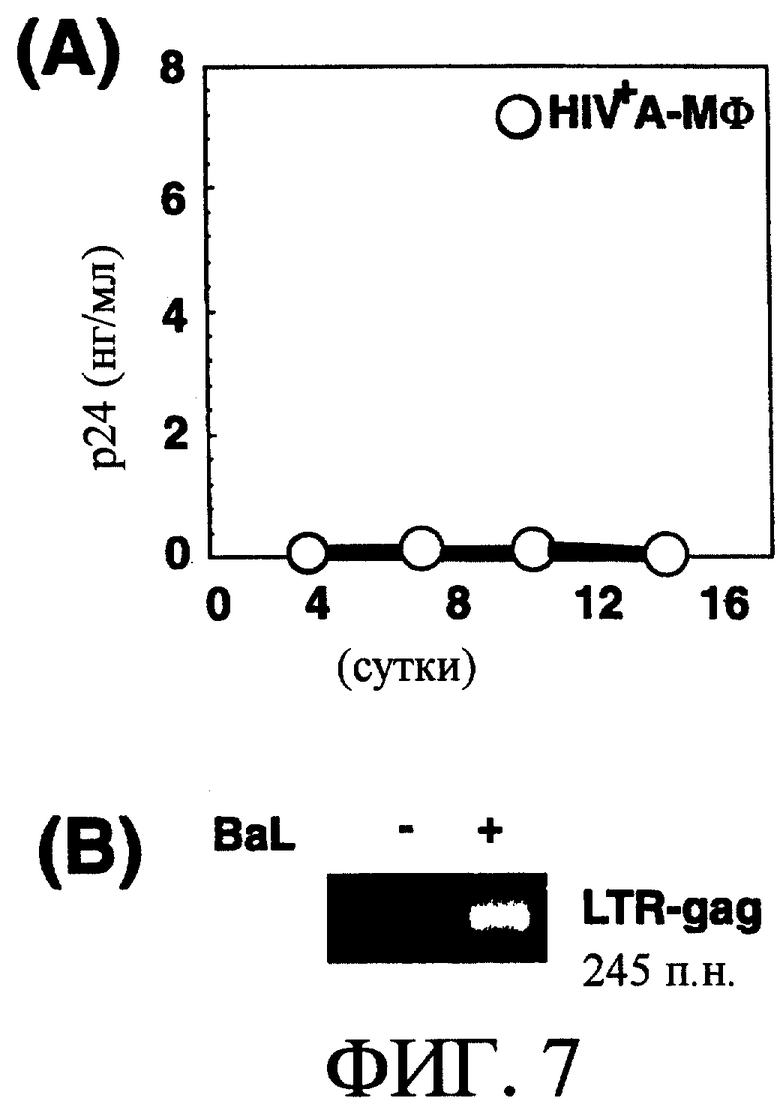
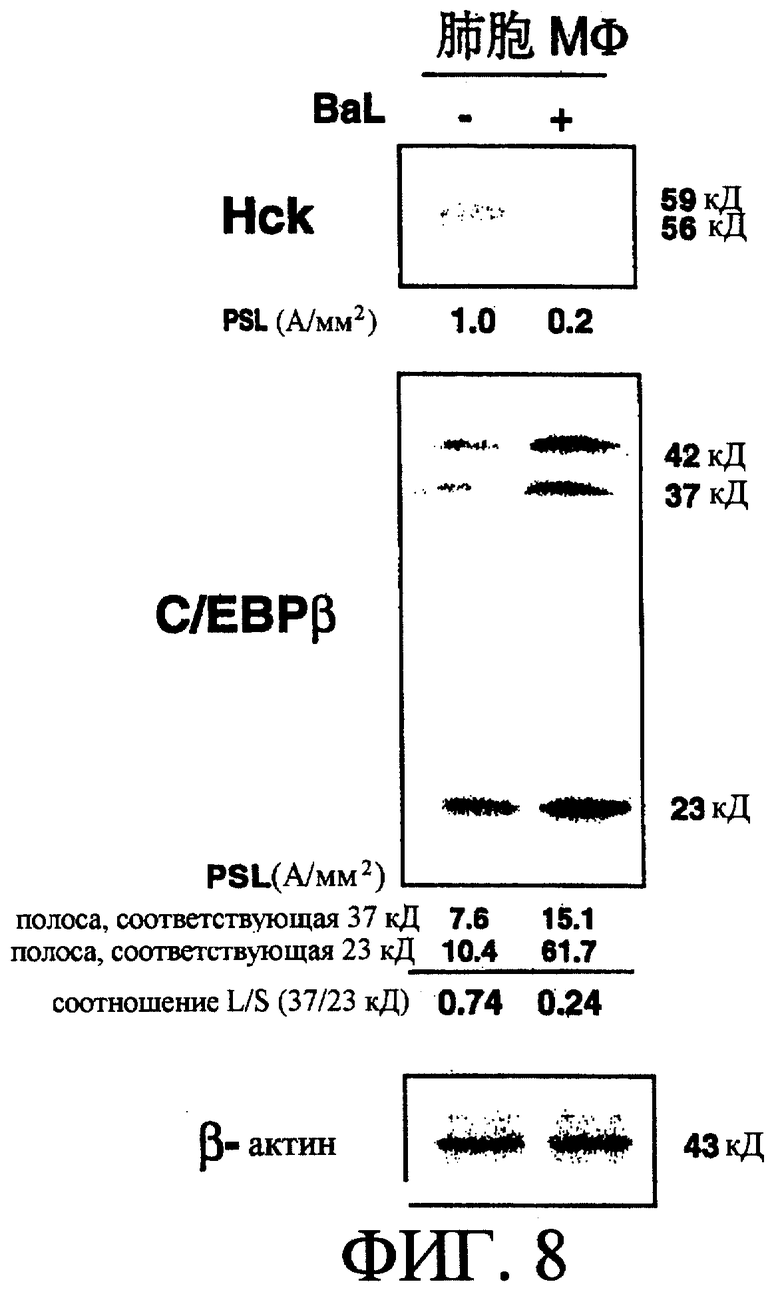

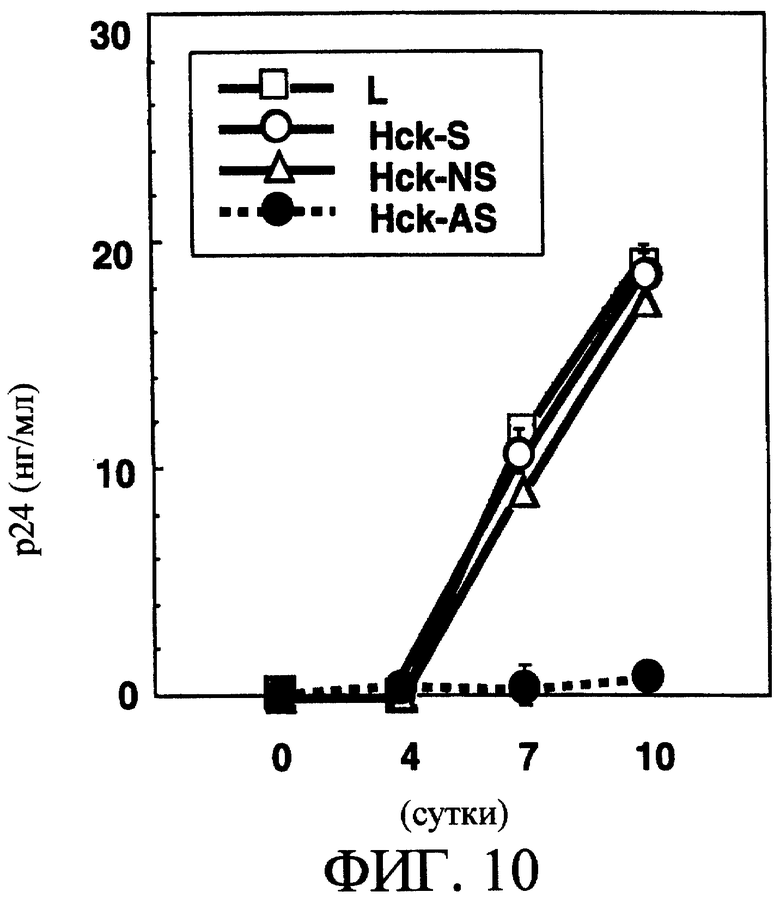
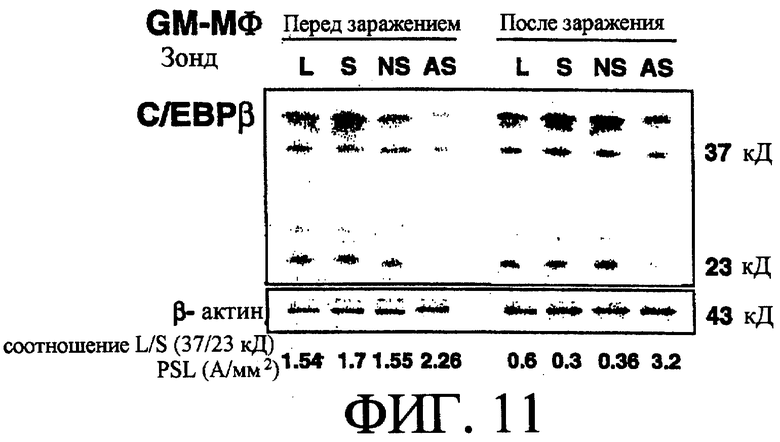
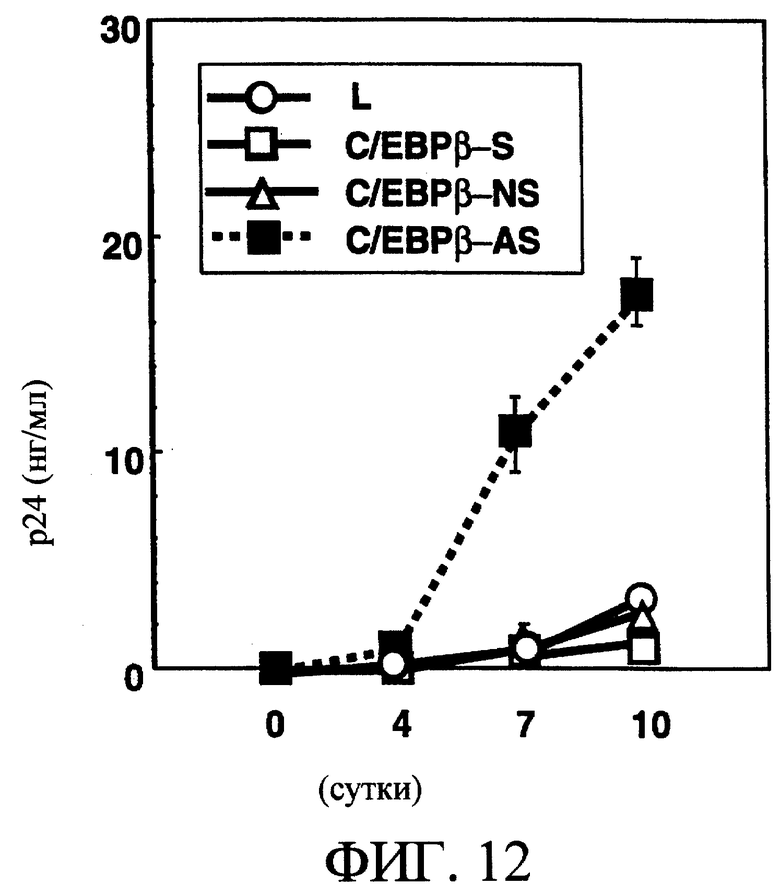
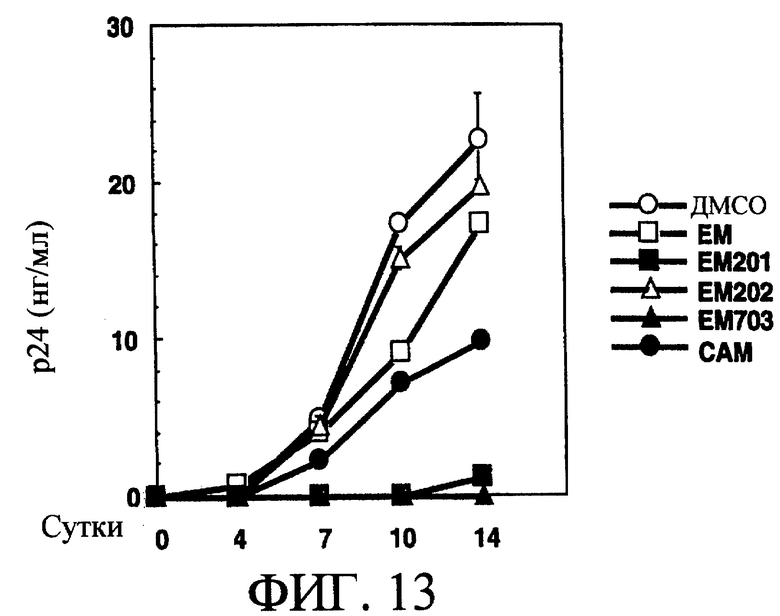
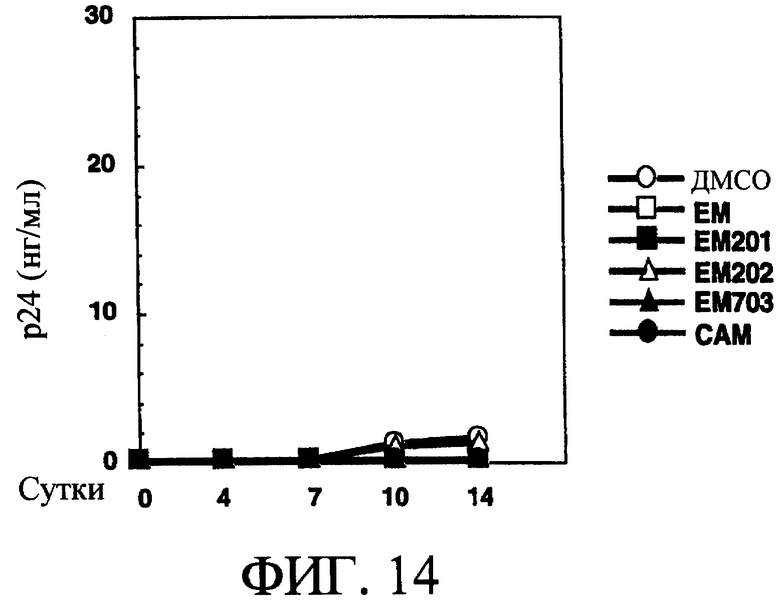
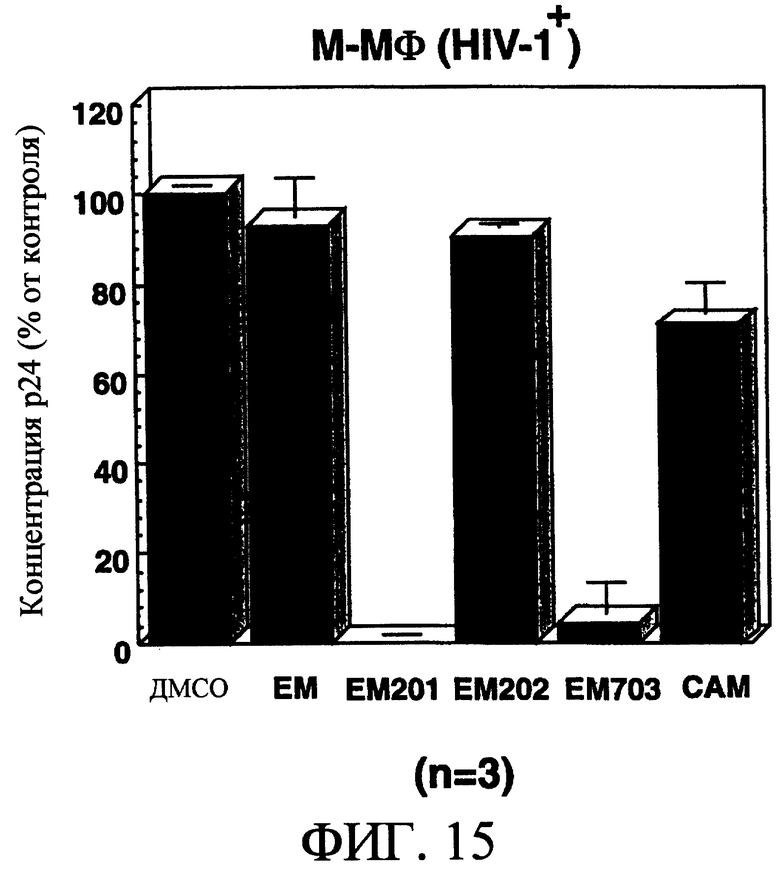
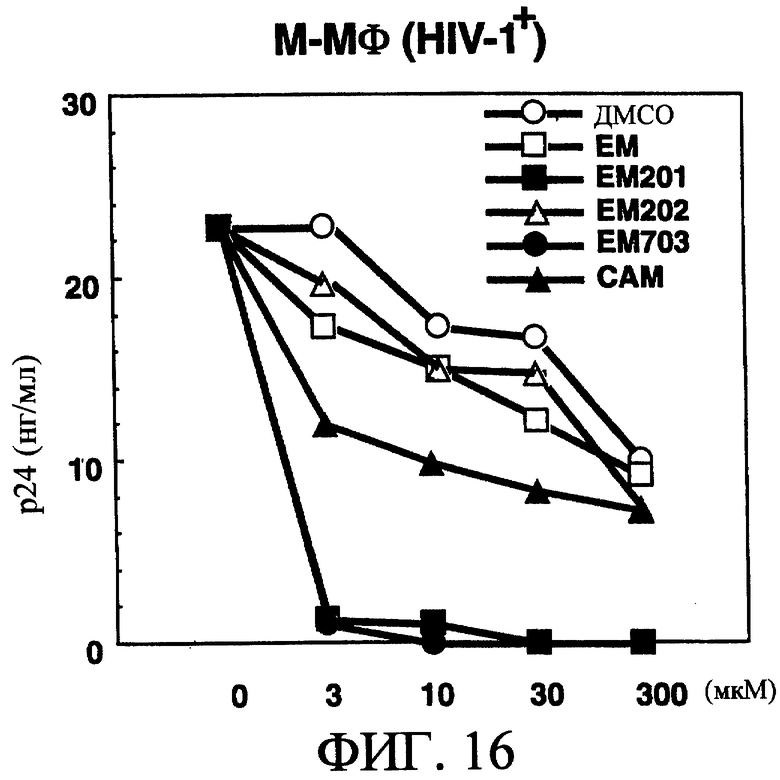
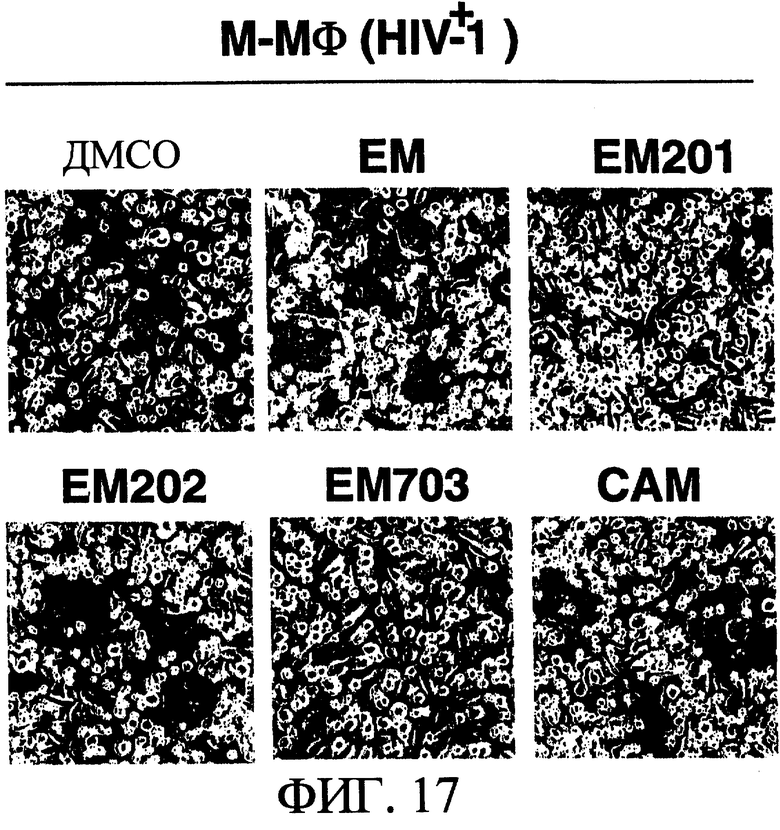
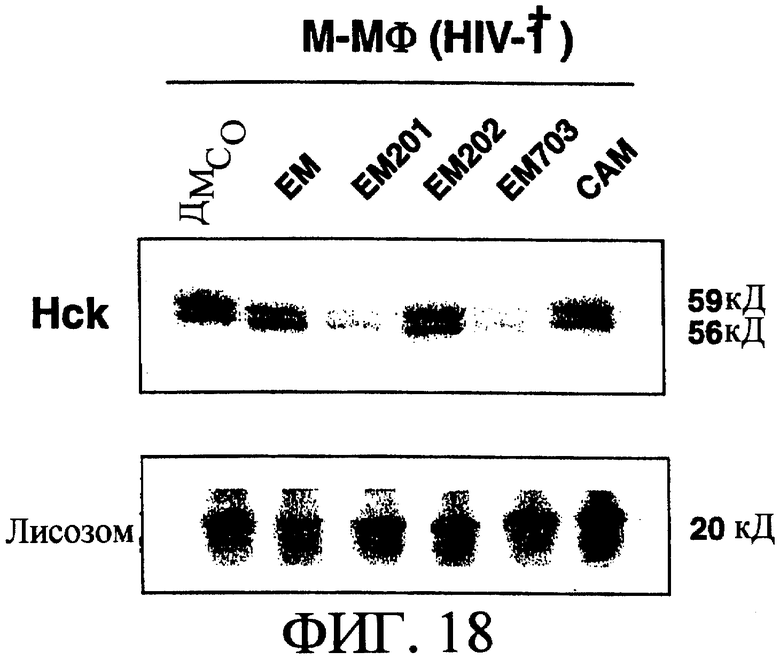
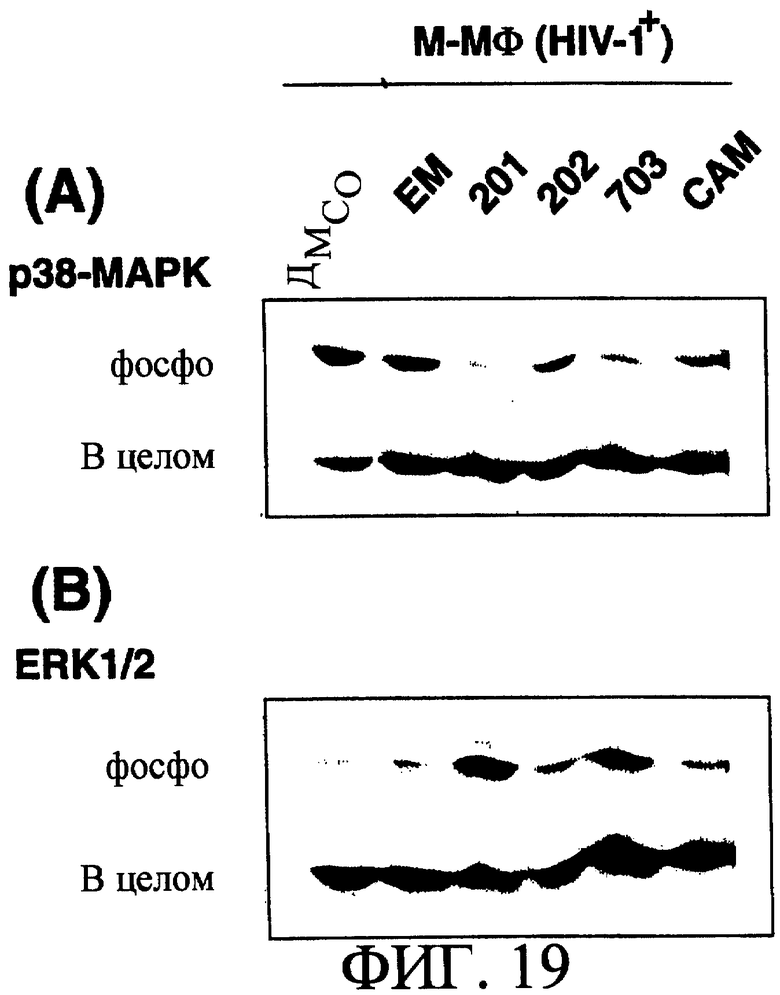
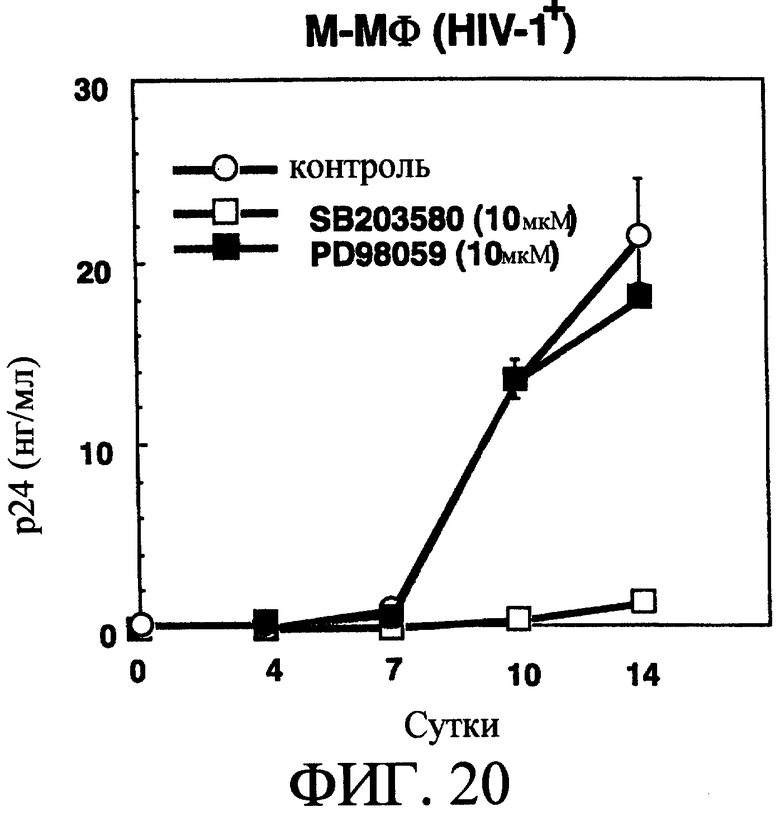
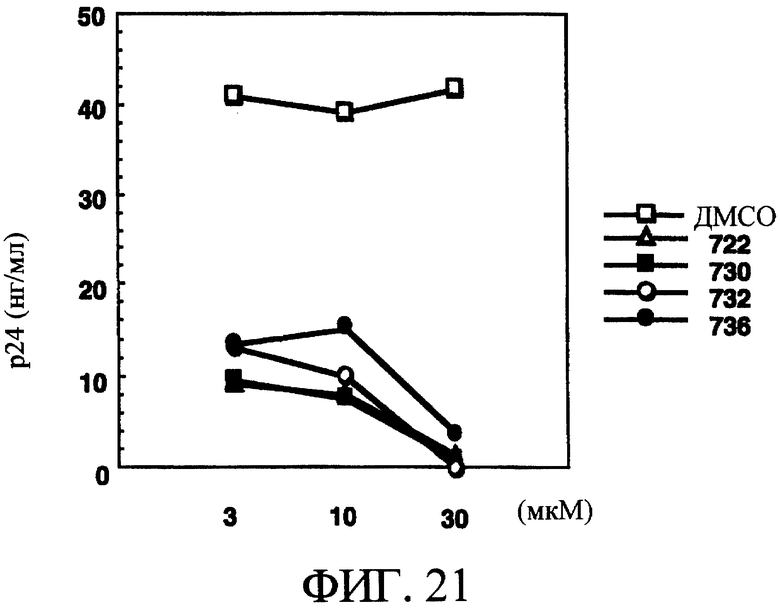
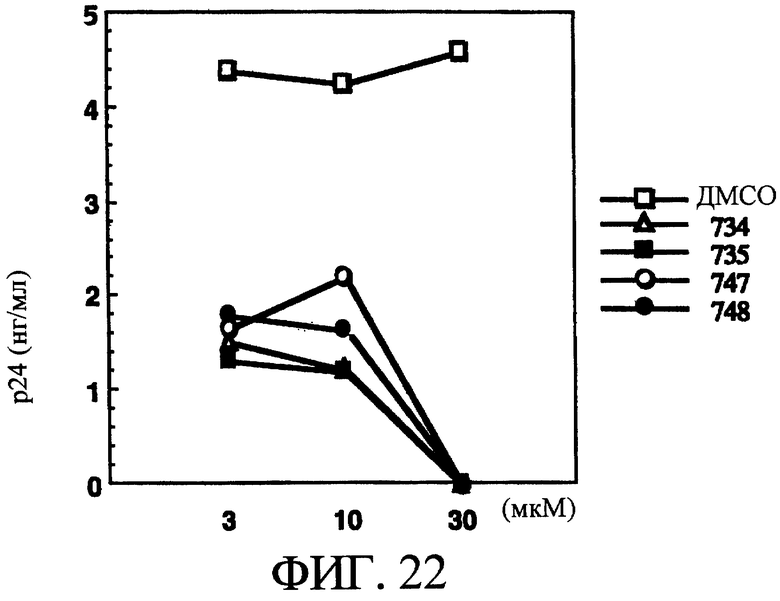
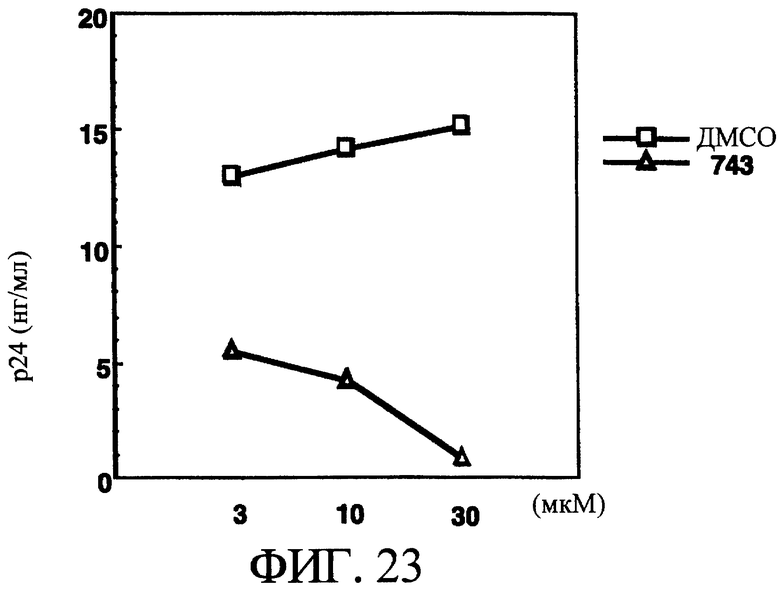
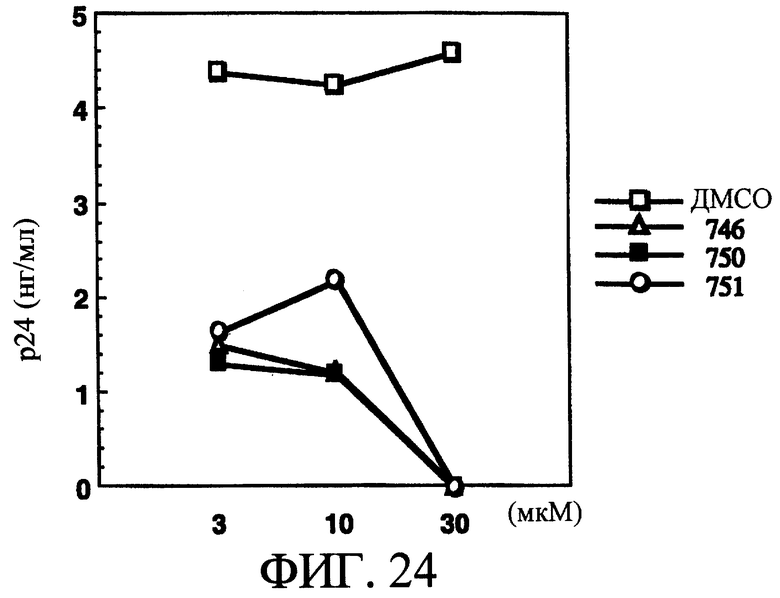
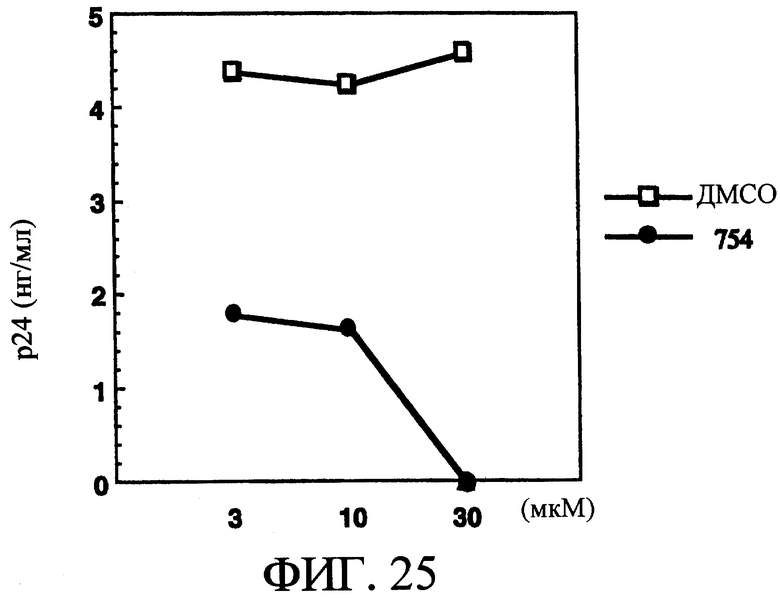
Изобретение относится к химико-фармацевтической промышленности и касается лекарственного средства для подавления заражения и пролиферации вируса иммунодефицита человека в макрофагах, которое содержит производные эритромицина. Данные макролидные соединения обладают высокой ингибирующей активностью в отношении белка тирозинкиназы, и эффективны для подавления заражения и пролиферации вируса иммунодефицита человека. 3 з.п. ф-лы, 25 ил.
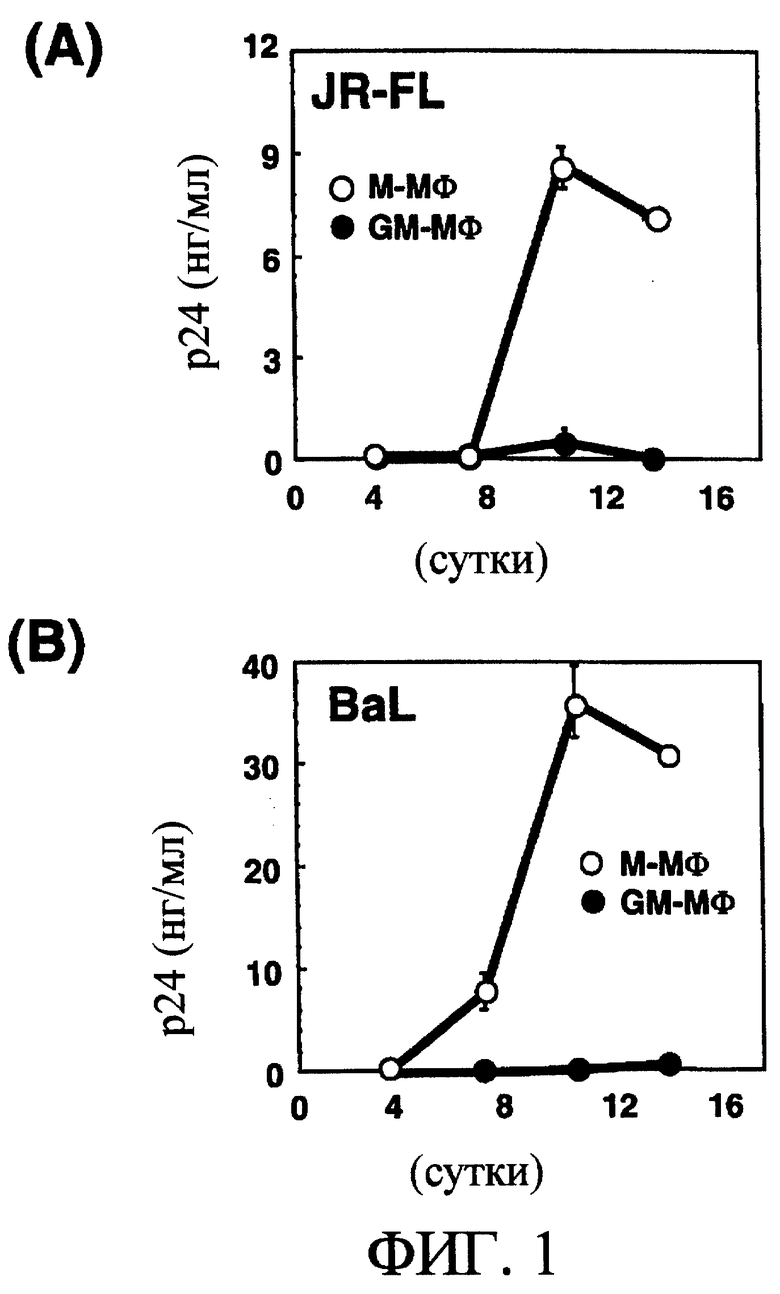
6,15,16-триоксатрицикло [10.2.1.11.4]гексадекана; 4,13-диоксабицикло [8.2.1]тридек-12-ен-5-она,7-[(2,6-дидезокси-3-С-метил-α-L-рибогексопиранозил)окси]-3-(1,2-дигидрокси-1-метилбутил)-2,6,8,10,12-пентаметил-9-[[3,4,6-тридезокси-3-(диметиламино)-β-D-ксило-гексопиранозил]окси]; оксацикло-тетрадекан-2,10-диона; 4-[(2,6-дидезокси-3-О-метил-α-L-рибо-гексопиранозил)окси]-14-этил-12,13-дигидрокси-7-метокси-3,5,7,9,11,13-гексаметил-6-[[3,4,6-тридезокси-3-(диметиламино)-β-D-ксило-гексопиранозил]окси];
де(3’-N-метил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя или его соли; де(3’-N-метил)-3’-N-сульфонил-6,9-ангидро-псевдоэритромицина А 6,9-гемикеталя или его соли; де(3’-N-метил)-[3’-N-(3-гидрокси-1-пропил)]-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя или его соли; де(3’-N-метил)-3’-N-(2-ацетоксиэтил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя или его соли; де(3’-N-метил)-3’-N-цианометил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя или его соли; де(3’-N-метил)-3’-N-(2-фторэтил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя или его соли; бис-де(3’-N-метил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя или его соли;
бис-де(3’-N-метил)-3’-N-этил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя или его соли;
бис-де(3’-N-метил)-3’,3’-N,N-диэтил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя или его соли;
бис-де(3’-N-метил)-3’-N-аллил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя или его соли;
бис-де(3’-N-метил)-3’,3’-N,N-диаллил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя или его соли;
бис-де(3’-N-метил)-3’-N-пропаргил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя или его соли;
бис-де(3’-N-метил)-3’,3’-N,N--дипропил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя или его соли;
бис-де(3'-N-метил)-3'-N-гексил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя или его соли; бис-де(3'-N-метил)-3',3'-N,N-дигексил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя или его соли;
бис-де(3'-N-метил)-3'-N-бензил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя или его соли;
бис-де(3'-N-метил)-3',3'-N,N-дибензил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя или его соли;
бис-де(3'-N-метил)-3'-N-(2-пропил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя или его соли;
бис-де(3'-N-метил)-3',3'-N,N-ди-(10-бром-1-деканил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя или его соли;
бис-де(3'-N-метил)-3'-N-ацетил-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя ил его соли; де(3'-диметиламино)-3'-пиперидино-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя или его соли; де(3'-диметиламино)-3'-пирролидино-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя или его соли;
де(3'-диметиламино)-3'-морфолино-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя или его соли;
де(3'-диметиламино)-3'-[гексагидро-1-(1H)-азепинил]-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя или его соли;
де(12-гидрокси)-де[12-(1-гидроксипропил)]-12-гидроксиоксим-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя или его соли;
де[12-(1-гидроксипропил)]-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя или его соли; де(12-гидрокси)-де-[12-(1-гидроксипропил)]-12-амино-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя или его соли;
де(3’-N-метил)-де[12-(1-гидроксипропил)]-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя или его соли;
де(3-O-кладинозил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя или его соли и де(3-O-кладинозил)-де(3’-N-метил)-8,9-ангидро-псевдоэритромицина А 6,9-гемикеталя или его соли.
Конвенционный приоритет от 07.03.2002 (JP 2002-61788) по пп.1-3 и 4 в части признаков: соединения, перечисленные с начала и до “оксацикло-тетрадекан-2,10-диона-4-[2,6-дидезокси-3-O-метил-α-L-рибозо-гексопиранозил)окси]-14-этил-12,13-дигидрокси-7-метокси-3,5,7,9,11,13-гексаметил-6-[[3,4,6-тридезокси-3-(диметиламино)-β-D-ксило-гексопиранозил]окси]” включительно, а по всем остальным соединениям по п.4 имеют приоритет от 06.09.2002 (JP 2002-261024).
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Pontani DR et all | |||
| Inhibition of HIV replication by liposomal encapsulated amphotericin B | |||
| Antiviral Res | |||
| Механизм для сообщения поршню рабочего цилиндра возвратно-поступательного движения | 1918 |
|
SU1989A1 |
| СПОСОБ СНИЖЕНИЯ ТЯЖЕСТИ ТОКСОПЛАЗМОЗА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ПРИМЕНЕНИЕ ПРОИЗВОДНЫХ РИФАМИЦИНА ДЛЯ ПОЛУЧЕНИЯ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ ДЛЯ ЛЕЧЕНИЯ ТОКСОПЛАЗМОЗА | 1994 |
|
RU2121838C1 |
Авторы
Даты
2005-04-27—Публикация
2002-11-20—Подача