Группа изобретений относится к медицине, в частности, к фармакологии - к растворам для инъекций на основе налфубина гидрохлорида, обладающим ярко выраженным анальгетическим действием, и способам их получения. Группа изобретений может найти применение для устранения болевых синдромов средней и выраженной интенсивности при инфаркте миокарда, при подготовке к операции (профилактика) и в послеоперационном периоде, а также в качестве дополнительного средства обезболивания при общей анестезии.
Налфубина гидрохлорид (химическое название: (5 альфа, 6 альфа)-17-(Циклобутилметил)-4,5-эпоксиморфинан-3,6,14-триол) относится к фармакологической группе опиоидов и является производным морфина, однако характерной особенностью его молекулы является наличие метилциклобутильного радикала.
Фармакологическое действие - анальгезирующее (наркотическое). Обладает свойствами агониста-антагониста опиатных рецепторов. Угнетает ЦНС, оказывает анальгезирующее, снотворное, противокашлевое действие. Возбуждает мю-рецепторы и блокирует каппа-рецепторы.
Наиболее близкий раствор для инъекций, обладающий выраженным анальгетическим действием, раскрыт в “Инструкции по медицинскому применению препарата НУБАИН (Nubain)” (одобрено Фармакологическим государственным комитетом Минздрава России 12 ноября 1998, протокол №9-1). Раствор для инъекций содержит 10 мг налфубина гидрохлорида в 1 мл раствора и вспомогательные вещества: буферные вещества (лимонную кислоту и цитрат натрия водный), стабилизаторы (хлорид натрия) и воду для инъекций.
Налфубина гидрохлорид представляет собой белый или почти белый кристаллический порошок, растворимый в воде. Известный раствор налфубина устойчив в слабокислой среде, однако при повышении рН выше 6 две молекулы налфубина реагируют между собой с образованием бисмалбуфина. Интенсивность этого процесса возрастает при повышении температуры, под воздействием света и в присутствии ионов тяжелых металлов, что приводит к потере устойчивости лекарственной формы в течение срока годности препарата.
Задачей изобретения является получение отечественного препарата с сильным анальгезирующим действием, соответствующего требованиям ГФ XI, стабильного при хранении более 2,5 лет.
Поставленная задача решается раствором для инъекций, обладающим выраженным анальгетическим действием, содержащим налбуфина гидрохлорид, буферную смесь, стабилизатор и воду для инъекций, при этом раствор дополнительно содержит комплексообразующий компонент при следующем соотношении, мас.%:
Налбуфина гидрохлорид 0,8-2,2
Буферная смесь 0,5-3,5
Стабилизатор 0,15-0,25
Комплексообразующий компонент 0,001-0,2
Вода Остальное
В частных воплощениях изобретения поставленная задача решается тем, что:
в качестве комплексообразующего компонента раствор может содержать динатриевую соль этилендиаминтетрауксусной кислоты (трилон Б) или другой известный комплексообразователь, например, тетацин кальция;
в качестве буферной смеси он может содержать смесь лимонной кислоты и, по меньшей мере, одного вещества, выбранного из группы, включающей натрия цитрат, натрия дигидроцитрат, натрия гидрофосфат, натрия дигидрофосфат или кристаллогидраты упомянутых веществ;
упомянутая смесь может содержать 0,1-3,4 мас.% кислоты лимонной, в качестве стабилизатора раствор может содержать натрия хлорид, в частности 0,18-0,22 мас.% натрия хлорида;
дополнительно раствор может содержать антиоксиданты в количестве 0,2-2,0 мас.%, в качестве которых могут быть использованы натрия гидросульфит и/или натрия метабисульфит, и/или натрия тиосульфат.
Поставленная задача также решается способом получения раствора для инъекций, в соответствии с которым осуществляют барботаж воды для инъекций инертным газом при 25-30°С в течение 30-60 минут, затем, не прерывая барботажа, в воду последовательно вносят буферную смесь, стабилизатор, комплексообразователь и налбуфина гидрохлорид, затем полученный раствор охлаждают до 20°С, проводят стерилизующую фильтрацию, наполнение ампул, их запайку и стерилизацию.
Желательно стерилизующую фильтрацию, наполнение ампул и их запайку осуществлять в атмосфере инертного газа, а стерилизацию ампул проводить при 120±5°С в течение 5-12 минут.
Сущность изобретения состоит в следующем.
Использование в качестве вспомогательных веществ буферной смеси, стабилизаторов и дополнительное введение комплексообразующего компонента в заявляемых количествах позволяет улучшить стабильность раствора налфубина.
Большое влияние на процесс окисления лекарственного средства оказывает присутствие ионов тяжелых металлов Fe+3, Mn2+и т.п., которые являются катализаторами окисления. Ионы тяжелых металлов часто переходят в растворы из стекла, аппаратуры или могут присутствовать в качестве производственной примеси.
Для стабилизации легкоокисляющихся веществ используются комплексообразующие вещества ЭДТА - этилендиаминтетрауксусная кислота. Комплексообразователь придает способность к образованию внутрикомплексных водорастворимых соединений с большим числом катионов. Наилучшими в данном случае свойствами в качестве комплексообразователя обладает трилон Б, представляющий собой динатриевую соль этилендиаминтетрауксусной кислоты. В этом случае устойчивость комплексных соединений настолько велика, что невозможно обнаружить соответствующий катион.
Буферная смесь в заявленном количестве вводится в раствор для создания оптимальных границ рН. Нами было установлено, что в качестве альтернативы к цитрату натрия, используемого в качестве компоненты буферной смеси в известном растворе, также могут быть использованы такие натрийсодержащие вещества, как натрия дигидроцитрат, натрия гидрофосфат, натрия дигидрофосфат или кристаллогидраты упомянутых веществ. При общем количестве буферной смеси в растворе 0,5-3,5 мас.%, будет желательно, чтобы содержание лимонной кислоты в ней составляло 0,1-3,4 мас.%. Для более быстрой стабилизации рН препарата добавляют натрия хлорид.
Для получения стабильного в течение длительного времени препарата важным также является то, как этот препарат получен.
В нашем способе осуществляется предварительное насыщение воды для инъекций инертным газом, и все последующие операции также проводятся в среде нейтрального газа.
Изобретение осуществляется следующим образом.
Система приготовления раствора и розлива продувается инертным газом (аргоном или азотом). Все производственные операции проводятся под защитой инертного газа.
Вода для инъекций предварительно насыщается инертным газом при температуре 25-30°С в течение 30-60 минут. В воду вносят последовательно при поддержании указанной температуры и, не прекращая барботирования, расчетное количество буферной смеси (лимонной кислоты и, по меньшей мере, одного вещества, выбранного из группы, включающей натрия цитрат, натрия дигидроцитрат, натрия гидрофосфат, натрия дигидрофосфат или кристаллогидраты упомянутых веществ). Затем вносят отмеренное количество натрия хлорида и трилона Б. Потом добавляют отмеренное количество налфубина гидрохлорид и, при необходимости, антиоксиданты, доводят объем раствора до необходимого водой для инъекций. Раствор охлаждают до температуры 20°С и проводят стерилизующую фильтрацию на фильтрационной установке системы Pall с величиной пор 0,45 и 0,22 мкм. Фильтрацию ведут передавливанием инертным газом. Наполнение ампул и их запайку ведут в токе инертного газа. Стерилизацию ампул ведут при 120±2°С в течение 8 минут.
Пример 1.
Приготовляли опытные составы, содержащие от 9,0 до 21,0 г/л (0,9-2,1 мас.%) нафлубина, натрия хлорид (0,15-0,25 мас.%), раствор кислоты соляной с концентрацией 0,1-1 моль/л или раствор натрия гидроксида с концентрацией 0,1-1 моль/л до рН 3,0-5,5, трилона Б 0,02 мас.%, воды для инъекций - остальное.
Составы получали в обычных условиях. В ходе наблюдений установлено, что данные составы недостаточно стабильны: после стерилизации значения рН препаратов возрастало до 5,5 и более, что приводило к изменению внешнего вида раствора (появление опалесценции и желтоватой окраски).
Пример 2. То же, что и в примере 1. Все операции проводились под инертным газом - азотом или аргоном. Это позволило уменьшить опалесценцию растворов и нарастание интенсивности краски не только при получении препаратов в светозащищенном оборудовании, но и без защиты от света. Значение рН с 4,02 достигло 5,95 через 6 месяцев хранения препарата.
Пример 3.
То же, что и в примере 2, но дополнительно в растворы вводили лимонную кислоту в количестве от 0,1 до 0,15 мас.%. В данном случае лимонная кислота выполняла функции кислотного агента, стабилизирующего значение рН в заданном диапазоне 3,0-5,5. Однако несмотря на стабилизацию рН постоянство конечного продукта сильно зависит от качества исходного сырья и вспомогательных веществ.
Пример 4 (в соответствии с изобретением)
То же, что и в примере 3, но дополнительно вводили 0,5-1,2 мас.%, по меньшей мере, одного вещества, выбранного из группы, включающей натрия цитрат, натрия дигидроцитрат, натрия гидрофосфат, натрия дигидрофосфат или кристаллогидраты упомянутых веществ. Данные компоненты, взятые в соответствующих соотношениях с лимонной кислотой, образуют буферные системы с заранее заданным оптимальным стабильным значением рН 3,0-5,5 раствора препарата. Отсутствие в составах натрия гидросульфита, натрия метабисульфита и/или натрия тиосульфата позволяет применять данные составы у астматических больных, чувствительных к серосодержащим компонентам.
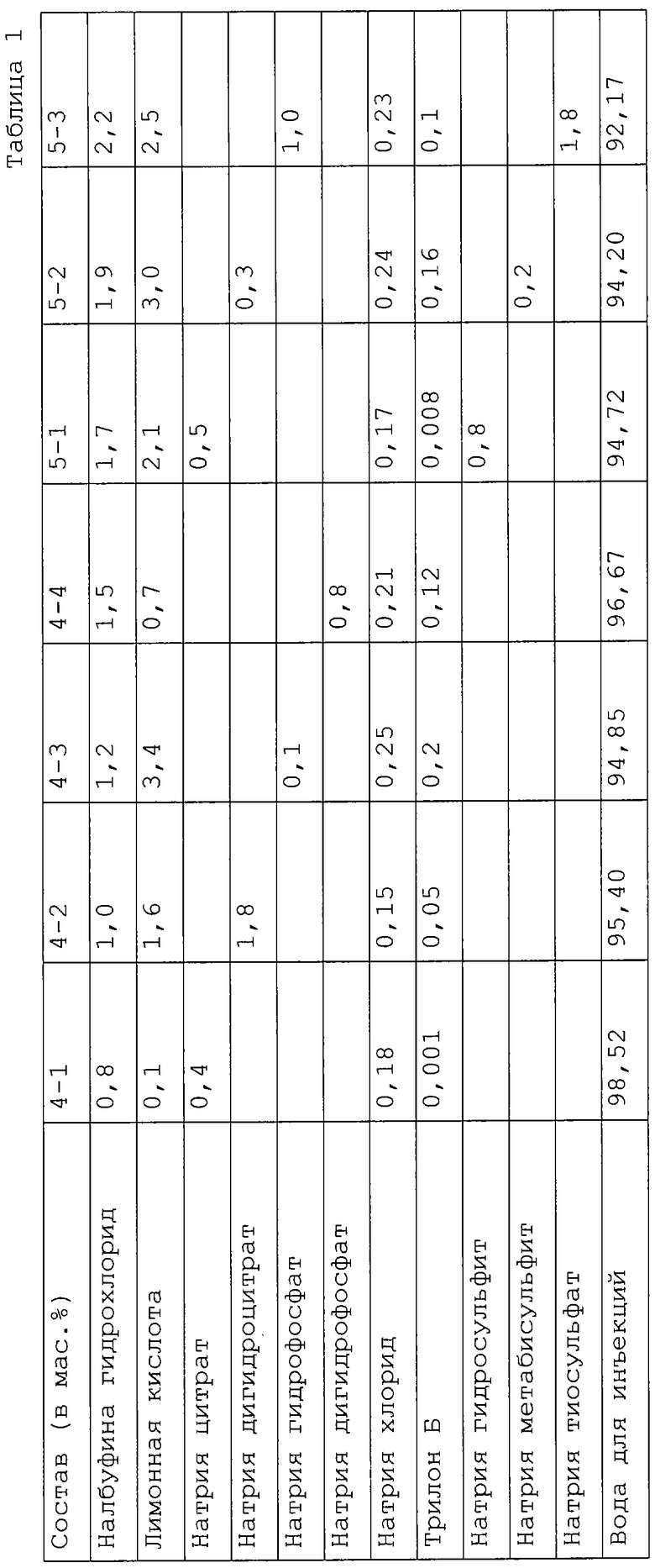
В таблице 1 приведены составы, полученные в соответствии с данным примером (составы 4-1, 4-2, 4-3 и 4-4).
В результате препараты имели вид слабоопалесцирующей и слабоокрашенной жидкости. Для всех составов значения рН в течение 10 месяцев наблюдений практически не изменялись и находились на уровне 3,61-3,65 для составов с содержанием налфубина около 1,0 мас.% и 4,53-4,57 с содержанием налфубина около 2,0 мас.%.
Пример 5.
То же, что и в примере 4, но дополнительно вводили антиоксиданты.
Препараты имели вид слабоопалесцирующей и практически бесцветной жидкости. Для всех составов значения рН в течение 10 месяцев наблюдений практически не изменялись и находились на уровне 4,72-4,76 для составов с содержанием налфубина около 1,0 мас.% и 4,85-4,94 с содержанием налфубина около 2,0 мас.%.
| название | год | авторы | номер документа |
|---|---|---|---|
| РАСТВОР ДЛЯ ИНЪЕКЦИЙ НА ОСНОВЕ БУТОРФАНОЛА, ОБЛАДАЮЩИЙ АНАЛЬГЕТИЧЕСКИМ ДЕЙСТВИЕМ | 2006 |
|
RU2312662C1 |
| РАСТВОР ДЛЯ ИНЪЕКЦИЙ, СОДЕРЖАЩИЙ НАЛБУФИН | 2012 |
|
RU2483731C1 |
| СРЕДСТВО ДЛЯ ЭФФЕКТИВНОГО КУПИРОВАНИЯ ОСТРОГО И/ИЛИ ХРОНИЧЕСКОГО БОЛЕВОГО СИНДРОМА И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2016 |
|
RU2622980C1 |
| ИНЪЕКЦИОННАЯ ЛЕКАРСТВЕННАЯ ФОРМА ДЛЯ ЛЕЧЕНИЯ ОСТРОГО ИШЕМИЧЕСКОГО ИНСУЛЬТА И ЧЕРЕПНО-МОЗГОВОЙ ТРАВМЫ, СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ И ПРИМЕНЕНИЕ | 2009 |
|
RU2431496C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ В ИНЪЕКЦИОННОЙ ФОРМЕ С АНАЛЬГЕТИЧЕСКОЙ АКТИВНОСТЬЮ (ВАРИАНТЫ) | 2013 |
|
RU2563211C2 |
| РАСТВОР ДЛЯ ВНУТРИВЕННОГО И ВНУТРИМЫШЕЧНОГО ВВЕДЕНИЯ НА ОСНОВЕ БРОМДИГИДРОХЛОРФЕНИЛБЕНЗОДИАЗЕПИНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2015 |
|
RU2605824C1 |
| ЖИДКИЙ ПРЕПАРАТ, СОДЕРЖАЩИЙ ПРОИЗВОДНОЕ КАМПОТОТЕЦИНА, И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ПОЛУЧАЕМАЯ ПУТЕМ ЛИОФИЛИЗАЦИИ ПРЕПАРАТА | 2003 |
|
RU2315623C2 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ДЕГЕНЕРАТИВНЫХ ПРОЦЕССОВ ОПОРНО-ДВИГАТЕЛЬНОГО АППАРАТА | 2024 |
|
RU2827071C1 |
| СРЕДСТВО ДЛЯ КУПИРОВАНИЯ ГЛУТАМАТ-ИНДУЦИРОВАННОГО АПОПТОЗА И ИНГИБИРОВАНИЯ NMDA-РЕЦЕПТОРОВ, ОБЛАДАЮЩЕЕ ИММУНОМОДУЛИРУЮЩИМ ДЕЙСТВИЕМ, ДЛЯ ЛЕЧЕНИЯ РАССТРОЙСТВ НЕРВНОЙ СИСТЕМЫ, ПОСЛЕДСТВИЙ ЧЕРЕПНО-МОЗГОВОЙ ТРАВМЫ И ИШЕМИЧЕСКОГО И ГЕМОРРАГИЧЕСКОГО ИНСУЛЬТА | 2013 |
|
RU2605339C2 |
| ГЛАЗНЫЕ КАПЛИ ДЛЯ ЛЕЧЕНИЯ ВОЗРАСТНОЙ КАТАРАКТЫ ЯДЕРНОГО ВИДА | 2019 |
|
RU2720676C2 |
Изобретение относится к медицине, в частности, к фармакологии - к раствору для инъекций на основе налфубина гидрохлорида, обладающему выраженным анальгетическим действием, и способу его получения. Раствор для инъекций содержит компоненты в мас.%: налбуфина гидрохлорид 0,8-2,2, буферную смесь 0,5-3,5, стабилизатор 0,15-0,25, трилон Б (комплексообразующий компонент) 0,001-0,2 и воду - остальное. Техническим результатом является получение отечественного препарата с анальгезирующим действием, стабильного при хранении более 2,5 лет. 2 н. и 9 з.п. ф-лы, 1 табл.
Налбуфина гидрохлорид 0,8-2,2
Буферная смесь 0,5-3,5
Стабилизатор 0,15-0,25
Комплексообразующий компонент 0,001-0,2
Вода Остальное
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ БОЛЕУТОЛЯЮЩЕГО СРЕДСТВА И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1996 |
|
RU2141845C1 |
| АНЕСТЕЗИРУЮЩИЙ СОСТАВ ПРОЛОНГИРОВАННОГО ДЕЙСТВИЯ | 1999 |
|
RU2180557C2 |
| US 5204118 А, 20.04.1993 | |||
| US 5709833 A, 20.07.1998 | |||
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
Авторы
Даты
2005-06-27—Публикация
2004-01-23—Подача