Изобретение относится к медицине, в частности к клинической фармакологии и восстановительной терапии.
Как известно, многие липидзависимые заболевания сопровождаются нарушениями в работе иммунной системы. Так, сердечно-сосудистые заболевания сочетаются с повреждением системы не специфической резистентности, вызванным значительной антигенной нагрузкой со стороны накапливающихся липопротеидов. Поэтому крайне актуальным является поиск профилактических средств, обладающих наряду с липидкоригирующими эффектами и иммунокорригирующими свойствами.
Традиционная схема лечения больных с дислипидемиями основана на диетотерапии, включающей пониженное содержание в пище липидов, умеренное содержание углеводов, обеспечивающей нормальное течение жизненных процессов и необходимой для поддержания высокого уровня функционирования организма. В комплексе с диетой больным назначаются синтетические препараты различного спектра действия, снижающие уровень холестерина и триглицеридов в крови. Данные методы лечения не всегда способствуют восстановлению нарушенного в результате болезни физиологического состояния организма, так как не предусматривают коррекцию состояния иммунитета, который в значительной степени повреждается в результате нарушения обмена липидов. В связи с этим, целесообразен поиск препаратов и пищевых продуктов, обладающих помимо липидкоригирующих свойств иммуномодулирующей активностью.
В последние годы большое внимание привлекают жиры морских гидробионтов, содержащие ω3 полиненасыщенные жирные кислоты (ПНЖК). Доказаны их разнообразные биологические эффекты, позволяющие использовать их в качестве источников биологически активных веществ для профилактике и лечении целого ряда заболеваний. Известно, что ω3 ПНЖК включаются в клеточные структуры организма и оказывают модифицирующее влияние на структурно-функциональную организацию клеточных мембран, активность мембраносвязанных ферментов и биосинтез эйкозаноидов. Довольно часто морские гидробионты используются как потенциальные источники именно ω3 ПНЖК. В то же время в состав суммарной липидной фракции жиров морских гидробионтов могут входить и другие липиды. Именно разнообразный состав липидов из различных морских источников определяет специфичность действия используемых средств и не позволяет подходить к их применению по принципу аналогии, что требует детального изучения механизма биологического действия, анализа эффективности и безопасности их использования в клинической практике. Так, например, жиры из печени морских моллюсков, в частности кальмаров, богаты неомыляемыми веществами (Hayashi К., Okawa Y., Kawasaki К. Liver lipids of gonatid squid Berryteuthis magister: a rich source of alkyi glyceryl ethers. 1985, Bull. Jap. Soc. Sci. Fish., vol.51, №9, p.1523-1526), имеющими высокую биологическую активность, отличающуюся от свойств ω3 ПНЖК. Бессистемное и бесконтрольное использование разнообразных природных источников биологически активных веществ, в том числе и морских гидробионтов, могут вызвать тяжелые осложнения и нести огромный риск для генофонда страны.
Большинство натуральных жиров и масел представляют собой триглицериды - эфиры глицерина и жирных кислот:
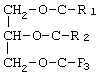
Среди разнообразия жиров нередки случаи присутствия в них значительных количеств алкил-диацилглицеридов (АДГ). В этих соединениях в 1-ом положении молекулы находится алкильный остаток, связанный с глицерином простой эфирной связью:
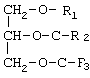
Если из молекулы удалить свободные жирные кислоты, то получаются спирты общей формулы:
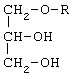
Если R=16:0 (С16Н33)* (* - Примечание: 16:0 - обозначает наличие в радикале 16-ти атомов углерода и 0 двойных связей; в скобках приведен элементный состав.), то спирт химиловый, если R=18:0 (С18Н37), то батиловый, если R=18:1 (C18H35), то селахиловый. Сумма трех этих спиртов от их общей суммы в природных липидах составляет 90 % и более (Hayashi К., Okawa Y., Kawasaki К. Liver lipids of gonatid squid Berryteuthis magister: a rich source of alkyi glyceryl ethers. 1985, Bull. Jap. Soc. Sci. Fish., vol.51, №9, p.1523-1526). В научной литературе эта суммарная композиция спиртов получила название алкил-глицериловых эфиров (АГЭ).
Известно местное применение (Bodman J., Maisin J.H. The α-glyceryl ethers//Clinica Chimica Acta, 1958, v.3, p.253-274) алкил-глицериловых эфиров на заживление ран у крыс Вистар от лучевой травмы. Одни крысы обрабатывались АГЭ, другие тальком, содержащим антибиотик. Результаты продемонстрировали почти 2-х кратное ускорение заживления раны от стадии некроза до повторного роста волос.
АГЭ были апробированы на некоторых пациентах с серьезными наружными поражениями:
а) незаживающая гнойная рана
Местное применение АГЭ в течение одной недели инициировало грануляцию ран.
б) незаживающие раны, связанные с хирургическим удалением злокачественных
опухолей
Пациентке с удаленной карциномой груди ежедневно внутримышечно вводили по 100 мг АГЭ в 2,5 мл арахисового масла. Инъекции были безболезненные и не вызывали каких-либо реакций. После 4-х дней на ране была видна свежая грануляционная ткань. Через 1,5 месяца рана имела здоровый вид, а на 3-м месяце лечение было прекращено.
в) незаживающие гнойные раны, связанные с хирургической обработкой переломов
Больным ставили инъекции АГЭ, как в предыдущем случае, и одновременно наносили порошок АГЭ на рану. Лечение продолжали в течение всего периода трансплантаций. Другая терапия ввиду хороших результатов даже не рассматривалась.
г) незаживающие раны, связанные с лучевым поражением
Местное применение АГЭ с внутримышечной их инъекцией приводило к немедленному началу заживления радиационных ожогов.
д) заживление обыкновенных ран, заводских или случайных ожогов
Никакого эффекта в этом случае не наблюдали. АГЭ замедляли заживление и лечение ими останавливали.
Известны примеры внутреннего потребления АГЭ при лечении лучевых поражений.
Было проведено клиническое исследование (Brohult A., Holmberg J. Alkoxyglycerols in the treatment of leucopenia caused by irradiation/Nature, 1954, v.174, №4441, p.1102-1103) по влиянию АГЭ, выделенных из жира костного мозга животных, на лейкопению у пациентов, в основном детей, вызванную облучением. АГЭ назначались перорально в течение длительного периода (несколько месяцев). Были изучены 36 больных, из них у 25 назначенная терапия вызвала немедленное увеличение количества лейкоцитов в крови: в 1,5 раза за несколько дней, и в конце лечения более, чем в 2 раза.
Было проведено исследование (Brohult A. Alkoxyglycerols in irradiation treatment/Nature, 1962) на 300-х женщинах, получавших лучевую терапию при раке шейки матки. Пациенки профилактических групп получали по 1,2 г АГЭ. Результативность оценивали по выживаемости больных через 1 год и 5 лет лечения. Приведенные данные, особенно для II стадии рака, показали значительно большую выживаемость в профилактической группе, чем в контрольной.
Известно исследование влияния АГЭ на лейкопению от лучевой терапии (Ghys R. Effets des alkoxyglycerols (Kaby 700) sur la leucopenie consecutive a le radiotherapie/Laval Medical, 1960, v.30, №3, p.331-342). Больные, выбранные для обследования, всего 30 человек, имели разные диагнозы: рак легкого, саркома бицепса, рак груди с костными метастазами, рак шейки матки с метастазами в брюшину, рак желудка, рак поджелудочной железы, рак прямой кишки, анальная саркома, венечная астроцитома, рак гортани и еще 4-е специфические опухоли. Пациенты получали стандартную радиотерапию и АГЭ. Препарат был получен из жира печени полярной акулы и имел фирменное название Kaby 700. В первый день больным назначали 3,4 г жира после фракционирования (с насыщенными жирными кислотами), с содержанием приблизительно 30% батилового спирта, в последующие дни по 1,1 г жира. Автором получены противоречивые результаты, показывающие с одной стороны эффективность воздействия АГЭ, а с другой - отсутствие лечебного эффекта. В отношении интерпретируемости результатов, следует высказать главный недостаток - малое количество наблюдаемых больных при столь значительном наборе патологий.
Известно применение АГЭ при аллергических заболеваниях (European Patent 0333678, 02.01.89, МКИ5 A 61 K 31/08 / Brohult S., Brohult A. Use of glycerol ethers in the treatment of allergic diseases). Средство выделяли из жира печени гренландской акулы, удаляя из него все жирные кислоты. В качестве примера приводятся результаты лечения астмы. После 3-4 месяцев дискомфорт (от болезни) исчезал. В отдельных случаях полное его исчезновение наблюдалось после 6-ти месяцев. В качестве примера приведен случай, когда больной страдал жестокими приступами астмы в течение 15 лет и был полностью зависим от различных медикаментов (кортикостероидов и прочих). После 3,5 месяцев дискомфорт прошел, а медикаментозное лечение было сокращено. Спустя еще 3 месяца от него отказались полностью. Фирменное название препарата - "Ecomer". Каждая капсула содержит 50 мг активного вещества - АГЭ. Дозировка в описании не указана.
Однако все исследователи использовали АГЭ из разрушенного природного комплекса, где они находились вместе с полиненасыщенными жирными кислотами, отбрасывая при этом важную биологическую составляющую. Тем самым снижался общий лечебный эффект, а в многостадийном процессе получения препарата использовалась жесткая химическая обработка и соответствующим образом поднималась стоимость конечного продукта. Полиненасыщенные жирные кислоты рассматривали как балласт, который нужно удалить, чтобы «сконцентрировать» препарат. И в дальнейшем такие исследователи для удобства использования препарата растворяли его в обычных растительных маслах (Bodman J., Maisin J.H. The α-glyceryl ethers/ Clinica Chimica Acta, 1958, v.3, p.253-274).
Наиболее близким техническим решением к заявляемому изобретению является способ производства полуфабриката из кальмара и его использование в лечебном, диетическом и детском питании (патент RU 20046580 C1 от 27.10.1995).
Недостатком данного изобретения является то, что средство, полученное данным способом, не обладает выраженными липидкорригирующими и иммуномодулирующими свойствами, так как в качестве сырья в данном случае используют не внутренности кальмара, в частности печень, а мантию - известный полезный белковый продукт, содержащий крайне незначительное количество полиненасыщенных жирных кислот омега-3 серии.
Задача, решаемая изобретением - расширение арсенала средств природного происхождения с выраженными липидкорригирующими и иммуномодулирующими свойствами на основе применения природного комплекса липидов, выделенных из печени кальмара, сочетающего в себе АГЭ и полиненасыщенные жирные кислоты.
Сущность изобретения заключается в том, что найден биологически активный комплекс липидов, являющийся фракцией липидов из печени командорского кальмара Berryteuthis magister, который содержит 10% полиненасыщенных жирных кислот и 50% алкил-диацилглицеридов и обладает липидкорригирующими и иммуномодулирующими свойствами.
Средство, обладающее вышеуказанными биологическими свойствами, получают следующим образом: жир-сырец из печени командорского кальмара Berryteuthis magister выделяют путем тепловой обработки печени при t=90°C с последующей сепарацией смеси и отделением жира, далее проводят его рафинацию с получением фракции, содержащей 10% полиненасыщенных жирных кислот и 50% алкил-диацилглицеридов.
Применение нами предложенного средства, полученного из печени командорского кальмара Berryteuthis magister, при модельной сердечной патологии дало неожиданный по эффективности результат, превосходящий ожидаемые от его назначения прогнозы и заключающийся в направленном профилактическом действии на больной организм как липидкорригирующего и иммуномодулирующего средства за счет присутствия алкил-диацилглицеридов (АДГ) - комплекса полиненасыщенных жирных кислот и алкил-глицериловых эфиров (АГЭ).
ПРИМЕР 1. Применение средства, полученного из печени кальмара Berryteuthis magister, при экспериментальной кардиовазопатии с выраженными нарушениями параметров иммунитета
В эксперименте на крысах изучено средство, выделенная из печени командорского кальмара Berryteuthis magister, содержащая в своем составе 10 % полиненасыщенных жирных кислот и 50 % алкил-диацилглицеридов (АДГ) (от общей массы липидов).
В таблице 1 представлен состав суммарной липидной фракции печени командорского кальмара после рафинации, используемой в качестве средства.
Объектом исследования являлись белые крысы-самцы линии Вистар весом от 235 до 350 грамм, выведенные в питомнике лабораторных животных РАМН «Столбовая» (г. Чехов, Московская обл.), ветеринарное свидетельство № 32-361061, 2002 г. Животные содержались в виварии в соответствии с санитарными правилами по устройству, оборудованию и содержанию экспериментально-биологических клиник, в пластмассовых клетках по 4-5 голов в каждой, на подстилке из лиственных пород дерева при естественном освещении и температуре 19±2°С. Карантирование крыс осуществлялось 14 дней и более. Исследования проводились в соответствии с «Правилами проведения работ с использованием экспериментальных животных» (1977). Использованы половозрелые особи в возрасте 6 месяцев.
В качестве экспериментальной модели, сопровождающейся дислипидемией с выраженными нарушениями параметров иммунитета, в исследовании воспроизводилась кардиовазопатия по разработанной ранее методике (патент РФ №2192048 Ru, МПК 7 G 09 В 23/28. Способ моделирования инфарктоидной кардиовазопатии у крыс/Т.П.Новгородцева, О.Г.Вострикова, И.В.Добрынченко. - Опубл. 27.10.2002, Бюл. №30). Для исследования выделено 3 группы крыс:
1-я группа - интактные животные;
2-я группа - крысы с моделированной кардиовазопатией;
3-я группа - крысы с кардиовазопатией, получавшие БАД с пищей в расчете 1 г/кг массы животного.
Моделирование кардиовазопатии у крыс осуществлялось 15 суток, после чего крысы переводились на стандартный рацион вивария и в течение 30 дней опытные животные ежедневно per os получали изучаемое средство. Эвтаназию животных осуществляли путем декапитации под эфирным наркозом. Оценивались интегральные показатели состояния животных, липидный спектр сыворотки крови, гематологические и иммунологические показатели в крови. Липидный спектр сыворотки крови исследовали на автоанализаторе, определяли уровень общего холестерина (ХС), триглицеридов (ТГ), ХС липопротеидов высокой плотности (ХС ЛПВП), результаты выражали в ммоль/л. Холестерин липопротеидов низкой (ЛПНП) и очень низкой плотности (ЛПОНП) определяли расчетным методом по формулам Фридвальда. Индекс атерогенности (ИА) рассчитывали по формуле ОХС-ХС ЛПВП/ХС ЛПВП.Подсчет количества эритроцитов, тромбоцитов, лейкоцитов, лимфоцитов производили в камере Горяева; рассчитывали цветной показатель; определение гемоглобина проводилось гемоглобинцианидным методом (набор реактивов ООО «Агат-Мед») с использованием спектрофотометра СФ-56 («ЛОМО», Россия), определяли время свертывания крови. Для оценки функционирования системы иммунологической резистентности использовали тесты 3 уровня: определение фагоцитарной активности нейтрофилов (ФАН) по оценке поглощения частиц латекса (диаметр частиц 1,3 мкм, Москва) нейтрофильными гранулоцитами периферической крови; фагоцитарного резерва (ФР) по отношению числа фагоцитов, стимулированных продигиозаном к нестимулированным; поглотительной активности (ФЧ) и ее резерва (ФЧР), динамики фагоцитарного процесса (суммарный процент завершающих стадий), его завершенности после инкубации клеток в термостате при 37°С в течение 2 часов (Моделирование и клиническая характеристика фагоцитарных реакций/Под ред. Маянского А.Н. - Горький: Изд-во Горьк. Мед. институт, 1989. - 242 с.). Количественные и качественные параметры окислительного метаболизма (НСТ, НСТР, ИАН, ИАНР) определялись по методу Шмелева Е.В. (Шмелев Е.В., Бумагина Т.К., Митеров Г.Г. Модификация метода Park//Лаб. дело. - 1979. - № 9. - С.13-15). Подсчет клеток производили визуальным способом на микроскопе МБИ-15 фирмы «ЛОМО» (Россия). Содержание циркулирующих иммунных комплексов малых (С3) и больших (С4) размеров, их соотношение (К) определяли по методу Стручкова П.В. (Стручков П.В. Скрининг-тест для оценки патогенных свойств иммунных комплексов//Лаб. дело. - 1985. - №7. - С.410-413). Измерения проводили на спектрофотометре СФ-56 фирмы «ЛОМО» (Россия).
Результаты исследования представлены в таблицах 2-4.
Как следует из представленных данных, развитие модели кардиовазопатии сопровождалось изменениями в показателях липидного обмена (табл. 2). У крыс с кардиовазопатией наблюдалось увеличение уровня общего холестерина на 28,5%, ХС ЛПНП на 60,7%, ХС ЛПОНП на 37,4%. Показатель ХС ЛПВП снижался, уровень ТГ увеличивался. Индекс атерогенности у крыс с кардиовазопатией был выше чем в контрольной группе животных в 2,5 раза.
Развитие модели сопровождалось и значительными нарушениями параметров периферической крови: наблюдалось увеличение скорости ее свертывания (на 82%), связанное с высоким уровнем тромбоцитов (в 2 раза выше, чем у интактных животных); повышение количества эритроцитов (на 58%) сопровождалось снижением среднего содержания в них гемоглобина и цветного показателя (на 76%), что может быть обусловлено уменьшением синтеза гемоглобина; общее количество лейкоцитарных клеток увеличивалось (на 32%); процентное содержания лимфоцитов было пониженным (на 45%). Нарушения иммунологической резистентности характеризовались снижением фагоцитарной активности нейтрофилов на 53%, фагоцитарного числа - на 32%, суммарного процента завершающих стадий - на 54%. Резко возрастало количество клеток, восстанавливающих диформазан (НСТ) на 121%, интенсивность окислительного метаболизма (ИАН) увеличивалась на 65%, наблюдалось уменьшение показателей функционального резерва фагоцитов - ФР на 10%, ФЧР на 27%, НСТР на 29%, ИАНР на 55% по сравнению с интактными животными. Более чем в 2 раза замедлялся процесс киллинга, определяющий завершенность фагоцитоза.
Курсовое введение заявляемого средства, представляющего собой фракцию липидов из печени командорского кальмара Berryteuthis magister, содержащего 10% полиненасыщенных жирных кислот и 50% алкил-диацилглицеридов, помимо ожидаемого липидкорригирующего действия (достоверного снижения уровня общего ХС и ХС атерогенных классов липопротеидов практически до уровня интактных животных, снижения ТГ) оказывало иммуномодулирующий и гомеостатический эффекты. Наибольшее влияние средство оказывало на эритро- и лимфопоэз. Возрастало содержание эритроцитов (в 3 раза), повышался уровень гемоглобина в периферической крови (на 79%). За счет уменьшения количества тромбоцитов (на 87%) в 2 раза увеличивалось время свертываемости крови. Уменьшались воспалительные реакции: СОЭ снижалась на 23%, уровень лейкоцитов - на 31%. Практически до нормы восстанавливался уровень лимфоцитов (табл.4).
Иммуномодулирующая активность средства проявлялась в нормализации функционального резерва нейтрофилов, поглотительной способности фагоцитов, окислительного метаболизма. Наблюдалось увеличение скорости и эффективности процесса переработки антигенов (табл.3). Средство из липидов печени командорского кальмара повышало уровень основных параметров фагоцитоза: на 30% увеличивался фагоцитарный резерв нейтрофильных гранулоцитов, на 22% фагоцитарное число, на 14% резерв фагоцитарного числа. На треть изменялся индекс завершенности процесса и количество клеток, выходящих на завершающие стадии процесса.
Таким образом, предлагаемое средство, полученное из печени командорского кальмара Berryteuthis magister, содержащее в своем составе 10% полиненасыщенных жирных кислот и 50% алкил-диацилглицеридов, обладает выраженными липидкорригирующими и иммуномодулирующими свойствами, проявляющимися в активации фагоцитарной активности нейтрофилов посредством воздействия на процесс поглощения и элиминации чужеродного агента, стимуляции развития адекватного ответа на дополнительную нагрузку. Средство, полученное из печени командорского кальмара, нормализует окислительный метаболизм фагоцитов при экспериментальной кардиопатии, вероятно, за счет снижения уровня респираторного взрыва в клетках, увеличения их функционального резерва. Впервые выявленные иммуномодулирующие свойства липидкорригирующего средства природного происхождения позволяют использовать средство, полученное из печени кальмара в качестве эффективного инструмента профилактики заболеваний, сопровождающихся нарушениями, как липидного обмена, так и системы иммунитета.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ЛИПИДКОРРИГИРУЮЩИМИ, ГИПОКОАГУЛЯЦИОННЫМИ И АНТИОКСИДАНТНЫМИ СВОЙСТВАМИ | 2005 |
|
RU2302248C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛ-ГЛИЦЕРИНОВЫХ ЭФИРОВ ИЗ МОРСКИХ ЖИРОВ | 2009 |
|
RU2415125C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ЛИПИДКОРРИГИРУЮЩИМ ДЕЙСТВИЕМ | 2015 |
|
RU2589285C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛ-ГЛИЦЕРИНОВЫХ ЭФИРОВ ИЗ МОРСКИХ ЖИРОВ | 2011 |
|
RU2476211C1 |
| Способ получения концентрата ненасыщенных алкил-глицериновых эфиров из морских липидов | 2017 |
|
RU2649014C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ЛИПИДКОРРИГИРУЩИМИ И АНТИОКСИДАНТНЫМИ СВОЙСТВАМИ | 2005 |
|
RU2309763C2 |
| Способ получения ненасыщенных алкил-глицериновых эфиров из морских жиров | 2019 |
|
RU2698715C1 |
| Способ получения концентрата ненасыщенных алкил-глицериновых эфиров из морских гидробионтов | 2017 |
|
RU2642294C1 |
| Липидкоррегирующее средство из морских водорослей | 2021 |
|
RU2767908C1 |
| Средство для стимулирования адаптации организма к экстремальным и стрессовым факторам и способ стимулирования адаптации организма к экстремальным и стрессовым факторам | 2018 |
|
RU2683311C1 |
Изобретение относится к медицине, в частности к клинической фармакологии и восстановительной терапии. Средство, представляющее собой липидную фракцию, выделенную из печени командорского кальмара Berryteuthis magister, содержащую 10% полиненасыщенных жирных кислот и 50% алкил-диацилглицеридов, обладающее выраженными липидкорригирующими и иммуномодулирующими свойствами. Изобретение позволяет расширить арсенал липидкорригирующих средств природного происхождения с выраженным иммуномодулирующим эффектом. Может быть использовано в качестве эффективного средства профилактики и лечения заболеваний, сопровождающихся нарушениями как липидного обмена, так и системы иммунитета. 4 табл.
Средство, обладающее липидкорригирующими и иммуномодулирующими свойствами, представляющее собой фракцию липидов из печени командорского кальмара Berryteuthis magister, содержащую 10% полиненасыщенных жирных кислот и 50% алкил-диацилглицеридов.
| СПОСОБ ДУБЛЕНИЕ КОЖИ | 1992 |
|
RU2045580C1 |
| Способ получения комплекса фосфолипидов | 1983 |
|
SU1175486A1 |
| Способ нагрева воздуха и вращающийся регенеративный воздухоподогреватель | 1982 |
|
SU1076707A1 |
| US 4701339 А, 20.10.1987 | |||
| ТЕРМОЭЛЕКТРОННЫЙ ПРЕОБРАЗОВАТЕЛЬ ТЕПЛОВОЙ ЭНЕРГИИ В ЭЛЕКТРИЧЕСКУЮ | 1996 |
|
RU2124782C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ИЗДЕЛИЙ НЕКРУГЛОЙ ФОРМЫ | 1995 |
|
RU2088366C1 |
| JP 7147940 А, 13.06.1995 | |||
| МНОГООТВОДНАЯ ЛИНИЯ ЗАДЕРЖКИ | 0 |
|
SU333678A1 |
Авторы
Даты
2005-09-10—Публикация
2003-11-06—Подача