Изобретение относится к области органической химии, а именно к способу получения миртеновой кислоты, а также сложных эфиров, применяемых в качестве душистых веществ и синтонов для получения биологически активных соединений.
Общеизвестно, что для получения карбоновых кислот используют соответствующие первичные спирты или альдегиды, применяя в качестве окислителей соединения хрома (VI), перманганат калия, оксид серебра, диоксид марганца, соединения рутения, меди, платины, ванадия.
Известен способ получения миртеновой кислоты (Кучин А.В. и др. Диоксид хлора - новый мягкий окислитель аллильных спиртов. Известия Академии Наук, серия химическая, 1996, №7, стр.1871-1872), включающий окисление миртенола диоксидом хлора в среде органического растворителя, такого как CCl4, при температуре 50°С с последующим выделением сырой кислоты и миртеналя. Выход миртеновой кислоты составляет 4%, а выход миртеналя - 41%, при степени конверсии миртенола - 61%.
Недостатками данного способа являются очень низкий выход целевого продукта и неполная конверсия миртенола.
Задача состоит в разработке нового более эффективного способа получения миртеновой кислоты.
Предлагаемое изобретение позволяет повысить выход сырого целевого продукта до 66% в расчете на исходный субстрат, удешевить технологию получения миртеновой кислоты, сократить время реакции.
Технический результат достигается тем, что способ получения миртеновой кислоты или миртеновой кислоты и ее сложного эфира, включающий окисление субстрата диоксидом хлора в среде органического растворителя, согласно изобретению субстрат выбирают из миртеналя или миртенола и окисление проводят при температуре 40-50°С, в среде органического растворителя, выбранного из группы: ацетон, бензол, спирт, при мольном соотношении миртенола или миртеналя к диоксиду хлора, составляющем 1:(0,5÷3,5) с последующим переводом в водорастворимую соль и выделением миртеновой кислоты, а также, с случае использования в качестве растворителя спирта, - сложного эфира миртеновой кислоты. Кроме того, при окислении осуществляют контроль за ходом реакции по ТСХ до исчезновения пятна исходного субстрата; сырую миртеновую кислоту дополнительно очищают хроматографией или кристаллизацией из легких углеводородов, типа гексан, пентан.
Одновременно с получением миртеновой кислоты дополнительно получают соответствующий сложный эфир при условии окисления субстрата в среде спирта.
Способ осуществляется следующим образом.
В качестве субстрата берут миртеналь или миртенол. Процесс ведут в среде органического растворителя при температуре 20-50°С. В качестве растворителя используют ацетон, или бензол, или спирт.
Через субстрат пропускают газообразный диоксид хлора, при мольном соотношении субстрат: диоксид хлора 1:0,5÷3,5. Контроль за ходом реакции осуществляют по ТСХ до исчезновения пятна исходного субстрата. По окончании реакции смесь промывают водой, сушат и удаляют растворитель. Затем из реакционной массы выделяют кислоту известным способом, путем перевода в водорастворимую соль [Петрова Л.Н., Зеленецкая А.А., Скворцова А.Б. Анализ синтетических душистых веществ и эфирных масел. - М.: Пищевая промышленность. - 1972, - стр.213]. Полученную массу встряхивают в делительной воронке или интенсивно перемешивают на магнитной мешалке с 5%-ным водным раствором NaHCO3 или 3%-ным водным раствором NaOH при мольном соотношении кислота: NaHCO3(NaOH), равном 1:1,5÷5,0. Затем водный слой отделяют от масляного, промывают диэтиловым эфиром, подкисляют разбавленной (5-10%) H2SO4 и экстрагируют эфиром. Эфирные экстракты промывают водой до нейтральной реакции, высушивают и отгоняют эктрагент. Сырая миртеновая кислота выделяется в виде густого вязкого масла темного цвета.
Дальнейшая очистка кислоты осуществляется хроматографией или кристаллизацией из легких углеводородов (гексан, пентан).
Ниже приведены варианты схем, поясняющие способ.
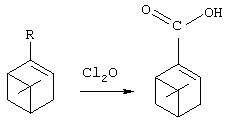
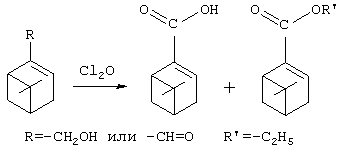
Схема 2 приведена для процесса получения миртеновой кислоты с использованием в качестве растворителя спирта, в частности этанола. При ведении этого процесса одновременно образуется 20-40% сложного эфира, в частности этилмиртеноат. При использовании других спиртов получают соответствующие эфиры.
Образующийся сложный эфир выделяют хроматографией на SiO2 масляного слоя после выделения миртеновой кислоты.
Время, затрачиваемое для получения миртеновой кислоты, составляет 5-11 часов.
Пример 1
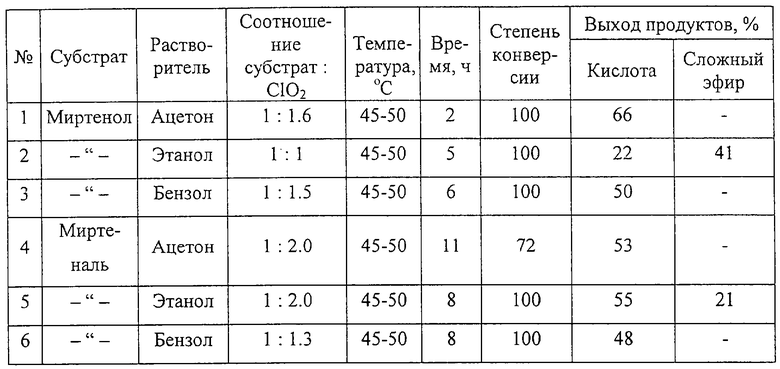
0,47 г (0,0038 моль) миртенола растворяют в 10 мл ацетона, нагревают до 50°С и при перемешивании пропускают ток ClO2 в течение двух часов. Мольное соотношение миртенол: ClO2 1:1,6. После удаления ацетона реакционную массу встряхивают в делительной воронке с 10 мл 3% раствора NaOH, экстрагируют диэтиловым эфиром и отделяют водный слой. После подкисления водного слоя 10% раствором H2S04, экстракции эфиром, промывки водой, сушки и удаления растворителя получают 0,31 г сырой кислоты (выход - 66% на исходный миртенол или 61% от теоретически возможного).
Пример 2
4,93 г (0,032 моль) миртенола растворяют в 50 мл EtOH, пропускают ток ClO2 в течение 5 часов при перемешивании и нагревании до 50°С. Соотношение спирт: ClO2 1:1. По окончании реакции большую часть растворителя упаривают, реакционную массу переносят в делительную воронку, разбавляют водой и экстрагируют диэтиловым эфиром (3×50). После сушки и удаления растворителя массу обрабатывают 50 мл 5% водного раствора NaHCO3 при мольном соотношении кислота: NaHCO3 1:4. Получают 1,11 г миртеновой кислоты (22,5% от исходного спирта). Масляная фракция (3,35 г), оставшаяся после выделения кислоты, имеет приятный запах и содержит по ГЖХ 61,0% (41,1% на миртенол) сложного эфира, который является этилмиртеноатом.
После хроматографической очистки структура эфира была установлена с использованием ИК, ЯМР 1Н и 13С спектроскопии.
Физико-химические характеристики.
Миртеновая кислота:
С10Н14О2, Т.пл. 53-54.5°С, [α]D 20+18.6° (с 1.0, EtOH).
ИК-спектр: 2500-3100 (ОН), 1690 (С=O), 1630 (С=С), 1430, 1280 (С-O), 1080, 960 (O-Н), 790, 760, 720.
Спектр ЯМР 13С: 171.8 (С10), 139.8 (C2), 139.3 (С3), 40.8 (C1), 40.2 (C5), 37.6 (С6), 32.3 (С4), 31.2 (С7), 25.8 (С8), 20.9 (С9).
Спектр ЯМР 1Н: 0.8, 1.12, 1.34, 2.13, 2.46, 2.79, 6.99, 12.1.
Этилмиртеноат:
C12H18O2
ИК-спектр: 2988, 1718,1632, 1376, 1256, 1076, 756.
Спектр ЯМР 13С: 166.2, 140.3, 135.3, 60.1, 41.1, 40.3, 37.6, 32.1, 31.2, 26.3, 20.8, 14.3.
Спектр ЯМР 1Н: 1.25, 1.75, 1.79, 2.58, 2.82, 2.88, 2.95, 3.25, 4.62, 7.27.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения цис-миртановой кислоты | 2021 |
|
RU2756658C1 |
| СПОСОБ ПОЛУЧЕНИЯ МИРТЕНОЛА | 2000 |
|
RU2176994C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВЕРБЕНОНА | 2003 |
|
RU2250208C2 |
| Способ получения (1S,5R)-6,6-диметилбицикло[3.1.1]гептанона-2 ((-)-нопинона) | 2023 |
|
RU2809009C1 |
| Способ получения монотерпеновых сульфокислот | 2016 |
|
RU2651791C2 |
| Способ получения транс-миртановой кислоты | 2022 |
|
RU2794756C1 |
| Сульфопроизводные на основе бета-пинена и способ их получения | 2019 |
|
RU2708617C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,6-ДИИЗОБОРНИЛБЕНЗОХИНОНА | 2011 |
|
RU2457196C1 |
| Хиральные 18-сульфопроизводные дегидроабиетана и способ их получения | 2020 |
|
RU2726793C1 |
| СПОСОБ ПОЛУЧЕНИЯ СУЛЬФОКСИДОВ | 1997 |
|
RU2127258C1 |
Настоящее изобретение относится к способу получения миртеновой кислоты или миртеновой кислоты и ее сложного эфира, включающему окисление субстрата диоксидом хлора в среде органического растворителя. При этом субстрат выбирают из миртеналя или миртенола и окисление проводят при температуре 40-50°С, в среде органического растворителя, выбранного из группы: ацетон, бензол, спирт, при мольном соотношении миртенола или миртеналя к диоксиду хлора, составляющем 1:(0,5÷3,5) с последующим переводом в водорастворимую соль и выделением миртеновой кислоты, а также, в случае использования в качестве растворителя спирта, - сложного эфира миртеновой кислоты. Предлагаемое изобретение позволяет повысить выход сырого целевого продукта до 66% в расчете на исходный субстрат, удешевить технологию получения миртеновой кислоты, сократить время реакции. 2 з.п. ф-лы, 1 табл.
| КУЧИН А.В | |||
| и др | |||
| Диоксид хлора - новый мягкий окислитель аллильных спиртов | |||
| Известия Академии наук | |||
| Серия химическая | |||
| Предохранительное устройство для паровых котлов, работающих на нефти | 1922 |
|
SU1996A1 |
| Syntheses dans la seria du myrtenol | |||
| Приспособление для забивки костылей | 1925 |
|
SU1935A1 |
Авторы
Даты
2005-09-20—Публикация
2004-04-06—Подача