Изобретение относится к медицине и может быть использовано для оценки защитных свойств иммуномодулирующих препаратов, отбираемых для экстренной защиты при бактериальной или вирусной инфекции, при биотеррористических актах или возникновении чрезвычайных ситуаций.
Известен способ первичного скрининга химических соединений на иммуномодулирующую активность, предусматривающий предварительное определение нетоксичных препаратов и оценку их эффекта (RU, №1704084, G 01 N 33/53, 1992).
Однако описанный способ предназначен только для оценки новых препаратов, обладающих иммуномодулирующей активностью. Указанный способ не дает представления о влиянии этих препаратов на резистентность к инфекциям бактериальной или вирусной этиологии.
Технический результат заявленного способа заключается в оценке защитного эффекта иммуномодулирующих препаратов при испытании на иммунокомпетентных мышах, зараженных бактериями, или при вирусной инфекции у мышей с индуцированной иммуносупрессией, формирующейся под влиянием гетерологичного патогена - вируса Тахиня.
Для достижения указанного технического результата способ оценки защитных свойств иммуномодулирующих препаратов, согласно изобретению, характеризуется тем, что при бактериальной инфекции используют иммунокомпетентных (здоровых) мышей, а при вирусной инфекции - животных с иммуносупрессией, индуцированной вирусом Тахиня. В организм указанных животных инокулируют исследуемый иммуномодулирующий препарат в человеко-дозе, рассчитанной на 1 г веса животного, в объеме 0,2-0,5 мл, и тест-штаммы в летальной дозе. Наблюдают животных 21 день, ежедневно регистрируя количество выживших и погибших животных, расчитывают среднюю продолжительность жизни или % выживаемости в опытных и контрольных группах, оценивают эффективность исследуемого препарата и признают его эффективным при бактериальной инфекции - если Т2>Т0 при р<0,05, а при вирусной инфекции - если T2≥T0>T1 при р<0,05, где
Т0 - средняя продолжительность жизни или % выживаемости мышей после заражения тест-штаммом;
T1 - средняя продолжительность жизни или % выживаемости мышей с индуцированной иммуносупрессией, которым ввели тест-штамм;
Т2 - средняя продолжительность жизни или % выживаемости мышей иммунокомпетентных или иммуносупрессированных, получивших тест-штамм и исследуемый иммуномодулирующий препарат.
В качестве тест-штаммов используют вирулентные для мышей штаммы Salmonella typhimurium или вирус Лангат.
Сущность изобретения поясняется на конкретных примерах выполнения способа.
Пример 1. Исследование защитного действия иммуномодулирующего препарата (ликопида) при вирусной инфекции у мышей со вторичным иммунодефицитом, сформировавшимся под влиянием гетерологичного патогена.
В опытах формировали три группы животных численностью по 20 особей каждая. Мышам линии СВА массой 19±1 г вирус Тахиня вводили внутрибрюшинно (в дозе 104 ЛД50 в 0,3 мл). Через 4 дня, когда индуцированная иммуносупрессия достигала максимума, инокулировали внутривенно летальную дозу тест-штамма вируса Лангат (104 ЛД50 в 0,3 мл). Одновременно животные получали через рот 10 мкг/мышь ликопида. Зараженных животных наблюдали 21 день. Средняя продолжительность жизни (СПЖ) иммунокомпетентных мышей после заражения вирусом Лангат равнялась 29,4±1,2 дня (Т0 - контроль), при введении тест-штамма (вирус Лангат) на пике индуцированной иммуносупрессии (T1 - опыт 1) СПЖ уменьшалась до 14,3±2,1 дня. При одновременной инокуляции теста-штамма и ликопида в дозе 10 мкг/мышь (Т2 - опыт 2) СПЖ восстанавливалась до показаний контроля и равнялась 30,2±1,8 дня. Сравнение Т0 и T1 говорит о развитии супрессии резистентности после введения вируса Тахиня (T0>T1 при р<0,05). Сравнение Т0 и Т2 свидетельствует о том, что под влиянием ликопида подавленная резистентность к вирусу восстанавливалась до показателей иммнокомпетентных животных (Т2=Т0 при р<0,05).
Средняя продолжительность жизни рассчитывалась по формуле:
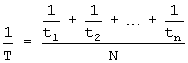
Т, t1, t2...tn - продолжительность жизни (в днях) каждого животного в группе из N животных, зараженных данной дозой.
Пример 2. Отсутствие защитного действия препарата (ликопида) при вирусной инфекции у иммунокомпетентных мышей.
Опыты проводили на двух группах мышей линии СВА массой (19±1) г по 20 особей каждая. Летальную дозу вируса Лангат вводили внутривенно. Одновременно животные получали через рот 10 мкг/мышь ликопида. Зараженных животных наблюдали 21 день. СПЖ иммунокомпетентных мышей равнялась 31,2±1,3 дня (Т0 - контроль). При одновременном введении вируса Лангат и ликопида в дозе 10 мкг/мышь (T1 - опыт) СПЖ равнялась 30,1±1,9 дня. Сравнение Т0 и T1 свидетельствует о том, что применение ликопида не повлияло на чувствительность иммунокомпетентных мышей к вирусу Лангат (T0=T1).
Пример 3. Исследование защитного действия иммуномодулирующего препарата анатоксина стафилококкового очищенного (АСО) при вирусной инфекции (вирус Лангат) у иммунокомпетентных мышей и у мышей со вторичным иммунодефицитом, сформировавшимся под влиянием гетероличного патогена (вирус Тахиня).
Опыты проводили на четырех группах мышей линии СВА массой 19±1 г по 20 особей каждая. Вирус Тахиня вводили внутрибрюшинно. При этих условиях индуцированная иммуносупрессия достигала масимума на 4 день. На пике иммуносупрессии внутривенно инокулировали летальную дозу тест-штамма вируса Лангат. Две группы иммунокомпетентных животных получали вирус Лангат или вирус Лангат совместно с АСО. Выживаемость иммунокомпетентных мышей после заражения вирусом Лангат равнялась 88,7±1,5% (Т0 - контроль). При инокуляции иммунокомпетентным мышам вируса Лангат и АСО выживаемость достигала 86,7±1,9% (T1 - опыт 1). После введения вируса Лангат в дозе 104 ЛД50 в 0,3 мл иммуносупрессированным мышам выживаемость соответствовала 52,5±3,0% (T2 - опыт 2). При одновременной инокуляции тест-штамма и АСО показатели выживаемости иммуносупрессированных мышей соответствовали показателям контроля (Т3 опыт 3). Сравнение Т3 и Т0 с парой Т2 и Т0 свидетельствует о том, что под влиянием АСО подавленная резистентность к вирусу Лангат (Т2) восстанавливалась до показателей у иммунокомпетентных животных (Т3=Т0). В то же время не выявлено защитного действия АСО при вирусной инфекции у иммунокомпетентных мышей (T1=T0).
Пример 4. Оценка защитного эффекта иммуномодулирующих препаратов на модели заражения иммунокомпетентных мышей S. typhimurium (штамм №415).
Опыт проводили на двух группах мышей линии С57BL /6 массой 15±1 г по 20 особей каждая. Сначала вводили исследуемый препарат парентерально в объеме 0,5 мл. Через сутки мышей заражали штаммом № 415 внутрибрюшинно в дозе 106 микробных клеток/мышь (100% летальная доза). Животных наблюдали 21 день и ежедневно регистрировали количество погибших мышей. По формуле (см. пример 1) рассчитывалась СПЖ животных.
Опыт 1. Оценка защитного свойства иммуномодулирующего препарата (ликопида) у иммунокомпетентных мышей, зараженных Salmonella typhimurium (штамм №415).
Опыты проводили на трех группах мышей линии C57BL/6 массой (15±1) г по 20 животных каждая. Сначала вводили исследуемый препарат ликопид в дозе 0,5 мг на 1 кг массы тела животного (из расчета 35 мг на взрослого человека массой 70 кг). Через сутки мышей заражали через рот штаммом №415 в дозе 106 микробных клеток/мышь (абсолютно смертельная доза). Животных наблюдали 21 день и ежедневно регистрировали количество выживших и погибших особей.
Результаты опытов учитывали только в тех случаях, когда в контроле имела место 100% гибель животных. Средняя продолжительность жизни иммунокомпетентных мышей после заражения Salmonella typhimurium (T0) равнялась 4,7±0,6 дней. Средняя продолжительность жизни животных, получивших тест-штамм и ликопид (Т2), составила 7,6±1,4 дней. Исследуемый иммуномодулирующий препарат ликопид оценивается как эффективное средство для защиты от бактериальной инфекции, поскольку Т2>Т0 при р<0,05.
Опыт 2. Иммуномодулятор полиоксидоний вводили в дозе 17 мкг/мышь (эквивалентная человеко-доза). Результат: СПЖ иммунокомпетентных мышей после заражения S. typhimurium (T0) равнялась 3,9±1,7 дней. СПЖ животных, получивших тест-штамм и полиоксидоний (T2) составила 12,8±1,9 дней. Исследуемый препарат полиоксидоний оценивался как эффективное средство для защиты от бактериальной инфекции, поскольку Т2>Т0 при р<0,05.
Опыт 3. Иммуномодулятор миелопид вводили в дозе 1,4 мкг/мышь (эквивалентная человеко-дозе). Результат: СПЖ иммунокомпетентных мышей после заражения S. typhimurium (T0) равнялась 3,9±1,7 дней. СПЖ животных, получивших тест-штамм и миелопид (Т2), составила 3,7±1,8 дней. Исследуемый препарат миелопид оценивался как средство, не повышающее неспецифическую резистентность организма к данной инфекции.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОВЫШЕНИЯ ЭФФЕКТИВНОСТИ ЭКСТРЕННОЙ ПРОФИЛАКТИКИ ЭКСПЕРИМЕНТАЛЬНОГО МЕЛИОИДОЗА | 2016 |
|
RU2618425C1 |
| СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ОПАСНЫХ НЕЙРОВИРУСНЫХ ИНФЕКЦИЙ | 2016 |
|
RU2642312C1 |
| КОМПОЗИЦИЯ С ПРОТИВОИНФЕКЦИОННОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2476205C1 |
| АЗОЛОАЗИНИЕВЫЕ СОЛИ ФТОРХИНОЛОНОВ, ОБЛАДАЮЩИЕ АНТИБАКТЕРИАЛЬНЫМ И ПРОТИВОВИРУСНЫМ ДЕЙСТВИЕМ | 2014 |
|
RU2547835C1 |
| СПОСОБЫ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, ВЫЗВАННЫХ ВИРУСОМ ГРИППА ПТИЦ A/H5N1, С ИСПОЛЬЗОВАНИЕМ ИНДУКТОРА ИНТЕРФЕРОНА И ИНГИБИТОРА НЕЙРАМИНИДАЗЫ | 2008 |
|
RU2398596C2 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ВИРУСНОГО КЛЕЩЕВОГО ЭНЦЕФАЛИТА, ИНДУЦИРОВАННОГО В ЭКСПЕРИМЕНТЕ | 1986 |
|
RU2025126C1 |
| СПОСОБ ИММУНОПРОФИЛАКТИКИ ЭКСПЕРИМЕНТАЛЬНОГО МЕЛИОИДОЗА ИНКАПСУЛИРОВАННЫМИ АНТИГЕНАМИ Burkholderia pseudomallei | 2008 |
|
RU2373955C1 |
| СПОСОБ ПРОФИЛАКТИКИ ПОСТНАТАЛЬНОГО ЗАРАЖЕНИЯ ВИРУСОМ ЛЕЙКОЗА КРУПНОГО РОГАТОГО СКОТА МОЛОДНЯКА КРУПНОГО РОГАТОГО СКОТА | 2016 |
|
RU2621146C1 |
| Интраназальное противовирусное средство | 2023 |
|
RU2833350C1 |
| СПОСОБ ПРОФИЛАКТИКИ ЗАБОЛЕВАНИЯ, ВЫЗВАННОГО ВИРУСОМ ГРИППА ПТИЦ А/Н5N1 | 2008 |
|
RU2395295C2 |
Изобретение относится к области лекарственных средств и может быть использовано для оценки защитных свойств иммуномодулирующих препаратов. Сущность изобретения заключается в том, что иммунокомпетентным мышам инокулируют исследуемый иммуномодулирующий препарат в человеко-дозе, рассчитанной на 1 г веса животного в объеме 0,2-0,5 мл, затем вводят тест-штамм в летальной дозе, животных наблюдают 21 день, рассчитывают среднюю продолжительность жизни или выживаемость в опытной и контрольной группах и при увеличении продолжительности жизни или выживаемости в опытной группе по сравнению с контрольной иммуномодулирующий препарат обладает защитными свойствами, при вирусной инфекции в качестве опытной группы используют мышей с иммуносуппрессией, индуцированной вирусом Тахиня, и при увеличении или равных показателях средней продолжительности жизни животных или их выживаемости в опытной группе по сравнению с контрольной иммуномодулирующий препарат обладает защитными свойствами. Техническим результатом является создание модели для оценки защитного эффекта иммуномодулирующих препаратов. 3 з.п. ф-лы.
| Способ первичного скрининга химических соединений на иммуномодулирующую активность | 1989 |
|
SU1704084A1 |
| МЕЛЬНИКОВА Л.А | |||
| Оценка иммуномодулирующих свойств препаратов по изменению экспрессии рецепторов и антигенов лимфоцитов | |||
| Автореф | |||
| канд.дисс | |||
| - Минск, 1993. | |||
Авторы
Даты
2006-01-20—Публикация
2003-10-24—Подача