Изобретение относится к медицине и ветеринарии и может быть использовано для увеличения продолжительности жизни и замедления наступления болезненных состояний, связанных с увеличением возраста.
Известны различные способы замедления старения, основанные на применении антиоксидантов, иммуномодуляторов, гормонов, метаболических модуляторов (Ann. N.Y. Acad. Sci., 2002; vol.959), однако единственным способом коррекции (удлинения) продолжительности жизни с доказанной эффективностью является нелекарственный метод ограничения потребляемых с пищей калорий (CALORIE RESTRICTION, AGING, AND CANCER PREVENTION: Mechanisms of Action and Applicability to Humans; Stephen D. et al., Annual Review of Medicine, February, 2003, Vol. 54, pp. 131-152).
Согласно современным представлениям в основе старения лежит наступающая с возрастом потеря соматическими клетками организма способности к репликации (Hayflick and Moorhead, 1961, Exp. Cell Res. 25: 585-621; Hayflick, 1965, Exp. Cell Res. 37: 614-636; and Hayflick, 1970, Exp. Geront. 5: 291-303) и сопутствующее этому изменение профиля экспрессии генов в стареющих клетках (West, 1994, Arch. Derm. 130: 87-95), что ведет к нарушению их характерных функций. Наступающее с возрастом накопление подобных клеток в органах и тканях организма (причем в первую очередь это касается высокоспециализированных клеток) формирует основу проявления болезней и патологических состояний, характерных для стареющего организма.
Причины возрастной потери или извращения репликативной активности клеток до конца не раскрыты. В соответствии с современными представлениями в основе этого могут лежать либо механизмы, детерминирующие лимит репликативной активности клеток, например, истощение теломер (Harley, 1991, Telomere loss: Mitotic clock or genetic time bomb. Mut. Res. 256:271-282), либо вероятностные механизмы, например, связанное с возрастом накопление соматических мутаций в геноме соматических клеток (Woodruff R.C., et al., J Anti Aging Med, 2003 Spring 6: pp.29-39).
В соответствии с этими представлениями современные способы лекарственного увеличения продолжительности жизни воздействуют на внутриклеточный генетический аппарат клеток. Таковы, например, способы ингибиторования фермента поли (АДФ-рибоза)полимеразы (Патент US 5874444) или активация фермента теломеразы (Заявка: WO 0031238).
Общим недостатком способов активного лекарственного воздействия на генетический аппарат стареющей клетки является опасность непредсказуемых побочных эффектов (Cellular senescence, aging and cancer. Campisi J, Scientific World Joumal, 2001, Jan 11:1 Suppl 3 65).
В настоящее время отсутствуют какие-либо способы, которые позволяли бы эффективно замедлить наступление болезненных состояний, связанных с увеличением возраста человека. В связи с этим отсутствует возможность принять какое-либо известное техническое решение за прототип настоящего изобретения.
В основу настоящего изобретения положено решение задачи создания эффективного способа замедления наступления болезненных состояний, связанных с увеличением возраста человека, при отсутствии прямого воздействия на генетический аппарат стареющих клеток, в частности снижения половой активности и способности к воспроизводству, климакса, изменения глюкозотолерантности, снижения когнитивных и/или мнестических функций, снижения резистентности к стрессу, развития склероза органов и тканей.
Согласно изобретению эта задача решается за счет того, что в циркуляцию крови вводят агент, инактивирующий внеклеточную ДНК крови; в качестве агента, инактивирующего внеклеточную ДНК крови, могут использовать агент, разрушающий внеклеточную ДНК крови; в качестве агента, разрушающего внеклеточную ДНК крови, могут использовать фермент ДНКазу; в качестве агента, инактивирующего внеклеточную ДНК крови, могут использовать агент, связывающий внеклеточную ДНК крови; в качестве агента, связывающего внеклеточную ДНК крови, могут использовать анти-ДНК антитела; в качестве агента, инактивирующего внеклеточную ДНК крови, могут вводить фермент, изменяющий химическую структуру внеклеточной ДНК крови; в качестве агента, инактивирующего внеклеточную ДНК крови, могут использовать агент, стимулирующий синтез или активность эндогенной дезоксирибонуклеазы или агент, стимулирующий синтез антител, связывающих внеклеточную ДНК крови.
Возникновение и развитие болезненных состояний, связанных с процессом старения, сопровождается качественными и количественными изменениями внеклеточной ДНК крови, однако в известных заявителю источниках отсутствуют знания о генетическом репертуаре внеклеточной ДНК крови больных при старении, биологической роли внеклеточной ДНК крови при старении и возможном терапевтическом эффекте ее уничтожения для увеличения продолжительности жизни.
Как установили заявители, внеклеточная ДНК крови больных при старении содержит уникальный по своему качественному и количественному составу репертуар генов и регуляторных генетических элементов, резко отличающийся от репертуара ДНК, описанного в геноме человека. В отличие от внутриклеточной ДНК внеклеточная ДНК крови при старении содержит, в основном, уникальные гены человека.
Установлено, что внеклеточная ДНК крови при старении негативно влияет на жизнеспособность клеток организма.
Установлено, что инактивация внеклеточной ДНК крови при старении замедляет процесс старения.
Указанные выше новые свойства заявленного изобретения, базирующиеся на принципиально новых представлениях о роли внеклеточной ДНК плазмы крови при старении, позволяют сделать вывод о соответствии заявленного способа критерию «изобретательский уровень».
Заявленный способ реализуется следующим образом:
Материалы и методы:
Использовали следующие агенты, разрушающие внеклеточную ДНК крови: фермент бычью панкреатическую ДНКазу (производство Sigma), фермент рекомбинантную человеческую ДНКазу I (производство Genetech),
В качестве агента, связывающего ДНК, использовали антитела против ДНК, выделяемые из крови больных системной красной волчанкой по методике Shuster A.M. (Shuster A.M. et al., Science, v.256, 1992, pp.665-667). Подобные анти-ДНК антитела способны не только связывать, но и осуществлять гидролиз ДНК.
В качестве агента, стимулирующего синтез и/или активность эндогенных биополимеров, связывающих или разрушающих или модифицирующих химический состав и/или конформацию и/или полимерность внеклеточной ДНК крови без ее разрушения, использовали антиG-f актин антитела (Calbiochem). G-Актин является ингибитором активности эндогенной ДНКазы I. Связывание актина антителами увеличивает активность эндогенной ДНКазы I.
В качестве агента, модифицирующего ДНК, использовали бактериальную Sss I Метилазу (CpG Methylase), (NewEngland Biolabs). В экспериментах Sss I Метилазу включали в состав малых однослойных липосом (SUV) в соотношении 1u фермента на 1 мкг липидов (энзаймосомы).
ДНК плазмы крови выделяли следующим образом: свежую (не более 3-4 часов после забора) плазму крови с добавленным антикоагулянтом (цитрат натрия) откручивали на подушке из Ficoll-Plaque Plus (Amersham-Pharmacia) при 1500 g 20 минут при комнатной температуре. Плазму (1/2 от всего количества) аккуратно отбирали, не задевая остаток клеток, на подушке фиколла и откручивали при 10000 g 30 минут, чтобы избавиться от обломков клеток и дебриса. Супернатант отбирали, не затрагивая осадок, добавляли до 1% саркозила, до 50 мМ трис-HCl, рН 7,6, до 20 мМ ЭДТА, до 400 мМ NaCl и равный объем смеси фенол-хлороформ 1:1. Полученную эмульсию инкубировали при 65°С 2 часа, затем отделяли фенол-хлороформ центрифугированием при 5000 g в течение 20 минут при комнатной температуре. Процедуру депротеинизации фенол-хлороформом повторяли идентичным способом трижды, после чего водную фазу обрабатывали хлороформом, затем диэтиловым эфиром. Отделение от органических растворителей производили центрифугированием при 5000 g в течение 15 минут. К полученной водной фазе добавляли равный объем изопропанола и инкубировали в течение ночи при 0°С. После осаждения нуклеиновые кислоты отделяли центрифугированием при 0°С, 10000 g в течение 30 минут. Осадок нуклеиновых кислот растворяли в буфере, содержащем 10 мМ трис-HCl, рН 7,6, 5 мМ ЭДТА, и наносили на подушку из ступенчатого хлористого цезия (1 М, 2.5 М, 5.7 М) в центрифужной пробирке для ротора SW60Ti. Объем ДНК составлял 2 мл, объем каждой ступеньки CsCl - по 1 мл. Ультрацентрифугирование проводили в приборе L80-80 (Beckman) 3 часа при 250000 g. ДНК отбирали с поверхности ступеньки 5.7 М по фракциям. Фракции диализировали 12 часов при 4°С. Наличие ДНК во фракциях определяли агарозным электрофорезом, с визуализацией ДНК бромистым этидием. Количество ДНК определяли спектрофотометрически (Beckman DU70) в кювете объемом 100 мкл, снимая спектр от 220 до 320 нм.
Пример 1. Увеличение продолжительности жизни.
Использовали бычью панкреатическую ДНКазу (Sigma), коньюгированную с полимером сиаловой кислоты массой 36 kDA. В опыте использовали 24-месячных белых беспородных крыс. В опытной группе (15 животных) крысам, начиная с 24 месячного возраста, вводили препарат в количестве 500 мг/кг внутривенно два раза в неделю на протяжении 2 месяцев. Крысам контрольной группы (15 животных) вводили фосфатный буфер. Продолжительность жизни крыс в контрольной группе составила в среднем 27,8 месяца. Продолжительность жизни крыс в опытной группе составила в среднем 30,1 месяц.
Таким образом, разрушение внеклеточной ДНК крови ферментом ДНКазой замедляет процесс старения согласно заявляемому способу.
Пример 2. Использование ДНКазы для предотвращения негативного влияния внеклеточной ДНК крови пожилого донора на жизнеспособность клеток.
Использовали линию фибробластов, субкультивированную из биопсийного материала 73-летнего здорового мужчины. Клетки культивировали без добавления антибиотиков в минимальной необходимой среде (MEM) с добавлением 2 мМ глютамина и 10% эмбриональной телячьей сыворотки. Для эксперимента клетки высевали в объеме 10000 на см2 поверхности в чашки Петри и растили в атмосфере 5% CO2 при 37°С. Включение [3Н] тимидина использовали для определения интенсивности синтеза ДНК в начальном периоде роста. На второй день после высевания в культуры добавляли [3Н] тимидин до финальной концентрации 0,1 mCi/мл и инкубировали клетки еще 24 часа, после чего отмывали, растворяли в формамиде и измеряли радиоактивность.
В первой серии (6 чашек) клетки культивировали без добавления ДНК
Во второй серии (6 чашек) в инкубационную среду добавляли внеклеточную ДНК, выделенную из крови донора клеток в концентрации 0,005 мкг/мл.
В третьей серии (6 чашек) в инкубационную среду добавляли внеклеточную ДНК, выделенную из крови здорового молодого добровольца 24 лет в концентрации 0,005 мкг/мл.
В четвертой серии (6 чашек) в инкубационную среду добавляли внеклеточную ДНК, выделенную из крови донора клеток в концентрации 0,005 мкг/мл, и рекомбинантную дорназу - альфа (Genetech) в концентрации 0,5 мкг/мл.
В пятой серии (6 чашек) в инкубационную среду добавляли рекомбинантную дорназу - альфа (Genetech) в концентрации 0,5 мкг/мл.
Результаты эксперимента представлены на диаграмме 1 (фиг.1).
Включение клетками [3Н] тимидина через 48 часов после пассирования.
Таким образом, внеклеточная ДНК плазмы крови пожилого донора негативно влияет на синтез ДНК в клетках. Разрушение внеклеточной ДНК крови больного ферментом ДНКазой препятствует этому согласно заявляемому способу.
Пример 3. Использование связывания и модификации для предотвращения негативного влияния внеклеточной ДНК крови старого донора на жизнеспособность клеток.
Использовали линию фибробластов, субкультивированную из биопсийного материала 73-летнего здорового мужчины. Клетки культивировали без добавления антибиотиков в минимальной необходимой среде (MEM) с добавлением 2мМ глютамина и 10% эмбриональной телячьей сыворотки. Для эксперимента клетки высевали в объеме 10000 на см2 поверхности в чашки Петри и растили в атмосфере 5% CO2 при 37°С. Включение [3Н] тимидина использовали для определения интенсивности синтеза ДНК в начальном периоде роста. На второй день после высевания в культуры добавляли [3Н] тимидин до финальной концентрации 0,1 mCi/мл и инкубировали клетки еще 24 часа, после чего отмывали, растворяли в формамиде и измеряли радиоактивность.
В первой серии (6 чашек) клетки культивировали без добавления ДНК
Во второй серии (6 чашек) в инкубационную среду добавляли внеклеточную ДНК, выделенную из крови донора клеток в концентрации 0,005 мкг/мл.
В третьей серии (6 чашек) в инкубационную среду добавляли внеклеточную ДНК, выделенную из крови здорового молодого добровольца 24 лет, в концентрации 0,005 мкг/мл.
В четвертой серии (6 чашек) в инкубационную среду добавляли внеклеточную ДНК, выделенную из крови донора клеток в концентрации 0,005 мкг/мл и анти-ДНК антитела в концентрации 5 мкг/мл.
В пятой серии (6 чашек) в инкубационную среду добавляли среду добавляли внеклеточную ДНК, выделенную из крови донора клеток в концентрации 0,005 мкг/мл и энзаймосомы в концентрации 20 мкг/мл.
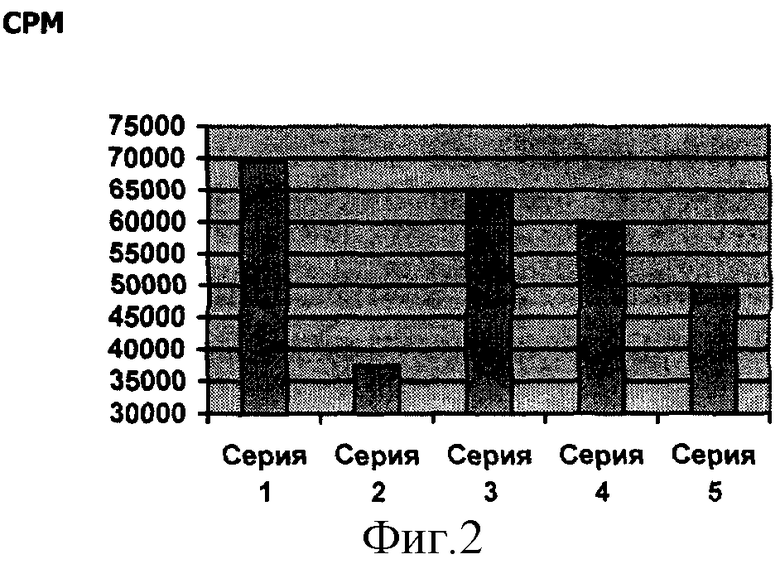
Результаты эксперимента представлены на диаграмме (фиг.2).
Включение клетками [3Н] тимидина через 48 часов после пассирования.
Таким образом, внеклеточная ДНК плазмы крови пожилого донора негативно влияет на синтез ДНК в клетках. Связывание и модификация внеклеточной ДНК крови больного препятствует этому согласно заявляемому способу.
Пример 4. Предотвращение связанного с возрастом снижения репродуктивной функции
В эксперименте использовали 20месячных самцов мышей линии С57В1. Самцы опытной группы (9 мышей), начиная с 18 месячного возраста, получали внутривенные инъекции фракции мышиных антиG-f актин антител (Calbiochem) по 200 мкг на мышь 1 раз в неделю еженедельно на протяжении 8 недель. 9 мышей контрольной группы получали внутривенные инъекции фосфатного буфера. В возрасте 20 месяцев самцы опытной и контрольной групп были рассажены в клетки по 3 самца в каждую, и к ним были подсажены 2месячные самки линии С57В1 (по 3 самки на клетку). Через неделю самок отсаживали в отдельные клетки и еще через 23 дня оценивали количество жизнеспособного потомства у мышей опытной и контрольной групп. В качестве дополнительного контроля использовали 10 самцов линии С57В1 пятимесячного возраста, спариваемых с двухмесячными самками той же линии.
Результаты приведены в таблице 1.
Таким образом, введение агента, подавляющего эндогенный ингибитор собственной ДНКазы 1, биополимера, разрушающего внеклеточную ДНК крови, замедляет связанное с возрастом снижение репродуктивной функции.
Пример 5. Предотвращение связанного с возрастом снижения иммунитета.
В эксперименте использовали 20месячных самцов мышей линии С57В1. Самцы опытной группы (10 мышей), начиная с 18 месячного возраста, получали внутривенные инъекцию фракции человеческих анти-ДНК антител (IgG) по 200 мкг на мышь раз в неделю еженедельно на протяжении 8 недель. Самцы контрольной группы (10 мышей) получали внутривенные инъекции фосфатного буфера. В возрасте 20 месяцев самцам опытной и контрольной групп вводили подкожно по 30 мкг вирусного белка (грипп, штамм PR8) и оценивали титр антител через 15 дней после иммунизации. В качестве дополнительного контроля использовали 10 самцов линии С57В1 5месячного возраста.
Результаты приведены в таблице 2.
Таким образом, введение агента, связывающего внеклеточную ДНК крови, замедляет связанное с возрастом снижение иммунитета.
Пример 6. Замедление связанного с возрастом снижения моторной активности.
В эксперименте использовали 20месячных самцов мышей линии С57В1. Самцы опытной группы (10 мышей), начиная с 19 месячного возраста, получали ежедневные внутримышечные инъекции липосомальной ДНКазы 1 (200 мкг ДНКазы 1 в 100 мкг смеси соевого фосфатидилхолина и холестерола (7:3)). Самцы контрольной группы (10 мышей) получали внутримышечные инъекции «пустых» липосом такого же состава. В возрасте 20 месяцев измеряли подвижность животных при однократном видеонаблюдении в течение 30 минут с последующей компьютерной обработкой. В качестве дополнительного контроля использовали 10 самцов линии С57В1 5месячного возраста. Получасовая активность 5месячных мышей была принята за 100%.
Результаты приведены в таблице 3.
Таким образом, введение агента, разрушающего внеклеточную ДНК крови, замедляет связанное с возрастом снижение локомоторной активности.
Пример 7. Замедление биологического старения у человека. В качестве агента, инактивирующего внеклеточную ДНК крови, использовали фермент - панкреатическую бычью Дорназу. В исследовании участвовало 10 клинически здоровых мужчин в возрасте от 50 до 55 лет. До начала исследования участники рандомизировались в опытную (5 человек) и контрольную (5 человек) группы. В опытной группе мужчины получали капсулы с панкреатической бычьей Дорназой в количестве 900000 ед. Кунца в сутки (5 капсул по 100 мг) ежедневно в течение 6 месяцев. В контрольной группе мужчины получали по 5 капсул, содержащих плацебо, ежедневно в течение 6 месяцев.
Исследовали ДНК-гидролитическую активность в суточной моче, содержание внеклеточной ДНК плазмы крови. До начала исследования и по его завершении определяли биологический возраст испытуемых по следующей методике:
БВ=26,985+0,215*САД-0,149*ПК-0,151*ИБ+0,723*ИЗ
САД - систолическое артериальное давление
ПК - потребление кислорода (время задержки дыхания в секундах)
ИБ - время статической балансировки в секундах
ИЗ - индекс субъективной оценки здоровья (в настоящем исследовании принят за 0,75)
(См. Геронтология, 1999, вып.2 «КОЛИЧЕСТВЕННАЯ ОЦЕНКА ПОКАЗАТЕЛЕЙ СМЕРТНОСТИ, СТАРЕНИЯ, ПРОДОЛЖИТЕЛЬНОСТИ ЖИЗНИ И БИОЛОГИЧЕСКОГО ВОЗРАСТА» А.А.Подколзин, В.Н.Крутько, В.И.Донцов: Институт системного анализа РАН, Москва Национальный геронтологический центр, Москва Московский государственный медико-стоматологический университет Минздрава РФ) Результаты исследования приведены в таблице 4.
**Усредненный показатель количества внеклеточной ДНК крови, определенный путем измерения флюоресценции этидия бромида в плазме, принят за 100%
Таким образом, применение заявленного способа улучшает показатели биологического возраста человека.
Пример 8. Замедление наступления связанной с возрастом естественной смерти.
В качестве агента, стимулирующего синтез эндогенной дезоксирибонуклеазы, использовали стволовые клетки пуповинной крови человека (СКПК), трансфецированые in vitro кДНК гена Дезоксирибонуклеазы 1 человека.
В опыте использовали 40 белых беспородных крыс. В опытной группе 1 (10 животных) крысам, начиная с 24 месячного возраста, вводили препарат, содержащий трансген, в количестве 50000000 клеток на одно животное внутривенно ежемесячно до момента гибели животного. Крысам опытной группы 2, начиная с 24-месячного возраста, вводили подкожно ДНК тимуса теленка, 1 раз в месяц в дозе 50 мг/животное до момента гибели животных. Крысам контрольной группы 1 (10 животных) вводили интактные СКПК. Крысам контрольной группы 2 (10 животных) вводили физиологический раствор. Продолжительность жизни крыс в контрольной группе 1 составила в среднем 29 месяцев. Продолжительность жизни крыс в контрольной группе 2 (естественная продолжительность жизни) составила в среднем 27 месяцев Продолжительность жизни крыс в опытной группе 1 составила в среднем 35 месяцев, в опытной группе 2-33 месяца.
Изобретение относится к медицине и может быть использовано для увеличения продолжительности жизни за счет замедления наступления болезненных состояний, связанных с увеличением возраста. Для этого в циркуляцию крови вводят агент, инактивирующий внеклеточную ДНК крови. В качестве такого агента могут быть использованы ДНКаза, анти-ДНК антитела, ферменты, изменяющие химическую структуру внеклеточной ДНК крови, а также агенты, стимулирующие синтез или активность эндогенной ДНКазы или стимулирующие синтез антител, связывающих внеклеточную ДНК крови. Способ обеспечивает эффект лечения при отсутствии прямого воздействия на генетический аппарат стареющих клеток. 6 з.п. ф-лы, 2 ил. 4 табл.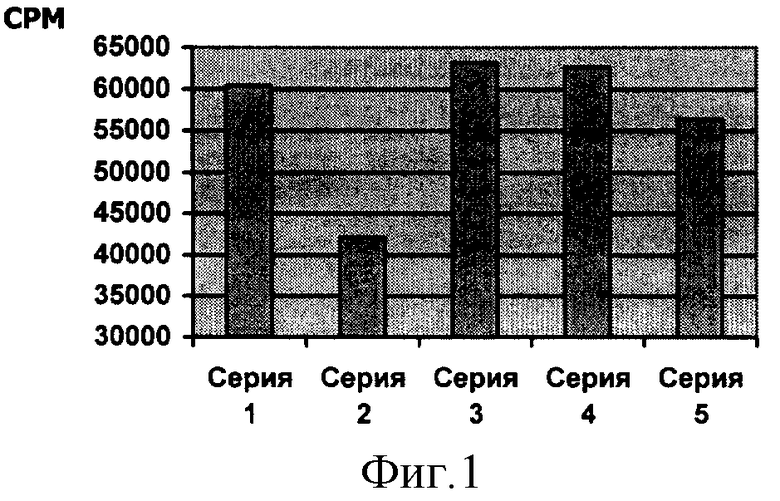
| US 5484589, 16.01.1996 | |||
| US 2004001817, 01.01.2004 | |||
| DE 10221194, 04.12.2003 | |||
| ОСИВАЦ Х.Д | |||
| и др | |||
| Реорганизация ДНК и биологическое старение | |||
| Биохимия, 1997, 62, №11, с | |||
| Высоковольтный вольтметр | 1924 |
|
SU1491A1 |
| КАЛАНДАРИШВИЛИ Ф | |||
| Накопление спонтанно поврежденной ДНК в не- и постгепатэктомированной печени у старых крыс | |||
| Мед | |||
| новости Грузии, 1998, № 5, с | |||
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
| RAO K.S | |||
| et al. | |||
Авторы
Даты
2006-02-10—Публикация
2004-03-12—Подача