Изобретение относится к новым биологически активным N-ациламинокетонам ряда 1,4-бензодиоксана, а именно к 6-(4'-хлорбензоил)-7-(N-4''-нитробензоил)амино-1,4-бензодиоксану и его аналогам с общей формулой I, обладающим противосудорожной активностью.
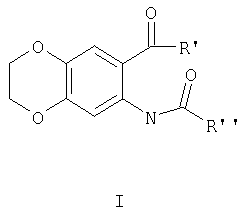
где R'=алкил(C3-C4), Ar-Х (Х=Н, п-СН3, o-, п-Hal);
R''=CH2Cl, Ar-X (Х=п-СН3, м-, п-ОСН3, п-Hal, м-, п-NO2, 2-тиофенил, 6-бензо-1,4-диоксанил).
Это свойство позволит применять их в медицинской практике в качестве высокоэффективных и малотоксичных противосудорожных препаратов нового поколения.
Структурным аналогом предлагаемых соединений может служить 7-бромацетиламино-6-пропионил-1,4-бензодиоксан (статья авторов Мочалова С.С., Шабарова Ю.С. и других в журнале ХГС, 1994, N 5, с.601) со следующей формулой:
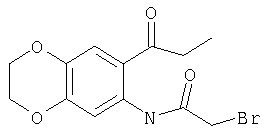
7-бромацетиламино-6-пропионил-1,4-бензодиоксан на биологическую активность не испытывался, но может найти применение в качестве исходного соединения в синтезе лекарственных веществ класса транквилизаторов.
Аналогом предлагаемых соединений по противосудорожным свойствам является карбамазепин (дибенз[b,1f]азепин-5-карбоксамид), (Машковский М.Д. Лекарственные средства, М., "Медицина", 1985, т.2, с.148.), успешно применяемый в медицинской практике, с формулой
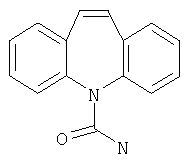
Многие из предлагаемых нами соединений являются более эффективными (почти на порядок) и менее токсичными чем карбамазепин.
При судорогах, вызванных максимальным электрошоком, ЕД50 вещества 1 (R'=п-CI-Ph, R''=п-NO2-Ph), одного из самых эффективных среди предлагаемых, равна 1,16 мг/кг, следовательно, ее эффективность по сравнению с известным противосудорожным средством карбамазепином (ЕД50=20 мг/кг) выше примерно в 17 раз.
Соединения формулы I не описаны ни в научно-технической, ни в патентной литературе.
Вещества формулы I получают исходя из 1,4-бензодиоксана четырехстадийным синтезом.
Стадия 1. Ацилирование 1,4-бензодиоксана требуемыми хлорангидридами кислот в положение 6 по реакции Фриделя-Крафтса.
Стадия 2. Нитрование полученных 6-ацил-1,4-бензодиоксанов в положение 7 нитрующей смесью в ледяной уксусной кислоте.
Стадия 3. Восстановление полученных на предыдущей стадии 6-ацил-7-нитро-1,4-бензодиоксанов активированным железом.
Стадия 4. N-ацилирование 6-ацил-7-амино-1,4-бензодиоксанов требуемыми хлорангидридами кислот.
Согласно настоящему изобретению предложены соединения общей формулы I, обладающие противосудорожной активностью.
Примерами осуществления изобретения могут служить следующие соединения, охарактеризованные в таблице 1:
1. 6-(4'-хлорбензоил)-7-(N-4''-нитробензоил)амино-1,4-бензодиоксан.
2. 6-изобутироил-7-(N-2'-тиофенкарбоноил)амино-1,4-бензодиоксан.
3. 6-бутироил-7-(N-2'-тиофенкарбоноил)амино-1,4-бензодиоксан.
4. 6-бутироил-7-(N-4'-метилбензоил)амино-1,4-бензодиоксан.
5. 6-бутироил-7-(N-4'-метоксибензоил)амино-1,4-бензодиоксан.
6. 6-бензоил-7-(N-хлорэтаноил)амино-1,4-бензодиоксан.
7. 6-бензоил-7-(N-4'-метоксибензоил)амино-1,4-бензодиоксан.
8. 6-(4'-метилбензоил)-7-(N-3''-метоксибензоил)амино-1,4-бензодиоксан.
9. 6-(2'-хлорбензоил)-7-(N-4''-нитробензоил)амино-1,4-бензодиоксан.
10. 6-(2'-бромбензоил)-7-(N-6''-бензо-1,4-диоксанкарбоноил)-амино-1,4-бензодиоксан.
11. 6-(4'-хлорбензоил)-7-(N-2''-тиофенкарбоноил)амино-1,4-бензодиоксан.
Пример 1.
Синтез 6-(4'-хлорбензоил)-7-(N-4''-нитробензоил)амино-1,4-бензодиоксана.
Стадия 1. Синтез 6-(4'-хлорбензоил)-1,4-бензодиоксана.
К взвеси 100 г (0,75 моль) безводного AlCI3 в 300 мл сухого CCI4 при перемешивании и температуре 0°С прибавляют раствор 105 г (0,50 моль) п-хлорбензоилхлорида в 200 мл сухого CCI4. Затем прибавляют по каплям 68 г 1,4-бензодиоксана. Перемешивают в течение 1 часа, выливают смесь в ледяную воду с HCI. Органический продукт реакции выделяют, сушат на воздухе. Выход 6-(4'-хлорбензоил)-1,4-бензодиоксана 96,08 г (около 70% от теоретического).
Т.пл. 103-104°С (из этанола).
Стадия 2. Синтез 6-(4'-хлорбензоил)-7-нитро-1,4-бензодиоксана.
К раствору 77 г (0,28 моль) 6-(4'-хлорбензоил)-1,4-бензодиоксана в 490 мл ледяной уксусной кислоты при температуре -20°С и перемешивании приливают по каплям предварительно приготовленную нитрующую смесь. Перемешивают 1 час, выливают в воду, выделяют нитросоединение, сушат на воздухе. Выход 114,84 г (примерно 90% от теоретического). Т.пл. 171-172°С (из этанола).
Стадия 3. Синтез 6-(4'-хлорбензоил)-7-амино-1,4-бензодиоксана.
К 95,85 г (0,3 моль) 6-(4'-хлорбензоил)-7-нитро-1,4-бензодиоксана в 300 мл бензола при перемешивании приливают 300 мл воды и присыпают активированное железо и кипятят при энергичном перемешивании в течение 6-10 часов. Органический слой отделяют, остаток железа несколько раз экстрагируют бензолом. Объединенные вытяжки бензола сушат и упаривают досуха. Выход 6-(4'-хлорбензоил)-7-амино-1,4-бензодиоксана 64,2 г (около 75% от теоретического). Т.пл. 123-124°С (из этанола).
Стадия 4. Синтез 6-(4'-хлорбензоил)-7-(N-4''-нитробензоил) амино-1,4-бензодиоксана.
К раствору 57,9 г (0,2 моль) 6-(4'-хлорбензоил)-7-амино-1,4-бензодиоксана в 400 мл диоксана прибавляют по каплям эквивалентные количества п-нитробензоилхлорида (37,1 г; 0,2 моль) в 100 мл диоксана и трехнормального NaOH (67 мл; 0,2 моль). Далее реакционную смесь перемешивают 1 час при температуре 80°С и выливают в воду. Выпавшее вещество отфильтровывают, сушат на воздухе. Выход 70,2 г (примерно 80% от теоретического).
Соединение 1 - светло-желтое кристаллическое вещество с т.пл. 227-228°С (из этанола).
ИК спектр, νmax/см-1: 3480-3500 (NH), 1670 (СО, амидный), 1640 (СО, ацильный), 1545 (NO2), 1485, 1324, 1292, 1270, 1256, 1190, 1140, 1078, 1023, 960, 880, 720.
Результаты анализа и данные ЯМР спектра соединения I приведены в таблице 1.
Соединения со 2-го по 23-е общей формулы I получены по подобной схеме и охарактеризованы в таблице 1.
Орто-ацил-N-ациламино-1,4-бензодиоксаны общей формулы I, полученные по описанной схеме.
Пример 2.
Фармакологические исследования.
Фармакологические исследования проводились на белых беспородных мышах-самцах массой тела 18-24 г. Животные получали через корнеальные электроды электрические стимулы (50 Hz, 50 mA) длительностью 0,2 секунды. Используемый показатель - максимальная тоническая экстензия задних конечностей, которая возникает у 100% контрольных животных. Оценивалась способность исследуемых веществ предупреждать развитие тонической экстензии при их введении внутрибрюшинно. Для определения ЕД50 - эффективной дозы вещества, оказывающей противосудорожный эффект у 50% животных, использовали по меньшей мере 3 дозы вещества, и каждую дозу испытывали на 8-10 животных.
Влияние вещества 1 на судороги, вызванные максимальным электрошоком.
Проведенные исследования показали, что соединение I (6-(4'-хлорбензоил)-7-(N-4''-нитробензоил)амино-1,4-бензодиоксан), одно из самых эффективных среди предлагаемых, оказывает защитный эффект на клонические и тонические судороги, вызванные максимальным электрошоком у мышей с ЕД50=1,16 мг/кг.
При судорогах, вызванных максимальным электрошоком, эффективность нашего вещества выше на порядок эффективности карбамазепина.
Исследования показали, что вещество 1 не обладает токсичностью при терапевтических дозах (LD50>500 мг/кг в/б). A LD50 карбамазепина равна 160 мг/кг и 200 мг/кг в/б для мышей и крыс соответственно.
Со 2-го по 11-е соединения, приведенные в таблице 1, исследованы аналогично соединению I (ED50 всех исследованных соединений и карбамазепина приведены в таблице 3). Все они обладают противосудорожной активностью и не обладают токсичностью при терапевтических дозах.
ED50 соединений 1-11 и карбамазепина (12).
| название | год | авторы | номер документа |
|---|---|---|---|
| Производные кумарина, тиокумарина и хинолинона, обладающие противосудорожной активностью | 2017 |
|
RU2720510C2 |
| Производные 4-фенилпирролидона, обладающие противосудорожной и ноотропной активностью, как средства лечения эпилепсии и пароксизмальных состояний | 2017 |
|
RU2748419C2 |
| 4-П-ИЗОПРОПОКСИФЕНИЛ-2-ПИРРОЛИДОН, ОБЛАДАЮЩИЙ ПРОТИВОСУДОРОЖНОЙ АКТИВНОСТЬЮ | 1985 |
|
SU1269456A1 |
| Производные оксимов 4-бензоилпиридина, обладающие противосудорожной активностью, как средства лечения эпилепсии и пароксизмальных состояний | 2016 |
|
RU2643091C2 |
| 2-МЕТИЛАМИНО-4-ОКСО-3,6,6-ТРИМЕТИЛ-5,6-ДИГИДРО-8Н-ПИРАНО[4′,3′ : 4,5]ТИЕНО[2,3-D]ПИРИМИДИН ИЛИ ЕГО СОЛИ, ОБЛАДАЮЩИЕ ПРОТИВОСУДОРОЖНОЙ АКТИВНОСТЬЮ | 1983 |
|
SU1132513A1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ПАРОКСИЗМАЛЬНЫХ СОСТОЯНИЙ | 2011 |
|
RU2469722C1 |
| ЦИННАМОИЛЬНЫЕ ПРОИЗВОДНЫЕ ОКСИМА ДИБЕНЗОФУРАНОНА, ОБЛАДАЮЩИЕ ПРОТИВОСУДОРОЖНОЙ АКТИВНОСТЬЮ | 2023 |
|
RU2810250C1 |
| АМИНОАЛКИЛЬНЫЕ ПРОИЗВОДНЫЕ ОКСИМА ДИБЕНЗОФУРАНОНА, ОБЛАДАЮЩИЕ ПРОТИВОСУДОРОЖНОЙ АКТИВНОСТЬЮ | 2020 |
|
RU2773021C2 |
| 4-(3,4-Дибромтиофенкарбонил)-2,6,8,12-тетраацетил-2,4,6,8,10,12-гексаазатетрацикло[5,5,0,0,0]додекан в качестве противосудорожного средства | 2018 |
|
RU2684107C1 |
| 4'-Гидрокси-1'-(2-гидроксифенил)-3'-(4-R-бензоил)спиро[бензо[b][1,4]тиазин-2,2'-пиррол]-3,5'(1'H,4H)-дион | 2022 |
|
RU2783263C1 |
Изобретение относится к 6-(4'-хлорбензоил)-7-(N-4''-нитробензоил)амино-1,4-бензодиоксану и его аналогам общей формулы I, обладающим противосудорожной активностью
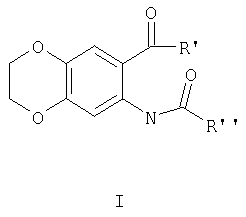
где R'=алкил(С3-С4), Ar-Х (Х=Н, п-СН3, о-, п-Hal); R''=CH2CI, Ar-X (X=п-СН3, м-, п-ОСН3, п-NO2, 2-тиофенил, 6-бензо-1,4-диоксанил). Технический результат - получение новых соединений, которые могут быть использованы в фармакологии. 3 табл.
6-(4'-Хлорбензоил)-7-(N-4''-нитробензоил)амино-1,4-бензодиоксан и его аналоги с общей формулой I, обладающие противосудорожной активностью
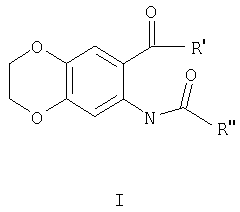
где R'=алкил(С3-С4), Ar-Х (Х=Н, п-СН3, о-, п-Hal);
R''=CH2Cl, Ar-X (Х=п-СН3, м-, п-ОСН3, п-NO2, 2-тиофенил, 6-бензо-1,4-диоксанил).
| Catalog: Interchim Intermediates, 09.07.2002 | |||
| Ambinter Screening Library, 01.01.2004 | |||
| Ambinter Stock Screening Collection, 01.01.2004 | |||
| ПРОИЗВОДНЫЕ 5-НАФТАЛИН-1-ИЛ-1,3-ДИОКСАНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ЛЕКАРСТВЕННОЕ СРЕДСТВО И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1996 |
|
RU2163601C2 |
Авторы
Даты
2006-05-27—Публикация
2004-01-30—Подача