Предлагается новое химическое соединение, а именно 4-п-изопропоксифенил-2-пирролидон формулы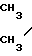 CH
CH O
O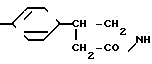 обладающее противосудорожной активностью.
обладающее противосудорожной активностью.
Целью изобретения является поиск новых соединений в ряду пирролидина, обладающих выраженным противосудорожным действием с высоким терапевтическим индексом.
П р и м е р 1. Диэтиловый эфир п-изопропоксибензилиденбисацетоуксусной кислоты.
Смесь 8,2 г (0,05 моль) п-изопропоксибензальдегида, 13 г (0,1 моль) ацетоуксусного эфира, 1,1 мл пиперидина и 3 мл 95%-ного этилового спирта оставляют на 24 ч при комнатной температуре. Затвердевшую массу отфильтровывают и перекристаллизовывают из 50%-ного этилового спирта. Выход 27 г (72% ), т.пл. 109-110оС, Rf 0,52 (на закрепленном слое силикагель-гипс; элюент-эфир: петролейный эфир, 24:16; проявитель пары йода).
Найдено, C 65,09; H 7,30.
C22H30O7
Вычислено, C 65,01; H 7,36.
Молекулярная масса 406 (масс-спектрометрически).
П р и м е р 2. β-(п-Изопропоксифенил)глутаровая кислота.
Смесь 14 г (0,03 моль) диэтилового эфира п-изопропоксибензилиденбис-ацетоуксусной кислоты, 3,6 г (0,09 моль) гидроокиси натрия, 50 мл этилового спирта и 50 мл воды кипятят при перемешивании 10 мин. После отгонки спирта реакционную массу экстрагируют эфиром, водный слой обрабатывают активированным углем, отфильтровывают и подкисляют соляной кислотой. Полученное кристаллическое соединение отфильтровывают из 50%-ного этилового спирта. Выход 5,66 г (71% ), т.пл. 115-116оС (по литературным данным т.пл. 98-100оС), Rf 0,22 (на закрепленном слое силикагель-гипс; элюент-бутанол: аммиак, 35:15; проявитель бромкрезоловый пурпуровый).
Найдено, C 63,58; H 6,53.
C14H18O5
Вычислено, C 63,14; H 6,81.
Молекулярная масса определена масс-спектрометрически.
П р и м е р 3. Моноамид β-(п-изопропоксифенил)глутаровой кислоты.
Смесь 13 г (0,04 моль) β-(п-изопропоксифенил)глутаровой кислоты и 8,16 г (0,08 моль) уксусного ангидрида нагревают при 80-90оС в течение 3 ч. Избыток уксусного ангидрида и полученную уксусную кислоту отгоняют при уменьшенном давлении. К оставшейся маслообразной массе, растворенной в 50 мл этилацетата, прибавляют насыщенный аммиаком этилацетат до щелочной реакции. Выпавший осадок отфильтровывают, промывают абсолютным эфиром, растворяют в воде и подкисляют соляной кислотой до рН 3. Полученные кристаллы отфильтровывают, промывают водой до нейтральной реакции. Выход 10 г (83%), т.пл. 161оС, Rf 0,40 (на закрепленном слое силикагель-гипс; элюент-бутанол; аммиак 35:15; проявитель бромкрезоловый пурпуровый).
Найдено, C 63,59; H 7,42; N 5,63.
C14H13NO4
Вычислено, C 63,38; H 7,21; N 5,28.
Молекулярная масса определена масс-спектрометрически.
П р и м е р 4. β-(п-Изопропокси)фенил- γ-аминомасляная кислота.
К холодному раствору (0-5оС) 10,8 г (0,18 моль) гидроокиси калия в 90 мл дистиллированной воды прибавляют 2,6 г (0,02 моль) брома. Раствор охлаждают до 0оС, добавляют 5,3 г (0,02 моль) моноамина β-(п-изопропоксифенил)глутаровой кислоты, нагревают при 55-60оС в течение 4 ч и оставляют при комнатной температуре на ночь. Реакционную смесь нейтрализуют разбавленной соляной кислотой до рН 7, выпавший осадок отфильтровывают и перекристаллизовывают из абсолютного этилового спирта. Выход 3,3 г (72%), т.пл. 225оС. Rf 0,20 (на закрепленном слое силикагель-гипс; элюент-бутанол: аммиак, 35:15; проявитель ингидрин).
Найдено, C 65,36; H 8,11; N 5,76.
C13H13NO3
Вычислено, C 65,79; H 8,07; N 5,90.
ИК-спектр, ν, см-1: 1670 (C=O); 2560 (NH
П р и м е р 5. 4-п-Изопропоксифенил-2-пирролидон (I).
2,3 г (0,01 моль) β-(п-изопропокси)фенил-γ-аминомасляной кислоты нагревают при 225оС в течение 20 мин. После охлаждения расплав кристаллизуется. Перекристаллизовывают из 50%-ного этилового спирта. Выход 1,2 г (60%), т.пл. 97-98оС, Rf 0,52 (на закрепленном слое силикагель-гипс; элюент-эфир: петролейный эфир, 6:4; проявитель пары йода).
Найдено, C 71,62; H 7,56; N 6,54.
C13H17NO2
Вычислено, C 71,20; H 7,81; N 6,38.
ИК-спектр, ν, см-1: 1665, 1680 (C=O); 3090, 3180 (NH).
Молекулярная масса 219 (масс-спектрометрически).
4-п-Изопропоксифенил-2-пирролидон (соединение I) представляет собой белое кристаллическое вещество без запаха, растворимое в этиловом спирте, эфире, хлороформе, нерастворимое в воде.
Фармакологические исследования соединения I проводили в сравнении с чистой субстанцией препарата пуфемид. Введение вещества осуществляли за 45 мин до начала эксперимента во взвеси с карбоксиметилцеллюлозой. Действие соединений в каждой дозе изучено на 10-12 животных. Всего в опытах использовано 240 белых беспородных мышей массой 18-24 г.
Противосудорожное действие оценивали по предупреждению клонических судорог при подкожном введении коразола, по защите от тонической экстензии максимального электрошока. О нейротоксическом эффекте судили по явлениям миорелаксации, нарушению координации, атаксии, применяя методику "вращающегося стержня". Определяли также острую суточную токсичность. Вычисляли 50%-ные эффективную (ЕД50), нейротоксическую (ТД50) и летальную (ЛД50) дозы, а также защитный ЗИ (ТД50/ЕД50) и терапевтический ТИ (ЛД50/ЕД50) индексы.
Соединение I, введенное за 45 мин до коразола в дозе 20 мг/кг, предупреждает клонические судороги у 50% животных. Примерно в этой же дозе отмечается защита от тонической экстензии максимального электрошока (ЕД50 19,5 мг/кг). Десятикратное повышение противосудорожных доз до 200 мг/кг приводит к миорелаксации, нарушению координации движений и атаксии явлениям, характеризующим "неврологический дефицит" антиконвульсантов. ЛД50 составляет 1550 мг/кг, т.е. превосходит ЕД50 по антагонизму с коразолом и электрошоком почти в 80 раз (см. таблицу).
Антикоразоловая активность пуфемида проявляется лишь в дозе 86 мг/кг, а предупреждение тонической экстензии в дозе 77 мг/кг, "неврологический дефицит" отмечается от 450 мг/кг. Дальнейшее повышение дозы препарата до 2150 мг/кг приводит к гибели 50% животных (см. таблицу).

4-п-Изопропоксифенил-2-пирролидон формулы
обладающий противосудорожной активностью.
4-п-Изопропоксифенил-2-пирролидон формулы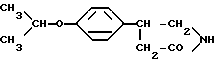
обладающий противосудорожной активностью.
| Мнджоян О | |||
| Л., Аветисян С | |||
| А., Акопян Н | |||
| Е., Герасимян Д | |||
| А., Джагацпанян И | |||
| А., Пашинян С | |||
| А | |||
| Новый отечественный противоэпилептический препарат пуфемид | |||
| - Хим.-фарм | |||
| ж | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
Авторы
Даты
1996-02-10—Публикация
1985-03-29—Подача