Изобретение относится к химии биологически активных веществ, обладающих противосудорожной активностью, конкретно к новой группе замещенных O-(фенилакрилоил)оксимов 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она общей формулы (1):
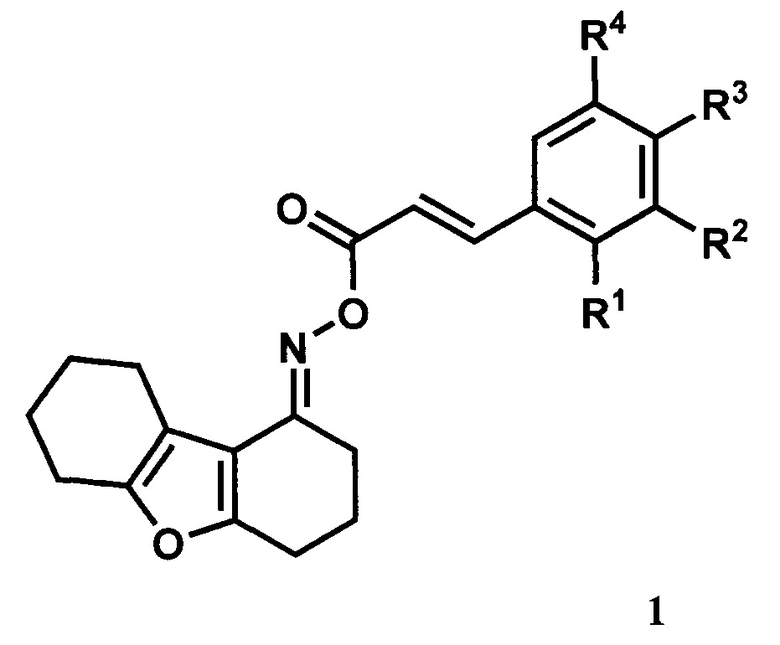
где один или несколько из заместителей R1-R4 могут быть атомами галогенов, алкильными группами, алкоксигруппами, трифторметильными группами, при этом остальные заместители являются водородами; или где два из заместителей R1-R4 одновременно являются -О-СН2-О-группой, при этом остальные заместители являются водородами.
Эпилепсия является одним из самых распространенных неврологических заболеваний в мире, которым страдает порядка 50 млн. человек по данным на 2022 год. По оценкам Всемирной Организации Здравоохранения (ВОЗ), доля общего населения с активной формой эпилепсии (то есть с продолжающимися припадками или потребностью в лечении) на данный момент времени составляет от 4 до 10 на 1000 человек. По оценкам, в глобальных масштабах эпилепсия ежегодно диагностируется у 5 млн человек [Информационных бюллетень ВОЗ. Эпилепсия. 9.02.2022. https://www.who.int/ru/news-room/fact-sheets/detail/epilepsy].
Экономический ущерб, связанный с эпилепсией, оценивался в 2015 году в 28 миллиардов долларов в США [С.Е. Begley, T.L. Durgin. Epilepsia. 2015. 56(9), 1376-1387] и в 20 миллиардов долларов в Европе в 2010 году [International League Against Epilepsy, International Bureau for Epilepsy and WHO. Epilepsy in the WHO European Region: fostering epilepsy care in Europe. Hoofddorp, The Netherlands: Global Campaign Against Epilepsy; 2010].
Существующие на сегодняшний день средства для лечения эпилепсии не в полной мере удовлетворяют требованиям клиники вследствие сложной мультифункциональной этиологии этого заболевания и большого количества его форм. Кроме того, известные препараты имеют массу нежелательных явлений. По этой причине задача по разработке новых эффективных противосудорожных препаратов, купирующих эпилептические приступы, стоит остро. Это подтверждает и существенное количество поисковых работ и обзоров литературы, посвященных разработке и поиску новых средств для лечения эпилепсии, которое с каждым годом увеличивается. Согласно данным базы данных pubmed.gov по запросу «design, synthesis, anticonvulsant» выявляется 2767 результатов, из которых на 2020-ые годы приходится порядка 400 работ; а по запросу «anticonvulsant» - 172075 результатов, из которых примерно 12500 работ опубликованы в 2020-ые годы (данные на ноябрь 2022 года).
Задачей настоящего изобретения является поиск новых биологически-активных соединений с противосудорожной активностью, обладающих высокой эффективностью, высоким теоретически сродством как к ГАМКА-, так и к 5-НТ2(A, B, C)-рецепторам, согласно методам молекулярного моделирования, и имеющих благоприятный профиль расчетных ADMET-параметров.
Неожиданно искомые характеристики были обнаружены у некоторых соединений группы замещенных O-(циннамоил)оксимов 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она общей формулы (1).
Соединения общей формулы (1), их свойства и способ получения в специальной и патентной литературе не описаны.
Примеры соединений формулы (1) по настоящему изобретению:
O-((4-фторфенил)акрилоил)оксим 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она (MBS-4),
O-((2-фторфенил)акрилоил)оксим 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2Н)-она (MBS-7),
O-((3-фторфенил)акрилоил)оксим 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она (MBS-8),
O-((3-хлорфенил)акрилоил)оксим 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она (MBS-9),
O-((4-бромфенил)акрилоил)оксим 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она (MBS-28),
O-((3,4-диметоксифенил)акрилоил)оксим 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она (MBS-30),
O-((4-хлорфенил)акрилоил)оксим 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она (ГИЖ-348),
O-((2-хлорфенил)акрилоил)оксим 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она (ГИЖ-351),
O-((3,4-дихлорфенил)акрилоил)оксим 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она (ГИЖ-352),
O-((3,4-метилендиоксифенил)акрилоил)оксим 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она (SD-16),
O-((4-метилфенил)акрилоил)оксим 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она (SD-17),
O-((4-метоксифенил)акрилоил)оксим 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она (SD-18),
O-((3,4,5-триметоксифенил)акрилоил)оксим 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она (SD-19),
O-((4-трифторметилфенил)акрилоил)оксим 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она (SD-20).
Техническим результатом изобретения является расширение арсенала лекарственных средств для лечения эпилепсии и судорожных состояний, обладающих высокой эффективностью, высоким сродством как к ГАМКА-, так и к 5-НТ2(A, B, C)-рецепторам.
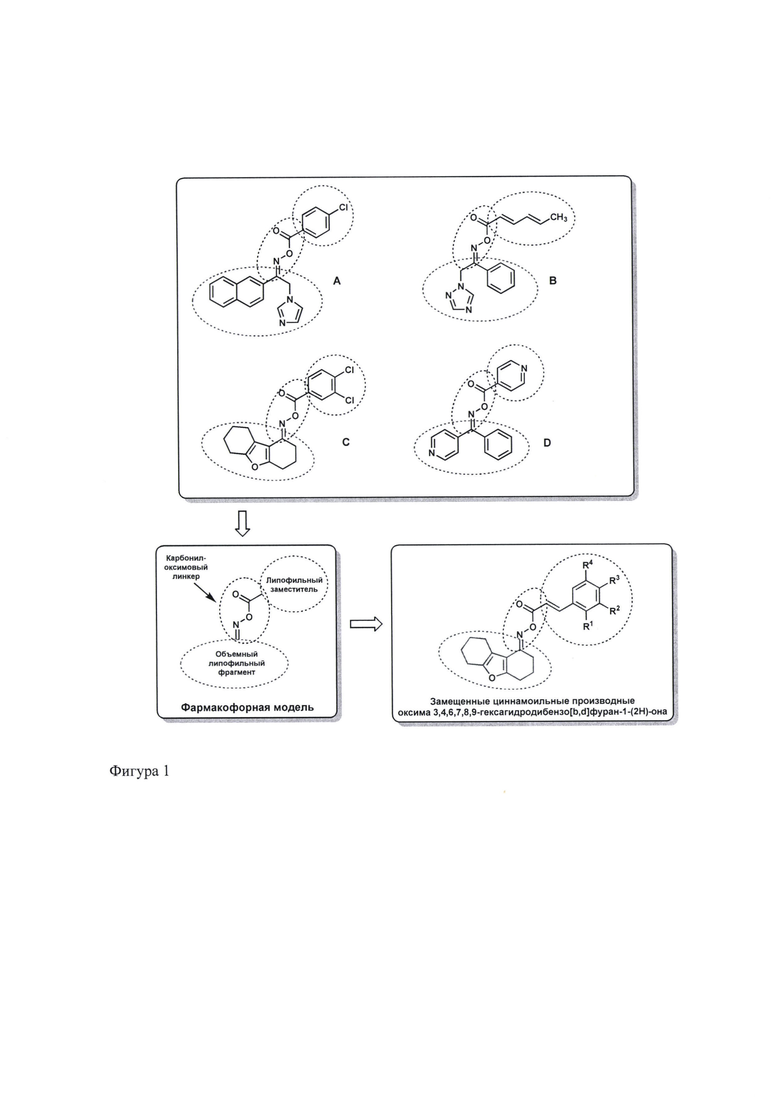
Дизайн замещенных циннамоильных производных оксима 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она с потенциальной противосудорожной активностью
Анализ существующих соединений, обладающих противосудорожной активностью, позволяет идентифицировать отдельную группу веществ, соответствующих обобщенной фармакофорной модели, представленной на фигуре 1. В эту модель входит объемный липофильный фрагмент, который через карбонил-оксимовый линкер соединен с другим липофильным заместителем, в качестве которого чаще всего используются арил/гетарил-содержащие группы или другие ненасыщенные группы. Этой фармакофорной модели соответствуют, например, такие вещества, как представитель группы оксимов 1-(2-нафтил)-2-(имидазол-1-ил)этанона (А), проявляющий противосудорожную активность в тесте подкожного введения пентилентетразола (метразола) [A. Karakurt, М.А. Alagöz, В. Sayoğlu et al., Eur. J. Med. Chem. 2012. 57, 275-282]; карбонилоксим-содержащее производное 1,2,4-триазола (В), обладавшее эффективностью в тестах МЭШ и судорог, инуцированных током 6 Гц у мышей [Sari, F.B. Kaynak, S. Dalkara, Pharmacological Reports. 2018. 70(6), 1116-1123]; бензоилсодержащее производное оксима гексагидродибензофурана (С), активное в тесте с МЭШ у крыс [Л.А. Жмуренко, С.А. Литвинова, И.С. Кутепова и др. Хим.-фарм. журн., 2019. 53(11), 9-16]; производное бензоилпиридина (D), показавшее противосудорожную активность в тесте антагонизма с коразолом [Л.А. Жмуренко, Т.А. Воронина, С.А. Литвинова и др., Хим.-фарм. журн. 2018. 52(1), 19 - 28] (фигура 2).
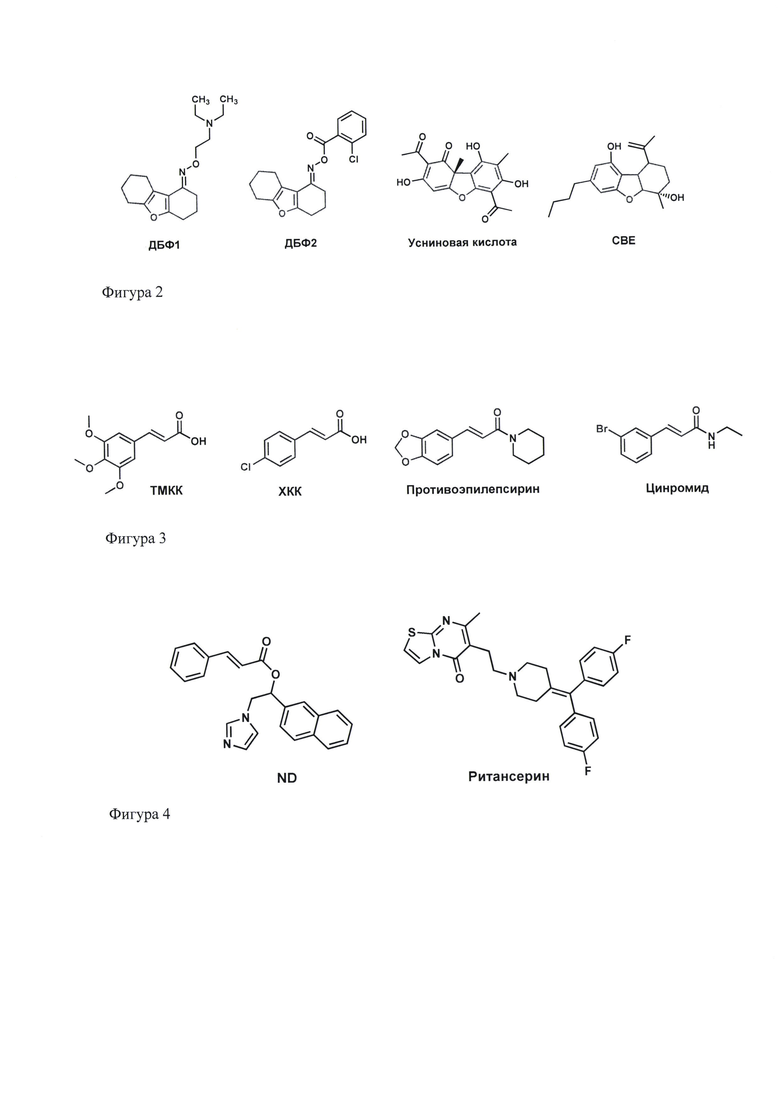
В соответствии с выявленной фармакофорной моделью нами были предложены новые соединения, относящиеся к группе замещенных циннамоильных производных оксима 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она (фигура 1). В качестве объемного липофильного фрагмента в этих структурах был использован гексагидродибензофурановый фармакофор, который эффективно используется в медицинской химии для конструирования потенциальных лекарственных средств (фигура 2). В частности, некоторые производные оксима дибензофуранона, например, ДБФ1 и ДБФ2, обладают противосудорожным действием [Л.А. Жмуренко, 2019; Л.А. Жмуренко, С.А. Литвинова, Г.В. Мокров и др., Хим.-фарм. журн., 2020. 54(10), 15-20]; усниновая кислота обладает гастропротекторными, кардиопротекторными, цитопротекторными и иммуностимулирующими эффектами [ЕР 1885709 А2]; известны производные бензофурана (например, СВЕ), выделеные из растительного материала, обладающие нейропротекторной активностью [X. Hu, М. Wang, G.R. Yan., Journal of Asian Natural Products Research. 2012. 14, 1103-1108].
В качестве липофильного заместителя было предолжено использование остатков замещенных коричных кислот. Такой выбор был обусловлен тем фактом, что коричный фармакофор широко известен в медицинской химии противосудорожных средств (фигура 3). Известно наличие противоэпилептических свойств у 3,4,5-триметоксикоричной кислоты [C.Y. Chen, X.D. Wei, C.R. Chen., Journal of Pharmacological Sciences. 2015. 131, 1-5], 4-хлоркоричной кислоты [Y. Cuan, X. He, Y. Zhao et al., Journal of Pharmacological Sciences. 2017. 23, 76]. Из растений вида Piper (семейство Piperaceae) был выделен амид коричной кислоты, обладающий противосудорожной активностью - противоэпилепсирин [A. Gunia-Krzyżak, K. Pańczyk, A.M. Waszkielewicz, et al., ChemMedChem. 2015. 10(8), 1302-25]. Известен амид замещенной коричной кислоты с антиэпилептическими свойствами - цинромид [Е. Perucca, J. French, М. Bialer. Lancet Neurol, 2007. 6(9), 793-804].
Для выбора новых молекул в сконструированной группе замещенных O-(фенилакрилоил)оксимов 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она общей формулы (1) нами была сгенерирована библиотека соединений, в которых широко варьировались заместители R1-R4 с целью наиболее полного анализа перспективных соединений. При этом в качестве радикалов использовались атомы галогенов, алкильные и алкоксильные группы, трифторметильные группы.
Известно что циннамоильные производные оксима гексагидродибензофурана общей формулы (1) имеют структурное родство с соединениями, обладающими свойствами блокаторов ГАМКА-рецептора (например, циннамоильное производное нафимидона, ND) [M.F. Acar, S. Sari, S. Dalkara. Drug Development Research. 2019. 80(5), 606-616], и ингибиторов серотониновых рецепторов 5-НТ2(A, B, C)-подтипов (например, ретансерин) [Р. Bruno, D.G. Giuseppe. Frontiers in Pharmacology. 2015. 6, 46] (фигура 4).
В связи с этим для синтезированных соединений проводился анализ значений теоретической аффинности к ГАМКа - рецептору и серотониновым рецепторам подтипов 2А, 2В и 2С с использованием метода молекулярного докинга. Кроме того, для них оценивался профиль расчетных ADMET-показателей (absorption, distribution, metabolism, excretion, toxicity - всасывание, распределение, метаболизм, выведение, токсичность).
Молекулярный докинг проводился с использованием белков серотониновых рецепторов 6DRY, 6BQH, 6А93 (5-НТ2(A, B, C), соответственно), взятых из PDB, и белка ГАМКА-рецептора (PDB: 6D6T) в программе Glide v8.1 [https://www.schrodinger.com/products/glide]. Белки рецепторов были подготовлены с помощью Schrodinger Protein Preparation Wizard с использованием стандартного протокола, вода была удалена [Schrödinger Release 2015-2: LigPrep, Schrödinger, LLC, New York, NY, 2015].
Конформации лигандов были рассчитаны в LigPrep
[https://www.schrodinger.com/products/ligprep]. Координаты центра кубической сетки для 6D6T: х 120,36; у 169,18; z 154.23; 20А; для 6BQH: х 38,67; у 0.744; z 56.76; 20А; для 6DRY: х -23.38; у -17.81; z 9.37; 20А; для 6А93: х 15.42; у -17.81; z 17.94; 20А. Стыковка выполнена в Glide ХР. Позы были визуализированы в Maestro 12.8 [https://www.schrodinger.com/products/maestro].
Параметры ADMET рассчитывались в программе QikProp v6.8 от Schrodinger. Среди ключевых характеристик оценивались следующие: молекулярный вес, дипольный момент, молекулярный объем, количество доноров и акцепторов водородных связей, ионизационный потенциал, параметры липофильности в различных системах, степень связываемости с белками плазмы крови, параметр проникновения через гемато-энцефалический барьер, аффинность к hERG-инному каналу, уровень проникновения через мембраны, соответствие «правилу 5» Липинского и «правилу 3» Йоргенсена, оральная биодоступность и ряд других.
Токсикологические параметры оценивались с использованием программы ADMETlab 2.0 [ADMETlab 2.0: an Integrated Online Platform for Accurate and Comprehensive Predictions of ADMET Properties, 2021. https://admetmesh.scbdd.com/]. Рассчитывался токсикологический риск соединений в тесте Эймса, острая токсичность у крыс, канцерогенный потенциал, воспалительные свойства по отношению к различным тканям и ряд других параметров.
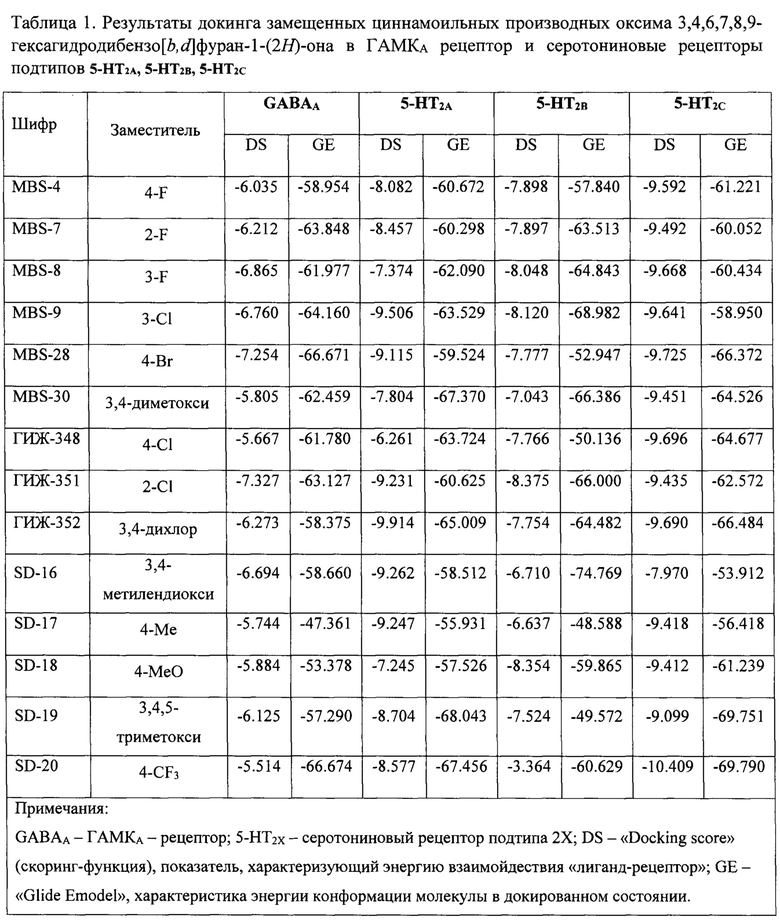
Результаты молекулярного моделирования и результаты оценки расчетных параметров сконструированных соединений представлены в таблице 1 и таблице 2. Все эти молекулы продемонстрировали высокую теоретическую аффинность по отношению активным центрам ГАМКА - рецептора и серотониновых 5-НТ2 - рецепторов. Скоринг функция DS (Docking score), определяющая энергию взаимодействия «лиганд-рецептор», для веществ в отношении ГАМКА-рецептора была ниже значения - 5.5; в отношении 5-НТ2А-рецептора - ниже -6.2; в отношении 5-НТ2В - рецептора - ниже -6.6 (исключение SD-20); в отношении 5-НТ2С - рецептора - ниже -8.0 (Таблица 1). Таким образом, лучшие характеристики теоретического связывания предложенные соединения продемонстрировали относительно серотониновых рецепторов 5-НТ2А- и 5-HT2C-подтипов.
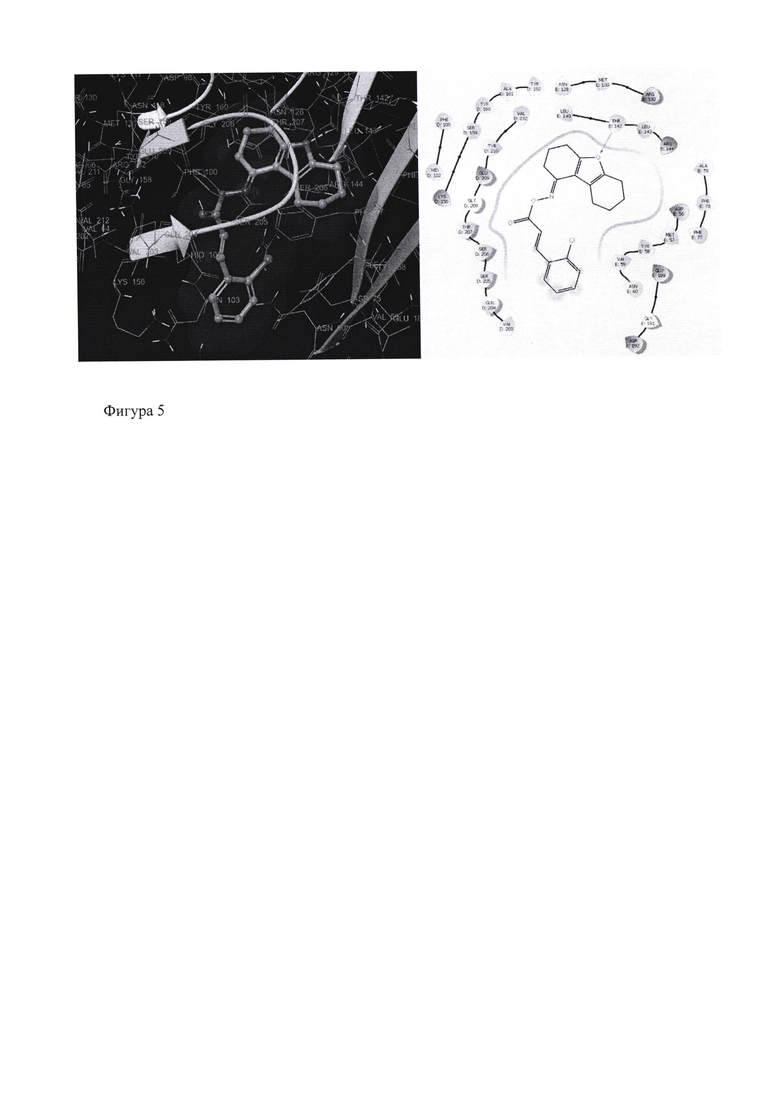
В качестве примера на фигуре 5 представлены результаты докинга 2-Cl замещенного циннамоильного производного оксима гексагидродибензофурана в активный сайт ГАМКА-рецептора в 2D- и 3D-проекциях.
Ключевыми взаимодействиями «лиганд-рецептор» для данного соединения являются водородная связь Thr-142 с кислородом фуранового ядра и липофильное взаимодействие дибензофуранового ядра с последовательностью Asp56-Val59.
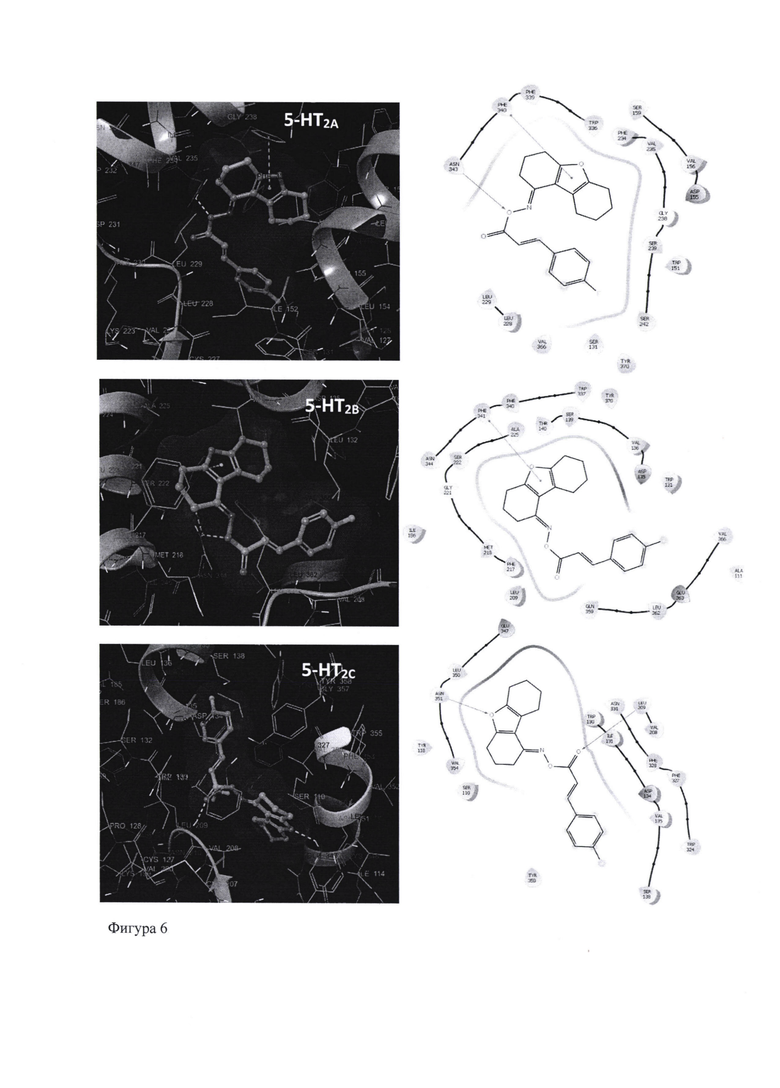
На фигуре 6 представлены визуализированные результаты докинга 4-F-замещенного циннамоильного производного в активные сайты 5-НТ2А-, 5-HT2B- и 5-HT2C-рецепторов в 2D- и 3D-проекциях. Ключевыми взаимодействиями «лиганд-5НТ2А-рецептор» (p-F-5HT2A) являются π-π стекинг Phe340 с фурановым ядром и водородная связь Asn343 с кислородом оксимной группы; «лиганд-5HT2B-рецептор»: π-π стекинг Phe-341 с фурановым ядром; «лиганд-5HT2C-рецептор»: водородные связи Asn351 с кислородом фуранового ядра и Leu209 с карбонильной группой.
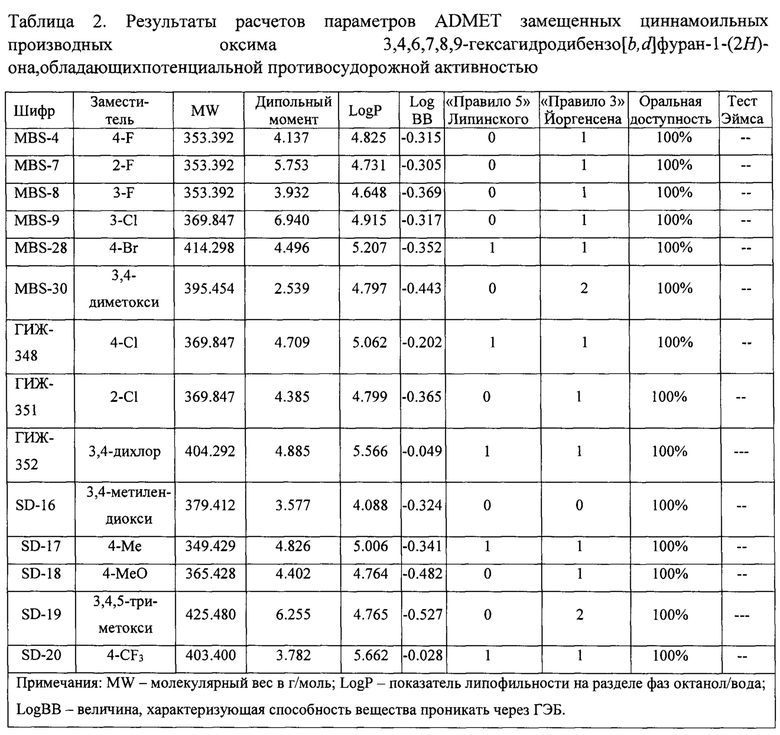
Результаты оценки основных ADMET-параметров отобранных соединений представлены в таблице 2. Значения молекулярного веса находились для всех соединений в пределах 350-425 г/моль, что попадает в интервал 130-725 г/моль, соответствующий 95% известных лекарственных препаратов. Дипольные моменты соединений составляли от 2.5 до 6.9, что вписывается в рекомендуемые параметры для потенциальных лекарственных средств (от 1.0 до 12.5). Липофильность соединений оценивалась путем расчета, прежде всего, параметра LogP (липофильность на разделе фаз октанол/вода). Расчетные значения LogP новых соединений находились в диапазоне от 4.1 до 5.7, что свидетельствует об их достаточной липофильности, которая необходима для достижения органа-мишени мозга. Уровень проникновения веществ через гематоэнцефалический барьер (LogBB) также находился в рекомендуемых пределах от -3.0 до 1.2. Все новые соединения соответствовали правилам Липинского и Йоргенсена, определяющим необходимые требования к строению перорально активных лекарственных средств (расчетные значения для веществ не должны превышать 4 и 3 баллов, соответственно). Оральная биодоступность новых соединений была максимально высокой (100% для всех веществ). Расчетные параметры токсичности отобранных молекул свидетельствовали об их перспективности для разработки в качестве потенциальных лекарственных соединений. Все они по расчетам в тесте Эймса показали полное отсутствие токсичности (значения «---» и «- -»).
Краткое описание чертежей.
Фигура 1. Фармакофорный дизайн замещенных циннамоильных производных оксима 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она
Фигура 2. Биологически-активные производные дибензофуранов
Фигура 3. Коричные кислоты и их производные, обладающие противосудорожными свойствами
Фигура 4. Структуры соединения ND и ритансерина
Фигура 5. 3D- и 2D-проекция результата докинга 2-Cl-замещенного циннамоильного производного в активный сайт ГАМК-А.
Фигура 6. Результаты докинга 4-F-замещенного производного в активный сайт 5НТ2А-, 5HT2B-и 5HT2C-рецептора в 3D- и 2D-проекции
Синтез замещенных циннамоильных производных оксима 3,4,6,7,8,9-гексагидродибен-зо[b,d]фуран-1-(2H)-она.
Представляемые в настоящем изобретении соединения общей формулы (1) можно получить по следующей схеме:
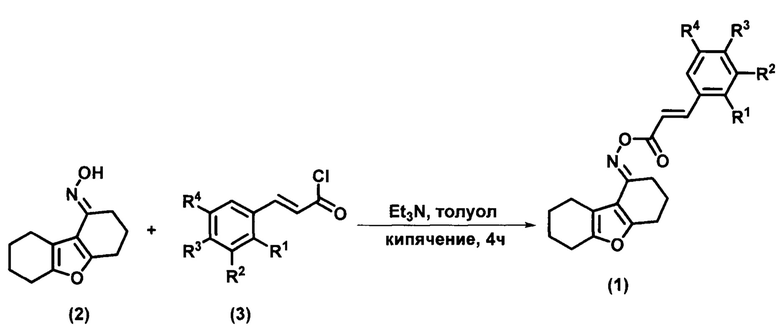
Оксим 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она (2) получают в соответствии со схемой, представленной в работе [Л.А. Жмуренко, 2019]. Оксим 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она (2) вводят во взаимодействие с хлорангидридами замещенных коричных кислот (3) в толуоле, в присутствии триэтиламина в качестве основного катализатора, в результате чего образуются соответствующие замещенные циннамоильные производные оксима 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она (1).
Строение веществ общей формулы (1) подтверждено данными спектров ЯМР 1Н и ЯМР 13С, а их чистота - данными ТСХ.
Для определения физико-химических характеристик полученных веществ использовали следующую аппаратуру. Температуры плавления определяли на приборе Optimelt МРА100 (Stanford Research Systems, США) в открытых капиллярах без корректировки. Строение целевых и промежуточных соединений устанавливали методами одномерной 1Н-,13С- и двумерной (COSY - гомоядерная корреляция, HSQC - гетероядерная одноквантовая корреляция) ЯМР-спектроскопии. Спектры 1Н- и 13С-ЯМР регистрировали в шкале δ, м.д. на спектрометре Bruker FOURIER 300 HD (Bruker Corporation, Leipzig, Germany, 300 и 75 МГц для ядер 1Н- и 13С соответственно) в растворах CDCl3, внутренний стандарт тетраметилсилан (0 м.д.). Константа спин-спинового взаимодействия J, Гц. Для обозначения резонансных сигналов использовали следующие сокращения: с - синглет, д - дублет, т - триплет, м - мультиплет. ИК спектры синтезированных соединений снимали на спектрометре Bruker Vertex 70 (ПО - OPUS 5.5), в таблетках KBr (1 мг в-ва на 10 мг KBr). Тонкослойную хроматографию (ТСХ) выполняли на алюминиевых силикагелевых пластинах DC-Kieselgel 60 G/F254 (Merck, Германия) с обнаружением в УФ-свете и парах иода.
Пример 1. Синтез O-((4-фторфенил)акрилоил)оксима 3,4,6,7,8,9-гексагидродибен-зо[b,d]фуран-1-(2H)-она.
а. 3,4,6,7,8,9-Гексагидродибензо[b,d]фуран-1-(2H)-он.
В 2-горлую кругло донную колбу объемом 500 мл, снабженную хлоркальциевой трубкой, добавляют 20,183 г (180 ммоль) циклогексан-1,3-диона и прибавляют 150 мл дихлорметана при перемешивании на магнитной мешалке до растворения, добавляют 21,857 г (216 ммоль) триэтиламина, после чего прикапывают раствор 26,25 г (198 ммоль) 2-хлорциклогексанона в 50 мл дихлорметана из капельной воронки и перемешивают на магнитной мешалке 24 ч. Реакцию контролируют по ТСХ. Реакционную смесь промывают дистиллированной водой 3 раза порциями по 50 мл, органический слой (нижний) сушат над безводным сульфатом натрия и упаривают на роторном испарителе. Остаток перекристаллизовывают из 50% этилового спирта, выпавшие кристаллы фильтруют на воронке Бюхнера и сушат на масляном насосе. Бесцветные кристаллы, m=20,6 г. Выход 60%. Т. пл. 50-52°С (Т. пл. лит. 50°С [Peng Yi, Eur. J. Org. Chem. 2016. 30, 5169-5179]).
б. Оксим 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она.
В круглодонной колбе объемом 250 мл растворяют 18,878 г (99 ммоль) 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она в 60 мл этилового спирта при перемешивании на магнитной мешалке, добавляют 10,34 г гидроксиламина солянокислого, после растворения осадка добавляют 20 г (500 ммоль) гидроксида натрия и 6 мл дистиллированной воды. Смесь кипятят с обратным холодильником 5 минут, охлаждают до комнатной температуры и выливают в 10% раствор соляной кислоты. Выпавший осадок фильтруют и промывают дистиллированной водой, сушат на воздухе и перекристаллизовывают из спирта. Бесцветные пластинчатые кристаллы, m=16,5 г. Выход 81%. Т. пл. 190-192°С (Т. пл. лит. 192-194°С [Жмуренко Л.А. и др., Хим.-фарм. журн., 2019, 53(11), 9-16]). Спектр ЯМР 1Н (CDCl3, δ, м.д.): 1,77-1,98, 2,57-2,76 (два м, 14Н, м-кольцо); 9,22 (с, 1Н, N-OH). Спектр ЯМР 13С (CDCl3, δ, м.д.): 154.14 (C=N-OH), 151,68 (С4а), 149,55 (С5а), 115.54 (С9а), 114.62 (C9b), 23.01/22.75/22.4 (С2, С4, С3, С6-С8), 21.9 (С9). ИК спектр (KBr, см-1): 3254 (R2C=N-OH), 2935 (-СН), 1586 (R2C-N-OH), 1438 (-НС=СН-), 1361 (-C=N-), 1275 (-C-N-Амид III), 1136(R-O-R).
в. O-((4-фторфенил)акрилоил)оксим 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она (MBS-4).
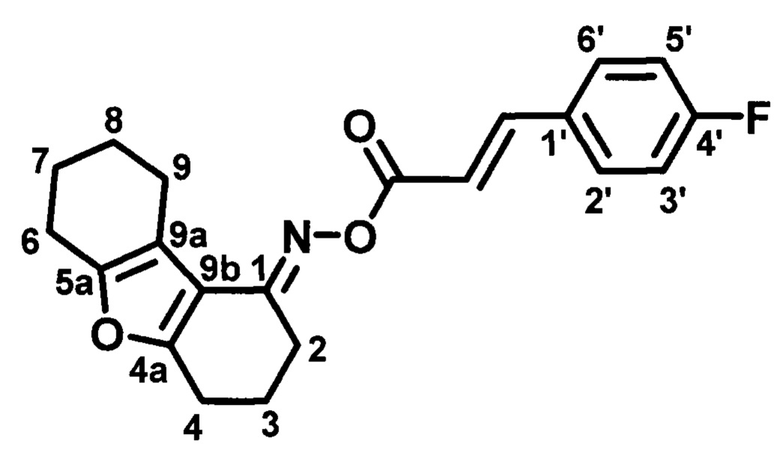
В кругло донную колбу объемом 50 мл помещают 1,03 г (5 ммоль) оксима 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она, добавляют 1,108 г (6 ммоль) хлорангидрида транс-4-фторкоричной кислоты и приливают 30 мл толуола в качестве растворителя. После растворения добавляют 0,61 г (6 ммоль) триэтиламина и нагревают при кипячении с обратным холодильником, снабженным хлоркальциевой трубкой, в течениие 4 ч. Реакционную массу обрабатывают 5% раствором гидрокарбоната натрия (2×25 мл), после чего промывают водой (1×25 мл). Органический слой сушат над безводным сульфатом натрия и упаривают на роторном испарителе. Остаток перекристаллизовывают из этилового спирта и сушат в вакууме масляного насоса 3-4 ч. Кремовые кристаллы, m=1,4 г. Выход 79%. Т. пл. 145-147°С. Rƒ=0.59 (гексан-этилацетат 3:1). Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Гц): 1.75-1.83 (м., 4Н, CH2-7,8); 2.02 (м., 2Н, СН2-3); 2.58 (м., 2Н, СН2-9); 2.72-2.76 (м., 4Н, СН2-2,4); 2.81 (д.т., J1=6.7, J2=12.8, 2Н, СН2-6); 6.57 (д., 1Н, J=16.0,=СН-СО-); 7.10 (м., 2Н, CHAr-3',5'); 7.54-7.57 (м., 2Н, CHAr-2',6'); 7.77 (д., 1Н, J=16.0, Ar-СН=). Спектр ЯМР 13С (CDCl3, δ, м.д.): 165.64 (С=O), 165.02 (C4'-F), 160.69 (С4а), 157.76 (С5а), 150.72 (C1=N), 144.18 (Ar-СН=), 130.77 (С1'), 130.12 (С3'-,5'), 116.23 (СН-СОО), 115.94 (С2',6'), 115.12 (С9а), 114.12 (C9b), 24.2/23.03/22.88/22.79/22.67/21.89 (С2, С4, С3 С6-С9). ИК спектр (KBr, см-1): 3285 (R2C=N-O-R'); 2936 (-СН); 1713 (-СОО-); 1635 (R2C=N-O-R'); 1539 (-НС=СН-, аромат.); 1409 (-C=N-); 1253 (-C-N- амид III); 1187 (=C-F).
Пример 2. Синтез O-((2-фторфенил)акрилоил)оксим 3,4,6,7,8,9-гексагидродибен-зо[b,d]фуран-1-(2H)-она (MBS-7).
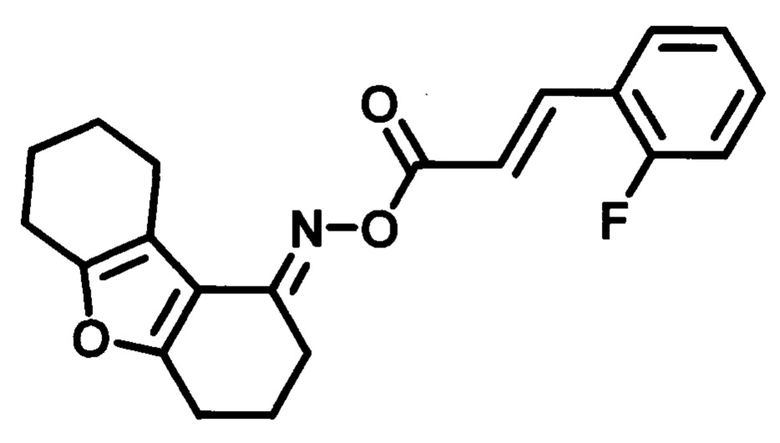
Получают в соответствии с примером 1 (пункт в) из хлорангидрида 2-фторкоричной кислоты и оксима 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она. Белые кристаллы, m=1,35 г. Выход 76%. Т. пл. 149-151°С. Rƒ=0.52 (гексан-этилацетат 3:1). Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Гц): 1.77-1.83 (м., 4Н, СН2-7,8); 2.02 (м., 2Н, СН2-3); 2.58 (м., 2Н, СН2-9); 2.72-2.76 (м., 4Н, СН2-2,4); 2.82 (д.т., J1=6.3, J2=12.7, 2Н, СН2-6); 6.77 (д., J=16.2, 1Н,=СН-СО); 7.19 (м., 2Н, CHAr-5',6'); 7.38 (м., 1Н, CHAr-4'); 7.57 (т., J=7.5, 1Н, CHAr-3'); 7.92 (д., J=16.2, 1H, Ar-СН=). Спектр ЯМР 13С (CDCl3, δ, м.д.): 164.96 (С=O), 160.63 (Cr-F), 157.76 (С4а), 150.65 (C=N), 138.14 (С5а), 131.87 (Ar-CH=), 129.44 (Or), 128.00 (С6-), 124.51 (С5'), 122.62 (С1'), 116.37 (СН-СОО), 116.08 (С3'), 115.13 (С9а), 114.11 (C9b), 24.14/23.02/22.88/22.80/22.67/21.88 (С2, С4, С3, С6-С9). ИК спектр (KBr, см-1): 3282 (R2C=N-O-R'); 2931 (-СН); 1713 (-СОО-); 1653 (R2C=N-O-R'); 1539 (-НС=СН-, аромат.); 1408 (-C=N-); 1250 (-C-N- амид III); 1186 (=C-F).
Пример 3. Синтез O-((3-фторфенил)акрилоил)оксим 3,4,6,7,8,9-гексагидродибен-зо[b,d]фуран-1-(2H)-она (MBS-8).
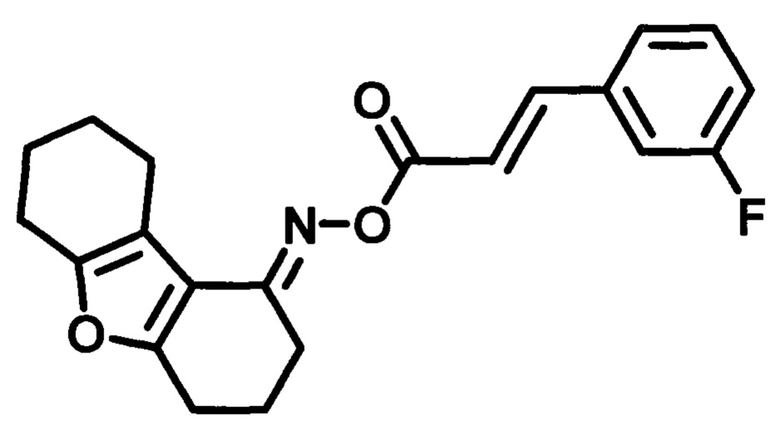
Получают в соответствии с примером 1 (пункт в) изхлорангидрида 3-фторкоричной кислоты и оксима 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она. Кремовые кристаллы, m=1,53 г. Выход 87%. Т. пл. 141-142°С. Rƒ=0.53 (гексан-этилацетат 3:1). Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Гц): 1.77-1.83 (м., 4Н, СН2-7,8); 2.02 (м., 2Н, СН2-3); 2.58 (м., 2Н, СН2-9); 2.72-2.76 (м., 4Н, СН2-2,4); 2.82 (д.т., J1=6.7, J2=12.9, 2Н, СН2-6); 6.64 (д., J=16.0, 1Н, =СН-СО); 7.08-7.14 (м., 1Н, CHAr-6'); 7.26-7.43 (м., 3Н, CHAr-2',4',5); 7.76, 7.85 (два д., J;=16, J2=16, 1Н, Ar-СН=). Спектр ЯМР 13С (CDCl3, δ, м.д.): 164,78 (С=O), 161.38 (С3'-F), 157.84 (С4а), 150.75 (C=N), 144.07 (C4'), 136.76 (Ar-СН=), 130.55 (С1'), 124.27 (С5'), 117.62 (С6'), 117.15 (СН-СОО), 115.12 (С5а), 114.45 (С9а), 114.16 (С2'), 114.07 (C9b), 24.19/23.04/22.87/22.79/22.70/21.90 (С2, С4, С3, С6-С9). ИК спектр (KBr, см-1): 3285 (R2C=N-O-R'); 2935 (-СН); 1713 (-СОО-); 1653 (R2C=N-O-R'); 1539 (-НС=СН-, аромат.); 1408 (-C=N-); 1254 (-C-N-, амид III); 1186 (=C-F-).
Пример 4. Синтез O-((3-хлорфенил)акрилоил)оксим 3,4,6,7,8,9-гексагидродибен-зо[b,d]фуран-1-(2H)-она (MBS-9).
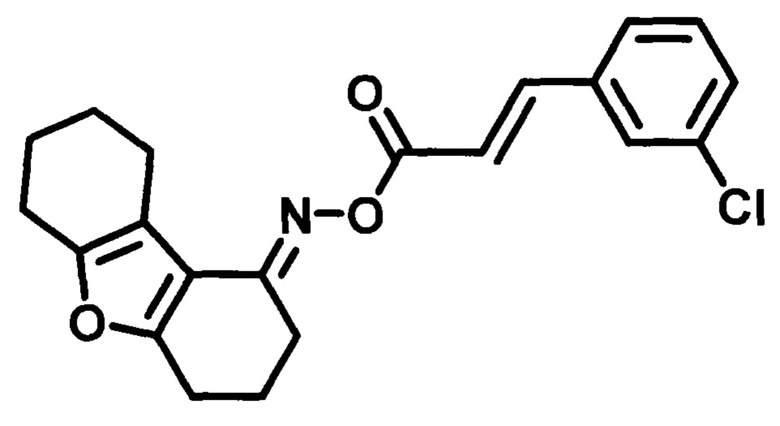
Получают в соответствии с примером 1 (пункт в) из хлорангидрида 3-хлоркоричной кислоты и оксима 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она. Белые кристаллы, m=1,4 г. Выход 76%. Т. пл. 136-137°С. Rƒ=0.56 (гексан-этилацетат 3:1). Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Гц): 1.75-1.83 (м., 4Н, СН2-7,8); 2.02 (м., 2Н, СН2-3); 2.58 (м., 2Н, СН2-9); 2.72-2.76 (м., 4Н, СН2-2,4); 2.81 (д.т., J1=6.7, J2=12.8, 2Н, СН2-6); 6.66 (д., J=16.0, 1Н,=СН-СО); 7.37-7.43 (м., 3Н, CHAr-4',5',6'); 7.57 (с, 1Н, CHAr-2'); 7.74 (д., J=16.0, 1H, Ar-СН=). Спектр ЯМР 13С (CDCl3, δ, м.д.): 164.74 (С=O), 160.78 (С3'-С1), 157.84 (С4а), 150.75 (C=N), 143.81 (Ar-СН=), 136.29 (С1'), 134.95 (С5а), 130.27 (С5'), 130.18 (С4'), 127.7 (С6'), 126.45 (С2'), 117.71 (СН-СОО), 115.11 (С9а), 114.08 (C9b), 24.18/23.04/22.87/22.79/22.68/21.89 (С2, С4, С3, С6-С9). ИК спектр (KBr, см-1): 3291 (R2C=N-O-R'); 2936 (-СН); 1713 (-СОО-); 1653 (R2C=N-O-R'); 1539 (-НС=СН-, аромат.); 1436 (-C=N-); 1253 (-C-N- амид III); 1187 (=С-Cl-).
Пример 5. Синтез O-((4-бромфенил)акрилоил)оксим 3,4,6,7,8,9-гексагидродибен-зо[b,d]фуран-1-(2H)-она (MBS-28).
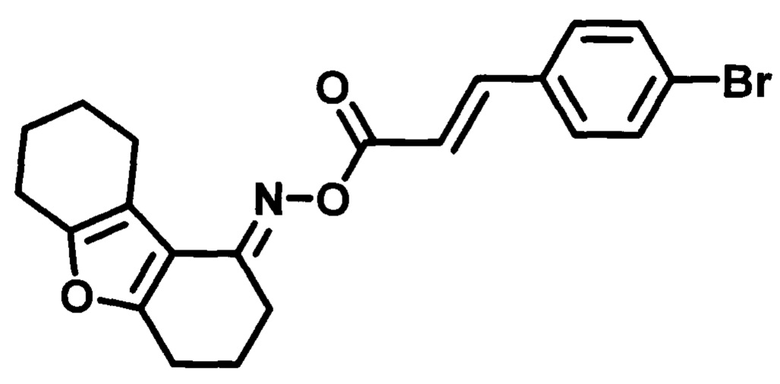
Получают в соответствии с примером 1 (пункт в) из хлорангидрида 4-бромкоричной кислоты и оксима 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она. Кремовые кристаллы, m=1,9 г. Выход 92%. Т. пл. 161-163°С. Rƒ=0.22 (гексан-этилацетат 3:1). Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Гц): 1.72-1.88 (м., 4Н, СН2-7,8); 2.02 (м., 2Н, СН2-3); 2.58 (м., 2Н, СН2-9); 2.72-2.76 (м., 4Н, СН2-2,4); 2.81 (д.т., J1=6.8, J2=13.0, 2Н, СН2-6); 6.52, 6.63 (два д., J=16.0, 1H,=СН-СО-); 7.42-7.45 (м., 2Н, CHAr-3',5'); 7.54-7.57 (м., 2Н, CHAr-2',6'); 7.77 (д., J=16.0, 1H, Ar-СН=). Спектр ЯМР 13С (CDCl3, δ, м.д.): 164.77 (С=O), 160.66 (С4а), 157.76 (С5а), 150.68 (C=N), 143.99 (Ar-СН=), 133.39 (С1'), 133.39 (С3',5'), 129.52 (С2',6'), 124.65 (С4'-Br), 116.93 (СН-С=O), 115.10 (С9а), 114.09 (C9b), 24.15/23.02/22.88/22.80/22.68/21.88 (С2, С4, С3, С6-С9). ИК спектр (KBr, см-1): 3443 (R2C=N-O-R'); 2934 (-СН); 1757 (-СОО-); 1737 (R2C=N-O-R'); 1638, 1601 (-НС=СН-, аромат.); 1455 (-C=N-); 1275(-C-N-амид III); 1187(-СН-); 1144(=С-Br-).
Пример 6. Синтез O-((4-хлорфенил)акрилоил)оксим 3,4,6,7,8,9-гексагидродибен-зо[b,d]фуран-1-(2H)-она (ГИЖ-348).
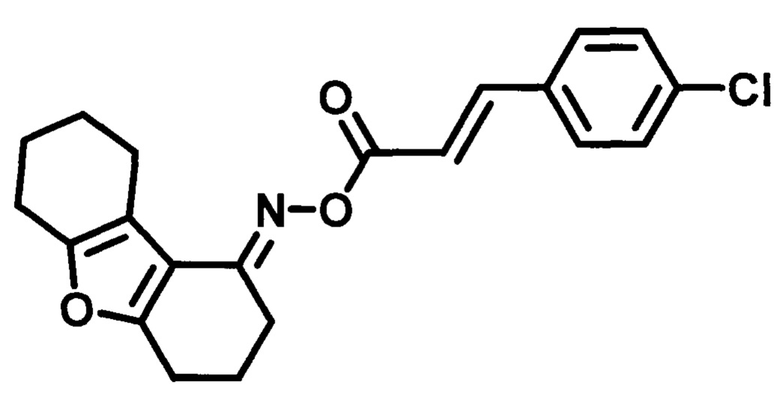
Получают в соответствии с примером 1 (пункт в) изхлорангидрида4-хлоркоричной кислоты и оксима 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она. Белые кристаллы, m=1,04 г. Выход 54%. Т. пл. 158-159°С. Rƒ=0,85 (гексан-этилацетат 3:1). Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Гц): 1.72-1.89 (м., 4Н, СН2-7,8), 1.98-2.11 (м., 2Н, СН2-3), 2.56-2.60 (м., 2Н, СН2-9), 2.72-2.76 (м., 4Н, СН2-2,4), 2.81 (д.т., J1=6.8, J2=12.9, 2Н, СН2-6), 6.62 (д., 1Н, J=16.0, =СН-СО-), 7.37-7.41 (м., 2Н, CHAr-3',5'), 7.49-7.52 (м., 2Н, CHAr-2',6'), 7.76 (д., 1H, J=16.0, p-Cl-Ph-CH=). Спектр ЯМР 13С (CDCl3, δ, м.д.): 164.85 (С=O), 160.70 (С4а), 157.77 (С5а), 150.73 (C=N), 143.97 (Ar-СН=), 136.32 (С1'), 133.00 (С3',5'), 129.31 (С2',6'), 129.19 (С4'-Cl), 116.82 (СН-С=O), 115.19 (С9а), 114.12 (C9b), 24.17/23.04/22.88/22.80/22.67/21.89 (С2, С4, С3, С6-С9). ИК спектр (KBr, см-1): 3442 (R2C=N-O-R'); 2936 (-СН); 1736 (-СОО-); 1639, 1601 (R2C=N-O-R'); 1493 (-НС=СН-); 1327(-C=N-); 1275 (-C-N- амид III); 1145 (=С-Cl-).
Пример 7. Синтез O-((2-хлорфенил)акрилоил)оксим 3,4,6,7,8,9-гексагидродибен-зо[b,d]фуран-1-(2H)-она (ГИЖ-351).
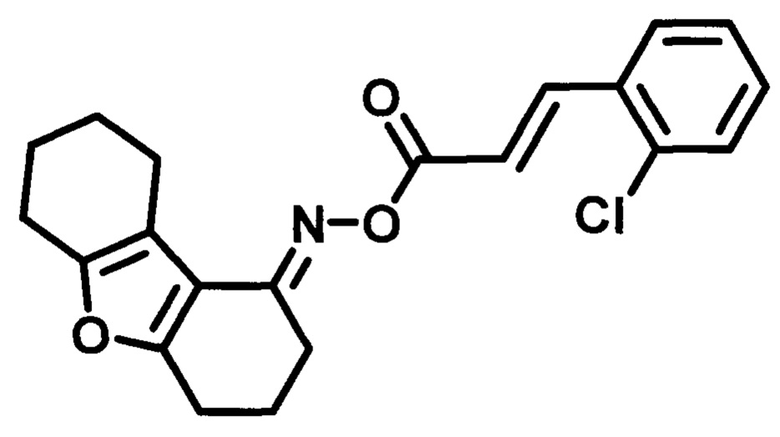
Получают в соответствии с примером 1 (пункт в) из хлорангидрида 2-хлоркоричной кислоты и оксима 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она. Бесцветные кристаллы, m=0,76 г. Выход 40%. Т. пл. 140-142°С. Rƒ=0,76 (гексан-этилацетат 3:1). Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Гц): 1.72-1.89 (м., 4Н, СН2-7,8); 1.98-2.09 (м., 2Н, СН2-3); 2.57-2.61 (м., 2Н, СН2-9); 2.72-2.76 (м., 4Н, СН2-2,4); 2.83 (д.т., J1=6.8, J2=12.94, 2Н, СН2-6); 6.65 (д., J=16.0, 1Н,=СН-СО-); 7.30-7.38 (м., 2Н, CHAr-5',6'); 7.44-7.47 (м., 1Н, CHAr-4'); 7.66-7.69 (м., 1Н, CHAr-3'); 8.22 (д., 1H, J=16.0, o-Cl-Ph-CH=). Спектр ЯМР 13С (CDCl3, δ, м.д.): 164.52 (С=O), 160.75 (С4а), 157.77 (С5а), 150.72 (C=N), 141.18 (Ar-СН=), 135.06 (С2'-С1), 132.80 (С4'), 131.13 (С6'), 130.24 (С5'), 127.72 (С1'), 127.09 (СН-СОО), 119.01 (С3'), 115.17 (С9а), 114.13 (C9b), 24.17/23.05/22.89/22.81/22.67/21.91 (С2, С4, С3, С6-С9). ИК спектр (KBr, см-1): 3453 (R2C=N-O-R'); 2947 (-СН), 1739 (-СОО-); 1638, 1606 (R2C=N-O-R'); 1470, 1443 (-НС=СН-); 1311 (-C=N-); 1267 (-C-N- амид III); 1187 (-СН-); 1137 (=С-Cl-).
Пример 8. Синтез O-((3,4-дихлорфенил)акрилоил)оксим 3,4,6,7,8,9-гексагидроди-бензо[b,d]фуран-1-(2H)-она(ГИЖ-352).
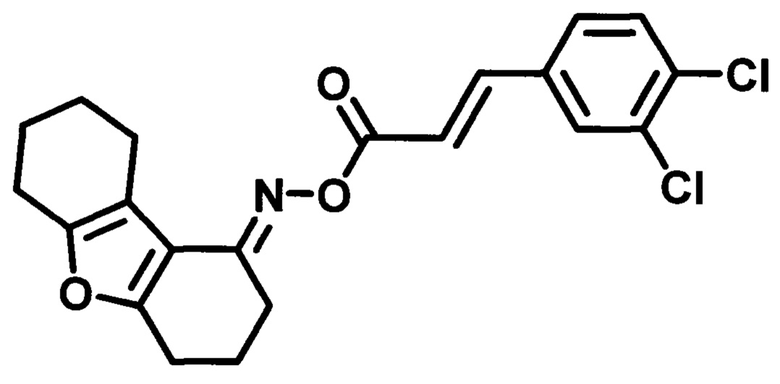
Получают в соответствии с примером 1 (пункт в) из хлорангидрида 3,4-дихлоркоричной кислоты и оксима 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она. Бесцветные кристаллы, m=1 г. Выход 48%). Т. пл. 159-162°С. Rƒ=0,83 (гексан-этилацетат 3:1). Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Гц): 1.72-1.89 (м., 4Н, СН2-7,8); 1.98-2.11 (м., 2Н, СН2-3); 2.56-2.60 (м, 2Н, СН2-9); 2.71-2.76 (м, 4Н, СН2-2,4); 2.81 (д.т., J1=6.8, J2=12.9, 2Н, СН2-6); 6.64 (д, J=16.0, 1Н,=CH-CO-); 7.37-7.41 (1H, м., CHAr-2'); 7.50 (1Н, J=8.4, д., CHAr-5'); 7.66 (с, 1Н, CHAr-6'); 7.70 (д., J=16.4, 1Н, o-Cl-Ph-CH=). Спектр ЯМР 13С (CDCl3, δ, м.д.): 164.51 (С=O), 160.79 (С4а), 157.85 (С5а), 150.79 (C=N), 142.61 (Ar-СН=), 134.55 (С3'-Cl), 134.32 (С4'-Cl), 133.30 (С6'), 130.92 (С5'), 129.60 (С1'), 127.18 (СН-СОО), 118.18 (С3'-Ar), 115.10 (С9а), 114.06 (C9b), 24.18/23.03/22.87/22.79/22.68/21.88 (С2, С4, С3, С6-С9). ИК спектр (KBr, см-1): 3450 (R2C=N-O-R'); 2934 (-СН), 1740(-СОО-), 1642, 1604 (R2C=N-O-R'), 1473 (-НС=СН-), 1308 (-C=N-), 1258 (-C-N- амид III), 1200 (-СН-), 1129 (=С-Cl-).
Пример 9. Синтез O-((3,4-диметоксифенил)акрилоил)оксим 3,4,6,7,8,9-гексагидро-дибензо[b,d]фуран-1-(2H)-она (MBS-30).
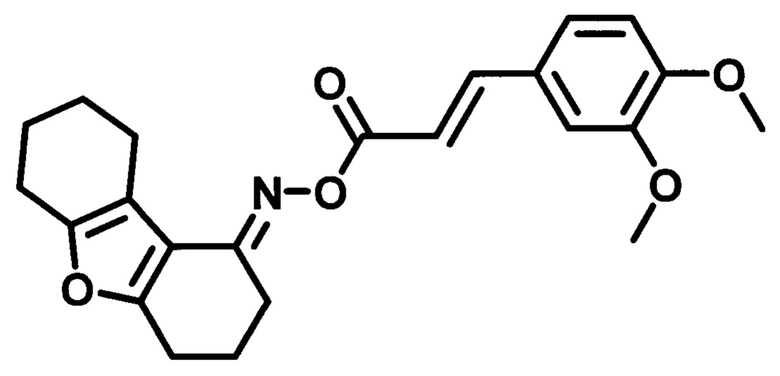
Получают в соответствии с примером 1 (пункт в) из хлорангидрида 3,4-диметоксикоричной кислоты и оксима 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она. Кремовый порошок, m=1,4 г. Выход 71%. Т. пл. 143-145°С. Rƒ=0,14 (гексан-этилацетат 3:1). Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Гц): 1.73-1.86 (м, 4Н, СН2-7,8); 1.97-2.05 (м, 2Н, СН2-3); 2.57-2.59 (м, 2Н, СН2-9); 2.72-2.76 (м., 4Н, СН2-2,4); 2.82 (д.т., J1=6.6, J2=12.9, 2Н, СН2-6); 3.93 (с, 3Н, СН3-О); 3.94 (с, 3Н, СН3-O); 6.55 (д., J=15.9, 1Н,=СН-СО-); 6.88 (д., J=8.2, 1Н, CHAr-5'); 7.11 (с, 1Н, CHAr-2'); 7.15 (д., J=8.2, 1H, CHAr-6'); 7.76 (д., J=15.9, 1H, Ar-СН=). Спектр ЯМР13С (CDCl3, δ, м.д.): 165.49 (С=O), 160.28 (С4а), 157.6 (С5а), 151.25 (C=N), 150.61 (С4'), 149.19 (С3'), 145.44 (Ar-СН=), 127.46 (С1'), 122.86 (С6'), 115.04 (СН-СОО), 114.13 (С9а), 113.6 (C9b), 111.03 (С2'), 109.56 (С5'), 55.82 (3,4-ОМе), 24.11/23.00/22.87/22.77/22.66/21.86 (С2, С4, С3, С6-С9). ИК спектр (KBr, см-1): 3454 (R2C=N-O-R'); 2933 (-СН); 1738 (-СОО-); 1635, 1583 (R2C=N-O-R'); 1514 (-НС=СН-), 1465 (-C=N-), 1359- (-C-N- амид III), 1264 (R-O-R'), 1129 (R-O-C-O-R').
Пример 10. Синтез O-((3,4-метилендиоксифенил)акрилоил)оксим 3,4,6,7,8,9-гекса-гидродибензо[b,d]фуран-1-(2H)-она (SD-16).
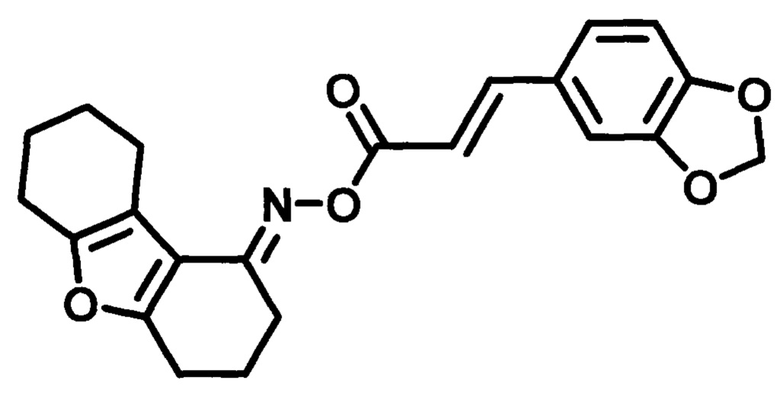
Получают в соответствии с примером 1 (пункт в) из хлорангидрида транс-3,4-метилендиоксикоричной кислоты и оксима 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она. Серо-коричневый порошок, m=1,06 г. Выход 60%. Т. пл. 157-158°С. Rƒ=0,64 (гексан-этилацетат 3:1). Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Гц): 1,74-1,84 (м, 4Н, СН2-7,8); 2,01 (м, 2Н, СН2-3); 2,57 (м, 2Н, СН2-9); 2,73 (м, 4Н, СН2-2,4); 2,81 (д.т., J1=6.6, J2=12.9, 2Н, СН2-6); 6,03 (с, 2Н, CH2O2); 6,47 (д, J=16, 1H, СН-С=O); 6,83 (д, J=8, 1Н, CHAr-5'); 7,08 (м, 2Н, CHAr-2',6'); 7,71 (д, J=16, 1Н, Ar-СН=). Спектр ЯМР13С (CDCl3, δ, м.д.): 165.34 (С=O), 160.43 (С4а), 157.64 (С5а), 150.64 (C=N), 149.75 (С4'), 148.38 (С3'), 145.19 (Ar-СН=), 128.94 (С1'), 124.65 (С6'), 115.14 (СН-СОО), 114.18 (С9а), 113.99 (C9b), 108.55 (С5'), 106.48 (С2'), 101.2 (С-диокс), 24.14/23.03/22.88/22.80/22.68/21.89 (С2, С4, С3, С6-С9). ИК спектр (KBr, см-1): 3449 (R2C=N-O-R'); 2933 (-СН); 1735 (-СОО-); 1604 (R2C=N-O-R'); 1448 (-НС=СН-); 1259 (-C=N-); 1199 (-C-N-, амид III); 1121 (С-О-С, R-O-R', -СОО-).
Пример 11. Синтез O-((4-метилфенил)акрилоил)оксим 3,4,6,7,8,9-гексагидродибен-зо[b,d]фуран-1-(2H)-она (SD-17).
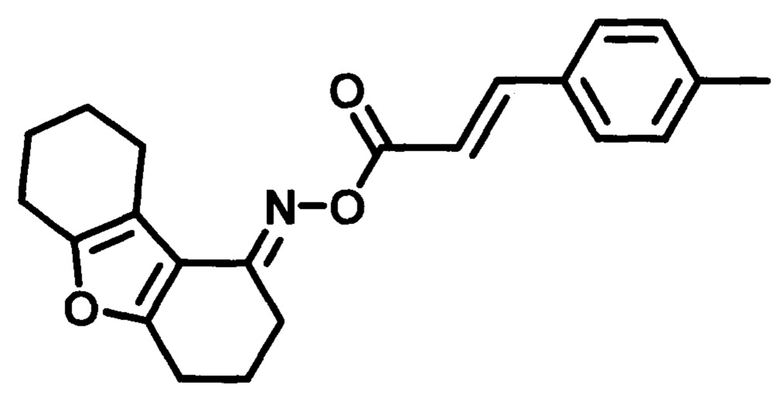
Получают в соответствии с примером 1 (пункт в) из хлорангидрида 4-метилкоричной кислоты и оксима 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она. Бесцветные кристаллы, m=1,27 г. Выход 80%. Т. пл. 131-132°С. Rƒ=0,75 (гексан-этилацетат 3:1). Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Гц): 1.75-1.86 (м, 4Н, СН2-7,8); 1.98-2.04 (м, 2Н, СН2-3); 2.41 (с, 3Н, р-Ме); 2.58 (м, 2Н, СН2-9); 2.72-2.76 (м, 4Н, СН2-2,4); 2.82 (д.т., J1=6.6, J2=12.9, 2Н, СН2-6); 6.61 (д, J=15.9, 1Н, СН-С=O); 7.22 (д, J=8, 2Н, CHAr-3',5'); 7.48 (д, J=8.1, 2Н, CHAr-2',6'); 7.79 (д, J=16.0, 1Н, Ar-СН). Спектр ЯМР13С (CDCl3, δ, м.д.): 165.34 (С=O), 160.51 (С4а), 157.66 (С5а), 150.64 (C=N), 145.52 (Ar-СН=), 140.89 (С4'), 131.79 (С1'), 129.65 (С3',5'), 128.17 (С2',6'), 115.17 (СН-СОО), 115.03 (С9а), 114.2 (C9b), 24.17/23.05/22.90/22.81/22.69/21.90/21.50 (С2, С4, С3, С6-С9, р-Ме). ИК спектр (KBr, см-1): 3445 (R2C=N-O-R'); 2927 (-СН); 1740, 1721 (-СОО-); 1639, 1606 (R2C=N-O-R'); 1443 (-НС=СН-); 1264 (-C=N-); 1186 (-C-N-, амид III); 1132 (С-О-С, R-O-R', -СОО-).
Пример 12. Синтез O-((4-метоксифенил)акрилоил)оксим 3,4,6,7,8,9-гексагидродибен-зо[b,d]фуран-1-(2H)-она (SD-18).
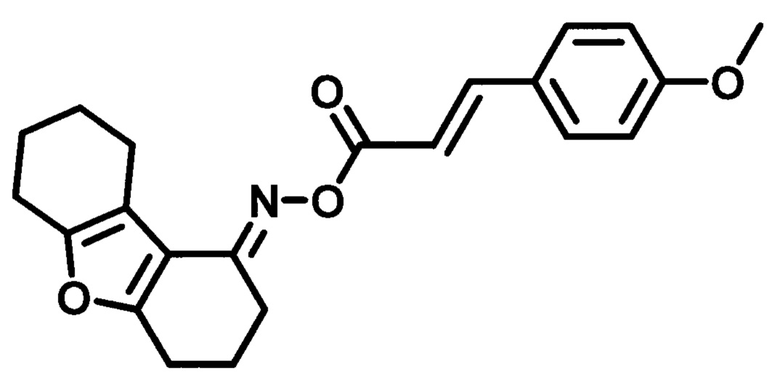
Получают в соответствии с примером 1 (пункт в) из хлорангидрида 4-метоксикоричной кислоты и оксима 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она. Желтый порошок, m=1,2 г. Выход 71%. Т. пл. 160-161°С. Rƒ=0,60 (гексан-этилацетат 3:1). Спектр ЯМР 1H (CDCl3, δ, м.д., J/Гц): 1.76-1.82 (м, 4Н, СН2-7,8), 2.01 (м, 2Н, СН2-3), 2.58 (м, 2Н, СН2-9), 2.73 (м, 4Н, СН2-2,4), 2.81 (д.т., J1=6.6, J2=12.9, 2Н, СН2-6), 3.85 (с, 3H, p-MeO), 6.52 (д, J=16.0, 1Н, СН-С=O), 6.93 (д, J=8.8, 2Н, CHAr-2',6'), 7.53 (д, J=8.8, 2Н, CHAr-3',5'), 7.75 (д, J=15.9, 1Н, Ar-СН). Спектр ЯМР13С (CDCl3, δ, м.д.): 165.51 (С=O), 161.51 (С4'), 160.40 (С4а), 157.61 (С5а), 150.63 (C=N), 145.19 (Ar-СН=), 129.85 (С2',6'), 127.26 (С1'), 115.16 (СН-С=O), 114.35 (С3',5'), 114.22 (С9а), 113.53 (C9b), 55.40 (р-МеО), 24.16/23.04/22.90/22.81/22.69/21.90 (С2, С4, С3, С6-С9). ИК спектр (KBr, см-1): 3448 (R2C=N-O-R'); 2990 (-СН); 1740 (-СОО-); 1603 (R2C=N-O-R'); 1510 (С-Н); -1309 (-НС=СН-); 1303 (-C=N-); 1207 (-C-N-, амид III); 1124 (С-О-С, R-O-R', -СОО-).
Пример 13. Синтез O-((3,4,5-триметоксифенил)акрилоил)оксим 3,4,6,7,8,9-гексагид-родибензо[b,d]фуран-1-(2H)-она (SD-19).
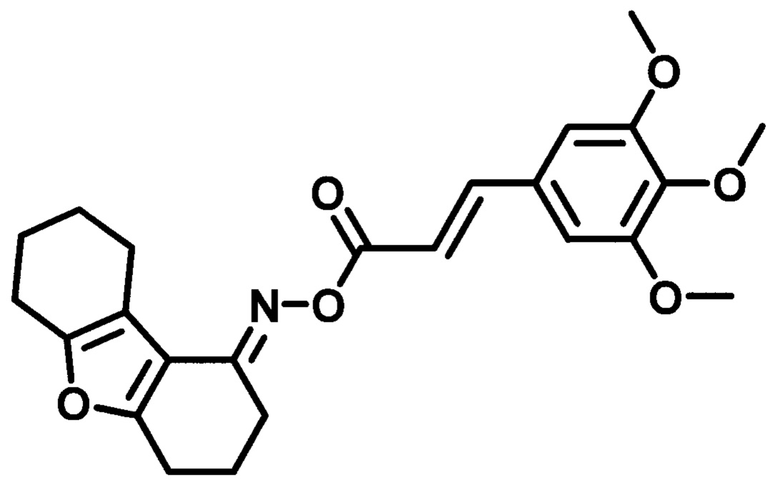
Получают в соответствии с примером 1 (пункт в) из хлорангидрида 3,4,5-триметоксикоричной кислоты и оксима 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она. Желтый порошок, m=1,73 г. Выход 80%. Т. пл. 143-145°С. Rƒ=0,25 (гексан-этилацетат 3:1). Спектр ЯМР lH (CDCl3, δ, м.д., J/Гц): 1.74-1.82 (м, 4Н, СН2-7,8); 1.99 (м, 2Н, СН2-3); 2.56 (м, 2Н, СН2-9); 2.72 (м, 4Н, СН2-2,4); 2.81 (д.т., J1=6.6, J2=12.9, 2Н, СН2-6); 3.90 (с, 9Н, 3,4,5-МеО); 6.62 (д, J=16.0, 1H, СН-С=O); 6.79 (с, 2Н, CHAr-2',6'); 7.20 (д, J=15.9, 1Н, Ar-СН). Спектр ЯМР 13С (CDCl3, δ, м.д.): 165.24 (С=O), 160.43 (С4а), 157.73 (С5а), 153.0 (C3',5'), 150.68 (С4'), 145.49 (Ar-СН=), 140.21 (С4'), 129.98 (С1'), 115.27 (СН-С=O), 115.04 (С9а), 114.10 (C9b), 105.28 (С2',6'), 60.97 (р-МеО), 58.38 (3,5-МеО), 24.16/23.25/23.03/22.88/22.68/21.88 (С2, С4, С3, С6-С9). ИК спектр (KBr, см-1): 3450 (R2C=N-O-R'); 2939 (-СН); 1717(-СОО-); 1582 (R2C=N-O-R'), 1505 (-НС=СН-), 1320 (-C=N-), 1276 (-C-N-, амид III), 1128 (С-О-С, R-O-R', -СОО-).
Пример 14. Синтез O-((4-трифторметилфенил)акрилоил)оксим 3,4,6,7,8,9-гексагид-родибензо[b,d]фуран-1-(2H)-она (SD-20).
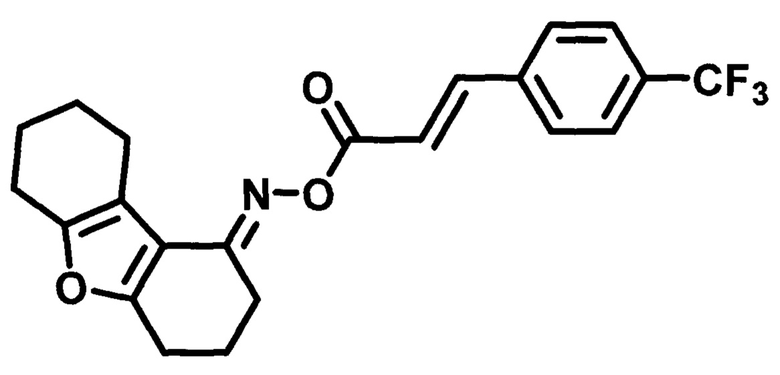
Получают в соответствии с примером 1 (пункт в) из хлорангидрида 4-трифторметилкоричной кислоты и оксима 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она. Кремовые кристаллы, m=1,13 г. Выход 60%. Т. пл. 138-139°С. Rƒ=0,67 (гексан-этилацетат 3:1). Спектр ЯМР 1Н (CDCl3, δ, м.д., J/Гц): 1.77-1.83 (м, 4Н, СН2-7,8), 2.02 (м, 2Н, СН2-3), 2.58 (м, 2Н, СН2-9), 2.74 (м, 4Н, СН2-2,4), 2.82 (д.т., J1=6.6, J2=12.9, 2Н, СН2-6), 6.72 (д, J=16.1, 1Н, СН-С=O), 7.67 (с, 4Н, СН-2,3,5,6), 7.82 (д, J=16.0, 1Н, Ar-СН). Спектр ЯМР13С (CDCl3, δ, м.д.): 164.54 (С=O), 160.91 (С4а), 157.89 (С5а), 143.53 (Ar-СН=), 137.84 (С4'), 128.27 (С2',3',5',6'), 125.91 (С1'), 118.84 (-CF3), 115.09 (С9а), 114.04 (C9b), 24.19/23.02/22.87/22.78/22.67/21.88 (С2, С4, С3, С6-С9). ИК спектр (KBr, см-1): 3455 (R2C=N-O-R'); 2940 (-СН); 1740 (-СОО-); 1640, 1602 (R2C=N-O-R'); 1445 (-НС=СН-); 1323 (-C=N-); 1285(C-F); 1242(-C-N- амид III); 1139 (С-О-С, R-O-R', -COO-).
Экспериментальная фармакологическая часть
Организация и проведение работ осуществлялись в соответствии с приказом Минздрава России №199 от 01 апреля 2016 года «Об утверждении правил надлежащей лабораторной практики». Животные содержались в соответствии с СП 2.2.1.3218-14 «Санитарно-эпидемиологические требования к устройству, оборудованию и содержанию экспериментально-биологических клиник (вивариев)» от 29 августа 2014 г. №51. Проведение экспериментов одобрено Комиссией по биомедицинской этике ФГБНУ «НИИ фармакологии имени В.В. Закусова».
Эксперименты проводили на белых беспородных мышах-самцах, массой 22-26 г, полученных из питомника «Столбовая» ГУ НЦБМТ (Московская область).
Статистическую обработку результатов проводили с помощью MS Excel 2010 и BioStat 2009 (Analyst Soft Inc.). Нормальность распределения данных определяли по критерию Шапиро-Уилка. Достоверность различий значений между группами определяли с помощью непараметрических критериев: Крускала-Уолиса и точного критерия Фишера.
Пример 15. Противосудорожное действие производных оксима дибензофуранона на модели первично-генерализованных судорог, вызванных максимальным электрошоком (МЭШ)
Противосудорожное действие производных оксима дибензофуранона исследовали на моделях первично-генерализованных судорог, вызванных максимальным электрошоком (МЭШ), моделирующим так называемые «большие» (Grandmal) судорожные припадки [Т.А. Воронина, Л.Н. Неробкова, Методические указания по изучению противосудорожной активности фармакологических веществ. «Руководство по проведению доклинических исследований лекарственных средств» Часть. 1. ФГБУ «НЦЭМСП»., Гриф и К, Москва (2012), сс. 235-250; W. Löscher, С.Р. Fassbender, В. Nolting, EpilepsyRes., 8(2), 79-94 (1991); Е.А. Swinyard, Epilepsia, 10, 107-119(1969).].
Электросудорожный припадок (МЭШ) создавали с использованием сертифицированной установки «Rodent Shocker RS», type 221 (Harvard Apparatus, GmbH, Германия). Животные через специальные корнеальные электроды получали электрические стимулы (режим 1: 250 V, 11 mA, длительность 0,2 с; режим 2: 250 V, 11 mA, длительность 0,3 с; режим 3: 250 V, 12 mA, длительность 0,3 с; режим 4: 250 V, 9 mA, длительность 0,3 с; режим 5: 250 V, 10 mA, длительность 0,3 с). Регистрировали следующие показатели: клонические судороги, тоническую экстензию задних и передних конечностей и гибель животных. Противосудорожный эффект заявляемых соединений оценивали по способности предотвращать гибель животных, по способности предотвращать тоническую экстензию относительно соответствующих контрольных групп, а также по балльной шкале: 0 баллов - нет судорожных реакций, 1 балл - клонические судороги без потери рефлекса переворачивания, 2 балла - клонические судороги с потерей рефлекса переворачивания, 3 балла - тонические судороги, 4 балла - тонические судороги заканчивающиеся гибелью животного. Исследуемые соединения растворяли в физиологическом растворе с Твин 80 и вводили внутрибрюшино (в/б) за 40 минут до проведения МЭШ. Препарат сравнения вальпроевая кислота (субстанция, Sigma) растворяли в физиологическом растворе и вводили в дозе 150-200 мг/кг в аналогичном режиме. Животным контрольных групп вводился физиологический раствор.
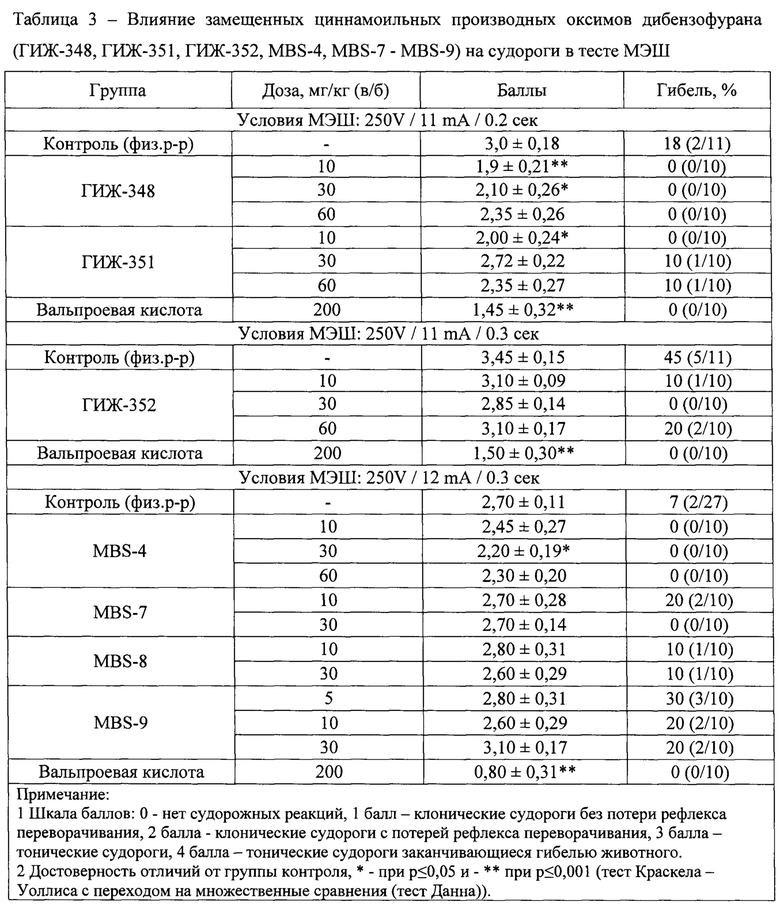
Результаты оценки влияния замещенных циннамоильных производных оксимов дибензофурана ГИЖ-348, ГИЖ-351, ГИЖ-352, MBS-4, MBS-7 - MBS-9 на судороги в тесте МЭШ представлены в таблице 3, а соединений MBS-28, MBS-30, SD-16 - SD-20 - в таблице 4.
Установлено, что в тесте МЭШ соединение ГИЖ-348 в дозе 10 мг/кг достоверно уменьшало тяжесть судорожных проявлений до 1,9 баллов, а в дозе 30 мг/кг - до 2,1 баллов, в то время как в дозе 60 мг/кг противоэпилептический эффект наблюдался лишь на уровне тенденции. При этом во всех исследованных дозах соединение ГИЖ-348 полностью предотвращало гибель животных на фоне применения максимального электрошока.
Соединение ГИЖ-351 (10 мг/кг) достоверно уменьшало тяжесть судорожных проявлений до 2 баллов, предотвращая тоническую фазу, относительно контрольных значений, тяжесть судорожных проявлений которых составила 3 балла. В этой дозе соединения ГИЖ-351 полностью предотвращало гибель животных. В остальных дозах (30 и 60 мг/кг) соединение не защищало от развития судорожных реакций, при этом в обеих группах регистрировалась гибель одного животного (таблица 3).
Соединение ГИЖ-352 не проявило какого-либо эффекта ни в одной из исследуемых доз - 10, 30 и 60 мг/кг. Можно отметить лишь тот факт, что в дозе 30 мг/кг на фоне приема соединения ГИЖ-352 не было зарегистрировано гибели животных, в то время, как в контрольной группе погибло 45% мышей.
Пара-фтор-замещенное соединение MBS-4 в дозе 30 мг/кг в тесте МЭШ умеренно, но статистически достоверно, уменьшало тяжесть судорожных проявлений до 2,2 баллов относительно контрольных значений, которые в сумме на группу составили 2,7 балла. В дозах 10 и 30 мг/кг противосудорожный эффект соединения исчезал. Кроме того, на фоне приема соединения MBS-4 не наблюдалось ни одной гибели животных (таблица 3).
Соединения MBS-7, MBS-8 и MBS-9 не защищали от развития МЭШ-индуцированных судорожных реакций ни в одной из исследуемых доз.
3,4-Диметоксипроизводное MBS-30 в дозе 10 мг/кг умеренно, но статистически достоверно, уменьшало тяжесть судорожных проявлений, вызванных МЭШ, относительно контрольных значений. При увеличении дозы в 3 и 6 раз противосудорожный эффект соединения не проявлялся. В дозах 5, 10 и 30 мг/кг на фоне приема MBS-30 не наблюдалось гибели животных и животных с тонической экстензией (таблица 4).
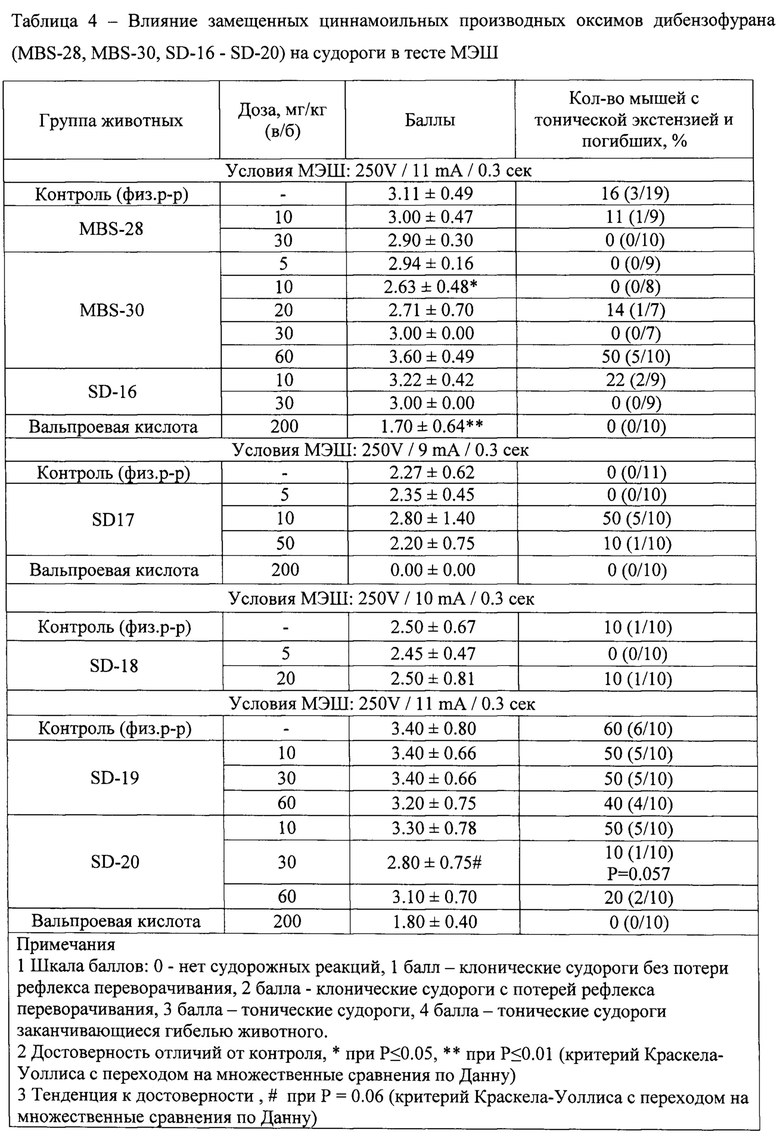
Соединения MBS-28 и SD-16 в дозах 10 и 30 мг/кг не оказывали влияние на судороги мышей в тесте МЭШ, хотя в дозах 30 м/кг на фоне их приема не наблюдалось гибели животных и животных с тонической экстензией, в то время как в контрольной группе таких животных было 16%.
Среди соединений SD-17 - SD-20 только SD-20 в дозе 30 мг/кг проявляло противосудорожную активность по показателям снижения выраженности судорожных реакций и гибели животных после тонической экстензии (р=0.06).
Препарат сравнения вальпроевая кислота в дозе 200 мг/кг обладала достоверным эффектом, снижая судорожные проявления до значений от 0 до 1,8 балла при различных силах тока и полностью предотвращая гибель животных (таблица 3, 4).
Таким образом, в группе замещенных циннамоильных производных оксима дибензофуранона наиболее активными оказались соединения, содержащие в фенильном кольце атом галогена (ГИЖ-348, ГИЖ-351, MBS-4), причем предпочтительнее было его наличие в пара-положении. Пара-хлор-производное было более активным (ГИЖ-348), чем фтор-производное (MBS-4) и чем бром-производное (MBS-28). Также умеренная активность выявлялсь у веществ с 3,4-диметоксифенильной группой (MBS-30) и 4-трифторметильной группой (SD-20).
Наиболее активным по выраженности противосудорожного эффекта было соединение ГИЖ-348 в дозе 10 мг/кг.
| название | год | авторы | номер документа |
|---|---|---|---|
| АМИНОАЛКИЛЬНЫЕ ПРОИЗВОДНЫЕ ОКСИМА ДИБЕНЗОФУРАНОНА, ОБЛАДАЮЩИЕ ПРОТИВОСУДОРОЖНОЙ АКТИВНОСТЬЮ | 2020 |
|
RU2773021C2 |
| Производные оксимов дибензофуранов, обладающие противосудорожной и нейропротективной активностью | 2018 |
|
RU2744758C2 |
| ПРОИЗВОДНЫЕ 1,2,3,4-ТЕТРАГИДРОПИРИДО[4,3-b]ИНДОЛСОДЕРЖАЩИХ ФЕНОТИАЗИНОВ В КАЧЕСТВЕ ИНГИБИТОРОВ ХОЛИНЭСТЕРАЗ И БЛОКАТОРОВ СЕРОТОНИНОВЫХ РЕЦЕПТОРОВ 5-HT, СПОСОБЫ ПОЛУЧЕНИЯ ИХ ХЛОРГИДРАТОВ И ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО НА ИХ ОСНОВЕ | 2013 |
|
RU2530881C1 |
| СРЕДСТВО, УЛУЧШАЮЩЕЕ КРОВОСНАБЖЕНИЕ ИШЕМИЗИРОВАННОГО МОЗГА | 2019 |
|
RU2747202C2 |
| ГИБРИДНЫЕ СОЕДИНЕНИЯ НА ОСНОВЕ ФУРАН-2(3Н)-ОНА И ХРОМЕН-4(4Н)-ТИОНА, ОБЛАДАЮЩИЕ АНТИБАКТЕРИАЛЬНОЙ АКТИВНОСТЬЮ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2024 |
|
RU2830172C1 |
| Способ получения замещенных 3-арилпирролов | 2024 |
|
RU2831117C1 |
| СЕЛЕКТИВНЫЕ ИНГИБИТОРЫ ЦИКЛООКСИГЕНАЗЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2016 |
|
RU2631317C1 |
| Оксазолидиноны на основе производных пиридоксина, обладающие антибактериальной активностью | 2024 |
|
RU2836570C1 |
| 5-АМИНО-3-(МОРФОЛИН-4-КАРБОНИЛ)-1-(2-ОКСО-2-(4-ФТОРФЕНИЛ)ЭТИЛИДЕН)-6,7,8,9-ТЕТРАГИДРОБЕНЗО[4,5]ТИЕНО[3,2-Е]ПИРРОЛО[1,2-А]ПИРИМИДИН-2(1H)-ОН, ОБЛАДАЮЩИЙ ПРОТИВОВОСПАЛИТЕЛЬНОЙ АКТИВНОСТЬЮ | 2024 |
|
RU2831363C1 |
| 1-АМИНО-1,6-ДИОКСО-6-(П-ТОЛИЛ)-2-ЦИАНО-4-((3-ЦИАНО-4,5,6,7-ТЕТРАГИДРОБЕНЗО[B]ТИОФЕН-2-ИЛ)АМИНО)ГЕКСА-2,4-ДИЕН-3-ОЛАТ НАТРИЯ, ОБЛАДАЮЩИЙ АНАЛЬГЕТИЧЕСКОЙ АКТИВНОСТЬЮ | 2024 |
|
RU2831124C1 |
Изобретение относится к химии биологически активных соединений, конкретно к новым замещенным O-(фенилакрилоил)оксимам 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она общей формулы (1), которые обладают противосудорожной активностью. В формуле (1) один или несколько из заместителей R1-R4 могут быть атомами галогенов, алкильными группами, алкоксигруппами, трифторметильными группами, при этом остальные заместители являются водородами; или два из заместителей R1-R4 одновременно являются -О-CH2-О-группой, при этом остальные заместители являются водородами. 6 з.п. ф-лы, 6 ил., 4 табл., 15 пр.
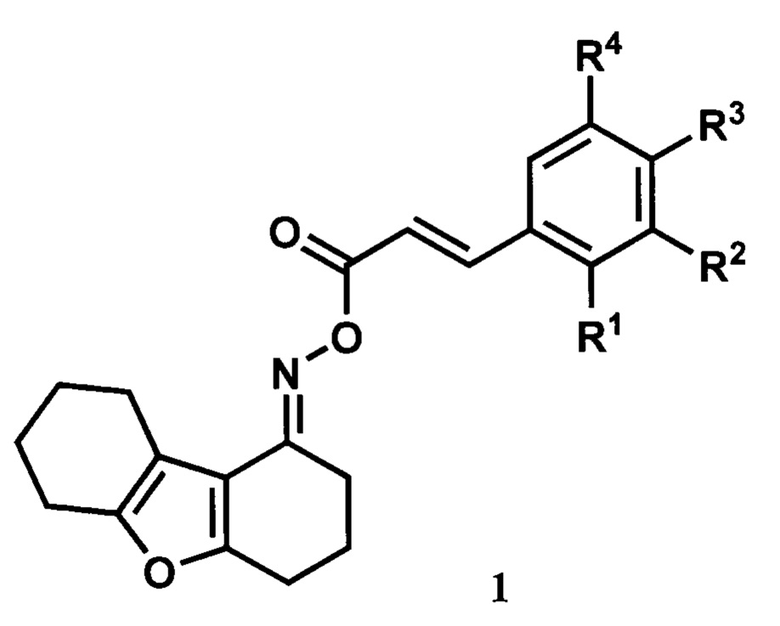
1. Замещенные O-(фенилакрилоил)оксимы 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она общей формулы (1)
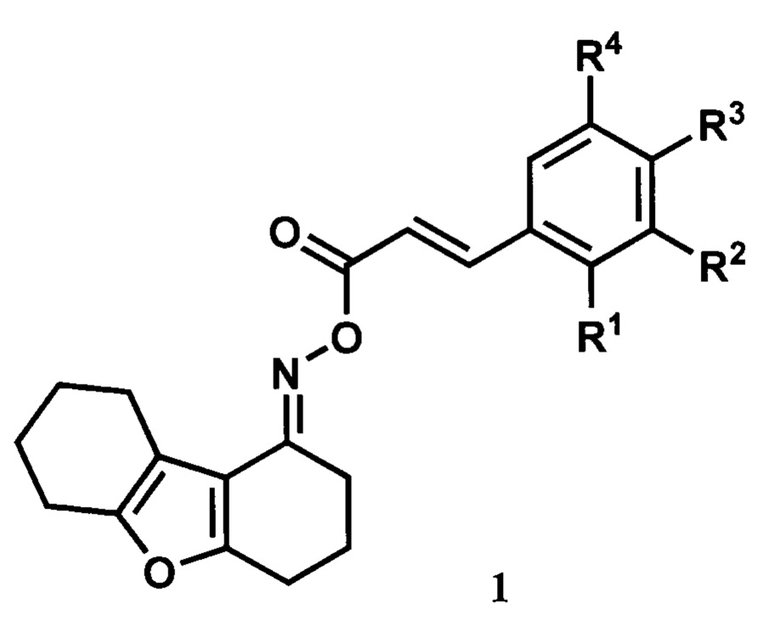 ,
,
где один или несколько из заместителей R1-R4 могут быть атомами галогенов, алкильными группами, алкоксигруппами, трифторметильными группами, при этом остальные заместители являются водородами; или где два из заместителей R1-R4 одновременно являются -О-CH2-О-группой, при этом остальные заместители являются водородами.
2. Соединение по п. 1, представляющее собой O-((4-хлорфенил)акрилоил)оксим 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она (ГИЖ-348).
3. Соединение по п. 1, представляющее собой O-((2-хлорфенил)акрилоил)оксим 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она (ГИЖ-351).
4. Соединение по п. 1, представляющее собой O-((4-фторфенил)акрилоил)оксим 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она (MBS-4).
5. Соединение по п. 1, представляющее собой O-((3,4-диметоксифенил)акрилоил)оксим 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она (MBS-30).
6. Соединение по п. 1, представляющее собой O-((4-трифторметилфенил)акрилоил)оксим 3,4,6,7,8,9-гексагидродибензо[b,d]фуран-1-(2H)-она (SD-20).
7. Соединения по пп. 2-6, обладающие противосудорожной активностью.
| Производные оксимов дибензофуранов, обладающие противосудорожной и нейропротективной активностью | 2018 |
|
RU2744758C2 |
| АМИНОАЛКИЛЬНЫЕ ПРОИЗВОДНЫЕ ОКСИМА ДИБЕНЗОФУРАНОНА, ОБЛАДАЮЩИЕ ПРОТИВОСУДОРОЖНОЙ АКТИВНОСТЬЮ | 2020 |
|
RU2773021C2 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
Авторы
Даты
2023-12-25—Публикация
2023-02-20—Подача