Область техники, к которой относится изобретение
Изобретение относится к области медицинской химии и касается производных хинолина, изохинолина или фталазина, проявляющих антагонистическую активность в отношении гонадотропин высвобождающего гормона, а также способа получения этих производных.
Уровень техники
Гонадотропин высвобождающий гормон (ГВГ) является гормоном, который синтезируется в основном в нервных клетках гипоталамуса млекопитающих, но не только в них, поступает через воротную вену гипофиза и его поступление регулируется в гонадотропных клетках. За счет взаимодействия с семью трансмембранными доменами соответствующего рецептора ГВГ стимулирует образование и высвобождение гонадотропного гормона (ГГ), которое опосредовано вторичным мессенджером - инозитол-1,4,5-трифосфатом и ионами Ca2+. Индуцированные гонадотропином, опосредованным ГВГ, лютеинизирующий гормон (ЛГ) и фолликул-стимулирующий гормон (ФСГ), в свою очередь, стимулируют образование половых стероидов и созревание половых клеток обоих полов. Кроме ГВГ (назван также ГВГ1) существуют две другие формы ГВГ, а именно ГВГ2 и 3.
Рецептор ГВГ используют в качестве фармакологической мишени в ряде заболеваний, связанных с функциональным продуцированием половых гормонов, например, рак предстательной железы, предклимактерический рак молочной железы, эндометриоз и фиброма матки. При таких заболеваниях можно эффективно использовать суперагонисты ГВГ или антагонисты ГВГ. Другой возможной областью применения таких соединений является, прежде всего, контроль репродуктивной функции у мужчин в комбинации с замещающей дозой андрогена.
Преимуществом антагонистов ГВГ по сравнению с суперагонистами является их непосредственное действие с помощью подавления секреции ГГ. Суперагонисты в основном действуют за счет суперстимуляции гипофиза, что приводит к повышенному высвобождению ГГ и половых стероидов. Такая гормональная реакция завершается в первую очередь определенным замедлением по причине десенсибилизации и нарушения регуляции концентрации рецептора ГВГ. Возможно поэтому суперагонисты ГВГ в отдельности или в комбинации с тестостероном не подавляют продукцию спермы у мужчин и в связи с этим не подходят для контроля репродуктивной функции у мужчин. И наоборот, пептидные антагонисты ГВГ, прежде всего, при необходимости в комбинации с замещающей дозой андрогена, вызывают значительную олигозооспермию у мужчин.
Однако пептидные антагонисты ГВГ характеризуются рядом недостатков. Так, например, они проявляют незначительное действие в качестве суперагонистов и в связи с этим их следует вводить в чрезвычайно высоких дозах. Кроме того, пероральная биодоступность таких веществ также мала, следовательно, их следует вводить с помощью инъекции. Повторные инъекции также приводят к ухудшению режима приема пациентом лекарства. Более того, синтез пептидных антагонистов ГВГ по сравнению с непептидными соединениями является трудоемким и дорогостоящим.
Например, в заявке WO 97/14682 описаны производные хинолина в качестве непептидных антагонистов ГВГ. Однако до настоящего времени непептидные антагонисты ГВГ не выпускаются коммерческими фирмами.
Сущность изобретения
Задачей настоящего изобретения является получение новых антагонистов ГВГ, которые превосходят по свойствам известные пептидные соединения и представляют активный вариант известных непептидных соединений. Новые антагонисты ГВГ должны проявлять высокую активность, а также обладать высокой пероральной биодоступностью. Кроме того, синтез таких соединений должен быть простым и по возможности недорогостоящим.
Поставленная задача решается с помощью соединений формулы (1)
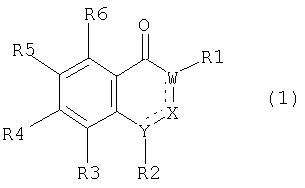
где R1
(а) означает ацилгруппу -СО-R11 или CN, где R11 означает насыщенный, ненасыщенный, циклический и/или (гетеро)ароматический органический остаток, в частности прямую или разветвленную алкильную цепь, содержащую 1-10 атомов углерода, или фенильную, фуранильную или тиофеновую группу, замещенную алкильной группой или галогеном,
(б) остаток сложного эфира карбоновой кислоты -CO-OR12 или остаток амида карбоновой кислоты -CO-NR12R13, или группу -SOx-R12, где х равно 0, 1 или 2, или -SO2-NR12R13, где R12 означает насыщенный, ненасыщенный, циклический и/или (гетеро)ароматический органический остаток, в частности прямую или разветвленную алкильную цепь, содержащую 1-10 атомов углерода, аралкильную группу, содержащую 7-20 атомов углерода, причем арильный остаток замещен алкильными группами или атомами галогена, или фенильный остаток, замещенный алкильными группами или атомами галогена, a R13 может означать атом водорода или прямую или разветвленную алкильную цепь, содержащую 1-10 атомов углерода, или
(в) группу -A-NR14-CO-NR15R16, где А означает алкиленовую группу, которая содержит 1-4 атомов углерода, в частности 1 атом углерода, замещенную C1-C6-алкильной группой, карбонильную группу, атом кислорода или группу -SOx-, где х равно 0, 1 или 2, R14 и R15 каждый независимо означает атом водорода или прямую или разветвленную алкильную цепь, содержащую 1-10 атомов углерода, a R16 означает прямую или разветвленную алкильную цепь, содержащую 1-10 атомов углерода, циклоалкильную группу, включающую 3-10 атомов углерода, циклоалкилалкильную группу, включающую 7-20 атомов углерода, аралкильную группу, включающую 7-20 атомов углерода, причем арильный остаток может быть замещен алкильными группами или атомами галогена, фенильную группу, замещенную алкильными группами или атомами галогена, или гетероциклическое кольцо, замещенное алкильными группами или атомами галогена;
R2 означает группу -CH(R21)R22, где R21 означает атом водорода, С1-С10-алкильную группу или замещенное фенильное кольцо, a R22 означает замещенные фенильное кольцо или нафтильное кольцо, или R2 означает группу -СН2СН(R23)R24, где R23 и R24 имеют значения замещенных фенильных колец;
R3 и R4 независимо означают атом водорода или алкильную группу, включающую 1-10 атомов углерода, и R3 может также означать атом галогена;
R5 означает группу, присоединенную через остаток Z
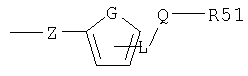
где G означает -С=С-, -C=N-, -N=C-, атом кислорода или атом серы, Z означает прямую связь, атом кислорода или атом серы, группу CH-R52 или -CHR52-CH-R53, где R52 и R53 независимо означают атомы водорода или алкильную группу, а n равно 1 и 2, тройную связь -С≡С-, или группу -CR52=CR53- или С=CR52R53 в Е- или Z-конфигурации, и где R52 и R53 независимо означают атомы водорода или алкильную группу, L означает CH2- или NH-группу, Q означает карбонил или -SOx, где х равно 0, 1 или 2, a R51 означает аминогруппу, замещенную алкильной группой, или прямую или разветвленную алкильную группу, замещенную атомами галогена, гидроксильной или алкоксигруппами, или циклоалкильную группу, содержащую 3-7 циклических атомов и замещенную атомами галогена, гидроксильной или алкоксигруппами;
R6 означает группу CH2-N(R61)R62, где R61 независимо означает атом водорода или алкильную группу, a R62 означает алкильную группу или замещенную аралкильную группу или гетероарилалкильную группу, включающую 7-20 атомов углерода, а группы
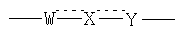
могут означать одну из групп
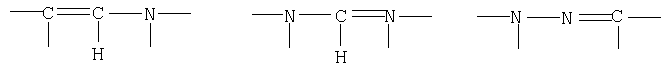
в любой ориентации, а также все стереоизомеры указанных соединений и их соли с физиологически приемлемыми кислотами или основаниями.
Заместители в соединениях формулы (1) могут, например, иметь следующие значения:
R1 означает прямую или разветвленную алкильную цепь: метил, этил, н-пропил, изо-пропил, н-, изо-, трет-бутил, н-пентил, 2,2-диметилпропил или 3-метилбутил, н-гексил, н-гептил, н-октил, н-нонил, н-децил. Предпочтительными являются метил или этил.
Фенильную группу, замещенную алкильной группой или атомом галогена: фенил-, орто-, мета-, пара-метил-, этил-, пропил-, изопропилфенил, 2,3-, 2,4-, 2,5-, 2,6-, 3,4-, 3,5-диметил- илидиэтилфенил, орто-, мета-, пара-фтор-, хлор-, бром-, иодфенил, 2,3-, 2,4-, 2,5-, 2,6- 3,4-, 3,5-дифтор-, дихлор-, дибром- или дииодфенил, или нафтил. Предпочтительной является фенильная группа.
Замещенные фурановую или тиофеновую группы: незамещенные 2- или 3-тиенил или 2- или 3-фурил или 3-метил-, 3-этил-, 3-фтор-, 3-хлор-, 3-бром-, 3-иод-2-фурил- или -2-тиенилгруппы, 4- метил-, 4-этил-, 4-фтор-, 4-хлор-, 4-бром-, 4-иод-2-фурил- или 2-тиенилгруппы, 5-метил-, 5-этил-, 5-фтор-, 5-хлор-, 5-бром-, 5-иод-2-фурил- или -2-тиенилгруппы, 2-метил-, 2-этил-, 2-фтор-, 2-хлор-, 2-бром-, 2-иод-З-фурил- или -3-тиенилгруппы, 4-метил-, 4-этил-, 4-фтор-, 4-хлор-, 4-бром-, 4-иод-3-фуранил- или -3-тиенилгруппы, 5-метил-, 5-этил-, 5-фтор-, 5-хлор-, 5-бром-, 5-иод-3-фурил- или -3-тиенилгруппы. Предпочтительной является 2-тиенил или 2-фуранилгруппа.
Аралкильную группу, включающую 7-20 атомов углерода: бензил, 1-фенилэтил-, -пропил-, -бутил-, -гексил-, -2-метилэтил-, -2-этилэтил-, -2,2-диметилэтилгруппы, орто-, мета-, пара-метил-, этил-, пропил-, изопропилбензилгруппы, 2',3'-, 2',4'-, 2',5'-, 2',6'-, 3',4'-, 3',5'-диметил- или -диэтилбензилгруппы, 2'-, 3'-, 4'-фтор-, хлор-, бром-, иодбензилгруппы, 2',3'-, 2',4'-, 2',5'-, 2',6'-, 3',4'-, 3',5'-, дифтор-, дихлор-, дибром- или дииодбензилгруппы или 2- или 3-нафтилметилгруппы, 2-фенилэтил-, 3-фенилпропил-, 4-фенилбутил-, 5-фенилпентилгруппы.
C1-C6-алкильную группу: прямая или разветвленная алкильная группа, включающая 1-6 атомов углерода, такая как метил-, этил-, н-пропил-, изопропил-, н-, изо-, трет-бутил-, н-пентил-, 2,2-диметилпропил- или 3-метилбутилгруппы.
Циклоалкильный остаток: циклопропан-, циклобутан-, циклопентан-, циклогексан-, циклогептан-, декагидронафталиновый остаток.
Циклоалкилалкильный остаток: циклопропил-, циклобутил-, циклопентил-, циклогексил-, циклогептилметил-остаток, 1-циклопропил-, 1-циклобутил-, 1-циклопенил-, 1-циклогексил-, 1-циклогептилэтиловый остаток, 2-циклопропил-, 2-циклобутил-, 2-циклопентил-, 2-циклогексил-, 2-циклогептилэтиловый остаток.
Гетероциклическое кольцо: незамещенный 2- или 3-тиенил- или 2- или 3-фурилгруппы или 3-метил-, 3-этил-, 3-фтор-, 3-хлор-, 3-бром-, 3-иод-2-фурил- или -2-тиенилгруппы, 4-метил-, 4-этил-, 4-фтор-, 4-хлор-, 4-бром-, 4-иод-2-фурил- или 2-тиенилгруппы, 5-метил-, 5-этил-, 5-фтор-, 5-хлор-, 5-бром-, 5-иод-2-фурил- или -2-тиенилгруппы, 2-метил-, 2-этил-, 2-фтор-, 2-хлор-, 2-бром-, 2-иод-3-фурил- или -3-тиенилгруппы, 4-метил-, 4-этил-, 4-фтор-, 4-хлор-, 4-бром-, 4-иод-3-фурил- или -3-тиенилгруппы, 5-метил-, 5-этил-, 5-фтор-, 5-хлор-, 5-бром-, 5-иод-З-фурил- или -3-тиенилгруппы; незамещенные 2-, 3- или 4-пиридилгруппы или 3-метил-, 3-этил-, 3-фтор-, 3-хлор-, 3-бром-, 3-иод-2-пиридилгруппы, 4- метил, 4-этил, 4-фтор-, 4-хлор-, 4-бром-, 4-иод-2-пиридилгруппы, 5-метил-, 5-этил-, 5-фтор-, 5-хлор-, 5-бром-, 5-иод-2-пиридилгруппы, 2-метил-, 2-этил-, 2-фтор-, 2-хлор-, 2-бром-, 2-иод-3-пиридилгруппы, 4-метил-, 4-этил-, 4-фтор-, 4-хлор-, 4-бром-, 4-иод-3-пиридилгруппы, 5-метил-, 5-этил-, 5-фтор-, 5-хлор-, 5-бром-, 5-иод-3-пиридилгруппы, 2-, 4-, 5-, 6-пиримидилгруппы, 3-, 4-, 5-, 6-пиридазинилгруппы или 2- или 3-пиразинилгруппы.
R2 означает
Алкильную группу: прямой или разветвленный алкил, включающий 1-6 атомов углерода, такой как метил-, этил-, н-пропил-, изопропил-, н-, изо-, трет-бутил-, н-пентил-, 2,2-диметилпропил-, или 3-метилбутил группы. Предпочтительным является атом водорода.
Замещенное фенильное или нафтильное кольцо: фенил- орто-, мета-, пара-метил-, этил-, пропил-, изопропилфенилгруппы, 2,3-, 2,4-, 2,5-, 2,6- 3,4-, 3,5-диметил- или диэтилфенилгруппы, орто-, мета-, пара-фтор-, хлор-, бром-, иодфенилгруппы, 2,3-, 2,4-, 2,5-, 2,6- 3,4-, 3,5-дифтор-, дихлор-, дибром- или дииодфенилгруппы, орто-, мета-, пара-тригалогенметилфенилгруппы, 2,3-, 2,4-, 2,5-, 2,6- 3,4- или 3,5-дигалогенфенилгруппы, орто-, мета-, пара-метокси-, -этокси-, -пропокси-, -изопропоксифенилгруппы или нафтилгруппы. Предпочтительным является 2,5-дифторфенил.
R3 и R4 означают
Алкильную группу: прямая или разветвленная алкильная группа, включающая 1-6 атомов углерода, такая как метил-, этил-, н-пропил-, изопропил-, н-, изо-, трет-бутил-, н-пентил-, 2,2-диметилпропил- или 3-метилбутилгруппы. Предпочтительным является атом водорода.
R5 означает
Алкильную группу: прямая или разветвленная алкильная группа, включающая 1-6 атомов углерода, такая как метил-, этил-, н-пропил-, изопропил-, н-, изо-, трет-бутил-, н-пентил-, 2,2-диметилпропил- или 3-метилбутилгруппы. Предпочтительным является атом водорода.
R6 означает
Алкильную группу: прямая или разветвленная алкильная группы, включающая 1-6 атомов углерода, такая как метил-, этил-, н-пропил-, изопропил-, н-, изо-, трет-бутил-, н-пентил-, 2,2-диметилпропил- или 3-метилбутилгруппа. Предпочтительной является метильная группа.
Аралкильную группу, включающую 7-20 атомов углерода: бензильная группа, 1-фенилэтил-, -пропил-, -бутил-, -гексил-, -2-метилэтил-, -2-этилэтил-, -2,2-диметилэтилгруппа, орто-, мета-, пара-метил-, этил-, пропил, изопропилбензилгруппа, 2',3'-, 2',4'-, 2',5'-, 2',6'-, 3',4'-, 3',5'-диметил- или -диэтилбензилгруппа, 2'-, 3'-, 4'-фтор-, хлор-, бром-, иодбензилгруппа, 2',3'-, 2',4'-, 2',5'-, 2',6'-, 3',4'-, 3',5'-, дифтор-, дихлор-, дибром- или дииодбензилгруппа или 2- или 3-нафтилметилгруппа, 2-фенилэтил-, 3-фенилпропил-, 4-фенилбутил-, 5-фенилпентилгруппа.
Гетероаралкильную группу, включающую 7-20 атомов углерода: 2-, 3- или 4-пиридилметил-, -этил- или -пропилгруппа, 2- или 3-фурилметил-, -этил- или -пропилгруппа, 2- или 3-тиенилметил-, -этил- или -пропилгруппа, 2-, 3-, 4-, 5-, 6- или 7-индолилметил-, -этил- или -пропилгруппа. Предпочтительной является бензилгруппа.
Предпочтительными являются соединения формулы (1), в которых
группа 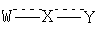 означает
означает 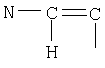 или
или 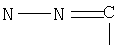 .
.
Если R1 означает -СО-R11, то R11 предпочтительно имеет следующие значения: метил, этил, изопропил, фенил, 2-тиенил и 2-фурил. Если R1 означает -CO-OR12, то R12 предпочтительно имеет следующие значения: метил, этил или изопропил.
Кроме того, предпочтительными являются соединения, в которых R2 означает ароматическое кольцо, замещенное одним или более атомов галогена, в частности ароматическая группа, замещенная атомами фтора, например бензильная группа, например 2',6'-дифторбензил. Наиболее предпочтительными являются соединения, в которых по крайней мере один из R3 и R4, в частности оба, означают атомы водорода.
Предпочтительным значением Z является прямая связь или атом кислорода, в то время как G предпочтительно означает группу -С=С-. L предпочтительно означает NH-группу, в то время как Q предпочтительно означает карбонил, a R51 означает С1-С6-алкилгруппу. Наиболее предпочтительными значениями R61 является атом водорода или С1-С3-алкилгруппа, в частности, метил, а предпочтительным значением R62 является аралкил, например бензилгруппа.
Соединения (1) предпочтительно получают c использованием следующих превращений:
(а) взаимодействие соединения общей формулы (2)
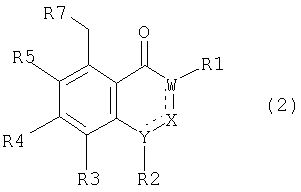
где R7 означает удаляемую группу, например, атом галогена или алкил-, перфторалкил- или арилсульфонилгруппу, а все остальные остатки имеют значения, определенные выше для соединения (1), с соединением общей формулы (3)
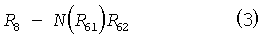
где R8 означает атом водорода или атом металла, такой как, например, литий, натрий, калий, цезий, кальций или барий, a R61 и R62 имеют значения, указанные для соединения (1);
(б) взаимодействие соединения общей формулы (4)
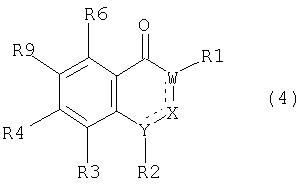
где R9 означает группу -OSO2СnF2n+1, атом галогена, в частности бром или иод, или другую удаляемую группу, а другие остатки имеют значения, определенные для соединения (1), с соединением общей формулы (5)
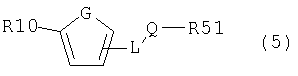
где R10 означает металл-содержащую группу, такую как триалкилцинк, галогенид магния, или несодержащую металл группу, такую как группу, содержащую бор, кремний и т.п., группу, содержащую диалкоксибор- или дигидроксиборгруппу, модифицированные гидрокси- и меркаптогруппы в форме соли с металлом, таким как литий, натрий, калий, цезий, кальций, барий, серебро и медь, группу -С≡С-R31 или группу -CR52=CR53R31 или -CR31=CR52R53, где R31 означает группу, содержащую металл или неметалл, такой как бор, кремний и т.п., такую как триалкилцинк, галогенид магния, диалкоксибор- или дигидроксиборгруппа, а остальные остатки имеют значения, определенные для соединения (1), причем реакцию проводят в присутствии или отсутствии катализатора, такого как, например, медь, никель, палладий, платина или органическое производное указанных металлов;
(в) если Y в соединении (1) означает атом азота, то взаимодействие соединения общей формулы (6)
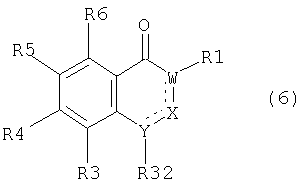
где R32 означает атом водорода или атом металла, такой как, например, литий, натрий, калий, цезий, кальций, барий, серебро или медь, а другие остатки имеют значения, определенные для соединения (1), с соединением общей формулы (7)
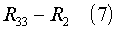
где R33 означает удаляемую группу, например, атом галогена или алкил, перфторалкил или арилсульфонилгруппу, a R2 имеет значение, определенное для соединения (1), или
(г) если W в соединении (1) означает атом азота, то взаимодействие соединения общей формулы (8)
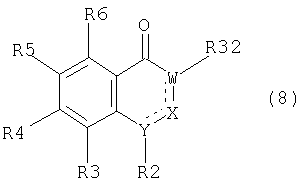
где R32 означает атом водорода или металла, например литий, калий, цезий, кальций, барий, серебро или медь, а остальные остатки имеют значения, определенные для соединения (1), с соединением общей формулы (9)
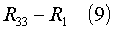
где R33 означает удаляемую группу, например, атом галогена или алкил-, перфторалкил- или арилсульфонилгруппу, a R1 имеетзначение, определенное для соединения (1).
Сведения, подтверждающие возможность осуществления изобретения
Соединения (1) по настоящему изобретению могут быть использованы в качестве антагонистов ГВГ, например, для контроля репродуктивной функции у мужчин, для гормональной терапии, для лечения недостаточности репродуктивной функции и бесплодия у женщин, в качестве противозачаточных средств для женщин и для лечения онкологических заболеваний. При контроле репродуктивной функции у мужчин соединения по настоящему изобретению приводят к снижению сперматогенеза. Предпочтительно осуществляют комбинированное введение совместно с андрогеном, например с производными тестостерона, такими как эфиры тестостерона. Введение производного тестостерона можно осуществлять, например, с помощью инъекции, например внутримышечной инъекции пролонгированного действия.
Соединения (1) могут быть также использованы при гормональной терапии при необходимости в комбинации с другими гормонами, например эстрогенами и/или прогестинами, для лечения, например, эндометриоза, леомиомы матки и фибромы матки. Прежде всего, предпочтительными являются комбинации антагонистов ГВГ по настоящему изобретению с тканеспецифичными частичными агонистами эстрогенов, такими как ралоксифен®. Более того, соединения (1) по настоящему изобретению могут быть использованы для стимуляции репродуктивной функции у женщин, например за счет индуцирования овуляции, и для лечения бесплодия.
С другой стороны соединения (1) могут быть использованы в качестве противозачаточных средств для контрацепции у женщин. Например, антагонист ГВГ можно вводить в период от первого до 15 дня цикла вместе с эстрогеном, последний предпочтительно вводят в чрезвычайно низкой дозе. В период от 16 до 21 дня приема в комбинацию эстрогена с антагонистом ГВГ добавляют прогестаген. Антагонист ГВГ можно непрерывно вводить в течение всего цикла. Таким образом можно обеспечивать снижение гормональной дозы и, следовательно, снизить побочные действия нефизиологических уровней гормонов. Более того, можно обеспечивать благоприятное действие на женщин, страдающих от синдрома поликистозного яичника и андрогензависимого заболевания, такого как угри, себорея и гирсутизм. Следует также ожидать улучшенного контроля цикла по сравнению с известными методами введения. Другими показаниями являются доброкачественная гиперплазия предстательной железы, гонадная защита при химиотерапии, контролируемая стимуляция яичников/искусственное оплодотворение, нарушения развития у младенцев, например преждевременное половое развитие и поликистозный яичник.
И наконец антагонисты ГВГ по настоящему изобретению могут быть использованы для лечения гормонзависимых онкологических заболеваний, таких как, предклимактерический рак молочной железы, рак предстательной железы и рак эндометрия, при этом такие соединения подавляют эндогенные половые стероидные гормоны.
Соединения (1) по настоящему изобретению используют в качестве антагонистов ГВГ для введения человеку, а также в ветеринарной практике, например, для лечения домашних, сельскохозяйственных и диких животных.
Введение можно осуществлять известным способом, например, пероральным, местным, ректальным, внутривагинальным, интраназальным способами или с помощью инъекции. Предпочтительным является пероральное введение. Соединения (1) можно получить в виде соответствующей лекарственной формы и при необходимости их смешивают с фармацевтически приемлемыми носителями или разбавителями. Для перорального введения можно использовать, например твердые формы, такие как таблетка, капсула, драже или порошок, а также жидкие формы в виде питьевых растворов. В качестве непероральных форм для введения можно использовать, например, внутривенную, подкожную или внутримышечную инъекции или мази, кремы или суппозитории. При необходимости можно использовать формы пролонгированного действия. Величина дозы может зависеть от типа показания, тяжести заболевания, возраста, пола, массы тела и чувствительности пациента, для которого необходимо проводить лечение. Предпочтительная доза при введении составляет от 0,01 до 30 мг, более предпочтительно от 0,1 до 3 мг и наиболее предпочтительно от 0,1 до 1 мг/кг массы тела в сутки. Введение можно осуществлять в виде одной дозы или нескольких разделенных доз.
В следующей таблице приведен список наиболее предпочтительных соединений (1).
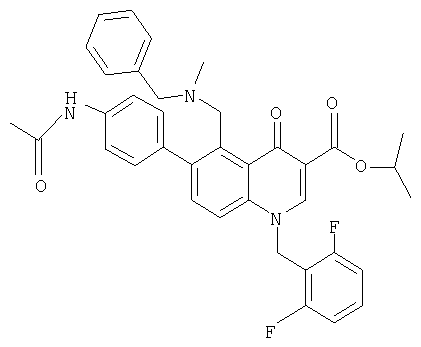
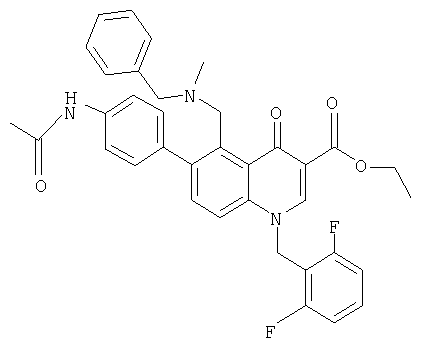
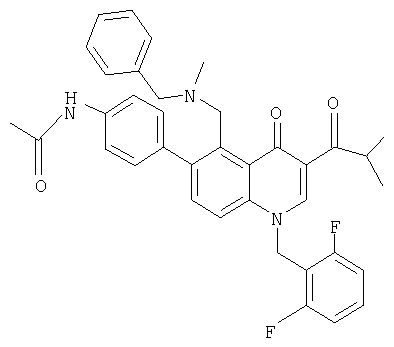
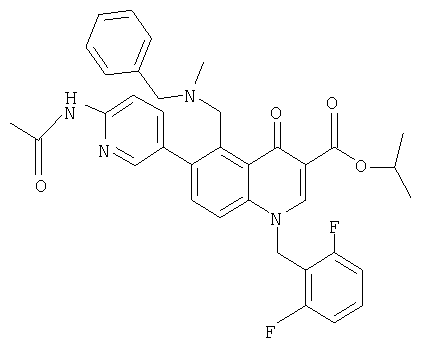
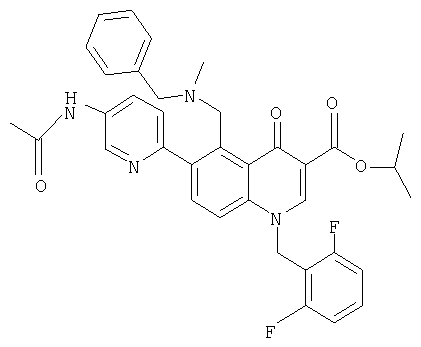
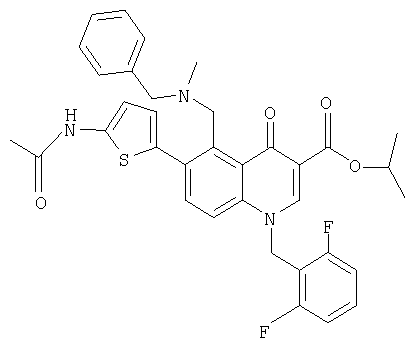
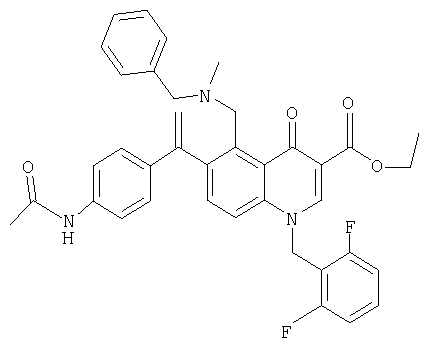
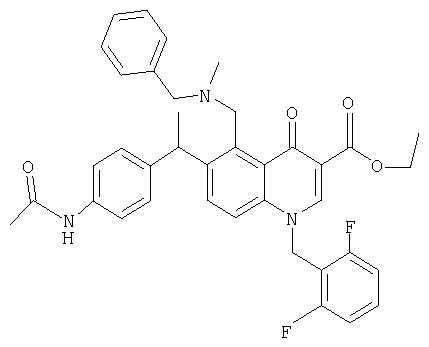
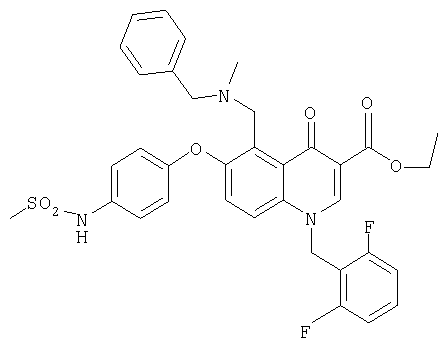
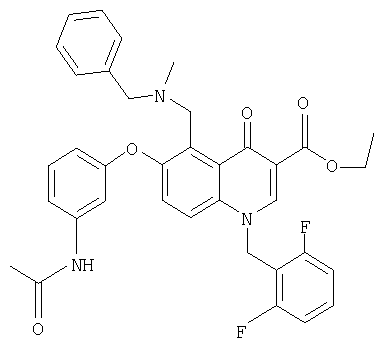
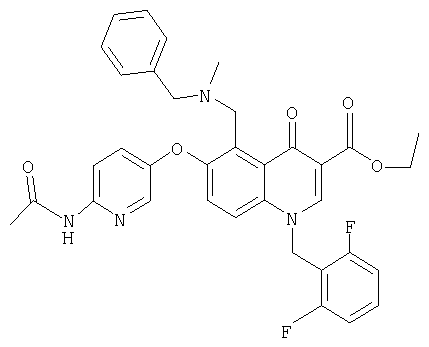
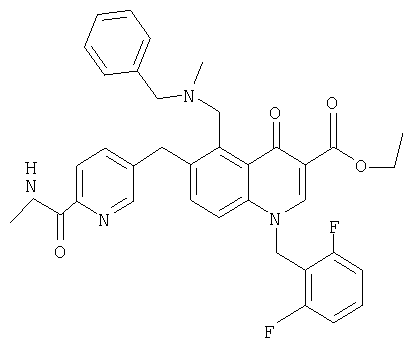
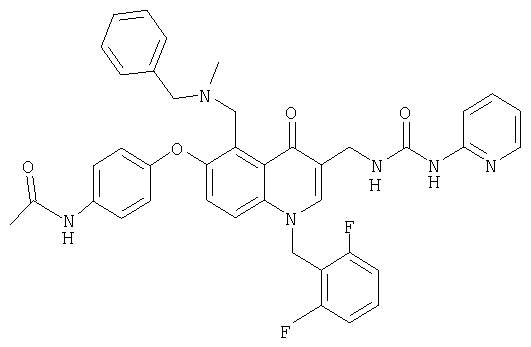
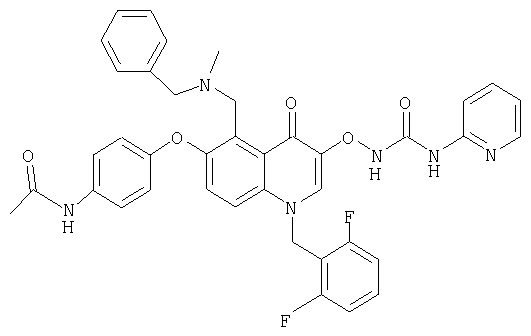
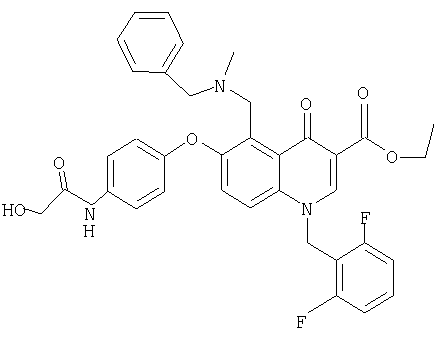
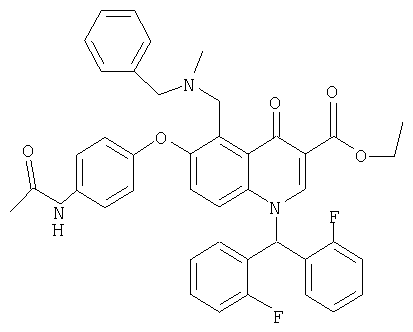
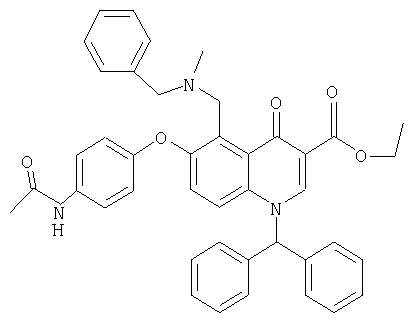
Далее изобретение поясняется примерами воплощения настоящего изобретения.
Пример 1. Этиловый эфир 6-(4-ацетамидофенокси)-5-(N-бензил-N-метиламинометил)-1-(2',6'-дифторбензол)-1,4-дигидро-4-оксохинолин-3-карбоновой кислоты
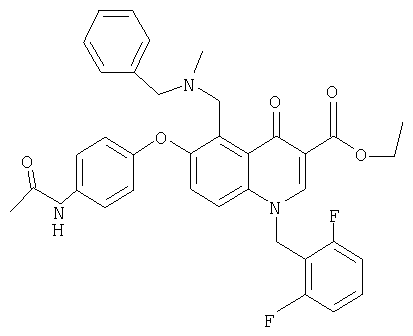
78 мг Этилового эфира 6-(4-ацетамидофенокси)-5-(хлорметил)-1-(2',6'-дифторбензил)-1,4-дигидро-4-оксохинолин-3-карбоновой кислоты, растворенного в 3 мл диметилформамида, смешивают при 0°С с 84 мкл N-метилбензиламина и 84 мкл N,N-диизопропилэтиламина, перемешивают при комнатной температуре в течение 20 ч. После добавления 20 мл водного раствора бикарбоната натрия осадок отфильтровывают в вакууме, промывают водой и н-гексаном, сушат при комнатной температуре в вакууме, при этом получают 70 мг указанного в заголовке соединения. ЯМР, δ 1,3 (t, 3H, СН3), 1,9 (s, 3H, NCH3), 2,05 (s, 3H, СН3), 3,55 (s, 2H, NCH2), 4,27 (q, 2H, ОСН2), 4,91 (s, 2H, NCH2), 5,68 (s, 2H, NCH2), 6,85 (d, 2H, ArCH), 7,1-7,22 (m, 7H, ArCH), 7,26 (d, 1H, ArCH), 7,42-7,6 (m, 4H, ArCH), 8,72 (s, 1H, NCH), 9,9 (s, 1H, NH). MC: FAB, M++1=526 [M=525].
Исходное соединение, этиловый эфир 6-(4-ацетамидофенокси)-5-(хлорметил)-1-(2',6'-дифторбензил)-1,4-дигидро-4-оксохинолин-3-карбоновой кислоты получают по следующей схеме синтеза:
а) Этиловый эфир 1,4-дигидро-6-фтор-5-нитро-4-оксохинолин-3-карбоновой кислоты
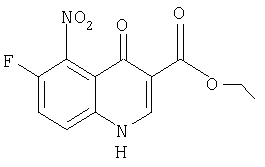
50 г 4-Фтор-3-нитроанилина и 69 г диэтилового эфира этоксиметиленмалоновой кислоты нагревают при 120°С в течение 3 ч. Смесь переносят в н-гексан, перемешивают в течение 2 ч и кристаллический материал отфильтровывают в вакууме, сушат в вакууме при комнатной температуре, при этом получают 93 г диэтилового эфира N-(4-фтор-3-нитрофенил)аминометиленмалоновой кислоты. Затем продукт тремя порциями добавляют в 150 мл предварительно нагретой до 260°С смеси, содержащей 26,5% дифенила и 73,5% дифенилового эфира (фирмы Dowtherm А), и перемешивают при указанной температуре в течение 30 мин. После охлаждения смесь разбавляют 500 мл н-гексана и осадок отфильтровывают в вакууме, всего получают 64 г смеси этилового эфира 1,4-дигидро-6-фтор-5-нитро-4-оксохинолин-З-карбоновой кислоты и этилового эфира 1,4-дигидро-6-фтор-7-нитро-4-оксохинолин-3-карбоновой кислоты. ЯМР, δ 1,31 (t, 3Н, СН3), 4,25 (q, 2Н, ОСН2), 7,88 (s, 1Н, ArCH, изомер А), 7,92 (s, 1H, ArCH, изомер А), 8,1 (d, 1H, ArCH, изомер В), 8,45 (d, 1H, ArCH, изомер В), 8,59+8,69 (2s, 1H от каждого изомера, NCH, А+В). МС: EI М+=280 [М=280].
б) Этиловый эфир 1-(2',6'-дифторбензил)-1,4-дигидро-6-фтор-5-нитро-4-оксохинолин-3-карбоновой кислоты
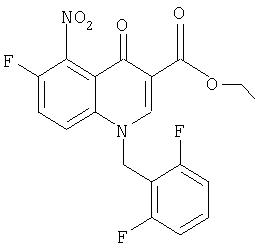
22 г Описанной выше смеси перемешивают в 500 мл диметилформамида в смеси с 16 г карбоната калия и 23,7 г 2,6-дифторбензилбромида в течение 5 ч при комнатной температуре. Реакционную смесь переносят в 1 л водного раствора хлорида аммония и экстрагируют три раза этилацетатом. После сушки над сульфатом натрия и упаривания в вакууме к остатку добавляют 500 мл н-гексана и перемешивают в течение 15 мин. После декантирования слоя гексана остаток перекристаллизовывают из этилацетата, при этом получают 10,4 г указанного в заголовке соединения. ЯМР, δ 1,3 (t, 3Н, СН3), 4,25 (q, 2H, ОСН2), 5,84 (s, 2H, NCH2), 7,15-7,25 (m, 2H, ArCH), 7,45-7,55 (m, 1H, ArCH),
7,92 (dd, 1H, ArCH, 8,04-8,14 (m, 2H, ArCH), 8,96 (s, 1H, NCH). MC:EI M+=406 [М=406].
в) Этиловый эфир 6-(4-ацетамидофенокси)-1-(2',6'-дифторбензил)-1,4-дигидро-5-нитро-4-оксохинолин-3-карбоновой кислоты
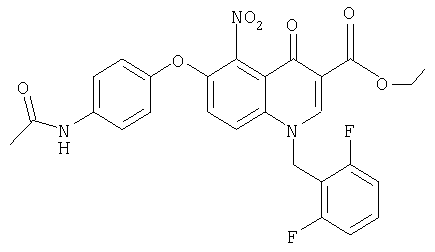
3,74 г 4-Ацетамидофенола в 40 мл диметилформамида смешивают с 733 мг гидрида натрия (80%-ный в минеральном масле) и перемешивают в течение 15 мин при комнатной температуре. Затем этот раствор добавляют к 5 г описанного выше соединения, растворенного в 40 мл диметилформамида. После перемешивания при комнатной температуре в течение 5 ч смесь переносят в ледяную воду и осадок отфильтровывают в вакууме. После хроматографии на кизельгеле (элюент дихлорметан/2-пропанол, 95:5) получают 5,17 г указанного в заголовке соединения. ЯМР, δ 1,3 (t, 3Н, СН3), 2,03 (s, 3Н, СН3), 4,27 (q, 2H, ОСН2), 5,79 (s, 2H, NCH2), 7,01 (d, 2H, ArCH), 7,13-7,23 (m, 2H, ArCH), 7,43-7,56 (m, 2H, ArCH), 7,61 (d, 2H, ArCH), 7,8 (d, 1H, ArCH), 8,93 (s, 1H, NCH), 9,97 (s, 1H, NH). MC: El, M+=537 [M=537].
г) Этиловый эфир 6-(4-ацетамидофенокси)-5-амино-1-(2',6'- дифторбензил)-1,4-дигидро-4-оксохинолин-3-карбоновой кислоты
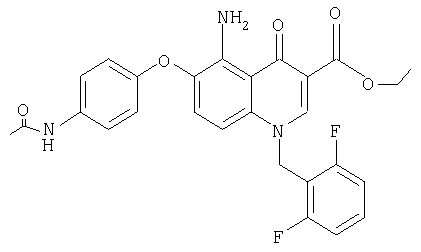
5,1 г описанного выше соединения в 650 мл метанола гидрируют в присутствии 510 мг палладия на угле (10%-ный). После удаления катализатора фильтрованием и упаривания получают 4,55 г указанного в заголовке соединения. ЯМР, δ 1,29 (t, 3Н, СН3), 2,02 (s, 3Н, СН3), 3,25 (s, 2H, NH2,), 4,25 (q, 2H, ОСН2), 5,55 (s, 2H, NCH2), 6,55 (d, 1H, ArCH), 6,86 (d, 2H, ArCH), 7,07 (d, 1H, ArCH), 7,1-7,22 (m, 2H, ArCH), 7,4-7,55 (m, 3H, ArCH), 8,71 (s, 1H, NCH), 9,8 (s, 1H, NH). MC: El, M+=507 [M=507].
д) Этиловый эфир 6-(4-ацетамидофенокси)-1-(2',6'-дифторбензил)-1,4-дигидро-5-иод-4-оксохинолин-3-карбоновой кислоты
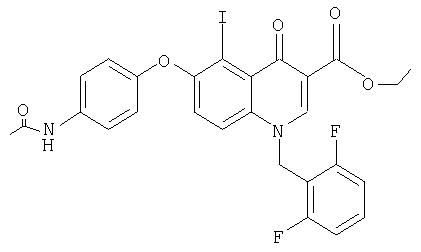
2 г Указанного выше соединения растворяют в смеси 24 мл концентрированной серной кислоты и 12 мл воды, затем при 0°С смешивают с 325 г нитрита натрия в 4 мл воды. Через 15 мин рН среды доводят до 3 раствором бикарбоната натрия и добавляют 100 мг мочевины. Затем добавляют 723 мг иодида калия в 0,5 мл воды и перемешивают при комнатной температуре в течение 1 ч. После экстракции смесью дихлорметан/метанол, 95:5 об./об.) органическую фазу промывают водным раствором тиосульфата натрия, сушат и упаривают. После хроматографии на кизельгеле (элюентдихлорметан, содержащий 0-15% изопропанола) получают 697 мг указанного в заголовке соединения. ЯМР, δ 1,3 (t, 3Н, СН3), 2,02(s, 3Н, СН3), 4,25 (q, 2Н, OCH2), 5,71 (s, 2H, NCH2), 6,83 (d, 2H, ArCH), 7,1-7,2 (m, 2H, ArCH), 7,3 (d, 1Н, ArCH), 7,41-7,63 (m, 4H, ArCH), 8,83 (s, 1Н, N-CH), 9,95 (s, 1Н, NH). MC: ES, M++1=493 [M=492].
е) Этиловый эфир 6-(4-ацетамидофенокси)-1-(2',6'-дифторбензил)-1,4-дигидро-4-оксо-5-стирилхинолин-3-карбоновой кислоты
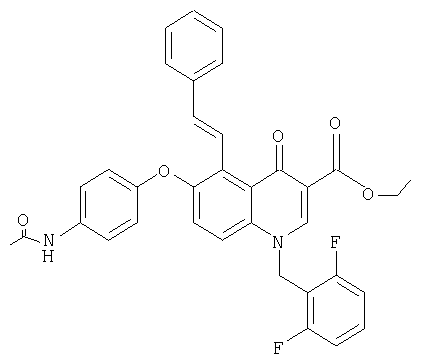
550 мг указанного выше иодпроизводного, 198 мг стирилбороновой кислоты, 55 мг тетракис-трифенилфосфинпалладия (0), 1,1 мл 2 M раствора карбоната натрия, 2,2 мл этанола и 22 мл толуола перемешивают в течение 6 ч при 80°С. Затем добавляют воду, экстрагируют дихлорметаном и органическую фазу промывают солевым раствором, сушат и упаривают. Остаток очищают хроматографией на кизельгеле (элюент: дихлорметан, содержащий 0-10% изопропанола), при этом получают 902 мг указанного в заголовке соединения. ЯМР, δ 1,28 (t, 3Н, СН3), 2,0 (s, 3Н, СН3), 4,24 (q, 2H, ОСН2), 5,7 (s, 2H, N-CH2), 6,75-6,85 (m, 3Н, ArCH, CH=CH), 7,08-7,28 (m, 3Н, ArCH), 7,3-7,68 (m, 9Н, ArCH), 7,86 (d, 1Н, СН=СН), 8,75 (s, 1H, NCH), 9,72 (s, 1Н, NH). MC: ES, М++1=595 [М=594].
ж) Этиловый эфир 6-(4-ацетамидофенокси)-1-2',6'-дифторбензил)-1,4-дигидро-5-формил-4-оксохинолин-3-карбоновой кислоты
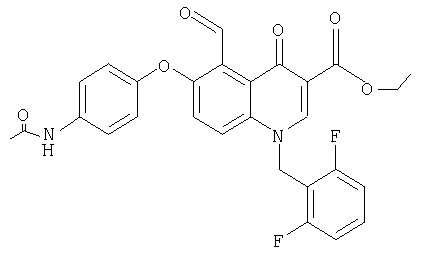
450 мг описанного выше стирилпроизводного растворяют в 25 мл тетрагидрофурана и 7 мл воды, смешивают с 0,11 мл 2,5%-ного раствора тетраоксида осмия в трет-бутаноле. Через 15 мин перемешивания при комнатной температуре добавляют 482 мг, через 20 и 22 ч по 100 мг и через 24 ч еще 100 мг периодата натрия. Через 26 ч смесь разбавляют водой и экстрагируют этилацетатом. После высушивания органической фазы над сульфатом натрия ее упаривают, при этом получают 352 мг указанного в заголовке соединения в виде пены. ЯМР, δ 1,29 (t, 3Н, СН3), 2,01 (s, 3H, СН3), 4,27 (q, 2Н, OCH2), 5,71 (s, NCH2), 6,91 (d, 2H, ArCH), 7,12-7,22 (m, 2H, ArCH), 7,4 (d, 1 H, ArCH), 7,43-7,64 (m, 3H, ArCH), 7,72 (d, 1 H, ArCH), 9,0 (d, 1 H, NCH), 9,97 (s, 1H, NH), 10,44 (s, 1H, СНО). МС: FAB, M++1=521 [М=520].
з) Этиловый эфир 6-(4-ацетамидофенокси)-1-(2',6'-дифторбензил)-1,4-дигидро-5-гидроксиметил-4-оксохинолин-3-карбоновой кислоты
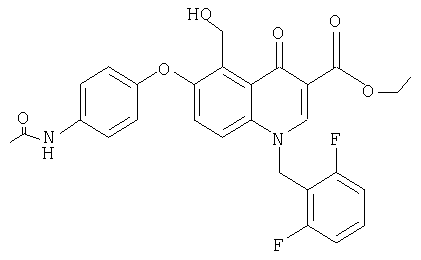
300 мг описанного выше альдегида растворяют в 13,8 мл уксусной кислоты и тремя порциями по 10 мг с интервалом в 10 мин добавляют боргидрид натрия. После разбавления водой смесь экстрагируют этилацетатом и органическую фазу промывают раствором бикарбоната натрия до нейтрального значения рН. После высушивания над сульфатом натрия смесь упаривают. После хроматографии на кизельгеле (элюент дихлорметан, содержащий 0-10% изопропанола) получают 129 мг указанного в заголовке соединения в виде пены. ЯМР, δ 1,31 (t, 3Н, СН3), 2,02 (s, 3Н, СН3), 4,27 (q, 2Н, OCH2), 4,86 (d, 2Н, ОСН2), 5,12 (t, 1Н, ОН), 5,8 (s, 2H, NCH2), 6,85 (d, 2H, ArCH), 7,12-7,22 (m, 2H, ArCH), 7,38 (d, 1Н, ArCH), 7,42-7,59 (m, 3Н, ArCH), 7,63 (d, 1H, ArCH), 8,94 (s, 1H, NCH), 9,5 (s, 1H, NH). MC: FAB, М++1=523 [М=522].
и) Этиловый эфир 6-(4-ацетамидофенокси)-5-хлорметил-1-(2',6'-дифторбензил)-1,4-дигидро-4-оксохинолин-3-карбоновой кислоты
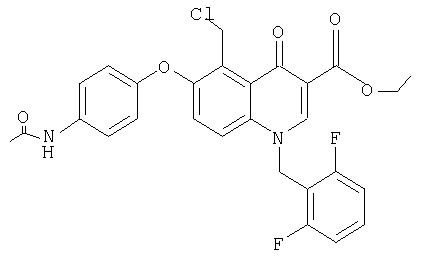
80 мг указанного выше спирта растворяют в 2 мл дихлорметана и смешивают с 0,1 мл тионилхлорида. Через 20 мин выдерживания при комнатной температуре добавляют воду, экстрагируют дихлорметаном и органическую фазу промывают солевым раствором. После высушивания над сульфатом натрия смесь упаривают, при этом получают 80 мг указанного в заголовке соединения в виде пены. ЯМР, δ 1,33 (t, 3Н, СН3), 2,07 (s, 3Н, СН3), 4,3 (q, 2H, ОСН2), 5,66 (s, 2H, CH2Cl), 5,75 (s, 2H, NCHg), 6,98 (d, 2H, ArCH), 7,13-7,25 (m, 2H, ArCH), 7,3 (d, 1H, ArCH), 7,53 (t, 1H, ArCH), 7,61 (d, 2H, ArCH), 7,68 (d, 1H ArCH), 8,82 (s, 1H, NCH), 9,98 (s, 1H, NH). MC: ES, М++1=541/543 [М=540/542].
Пример 2. 2-Пропиловый эфир 6-(4-ацетамидофенокси)-5-(N-бензил-N-метиламинометил)-1-(2',6'-дифторбензил)-1,4-дигидро-4-оксохинолин-3-карбоновой кислоты
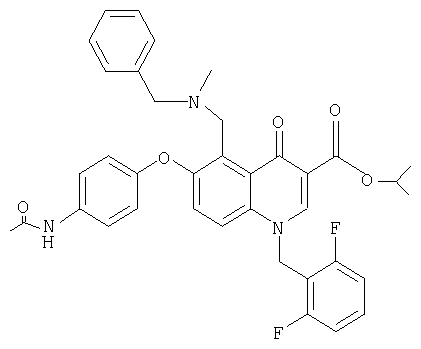
Указанное соединение получают из этилового эфира 6-(4-ацетамидофенокси)-5-(N-бензил-N-метиламинометил)-1-(2',6'-дифторбензил)-1,4-дигидро-4-оксохинолин-3-карбоновой кислоты при нагревании в присутствии тетраизопропилата титана в изопропаноле.
Пример 3. Этиловый эфир 5-(N-бензил-N-метиламинометил)-1-(2',6'-дифторбензил)-1,4-дигидро-6-(4-изобутирамидофенокси)-4-оксохинолин-3-карбоновой кислоты
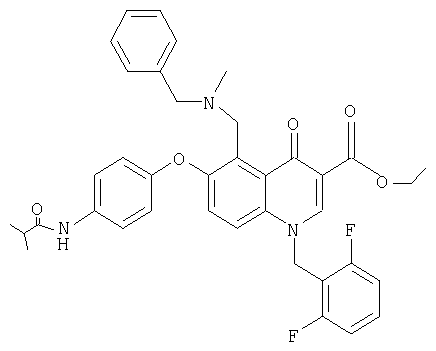
Указанное соединение, которое является аналогом соединения, описанного в примере 1, получают в виде пены из этилового эфира 5-(хлорметил)-1-(2',6'-дифторбензил)-1,4-дигидро-6-(4-изобутирамидофенокси)-4-оксохинолин-3-карбоновой кислоты и N-метилбензиламина.
а) Этиловый эфир 5-(хлорметил)-1-(2',6'-дифторбензил)-1,4-дигидро-6-(4-изобутирамидофенокси)-4-оксохинолин-3-карбоновой кислоты
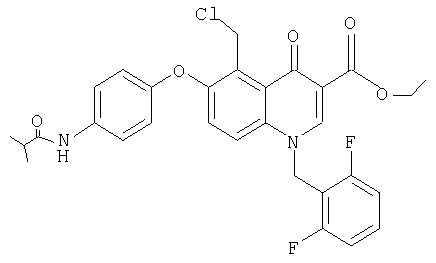
Указанное соединение получают, как описано в примере 1в, но с использованием 4-изобутирамидофенола вместо 4-ацетамидофенола и превращением в аналогичных условиях, описанных в примерах 1г-1и.
Пример 4. 3-Ацетил-6-(4-ацетамидофенил)-1-бензил-5-(N-бензил-N-метиламинометил)фталазин-4-он
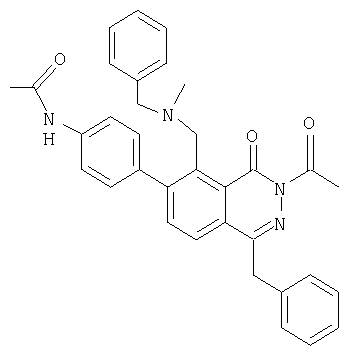
Указанное в заголовке соединение получают при обработке 6-(4-ацетамидофенил)-1-бензил-5-(N-бензил-N-метиламинометил)фталазин-4-она в присутствии основания, такого как карбонат натрия или гидроксид натрия, ацетилхлоридом или ацетангидридом.
6-(4-Ацетамидофенил)-1-бензил-5-(N-бензил-N-метиламинометил)-фталазин-4-он получают по следующей схеме:
а) 6-(4-Ацетамидофенил)-1 -бензил-5-иодфталазин-4-он
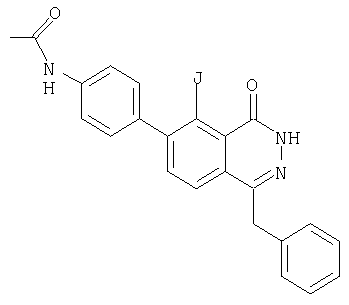
1-Бензил-5,6-дииодфталазин-4-он (см. статью Indian J. Chem., (1978) т.16В, стр.301-304) обрабатывают, как описано в примере 1е, 1 экв. 4-ацетамидофенилбороновой кислоты. Указанное в заголовке соединение получают в очищенном виде после хроматографии на кизельгеле.
б) 6-(4-Ацетамидофенил)-1 -бензил-5-хлорметилфталазин-4-он
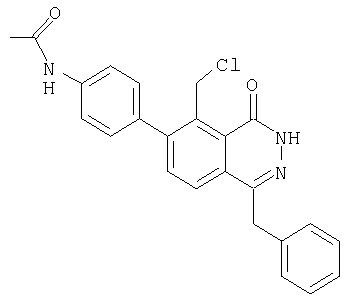
6-(4-Ацетамидофенил)-1-бензил-5-иодфталазин-4-он превращают в указанное в заголовке соединение в аналогичных условиях, описанных в примерах 1е)-и).
Пример 5. Этиловый эфир 6-(4-Ацетамидофенокси)-5-(N-бензил-N-метиламинометил)-1,4-дигидро-4-оксо-1-(2'-трифторметил)хинолин-3-карбоновой кислоты
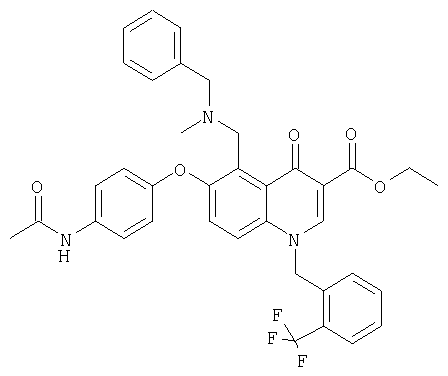
130 мг (0,226 ммоль) этилового эфира 6-(4-ацетамидофенокси)-5-(хлорметил)-1,4-дигидро-4-оксо-1-(2'-трифторметилбензил)-хинолин-3-карбоновой кислоты, растворенного в 5 мл ДМФ смешивают при -5°С с 125 мкл N,N-диизопропилэтиламина и 126 мкл (0,97 ммоль) N-бензилметиламина. После нагревания смеси до комнатной температуры и перемешивания при комнатной температуре в течение 20 ч реакционную смесь переносят в 50 мл насыщенного раствора бикарбоната натрия. Осадок отфильтровывают в вакууме, промывают водой и сушат в вакууме. Дальнейшую очистку продукта проводят с помощью хроматографии на кизельгеле с использованием в качестве элюента смеси, содержащей 90 частей дихлорметана, 10 частей этанола и 1 часть конц.аммиака (Rf 0,38). При этом получают 45 мг указанного в заголовке соединения в виде пены. МС, молекулярный пик М+=658.
Исходное соединение этиловый эфир 6-(4-ацетамидофенокси)-5-(хлорметил)-1,4-дигидро-4-оксо-1-(2'-трифторметилбензил)хинолин-3-карбоновой кислоты получают, как описано в примерах 1а-и, при использовании 2'-трифторметилбензилбромида вместо 2,6-дифторметилбензилбромида.
Пример 6. Этиловый эфир 6-(4-метиламинокарбонилфенокси)-5-(N-бензил-N-метиламинометил)-1-(2',6'-дифторбензил)-1,4-дигидро-4-оксо-хинолин-3-карбоновой кислоты
35 мг (0,061 ммоль) этилового эфира 6-(4-метиламинокарбонил-фенокси)-5-(хлорметил)-1-(2',6'-дифтобензил)-1,4-дигидро-4-оксо-хинолин-3-карбоновой кислоты, растворенного в 1,3 мкл ДМФ, смешивают при 0°С с 35 мкл N,N-диизопропилэтиламина и 35 мкл (0,25 ммоль) N-метилбензиламина. После нагревания до комнатной температуры смесь перемешивают при комнатной температуре в течение 20 ч и переносят в 10 мл насыщенного раствора бикарбоната натрия. Образующийся осадок отфильтровывают в вакууме, промывают водой и гексаном, сушат над пентаоксидом фосфора в вакууме, при этом получают 27 мг указанного в заголовке соединения в виде пены. МС (ESI): M++1=626 [М=625].
Исходное соединение этиловый эфир 6-(4-метиламинокарбонил-фенокси)-5-(хлорметил)-1-(2',6'-дифторбензил)-1,4-дигидро-4-оксо-хинолин-3-карбоновой кислоты получают, как описано в примерах 1а-1и, при использовании амида 4-гидрокси-М-метилбензойной кислоты вместо 4-ацетамидофенола.
Пример 7. Этиловый эфир 6-(4-ацетамидофенокси)-5-(N-бензил-N-метиламинометил)-1-(1-нафтилметил)-1,4-дигидро-4-оксохинолин-3-карбоновой кислоты
45 мг (0,081 ммоль) этилового эфира 6-(4-ацетамидофенокси)-5-(хлорметил)-1-(1-нафтилметил)-1,4-дигидро-4-оксо-хинолин-3-карбоновой кислоты, растворенного в 1,7 мкл ДМФ, смешивают при 0°С с 46 мкл N,N-диизопропилэтиламина и 46 мкл (0,33 ммоль) N-метилбензиламина. После нагревания до комнатной температуры смесь перемешивают при комнатной температуре в течение 20 ч и переносят в 15 мл насыщенного раствора бикарбоната натрия. Образующийся осадок отфильтровывают в вакууме, промывают водой и гексаном, сушат над пентаоксидом фосфора в вакууме, при этом получают 32 мг указанного в заголовке соединения в виде пены. МС (ESI): M++1=639 [M=638].
Исходное соединение этиловый эфир 6-(4-ацетамидофенокси)-5-(хлорметил)-1-(1-нафтилметил)-1,4-дигидро-4-оксохинолин-3-карбоновой кислоты получают, как описано в примерах 1а-1и, при использовании 1-хлорметилнафталина вместо 2,6-дифторметилбензилбромида.
Пример 8. Определение антагонистической активности
а) Материалы
Бусерелин получают на фирме Welding (Франкфурт-на-Майне, Германия). В соединение вводят метку 125(по методике с использованием хлорамина Т и Na125((4000 Ки/ммоль, фирма Amersham-Buchler, Брауншвайг, Германия). Меченое соединение очищают методом обращенно-фазной ВЭЖХ на колонке Spherisorb ODS II (250×4 мм, размер частиц 3 мкм), в качестве элюента используют смесь 50% ацетонитрил/0,15% трифторуксусная кислота, скорость элюции составляет 0,5 мл/мин. Удельная активность составляет 2000 Ки/ммоль.
Остальные реактивы с высокой степенью очистки получали на коммерческих фирмах.
б) Клеточная культура
Клетки альфа-Т3-1 (см. статью Bilezikjian и соавт., MoI. Endocrinol., (1991), т. 5, стр. 347-355) культивируют в среде DMEM (фирмы Gibco-BRL, Eggenstein-Leopoldshafen, Германия) в присутствии пеницилина (100 Межд.ед/мл), стрептомицина (0,1 мг/мл), глютамина (0,01 моль/л) и 10%-ной эмбриональной сыворотки коров (FCS, фирма РРА, Coelbe, Германия) в пластиковых планшетах для культивирования клеток (фирмы Nunc, 245×245×20 мм). Клетки СНО-3 (см. статью Schmid и соавт., J. Biol. Chem., (2000) т.275, стр.9193-9200) культивируют в аналогичных условиях, но с использованием среды Ham F12 (фирмы Gibco-BRL).
10 планшетов с культуральными конфлюентными клетками два раза промывают 50 мл фосфатного буферного раствора, содержащего хлористый натрий (ФСБ). Клетки собирают с помощью выскабливания специальным резиновым скребком в 5 мл ФБС и осаждают при центрифугировании при 800 об/мин в течение 10 мин на лабораторной центрифуге (фирмы Heraeus). Осадок клеток ресуспендируют в 5 мл смеси 0,25 моль/л сахарозы/0,01 моль/л триэтаноламина, рН 7,4. Клетки лизируют с использованием двух стадий замораживания (в бане со смесью сухой лед/этанол) и размораживания при комнатной температуре. Лизат центрифугируют при 900 об/мин в течение 10 мин и осадок отбрасывают. Супернатант центрифугируют при 18000 об/мин на роторе Sorvall SS34 в течение 30 мин. Осадок (мембранную фракцию) суспендируют с помощью гомогенизатора в 5 мл буферного раствора для анализа (0,25 моль/л сахарозы, 0,01 моль/л триэтаноламина, рН 7,5, 1 мг/мл овальбумина) и хранят аликвотными порциями по 200 мкл при -20°С. Содержание белка определяют методом Бредфорда (см. статью Anal. Biochem., (1976) т.72, стр.248-254).
в) Анализ связывания с рецептором
Анализ связывания для получения кривых конкурентной реакции проводили с использованием трех параллельных образцов. Реакционная смесь образца для исследования содержит 60 мкл суспензии мембранной фракции (10 мкг белка для клеток αТ3-1 или 40 мкг белка для клеток СНОЗ), 20 мкл бусерелина, меченого 125I (по 100000 имп/мин в образце для получения кривых конкурентной реакции и от 1500 до 200000 имп/мин для получения кривых насыщения), и 20 мкл буферного раствора для анализа или раствора исследуемого соединения. Исследуемые соединения растворяют в дистиллированной воде или 50%-ном этаноле. Затем готовят серийные разведения в буфере для анализа (от 5×10-6 моль/л до 5×10-12 моль/л). Неспецифическое связывание определяют в присутствии избытка немеченого бусерелина (10-6 моль/л). Исследуемые образцы инкубируют в течение 30 мин при комнатной температуре. Связанный и свободный лиганды разделяют методом фильтрации на фильтрах CF/C диаметром 2,5 см с использованием прибора для сбора клеток Amicon 10х, затем фильтры промывают два раза 5 мл буферного раствора 0,02 моль/л Трис/HCl, рН 7,4. Фильтры смачивают 0,3%-ным раствором полиэтиленимина (фирмы Serva, Heidelberg, Германия) в течение 30 мин для подавления неспецифического связывания. Радиоактивность на фильтре измеряют на 5-канальном счетчике γ-излучения (фирмы Wallac-LKB 1470 Wizard).
По результатам рецепторного анализа (неспецифического связывания с рецептором гонадотропин высвобождающего гормона) были получены следующие значения антагонистической активности: для вещества по примеру 1 ЕС50 составило величину 0,100-0,150 μМ, что говорит об очень высокой активности соединения, для веществ по примерам 6 и 7 значения активностей были только несколько ниже. Для сравнения были исследованы также близкие к заявляемым веществам соединения, такие как промежуточное соединение по примеру 1, 1d. для которого ЕС50 составило величину 2-3 μМ, и близкое к примеру 4 соединение, однако не содержащее заместителей, предусмотренных Формулой 1, а именно: этиловый эфир 7-(4-ацетиламино-фенил)-4-(2,6-дифтор-бензил)-8-метокси-1-оксо-1Н-фталазин-2-карбоновой кислоты, общей формулы
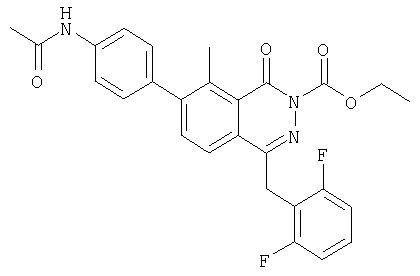
для которого ЕС50 составило величину 0,7-0,8 μМ.
Изобретение относится к новым производным хинолина проявляющим антагонистическую активность в отношении гонадотропин высвобождающего гормона. Описываются производные хинолина общей формулы (1)
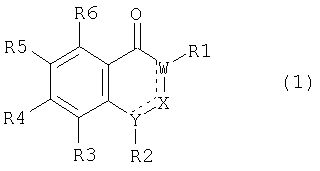
где R1 означает остаток сложного эфира карбоновой кислоты -CO-OR12, где R12 означает прямую или разветвленную алкильную цепь, содержащую 1-10 атомов углерода; R2 означает группу -CH(R21)R22, где R21 означает атом водорода, a R22 означает замещенное атомом галогена или -CF3 фенильное кольцо или нафтильное кольцо; R3 и R4 каждый независимо означает атом водорода; R5 означает группу, присоединенную через остаток Z
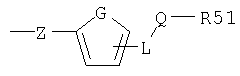
где G означает -С=С-, Z означает атом кислорода, L означает NH-группу, Q означает карбонил, a R51 означает прямую или разветвленную C1-С6алкильную группу; R6 означает группу CH2-N(R61)R62, где R61 независимо означает атом водорода, a R62 означает незамещенную бензильную группу, W и Х означают углерод, a Y означает азот; а также их соли с физиологически приемлемыми кислотами или основаниями. Также описываются применение производных хинолина и способ получения производных хинолина (варианты). 5 н. и 2 з.п. ф-лы, 1 табл.
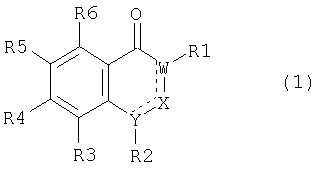
где R1 означает остаток сложного эфира карбоновой кислоты -CO-OR12, где R12 означает прямую или разветвленную алкильную цепь, содержащую 1-10 атомов углерода;
R2 означает группу -CH(R21)R22, где R21 означает атом водорода, a R22 означает замещенное атомом галогена или -CF3 фенильное кольцо или нафтильное кольцо;
R3 и R4 каждый независимо означает атом водорода;
R5 означает группу, присоединенную через остаток Z
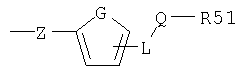
где G означает -C=C-, Z означает атом кислорода, L означает NH-группу, Q означает карбонил, a R51 означает прямую или разветвленную C1-С6алкильную группу;
R6 означает группу CH2-N(R61)R62, где R61 независимо означает атом водорода, a R62 означает незамещенную бензильную группу, W и Х означают углерод, a Y означает азот;
а также их соли с физиологически приемлемыми кислотами или основаниями.
осуществляют взаимодействие соединения общей формулы (2)
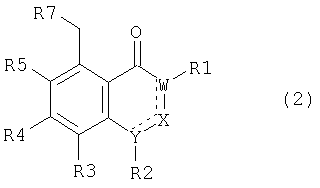
где R7 означает удаляемую группу, а все остальные остатки имеют значения, определенные выше для соединения (1), с соединением общей формулы (3)
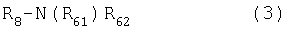
где R8 означает атом водорода или атом металла, a R61 и R62 имеют значения, определенные для соединения (1).
осуществляют взаимодействие соединения общей формулы (4)
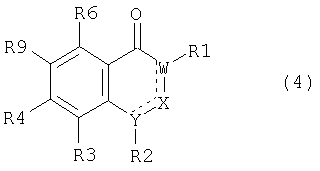
где R9 означает группу атом галогена или другую удаляемую группу, а другие остатки имеют значения, определенные для соединения (1), с соединением общей формулы (5)
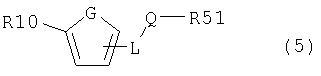
где R10 означает металлсодержащую группу или несодержащую металл группу, гидрокси- и меркаптогруппы в форме соли металла, группу -С≡С-R31 или группу -CR52=CR53R31 или -CR31=CR52R53 в Е- или Z-конфигурации, где R31 означает группу, содержащую металл или неметалл, а остальные остатки имеют значения, определенные для соединения (1), причем при необходимости взаимодействие проводят в присутствии катализатора.
осуществляют взаимодействие соединения общей формулы (6)
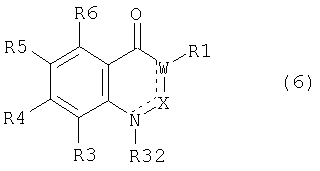
где R32 означает атом водорода или атом металла, а другие остатки имеют значения, определенные для соединения (1), с соединением общей формулы (7)

где R33 означает удаляемую группу, а R2 имеет значение, определенное для соединения (1), с получением соединения общей формулы (1), где Y означает атом азота.
| Бесколесный шариковый ход для железнодорожных вагонов | 1917 |
|
SU97A1 |
| US 5807869 А, 15.09.1998 | |||
| Бесколесный шариковый ход для железнодорожных вагонов | 1917 |
|
SU97A1 |
| RU 2056411 C1, 20.03.1996. | |||
Авторы
Даты
2006-07-20—Публикация
2002-02-21—Подача