Изобретение относится к области электротехники, а именно к созданию источников постоянного тока с высокой энергоемкостью и большим сроком службы. Оно может быть использовано как в отдельных элементах и батареях для бытовых приборов, так и для промышленных целей.
Известен химический источник тока в которых задача повышения энергоемкости решается за счет совместной работы минерального и органического электрода (Rn 2123741 Н 01 М 6/04) [1].
Известны химические источники тока, в которых эта задача решается за счет выбора конструкции электродов и специальных материалов для их покрытия (заявка №2000113905/09 Н 01 М 6/16) [2], сочетания материала электродов и электролита на основе фторидов (заявка №99121067/09) [3]. Наиболее близким к заявленному является источник постоянного тока (заявка №98115948/09) [4] на основе лития. Известный химический источник тока сдержит корпус, положительный электрод и систему «отрицательный электрод - электролит - активный компонент положительного электрода в виде оксигалоидного аниона». В качестве отрицательного электрода используют литий, литийсодержащий сплав, интеркалат лития или металл II-VIII групп, в качестве электролита - неводный или водный электролит, а в качестве оксигалоидного аниона - хлор в степени окисления +5 или бром в степени окисления +5 или +7, йод в степени окисления +5 или +7 или их смесь.
Техническая задача заключается в изготовлении гальванических источников тока с повышенной энергоемкостью, повышенным током разряда, а также большим сроком службы.
Технический результат достигается за счет использования в первичном источнике тока в качестве электролита гетерополикислоты 2-18 ряда, имеющей химическую формулу H6[P2W18O62] с активизированной электронной оболочкой анионного комплекса, который способен накапливать в себе заряды высокой плотности, делая тем самым вещество сильно реакционноспособным (патенты №2168289, №2218320. La Revue Polytechnique N 1620 Prix Nobel: la mecanique quantique a l honneur. Revue du palais de decouverte N 264, janvier 99. «Наука и жизнь» N 1, 1999 г. Нобелевские премии 1998 года.). Благодаря этому свойству, при пропускании постоянного электрического тока даже малой величины через гетерополикислоту, она начинает проявлять себя как сильнейший окислитель с выделением электрической энергии.
Сущность заявленного технического решения сводится к тому, что в гальваническом источнике постоянного тока, содержащем сосуд с электролитом, в котором размещены, один из металла, а другой из угля или графита, в качестве электролита использована гетерополикислота 2-18 ряда, имеющая химическую формулу H6[P2W18O62] с активизированной электронной оболочкой анионного комплекса, а внутренняя полость сосуда покрыта непроводящим инертным материалом, а металл катода выбран из ряда: медь, железо, никель, цинк, алюминий, марганец или свинец.
На чертеже представлен гальванический источник постоянного тока согласно настоящему изобретению он состоит из сосуда 1, внутренняя часть которого должна быть покрыта непроводящим инертным материалом (диэлектрическими полимерами, инертной смолой и т.д.). Сосуд может быть выполнен также из стекла или непроводящей керамики. В сосуд погружаются два электрода. В качестве анода используется угольный или графитовый электрод 2. В качестве катода используется металлический электрод 3, который может быть выполнен например из меди, железа, никеля, цинка, алюминия, магния или свинца. В сосуд с электродами заливают электролит 4 в виде 20-60%-ного раствора гетерополикислоты 2-18 ряда, имеющей химическую форму Н6[Р2W18O62] с активизированной электронной оболочкой анионного комплекса. Начинается реакция металла с кислотой. Химическую реакцию в общем виде можно записать следующим образом:
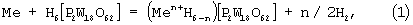
где n - степень окисления металла Me.
Степень окисления анионного комплекса не меняется. Металл, растворяясь в кислоте, отдает положительно заряженные ионы в раствор, при этом металлический электрод заряжается отрицательно. Между угольным или графитовым и металлическим электродом возникает разность потенциалов и, если к электродам подключить электрическую нагрузку 5, то в цепи возникнет электрический ток. Как уже говорилось, при воздействии даже слабого электрического постоянного тока, на катоде начинается окислительно-восстановительный процесс.
В общем виде его можно изобразить следующим образом:
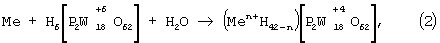
где n - степень окисления металла.
В водном растворе соединение диссоциирует на ионы (уравнение 3)
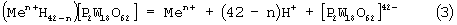
Вольфрам принимает на себя два электрона, изменяя степень окисления с +6 до +4. При этом анионный гетерополикомплекс изменяет свой заряд с 6- до 42-. В цепи возникает постоянный электрический ток.
На катоде выделяется газообразный кислород, который вновь окисляет восстанавливаемый комплекс до степени окисления 6-.
На чертеже большими стрелками показана окисленная форма геетерополикомплекса и черными восстановленная. Таким образом благодаря восстановлению на катоде происходит рециркуляция гетерополикомплекса (уравнение 2). В результате чего гальванический источник постоянного тока работает непрерывно.
Расходными материалами является гетерополикислота и вода. Последняя расходуется частично, так как связать полностью выделяющийся газовый кислород и водород практически не возможно.
Далее приведен пример работы конкретного источника постоянного тока согласно настоящему изобретению с медным и графитовым электродами и электролитом из 30% водного раствора гетерополикислоты.
В стеклянный сосуд 1 емкостью 500 мл погрузили медный и графитовый электрод 2, 3. Между ними установили электрическую нагрузку в виде сопротивления. Резистор номиналом 10 Ом, обозначенный на чертеже RH, и переключатель 5. В сосуд налили 30%-ный водный раствор гетерополикислоты 2-18 ряда и имеющую химическую формулу Н6[Р2W18O62] с активизированной электронной оболочкой анионного комплекса.
До того пока цепь не замкнута, произошла реакция взаимодействия меди с кислотой:
Cu+H6[P2W18O62]=CuH4[P2W18O62]+H2↑
Произошла реакция присоединения. Медь, растворяясь в кислоте, отдавая положительные заряженные ионы в раствор, зарядилась отрицательно. Между электродами возникла разность потенциалов.
Созданный таким образом гальванический источник тока будет работать до полной выработки кислоты.
Расход кислоты и воды на 1 Вт/ч электроэнергии составляет соответственно 10-9 г кислоты и 10-4 г воды.
Таким образом, используя в заявленном техническом решении в качестве электролита гетерополикислоту 2-18 ряда с активизированной электронной оболочкой анионного комплекса, который способен накапливать в себе заряды высокой плотности, делая тем самым выбранное в качестве электролита вещество сильно реактивноспособным, можно создавать источники постоянного тока с высокой энергоемкостью и большим сроком службы.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЩЕЛОЧНЫХ И ЩЕЛОЧНО-ЗЕМЕЛЬНЫХ МЕТАЛЛОВ | 2005 |
|
RU2283371C1 |
| СПОСОБ ПОЛУЧЕНИЯ СИНТЕТИЧЕСКОЙ САХАРОЗЫ | 2022 |
|
RU2799063C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЖИДКОГО УГЛЕВОДОРОДНОГО ТОПЛИВА ИЗ БИОМАССЫ РАСТИТЕЛЬНОГО ПРОИСХОЖДЕНИЯ | 2020 |
|
RU2733394C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИТИЯ ПУТЕМ ЭЛЕКТРОЛИЗА ИЗ ВОДНЫХ РАСТВОРОВ, СОДЕРЖАЩИХ ИОНЫ ЛИТИЯ | 2020 |
|
RU2742097C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЖИДКОГО БИОТОПЛИВА РАСТИТЕЛЬНОГО ПРОИСХОЖДЕНИЯ | 2020 |
|
RU2747560C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЖИДКИХ ОРГАНИЧЕСКИХ ТОПЛИВ ИЗ УГЛЕКИСЛОГО ГАЗА, ОКИСИ УГЛЕРОДА И ВОДЫ | 2015 |
|
RU2582125C1 |
| Электрохимическая твердотельная топливная ячейка | 2016 |
|
RU2628760C1 |
| ПОЛИМЕРНЫЙ ФОТОЭЛЕТРИЧЕСКИЙ МОДУЛЬ И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2013 |
|
RU2519937C1 |
| СПОСОБ ПОЛУЧЕНИЯ СИНТЕТИЧЕСКОЙ ЦЕЛЛЮЛОЗЫ | 2017 |
|
RU2663434C1 |
| Фотохимический способ преобразования электромагнитного излучения в электрическую энергию | 2020 |
|
RU2747914C1 |
Изобретение относится к области электротехники и может быть использовано при производстве гальванических источников постоянного тока. Техническим результатом изобретения является увеличение тока разряда и повышение электрической емкости. Согласно изобретению в источнике тока в качестве электролита используется гетерополикислота 2-18 ряда, имеющая химическую формулу H6[P2W18O62] с активизированной электронной оболочкой анионного комплекса, который способен накапливать в себе заряды высокой плотности, делая тем самым вещество сильно реакционноспособным. 1 ил.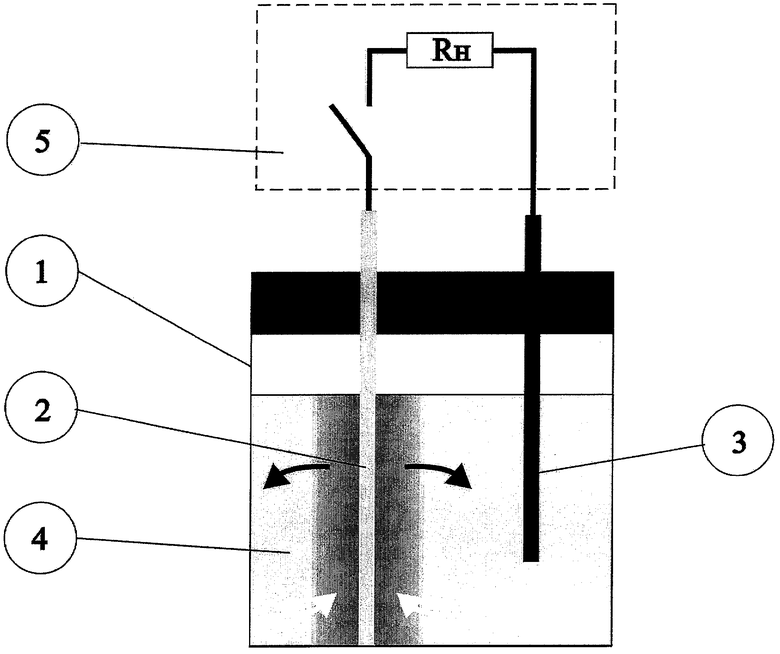
Гальванический источник постоянного тока, содержащий сосуд с электролитом, в котором размещены электроды, один из металла, а другой из угля или графита, отличающийся тем, что в качестве электролита использована гетерополикислота 2-18 ряда, имеющая формулу H6[P2W18O62] с активизированной электронной оболочкой анионного комплекса, внутренняя полость сосуда покрыта непроводящим инертным материалом, а металл катода выбран из группы: медь, железо, никель, цинк I, алюминий, марганец или свинец.
| ХИМИЧЕСКИЙ ИСТОЧНИК ТОКА | 1998 |
|
RU2144245C1 |
| US 5510209 А, 23.04.1999 | |||
| УСТРОЙСТВО для ФОРМИРОВАНИЯ в НАКОПИТЕЛЯХ | 0 |
|
SU211394A1 |
| ЭЛЕКТРОЛИТ НА ОСНОВЕ ПОВЕРХНОСТНО-АКТИВНЫХ ВЕЩЕСТВ | 1995 |
|
RU2123741C1 |
Авторы
Даты
2006-08-27—Публикация
2005-02-10—Подача