Изобретение относится к области электротехники и может быть использовано при эксплуатации устройств, реализующих элементы электрохимии, в частности в аккумуляторах, при электротравлении и пр.
Обычно электропроводящие среды с ионной проводимостью представляют собой, как правило, растворы кислот, щелочей и солей, диссоциирующих в растворителе на ионы, предусматривая наличие в данной системе по крайней мере двух элементов: растворителя и растворяющегося вещества, т. е. вещества, атомы или группы атомов которых обладают достаточно большим потенциалом для разделения их полярными молекулами растворителя с образованием разнополярных ионов, способных передавать заряды, в том числе и электрические. Такие среды используют обычно в обменных процессах, когда передача электрических зарядов сопряжена с осаждением ионизированных групп веществ на элементах, выполняющих функцию электродов, либо уносом вновь образующихся ионов с поверхности электрода в его расходном варианте. Подобные реакции обычно носят характер необратимых. Но это хорошо только в тех технологиях, где либо наносят покрытие, либо растворяют обрабатываемую поверхность, т. е. когда равновесная концентрация ионов поддерживается за счет растворяемого элемента.
Во всех же остальных случаях, когда расход электродов недопустим либо образующееся покрытие вредно, например, как в электроаккумуляторах, возникает противоречие между необходимостью передачи заряда ионов и восстановления его на электроде до химически инертного (нерастворимого) вещества и одновременной необходимостью сохранения поверхностей электродов для долговечной работы системы. Т. е. ионы должны лишь передавать заряд, но не должны взаимодействовать с электродами.
Таким образом, задача решается либо введением изолирующего слоя между электродом и объемом обычного бисистемного (растворитель + растворяемое вещество) электролита или замещением всего межэлектродного пространства одноосновным полярным веществом.
Известна широкая гамма поверхностно-активных веществ (ПАВ), функциональная особенность которых определяется наличием в их молекулах центров разной полярности, что определяет объективную возможность их поляризации электрическим током и использование в качестве электропроводящих сред. Подобными свойствами обладают сложные соли сильных кислот, органические соединения с активными элементами, например функциональные фторорганические соединения или соли щелочных металлов, а также некоторые другие соединения, имеющие ярко выраженный полярный характер. Функциональная особенность ПАВ выражается также во влиянии на поверхностное натяжение поверхностей раздела их фаз, что в свою очередь сказывается на увеличении подвижности частиц вещества относительно друг друга. Соответственно, учитывая их полярную природу, воздействие электрического поля вызывает в данном случае ориентацию силовых линий поля вдоль поверхностей раздела фаз вещества, спрямляя их, в свою очередь резко снижая внутреннее сопротивление среды и, следовательно, позволяет работать на значительно меньших напряжениях при сохранении номинала тока, что представляет существенное преимущество, особенно в условиях отрицательных температур при снижении емкости и напряжения, например, в электроаккумуляторах.
Известны технические решения по рецептуре электролитов с очень небольшими добавками ПАВ, решающие узкие, часто второстепенные задачи. Так, электролит по японской заявке N 46-290601 (опубл. 16.11.71, МКИ H 01 M 39/00, 39/04) имеет добавку амида никотиновой кислоты, снижающей выделение водорода на аноде.
Известен электролит на основе ПАВ по японской заявке N 593026 (опубл. 21.01.84, МКИ H 01 M 4/20) с добавками порошка фторопластовой смолы. Фторопласт обеспечивает хорошие условия для сдвига поверхностей сопряжения фаз среды, а ПАВ создает условия лишь электрического взаимодействия зарядов без разрушения электродов. Однако, приведенное решение предусматривает введение ПАВ на поверхность электродов механически без комплексного взаимодействия со средой электролита.
Известен электролит на основе ПАВ по заявке ФРГ N 3922100 (опубл. 10.01.91, МКИ H 01 M 2/16, 10/06) с добавками по крайней мере одного дополнительного ПАВ с отличающейся структурной формулой. Такое решение позволяет полярным молекулам ПАВ с разным потенциалом более равномерно заполнять межэлектродное пространство вдоль силовых линий электрического поля, концентрируя молекулы ПАВ с большим потенциалом около соответствующего по заряду электрода, сохраняя остальное пространство с электролитом заполненным полярными молекулами остальных добавок. Это также снижает внутреннее сопротивление среды. Однако ПАВ приведенных в заявке структурных формул недостаточно активны для решения всей совокупности сформулированных выше задач.
Наиболее близким по технической сущности и достигаемому результату аналогом-прототипом является электролит на основе ПАВ по патенту США N 5108856 (опубл. 28.04.94, МКИ H 01 M 6/16, 6/04) с добавкой ПАВ с гидрофильными и гидрофобными группами, позволяющими пространственное разделение функциональных свойств ПАВ относительно объема вокруг электродов и проводящей среды в целом. Однако эффективность данного решения существенно снижается, учитывая отсутствие прочных химических связей вводимого ПАВ с поверхностью электродов.
Целью изобретения является создание электропроводящей среды с ионной или ей подобной проводимостью, обеспечивающей одновременную коррозионную защиту электродов, а также придание ей свойств, определяющих существенное снижение внутреннего электросопротивления, особенно при отрицательных температурах.
Поставленная цель достигается тем, что электролит на основе ПАВ с добавками содержит фторорганическое сульфопроизводное общей формулы
RfSO2A,
где
Rf является альтернативой из ряда функционально однородных веществ типа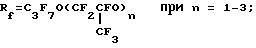
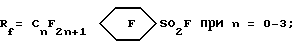
Rf = XCnF2n, X = F или Cl при n = 6 - 9;
Rf = H(CF2)nCH2O при n = 1 - 8;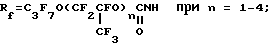
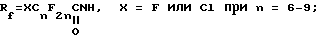
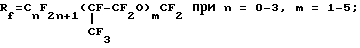
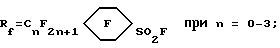
A является альтернативой из ряда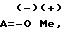
где
Me = K, Na, NH4, NH(Alk)3, Alk - алкил;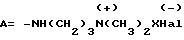
где
Hal = Cl, Br, J, при X = CH2CH2OH или CH2COOH;
или содержит фторсодержащее вещество общей формулы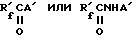
где
Rf является альтернативой из ряда функционально однородных веществ типа
R'f = XCnF2n, X = F или Cl при n = 6 - 9;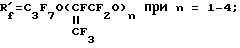
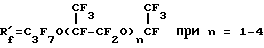
A' является альтернативой из ряда:
A' = CnH2n+1 при n = 1 - 3;
A' = NH4, K, Na, NH4(CH2)3N(CH3)2XHal, где Hal = J, Cl, Br; X = CH2CH2OH, CH2COOH;
A' = Cn H2n+1 при n = 1 - 3
или любые их комбинаторные сочетания в эффективном количестве 0,001 - 99,9 мас.%.
Кроме этого, электролит дополнительно содержит воду в количестве 0,1 - 99,9 мас.%.
Электролит дополнительно содержит минеральную кислоту в количестве 0,1 - 99,9 мас.%.
Электролит дополнительно содержит органический растворитель.
Ярко выраженная полярность молекул используемого в качестве основы (активного начала) электролита фторорганического сульфопроизводного или фторсодержащего вещества упомянутых общих формул или их комбинаторных сочетаний создает хорошие условия электропроводимости без переноса нерастворимых вновь образующихся при прохождении электролитических процессов веществ (как, например, в свинцовых аккумуляторах водород и сульфат свинца). ПАВ электролита входит в поверхностную химическую связь с веществом электрода без образования барьерных дополнительных соединений, являясь как бы естественным пространственным продолжением электропередающего средства (электрода), существенно смягчая этим процессы перенапряжения и, соответственно, значительно повышая емкость заряда. При комбинаторных сочетаниях выше перечисленных веществ последние выстраиваются вдоль силовых линий электрического поля в соответствии с их потенциалом, т. е. энергетической склонностью к электроду определенной полярности, равномерно заполняя объем межэлектродного пространства, создавая этим равномерное распределение проводящих элементов в объеме и одновременно создавая условия объемного накопления заряда, т. к. в этом случае заряды накапливаются не только на поверхностях раздела сред электрода и вещества электролита, но и на поверхностях раздела молекул электролита с разными потенциалами, учитывая их химическую связь лишь на полярном уровне и четкое разделение на самостоятельные заряженные группы.
Под добавками понимаются вещества стабилизаторы. В некоторых случаях ими могут быть естественные технологические загрязнители, такие как минеральные в виде коагулянтов или органические, например масла как естественные диэлектрические разделители поляризованных ячеек объемной электронакопительной среды. Причем, учитывая вязкую природу такого электролита в виде геля или стеариноподобного вещества, добавками могут стать и проводящие частицы в виде порошков графита или металлов.
Полярность молекул ПАВ основы электролита позволяет использовать как органические растворители, так и воду. Используемые растворители позволяют создавать составы, наиболее оптимальные для конкретных устройств, в которых требуется как различная вязкость среды, так и электрическая проводимость.
Добавка минеральной кислоты в сочетании с ранее введенной добавкой воды создает взаимодействующую бисистему минерального и органического электролитов. При этом ПАВ покрывает поверхность электродов за счет своей поверхностной активности, параллельно создавая хорошую электрическую связь электродов с органическим электролитом, окружающим пластины электродов, и минеральным, заполняющим пространство между ними, одновременно растворяя часть органики, улучшающей проводимость минеральной части электролита и, соответственно, снижающей внутреннее сопротивление системы в целом. Совместная работа минерального и органического электролитов создает саморегулирующуюся систему, автоматически воздействующую на процессы перенапряжения и управляющую оптимизацией объемного заряда, существенно повышая емкость устройств электронакопления и сглаживая технологические неоднородности прочих технологических процессов, в которых заявляемый электролит будет задействован.
Оценка степени достижения сформулированного технического результата за счет использования в электролите заявляемых поверхностно-активных веществ с добавками осуществлялась на экспериментальном стенде, включающем электрохимическую ячейку или каскад ячеек, соединенных последовательно, блок терморегулирования, нагрузочный блок, зарядно-разрядный блок и систему контрольно-измерительной аппаратуры.
Исследования влияния различных составов электролита проводились при температуре ячейки от +20 до -25oC и эффективном количестве активного начала от 0,001 мг до 1200 г на 1 л электролита измерением электрических характеристик ячейки в условиях саморазряда, выделения водорода, таких как сила разрядного тока, емкость, внутреннее сопротивление и др.
В табл. 1 - 4 представлены наиболее характерные результаты.
Для сравнения использовали стандартный сернокислотный электролит с плотностью 1,28 г/см2 при 25oC.
Для более удобного последующего цитирования формулам химических веществ, использованных в испытаниях, присвоены следующие условные наименования в рамках данной заявки:
Соединение 1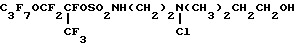
Соединение 2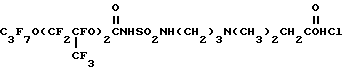
Соединение 3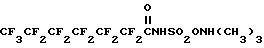
Соединение 4
Соединение 5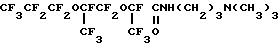
Соединение 6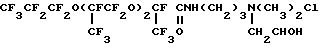
Соединение 7
CF3CF2CF2CF2CF2CF2 SO2ONH4
Соединение 8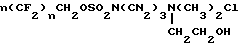
Соединение 9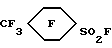
Соединение 10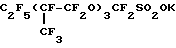
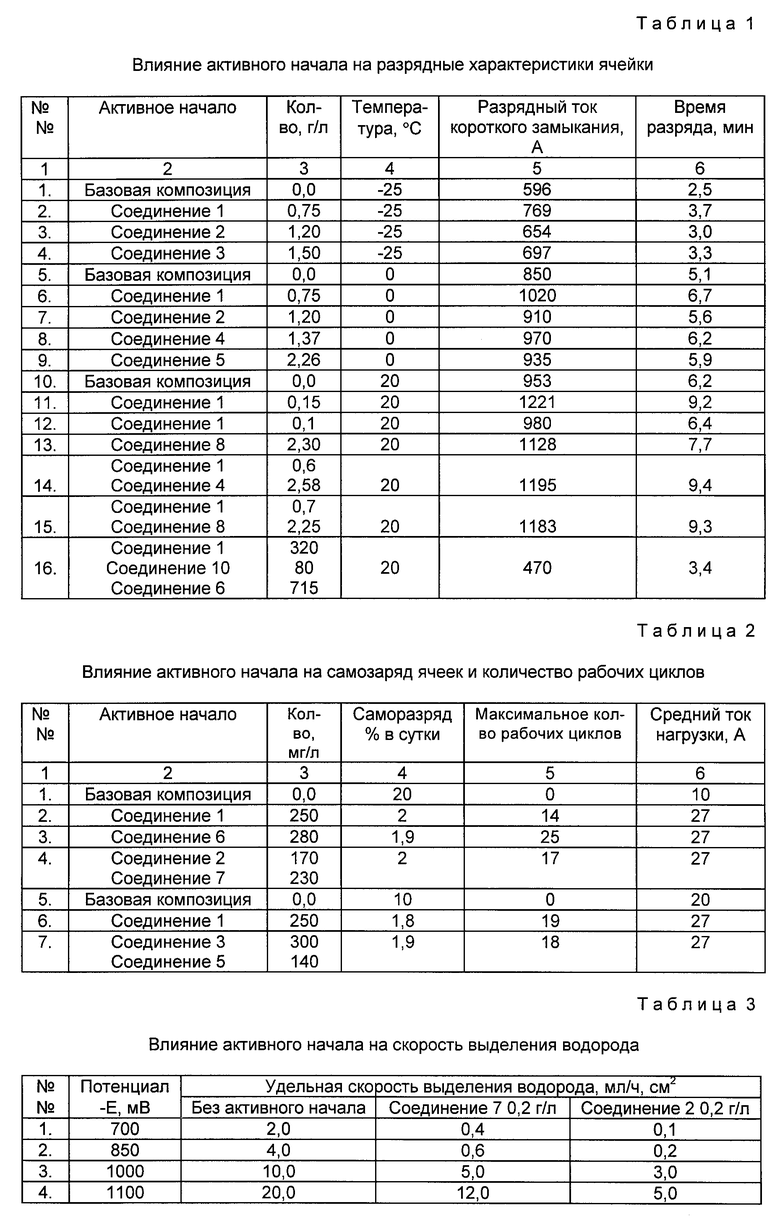
В табл. 1 показано влияние активного начала на разрядные характеристики ячейки.
В табл. 2 показано влияние активного начала на саморазряд ячеек и количество рабочих циклов.
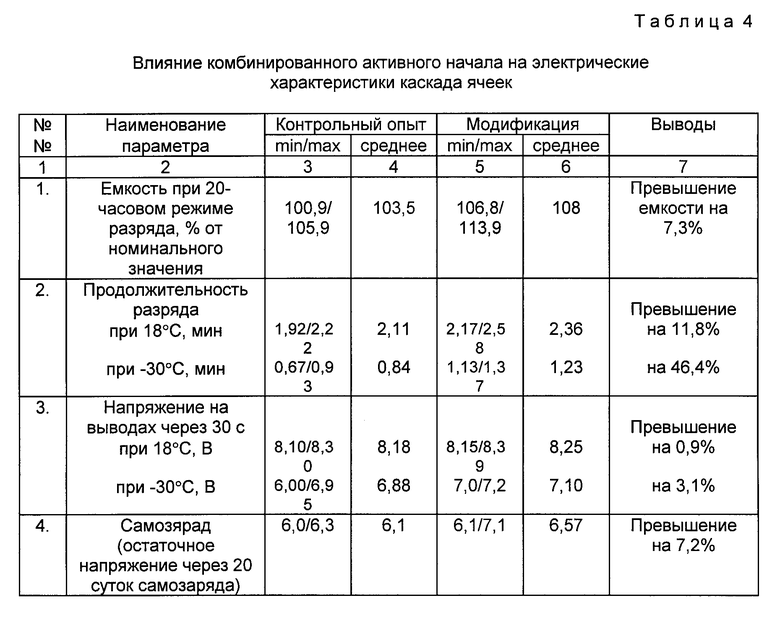
В табл. 3 показано влияние активного начала на скорость выделения водорода.
В табл. 4 показано влияние комбинированного активного начала на электрические характеристики каскада ячеек.
Примечание к табл. 4.
Состав активного начала: соединение 1+соединение 3+соединение 6 в количестве 120, 170 и 185 мг соответственно на 1 л электролита или 0,009; 0,013; 0,014 мас. % при суммарном содержании активного начала 0,040 мас.%. В испытаниях электролитов был использован каскад из 6 последовательно соединенных ячеек.
Результаты, приведенные в табл. 1 - 4, позволяют сделать вывод о доказанности причинно-следственных связей между модифицированным электролитом заявляемого состава и его существенными преимуществами по сравнению с прототипом.
Примеры, приведенные в табл. 1 - 4 охватывают лишь наиболее характерные результаты, полученные при испытаниях всей совокупности заявляемой композиции.
Не являясь оптимальными по составу, но тем не менее демонстрирующими появление означенного технического результата могут стать следующие примеры конкретного применения заявляемой композиции при граничных и других характерных значениях содержания активного начала.
1. Сернокислый электролит, содержащий соединение 1 в количестве 0,001 мас.%, имеет ток короткого замыкания 959 А, время разряда 6,2 мин при 20oC.
2. Электролит, содержащий 56,8 мас.% соединения 1, 26,6 мас.% соединения 4, 10, 3 мас.% соединения 7, 6, 2 мас.% соединения 10 и 0,1 мас.% воды, при 25oC и напряжении 2,8 В имеет саморазряд 0,17% в сутки.
3. Электролит, содержащий 99,899 мас.% воды, 0,1 мас.% кислоты и 0,001 мас.% соединения 7 при 25oC и напряжении 3,2 В.
4. Электролит, содержащий 99,899 мас.% кислоты и 0,1 мас.% соединения 10, имеет удельную скорость выделения водорода 0,083 мл (ч • см2) при потенциале ячейки 850 мВ.
5. Электролит, содержащий 2,2 мас.% соединения 7, 12,1 мас.% трифторметансульфокислоты в смесевом растворителе общей формулы (CF3)2CFO(CF2)nCF3 при n = 1 - 4, имеет разрядные характеристики ячейки: напряжение 3,4 В, время разряда 3,8 суток при 20oC.
Заявляемый электролит может быть реализован любыми веществами, сходными с упомянутыми по функциональному признаку в сочетании как с нейтральными носителями из круга традиционно применяющихся в композициях этого назначения, так и с заявляемыми добавками, обеспечивающими усиление основного технического результата в силу известных рассмотренных выше физических эффектов.
Изобретение может быть использовано в устройствах и технологических процессах любого назначения при предъявлении повышенных требований к чистоте и саморегулируемости электролитических процессов.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПЕПТИД, ОБЛАДАЮЩИЙ ИММУНОМОДУЛИРУЮЩЕЙ АКТИВНОСТЬЮ, И ПРЕПАРАТ НА ЕГО ОСНОВЕ | 1997 |
|
RU2142958C1 |
| МЕТАЛЛОГАЛОГЕННАЯ ЛАМПА | 1995 |
|
RU2084045C1 |
| КОМПОЗИЦИЯ ДЛЯ АМОРФНОГО ФОСФАТИРОВАНИЯ МЕТАЛЛИЧЕСКИХ ПОВЕРХНОСТЕЙ | 1998 |
|
RU2143012C1 |
| МОЮЩАЯ КОМПОЗИЦИЯ | 1994 |
|
RU2054035C1 |
| УСТРОЙСТВО ДЛЯ ЗАРЯДА АККУМУЛЯТОРНОЙ БАТАРЕИ | 1997 |
|
RU2126581C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ЭЛЕКТРОДОВ СВИНЦОВОГО АККУМУЛЯТОРА | 2000 |
|
RU2168804C1 |
| СОСТАВ ДЛЯ ИЗГОТОВЛЕНИЯ ПОЛИМЕРНОЙ ДИАФРАГМЫ ДЛЯ ЭЛЕКТРОЛИЗА ХЛОРИДОВ ЩЕЛОЧНЫХ МЕТАЛЛОВ И СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ | 1993 |
|
RU2102409C1 |
| СОСТАВ ДЛЯ ОБРАБОТКИ ПРИЗАБОЙНОЙ ЗОНЫ ПЛАСТА | 1995 |
|
RU2112871C1 |
| СПОСОБ ОБРАБОТКИ ПРИЗАБОЙНОЙ ЗОНЫ СКВАЖИНЫ | 1994 |
|
RU2068086C1 |
| СПОСОБ ИЗМЕРЕНИЯ ПОТЕНЦИАЛА РАБОЧЕГО ЭЛЕКТРОДА ЭЛЕКТРОХИМИЧЕСКОЙ ЯЧЕЙКИ ПОД ТОКОМ | 1996 |
|
RU2106620C1 |
Использование: химические источники тока, электрохимия. Сущность изобретения: электролит содержит фторорганическое сульфопроизводное общей формулы RfS O2A, где Rf является альтернативой из ряда функционально однородных веществ типа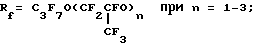
Rf = XCnF2n, X = F или Cl при n = 6-9;
Rf = H(CF2)nCH2O при n = 1-8;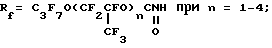
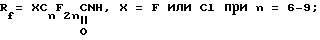
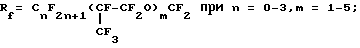
A является альтернативой из ряда 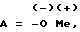 где Me = K, Na, NH4, NH(Alk)3, AlK - алкил:
где Me = K, Na, NH4, NH(Alk)3, AlK - алкил: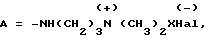 где Hal = Cl, Br, J при X = -CH2CH2OH или -CH2COOH;
где Hal = Cl, Br, J при X = -CH2CH2OH или -CH2COOH;
или содержит фторсодержащее вещество общей формулы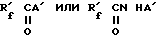
где R'f является альтернативой из ряда функционально однородных веществ типа
R'f = XCnF2n X = F или Cl при n = 6-9;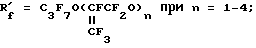
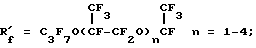
A' является альтернативой из ряда:
A' = CnH2n+1 при n = 1-3;
A' = NH4, K, Na, NH4(CH2)3N(CH3)2Xhal, где Hal = J, Cl, Br; X = CH2CH2OH, CH2COOH;
A' = CnH2n+1 при n = 1-3. Электролит имеет низкое внутренее электросопротивление, особенно при отрицательных температурах, и обеспечивает коррозионную защиту электродов. 3 з.п. ф-лы, 4 табл.
RfSO2A0
где Rf является альтернативой из ряда функционально однородных веществ типа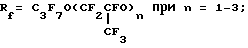
Rf = XCnF2n, X = F или Cl при n = 6 - 9; Rf = H(CF2)nCH2O при n = 1 - 8;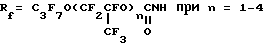
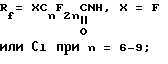
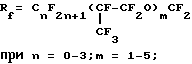
A является альтернативной из ряда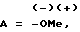
где Me = K, Na, NH4, NH(AlK)3, AlK-алкил;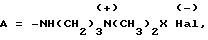
где Hal = Cl, Br, J, при X = -CH2CH2OH или -CH2COOH,
или содержит фторсодержащее вещество общей формулы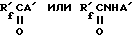
где 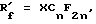 является альтернативой из ряда функционально однородных веществ типа
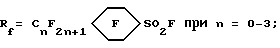
является альтернативой из ряда функционально однородных веществ типа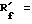 X = F или Cl при n = 6 - 9;
X = F или Cl при n = 6 - 9;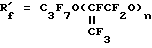
при n = 1 - 4;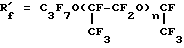
при n = 1 - 4;
A' является альтернативой из ряда
A' = CnH2n+1 при n = 1 - 3;
A' = NH4, K, Na, NH4(CH2)3 N(CH3)2X Hal, где Hal = J, Cl, Br; X = CH2CH2OH, CH2COOH;
A' = CnH2n+1 при n = 1 - 3, или любые их комбинаторные сочетания в эффективном количестве 0,001 - 99,9 мас.%.
| Способ изготовления звездочек для французской бороны-катка | 1922 |
|
SU46A1 |
| Устройство для охлаждения водою паров жидкостей, кипящих выше воды, в применении к разделению смесей жидкостей при перегонке с дефлегматором | 1915 |
|
SU59A1 |
| DE 3922100, H 01 M 2/16, 1991 | |||
| US 4108856, H 01 M 6/16, 1994. | |||
Авторы
Даты
1998-12-20—Публикация
1995-05-17—Подача