Предлагаемое изобретение относится к медицине, а именно к эндокринологии, и может быть использовано для прогнозирования развития сахарного диабета типа 1 (СД типа 1) у башкир, татар и русских Республики Башкортостан.
В настоящее время наблюдается рост заболеваемости СД типа 1 во всем мире. Это обусловлено рядом факторов, в том числе увеличением продолжительности жизни больных диабетом вследствие улучшения диагностической и лечебной помощи, повышением фертильности и ухудшением экологической ситуации.
Сахарный диабет, в том числе СД типа 1, является тяжким бременем для здравоохранения. Большая социальная значимость сахарного диабета состоит в том, что он приводит к ранней инвалидизации и летальности в связи с поздними сосудистыми осложнениями диабета, в числе которых - микроангиопатии (ретинопатия и нефропатия), макроангиопатии (инфаркт миокарда, инсульт, гангрена нижних конечностей), невропатии. Сахарный диабет - очень частая причина слепоты, смерти от уремии. У больного диабетом велик риск развития сердечно-сосудистых заболеваний. По данным доклада Комитета экспертов ВОЗ (1981), продолжительность жизни при развитии диабета в детском возрасте составляет около 30 лет.
Самым эффективным и экономичным направлением в диабетологии считают профилактику заболевания. Первичная профилактика предполагает формирование групп риска СД типа 1 с использованием молекулярно-генетических маркеров заболевания и меры предупреждения развития болезни. Применение разработанного способа обеспечит выявление лиц с высоким риском развития СД типа 1 для того, чтобы осуществить мероприятия по профилактике развития данной патологии.
Эндокринологическим научным центром РАМН разработаны методические рекомендации №2000/70 по медико-генетическому консультированию в семьях больных СД типа 1. В них предлагаются следующие методы определения повышенного генетического риска развития СД типа 1:
1. Эмпирический метод. Он предполагает определение абсолютного риска развития СД типа 1 у консультируемого лица по таблицам оценки эмпирического риска, созданным на основе многолетнего наблюдения за семьями больных СД типа 1.
2. Метод гаплоидентичности. Позволяет оценить риск развития СД типа 1 у здоровых лиц, имеющих а) больных СД типа 1 сибсов или б) родителей. Для этого необходимо провести молекулярно-генетическое исследование полиморфизма генов HLA-DRB1 и HLA-DQB1 а) консультируемого лица, больного сибса и их родителей, б) консультируемого лица и больного родителя. При идентичности консультируемого лица с а) больным сибсом или б) больным родителем по двум гаплотипам риск развития СД типа 1 у консультируемого лица оценивают как «высокий», по одному гаплотипу - «средний», по 0 гаплотипам - «низкий».
3. Метод HLA-типирования. Предполагает проведение у консультируемого лица молекулярно-генетического или серологического типирования генов (или антигенов) HLA-DRB1 (HLA-DR) и/или HLA-DQB1 (HLA-DQ) и/или DQA1 (HLA-DQ). При выявлении определенных аллелей (антигенов) или их комбинаций констатируют наличие «высокого», «среднего» или «низкого» риска развития СД типа 1 у консультируемого лица. Данный способ взят за прототип.
Таким образом, вышеперечисленные методы дают возможность прогнозировать развитие СД типа 1 как в семьях больных, так и в общей популяции в целом. Методы доступы по реактивам и оборудованию.
Однако данные методы имеют существенные недостатки:
1. Метод гаплоидентичности отличается высокой дороговизной и трудоемкостью, поскольку предполагает проведение молекулярно-генетического исследования одновременно двух высокополиморфных генетических локусов (HLA-DRB1, HLA-DQB1) у 2-4 лиц.
2. Методы гаплоидентичности и метод HLA-типирования не позволяют оценить риск развития СД типа 1 в количественном отношении.
3. Все три метода разработаны на основе изучения генетической предрасположенности к СД типа 1 в русской популяции г.Москвы, и поэтому не приемлемы для медико-генетического консультирования по СД типа 1 в других регионах, в частности в Башкортостане. Это обусловлено тем, что генетическая предрасположенность к СД типа 1, как и к другим многофакторным заболеваниям, формируется в зависимости от особенностей популяционно-генетической структуры этноса.
Задачей изобретения стала разработка объективного высокоинформативного способа прогнозирования развития СД типа 1, позволяющего в количественном отношении оценить риск возникновения данного заболевания у башкир, русских и татар, проживающих в Башкортостане.
Технический результат при использовании изобретения - повышение точности прогнозирования СД типа 1 у башкир, русских и татар, проживающих в Башкортостане.
Указанный технический результат достигается тем, что выделяют ДНК из лимфоцитов периферической венозной крови, методом полимеразной цепной реакции синтеза ДНК амплифицируют специфичности гена HLA класса II DQB1 и при выявлении аллеля DQB1*0302/07/08 и генотипа DQB1*02/DQB1*03 у башкир, аллеля DQB1*0302/08 у русских, специфичности DQB1*02 и аллеля DQB1*0302/08 у татар прогнозируют риск развития СД типа 1 у обследуемого.
Способ осуществляется следующим образом.
ДНК выделяют из лимфоцитов периферической крови. В качестве консерванта используют раствор следующего состава: 0,48% лимонной кислоты, 1,32% цитрата натрия, 1,47% глюкозы. При заборе крови к 1 мл консерванта добавляют 6 мл крови и хорошо перемешивают.
Для получения ДНК необходимой степени чистоты и достаточного молекулярного веса используется метод выделения ДНК из крови фенольно-хлороформной экстракцией, описанный Мэтью (Mathew C.C. The isolation of high molecular weight eukaryotic DNA // Methods in Molecular Biology / Ed. Walker J.M., N.Y., L.: Human Press. - 1984. - V.2. - P.31-34).
1. Кровь в пробирке с консервантом тщательно перемешивается и переливается в центрифужный стакан на 100 мл, туда же добавляют 50 мл охлажденного лизирующего буфера, содержащего 320 мМ сахарозы, 1% раствор тритона Х-100, 5 мМ MgCl2, 10 мМ трисHCl (рН 7,6).
2. Смесь центрифугируют 20 мин при 4000 об/мин.
3. Надосадочную жидкость сливают, к получившемуся осадку приливают 8 мл 25 мМ ЭДТА, рН 8,0, суспензируют.
4. К суспензии добавляют 0,8 мл 10% SDS и протеиназу К (концентрация - 10 мг/мл). Смесь для лизиса оставляют на ночь в термостате при температуре 38°С.
Экстракцию ДНК осуществляют в следующем порядке.
1. Для депротеинизации к лизату добавляют 0,5 мл 5М перхлората натрия и 8 мл фенола, насыщенного 1М трисHCl до рН 7,8.
2. Смесь центрифугируют при 3000 об/мин в течение 10 мин.
3. Отбирают водную фазу, содержащую ДНК, РНК и неденатурированные белки.
4. Отобранную фазу обрабатывают смесью фенол-хлороформа (1:1), а затем - хлороформом.
5. Препараты осаждают двумя объемами 96% этанола.
6. Образовавшийся осадок ДНК растворяют в 1,5 мл деионизированной Н2О; раствор хранят при -20°С.
В дальнейшем полученную ДНК используют в качестве матрицы для мультипраймерной полимеразной цепной реакции (ПЦР) для амплификации нужного фрагмента гена HLA-DQB1. Применяют набор реагентов для типирования гена HLA-DQB1 фирмы «Protrans» (Германия).
Амплификацию специфичностей гена DQB1 проводят в реакционной смеси, содержащей 35 мкл геномной ДНК (концентрация 50-300 нг/мкл), 1,1 мкл Taq-полимеразы (5 Ед/мкл), 46 мкл буфера R, 93 мкл буфера Y. Реакционную смесь распределяют по 10 мкл в 16 эппендорфов, но дно которых нанесены олигонуклеотидные праймеры. Режим амплификации следующий: начальная денатурация при 94°С в течение 2 мин; 10 циклов, включая денатурацию при 94°С - 10 с, отжиг, праймеров и синтез ДНК при 65°С - 1 мин; 20 циклов, включая денатурацию при 94°С - 10 с, отжиг праймеров при 61°С - 50 с, синтез ДНК при 72°С - 30 с. Амплифицированные фрагменты ДНК разделяют электрофоретически в 1% агарозном геле и после окрашивания геля бромидом этидия идентифицируют в ультрафиолетовом свете. В качестве электролита для электрофореза применяют 0,5Х боратный буфер (0,089 М трисHCl, рН 7,9; 0,089 М борная кислота, 0,002 ЭДТА с рН 8,0).
Электрофорез проводят при постоянном напряжении 150 В после 5-минутного преэлектрофореза. Детекцию результатов проводят путем, окрашивания агарозного геля бромистым этидием в течение 10 минут с последующей визуализацией в ультрафиолетовом света на трансиллюминаторе. Продукт амплификации виден в виде светящейся полосы красно-оранжевого цвета.
Идентифицированные аллели гена HLA-DQB1 классифицировались согласно общепринятой в мире номенклатуре (Nomenclature for factors of the HLA system, 1995 / J.G.Bodmer, S.G.E.Marsh, E.D.Albert [et al.] // Hum. Immunol. - 1995. - Vol.43. - P.149-164).
Нами были исследованы образцы ДНК у 107 больных СД типа 1. Контрольная группа включала 92 здоровых добровольных доноров без клинических и лабораторных признаков сахарного диабета и имеющих неотягощенный семейный анамнез по сахарному диабету.
В группе больных СД типа 1 башкир (n=32) по сравнению со здоровыми лицами той же этнической принадлежности (n=40) установлена достоверно более высокая частота встречаемости аллеля DQB1*0302/07/08 (12,1% и 0,0% соответственно, Р<0,05) и генотипа DQB1*02/DQB1*03 (34,4% и 7,5% соответственно, Р<0,05). Среди больных СД типа 1 русских (n=30) достоверно чаще встречаются обладатели аллеля DQB1*0302/08 (28,8% относительно 11,8% в контрольной выборке лиц (n=30) той же этнической принадлежности, Р<0,05). В когорте татар, страдающих СД типа 1 (n=45), в сравнении со здоровыми представителями той же этнической принадлежности (n=22), обнаружено большее количество людей, имеющих в своем генотипе специфичность DQB1*02 (33,7% и 15,9% соответственно, Р<0,05) и аллель DQB1*0302/08 (26,1% и 6,8% соответственно, Р<0,05).
Таким образом, повышенный генетический риск СД типа 1 у башкир ассоциирован с аллелем DQB1*0302/07/08 и генотипом DQB1*02/DQB1*03; у русских - с аллелем DQB1*0302/08; у татар - с аллелем DQB1*0302/08 и специфичностью DQB1*02. Для количественной оценки относительного риска развития заболевания для каждого из вышеуказанных генетических маркеров мы вычислили показатель соотношения шансов (odds ratio - OR). Для этого мы использовали формулу, предложенную Бландом (Bland, J.M. The odds ratio / J.M.Bland, D.G.Altman // Br. Med. J. - 2000. - Vol.320. - P.1468):
OR=(a×d)/(b×c)
где a - число лиц с наличием, b - с отсутствием маркера (аллеля или генотипа) среди больных; c и d - число лиц соответственно с наличием и отсутствием маркера среди здоровых. Повышенный риск развития СД типа 1 констатируют при OR>1.
Приводим пример конкретного расчета. В группе больных СД типа 1 башкир идентифицировано 11 человек, имеющих генотип DQB1*02/DQB1*03, т.е. а=11. У 21 больного СД типа 1 генотип DQB1*02/DQB1*03 не идентифицирован, поэтому b=21. В выборке здоровых башкир выявлено 3 лица с генотипом DQB1*02/DQB1*03, следовательно, с=3. Среди башкир контрольной группы генотип DQB1*02/DQB1*03 не обнаружен у 37 человек, это значит, что d=37. Подставив эти значения в вышеприведенную формулу, получим:
OR=(11×37)/(21×3)=407/63=6,46.
Следовательно, у башкир, имеющих генотип DQB1*02/DQB1*05, риск развития СД типа 1 повышен в 6,46 раз по сравнению с лицами, обладающими любым другим генотипом. Вычисленные по результатам исследования показатели OR в дальнейшем используются в ходе медико-генетического консультирования по СД типа 1.
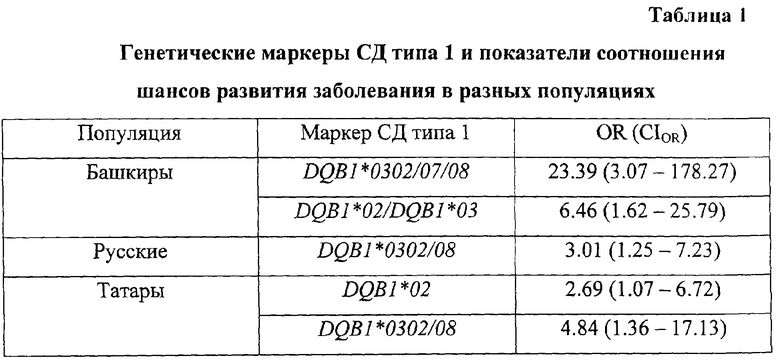
Полученные в нашем исследовании показатели OR при наличии маркерных специфичностей, аллелей и генотипов гена DQB1 представлены в табл.1.
Пример 1.
Больная К., 13 лет, поступила в эндокринологическое отделение по направлению участкового педиатра. При поступлении предъявляла жалобы на жажду, учащенное мочеиспускание, похудание, слабость, боли в животе, тошноту.
Анамнез: старшая сестра больной страдает СД типа 1, получает постоянную заместительную инсулинотерапию по интенсифицированной схеме.
Соматический статус: состояние девочки тяжелое. Сознание не нарушено. Правильного телосложения, пониженного питания. Кожа сухая, рубеоз щек. Тургор мягких тканей снижен. Дыхание шумное, глубокое, с участием вспомогательной мускулатуры. Аускультативно в легких жесткое дыхание. Тоны сердца приглушены. Пульс 108 уд. в минуту. Артериальное давление 110/70 мм рт.ст. Язык обложен густым коричневым налетом. В выдыхаемом воздухе - резкий запах ацетона. Живот при пальпации болезненный в околопупочной области. Печень у края реберной дуги. Симптом «поколачивания» отрицательный. Отеков нет. Мочеиспускание учащенное, безболезненное. Стула не было 2 дня.
Лабораторные исследования: гликемический профиль в течение дня 800 ч - 8.7 ммоль/л, 100 ч - 12.8 ммоль/л, 1300 ч - 9.7 ммоль/л, 1500 ч - 11.9 ммоль/л, 2200 ч - 11.7 ммоль/л; удельный вес мочи 1042, глюкозурия 4%, кетонурия 4(+); в биохимическом анализе крови выявлена гипокалиемия (К+ 3.9 ммоль/л).
Клинический диагноз: сахарный диабет типа 1, впервые выявленный. Диабетический кетоацидоз.
Результаты генотипирования: для выявления генотипа гена HLA класса II DQB1 у больной было взято 4 мл венозной крови с последующим выделением ДНК методом фенольно-хлороформной экстракции и амплификацией специфичностей гена DQB1 с использованием коммерческого набора фирмы Protrans (Германия). Амплификацию специфичностей гена DQB1 проводили в реакционной смеси, содержащей 35 мкл геномной ДНК (концентрация 50-300 нг/мкл), 1,1 мкл Taq-полимеразы (5 Ед/мкл), 46 мкл буфера R, 93 мкл буфера Y, распределенной по 10 мкл в 16 эппендорфов, но дно которых нанесены олигонуклеотидные праймеры. Электрофорез фрагментов ДНК проводили в агарозном геле при постоянном напряжении. После окончания электрофореза гель окрашивали раствором бромистого этидия в течение 10 мин. И анализировали при ультрафиолетовом освещении на трансиллюминаторе. У обследованной больной изучение специфичностей гена DQB1 позволило выявить наличие генотипа *02/*0302/08. Учитывая этническую принадлежность пациентки (русская), показатель соотношения шансов развития СД типа 1 составил для нее 3,01 (см. табл.1).
Вывод: учитывая отягощенный семейный анамнез, у наблюдаемой пациентки необходимо было провести генетический анализ на доклиническом уровне СД типа 1, что позволило бы определить высокий риск развития данного патологического состояния и вовремя принять профилактические меры для предупреждения развития как самого заболевания, так и его острого осложнения (кетоацидоз).
Пример 2.
Пациент Г, 28 лет, болен СД типа 1 в течение 1 года, состоит на учете у эндокринолога одной из поликлиник г.Уфы. Обратился к врачу-генетику с просьбой оценить риск развития СД типа 1 у его трехлетней дочери. Супруга здорова, больных СД типа 1 родственников не имеет.
Результат генотипирования ребенка: для выявления генотипа гена HLA класса // DQB1 у ребенка было взято 4 мл венозной крови с последующим выделением ДИК методом фенольно-хлороформной экстракции и амплификацией специфичностей гена DQB1 с использованием коммерческого набора фирмы Protrans (Германия). Амплификацию специфичностей гена DQB1 проводили в реакционной смеси, содержащей 35 мкл геномной ДНК (концентрация 50-300 нг/мкл), 1,1 мкл Taq-полимеразы (5 Ед/мкл), 46 мкл буфера R, 93 мкл буфера Y, распределенной по 10 мкл в 16 эппендорфов, но дно которых нанесены олигонуклеотидные праймеры. Электрофорез фрагментов ДНК проводили в агарозном геле при постоянном напряжении. После окончания электрофореза гель окрашивали раствором бромистого этидия в течение 10 мин. И анализировали при ультрафиолетовом освещении на трансиллюминаторе. У обследованного ребенка изучение специфичностей гена DQB1 позволило выявить наличие генотипа *02/*05. Учитывая этническую принадлежность ребенка (татарка), показатель соотношения шансов развития СД типа 1 при наличии в генотипе специфичности DQB1*02 составляет 2,69 (см. табл.1).
Вывод: учитывая высокий генетический риск СД типа 1 у дочери пациента, родителям были предложены превентивные мероприятия, включающие исключение из рациона ребенка продуктов с нитрозосодержащими консервантами и красителями, профилактический прием никотинамида (20-25 мг/кг массы тела в сутки).
Катамнез: предложенные превентивные мероприятия осуществляются в течение 2 лет. При ежегодном иммунологическом, гормональном и метаболическом мониторинге ребенка данных за раннюю доклиническую фазу СД типа 1 не выявлено.
Таким образом, полученные данные указывают на несомненную связь между полиморфизмом гена HLA-DQB1 с генетической предрасположенностью к сахарному диабету типа 1 у жителей Башкортостана, что дает возможность прогнозировать риск возникновения сахарного диабета типа 1 и проводить превентивную терапию.
Предложенный способ современен и позволяет с высокой степенью достоверности прогнозировать развитие СД типа 1.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ САХАРНОГО ДИАБЕТА ТИПА 1 В ПОПУЛЯЦИЯХ НАРОДОВ БАШКОРТОСТАНА | 2008 |
|
RU2368325C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ПЫЛЬЦЕВОЙ БРОНХИАЛЬНОЙ АСТМЫ | 2010 |
|
RU2441242C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА ВОЗНИКНОВЕНИЯ ПЕРЕЛОМОВ | 2012 |
|
RU2526189C2 |
| Способ прогнозирования развития острого панкреатита у жителей Республики Башкортостан | 2020 |
|
RU2731693C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА ВОЗНИКНОВЕНИЯ РЕЦИДИВОВ У БОЛЬНЫХ ЛЕПРОЙ | 2008 |
|
RU2373529C1 |
| СПОСОБ ВЫЯВЛЕНИЯ ПРЕДРАСПОЛОЖЕННОСТИ И РЕЗИСТЕНТНОСТИ К ЗАБОЛЕВАНИЮ ЦИСТНЫМ ЭХИНОКОККОЗОМ У ДЕТЕЙ | 2008 |
|
RU2387383C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ НАГНОЕНИЯ ОДНОКАМЕРНОЙ ЭХИНОКОККОВОЙ КИСТЫ У ИНВАЗИРОВАННЫХ ДЕТЕЙ | 2007 |
|
RU2348039C1 |
| СПОСОБ ГЕНЕТИЧЕСКОГО ПРОГНОЗИРОВАНИЯ ТУБЕРКУЛЕЗА ОРГАНОВ ДЫХАНИЯ | 2009 |
|
RU2406447C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ БРОНХИАЛЬНОЙ АСТМЫ | 2012 |
|
RU2510508C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ БРОНХИАЛЬНОЙ АСТМЫ | 2006 |
|
RU2324937C1 |
Изобретение относится к медицине, а именно к эндокринологии, и касается способа прогнозирования развития сахарного диабета типа 1 в популяциях народов Башкортостана. Сущность изобретения заключается в выделении ДНК из лимфоцитов периферической венозной крови методом полимеразной цепной реакции синтеза ДНК, амплифицикации специфичности гена HLA класса II DQB1. При выявлении аллеля DQB1*0302/07/08 и генотипа DQB1*02/DQB1*03 у башкир, аллеля DQB1*0302/08 у русских, специфичности DQB1*02 и аллеля DQB1*03 02/08 у татар прогнозируют риск развития СД типа 1 у обследуемого. Преимущество изобретения заключается в разработке прогноза развития заболевания.
Способ прогнозирования развития сахарного диабета (СД) типа 1, включающий выделение ДИК из лимфоцитов периферической венозной крови, амплификацию специфичности гена HLA класса II DQB1 методом полимеразной цепной реакции синтеза ДНК, отличающийся тем, что при выявлении аллеля DQB1*0302/07/08 и генотипа DQB1*02/DQB1*03 у башкир, аллеля DQB1*0302/08 у русских, специфичности DQB1*02 и аллеля DQB1*0302/08 у татар прогнозируют риск развития СД типа 1 у обследуемого.
| ALHARBI Е.М | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Clin | |||
| Diagn | |||
| Lab | |||
| Jmmunol | |||
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| GALGANI A et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Hum | |||
| Jmmunol. | |||
Авторы
Даты
2006-10-20—Публикация
2005-02-08—Подача