Изобретение относится к области медицины, а именно к аллергологии и иммунологии, и может быть использовано для прогнозирования развития пыльцевой бронхиальной астмы.
Из практики медицины известен способ прогнозирования пыльцевой бронхиальной астмы (Woszczek G., Kowalski M.I., Borowiec M. Association of asthma and total IgE levels with human leukocyte antigen-DR in patients with grass allergy // Eur Respir J. - 2002. - Vol.20. - P.79-85), заключающийся в типировании генов HLA II класса.
Недостатком способа является то, что способ известен только у больных пыльцевой аллергией польской национальности. Известно, что существуют межрасовые, межэтнические и внутриэтнические различия между одним и тем же заболеванием и аллельными вариантами генов HLA. Следовательно, в разных популяционных группах HLA-маркерами пыльцевой аллергии могут быть разные варианты HLA-генов и HLA-гаплотипов. Это обстоятельство не позволяет применить известный способ прогнозирования пыльцевой бронхиальной астмы.
Изобретение направлено на повышение точности прогнозирования развития пыльцевой бронхиальной астмы.
Указанный технический результат достигается тем, что в венозной крови методом полимеразной цепной реакции определяют гены локусов DRB1 и DQB1 системы HLA и при наличии специфичностей HLA-DRB1*01 и/или DQB1*05 прогнозируют высокий риск развития пыльцевой бронхиальной астмы у больных сезонным аллергическим ринитом; при наличии специфичности HLA-DQB1*06 прогнозируют резистентность к развитию пыльцевой бронхиальной астмы у больных сезонным аллергическим ринитом.
Известно, что у лиц, сенсибилизированных к аллергенам пыльцы, чаще всего наблюдают клинику аллергического риноконъюнктивита и пыльцевой бронхиальной астмы. Неясно, почему у одних пациентов атопический процесс ограничивается аллергическим ринитом, в то время как у других развивается клиническая картина пыльцевой бронхиальной астмы. Как известно, поллиноз является полигенным заболеванием со сложным типом наследования. Еще в 70-е годы XX века серологическими методами было установлено, что пыльцевая аллергия является заболеванием, ассоциированным с генами HLA. В результате перехода с серологического типирования HLA-антигенов на молекулярно-генетические методы идентификации на основе полимеразной цепной реакции появились огромные возможности изучения непосредственно полиморфизма генов HLA, а также их роли в развитии атопических заболеваний, в том числе поллиноза. Подобные исследования, относящиеся к предсказательной медицине, позволят формировать группы риска не только по пыльцевой аллергии, но и по развитию пыльцевой бронхиальной астмы у больных сезонным аллергическим ринитом. Это особенно ценно при планировании стратегических первичных профилактических мер.
Все вышесказанное дает основание для применения способа прогнозирования развития пыльцевой бронхиальной астмы у больных поллинозом.
Представленным способом апробирована группа из 61 человека - коренных жителей Астраханской области русской национальности, страдающих пыльцевой аллергией. Случайным образом нами были отобраны пациенты, находившиеся на стационарном лечении на аллергологических койках Александро-Мариинской областной клинической больницы г.Астрахани или обратившиеся за медицинской помощью к аллергологу-иммунологу консультативной поликлиники Александро-Мариинской областной клинической больницы г.Астрахани. Контрольную группу составили 94 здоровых донора - коренных астраханцев русской национальности, не имевших аллергической патологии.
У всех пациентов было проведено аллергологическое обследование, которое включало: сбор подробного аллергологического анамнеза, кожное аллергологическое тестирование, определение общего IgE в сыворотке крови.
Кожное тестирование осуществлялось при помощи скарификационных кожных проб с водно-солевыми экстрактами аллергенов из пыльцы растений производства ФГУП НПО «Аллерген» (г.Ставрополь). В 1 мл водно-солевого экстракта каждого аллергена содержалось 10000 PNU. Диагностический набор включал 23 пыльцевых аллергена: лещина, ольха, дуб, береза, ясень, клен, тимофеевка, овсяница, ежа, рожь, мятлик, райграс, лисохвост, пырей, кукуруза, конопля, полевица, одуванчик, лебеда, амброзия, подсолнечник, полынь, циклахена. Кожное тестирование проводилось в период ремиссии заболевания вне сезона цветения растений.
Метод типирования антигенов HLA II класса. Определение аллелей HLA-DRB1 и HLA-DQB1 генов в основной группе проводили методом полимеразной цепной реакции (ПЦР) с помощью наборов реагентов «Biotest» (Германия). В контрольной группе HLA-типирование проводилось с помощью коммерческих наборов «HLA-ДНК-ТЕХ» (научно-производственное объединение «ДНК-Технология», Москва, Россия).
Геномную ДНК для исследования выделяли из мононуклеарных клеток стабилизированной EDTA периферической крови, свежей или свежезамороженной и сохраняемой при -20°С. Кровь в количестве 500,0 мкл центрифугировали при 13000g в течение 1 минуты в пластиковой пробирке типа «Eppendorf». Затем эритроциты удаляли путем обработки осадка 500,0 мкл лизирующего буфера (0.32М сахарозы; 10 mM трис-HCl (рН 7,5); 5 mM MgCl2; 2,1% тритона Х-100) с последующим центрифугированием при 13000g в течение 1 минуты. Процедуру лизиса повторяли до тех пор, пока надосадочная жидкость не становилась совершенно прозрачной (до 6 раз).
После окончательного удаления надосадочной жидкости при помощи автоматического дозатора к осадку добавляли 60,0 мкл буфера (50 mM KСl; 10 mM трис-HCl (рН 8,3); 2,5 ml MgCl2; 0,45% NP-40; 0,45% Tween 20), содержащего 250 мкг/мл протеиназы К, и ресуспендировали. Инкубировали с ферментом в течение 60 минут при t=+55°C.
Инактивацию протеиназы после инкубации проводили нагреванием пробирки на водяной бане при t=+95°C в течение 10 минут. После остывания конденсат осаждали центрифугированием при 13000g в течение 10-15 секунд. Раствор ДНК хранили при +4°С до использования.
Типирование аллелей HLA-DRB1-гена. Определение аллелей HLA-DRB1-гена проводили с использованием набора сиквенс-специфических праймеров, позволяющих определить 13 групп аллелей (базовое разрешение): DRB1*01, 03, 04, 07, 08, 10, 11, 12, 13, 14, 15, 16. Амплификацию проводили в 2 этапа:
1 этап - амплификация II экзона DRB1-гена из выделенной ДНК. Проводилась по следующему температурно-временному режиму:
1. 94°С - 1 минута
2. 93°С - 0 минут 20 секунд
60°С - 0 минут 5 секунд (7 циклов)
3. 92°С - 0 минут 1 секунда
65°С - 0 минут 1 секунда (28 циклов).
Продукт амплификации первого этапа длиной 247 пар нуклеотидов после 10-кратного разведения разбавителем использовался как исследуемый материал на втором этапе типирования.
2 этап - серия амплификации со специфическими парами праймеров по следующему температурно-временному режиму:
93°С - 0 минут 1 секунда
65°С - 0 минут 2 секунды (15 циклов).
Продукт, полученный в ходе амплификации, определяли методом горизонтального электрофореза в окрашенном бромистым этидием 3,3%-ном агарозном геле в ультрафиолетовом свете (310 нм). Специфичность продукта амплификации на всех этапах исследования оценивали в соотношении со стандартным маркером длин ДНК (PUC-19).
Типирование аллелей HLA-DQB1-гена. Определение аллелей HLA-DQB1-гена проводили с использованием набора сиквенс-специфических праймеров, позволяющих определить 9 специфичностей DQB1*0201, 0301, 0302, 0303, 0304, 0305, 0401/02, 05, 06.
Амплификацию проводили в два этапа:
1 этап - амплификация II экзона DQB1-гена из выделенной ДНК проводилась по следующему температурно-временному режиму:
1. 94°С - 2 минуты
2. 94°С - 0 минут 20 секунд
69°С - 0 минут 5 секунд (7 циклов)
3. 93°С - 0 минут 1 секунда
67°С - 0 минут 2 секунды (28 циклов)
4. 93°С - 0 минут 1 секунда
60°С - 0 минут 2 секунды (7 циклов).
Продукт амплификации первого этапа длиной 264 пары нуклеотидов после 10-кратного разведения разбавителем использовали на следующих этапах типирования как исследуемый материал.
2 этап - серия амплификации со специфическими парами праймеров, позволяющими определить отдельные аллели по следующему температурно-временному режиму:
93°С - 0 минут 1 секунда
67°С - 0 минут 2 секунды (12 циклов).
Продукт, полученный в ходе амплификации, определяли методом горизонтального электрофореза в 3,3%-ном агарозном геле. Специфичность продукта амплификации на всех этапах исследования оценивали в соотношении со стандартными маркерами длин ДНК (PUC-19).
При обработке полученных результатов были использованы методы статистического анализа. Для оценки результатов типирования вычислялись частоты антигенов HLA. Частоты гаплотипов HLA вычислялись непрямым методом с использованием показателя степени неравновесного сцепления по формуле Маттиуса. Для определения показателя достоверности результатов рассчитывался непараметрический критерий X2 с поправкой Йетса. Значение X2, превышавшее 3,841 (что соответствует р<0,05), рассматривалось как показатель достоверной разницы между частотами в сравниваемых группах. Для повышения точности результатов анализа использовалась поправка Бонферрони. Для определения силы ассоциации между гаплотипом и изучаемым заболеванием рассчитывался показатель относительного риска (RR) для малых выборок по формуле Holdene-Woolf. Величина RR, равная 1, указывает на отсутствие различий в частоте встречаемости антигенов HLA у больных и в контроле. RR>1 (положительная ассоциация) означает, что данная специфичность HLA чаще регистрируется в группе больных. Этиологическая фракция (или атрибутивный риск) вычислялась для RR>1. Наибольшая величина этиологической фракции указывает на первичность ассоциативной связи исследуемой патологии с конкретным антигеном HLA. Если RR<1 (отрицательная ассоциация), то определяется величина превентивной фракции (PF). Величина PF показывает ту часть случаев, когда заболевание не развилось благодаря наличию ассоциированного HLA-гена.
Нами проведен сравнительный анализ HLA-фенотипов больных поллинозами (1 группа), сезонным аллергическим ринитом (2 группа), пыльцевой бронхиальной астмой (3 группа) и здоровых лиц (таблица 1). Сравнительная оценка в локусе DR динамики частотных характеристик для таких аллельных групп как HLA-DRB1*16(02), DRB1*17(03), DRB1*04, DRB1*11(05), DRB1*12(05), DRB1*14(06), DRB1*09 и DRB1*10 не показала статистически различий от контрольных значений как в общей группе «поллинозы», так и в выборках «сезонный аллергический ринит» и «пыльцевая бронхиальная астма».
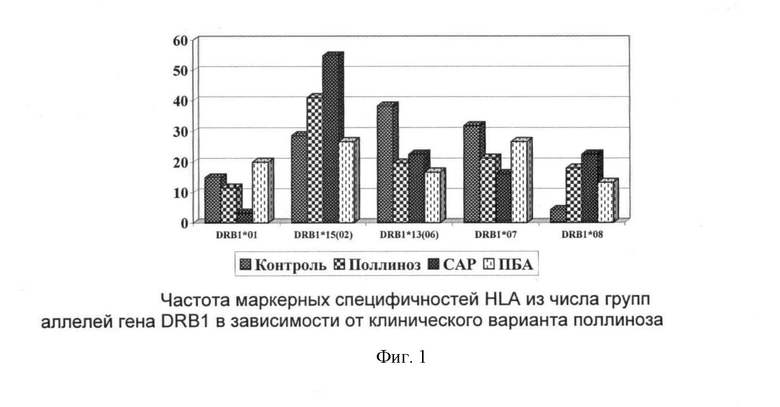
Частотная характеристика таких маркерных специфичностей HLA локуса DR как HLA-DRB1*01, DRB1*15(02), DRB1*13(06), DRB1*07 и DRB1*08 в зависимости от клинического варианта поллиноза представлена на фиг.1.
Установлено, что частота группы аллелей HLA-DRB1*01 мало отличалась от контрольного значения в группе «поллинозы» (11,5%<14,9%) и была достоверно ниже контрольной в группе больных сезонным аллергическим ринитом (3,2%<14,9%), а в группе пациентов с пыльцевой бронхиальной астмой, наоборот, повышалась (20,0%>14,9%), и это увеличение приближалось к статистически значимому. Сравнительный анализ уровня HLA-DRB1*01 между группами больных сезонным аллергическим ринитом и пыльцевой бронхиальной астмой показал высокую степень достоверности выявленных изменений (20,0%>3,2%; RR=5,4; EF=0,16; X2=4,133; р<0,05).
Таким образом, специфичность HLA-DRB1*01, с одной стороны, маркирует резистентность к развитию аллергического ринита, а с другой стороны, - ее наличие в HLA-фенотипе больного является маркером повышенного риска присоединения пыльцевой бронхиальной астмы. С учетом количественных показателей установленной нами закономерности можно утверждать следующее: риск возникновения пыльцевой бронхиальной астмы у DRB1*01-позитивных больных сезонным аллергическим ринитом в 5,4 раза выше, чем у DRB1*01-негативных пациентов.
Частотная характеристика таких маркерных специфичностей HLA локуса DQ как HLA-DQВ1*0301, DQB1*0302, DQB1*0401/02, DQB1*05 и DQB1*06 в зависимости от клинического варианта поллиноза представлена на фиг.2.
Частота типирования аллеля HLA-DQB1*05 была незначимо повышена в общей группе «поллинозы» (34,4% >22,3%; X2=2,158; p>0,05) и несколько снижена в группе «сезонный аллергический ринит» (19,4% <22,3%; X2=0,363; p>0,05). Максимального уровня частота аллеля HLA-DQB1*05 достигала в 3-й анализируемой выборке, где он регистрировался у 15 из 30 больных пыльцевой бронхиальной астмой, т.е. у каждого второго пациента (50,0% >22,3%; X2=7,155; pcorr<0,05). Причем уровень специфичности HLA-DQB1*05 у больных пыльцевой бронхиальной астмой был достоверно повышен не только по сравнению с контрольной группой, но и, что особенно важно, по сравнению с группой больных сезонным аллергическим ринитом (50,0% >19,4%; RR=3,9; EF=0,37; X2=5,058; pcorr<0,05). Таким образом, специфичность HLA-DQB1*05 может служить прогностическим фактором высокого риска формирования бронхиальной астмы у пациентов с уже имеющимся аллергическим ринитом.
С учетом количественных показателей силы и направленности выявленных ассоциаций можно заключить, что риск присоединением клиники пыльцевой бронхиальной астмы у DQВ1*05-позитивных больных сезонным аллергическим ринитом в 3,9 раза выше, чем у DQВ1*05-негативных лиц.
Несколько иным был характер частотных изменений для аллельного варианта HLA-DQB1*06: умеренное и недостоверное снижение в 1-й группе (44,3% <56,4%; X2=2,689; p>0,05), некоторое повышение во 2-й группе (64,5% >56,4%; X2=0,344; p>0,05) и более чем двукратное снижение в 3-й анализируемой группе как по сравнению с контролем (23,3% <56,4%; X2=11,314; pc<0,05), так и по сравнению со 2-й выборкой «сезонный аллергический ринит» (23,3% <64,5%; RR=0,18; PF=0,52; X2=12,217; pc<0,05). Следовательно, наличие в HLA-фенотипе специфичности HLA-DQB1*06 маркирует резистентность к развитию пыльцевой бронхиальной астмы как у здоровых, так у больных сезонным аллергическим ринитом.
Таким образом, специфичности HLA-DRB1*01 и HLA-DQB1*05 являются прогностическим факторами высокого риска формирования пыльцевой бронхиальной астмы у пациентов с уже имеющимся сезонным аллергическим ринитом. Напротив, наличие в фенотипе больного сезонным аллергическим ринитом специфичности HLA-DQB1*06 препятствует развитию пыльцевой бронхиальной астмы.
Ниже приводятся результаты апробации.
Пример 1. Больная М., 1978 г.р., русская. Обратилась на прием к врачу-аллергологу консультативной поликлиники Александро-Мариинской областной клинической больницы г.Астрахани с жалобами на обильные водянистые выделения из носа, зуд и заложенность носа, слезотечение, зуд глаз, зуд неба, приступы удушья до 4-5 раз в сутки, приступообразный кашель, появление отечных зудящих полос после раздражения кожи. Указанные симптомы беспокоят сезонно в период цветения растений.
Анамнез заболевания и аллергологический анамнез: Больной считает себя с 1996 г., когда впервые стала отмечать симптомы риноконъюнктивита в сезон цветения сорных растений (июль-октябрь). В 2004 году в период палинации появились симптомы пыльцевой бронхиальной астмы: приступы удушья, сухой приступообразный кашель, сопровождающийся хрипами и свистами в груди.
За медицинской помощью не обращалась, занималась самолечением. В период обострений лечится антигистаминными препаратами, деконгестантами, дипроспаном, эпизодически прибегает к метилксантинам (эуфиллину). У бабушки по материнской линии - бронхиальная астма. Бытовой, эпидермальной, грибковой аллергии нет. Был однократный эпизод ангиоотека лица после употребления в пищу щучьей икры. Лекарственной непереносимости нет. По профессии парикмахер.
Status praesens: Кожные покровы розовые, уртикарный дермографизм (с детства). Гиперемия конъюнктив обоих глаз. Носовое дыхание затруднено. Периферические лимфатические узлы не увеличены. В легких везикулярное дыхание, рассеянные сухие хрипы по всем легочным полям. ЧДД - 24 в 1'. Границы абсолютной и относительной сердечной тупости в пределах нормы. Тоны сердца приглушены, ритмичные. PS - 90 уд. в 1 мин. АД - 120/80 мм рт.ст. Живот мягкий, не вздут, безболезненный. Печень не увеличена. Кишечник мягкий, безболезненный на всем протяжении. Дизурии и периферических отеков нет.
Данные обследования: OAК: Еr - 3,5×1012/л, Нв - 110 г/л, ЦП - 1,0; Tr - 286,6×109/л, Le - 4,2×109/л, эозинофилы - 0, б - 1, п - 5, с - 57, л - 27, м - 2, СОЭ - 9 мм/ч.
Общий иммуноглобулин Е - 134,7 МЕ/мл.
Спирография: ЖЕЛ - 3,07 л (72%), ФЖЕЛ - 3,45 л (65%), OФB1 - 1,79 л (53%), т.Тиффно - 63%, ПОС - 2,5 л (41%), MOC1 - 41%, MOC2 - 29%, МОС3 - 56%. Бронходилятационный тест с сальбутамолом - ΔOФB1+19%.
Результаты скарификационных кожных тестов с пыльцевыми аллергенами (тесты проведены в период ремиссии заболевания): полынь +++, лебеда ++, амброзия +. Результаты скарификационных кожных тестов с бытовыми, эпидермальными, пищевыми аллергенами отрицательные.
По результатам клинико-лабораторного обследования установлен заключительный клинический диагноз: Бронхиальная астма, аллергическая форма, интермиттирующее течение, фаза среднетяжелых приступов удушья. Аллергический ринит, средней степени тяжести, интермиттирующее течение. Аллергический конъюнктивит. Пыльцевая аллергия (полынь, лебеда, амброзия). Уртикарный дермографизм.
HLA-фенотип пациентки: DRB1*01, DQB1*05.
Таким образом, наличие в профиле HLA специфичностей DRB1*01 и DQB1*05 определило у больной высокий риск развития пыльцевой бронхиальной астмы.
Пример 2. Больной П., 1982 г.р., русский. Обратился на прием к аллергологу консультативной поликлиники Александро-Мариинской областной клинической больницы г.Астрахани с жалобами на зуд глаз, слезотечение, выделения из носа, зуд неба, приступообразный кашель со слизистой скудной мокротой, ежедневные приступы удушья преимущественно в ранние утренние часы, купируемые приемом 1-2 таблеток эуфиллина.
Анамнез заболевания и аллергологический анамнез: Болен с 1996 г., когда впервые в сезон август-сентябрь отметил появление симптомов ринита и конъюнктивита. С 2003 г.в сезон цветения растений беспокоят приступы экспираторного удушья, кашля. В период обострений принимает антигистаминные препараты, деконгестанты, метилксантины. За медицинской помощью не обращался, лечился самостоятельно. У матери, отца и сестры - пыльцевая аллергия в форме сезонного аллергического риноконъюнктивита. Бытовой, эпидермальной, грибковой, пищевой аллергии нет. Лекарственной непереносимости нет. Работает водителем.
Status praesens: Умеренного питания. Кожные покровы чистые, обычной окраски. Слабая отечность глаз. Гиперемия склер и конъюнктив обоих глаз. Дыхание через нос затруднено. Периферические лимфатические узлы не увеличены. В легких ослабленное везикулярное дыхание. Сухие свистящие хрипы по всем легочным полям. ЧДД - 20 в 1'. Границы абсолютной и относительной сердечной тупости в пределах нормы. Тоны сердца приглушены, ритмичные. PS - 82 уд. в 1 мин. АД - 125/80 мм рт.ст. Живот мягкий, не вздут, безболезненный. Печень не увеличена. Дизурии и периферических отеков нет.
Данные обследования: OAК: Еr - 4,5×1012/л, Нв - 137 г/л, ЦП - 0,9; Tr - 325,8×109/л, Le - 4,9×109/л, эозинофилы - 1, б - 1, п - 4, с - 64, л - 27, м - 2, СОЭ - 12 мм/ч.
Общий иммуноглобулин Е - 1255,65 МЕ/мл.
Спирометрия: ЖЕЛ - 5,32 л (94%), ФЖЕЛ - 3,26 л (59%), ОФВ1 - 2,52 л (54%), т. Тиффно - 77%, ПОС - 8,57 л (65%).
Результаты скарификационных кожных тестов с пыльцевыми аллергенами (проведены в период ремиссии заболевания): тимофеевка +++, подсолнечник +++, одуванчик +, полынь +++, лебеда ++++, амброзия +, циклахена ++. Результаты скарификационных кожных тестов с бытовыми, эпидермальными, пищевыми аллергенами отрицательные.
По результатам обследования установлен заключительный клинический диагноз: Бронхиальная астма, аллергическая форма, интермиттирующее течение, фаза среднетяжелых приступов удушья. Аллергический ринит, интермиттриующее течение, средней степени тяжести. Аллергический конъюнктивит. Пыльцевая аллергия (злаковые, сорные травы).
HLA-фенотип пациента: DRB1*01, DRB1*11, DQB1*0302.
Результаты иммуногенетического исследования показали, что присутствующая в HLA-фенотипе пациента специфичность DRB1*01 явилась генетическим фактором, определившим высокий риск развития пыльцевой бронхиальной астмы.
Пример 3. Больная Ш., 1962 г.р., русская. Обратилась на прием к аллергологу консультативной поликлиники с жалобами на слезотечение, отек век, жжение глаз, выделения из носа, заложенность и зуд носа.
Анамнез заболевания и аллергологический анамнез: Больной считает себя с 1975 г.В сезон с июля по сентябрь беспокоят симптомы риноконъюнктивита. Консультативной помощи аллерголога не получала, лечится самостоятельно антигистаминными препаратами 2 поколения, деконгестантами, интраназальными глюкокортикостероидами, дипроспаном. Перекрестная пищевая аллергия на бахчевые, томаты, баклажаны, картофель (оральный аллергический синдром). Приступов удушья в период обострения не отмечала. У матери бронхиальная астма (пыльцевая аллергия). Бытовой, эпидермальной, грибковой аллергии нет. Лекарственной непереносимости не отмечено.
Status praesens: Кожные покровы чистые, обычной окраски. Дыхание через нос затруднено. Веки отечны. Конъюнктивы обоих глаз гиперемированы. Периферические лимфатические узлы не увеличены. Дыхание через нос свободное. В легких везикулярное дыхание. Хрипов нет. ЧДД - 14 в 1 минуту. Тоны сердца ясные, ритмичные. PS - 82 уд. в 1 мин. АД - 100/65 мм рт.ст. Живот мягкий, не вздут, безболезненный. Печень не увеличена. Кишечник мягкий, безболезненный на всем протяжении. Дизурии и периферических отеков нет.
Данные обследования: OAК: Еr - 3,25×1012/л, Нв - 110 г/л, ЦП - 0,9; Tr - 287×109/л, Le - 4,8×109/л, п - 2, с - 64, л - 28, м - 2, СОЭ - 9 мм/ч.
Общий иммуноглобулин Е - 9,0 МЕ/мл.
Результаты скарификационных кожных тестов с пыльцевыми аллергенами (проведены в период ремиссии заболевания): конопля ++++. Результаты скарификационных кожных тестов с бытовыми, эпидермальными, пищевыми аллергенами отрицательные.
По результатам клинико-лабораторного обследования установлен заключительный клинический диагноз: Аллергический ринит, средней степени тяжести, интермиттирующее течение. Аллергический конъюнктивит. Пыльцевая аллергия (конопля).
HLA-фенотип пациентки: DRB1*13, DRB1*15, DQB1*06.
Как видно, несмотря на наследственную предрасположенность и длительный срок болезни у больной не развилась пыльцевая бронхиальная астма. При иммуногенетическом исследовании у больной была выявлена протекторная специфичность HLA-DQB1*06, что позволяет прогнозировать резистентность к развитию пыльцевой бронхиальной астмы.
Предлагаемым способом достигнуто повышение точности прогнозирования развития пыльцевой бронхиальной астмы на 70%. Определение иммуногенетических маркеров позволит выявлять пациентов, подверженных риску возникновения пыльцевой бронхиальной астмы, что позволит своевременно осуществлять мероприятия первичной профилактики этого социально-значимого заболевания.
Достоинством способа является его высокая достоверность, простота лабораторного выполнения, что указывает на возможность широкого применения в аллергологических стационарах и кабинетах.
СПОСОБ ПРОГНОЗИРОВАНИЯ ПЫЛЬЦЕВОЙ БРОНХИАЛЬНОЙ АСТМЫ
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ПЫЛЬЦЕВОЙ БРОНХИАЛЬНОЙ АСТМЫ | 2010 |
|
RU2433408C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ ПОЛЛИНОЗА | 2010 |
|
RU2430360C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ БРОНХИАЛЬНОЙ АСТМЫ | 2012 |
|
RU2510508C1 |
| Способ определения фенотипа хронических воспалительных заболеваний носа и околоносовых пазух при наличии показаний к таргетной терапии | 2023 |
|
RU2826780C1 |
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКИХ РЕЦИДИВИРУЮЩИХ АЛЛЕРГИЧЕСКИХ ЗАБОЛЕВАНИЙ СЛИЗИСТОЙ НОСА И ОКОЛОНОСОВЫХ ПАЗУХ МЕТОДОМ ЭНДОНАЗАЛЬНОЙ АУТОЛИМФОЦИТОТЕРАПИИ | 2009 |
|
RU2411048C1 |
| УЛЬТРАЗВУКОВОЙ ЭНДОНАЗАЛЬНЫЙ ДИАГНОСТИЧЕСКИЙ ТЕСТ РЕСПИРАТОРНЫХ АЛЛЕРГОЗОВ | 2000 |
|
RU2193863C2 |
| СПОСОБ ЛЕЧЕНИЯ АЛЛЕРГИЧЕСКИХ ЗАБОЛЕВАНИЙ МЕТОДОМ АУТОЛИМФОЦИТОТЕРАПИИ | 2009 |
|
RU2395305C1 |
| Способ диагностики аллергической тяжелой бронхиальной астмы | 2022 |
|
RU2786010C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ САХАРНОГО ДИАБЕТА ТИПА 1 В ПОПУЛЯЦИЯХ НАРОДОВ БАШКОРТОСТАНА | 2005 |
|
RU2285921C1 |
| СПОСОБ ВЫЯВЛЕНИЯ ПРЕДРАСПОЛОЖЕННОСТИ И РЕЗИСТЕНТНОСТИ К ЗАБОЛЕВАНИЮ ЦИСТНЫМ ЭХИНОКОККОЗОМ У ДЕТЕЙ | 2008 |
|
RU2387383C1 |

Изобретение относится к области медицины и описывает способ прогнозирования пыльцевой бронхиальной астмы путем иммуногенетического исследования, при этом в венозной крови методом полимеразной цепной реакции определяют гены локусов DRB1 и DQB1 системы HLA и при наличии специфичностей HLA-DRB1*01 и/или DQB1*05 прогнозируют высокий риск развития пыльцевой бронхиальной астмы у больных сезонным аллергическим ринитом; при наличии специфичности HLA-DQB1*06 прогнозируют резистентность к развитию пыльцевой бронхиальной астмы у больных сезонным аллергическим ринитом. Данный способ обеспечивает повышение точности прогнозирования развития пыльцевой бронхиальной астмы. 1 табл., 2 ил.
Способ прогнозирования пыльцевой бронхиальной астмы путем иммуногенетического исследования, отличающийся тем, что в венозной крови методом полимеразной цепной реакции определяют гены локусов DRB1 и DQB1 системы HLA и при наличии специфичностей HLA-DRB1*01 и/или DQB1*05 прогнозируют высокий риск развития пыльцевой бронхиальной астмы у больных сезонным аллергическим ринитом; при наличии специфичности HLA-DQB1*06 прогнозируют резистентность к развитию пыльцевой бронхиальной астмы у больных сезонным аллергическим ринитом.
| Woszczec G | |||
| et al | |||
| Association of asthma and total IgE levels with human leukocyte antigen-DR in patients with grass allergy // Eur Respir J | |||
| Топчак-трактор для канатной вспашки | 1923 |
|
SU2002A1 |
| Прибор для промывания газов | 1922 |
|
SU20A1 |
| Цилиндрический сушильный шкаф с двойными стенками | 0 |
|
SU79A1 |
| Jahn-Schmid B | |||
| et al | |||
| Antigen presentation of the immunodominant T-cell epitope of the major mugwort pollen allergen, Art v 1, is associated with the expression of HLA-DRB1*01 | |||
| J | |||
Авторы
Даты
2012-01-27—Публикация
2010-11-08—Подача