Область техники, к которой относится изобретение
Настоящее изобретение относится к средству для роста волос, содержащему в качестве активного компонента производное циклоспорина, в частности к средству для роста волос, содержащему в качестве активного компонента производное циклоспорина, модифицированное по положению 3.
Уровень техники
Число волос на волосистой части головы человека составляет в среднем от 100000 до 150000. Каждый волос имеет три основные фазы развития - анаген, катаген и телоген, после чего он выпадает. Этот цикл развития волос повторяется, причем один цикл отличается от других циклов по продолжительности, которая колеблется от 3 до 6 лет. Взрослый человек ежедневно теряет в среднем от 50 до 100 волос. В большинстве случаев алопеция, или облысение, представляет собой явление, характеризующееся сокращением продолжительности анаген-фазы роста волос и увеличением процентной доли волос в катаген- и телоген-фазах, вследствие чего количество выпадающих волос чрезмерно увеличивается, превышая общепринятые нормы.
Существует много теорий, объясняющих выпадение волос, в том числе, например, плохой циркуляцией крови, избыточной активностью мужских половых гормонов, чрезмерным образованием и выделением кожного сала, травмированном кожи головы перекисями, бактериями и др., наследственными факторами, старением, стрессами и т.п. Однако подлинные механизмы выпадения волос до настоящего времени не выявлены. В последние годы прогрессирует тенденция к увеличению числа людей, страдающих выпадением волос, что объясняется изменением привычек питания и увеличением факторов стресса в современных социальных условиях и др. Кроме того, отмечаются процесс "омолаживания" алопеции и стремительный рост числа женщин, страдающих облысением.
Одним из препаратов, наиболее широко используемых для лечения и предупреждения облысения, является препарат, содержащий миноксидил. Существуют два вида препаратов, способствующих росту волос, которые одобрены к использованию Управлением по контролю качества пищевых продуктов, медикаментов и косметических средств Министерства торговли США, и миноксидил является одним из них. Изначально миноксидил был разработан как гипертензивное средство для снижения кровяного давления. Однако при употреблении этого препарата отмечался побочный трихогенный эффект, поэтому позднее препарат стал популярен как средство для восстановления роста волос. Хотя механизмы действия миноксидила как средства для восстановления роста волос еще полностью не изучены, выдвинуто предположение, что миноксидил увеличивает ток крови за счет расширения кровеносных сосудов, благодаря чему корни волос получают больше питания, что, естественно, благоприятствует их росту.
Предполагаемая модель увеличения тока крови была косвенно подтверждена в недавнем сообщении о том, что миноксидил способствует активизации сосудистого эндотелиального фактора роста (VEGF), т.е. фактора роста, связанного с вазодилатацией в сосочках кожи, которые служат основными клетками, формирующими корни волос. Помимо сосудорасширяющего эффекта миноксидила в механизмах восстановления волос, сообщалось также о том, что миноксидил активизировал папиллярные клетки в корнях волос при инкубировании in vitro и рост волосяных фолликул в тканевой культуре in vitro. Эти факты указывают на то, что миноксидил может воздействовать непосредственно на корни волос как фактор роста.
Для лечения облысения применяется и финастерид, используемый в качестве активного компонента в препарате Propecia (Пропеция), выпущенном в продажу фирмой Merck. Он ингибирует реакцию превращения мужского гормона тестостерона в дигидротестостерон, который является более активным мужским гормоном, чем тестостерон. В декабре 1997 г. финастерид в таблетках по 1 мг был допущен Управлением по контролю качества пищевых продуктов, медикаментов и косметических средств Министерства торговли США к использованию в качестве средства для восстановления роста волос при лечении облысения только у мужчин; в настоящее время указанный препарат имеется в продаже. Клиническими исследованиями подтвержден его трихогенный эффект. Однако позднее появилось сообщение о том, что финастерид обладает побочным действием, проявляющимся в снижении половой функции у мужчин. Поскольку ни финастерид, ни миноксидил не показали достаточно высокого эффекта в клинических испытаниях и имеются сведения об их побочных действиях, многие исследователи занимаются проблемой разработки новых, более эффективных средств для восстановления роста волос.
Препараты семейства циклоспорина обладают иммунодепрессивной активностью. Они достаточно эффективно подавляют рост вирусов, грибов, простейших и др. и в качестве побочного действия проявляют различный физиологический эффект, например нефротоксический, гепатотоксический, гипертензивный, периодонтический, трихогенный и т.п. Циклоспорин А, являющийся наиболее типичным представителем циклоспоринов, представляет собой циклический пептид, химическая формула которого (см. ниже) включает 11 аминокислот, в том числе несколько N-метил-аминокислот и D-аланин (остаток №8):
[Структурная формула 1]

где:
MeBmt - N-метил-(4R)-4-[(Е)-2-бутенил]-4-метил-L-треонин, Abu - L-α-аминомасляная кислота, Sar - саркозин, MeLeu - N-метил-L-лейцин, Val - L-валин. Ala - L-аланин, DAla - D-аланин. MeVal - N-метил-L-валин.
Аминокислотная форма циклоспорина А, имеющая вышеприведенную химическую формулу 1, представляет собой L-конфигурацию, другой пока не выявлено. Нумерация остатков аминокислот начинается с MeBmt и продолжается далее по часовой стрелке, т.е. 1 - MeBmt и последний 11 - MeVal (N-метил-L-валин), как показано в структурной формуле 1. Номенклатура различных производных, включая циклоспорины от А до Z, соответствует традиционно используемым методам (Helv. Chim. Acta, 1987, 70:13-36). Например, если L-α-масляная кислота (Abu) в положении 2 циклоспорина А замещается L-аланином, L-треонином, L-валином или L-норвалином, то полученные производные обозначаются соответственно циклоспорин В, циклоспорин С, циклоспорин D или циклоспорин G. Если аминокислотные остатки производных циклоспорина отличаются от аминокислотных остатков циклоспорина А, то производные обозначаются по названию заместителя. Например, если саркозин, будучи аминокислотным остатком 3 циклоспорина А, замещается N-метил-D-Abu3 или N-метил-D-Nva3, то полученные производные обозначаются как [N-метил-D-Abu3] циклоспорин А или [N-метил-D-Nva3] циклоспорин А соответственно. То есть используется традиционный метод сокращения названий (аббревиатуры) аминокислот, а именно: N-метил-L-лейцин сокращенно обозначается как MeLeu, N-метил-L-изолейцин - как MeIle, N-метил-L-валин - как MeVal, N-метил-L-аланин - как MeAla, N-метил-L-норвалин - как MeNva, L-лейцин - как Leu, L-изолейцин - как Ile, саркозин - как Sar, L-серин - как Ser, L-валин - как Val, L-аланин - как Ala, D-аланин - как DAla, L-аминомасляная кислота - как Abu, L-треонин - как Thr и L-норвалин - как Nva. Что касается производного циклоспорина, замещенного серой вместо карбонила в положении аминокислотного остатка 7, то оно может быть обозначено как циклоспорин 7-тиоамид, или [7ψ8CS-NH] циклоспорин, в соответствии с различными ссылками (Helv. Chim. Acta. 74: 1953-1990, 1991; J. Org. Chem. 58: 673-677, 1993; J. Org. Chem. 59: 7249-7258, 1994).
Таким образом, попытки использовать циклоспорины в качестве восстановителей роста волос предпринимались многими группами ученых. В частности, широко проводились исследования, включающие проведение экспериментов по восстановлению волосяного покрова на животных, по лечению гнездной алопеции человека (J. Am. Acad. Dermatol., 1990, 22:242-250), облысения по мужскому типу (J. Am. Acad. Dermatol., 1990, 22:251-253 и Skin Pharmacol., 1994, 7:101-104), по предупреждению выпадения волос химиотерапией на животных моделях (Am. J. Pathol, 1997, 150:1433-1441). В сравнительных экспериментах на мышах было показано, что оказываемый циклоспорином эффект восстановления роста волос в 100 раз превышает эффект миноксидила. Основываясь на этом открытии, исследователи предпринимали попытки использовать циклоспорин для лечения облысения по мужскому типу, о чем свидетельствует большое количество заявок на патенты.
Например, в заявках Японии №60-243008, 62-19512 и 62-19513 описаны способы использования производных циклоспорина в качестве средства для восстановления роста волос. Заявка на Европейский патент №0414632 В1 касается производного циклоспорина, модифицированного по положению 8, а заявка РСТ №93/17039 - изоциклоспорина. Патент США №5807820 и патент Великобритании №2218334А выданы на циклоспорины с высокой способностью к всасыванию через кожу, что делает возможным их использование в качестве восстановителей роста волос.
Сущность изобретения
Настоящее изобретение создавалось с учетом вышерассмотренных проблем, связанных с побочными действиями циклоспорина А; целью настоящего изобретения является средство для роста волос, которое в качестве активного компонента содержит производное циклоспорина с высокой способностью к стимуляции роста волос.
Согласно одному из аспектов настоящего изобретения указанная цель, а также другие цели достигаются путем создания средства для роста волос, которое содержит в качестве активного компонента аналог циклоспорина по положению 3, имеющий приведенную ниже формулу 1 и полученный путем синтеза множества производных циклоспорина с оценкой их способности к стимуляции роста волос с целью создания нового средства для роста волос.
[Формула 1]

где:
А представляет собой N-метил-(4R)-4-[(Е)-2-бутенил]-4-метил-L-треонин,
(2S,3R,4R,6Е)-3-сульфгидрил-4-метил-2-(метиламино)-6-октеновую кислоту или (2S,4R,6Е)-3-оксо-4-метил-2-(метиламино)-6-октеновую кислоту;
В представляет собой L-аминомасляную кислоту (Abu), L-аланин (Ala), L-треонин (Thr), L-валин (Val) или L-норвалин (Nva);
С представляет собой D-аминокислоту следующей общей формулы:
CH3NH-CH(R)-COOH,
в которой
R выбирается из группы, включающей водород, C1-C6 прямые или разветвленные алкил, алкенил или алкинил остатки, замещенные или не замещенные одной или более группой, выбираемой из перечня, включающего амино, окси, гало, галоалкил, эфирные, алкокси, циано, нитро, алкиламино и диалкиламино группы и -X-R' следующей общей формулы (см. ниже):
-X-R',
в которой:
Х - кислород или сера;
R' выбирается из группы, включающей водород, C1-С6 прямые или разветвленные алкил, алкенил или алкинил остатки, замещенные или не замещенные одной или более группой, выбираемой из перечня, включающего амино, окси, гало, галоалкил, эфирные, алкокси, циано, нитро, алкиламино и диалкиламино группы;
D представляет собой N-метил-L-лейцин, γ-окси-N-метил-L-лейцин или L-валин;
Е представляет собой L-валин или L-норвалин;
F представляет собой N-метил-L-лейцин, γ-окси-N-метил-L-лейцин или L-лейцин;
G представляет собой L-аланин или L-аланин тиоамид ([7ψ8CS-NH], NH-СНСН3-CS-);
Н представляет собой D-аминокислоту следующей общей формулы:
-NH-CH(CH2R)-COOH,
в которой:
R - водород или X-R' следующей общей формулы:
-X-R',
в которой:
Х - кислород или сера,
R' выбирается из группы, включающей водород и C1-С6 прямые или разветвленные алкил, алкенил или алкинил остатки, замещенные или не замещенные одной или более группой, выбираемой из перечня, включающего амино, окси, гало, галоалкил, эфирные, алкокси, циано, нитро, алкиламино или диалкиламино группы;
I представляет собой N-метил-L-лейцин, γ-окси-N-метил-L-лейцин или L-лейцин;
J представляет собой N-метил-L-лейцин, γ-окси-N-метил-L-лейцин или L-лейцин;
К представляет собой N-метил-L-валин или L-валин.
Согласно другому аспекту настоящего изобретения заявлено средство для роста волос, содержащее в качестве активного компонента аналог циклоспорина по положению 3, который обладает высоким эффектом стимуляции роста волос и имеет приведенную ниже формулу 2:
[Формула 2]

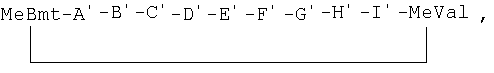
где:
MeBmt представляет собой N-метил-(4R)-4-[(Е)-2-бутенил]-4-метил-L-треонин;
А' представляет собой L-аминомасляную кислоту, L-аланин, L-треонин, L-валин или L-норвалин;
В' представляет собой N-метил-D-аминомасляную кислоту, N-метил-D-норвалин, D-2-(метиламино)гекса-4-иноил, D-2-(метиламино)пент-4-иноил, D-2-метилтио-саркозин, N-метил-О-пропенил-D-серин или N-метил-D-серин;
С' представляет собой N-метил-L-лейцин, γ-окси-N-метил-L-лейцин или L-валин;
D' представляет собой L-валин или L-норвалин;
Е' представляет собой N-метил-L-лейцин, γ-окси N-метил-L-лейцин или L-лейцин;
F'представляет собой L-аланин или L-аланин тиоамид ([7ψ8CS-NH], NH-СНСН3-CS-);
G' представляет собой D-аланин или D-серин;
Н' представляет собой N-метил-L-лейцин, γ-окси-N-метил-L-лейцин или L-лейцин;
I' представляет собой N-метил-L-лейцин, γ-окси-N-метил-L-лейцин или L-лейцин;
MeVal представляет собой N-метил-L-валин.
Согласно следующему аспекту настоящего изобретения заявлено средство для роста волос, которое содержит в качестве активного компонента аналог циклоспорина по положению 3, обладающий высоким эффектом стимуляции роста волос и имеющий формулу 3 (см. ниже).
[Формула 3]

где:
MeBmt представляет собой N-метил-(4R)-4-[(Е)-2-бутенил]-4-метил-L-треонин;
А'' представляет собой L-аланин, L-треонин, L-валин или L-норвалин;
В'' представляет собой N-метил-D-аминомасляную кислоту, N-метил-D-норвалин, D-2-(метиламино)гекса-4-иноил, D-2-(метиламино)пент-4-иноил, D-2-метилтио-саркозин, N-метил-О-пропенил-D-серин или N-метил-D-серин;
MeLeu представляет собой N-метил-L-лейцин;
Val представляет собой L-валин;
Ala представляет собой L-аланин;
DAla представляет собой D-аланин;
MeVal представляет собой N-метил-L-валин.
Согласно еще одному аспекту настоящего изобретения заявлено средство для роста волос, которое содержит аналог циклоспорина по положению 3 и может использоваться для приготовления жидких композиций, спреев, гелей, паст, эмульсий, кремов, кондиционеров или шампуней.
Перечень фигур
Вышеприведенные и другие цели, отличительные особенности и преимущества настоящего изобретения станут более понятны из подробного описания приложенных рисунков [сокращения 1H-NMR и 13C-NMR обозначают ядерный магнитный резонанс (ЯМР) стабильными изотопами водорода 1Н и углерода 13С]:
фиг.1 - 1H-ЯМР-спектр [N-метил-D-Abu3] циклоспорина А;
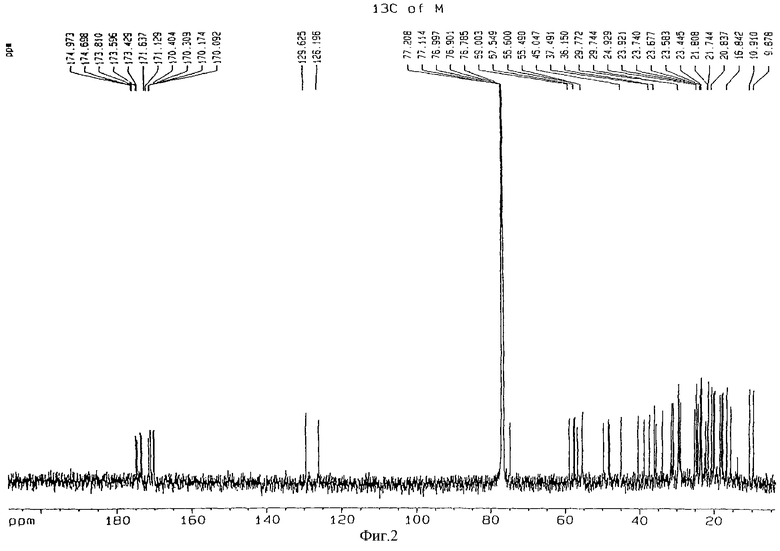
фиг.2 - 13С-ЯМР-спектр [N-метил-D-Abu3] циклоспорина А;
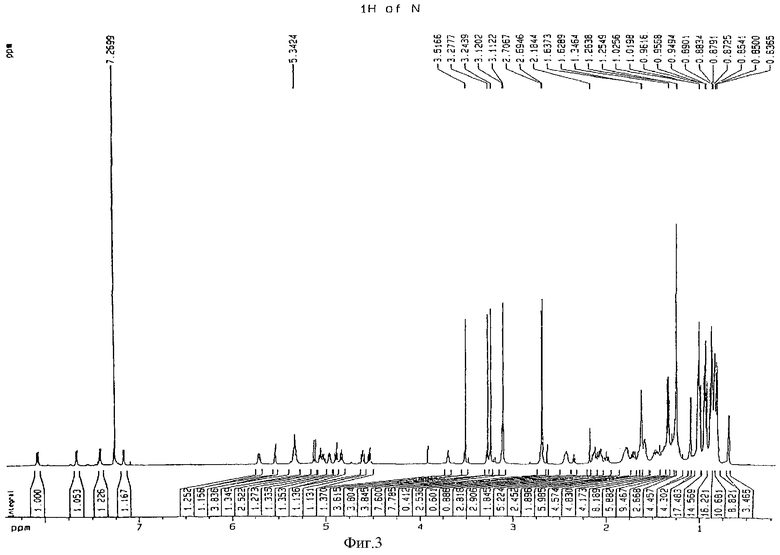
фиг.3 - 1H-ЯМР-спектр [N-метил-D-Nva3] циклоспорина А;
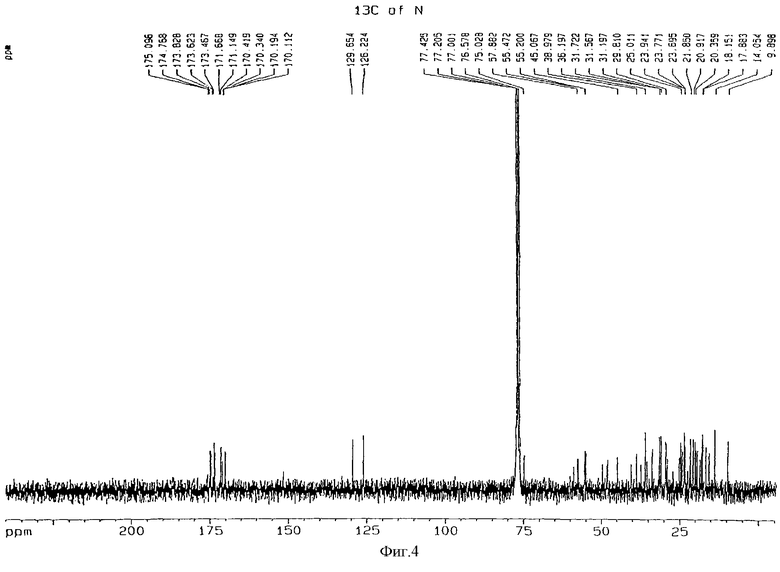
фиг.4 - 13С-ЯМР спектр [N-метил-D-L-Nva3] циклоспорина А;
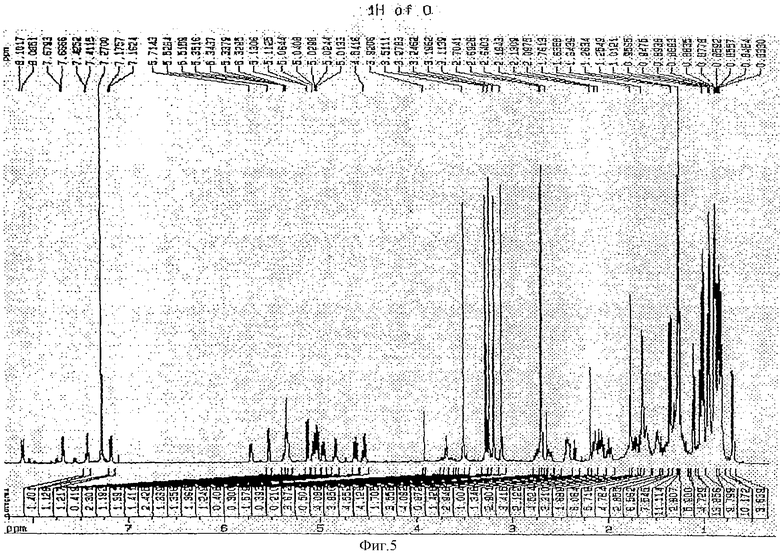
Фиг.5 - 1Н-ЯМР-спектр[D-2-(метиламино)гекса-4-иноил3]циклоспорина А;
Фиг.6 - 13C-ЯМР-спектр[D-2-(метиламино)гекса-4-иноил3]циклоспорина А;
Фиг.7 - 1Н-ЯМР-спектр[D-2-(метиламино)пент-4-иноил3]циклоспорина А;
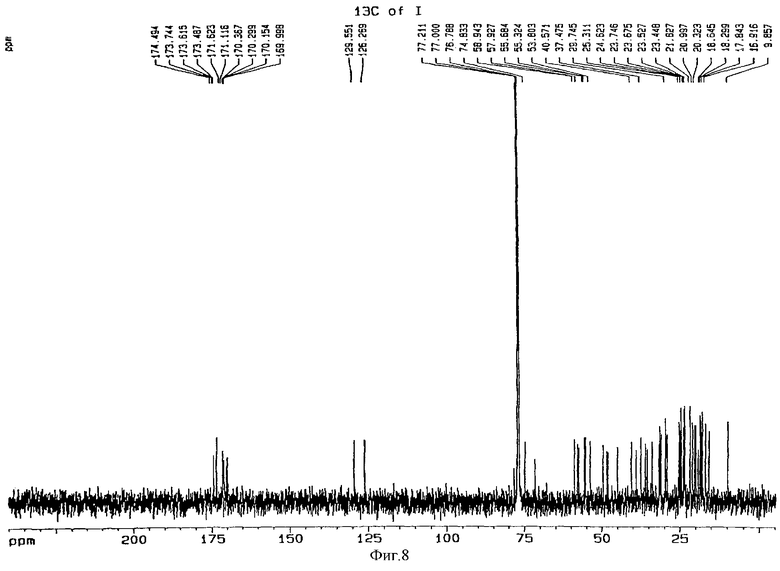
Фиг.8 - 13С-ЯМР-спектр[D-2-(метиламино)пент-4-иноил3]циклоспорина А;
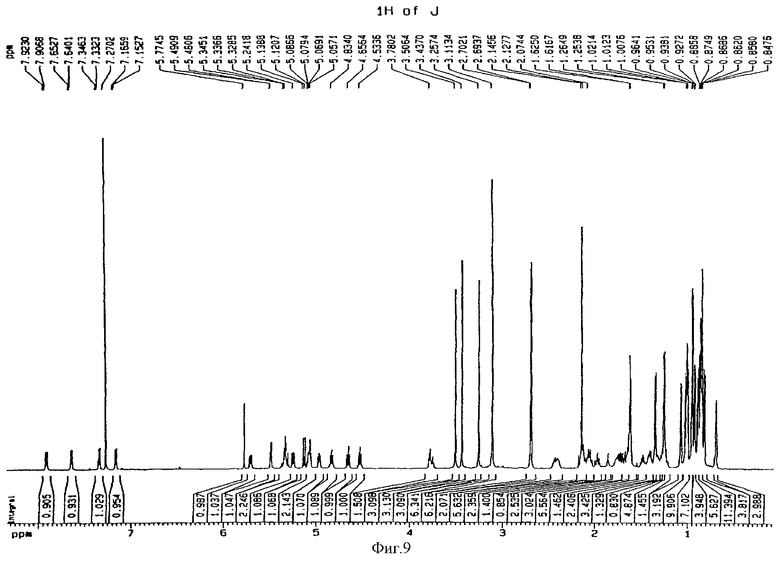
Фиг.9 - 1Н-ЯМР-спектр[D-2-метилтио-Sar3]циклоспорина А;
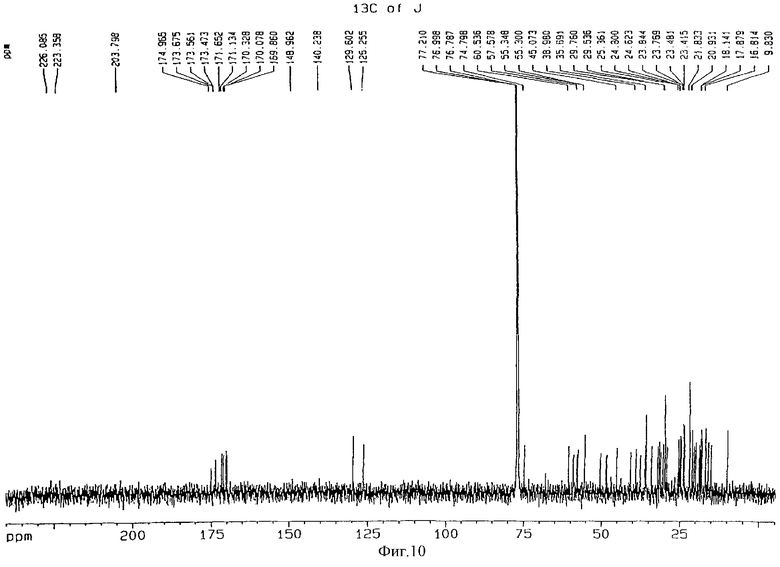
Фиг.10 - 13С-ЯМР-спектр[D-2-метилтио-Sar3]циклоспорина А;
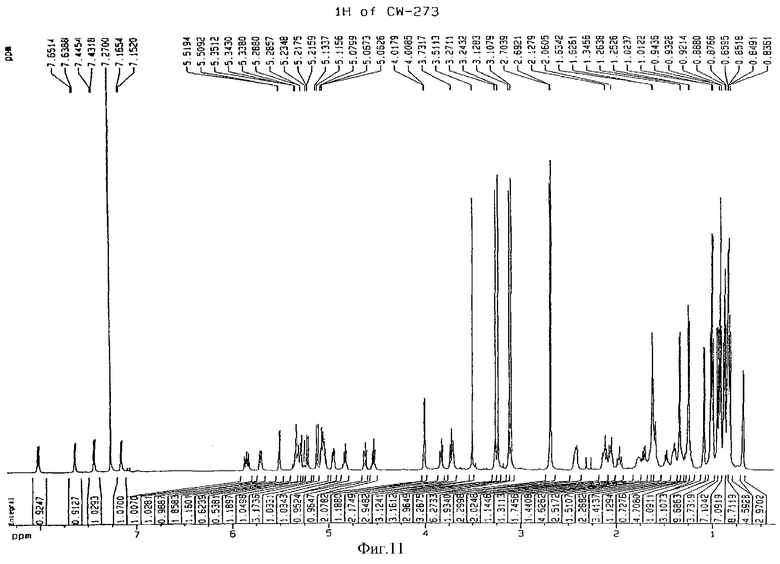
Фиг.11 - 1Н-ЯМР-спектр[N-метил-О-пропенил-D-Ser3]циклоспорина А;
Фиг.12 - 13C-ЯМР-спектр[N-метил-О-пропенил-D-Ser3]циклоспорина А;
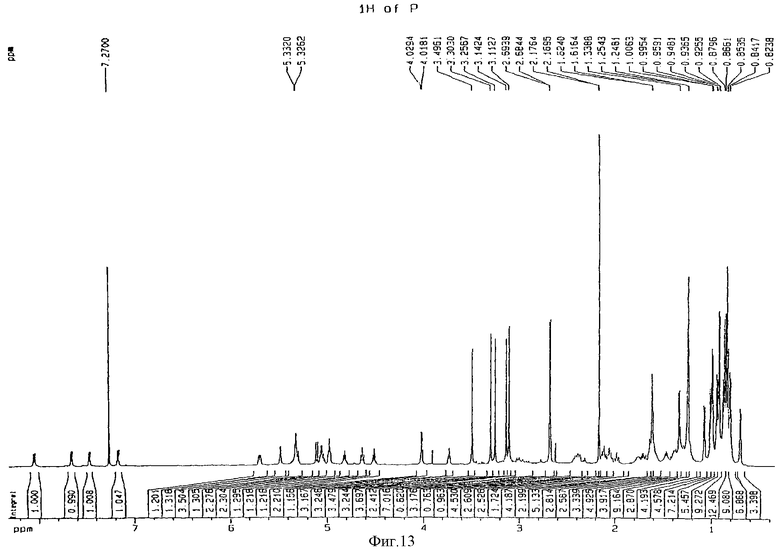
Фиг.13 - 1Н-ЯМР-спектр[N-метил-О-Ser3]циклоспорина А;
Фиг.14 - 13C-ЯМР-спектр[N-метил-D-Ser3]циклоспорина А.
Сведения, подтверждающие возможность осуществления изобретения
Ниже сущность настоящего изобретения более подробно раскрывается в примерах. Эти примеры приводятся в качестве показательных, поскольку осуществление настоящего изобретения не ограничивается только ими.
С целью разработки нового средства для роста волос авторы настоящего изобретения синтезировали химическим путем множество аналогов циклоспорина по положению 3 и проводили сравнительную оценку их эффекта стимуляции роста волос. Поэтому настоящее изобретение касается средства для роста волос, содержащего в качестве активного компонента производное циклоспорина.
Пример 1: Синтез аналога циклоспорина по положению 3
Алкилирование циклоспорина А проводили по следующей общераспространенной методике. Тетрагидрофуран (THF) смешивали с диизопропиламином ((i-Pr)2NH) и добавляли к смеси раствор n-бутил лития (BuLi) в гексане в атмосфере азота при -78°С с последующим перемешиванием в течение 30 минут. К полученному раствору литий-диизопропиламида (LDA) добавляли циклоспорин А в тетрагидрофуране и после перемешивания в течение 1 часа добавляли электрофил,
1-1: Синтез [N-метил-D-Abu3]циклоспорина А: соединение 1
(Abu = L-аминомасляная кислота)
В соответствии с вышеописанной общераспространенной методикой к раствору 10 эквивалентов литий-диизопропиламида (LDA) добавляли 1,0 г циклоспорина А в 50 мл тетрагидрофурана (THF) при -78°С. Реакционную смесь перемешивали в течение 2 часов при -78°С, после чего добавляли 0,4 мл этил-йодида. По достижении раствором комнатной температуры его перемешивали в течение еще 24 часов, затем добавляли 20 мл воды и концентрировали. Остаток смешивали с эфиром (Et2O), промывали последовательно водой и насыщенным раствором хлорида натрия и высушивали над безводным MgSO4. После концентрирования остаток подвергали хроматографии на колонке с силикагелем (100 г силикагеля, дихлорметан: метиловый спирт = 96:4) с последующей жидкостной хроматографией высокого разрешения с получением 0,1 г вышеназванного соединения.
Молекулярную массу соединения определяли методом масс-спектрометрии в режиме бомбардировки быстрыми атомами (на масс-спектрометре ZMS AX 505H). Для подтверждения молекулярной структуры проводили измерения ядерного магнитного резонанса (NMR) изотопом 1Н при 600 МГц (спектрофотометр фирмы Bruker) и изотопом 13С при 150 МГц (Bruker); полученные спектры представлены на фиг.1 и 2 соответственно.
1-2: синтез [N-метил-D-Nva3] циклоспорина А: соединение 2
(Nva = L-норвалин)
В соответствии с общераспространенной методикой к раствору 10 эквивалентов литий-диизопропиламида (LDA) добавляли 1,0 г циклоспорина А в 50 мл тетрагидрофурана при -78°С. Реакционную смесь перемешивали в течение 2 часов при -78°С, после чего добавляли 0,41 мл пропил-йодида. По достижении раствором комнатной температуры его перемешивали в течение еще 24 часов, затем добавляли 20 мл воды и концентрировали. К остатку добавляли эфир (Et2О), промывали последовательно водой и насыщенным раствором хлорида натрия и высушивали над безводным MgSO4. После концентрирования остаток подвергали хроматографии на колонке с силикагелем (100 г силикагеля, дихлорметан:метиловый спирт = 96:4) с последующей жидкостной хроматографией высокого разрешения с получением 0,12 г вышеназванного соединения. Молекулярную массу соединения определяли методом масс-спектрометрии в режиме бомбардировки быстрыми атомами (на масс-спектрометре ZMS AX 505H). Для подтверждения молекулярной структуры проводили измерения ядерного магнитного резонанса (NMR) изотопом 1H при 600 МГц (спектрофотометр фирмы Bruker) и изотопом 13С при 150 МГц (Bruker); полученные спектры представлены на фиг.3 и 4 соответственно.
1-3: синтез [D-2-(метиламино)гекса-4-иноил3] циклоспорина А: соединение 3
В соответствии с общераспространенной методикой к раствору 10 эквивалентов литий-диизопропиламида (LDA) добавляли 1,0 г циклоспорина А в 50 мл тетрагидрофурана при -78°С. Реакционную смесь перемешивали в течение 2 часов при -78°С, после чего добавляли 0,73 мл 1-бромо-2-бутина. По достижении раствором комнатной температуры его перемешивали в течение еще 24 часов, затем добавляли 20 мл воды и концентрировали. К остатку добавляли эфир (Et2O), промывали последовательно водой и насыщенным раствором хлорида натрия и высушивали над безводным MgSO4. После концентрирования остаток подвергали хроматографии на колонке с силикагелем (100 г силикагеля, дихлорметан:метиловый спирт = 96:4) с последующей жидкостной хроматографией высокого разрешения с получением 0,13 г вышеназванного соединения. Молекулярную массу соединения определяли методом масс-спектрометрии в режиме бомбардировки быстрыми атомами (на масс-спектрометре ZMS AX 505H). Для подтверждения молекулярной структуры проводили измерения ядерного магнитного резонанса (NMR) изотопом 1Н при 600 МГц (спектрофотометр фирмы Bruker) и изотопом 13С при 150 МГц (Bruker); полученные спектры представлены на Фиг.5 и 6 соответственно.
1-4: Синтез [D-2-(метиламино)пент-4-иноил3]циклоспорина А: соединение 4
Алкилирование проводили по общераспространенной методике с использованием тетрагидрофурана (THF) (200 мл), диизопропиламина ((i-Pr)2NH) (3,2 мл), раствора n-бутил лития (BuLi) (8 мл), циклоспорина А (3,76 г) в 50 мл тетрагидрофурана (THF) и пропаргил бромида (3,57 г). По достижении раствором комнатной температуры его перемешивали в течение еще 24 часов, затем добавляли 40 мл воды и концентрировали. К остатку добавляли эфир (Et2O), промывали последовательно водой и насыщенным раствором хлорида натрия и высушивали над безводным MgSO4. После концентрирования остаток подвергали хроматографии на колонке с силикагелем (100 г силикагеля, дихлорметан:метиловый спирт=96: 4) с последующей жидкостной хроматографией высокого разрешения с получением вышеназванных соединений 3 (0,18 г) и 4 (0,08 г). Молекулярную массу соединений определяли методом масс-спектрометрии в режиме бомбардировки быстрыми атомами (на масс-спектрометре ZMS АХ 505 Н). Для подтверждения молекулярной структуры проводили измерения ядерного магнитного резонанса (NMR) изотопом 1Н при 600 МГц (спектрофотометр фирмы Bruker) и изотопом 13С при 150 МГц (Bruker); полученные спектры представлены на Фиг.7 и 8 соответственно.
1-5: Синтез [D-2-метилтио-Sar3]циклоспорина А: соединение 5
(Sar = саркозин)
В соответствии с общераспространенной методикой алкилирование проводили с использованием тетрагидрофурана (THF) (100 мл), диизопропиламина ((i-Pr)2NH) (1,6 мл), n-бутил лития (BuLi) (4,0 мл), циклоспорина А (1,0 г) в 30 мл тетрагидрофурана (THF) и метилдисульфида (Me2S2) (1,5 мл). Раствор перемешивали в течение 14 часов при 0°С, после чего добавляли 20 мл воды и концентрировали. К остатку добавляли эфир (Et2O), промывали последовательно водой и насыщенным раствором хлорида натрия и высушивали над безводным MgSO4. После концентрирования остаток подвергали хроматографии на колонке с силикагелем (100 г силикагеля, дихлорметан:метиловый спирт = 50:1˜96:4) с последующей жидкостной хроматографией высокого разрешения с получением вышеназванных соединений 5 (0,36 г) и 6 (0,05 г). Молекулярную массу соединения определяли методом масс-спектрометрии в режиме бомбардировки быстрыми атомами (на масс-спектрометре ZMS AX 505H). Для подтверждения молекулярной структуры проводили измерения ядерного магнитного резонанса (NMR) изотопом 1H при 600 МГц (спектрофотометр фирмы Bruker) и изотопом 13С при 150 МГц (Bruker); полученные спектры представлены на фиг.9 и 10 соответственно.
1-6: синтез [N-метил-O-пропенил-D-Ser3] циклоспорина А: соединение 6
В соответствии с общераспространенной методикой [D-метилсерин3] циклоспорин А (0,62 г, 0,5 ммол), хлорид тетрабутиламмония (0,11 г, 0.5 ммол) и арилбромид (0,24 г, 2,0 ммол) растворяли в дихлорметане (50 мл), затем добавляли 30% NaOH (1,5 мл) и полученную смесь перемешивали в течение 2 часов. После добавления 50 мл дихлорметана раствор промывали последовательно водой и насыщенным раствором хлорида натрия и высушивали над безводным MgSO4. Концентрированный остаток подвергали хроматографии на колонке с силикагелем (100 г силикагеля, дихлорметан:метиловый спирт = 97:3) с последующей жидкостной хроматографией высокого разрешения с получением 0,4 г вышеназванного соединения. Молекулярную массу соединения определяли методом масс-спектрометрии в режиме бомбардировки быстрыми атомами (на масс-спектрометре ZMS АХ 505 Н). Для подтверждения молекулярной структуры проводили измерения ядерного магнитного резонанса (NMR) изотопом 1Н при 600 МГц (спектрофотометр фирмы Bruker) и изотопом 13С при 150 МГц (Bruker); полученные спектры представлены на фиг.11 и 12 соответственно.
1-7: синтез [N-метил-D-Ser3] циклоспорина А: соединение 7
В соответствии с общераспространенной методикой к раствору 10 эквивалентов литий-диизопропиламида (LDA) добавляли 1,0 г циклоспорина А в 50 мл тетрагидрофурана (THF) при -78°С. Реакционную смесь перемешивали в течение 2 часов при -78°С и добавляли 2,0 г параформальдегида. По достижении раствором комнатной температуры его перемешивали в течение еще 24 часов, после чего добавляли 20 мл воды и концентрировали. К остатку добавляли эфир (Et2O), промывали последовательно водой и насыщенным раствором хлорида натрия и высушивали над безводным MgSO4. После концентрирования остаток подвергали хроматографии на колонке с силикагелем (100 г силикагеля, дихлорметан:метиловый спирт = 96:4) с последующей жидкостной хроматографией высокого разрешения с получением 0,3 г вышеназванного соединения. Молекулярную массу соединения определяли методом масс-спектрометрии в режиме бомбардировки быстрыми атомами (на масс-спектрометре ZMS AX 505H). Для подтверждения молекулярной структуры проводили измерения ядерного магнитного резонанса (NMR) изотопом 1Н при 600 МГц (спектрофотометр фирмы Bruker) и изотопом 13С при 150 МГц (Bruker); полученные спектры представлены на фиг.13 и 14 соответственно.
Пример 1 на приготовление тоника для волос
1-1: приготовление тоника для волос, содержащего [N-метил-D-Abu3] циклоспорин А
(Abu = L-аминомасляная кислота)
Отдельные компоненты смешивали и перемешивали до полного растворения с получением трех видов тоника для роста волос, рецептуры которых приводятся ниже в таблице 1. Установлено, что состав 1 таблицы 1 оказывает такой же эффект стимуляции роста волос, что и обычный тоник для волос, содержащий 0,1% циклоспорина А, что подтвердили эксперименты на животных (см. ниже пример на проведение теста).
1-2: приготовление тоника для волос, содержащего [N-метил-D-Nva3] циклоспорин А
(Nva = L-норвалин)
Отдельные компоненты смешивали и перемешивали до полного растворения с получением трех видов тоника, рецептуры которых приводятся ниже в таблице 2. Установлено, что состав 1 таблицы 2 проявляет такой же эффект стимуляции роста волос, что и обычный тоник для волос, содержащий 0,1% циклоспорина А, что подтвердили эксперименты на животных (см. ниже пример на проведение теста).
1-3: приготовление тоника для волос, содержащего [D-2-(метиламино)гекса-4-иноил3] циклоспорин А
Отдельные компоненты смешивали и перемешивали до полного растворения с получением трех видов тоника для роста волос, рецептуры которых приводятся ниже в таблице 3. Установлено, что состав 1 таблицы 3 оказывает такой же эффект стимуляции роста волос, что и обычный тоник для волос, содержащий 0,1% циклоспорина А, что подтвердили эксперименты на животных (см. ниже пример на проведение теста).
1-4: приготовление тоника для волос, содержащего [D-2-(метиламино)пент-4-иноил3] циклоспорин А
Отдельные компоненты смешивали и перемешивали до полного растворения с получением трех видов тоника для роста волос, рецептуры которых приводятся ниже в таблице 4. Установлено, что состав 1 таблицы 4 проявляет такой же эффект стимуляции роста волос, что и обычный тоник для волос, содержащий 0,1% циклоспорина А, что подтвердили эксперименты на животных (см. ниже Пример на проведение теста).
1-5: Приготовление тоника для волос, содержащего [D-2-метилтио-Sar3] циклоспорин А
(Sar = саркозин)
Отдельные компоненты смешивали и перемешивали до полного растворения с получением трех видов тоника для роста волос, рецептуры которых приводятся ниже в таблице 5. Установлено, что состав 1 таблицы 5 оказывает такой же эффект стимуляции роста волос, что и обычный тоник для волос, содержащий 0,1% циклоспорина А, что подтвердили эксперименты на животных (см. ниже Пример на проведение теста).
1-6: Приготовление тоника для волос, содержащего [N-метил-О-пропенил-D-Ser3] циклоспорин А
Отдельные компоненты смешивали и перемешивали до полного растворения с получением трех видов тоника для роста волос, рецептуры которых приводятся ниже в таблице 6. Установлено, что состав 1 таблицы 6 проявляет такой же эффект стимуляции роста волос, что и обычный тоник для волос, содержащий 0,1% циклоспорина А, что подтвердили эксперименты на животных (см. ниже пример на проведение теста).
1-7: приготовление тоника для волос, содержащего [N-метил-D-Ser3] циклоспорин А
Отдельные компоненты смешивали и перемешивали до полного растворения с получением трех видов тоника для роста волос, рецептуры которых приводятся ниже в таблице 7. Установлено, что состав 1 таблицы 7 проявляет такой же эффект стимуляции роста волос, что и обычный тоник для волос, содержащий 0,1% циклоспорина А, что подтвердили эксперименты на животных (см. ниже пример на проведение теста).
Пример 2 на приготовление крема для волос
2-1: приготовление крема для волос, содержащего [N-метил-D-Abu3] циклоспорин А
(Abu = L-аминомасляная кислота)
Отдельные компоненты масляной и водной фаз смешивали в отдельных сосудах, каждую смесь доводили до полного растворения путем нагрева до 80°С. Затем смешивали обе фазы компонентов, полученные смеси эмульгировали и охлаждали до комнатной температуры. Примешивали добавки (отдушку и краситель) с получением трех видов крема для волос, рецептуры которых приводятся ниже в таблице 8. Воду добавляли до 100% общей массы, включая компоненты масляной и водной фаз.
Установлено, что состав 1 таблицы 8 проявляет такой же эффект стимуляции роста волос, что и обычный крем для волос, содержащий 0,1% циклоспорина А, что подтвердили эксперименты на животных (см. ниже пример на проведение теста).
2-2: приготовление крема для волос, содержащего [N-метил-D-Nva3]циклоспорин А
(Nva = L-норвалин)
Отдельные компоненты масляной и водной фаз смешивали в отдельных сосудах; каждую полученную смесь доводили до полного растворения путем нагрева до 80°С. Затем смешивали компоненты обеих фаз, полученную смесь эмульгировали и охлаждали до комнатной температуры. Примешивали добавки (отдушку и краситель) и получали три вида крема для волос, рецептуры которых приводится ниже в таблице 9. Воду добавляли до 100% общей массы, включая компоненты масляной и водной фаз.
Установлено, что состав 1 таблицы 9 проявляет такой же эффект стимуляции роста волос, что и обычный крем для волос, содержащий 0,1% циклоспорина А, что подтвердили эксперименты на животных (см. ниже пример на проведение теста).
2-3: приготовление крема для волос, содержащего [D-2-(метиламино)гекса-4-иноил3] циклоспорин А
Отдельные компоненты масляной и водной фаз смешивали в отдельных сосудах; каждую полученную смесь доводили до полного растворения путем нагрева до 80°С. Затем смешивали обе фазы компонентов, полученные смеси эмульгировали и охлаждали до комнатной температуры. Примешивали добавки (отдушку и краситель) с получением трех видов крема для волос, рецептуры которых приводятся ниже в таблице 10. Воду добавляли до 100% общей массы, включая компоненты масляной и водной фаз.
Установлено, что состав 1 таблицы 10 проявляет такой же эффект стимуляции роста волос, что и обычный крем для волос, содержащий 0,1% циклоспорина А, что подтвердили эксперименты на животных (см. ниже пример на проведение теста).
Эфир
2-4: приготовление крема для волос, содержащего [D-2-(метиламино)пент-4-иноил3] циклоспорин А
Отдельные компоненты масляной и водной фаз смешивали в отдельных сосудах, полученные смеси доводили до полного растворения путем нагрева до 80°С. Затем смешивали обе фазы компонентов, смеси эмульгировали и охлаждали до комнатной температуры. Примешивали добавки (отдушку и краситель) и получали три вида крема для волос, рецептуры которых приводятся ниже в таблице 11. Воду добавляли до 100% общей массы, включая компоненты масляной и водной фаз.
Установлено, что состав 1 таблицы 11 проявляет такой же эффект стимуляции роста волос, что и обычный крем для волос, содержащий 0,1% циклоспорина А, что подтвердили эксперименты на животных (см. ниже пример на проведение теста).
2-5: приготовление крема для волос, содержащего [D-2-метилтио-Sar3] циклоспорин А
(Sar = саркозин)
Отдельные компоненты масляной и водной фаз смешивали в отдельных сосудах; полученные смеси доводили до полного растворения путем нагрева до 80°С. Затем смешивали обе фазы компонентов, полученные смеси эмульгировали и охлаждали до комнатной температуры. Примешивали добавки (отдушку и краситель) и получали три вида крема для волос, рецептуры которых приводятся ниже в таблице 12. Воду добавляли до 100% общей массы, включая компоненты масляной и водной фаз.
Установлено, что состав 1 таблицы 12 проявляет такой же эффект стимуляции роста волос, что и обычный крем для волос, содержащий 0,1% циклоспорина А, что подтвердили эксперименты на животных (см. ниже пример на проведение теста).
2-6: приготовление крема для волос, содержащего [N-метил-O-пропенил-D-Ser3] циклоспорин А
Отдельные компоненты масляной и водной фаз смешивали в отдельных сосудах; полученные смеси доводили до полного растворения путем нагрева до 80°С. Затем смешивали обе фазы компонентов, полученные смеси эмульгировали и охлаждали до комнатной температуры. Примешивали добавки (отдушку и краситель) и получали три вида крема для волос, рецептуры которых приводятся ниже в таблице 13. Воду добавляли до 100% общей массы, включая компоненты масляной и водной фаз.
Установлено, что состав 1 таблицы 13 проявляет такой же эффект стимуляции роста волос, что и обычный крем для волос, содержащий 0,1% циклоспорина А, что подтвердили эксперименты на животных (см. ниже пример на проведение теста).
2-7: приготовление крема для волос, содержащего [N-метил-D-Ser3] циклоспорин А
Отдельные компоненты масляной и водной фаз смешивали в отдельных сосудах; полученные смеси доводили до полного растворения путем нагрева до 80°С. Затем смешивали обе фазы компонентов, полученные смеси эмульгировали и охлаждали до комнатной температуры. Примешивали добавки (отдушку и краситель) и получали три вида крема для волос, рецептуры которых приводятся ниже в таблице 14. Воду добавляли до 100% общей массы, включая компоненты масляной и водной фаз.
Установлено, что состав 1 таблицы 14 проявляет такой же эффект стимуляции роста волос, что и обычный крем для волос, содержащий 0,1% циклоспорина А, что подтвердили эксперименты на животных (см. ниже пример на проведение теста).
Пример 3 на приготовление шампуня
3-1: приготовление шампуня, содержащего [N-метил-D-Abu3] циклоспорин А
(Abu = L-аминомасляная кислота)
Смешивали вместе отдельные компоненты за исключением отдушки, красителя и воды; полученную смесь доводили до полного растворения путем нагревания при непрерывном перемешивании. После охлаждения до комнатной температуры к смеси примешивали отдушку и краситель. В заключение добавляли воду до 100% общей массы с получением трех видов шампуней, рецептуры которых приводятся ниже в таблице 15.

3-2: приготовление шампуня, содержащего [N-метил-D-Nva3] циклоспорин А
(Nva = L-норвалин)
Смешивали вместе отдельные компоненты за исключением отдушки, красителя и воды; полученную смесь доводили до полного растворения путем нагревания при непрерывном перемешивании. После охлаждения до комнатной температуры к смеси примешивали отдушку и краситель. В заключение добавляли воду до 100% общей массы с получением трех видов шампуней, рецептуры которых приводятся ниже в таблице 16.
3-3: приготовление шампуня, содержащего [D-2-(метиламино)гекса-4-иноил3] циклоспорин А
Смешивали вместе отдельные компоненты за исключением отдушки, красителя и воды; полученную смесь доводили до полного растворения путем нагревания при непрерывном перемешивании. После охлаждения до комнатной температуры к смеси примешивали отдушку и краситель. В заключение добавляли воду до 100% общей массы с получением трех видов шампуней, рецептуры которых приводятся ниже в таблице 17.
3-4: приготовление шампуня, содержащего [D-2-(метиламино)пент-4-иноил3] циклоспорин А
Смешивали вместе отдельные компоненты за исключением отдушки, красителя и воды; полученную смесь доводили до полного растворения путем нагревания при непрерывном перемешивании. После охлаждения до комнатной температуры к смеси примешивали отдушку и краситель. В заключение добавляли воду до 100% общей массы с получением трех видов шампуня, рецептуры которых приводятся ниже в таблице 18.
3-5: приготовление шампуня, содержащего [D-2-метилтио-Sar3] циклоспорин А (Sar=саркозин)
Смешивали вместе отдельные компоненты за исключением отдушки, красителя и воды; полученную смесь доводили до полного растворения путем нагревания при непрерывном перемешивании. После охлаждения до комнатной температуры к смеси примешивали отдушку и краситель. В заключение добавляли воду до 100% общей массы с получением трех видов шампуня, рецептуры которых приводятся ниже в таблице 19.
3-6: приготовление шампуня, содержащего [N-метил-O-пропенил-D-Ser3] циклорин А
Смешивали вместе отдельные компоненты за исключением отдушки, красителя и воды; полученную смесь доводили до полного растворения путем нагревания при непрерывном перемешивании. После охлаждения до комнатной температуры к смеси примешивали отдушку и краситель. В заключение добавляли воду до 100% общей массы с получением трех видов шампуня, рецептуры которых приводятся ниже в таблице 20.
3-7: приготовление шампуня, содержащего [N-метил-D-Ser3] циклоспорин А
Смешивали вместе отдельные компоненты за исключением отдушки, красителя и воды; полученную смесь доводили до полного растворения путем нагревания при непрерывном перемешивании. После охлаждения до комнатной температуры к смеси примешивали отдушку и краситель. В заключение добавляли воду до 100% общей массы с получением трех видов шампуня, рецептуры которых приводятся ниже в таблице 21.
Пример 4 на приготовление кондиционера для волос
4-1: приготовление кондиционера для волос, содержащего [N-метил-D-Abu3] циклоспорин А
(Abu = L-аминомасляная кислота)
Отдельные компоненты масляной и водной фаз смешивали в отдельных сосудах; каждую полученную смесь доводили до полного растворения путем нагрева до 80°С. Затем смешивали обе фазы компонентов, полученные смеси эмульгировали и охлаждали до комнатной температуры. Примешивали добавки (отдушку и краситель) и получали три вида кондиционера для волос, рецептуры которых приводятся ниже в таблице 22. Воду добавляли до 100% общей массы, включая компоненты масляной и водной фаз.
4-2: приготовление кондиционера для волос, содержащего [N-метил-D-Nva3] циклоспорин А
(Nva = L-норвалин)
Отдельные компоненты масляной и водной фаз смешивали в отдельных сосудах; каждую полученную смесь доводили до полного растворения путем нагрева до 80°С. Затем смешивали обе фазы компонентов, полученные смеси эмульгировали и охлаждали до комнатной температуры. Примешивали добавки (отдушку и краситель) и получали три вида кондиционера для волос, рецептуры которых приводятся ниже в таблице 23. Воду добавляли до 100% общей массы, включая компоненты масляной и водной фаз.
4-3: приготовление кондиционера для волос, содержащего [D-2-(метиламино)гекса-4-иноил3] циклоспорин А
Отдельные компоненты масляной и водной фаз смешивали в отдельных сосудах; каждую полученную смесь доводили до полного растворения путем нагрева до 80°С. Затем смешивали обе фазы компонентов, полученные смеси эмульгировали и охлаждали до комнатной температуры. Примешивали добавки (отдушку и краситель) и получали три вида кондиционера для волос, рецептуры которых приводятся ниже в таблице 24. Воду добавляли до 100% общей массы, включая компоненты масляной и водной фаз.
4-4: приготовление кондиционера для волос, содержащего [D-2-(метиламино)пент-4-иноил3] циклоспорин А
Отдельные компоненты масляной и водной фаз смешивали в отдельных сосудах; каждую полученную смесь доводили до полного растворения путем нагрева до 80°С. Затем смешивали обе фазы компонентов, полученные смеси эмульгировали и охлаждали до комнатной температуры. Примешивали добавки (отдушку и краситель) и получали три вида кондиционера для волос, рецептуры которых приводятся ниже в таблице 25. Воду добавляли до 100% общей массы, включая компоненты масляной и водной фаз.
4-5: приготовление кондиционера для волос, содержащего [D-2-метилтио-Sar3] циклоспорин А
(Sar = саркозин)
Отдельные компоненты масляной и водной фаз смешивали в отдельных сосудах; каждую полученную смесь доводили до полного растворения путем нагрева до 80°С. Затем смешивали обе фазы компонентов, полученные смеси эмульгировали и охлаждали до комнатной температуры. Примешивали добавки (отдушку и краситель) и получали три вида кондиционера для волос, рецептуры которых приводятся ниже в таблице 26. Воду добавляли до 100% общей массы, включая компоненты масляной и водной фаз.
4-6: приготовление кондиционера для волос, содержащего [N-метил-О-пропенил-D-Ser3] циклоспорин А
Отдельные компоненты масляной и водной фаз смешивали в отдельных сосудах; каждую полученную смесь доводили до полного растворения путем нагрева до 80°С. Затем смешивали обе фазы компонентов, полученные смеси эмульгировали и охлаждали до комнатной температуры. Примешивали добавки (отдушку и краситель) и получали три вида кондиционера для волос, рецептуры которых приводятся ниже в таблице 27. Воду добавляли до 100% общей массы, включая компоненты масляной и водной фаз.
4-7: приготовление кондиционера для волос, содержащего [N-метил-D-Ser3] циклоспорин А
Отдельные компоненты масляной и водной фаз смешивали в отдельных сосудах; каждую полученную смесь доводили до полного растворения путем нагрева до 80°С. Затем смешивали обе фазы компонентов, полученные смеси эмульгировали и охлаждали до комнатной температуры. Примешивали добавки (отдушку и краситель) и получали три вида кондиционера для волос, рецептуры которых приводятся ниже в таблице 28. Воду добавляли до 100% общей массы, включая компоненты масляной и водной фаз.
Пример на проведение теста: тест-оценка эффекта стимуляции роста волос циклоспорин-производных, являющихся предметом настоящего изобретения
Эксперименты проводились на самках мышей C57BL/6 в возрасте 6-7 недель. После удаления волосяного покрова с середины спины с помощью электробритвы животных взвешивали и распределяли по группам соответственно их массе. Один день был отведен для адаптации животных, а в течение последующих 30 дней на выбритый участок спины животных один раз в день наносили циклоспорин А и производные циклоспорина А (соединения с 1 по 7), полученные методом жидкостной хроматографии высокого разрешения в примере 1 в количестве 100 мкл (конц. 0,1 мас.%/об.). Результаты теста оценивали визуально по степени восстановления волосяного покрова. Контролировали и сравнивали между собой степень роста новых волос на выбритых участках спины животных.
Как видно из данных таблицы 29, производные циклоспорина, являющиеся предметом настоящего изобретения, показали более высокий эффект стимуляции роста волосяного покрова у мышей экспериментальных групп по сравнению с контрольной группой, в которой животных обрабатывали только обычным средством, при этом указанный эффект циклоспорин-производных был аналогичен эффекту стимуляции волосяного покрова циклоспорином А. Внешне не было отмечено никаких признаков раздражения кожи спины у животных контрольной и экспериментальных групп в течение всех 30 дней.
На основании вышеприведенных результатов сделан вывод, что производные циклоспорина, являющиеся предметом настоящего изобретения, можно вводить в рецептуры средств для роста волос любых форм, например в форме жидких составов, спреев, гелей, паст, эмульсий, кремов, кондиционеров, шампуней и т.п. В описании к настоящему изобретению приведены примеры на приготовление тоников, кремов, кондиционеров и шампуней для волос как средств, пользующихся самым высоким спросом среди потребителей. Как отмечалось в вышеприведенном примере на проведение теста на животных, производные циклоспорина показали более высокий эффект стимуляции роста волос по сравнению с контролем.
Промышленное использование настоящего изобретения
Из вышеприведенного описания очевидно, что настоящее изобретение касается средства для роста волос, содержащего в качестве активного компонента замещенное по положению 3 производное циклоспорина А, которое обладает высоким эффектом стимуляции роста волос.





Изобретение касается средства для роста волос, которое содержит в качестве активного компонента аналог циклоспорина по положению 3, полученный путем синтеза множества производных циклоспорина с оценкой их способности к стимуляции роста волос с целью создания нового средства для роста волос. Полученное средство для роста волос обладает высокой способностью к стимуляции роста волос и не проявляет побочных действий. 10 з.п. ф-лы, 29 табл., 14 ил.
[Формула 1]
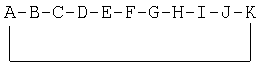
в которой А представляет собой N-метил-(4R)-4-[(Е)-2-бутенил]-4-метил-L-треонин, (2S,3R.4R.6Е)-3-сульфгидрил-4-метил-2-(метиламино)-6-октеновую кислоту или (2S,4R,6Е)-3-оксо-4-метил-2-(метиламино)-6-октеновую кислоту;
В представляет собой L-аминомасляную кислоту (Abu), L-аланин (Ala), L-треонин (Thr), L-валин (Val) или L-норвалин (Nva);
С представляет собой D-аминокислоту следующей общей формулы:
СН3NH-СН(R)-СООН,
в которой R выбирают из группы, включающей водород, C1-С6 прямые или разветвленные алкил, алкенил или алкинил остатки, замещенные или не замещенные одной или более группой, выбираемой из группы, включающей амино, окси, гало, галоалкил, эфирные, алкокси, циано, нитро, алкиламино и диалкиламино группы и -X-R' где Х - кислород или сера; R' выбирают из группы, включающей водород и C1-С6 прямые или разветвленные алкил, алкенил или алкинил остатки, замещенные или не замещенные одной или более группой, выбираемой из группы, включающей амино, окси, гало, галоалкил, эфирные, алкокси, циано, нитро, алкиламино и диалкиламино группы;
D представляет собой N-метил-L-лейцин, γ-окси-N-метил-L-лейцин или L-валин;
Е представляет собой L-валин или L-норвалин;
F представляет собой N-метил-L-лейцин, γ-окси-N-метил-L-лейцин или L-лейцин;
G представляет собой L-аланин или L-аланин тиоамид ([7ψ8CS-NH], NH-СНСН3-CS-);
Н представляет собой D-аминокислоту следующей общей формулы:
-NH-CH(CH2R)-COOH,
в которой R - водород или -X-R', где Х - кислород или сера; R' выбирают из группы, включающей водород и C1-C6 прямые или разветвленные алкил, алкенил или алкинил остатки, замещенные или не замещенные одной или более группой, выбираемой из группы, включающей амино, окси, гало, галоалкил, эфирные, алкокси, циано, нитро, алкиламино или диалкиламино группы;
I представляет собой N-метил-L-лейцин, γ-окси-N-метил-L-лейцин или L-лейцин;
J представляет собой N-метил-L-лейцин, γ-окси-N-метил-L-лейцин или L-лейцин;
К представляет собой N-метил-L-валин или L-валин.
[Формула 2]

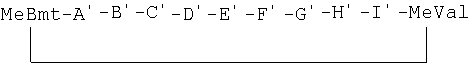
в которой MeBmt представляет собой N-метил-(4R)-4-[(Е)-2-бутенил]-4-метил-L-треонин;
А' представляет собой L-аминомасляную кислоту, L-аланин, L-треонин, L-валин или L-норвалин;
В' представляет собой N-метил-D-аминомасляную кислоту, N-метил-D-норвалин, D-2-(метиламино)гекса-4-иноил, D-2-(метиламино)пент-4-иноил, D-2-метилтио-саркозин, N-метил-О-пропенил-D-серин или N-метил-D-серин;
С' представляет собой N-метил-L-лейцин, γ-окси-N-метил-L-лейцин или L-валин;
D' представляет собой L-валин или L-норвалин;
Е' представляет собой N-метил-L-лейцин, γ-окси-N-метил-L-лейцин или L-лейцин;
F' представляет собой L-аланин и L-аланин тиоамид ([7ψ8CS-NH], NH-CHCH3-CS-)
G' представляет собой D-аланин или D-серин;
Н' представляет собой N-метил-L-лейцин, γ-окси-N-метил-L-лейцин или L-лейцин;
I' представляет собой N-метил-L-лейцин, γ-окси-N-метил-L-лейцин или L-лейцин;
MeVal представляет собой N-метил-L-валин.
[Формула 3]

в которой MeBmt представляет собой N-метил-(4R)-4-[(Е)-2-бутенил]-4-метил-L-треонин;
А'' представляет собой L-аланин, L-треонин, L-валин или L-норвалин;
В'' представляет собой N-метил-D-аминомасляную кислоту, N-метил-D-норвалин, D-2-(метиламино)гекса-4-иноил, D-2-(метиламино)пент-4-иноил, D-2-метилтио-саркозин, N-метил-О-пропенил-D-серин или N-метил-D-серин;
MeLeu представляет собой N-метил-L-лейцин;
Val представляет собой L-валин;
Ala представляет собой L-аланин;
DAla представляет собой D-аланин;
MeVal представляет собой N-метил-L-валин.
| 1972 |
|
SU414632A1 | |
| US 5807820 А, 15.09.1998 | |||
| ПРЕПАРАТЫ ЛИПОФИЛЬНЫХ НОСИТЕЛЕЙ | 1995 |
|
RU2127124C1 |
Авторы
Даты
2007-01-20—Публикация
2002-05-11—Подача