Область техники, к которой относится изобретение
Настоящее изобретение относится к полипептиду, обладающему антибактериальной активностью, композиции для профилактики или лечения сепсиса, которая включает его, а также к антибактериальной композиции и подобным.
Данная заявка испрашивает приоритет и преимущества корейской патентной заявки № 10-2019-0023534, поданной 28 февраля 2019 г., и корейской патентной заявки № 10-2020-0023629, поданной 26 февраля 2020 г., описания которых полностью включены в настоящий документ посредством ссылки.
Предшествующий уровень техники
Сепсис - это воспалительная реакция, вызванная чрезмерной активацией иммунной системы организма липополисахаридом (ЛПС), который является компонентом клеточной стенки, действующим как токсин, когда организм инфицирован патогенными грамотрицательными бактериями, и может вызывать инфекцию во всем организме или может сопровождаться шоком при наличии тяжелых симптомов. В частности, сепсис обычно возникает у пациентов с основными заболеваниями, такими как злокачественные опухоли, лейкемия, злокачественная лимфома, синдром приобретенного иммунодефицита (СПИД), коллагеновая болезнь, почечная недостаточность, заболевание печени, цереброваскулярные расстройства и диабет или у слаборезистентных хозяев с гуморальным или клеточным иммунодефицитом, например, у пожилых и недоношенных детей, проходящих химиотерапию стероидами надпочечников или противоопухолевыми препаратами, лучевую терапию, такую как облучение кобальтом, или лечение и хирургическое вмешательство, такие как постоянные катетеры, гемодиализ, трансплантация органов и хирургия сердца. Сепсис стал основной причиной смерти пациентов, госпитализированных в отделение интенсивной терапии больницы, и является очень серьезным заболеванием, летальность которого обычно составляет 30% и более. Несмотря на достижения в области медицинских технологий, во всем мире существует много случаев сепсиса, вызванного инфекцией, как следствие хирургического вмешательства, а инфицирование человека со слабым иммунитетом в организме, например новорожденного или пожилого человека, часто перерастает в сепсис. Обычно, как известно, неонатальный сепсис возникает примерно у 3 из 1000 доношенных новорожденных, а частота его возникновения у недоношенных детей возрастает в 3-4 раза.
В то время как сепсис обычно лечат антибиотиками, однако в случае, если лечение откладывается, так что размножается большое количество бактерий, или в случае заражения штаммом, имеющим устойчивость к антибиотикам, то лечение только антибиотиками неэффективно, при этом количество патогенов, устойчивых к различным антибиотикам, постепенно увеличивается. По этой причине существует острая потребность в разработке нового терапевтического средства от сепсиса.
Между тем, устойчивые к противомикробным препаратам бактерии относятся к бактериям, которые устойчивы к определенному антибактериальному средству, и, таким образом, средство не действует. Например, устойчивые к противомикробным препаратам бактерии включают устойчивый к пенициллину Staphylococcus aureus, который приводит к полной неэффективности пенициллина. Кроме того, известен устойчивый к метициллину золотистый стафилококк (МРЗС), о котором впервые было сообщено в академических кругах в 1961 году и который стал основной патогенной инфекционной бактерией во всем мире, а в 1988 году в Европе впервые был обнаружен устойчивый к ванкомицину энтерококк (ВРЭ). Кроме того, центры США по контролю и профилактике заболеваний впервые сообщили об устойчивом к ванкомицину золотистом стафилококке (ВРЗС), проявляющем высокую устойчивость к ванкомицину, известному как последний терапевтический агент против Staphylococcus aureus, который является наиболее частой причиной инфицирования человека в 2002 году. Взяв все вышеперечисленное вместе, можно увидеть, что распространение так называемых супербактерий резко увеличивается.
Описание изобретения
Техническая проблема, решаемая изобретением
В силу вышеизложенных обстоятельств, в результате повторных исследований, направленных на удовлетворение вышеописанных потребностей, изобретатели подтвердили, что пептид, имеющий конкретную аминокислотную последовательность, эффективен для ингибирования бактериальной пролиферации, а также для лечения сепсиса благодаря превосходному эффекту удаления эндотоксина, выделяемого из мертвых бактерий, и избирательно проявляет превосходную антибактериальную активность против грамположительных/грамотрицательных бактерий, и, таким образом, настоящее изобретение было завершено.
Соответственно, технические проблемы, которые должны быть решены в настоящем изобретении, направлены на обеспечение пептида, обладающего антибактериальной активностью, композиции для профилактики или лечения сепсиса, которая включает его, а также антибактериальной композиции и т.п.
Однако, технические проблемы, которые должны быть решены в настоящем изобретении, не ограничиваются вышеописанными, при этом другие проблемы, которые не описаны в данном документе, будут полностью понятны специалистам в данной области техники из последующих описаний.
Техническое решение
Для достижения цели настоящего изобретения, настоящее изобретение обеспечивает полипептид, представленный следующей общей формулой последовательности:
[Общая формула]
Ln-X1-L-X2-V-X3-X4-X5-R-X6-L-X7
В общей формуле,
n представляет собой 0 или 1;
L представляет собой лейцин;
V представляет собой валин;
R представляет собой аргинин;
X1 представляет собой лизин (K) или аргинин (R);
X2 представляет собой глицин (G) или аргинин (R);
X3 представляет собой глутаминовую кислоту (E) или лизин (K);
X4 представляет собой аланин (A) или лейцин (L);
X5 представляет собой лизин (K) или аргинин (R);
X6 представляет собой тирозин (Y), аланин (A), триптофан (W), лизин (K) или аспарагиновую кислоту (D); и
X7 представляет собой аспарагиновую кислоту (D) или аргинин (R),
однако, в общей формуле, полипептид, представленный последовательностью K-L-G-V-E-A-K-R-Y-L-D, исключен.
В одном варианте осуществления настоящего изобретения, обеспечивается любой из 9 типов полипептидов, состоящих из 1) - 9), как указано ниже:
1) полипептид, представленный общей формулой, в которой
n представляет собой 0;
X1 представляет собой лизин (K);
X2 представляет собой глицин (G);
X3 представляет собой глутаминовую кислоту (E);
Х4 представляет собой аланин (А);
Х5 представляет собой лизин (К);
X6 представляет собой тирозин (Y), и
X7 представляет собой аргинин (R);
2) полипептид, представленный общей формулой, в которой
n представляет собой 1;
X1 представляет собой аргинин (R);
X2 представляет собой глицин (G);
X3 представляет собой глутаминовую кислоту (E);
Х4 представляет собой аланин (А);
Х5 представляет собой лизин (К);
X6 представляет собой тирозин (Y), и
X7 представляет собой аргинин (R);
3) полипептид, представленный общей формулой, в которой
n представляет собой 1;
X1 представляет собой аргинин (R);
X2 представляет собой глицин (G);
X3 представляет собой глутаминовую кислоту (E);
X4 представляет собой лейцин (L);
Х5 представляет собой лизин (К);
X6 представляет собой тирозин (Y), и
X7 представляет собой аргинин (R);
4) полипептид, представленный общей формулой, в которой
n представляет собой 0;
X1 представляет собой лизин (K);
X2 представляет собой глицин (G);
X3 представляет собой глутаминовую кислоту (E);
Х4 представляет собой аланин (А);
X5 представляет собой лейцин (L);
X6 представляет собой тирозин (Y), и
X7 представляет собой аспарагиновую кислоту (D);
5) полипептид, представленный общей формулой, в которой
n представляет собой 0;
X1 представляет собой аргинин (R);
X2 представляет собой аргинин (R);
Х3 представляет собой лизин (К);
X4 представляет собой лейцин (L);
X5 представляет собой аргинин (R);
X6 представляет собой тирозин (Y), и
X7 представляет собой аргинин (R);
6) полипептид, представленный общей формулой, в которой
n представляет собой 0;
X1 представляет собой лизин (K);
X2 представляет собой аргинин (R);
Х3 представляет собой лизин (К);
X4 - представляет собой лейцин (L);
X5 представляет собой аргинин (R);
X6 представляет собой тирозин (Y), и
X7 представляет собой аргинин (R);
7) полипептид, представленный общей формулой, в которой
n представляет собой 0;
X1 представляет собой лизин (K);
X2 представляет собой аргинин (R);
Х3 представляет собой лизин (К);
X4 представляет собой лейцин (L);
X5 представляет собой аргинин (R);
X6 представляет собой аланин (A), и
X7 представляет собой аргинин (R);
8) полипептид, представленный общей формулой, в которой
n представляет собой 0;
X1 представляет собой лизин (K);
X2 представляет собой аргинин (R);
Х3 представляет собой лизин (К);
X4 представляет собой лейцин (L);
X5 представляет собой аргинин (R);
X6 представляет собой триптофан (W), и
X7 представляет собой аргинин (R); и
9) полипептид, представленный общей формулой, в которой
n представляет собой 0;
X1 представляет собой лизин (K);
X2 представляет собой аргинин (R);
Х3 представляет собой лизин (К);
X4 представляет собой лейцин (L);
X5 представляет собой аргинин (R);
X6 представляет собой лизин (K), и
X7 представляет собой аргинин (R).
В одном варианте осуществления настоящего изобретения, полипептид относится к пептидомиметику, включая пептид L-типа, пептид D-типа и пептоид, или содержит неприродные аминокислоты.
В одном варианте осуществления настоящего изобретения, конец полипептида алкилирован, ПЭГилирован или амидирован.
В одном варианте осуществления настоящего изобретения, аминогруппа (NH2) добавляется к С-концу полипептида.
В одном варианте осуществления настоящего изобретения, полипептид имеет одну или несколько из следующих характеристик:
связывающую способность к липополисахариду (ЛПС) грамотрицательных бактерий;
способность избирательного разрушения мембраны бактериальных клеток;
устойчивость к протеолитическим ферментам;
способность разрушать клеточную мембрану против грамположительных бактерий; и
способность связываться с липотейхоевой кислотой (ЛТК) или липопротеином (LPP), полученным из грамположительных бактерий.
Кроме того, настоящее изобретение обеспечивает производное полипептида с замещением ацетатной солью трифторуксусной кислоты (ТФЛ), представленного общей формулой последовательности.
Кроме того, настоящее изобретение обеспечивает композицию для профилактики, облегчения или лечения сепсиса, которая включает полипептид, представленный общей формулой последовательности, или его производное с замещением ацетатной солью трифторуксусной кислоты в качестве активного ингредиента.
Кроме того, настоящее изобретение обеспечивает фармацевтическую/пищевую/диетическую/косметическую/квазилекарственную/кормовую композицию для профилактики, облегчения или лечения сепсиса, которая включает полипептид, представленный общей формулой последовательности, или его производное с замещением ацетатной солью трифторуксусной кислоты в качестве активного ингредиента.
Настоящее изобретение обеспечивает способ профилактики или лечения сепсиса, который включает введение полипептида, представленного общей формулой последовательности, или его производного с замещением ацетатной солью трифторуксусной кислоты субъекту, нуждающемуся в этом
Кроме того, настоящее изобретение обеспечивает применение полипептида, представленного общей формулой последовательности, или его производного с замещением ацетатной солью трифторуксусной кислоты для профилактики, облегчения или лечения сепсиса.
Кроме того, настоящее изобретение обеспечивает применение полипептида, представленного общей формулой последовательности, или его производного с замещением ацетатной солью трифторуксусной кислоты для приготовления препарата для профилактики, облегчения или лечения сепсиса.
Кроме того, настоящее изобретение обеспечивает антибактериальную композицию, которая включает полипептид, представленный общей формулой последовательности, или его производное с замещением ацетатной солью трифторуксусной кислоты в качестве активного ингредиента.
Кроме того, настоящее изобретение обеспечивает антибактериальную фармацевтическую/пищевую/диетическую/косметическую/квазилекарственную/кормовую композицию, которая включает полипептид, представленный общей формулой последовательности, или его производное с замещением ацетатной солью трифторуксусной кислоты в качестве активного ингредиента.
Настоящее изобретение обеспечивает антибактериальный способ, который включает введение полипептида, представленного общей формулой последовательности, или его производного с замещением ацетатной солью трифторуксусной кислоты нуждающемуся в этом субъекту.
Кроме того, настоящее изобретение обеспечивает антибактериальное применение полипептида, представленного общей формулой последовательности, или его производного с замещением ацетатной солью трифторуксусной кислоты.
Кроме того, настоящее изобретение обеспечивает применение полипептида, представленного общей формулой последовательности, или его производного с замещением ацетатной солью трифторуксусной кислоты для получения антибактериального агента.
В одном варианте осуществления настоящего изобретения, бактерии, на которые нацелена антибактериальная композиция, включают один или несколько типов, выбранных из группы, состоящей из Escherichia coli DH5α, Escherichia coli K1, Acinetobacter baumannii, Pseudomonas aeruginosa, Salmonella enteritidis, Salmonella typhimurium, Klebsiella pneumoniae, Staphylocus и Staphylococcus epidermidis.
В одном варианте осуществления настоящего изобретения, бактерии, на которые нацелена антибактериальная композиция, включают один или несколько типов устойчивых к антибиотикам бактерий, выбранных из группы, состоящей из бактерий, устойчивых к бета-лактамазе расширенного спектра (БЛРС), устойчивых к карбапенемам бактерий и бактерий, устойчивых к колистину.
В одном варианте осуществления настоящего изобретения, устойчивые к антибиотикам бактерии включают один или несколько типов, выбранных из группы, состоящей из БЛРС (E. coli), устойчивого к карбапенемам (CR)-Acinetobactor baumannii, CR-Klebsiella pneumoniae, CR-Pseudomonas aeruginosa, и устойчивого к колистину Acinetobactor baumannii.
Кроме того, настоящее изобретение обеспечивает композицию для профилактики, облегчения или лечения инфекционного заболевания, которая включает полипептид, представленный общей формулой последовательности, или его производное с замещением ацетатной солью трифторуксусной кислоты в качестве активного ингредиента.
Кроме того, настоящее изобретение обеспечивает фармацевтическую/пищевую/диетическую/косметическую/квазилекарственную/кормовую композицию для профилактики, облегчения или лечения инфекционного заболевания, которая включает полипептид, представленный общей формулой последовательности, или его производное с замещением ацетатной солью трифторуксусной кислоты в качестве активного ингредиента.
Настоящее изобретение обеспечивает способ профилактики или лечения инфекционного заболевания, который включает введение полипептида, представленного общей формулой последовательности, или его производного с замещением ацетатной солью трифторуксусной кислоты нуждающемуся в этом субъекту.
Кроме того, настоящее изобретение обеспечивает применение полипептида, представленного общей формулой последовательности, или его производного с замещением ацетатной солью трифторуксусной кислоты для профилактики, облегчения или лечения инфекционного заболевания.
Кроме того, настоящее изобретение обеспечивает применение полипептида, представленного общей формулой последовательности, или его производного с замещением ацетатной солью трифторуксусной кислоты для приготовления препарата для профилактики, облегчения или лечения инфекционного заболевания.
В одном варианте осуществления настоящего изобретения, инфекционное заболевание представляет собой заболевание, связанное с инфекцией грамотрицательных бактерий, выбранное из группы, состоящей из пневмонии, перитонита, менингита, раневой инфекции, остеоартрита, холецистита, инфекции мочевыводящих путей, эндокардита, миокардита, перикардита, артрита, фарингита, гонореи, бактериальной дизентерии, энтерита, конъюнктивита, гастрита, среднего отита, цистита и лимфангита.
В одном варианте осуществления настоящего изобретения инфекционное заболевание представляет собой заболевание, связанное с инфицированнием грамположительными бактериями, выбранное из группы, состоящей из ларингофарингита, импетиго, ревматической лихорадки, гломерулонефрита, неонатального сепсиса, менингита, фарингита, пневмонии, эндокардита, скарлатины, SSTI (инфекции кожи и мягких тканей), глубокой инфекции мягких тканей, эмпиемы и вагинита.
Кроме того, настоящее изобретение обеспечивает полинуклеотид, кодирующий полипептид, представленный общей формулой последовательности.
Кроме того, настоящее изобретение обеспечивает рекомбинантный вектор, включающий полинуклеотид.
Кроме того, настоящее изобретение обеспечивает способ получения полипептида, представленного общей формулой последовательности, который включает культивирование клеток-хозяев, трансформированных рекомбинантным вектором.
Благоприятные эффекты
Пептид в соответствии с настоящим изобретением обладает превосходными эффектами не только ингибирования размножения стандартных бактерий и устойчивых к антибиотикам бактерий, но также удаления эндотоксина бактериального происхождения, тем самым проявляя превосходный эффект лечения сепсиса, причем при использовании в сочетании с антибиотиком пептид может минимизировать побочные эффекты, вызванные антибиотиком, и, таким образом, может быть эффективно использован для профилактики или лечения сепсиса.
Кроме того, пептид согласно настоящему изобретению избирательно обладает превосходной антибактериальной активностью против грамположительных/грамотрицательных бактерий и, таким образом, может быть эффективно использован в антибактериальной композиции против грамположительных/грамотрицательных бактерий или для профилактики или лечения различных инфекционных заболеваний, вызванных грамположительными/грамотрицательными бактериями.
Кроме того, пептид согласно настоящему изобретению не только безопасен для человеческого организма, но также демонстрирует стабильность против протеолитических ферментов и, таким образом, может использоваться для множества целей.
Описание чертежей
Фиг.1 представляет собой набор графиков, иллюстрирующих результат измерения гемолитической активности согласно примеру 4 настоящего изобретения:
Слева направо вверху: FP12-NH2 (SEQ ID NO: 6)/allD_FP12-NH2 (SEQ ID NO: 8); и FP13-NH2 (SEQ ID NO: 7)/allD_FP13-NH2 (SEQ ID NO: 9).
Слева направо снизу, allD_FP13_9A (SEQ ID NO: 10)/allD_FP13_9D (SEQ ID NO: 18); и allD_FP13_9W (SEQ ID NO: 11)/allD_FP13_9K (SEQ ID NO: 12).
Фиг.2 представляет собой набор графиков, иллюстрирующих результат измерения вторичных структур пептидов с помощью спектроскопии дихроизма с круговой поляризацией согласно примеру 5 настоящего изобретения.
Фиг.3 представляет собой набор графиков, показывающих результат измерения разрушающей способности пептидов по отношению к липосомам, имитирующим мембрану бактериальных клеток (вверху) и мембрану красных кровяных телец (внизу) согласно примеру 6 настоящего изобретения.
Фиг.4 иллюстрирует антибиотический эффект пептида allD FP13-NH2 согласно примеру 8 настоящего изобретения. Слева направо - антибиотический эффект пептида allD FP13-NH2 против стандартного штамма Escherichia coli K1; антибиотический эффект пептида allD FP13-NH2 против клинического штамма Escherichia coli (БЛРС); и антибиотический эффект пептида allD FP13-NH2 против клинического штамма Acinetobacter baummanii, устойчивого к карбапенемам.
Фиг.5A-5C иллюстрируют антибиотический эффект, токсический эффект и противовоспалительный цитокин-ингибирующий эффект пептида allD FP13-NH2 (AcOH) согласно примеру 9 настоящего изобретения:
Фиг.5А показывает сравнение эффектов антибиотиков AllD FP13-NH2 (TFA) (вверху) и AllD FP13-NH2 (AcOH) (внизу) против Escherichia coli (БЛРС);
Фиг.5В показывает сравнение токсичности in vivo между AllD FP13-NH2 (TFA) (вверху) и AllD FP13-NH2 (AcOH) (внизу); и
Фиг.5C показывает сравнение противовоспалительного цитокин(IL-6)- ингибирующего эффекта между AllD FP13-NH2 (TFA; вверху) и AllD FP13-NH2 (AcOH; внизу).
Фиг.6 представляет собой набор графиков, показывающих результат измерения разрушающей способности пептидов по отношению к липосомам, имитирующим клеточные мембраны грамположительных бактерий, согласно варианту осуществления 11 настоящего изобретения.
Способы изобретения
Настоящее изобретение относится к полипептиду, представленному следующей общей формулой последовательности:
[Общая формула]
Ln-X1-L-X2-V-X3-X4-X5-R-X6-L-X7
В общей формуле
n представляет собой 0 или 1;
L представляет собой лейцин;
V представляет собой валин;
R представляет собой аргинин;
X1 представляет собой лизин (K) или аргинин (R);
X2 представляет собой глицин (G) или аргинин (R);
X3 представляет собой глутаминовую кислоту (E) или лизин (K);
X4 представляет собой аланин (A) или лейцин (L);
X5 представляет собой лизин (K) или аргинин (R);
X6 представляет собой тирозин (Y), аланин (A), триптофан (W), лизин (K) или аспарагиновую кислоту (D); и
X7 представляет собой аспарагиновую кислоту (D) или аргинин (R),
однако полипептид, имеющий аминокислотную последовательность K-L-G-V-E-A-K-R-Y-L-D, исключен.
В одном варианте осуществления настоящего изобретения один или несколько полипептидов 9 типов полипептидов, представленных общей формулой 1) - 9), имеют следующие значения:
1) полипептид, представленный общей формулой, в которой
n равно 0;
X1 представляет собой лизин (K);
X2 представляет собой глицин (G);
X3 представляет собой глутаминовую кислоту (E);
Х4 представляет собой аланин (А);
Х5 представляет собой лизин (К);
X6 представляет собой тирозин (Y), и
X7 представляет собой аргинин (R),
то есть полипептид, имеющий аминокислотную последовательность KLGVEAKRYLR (SEQ ID NO: 2);
2) полипептид, представленный общей формулой, в которой
n представляет собой 1;
X1 представляет собой аргинин (R);
X2 представляет собой глицин (G);
X3 представляет собой глутаминовую кислоту (E);
Х4 представляет собой аланин (А);
Х5 представляет собой лизин (К);
X6 представляет собой тирозин (Y), и
X7 представляет собой аргинин (R),
то есть полипептид, имеющий аминокислотную последовательность LRLGVEAKRYLR (SEQ ID NO: 3);
3) полипептид, представленный общей формулой, в которой
n представляет собой 1;
X1 представляет собой аргинин (R);
X2 представляет собой глицин (G);
X3 представляет собой глутаминовую кислоту (E);
X4 представляет собой лейцин (L);
Х5 представляет собой лизин (К);
X6 представляет собой тирозин (Y), и
X7 представляет собой аргинин (R),
то есть полипептид, имеющий аминокислотную последовательность LRLGVELKRYLR (SEQ ID NO: 4);
4) полипептид, представленный общей формулой, в которой
n представляет собой 0;
X1 представляет собой лизин (K);
X2 представляет собой глицин (G);
X3 представляет собой глутаминовую кислоту (E);
Х4 представляет собой аланин (А);
X5 представляет собой- лейцин (L);
X6 представляет собой тирозин (Y), и
X7 представляет собой аспарагиновую кислоту (D),
то есть полипептид, имеющий аминокислотную последовательность KLGVEALRYLD (SEQ ID NO: 5);
5) полипептид, представленный общей формулой, в которой
n представляет собой 0;
X1 представляет собой аргинин (R);
X2 представляет собой аргинин (R);
Х3 представляет собой лизин (К);
X4 представляет собой лейцин (L);
X5 представляет собой аргинин (R);
X6 представляет собой тирозин (Y), и
X7 представляет собой аргинин (R),
то есть полипептид, имеющий аминокислотную последовательность RLRVKLRRYLR (SEQ ID NO: 15);
6) полипептид, представленный общей формулой, в которой
n представляет собой 0;
X1 представляет собой лизин (K);
X2 представляет собой аргинин (R);
Х3 представляет собой лизин (К);
X4 представляет собой лейцин (L);
X5 представляет собой аргинин (R);
X6 представляет собой тирозин (Y), и
X7 представляет собой аргинин (R),
то есть полипептид, имеющий аминокислотную последовательность KLRVKLRRYLR (SEQ ID NO: 16);
7) полипептид, представленный общей формулой, в которой
n представляет собой 0;
X1 представляет собой лизин (K);
X2 представляет собой аргинин (R);
Х3 представляет собой лизин (К);
X4 представляет собой лейцин (L);
X5 представляет собой аргинин (R);
X6 представляет собой аланин (A), и
X7 представляет собой аргинин (R),
то есть полипептид, имеющий аминокислотную последовательность KLRVKLRRALR (SEQ ID NO: 10);
8) полипептид, представленный общей формулой, в которой
n представляет собой 0;
X1 представляет собой лизин (K);
X2 представляет собой аргинин (R);
Х3 представляет собой лизин (К);
X4 представляет собой лейцин (L);
X5 представляет собой аргинин (R);
X6 представляет собой триптофан (W), и
X7 представляет собой аргинин (R),
то есть полипептид, имеющий аминокислотную последовательность KLRVKLRRWLR (SEQ ID NO: 11); и
9) полипептид, представленный общей формулой, в которой
n равно 0;
X1 представляет собой лизин (K);
X2 представляет собой аргинин (R);
Х3 представляет собой лизин (К);
X4 представляет собой лейцин (L);
X5 представляет собой аргинин (R);
X6 представляет собой лизин (K), и
X7 представляет собой аргинин (R),
то есть полипептид, имеющий аминокислотную последовательность KLRVKLRRKLR (SEQ ID NO: 12).
Используемый здесь термин «полипептид» относится к линейной молекуле, образованной соединением аминокислотных остатков пептидными связями. Полипептид по настоящему изобретению может быть получен методом химического синтеза, известным в данной области (например, метод твердофазного синтеза), а также методами молекулярной биологии (Merrifield, J. Amer. Chem. Soc. 85: 2149-54 (1963); Stewart, et al., Solid Phase Peptide Synthesis, 2nd. ed., Pierce Chem. Co .: Rockford, 111 (1984)).
Кроме того, в полипептиды по настоящему изобретению охватывают биологически функциональные эквиваленты, имеющие вариацию в аминокислотной последовательности, проявляющей биологическую активность, эквивалентную полипептиду по настоящему изобретению. Вариация аминокислотной последовательности может быть создана на основе относительного сходства, например, гидрофобности, гидрофильности, заряда или размера аминокислотного заместителя. Анализируя размер, форму и тип заместителя боковой цепи аминокислоты, можно увидеть, что все аргинин, лизин и гистидин являются положительно заряженными остатками; аланин, глицин и серин имеют схожие размеры; а фенилаланин, триптофан и тирозин имеют похожие формы. Следовательно, исходя из этих соображений, аргинин, лизин и гистидин; аланин, глицин и серин; или фенилаланин, триптофан и тирозин могут быть биологически функциональными эквивалентами.
Для введения вариации, можно рассмотреть индекс гидрофобности аминокислот. Индекс гидрофобности присваивается каждой аминокислоте в соответствии с гидрофобностью и зарядом. Кроме того, также известно, что замена аминокислот, имеющих сходную гидрофильность, приводит к получению пептидов, обладающих эквивалентной биологической активностью.
Аминокислотный обмен в пептидах, которые не полностью изменяют молекулярную активность, известен в данной области (H. Neurath, R. L. Hill, The Proteins, Academic Press, New York, 1979). Наиболее часто встречающийся обмен - это обмен между аминокислотными остатками, например, Ala/Ser, Val/Ile, Asp/Glu, Thr/Ser, Ala/Gly, Ala/Thr, Ser/Asn, Ala/Val, Ser/Gly, Thy/Phe, Ala/Pro, Lys/Arg, Asp/Asn, Leu/Ile, Leu/Val, Ala/Glu и Asp/Gly.
Принимая во внимание вариации с описанной выше биологически эквивалентной активностью, полипептид по настоящему изобретению должен включать последовательность, проявляющую существенную идентичность с последовательностью, указанной в приложенном списке последовательностей. Существенная идентичность может относиться к последовательности, проявляющей по меньшей мере 80%, 90% или 95% гомологии, когда любая другая последовательность выравнивается в максимально возможной степени с последовательностью по настоящему изобретению и анализируется с использованием алгоритма, обычно используемого в данной области. Метод выравнивания для сравнения последовательностей известен в данной области (Huang et al., Comp. Appl. BioSci. 8: 155-65 (1992); Pearson et al., Meth. Mol. Biol. 24: 307-31 (1994)).
Кроме того, в одном варианте осуществления настоящего изобретения полипептид, представленный общей формулой последовательности согласно настоящему изобретению, может быть пептидомиметиком, включая пептид L-типа, пептид D-типа и пептоид, или содержащим неприродные аминокислоты.
Полипептид D-типа представляет собой энантиомер, который имеет ту же аминокислотную последовательность, что и полипептид L-типа, и относится к полипептиду алломерного типа.
В примерном варианте осуществления настоящего изобретения, например, в качестве полипептида алломерного типа, который имеет ту же аминокислотную последовательность, что и FP12-NH2 (SEQ ID NO: 6), предоставляется allD FP12-NH2 (SEQ ID NO: 8).
Термин «allD», используемый здесь для обозначения полипептида, относится к полипептиду D-типа.
Полипептид, который представляет собой пептидомиметик, включающий L-тип, D-тип и пептоид или содержащий неприродные аминокислоты, может быть получен различными способами, известными в данной области, в соответствии с заранее определенной аминокислотной последовательностью.
В одном варианте осуществления настоящего изобретения конец полипептида, представленного общей формулой последовательности согласно настоящему изобретению, алкилирован, ПЭГилирован или амидирован.
В примерном варианте осуществления настоящего изобретения в полипептиде согласно настоящему изобретению N-конец allD FP13-NH2 (AcOH) (SEQ ID NO: 13) был ПЭГилирован, тем самым обеспечивая PEG-allD FP13-NH2 (AcOH) (SEQ ID NO: 14). Для ПЭГилирования полипептид согласно настоящему изобретению может реагировать с Fmoc-NH-PEG2-CH2COOH, но настоящее изобретение этим не ограничивается. В данном случае, молекулярная масса (MW) полиэтиленгликоля составляет 385,4 Да.
Условия для ПЭГилирования могут быть скорректированы специалистами в данной области в соответствии с выбранным полипептидом, и ПЭГилирование может быть выполнено различными способами, известными в данной области.
Условия для алкилирования или амидирования также могут быть отрегулированы средним специалистом в данной области в зависимости от выбранного полипептида, и алкилирование или амидирование можно проводить различными способами, известными в данной области.
В одном варианте осуществления настоящего изобретения аминогруппа (NH2) может быть добавлена к С-концу полипептида, представленного общей формулой последовательности согласно настоящему изобретению.
В примерном варианте осуществления настоящего изобретения, в качестве полипептида, к которому аминогруппа (NH2) добавлена к С-концу FP12 (SEQ ID NO: 15) в полипептиде согласно настоящему изобретению, обеспечивается FP12-NH2 (SEQ ID NO: 6).
Термин «-NH2», используемый здесь для обозначения полипептида, относится к С-концу полипептида, к которому добавлена аминогруппа (NH2).
Добавление аминогруппы (NH2) к С-концу полипептида может быть выполнено различными способами, известными в данной области.
Кроме того, полипептид по настоящему изобретению также может охватывать его фармацевтически приемлемую соль.
Используемый здесь термин «фармацевтически приемлемый» относится к пептиду, который подходит для использования в контакте с тканью субъекта (например, человека) из-за разумного соотношения польза/риск без чрезмерной токсичности, раздражителя, аллергической реакции или других проблем, или осложнения, и включен в объем здравого медицинского заключения. Фармацевтически приемлемая соль включает, например, кислотно-аддитивную соль, образованную фармацевтически приемлемой свободной кислотой и фармацевтически приемлемой солью металла.
Примерами подходящих кислот включают соляную кислоту, бромную кислоту, серную кислоту, азотную кислоту, перхлорную кислоту, фумаровую кислоту, малеиновую кислоту, фосфорную кислоту, гликолевую кислоту, молочную кислоту, салициловую кислоту, янтарную кислоту, п-толуолсульфоновую кислоту, винную кислоту, уксусную кислоту, лимонную кислоту, метансульфоновую кислоту, муравьиную кислоту, бензойную кислоту, малоновую кислоту, глюконовую кислоту, нафталин-2-сульфоновую кислоту и бензолсульфоновую кислоту. Соль присоединения кислоты может быть получена обычным способом, например, растворением соединения в избыточном количестве водного раствора кислоты и осаждением соли с использованием смешивающегося с водой органического растворителя, такого как метанол, этанол, ацетон или ацетонитрил. Кроме того, кислотно-аддитивная соль может быть получена нагреванием эквимолярных количеств соединения и кислоты или спирта в воде и выпариванием, а затем сушкой смеси или отсасыванием осажденной соли.
Соли, полученные из подходящих оснований, могут включать щелочные металлы, такие как натрий и калий, щелочноземельные металлы, такие как магний, и аммоний, но настоящее изобретение этим не ограничивается. Щелочные металлы или щелочноземельные металлы могут быть получены, например, растворением соединения в избыточном растворе гидроксида щелочного металла или гидроксида щелочноземельного металла, фильтрованием нерастворенной соли соединения и выпариванием и сушкой фильтрата. В данном случае фармацевтически подходящим является приготовление соли металла, в частности соли натрия, калия или кальция, и, кроме того, соответствующая ей соль серебра может быть получена путем взаимодействия соли щелочного или щелочноземельного металла с подходящей солью серебра. (например, нитрат серебра).
В качестве фармацевтически приемлемой соли описанного выше полипептида настоящее изобретение обеспечивает ацетатную соль описанного выше полипептида.
Более конкретно, обеспечивается производное полипептида с замещением ацетатной солью трифторуксусной кислоты (ТФК) согласно настоящему изобретению.
Более конкретно, настоящее изобретение обеспечивает ацетатную соль полипептида, представленного описанной выше общей формулой последовательности; полипептид, который представляет собой пептидомиметик, включая пептид L-типа, пептид D-типа и пептоид или содержащего неприродные аминокислоты; полипептид, конец которого алкилирован, ПЭГилирован или амидирован; или полипептид, к С-концу которого добавлена аминогруппа (NH2).
Термин «АсОН», используемый здесь для названия полипептида, означает ацетатную соль полипептида.
Полипептид по настоящему изобретению и его солевое производное имеют одну или несколько следующих характеристик:
связывающую способность к липополисахариду (ЛПС) грамотрицательных бактерий;
способность избирательного разрушения мембраны бактериальных клеток;
устойчивость к протеолитическим ферментам;
способность разрушать клеточную мембрану против грамположительных бактерий; и
способность связываться с липотейхоевой кислотой (ЛТК) или липопротеином (ЛПП), полученной из грамположительных бактерий.
В примерном варианте осуществления настоящего изобретения были подтверждены следующие характеристики полипептида согласно настоящему изобретению и его солевого производного, но настоящее изобретение этим не ограничивается.
В примерном варианте осуществления настоящего изобретения было подтверждено, что полипептид согласно настоящему изобретению и его солевое производное обладают сильной связывающей способностью с липополисахаридом (ЛПС) (Пример 1).
Кроме того, в примерном варианте осуществления настоящего изобретения было подтверждено, что полипептид согласно настоящему изобретению и его солевое производное обладают способностью разрушать мембрану бактериальной клетки (примеры 6 и 11). В частности, он не проявлял разрушающей способности клеточной мембраны эритроцита, что доказывает безопасность (Пример 6).
Кроме того, в примерном варианте осуществления настоящего изобретения было подтверждено, что полипептид согласно настоящему изобретению и его солевое производное обладают превосходной устойчивостью к протеолитическим ферментам (Пример 7). Даже при обработке вместе с протеолитическим ферментом полипептид по настоящему изобретению и его солевое производное проявляют превосходную антибактериальную активность, подтверждая, что обеспечивается стабильность против протеолитических ферментов.
Кроме того, в примерном варианте осуществления настоящего изобретения было подтверждено, что полипептид согласно настоящему изобретению и его солевое производное обладают превосходной связывающей способностью с липотейхоевой кислотой (ЛТК) и липопротеином (ЛПП), которые являются компонентами клеточной стенки грамположительных бактерий (Пример 12).
Кроме того, в примерном варианте осуществления настоящего изобретения было подтверждено, что полипептид согласно настоящему изобретению и его солевое производное проявляют незначительную гемолитическую активность, подтверждая, что токсичность очень низкая (Пример 4).
Кроме того, настоящее изобретение обеспечивает композицию для профилактики, облегчения или лечения сепсиса, которая включает полипептид, представленный общей формулой последовательности, или его производное с замещением ацетатной солью трифторуксусной кислоты в качестве активного ингредиента.
Кроме того, настоящее изобретение обеспечивает фармацевтическую/пищевую/диетическую/косметическую/квазилекарственную/кормовую композицию для профилактики, облегчения или лечения сепсиса, которая включает полипептид, представленный общей формулой последовательности, или его производное с замещением ацетатной солью трифторуксусной кислоты в качестве активного ингредиента.
Настоящее изобретение обеспечивает способ профилактики или лечения сепсиса, который включает введение полипептида, представленного общей формулой последовательности, или его производного с замещением ацетатной солью трифторуксусной кислоты субъекту, нуждающемуся в этом.
Кроме того, настоящее изобретение обеспечивает применение полипептида, представленного общей формулой последовательности, или его производного с замещением ацетатной солью трифторуксусной кислоты для профилактики, облегчения или лечения сепсиса.
Кроме того, настоящее изобретение обеспечивает применение полипептида, представленного общей формулой последовательности, или его производного с замещением ацетатной солью трифторуксусной кислоты для приготовления препарата для профилактики, облегчения или лечения сепсиса.
Используемый здесь термин «сепсис» относится к состоянию, при котором во всем организме возникает тяжелая воспалительная реакция в результате инфицирования микроорганизмами. Когда два или более симптома среди лихорадки, при которой температура тела повышается до 38°С или более, переохлаждение, при котором температура тела снижается до 36°С или меньше, увеличение частоты дыхания до 24 ударов в минуту (тахипноэ), учащенное сердцебиение частота до 90 ударов в минуту (тахикардия) или увеличение или значительное уменьшение количества лейкоцитов наблюдается при анализе крови, это называется синдромом системного воспалительного ответа (SIRS). Когда ССВО вызвано микробной инфекцией, это называется сепсисом. Патогены постоянно или периодически попадают в кровоток из инфекционных поражений тела и оседают в различных тканях органов, образуя поражения и проявляя тяжелые системные симптомы. Возбудители бактерий включают Staphylococcus, Streptococcus, Escherichia, Pseudomonas aeruginosa, Mycobacterium tuberculosis, Klebsiella pneumoniae, грибы и анаэробы, но настоящее изобретение этим не ограничивается.
Кроме того, настоящее изобретение обеспечивает антибактериальную композицию, которая включает полипептид, представленный общей формулой последовательности, или его производное с замещением ацетатной солью трифторуксусной кислоты в качестве активного ингредиента.
Кроме того, настоящее изобретение обеспечивает антибактериальную фармацевтическую/пищевую/здоровую пищу/косметическую/квазилекарственную композицию/корм, которая включает полипептид, представленный общей формулой последовательности, или его производное с замещением ацетатной солью трифторуксусной кислоты в качестве активного ингредиента.
Настоящее изобретение обеспечивает антибактериальный способ, который включает введение полипептида, представленного общей формулой последовательности, или его производного с замещением ацетатной солью трифторуксусной кислоты нуждающемуся в этом субъекту.
Кроме того, настоящее изобретение обеспечивает антибактериальное применение полипептида, представленного общей формулой последовательности, или его производного с замещением ацетатной солью трифторуксусной кислоты.
Кроме того, настоящее изобретение обеспечивает применение полипептида, представленного общей формулой последовательности, или его производного с замещением ацетатной солью трифторуксусной кислоты для получения антибактериального агента.
Термин «антибактериальная» или «антибактериальная активность», используемый здесь, относится к характеристике устойчивости к микроорганизмам, таким как бактерии или грибы, и, более конкретно, к характеристике ингибирования роста или размножения бактерий антибиотическим материалом.
Термин «антибактериальная композиция», используемый здесь, представляет собой композицию, обладающую активностью подавления роста микроорганизмов, таких как бактерии или грибки, и может быть представлена в любой форме, используемой в различных областях, требующих антибактериального эффекта, например, в медикамента, косметического средства, квази- лекарства, пищевой добавки или кормовой и В частности, такая композиция может использоваться в качестве антибактериального, или противообрастающего агента в медицинских средствах, с целью консерванта или антибактериального действия в пищевых продуктах, с целью антибактериального, бактерицидного или антисептического действия в сельском хозяйстве, может использоваться в продуктах, непосредственно связанных с к микроорганизмам для профилактики перхоти, профилактики микоза, подавления запаха подмышек или борьбы с прыщами в косметике и бытовых товарах, или используемых с целью консерванта, антибактериального или бактерицидного действия в чистящих средствах или моющих средствах для мытья посуды, но настоящее изобретение не ограничивается этим.
В одном варианте осуществления настоящего изобретения антибактериальные мишени антибактериальной композиции согласно настоящему изобретению включают грамотрицательные бактерии, грамположительные бактерии, устойчивые к антибиотикам грамотрицательные бактерии и устойчивые к антибиотикам грамположительные бактерии.
Используемый здесь термин «грамотрицательные бактерии» относится к бактериям, окрашиваемым в красный цвет при окрашивании методом окрашивания по Граму, и обычно они обладают сильной устойчивостью к пигментам и сильной устойчивостью к поверхностно-активным веществам. Грамотрицательные бактерии по настоящему изобретению включают все типы грамотрицательных бактерий, содержащих эндотоксин, например, штаммы рода Escherichia, рода Pseudomonas, рода Acinetobacter, рода Salmonella, рода Klebsiella, рода Neisseria, род Enterobacter, род Shigella, род Moraxella, род Helicobacter, род Stenotrophomonas, род Bdellovibrio и род Legionella, но настоящее изобретение этим не ограничивается. В частности, грамотрицательные бактерии включают, помимо прочего, Escherichia coli, Pseudomonas aeruginosa, Pseudomonas fluorescens, Pseudomonas putida, Pseudomonas chlororaphis, Pseudomonas pertucinogena, Pseudomonas stutzeri, Pseudomonas syringae, Acinetobacter baumannii, Acinetobacter lwoffii, Acinetobacter calcoaceticus, Acinetobacter haemolyticus, Salmonella enterica, Salmonella bongori, Salmonella enteritidis, Salmonella typhimurium, Salmonella gallinarum, Salmonella pullorum, Salmonella mbandaka, Salmonella choleraesuis, Salmonella thompson, Salmonella infantis, Salmonella derby, Klebsiella pneumoniae, Klebsiella granulomatis, Klebsiella oxytoca, Klebsiella terrigena, Neisseria gonorrhoeae, Neisseria meningitidis, Enterobacter aerogenes, Enterobacter cloacae, Shigella boydii, Shigella dysenteriae, Shigella flexneri, Shigella sonnei, Moraxella catarrhalis, Moraxella lacunata, Moraxella bovis, Helicobacter pylori, Helicobacter heilmannii, Helicobacter felis, Helicobacter mustelae, Helicobacter fenelliae, Helicobacter rappini, Helicobacter hepaticus, Helicobacter bilis, Helicobacter pullorum, Stenotrophomonas maltophilia, Stenotrophomonas nitritireducens, Bdellovibrio bacteriovorus, Legionella pneumophila, Legionella anisa, Legionella birminghamensis, Legionella bozemanii, Legionella cincinnatiensis, Legionella dumoffii, Legionella feeleii, Legionella gormanii, Legionella hackelia, Legionella israelensis, Legionella jordanis, Legionella lansingensis, Legionella longbeachae, Legionella longbeachae, Legionella micdadei, Legionella oakridgensis, Legionella sainthelensi, Legionella tucsonensis, и Legionella wadsworthii.
Термин «грамположительные бактерии», используемый здесь, относится к бактериям, которые окрашиваются в ярко-синий или фиолетовый цвет в результате окрашивания по Граму, и могут включать штаммы рода Staphylococcus, рода Enterococcus, рода Streptococcus и рода Clostridium, но настоящее изобретение этим не ограничивается. В частности, грамположительные бактерии включают Staphylococcus aureus, Staphylococcus epidermidis, Enterococcus faecium, Streptococcus pneumoniae и Bacillus anthracis, но настоящее изобретение этим не ограничивается.
Термин «устойчивые к антибиотикам грамположительные бактерии», используемый здесь, включает, например, устойчивые к метициллину грамположительные бактерии, устойчивые к карбапенему грамположительные бактерии, устойчивые к ванкомицину грамположительные бактерии, макролиды и грамположительные бактерии с множественной лекарственной устойчивостью, но настоящее изобретение этим не ограничивается.
Используемые здесь «устойчивые к антибиотикам грамотрицательные бактерии» включают, например, устойчивые к стрептомицину грамотрицательные бактерии, устойчивые к колистину грамотрицательные бактерии, устойчивые к карбапенему грамотрицательные бактерии, устойчивые к хлорамфениколу грамотрицательные бактерии, тетрациклины. -резистентные грамотрицательные бактерии, устойчивые к цефотаксиму грамотрицательные бактерии, устойчивые к имипенему грамотрицательные бактерии, устойчивые к БЛРС грамотрицательные бактерии, устойчивые к тигециклину грамотрицательные бактерии и грамотрицательные бактерии с множественной лекарственной устойчивостью, но присутствующие изобретение этим не ограничивается.
В одном варианте осуществления настоящего изобретения бактерии, на которые нацелена антибактериальная композиция, могут быть одной или несколькими, выбранными из группы, состоящей из Escherichia coli DH5α, Escherichia coli K1, Acinetobacter baumannii, Pseudomonas aeruginosa, Salmonella enteritidis, Salmonella typhimurium, Klebsiella pneumoniae, Staphylocus и Staphylococcus epidermidis.
Кроме того, в одном варианте осуществления настоящего изобретения бактерии, на которые нацелена антибактериальная композиция, могут быть одной или несколькими устойчивыми к антибиотикам бактериями, выбранными из группы, состоящей из устойчивых к БЛРС бактерий, устойчивых к карбапенемам бактерий и устойчивых к колистину бактерий. Например, устойчивыми к антибиотикам бактериями могут быть БЛРС (E. coli), устойчивый к карбапенему (CR)-Acinetobactor baumannii, CR-Klebsiella pneumoniae, CR-Pseudomonas aeruginosa и устойчивый к колистину Acinetobactor baumannii, но настоящее изобретение не ограничивается им.
Кроме того, настоящее изобретение обеспечивает композицию для профилактики, облегчения или лечения инфекционного заболевания, которая включает полипептид, представленный общей формулой последовательности, или его производное с замещением ацетатной солью трифторуксусной кислоты в качестве активного ингредиента.
Кроме того, настоящее изобретение обеспечивает фармацевтическую/пищевую/диетическую/косметическую/квазилекарственную/кормовую композицию для профилактики, облегчения или лечения инфекционного заболевания, которая включает полипептид, представленный общей формулой последовательности, или его производное с замещением ацетатной солью трифторуксусной кислоты в качестве активного ингредиента.
Настоящее изобретение обеспечивает способ профилактики или лечения инфекционного заболевания, который включает введение полипептида, представленного общей формулой последовательности, или его производного с замещением ацетатной солью трифторуксусной кислоты нуждающемуся в этом субъекту.
Кроме того, настоящее изобретение обеспечивает применение полипептида, представленного общей формулой последовательности, или его производного с замещением ацетатной солью трифторуксусной кислоты для профилактики, облегчения или лечения инфекционного заболевания.
Кроме того, настоящее изобретение обеспечивает применение полипептида, представленного общей формулой последовательности, или его производного с замещением ацетатной солью трифторуксусной кислоты для приготовления препарата для профилактики, облегчения или лечения инфекционного заболевания.
Термин «инфекционное заболевание», используемый здесь, относится к заболеванию, вызываемому болезнетворными патогенами, такими как вирусы, бактерии, грибки и паразиты, которые распространяются на животных или людей, или поражают их, и для целей настоящего изобретения инфекционное заболевание означает все виды инфекционных заболеваний, вызываемых грамотрицательными бактериями или грамположительными бактериями.
Например, инфекционное заболевание включает инфекционные заболевания, вызываемые грамотрицательными бактериями, такие как пневмония, перитонит, менингит, раневая инфекция, остеоартрит, холецистит, инфекция мочевыводящих путей, эндокардит, миокардит, перикардит, артрит, фарингит, гонорея, бактериальная дизентерия, энтерит, конъюнктивит, гастрит, средний отит, цистит и лимфангит, но настоящее изобретение этим не ограничивается.
Например, инфекционное заболевание включает инфекционные заболевания, вызываемые грамположительными бактериями, такие как ларингофарингит, импетиго, ревматическая лихорадка, гломерулонефрит, неонатальный сепсис, менингит, фарингит, пневмония, эндокардит, скарлатина, SSTI (инфекции кожи и мягких тканей), инфекция глубоких мягких тканей, эмпиема и вагинит, но настоящее изобретение этим не ограничивается.
Фармацевтическая композиция по настоящему изобретению может дополнительно включать подходящий носитель, наполнитель и разбавитель, которые обычно используются при приготовлении фармацевтической композиции. Фармацевтическая композиция по настоящему изобретению может использоваться в пероральном составе, таком как порошок, гранула, таблетка, капсула, суспензия, эмульсия, сироп или аэрозоль, препарат для наружного применения, суппозиторий или стерилизованный раствор для инъекций по общепринятой методике.
Фармацевтическая композиция по настоящему изобретению может дополнительно включать подходящий носитель, наполнитель и разбавитель, которые обычно используются при приготовлении фармацевтической композиции. Фармацевтическая композиция по настоящему изобретению может использоваться в пероральном составе, таком как порошок, гранула, таблетка, капсула, суспензия, эмульсия, сироп или аэрозоль, препарат для наружного применения, суппозиторий или стерилизованный раствор для инъекций по общепринятой методике.
Фармацевтическая композиция по настоящему изобретению может быть составлена с разбавителем или наполнителем, таким как заполнитель, наполнитель, связующее, смачивающий агент, разрыхлитель, поверхностно-активное вещество, которые обычно используются. Твердая композиция для перорального введения может представлять собой таблетку, пилюлю, порошок, гранулы или капсулу, и такая твердая композиция может быть приготовлена путем смешивания по меньшей мере одного из эксципиентов, например крахмала, карбоната кальция, сахарозы, лактозы и желатина, с активным ингредиентом. Кроме того, в дополнение к простому наполнителю также могут использоваться смазывающие вещества, такие как стеарат магния и тальк. В качестве жидкого препарата для перорального введения можно использовать суспензию, пероральные жидкости, эмульсию или сироп, а также обычно используемый простой разбавитель, такой как вода или жидкий парафин, а также различные типы вспомогательных веществ, например, могут быть включены смачивающий агент, подсластитель, ароматизатор и консервант. Состав для парентерального введения может представлять собой стерилизованный водный раствор, неводный растворитель, суспензию, эмульсию, лиофилизированный продукт или суппозиторий. В качестве неводного растворителя или суспензии можно использовать пропиленгликоль, полиэтиленгликоль, растительное масло, такое как оливковое масло, или сложный эфир для инъекций, такой как этилолеат. В качестве основы для суппозиториев можно использовать витепсол, макрогол, твин 61, масло какао, лаурин или глицерогелатин.
Термин «профилактика», используемый здесь, относится ко всем действиям по предотвращению, подавлению или отсрочке появления симптомов, вызванных заболеванием, путем введения композиции согласно настоящему изобретению.
Термин «лечение» или «облегчение», используемый здесь, относится ко всем действиям, связанным с улучшением или благоприятным изменением симптомов путем введения композиции согласно настоящему изобретению.
Используемый здесь термин «введение» относится к предоставлению композиции по настоящему изобретению субъекту подходящим способом.
Используемый здесь термин «субъект» относится к цели, нуждающейся в профилактике или лечении. Например, субъектом может быть млекопитающее, такое как человек или примат, не являющийся человеком, мышь, собака, кошка, лошадь, овца или корова.
Композиция согласно настоящему изобретению вводится в фармацевтически эффективном количестве. В настоящем изобретении «фармацевтически эффективное количество», используемое здесь, относится к количеству, достаточному для лечения заболевания с разумным соотношением польза/риск, применимым для медицинского лечения, и эффективная доза может определяться параметрами, включая тип заболевания пациента , тяжесть заболевания, активность лекарства, чувствительность к лекарству, время введения, путь введения и скорость выведения, продолжительность лечения и одновременно применяемых лекарств, а также другие параметры, хорошо известные в области медицины. В частности, фармацевтическую композицию можно вводить в дозе от 0,001 до 1000 мг/кг, от 0,01 до 100 мг/кг, от 0,01 до 10 мг/кг, от 0,1 до 10 мг/кг или от 0,1 до 1 мг/кг однократно или раздельными порциями в день. Принимая во внимание все вышеупомянутые параметры, важно достичь максимального эффекта с минимальной дозой без побочного эффекта, и такая доза может быть определена специалистом в данной области. В частности, эффективное количество фармацевтической композиции согласно настоящему изобретению может быть определено в соответствии с возрастом, полом, состоянием, массой тела пациента, скоростью абсорбции активного ингредиента в организме, скоростью инактивации, скоростью выведения, тип заболевания или сопутствующий препарат.
Фармацевтическая композиция по настоящему изобретению может вводиться субъекту различными путями. Можно ожидать всех путей введения, и фармацевтическая композиция по настоящему изобретению может вводиться, например, перорально или интраректально, внутривенно, внутримышечно, подкожно, внутриматочно, интрадурально или внутрицереброваскулярной инъекцией.
Фармацевтическая композиция согласно настоящему изобретению может дополнительно включать один или несколько известных материалов, эффективных для облегчения, профилактики или лечения сепсиса или септического шока; предотвращение бактериальной инфекции; и облегчение, предотвращение или лечение инфекционного заболевания.
Фармацевтическая композиция по настоящему изобретению может дополнительно включать бронходилататор, антигистамин или противовоспалительное обезболивающее в дополнение к активному ингредиенту.
Например, бронходилататор может быть β-агонистом, антихолинергическим средством или метилксантином, антигистаминный препарат может представлять собой акривастин, цетиризин, дезлоратадин, фексофенадин, левоцетиризин, лоратадин, мизоластин, алимемазин, хлоцертизин, клэпрогемастин, клэпрогемастин, и противовоспалительным анальгетиком может быть аспирин, диклофенак, фенопрофен, флурбипрофен, ибупрофен, индометацин, кетопрофен, напроксен, пироксикам, сулиндак, целекоксиб, вальдекоксиб или рофекоксиб.
В примерном варианте осуществления настоящего изобретения было подтверждено, что полипептид согласно настоящему изобретению и его соль обладают высокой связывающей способностью с ЛПС, путем измерения связывающей способности полипептида согласно настоящему изобретению и его соли с ЛПС (Пример 1).
Кроме того, в примерном варианте осуществления настоящего изобретения было подтверждено, что полипептид согласно настоящему изобретению и его соль проявляют превосходную антибактериальную активность (примеры 2, 3 и 10).
Кроме того, в примерном варианте осуществления настоящего изобретения было подтверждено, что полипептид согласно настоящему изобретению и его соль проявляют сильный антибиотический эффект (примеры 8 и 9).
Кроме того, настоящее изобретение обеспечивает полинуклеотид, кодирующий полипептид.
Термин «полинуклеотид» представляет собой полимер дезоксирибонуклеотидов или рибонуклеотидов, которые присутствуют в одно- или двухцепочечной(ых) цепи(ях). Полинуклеотид включает последовательность генома РНК, ДНК (геномнойДНК и кДНК) и последовательность РНК, транскрибируемую из них, и включает аналог природного полинуклеотида, если не указано иное.
Полинуклеотид включает нуклеотидную последовательность, а также включает последовательность, комплементарную ей. Дополнительная последовательность включает не только совершенно комплементарную последовательность, но также по существу комплементарную последовательность, она относится к последовательности, способной гибридизоваться с нуклеотидной последовательностью в жестких условиях, известных в данной области.
Кроме того, полинуклеотид можно модифицировать. Модификация включает добавление, делецию, неконсервативную замену или консервативную замену нуклеотида. Полинуклеотид, кодирующий аминокислотную последовательность, интерпретируется как включающий также нуклеотидную последовательность, проявляющую существенную идентичность с нуклеотидной последовательностью. Существенная идентичность может быть последовательностью, имеющей по меньшей мере 80%, 90% или 95% гомологии, когда нуклеотидная последовательность выровнена с любой другой последовательностью так, чтобы они соответствовали максимальному соответствию, и выровненная последовательность анализируется с использованием алгоритма, обычно используемого в искусство.
Кроме того, настоящее изобретение обеспечивает рекомбинантный вектор, включающий полинуклеотид.
Используемый здесь термин «вектор» относится к средству для экспрессии гена-мишени в клетках-хозяевах. Например, вектор включает плазмидный вектор, космидный вектор, бактериофаговый вектор и вирусные векторы, такие как аденовирусный вектор, ретровирусный вектор и аденоассоциированный вирусный вектор. Вектор, который можно использовать в качестве рекомбинантного вектора, может быть сконструирован путем манипулирования плазмидой, часто используемой в данной области (например, pSC101, pGV1106, pACYC177, ColE1, pKT230, pME290, pBR322, pUC8/9, pUC6, pBD9, pHC79, pIJ61 , pLAFR1, pHV14, серия pGEX, серия pET или pUC19), фаг (например, λ λ λ λ Δ или M13) или вирус (например, CMV или SV40).
В рекомбинантном векторе полинуклеотид, кодирующий пептид, может быть функционально связан с промотором. Используемый здесь термин «функционально связанный» означает функциональную связь между регуляторной последовательностью нуклеотидной экспрессии (например, последовательностью промотора) и другой нуклеотидной последовательностью. Следовательно, регуляторная последовательность может регулировать транскрипцию и/или трансляцию различных нуклеотидных последовательностей.
Рекомбинантный вектор обычно может быть сконструирован как вектор для клонирования или экспрессии. Вектор экспрессии может быть обычным вектором, используемым для экспрессии чужеродного белка у растений, животных или микроорганизмов в данной области. Рекомбинантный вектор может быть сконструирован различными способами, известными в данной области.
Кроме того, настоящее изобретение относится к клетке-хозяину, трансформированной рекомбинантным вектором.
В качестве клетки-хозяина можно использовать любую клетку-хозяин, известную в данной области, и прокариотические клетки, например, штаммы семейства Enterobacteriaceae, включая E. coli JM109, E. coli BL21, E. coli RR1, E. coli LE392, E .coli B, E. coli X 1776 или E. coli W3110, штамм рода Bacillus, такой как Bacillus subtilis или Bacillus thuringiensis, Salmonella typhimurium, Serratia marcescens и различные виды Pseudomonas, могут быть использованы и при трансформации в эукариотические клетки, в качестве клеток-хозяев, дрожжевые клетки (Saccharomyces cerevisiae), клетки насекомых, клетки растений и клетки животных, например SP2/0, яичник китайского хомячка (CHO) K1, CHO DG44, PER.C6, W138, BHK, COS-7, 293, могут быть использованы клеточные линии HepG2, Huh7, 3T3, RIN и MDCK.
Настоящее изобретение обеспечивает способ получения полипептида, представленного общей формулой последовательности согласно настоящему изобретению, который включает культивирование клеток-хозяев.
Встраивание полинуклеотида или рекомбинантного вектора, включающего его, в клетки-хозяева можно осуществлять способом встраивания, широко известным в данной области. Методом доставки может быть, например, метод CaCl2 или метод электропорации, когда клетка-хозяин является прокариотической клеткой, и микроинъекция, фосфат кальция, преципитация, опосредованная липосомами трансфекция и генная бомбардировка, когда клетка-хозяин является эукариотической клеткой, но настоящее изобретение этим не ограничивается.
Способ отбора трансформированных клеток-хозяев можно легко осуществить с помощью метода, широко известного в данной области, с использованием фенотипа, выраженного маркером отбора. Например, когда маркер отбора представляет собой специфический ген устойчивости к антибиотикам, трансформант культивируют в среде, содержащей антибиотик, так что трансформант может быть легко выбран.
Далее, чтобы помочь в понимании настоящего изобретения, будут предложены примеры. Однако, следующие примеры приведены только для более легкого понимания настоящего изобретения, а не для ограничения настоящего изобретения.
Пример 1: Измерение ЛПС-связывающей способности пептидов-кандидатов, производных от ADK, для E. coli K1
FP1 (ADK 44-54) обозначали диким типом (WT), и производили пептиды, в которых в различных сайтах в WT произошла точечная мутация (FP3, FP5, FP6 и FP9). Чтобы увеличить взаимодействие с ЛПС в последовательности остатков FP3, пептиды разрабатывали на основе моделей связывания FP3 и ЛПС (FP12-NH2 и FP13-NH2), при этом пептиды разрабатывали путем дополнительного введения неприродной аминокислоты и изомера аминокислоты (алломерная аминокислота D-типа) (allD FP12-NH2, allD FP13-NH2, allD FP-13-9a, allD FP-13-9w, allD FP-13-9k и allD FP13-NH2 (AcOH)). Кроме того, N-концевой ПЭГилированный пептид (PEG-alld FP13-NH2 (AcOH)) был дополнительно разработан, синтезирован и предоставлен ANYGEN, Co. Ltd. Сродство связывания между каждым из предоставленных пептидов и липополисахаридом (ЛПС) было подтверждено путем измерения аффинности связывания (Kd) с использованием калориметра изотермического титрования (ITC).
В частности, метод анализа аффинности связывания (Kd) между пептидом и ЛПС заключается в следующем.
Измерения выполняли с использованием прибора для клеток Malvern MicroCal PEAQ-ITC, и проводили последующую предварительную обработку для подтверждения взаимодействия с ЛПС. Количество и морфология ячейки для образца составляла 300 мкл и имела форму монеты, закрепленную на месте, соответственно; скорость вращения шприца - 1200 об/мин; и температура была 30 °, 35 ° или 25 °.
Перед экспериментом ЛПС и пептид предварительно разбавляли PBS, получая таким образом 2 мМ ЛПС и 0,2 мМ пептида. 300 мкл пептида добавляли в клетки в приборе ITC, которые были промыты, и 40 мкл ЛПС помещали в шприц. После того, как были установлены условия измерения ITC (температура, количество инъекций), шприц вставляли в ячейку и начинали измерение ITC. Когда измерение было завершено, проводили анализ и рассчитывали значения Kd для ЛПС и пептида.
В результате измерения было подтверждено, что все типы пептидов FP3, FP5, FP6, FP9, FP12-NH2, FP13-NH2, allD FP12-NH2, allD FP13-NH2, allD FP-13-9a, allD FP -13-9w, allD FP-13-9k и allD FP13-NH2 (AcOH) обладают сильной аффинностью связывания с ЛПС, которая равна или выше, чем у FP1 (дикий тип, WT).
Таблица 1
Таблица 2
PEG: Fmoc-NH-PEG
(В таблицах 1 и 2 allD обозначает аминокислоту D-типа).
(В таблицах 1 и 2 (AcOH) указывает на солевое производное, при котором трифторуксусная кислота (TFA) на конце 9-й аминокислоты от N-конца пептида заменена ацетатной солью).
(В таблице 2 ПЭГ обозначает ПЭГилирование. Информация о ПЭГилировании N-конца пептида: полиэтиленгликоль (ПЭГ), молекулярная масса (Mw) = 385,4Da, Fmoc-NH-PEG2-CH2COOH).
Пример 2: Сравнительная оценка антибактериальной активности allD FP13-NH2 и четырех коммерчески доступных антибиотиков против грамположительных/грамотрицательных стандартных штаммов.
Сравнивали антибактериальную активность одного пептида (allD FP13-NH2), у которого было подтверждено сильное сродство к ЛПС среди пептидов, разработанных в примере 1, и четырех коммерчески доступных антибиотиков против грамположительных/грамотрицательных стандартных штаммов.
Для сравнения антибактериальной активности четырех имеющихся в продаже антибиотиков (ампициллин, гентамицин, левофлоксацин и имипенем) и пептида allD FP13-NH2 (AcOH) проводили тест на антибактериальную активность для измерения минимальных ингибирующих концентраций (МИК 50 и МИК 80) на грамотрицательные и грамположительные стандартные штаммы (Escherichia coli DH5α, Escherichia coli K1, Acinetobacter baumannii, Pseudomonas aeruginosa, Salmonella enteritidis, Salmonella typhimurium и Klebsiella pneumoniae).
Более конкретно, 100 мкл среды распределяли в каждую лунку 96-луночного планшета, а в первую колонку распределяли антибиотик и пептид в 200 мкл среды. 1/2 серийного разведения выполняли из колонок с 1 по 11, и грамотрицательные и грамположительные бактерии, которые ранее культивировали, разбавляли (значение OD600 нм в разведении: приблизительно 0,0025) и распределяли в каждую лунку. Планшет инкубировали в инкубаторе при 37° C в течение 4 часов и измеряли OD 600 нм. Скорость роста бактерий была определена как 100% при значении OD600 нм холостого опыта (лунка, содержащая только среду и бактерии), а MIC50 была определена путем подтверждения концентраций антибиотика и пептида, имеющих значение OD600 нм, при котором скорость ингибирования роста составляла 50 %, а MIC80 определяли путем подтверждения концентраций (мкг/мл), при которых было показано 80% ингибирования роста.
В результате, сравнивая пептид allD FP13-NH2 (AcOH) с четырьмя коммерчески доступными антибиотиками (ампициллин, гентамицин, левофлоксацин и имипенем), было подтверждено, что пептид allD FP13-NH2 (AcOH) обладает такими же или более эффективными антибактериальными свойствами против всех семи типов штаммов грамположительных/грамотрицательных бактерий.
Таблица 3
Ампициллин
Гентамицин
Левофлоксацин
Имипинем
allD FP13-NH2
Escherichia coli K1
Ампициллин
Гентамицин
Левофлоксацин
Имипинем
allD FP13-NH2
Acinetobacter baumannii (ATCC 19606)
Ампициллин
Гентамицин
Левофлоксацин
Имипинем
allD FP13-NH2
Pseudomonas aeruginosa PA01 (ATCC 47085D-5)
Ампициллин
Гентамицин
Левофлоксацин
Имипинем
allD FP13-NH2
Salmonella enteritidis (ATCC 13076)
Ампициллин
Гентамицин
Левофлоксацин
Имипинем
allD FP13-NH2
Salmonella typhimurium (ATCC 53648)
Ампициллин
Гентамицин
Левофлоксацин
Имипинем
allD FP13-NH2
Klebsiella pneumoniae (ATCC 13883)
Ампициллин
Гентамицин
Левофлоксацин
Имипинем
allD FP13-NH2
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
0,125-128
<0.5
<0.5
<4.0
<1.0
<4.0
<0.5
<0.5
<0.5
<2.0
<32
<1.0
<0.5
<8.0
<4.0
без эффекта
<0.5
<0.5
<32
<0.5
<4.0
<0.5
<0.5
<4.0
<1.0
<1.0
<0.5
<0.5
<4.0
<2.0
без эффекта
<0.5
<0.5
<2.0
<0.5
<1.0
<1.0
<8.0
<2.0
<8.0
<1.0
<1.0
<1.0
<4.0
<64
<2.0
<1.0
<16
<8.0
без эффекта
<1.0
<1.0
<54
<1.0
<8.0
<1.0
<1.0
<8.0
<2.0
<2.0
<1.0
<1.0
<8.0
<4.0
без эффекта
<1.0
<1.0
<8.0
<1.0
Пример 3: Сравнительная оценка антибактериальной активности пептидов и трех антибиотиков против устойчивых к антибиотикам бактерий (БЛРС и устойчивых к карбапенемам бактерий)
Проводили анализ антибактериальной активности 9 типов пептидов, антибактериальной активности против бактерий, устойчивых к ампициллину (AMP), имипенему, колистину и пяти другим антибиотикам (БЛРС-E.coli, устойчивый к карбапенемам A. baumannii, устойчивый к карбапенемам Klebsiella pneumoniae, карбапенем устойчивый Pseudomonas aeruginosa и устойчивый к колистину Acinetobactor baumannii).
Антибактериальную активность оценивали в соответствии с методом испытания антибактериальной активности для измерения минимальной ингибирующей концентрации 50 (MIC 50; минимальная концентрация, убивающая 50% бактерий).
Более конкретно, 100 мкл среды распределяли в каждую лунку 96-луночного планшета, в первую колонку распределяли антибиотик и пептид в 200 мкл среды. 1/2 серийного разведения выполняли в колонах 1-11 и пять типов устойчивых к антибиотикам бактерий (БЛРС-устойчивые E. coli, устойчивые к карбапенемам A. baumannii, устойчивые к карбапенемам Klebsiella pneumoniae, устойчивые к карбапенемам Pseudomonas aeruginosa, устойчивые к колистину Acinetobactor baumannii), которые ранее культивировали, разводили (значение OD600 нм в разведении: приблизительно 0,0025) и разливали в каждую лунку. Планшет инкубировали в инкубаторе при 37 ° C в течение 4 часов и измеряли OD600nm. Скорость роста бактерий была определена как 100% со значением OD600nm холостого опыта (лунка, содержащая только среду и бактерии), а значение MIC50 было измерено путем подтверждения концентраций антибиотика и пептида, которые имеют значение OD600nm, при котором скорость роста была показана 50%.
В результате было подтверждено, что пептид согласно настоящему изобретению обладает улучшенной антибактериальной активностью по сравнению с тремя сравнительными антибиотиками (ампициллин (AMP), имипенем и колистин). В частности, было подтверждено, что пептид согласно настоящему изобретению, также обладает антибактериальной активностью против бактерий, устойчивых к этим антибиотикам (в частности, устойчивый к карбапенему или колистину штамм).
Таблица 4
Пример 4: Измерение гемолитической активности пептида.
Следующий эксперимент проводили для определения токсичности пептида путем измерения гемолитической активности эритроцитов у человека.
Эритроциты человека разбавляли PBS для промывания и центрифугировали в течение 10 минут, процесс промывания повторяли три раза. 8,0% раствор эритроцитов, разбавленный PBS, загружали в 96-луночный микротитровальный планшет по 100 мкл и 100 мкл раствора пептида смешивали, смесь инкубировали при 37 ° C в течение 1 часа, а затем 96-луночный микротитрователь. планшет центрифугировали 5 минут. Отбирали 100 мкл супернатанта и переносили в другой 96-луночный микротитровальный планшет, а затем измеряли оптическую плотность при 405 нм. Здесь значение, полученное при обработке 0,1% Triton X-100, было рассчитано как 100% гемолиз, а гемолитическая активность пептида рассчитана как %гемолиза по уравнению 1 ниже.
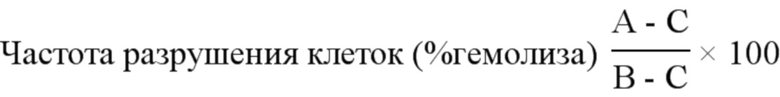
Здесь A - оптическая плотность при 405 нм в растворе пептида, B - оптическая плотность при 405 нм в 0,1% Triton X-100, а C - оптическая плотность при 405 нм в растворе PBS.
Здесь в качестве пептида для контроля использовали мелиттин, который представляет собой антибактериальный пептид, проявляющий сильную антибактериальную активность и сильную гемолитическую активность.
В результате, как показано на фиг.1 видно, что пептиды согласно настоящему изобретению почти не проявляют гемолитической активности даже при высокой концентрации 100 мкМ. С другой стороны, мелиттин в качестве контроля показал 100% гемолитическую активность даже при низкой концентрации, что указывает на очень высокую токсичность.
Пример 5: Измерение вторичной структуры пептида с помощью спектроскопии дихроизма круговой поляризации.
Для измерения вторичной структуры пептидов FP12-NH2 и FP13-NH2 проводили следующий эксперимент.
Для изучения вторичной структуры пептидов в среде, подобной биомембране, пептиды растворяли в 0,3 мл растворителя так, чтобы концентрация пептидов стала 100 мкМ на образец в водном растворе, 100 мМ SDS или 50 мМ DPC. Клетки с длиной пути 1 мм анализировали с использованием спектрофотометра кругового дихроизма Jasco J-720, таким образом получая значение поглощения на 0,1 нм при скорости введения 100 нм/мин, и шесть введений усредняли, таким образом получая значение измерения.
Спектроскопия кругового поляризационного дихроизма показывает характерную картину поглощения, зависящую от вторичной структуры основной цепи полипептида. Пептиды FP12-NH2 и FP13-NH2 не имели вторичной структуры в водном растворе, но имели две минимальные точки на длинах волн приблизительно 208 и 222 нм, что является характерной картиной поглощения α-спиральной структуры в мицеллах DPC. которая представляет собой биомембраноподобную среду (фиг. 2).
Из приведенных выше результатов можно предсказать, что эти пептиды будут проявлять антибактериальную активность при образовании α-спиральных структур в биомембране бактерий. С другой стороны, можно видеть, что пептиды allD (FP12-NH2) и allD (FP13-NH2), которые были подвергнуты замене D-аминокислоты, точно имеют зеркальное отображение исходного пептида. В отличие от спектра КД исходного пептида, показывающего структуру правой α-спирали, пептиды имеют отрицательную интенсивность, что указывает на то, что они имеют структуру левой α-спирали (фиг. 2).
Пример 6: Измерение разрушающей способности пептидов против липосом, имитирующих клеточную мембрану грамотрицательных бактерий и мембрану эритроцитов.
Чтобы изучить механизм действия пептидов FP12-NH2, FP13-NH2, allD FP12-NH2 и allD FP13-NH2, измеряли разрушающую способность пептидов против липосом, имитирующих мембрану бактериальной клетки и мембрану эритроцитов.
Чтобы подтвердить, проявляется ли антибактериальное действие пептидов в механизме уничтожения бактерий путем нацеливания на мембрану бактериальной клетки, изготавлилвали липосомы, в которые инкапсулированы флуоресцентный краситель, кальцеин, которые состоят из EYPC/EYPG (7:3, вес/вес), имитируя клеточную мембрану грамотрицательных бактерий и EYPC/CH (1:10, вес/вес), имитируя эритроцит человека, соответственно, для проведения анализа просачивания флуоресцентного красителя.
EYPG представляет собой аббревиатуру от L-α-фосфатидил-DL-глицерина яичного желтка, а EYPC представляет собой аббревиатуру аббревиатура от 1,2-диацил-sn-глицеро-3-фосфохолина яичного желтка. CH представляет собой аббревиатуру холестерина. После растворения фосфолипидов, составленных в соответствии с содержанием каждого компонента в хлороформе, хлороформ удаляли с использованием роторного испарителя и лиофилизацию проводили в течение ночи. После этого высушенную липидную пленку растворяли в растворе трис-буфера, а кальцеин растворяли в жидком азоте. После многократного замораживания и оттаивания липосомы, инкапсулированные в кальцеине, получали с использованием экструдера. Впоследствии, после того как длина волны возбуждения спектрофлуориметра (спектрофлуориметр Shimadzu RF 5301 PC, Япония) была установлена на 490 нм, а длина волны излучения была установлена на 520 нм, пептид вводили в липосомы для измерения относительной просачивания красителя при условии, что 100% просачивание красителя выражали как интенсивность флуоресценции при добавлении 0,01% Triton-X100.
Результат показан на фиг. 3. Верхние графики фиг. 3 показывают % просачивания красителя для липосом EYPC/EYPG (7:3, вес/вес), имитирующих бактериальные клетки, лирующих флуоресцентный краситель, кальцеин, пептид в соответствии с концентрацией пептида. Здесь в качестве контроля (пептид, проявляющий механизм действия нацеливания на клеточную мембрану) использовали антибактериальный пептид мелиттин. Нижние графики фиг. 3 показывают % просачивания красителя для липосомы EYPC/CH (10: 1, вес/вес), которая представляет собой триглицерид, имитирующий клетки эритроцитов человека, инкапсулирующий флуоресцентный краситель, кальцеин, пептид в соответствии с концентрацией пептида. Здесь антибактериальный пептид мелиттин использовали в качестве контроля (пептид, проявляющий механизм действия нацеливания на клеточную мембрану).
Как показано на фиг. 3, контрольный пептид отвечает за просачивание кальцеина из липосомы, состоящей из PC/PG (7:3, вес/вес), имитирующей мембрану бактериальной клетки даже при низкой концентрации. Для липосомы PC/CH (10:1, вес/вес), имитирующей эритроцит человека, поскольку почти 100% просачивание кальцеина может быть продемонстрирована при 0,25 мкМ мелиттина, можно предсказать отсутствие селективности в отношении бактериальных клеток и очень высокую токсичность.
С другой стороны, пептиды FP12-NH2, FP13-NH2, allD FP12-NH2 и allD FP13-NH2 вызвали высокое просачивание красителя для липосомы PC/PG (7:3, вес/вес), Имитирующей мембрану бактериальной клетки, что указывает на высокую способность разрушать мембрану бактериальной клетки. Пептиды FP12-NH2, FP13-NH2, allD FP12-NH2 и allD FP13-NH2 выборочно почти не показывают просачивания красителя для липосом PC/CH (1:1, вес/вес), имитирующей мембрану эритроцитов у млекопитающего, что соответствует низкой гемолитической активности. Таким образом, было замечено, что пептиды согласно настоящему изобретению обладают механизмом действия избирательного разрушения мембраны бактериальной клетки.
Пример 7: Оценка стабильности путем измерения устойчивости пептида к протеолитическим ферментам.
Стабильность в крови подтверждали путем измерения устойчивости к протеолитическим ферментам сконструированных пептидов allD FP12-NH2 и allD FP13-NH2.
Более конкретно, чтобы подтвердить устойчивость к трем типам протеолитических ферментов, таким как трипсин, протеаза К и химотрипсин, обрабатывали протеолитический фермент, а затем измеряли антибактериальную активность пептидов против E. coli, A. baumannii и S. aureus.
В результате было подтверждено, что пептиды allD FP12-NH2 и allD FP13-NH2, сконструированные путем замены D-аминокислоты, неприродной аминокислоты, обладают значительно улучшенной устойчивостью к протеолитическому ферменту.
В экспериментальных данных для E. coli и A. baumannii, представленных в таблице 5, пептиды allD FP12-NH2 и allD FP13-NH2 показали антибактериальную активность, которая аналогична или снижена в 2-4 раза по сравнению со случаем без обработки протеолитическими ферментами, подтверждая, что пептиды являются высокофункциональными пептидами с очень высокой стабильностью.
Кроме того, в экспериментальных данных для S. aureus, показанных в таблице 6, также было подтверждено, что пептиды allD FP12-NH2 и allD FP13-NH2 являются высокофункциональными пептидами с очень высокой стабильностью.
Таблица 5
Таблица 6
Пример 8: Антибиотический эффект allD FP13-NH2 на стандартный штамм E. coli K1 и два типа клинических штаммов.
Для оценки антибиотической активности пептида оценивали антибиотический эффект и терапевтический эффект пептида на E. coli K1 (стандартный штамм), E. coli (БЛРС) и устойчивые к карбапенемам бактерии (устойчивые к карбапенемам Acinetobacter baummanii (CRAB)). в эксперименте на животных.
За исключением E. coli K1 (стандартный штамм), E. coli (БЛРС) и устойчивые к карбапенемам бактерии (CRAB) были приготовлены из устойчивых к антибиотикам бактерий, полученных от пациентов с тяжелой инфекцией, предоставленных Отделением инфекционных заболеваний Медицинского центра Корейского университета. Экспериментальные бактерии получали путем сбора от 10 до 20 морфологически идентичных колоний, инокулировали в пробирку, содержащую 10 мл подходящей жидкой среды (бульон Мюллера-Хинтона), и культивировали в инкубаторе при 37 ° С в течение 12 часов. Жидкую культуру клеток помещали в стерилизованную криопробирку на 1 мл и хранили при -80 ° С.
Тестируемый штамм культивировали в течение 2 дней в инкубаторе при 37 ° [чашке с кровяным агаром (BAP)], готовили в жидкой среде бульона Мюллера-Хинтона (MHB) в соответствии с количеством инокулированного штамма (1x108 или 8x107) и вводили внутрибрюшинно (1 мл) 6-недельным мышам, чтобы вызвать инфекцию. Мышей разделили на группы для каждого эксперимента (n = 5 или 6 на группу), и allD FP13-NH2, смешанный с раствором HARTMANN'S DEX (носитель), вводили мышам внутрибрюшинно шесть раз при 0, 1, 2, 3, 4, или 5 часов с последующим наблюдением за выживаемостью с интервалом в 12 часов в течение 3 дней.
В результате на животной модели сепсиса, в которой были инфицированы Escherichia coli K1, Escherichia coli (БЛРС) и устойчивый к карбапенемам Acinetobacter baumannii, было подтверждено увеличение выживаемости (эффект антибиотика) в диапазоне концентраций от 3 мг. до 12 мг на кг (фиг. 4). Было подтверждено, что пептид, созданный в примере 1, также проявляет антибиотические и антисептические эффекты in vivo в моделях животных, инфицированных стандартным штаммом и клиническим штаммом.
Пример 9: Производное ацетатная соль пептида.
Чтобы подтвердить терапевтические и фармацевтические эффекты производного ацетатной соли allD FP13-NH2, экспериментальную модель сепсиса, индуцированного внутрибрюшинным введением каждого из штаммов Escherichia coli (стандартный штамм и БЛРС), или нормальную мышь обрабатывали пептидом allD FP13-NH2 (АсОН). Сравнивали эффект антибиотика, токсичность и ингибирующую активность противовоспалительного цитокина IL-6 у солевого производного пептида с аналогичным, у которого на конце трифторуксусная кислота (TFA).
Экспериментальный метод заключается в следующем:
В качестве экспериментальных животных использовали самок мышей ICR шестинедельного возраста (мыши SPF, Samtako) со средней массой тела 25 г. Экспериментальным животным давали стерильный корм и воду, их разводили менее чем с 10 мышами на клетку, а цикл день/ночь составлял 12 часов.
Тестируемый штамм культивировали в течение 2 дней в инкубаторе при 37 ° C [чашка с кровяным агаром (BAP)], готовили в жидкой среде бульона Мюллера-Хинтона (MHB) в соответствии с количеством инокулированного штамма (1 × 108) и вводили внутрибрюшинно (1 × 108/200 мкл) 6-недельным мышам, чтобы вызвать инфекцию. Мышей разделили на группы для каждого эксперимента (n = 5 или 6 на группу) и 6 раз внутрибрюшинно инъецировали allD FP13-NH2 (TFA) и allD FP13-NH2 (AcOH), смешанные с раствором HARTMANN'S DEX (носитель) при 0, 1, 2, 3, 4 и 5 часов с последующим наблюдением за выживаемостью с интервалом в 12 часов.
Для оценки токсичности in vivo мышей разделили на группы (n = 5 или 6 на группу) в каждом эксперименте и шесть раз внутрибрюшинно обрабатывали allD FP13-NH2 (TFA) и allD FP13-NH2 (AcOH), смешанные с раствором HARTMANN'S DEX. (носитель) через 0, 1, 2, 3, 4 или 5 часов с последующим наблюдением за выживаемостью с интервалами 12 часов в течение 72 часов.
Кроме того, был проведен тест на секрецию IL-6 дендритных клеток костного мозга (BMDC) путем сравнительного анализа цитокинов, секретируемых ЛПС, через 30 минут после обработки пептидом посредством оценки ЛПС-опосредованных иммунных ответов allD FP13-NH2 (TFA) и allD FP13-NH2 (AcOH).
В результате, согласно тесту на антибиотическую эффективность и токсичность на экспериментальной модели сепсиса (модель, вызванная БЛРС E. coli), поскольку ED50 составляет приблизительно 1 mpk (мг/кг), LD50 составляет 80 mpk, а соотношение доза лекарственного средства, проявляющая токсичность, по отношению к дозе лекарственного средства для проявления желаемого ответа (терапевтический индекс = LD50/ED50), превышает 80, ожидается, что будет обеспечен достаточный запас безопасности, подтверждающий, что существует отличная возможность разработки нового антисептического препарата. Кроме того, было подтверждено, что allD FP13-NH2 (AcOH) значительно снижает секрецию IL-6, повышенную из-за ЛПС (фиг. 5A-5C).
Пример 10: Оценка антибактериальной активности пептида allD-типа против трех типов грамположительных бактерий (два типа S. aureus и S. epidermidis).
Для анализа антибактериальной активности пептида allD-типа против грамположительных бактерий была подтверждена антибактериальная активность против трех типов грамположительных бактерий (два типа S. aureus и S. epidermidis).
Для измерения минимальных ингибирующих концентраций (MIC50, минимальная концентрация для уничтожения 50% бактерий; MIC100, минимальная концентрация, необходимая для полного уничтожения бактерий), осуществляли экспериментальное определение антибактериальной активностью.
Более конкретно, 100 мкл среды распределяли в каждую лунку 96-луночного планшета, а в первую колонку распределяли антибиотик и пептид в 200 мкл среды. 1/2 серийного разведения выполняли из колонок с 1 по 11, и три типа грамположительных бактерий (два типа S. aureus и S. epidermidis), которые были ранее культивированы, были разведены (значение OD600nm в разведении: приблизительно 0,0025) и распределены. в каждую скважину. Планшет инкубировали в инкубаторе при 37 ° C в течение 4 часов и измеряли OD600nm. Скорость роста бактерий была определена как 100% при значении OD600 nm холостого опыта (лунка, содержащая только среду и бактерии), а концентрации антибиотика и пептида, имеющие значение OD600nm, при которых степень ингибирования роста составляла 50% или 100%, были определяется для расчета значений MIC50 и MIC 100.
Следовательно, в результате анализа антибактериальной активности против грамположительных бактерий было подтверждено, что три типа пептидов (allD FP12-NH2, allD FP13-NH2 и allD FP21-NH2), к которым относятся неприродные аминокислоты и Изомер аминокислоты (алломерная аминокислота D-типа) проявляет превосходную антибактериальную активность против грамположительных бактерий на том же уровне, что и мелиттин.
Таблица 7
Пример 11: Измерение разрушающей способности пептида против липосомы, имитирующей мембрану грамположительных бактериальных клеток.
Для изучения механизмов действия пептидов FP12-NH2, FP13-NH2, allD FP12-NH2 и allD FP13-NH2 измеряли разрушающую способность пептидов против липосом, имитирующих мембрану бактериальной клетки.
Проводили эксперимент по подтверждению того, проявляет ли пептид антибактериальный механизм действия относительно уничтожения бактерий путем нацеливания на клеточную мембрану грамположительных бактерий, изготавливали липосому, состоящую из EYPG/EYPC (6:4, вес/вес), имитирующую клеточную мембрану грамположительных бактерий, инкапсулирующую флуоресцентный краситель, кальцеин, для анализа просачивания красителя.
В результате пептиды FP12-NH2, FP13-NH2, allD FP12-NH2 и allD FP13-NH2 вызвали сильное просачивание красителя для липосомы EYPG/EYPC (6:4, вес/вес), Имитирующей мембрану бактериальной клетки, что указывает на отличная способность разрушать мембрану бактериальной клетки. Следовательно, можно видеть, что пептиды FP12-NH2, FP13-NH2, allD FP12-NH2 и allD FP13-NH2 согласно настоящему изобретению обладают механизмом действия, разрушающим мембрану грамположительных бактериальных клеток (фиг.6).
Пример 12: Измерение LTA и LPP, полученных из грамположительных бактерий, связывающей способности allD FP13-NH2.
Следующий эксперимент был проведен для подтверждения механизма действия путем подтверждения антибактериальной активности пептида против грамположительных бактерий.
Аффинность связывания с липотейхоевой кислотой (LTA) и липопротеином (LPP), которые являются компонентами клеточной стенки грамположительных бактерий (S. aureus), подтверждали посредством анализа ITC с использованием allD FP13-NH2.
Аффинность связывания подтверждали с использованием метода анализа ITC, и экспериментальный метод из примера 1 применяли с соответствующими изменениями.
В результате было подтверждено, что allD FP13-NH2 связывается с LTA и LPP, которые являются компонентами клеточной стенки грамположительных бактерий. Было подтверждено, что LPP включен в LTA, но не связывается с LPP, включая мутированный LTA, и ожидалось, что LPP играет более важную роль в связывании FP13-NH2 и LTA. Соответственно, было подтверждено, что связывание LPP будет играть важную роль в механизме антибактериальной активности FP13-NH2 против грамположительных бактерий.
Вышеприведенное описание настоящего изобретения предназначено только для иллюстративных целей, и специалисты в данной области техники, к которой относится настоящее изобретение, могут понять, что иллюстративные варианты осуществления, раскрытые в данном документе, могут быть легко изменены в другие конкретные формы без отклонения от технического духа или сущности настоящего изобретения. Следовательно, описанные выше примерные варианты осуществления следует интерпретировать как иллюстративные во всех аспектах, а не как ограничивающие.
Промышленная применимость
Пептид по настоящему изобретению не только ингибирует размножение стандартных бактерий и устойчивых к антибиотикам бактерий, но также обладает отличным эффектом удаления эндотоксина, полученного из бактерий, тем самым проявляя отличный лечебный эффект против сепсиса. Кроме того, при использовании в сочетании с антибиотиками пептид может минимизировать побочные эффекты, вызываемые антибиотиком, и, таким образом, может эффективно использоваться для профилактики или лечения сепсиса. Кроме того, пептид согласно настоящему изобретению проявляет превосходную антибактериальную активность избирательно против грамположительных/грамотрицательных бактерий и, таким образом, может быть эффективно использован для профилактики или лечения различных инфекционных заболеваний, вызванных грамположительными/грамотрицательными бактериями, или антибактериальная композиция против грамположительные/грамотрицательные бактерии. Более того, поскольку пептид согласно настоящему изобретению не только безопасен для человеческого организма, но также демонстрирует стабильность против протеолитических ферментов, его использование может быть расширено для множества целей.
Свободный текст списка последовательностей
Далее, список последовательностей будет представлен следующим образом:
[SEQ ID NO:
Название полипептида
Аминокислотная последовательность]
1
FP1(WT)
Lys Leu Gly Val Glu Ala Lys Arg Tyr Leu Asp
2
FP3
Lys Leu Gly Val Glu Ala Lys Arg Tyr Leu Arg
3
FP5
Leu Arg Leu Gly Val Glu Ala Lys Arg Tyr Leu Arg
4
FP6
Leu Arg Leu Gly Val Glu Leu Lys Arg Tyr Leu Arg
5
FP9
Lys Leu Gly Val Glu Ala Leu Arg Tyr Leu Asp
6
FP12-NH2
Arg Leu Arg Val Lys Leu Arg Arg Tyr Leu Arg
7
FP13-NH2
Lys Leu Arg Val Lys Leu Arg Arg Tyr Leu Arg
8
allD FP12-NH2
Arg Leu Arg Val Lys Leu Arg Arg Tyr Leu Arg
9
allD FP13-NH2
Lys Leu Arg Val Lys Leu Arg Arg Tyr Leu Arg
10
allD FP-13-9a-NH2
Lys Leu Arg Val Lys Leu Arg Arg Ala Leu Arg
11
allD FP-13-9w-NH2
Lys Leu Arg Val Lys Leu Arg Arg Trp Leu Arg
12
allD FP-13-9k-NH2
Lys Leu Arg Val Lys Leu Arg Arg Lys Leu Arg
13
allD FP13-NH2 (AcOH)
Lys Leu Arg Val Lys Leu Arg Arg Tyr Leu Arg
14
PEG-allD FP13-NH2 (AcOH)
Lys Leu Arg Val Lys Leu Arg Arg Tyr Leu Arg
15
FP12
Arg Leu Arg Val Lys Leu Arg Arg Tyr Leu Arg
16
FP13
Lys Leu Arg Val Lys Leu Arg Arg Tyr Leu Arg
17
allD FP21-NH2
Arg Leu Arg Val Lys Leu Arg Arg Trp Leu Arg
18
allD FP-13-9d-NH2
Lys Leu Arg Val Lys Leu Arg Arg Asp Leu Arg
--->
<110> DanDi Bioscience Inc
<120> Polypeptide having antibacterial activity, composition for
preventing or treating sepsis comprising the same, and
antibacterial composition
<130> MPCT19-145
<150> KR 10/2019/0023534
<151> 2019-02-28
<150> KR 10-2020-0023629
<151> 2020-02-26
<160> 18
<170> KoPatentIn 3.0
<210> 1
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> FP1(WT)
<400> 1
Lys Leu Gly Val Glu Ala Lys Arg Tyr Leu Asp
1 5 10
<210> 2
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> FP3
<400> 2
Lys Leu Gly Val Glu Ala Lys Arg Tyr Leu Arg
1 5 10
<210> 3
<211> 12
<212> PRT
<213> Artificial Sequence
<220>
<223> FP5
<400> 3
Leu Arg Leu Gly Val Glu Ala Lys Arg Tyr Leu Arg
1 5 10
<210> 4
<211> 12
<212> PRT
<213> Artificial Sequence
<220>
<223> FP6
<400> 4
Leu Arg Leu Gly Val Glu Leu Lys Arg Tyr Leu Arg
1 5 10
<210> 5
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> FP9
<400> 5
Lys Leu Gly Val Glu Ala Leu Arg Tyr Leu Asp
1 5 10
<210> 6
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> FP12-NH2
<400> 6
Arg Leu Arg Val Lys Leu Arg Arg Tyr Leu Arg
1 5 10
<210> 7
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> FP13-NH2
<400> 7
Lys Leu Arg Val Lys Leu Arg Arg Tyr Leu Arg
1 5 10
<210> 8
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> allD FP12-NH2
<400> 8
Arg Leu Arg Val Lys Leu Arg Arg Tyr Leu Arg
1 5 10
<210> 9
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> allD FP13-NH2
<400> 9
Lys Leu Arg Val Lys Leu Arg Arg Tyr Leu Arg
1 5 10
<210> 10
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> allD FP-13-9a-NH2
<400> 10
Lys Leu Arg Val Lys Leu Arg Arg Ala Leu Arg
1 5 10
<210> 11
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> allD FP-13-9w-NH2
<400> 11
Lys Leu Arg Val Lys Leu Arg Arg Trp Leu Arg
1 5 10
<210> 12
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> allD FP-13-9k-NH2
<400> 12
Lys Leu Arg Val Lys Leu Arg Arg Lys Leu Arg
1 5 10
<210> 13
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> allD FP13-NH2 (AcOH)
<400> 13
Lys Leu Arg Val Lys Leu Arg Arg Tyr Leu Arg
1 5 10
<210> 14
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> PEG-allD FP13-NH2 (AcOH)
<400> 14
Lys Leu Arg Val Lys Leu Arg Arg Tyr Leu Arg
1 5 10
<210> 15
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> FP12
<400> 15
Arg Leu Arg Val Lys Leu Arg Arg Tyr Leu Arg
1 5 10
<210> 16
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> FP13
<400> 16
Lys Leu Arg Val Lys Leu Arg Arg Tyr Leu Arg
1 5 10
<210> 17
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> allD FP21-NH2
<400> 17
Arg Leu Arg Val Lys Leu Arg Arg Trp Leu Arg
1 5 10
<210> 18
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> allD FP-13-9d-NH2
<400> 18
Lys Leu Arg Val Lys Leu Arg Arg Asp Leu Arg
1 5 10
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИБАКТЕРИАЛЬНЫЕ ПЕПТИДЫ | 2007 |
|
RU2468033C2 |
| ПЕПТИДНАЯ КОМПОЗИЦИЯ ДЛЯ ПРОФИЛАКТИКИ ИЛИ ЛЕЧЕНИЯ БОЛЕЗНИ АЛЬЦГЕЙМЕРА | 2021 |
|
RU2816119C1 |
| АНТИБИОТИЧЕСКИЕ ПЕПТИДЫ | 2008 |
|
RU2472805C2 |
| ПОЛИПЕПТИДЫ ЛИЗИНА, АКТИВНЫЕ ПРОТИВ ГРАМОТРИЦАТЕЛЬНЫХ БАКТЕРИЙ | 2016 |
|
RU2724545C2 |
| ПРОИСХОДЯЩИЕ ИЗ БАКТЕРИОФАГОВ ПРОТИВОМИКРОБНЫЕ ПОЛИПЕПТИДЫ И ИХ ПРИМЕНЕНИЕ ПРОТИВ ГРАМОТРИЦАТЕЛЬНЫХ БАКТЕРИЙ | 2019 |
|
RU2804774C2 |
| ПОЛИПЕПТИДНЫЕ КОНСТРУКЦИИ ЛИЗИН-ПРОТИВОМИКРОБНЫЙ ПЕПТИД (AMP), ЛИЗИНЫ, ВЫДЕЛЕННЫЕ ПОЛИНУКЛЕОТИДЫ, КОДИРУЮЩИЕ ИХ, А ТАКЖЕ ВАРИАНТЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2803121C2 |
| ПОЛИПЕПТИДЫ ИЛИ ИХ СОЛИ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1992 |
|
RU2083589C1 |
| Пептид с антибактериальной активностью | 2024 |
|
RU2825930C1 |
| НОВЫЙ ПОЛИПЕПТИД И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ПРОТИВ ВИЧ-ИНФЕКЦИИ | 1994 |
|
RU2136696C1 |
| Пептид, обладающий антибактериальной активностью в отношении микроорганизмов с множественной лекарственной устойчивостью | 2021 |
|
RU2771493C1 |

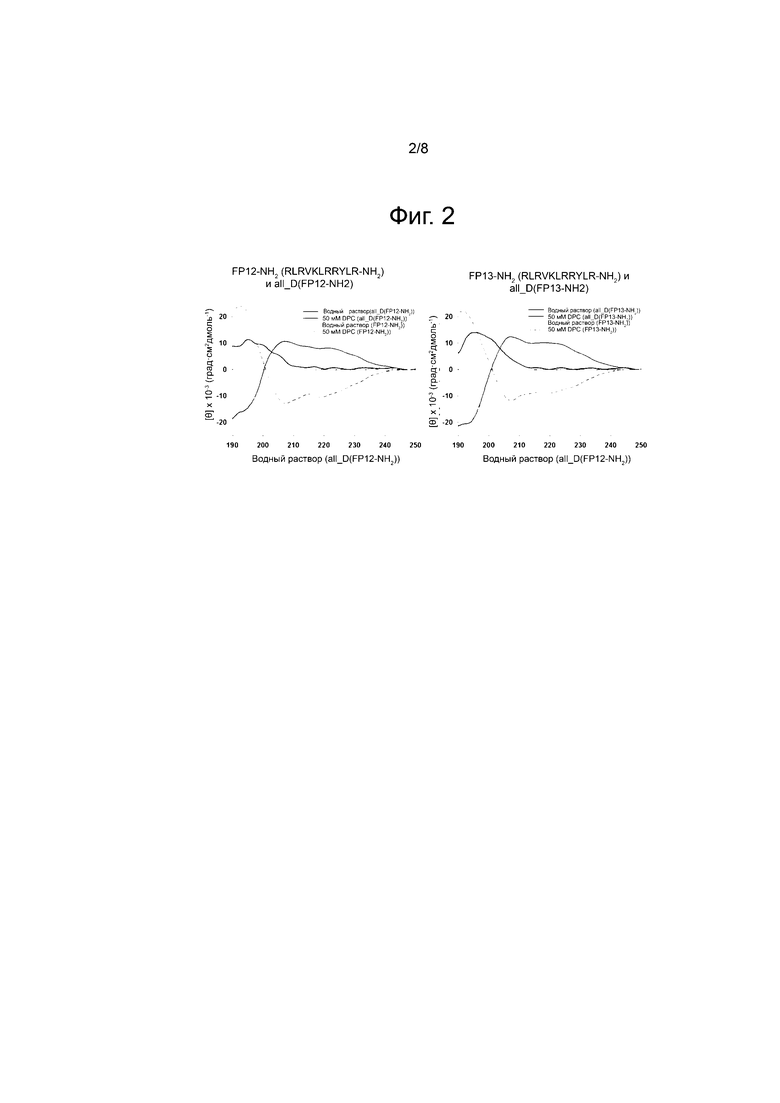

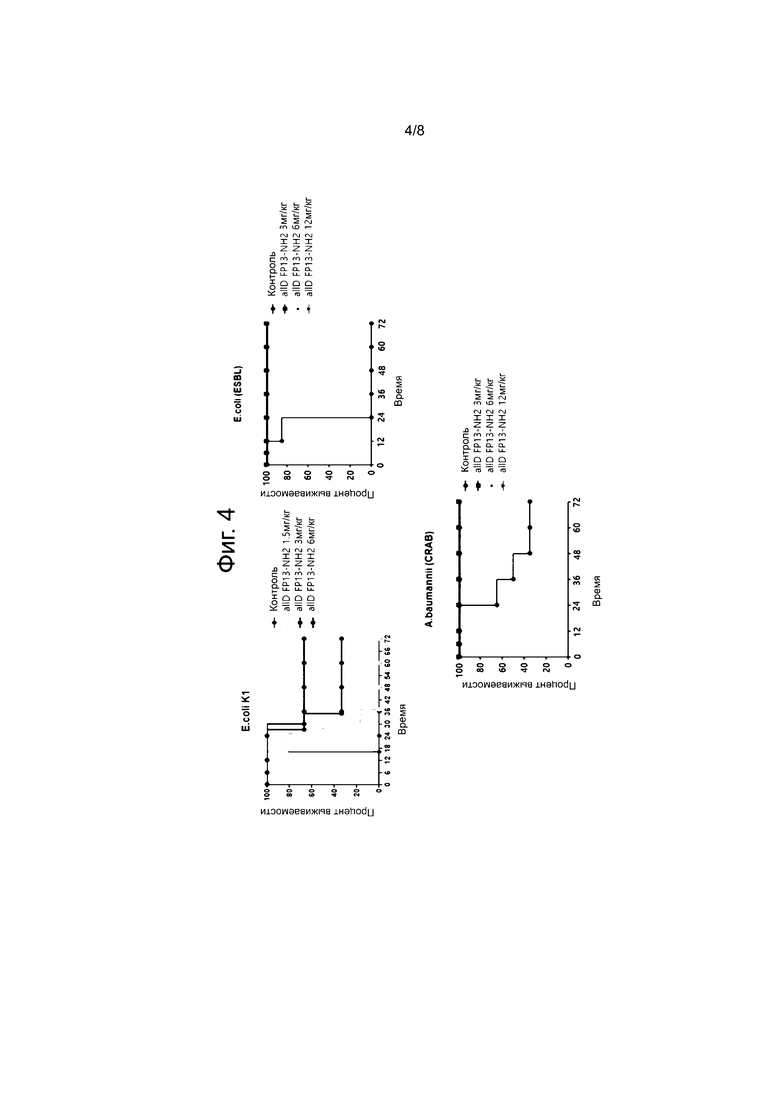
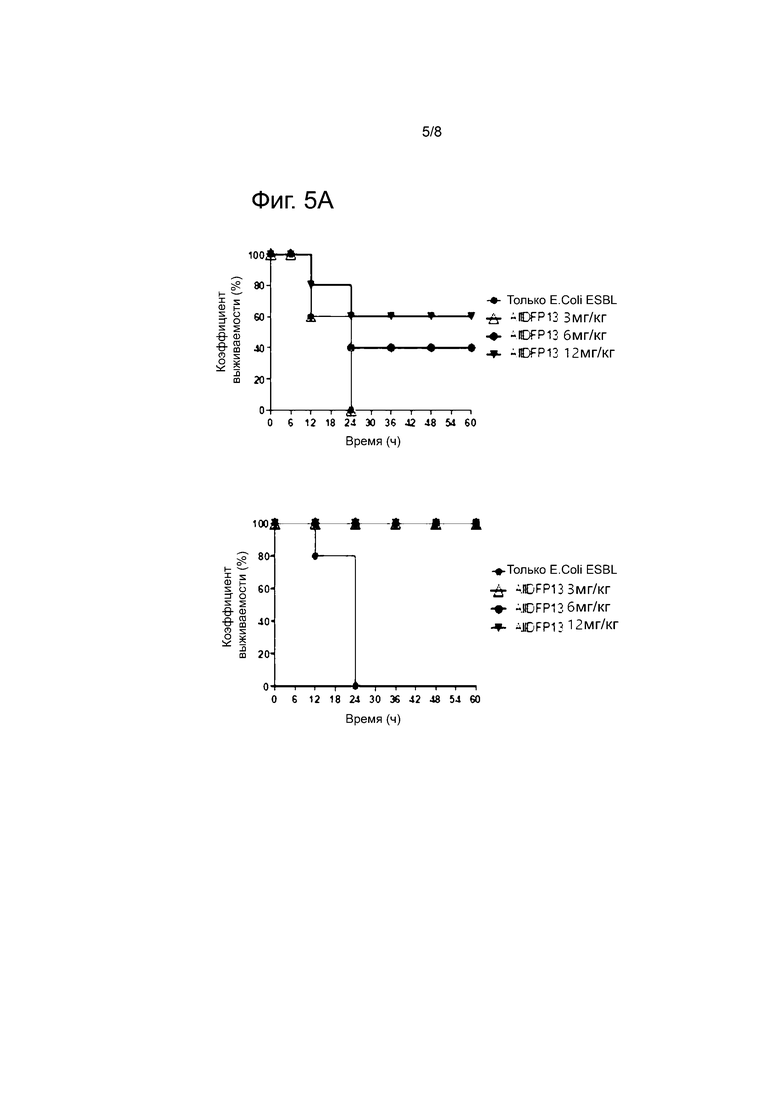
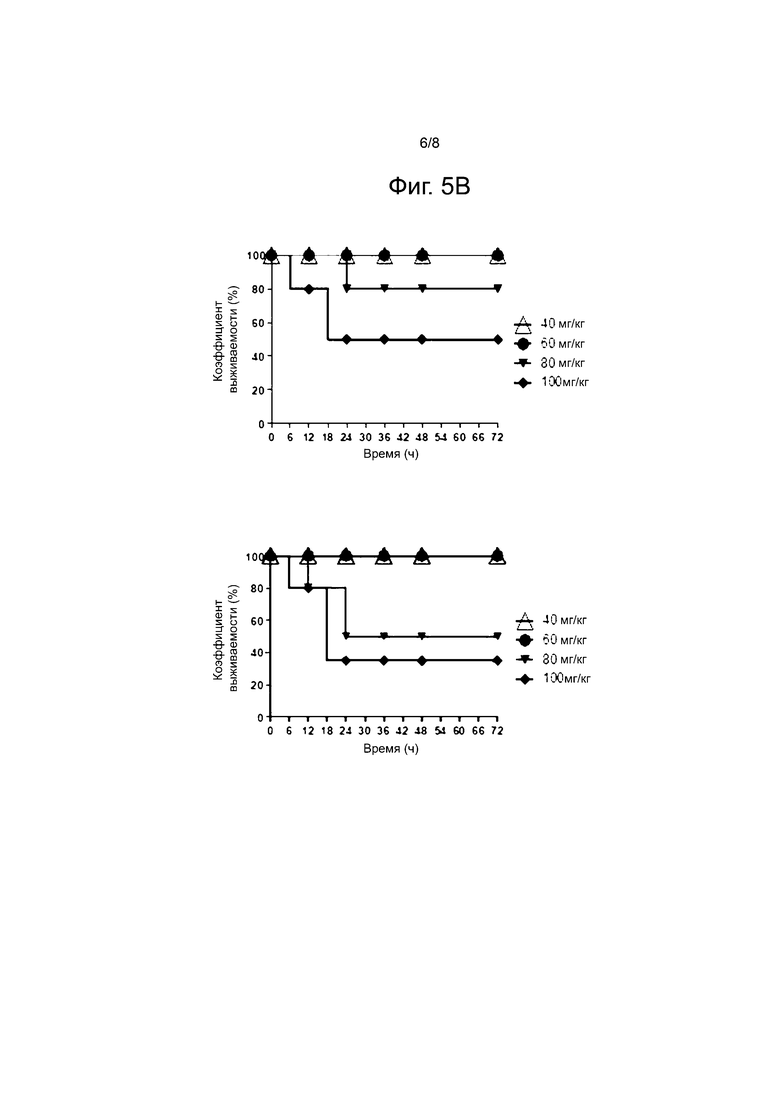
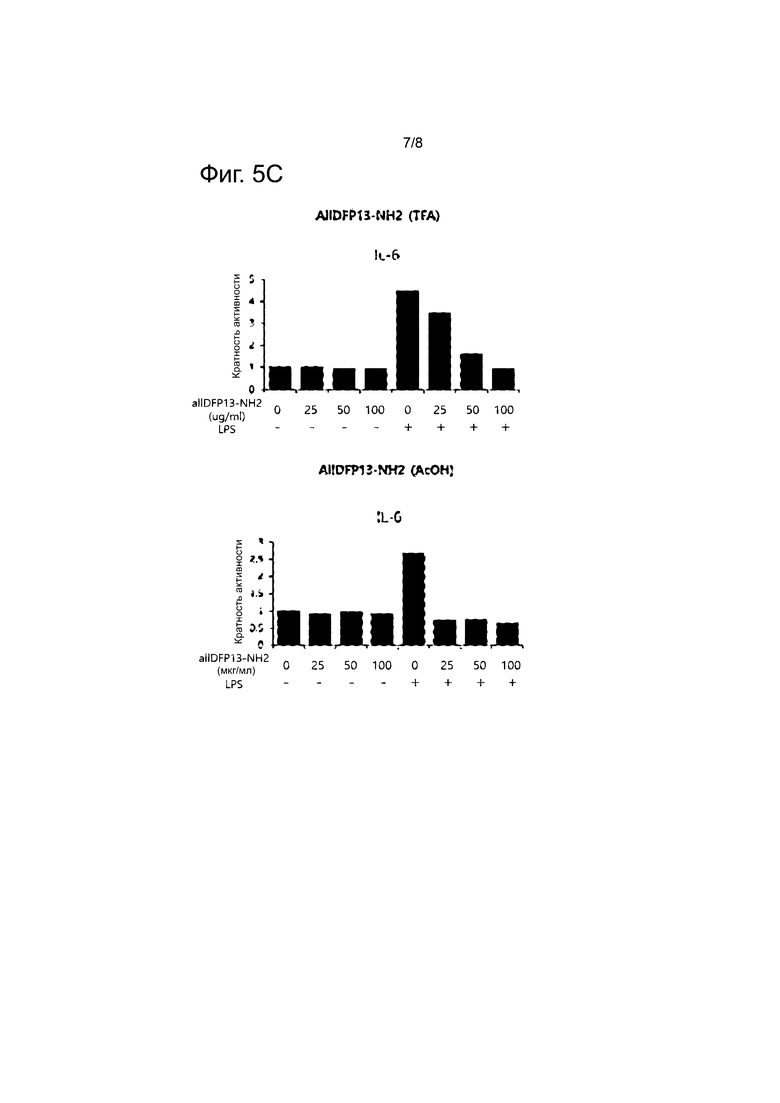

Изобретение относится к области биотехнологии, конкретно к пептидам с антибактериальной активностью, и может быть использовано в медицине для профилактики или лечения инфекционных заболеваний. Изобретение обеспечивает получение пептидов, обладающих эффективностью в подавлении роста грамположительных/грамотрицательных бактерий, что обеспечивает необходимый терапевтический эффект в лечении сепсиса. 25 н. и 10 з.п. ф-лы, 6 ил., 7 табл., 12 пр.
1. Полипептид, представленный следующей общей формулой последовательности:
[Общая формула]
Ln-X1-L-X2-V-X3-X4-X5-R-X6-L-X7,
в общей формуле,
n представляет собой 0 или 1;
L представляет собой лейцин;
V представляет собой валин;
R представляет собой аргинин;
X1 представляет собой лизин (K) или аргинин (R);
X2 представляет собой глицин (G) или аргинин (R);
X3 представляет собой глутаминовую кислоту (E) или лизин (K);
X4 представляет собой аланин (A) или лейцин (L);
X5 представляет собой лизин (K), лейцин (L) или аргинин (R);
X6 представляет собой тирозин (Y), аланин (A), триптофан (W), лизин (K) или аспарагиновую кислоту (D); и
X7 представляет собой аспарагиновую кислоту (D) или аргинин (R),
но в общей формуле исключен полипептид, представленный последовательностью K-L-G-V-E-A-K-R-Y-L-D,
где полипептид имеет антибактериальную активность против грамотрицательных бактерий, и
необязательно, где полипептид алкилирован, ПЭГилирован, или амидирован на конце полипептида, и
необязательно, где аминогруппа (NH2) добавлена к С-концу полипептида.
2. Полипептид по п.1, который представляет собой любой из 10 типов полипептидов, представленных общими формулами с 1) по 10):
1) полипептид, представленный общей формулой, в которой
n представляет собой 0;
X1 представляет собой лизин (K);
X2 представляет собой глицин (G);
X3 представляет собой глутаминовую кислоту (E);
Х4 представляет собой аланин (А);
Х5 представляет собой лизин (K);
X6 представляет собой тирозин (Y); и
X7 представляет собой аргинин (R),
2) полипептид, представленный общей формулой, в которой
n представляет собой 1;
X1 представляет собой аргинин (R);
X2 представляет собой глицин (G);
X3 представляет собой глутаминовую кислоту (E);
Х4 представляет собой аланин (А);
Х5 представляет собой лизин (K);
X6 представляет собой тирозин (Y); и
X7 представляет собой аргинин (R),
3) полипептид, представленный общей формулой, в которой
n представляет собой 1;
X1 представляет собой аргинин (R);
X2 представляет собой глицин (G);
X3 представляет собой глутаминовую кислоту (E);
X4 представляет собой лейцин (L);
Х5 представляет собой лизин (K);
X6 представляет собой тирозин (Y); и
X7 представляет собой аргинин (R),
4) полипептид, представленный общей формулой, в которой
n равно 0;
X1 представляет собой лизин (K);
X2 представляет собой глицин (G);
X3 представляет собой глутаминовую кислоту (E);
Х4 представляет собой аланин (А);
X5 представляет собой лейцин (L);
X6 представляет собой тирозин (Y); и
X7 представляет собой аспарагиновую кислоту (D),
5) полипептид, представленный общей формулой, в которой
n представляет собой 0;
X1 представляет собой аргинин (R);
X2 представляет собой аргинин (R);
Х3 представляет собой лизин (K);
X4 представляет собой лейцин (L);
X5 представляет собой аргинин (R);
X6 представляет собой тирозин (Y); и
X7 представляет собой аргинин (R),
6) полипептид, представленный общей формулой, в которой
n представляет собой 0;
X1 представляет собой лизин (K);
X2 представляет собой аргинин (R);
Х3 представляет собой лизин (K);
X4 представляет собой лейцин (L);
X5 представляет собой аргинин (R);
X6 представляет собой тирозин (Y); и
X7 представляет собой аргинин (R),
7) полипептид, представленный общей формулой, в которой
n представляет собой 0;
X1 представляет собой лизин (K);
X2 представляет собой аргинин (R);
Х3 представляет собой лизин (K);
X4 представляет собой лейцин (L);
X5 представляет собой аргинин (R);
Х6 представляет собой аланин (А); и
X7 представляет собой аргинин (R),
8) полипептид, представленный общей формулой, в которой
n представляет собой 0;
X1 представляет собой лизин (K);
X2 представляет собой аргинин (R);
Х3 представляет собой лизин (K);
X4 представляет собой лейцин (L);
X5 представляет собой аргинин (R);
X6 представляет собой триптофан (W); и
X7 представляет собой аргинин (R),
9) полипептид, представленный общей формулой, в которой
n представляет собой 0;
X1 представляет собой лизин (K);
X2 представляет собой аргинин (R);
Х3 представляет собой лизин (K);
X4 представляет собой лейцин (L);
X5 представляет собой аргинин (R);
Х6 представляет собой лизин (K); и
X7 представляет собой аргинин (R), и
10) полипептид, представленный общей формулой, в которой
n представляет собой 0;
X1 представляет собой аргинин (R);
X2 представляет собой аргинин (R);
X3 представляет собой лизин (K);
X4 представляет собой лейцин (L);
X5 представляет собой аргинин (R);
X6 представляет собой триптофан (W); и
X7 представляет собой аргинин (R).
3. Полипептид, представленный следующей общей формулой последовательности:
[Общая формула]
Ln-X1-L-X2-V-X3-X4-X5-R-X6-L-X7,
в общей формуле
n представляет собой 0 или 1;
L представляет собой лейцин;
V представляет собой валин;
R представляет собой аргинин;
X1 представляет собой лизин (K) или аргинин (R);
X2 представляет собой глицин (G) или аргинин (R);
X3 представляет собой глутаминовую кислоту (E) или лизин (K);
X4 представляет собой аланин (A) или лейцин (L);
X5 представляет собой лизин (K), лейцин (L) или аргинин (R);
X6 представляет собой тирозин (Y), аланин (A), триптофан (W), лизин (K) или аспарагиновую кислоту (D); и
X7 представляет собой аспарагиновую кислоту (D) или аргинин (R),
но в общей формуле исключен полипептид, представленный последовательностью K-L-G-V-E-A-K-R-Y-L-D,
где полипептид имеет антибактериальную активностью против грамотрицательных бактерий, и
необязательно, где полипептид алкилирован, ПЭГилирован, или амидирован на конце полипептида, и
необязательно, где аминогруппа (NH2) добавлена к С-концу полипептида, и
где полипептид представляет собой пептидомиметик, такой как пептид L-типа, пептид D-типа и пептоид, или модифицированный пептид, содержащий неприродные аминокислоты.
4. Полипептид по п. 1 или 3, который алкилирован, ПЭГилирован или амидирован на конце полипептида.
5. Полипептид по п. 1 или 3, отличающийся тем, что аминогруппа (NH2) добавлена к С-концу полипептида.
6. Полипептид по п. 1 или 3, отличающийся тем, что полипептид имеет одну или несколько из следующих характеристик:
связывающую способность к липополисахариду (ЛПС) грамотрицательных бактерий;
способность избирательного разрушения мембраны бактериальных клеток;
устойчивость к протеолитическим ферментам;
способность разрушать клеточную мембрану грамположительных бактерий; и
способность связываться с липотейхоевой кислотой (ЛТК) или липопротеином (ЛПП), полученной из грамположительных бактерий.
7. Производное полипептида по п. 1 или 3 с замещением трифторуксусной кислоты (ТФК) на ацетатную соль,
где трифторуксусная кислота (TFA) в полипептиде заменена ацетатной солью, и
где данное производное с замещением ацетатной солью имеет антибактериальную активность против грамотрицательных бактерий.
8. Композиция для профилактики или лечения сепсиса, содержащая:
фармацевтически эффективное количество полипептида по п. 1 или 3 или производного с замещением ацетатной солью по п. 7 в качестве активного ингредиента.
9. Антибактериальная композиция, содержащая:
фармацевтически эффективное количество полипептида по п. 1 или 3 или производного с замещением ацетатной солью по п. 7 в качестве активного ингредиента.
10. Антибактериальная композиция по п. 9, отличающаяся тем, что бактерии, на которые нацелена антибактериальная композиция, представляют собой одну или более бактерий, выбранных из группы, состоящей из Escherichia coli DH5α, Escherichia coli K1, Acinetobacter baumannii, Pseudomonas aeruginosa, Salmonella enteritidis, Salmonella typhimurium, Klebsiella pneumoniae, Staphylococcus aureus и Staphylococcus epidermidis.
11. Антибактериальная композиция по п. 9, отличающаяся тем, что бактерии, на которые нацелена антибактериальная композиция, представляют собой один или несколько типов устойчивых к антибиотикам бактерий, выбранных из группы, состоящей из бактерий, устойчивых к бета-лактамазе расширенного спектра (БЛРС), устойчивых к карбапенемам бактерий, и бактерий, устойчивых к колистину.
12. Антибактериальная композиция по п. 11, отличающаяся тем, что устойчивые к антибиотикам бактерии представляют собой одну или несколько бактерий, выбранных из группы, состоящей из БЛРС (E. coli), устойчивого к карбапенему (CR)-Acinetobactor baumannii, CR-Klebsiella pneumoniae, CR-Pseudomonas aeruginosa и устойчивого к колистину Acinetobactor baumannii.
13. Композиция для профилактики, облегчения или лечения инфекционного заболевания, содержащая:
фармацевтически эффективное количество полипептида по п. 1 или 3 или производного с замещением ацетатной солью по п. 7 в качестве активного ингредиента,
и где инфекционное заболевание вызвано грамотрицательными бактериями.
14. Композиция по п. 13, отличающаяся тем, что инфекционное заболевание представляет собой инфекционное заболевание, вызываемое грамотрицательными бактериями, которое выбрано из пневмонии, перитонита, менингита, раневой инфекции, остеоартрита, холецистита, инфекции мочевыводящих путей, эндокардита, миокардита, перикардита, артрита, фарингита, гонореи, бактериальной дизентерии, энтерита, конъюнктивита, гастрита, среднего отита, цистита и лимфангита.
15. Композиция для профилактики, облегчения или лечения инфекционного заболевания, содержащая:
фармацевтически эффективное количество полипептида, представленного общей формулой 5), 6) и 10) согласно п. 2, или его производного с замещением ацетатной солью в качестве активного ингредиента,
и где инфекционное заболевание вызвано грамположительными бактериями.
16. Композиция по п. 15, отличающаяся тем, что инфекционное заболевание представляет собой инфекционное заболевание, вызываемое грамположительными бактериями, которое выбрано из группы, состоящей из ларингофарингита, импетиго, ревматической лихорадки, гломерулонефрита, неонатального сепсиса, менингита, фарингита, пневмонии, эндокардита, скарлатины, SSTI (инфекции кожи и мягких тканей), инфекции глубоких мягких тканей, эмпиемы и вагинита.
17. Полинуклеотид, кодирующий полипептид по п. 1 или 3.
18. Рекомбинантный вектор, содержащий полинуклеотид по п. 17.
19. Способ получения полипептида по п. 1 или 3, включающий:
культивирование клеток-хозяев, трансформированных рекомбинантным вектором по п. 18.
20. Способ лечения сепсиса, включающий:
введение полипептида по п. 1 или 3 или производного с замещением ацетатной солью по п. 7 субъекту, нуждающемуся в лечении.
21. Применение полипептида по п. 1 или 3 или производного с замещением ацетатной солью по п. 7 для профилактики, облегчения или лечения сепсиса.
22. Применение полипептида по п. 1 или 3 или производного с замещением ацетатной солью по п. 7 для приготовления препарата для профилактики, облегчения или лечения сепсиса.
23. Способ лечения инфекционного заболевания, включающий:
введение полипептида по п. 1 или 3 или производного с замещением ацетатной солью по п. 7 субъекту, нуждающемуся в лечении,
и где инфекционное заболевание вызвано грамотрицательными бактериями.
24. Способ лечения инфекционного заболевания, включающий:
введение полипептида, представленного общей формулой 5), 6) и 10) согласно п. 2, или его производного с замещением ацетатной солью субъекту, нуждающемуся в лечении,
и где инфекционное заболевание вызвано грамположительными бактериями.
25. Применение полипептида по п. 1 или 3 или производного с замещением ацетатной солью по п.7 для профилактики, облегчения или лечения инфекционного заболевания, и где инфекционное заболевание вызвано грамотрицательными бактериями.
26. Применение полипептида, представленного общей формулой 5), 6) и 10) согласно п. 2, или его производного с замещением ацетатной солью для профилактики, облегчения или лечения инфекционного заболевания, и где инфекционное заболевание вызвано грамположительными бактериями.
27. Применение полипептида по п. 1 или 3 или производного с замещением ацетатной солью по п. 7 для приготовления препарата для профилактики, облегчения или лечения инфекционного заболевания, и где инфекционное заболевание вызвано грамотрицательными бактериями.
28. Применение полипептида, представленного общей формулой 5), 6) и 10) согласно п.2, или его производного с замещением ацетатной солью для приготовления препарата для профилактики, облегчения или лечения инфекционного заболевания, и где инфекционное заболевание вызвано грамположительными бактериями.
29. Способ профилактики бактериальной инфекции, включающий:
введение полипептида по п. 1 или 3 или производного с замещением ацетатной солью по п. 7 субъекту, нуждающемуся в лечении.
30. Применение полипептида по п. 1 или 3 или производного с замещением ацетатной солью по п. 7 против грамотрицательных бактерий.
31. Применение полипептида по п. 1 или 3 или производного с замещением ацетатной солью по п. 7 для получения антибактериального агента против грамотрицательных бактерий.
32. Применение полипептида, представленного общей формулой 5), 6) и 10) согласно п. 2, или его производного с замещением ацетатной солью против грамположительных бактерий.
33. Применение полипептида, представленного общей формулой 5), 6) и 10) согласно п. 2, или его производного с замещением ацетатной солью для получения антибактериального агента против грамположительных бактерий.
34. Полипептид по п. 2, где полипептид представлен общей формулой 5), 6) и 10) и имеет антибактериальную активность против грамположительных бактерий.
35. Производное с замещением трифторуксусной кислоты (ТФК) на ацетатную соль любого из полипептидов, представленных общей формулой 5), 6) и 10) согласно п. 2 и где
трифторуксусная кислота в полипептиде заменена на ацетатную соль,
и где производное с заменой на ацетатную соль имеет антибактериальную активность против грамположительных бактерий.
| АНТИБАКТЕРИАЛЬНЫЕ ПЕПТИДЫ | 2007 |
|
RU2468033C2 |
| WO 2000012542 A2, 09.03.2000 | |||
| CN 106749597 A, 31.05.2017 | |||
| YUAN J | |||
| et al., Site-directed mutagenesis of the hinge region of nisinZ and properties of nisinZ mutants, Applied microbiology and biotechnology, 2004, v | |||
| Нефтяной конвертер | 1922 |
|
SU64A1 |
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| HONG S | |||
| Y | |||
| et al., Effect of D-amino acid substitution on the stability, the secondary | |||
Авторы
Даты
2023-06-02—Публикация
2020-02-27—Подача