Область техники.
Изобретение относится к новым химическим соединениям, в частности к комплексам палладия с гетероциклическими лигандами общей формулы I
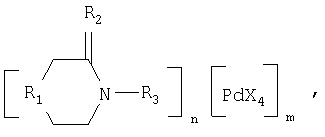
где R1-NH, О, СН2,
R2-2Н, О,
R3-Н, СН3, CH2-CH2-NH2, (СО)-СН3,
Х-Cl, Br,
n=1, m=1, при R1-NH, О; R2-2Н; R3-Н, СН3; CH2-CH2-NH2; (СО)-СН3,
n=2, m=1, при R1-О, СН2; R2-О, 2Н; R3-Н, СН3, (СО)-СН3,
n=2, m=3, при R1-NH; R2=2Н; R3-CH2-CH2-NH2, обладающим фармакологической активностью.
Предшествующий уровень техники.
Известны комплексные соединения платины (II), обладающие противоопухолевой активностью, такие как платин, цисплатин, карбоплатин (Машковский М.Д. "Лекарственные средства", издание тринадцатое, Харьков, издательство "Торсинг". 1997 г., том II, стр.458-460).
Данные соединения по механизму действия близки к алкилирующим соединениям, они взаимодействуют с ДНК с образованием меж- и внутримолекулярных сшивок. Механизм противоопухолевого действия препаратов платины связан со способностью к бифункциональному алкилированию нитей ДНК, ведущему к длительному подавлению биосинтеза нуклеиновых кислот и гибели клетки.
Известные препараты на основе платины высокотоксичны. Серьезным побочным эффектом платиновых препаратов является нефротоксичность. Из других побочных реакций, вызываемых платиновыми препаратами, следует отметить лейкопению, тошноту и рвоту.
Кроме того, поскольку препараты очень токсичны и легко всасываются кожей и слизистыми оболочками, они опасны для людей, связанных с их производством. Работать с ними необходимо в резиновых перчатках и респираторах.
И еще один немаловажный недостаток - высокая стоимость платины, которая приводит к удорожанию лекарственных препаратов на ее основе.
Поиск новых препаратов с высокой активностью и пониженной токсичностью на основе металлов платиновой группы является актуальной задачей.
Раскрытие изобретения
Задачей предлагаемого изобретения является расширение арсенала химических соединений, действующих на живой организм, в частности, обладающих противоопухолевым действием и характеризующихся пониженной токсичностью.
Задача решена тем, что согласно изобретению создано новое химическое соединение - комплексы палладия с гетероциклическими лигандами общей формулы I:

где R1-NH, О, СН2,
R2-2Н, О,
R3-Н, СН3, СН2-СН2-NH2, (СО)-СН3,
Х-Cl, Br,
n=1, m=1, при R1-NH, O; R2-2Н; R3-Н, СН3; СН2-СН2-NH2,
(СО)-СН3,
n=2, m=1, при R1-О, СН2; R2-О, 2Н; R3-Н, СН3, (СО)-СН3,
n=2, m=3, при R1-NH; R2-2Н; R3-CH2-CH2-NH2.
Согласно изобретению новые соединения обладают, в частности, высокой противоопухолевой активностью, пониженной токсичностью. Лучший вариант осуществления изобретения.
Заявляемые соединения общей формулы I представляют собой комплексы палладия катион-анионного типа, содержащие в своем составе анион [PdCl4]2-.
Способ получения соединений состоит из двух стадий.
На первой стадии органический лиганд в растворе подвергается протонированию галогеноводородной кислотой. На второй стадии протонированный лиганд в растворе подвергается взаимодействию с соединением палладия при стехиометрическом соотношении компонентов при температуре 30-80°C с последующим выделением целевого продукта из раствора.
Соединения получают как в водной, так и в неводной среде.
В частности получены следующие соединения, представленные в таблице 1.
Далее приведены примеры получения указанных соединений.
Пример 1. Синтез соединения I
Навеску 2,29 г (11,79 ммоль) гексагидрата пиперазина растворяют в 13 мл H2O и подкисляют 1,5 мл HCl до рН˜1. Навеску 2,09 г (11,78 ммоль) дихлорида палладия растворяют при нагревании (˜60°С) в смеси 25 мл H2O и 3 мл HCl. Растворы сливают вместе и упаривают на водяной бане до начала кристаллизации. После охлаждения отфильтровывают выделившиеся кристаллы, промывают этанолом. Сушат в сушильном шкафу при температуре 90°С и постоянном давлении. Выход 3,68 г, что составляет 93% от теоретического в расчете на введенный в реакцию палладий.
Для состава C4H10N2PdCl4 вычислено, %: Pd - 31,63; Cl - 42,16.
Найдено, %: Pd - 31,90; Cl - 41,50.
Пример 2. Синтез соединения II.
Навеску 1,66 г (16,30 ммоль) N-метилпиперазина растворяют в 15 мл Н2О и подкисляют 2,5 мл HCl до рН˜1. Навеску 2,89 г (16,30 ммоль) дихлорида палладия растворяли при нагревании в смеси 25 мл Н2О и 3 мл HCl, раствор профильтровывают, приливают к раствору лиганда и упаривают на водяной бане до начала кристаллизации. После охлаждения отфильтровывают выпавшие кристаллы, промывают этанолом. Сушат в сушильном шкафу при температуре 90°С и постоянном давлении. Выход 4,2 г, что составляет 74% от теоретического в расчете на введенный в реакцию палладий.
Для состава С5Н13N2PdCl4 вычислено, %: Pd - 30,36; Cl - 40,42.
Найдено, %: Pd - 30,90; Cl - 41,10.
Пример 3. Синтез соединения III.
Навеску 1,14 г (1,09 ммоль) 4-ацетилпиперазина растворяют в 15 мл ацетона и подкисляют 0,2 мл HCl для протонирования лиганда. Навеску 0,35 г (0,91 ммоль) бензонитрилпалладийдихлорида растворяют при нагревании в 15 мл ацетона, профильтровывают и приливают к раствору лиганда. В течение 3 часов смесь перемешивали на магнитной мешалке. Выделившийся осадок отфильтровывают, промывают ацетоном, сушат в сушильном шкафу при температуре 80°С и постоянном давлении. Выход 0,31 г, что составляет 74% от теоретического в расчете на введенный палладий.
Для состава С6Н13N2OPdCl4 вычислено, %: Pd - 28,01; Cl - 37,47.
Найдено, %: Pd - 29,12; Cl - 37,65.
Пример 4. Синтез соединения IV.
Навеску 1,52 г (11,77 ммоль) 1-(2-аминоэтил)пиперазина растворяют в 15 мл Н2O и подкисляют 3,5 мл HCl до рН˜1. Навеску 3,13 г (17,65 ммоль) дихлорида палладия растворяют при нагревании в смеси 25 мл Н2О и 4 мл HCl. Растворы сливают вместе и упаривали на водяной бане при температуре 70°С до начала кристаллизации. После охлаждения отфильтровывают выпавшие кристаллы, промывают этанолом. Сушат в сушильном шкафу при температуре 80°С и постоянном давлении. Выход 4,38 г, что составляет 74% от теоретического в расчете на введенный в реакцию палладий.
Для состава C12H32N6Pd3Cl12 вычислено, %: Pd - 32,16; Cl - 42,16.
Найдено, %: Pd - 32,64; Cl - 42,80.
Пример 5. Синтез соединения V.
Навеску 1,46 г (16,80 ммоль) морфолина растворяют в 10 мл Н2О и подкисляют HCl до рН˜1 (2 мл). Навеску дихлорида палладия 1,49 г (8,40 ммоль) растворяют при нагревании (55-60°С) в смеси 15 мл Н2О и 2 мл HCl, профильтровывают и приливают к раствору морфолина. Полученную смесь упаривают на кипящей водяной бане до начала кристаллизации, охлаждают и отфильтровывают кристаллический осадок от маточника. Сушат в сушильном шкафу при температуре 90°С при постоянном давлении до постоянного веса.
Выход 3,1 г, что составляет 86,8% от теоретического в расчете на введенный в реакцию палладий.
Для состава C8H18N2O2PdCl4 вычислено, %: Pd - 25,06; Cl - 33,41.
Найдено, %: Pd - 25,12; Cl - 32,52.
Пример 6. Синтез соединения VI.
Навеску 1,17 г (13,43 ммоль) морфолина растворяют в 15 мл Н2О и подкисляют HBr до рН˜1 (2,3 мл 46% HBr). Навеску 1,78 г (6,71 ммоль) PdBr2 растворяют при нагревании (55-60°С) в смеси 20 мл Н2О и 2 мл HBr, раствор отфильтровывают и приливают к раствору лиганда. Смесь упаривают на кипящей водяной бане до начала кристаллизации, охлаждают, кристаллический осадок отфильтровывают, промывают небольшим количеством этанола. Сушат в сушильном шкафу при 90°С и постоянном давлении до постоянного веса. Выход 2,68 г, что составляет 67,5% от теоретического в расчете на введенный в реакцию палладий. Для состава C8H18N2O2PdBr4 вычислено, %: Pd - 17,66; Br - 53,06. Найдено, %: Pd - 17,63; Br - 54,80.
Пример 7. Синтез соединения VII.
Навеску 1,84 г (18,19 ммоль) 4-метилморфолина растворяют в 20 мл воды и подкисляют 2 мл HCl до рН˜1. Навеску дихлорида палладия 1,61 г (9,08 ммоль) растворяют при нагревании (˜60°С) в смеси 15 мл воды и 2 мл HCl, раствор профильтровывают и приливают к раствору лиганда. Смесь упаривают на кипящей водяной бане до min объема, охлаждают, выделившийся кристаллический осадок отфильтровывают, сушат в сушильном шкафу при 90°С и постоянном давлении до постоянного веса. Выход 3,44 г, что составляет 84% от теоретического в расчете на введенный в реакцию палладий.
Для состава C10H24N2O2PdCl4 вычислено, %: Pd - 23,51; Cl - 31,33.
Найдено, %: Pd - 23,30; Cl - 31,33.
Пример 8. Синтез соединения VIII.
К навеске 0,31 г (2,40 ммоль) 4-ацетилморфолина в 5 мл ацетона добавяют 0,21 мл HCl. Навеску 0,46 г (1,20 ммоль) бензонитрилпалладийдихлорида растворяют при нагревании (˜30°С) в 15 мл ацетона, отфильтровывают и приливают к раствору лиганда. В течение 5 часов смесь перемешивают на магнитной мешалке. Выделившийся осадок отфильтровывают, промывают ацетоном, сушат в сушильном шкафу при 70°С и постоянном давлении. Выход 0,47 г, что составляет 77% от теоретического в расчете на введенный в реакцию палладий.
Для состава C12H24N2O4PdCl4 вычислено, %: Pd - 20,91; Cl - 27,84.
Найдено, %: Pd - 21,09; Cl - 28,51.
Пример 9. Синтез соединения IX.
Навеску 0,95 г (7,30 ммоль) 4-(2-аминоэтил)морфолина в 5 мл Н2О подкисляют HCl до рН˜1. Навеску дихлорида палладия 1,29 г (7,28 ммоль) растворяют при нагревании (˜60°С) в смеси 15 мл Н2O и 2 мл HCl, отфильтровывают и приливают к раствору лиганда. Смесь упаривают на водяной бане при температуре 80°С до min объема, охлаждают, выделившийся кристаллический осадок отфильтровывают от маточника, сушат в сушильном шкафу при температуре 60°С и постоянном давлении. Выход 1,85 г, что составляет 66% от теоретического в расчете на введенный в реакцию палладий. Соединение выделяется в виде моногидрата: [C6H16N2O][PdCl4]·Н2О.
Для состава C6H17N2O2PdCl4 вычислено, %: Pd - 27,53; Cl - 36,69.
Найдено, %: Pd - 28,16; Cl - 36,60.
Пример 10. Синтез соединения X.
Навеску 1,60 г (16,14 ммоль) 2-пиперидона растворяют в 15 мл Н2О и подкисляют 2 мл HCl до рН˜1. К этому раствору приливают солянокислый раствор 1,43 г (8,07 ммоль) дихлорида палладия в смеси 20 мл Н2О и 3 мл HCl. Смесь упаривают на водяной бане до начала кристаллизации, охлаждают и отфильтровывают выделившиеся кристаллы. Сушат в сушильном шкафу при температуре 110°С и постоянном давлении. Выход 2,32 г, что составляет 59% от теоретического в расчете на введенный в реакцию палладий.
Соединение кристаллизуется с 2 молекулами воды. Для состава C10H22NO4PdCl4 вычислено, %: Pd=21,96; Cl=29,96.
Найдено, %: Pd=21,64; Cl=29,20.
Строение полученных соединений было установлено методом ИК-спектроскопии.
Инфракрасные спектры были измерены в области 4000-100 см-1 на ИК Фурье-спектрометре Nicolet Magna-750 (США). Спектры в области 4000-400 см-1 измерены с разрешением 2 см-1 в таблетках с KBr. Спектры в области 600-100 см-1 получены с разрешением 4 см-1 в виде пасты с вазелиновым маслом.
Выводы о строении заявляемых соединений сделаны на основании сопоставления спектров комплексов со спектрами свободных лигандов (в виде гирохлоридов), а также солей, содержащих анион [PdCl4]2-.
Спектры соединений V, VII, VIII, IX, Х в области 2000-400 см-1 сходны со спектрами протонированных лигандов LH+ в гидрохлоридах L.HCl (L - молекула гетероциклического лиганда). Для соединений I, II, III, IV спектры в этой области близки к спектрам соответствующих катионов L'H2 2+ в дигидрохлоридах. Это однозначно указывает, что все изученные соединения содержат протонированные лиганды в качестве катиона. Некоторые сдвиги и расщепления полос по сравнению с гидрохлоридами вызваны заменой аниона. Заметные изменения в спектрах комплексов по сравнению с гидрохлоридами имеются в области 4000-2000 см-1. Наиболее заметно исчезновение широкой группы сильных полос с максимумами в области 2450-2700 см-1, обусловленных сильными водородными связями в твердом гидрохлориде. В комплексах эта система водородных связей разрушается, а вместо указанной группы полос появляется сильная широкая полоса в области 3000-3100 см-1, обусловленная валентными колебаниями N+-H. Для нейтральных молекул L поглощение в области выше 3000 см-1 отсутствует. Появление в спектре поглощения в этой области подтверждает вывод, что лиганд в палладиевом комплексе присутствует в протонированной катионной форме.
Низкочастотные ИК-спектры (500-100 см-1) содержат кроме полос, принадлежащих протонированному катиону лиганда, и близких по положению к соответствующим полосам в гидрохлоридах две новых полосы поглощения: сильную полосу в области 320-335 см-1 и более слабую полосу около 150-160 см-1. Эти полосы характерны для плоского квадратного аниона [PdCl4]2- и относятся соответственно к валентным колебаниям νPdCl, ν6(Е2u) и деформационным колебаниям δPdCl2, ν7(Eu). Для сравнения укажем, что в K2PdCl4 соответствующие частоты равны 321 и 161 см-1, а в спектре имеющего ионное строение комплекса с эфедрином [C10H16ON]2[PdCl4] они наблюдаются при 323 и 149 см-1. При переходе от аниона [PdCl4]2- к [PdBr4]2- (в соединении VI) они смещаются до 251 и 126 см-1, что подтверждает их отнесение к колебаниям палладийгалоид. Отметим, что для K2PdBr4 эти полосы лежат при 243 и 114 см-1 соответственно. Отсутствие в низкочастотном спектре других полос, которые можно было бы приписать колебаниям металл-лиганд, также согласуется с ионной структурой. Таким образом, ИК-спектры в средней и низкочастотной области однозначно свидетельствуют о том, что соединения имеют катионно-анионное строение [LH+]2[PdX4 2-] (X=Cl, Br) в случае соединений V-X, [LH2 2+][PdCl4 2-] для соединений I-III и [LH3 +3]2[PdX4 2-]3, для соединения IV (где L - соответствующий комплексу лиганд). Вывод согласуется с данными химических анализов о соотношении лиганд: металл в комплексах.
Положение некоторых характерных полос поглощения для предлагаемых соединений приведено в таблице 2.
Некоторые характерные полосы (частоты в см-1) в ИК-спектрах соединений
Была изучена специфическая активность ряда полученных соединений I, II, V, VI, VII, VIII, IX, Х и определена их острая токсичность.
| название | год | авторы | номер документа |
|---|---|---|---|
| Катионно - анионные комплексы палладия | 2018 |
|
RU2699809C1 |
| СОЕДИНЕНИЯ НА ОСНОВЕ ПАЛЛАДИЯ И ПРОИЗВОДНЫХ АРОМАТИЧЕСКИХ АМИНОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1992 |
|
RU2022968C1 |
| ПРОИЗВОДНЫЕ БИСАМИДОВ ДИКАРБОНОВЫХ КИСЛОТ, ИХ ПРИМЕНЕНИЕ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2013 |
|
RU2665688C2 |
| ПРОИЗВОДНОЕ БИСАМИДОВ ДИКАРБОНОВЫХ КИСЛОТ, ЕГО ПРИМЕНЕНИЕ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ, СПОСОБЫ ЕГО ПОЛУЧЕНИЯ | 2018 |
|
RU2725881C2 |
| Дипептидные лиганды TSPO, обладающие нейропсихотропной активностью | 2018 |
|
RU2756772C2 |
| ПРОИЗВОДНОЕ БИСАМИДОВ ДИКАРБОНОВЫХ КИСЛОТ, ЕГО ПРИМЕНЕНИЕ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ, СПОСОБЫ ЕГО ПОЛУЧЕНИЯ | 2021 |
|
RU2840866C2 |
| ПРОИЗВОДНОЕ БИСАМИДОВ ДИКАРБОНОВЫХ КИСЛОТ, ЕГО ПРИМЕНЕНИЕ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ, СПОСОБЫ ЕГО ПОЛУЧЕНИЯ | 2018 |
|
RU2721421C2 |
| ПРОИЗВОДНОЕ БИСАМИДОВ ДИКАРБОНОВЫХ КИСЛОТ, ЕГО ПРИМЕНЕНИЕ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ, СПОСОБЫ ЕГО ПОЛУЧЕНИЯ | 2018 |
|
RU2719464C2 |
| ПРОИЗВОДНОЕ БИСАМИДОВ ДИКАРБОНОВЫХ КИСЛОТ, ЕГО ПРИМЕНЕНИЕ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ, СПОСОБЫ ЕГО ПОЛУЧЕНИЯ | 2020 |
|
RU2815401C2 |
| ЗАМЕЩЕННЫЙ БИСДИПЕПТИД С НЕЙРОПРОТЕКТИВНЫМ И АНТИДЕПРЕССИВНЫМ ЭФФЕКТОМ | 2014 |
|
RU2559880C1 |
Изобретение относится к новым химическим соединениям, именно к комплексам палладия с гетероциклическими лигандами общей формулы I:
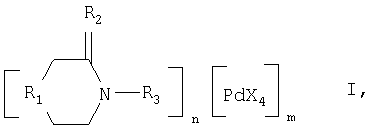
где R1-NH, O, CH2, R2-2H, O,
R3-H, СН3, CH2-CH2-NH2, (СО)-СН3, Х-Cl, Br, n=1, m-1, при R1-NH, O; R2-2Н; R3-Н, СН3; CH2-CH2-NH2; (СО)-СН3, n=2, m=1, при R1-О, СН2; R2-О, 2Н; R3-Н, СН3, (СО)-СН3,n=2, m=3, при R1-NH; R2-2Н; R3-CH2-CH2-NH2, проявляющим фармакологическую, в частности противоопухолевую активность. Соединения обладают высокой активностью и характеризуются пониженной токсичностью по сравнению с противоопухолевыми препаратами комплексов платины. 3 з.п. ф-лы, 2 табл.
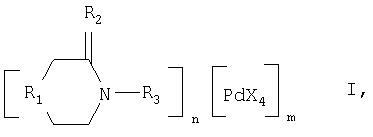
где R1 - NH, О, СН2;
R2 - 2H, O;
R3 - Н, СН3, CH2-CH2-NH2, (СО)-СН3;
Х - Cl, Br;
n-1, m=1, при R1 - NH, O; R2 - 2Н; R3 - Н, СН3; CH2-CH2-NH2; (СО)-СН3;
n=2, m=1, при R1 - О, СН2; R2 - О, 2Н; R3 - Н, СН3, (СО)-СН3;
n=2, m=3, при R1 - NH; R2 - 2Н; R3 - CH2-CH2-NH2.
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Комплексные соединения ди/2-хлорэтил/ аминобенз-2,1,3-тиадиазолов с палладием, обладающие противоопухолевой активностью" | 1976 |
|
SU646593A1 |
| DE 10062577 A1, 11.07.2002 | |||
| МЕТАЛЛООРГАНИЧЕСКИЕ КОМПЛЕКСЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, КАТАЛИЗАТОР ГИДРОФОРМИЛИРОВАНИЯ НА ИХ ОСНОВЕ И ПРОМЕЖУТОЧНЫЙ ПРОДУКТ | 1999 |
|
RU2188202C1 |
Авторы
Даты
2007-01-20—Публикация
2002-11-12—Подача