Настоящее изобретение относится к новым металлоорганическим комплексам, содержащим катионные гетероциклические карбены.
Оно относится также к двухкатионным гетероциклическим соединениям-предшественникам для получения металлоорганических комплексов.
Предметом изобретения является также способ получения указанных выше металлоорганических комплексов.
Наконец, изобретение включает также использование названных комплексов в качестве катализаторов для определенного ряда химических реакций.
Металлоорганические комплексы, содержащие гетероциклические карбены, были уже описаны ранее. Так, в патенте ЕР-А-0721953 описываются комплексы, содержащие некатионные гетероциклические карбены, получаемые из имидазолина или пиразолина и металла групп 8, 9 и 10 Периодической классификации элементов. В патенте ЕР-А-0798041 описываются комплексы, содержащие некатионные гетероциклические карбены, получаемые из различных соединений, имеющих 5, 6 или 7-членные циклы и содержащие один или несколько атомов азота и/или серы и металл, выбранный из палладия, родия, никеля, рутения и кобальта.
Такие комплексы представляют собой очень устойчивые соединения, имеющие, кроме того, то преимущество, что они не образуют при своем разложении токсичных продуктов. Однако они обладают недостатком, состоящим в том, что их нельзя использовать в чрезмерно кислой среде, а комплексы металлов с нулевой степенью окисления не растворимы в воде, что ограничивает область их применения.
Таким образом, настоящее изобретение относится прежде всего к металлоорганическим комплексам, содержащим гетероциклические карбены, отличающимся тем, что они соответствуют общей формуле (I):
[(Z+X-)mMLn]Y (I)
в которой Z+ обозначает ион 1,2,4-триазолий-5-илидена, у которого по крайней мере часть атомов цикла замещена углеводородными радикалами;
L обозначает ионный или нейтральный лиганд;
М обозначает металл, выбираемый из переходных элементов групп 1b, 2b, 3b, 4b, 5b, 6b, 7b и 8 периодической классификации элементов, такой, которая опубликована в "Handbook of Chemistry and Physics, 51st Edition" (1970-1971) фирмы The Chemical Rubber Company;
X- обозначает органический или неорганический анион;
m обозначает целое число от 1 до 6;
n обозначает целое число от 0 до 5;
сумма m и n равна или меньше 6;
Y обозначает анион или катион такого типа, который обеспечивает электрическую нейтральность металлического комплекса.
Для удобства в настоящем тексте металлорганическими или металлическими комплексами называют соединения формулы (I), включающие также противоион Y.
Ионы 1,2,4-триазолий-5-илидена Z+ соответствуют общей формуле (II):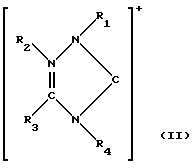
в которой R1, R2, R3 и R4, одинаковые или различные, обозначают:
нормальный или разветвленный алкильный радикал или циклоалкильный радикал,
арильный радикал,
алкильный радикал, содержащий один или несколько заместителей, таких как радикал арил, радикал алкокси, атом водорода, гидрофильную группу, такую как группы:
СООМ1, -SO3M1, -PO3M1, М1, представляющие собой неорганический или органический катионный остаток, выбираемый из протона, катионов щелочных или щелочноземельных металлов, аммониевых катионов - N(R)4, в формуле которых R, одинаковые или различные, обозначают атом водорода или радикал алкил с 1-4 атомами углерода;
N(R3)Ya, где R, одинаковые или различные, обозначают атом водорода или радикал алкил с 1-12 атомами углерода, a Ya обозначает неорганический или органический анион;
ОН;
радикал арил, арилалкил или циклоалкил, содержащий в цикле один или несколько заместителей, таких как радикал алкил, радикал алкокси, атом галогена, гидрофильная группа, такая как группы:
-COOM1, -SО3М1, -РО3М1, M1, представляющие собой неорганический или органический катионный остаток, выбираемый из протона, катионов щелочных или щелочноземельных металлов, аммониевых катионов;
-N(R)4, в формуле которых R, одинаковые или различные, обозначают атом водорода или радикал алкил с 1-12 атомами углерода;
-Н(R)3Yа, где R, одинаковые или различные, обозначают атом водорода или радикал алкил с 1-12 атомами углерода, а Ya обозначает неорганический или органический анион;
-ОН;
R3 обозначает атом водорода;
R1 и/или R4 могут также каждый обозначать органический лиганд, связанный с атомом азота иона 1,2,4-триазолий-5-илидена через алкиленовый или ариленовый радикал, причем этот лиганд может быть остатком фосфита, фосфонита, фосфинита, фосфина или остатком алифатического, циклоалифатического, ароматического или гетероциклического третичного амина, служащего в качестве лиганда L для металла М.
Названные выше органические лиганды могут быть, например, образованы из фенил- или алкилфосфитов, замещенных или не замещенных определенными выше заместителями, или фенил- или алкилфосфонитов, замещенных или не замещенных определенными выше заместителями, или фенил- или алкилфосфинитов, замещенных или не замещенных определенными выше заместителями, или фенил- или алкилфосфинов, замещенных или не замещенных определенными выше заместителями.
В этом случае ион 1,2,4-триазолий-5-илидена, замещенный определенными выше радикалами R1 и/или R4, представляет собой бидентатный или тридентатный лиганд.
L является ионным лигандом, таким как галогенид, цианид, или нейтральным лигандом, таким как окись углерода, изонитрил, фосфин, органический фосфит, фосфонат или фосфонит.
М является преимущественно металлом, выбранным из следующей группы металлов: кобальт, железо, рутений, родий, палладий, осмий, индий, платина, медь, серебро, золото, цинк, кадмий, ртуть.
Названные металлы могут иметь разные степени окисления, включая нулевую.
Анионы X- являются неорганическими или органическими анионами, такими, например, как галогениды, но выбираются предпочтительно из слабо координирующихся анионов по отношению к рассмотренному выше металлу М. Они образуют, главным образом, противоионы по отношению к ионам 1,2,4-триазолий-5-илидена.
В качестве не ограничивающих объема изобретения примеров таких слабо координирующихся анионов могут быть названы трифторметилсульфонат, тетрафторборат, гексафторфосфат, тетрахлорид алюминия, тетрабромид алюминия, тетрафторид алюминия, тетраиодид алюминия, тетрахлорид галлия, тетрабромид галлия, тетрафторид галлия, тетраиодид галлия.
Предметом настоящего изобретения является также использование двухкатионных гетероциклических соединений в качестве предшественников при получении металлоорганических комплексов общей формулы (I). Такие двухкатионные гетероциклические соединения соответствуют общей формуле (III):
в которой R1, R2, R3 и R4 имеют значения, приведенные выше для ионов 1,2,4-триазолий-5-илидена формулы (II);
- X- обозначает анион, такой как анионы, указанные для общей формулы (I).
Получение двухкатионных гетероциклических комплексов общей формулы (III) может быть осуществлено с использованием реакции соединения формулы XR2, в которой Х и R2 имеют указанные выше значения, с производным триазола, имеющим заместители XR2R1, R3 и R4. Синтез может также проводиться в несколько стадий, в каждой из которых производное триазола реагирует с соединением формулы XR1, ХR3 или XR4 в зависимости от того, какой заместитель предполагается вводить в формулу используемого для реакции триазола для получения двухкатионного гетероциклического соединения формулы (III). При этом могут быть использованы условия реакции, такие, которые описаны в статье T.J. Curphey и K.S. Prasad, Journal of Org. Chem., 1972, 37, 2259.
Получение металлоорганических комплексов формулы (I) может быть осуществлено реакцией двухкатионного гетероциклического соединения общей формулы (III) с соединением металла М в присутствии неорганического или органического основания. Таким основанием может быть ассоциированный анион соединения металла М либо независимо добавляться в реакционную среду. Эту реакцию можно проводить в жидкой среде, в общем случае добавляя соединение металла М, и в случае необходимости неорганическое или органическое основание, в раствор или в суспензию соединения (III). Разумеется, порядок ввода различных реагентов может меняться. Реакцию можно проводить при комнатной температуре или, преимущественно, при температуре от 25 до, например, 150oС. Удобно проводить синтез при температуре кипения жидкости, в которой этот синтез осуществляется. Отделение комплекса формулы (I) может быть осуществлено с использованием обычных в химической практике способов, например фильтрации, центрифугирования или экстракции. Структура комплексов формулы (I) и двухкатионные гетероциклические соединения формулы (III) обычно определяется с помощью ядерного магнитного резонанса (ЯМР), инфракрасной спектроскопии и дифракции рентгеновских лучей. Металлоорганические комплексы формулы (I) могут служить катализаторами в многочисленных химических реакциях.
Большинство металлоорганических комплексов формулы (I), так же, как и двухкатионные гетероциклические соединения формулы (III), плохо или совсем не растворимы в большинстве неполярных или полярных органических растворителей, таких как алканы, циклоалканы, галогеналканы, ароматические или алкилароматические углеводороды и простые эфиры. Напротив, эти соединения растворимы в полярных растворителях. В частности, двухкатионные соединения растворимы в тетрагидрофуране, диметилсульфоксиде (ДМСО), нитрилах (например, в ацетонитриле) и воде. Таким образом, металлоорганические комплексы настоящего изобретения растворимы, в частности, в нитрилах (например, в ацетонитриле), ДМСО и воде. Эти свойства облегчают разделение столь различных соединений, в частности, с использованием экстракции жидкость/жидкость. С другой стороны, такие свойства позволяют проведение катализа в двухфазной среде.
В качестве не ограничивающих объема изобретения примеров таких реакций можно назвать гидросилилирование алкенов или алкинов, в частности, в присутствии комплексов рутения, гидросилилирование кетонов в присутствии комплексов рутения или родия, реакцию Хека в присутствии комплексов палладия, гидрирование олефинов, альдегидов, кислот, енамидов и нитроароматических соединений в присутствии комплексов рутения, родия, платины или палладия, гидроформилирование и гидрокарбонилирование олефинов в присутствии комплексов родия, гидроцианирование олефинов в присутствии комплексов никеля, синтез фурана в присутствии комплексов рутения, диспропорционирование олефинов в присутствии комплексов рутения и полимеризацию акрилатов в присутствии комплексов никеля.
ПРИМЕРЫ СИНТЕЗОВ ПРЕДШЕСТВЕННИКОВ СОЕДИНЕНИЙ ФОРМУЛЫ (III)
Пример 1. Синтез соединения (IIIa):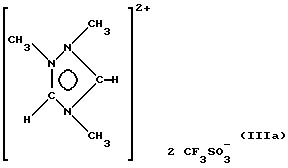
Используя последовательность операций, описанную в J. Org. Chem., 1972, 37, р. 2259, 1Н-1,2,4-метилтриазол дважды метилируют (в положениях 2 и 4 цикла) метиловым эфиром трифторметансульфокислоты в 1,2-дихлорэтане при кипении и перемешивании.
Образовавшийся бурый осадок отфильтровывают, затем промывают 1,2-дихлорэтаном до получения белого порошка. Полученное твердое вещество (IIIa) имеет температуру плавления 160-162oС.
Соединение имеет следующие характеристики
- ЯМР 1H (ДМСО-d6): δ 4,22 (с, 3Н, СН3N), 4,50 (с, 6Н, CH3N), 10,79 (с, 2Н, Нцикл).
- ЯМР 13С (Н) (СD3СN): δ 38,67 (с, СН3N), 38,87 (с, 2CH3N), 120,35 (кв, 1JCF=320, 1 Гц, СF3), 147,72 (с, 2Cцикл).
Пример 2. Синтез соединения (IIIb):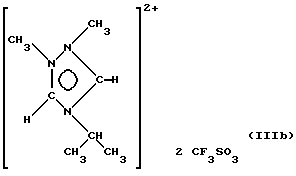
Синтез проводят в две стадии. Прежде всего вводят в положение 4 изопропильную группу (радикал R4) путем добавления стехиометрического количества 1Н-1,2,4-метилтриазола к раствору изопропилового эфира трифторметансульфокислоты в 1,2-дихлорэтане (кипячение при перемешивании в течение 3 час). Получают соединение в виде желтого масла, имеющее следующую формулу:
с выходом 91%.
К раствору 5 г (18 ммоль) этого соединения в 20 мл 1,2-дихлорэтана добавляют 2,5 мл метилового эфира трифторметансульфокислоты (22 ммоль) и кипятят при перемешивании в течение 24 час. Образовавшийся бурый осадок отфильтровывают и затем промывают 1,2-дихлорэтаном до получения белого порошка.
Полученное твердое вещество (IIIb) имеет температуру плавления 163-165oС, а его количество соответствует выходу 73% в расчете на взятое промежуточное соединение.
Соединение имеет следующие характеристики:
- ЯМР 1H (СD3СN): δ 1,65 (д, 3JHH=6,58 Гц, 6Н, СН3СН), 4,34 (с, 3Н, CH3N), 5,03 (септ, 3JHH=6,58 Гц, 1Н, [СН3]2СНN), 10,22 (с, 2Н, Нцикл.).
- ЯМР 13С (СD3СN): δ 21,51 (с, СН3СН), 38,71 (с, СН3N), 58,88 (с, [СН3] 2СНN), 120,35 (кв, 1JCF=320, 1 Гц, СF3), 145,22 (с, 2Сцикл.).
Пример 3. Синтез соединения (IIIc):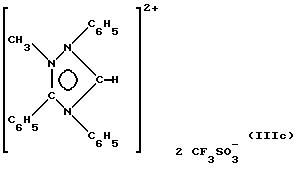
Синтез проводят в две стадии. Вначале соединение следующей формулы:
получают по методу, описанному в J. Prakt. Chem., 1988, 330, 3, 325.
Это соединение кипятят в метилтрифторметилсульфонате при перемешивании в течение 4 дней. Образовавшийся бурый осадок отфильтровывают и затем промывают 1,2-дихлорэтаном до получения белого порошка. Выход полученного твердого вещества (IIIc) составляет 50% в расчете на соединение, использованное для реакции во второй стадии.
Продукт имеет следующие характеристики:
- ЯМР 1H (CD3CN): δ 4,22 (с, 3Н, СН3N), 7,4-8,4 (массив, Н фенила), 10,34 (с, 1Н, Нцикл.).
Пример 4. Синтез соединения (IIId):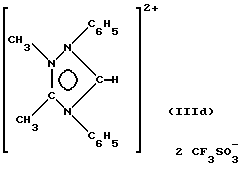
Синтез проводится в две стадии. В начале соединение следующей формулы: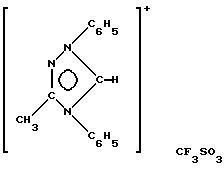
получают по методу, описанному в J. Prakt. Chem., 1988, 330, 3, 325.
Полученное соединение кипятят в 1,2-дихлорэтане с 3 эквивалентами метилтрифторметилсульфоната при перемешивании в течение 2 дней. Образовавшийся бурый осадок отфильтровывают и затем промывают 1,2-дихлорэтаном до получения белого порошка. Выход полученного твердого вещества (IIId) составляет 69% в расчете на соединение, использованное для реакции во второй стадии, а температура плавления продукта 190,5-191,3oС.
Соединение имеет следующие характеристики:
- ЯМР 1H (СD3СN): δ 3,04 (с, 3Н, СН3), 4,19 (с, 3Н, СН3N), 7,8-8,1 (массив, 10Н, 1Н фенила), 10,51 (с, 1H, Hцикл.);
- ЯМР 13C (СD3СN): δ 12, 31 (с, CH3C), 38, 04 (с, CH3N), 126,70 (с, 2СН фенила), 128,02 (с, С фенила), 128,49 (с, 2СН фенила), 130,07 (с, С фенила), 131,56 (с, 2СН фенила), 131,83 (с, 2СН фенила), 134,04 (с, 1СН фенила), 135,88 (с, 1СН фенила), 120,35 (кв, 1JCF=320, 1 Гц, СF3), 145, 58 (с, СНцикл.), 157,66 (с, Сцикл. СН3).
Спаренный спектр ПМР дает для СН триазольного цикла константу расщепления 1JCH=240 Гц.
Пример 5. Синтез соединения (IIIе):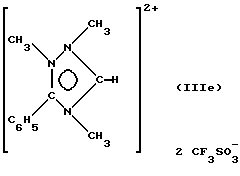
Синтез проводят в две стадии. Вначале соединение следующей формулы: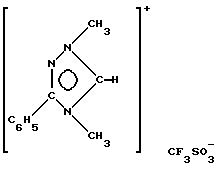
получают по методу, описанному в J. Prakt. Chem., 1988, 330, 3, 325.
Полученное соединение кипятят в 1,2-дихлорэтане с 3 эквивалентами метилтрифторметилсульфоната при перемешивании в течение 2 дней. Образовавшийся бурый осадок отфильтровывают и затем промывают 1,2-дихлорэтаном до получения белого порошка. Выход полученного твердого вещества (IIIе) составляет 71% в расчете на соединение, использованное для реакции на второй стадии, а температура плавления продукта 180oС.
Соединение имеет следующие характеристики:
- ЯМР 1H (CD3CN): δ 4, 08 (с, 3Н, СН3N), 4, 20 (с, 3Н, СН3N), 4, 46 (с, 3Н, СН3N), 7,8-8,1 (массив, 10Н, 5Н фенила), 10,16 (с, 1Н, Нцикл.);
- ЯМР 13С (CD3CN): δ 37, 88 (с, СН3N), 38,36 (с, СН3N), 39,42 (с, СН3N), 130,78 (с, С фенила), 131,97 (с, 2СН фенила), 132,15 (с, 2СН фенила), 137,35 (с, СН фенила), 131, 83 (с, 2СН фенила), 120,35 (кв, 1JCF=320, 1 Гц, СF3), 147, 35 (с, СНцикл.), 156, 48 (с, Сцикл.).
Пример 6. Синтез соединения (IIIf)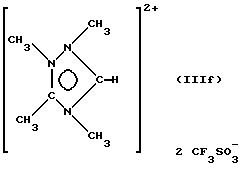
Синтез проводят в две стадии. Вначале соединение следующей формулы: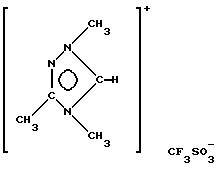
получают по методу, описанному в J. Prakt. Chem., 1988, 330, 3, 325.
Полученное соединение кипятят в 1,2-дихлорэтане с 3 эквивалентами метилтрифторметилсульфоната при перемешивании в течение 2 дней. Образовавшийся бурый осадок отфильтровывают и затем промывают 1,2-дихлорэтаном до получения белого порошка. Выход полученного твердого вещества (IIIf) составляет 95% в расчете на соединение, использованное для реакции на второй стадии, а температура плавления продукта 194,4oС.
Соединение имеет следующие характеристики:
- ЯМР 1H (Ацетон d6): δ 3,35 (с, 3Н, СН3C), 4,46 (с, 3Н, СН3N), 4,69 (с, 3Н, CH3N), 4,77 (с, 3Н, СН3N), 10,77 (С, 1Н, Нцикл.);
- ЯМР 13С (Ацетон d6): δ 10,53 (с, СН3C), 35, 91 (с, СН3N), 36,26 (с, СН3N), 37,99 (с, СН3N), 120,35 (кв, 1JCF= 320,1 Гц, СF3), 145,35 (с, СНцикл.), 157,31 (с, Cцикл. CН3).
ПРИМЕРЫ СИНТЕЗА МЕТАЛЛООРГАНИЧЕСКИХ КОМПЛЕКСОВ ФОРМУЛЫ (I)
Пример 7. Синтез соединения (Iа) с Аg(I):
К суспензии 1 г полученного в примере 1 двухкатионного соединения (IIIa) в 20 мл тетрагидрофурана добавляют 0,4 г (2,4 ммоль) ацетата серебра. Смесь кипятят в течение 2 час при перемешивании. Образовавшееся не смешивающееся с ТГФ бурое масло промывают несколько раз 10 мл ТГФ. После упаривания растворителя получают чувствительное к свету твердое вещество каштанового цвета (выход 82% а в расчете на двухкатионное соединение (IIIa)).
Полученный комплекс имеет следующие характеристики:
- ЯМР 1Н (CD3CN): δ 4,01 (с, 3Н, NCH3), 4,19 (с, 3Н, CH3N-NCH3), 4,22 (s, 3Н, CH3N-NCH3), 9,72 (с, 1Н, СН);
- ЯМР 13С (CD3CN): δ 37,2 (NCH3), 38,5 (NCH3), 38,6 (NCH3), 121,1 (кв, 1JCF=320,1 Гц, CF3), 144,8 (СН), 189,2 (САg).
Пример 8. Синтез соединения (Ib) с Нg (II):
К суспензии 0,43 г полученного в примере 5 двухкатионного соединения (IIIe) в 20 мл тетрагидрофурана добавляют 0,16 г диацетата ртути (предварительно высушенного в вакууме в течение 12 час при 50oС) и 1 мл диметилсульфоксида. Смесь перемешивают 24 часа при комнатной температуре. Образуется бурый осадок, растворимый только в очень полярных растворителителях. Полученное твердое вещество несколько раз промывают ТГФ для полного удаления следов уксусной кислоты. Полученный таким образом комплекс перекристаллизовывают путем медленной диффузии эфира в метанольный раствор этого комплекса. Перекристаллизованный комплекс (Ib) имеет температуру плавления 85,4-87oС. Выход составляет 86% в расчете на двухкатионное соединение (IIIe).
Полученный комплекс имеет следующие характеристики:
- ЯМР 1Н (CD3OD): δ 4, 70 (с, 12Н, NCH3, 4JH-Hg=12,8), 4,29 (с, 6Н, CH3N, 4JH-Hg=8,5 Гц), 7,9-8,2 (массив, 10Н, Н фенила);
- ЯМР 13С (CD3OD): δ 38,79 (СН3N-NCH3), 41,75 (NCH3), 121,1 (кв, 1JCF= 320,1 Гц, CF3), 156, 88 (C-Ph, (3J+2J)c-Hg=86 Гц), 183,78 (СНg, J
Структура комплекса была также установлена с помощью дифракции рентгеновских лучей.
Пример 9. Синтез соединения (1с) с Ni(II)
К суспензии 0,442 г диацетата никеля и 0,75 г иодида натрия в 50 мл ТГФ добавляют 2,4 г полученного в примере 5 двухкатионного соединения (IIIe). Смесь кипятят 2 часа при перемешивании. Образовавшийся окрашенный осадок отфильтровывают и несколько раз промывают ТГФ. Полученный таким образом комплекс перекристаллизовывают из смеси ацетон/эфир при -30oС. Перекристаллизованный комплекс (1с) имеет красную окраску и температуру плавления 310,7oС (разложение: кристаллы чернеют). Выход составляет 85% в расчете на двухкатионное соединение (IIIе).
Полученный комплекс имеет следующие характеристики:
- ЯМР 1H (Ацетон-d6): δ 7,8-8,0 (уширенный, 10Н, Н фенила), 4,88-4,84 (2s, 6H, NCH3), 4,54-4,49 (2s, 6H, CH3N), 4,42-4,41 (2s, 6H, CH3N);
- ЯМР 13C (CD3OD): δ 37,0 (CH3N), 37,9 (СН3N), 38,4 (CH3N), 121,1 (кв, 1JCF= 320,1 Гц, CF3), 130, 5-130, 8-134, 8 (С фенила), 153,4 (C-Ph), 188,2 (C-Ni).
Структура комплекса была также установлена с помощью дифракции рентгеновских лучей.
Пример 10. Синтез соединения (Id) с Ni(II)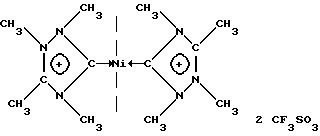
К суспензии 0,090 г диацетата никеля и 0,15 г иодида натрия в 25 мл ТГФ добавляют 0,425 г полученного в примере 6 двухкатионного соединения (IIIf). Смесь кипятят 2 часа при перемешивании. Образовавшийся окрашенный осадок отфильтровывают и несколько раз промывают ТГФ. Полученный таким образом комплекс перекристаллизовывают из смеси ацетон/эфир при -30oС. Перекристаллизованный комплекс (Id) имеет красную окраску и температуру плавления 300-305oС (разложение: кристаллы чернеют). Выход составляет 79% в расчете на двухкатионное соединение (IIIf).
Полученный комплекс имеет следующие характеристики:
- ЯМР 1H (Ацетон-d6): δ 4,88-4,84 (2с, 6Н, NCH3), 4,54-4,49 (2с, 6Н, СН3N), 4,42-4,41 (2с, 6Н, CH3N), 2,63 (с, 6Н, С-СН3);
- ЯМР 13С (СD3OD): δ 13,86 (С-СN3), 36,1 (СН3N), 37,6 (CH3N), 38,5 (СН3N), 121,1 (кв, 1JCF=320,1 Гц, СF3), 154,8 (С-Ме), 187,6 (C-Ni).
Структура комплекса была также установлена с помощью дифракции рентгеновских лучей.
Пример 11. Синтез соединения (Ie) с Ni(II)
К суспензии 0,200 г диацетата никеля и 0,34 г иодида натрия в 30 мл ТГФ добавляют 0,935 г полученного в примере 1 двухкатионного соединения (IIIa). Смесь кипятят 2 часа при перемешивании. Образовавшийся окрашенный осадок отфильтровывают и несколько раз промывают ТГФ. Полученный таким образом комплекс перекристаллизовывают путем медленной диффузии эфира в раствор этого комплекса в ацетонитриле и затем из смеси ацетон/эфир при -30oС. Перекристаллизованный комплекс (Ie) имеет красную окраску. Выход составляет 70% в расчете на двухкатионное соединение (IIIa).
Полученный комплекс имеет следующие характеристики:
- ЯМР 1H (Ацетон-d6): δ 4,38-4,35 (2с, 6Н, CH3N), 4,68-4,65 (2с, 6Н, CH3N), 4,99-4,96 (2с, 6Н, NCH3), 9,32 (с, 2Н, СН).
Пример 12. Синтез соединения (If) с Pd(II)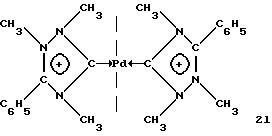
К суспензии 0,112 г диацетата палладия и 0,30 г иодида натрия в 60 мл ТГФ добавляют 0,472 г полученного в примере 5 двухкатионного соединения (IIIе). Смесь кипятят 2 часа при перемешивании. Образовавшийся окрашенный осадок отфильтровывают и несколько раз промывают эфиром. Полученный таким образом комплекс перекристаллизовывают из смеси ацетон/эфир при -30oС. Перекристаллизованный комплекс (If) представляет собой желтые кристаллы с температурой плавления 211-213oС (разложение: кристаллы буреют). В процессе реакции все трифторметилсульфонатные анионы замещаются иодиданионами. Выход составляет 51% в расчете на двухкатионное соединение (IIIe).
Полученный комплекс имеет следующие характеристики:
- ЯМР 1H (ДМСО-d6): δ 7,8-8,1 (укруп., 10Н, Н фенила), 4,49-4,53 (2с, 6Н, NСН3), 4,21 (с, 6Н, СН3N), 4,10-4,13 (2с, 6Н, СН3N);
- ЯМР 13С (ДМСО-d6); δ 37,2 (СН3N), 38,3 (СН3N), 39,9 (СН3N), 130,1-130,9-134,5 (С фенила), 152,4 (C-Ph), 174,5 (C-Pd).
Структура комплекса установлена также с помощью дифракции рентгеновских лучей.
Пример 13. Синтез соединения (Ig) с Pd(II):
К суспензии 0,112 г диацетата палладия и 0,30 г иодида натрия в 60 мл ТГФ добавляют 0,425 г полученного в примере 6 двухкатионного соединения (IIIf). Смесь кипятят 2 часа при перемешивании. Образовавшийся окрашенный осадок отфильтровывают и несколько раз промывают эфиром. Полученный таким образом комплекс перекристаллизовывают из смеси ацетон/эфир при -30oС. Перекристаллизованный комплекс (1g) имеет красную окраску и температуру плавления 206-212oС (разложение: кристаллы буреют). В процессе реакции все трифторметилсульфонатные анионы были замещены иодид-анионами. Выход составляет 60% в расчете на двухкатионное соединение (IIIf).
Полученный комплекс имеет следующие характеристики:
- ЯМР 1H (ДМСО-d6): δ 4,41-4,40 (2с, 6Н, NCН3), 4,29 (с, 6Н, СН3N), 4,16-4,15 (2с, 6Н, СН3N), 2,95 (6Н, С-СН3).
Пример 14. Синтез соединения (Ih) с Ni(0)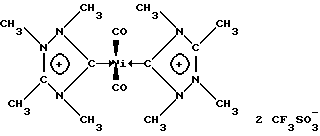
Метод синтеза А
1 мл тетракарбонила никеля разбавляют в 40 мл безводного и обезгаженного ацетонитрила. К полученному раствору добавляют 360 мкл пиридина и 660 мкл триэтиламина. Раствор 2,0 г полученного в примере 6 двухкатионного соединения (IIIf) в 60 мл безводного и обезгаженного ацетонитрила прибавляют по каплям с помощью капельной воронки. Наблюдается выделение газа и раствор окрашивается в желтый цвет. После добавления всего количества раствора продолжают перемешивание в течение еще 1 часа. Объем реакционного раствора после этого уменьшают на две трети упариванием растворителя в вакууме, после чего добавляют 200 мл обезгаженного эфира. После этого образуется осадок комплекса (Ih), который отфильтровывают и несколько раз промывают эфиром. Полученный таким образом комплекс перекристаллизовывают из смеси ацетон/эфир при -30oС. Комплекс (Ih) представляет собой желтые кристаллы, температуру плавления которых невозможно определить точно (разложение: кристаллы буреют). Выход составляет 26% в расчете на двухкатионное соединение (IIIf).
Полученный комплекс имеет следующие характеристики:
- ЯМР 1H (ДМСО-d6): δ 4,00 (с, 6Н, NСН3), 3,99 (с, 6Н, СН3N), 3,78 (с, 6Н, СН3N), 2,72(6Н, С-СН3).
В инфракрасном спектре имеются полосы при 1982 см-1 и 1906 см-1 (СО).
Структура комплекса установлена также с помощью дифракции рентгеновских лучей.
С помощью элементного анализа найдено:
- 28,99% С (теория 28,89%)
- 3,36% Н (теория 3,63%)
- 12,39% N (теория 12,62%).
Метод синтеза В
К раствору 0,2 г полученного в примере 10 металлоорганического комплекса (Id) в 10 мл безводного и обезгаженного ацетонитрила добавляют 150 мг активированного порошка металлического цинка (10 эквивалентов). Раствор помещают в атмосферу окиси углерода. Реакция начинается в тот момент, когда начинают перемешивание. Раствор становится желтым, затем его фильтруют с помощью трубочки, после чего обрабатывают так же, как в методе А (добавляя эфир для осаждения металлоорганического комплекса). Выход составляет 48% в расчете на использованный для реакции металлоорганический комплекс (Id). Производят те же анализы и получают те же характеристики, как в методе А. Полученные результаты совпадают.
Пример 15. Синтез соединения (Ij) с Rh(I)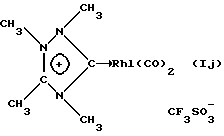
К суспензии 0,456 г полученного в примере 6 двухкатионного соединения (IIIf) и 0,16 г NaI в 40 мл ТГФ добавляют раствор 0,277 г ацетилацетоната дикарбонилродия в 10 мл ТГФ. Перемешивают в течение 2 дней при 50oС. После упаривания растворителя и нескольких промывок эфиром получают твердое вещество бурого цвета. Выход составляет 70% в расчете на двухкатионное соединение (IIIf).
Полученный комплекс имеет следующие характеристики:
- ЯМР 1Н (ДМСО-d6): δ 4,47 (с, 3Н, NCH3), 4,28 (с, 3Н, CH3N), 4,20 (с, 3Н, CH3N), 2,96 (с, 3Н, С-СН3);
- ЯМР 13С (ДМСО-d6): δ 10,5 (с, С-СН3), 35,2 (с, NCH3), 36,8 (с, CH3N), 37,9 (c, CH3N), 154,2 (с, С-СН3), 183,0 (д, 1J (Rh-C)=82,9 Гц, СО), 188, 1 (д, 1J(Rh-C)=42,2 Гц, С карбеновый).
В ИК-спектре имеется полоса при 1975 см-1 (СО).
Пример 16. Синтез соединения (Ik) с Rh(I)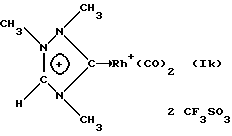
К суспензии 0,16 г полученного в примере 1 двухкатионного соединения (IIIa) в 10 мл ТГФ добавляют раствор 0,200 г ацетилацетоната дикарбонилродия в 10 мл ТГФ. Смесь перемешивают в течение 15 час при 50oС. Образовавшийся бурый твердый осадок несколько раз промывают эфиром. Выход комплекса (Ik) составляет 67% в расчете на двухкатионное соединение (IIIa).
Полученный комплекс имеет следующие характеристики:
- ЯМР 1H (ДМСО-d6): δ 4,20 (с, 3Н, NCH3), 4,22 (с, 3Н, CH3N), 4,25 (с, 3Н, CH3N), 9,66 (с, 1Н, СН);
- ЯМР 13С (ДМСО-d6): δ 38,6 (с, NCH3), 38,7 (с, NCH3), 39,1 (с, CH3N), 37,9 (с, CH3N), 121,1 (кв, 1JCF=320,1 Гц, СF3), 145,5 (с, СН), 186,1 (д, 1J(Rh-C)=76 Гц, СО), 187,9 (д, 1J(Rh-C)=43, 3 Гц, С карбеновый).
В ИК-спектре имеются полосы при 2029 (и) см-1 и 1985 (ср) см-1 (СО).
Пример 17. Катализ гидроформилирования стирола соединением (Ij) с Rh(I)
Реакцию гидроформилирования стирола проводят в 100-мл реакторе из нержавеющей стали с двойной оболочкой, позволяющей осуществление нагрева с помощью циркулирующего масла, при регулируемой термостатом температуре. Крышка реактора снабжена впускным вентилем или вентилем для выпуска газов под давлением, прецизионным манометром, предохранительным клапаном и шаровым затвором для переноса растворов с помощью шприца. Внутри автоклава находится тефлоновая полость с намагниченным стержнем, служащим для перемешивания реагирующих веществ.
Полученный в примере 15 комплекс (Ij) с Rh(I) (40 мг) загружают в тефлоновую полость вместе со 100 мг трифенилфосфина (5 эквивалентов в расчете на катализатор). Автоклав герметизируют и трижды продувают аргоном. После этого загружают 15 мл тетрагидрофурана, 5 мл стирола с 60 мг триэтиламина (4 эквивалента в расчете на катализатор) и устанавливают давление окиси углерода (15 бар) и водорода (15 бар). Содержимое автоклава нагревают при 60oС при перемешивании магнитной мешалкой. После 4 час реакции при этой температуре автоклав быстро охлаждают в смеси ацетона с жидким азотом и в течение 1 часа сбрасывают давление. Пробу реакционной смеси анализируют с помощью газовой хроматографии.
Получают следующие результаты:
- степень конверсии стирола: 95%
- селективность по альдегидам: 97%
- отношение разветвленный альдегид/линейный альдегид: 95/5
- частота оборота катализатора: 75 ч-1 (рассчитанная как среднее по времени реакции с использованием одинакового для всех продуктов коэффициента выходного сигнала газовой хроматографии).
Пример 18. Катализ гидроформилирования стирола соединением (Ik) с Rh(I)
Повторяют пример 17 с 40 мг полученного в примере 16 комплекса (Ik) без использования трифенилфосфина.
После 3 час реакции при 80oС автоклав быстро охлаждают в смеси ацетона с жидким азотом и в течение 1 часа сбрасывают давление. Пробу реакционной смеси анализируют с помощью газовой хроматографии.
Получают следующие результаты:
- степень конверсии стирола: 96%
- селективность по альдегидам: 100%
- отношение разветвленный альдегид/линейный альдегид: 25/75
- частота оборота катализатора: 79 ч-1 (рассчитанная как среднее по времени реакции с использованием одинакового для всех продуктов коэффициента выходного сигнала газовой хроматографии).
Описываются металлоорганические комплексы формулы I: [(Z+X-)mMLn]Y, в которой Z+ обозначает ион 1,2,4-триазолий-5-илидена формулы (II), где R1, R2 и R4 обозначают нормальный С1-С4 алкильный радикал; R3 обозначает водород, нормальный С1-С4 алкильный радикал или фенил; L обозначает ионный или нейтральный лиганд; М представляет собой металл, выбираемый из группы, состоящей из серебра, ртути, никеля, палладия или родия; n означает целое число от 0 до 2; m обозначает целое число от 1 до 3; Х- обозначает слабо координирующие анионы и представляет собой противоионы для ионов 1,2,4-триазолий-5-илидена; Y обозначает анион, обеспечивающий электрическую нейтральность металлического комплекса, способ их получения, катализатор гидроформилирования на основе указанных комплексов и промежуточный продукт формулы (III). 4 с. и 4 з.п.ф-лы.
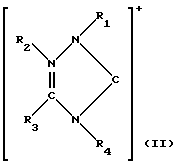

[(Z+X-)mMLn]Y,
в которой Z+ обозначает ион 1,2,4-триазолий-5-илидена формулы II
где R1, R2, и R4 обозначают нормальный С1-С4 алкильный радикал;
R3 обозначает водород, нормальный С1-С4 алкильный радикал или фенил;
L обозначает ионный или нейтральный лиганд;
М представляет собой металл, выбираемый из группы, состоящей из серебра, ртути, никеля, палладия или родия, n означает целое число от 0 до 2, m обозначает целое число от 1 до 3;
X- обозначает слабо координирующие анионы и представляют собой противоионы для ионов 1,2,4-триазолий-5-илидена;
Y обозначает анион, обеспечивающий электрическую нейтральность металлического комплекса.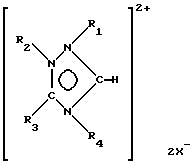
в которой R1, R2, R3 и R4 имеют значения, приведенные выше для ионов 1,2,4-триазолий-5-илидена формулы II;
X- обозначает анион, такой как анионы, указанные для общей формулы I,
вводят в реакцию с соединением металла M в виде раствора или суспензии при комнатной температуре или, предпочтительно, при температуре от 25 до 150oС.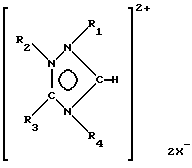
где R1, R2, и R4 обозначают нормальный С1-С4 алкильный радикал;
R3 обозначает водород, нормальный С1-С4 алкильный радикал или фенил;
L обозначает ионный или нейтральный лиганд;
М представляет собой металл, выбираемый из группы, состоящей из серебра, ртути, никеля, палладия или родия, n означает целое число от 0 до 2, m обозначает целое число от 1 до 3;
X- обозначает слабо координирующие анионы и представляют собой противоионы для ионов 1,2,4-триазолий-5-илидена;
Y обозначает анион, обеспечивающий электрическую нейтральность металлического комплекса.
| Бесколесный шариковый ход для железнодорожных вагонов | 1917 |
|
SU97A1 |
| ЕР 0721953 А, 17.07.1996 | |||
| Способ концентрирования электро-лиТичЕСКОй щЕлОчи | 1977 |
|
SU798041A1 |
| ЕР 0721951 А, 27.12.1995 | |||
| СПОСОБ ПОЛУЧЕНИЯ ДИКАРБОНИЛЬНЫХ КОМПЛЕКСОВ РОДИЯ (I) С БИДЕНТАТНЫМИ ЛИГАНДАМИ | 1992 |
|
RU2049790C1 |
| КОМПЛЕКСЫ МЕДИ (II) И НИКЕЛЯ (II) С 1-(БЕТА-ОКСИЭТИЛ)-2-МЕТИЛ-5-НИТРОИМИДАЗОЛОМ | 1997 |
|
RU2098421C1 |
Авторы
Даты
2002-08-27—Публикация
1999-05-11—Подача