Изобретение относится к области медицины, а именно к препаратам для лечения болезней суставов.
Болезнями суставов страдают около 70% населения старше 45 лет. Они выражаются в виде болей в суставе, усиливающихся при движении, ощущении скованности. Воспалительные процессы сопровождаются припухлостью, изменением формы и очертаний суставов.
Кроме того, при артрологических заболеваниях суставов постепенно разрушается хрящ, покрывающий суставные поверхности, а также костная ткань и внутренняя поверхность суставной сумки.
В настоящее время широкое распространение в мировой медицинской практике для лечения болезней суставов (артритов, артрозов, остеохондроза и т.п.) получили препараты на основе сахаридов (хондроитинсульфат, соли глюкозамина), в основном в форме таблеток, капсул и в виде инъекций. Лечение этими препаратами не только уменьшает воспаление и боли в суставах, но и продуцирует восстановление разрушенной хрящевой ткани [Насонов Е.Л. Клинические рекомендации и алгоритмы для практикующих врачей, Ревматология, М., 2004; K.Pavelka, Archives Internal Medicine, №10, 2002, №7, 2003].
Наиболее близким к заявляемому по составу является инъекционный препарат, содержащий в качестве активного ингредиента сахарид-глюкозамина гидрохлорид (кислый сахарид с рН водного раствора 1,2-2,5), нейтрализующее средство - этилендиамин, местно-анестезирующее средство - тримекаин и вспомогательные вещества [патент РФ №2118156]. Его недостатки состоят в следующем:
- препарат представляет собой двухкомпонентный раствор, содержащий ампулу с раствором глюкозамина гидрохлорида и ампулу с раствором этилендиамина. Приготовление препарата для введения больному заключается в смешивании содержимого двух ампул в шприце непосредственно перед введением инъекции;
- нейтрализующий агент - этилендиамин - жидкость с температурой кипения 116°С и, следовательно, не может быть использован для приготовления монокомпонентного препарата (ГА + нейтрализующий агент) в виде лиофилизата;
- применение этилендиамина в препарате в сравнительно высокой концентрации (более 3 мас.% по отношению к глюкозамину) требует дополнительного введения в состав препарата местно-анестезирующего средства - тримекаина, что, в свою очередь, обуславливает ряд побочных нежелательных эффектов.
Задача, решаемая предлагаемым изобретением, - разработка монокомпонентного инъекционного препарата для лечения болезней суставов в виде лиофилизата, сочетающего хондропротективное действие с высокими фармакокинетическими показателями и биодоступностью с исключением недостатков прототипа.
Технический результат от использования изобретения заключается в повышении удельной концентрации активного ингредиента в составе препарата и, как следствие, увеличении скорости и эффективности диффузии активной субстанции в зону сустава.
Для достижения поставленного результата предлагается средство для лечения болезней суставов, представляющее собой лиофилизат, содержащий сахарид - глюкозамина соль и нейтрализующий агент алифатический амин - трометамол при следующем соотношении компонентов, мас.%:
глюкозамина соль - 98,0-99,9
трометамол - 0,1-2,0
В качестве соли глюкозамина могут быть использованы известные фармацевтические субстанции (зарегистрированные в РФ или импортные, соответствующие требованиям Фармакопеи США 27 издания): гидрохлорид глюкозамина, натриевые или калиевые соли сульфата глюкозамина. Предпочтительным является использование динатриевой соли сульфата глюкозамина и гидрохлорида глюкозамина. Низкая молекулярная масса этих сахаридов (573,3 и 215,0 Дальтон, соответственно) и их высокая фармакологическая активность [Е.С.Цветкова, Научно-практическая ревматология, №2, 2003] в лечении болезней суставов обеспечивают создание эффективных хондропротективных препаратов.
Нейтрализующий агент - трисамин (торговое название), зарегистрирован в качестве фармацевтической субстанции в России за №78/702/1. Международное название - трометамол. Химическое название -2-Амино-2-(гидроксиметил)-1,3-пропандиол
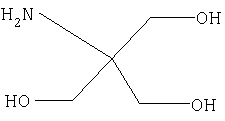
Количество добавляемого к глюкозамину трисамина определяется кислотностью коммерческого образца используемой соли и устанавливается в каждом опыте конкретно до получения перед розливом исходного раствора с физиологическим значением рН 5,0-8,0.
Экспериментально установлено, что введение в состав инъекционного препарата антацидного средства системного действия - трисамина, обладающего буферными свойствами и местно-анестезирующим действием, существенно ускоряет транспорт активного вещества в кровяное русло живого организма. Трисамин, проникая через клеточные мембраны, повышает транспорт, биодоступность и удельное содержание глюкозамина в зоне сустава. Указанное увеличение биодоступности активного ингредиента и усиление противовоспалительных свойств препарата связано также со способностью супрамолекулярной структуры, созданной в заявленной фармацевтической композиции, изменять состояние среды в микроокружении сахарида.
Фармакологическая группа - 8.8. Корректор метаболизма костной и хрящевой ткани (Регистр лекарственных средств России, 2005 г. издания).
Технология производства препарата осуществляется известными методами и заключается в растворении активных ингредиентов в воде, стерильной фильтрации с последующей расфасовкой в ампулы и лиофильной сушкой раствора.
Контроль количественного содержания активных ингредиентов (глюкозамин, трисамин) в препаратах проводится по известным методикам, принятым для аналогичных лекформ, зарегистрированных в РФ и содержащих активные ингредиенты (спектрофотометрически, нефелометрическое титрование).
Пример 1. 100 г глюкозамина сульфата ×2NaCl растворяют при температуре не выше 40°С в 400 мл дистиллированной воды, добавляют при перемешивании около 0,5 г трометамола (до рН 6,0-7,5). Раствор стерильно фильтруют через стерилизующие фильтры 0,22 мкм и разливают в стерильные ампулы по 2 мл. Режим лиофильной сушки препарата включает его замораживание при -80°С и высушивание в вакууме при комнатной температуре в течение 10 часов. В конечном препарате в 1 ампуле содержится 400 мг глюкозамина сульфата ×2NaCl и 2,0 мг (0,5 мас.%) трисамина.
Пример 2. 100 г глюкозамина сульфата ×2КСl растворяют при температуре не выше 40°С в 400 мл дистиллированной воды, добавляют при перемешивании около 0,1 г трометамола (до рН 6,0-7,5). Раствор стерильно фильтруют через стерилизующие фильтры 0,22 мкм и разливают в стерильные ампулы по 2 мл. Режим лиофилизации по примеру 1. В конечном препарате в 1 ампуле содержится 400 мг глюкозамина сульфата ×2КСl и 2,0 мг трисамина (0,1 мас.%).
Пример 3. 100 г глюкозамина гидрохлорида растворяют при температуре не выше 40°С в 400 мл дистиллированной воды, добавляют при перемешивании около 2 г трометамола (до рН 6,0-7,5). Раствор стерильно фильтруют через стерилизующие фильтры 0,22 мкм и разливают в стерильные ампулы по 2 мл. Режим лиофилизации по примеру 1. В конечном препарате в 1 ампуле содержится 400 мг глюкозамина сульфата ×2КСl и 8,0 мг трисамина (2,0 мас.%).
Эффективность действия препарата изучали на моделях посттравматического остеоартроза, коллапса ушных раковин кроликов и асептического воспаления конечности крыс.
При субхондральных дефектах головки бедренной кости крыс, вызванных хирургическим повреждением суставного хряща, предлагаемый препарат существенно уменьшает размер дефекта по сравнению с контрольными животными.
При внутривенном введении папаина у кроликов наблюдается коллапс ушных раковин - провисание их периферического конца. Использование предлагаемого препарата позволяет восстановить тургор ушных раковин, что свидетельствует об ингибировании разрушения хрящевой ткани ушных раковин.
Сравнительная оценка хондропротективного действия препаратов Глюкат-1 (получен по примеру 1 описания заявки) и Глюкат-2 (получен по примеру 1 описания прототипа) изучена в опытах на кроликах рентгенографически по изменению размера суставной щели по принятой методике (см. таблицу).
Проведенные биологические исследования безвредности препарата показали, что при однократном введении препарата в дозах, в 100-200 раз превышающих минимальные терапевтические для человека, он практически не токсичен. Препарат стабилен в течение 2 лет наблюдения.
Предварительные клинические испытания препарата подтвердили его высокую хондропротективную активность и хорошую переносимость при лечении артрозов и остеохондроза.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНЕЙ СУСТАВОВ | 2005 |
|
RU2290922C1 |
| СТАБИЛЬНОЕ СРЕДСТВО ЛЕЧЕНИЯ БОЛЕЗНЕЙ СУСТАВОВ | 2018 |
|
RU2680804C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНЕЙ СУСТАВОВ | 2005 |
|
RU2275199C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНЕЙ СУСТАВОВ | 2005 |
|
RU2275190C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНЕЙ СУСТАВОВ | 2004 |
|
RU2271811C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНЕЙ СУСТАВОВ | 2004 |
|
RU2271812C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ АРТРОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ В ЛИОФИЛИЗИРОВАННОЙ ФОРМЕ ДЛЯ ИНЪЕКЦИЙ | 2024 |
|
RU2827073C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНЕЙ СУСТАВОВ | 2004 |
|
RU2259204C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНЕЙ СУСТАВОВ | 2004 |
|
RU2260432C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНЕЙ СУСТАВОВ | 2005 |
|
RU2282437C1 |
Изобретение относится к области фармацевтики и касается средств для лечения суставов. Изобретение заключается в том, что средство представляет собой лиофилизат, содержащий глюкозамина соль и трометамол, при определенном соотношении компонентов. Изобретение обеспечивает повышение удельной концентрации активного ингредиента в составе препарата и, как следствие, увеличение скорости и эффективности диффузии активной субстанции в зону сустава. 1 з.п. ф-лы, 1 табл.
| КОМПОЗИЦИЯ - ЛЕКАРСТВЕННАЯ ФОРМА ПРОТИВОАРТРОЗНОГО СРЕДСТВА ГЛЮКОЗАМИНА ГИДРОХЛОРИДА ДЛЯ ИНЪЕКЦИЙ | 1996 |
|
RU2118156C1 |
| СРЕДСТВО ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ДЕГЕНЕРАТИВНО-ДИСТРОФИЧЕСКИХ ИЗМЕНЕНИЙ СУСТАВОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2001 |
|
RU2201757C1 |
| ЛЕЧЕНИЕ СОСТОЯНИЙ И ЗАБОЛЕВАНИЙ, КОМБИНАЦИИ И КОМПОЗИЦИИ, ПРЕДНАЗНАЧЕННЫЕ ДЛЯ ЛЕЧЕНИЯ, СПОСОБ ПОВЫШЕНИЯ АКТИВНОСТИ МАКРОФАГОВ И КОМБИНАЦИИ ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1990 |
|
RU2146139C1 |
| US 4870061 A, 26.09.1989. | |||
Авторы
Даты
2007-01-27—Публикация
2005-08-17—Подача