Настоящее изобретение относится к способам лечения ряда заболеваний с использованием аналогов витамина D3 и к способам получения таких аналогов. Настоящее изобретение прежде всего относится к сложным эфирам 3-дезокси-20-деметил-20-циклопилвитамина D3 и способам их получения и применения.
Остеопороз представляет собой наиболее распространенную форму метаболического заболевания костной ткани и его можно рассматривать, как симптоматическую переломную стадию потери костной ткани (нарушение остеогенеза). Хотя остеопороз может развиваться как вторичный процесс при ряде основных заболеваний, 90% всех случаев являются идиопатическими (неясного происхождения). Идиопатическим остеопорозом рискуют заболеть женщины в постклимактерическом периоде (постклимактерический или остеопороз типа I); другой группой особенно высокого риска заболевания остеопорозом являются пожилые люди любого пола (старческий или остеопороз типа II). Кроме того, остеопороз может развиваться при приеме кортикостероидов, малоподвижном образе жизни или при продолжительном постельном режиме, алкоголизме, диабете, гонадотоксичной химиотерапии, гиперпролактинемии, анорексии (отсутствии аппетита на нервной почве), первичной и вторичной аменорреи, иммуносупрессии трансплантата и овариоэктомии. Постклимактерический остеопороз характеризуется переломом позвоночника, в то время как переломы шейки бедра преобладают при старческом остеопорозе.
Принято считать, что механизм потери костной ткани при остеопорозе заключается в нарушении равновесия в процессе обновления скелета. Такой процесс называется реконструкцией костной ткани. Этот процесс происходит в ряде отдельных участков повышенной активности, которые спонтанно появляются в костном матриксе на данной поверхности костной ткани в качестве участков резорбции кости. За резорбцию части костной ткани, обычно постоянного объема, ответственны остеокласты (растворяющие кость клетки или резорбирующие клетки). Этот процесс резорбции завершается появлением остеобластов (клеток, образующих костную ткань), которые впоследствии заполняют новой костной тканью полости, образованные остеокластами.
У здорового взрослого субъекта остеокласты и остеобласты функционируют таким образом, что процессы образования и резорбции костной ткани находятся в состоянии равновесия. Однако при остепопорозе в процессе реконструкции костной ткани равновесие нарушается и образование костной ткани идет с меньшей скоростью, чем ее дезорбция. Хотя такое нарушение равновесия происходит в той или иной степени по мере старения у большинства людей, в гораздо более тяжелой форме оно развивается в более молодом возрасте при постклимактерическом остеопорозе, после овариэктомии или в ятрогенных ситуациях, например, при лечении кортикостероидами или при иммуносупрессии, используемой при трансплантации органов.
Для увеличения костной массы у людей, страдающих остеопорозом, предлагались различные подходы, которые включали введение андрогенов, фторсодержащих солей, паратироидного гормона и модификаций паратироидного гормона. Кроме того, для сохранения массы костной ткани предлагалось использовать бифосфонаты, кальцитонин, кальций, 1,25-дигидроксивитамин D3 и некоторые его аналоги и/или эстрогены, каждый в отдельности или в комбинации.
Витамин D3 является ключевым элементом в метаболизме кальция, активирующим всасывание кальция и фосфора в кишечнике, поддерживающим соответствующие уровни кальция и фосфора и стимулирующим приток и обратный поток кальция в костную ткань и обратно. Витамин D3 гидроксилируется in vivo с образованием 1α,25-дигидроксиметаболита, который является активным соединением. При исследовании 1,25-(ОН)2-витамина D3 на модельных животных было высказано предположение, что препарат обладает анаболической активностью в отношении костной ткани. Aerssens и др. (см. Calcif. Tissue Int., 55, 443-450 (1994)) сообщиют о влиянии 1α-гидроксивитамина D3 на прочность и состав костной ткани у растущих крыс в сочетании лечением кортикостероидами или без него. Однако применение для лечения человека ограничено антирезорбцией из-за низкого терапевтического индекса (гиперкальциурии и гиперкальциемии, а также нефроксичности).
Dechant и Goa в статье "Calcitriol. A review of its use in the treatment of postmenopausal osteoporosis and its potential in corticosteroid-induced osteporosis", Drugs Aging (New Zeiand), 5, №(4), 300-317 (1994), сообщают о том, что 1,25-гидроксивитамин D3 (кальцитриол) оказался эффективным при лечении постклимактерического остеопороза (и перспективен при остеопорозе, индуцированном кортикостероидами) по результатам клинических испытаний с участием 622 женщин с постклимактерическим остеопорозом. У пациентов, страдающих слабой или умеренной формой (но не тяжелой формой) заболевания и получавших кальцитриол (0,25 мкг дважды в день) через 3 года лечения наблюдалось практически в три раза меньше патологических переломов позвонков по сравнению с пациентами, получавшими кальций в дозе 1000 мг/сут. У пациентов, прошедших продолжительный курс лечения преднизоном или преднизолоном, прием кальцитриола в дозе от 0,5 до 1,0 мкг/сут и кальция в дозе 1000 мг/сут, которые вводили в сочетании с интраназальным введением кальцитонина 400 МЕ/сут или без кальцитонина, вызывал подавление стероид-индуцированной потери костной ткани. В общем случае кальцитриол характеризуется удовлетворительной переносимостью. При рекомендованных дозах наблюдались редкие случаи слабой формы гиперкальциемии, обычно в ответ на снижение потребления кальция и/или дозы кальцитриола. Однако в связи с узким лечебным диапазоном кальцитриола при его применении необходим соответствующий контроль, а также периодичествий анализ уровня кальция и креатинина в сыворотке крови. Эти исследования свидетельствовали о том, что главным ограничением при терапии кальцитриолом является перекрывание диапазонов лечебных и токсических доз.
Некоторые аналоги 3-дезокси-20-циклопропилвитамина D3 заявлены, как соединения, которые ингибируют клеточную пролиферацию in vitro линии клеток рака предстательной железы (M.Koike и др., 20-Cyclopropyl-Cholecalciferol Vitamin D3 Analogs, Anticancer Research, 19, 1689-1698 (1999)).
Гиперпаратиреоз
Вторичный гиперпаратиреоз является общим симптомом у пациентов с хронической почечной недостаточностью. Установлено, что снижение синтеза 1,25-(ОН)2-витамина D3 (кальцитриола) в почках является одним из главных механизмов, приводящих к вторичному гиперпаратиреозу у этих пациентов. Установлено также, что кальцитриол оказывает прямое супрессивное действие на синтез РТН. Следовательно, введение кальцитриола рекомендовано для лечения вторичного гиперпаратиреоза у таких пациентов. Однако, как описано выше, кальцитриол обладает сильным гиперкальциемическим действием из-за низкого терапевтического индекса, что ограничивает его применение, прежде всего в высоких дозах. Следовательно, необходимо располагать альтернативными средствами лечения гиперпаратиреоза, которые не оказывают такого нежелательного гиперкальциемического действия.
Для лечения указанных и других заболеваний используется множество соединений, однако многие из них оказывают нежелательное побочное действие и/или они являются относительно неустойчивыми, т.е. характеризуются коротким сроком хранения. Следовательно, существует необходимость в других соединениях, которые можно использовать при лечении указанных заболеваний.
Первым объектом настоящего изобретения является сложный эфир аналога 3-дезоксивитамина D3 формулы I
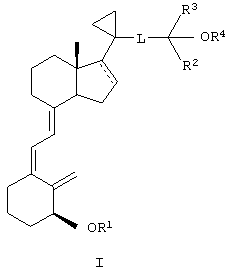
или его соль и способы его применения и получения, причем в формуле I пунктирная линия необязательно означает двойную связь,
L означает соединительный фрагмент, выбранный из ряда -СН2-СН2-СН2-, -СН2-СН=СН-, -CH2-C≡C, -CH2-CH2-C(=O)C- и -СН=СН-СН=СН-,
каждый R2 и R3 независимо означает алкил или галогеналкил, или R2 и R3 вместе с атомом углерода, к которому они присоединены, образуют циклоалкил, а
каждый R1 и R4 независимо означает водород, алкил, ацил или другую гидрокси-защитную группу,
при условии, что по меньшей мере один из R1 и R4 означает ацил.
"Ацетат" или "Ас" используются в тексте как равнозначные термины и означают остаток формулы -С(=O)СН3.
"Ацил" означает остаток формулы -C(O)R', где R' означает алкил, гетероалкил, циклоалкил, арил, гетероарил, аралкил или гетероаралкил.
"Алкил" означает линейный насыщенный углеводородный радикал, содержащий от одного до шести, предпочтительно от одного до четырех атомов углерода, или разветвленный насыщенный углеводородный радикал, содержащий от трех до шести атомов углерода.
"Аралкил" означает остаток формулы -Ra-Rb, где Ra означает алкил, а Rb означает арил, имеющие указанные в тексте значения.
"Арил" означает моноциклический или бициклический углеводородный радикал, в котором один или более, предпочтительно один, два или три атома водорода арильной группы заменены на галоген, нитро, циано, гидрокси, амино, алкил или алкокси. Примеры арильных групп включают фенил и нафталинил, замещенные одним или более заместителями, указанными выше. Предпочтительно арил означает фенил.
"Циклоалкил" означает насыщенный циклический углеводородный радикал, содержащий в цикле от трех до шести атомов углерода, например циклопропил, циклопентил и т.п.
"Сложный эфир" означает соединение, включающее остаток формулы -O-C(=O)-R', где R' означает алкил, гетероалкил, циклоалкил, арил, гетероарил, аралкил или гетероаралкил.
"Галогеналкил" означает алкил, имеющий значения, указанные выше, в котором один или более атомов водорода, связанных с углеродной цепью, заменены на один или более галогенов. Предпочтитеным галогеном является фтор.
"Гетероалкил" означает алкил, имеющий значения, указанные выше, содержащий один или более, предпочтительно один, два или три заместителя, выбранные из ряда -NRaRb, -ORc, где Ra, Rb и Rc независимо друг от друга означают водород, алкил или соответствующую защитную группу.
"Гетероаралкил" означает остаток формулы -Ra-Rb, где Ra означает алкил, а Rb означает гетероарил, имеющие значения, указанные выше.
"Гетероарил" означает моноциклический или бициклический радикал, содержащий от 5 до 12 атомов в цикле и включающий по меньшей мере один ароматический цикл, содержащий один, два или три гетероатома, выбранные из ряда N, О или S, а остальные атомы в цикле являются атомами углерода, причем подразумевается, что свободная связь в гетероарильном радикале находится в ароматическом цикле. Кроме того, в гетероарильном фрагменте один или более атомов водорода, предпочтительно один, два или три атома водорода, могут быть замещены группами, указанными выше для арильной группы.
Термин "гидроксизащитная группа" и "другая гидроксизащитная группа" используются в тексте как равнозначные и означают гидроксизащитные группы, известные специалисту в данной области, за исключением алкильных или ацильных групп, которые особо описаны в тексте заявки. Типичные гидроксизащитные группы включают силильные простые эфиры, карбонаты, карбаматы, замещенные простые метиловые эфиры, замещенные простые этиловые эфиры и т.п. Перечень других гидроксизащитных групп можно найти, например, в монографии T.W.Greene и P.G.M.Wuts, Protective Groups in Organic Synthesis, 3 ed., J.Wiley & Sons, New York (1999), включенной в качестве ссылки в текст заявки.
"Фармацевтически приемлемый эксципиент" означает носитель, который используется при получении фармацевтической композиции и который в основном безвреден, нетоксичен и является безопасным в биологическом и ином отношении, и включает эксципиент, приемлемый для применения как в ветеринарии, так и в медицине. "Фармацевтически приемлемый эксципиент", используемый в описании и пунктах формулы изобретения, включает один и более таких носителей.
"Терапевтически эффективное количество" означает количество соединения, которое при введении млекопитающему для лечения или профилактики заболевания, является достаточным, чтобы обеспечить такое лечение или профилактику заболевания. Терапевтически эффективное количество изменяется в зависимости от типа соединения, типа заболевания, тяжести заболевания, возраста, массы и других параметров пациента, подлежащего лечению.
"Терапия" или "лечение" заболевания включает: (1) профилактику заболевания, т.е. предотвращение развития клинических симптомов заболевания у млекопитающего, которое подвержено или предрасположено к заболеванию, но у которого указанные симтомы не обнаруживаются или не проявляются, (2) подавление заболевания, т.е. остановку или подавление развития заболевания или его клинических симптомов, или (3) ослабление заболевания, т.е. регрессии заболевания или его клинических симптомов.
В случае химических реакций термины "обработка", "контактирование" и "взаимодействие" используются как взаимозаменяемые и означают добавление или смешивание двух или более реагентов в соответствующих условиях с целью получения указанного и/или необходимого продукта. Предполагается, что указанный и/или необходимый продукт не обязательно образуется непосредственно при комбинации двух первоначально добавленных реагентов, т.е. в смеси может образоваться одно или более промежуточных соединений, из которых в конечном итоге образуется указанный и/или необходимый продукт.
Термины "имеющий значения, указанные выше" и "указанный в тексте заявки", используемые в тексте заявки и относящиеся к переменному параметру, включены в состав более широкого определения переменных параметров, а также предпочтительных, более предпочтительных и наиболее предпочтительных значений, если такие значения упоминаются в тексте.
"Пролекарство" означает любое соединение, которое высвобождает активное исходное соединение формулы (I) in vivo, когда такое пролекартво вводится млекопитающему. Пролекарства соединений формулы (I) получают модификацией функциональных групп, присутствующих в соединении формулы (I), таким образом, что модифицированные группы могут расщепляться in vivo с высвобождением исходного соединения. Пролекарства включают соединения формулы (I), в которых гидроксильная группа соединения (I) связана с любой группой, которая может отщепляться in vivo с регенерацией свободной гидроксильной группы. Примеры пролекарств включают, без ограничения перечисленным, сложные эфиры (например, ацетат, формиат и бензоат), карбаматы (например, N,N-диметиламинокарбонил) и простые эфиры гидроксильных функциональных групп в соединениях формулы (I), и т.п. Такие соединения специалист в данной области получает обычным ацилированием или этерификацией гидроксильной группы в исходной молекуле.
"Гидроксизащитная группа" означает группу атомов, которая при связывании с гидроксильной группой маскирует, снижает или блокирует реакционную способность гидроксигруппы. Примеры защитных групп можно найти в монографиях T.W.Greene и P.G.Futs, Protective Groups in Organic Chemistry, 2 ed., Wiley (1999) и Harrison и Harrison и др., Compendium of Synthetic Organic Methods, т. 1-8, J.Wiley и Sons (1971-1996). Типичные гидроксизащитные группы включают такие группы, в которых гидроксильная группа ацилирована или алкилирована, такие как бензиловые и тритильные простые эфиры, а также алкильные простые эфиры, тетрагидропиранильные простые эфиры, триалкилсилильные простые эфиры и аллильные простые эфиры.
Неожиданно было установлено, что некоторые соединения ряда 3-дезокси-1α-гидрокси-20-циклопропилхолекальциферола (витамина D3), до настоящего времени известные благодаря их антипролиферативной активности, являются неожиданно эффективными по сравнению с 1,25-дигидроксивитамином D3 в отношнии увеличения образования костной ткани. Следовательно, первым объектом настоящего изобретения является способ лечения остеопороза или гиперпаратиреоза, включающий введение аналога 3-дезокси-1α- гидроксивитамина D3 пациенту, причем указанный аналог 3-дезоксивитамина D3 означает соединение формулы

его пролекарство или соль, предпочтительно соединение формулы I или его соль, где
пунктирная линия необязательно означает двойную связь,
L означает соединительный фрагмент, выбранный из ряда -СН2-СН2-СН2-, -СН2-СН=СН-, -CH2-C≡C, -CH2-CH2-C(=O)C-, и -СН=СН-СН=СН-,
каждый R1 и R4 выбирают из группы, включающей водород и алкил, а
каждый R2 и R3 независимо выбирают из группы, включающей алкил и
галогеналкил, или R2 и R3 вместе с атомом углерода, к которому они присоединены, образуют циклоалкил.
Другим объектом настоящего изобретения является способ получения соединения формулы
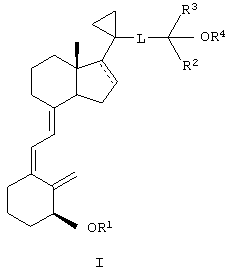
включающий взаимодействие кетона формулы
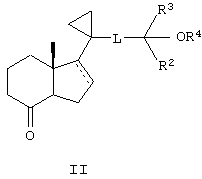
с фосфиноксидом формулы

в условиях, достаточных для образования указанного соединения формулы I, где каждый Ar1 и Ar2 независимо означает необязательно замещенный арил, пунктирная линия необязательно означает двойную связь,
L означает соедининтельный фрагмент, выбранный из ряда -СН2-СН2-СН2-, -СН2-СН=СН-, -CH2-C≡C, -CH2-CH2-C(=O)C-, и -СН=СН-СН=СН-,
каждый R1 и R4 выбирают из группы, включающей водород и алкил и гидроксизащитную группу, а каждый R2 и R3 независимо выбирают из группы, включающей алкил и
галогеналкил, или R2 и R3 вместе с атомом углерода, к которому они присоединены, образуют циклоалкил.
В первом варианте настоящего способа получения соединения формулы I R4 означает водород. В предпочтительном варианте способ также включает стадии защиты гидроксильной группы в указанном кетоне формулы II перед указанной стадией взаимодействия с указанным фосфиноксидом формулы III и удаление гидроксизащитной группы после взаимодействия указанного кетона формулы II с указанным фосфиноксидом формулы III с образованием указанного соединения формулы I.
Предпочтительным является соединение формулы

или его соль, предпочтительно соединение формулы I, где
пунктирная линия необязательно означает двойную связь,
L означает соединительный фрагмент, выбранный из ряда -СН2-СН2-СН2-, -СН2-СН=СН-, -CH2-C≡C, -CH2-CH2-C(=O)C- и -СН=СН-СН=СН-,
каждый R2 и R3 независимо означает алкил или галогеналкил, или R2 и R3 вместе с атомом углерода, к которому они присоединены, образуют циклоалкил, а
каждый R1 и R4 независимо означает водород, алкил, ацил или другую гидрокси-защитную группу, при условии, что по меньшей мере один из R1 и R4 означает ацил.
Кроме того, предпочтительным является соединение формулы
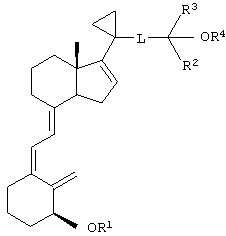
где R1, R2, R3, R4 и L имеют значения, указанные в пункте 1.
Другим предпочтительным объектом изобретения является соединение формулы
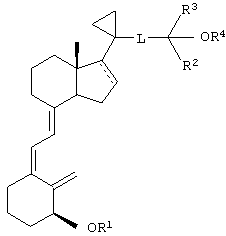
где L выбирают из группы, включающей -СН2-СН2-СН2-, -СН2-СН=СН-, -CH2-C≡C и -СН=СН-СН=СН-.
Кроме того, предпочтительным является соединение формулы I, где указанный соединительный фрагмент L выбирают из группы, включающей -СН2-СН=CH- и -CH2-C≡C-.
Кроме того, предпочтительным является соединение формулы I, где R1 означает ацил.
Другим предпочтительным объектом изобретения является соединение
формулы I, где R4 означает ацил.
Кроме того, предпочтительным является соединение формулы I, где R2 и R3 независимо выбирают из группы, включающей алкил и галогеналкил.
Другим предпочтительным объектом изобретения являются соединения формулы I, где R2 и R3 означают трифторметил.
Более предпочтительные соединения формулы I выбирают из ряда
[1R-(1α(Е),3аβ,7аα)]октагидро-7а-метил-1-[5,5,5-трифтор-4-гидрокси-4-(трифторметил)-2-пентинил]циклопропил]-4Н-инден-4-ол,
[1R-(1α(Е),3аβ,7аα)]октагидро-7а-метил-1-[1-[5,5,5-трифтор-4-гидрокси-4-(трифторметил)-2-пентинил]циклопропил]-4Н-инден-4-он,
[1R-[(1α(Е),3аβ,7аα)]]окстагидро-7а-метил-1-[1-[5,5,5-трифтор-4-трифторметил)-4-[(триметилсилил)окси]-2-пентинил]циклопропил]-4Н-инден-4-он,
3-дезокси-1,25-дигидрокси-20-метил-23-(Е)-ен-26,27-гексафтор-21,28-циклохолекальциферол,
3-дезокси-1,25-дигидрокси-20-метил-23-(Z)-ен-26,27-гексафтор-21,28-циклохолекальциферол,
3-дезокси-1,25-дигидрокси-20-метил-23-ин-21,28-циклохолекальциферол,
3-дезокси-1,25-дигидрокси-20-метил-23-ин-26,27-гексафтор-21,28-циклохолекальциферол,
3-дезокси-1,25-дигидрокси-20-метил-21,28-циклохолекальциферол,
3-дезокси-1α-ацетокси-25-гидрокси-20-циклопропил-23Е-ен-26,27-гексафторхолекальциферол и
3-дезокси-1α,25-диацетокси-20-циклопропил-23Е-ен-26,27-гексафторхолекальциферол.
Кроме того, предпочтительным является способ получения соединения формулы I, включающий
(а) взаимодействие кетона формулы
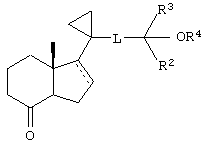
с фосфиноксидом формулы
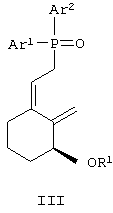
в условиях, достаточных для образования указанного соединения формулы I, где каждый Ar1 и Ar2 независимо означает необязательно замещенный арил, пунктирная линия необязательно означает двойную связь,
L означает соединительный фрагмент, выбранный из ряда -СН2-СН2-СН2-, -СН2-СН=СН-, -CH2-C≡C, -CH2-CH2-C(=O)C- и -СН=СН-СН=СН-,
каждый R2 и R3 независимо означает алкил или галогеналкил, или R2 и R3 вместе
с атомом углерода, к которому они присоединены, образуют циклоалкил, а каждый R1 и R4 независимо означает алкил, ацил или гидроксизащитную группу, и
(б) если R1 и R4 не означают ацил, ацилирование соединения формулы I ацилирующим агентом в условиях, достаточных для образования соединения формулы I, где по меньшей мере один из R1 и R4 означает ацильную группу.
Предпочтительным прежде всего является способ, где R1 и R4 означают гидрокси-защитные группы.
Кроме того, прежде всего предпочтительным является указанный способ, где указанная стадия ацилирования (б) включает (I) удаление гидроксигрупп при взаимодействии соединения, полученного на стадии (а), с соответствующим реагентом для удаления гидроксизащитных групп в условиях, достаточных для образования аналога 1-гидрокси-3-дезокси-витамина D3 формулы
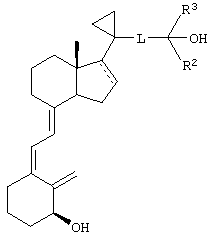
и
(II) взаимодействие аналога 1-гидрокси-3-дезокси-витамина D3 с ацилирующим агентом в условиях, достаточных для образования сложного эфира аналога 3-дезокси-витамина D3 формулы
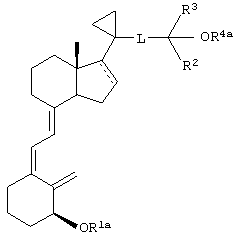
где R1a означает ацил, a R4a означает водород или ацил.
Более того, прежде всего предпочтительным является указанный способ, где R4a означает ацил.
Кроме того, предпочтительным является указанный способ, где Ar1 и Ar2 означают фенил.
Другим предпочтительным объектом изобретения является соединение формулы I, полученное по указанному способу.
Предпочтительной также является фармацевтическая композиция, включающая соединение формулы I и фармацевтически приемлемый эксципиент.
Кроме того, предпочтительными являются соединения формулы I для применения в качестве терапевтически активного соединения.
Другим предпочтительным объектом настоящего изобретения являются соединения формулы I для получения лекарственных препаратов, предназначенных для профилактики и лечения заболеваний, ассоциированных с костной тканью.
Предпочтительными являются соединения формулы I для получения лекарственных препаратов, предназначенных для профилактики и лечения гиперпаратиреоза, почечной остеодистрофии или остеопороза.
Предпочтительным также является способ лечения заболевания костной ткани, включающий введение пациенту соединения формулы I.
Кроме того, предпочтительным является способ применения соединения формулы I, где заболевание выбирют из ряда гиперпаратиреоз, вторичный гиперпаратиреоз, почечная остеодистрофия и остеопороз.
Другим предпочтительным объектом изобретения является способ лечения заболевания костной ткани, включающий введение пациенту соединения формулы

или его пролекарства или соли, предпочтительно соединения формулы I или его соли, наиболее предпочтительно соединения формулы I, где пунктирная линия необязательно означает двойную связь,
L означает соединительный фрагмент, выбранный из ряда -СН2-СН2-СН2-, -СН2-СН=СН-, -CH2-C≡C, -CH2-CH2-C(=O)C-, и -СН=СН-СН=СН-;
каждый R1 и R4 выбирают из группы, включающей водород или алкил, а каждый R2 и R3 независимо выбирают из группы, включающей алкил или
галогеналкил, или R2 и R3 вместе с атомом углерода, к которому они присоединены, образуют циклоалкил. Предпочтительным прежде всего является способ лечения заболевания костной ткани у пациента, включающий введение пациенту соединения формулы I.
Кроме того, предпочтительным является применение соединения формулы

или его пролекарства или соли, предпочтительно соединения формулы I или его соли, наиболее предпочтительно соединения формулы I для получения лекарственных препаратов, предназначенных для лечения и профилактики заболеваний костной ткани, где пунктирная линия необязательно означает двойную связь,
L означает соединителный фрагмент, выбранный из ряда -СН2-СН2-СН2-, -СН2-СН=СН-, -CH2-C≡C, -CH2-CH2-C(=O)C- и -СН=СН-СН=СН-;
каждый R1 и R4 выбирают из группы, включающей водород или алкил, а каждый R2 и R3 независимо выбирают из группы, включающей алкил или
галогеналкил, или R2 и R3 вместе с атомом углерода, к которому они присоединены, образуют циклоалкил.
Предпочтительным прежде всего является указанное применение, где заболевание включает гиперпаратиреоз, почечную остеодистрофию и остеопороз.
Предпочтительным также является указанный способ или применение, где соединение имеет формулу

в которой R1, R2, R3, R4 и L имеют значения, указанные выше.
Кроме того, предпочтительным является указанный способ или применение, где указанный соединительный фрагмент L выбирают из группы, включающей -СН2-СН2-СН2-, -CH2-СН=СН-, -CH2-C≡C и -СН=СН-СН=СН-.
Кроме того, предпочтительным является указанный способ или применение, как указано выше, где указанный соединительный фрагмент L выбирают из группы, включающей -СН2-СН=СН- и -СН2-С≡С.
Кроме того, предпочтительным является указанный способ или применение, где R1 означает водород.
Предпочтительным также является указанный способ или применение, где R1 и R4 означают водород.
Предпочтительным прежде всего является указанный способ или применение, где каждый R2 и R3 независимо выбирают из группы, включающей алкил и галогеналкил.
Другим прежде всего предпочтительным является способ или применение, как описано выше, где R2 и R3 оба означают трифторметил.
Более того, прежде всего предпочтительным является указанный способ или применение, где заболевание означает остеопороз.
Кроме того, предпочтительным является указанный способ или применение, где в результате лечения происходит заживление переломов или снижение возможности переломов.
Предпочтителен прежде всего указанный способ или применение, где пациент находится в группе риска получения перелома вследствие снижения уровня эстрогена.
Кроме того, предпочтительным является указанный способ или применение, при которых пациентом является женщина.
Предпочтителен также способ или применение, указанные выше, в результате которых у пациента увеличивается плотность минеральной составляющей костной ткани.
Предпочтителен прежде всего указанный способ или применение, где пациент подвергается лечению бифосфонатом, эстрогеном, селективным модулятором экстрогенового рецептора или анаболическим агентом.
Кроме того, предпочтительным является способ получения соединения формулы

включающий взаимодействие кетона формулы
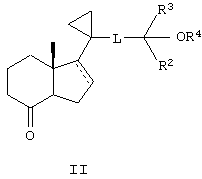
с фосфиноксидом формулы

в условиях, достаточных для образования указанного соединения формулы I, где
каждый Ar1 и Ar2 независимо означает необязательно замещенный арил, пунктирная линия необязательно означает двойную связь,
L означает соединительный фрагмент, выбранный из ряда -СН2-СН2-СН2-, -СН2-СН=СН-, -CH2-C≡C, -CH2-CH2-C(=O)C- и -СН=СН-СН=СН-,
каждый R1 и R4 выбирают из группы, включающей водород и алкил, а каждый R2 и R3 независимо выбирают из группы, включающей алкил и
галогеналкил, или R2 и R3 вместе с атомом углерода, к которому они присоединены, образуют циклоалкил.
Предпочтительным прежде всего является указанный способ, где R4 означает водород.
Кроме того, прежде всего предпочтительным является способ получения, включающий также стадии введения гидроксизащитной группы в указанном кетоне формулы II перед указанной стадией взаимодействия с указанным фосфиноксидом формулы III и удаление гидроксизащитной группы после взаимодействия кетона формулы II с указанным фосфиноксидом формулы III с образованием соединения формулы I.
Первым объектом настоящего изобретения является сложный эфир аналога 3-дезокси-20-деметил-20-циклопропил-витамина D3 формулы

или его соли, где пунктирная линия необязательно означает двойную связь,
L означает соединительный фрагмент, выбранный из ряда -СН2-СН2-СН2-, -СН2-СН=СН-, -CH2-C≡C, -CH2-CH2-C(=O)C- и -СН=СН-СН=СН-;
каждый R2 и R3 независимо означает алкил или галогеналкил, или R2 и R3 вместе с атомом углерода, к которому они присоединены, образуют циклоалкил, а каждый R1 и R4 независимо означает водород, алкил, ацил или другую гидроксизащитную группу, при условии, что по меньшей мере один из R1 и R4 означает ацил.
Неожиданно было установлено, что соединения формулы I, где по меньшей мере один из R1 и R4 означает ацил, оказались неожиданно устойчивыми и кристаллическими по сравнению с соединениями, в которых R1 и R4 оба означают водород, т.е. по сравнению с исходным диодом.
Если циклопентановый фрагмент в соединении формулы I не содержит двойной связи, т.е. пунктирная линия отсутствует, стереохимия боковой цепи циклопентановой циклической системы может образовывать α- или β-формы. Предпочтительно, стереохимия боковой цепи циклопентановой циклической системы находится в β-форме, т.е. соединение имеет формулу
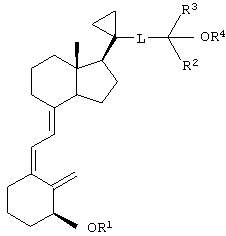
В другом предпочтительном варианте настоящего изобретения сложный эфир 3-дезокси-аналога витамина D3 имеет формулу

где R1, R2, R3, R4 и L имеют значения, указанные выше.
В другом варианте соединительный фрагмент L выбирают из группы, включающей -СН2-СН2-СН2-, -СН2-СН=СН-, -CH2-C≡C и -СН=СН-СН=СН-.
Предпочтительно L означает -СН2-СН=СН- или -СН2-С≡С-. Более предпочтительно L означает -СН2-СН=СН-, где двойная связь имеет трансконфигурацию.
В еще одном варианте R1 предпочтительно означает ацил, более предпочтительно ацетил.
В другом варианте R1 означает ацил, а R4 означает водород или ацил.
В еще одном варианте R1 означает ацил, а каждый R2 и R3 независимо выбирают из группы, включающей метил, этил и трифторметил.
В еще одном варианте R2 и R3 означают алкил или галогеналкил, предпочтительно метил или трифторметил, более предпочтительно трифторметил.
Выше приведен ряд предпочтительных заместителей и введение любых таких заместителей приводит к получению соединения по изобретению, которое является более предпочтительным, чем соединение, не содержащее таких заместителей. Однако эти предпочтительные заместители являются в общем случае независимыми, хотя некоторые предпочтительные заместители являются уникальными, и введение более одного таких предпочтительных заместителей приводит к получению более предпочтительного соединения по сравнению с теми соединениями, которые содержат меньшее количество таких заместителей. Примеры соединений по изобретению
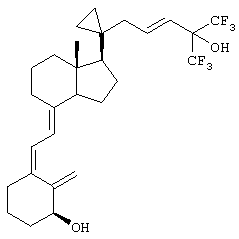
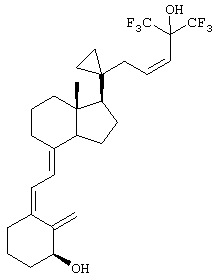
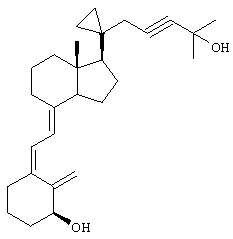
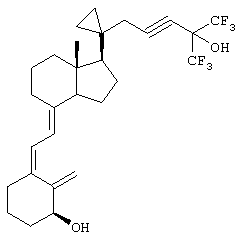
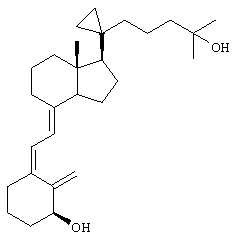
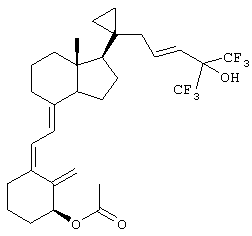
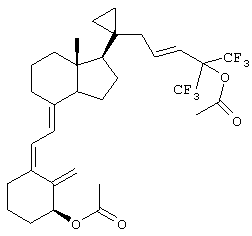
Предпочтительным объектом настоящего изобретения является способ лечения остеопопроза, гиперпаратиреоза или аутоиммунного заболевания введением пациенту аналога 3-дезоксивитамина D3 формулы I

где R1, R2, R3, R4 и L имеют значения, указанные в кратком описании изобретения.
Если циклопентановый фрагмент в соединении формулы I не содержит двойной связи, т.е. если отсутствует пунктирная линия и отсутствует двойная связь, стереохимия боковой цепи циклопентановой циклической системы может образовывать α- или β-формы. Предпочтительно, стереохимия боковой цепи циклопентановой циклической системы находится в β-форме, т.е. соединение имеет формулу

В одном из вариантов изобретения аналог 3-дезоксивитамина D3 имеет формулу

где R1, R2, R3, R4 и L имеют значения, указанные в кратком описании изобретения.
В еще одном варианте соединительный фрагмент L выбирают из группы, включающей -СН2-СН2-СН2-, -СН2-СН=СН-, -CH2-C≡C- и -СН=СН-СН=СН-.
Предпочтительно L означает -СН2-СН=СН-, -СН2-С=С-. Более предпочтительно L означает -СН2-СН=СН-, где двойная связь имеет трансконфигурацию.
В другом варианте R1 предпочтительно означает водород.
В еще одном варианте R4 предпочтительно означает водород.
В другом варианте R1 и R4 оба означают водород.
В еще одном предпочтительном варианте каждый из R2 и R3 независимо означает алкил или галогеналкил, предпочтительно метил или трифторметил.
Выше приведен ряд предпочтительных заместителей и введение любых таких заместителей приводит к получению соединения по изобретению, которое является более предпочтительным, чем соединение, не содержащее таких заместителей. Однако эти предпочтительные заместители являются в общем случае независимыми, хотя некоторые предпочтительные заместители являются уникальными, и введение более одного таких предпочтительных заместителей приводит к получению более предпочтительного соединения по сравнению с теми соединениями, которые содержат мельшее количество таких заместителей.
Общие схемы синтеза
В то время как для получения соединения формулы I пригодно множество методов синтеза, предпочтительный вариант получения соединений формулы I включает взаимодействие кетона с фосфиноксидом. Более конкретно соединения формулы I можно получить взаимодействием соединения формулы II

с фосфиноксидом формулы

в условиях, достаточных для образования соединения формулы I, где каждый Ar1 и Ar2 независимо означает необязательно замещенный арил, пунктирная линия необязательно означает двойную связь,
L означает соединительный фрагмент, выбранный из ряда -СН2-СН2-СН2-, -СН2-СН=СН-, -CH2-C≡C, -CH2-CH2-C(=O)C- и -СН=СН-СН=СН-;
каждый R2 и R3 независимо означает алкил или галогеналкил, или R2 и R3 вместе с атомом углерода, к которому они присоединены, образуют циклоалкил, а каждый R1 и R4 независимо означает алкил, ацил или гидроксизащитную группу, и
(б) если R1 и R4 не означают ацил, ацилированием соединения формулы I ацилирующим агентом в условиях, достаточных для образования соединения формулы I, где по меньшей мере один из R1 и R4 означает ацил.
В одном варианте R1 и R4 означают гидроксизащитные группы. В этом конкретном варианте стадия ацилирования (б) включает (I) удаление гидроксигрупп при взаимодействии соединения, полученного на указаной стадии (а), с соответствующим реагентом для удаления гидроксизащитных групп в условиях, достаточных для образования аналога 1-гидрокси-3-дезоксивитамина D3 формулы

и (II) взаимодействие аналога 1-гидрокси-3-дезоксивитамина D3 с ацилирующим агентом в условиях, достаточных для образования сложного эфира аналога 3-дезоксивитамина D3 формулы
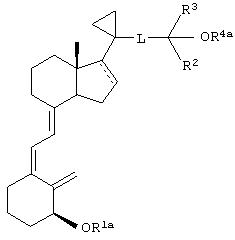
где R1a означает ацил, a R4a означает водород или ацил.
В другом варианте R4a означает ацил.
В еще одном варианте Ar1 и Ar2 означают фенил.
Пригодные гидроксизащитные группы известны специалисту в данной области техники и примеры таких гидроксизащитных групп описаны в монографиях Protective Groups in Organic Synthesis, 3rd ed., T.W.Greene и P.G.M.Wuts, J.Wiley & Sons, New York (1999) и Harrison и Harriso и др. Compendium of Synthetic Organic Methods, т.1-8, J.Wiley и Sons (1971-1996), которые включены в описание заявки в качестве ссылки. Типичные гидроксизащитные группы включают бензильные и тритильные простые эфиры, тетрагидропиранильные простые эфиры, триалкилсилильные простые эфиры, карбаматы и аллильные простые эфиры.
Обычно гидроксигруппы защищают в виде силильных эфиров, однако в объем изобретения включено применение альтернативных гидроксизащитных групп, известных в данной области техники, описанных в вышеуказанной монографии Protective Groups in Organic Synthesis, 3rd ed., и Compendium of Synthetic Organic Methods, т.1-8.
В общем случае, фосфиноксид формулы III в тетрагидрофуране взаимодействует с н-бутиллитием обычно приблизительно при -78°С. Затем к этой смеси добавляют раствор кетона формулы II в тетрагидрофуране с образованием соединения формулы I. Как указано выше, если R1 и/или R4 означают водород, такие групы защищают гидроксизащитными группами до проведения реакции конденсации. В таком случае указанные гидрокси-защитные группы затем удаляют с образованием соединения формулы I.
Методы синтеза и очистки соединений формулы III известны в данной области техники. См., например, монографию M.R.Uskokovic и др., Vitamin D Gene Regulation, Structure Function Analysis and Clinical Application, Париж, Франция, стр.139-145 (1991); патенты DeLuca и др., US 5086191 и 5616759; Baggiolini и др., US 5087619, Doran и др., US 5384314 и 5384314 и 5428029; Baggiolini и др., US 5451574; опубликованную заявку ЕР 0808832 А2; опубликованный патент Brasitus и др., WO 96/31216; статьи Shiuey и др., J. Org. Chem., 55, 243-247 (1990); Kiegel и др., Tetr. Lett, 32, 6057-6090 (1991); Perlman K.L. и др., Tetr. Lett., 32, 7663-7666 (1991).
Схема 1 иллюстрирует метод синтеза соединения формулы IA.
Схема 1
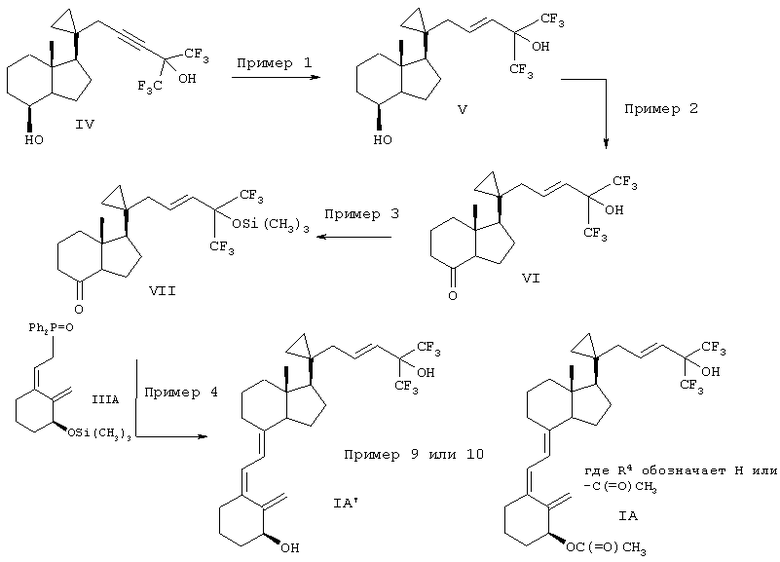
На схеме 1 соединение формулы IV является известным соединением, полученным по методу, описанному в WO 99/12894, опубликованному 18 марта 1999 г. (Preparation of 1,3-dihydroxy-20,20-dialkyl vitamin D3 analogs). Из соединения формулы IV получают соединение формулы V избирательным частичным восстановлением тройной связи до Е-двойной связи с использованием литийалюминийгидрида в инертном органическом растворителе, таком как тетрагидрофуран. Обычно реакцию проводят при добавлении соединения формулы IV к суспензии LiAlH4 в ТГФ при температуре от 0°С до 5°С. Реакционную смесь кипятят с обратным холодильником с образованием соединения формулы V. Затем из соединения формулы V получают кетон формулы VI при окислении окисляющим реагентом, таким как бихромат пиридиния. Обычно реакцию проводят в галогенированном растворителе, таком как хлористый метилен, при комнатной температуре. Затем гидроксигруппу в соединении формулы VI защищают с использованием силилирующего реагента, такого как 1-(триметилсилил)имидазол, триметилсилилхлорид или триметилсилилтрифлат, в инертном растворителе, таком как галогенированный растворитель (например, хлористый метилен), при комнатной температуре с образованием силильного простого эфира формулы VII. Соединение формулы IIIA вводят в реакцию с н-бутиллитием, а затем полученное соединение взаимодействует с соединеним формулы VII в тетрагидрофуране при температуре обычно приблизительно -78°С. Затем силильные группы удаляют, например, при взаимодействии с фторидом тетрабутиламмония в тетрагидрофуране с образованием соединения формулы IA'. Затем свободные гидроксильные группы ацетилируют с образованием соединения формулы IA, например, уксусным ангидридом в пиридине. Поскольку вторичная гидроксильная группа обычно является более реакционноспособной, ее можно ацетилировать избирательно в зависимости от количества используемого ацетилирующего агента и/или от условий проведения реакции, например в зависимости от температуры и/или от времени проведения реакции. В другом варианте и вторичные и третичные гидроксильные группы ацетилируют избытком ацетилирующего агента при более продолжительном времени проведения реакции.
Аналог Z-стереоизомера или аналог с насыщенной углеводородной цепью соединения формулы IA получают восстановлением соединения формулы IV водородом в присутствии соответствующего катализатора гидрирования, такого как Pd-S или Pd соответственно. Полученные соединения можно модифицировать аналогично тому, как показано на схеме I, с образованием аналога Z-изомера и аналога соединения формулы IA с насыщенной углеводородной цепью.
Как показано на схеме 2, соединение формулы II, включающее ацетиленовый спирт и различные алкильные, галогеналкильные и циклоалкильные группы R2 и R3, можно получить конденсацией ацетилид-аниона, полученного из соединения формулы VIII (где Pg означает гидроксизащитную группу), с соответствующим кетоном, галогенкетоном (например, гексафторацетоном) и циклокетоном, и удалением защитной группы.
Схема 2
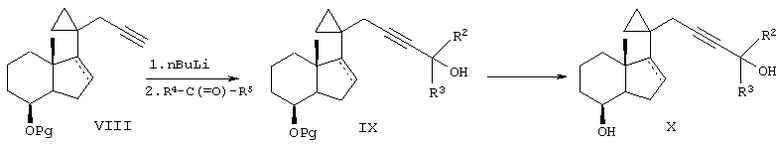
Затем аналогично тому, как показано на схеме I (т.е. окислением, введением гидроксизащитной группы и конденсацией), из соединения формулы Х получают соединение формулы I, содержащее ацетиленовый соединительный фрагмент.
В некоторых предпочтительных вариантах изобретения пунктирная линия означает двойную связь, т.е. соединение имеет формулу
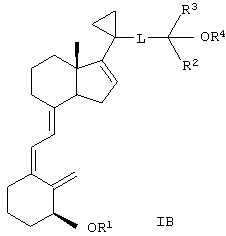
В другом предпочтительном варианте соединительный фрагмент L выбирают из группы, включающей -СН2-СН2-СН2-, -СН2-СН=СН-, -CH2-C≡C- и -СН=СН-СН=СН-.
Предпочтительно R1 означает ацил.
Предпочтительно R4 означает водород или ацил.
Предпочтительно каждый R2 и R3 независимо выбирают из группы, включающей метил, этил и трифторметил, или R2 и R3 вместе с атомом углерода, к которому они присоединены, образуют циклопентильный цикл.
Выше приведен ряд предпочтительных заместителей и введение любых таких заместителей приводит в получению соединения по изобретению, которое является более предпочтительным, чем соединение, не содержащее таких заместителей. Однако эти предпочтительные заместители являются в общем случае независимыми, хотя некоторые предпочтительные заместители являются уникальными, и введение более одного таких предпочтительных заместителей приводит к получению более предпочтительного соединения по сравнению с теми соединениями, которые содержат мельшее количество таких заместителей.
Другим объектом изобретения являются соли соединения формулы I.
В то время как для получения соединения формулы I пригодно множество методов синтеза, пример одного из более предпочтительных вариантов получения соединений формулы I приводится ниже.
Соединения формулы I можно получить при взаимодействии соединения формулы II

с фосфиноксидом формулы

где каждый Ar1 и Ar2 независимо означает необязательно замещенный арил, а пунктирная линия, R1, R2, R3, R4 и L имеют значения, указанные в кратком описании изобретения. Предпочтительно Ar1 и Ar2 означают фенил. Если R1 и/или R4 означают водород, соответствующие гидроксигруппы предпочтительно защищают гидроксизащитными группами, которые совместимы с условиями рекции конденсации, до проведения реакции конденсации кетона формулы II с фосфиноксидом формулы III. Пригодные гидроксизащитные группы известны специалисту в данной области техники и примеры таких гидроксизащитных групп описаны в монографиях Protective Groups in Organic Synthesis, 3rd ed., T.W.Greene и P.G.M.Wuts, J.Wiley & Sons, New York (1999) и Harrison и Harrison и др., Compendium of Synthetic Organic Methods, т.1-8, J.Wiley и Sons (1971-1996), которые включены в описание заявки в качестве ссылки. Типичные гидроксизащитные группы включают бензильные и тритильные простые эфиры, тетрагидропиранильные простые эфиры, триалкилсилильные простые эфиры, карбаматы и аллильные простые эфиры.
Обычно гидроксигруппы защищают в виде силильных простых эфиров, однако в объем изобретения включено применение альтернативных гидроксизащитных групп, известных в данной области техники, описанных в вышеуказанной монографии Protective Groups in Organic Synthesis, 3rd ed., и Compendium of Synthetic Organic Methods, т.1-8.
В общем случае, фосфиноксид формулы III в тетрагидрофуране взаимодействует с н-бутиллитием обычно приблизительно при -78°С. Затем к этой смеси добавляют раствор кетона формулы II в тетрагидрофуране с образованием соединения формулы I. Как указано выше, если R1 и/или R4 означают водород, их защищают гидроксизащитными группами до проведения реакции конденсации. В таком случае указанные гидроксизащитные группы затем удаляют с образованием соединения формулы I.
Методы синтеза и очистки соединений формулы III известны в данной области техники. См., например, монографию M.R.Uskokovic и др., Vitamin D Gene Regulation, Structure Function Analysis and Clinical Application, Париж, Франция, стр.139-145 (1991), патенты DeLuca и др., US 5086191 и 5616759, Baggiolini и др., US 5087619, Doran и др., US 5384314 и 5428029, Baggiolini и др., US 5451574, опубликованную заявку ЕР 0808832 А2, опубликованный патент Brasitus и др., WO 96/31216, статьи Shiuey и др., J. Org. Chem., 55, 243-247 (1990), Kiegel и др., Tetr. Lett., 32, 6057-6090 (1991), Perlman K.L. и др., Tetr. Lett., 32, 7663-7666 (1991).
Схема 1а иллюстрирует метод синтеза соединения формулы IA.
Схема 1a
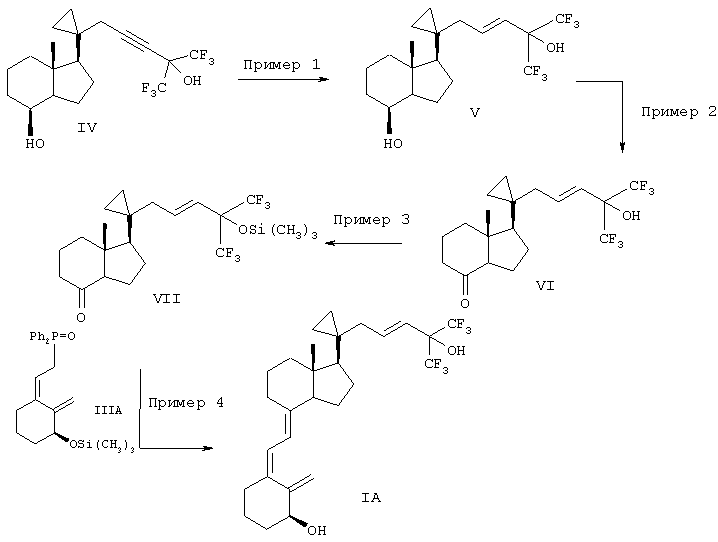
На схеме 1a соединение формулы IV является известным соединением, полученным по методу, описанному в WO 99/12894, опубликованному 18 марта 1999 г. (Preparation of 1,3-dihydroxy-20,20-dialkyl vitamin D3 analogs). Из соединения формулы IV получают соединение формулы V избирательным частичным восстановлением тройной связи до Е-двойной связи с использованием литийалюминийгидрида в инертном органическом растворителе, таком как тетрагидрофуран. Обычно реакцию проводят при добавлении соединения формулы IV к суспензии LiAlH в ТГФ при температуре от 0°С до 5°С. Реакционную смесь кипятят с обратным холодильником с образованием соединения формулы V. Затем из соединения формулы V получают кетон формулы VI при окислении окисляющим реагентом, таким как бихромат пиридиния. Обычно реакцию проводят в галогенированном растворителе, таком как хлористый метилен, при комнатной температуре. Затем гидроксигруппу в соединения формулы VI защищают с использованием силилирующего реагента, такого как 1-(триметилсилил)имидазол, триметилсилилхлорид или триметилсилилтрифлал, в инертном расторителе, таком как галогенированный растворитель (например, хлористый метилен), при комнатной температуре с образованием силильного эфира формулы VII. Соединение формулы IIIA вводят в реакцию с н-бутиллитием, а затем полученное соединение взаимодействует с соединеним формулы VII в тетрагидрофуране при температуре -78°С. Затем силильные группы удаляют, например, при взаимодействии с фторидом тетрабутиламмония в тетрагидрофуране с образованием соединения формулы IA.
Аналог Z-стереоизомера или аналог с насыщенной углеводородной цепью соединения формулы IA получают восстановлением соединения формулы IV водородом в присутствии соответствующего катализатора гидрирования, такого как Pd-S или Pd соответственно. Полученные соединения модифицируют аналогично тому, как показано на схеме 1а, с образованием соответствующего аналога Z-изомера и аналога соединения формулы IA с насыщенной углеводородной цепью.
Как показано на схеме 2а, соединение формулы II, включающее ацетиленовый спирт и различные алкильные, галогеналкильные и циклоалкильные группы R2 и R3, получают конденсацией ацетилиданиона, полученного из соединения формулы VIII (где Pg означает гидроксизащитную группу), с соответствующим кетоном, галогенкетоном (например, гексафторацетоном) и циклокетоном, и удалением защитной группы.
Схема 2а
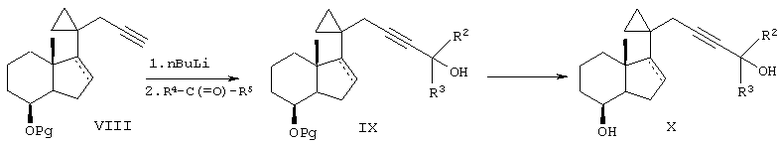
Затем аналогично тому, как показано на схеме 1а (т.е. окислением, введением гидроксизащитой группы и конденсацией), из соединения формулы Х получают соединение формулы I, содержащее ацетиленовый соединительный фрагмент.
Промышленная применимость
Соединения по настоящему изобретению применяются для профилактики и лечения различных состояний млекопитающих, при которые наблюдается потеря массы костной ткани. Все такие состояния называются "заболевания костной ткани" и более подробно описаны ниже. Соединения по настоящему изобретению предназначаются для профилактики и терапевтическрого лечения остеопороза и остеопении у млекопитающих, причем их применение не вызывает гиперкальциурии, гиперкальциемии и нефротоксичности. "Гиперкальциемия" означает избыточную концентрацию кальция в сыворотке; причем в организме человека (и крысы) это значение составляет более приблизительно 10,5 мг/дл. "Непереносимая гиперкальциемия", обычно наступающая при концентрации кальция в сыворотке более приблизительно 12 мг/дл, ассоциируется с эмоциональной неустойчивостью, дезориентацией во времени и пространстве, бредом, психозом, ступором и комой.
Соединения по настоящему изобретению применяются для лечения остеопороза типа I (постклимактерического), типа II (ятрогенного) и типа III (старческого), включая остеопороз, ассоциированный с лечением кортикостероидом (например, астмы), а также при лечении остеодистрофии при гемодиализе и гиперпаратиреоза. Лечение аналогами витамина D3, описанное в тексте заявки, приводит к увеличению плотности минеральной составляющей костной ткани и в отличие от обычных методов лечения к формированию прочной костной ткани. Следовательно, описанные способы лечения могут снизить вероятность перелома и привести к более быстрому заживлению имеющихся переломов. Такое лечение прежде всего применяется в отношении пациентов, которые в связи с отказом от приема эстрогена (например, пожилых женщин) попадают в группу риска и страдают от частых переломов. Типы излечиваемых переломов включают травматические и остеопорогенные переломы, например, переломы головки бедра, шейки бедренной кости, запястья, позвонков, позвоночника, ребер, грудины, гортани и трахеи, лучевой кости/локтя, большеберцовой кости, коленной чашечки, ключицы, таза, плечевой кости, ног, пальцев рук и пальцев стопы, травмы лица и голеностопного сустава.
Соединения по настоящему изобретению применяются также для лечения заболеваний, вызванных повышенным уровнем паратироидного гормона. С одной стороны, соединения по изобретению применяются для лечения вторичного гиперпаратиреоза, ассоциированного с почечной недостаточностью и прежде всего с обратимой или репонированной потерей костной ткани, ассоциированной с почечной недостаточностью. С другой стороны, изобретение включает лечение почечной остеодистрофии, ассоциированной с поздней стадией вторичного гиперпаратиреоза и лечение первичного гиперпаратиреоза.
Соединения формулы I применяются также для лечения опухолевых заболеваний, таких как лейкоз, рак толстой кишки, рак молочных желез и рак предстательной железы.
Обычно соединения по настоящему изобретению не приводят к повышенному уровню кальция, наблюдаемого при использовании других аналогов витамина D3, такого, как 1,25(ОН)2-витамин D3, и, следовательно, характеризуются улучшенным терапевтическим индексом или более эффективным лечением указанных выше заболеваний.
Способы введения и фармацевтические композиции
В общем случае, соединения по настоящему изобретению вводят в количестве от приблизительно 0,0002 до 0,5 мг/кг массы тела в сутки, предпочтительно от приблизительно 0,001 до приблизительно 0,1 мг/кг массы тела в сутки, более предпочтительно от приблизительно 0,002 до приблизительно 0,02 мг/кг массы тела в сутки, наиболее предпочтительно приблизительно от 0,005 до приблизительно 0,010 мг/кг массы тела в сутки. Для пациента массой 50 кг суточная доза активного ингредиента составляет от приблизительно 0,01 до приблизительно 25 мкг, предпочтительно от приблизительно 0,05 до приблизительно 10 мкг, наиболее предпочтительно от приблизительно 1,0 мкг до приблизительно 10 мкг в сутки. Указанную дозу можно вводить в составе фармацевтической композиции однократно, многократно или в виде композиции с контролируемым высвобождением, в соответствии с необходимостью достижения наиболее эффективных результатов, предпочтительно один или два раза в сутки пероральным способом. В некоторых случаях для достижения необходимого терапевтического результата может оказаться достаточной другая суточная доза.
Выбор точной дозы и композиции, а также наиболее пригодной схемы лечения зависит от фармакологических свойств состава, типа и тяжести патологического состояния, подлежащего лечению, физического и психического состояния пациента. В общем случае, при лечении остеопении, индуцированной кортикостероидами, требуемая доза выше при более высоких дозах используемых кортикостероидов.
Типичные способы доставки включают пероральный, парентеральный (включая подкожный, внутримышечный и внутривенный) способы введения, ректальный, трансбуккальный (включая сублингвальный), легочный, трансдермальный и назальный способы, наиболее предпочтительно пероральный. Ввведение можно проводить непрерывно или дробным введением (например, болюсной инъекцией).
Соответствующим объектом настоящего изобретения являются комбинационная терапия соединениями формулы I в сочетании с другими активными ингредиентами, такими как бифосфонаты, эстроген, SERMS (селективные модуляторы эстрогенового рецептора), кальцитонины или лечение анаболиками. Примеры бифосфонатов включают алендронат, ибандронат, памидронат, этидронат и ризедронат. Примеры SERMS включают ралоксифен, дигидроралоксифен и лазофоксифен. Кальцитонины включают кальцитонин человека и лосося. Анаболические агенты включают паратироидные гормоны (РТН), например, hPTH (1-34), РТН (1-84) и белки, родственные паратироидному гормону (PTHrP) и их аналоги. Конкретные аналоги PTHrP описаны в статье М. Chorev и др., Mono- and Bicyclic Analogs of Parathyroid Hormone-Related Protein. 1. Synthesis and Biological Studies, Biochemistry, 36, 3293-3299 (1997), и в патентах "Cyclic analogs РТН and PTHrP", WO 96/40193, US 5589452 и WO 97/07815. Другие активные агенты можно вводить одновременно, до или после соединения формулы I, причем такие агенты можно вводить иными способами.
Кроме того, объектом изобретения являются фармацевтические композиции, включающие в качестве активного ингредиента соединение по настоящему изобретению в смеси с фармацевтически приемлемым нетоксичным носителем. Как указано выше, такие композиции получают для парентерального (подкожного, внутримышечного и внутривенного) введения, прежде всего в форме жидких растворов или суспензий, для перорального или трансбуккального введения, прежде всего в форме таблеток или капсул, для легочного или интраназального введения, прежде всего в форме порошков, назальных капель или аэрозолей, и для ректального или чрескожного введения.
Композиции по настоящему изобретению можно вводить в виде стандартных доз и можно получать по любому методу, известному в фармацевтике, например, как описано в книге Remington's Pharmaceutical Sciences, 17th ed., Mack Publishing Company, Easton, PA (1985). Составы для парентерального введения могут содержать в качестве эксципиентов стерильную воду или солевой раствор, алкиленовые спирты, такие как пропиленгликоль, полиалкиленгликоли, такие как полиэтиленгликоль, масла растительного происхождения, гидрогенированные нафталины и т.п. Составы для интраназального введения могут быть твердыми и могут содержать эксципиенты, например, лактозу или декстран, или могут представлять собой водные или масляные растворы для применения в качестве назальных капель или дозированного аэрозоля. Для трансбуккального введения типичные эксципиенты включают сахара, стеарат кальция, стеарат магния, предварительно желатинизированный крахмал и т.п.
Композиции для перорального введения могут включать один или более физиологически совместимых носителей и/или эксципиентов и могут находиться в твердой или жидкой форме. Таблетки и капсулы получают смешиванием со связующими агентами, например, такими как сироп, аравийская камедь, желатин, сорбит, трагакант или поливинилпирролидон; наполнителями, такими как лактоза, сахароза, кукурузный крахмал, фосфат кальция, сорбит или глицин; замасливателями, такими как стеарат магния, тальк, полиэтиленгликоль или оксид кремния; и ПАВ, таким как лаурилсульфат натрия. Жидкие композиции могут включать соответствующие добавки, такие как суспендирующие агенты, например, сироп с сорбитом, метилцеллюлозу, сироп с сахарозой, желатин, карбоксиметилцеллюлозу или пищевые жиры; эмульгирующие агенты, такие как лецитин или аравийская камедь; растительные масла, такие как миндальное масло, кокосовое масло, жир печени трески или арахисовое масло; консерванты, такие как бутилированный гидроксианизол (ВНА) и бутилированный гидрокситолуол (ВНТ). Жидкие композиции можно инкапсулировать, например, в желативые капсулы для получения стандартных доз.
Предпочтительные твердые формы для перорального введения включают таблетки, двойные капсулы в твердой оболочке и мягкие эластичные желатиноые капсулы (SEG). Капсулы SEG представляют особый интерес, поскольу они обладают определенным преимуществом по сравнению с другими двумя формами (см. Seager H., Soft gelatin capsules: a solution to many tableting problems, Pharmaceutical Technology, 9 (1985)). Некоторые из преимуществ капсул SEG включают а) в капсулах SEG достигается оптимальная однородность распределения содержимого, поскольку лекарственное средство растворяется или диспергируется в жидкости, которую дозируют в капсулы достаточно точно, б) лекарственное средство в капсулах SEG обладает высокой биодоступностью, поскольку оно растворено, солюбилизировано или диспергировано в смешиваюшейся с водой жидкостью или в масле и, следовательно, высвобождается в организме в виде раствора, где растворяется или эмульгируется с образованием дисперсии, обладающей высокой площадью поверхности, в) предотвращается деградация лекарственного средства, которое чувствительно к окислению во время продолжительного хранения, поскольку сухая оболочка мягкой желатиновой капсулы препятствует диффузии кислорода.
Сухая оболочка состава обычно включает приблизительно от 40% до 60% желатина, приблизительно от 20% до 30% пластификатора (такого, как глицерин, сорбит или пропиленгликоль) и приблизительно от 30% до 40% воды. Кроме того, в облочке могут присутствовать другие материалы, такие как консерванты, красители, агенты, придающие непрозрачность, и ароматизаторы. Жидкое содержимое влючает твердое лекарственное средство, в растворенном, солюбилизированном или диспергированном состоянии (в присутствии диспергирующих агентов, таких, как пчелинный воск, гидрогенизированное касторовое масло или полиэтиленгликоль 4000), или жидкое лекарственное средство в носителе или комбинации носителей, таких как вазелин, растительные масла, триглицерилы, гликоли, полиолы и ПАВ.
Следующие примеры приведены с целью предоставить возможность специалисту в данной области более подробно ознакомиться с предлагаемым изобретением и использовать его на практике. Примеры приведены для иллюстрации изобретения и не ограничивают его объем.
Примеры
Следующие примеры приведены для иллюстрации изобретения и не ограничивают его объем.
Пример 1
В данном примере описан метод получения [1R-(1α(Е),3аβ,7аα)]октагидро-7а-метил-1-[5,5,5-трифтор-4-гидрокси-4-(трифторметил)-2-пентинил]циклопропил]-4Н-инден-4-ола.
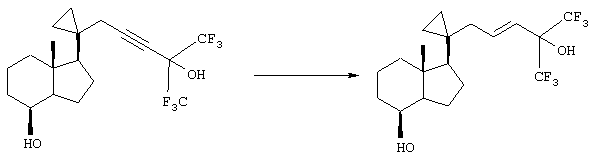
К перемешиваемой, охлажденной (5°С) суспензии LiAlH (237,2 мг, 6,25 ммоля) в безводном ТГФ (6,0 мл) добавляли порошкообразный NaOMe (338 мг, 6,25 ммоля). Смесь перемешивали в атмосфере аргона при 5°С в течение 15 мин, обрабатывали раствором [1R-(1α,3аβ,4α,7аα)]октагидро-7а-метил-1-[1-[5,5,5-трифтор-4-гидрокси-4-(трифторметил)-2-пентинил]циклопропил]-4Н-инден-4-ола (500 мг, 1,25 ммоля) в безводном ТГФ (6,0 мл), а затем кипятили с обратным холодильником в течение 2,5 ч. После охлаждения смесь разбавляли Et2О (25 мл), реакцию останавливали, добавляя по каплям воду (2,0 мл) и 2 М NaOH (2,0 мл), и перемешивали при комнатной температуре в течение 30 мин. Затем добавляли MgSO4 (5 г) и перемешивали в течение еще 30 мин. Смесь разбавляли Et2О (25 мл) и фильтровали через целит (15 г), который промывали EtOAc (3×20 мл). После упаривания получали смолу (508 мг), которую очищали экспресс-хроматографией (50 мг силикагеля, диаметр колонки 3,5 см, элюент: 30% EtOAc в гексане), при этом собирали фракции объемом 20 мл. После упаривания фракций 7-12 получали бесцветные кристаллы (486 мг), которые растирали с гексаном и отделяли фильтрованием, при этом получали указанное в заголовке соединение (442 мг, 88%). tпл. 122-123°С, [α]D+42,1° (EtOH, с 0,80).
MC: m/z 400 (М+, 10).
ИК-спектр: 3540, 1602, 965 см-1.
1Н ЯМР: δ 0,05 (1Н, m), 0,27 (1H, m), 0,34 (1H, m), 0,74 (1H, m), 0,98 (1H, m), 1,00 (3H, s), 1,17-1,25 (2H, m), 1,35-1,60 (6H, m), 1,65 (1H, dd, J 12,5), 1,75-1,87 (3H, m), 2,02 (1H, d, J 11), 2,78 (1H, dd, J 14, 8,5), 2,92 (1H, s, ОН), 4,05 (1H, ушир. s), 5,59 (1H, d, J 16), 6,30 (1H, ddd, J 16, 8,5, 6).
Элементный анализ:
рассч. для C19H26F6O2: С 56,99, Н 6,55, F 28,47,
найд.: С 56,87, Н 6,33, F 28,69.
Пример 2
В данном примере описан метод получения [1R-(1α(Е),3аβ,7аα)]октагидро-7а-метил-1-[1-[1-[5,5,5-трифтор-4-гидрокси-4-(трифторметил)-2-пентинил]цикло-пропил]-4Н-инден-4-она.
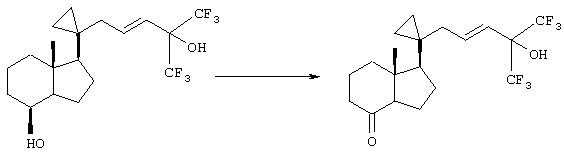
К перемешиваемому раствору [1R-(1α(Е),3аβ,4α,7аα)]октагидро-7а-метил-1-[5,5,5-трифтор-4-гидрокси-4-(трифторметил)-2-пентинил]циклопропил]-4Н-инден-4-ола (400 мг, 1,00 ммоля) в СН2Cl2 (8,0 мл) добавляли порошкообразный бихромат пиридиния (1,25 г, 3,3 ммоля). Смесь перемешивали при комнатной температуре в течение 4,5 ч, разбавляли диизопропиловым эфиром (15 мл) и обрабатывали в стандартных условиях, при этом получали 395 мг бесцветной смолы. Затем проводили экспресс-хроматографию (50 г силикагеля, колонка диаметром 3,5 см, элюент: 30% EtOAc в гексане), собирая фракции объемом 20 мл, и после упаривания фракций 7-12 получали указанное в заголовке соединение (376 мг, 94%) в виде бесцветных кристаллов. tпл 79-80°C, [α]D+6,9° (EtOH, с 1,00).
МС: m/z 398 (М+, 20).
ИК-спектр: 3334, 1704, 964 см-1.
1Н ЯМР: δ 0,14 (1Н, m), 0,33 (1H, m), 0,69 (1H, m), 0,70 (3H, s), 1,46-1,80 (5H, m), 1,91-2,30 (6H, m), 2,44 (1H, dd, J 11,6), 2,74 (1H, dd, J 15, 8,5), 2,98 (1H, s, ОН), 5,62 (1H, d, J 15), 6,33 (1H, ddd, J 15, 8,5, 6).
Элементный анализ:
рассч. для С19Н24F6О2: С 57,28, Н 6,07, F 28,61,
найд.: С 57,19, Н 6,25, F 28,71.
Пример 3
В данном примере описан метод получения [1R-(1α(Е),3aβ,7аα)]октагидро-7а-метил-1-[1-[5,5,5-трифтор-4-трифторметил-4-[(триметилсилил)окси]-2-пентинил]циклопропил]-4Н-инден-4-она.
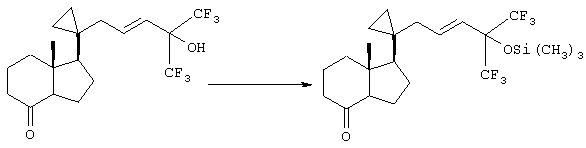
К перемешиваемому раствору [1R-(1α(Е),3аβ,7аα)]октагидро-7а-метил-1-[1-[5,5,5-трифтор-4-гидрокси-4-трифторметил-2-пентинил]циклопропил]-4Н-инден- 4-она (165 мг, 0,41 ммоля) в безводном СН2Cl2 (5,0 мл) добавляли 1-(триметилсилил)имидазол (0,5 мл, 3,4 ммоля) и полученную смесь перемешивали в течение 5 ч. После стандартной обработки получали указанное в заголовке неочищенное соединение (193 мг). После экспресс-хроматографии (25 г силикагеля, элюент: 20% EtOAc в гексане) получали указанное в заголовке соединение (161 мг, 83%) в виде масла;
[α]D +3,4° (CHCl3, c 1,0).
МС: m/z 470 (М+, 33).
ИК-спектр: 1706 см-1.
1Н ЯМР: δ 0,13 (1Н, т), 0,22 (9Н, s), 0,32 (1Н, т), 0,67 (1H, т), 0,70 (3Н, s), 1,10 (1H, т), 1,50-2,40 (11H, т), 2,44 (1H, dd, J 11,6), 2,68 (1H, dd, J 16, 8,5), 5,57 (1H, d, J 16), 6,16 (1H, ddd, J 16, 8,5, 6).
Элементный анализ:
рассч. для C22H32F6Si: С 56,15, Н 6,85, F 24,22,
найд.: С 56,42, Н 6,63, F 24,37.
Пример 4
В данном примере описан метод получения 3-дезокси-1,25-дигидрокси-20-метил-23-(Е)-ен-26,27-гексафтор-21,28-циклохолекальциферола.

Реагент Хорнера [R-(Z)][2-[3-[[(1,1-диметилэтил)диметилсилил]-окси]-2-метиленциклогексилиден]этил]дифенилфосфиноксид (395 мг, 0,872 ммоля) в безводном ТГФ (5,0 мл) депротонировали в присутствии 1,6 М раствора н-BuLi в гексане (0,55 мл, 0,88 ммоля) при -78°С в течение 8 мин, после чего проводили реакцию с кетоном [1S-(1α(Е),3аβ,7аα)]октагидро-7а-метил-1-[1-[5,5,5-трифтор-4-(трифторметил)-4-[(триметилсилил)окси]-2-пентенил]циклопропил]-4Н-инден-4-оном (170 мг, 0,361 ммоля) в безводном ТГФ (2,0 мл) в течение 3 ч и выделяли продукт. После экспресс-хроматографии (45 г силикагеля, элюент: 20% EtOAc в гексане) получали смолу (215 мг), которую растворяли в ТГФ (3 мл), обрабатывали 1,0 М раствором н-Bu4N+F- в ТГФ (2,8 мл) и перемешивали в течение 19 ч. Смолу очищали экспресс-хроматографией (40 г силикагеля, элюент: 40% EtOAc в гексане), продукт получали в виде смолы, которую растворяли в НСО Me (5,0 мл), раствор фильтровали через фильтр с диаметром пор 0,45 мкм и упаривали. Остаток высушивали в высоком вакууме (3 ч), при этом получали указанное в заголовке соединение (144 мг) в виде бесцветной пены. [α]D 4,0° (МеОН, с 0,35).
МС (FAB) m/z 535 (M+ +H).
УФ-спектр: λmax 265 (ε 15,837), 211 (ε 14,458) нм.
ИК-спектр: 3598, 1651 см-1.
1Н ЯМР: δ 0,11 (1Н, m), 0,29 (2Н, m), 0,60 (3Н, s), 0,61 (1H, m), 1,10 (1H, m), 1,21-1,35 (1H, m), 1,50 (6H, m), 1,70 (2H, m), 1,90 (2Н, m), 2,00 (3Н, m), 2,30 (2Н, m), 2,60 (1H, d, J 12), 2,85 (2H, m), 2,90 (1H, s), 4,22 (1H, s), 4,42 (1H, s), 4,99 (1H, s), 5,32 (1H, s), 5,42 (1H, d, J 12), 5,99 (1H, d, J 11), 6,10 (1H, ddd, J 12, 7, 6), 6,36 (1H, d, J 11).
Пример 5
В данном примере описан метод получения 3-дезокси-1,25-дигидрокси-20-метил-23-(2)-ен-26,27-гексафтор-21,28-циклохолекальциферола.
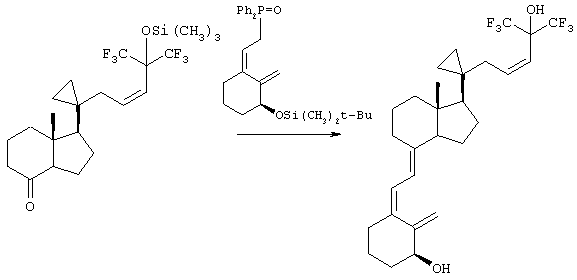
Реагент Хорнера [R-(Z)][2-[3-[[(1,1-диметилэтил)диметилсилил]окси]-2-метиленциклогексилиден]этил]дифенилфосфиноксид (236 мг, 0,5 ммоля) в ТГФ (3,0 мл) обрабатывали 1,6 М раствором н-BuLi в гексане (0,32 мл, 0,512 ммоля) в течение 8 мин, затем добавляли кетон [1S-(1α(г),3аβ,7аα)]октагидро-7а-метил-1-[1-[5,5,5-трифтор-4-(трифторметил)-4-[(триметилсилил)окси]-2-пентенил]циклопропил]-4Н-инден-4-он (117,5 мг, 0,25 ммоля) в ТГФ (2,0 мл) и перемешивали в течение еще 2,5 ч. После обработки реакционной смеси получали смолу, которую очищали экспресс-хроматографией (40 г силикагеля, элюент: 20% EtOAc в гексане). При этом получали смолу (120 мг), которую растворяли в ТГФ (2,0 мл), обрабатывали 1 М раствором н-Ви N F в ТГФ (2,0 мл) и перемешивали при комнатной температуре в течение 20 ч. Полученный продукт очищали экспресс-хроматографией (40 г силикагеля, элюент: 40% EtOAc в гексане), при этом получали указанное в заголовке соединение (29 мг) в виде бесцветной пены. [α]D -41° (МеОН, с 0,14).
MC: m/z 518 (M+, 22).
ИК-спектр: 3569 см-1.
УФ-спектр: λmax 214 (10,968), 219 (12,931), 259 (12,818) нм.
1H ЯМР: δ 0,02 (1Н, m), 0,32 (2Н, m), 0,60 (1Н, m), 0,61 (3Н, s), 1,1-1,7 (11Н, m), 1,85 (2Н, m), 2,0 (3Н, m), 2,2 (3Н, m), 2,85 (3Н, m), 4,12 (1Н, ушир. s), 4,90 (1Н, s), 5,30 (1Н, s), 5,40 (1Н, d, J 12,8), 6,0 (1Н, d, J 11), 6,12 (1Н, dd, J 12,8, 6,8), 6,29 (1Н, d, J 11), 6,12 (1Н, dd, J 12,8, 6,8), 6,29 (1Н, d, J 11).
Пример 6
В данном примере описан метод получения 3-дезокси-1,25-дигидрокси-20-метил-23-ин-21,28-циклохолекальциферола.
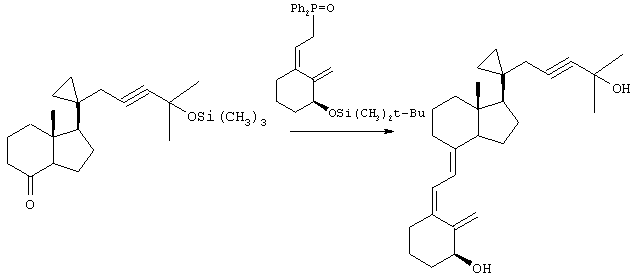
Реагент Хорнера [R-(Z)][2-[3-[[(1,1-диметилэтил)диметилсилил]окси]-2-метиленциклогексилиден]этил]дифенилфосфиноксид (375 мг, 0,828 ммоля) в ТГФ (5,0 мл) обрабатывали 1,6 М раствором н-BuLi в гексане (0,51 мл, 0,81 ммоля) в течение 8 мин, а затем добавляли [1R-(1α,3аβ,7аα)]октагидро-7а-метил-1-[4-метил-4-[(триметилсилил)окси]-2-пентинил]циклопропил]-4Н-инден-4-он (180 мг, 0,50 ммоля) в ТГФ (4,0 мл) и смесь обрабатывали через 3,5 ч. После экспресс-хроматографии (45 г силикагеля, элюент: 7% EtOAc в гексане) получали сироп (273 мг), который растворяли в ТГФ (3,3 мл) и перемешивали в смеси с 1,0 М раствором н-Bu4N+F- в ТГФ (3,3 мл) в течение 28 ч. Продукт очищали экспресс-хроматографией (45 г силикагеля, элюент: 40% EtOAc в гексане), при этом получали указанное в заголовке соединение (114 мг) в виде бесцветной пены. [α]D -70,32° (EtOH, с 0,539).
МС: m/z 408,9 (М+, 60).
УФ-спектр: λmax 215 (ε 13,326), 262 (ε 17,661) нм.
ИК-спектр: 3601 см-1.
1H ЯМР: δ 0,28 (2Н, m), 0,41 (1H, m), 0,59 (1H, m), 0,60 (3H, s), 1,10 (1H, m), 1,50 (6H, s), 1,55-2,0 (18H, m), 2,09 (1H, d, J 17), 2,22 (2Н, m), 2,60 (1H, d, J 17), 2,80 (1H, d, J 11), 4,11 (1H, ушир. s), 4,91 (1H, s), 5,30 (1H, s), 5,99 (1H, d, J 11), 6,27 (1H, d, J 11).
Пример 7
В данном примере описан метод получения 3-дезокси-1,25-дигидрокси-20-метил-23-ин-26,27-гексафтор-21,28-циклохолекальциферола.
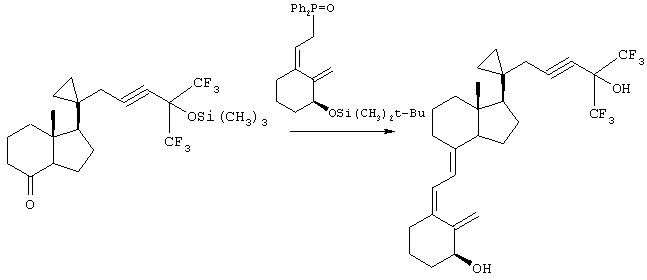
Реагент Хорнера [R-(Z)][2-[3-[[(1,1-диметилэтил)диметилсилил]окси]-2-метиленциклогексилиден]этил]дифенилфосфиноксид (350 мг, 0,773 ммоля) в ТГФ (5,0 мл) депротонировали 1,6 М раствором н-BuLi в гексане (0,49 мл, 0,784 ммоля) при -78°С в течение 8 мин, а затем обрабатывали кетоном [1S-(1α,3аβ,7аα)]октагидро-7а-метил-1-[1-[5,5,5-трифтор-4-гидрокси-4-(трифторметил)-2-пентинил]цикло-пропил]-4Н-инден-4-оном (158 мг, 0,40 ммоля) в течение 3,0 ч. Неочищенный продукт очищали экспресс-хроматографией (45 г силикагеля, элюент: 20% EtOAc в гексане) и десилилировали в 1 М растворе н-Bu4N+F- в ТГФ (1,8 мл) при комнатной температуре в течение 18 ч. Продукт очищали экспресс-хроматографией (45 г силикагеля, элюент: 40% EtOAc в гексане), при этом получали указанное в заголовке соединение (117 мг) в виде бесцветной пены. [α]D -58,3° (EtOH, с 0,456).
МС: m/z 516,2 (M+, 90).
УФ-спектр: λmax 214 (s 12,900), 260 (в 15,701) нм.
1Н ЯМР: δ 0,29 (1H, m), 0,35 (1H, m), 0,37 (1H, m), 0,59 (3H, s), 0,64 (1H, m), 1,4-1,90 (12H, m), 2,00 (4H, m), 2,18 (1H, d, J 17), 2,25 (2H, m), 2,72 (1H, d, J 17), 2,81 (1H, m), 3,34 (1H, s, ОН), 4,12 (1H, ушир. s), 4,92 (1H, s), 5,28 (1H, s), 5,98 (1H, d, J 11), 6,27 (1H, d, J 11),
Пример 8
В данном примере описан метод получения 3-дезокси-1,25-дигидрокси-20-метил-21,28-циклохолекальциферола.
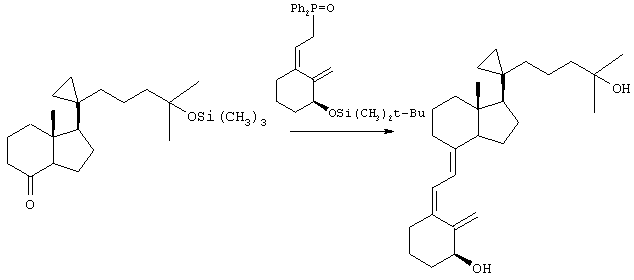
В трехгорлую круглодонную колбу объемом 25 мл с магнитной мешалкой, снабженную термометром, резиновой мембраной в боковой части и насадкой Кляйзена, содержащей отвод для подачи азота и центральную резиновую мембрану, загружали 0,564 г (1,246 ммоля) [R-(Z)][2-[3-[[(1,1-диметилэтил)-диметилсилил]окси]-2-метиленциклогексилиден]этил]дифенилфосфиноксида. Указанный материал сушили в высоком вакууме, добавляли 5 мл ТГФ, раствор перемешивали, охлаждали до -70°С и добавляли 0,78 мл (1,246 ммоля) 1,6 М BuLi в гексане. (После добавления первых 0,16 мл реагента наблюдается устойчивое красное окрашивание раствора). Раствор перемешивали при -70°С в течение 10 мин, а затем добавляли по каплям раствор 0,2904 г (0,796 ммоля) [1S-(1α,3аβ,7аα)] октагидро-7а-метил-1-[1-[4-метил-4-окси]-2-пентанилциклопропил]-4Н-инден-4-она в 8 мл ТГФ. После завершения реакции (по данным ТСХ, элюент: этилацетат/гексан 1:9) смесь нагревали до -30°С, через центральное отверстие добавляли по каплям 12 мл фосфатного буферного раствора, рН 7 (139,4 г однозамещенного фосфата калия в 400 мл воды и 10 мл 2 М раствора фосфорной кислоты). Смесь перемешивали в течение 5 мин, переносили в делительную воронку в смеси с 35 мл гексана и водную фазу вторично экстрагировали 30 мл гексана. Два слоя гексана объединяли, промывали 20 мл солевого раствора, сушили фильтрованием через слой сульфата натрия и упаривали до получения бесцветного сиропа. Указанный материал переносили в гексан, при этом получали суспензию твердого вещества белого цвета в гексане, которую фильтровали через экспресс-колонку (25×120 мм). После сбора двух фракций объемом по 20 мл каждая элюент заменяли на этилацетат/гексан, 1:79. Фракции 11-18 объединяли (по данным ТСХ, элюент: этилацетате/гексан, 1:19) и упаривали, при этом получали 0,4202 г (88,1%) силилированного соединения, указанного в заголовке.
В круглодонную колбу объемом 100 мл из коричневого стекла загружали 0,4202 г силилированного соединения, указанного в заголовке, добавляли 5 мл ТГФ и 3,5 мл 1 М раствора фторида тетрабутиламмония в ТГФ и перемешивали при комнатной температуре в течение 17 ч, после чего при анализе пробы методом ТСХ (элюент: этилацетат/гексан, 1:1, и этилацетат) наблюдали одно пятно основного продукта. Реакционную смесь разбавляли 13 мл солевого раствора, перемешивали в течение 15 мин и переносили в делительную воронку в смеси с 40 мл этилацетата. Водный слой вторично экстрагировали 20 мл этилацетата. Оба органических слоя объединяли, промывали водой (5×35 мл) и солевым раствором, пропускали через слой сульфата натрия и упаривали до получения кристаллического остатка белого цвета (0,3523 г). Полученный материал очищали хроматографией на колонке (25×110 мм, элюент: этилацетат/гексан, 1:1), при этом во фракциях 3-4 продукт кристаллизовался непосредственно в пробирках. Полученную суспензию концентрировали до приблизительно 5 мл, разбавляли гексаном, концентрировали и фильтровали, при этом получали указанное в заголовке соединение в виде кристаллов (0,2567 г), [α]D -59,1° (с 0,325, EtOH).
УФ-спектр: λmax (MeOH) 214, 262, λплечо 222 нм.
Элементный анализ:
рассч. для С28Н44О: С 81,50, Н 10,75, О 7,75,
найд.: С 81,43, Н 10,69, О 7,48.
Примеры соединений формулы I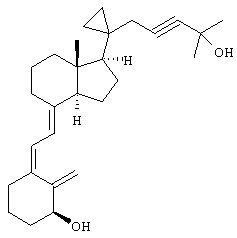
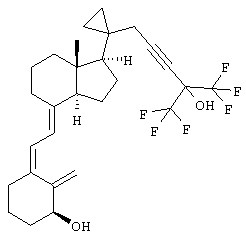
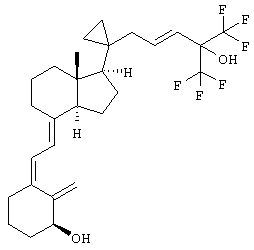
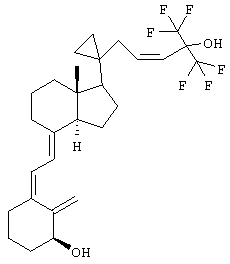
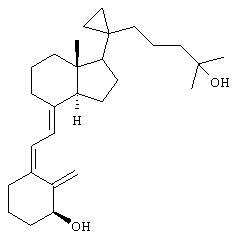
В приведенных выше соединениях по свободной валентности атома кислорода присоединен атом водорода.
Пример 9
В данном примере описан метод получения 3-дезокси-1α-ацетокси-25-гидрокси-20-циклопропил-23Е-ен-26,27-гексафторхолекальциферола.
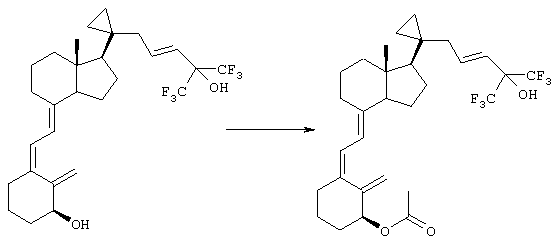
В круглодонную колбу объемом 25 мл загружали 0,1702 г 3-дезокси-1α,25-дигидрокси-20-циклопропил-23Е-ен-26,27-гексафторхолекальциферола и 2,85 г пиридина. Раствор перемешивали и охлаждали на ледяной бане, затем добавляли 0,5 мл уксусного ангидрида, перемешивали при охлаждении на ледяной бане в течение еще 1 ч, а затем раствор выдерживали в холодильнике в течение ночи. Колбу вновь помещали в ледяную баню, добавляли 0,2 мл уксусного ангидрида и выдерживали в течение 6 ч. Затем при охлаждении на ледяной бане реакционную смесь разбавляли 10 мл этилацетата, добавляли 2 мл воды, перемешивали в течение 5 мин и переносили в делительную воронку в смеси с 20 мл воды и 20 мл этилацетата/гексана, 1:4. Водную фазу вторично экстрагировали 10 мл этилацетата/гексана, 1:4. По данным ТСХ (элюент: этилацетат/гексан, 1:2) второй экстракт не содержал продукта реакции. Поэтому первый экстракт промывали водой (4×20 мл), 10 мл солевого раствора, пропускали через слой сульфата натрия и упаривали. Остаток переносили в этилацетат/гексан, 1:4, и очищали экспресс-хроматографию на колонке (15×150 мм, элюент: этилацетат/гексан, 1:4), собирая фракции по 10 мл. При этом основное количество продукта (0,1050 г) содержалось во фракции 3. Однако во фракции 3 присутствовали следы материала с меньшим временем удерживания (из фракции 2). При попытке растворить остаток в этилацетате/гексане, 1:6, наблюдался процесс кристаллизации. Поэтому после добавления небольшого количества пентана смесь кристаллизовали в холодильнике. Маточный раствор отделяли и упаривали (0,0068 г). Кристаллы однократно промывали пентаном и сушили, при этом получали 0,0899 г указанного в заголовке соединения, [α]D -30,8° (0,54%, МеОН).
УФ: λmax (погл.) 121 (0,3639), 250 (0,4591), 262 (4486), λплечо 244 (0,4482) нм. ЯМР (CDCl3): 2,07 (ОАс).
Элементный анализ:
рассч.: С 64,27, Н 6,83;
найд.: С 64,63, Н 6,93; С 64,52, Н 6,94.
Пример 10
В данном примере описан метод получения 3-дезокси-1α,25-диацетокси-20-циклопропил-23Е-ен-26,27-гексафторхолекальциферола.
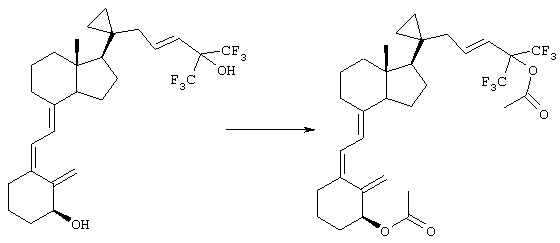
В круглодонную колбу объемом 25 мл, снабженную магнитной мешалкой и насадкой Клайзена, содержащей отвод для подачи азота и пробку, загружали 0,315 г (0,6 ммоля) 3-дезокси-1α,25-дигидрокси-20-циклопропил-26,27-гексафтор-холекальциферола, 60 мг диметиламинопиридина и 5 мл пиридина, причем пиридин добавляли после погружения колбы в ледяную баню. Через 10 мин добавляли по каплям 1,0 мл уксусного ангидрида и перемешивали при охлаждении на ледяной бане. Через 1 ч в реакционной смеси исходный материал не обнаруживался. Через 2 ч в раствор разбавляли 10 мл этилацетата и через 10 мин при охлаждении на ледяной бане добавляли по каплям 2 мл воды. Смесь перемешивали в течение 10 мин и переносили в делительную воронку в смеси с 20 мл воды и 20 мл этилацетата/гексана, 1:4. Водную фазу вторично экстрагировали 10 мл этилацетата/гексана, 1:4. По данным ТСХ (элюент: этилацетат/гексан, 1:2) второй экстракт не содержал продукта реакции. Поэтому первый экстракт промывали водой (4×20 мл), солевым раствором (20 мл), а затем пропускали через слой сульфата натрия и упаривали. Остаток переносили в этилацетат/гексан, 1:6, и очищали экспресс-хроматографией на колонке (25×150 мм, элюент: этилацетат/гексан, 1:6), собирая фракции объемом 20 мл. Чистый продукт содержался во фракции 3, во фракциях 4-6 содержался продукт с примесью компонентов, которые характеризуются меньшей скоростью миграции (по данным ТСХ, элюент: этилацетат/гексан, 1:2). Поэтому фракции 4-6 собирали, упаривали, остаток очищали хроматографией вторично (колонка: 15×150 мм, элюент: этилацетат/гексан, 1:9), собирая фракции объемом 20 мл. Основное количество очищенного продукта содержалось во фракциях 2 и 3. Указанные фракции объединяли с фракцией 3, полученной после первой хроматографии, и упаривали. Остаток переносили в этилацетат/гексан, 1:9, фильтровали и концентрировали, разбавляли пентаном и хранили в холодильнике. Маточный раствор отделяли, кристаллы промывали пентаном и сушили в высоком вакууме в течение 2 ч, при этом получали 0,190 г указанного в заголовке соединения.
ЯМР (CDCl3): δ 2,08 и 2,20 (2OАс).
[α]D -110,3° (0,59%, МеОН).
УФ-спектр: λmax (погл.) 212 (0,3573), 251 (0,4392), 261 (0,4276) нм.
Элементный анализ:
рассч.: С 63,78, Н 6,69,
найд.: С 63,99, Н 6,62.
Пример 11
В данном примере описан метод определения эффективности соединений по настоящему изобретению при лечении костного анаболизма у крыс.
Крысам возрастом три месяця удаляли яичники (OVX) и вводили перорально либо 1,25-дигидроксивитамин D3, либо одно из соединений по настоящему изобретению один раз в сутки, начиная через 3 недели после операции по удалению яичников и до умерщвления через 6 недель после операции. Контрольные группы животных, крысы после фиктивной операции и крысы после операции OVX, получали только наполнитель. Через 4 и 6 недель после операции у крыс отбирали образцы крови и мочи и определяли количество кальция в крови и моче. После умерщвления определяли конечное количество кальция в бедренной кости через 6 недель после операции.
Плотность минеральной составляющей в правой берцовой кости определяли на костном денситометре QDR-1000W (фирмы Hologic, Walthan, MA) с использованием программного обеспечения высокого разрешения. Животных сканировали, помещая в блок для сканирования в положении лежа на спине таким образом, чтобы правая нога была расположена перпендикулярно телу, а большая берцовая кость была перпендикулярна бедру.
Пример 12
В данном примере описан метод определения эффективности соединений
по настоящему изобретению in vivo по сравнению с 1,25-(ОН)2-витамином D3.
Сравнение эффективности соединений по настоящему изобретению с эффективностью 1,25-дигидроксивитамином D3 можно проводить на стандартной модели животных с постклимактерическим остеопорозом, а именно на модели крыс с удаленными яичниками. Крысам возрастом 3 месяца удаляли яичники, а затем лечили в течение 8 недель, начиная через 1 неделю после операции OVX. Лекарственные средства вводили один раз в сутки перорально в миглиоле (средне-цепочечный триглицерид). Образцы крови и мочи отбирали через 3 и 6 недель, минеральную плотность кости (BMD) определяли in vivo через 6 недель с использованием абсорбциометрии и рентгеновского излучения (Dual Energy X-ray, прибор для сканирования костей фирмы Hologic QDR-4500). Через 8 недель животных забивали и извлекали поясничные позвонки и бедренную кость для определения BMD ex vivo (сканнер Lunar PixiMus Bone Scanner) и испытаний на биомеханическую прочность. Затем для каждого соединения определяли данные, соответствующие самой высокой безопасной дозе. Самая высокая безопасная доза означает дозу соединения, при которой не наблюдается гиперкальциемии (при этом заболевании содержание кальция в сыворотке крови составляет более 10 мг/дл).
Пример 13
В данном примере описан метод определения эффективности in vivo соединения 27 по сравнению с 1,25-(ОН)2-витамином D3.
Сравнение эффективности действия соединения 27 с действием 1,25-дигидроксивитамина D3 (VD3) проводили на стандартной модели животных с постклимактерическим остеопорозом, а именно на модели крыс с удаленными яичниками. Крысам возрастом 3 месяца массой 285 г удаляли яичники (OVX), a затем лечили в течение 8 недель, начиная через 1 неделю после операции OVX. Лекарственные средства вводили один раз в сутки перорально миглиоле (триглицерид со средним размером цепи). Образцы крови и мочи отбирали через 3 и 6 недель, минеральную плотность кости (BMD) определяли in vivo через 6 недель с использованием абсорбциометрии и рентгеновского излучения (Dual Energy X-ray, прибор для сканирования костей фирмы Hologic QDR-4500). Через 8 недель животных забивали и извлекали поясничные позвонки и бедренную кость для определения BMD ex vivo (сканнер Lunar PixiMus Bone Scanner) и испытаний на биомеханическую прочность. Данные для каждого соединения, соответствующие самой высокой безопасной дозе, приведены в прилагаемых таблицах. Самая высокая безопасная доза означает дозу соединения, которая не вызывает гиперкальциемии (при этом заболевании содержание кальция в сыворотке крови составляет более 10 мг/дл).
В таблице 3 представлены результаты безопасного действия (содержание кальция в сыворотке и содержание кальция в моче). При введении всех сравниваемых доз уровни кальция в сыворотке через 3 недели составляли 9,3 мг/дл и через 6 недель 9,8±0,1 мг/дл. Выброс кальция в моче через 24 ч был идентичен при введении витамина D3 в дозе 0,4 нмоль/кг и введении соединения 27 в дозе 0,5 нмоль/кг. В таблице 4 приведены параметры эффективности (BMD, биомеханические свойства и содержание дезоксипиридинолинов в моче) для двух соединений. Величина BMD для всех перечисленных костных тканей значительно выше у животных, которым вводили соединение 27, по сравнению с животными, которым вводили витамин D3 в дозах, при которых наблюдается эквивалентные уровни кальция в сыворотке крови. Ожидается, что при этих дозах достигается максимальная эффективность и безопасность действия, так как известно, что более высокие дозы каждого соединения вызывают гиперкальциемию. При введении соединения 27 содержание дезоксипиридинолинов, как маркеров резорбции кости, через 6 недель значительно ниже по сравнению с введением витамина D3, что свидетельствует о более высокой способности соединения 27 ингибировать резорбцию кости. Лечение соединением 27 приводит к повышению прочности кости позвонков. Величину разрушающей нагрузки, то есть силу, необходимую для разрушения позвонка L5, определяли методом осевого сжатия. Сила, необходимая для разрушения позвонков животных, которых лечили соединением 27, значительно выше по сравнению с лечением витамином D при самых высоких безопасных дозах.
Сравнение безопасного действия соединения 27 и 1,25-дигидроксивитамина D3 (VitD)
(мг/дл)
SEM
число жив. в группе
0,1
10
0,1
10
0,1
10
0,1
10
0,1
0
SEM
число жив. в группе
0,1
10
0,1
10
0,1
10
0,1
9
0,2
10
SEM
число жив. в группе
0,02
10
0,05
10
0,04
10
0,05
10
10
SEM
число жив. в группе
0,03
10
0,05
10
10
0,05
9
10
н/о - нет достоверного отличия
* - p<0,05, ** - p<0,01 по сравнению с контролем OVX
+ - p<0,05, ++ - p<0,01 по сравнению с контролем OVX
$ - p<0,05, $$ - p<0,01 по сравнению с Vit-D
Сравнение эффективности действия соединения 27 и 1,25-дигидроксивитамина D3 (VitD)
SEM
число жив. в группе
1,9
9
1,6
9
1,6
10
1,6
9
2,1
10
SEM
число жив. в группе
1,2
9
1,2
9
2,3
10
1,4
9
2,0
10
SEM
число жив. в группе
1,1
10
0,8
10
1,7
10
1,7
9
1,1
10
SEM
число жив. в группе
1,5
9
1,4
9
1,7
10
1,5
9
1,2
10
SEM
число жив. в группе
1,2
9
1,1
9
1,8
10
9
1,3
10
SEM
число жив. в группе
10
0,002
7
0,003 9
0,002
10
SEM
число жив. в группе
0,001
10
7
0,002 9
0,001
10
27
SEM
число жив. в группе
0,04
10
10
0,09
9
9
0,09
10
SEM
число жив. в группе
0,03
10
10
10
8
0,06
10
SEM
число жив. в группе
32
7
20
6
26
9
23
10
SEM - стандартное отклонение
н/о - нет достоверного отличия
* - р<0,05, ** - р<0,01 по сравнению с контролем OVX
+ - р<0,05, ++ - р<0,01 по сравнению с контролем OVX
$ - р<0,05, $$ - р<0,01 по сравнению с Vit-D
Соединения по настоящему изобретению обладают биологической активностью, сопоставимой с активностью соединения 27.
Настоящее изобретение описано со ссылкой на иллюстрации и примеры с целью пояснения и понимания сущности изобретения. Для специалиста в данной области представляется очевидным, что в пределах объема и заявленных пунктов формулы изобретения возможны различные изменения и модификации. Следовательно, предполагается, что описание заявки лишь иллюстрирует изобретение и не ограничивает его объем. Объем изобретения определяется со ссылкой на заявленные пункты формулы изобретения, включая весь объем эквивалентов, на который претендуют указанные пункты.
Патенты, патентные заявки и публикации, цитированные в описании, включены в текст заявки в качестве ссылки в полном объеме в каждом случае в той же степени, как, если бы каждый патент, патентная заявка и публикация цитировались отдельно.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И СПОСОБЫ, ВКЛЮЧАЮЩИЕ КОМБИНАЦИИ 2-АЛКИЛИДЕНОВЫХ ПРОИЗВОДНЫХ 9-НОР-ВИТАМИНА D И БИСФОСФОНАТА | 2004 |
|
RU2326695C2 |
| СПОСОБ И КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ | 2006 |
|
RU2440338C2 |
| АНАЛОГИ ВИТАМИНА D3 | 2000 |
|
RU2235721C2 |
| ПРОИЗВОДНЫЕ АМИДА ВИТАМИНА D И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1992 |
|
RU2139276C1 |
| ПРОИЗВОДНЫЕ АНТРАЦИКЛИНОНА И ИХ ИСПОЛЬЗОВАНИЕ ПРИ АМИЛОИДОЗЕ | 1995 |
|
RU2167661C2 |
| СУЛЬФОНИЛАМИНОКАРБОНОВЫЕ КИСЛОТЫ | 1998 |
|
RU2193027C2 |
| СТЕРОИДЫ, ВЫСВОБОЖДАЮЩИЕ ОКСИД АЗОТА | 2008 |
|
RU2442790C2 |
| НОВЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ ФТОРГЛИКОЗИДНЫЕ ПРОИЗВОДНЫЕ, СОДЕРЖАЩИЕ ЭТИ СОЕДИНЕНИЯ ЛЕКАРСТВЕННЫЕ СРЕДСТВА И ИХ ПРИМЕНЕНИЕ | 2003 |
|
RU2339641C2 |
| Производные фосфиновых и фосфоновых кислот, способ их получения и фармацевтическая композиция на их основе | 1999 |
|
RU2224762C2 |
| ЗАМЕЩЕННЫЕ ДИАМИНОКАРБОНОВЫЕ КИСЛОТЫ | 1998 |
|
RU2196768C2 |
Описаны соединения общей формулы (I) или их соли, где пунктирная линия необязательно означает двойную связь, L означает фрагмент из группы, включающей -СН2-СН2-СН2-, -СН2-СН=СН- и -СН2-С≡С-, каждый R2 и R3 независимо алкил или галогеналкил, a R1 и R4 независимо водород, ацильная группа или гидроксизащитная группа, при условии, что по меньшей мере один из R1 и R4 - ацильная группа. Изобретение также относится к применению соединений формулы (I) или их солей в качестве лекарственных средств для лечения гиператиреоза, почечной остеодистрофии или остеопороза. 4 н. и 24 з. п. ф-лы, 4 табл.
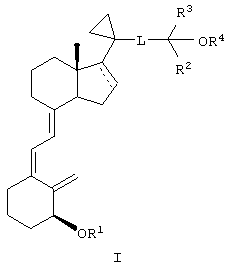
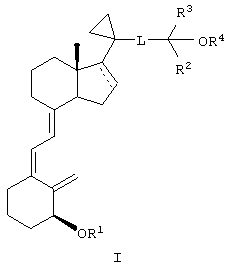
или его соль,
где пунктирная линия необязательно означает двойную связь,
L означает соединительный фрагмент, выбранный из группы, включающей -СН2-СН2-СН2-, -СН2-СН=СН- и -СН2-С≡С-,
каждый R2 и R3 независимо означает алкил или галогеналкил, а
каждый R1 и R4 независимо означает водород, ацильную группу или другую гидроксизащитную группу,
при условии, что по меньшей мере один из R1 и R4 означает ацильную группу.
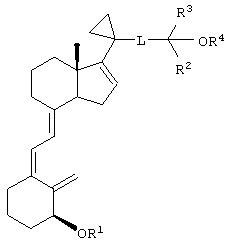
где R1, R2, R3, R4 и L имеют значения, указанные в п.1.
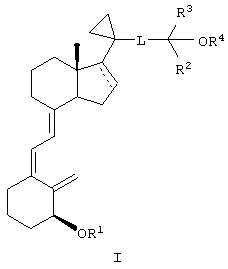
где L выбирают из группы, включающей -СН2-СН2-СН2-, -СН2-СН=СН- и -СН2-С≡С-.
[1R-(1α(Е),3aβ,7aα)]-октагидро-7а-метил-1-[5,5,5-трифтор-4-гидрокси-4-(трифторметил)-2-пентинил]циклопропил]-4Н-инден-4-ол,
[1R-(1α(Е),3аβ,7аα)]-октагидро-7а-метил-1-[1-[1-[5,5,5-трифтор-4-гидрокси-4-(трифторметил)-2-пентинил]циклопропил]-4Н-инден-4-он,
[1R-(1α(Е),3aβ,7аα)]-окстагидро-7а-метил-1-[1-[5,5,5-трифтор-4-трифторметил)-4-[(триметилсилил)окси]-2-пентинил]циклопропил]-4Н-инден-4-он,
3-дезокси-1,25-дигидрокси-20-метил-23-(Е)-ен-26,27-гексафтор-21,28-циклохолекальциферол,
3-дезокси-1,25-дигидрокси-20-метил-23-(Z)-ен-26,27-гексафтор-21,28-циклохолекальциферол,
3-дезокси-1,25-дигидрокси-20-метил-23-ин-21,28-циклохолекальциферол,
3-дезокси-1,25-дигидрокси-20-метил-23-ин-26,27-гексафтор-21,28-циклохолекальциферол,
3-дезокси-1,25-дигидрокси-20-метил-21,28-циклохолекальциферол,
3-дезокси-1α-ацетокси-25-гидрокси-20-циклопропил-23Е-ен-26,27-гексафторхолекальциферол и
3-дезокси-1α,25-дицетокси-20-циклопропил-23Е-ен-26,27-гексафторхолекальциферол.
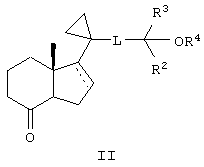
с фосфиноксидом формулы
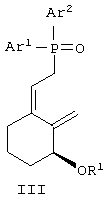
в условиях, достаточных для образования соединения формулы I, где каждый Ar1 и Ar2 независимо означает необязательно замещенный арил, пунктирная линия необязательно означает двойную связь,
L означает соединительный фрагмент, выбранный из ряда -СН2-СН2-CH2-, -СН2-СН=СН- и -СН2-С≡С-;
каждый R2 и R3 независимо означает алкил или галогеналкил, а
каждый R1 и R4 независимо означает гидроксизащитную группу, и
(б) если ни один из R1 и R4 не означает ацильную группу, ацилирование соединения формулы I ацилирующим агентом в условиях, достаточных для образования соединения формулы I, где по меньшей мере один из R1 и R4 означает ацильную группу.
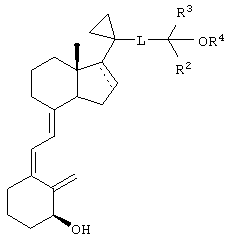
и (II) взаимодействие аналога 1-гидрокси-3-дезокси-витамина D3 с ацилирующим агентом в условиях, достаточных для образования сложного эфира аналога 3-дезокси-витамина D3 формулы
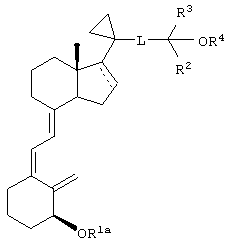
где R1a означает ацильную группу, a R4a означает водород или ацильную группу.

или его пролекарства или соли,
где пунктирная линия необязательно означает двойную связь,
L означает соединительный фрагмент, выбранный из группы, включающей -СН2-СН2-СН2-, -СН2-СН=СН- и -СН2-С≡С-,
каждый R1 и R4 означает водород, а
каждый R2 и R3 независимо выбирают из группы, включающей алкил или галогеналкил.
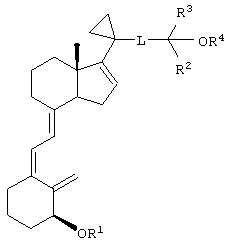
где R1, R2, R3, R4 и L имеют значения, указанные в п.1.
| WO 9912894, А, 18.03.1999 | |||
| Устройство для автоматического программного управления производственными процессами | 1954 |
|
SU104089A1 |
| Тензометр | 1979 |
|
SU808832A1 |
| KOIKE, MICHIAKI et al | |||
| Anticancer Research | |||
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
Авторы
Даты
2007-03-27—Публикация
2002-09-12—Подача