Область изобретения
Настоящее изобретение относится к стероидным соединениям, обладающим улучшенной фармакологической активностью и пониженными побочными эффектами, к способу их получения и содержащему их фармацевтическому составу.
Соединения настоящего изобретения могут использоваться в качестве лекарств, обладающих противовоспалительной активностью на периферийном уровне, для лечения респираторных заболеваний, таких как астма и хроническое обструктивное заболевание легких (ХОБЛ), для лечения глазных заболеваний, таких как глазная гипертония, возрастная макулярная дистрофия, диабетический отек желтого пятна, диабетическая ретинопатия, гипертоническая ретинопатия и ретинальная васкулопатия, или для лечения дерматологических заболеваний, таких как дерматоз, атопический дерматит, воспаление, экзема, эритема, образование папул, снятие зубных отложений, изъязвление, мокнутие, покрытие струпьями, прурит, псориаз, буллезный дерматит, гнойный гидраденит, бородавки, опрелость, паховая эпидермофития. В особенности соединения настоящего изобретения полезны для лечения глазных заболеваний.
Предпосылки создания изобретения
В литературе описаны нитрооксипроизводные стероидов, которые полезны в качестве сердечно-сосудистых агентов для лечения сердечной недостаточности или стенокардии.
Например, патент Германии DE 2222491 описывает получение прегнановых производных, имеющих в положении 21 группу CH2-O-NO2. В указанном патенте утверждается, что названные соединения обладают кардиотропной активностью. Обладающие такой активностью указанные соединения имеют тот недостаток, что они изменяют частоту пульса.
Патент США US 3494941 описывает стероидные производные 3-гидроксиэстрана или эстр-4-ен-3-она, полезные в качестве вазодилататоров при лечении кардиотонических повреждений, таких как сердечная недостаточность и стенокардия. В структуре указанных соединений группа ONO2 расположена на свободном конце алкиленовой цепи, которая связана со стероидом эфирной связью в положении 17. В соответствии с указанным патентом в положении 3 и 16 стероидной структуры также могут находиться нитратные группы. В отношении соединений этого патента могут быть повторены те же указанные выше недостатки, касающиеся влияния на частоту пульса.
Патент США US 3183252 описывает производные 16-нитрат-алкиленпрегнанов хх, где алкильная группа связана с прегнановой структурой углерод-углеродной связью. Согласно этому патенту соединения могут использоваться в качестве вазодилататоров. По отношению к ним могут быть повторены те же указанные выше недостатки.
WO 98/15568 и WO 03/064443 описывают нитроэфиры стероидных соединений, где между стероидной структурой и нитроокси группой находится двухвалентная связующая группа. Указанные соединения показывают хорошую эффективность и/или толерантность по отношению к соответствующим предшественникам.
Патентная заявка WO 00/61604 описывает нитрооксипроизводные стероидных соединений с различными связующими группами, имеющими на одном конце нитроокси группу, а другим концом ковалентно связанными со стероидным соединением. В указанной заявке применение касается соединений, используемых для лечения окислительного стресса. Указанные соединения также содержат в молекуле двухвалентную связующую группу, которая может предотвратить производство свободных радикалов и выбрана на основе приводимых в них тестов.
Краткое описание изобретения
Заявитель неожиданно нашел класс соединений, высвобождающих оксид азота, с улучшенной биодоступностью и/или пролонгированным высвобождением (выделением) NO по сравнению с известными в предшествующем уровне техники соединениями. В основном соединения настоящего изобретения обладают улучшенной терапевтической способностью по сравнению с известными соединениями.
Детальное описание изобретения
Объектом настоящего изобретения являются соединения общей формулы (I) и их фармакологически приемлемые соли или стереоизомеры
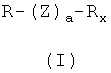
где R представляет остаток кортикостероида формулы (II):
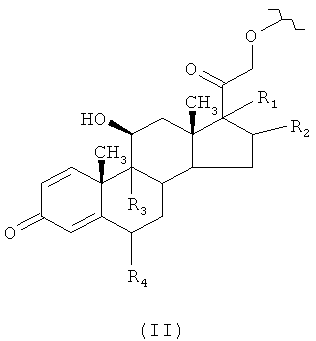
где:
R1 представляет ОН, R2 представляет СН3 или R1 и R2, взятые вместе, образуют группу формулы (III)
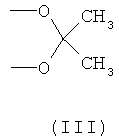
R3 представляет Cl или F;
R4 представляет Н или F;
где R1, R2, R3 и R4 могут быть присоединены к соответствующим атомам углерода стероидной структуры в положении α или β;
при условии, что:
когда R1 и R2 представляют группу формулы (III), тогда R3 представляет F и R4 представляет Н или F;
когда R1 представляет ОН и R2 представляет -СН3, тогда R4 представляет Н и R3 представляет Cl или F;
предпочтительными кортикостероидными радикалами являются R формулы (II),
где:
R1 представляет ОН в положении α, R2 представляет -СН3 в положении β, R3 представляет Cl в положении α и R4 представляет Н; или
R1 представляет ОН в положении α, R2 представляет -СН3 в положении β, R3 представляет F в положении α и R4 представляет Н; или
R1 и R2, взятые вместе, образуют группу формулы (III)

R3 представляет F и R4 представляет Н; R1, R2 и R3 находятся в положении α; или
R1 и R2, взятые вместе, образуют группу формулы (III)

R3 и R4 представляют F; R1, R2, R3 и R4 находятся в положении α;
а в формуле (I) равно 0 или 1;
Z представляет группу, способную связываться с Rx и выбранную из -С(O)- или -CH(R′)-O-, где R′ выбран из H или прямого или разветвленного C1-С4алкила, предпочтительно R' представляет собой Н или -СН3;
Rx представляет собой радикал и выбран из следующих значений:
А)
(a1) -HN-CH(R1)-C(O)-(T-Y-ONO2)
(а2) -С(О)-CH(R1)-NH-(T'-Y-ONO2)
(а3) -HN-CH(R1a-Т′′-Y′-ONO2)-COOR3a
(а4) -С(O)-CH(R1a-T′′-Y′-ONO2)-NHR4a
(а5) -R1b-CH(NHR4a)-С(О)-(T-Y-ONO2)
(а6) -R1b-СН(COOR3a)NH-(Т′-Y-ONO2)
(а7) -HN-CH(R1a-Т′′-Y′-ONO2)-С(О)-(T-Y-ONO2)
(а8) -С(О)-СН(R1a-Т′′-Y′-ONO2)-NH-(Т′-Y-ONO2)
(а9) -R1b-CH(NH-T′-Y′-ONO2)-С(О)-(T-Y-ONO2)
(а10) -R1b-CH(С(О)-T-Y′-ONO2)-NH-(T′-Y-ONO2)
где:
R1 выбран из:
A1) Н, -СН3, изопропила, изобутила, втор-бутила, трет-бутила, метилтио-(СН2)-, фенила, бензила, С6Н5-СН2-СН2-, 2-монозамещенного бензила, или 3-монозамещенного бензила, или 4-монозамещенного бензила, где заместитель у бензила выбран из -F, -Cl, -I, -NO2, -CF3, -СН3, CN, С6Н5СО-; 2,4-дихлорбензила, 3,4-дихлорбензила, 3,4-дифторбензила, 2-пирролидила, 3-триптофанил-СН2-, 3-бензотиенил-СН2-, 4-имидазолил-СН2-, 9-антранил-СН2-, циклогексила, циклогексил-СН2-, циклогексил-(СН2)2-, циклопентил-СН2-, (С6Н5)2СН-, 4-В(ОН)2-бензила, 4-хинолил-СН2-, 3-хинолил-СН2-, 2-хинолил-СН2-, 2-хиноксалил-СН2-, 2-фурил-СН2-, 1-нафтил-СН2-, 2-нафтил-СН2-, 2-пиридил-СН2-, 3-пиридил-СН2-, 4-пиридил-СН2-, 2-тиенил-СН2-, 3-тиенил-СН2-, С6Н4-СН=СН-CH2-, СН2=СН-СН2-, CH=СН-СН2-, NH2-СО-СН2-, NH2-CO-(CH2)2-, NH2(=NH)NH-(CH2)3-, Р(=0)(ОСН3)2, I-CH2-,
предпочтительно R1 представляет Н, -СН3, изопропил, бензил;
A2) -CH2-SH, -СН2-OH; -СН(СН3)-OH, -СН2[(С6Н4)-(4-ОН)], -СН2-[(С6Н2)-(3,5-дииодо)-(4-ОН)], -CH2-[(С6Н3)-(3-нитро)-(4-ОН)],
предпочтительно R1 представляет -СН2-ОН или -СН2[(С6Н4)-(4-ОН)];
A3) -CH2-NHR′′, - (CH2)2-NHR′′, - (СН2)3-NHR′′, -(CH2)4-NHR′′, где R′′ представляет Н, -С(O)СН3 или
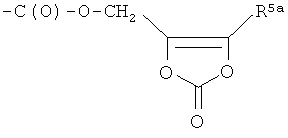
где R5a представляет Н или линейную или разветвленную алкильную цепь C1-С10, предпочтительно R5a представляет Н или линейный (C1-C5)алкил,
предпочтительно R1 представляет -(CH2)4-NHR′′, где R′′, как указано выше;
А4) -CH2-C(O)R′′′, -(CH2)2-C(O)R′′′, -(СН2)4-С(О)R′′′, где R′′′ представляет -OR5a или
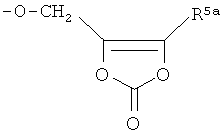
где R5a, как указано выше, предпочтительно R1 представляет -СН2-С(О)R′′′,
где R′′′, как указано выше;
R1a выбран из:
А5) -CH2-S-, -СН2-O-, -СН(СН3)-O-, -СН2[(С6Н4)-(4-O)-], -СН2-[(3,5-дииодо)-(С6Н2)-(4-O)-], -CH2-[(3-нитро)-(С6Н3)-(4-O)-],
предпочтительно R1a представляет -СН2-O-;
А6) -CH2-NH-, -(CH2)2-NH-, -(СН2)3-NH-, -(CH2)4-NH-, предпочтительно
R1a представляет -(СН2)4-NH- или -CH2-NH-;
А7) -СН2-С(O)-, -(СН2)2-С(О)-, -(СН2)4-С(O)-, предпочтительно R1a представляет -СН2-С(O)-;
R3a выбран из Н, -R5a или

где R5a, как указано выше;
R4a выбран из Н или -С(O)СН3 или

где R5a, как указано выше;
R1b выбран из
А8) -S-CH2-, -О-СН(СН3)-, -O-СН2-, [-(4-O)-(C6H4)]-СН2-, [-(4-O)-(3,5-дииодо)-(С6Н2)]-СН2-, [-(4-O)-(3-нитро)-(С6Н3)]-СН2-, предпочтительно R1b представляет -O-СН2- или [-(4-O)-(С6Н4)]-СН2-;
А9) -HN-CH2-, -HN-(CH2)2-, -HN-(СН2)3-, -HN-(CH2)4-, предпочтительно R1b представляет -HN-(CH2)4- или -HN-CH2-;
А10) -С(O)-СН2-, -С(O)-(СН2)2-, -С(O)-(СН2)4-, предпочтительно R1b представляет -С(O)-СН2-;
Т выбран из -O-, -S-, -NR′-, -O-CH(R′)-O-C(О)- или
-O-CH(R′)-O-C(O)O-, где R′, как указано выше;
Т′ представляет -С(O)-, -С(O)-Х′′-, где X′′ представляет -О- или -S-, или Т′ представляет -C(O)-NR′-, где R′, как указано выше;
Т′′ независимо выбран из -С(O)-, -С(O)-Х′′-, -C(O)-NR′-, -O-, -S-, -NR′-, -O-CH(R′)-O-C(O)-, -O-CH(R′)-O-C(O)O-, где X′′ и R′, как указано выше, при условии, что Т′′ представляет -С(O)-, -С(O)-Х′′- или -C(O)-NR′-, когда Т′′ связан с -NH-, -О- или -S-; или
Т′′ представляет -O-, -S-, -NR′-, -O-CH(R′)-O-C(O)-, -O-CH(R′)-O-C(O)O-, когда Т′′ связан с -С(O)-;
Y and Y′, как указано ниже;
В)
(b1) -HN-CH(R2)-CH2C(О)-(T-Y-ONO2)
(b2) -С(О)-СН2-СН(R2)-NH-(Т′′-Y-ONO2)
(b3) -HN-CH(R2a-T′′-Y′-ONO2)-CH2COOR3a
(b4) -С(О)-СН2-СН(R2a-T′′-Y′-ONO2)-NHR4a
(b5) -R2b-CH(NHR4a)-CH2C(О)-(T-Y-ONO2)
(b6) -R2b-CH(CH2COOR3a)NH-(Т′-Y-ONO2)
(b7) -HN-CH(R2a-T′′-Y′-ONO2)-CH2-C(O)-(T-Y-ONO2)
(b8) -C(O)-СН2-СН(R2a-T′′-Y′-ONO2)-NH-(T′-Y-ONO2)
(b9) -R2b-CH(NH-T′-Y′-ONO2)-CH2C(О)-(T-Y-ONO2)
(b10) -R2b-CH(CH2C(О)-Т-Y′-ONO2)-NH-(T′-Y-ONO2)
где
R2 выбран из
B1) Н, -СН3, CF3, изопропила, изобутила, втор-бутила, метилтио-(СН2)2-, фенила, бензила, 3-триптофанил-СН2-, NH2-C(O)-СН2-, NH2-С(O)-(СН2)2~, NH2(=NH)NH-(CH2)3-, трет-BuO-СН(СН3)-, бензил-O-СН2-, 4-третбутокси-бензила, 4-фенилбензила, предпочтительно R2 представляет Н, -СН3, изопропил, бензил;
B2) -CH2-SH, -СН2-ОН, -СН(СН3)-ОН, -СН2[(С6Н4)-(4-ОН)],
-СН2-[(С6Н2)-(3,5-дииодо)-(4-ОН)], -СН2-[(С6Н3)-(3-нитро)-(4-ОН)];
B3) -CH2-NHR′′, - (CH2)2-NHR′′, - (CH2)3-NHR′′, -(CH2)4-NHR′′, где R′′, как указано выше, предпочтительно R2 представляет -(СН2)4-NHR′′;
B4) -CH2-C(O)-R′′′, -(CH2)2-C(O)-R′′′, -(СН2)4-С(O)-R′′′, где R′′′, как указано выше, предпочтительно R2 представляет -CH2-C(O)-R′′′;
R2a выбран из
B5) -CH2-S-, -СН2-O-, -СН(СН3)-O- или -СН2[(С6Н4)-(4-O)-], -СН2-[(3,5-дииодо)-(С6Н2)-(4-O)-], -СН2-[(3-нитро)-(С6Н3)-(4-O)-], предпочтительно
R2a представляет -СН2-O-;
В6) -СН2-NH-, -(CH2)2-NH-, -(CH2)3-NH-, -(CH2)4-NH-, предпочтительно R2a представляет -(CH2)4-NH- или -CH2-NH-;
B7) -СН2-С(O)-, -(СН2)2-С(O)-, -(СН2)4-С(O)-, предпочтительно R2a представляет -СН2-С(O)-;
R2b выбран из
B8) -S-CH2-, -О-СН(СН3)-, -O-СН2-, [-(4-O)-(С6Н4)]-СН2-, [-(4-O)-(3,5-дииодо)-(С5Н2)]-СН2-, [-(4-O)-(3-нитро)-(С6Н3)]-СН2-, предпочтительно R2b представляет -О-СН2- или [-(4-O)-(С6Н4)]-СН2-;
B9) -HN-CH2-, -HN-(CH2)2-, -HN-(CH2)3-, -HN-(CH2)4-, предпочтительно R2b представляет -HN-(CH2)4- или -HN-CH2-;
В10) -С(O)-СН2-, -С(O)-(СН2)2-, -С(O)-(СН2)4-, предпочтительно R2b представляет -С(O)-СН2-;
R3a и R4a, как указано выше;
Т, Т′ и Т′′, как указано выше, и Y и Y′, как указано ниже;
C)
(c1) -HN-(CH2)b-C(O)-(T-Y-ONO2);
(с2) -С(O)-(СН2)b-NH-(T′-Y-ONO2);
где b - целое число от 3 до 6,
Т и Т′, как указано выше, и Y и Y′, как указано ниже;
D)
(d1) -HN-CH(R12)-CH2-O-(T′′′-Y-ONO2)
(d2) -O-CH2-CH(R12)-NH-(T′-Y-ONO2)
(d3) -HN-CH(R12a-T′′-Y′-ONO2)-CH2OH
(d4) -O-CH2-CH(R12a-T′′-Y′-ONO2)-NHR4a
(d5) -R12D-CH(NHR4a)-CH2-O-(T′′′-Y-ONO2)
(d6) -R12b-CH(CH2OH)-NH-(T′-Y-ONO2)
(d7) -HN-CH(R12a-T′′-Y′-ONO2)-CH2-O-(T′′′-Y-ONO2)
(d8) -O-CH2-CH(R12a-Т′′-Y′-ONO2)-NH-(T′-Y-ONO2)
(d9) -R12b-CH(NH-T′-Y′-ONO2)-CH2-O-(T′′′-Y-ONO2)
(d10) -R12b-CH(СН2-O-T′′′-Y′-ONO2)-NH-(T′-Y-ONO2)
где
Т′′′ независимо выбран из -С(O)-, -С(O)Х′′-, где Х′′ представляет -О- или -S-, или -C(O)-NR′-, где R′, как указано выше;
Т′ и Т′′, как указано выше;
Y и Y′, как указано выше;
R12 выбран из:
D1) H, -СН3, изопропила, изобутила, втор-бутила, метилтио-(СН2)2-, бензила, 3-триптофанил-СН2-, 4-имидазолил-СН2-, NH2-CO-CH2-, NH2-CO-(CN2)2-, NH2(=NH)NH-(CH2)3-, предпочтительно R12 представляет H;
D2) -СН2-ОН, -СН(СН3)-ОН, -СН2[(С6Н4)-(4-ОН)], -CH2-[(С6Н3)-(3,5-дииодо)-(4-ОН)], -СН2-[(С6Н3)-(3-нитро)-(4-ОН)], предпочтительно R12 представляет -СН2-ОН или -CH2[(C6H4)-(4-ОН)];
D3) -CH2-NHR′′, -(CH2)2-NHR′′, -(CH2)3-NHR′′, -(СН2)4-NHR′′, где R′′, как указано выше, предпочтительно R12 представляет -(СН2)4-NHR′′;
D4) -CH2-C(O)R′′′, -(CH2)2-C(O)R′′′, -(СН2)4-С(О)R′′′, где R′′′, как указано выше, предпочтительно R12 представляет -CH2-C(O)R′′′;
R12a выбран из
D5) -СН2-O-, -СН(СН3)-O- или -СН2[(С6Н4)-(4-O)-], -СН2-[3,5-дииодо-(С6Н2)-(4-O)-], -СН2-[3-нитро-(С6Н3)-4-O-], предпочтительно R12a представляет CH2-О- или -СН2[(С6Н4)-(4-O)-];
D6) -CH2-NH-, -(CH2)2-NH-, -(СН2)3-NH-, -(CH2)4-NH-, предпочтительно R12a представляет -(CH2)4-NH- или -CH2-NH-;
D7) -СН2-С(O)-, -(СН2)2-С(O)-, -(СН2)4-С(O)-, предпочтительно R12a представляет -СН2-С(O)-;
R12b выбран из
D8) -O-СН2-, -О-СН(СН3)-, [-(4-O)-(С6Н4)]-СН2-, [-(4-O)-(3,5-дииодо)-(С6Н2)]-СН2, [-(4-O)-(3-нитро)-(С5Н3)]-СН2-, предпочтительно R12b представляет -O-СН2- или [-(4-O)-(С6Н4)]-СН2-;
D9) -HN-CH2-, -HN-(CH2)2-, -HN-(CH2)3-, -HN-(CH2)4-, предпочтительно R12b представляет -HN-(CH2)4- или -HN-CH2-;
D10) -C(O)-CH2-, -C(O)-(CH2)2-, -C(O)-(CH2)4-, предпочтительно R12b представляет -С(O)-СН2-;
R4a, как указано выше;
E)
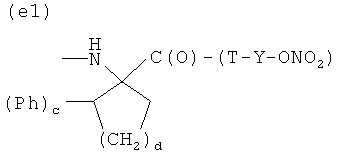
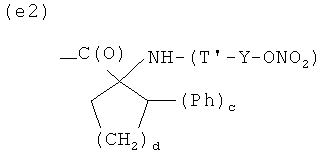
где с равно 0 или 1, d - целое число от 0 до 3, при условии, что с равно 0 или 1, когда d равно 0, и с равно 0, когда d равно 1, 2 или 3, Т и Т′, как указаны выше, и Y, как указано ниже;
F)
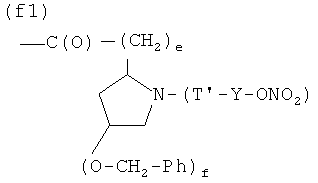
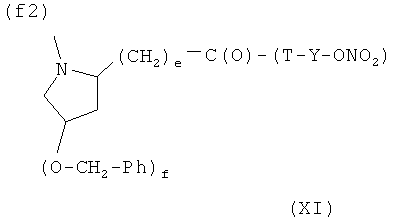
где е и f равны 0 или 1, при условии, что f равно 0, когда е равно 0, и f равно 0 или 1, когда е равно 1, Т и Т′, как указаны выше, и Y, как указано ниже;
G)
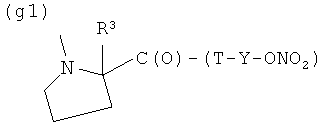
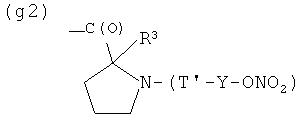
где R3 представляет Н, СН3, пропил, (С6Н5)2СН-, 1-нафтил-СН2-, бензил, аллил, 2-бромбензил, 2-хлорбензил, 3-хлорбензил, 4-фторбензил, 4-бромбензил, 4-метилбензил, предпочтительно R′′ представляет Н, Т и Т′, как указаны выше, и Y, как указано ниже;
H)
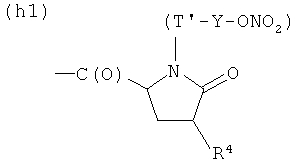
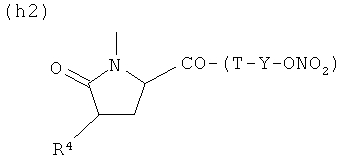
где R4 представляет Н, бензил, 4-бромбензил, 2-бромбензил, Т и Т′, как указаны выше, и Y, как указано ниже;
I)
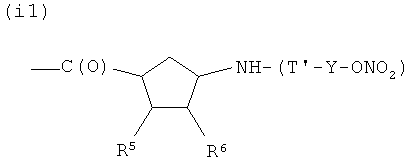
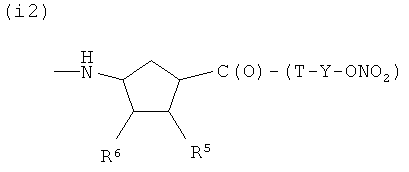
где R5 представляет Н, R6 представляет Н, или R5 и R6, взятые вместе, представляют двойную связь, Т и Т′, как указаны выше, и Y, как указано ниже;
L)
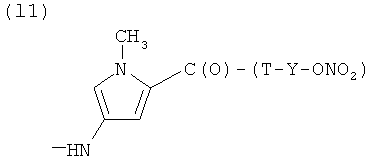
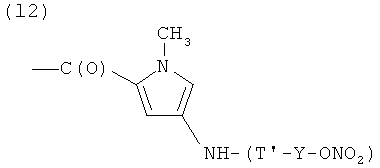
где Т и Т′, как указаны выше, и Y, как указано ниже;
M)
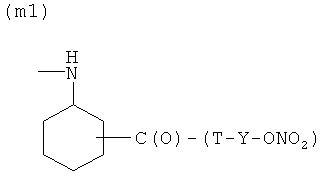
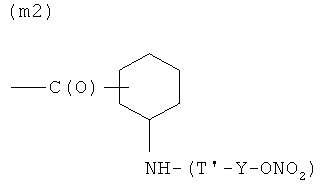
где Т и Т′, как указаны выше, и Y, как указано ниже;
N)
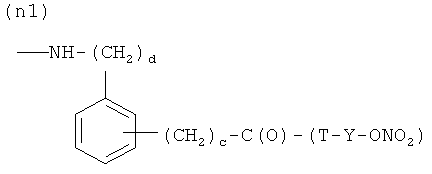
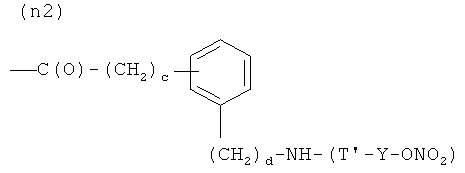
где c, как указано выше, d равно 0 или 1, Т и Т′, как указаны выше, и Y, как указано ниже;
O)
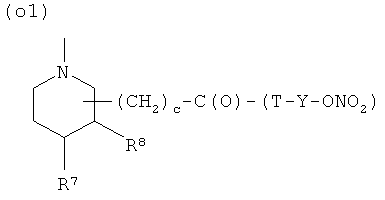
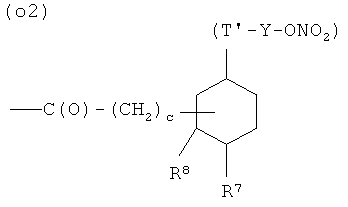
где R7 представляет Н, R8 представляет Н или R7 и R8, взятые вместе, представляют двойную связь, с, как указано выше, Т и Т′, как указаны выше, и Y, как указано ниже;
P)
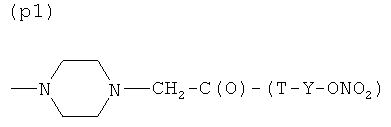
где Т и Т′, как указаны выше, и Y, как указано ниже;
Q)
где Т и Т′, как указаны выше, и Y, как указано ниже;
R)
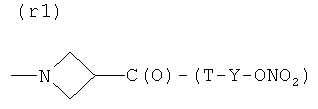
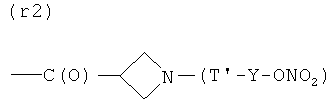
где Т и Т′, как указаны выше, и Y, как указано ниже;
S)
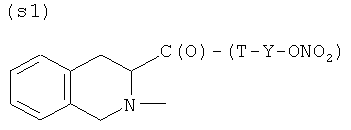
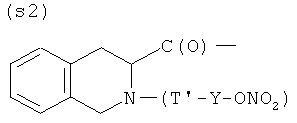
где Т и Т′, как указаны выше, и Y, как указано ниже;
T)
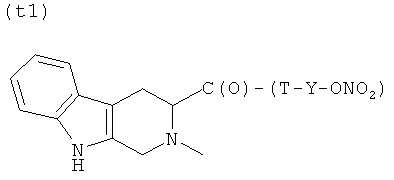
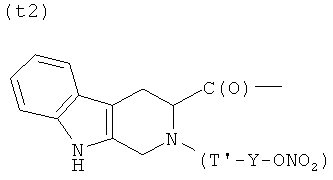
где Т и Т′, как указаны выше, и Y, как указано ниже;
U)
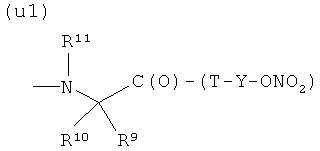
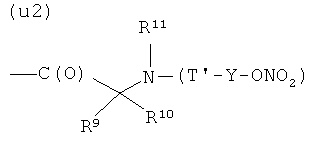
где R9 и R13 представляют Н, СН3, R11 представляет СН3 или 4-пиперидинил, при условии, что R9 и R10 представляют Н, когда R11 представляет 4-пиперидинил, и R9 и R10 представляют СН3, когда R11 представляет СН3, Т и Т′, как указаны выше, и Y, как указано ниже;
V)
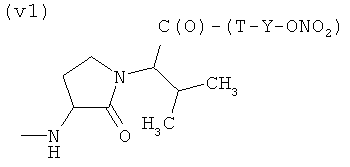
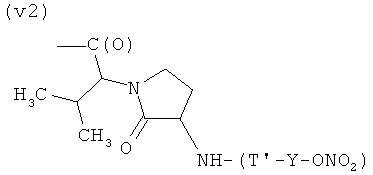
где Т и Т′, как указаны выше, и Y, как указано ниже;
при условии, что в формуле (I):
а равно 0 или а равно 1 и Z представляет -CH(R′)~O-, где R′, как указано выше, когда Rx представляет:
- (а2), (а4) или (а8);
- (а5), (а6), (а9) или (а10) и R1b выбран из группы А10);
- (b2), (b4) или (b8);
- (b5), (b6), (b9) или (b10) и R2b выбран из группы В10);
- (с2);
- (d5), (d6), (d9) или (d10) и R12b выбран из группы D10);
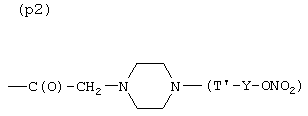
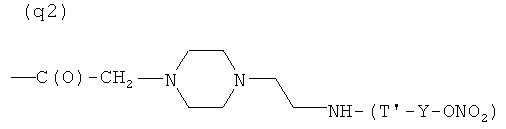
- (е2), (f1), (g2), (h1), (i1), (l2), (m2), (n2), (o2), (p2), (q2), (r2), (s2), (t1) или (u2);
а равно 1 и Z представляет -С(O)-, когда Rx представляет:
- (a1), (a3) или (а7);
- (а5), (а6), (а9) или (а10) и R1b выбран из групп А8) и А9);
- (b1), (b3) или (b7);
- (b5), (b6), (b9) или (b10) и R2b выбран из групп B8) или B9);
- (c1);
- (d1), (d2), (d3), (d4), (d7) или (d8);
- (d5), (d6), (d9) или (d10) и R12b выбран из групп D8) или D9);
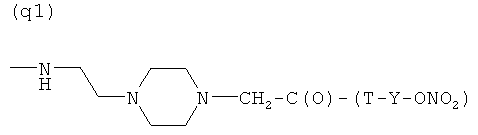
- (e1), (f2), (g1), (h2), (i2), (l1), (m1), (n1), (o1), (p1), (q1), (r1), (s1), (t2) или (u1).
Y и Y′ представляют двухвалентные радикалы, где каждый независимо выбран из следующих значений:
а)
- прямой или разветвленный С1-С20алкилен, предпочтительно прямой или разветвленный C1-С10алкилен,
- прямой или разветвленный C1-С20алкилен, замещенный одним или более заместителями, выбранными из следующей группы: атомы галоида, гидрокси, -ONO2 или Т2, где Т2 представляет -ОС(O)(C1-С10алкил)-ONO2 или -O(C1-С10алкил)-ONO2, предпочтительно Y или Y′ представляет прямой или разветвленный C1-С10алкилен, замещенный группой -ONO2;
- циклоалкилен с от 5 до 7 углеродных атомов в циклоалкиленовом кольце, где кольцо необязательно замещено одной или более прямой или разветвленной C1-С10 алкильной цепью, предпочтительно кольцо необязательно замещено СН3;
b)
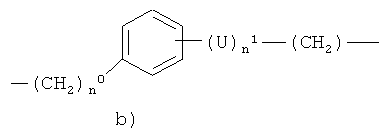
где
n0 представляет целое число от 0 до 20, предпочтительно n0 представляет 0 или 1;
n1 представляет 0 или 1, предпочтительно n1 представляет 1;
U представляет линейный или разветвленный C1-С20алкилен, необязательно замещенный группой -ONO2, предпочтительно U представляет линейный C1-С10алкилен или U представляет линейный или разветвленный С1-С10алкилен, замещенный группой -ONO2;
c)
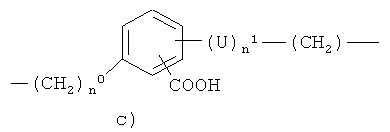
где
n0 представляет целое число от 0 до 20, предпочтительно n0 представляет 0 или 1;
n1 представляет 0 или 1, предпочтительно n1 представляет 1;
U представляет линейный или разветвленный С1-С20алкилен, необязательно замещенный группой -ONO2, предпочтительно U представляет линейный С1-С10алкилен или U представляет линейный или разветвленный C1-С10алкилен, замещенный группой -ONO2;
d)
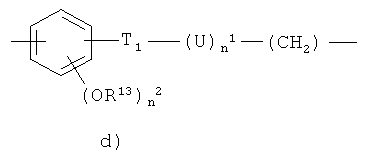
где
n2 представляет целое число от 0 до 2, R13 представляет Н или СН3, T1 представляет -O-С(О) - или -С(O)O-;
n1 и U указано выше;
e)
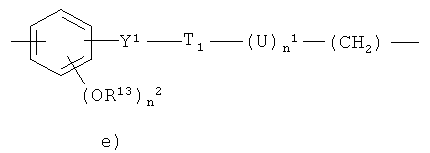
n2 представляет целое число от 0 до 2, предпочтительно n2 представляет 1;
R13 представляет Н или СН3, предпочтительно R13 представляет СН3;
Y1 представляет -СН2-СН2- или -CH=CH-(CH2)n 2'-, где n2' представляет 0 или 1, предпочтительно Y1 представляет -СН=СН-(СН2)n 2′- и n2′ представляет 0;
T1=-О-С(О)- или -С(O)O-, предпочтительно T1 представляет -С(O)O-;
n1 представляет 0 или 1, предпочтительно n1 представляет 1;
U представляет линейный или разветвленный C1-С20алкилен, необязательно замещенный группой -ONO2, предпочтительно U представляет линейный С1-С10алкилен или U представляет линейный или разветвленный C1-С10алкилен, замещенный группой -ONO2;
более предпочтительно n2 представляет 1, R13 представляет СН3, Y1 представляет -СН=СН-(СН2)n 2′- и n2′ представляет 0, T1 представляет -С(O)O- и U представляет линейный C1-С10алкилен;
е′)
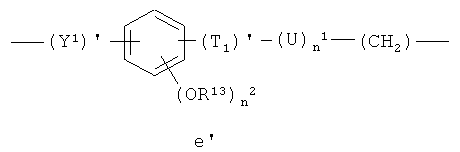
где
n2 представляет целое число от 0 до 2, предпочтительно n2 представляет 1;
R13 представляет Н или СН3, предпочтительно R13 представляет СН3;
Y1 представляет -CH2-CH2- или - (CH2)n 2′-CH=CH-, где n2′ представляет 0 или 1, предпочтительно Y1 представляет -(СН2)n 2′-СН=СН- и n2′ представляет 0;
(Т1)′=-О-С(О)-;
n1 представляет 0 или 1, предпочтительно n1 представляет 1;
U представляет линейный или разветвленный C1-С20алкилен, необязательно замещенный группой -ONO2, предпочтительно U представляет линейный C1-С10алкилен или U представляет линейный или разветвленный C1-С10алкилен, замещенный группой -ONO2;
более предпочтительно n2 представляет 1, R13 представляет СН3, Y1 представляет -СН=СН-(СН2)n 2′- и n2′ представляет 0, T1 представляет -ОС(O)- и U представляет линейный C1-С10алкилен;
когда Y и Y′ выбраны из b), с), d), e) или е′), группа -ONO2 в -(T-Y-ONO2), -(T′-Y-ONO2), -(Т′′-Y′-ONO2), -(Т′-Y′-ONO2), -(T′′′-Y-ONO2) и -(T′′′-Y′-ONO2) связана с группой -(СН2)-;
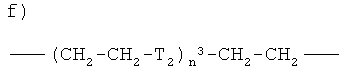
где Т2 представляет -О- или -S-, -NH-, предпочтительно Т2 представляет -O-,
n3 представляет целое число от 1 до 6, предпочтительно n3 представляет 1;
g)
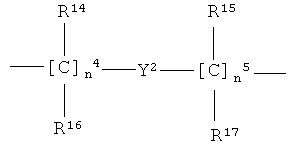
где:
n4 представляет целое число от 0 до 10, предпочтительно n4 представляет 0 или 1;
n5 представляет целое число от 1 до 10, предпочтительно n5 представляет 1;
R14, R15, R16, R17 - одинаковые или разные, и представляют Н или прямой или разветвленный C1-C4 алкил, предпочтительно R14, R15, R16, R17 представляют Н;
где
группа -ONO2 связана с
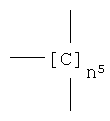
где n5, как указано выше;
Y2 представляет гетероциклическое, насыщенное, ненасыщенное или ароматическое 5- или 6-членное кольцо, содержащее один или более гетероатомов, выбранных из азота, кислорода или серы, и выбран из группы, состоящей из:
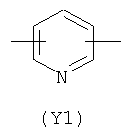 ,
, 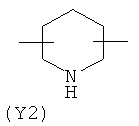 ,
, 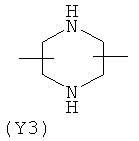 ,
, 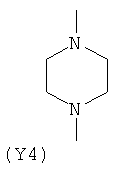 ,
, 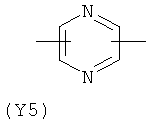 ,
,
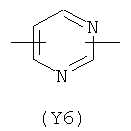 ,
, 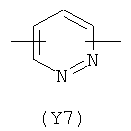 ,
, 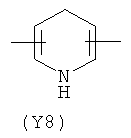 ,
, 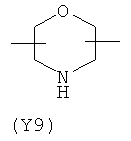 ,
, 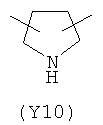 ,
,
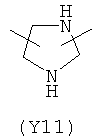 ,
, 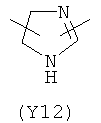 ,
, 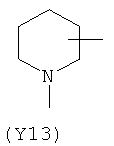 .
.
Используемый здесь термин "C1-С10алкил" относится к прямым или разветвленным алкильным группам, включающим метил, этил, н-пропил, изопропил, н-бутил, изобутил, трет-бутил, пентил, гексил, октил и тому подобное.
Используемый здесь термин "циклоалкилен" относится к имеющему от 5 до 7 углеродных атомов кольцу, включая, но не ограничиваясь ими, циклопентил, циклогексил, необязательно замещенные боковыми цепями, такими как прямой или разветвленный (С1-С10)-алкил, предпочтительно СН3.
Используемый здесь термин "гетероциклил" относится к насыщенному, ненасыщенному или ароматическому 5- или 6-членному кольцу, содержащему один или более гетероатомов, выбранных из азота, кислорода и серы, такому как, например, пиридин, пиразин, пиримидин, пирролидин, морфолин, имидазол и тому подобное.
Предпочтительными соединениями формулы (I) для лечения глазных заболеваний, в особенности глазной гипертонии, возрастной макулярной дистрофии диабетического отека желтого пятна, диабетической ретинопатии, гипертонической ретинопатии и ретинальной васкулопатии, являются такие, где кортикостероидный остаток R выбран из группы, состоящей из бетаметазона, фторцинолон ацетонида, триамцинолон ацетонида.
Другое воплощение изобретения относится к соединениям формулы (I), где в кортикостериодном остатке R формулы (II) R1, R2, R3 и R4 имеют следующие значения:
R1 представляет ОН в положении α, R2 представляет -СН3 в положении β, R3 представляет Cl в положении α и R4 представляет H; или
R1 представляет ОН в положении α, R2 представляет -СН3 в положении β, R3 представляет F в положении α и R4 представляет Н; или
R1 и R2, взятые вместе, образуют группу формулы (III)

R3 представляет F и R4 представляет Н; R1, R2 и R3 находятся в положении α;
или
R1 и R2, взятые вместе, образуют группу формулы (III)

R3 и R4 представляют F; R1, R2, R3 и R4 находятся в положении α;
в формуле (I):
а равно 0 и
Rx выбран из:
(а2)-C(O)-CH(R1)-NH-(T′-Y-ONO2)
где
R1 группы А1) выбран из Н, изобутила, бензила, С6Н5-СН2-СН2-, 2-монозамещенного бензила, или 3-монозамещенного бензила, или 4-монозамещенного бензила, где заместитель бензильного радикала выбран из -F, -Cl, I, -NO2, -CF3, -СН3, CN, С6Н5СО-;
R1 группы А2) выбран из -СН2-ОН, -СН(СН3)ОН- или -СН2[(С6Н4)-(4-ОН)]
или
R1 группы A3) выбран из -CH2-NHR′′, -(СН2)2-NHR′′, -(CH2)3-NHR′′, -(CH2)4-NHR′′, где R′′ представляет Н или -С(O)СН3;
R1 группы А4) выбран из -CH2-С(О)R′′′, -(CH2)2-C(O)R′′′, -(CH2)4-C(O)R′′′,
где R′′′ представляет OR5a, где R5a представляет Н или линейный (С1-С5)алкил;
Т′ представляет -С(O)-, -С(O)-Х′′, где X′′ представляет -S- или -O-,
предпочтительно Т′ представляет -С(O)-;
Y, как указано ниже;
или Rx представляет
(а4) -С(О)-СН(R1a-Т′′-Y′-ONO2)-NHR4a,
где R1a формулы А5) выбран из -CH2-О-, -СН(СН3)O- или -СН2[(С6Н4)-(4-O)-], или
R1a группы А6) выбран из -CH2-NH-, -(CH2)2-NH-, -(CH2)3-NH-, -(CH2)4-NH-
или
R1a группы А7) выбран из -СН2-С(O)-, -(CH2)2-С(О)-, -(СН2)4-С(O)-;
R4a представляет Н или -С(O)СН3;
Т′′ представляет -С(O)- или -С(O)-Х′′, где X′′ представляет -S- или -O-, когда
R1a выбран из группы А5) или А6), предпочтительно Т′′ представляет -С(O)-;
Т′′ представляет -О′′, -S-, -NR′- или -O-CH(R′)-O-C(O)-, где R′ представляет Н или -СН3, когда R1a выбран из группы А7);
Y′, как указано ниже;
или Rx выбран из
(а5) -R1b-CH(NHR4a)-С(О)-(T-Y-ONO2)
(а6) -R1b-CH(COOR3a)NH-(T′-Y-ONO2)
(а9) -R1b-CH(NH-T′-Y′-ONO2)-C(О)-(T-Y-ONO2) или
(а10) -R1b-CH(С(О)-T-Y′-ONO2)-NH-(T'-Y-ONO2),
где
R1b группы А10) выбран из -С(O)-СН2-, -С(О)-(СН2)2-,
-С(O)-(СН2)4-;
R3a представляет Н или (C1-C5)алкил:
R4a представляет Н или -С(O)СН3;
Т представляет -O-, -S-, -NR′- или -O-CH(R′)-O-C(O) -, где R′ представляет Н или -СН3, предпочтительно Т представляет -O-;
Т′ представляет -С(O)- или -С(O)-Х′′, где X′′ представляет -S- или -O-, предпочтительно Т′ представляет -С(O)-;
Y и Y′, как указано ниже;
или Rx представляет
(а8) -С(О)-СН(R1a-Т′′-Y′-ONO2)-NH-(T′-Y-ONO2),
где
R1a группы А5) выбран из -СН2-О-, -СН(СН3)-O- или
-СН2[(С6Н4)-(4-O)-], или
R1a группы А6) выбран из -CH2-NH-, -(CH2)2-NH-, -(CH2)3-NH-, -(CH2)4-NH-,
или
R1a группы А7) выбран из -СН2-С(O)-, -(СН2)2-C(О)-, -(СН2)4-С(O)-;
Т′′ представляет -С(O)- или -С(O)-Х′′, где X′′ представляет -S- или -O-, когда
R1a выбран из группы А5) или А6), предпочтительно Т′′ представляет -С(O)-;
Т′′ представляет -O-, -S-, -NR′- или -O-CH(R′)-O-C(O)-, где R′ представляет Н или -СН3, когда R1a выбран из группы А7);
Т′ представляет -С(O)- или -С(O)-Х′′, где X′′ представляет -S- или -O-,
предпочтительно Т′ представляет -С(O)-;
Y и Y′, как указано ниже;
или Rx представляет
(b2) -С(О)-СН2-СН(R2)-NH-(T′-Y-ONO2),
где
R2 группы В1) выбран из Н, СН3, изобутила, изопропила, бензила;
Т′ представляет -С(O)-, -С(O)-Х′′, где X′′ представляет -S- или -O-, предпочтительно Т′ представляет -С(O)-;
Y и Y′, каждый, независимо выбраны из
а)
- прямого или разветвленного C1-С10алкилена,
- прямого или разветвленного C1-С10алкилена, замещенного группой -ONO2;
d)
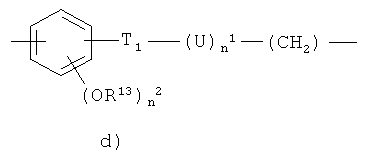
где
n2 представляет целое число от 0 до 2, R13 представляет Н или СН3, T1 представляет -O-С(О)- или -С(O)O-;
n1 представляет 1 и U представляет линейный C1-С10алкилен или U представляет линейный или разветвленный C1-С10алкилен, замещенный группой -ONO2;
e)
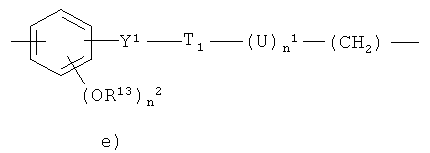
n2 представляет 1, R13 представляет СН3, Y1 представляет -СН=СН-(СН2)n 2′- и n2′ представляет 0; T1 представляет -О-С(О)- и U представляет линейный C1-С10алкилен;
e′)
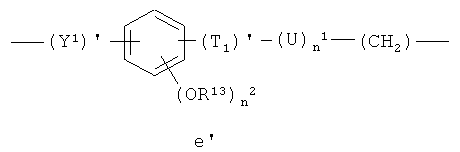
где
n2 представляет 1; R13 представляет СН3;
Y1 представляет -(CH2)n 2′-CH=CH- и n2′ представляет 0;
(Т1)′=-О-С(О)-;
n1 представляет 1 и U представляет линейный C1-С10алкилен или U представляет линейный или разветвленный C1-С10алкилен, замещенный группой -ONO2;
когда Y и Y′ выбраны из d), е) или е′), группа -ONO2 групп -(Т-Y-ONO2), -(T'-Y-ONO2), -(T′′-Y′-ONO2), -(Т′-Y′-ONO2), -(T′′′-Y-ONO2) и -(T′′′-Y′-ONO2) связана с группой -(СН2)-;
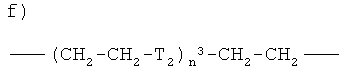
где Т2 представляет -О- или -S-, -NH-, предпочтительно T2 представляет -O-,
n3 представляет 1 или 2;
Другое воплощение изобретения относится к соединениям формулы (I), где в кортикостериодном остатке R формулы (II) R1, R2, R3 и R4 имеют следующие значения:
R1 представляет ОН в положении α, R2 представляет -СН3 в положении β, R3
представляет Cl в положении α и R4 представляет Н; или
R1 представляет ОН в положении α, R2 представляет -СН3 в положении β, R3 представляет F в положении α и R4 представляет Н; или
R1 и R2, взятые вместе, образуют группу формулы (III)

R3 представляет F и R4 представляет Н, R1, R2 и R3 находятся в положении α;
или
R1 и R2, взятые вместе, образуют группу формулы (III)

R3 и R4 представляют F; R1, R2, R3 и R4 находятся в положении α;
в формуле (I):
а равно 1 и Z представляет -С(O)-;
Rx представляет
(а1) -HN-CH(R1)-С(O)-(T-Y-ONO2),
где
R1 группы А1) выбран из Н, изобутила, бензила, С6Н5-СН2-СН2-, 2-монозамещенного бензила, или 3-монозамещенного бензила, или 4-монозамещенного бензила, где заместитель бензильного радикала выбран из -F, -Cl, I, -NO2, -CF3, -СН3, CN, С6Н5СО-;
или
R1 группы А2) выбран из -СН2-ОН, -СН(СН3)ОН- или -СН2[(С6Н4)-(4-ОН)]
или
R1 группы A3) выбран из -CH2-NHR′′, -(CH2)2-NHR′′, -(CH2)3-NHR′′, -(CH2)4-NHR′′, где R′′ представляет Н или -С(O)СН3;
R1 группы А4) представляет -CH2-С(О)R′′′, -(CH2)2-C(O)R′′′, -(CH2)4-C(O)R′′′, где R′′′ представляет OR5a, где R5a представляет Н или линейный (С1-С5)алкил;
Т представляет -O-, -S-, NR′-, -O-CH(R′)-O-C(O)-, где R′ представляет Н или прямой или разветвленный C1-С4алкил, предпочтительно Т представляет -O-;
Y, как указано ниже;
или Rx представляет
(а3) -HN-CH(R1a-Т′′-Y′-ONO2)-COOR3a,
где
R1a группы А5) выбран из -CH2-О-, -СН(СН3)O- или -СН2[(С6Н4)Ор-], или
R1a группы А6) выбран из -CH2-NH-, -(СН2)2-NH-, -(CH2)3-NH-, -(CH2)4-NH-
или
R1a группы А7) выбран из -СН2-С(О)-, -(CH2)2-С(О)-, -(СН2)4-С(O)-;
R3a представляет Н или (С1-C5)алкид;
Т′′ представляет -С(O)- или -С(O)-Х′′, где X′′ представляет -S- или -O-, когда
R1a выбран из группы А5) или А6), предпочтительно Т′′ представляет -С(O)-;
Т′′ представляет -O-, -S-, -NR′- или -O-CH(R′)-O-C(O)-, где R′ представляет Н или прямой или разветвленный C1-С4алкил, когда R1a выбран из группы А7);
Y′, как указано ниже;
или Rx выбран из
(а5) -R1b-CH(NHR4a)-С(О)-(T-Y-ONO2)
(а6) -Rlb-CH(COOR3a)NH-(T′-Y-ONO2)
(а9) -R1b-CH(NH-T′-Y′-ONO2)-C(О)-(T-Y-ONO2) или
(а10) -R1b-CH(С(О)-T-Y′-ONO2)-NH-(Т′-Y-ONO2),
где
R1b группы А8) выбран из -О-СН(СН3)-, -О-CH2-, [-(4-O)-(С6Н4)]-СН2-, или
R1b группы А9) выбран из -HN-CH2-, -HN-(CH2)2-, -HN-(CH2)3-, -HN-(CH2)4-;
R3a представляет Н или (C1-C5)алкил:
R4a представляет Н или -С(O)СН3;
Т представляет -O-, -S-, -NR′- или -O-CH(R′)-O-C(O) -, где R′ представляет Н или прямой или разветвленный C1-C4 алкил, предпочтительно Т представляет -O-;
Т′ представляет -С(O)- или -С(O)-Х′′, где X′′ представляет -S- или -O-,
предпочтительно Т′ представляет -С(O)-;
Y и Y′, как указано ниже;
или Rx представляет
(а7) -HN-CH(R1a-T′′-Y′-ONO2)-C(О)-(T-Y-ONO2),
где
R1a группы А5) выбран из -СН2-O-, -СН(СН3)-O- или
-СН2[(С6Н4)-(4-O)-], или
R1a группы А6) выбран из -CH2-NH-, -(CH2)2-NH-, -(CH2)3-NH-, -(CH2)4-NH-,
или
R1a группы А7) представляет -СН2-С(О)-, -(CH2)2-С(О)-, -(СН2)4-С(O)-;
Т′′ представляет -С(O)- или -С(O)-Х′′, где X′′ представляет -S- или -O-,
предпочтительно Т′′ представляет -С(O)-, когда R1a выбран из группы А5) или А6);
Т′′ представляет -O-, -S-, -NR′- или -O-CH(R′)-O-C(O)-, где R′ представляет Н или прямой или разветвленный C1-С4алкил, предпочтительно Т′′ представляет -O-, когда R1a выбран из группы А7);
Т представляет -O-, -S-, -NR′-, -O-CH(R′)-O-C(O) -, где R′ представляет Н
или прямой или разветвленный C1-С4алкил, предпочтительно Т представляет -O-;
Y и Y′, как указано ниже;
или Rx представляет
(b1) -HN-CH(R2)-СН2С(О)-(T-Y-ONO2),
где
R2 группы В1) выбран из Н, СН3, изобутила, изопропила, бензила;
R2 группы В2) выбран из -CH2-ОН, -СН(СН3)-ОН или -СН2[(С6Н4)(4-ОН),
или
R2 группы В3) выбран из -CH2-NHR′′, -(CH2)2-NHR′′, -(CH2)3-NHR′′, -(СН2)4-NHR′′, где R′′ представляет Н или -С(O)СН3,
R2 группы В4) представляет -CH2-С(О)R′′′, -(СН2)2-С(О)R′′′, -(CH2)4-C(O)R′′′, где R′′′ представляет OR5a, где R5a представляет Н или линейный (С1-С5)алкил;
Т представляет -O-, -S-, -NR′-, -O-CH(R′)-O-C(O)-, где R′ представляет Н или прямой или разветвленный C1-С4алкил, предпочтительно Т представляет -O-;
Y, как указано ниже;
или Rx выбран из
(d1) -HN-CH(R12)-CH2-O-(T′′′-Y-ONO2)
(d2) -O-CH2-CH(R12)-NH-(T′-Y-ONO2),
где
R12 группы D1) выбран из Н, СН3, изобутила, изопропила, бензила, или
R12 группы D2) выбран из -CH2-ОН, -СН(СН3)ОН- или -CH2(С6Н4)-(4-ОН)],
или
R12 группы D3) выбран из -CH2-NHR′′, -(СН2)2-NHR′′, -(CH2)3-NHR′′, -(CH2)4-NHR′′, где R′′ представляет Н, или
R12 группы D4) представляет -CH2-С(О)R′′′, -(CH2)2-С(О)R′′′, -(CH2)4-C(O)R′′′, где R′′′ представляет OR5a, где R5a представляет Н или линейный (C1-C5)алкил;
Т′ и Т′′′, каждый, независимо выбраны из -С(O)- или -С(O)-Х′′, где X′′ представляет -S- или -O-, предпочтительно Т′′ и Т′′′ представляют (О)-;
Y, как указано ниже;
или Rx выбран из
(d3) -HN-CH(R12a-Т′′-Y′-ONO2)-CH2OH
(d4) -O-CH2-CH(R12a-T′′-Y′-ONO2)-NHR4a
(d7) -HN-CH(R12a-T′′-Y′-ONO2)-CH2-O-(T′′′-Y-ONO2) или
(d8) -O-CH2-CH(R12a-T′′-Y′-ONO2)-NH-(T′-Y-ONO2)
где
R12a группы D5) выбран из -СН2-O-, -СН(СН3)-O- или -СН2[(С6Н4)-(4-O)-],
или
R12a группы D6) выбран из -CH2-NH-, -(CH2)2-NH-, -(CH2)3-NH-, -(CH2)4-NH-,
или
R12a группы D7) представляет -СН2-С(O)-, -(СН2)2-С(О)-, -(CH2)4-С(О)-;
R4a представляет Н или -С(O)СН3;
Т′′ выбран из -С(О)- или -С(O)-Х′′, где X′′ представляет -S- или -O-,
предпочтительно Т′ и Т′′′ представляют -С(O)-, когда R12a выбран из D5) или D6);
Т′′ представляет -O-, -S-, -NR′-, -O-CH(R′)-O-C(O)-, где R′ представляет Н или прямой или разветвленный С1-С4алкил, предпочтительно Т представляет -O-, когда R12a выбран из D7);
Т′′′ выбран из -С(О)- или -С(O)-Х′′, где X′′ представляет -S- или -O-, предпочтительно Т′′′′ представляет -С(O)-,
Y и Y′, как указано ниже;
или Rx выбран из
(d5) -R12b-CH(NHR4a)-СН2-O-(T′′′-Y-ONO2)
(d6) -R12b-CH(СН2ОН)-NH-(T'-Y-ONO2)
(d9) -R12b-CH(NH-T′-Y′-ONO2)-CH2-O-(T′′′-Y-ONO2) или
(d10) -R12D-CH(CH2-O-T′′′-Y′-ONO2)-NH-(T′-Y-ONO2)
где
R12b группы D8) выбран из -О-СН(СН3)-, -O-СН2-, [-OP(С6Н4)]-СН2-, или
R12b группы D9) выбран из -HN-CH2-, -HN-(CH2)2-, -HN-(СН2)3-, -HN-(CH2)4-;
R4a представляет Н или -С(O)-СН3,
Т′ и Т′′′, каждый, независимо выбраны из -С(O)-, -С(O)-Х′′, где X′′ представляет -S- или -O-, предпочтительно Т' и Т'" представляют -С(O)-;
Y и Y′, каждый, независимо выбраны из
а)
- прямой или разветвленный С1-С10алкилен,
- прямой или разветвленный C1-С10алкилен, замещенный -ONO2 группой;
d)
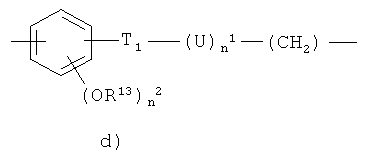
где
n2 представляет целое число от 0 до 2, R13 представляет Н или СН3, T1 представляет -O-С(О)- или -С(O)O-;
n1 представляет 1 и U представляет линейный C1-С10алкилен или U
представляет линейный или разветвленный С1-С10алкилен, замещенный группой -ONO2;
e)
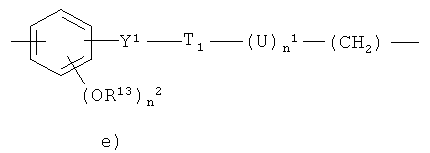
n2 представляет 1, R13 представляет СН3, Y1 представляет -СН=СН-(СН2)n 2'- и n2' представляет 0; T1 представляет -О-С(О)- и U представляет линейный C1-С10 алкилен;
e′)
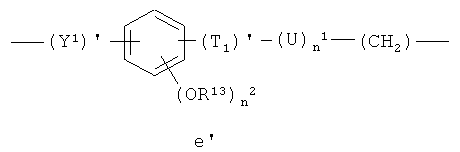
где
n2 представляет 1; R13 представляет СН3;
Y1 представляет -(CH2)n 2′-CH=CH- и n2′ представляет 0;
(Т1)′=-O-С(O)-;
n1 представляет 1 и U представляет линейный C1-С10 алкилен или U представляет линейный или разветвленный С1-С10алкилен, замещенный группой -ONO2;
когда Y и Y′ выбраны из d), e) или е′), группа -ONO2 групп -(T-Y-ONO2), -(T′-Y-ONO2), -(T′′-Y′-ONO2), -(T′-Y′-ONO2), -(T′′′-Y-ONO2) и -(T′′′-Y′-ONO2) связана с группой -(СН2)-;
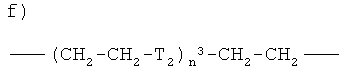
где Т2 представляет -О- или -S-, -NH-, предпочтительно Т2 представляет -O-,
n3 представляет 1 или 2.
Другое воплощение изобретения относится к соединениям формулы (I), где
R представляет кортикостероид формулы (II), как указано выше;
а представляет 0,
Rx представляет
(а2) -С(О)-CH(R1)-NH-(T′-Y-ONO2),
где
R1 группы А1) выбран из Н,
Т′ представляет -С(O)-;
Y выбран из
а)
- прямого или разветвленного C1-С10алкилена,
- прямого или разветвленного С1-С10алкилена, замещенного группой -ONO2;
d)
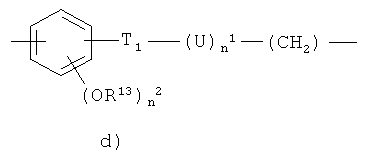
где
n2 представляет целое число от 0 до 2, R13 представляет Н или СН3, T1 представляет -O-С(О)- или -С(O)O-;
n1 представляет 1 и U представляет линейный C1-С10алкилен или U
представляет линейный или разветвленный C1-С10алкилен, замещенный группой -ONO2;
e)
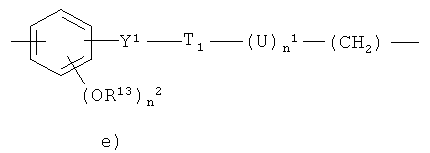
n2 представляет 1, R13 представляет СН3, Y1 представляет -СН=СН-(СН2)n 2'- и n2' представляет 0; T1 представляет -О-С(О)- и U представляет линейный C1-С10 алкилен;
e′)
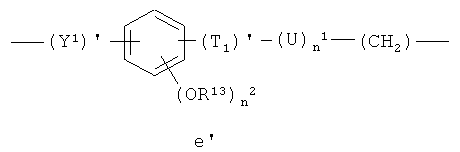
где
n2 представляет 1; R13 представляет СН3;
Y1 представляет -(CH2)n 2′-CH=CH- и n2′ представляет 0;
(Т1)′=-О-С(О)-;
n1 представляет 1 и U представляет линейный C1-С10алкилен или U представляет линейный или разветвленный C1-С10алкилен, замещенный группой -ONO2;
когда Y и Y′ выбраны из d), e) или е′), группа -ONO2 группы -(Т′-Y-ONO2) связана с группой -(СН2)-;
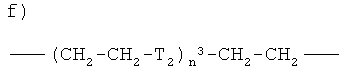
где Т2 представляет -О- или -S-, -NH-, предпочтительно Т2 представляет -O-,
n3 представляет 1 или 2.
Другое воплощение изобретения относится к соединениям формулы (I), где
R представляет кортикостероид формулы (II), как указано выше;
а равно 0,
Rx представляет
(а5) -R1b-CH(NHR4a)-C(O)-(T-Y-ONO2) или
(а9) -R1b-CH(NH-T′-Y′-ONO2)-С(О)-(T-Y-ONO2), где
R1b группы А10) представляет -С(O)-СН2-,
R4a представляет Н или -С(О)СН3;
Т выбран из -O-, -S-, -NR′-, где R′, как указано выше,
Т′ представляет -С(O)- и
Y и Y′, каждый, независимо выбраны из
а)
- прямого или разветвленного С1-С10алкилена,
- прямого или разветвленного C1-С10алкилена, замещенного группой -ONO2;
d)
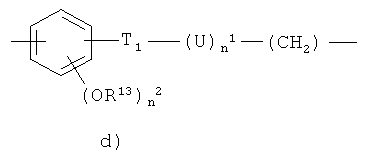
где
n2 представляет целое число от 0 до 2, R13 представляет Н или СН3, T1
представляет -O-С(О)- или -С(O)O-;
n1 представляет 1 и U представляет линейный C1-С10алкилен или U
представляет линейный или разветвленный C1-С10алкилен, замещенный группой -ONO2;
e)
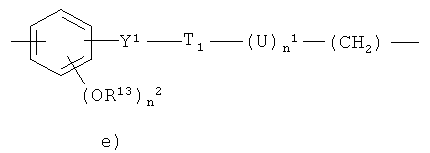
n2 представляет 1, R13 представляет СН3, Y1 представляет -СН=СН-(СН2)n 2′- и n2′ представляет 0; T1 представляет -О-С(О)- и U представляет линейный C1-С10алкилен;
e′)
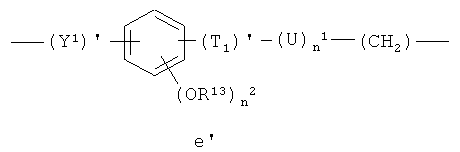
где
n2 представляет 1; R13 представляет СН3;
Y1 представляет -(CH2)n 2′-CH=CH- и n2′ представляет 0;
(Т1)′=-O-С(O)-;
n1 представляет 1 и U представляет линейный C1-С10алкилен или U представляет линейный или разветвленный C1-С10алкилен, замещенный группой -ONO2;
когда Y и Y′ выбраны из d), е) или е′), группа -ONO2 групп -(T-Y-ONO2), (Т′-Y-ONO2), -(T′′-Y′-ONO2), -(T′-Y′-ONO2), -(T′′′-Y-ONO2) и -(T′′′-Y′-ONO2) связана с группой -(СН2)-;
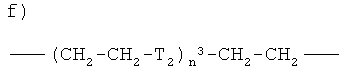
где Т2 представляет -О- или -S-, -NH-, предпочтительно Т2 представляет -O-,
n3 представляет 1 или 2.
Другое воплощение изобретения относится к соединениям формулы (I), где
R представляет кортикостероид формулы (II), как указано выше;
а представляет 0,
Rx представляет
(b2) -С(О)-СН2-СН(R2)-NH-(Т′-Y-ONO2),
где
R2 группы В1) выбран из Н,
Т′ представляет -С(O)-,
Y и Y′, каждый, независимо выбраны из
а)
- прямого или разветвленного C1-С10алкилена,
- прямого или разветвленного C1-С10алкилена, замещенного группой -ONO2;
d)
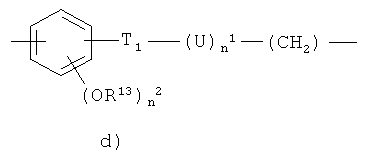
где
n2 представляет целое число от 0 до 2, R13 представляет Н или СН3, T1 представляет -O-С(О)- или -С(O)O-;
n1 представляет 1 и U представляет линейный C1-С10алкилен или U представляет линейный или разветвленный С1-С10алкилен, замещенный группой -ONO2;
e)
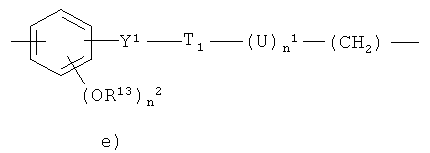
n2 представляет 1, R13 представляет СН3, Y1 представляет -СН=СН-(СН2)n 2′- и n2′ представляет 0; T1 представляет -О-С(О)- и U представляет линейный C1-С10 алкилен;
e′)
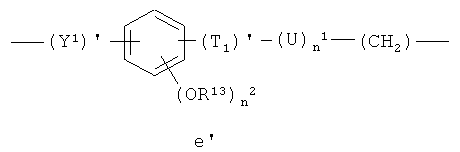
где
n2 представляет 1; R13 представляет СН3;
Y1 представляет -(CH2)n 2'-СН=СН- и n2′ представляет 0;
(T1)′=-O-C(O)-;
n1 представляет 1 и U представляет линейный C1-С10алкилен или U представляет линейный или разветвленный С1-С10алкилен, замещенный группой -ONO2;
когда Y и Y′ выбраны из d), е) или е′), группа -ONO2 групп -(T-Y-ONO2), -(T′-Y-ONO2), -(T′′-Y′-ONO2), -(T′-Y′-ONO2), -(T′′′-Y-ONO2) и -(T′′′-Y′-ONO2) связана с группой -(CH2)-;
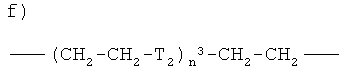
где Т2 представляет -О- или -S-, -NH-, предпочтительно Т2 представляет -O-,
n3 представляет 1 или 2.
Предпочтительными воплощениями настоящего изобретения являются соединения, формулы которых приведены ниже:
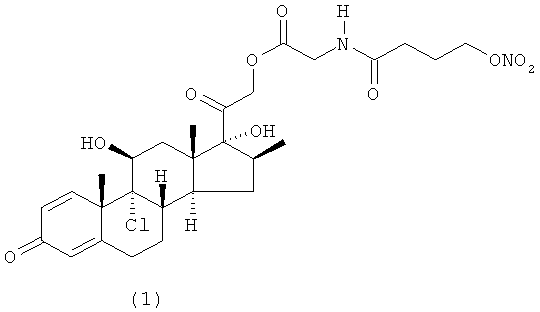
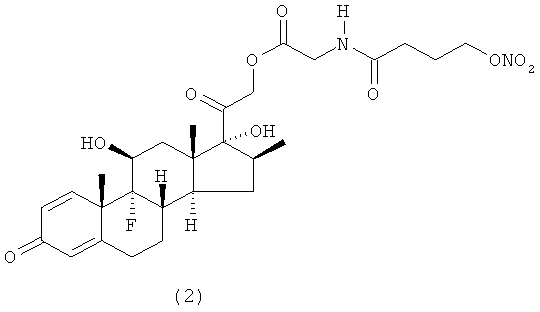
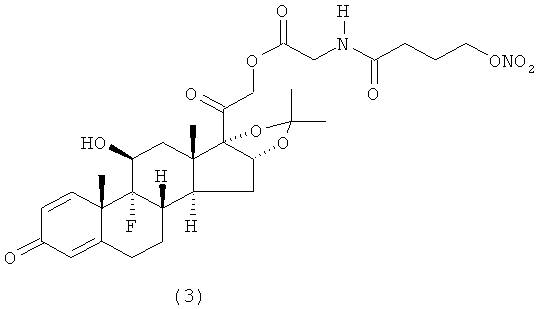
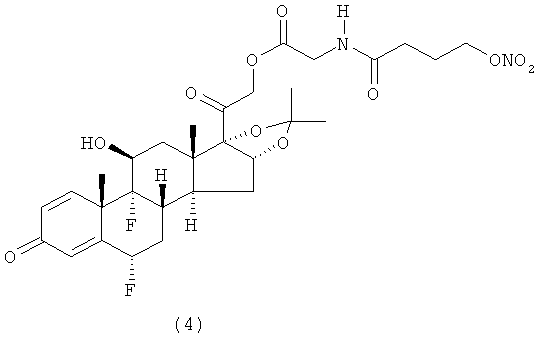
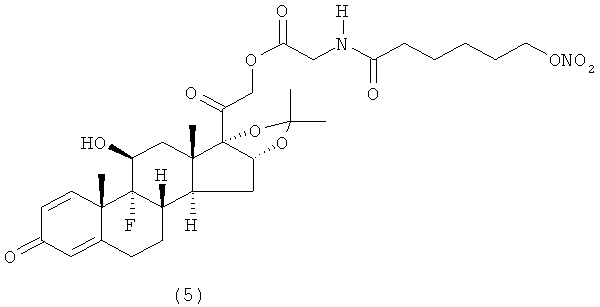
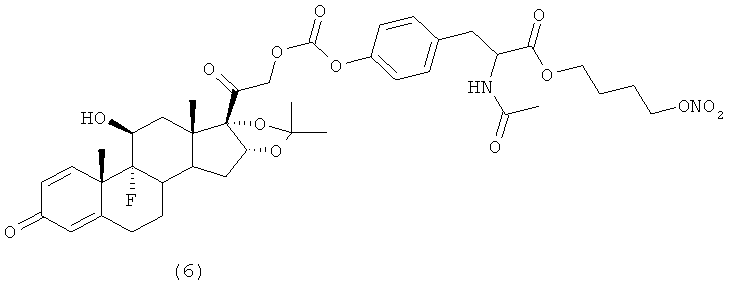
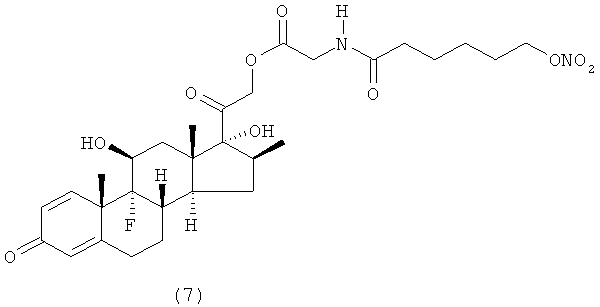
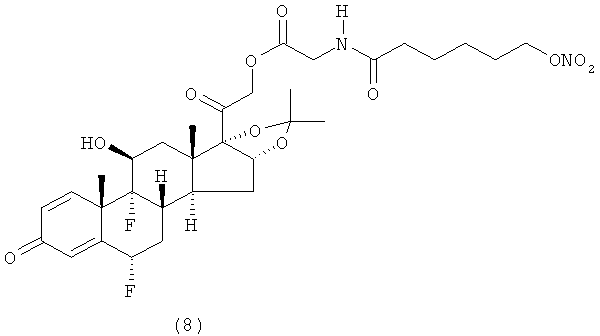

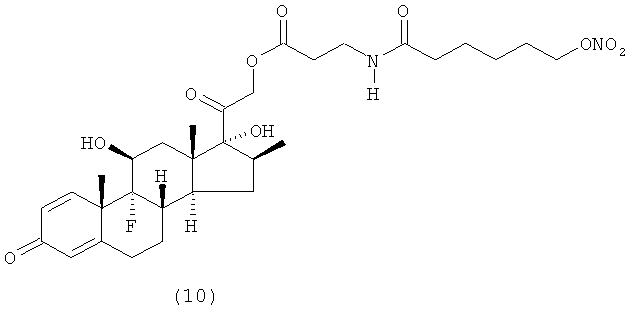
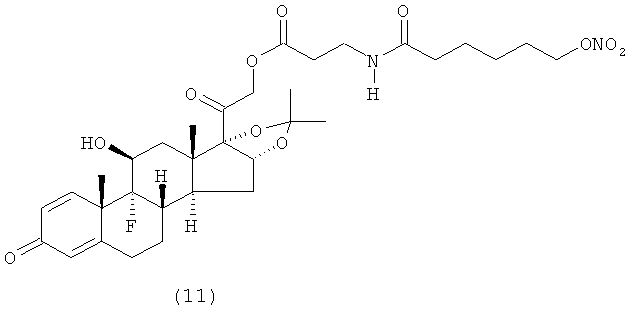
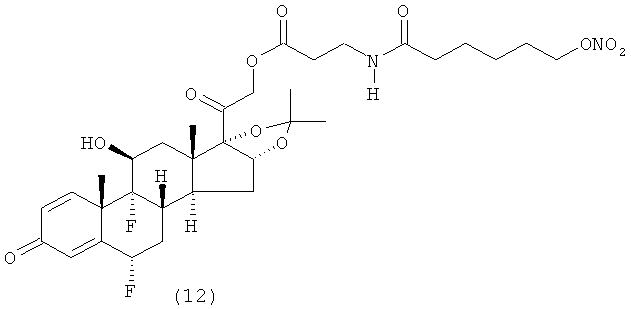
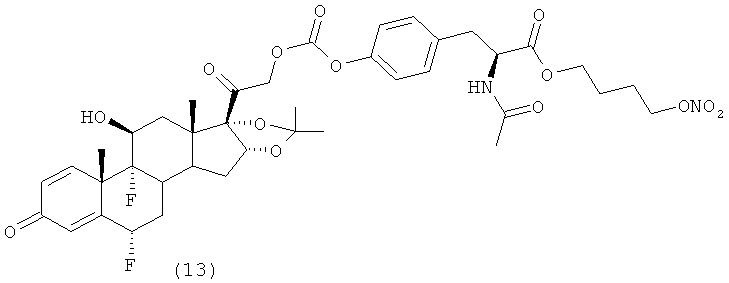
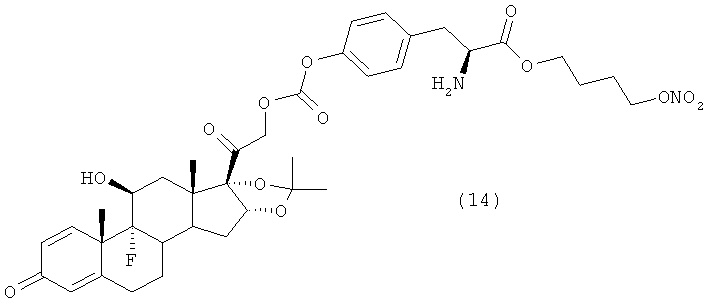
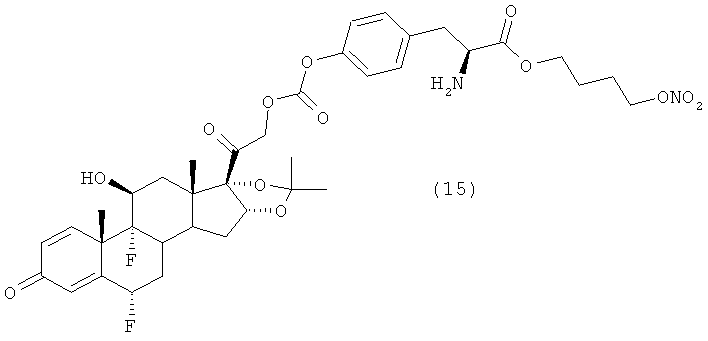
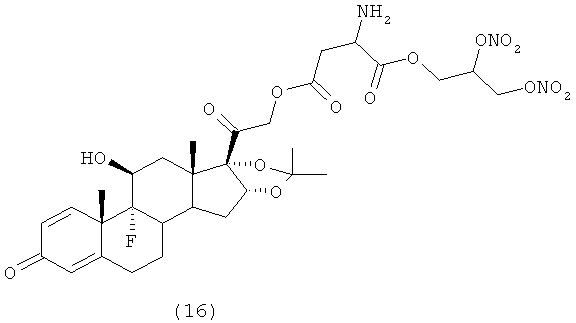
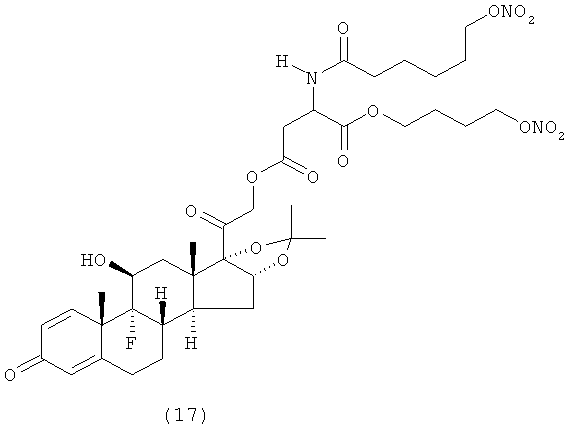
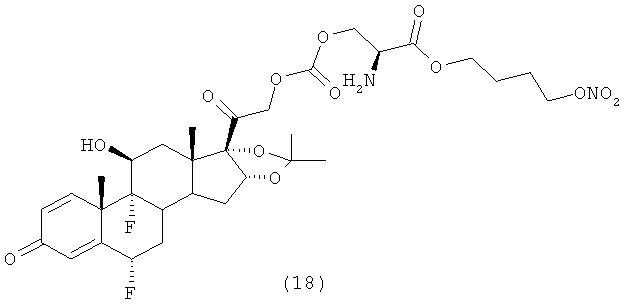
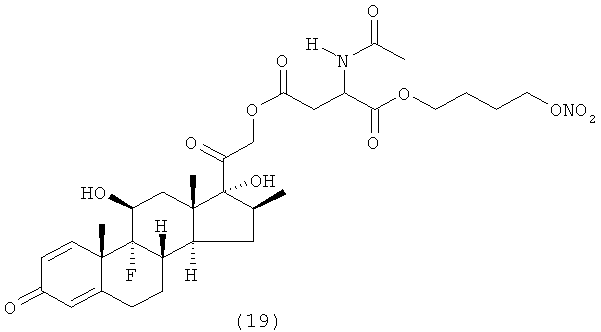
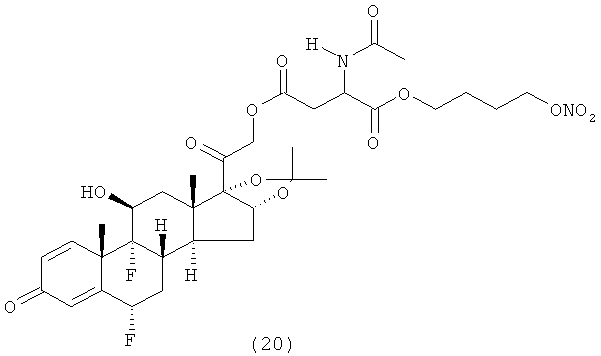
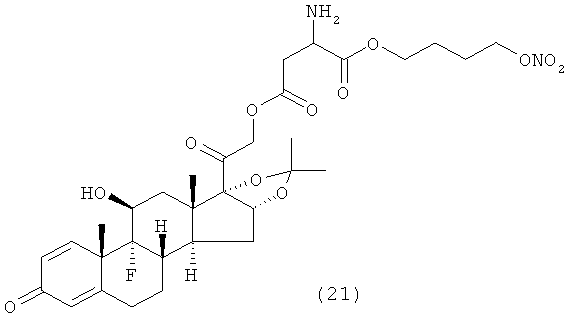
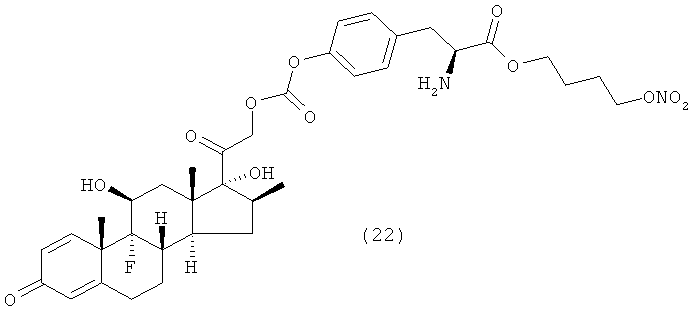
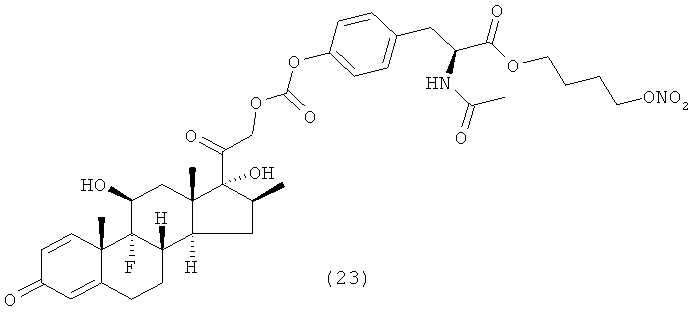
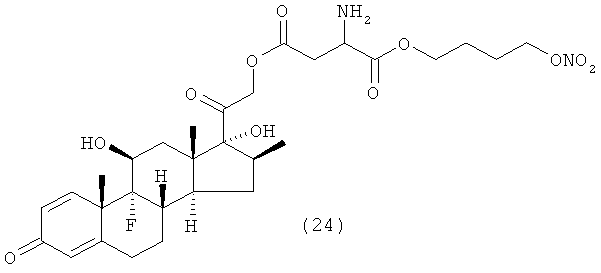
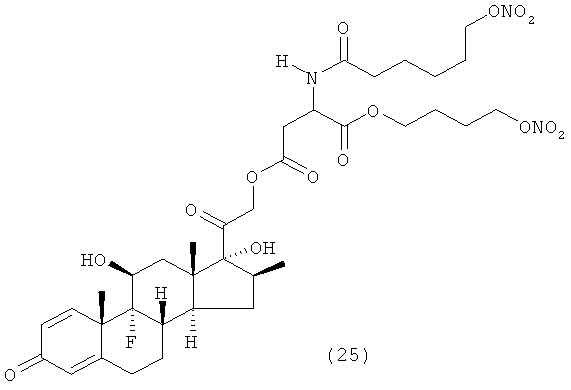
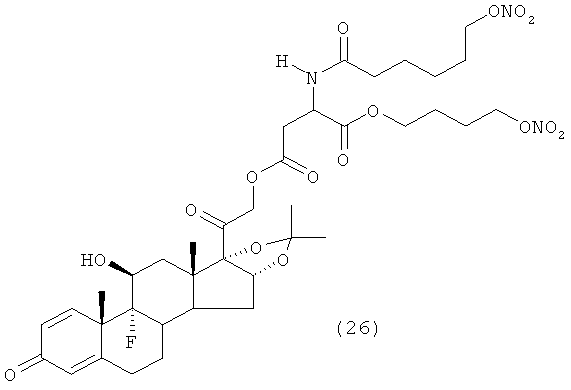
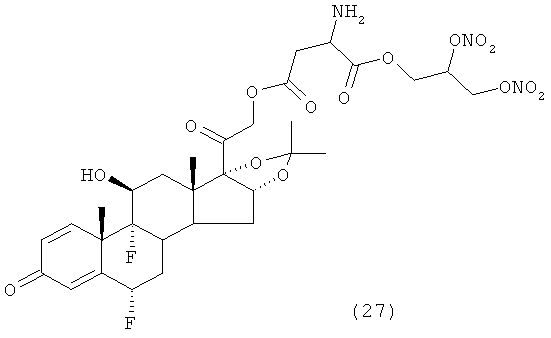

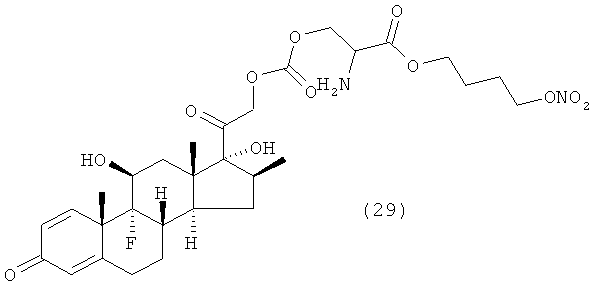
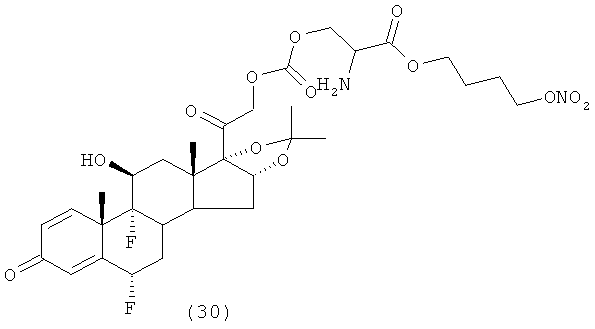
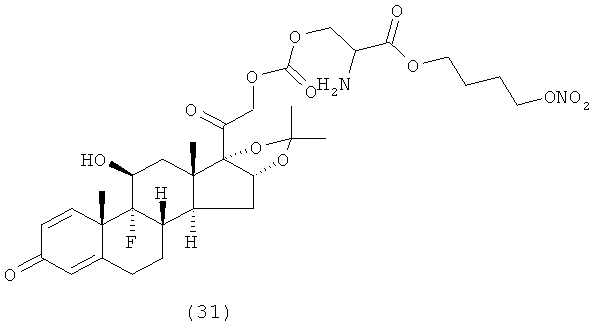
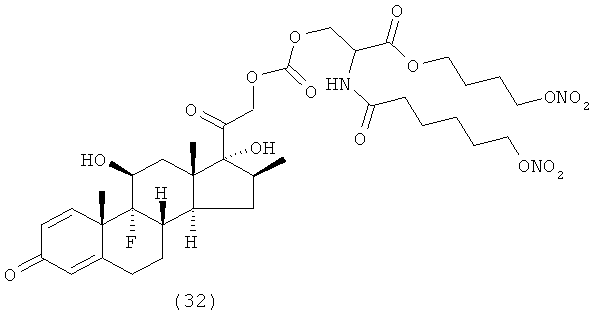
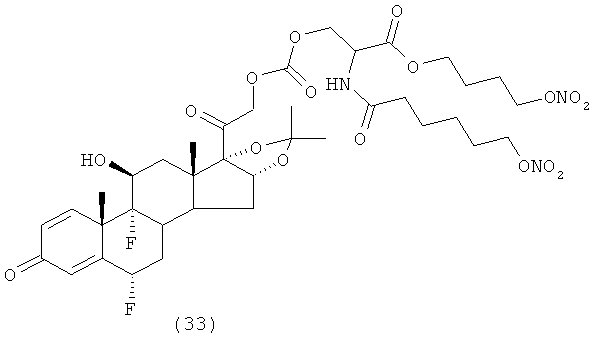
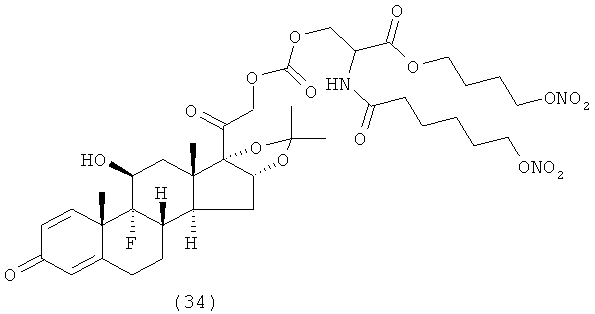
Как указано выше, настоящее изобретение включает также фармацевтически приемлемые соли соединений формулы (I) и их стереоизомеры.
Примерами фармацевтически приемлемых солей являются соли с неорганическими основаниями, такими как гидроксиды натрия, калия, кальция и алюминия, или органическими основаниями, такими как лизин, аргинин, триэтиламин, дибензиламин, пиперидин и другие приемлемые органические амины.
В соответствии с настоящим изобретением соединения, содержащие в молекуле один солеобразующий атом азота, могут быть превращены в соответствующие соли реакцией в органическом растворителе, таком как ацетонитрил, тетрагидрофуран, с соответствующими органическими или неорганическими кислотами.
Примерами органических кислот являются: щавелевая, винная, малеиновая, янтарная, лимонная кислоты. Примерами неорганических кислот являются: азотная, хлористоводородная, серная, фосфорная кислоты. Предпочтительными являются соли с азотной кислотой.
Соединения настоящего изобретения, которые имеют один или более асимметричных атомов углерода, могут находиться в виде оптически чистых энантиомеров, чистых диастереомеров, смесей энантиомеров, смесей диастереомеров, энантиомерных рацемических смесей, рацематов или рацемических смесей. Объектом настоящего изобретения являются также все возможные изомеры, стереоизомеры соединений формулы (I) и их смеси.
Соединения настоящего изобретения сформированы в соответствующие фармацевтические композиции с замедленным высвобождением для парэнтерального, перорального и местного применения, например для сублингвального введения, введения с помощью ингалятора, суппозитория или клизмы, или для трансдермального введения в соответствии с хорошо известными в данной области технологиями, вместе с обычно используемыми эксципиентами; см., например, публикацию "Remington′s Pharmaceutical Sciences" 15th Ed.
Количество молей основы действующего начала в указанных композициях то же или меньше, чем количество соответствующего пролекарства.
Ежедневно вводимые дозы являются теми же, что и для пролекарства или ниже. Ежедневные пролекарственные дозы можно найти в соответствующих публикациях, таких как, например, "Physician's Desk reference".
Соединения настоящего изобретения используются в основном для лечения глазных заболеваний, таких как глазная гипертония, возрастная макулярная дистрофия, диабетический отек желтого пятна, диабетическая ретинопатия, гипертоническая ретинопатия и ретинальная васкулопатия.
Способы синтеза
1) Соединения указанной выше общей формулы (I), где а равно 0, радикал Rx выбран из (а2), (а4), (а8), (b2), (b4), (b8), (c2), (e2), (f1), (g2), (hi), (i1), (l2), (m2), (n2), (o2), (p2), (q2), (r2), (s2), (t2), (u2), (v2), могут быть получены:
1-i) реакцией соединения (IIa)
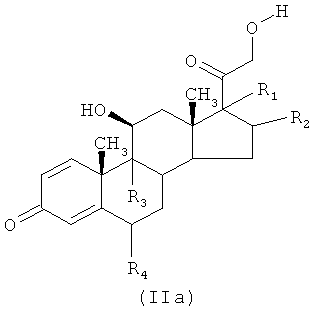
где R1, R2, R3, R4, как указано выше, с соединением формулы (Ia)
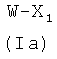
где W представляет -ОН, Cl, O-Ra, где Ra представляет пентафторфенил, 4-нитрофенил или -(N-сукцимидил), X1, как указано ниже, с получением соединения формулы (IIa′)
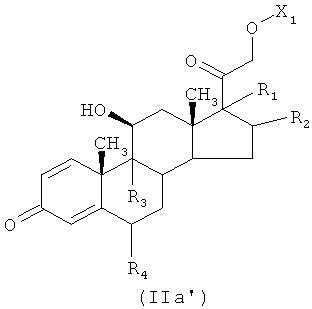
где R1, R2, R3, R4, как указано выше, и X1, как указано ниже,
X1 представляет радикал, имеющий следующее значение:
-(а2′) -С(O)-CH(R1′)-NH-(T′-Y-Q),
где R1′ выбран из
А1), как указано выше, или
А2′) -CH2-SP1, -СН2-ОР′, -СН(СН3)-ОР1, -CH2[(С6Н4)-4-ОР1], -СН2-[(С6Н3)-(3,5-дииодо)-4-ОР1], -СН2-[(С6Н3)-3-нитро-4-ОР1] или
A3′) -CH2-NHR′′′′, -(CH2)2-NHR′′′′, -(СН2)3-NHR′′′′, -(CH2)4-NHR′′′′,
где R′′′′ представляет Р3 или -С(O)СН- или

где R5a, как указано выше;
А4′) -CH2-C(O)R′′′′′, -(CH2)2-C(O)R′′′′′, -(CH2)4-С(O)R′′′′′,
где R′′′′′ представляет Р2, -OR5a или

где R5a, как указано выше;
- (а4′) -С(О)-СН(R1a-Т′′-Y′-Q)-NHR4a′
- (а8′) -С(О)-СН(R1a-T′′-Y′-Q)-NH-(Т′-Y-Q),
где R1a, как указано выше;
-(b2′) -С(O)-CH2-CH(R2′)-NH-(T′-Y-Q),
где R2′ выбран из
В1), как указано выше, или
В2′) -СН(СН3)-ОР1, -СН2-[(С6Н4)-4-ОР1];
В3′) -CH2-NHR′′′′, -(CH2)2-NHR′′′′, -(СН2)3-NHR′′′′, -(СН2)4-NHR′′′′,
где R′′′′, как указано выше;
В4′) -CH2-C(O)-R′′′′′, -(CH2)2-C(O)-R′′′′′, -(СН2)4-С(О)-R′′′′′, где
R′′′′′, как указано выше;
R4a′ представляет Р3 или -С(O)-СН3 или

- (b4′) -С(О)-СН2-CH(R2a-Т′′-Y′-О)-NHR4a′
- (b8′) -С(О)-СН2-СН(R2a-T′′-Y′-Q)-NH-(Т′-Y-Q),
где R2a и R4a′, как указано выше;
- (с2′) -C(O)-(CH2)b-NH-(T′-Y-Q);
- (e2′)
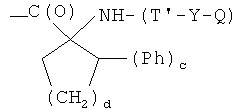
- (f1′)
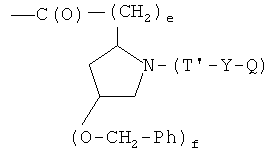
- (g2′)
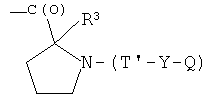
- (h1′)
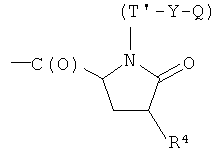
- (i1′)

- (l2′)
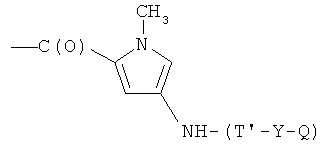
- (m2′)
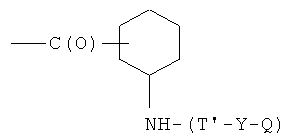
- (n2′)
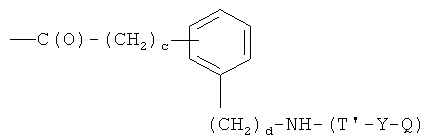
- (o2′)
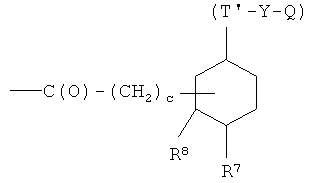
- (p2′)
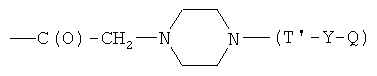
- (q2′)
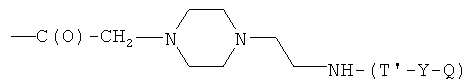
- (r2′)
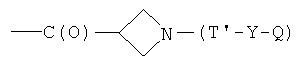
- (s2′)
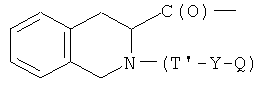
- (t2′)
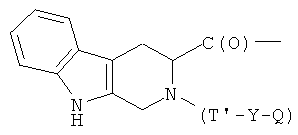
- (u2′)
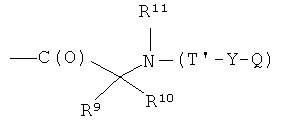
- (v2′)
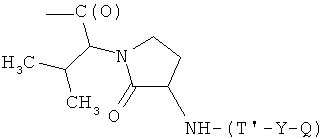
где R3, R4, R5, R6, R7, R8, R9, R10, R11, b, c, d, e и f, как указано выше;
где Р1 представляет гидроксил- или тиолзащищающие группы, такие как силиловые эфиры, например триметилсилил, трет-бутил-диметилсилил или трифенилметил и которые описаны в Т.W.Greene "Protective groups in organic synthesis", Harvard University Press, 1980, Р2 представляет карбоксилзащищающую группу, такую как третбутиловый эфир и которые описаны в Т.W.Greene "Protective groups in organic synthesis", Harvard University Press, 1980, Р3 представляет аминзащищающую группу, такие как трет-бутоксикарбонил (Boc), флуоренилметилоксикарбонил (Fmoc) или описанные в Т.W.Greene "Protective groups in organic synthesis", Harvard University Press, 1980.
Т, Т′, Т′′, Y и Y′, как указано выше,
Q независимо представляет -ONO2 или Z2, где Z2 выбран из группы,
состоящей из: хлор, бром, иод, мезил или тозил, и
1-ii)
когда Q представляет Z2, превращением полученного на стадии 1-i) соединения в нитропроизводное путем взаимодействия с источником нитрата, таким как нитрат серебра, нитрат лития, нитрат натрия, нитрат калия, нитрат магния, нитрат кальция, нитрат железа, нитрат цинка или нитрат татраалкиламмония (где алкил представляет C1-С10алкил), в подходящем органическом растворителе, таком как ацетонитрил, тетрагидрофуран, метилэтилкетон, этилацетат, ДФА, в темноте при температуре от комнатной до температуры кипения растворителя; предпочтительным источником нитрата является нитрат серебра, и
1-iii) необязательным снятием защитных групп с полученных на стадии 1-i) или 1-ii) соединений, как описано в Т.W.Greene "Protective groups in organic synthesis", Harvard University Press, 1980, 2nd edition. Ионы фтора являются предпочтительными для удаления силильной эфирной защитной группы.
Для удаления (Boc) защитной группы предпочтительной является трифторуксусная кислота или безводная неорганическая кислота, для удаления трифенилметильной защитной группы предпочтительной является безводная органическая или неорганическая кислота. Для удаления (Fmoc) защитной группы предпочтительным является органическое основание, такое как пиперидин. Для удаления третбутилэфирной защитной группы предпочтительной является водная или безводная органическая или неорганическая кислота.
1-i-1) Реакцию соединения формулы (Ia), где W=-ОН и X1, как указано выше, с соединением формулы (IIa) можно проводить в присутствии конденсирующего агента, такого как дициклогексилкарбодиимид (DCC), N′-(3-диаминопропил-N-этилкарбодиимид гидрохлорид (EDAC), N,N′-карбонилдиимидазол (CDI), в присутствии или нет основания, такого как, например, N,N-диметиламинопиридин (DMAP).
Реакцию ведут в инертном сухом органическом растворителе, таком как N,N′-диметилформамид, тетрагидрофуран, бензол, толуол, диоксан, полигалогенированный алифатический углеводород, при температуре от -20°С и 50°С. Реакция заканчивается в интервале от 30 минут до 36 часов.
1-i-2) Реакцию соединения формулы (Ia), где W=-O-Ra, где Ra и X1, как указано выше, с соединением формулы (IIa) можно проводить в присутствии катализатора, такого как N,N-диметиламинпиридин (DMAP), или в присутствии DMAP и кислоты Льюиса, такой как Sc(OTf)3 или Bi(OTf)3. Реакцию ведут в инертном органическом растворителе, таком как N,N′-диметилформамид, тетрагидрофуран, бензол, толуол, диоксан, полигалогенированный алифатический углеводород, при температуре от -20°С и 40°С. Реакция заканчивается в интервале от 30 минут до 36 часов.
1-i-3) Реакцию соединения формулы (Ia), где W=-Cl и X1, как указано выше, с соединением формулы (IIa) можно проводить в присутствии органического основания, такого как N,N-диметиламинопиридин (DMAP), триэтиламин, пиридин. Реакцию ведут в инертном органическом растворителе, таком как N,N′-диметилформамид, тетрагидрофуран, бензол, толуол, диоксан, полигалогенированный алифатический углеводород, при температуре от -20°С и 40°С. Реакция заканчивается в интервале от 30 минут до 36 часов.
Соединения формулы (IIa) являются коммерчески доступными соединениями.
1a) Соединения формулы (Ia), где W представляет -ОН, Т и Т′′ представляет С(O) и X1 представляет радикал, выбранный из (а2′), (а4′), (b2′), (b4′), (с2′), (е2′), (f1′), (g2′), (h1′), (i1′), (l2′), (m2′), (n2'), (o2′), (p2′), (q2′), (r2′), (s2′), (t2′), (u2′), (v2′), где R1′ выбран из A1), А2′), A3′), А4′), R1a выбран из А5) или А6), R2a выбран из В5) или В6) и R2′ выбран из В1), B2′), В3′), B4′) и Y, Y′ и R4a′, как указано выше, могут быть получены
1a-i) реакцией соединения формулы (IIIa)
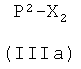
где Р2, как указано выше, Х2 представляет радикал, имеющий следующие значения
- (а2′′) -С(О)-CH(R1′)-NH2,
- (а4′′) -С(О)-CH(R1a-H)-NHR4a′,
где R1′ выбран из А1), А2′), A3′), А4′), R1a выбран из А5) или А6) и R4a', как указано выше,
- (b2′′) -С(O)-СН2-CH(R2')-NH2,
- (b4′′) -С(O)-СН2-СН(R2a-H)-NHR4a′,
где R2′ из В1), В2′), В3′), В4′), R2a выбран из В5) или В6) и R4a′, как указано выше,
- (с2′′) -C(O)-(CH2)b-NH2,
- (e2′′)
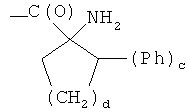
- (f1′′)
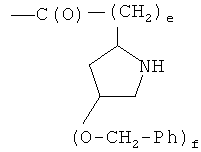
- (g2′′)
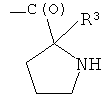
- (h1′′)
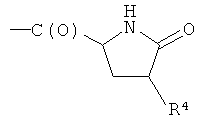
- (i1′′)
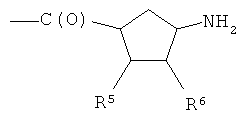
- (l2′′)
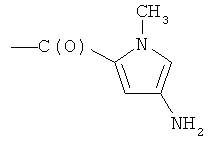
- (m2′′)
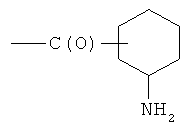
- (n2′′)
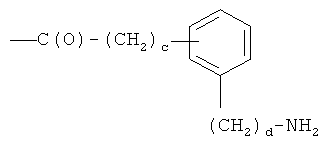
- (o2′′)
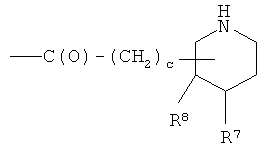
- (p2′′)
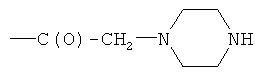
- (q2′′)
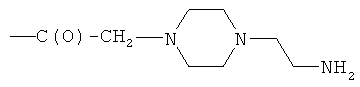
- (r2′′)
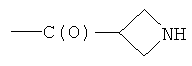
- (s2′′)
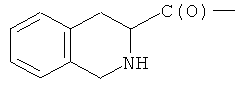
- (t2′′)
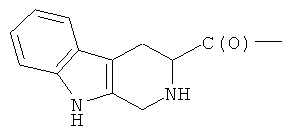
- (u2′′)
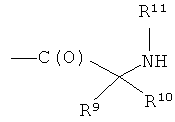
- (v2′′)
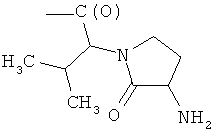
где R3, R4, R5, R6, R7, R8, R9, R10, R11, b, c, d, e и f, как указано выше, с соединением формулы (IVa)
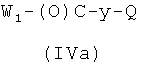
где W1 представляет ОН или O-Ra и Ra и Q, как указано выше, у представляет радикал Y, когда Х2 выбран из (а2′), (b2′), (с2′), (е2′), (f1′), (g2′), (h1′), (i1′), (l2′), (m2′), (n2′), (o2′), (p2′), (q2′), (r2′), (s2′), (t2′), (u2′), (v2′), и у представляет радикал Y′, когда Х2 выбран из (а4′) или (b4′), где Y и Y′, как указано выше, и 1a-ii), когда Q представляет Z2, превращением соединения, полученного на стадии 1a-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
1a-iii) необязательным снятием защитных групп с полученного на стадии 1a-i) или 1a-ii) соединения, как указано выше.
Реакцию соединения формулы (IIIa), где Р2 и Х2, как указано выше, с соединением формулы (IVa), где W1 представляет ОН, y, Q, как указано выше, можно проводить так, как описано в 1-i-1), или в присутствии других известных конденсирующих реагентов, таких как O-(7-азабензотриазол-1-ил)-N,N,N1,N′-тетраметилурониумгексафторфосфат (HATU).
Реакцию соединения формулы (III), где Р2 и X2, как указано выше, с соединением формулы (IVa), где W1 представляет O-Ra, y, Q, как указано выше, можно проводить, как описано в 1-i-2).
Соединения формулы (IIIa) являются коммерчески доступными или могут быть получены известными в литературе методами.
Соединения формулы (IVa), где W1 представляет ОН, y и Q, как указано выше, могут быть получены из соответствующих спиртов формулы НООС-y-ОН (IVb) реакцией с азотной кислотой и уксусным ангидридом при температуре от -50°С до 0°С или из соответствующих производных формулы HOOC-y-Z2 (IVc), где Z2, как указано выше, реакцией с источником нитрата, как описано выше. Альтернативно реакцию с AgNO3 можно осуществлять под воздействием микроволнового излучения в растворителе, таком как ацетонитрил ацетонитрил или ТГФ, при температуре 100-180°С за 1-60 мин.
Соединения формулы (IVb) являются коммерчески доступными.
Соединения формулы (IVc) являются коммерчески доступными или могут быть получены известными в литературе методами.
Соединения формулы (IVc) являются коммерчески доступными или получены известными в литературе методами.
Соединения формулы (IVa), где W1 представляет O-Ra, y, Q, как указано выше, могут быть получены из соответствующих кислот формулы (IVa), где W1 представляет ОН, как описано в литературе.
Соединения формулы (Ia), где W=Cl или O-Ra, X1 выбран из (а2′), (а4′), (b2′), (b4′), (c2′), (е2′), (f1′), (g2′), (h1′), (i1′), (l2′), (m2′), (n2′), (o2′), (p2′), (q2′), (r2′), (s2′), (t2′), (u2′), (v2′), где R1′ выбран из A1), А2′), A3′), А4′), R1a выбран из А5) или А6), R2a выбран из В5) или В6) и R2′ выбран из B1), B2′), В3′)/В4′), и где Y, Y′ и Q, как указано выше, и Т и Т′′ представляют С (О), могут быть получены из соответствующих кислот (Ia), где W представляет -ОН, известными из литературы методами.
1b) Соединения формулы (Ia), где W представляет -ОН, X1 представляет радикал, выбранный из (а2′), (а4′), (b2′), (b4′) (c2′), (e2′), (f1′), (g2′), (h1′), (i1′), (L2′), (m2′), (n2′), (o2′), (p2′), (q2′), (r2′), (s2′), (t2′), (u2′), (v2′), где R1′ выбран из A1), А2′), A3′), A4′), RIa выбран из А5) или А6), R2a выбран из В5) или В6) и R2′ выбран из B1), B2′), В3′), B4′), Y и Y′, как указано выше, T′ и Т′′ представляют С(O)-Х′′, где X′′ представляет -О- или -S-, могут быть получены
1b-i) реакцией соединения формулы (IIIa)
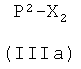 ,
,
где Р2 и Х2, как указано выше, с соединением формулы (IVd)
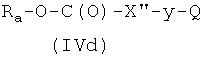 ,
,
где Ra, X′′ и Q, как указано выше, у представляет радикал Y, когда Х2 выбран из (а2′), (b2′), (c2′), (e2′), (f1′), (q2′), (h1′), (i1′), (l2′), (m2′), (r2′), (s2′), (t2′), (u2′), (v2′), и y представляет радикал Y′, когда Х2 выбран из (а4′) или (b4′), где Y и Y′, как указано выше, и
1b-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 1b-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
1b-iii) необязательным снятием защитных групп с полученного на стадии 1b-i) или 1b-ii) соединения, как указано выше.
Реакцию соединения формулы (IIIa), где Р2 и Х2, как указано выше, с соединением формулы (IVd), где Ra, X′′, y и Q, как указано выше, можно проводить так, как описано в 1-i-2).
Соединения формулы (IVd), где Ra, X′′, y, Q, как указано выше, могут быть получены из соединений формулы HX′′-y-Q (IVe), где X′′, y, Q, как указано выше, известными из литературы методами.
Соединения формулы (IVe) являются коммерчески доступными или известны из литературы.
Соединения формулы (Ia), где W представляет -Cl или O-Ra, X1 выбран из (а2′), (а4′), (b2′), (b4′), (c2′), (e2′), (f1′), (g2′), (h1′), (i1′), (l2′), (m2′), (n2′), (o2′), (p2′), (q2′), (r2′), (s2′), (t2′), (u2′), (v2′), где R1′ выбран из A1), А2′), A3′), А4′), RIa выбран из A5) или A6), R2a выбран из В5) или В6) и R2′ выбран из B1), B2′), В3′), В4′), Y, Y′ и Q, как указано выше, Т′ и Т′′ представляют С(O)-Х′′, где X′′ представляет О или S, могут быть получены из соответствующих кислот (Ia), где W представляет -ОН, известными из литературы методами.
1c) Соединения формулы (Ia), где W представляет -ОН и X1 представляет радикал, выбранный из (а8′) или (b8′), где RIa выбран из A5) или A6), R2a выбран из В5) или В6), Q, как указано выше, Т и Т′′ представляют С(O), Y и Y′ являются одинаковыми и имеют указанные выше значения, могут быть получены
1c-i) реакцией соединения формулы (IIIb),
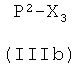 ,
,
где Р2, как указано выше, Х3 представляет радикал формулы
- (а8′′) -С(O)-CH(R1a-Н)-NH2
-(b8′′) -С(O)-СН2-CH(R2a-Н)-NH2,
где R1a выбран из A5) или A6), R2a выбран из В5) или В6), с соединением формулы (IVa)
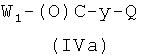
где W1 и Q, как указано выше, у представляет радикал Y или Y′, где Y и Y′, как указано выше, и,
1c-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 1c-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
1c-iii) необязательным снятием защитных групп с полученных на стадии 1c-i) или 1c-ii) соединений, как указано выше.
Реакцию соединения формулы (IIIb), где Р2 и Х3, как указано выше, с соединением формулы (IVa), где W1 представляет ОН, y и Q, как указано выше, можно проводить так, как описано в 1a-i), используя соотношение (IIIb)/(IVa) 1:2.
Реакцию соединения формулы (IIIb), где Р2 и Х3, как указано выше, с соединением формулы (IVa), где W1 представляет ORa, y и Q, как указано выше, можно проводить так, как описано в 1-i-2), используя соотношение (IIIb)/(IVa) 1:2.
Соединения формулы (IIIb) являются коммерчески доступными или могут быть получены известными из литературы методами.
Соединения формулы (Ia), где W представляет -Cl или O-Ra, X1 представляет радикал, выбранный из (а8′) или (b8′), где R1a выбран из А5) или А6), R2a выбран из В5) или В6) и где Y, Y′ и Q, как указано выше, и Т′ и Т′′ представляют С(О), могут быть получены из соответствующих кислот (Ia), где W представляет -ОН, известными из литературы методами.
1d) Соединения формулы (Ia), где W представляет -ОН, X1 представляет радикал, выбранный из (а8′) или (b8′), где R1a выбран из А5) или А6), R2a выбран из В5) или В6), Q, Y и Y′, как указано выше, Т′ представляет С(O) или С(O)-Х′′, где X′′, как указано выше, Т′′ представляет С(О), могут быть получены
1d-i) реакцией соединения формулы (Ib)
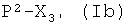
где Р2, как указано выше, Х3 представляет радикал формулы
- (а8′′′) -С(О)-СН(R1a-H)-NH-(Т′-Y-Q)
- (b8′′′) -С(О)-СН2-СН(R2a-H)-NH-(Т′-Y-Q),
где R1a выбран из А5) или А6), R2a выбран из В5) или В6), с соединением формулы (IVa)
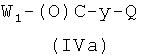
где W1 и Q, как указано выше, у представляет радикал Y′, где Y′, как указано выше, и
1d-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 1d-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
1d-iii) необязательным снятием защитных групп с полученных на стадии 1d-i) или 1d-ii) соединений, как указано выше.
Реакцию соединения формулы (Ib), где Р2 и Х3', как указано выше, с соединением формулы (IVa), где W1 представляет ОН, y и Q, как указано выше, можно проводить так, как описано в 1a-i).
Реакцию соединения формулы (Ib), где Р2 и Х3', как указано выше, с соединением формулы (IVa), где W1 представляет OR2, y и Q, как указано выше, можно проводить так, как описано в 1-i-2).
Соединения формулы (Ib), где Т′ представляет С(O), Р2 и Х3', как указано выше, получены, как описано в 1а).
Соединения формулы (Ib), где Т′ представляет С(O)-Х′′, Р2 и Х3', как указано выше, получены, как описано в 1b).
Соединения формулы (Ia), где W представляет -Cl или O-Ra′, X1 представляет радикал, выбранный из (а8′) или (b8′), где R1a выбран из А5) или А6), R2a выбран из В5) или В6) и где Q, Y и Y′,как указано выше, Т′ представляет С(O) или С(O)-Х′′, где X′′, как указано выше, Т′′ представляет С(O), могут быть получены из соответствующих кислот (Ia), где W представляет -ОН, известными из литературы методами.
1e) Соединения формулы (Ia), где W представляет -ОН, X1 представляет радикал, выбранный из (а8′) или (b8′), где R1a выбран из А5) или А6), R2a выбран из В5) или В6), Q, как описано выше, Y и Y' имеют одинаковые описанные выше значения, Т′′ и Т′′ представляют С(O)-Х′′-, где X′′, как указано выше, могут быть получены
1e-i) реакцией соединения формулы (IIIb)
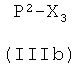 ,
,
где Р2 и Х3, как указано выше, с соединением формулы (IVd)
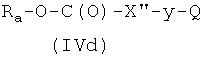
где Ra и Q, как указано выше, y представляет радикал Y′, где Y′, как указано выше, и,
1e-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 1e-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
1e-iii) необязательным снятием защитных групп с полученных на стадии 1e-i) или 1e-ii) соединений, как указано выше.
Реакцию соединения формулы (IIIb), где Р2 и Х3, как указано выше, с соединением формулы (IVd), где Ra, y и Q, как указано выше, можно проводить так, как описано в 1-i-2), используя соотношение (IIIb)/(IVd) 1:2.
Соединения формулы (Ia), где W представляет -Cl или O-Ra, X1 представляет радикал, выбранный из (а8′) или (b8′), где R1a выбран из А5) или А6), R2a выбран из В5) или В6) и где Y, Y′ и Q, как указано выше, и Т′ и Т′′ представляют С(O)-Х′′-, где X′′, как указано выше, могут быть получены из соответствующих кислот (Ia), где W представляет -ОН, известными из литературы методами.
1f) Соединения формулы (Ia), где W представляет -ОН, X1 выбран из (а8′) или (b8′), где R1a выбран из А5) или А6), R2a выбран из В5) или В6), Q, Y и Y′, как указано выше, Т′ представляет С(O) или С(O)-Х′′, где X′′, как указано выше, Т′′ представляет С(О)-X′′, могут быть получены
1f-i) реакцией соединения формулы (Ib)
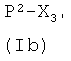
где Х3' и Р2, как указано выше, с соединением формулы (IVd)
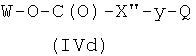
где Wx и Q, как указано выше, у представляет радикал Y′,
где Y′, как указано выше, и,
1f-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 1f-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
1f-iii) необязательным снятием защитных групп с полученных на стадии 1f-i) или 1f-ii) соединений, как указано выше.
Реакцию соединения формулы (Ib), где Р2 и Х3', как указано выше, с соединением формулы (IVd), где W1 представляет ОН, y и Q, как указано выше, можно проводить так, как описано в 1a-i).
Реакцию соединения формулы (Ib), где Р2 и Х3', как указано выше, с соединением формулы (IVd), где W1 представляет ORa, у и Q, как указано выше, можно проводить так, как описано в 1-i-2).
Соединения формулы (Ib) где Т' представляет С(O), Р2 и Х3', как указано выше, получены, как описано в 1а).
Соединения формулы (Ib) где Т′ представляет С(O)-Х′′, Р2 и Х3', как указано выше, получены, как описано в 1b).
Соединения формулы (Ia), где W представляет -Cl или O-Ra′, X1 представляет радикал, выбранный из (а8′) или (b8′), где R1a представляет А5) или А6), R2a представляет В5) или В6) и где Q, Y и Y′, как указано выше, Т′ представляет С(O) или С(O)-Х′′ и Т′′ представляет С(O)-Х, где X′′, как указано выше, могут быть получены из соответствующих кислот (Ia), где W представляет -ОН, известными из литературы методами.
1g) Соединения формулы (Ia), где W представляет -ОН, X1 представляет радикал, выбранный из (а8′) или (b8′), где R1a выбран из А5), А6), R2a выбран из В5), В6), Q, Y и Y′, как указано выше, Т′ представляет С(O) или С(O)-Х′′, где X′′, как указано выше, Т′′ представляет C(O)-NR′, где R′, как указано выше, могут быть получены
1g-i) реакцией соединения формулы (Ib)
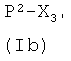
где Х3' и Р2, как указано выше, с соединением формулы
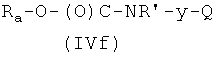
где Ra, R′ и Q, как указано выше, y представляет радикал Y′, где Y′, как указано выше, и,
1g-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 1g-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
1g-iii) необязательным снятием защитных групп с полученных на стадии 1g-i) или 1g-ii) соединений, как указано выше.
Реакцию соединения формулы (Ib), где Р2 и Х3', как указано выше, с соединением формулы (IVf), где Ra, R′, y, Q, как указано выше, можно проводить так, как описано в 1-i-2).
Соединения формулы (Ib), где Т′ представляет С(O), Р2 и Х3', как указано выше, получены, как описано в 1a-i), 1a-ii).
Соединения формулы (Ib), где Т′ представляет С(O)-Х′′, Р2 и Х3', как указано выше, получены, как описано в 1b-i), 1b-ii).
Соединения формулы (IVf), где R′, y и Q, как указано выше, могут быть получены из соединения формулы 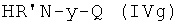 реакцией с эфиром хлормуравьиной кислоты известными из литературы методами.
реакцией с эфиром хлормуравьиной кислоты известными из литературы методами.
Соединения формулы (IVg), где у, как указано выше, и Q представляет Z2, являются коммерчески доступными соединениями, соединения формулы (IVg), где у, как указано выше, и Q представляет -ONO2, могут быть получены из соединения формулы 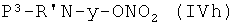 , где Р3, как указано выше, снятием защиты с аминогруппы известными из литературы методами. Соединения формулы (IVh), где Р3, у, как указано выше, могут быть получены из спирта
, где Р3, как указано выше, снятием защиты с аминогруппы известными из литературы методами. Соединения формулы (IVh), где Р3, у, как указано выше, могут быть получены из спирта 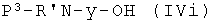 реакцией с нитратом тетраалкиламмония, как уже описано для аналогичных соединений. Соединения формулы (IVi) являются коммерчески доступными или известны из литературы. Альтернативно, соединения формулы (IVh), где Р3, у, как указано выше, могут быть получены из соответствующих соединений формулы
реакцией с нитратом тетраалкиламмония, как уже описано для аналогичных соединений. Соединения формулы (IVi) являются коммерчески доступными или известны из литературы. Альтернативно, соединения формулы (IVh), где Р3, у, как указано выше, могут быть получены из соответствующих соединений формулы 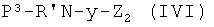 , где Р3, у, Z2, как указано выше, реакцией с источником нитрата, как описано выше.
, где Р3, у, Z2, как указано выше, реакцией с источником нитрата, как описано выше.
Соединения формулы (Ia), где W представляет -Cl или O-Ra, X1 представляет радикал, выбранный из (а8′) или (b8′), где R1a выбран из А5) или А6), R2a выбран из В5) или В6) и где Y, Y′ и Q, как указано выше, и Т′ представляет С(O) или С(O)-Х′′, Т′′ представляет C(O)-NR′-, где X′′ и R′, как указано выше, могут быть получены из соответствующих кислот (Ia), где W представляет -ОН, известными в литературе методами.
1h) Соединения формулы (Ia), где W представляет -ОН, X1 представляет радикал, выбранный из (а8′) или (b8′), где R1a выбран из А7), R2a выбран из В7), Q, Y и Y′, как указано выше, Т′ представляет С(O) или С(O)-Х′′, Т′′ представляет X′′, где X′′, как указано выше, могут быть получены
1h-i) реакцией соединения формулы (Ie),
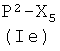 ,
,
где Р2, как указано выше, Х5 представляет радикал формулы
- (а8′′′) -С(О)-СН(R1a-OH)-NH-(T′-Y-Q)
- (b8′′′) -С(О)-СН2-СН(R2a-OH)-NH-(Т′-Y-Q),
где R1a выбран из А7), R2a выбран из В7), с соединением формулы (IVe)
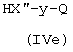 ,
,
где X′′ и Q, как указано выше, y представляет радикал Y′, где Y′, как указано выше, и
1h-ii), когда Q представляет Z2, превращением соединения, полученного на стадии 1h-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
1h-iii) необязательным снятием защитных групп с полученных на стадии 1h-i) или 1h-ii) соединений, как указано выше.
Реакцию соединения формулы (Ie), где Р2 и Х5, как указано выше, с соединением формулы (IVe), где y, X′′ и Q, как указано выше, можно проводить так, как описано в 1-i-1).
Соединения формулы (Ie), где Т' представляет С(O), Р2 и Х5, как указано выше, получены, как описано в 1a-i), 1a-ii).
Соединения формулы (Ie), где Т′ представляет С(O)-Х′′, Р2 и Х5, как указано выше, получены, как описано в 1b-i), 1b-ii).
Соединения формулы (Ia), где W представляет -Cl или O-Ra, X1 представляет радикал, выбранный из (а8′) или (b8′), где R1a выбран из А5) или А6), R2a выбран из В5) или В6) и где Y, Y′ и Q, как указано выше, и Т′ представляет С(O) или С(O)-Х′′, Т′′ представляет X′′, где X′′, как указано выше, могут быть получены из соответствующих кислот (Ia), где W представляет -ОН, известными в литературе методами.
1i) Соединения формулы (Ia), где W представляет -ОН, X1 представляет радикал, выбранный из (а8′) или (b8′), где R1a выбран из А7), R2a выбран из В7), Q, Y и Y′, как указано выше, Т′ представляет С(O) или С(O)-Х′′, где X′′, как указано выше, Т′′ представляет -NR′, где R', как указано выше, могут быть получены
1i-i) реакцией соединения формулы (Ie),
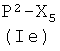 ,
,
где Р2 и Х5, как указано выше, с соединением формулы (IVg)
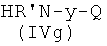 ,
,
где R′ и Q, как указано выше, у представляет радикал Y′, где Y′, как указано выше, и
1i-ii), когда Q представляет Z2, превращением соединения, полученного на стадии 1i-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
1i-iii) необязательным снятием защитных групп с полученных на стадии 1i-i) или 1i-ii) соединений, как указано выше.
Реакцию соединения формулы (Ie), где Р2 и Х5, как указано выше, с соединением формулы (IVg), где R′, y и Q, как указано выше, можно проводить так, как описано в 1a-i).
Соединения формулы (Ia), где W представляет -Cl или O-Ra, X1 представляет радикал, выбранный из (а8′) или (b8′), где R1a выбран из А5) или А6), R2a выбран из В7) и где Y, Y′ и Q, как указано выше, Т′ представляет С(O) или С(O)-Х′′, где X′′, как указано выше, и Т′′ представляет -NR′, где R′, как указано выше, могут быть получены из соответствующих кислот (Ia), где W представляет -ОН, известными в литературе методами.
1l) Соединения формулы (Ia), где W представляет -ОН, X1 представляет радикал, выбранный из (а8′) или (b8′), где R1a выбран из А7), R2a выбран из В7), Q, Y и Y′, как указано выше, Т′ представляет С(O) или С(O)-Х′′, где X′′, как указано выше, Т′′ представляет -O-CH(R′)-O-C(O)-, где R′, как указано выше, могут быть получены
Il-i) реакцией соединения формулы (Ie),
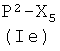 ,
,
где Р2 и Х5, как указано выше, с соединением формулы (IVm)
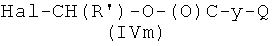 ,
,
где R′ и Q, как указано выше, Hal представляет атом галоида, y представляет радикал Y′, где Y′, как указано выше, и
1l-ii), когда Q представляет Z2, превращением соединения, полученного на стадии 1l-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
1l-iii) необязательным снятием защитных групп с полученных на стадии 1l-i) или 1l-ii) соединений, как указано выше.
Реакцию соединения формулы (Ie), где Р2 и Х5, как указано выше, с соединением формулы (IVm), где R′, y и Q, как указано выше, можно проводить в присутствии неорганического или органического основания в апротонном полярном/неполярном растворителе, таком как ДФА, ТГФ или CH2Cl2, при температуре в диапазоне от 0°С до 100°С или в двухфазной системе Н2О/EtO при температуре от 20°С до 40°С.
Соединения формулы (IVm), где y, Q, R′, как указано выше, Hal представляет атом галогена, могут быть получены реакцией коммерчески доступного соединения R′-CH2-CHO с соединением формулы Hal-(O)C-y-Q (IVn), где y и Q, как указано выше, Hal представляет атом галоида, и ZnCl2 известными из литературы методами.
Соединения формулы (IVn) могут быть получены известными из литературы методами.
Соединения формулы (Ia), где W представляет -Cl или O-Ra, X1 представляет радикал, выбранный из (а8′) или (b8′), где R1a выбран из А7), R2a выбран из В7) и где Y, Y′ и Q, как указано выше, Т′ представляет С(O) или С(O)-Х′′, где X′′, как указано выше, и Т′′ представляет -O-CH(R′)-O-C(O)-, где R′, как указано выше, могут быть получены из соответствующих кислот (Ia), где W представляет -ОН, известными в литературе методами.
1m) Соединения формулы (Ia), где W представляет -ОН, X1 представляет радикал, выбранный из (а8′) или (b8′), где R1a выбран из А7), R2a представляет В7), Q, Y и Y′, как указано выше, Т′ представляет С(O) или С(O)-Х′′, где X′′, как указано выше, Т′′ представляет -O-CH(R′)-O-C(O)-, где R′, как указано выше, могут быть получены
1m-i) реакцией соединения формулы (Ie),
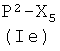 ,
,
где Р2 и Х5, как указано выше, с соединением формулы (IVo)
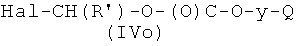
где R′ и Q, как указано выше, y представляет радикал Y′, где Y′, как указано выше, Hal представляет атом галоида, и
1m-ii), когда Q представляет Z2, превращением соединения, полученного на стадии 1m-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
1m-iii) необязательным снятием защитных групп с полученных на стадии 1m-i) или 1m-ii) соединений, как указано выше.
Реакцию соединения формулы (Ie), где Р2 и Х5, как указано выше, с соединением формулы (IVo), где R′, y, Q, Hal, как указано выше, можно проводить, как описано в 1l-i).
Соединения формулы (IVo), где y, Q, R′, как указано выше, могут быть получены реакцией коммерчески доступного соединения формулы Hal-(R′)CH-OC(O)Hal, где Hal, как указано выше, с соединением формулы 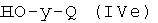 , где y, Q, как указано выше, в присутствии неорганического или органического основания в апротонном полярном или апротонном неполярном растворителе, таком как ДФА, ТГФ или CH2Cl2, при температуре в диапазоне от 0°С до 65°С.
, где y, Q, как указано выше, в присутствии неорганического или органического основания в апротонном полярном или апротонном неполярном растворителе, таком как ДФА, ТГФ или CH2Cl2, при температуре в диапазоне от 0°С до 65°С.
Соединения формулы (Ia), где W представляет -Cl или O-Ra, X1 представляет радикал, выбранный из (а8′) или (b8′), где R1a выбран из А7), R2a выбран из В7) и где Y, Y′ и Q, как указано выше, Т′ представляет С(O) или С(O)-Х′′, где X′′, как указано выше, и Т′′ представляет -O-CH(R′)-O-C(O)O-, могут быть получены из соответствующих кислот (Ia), где W представляет -ОН, известными в литературе методами.
1n) Соединения формулы (Ia), где W представляет -ОН, X1 представляет радикал, выбранный из (а4′) или (b4′), где R1a выбран из А7), R2a выбран из В7), Q, Y′ и R4a', как указано выше, и Т′′ представляет X′′, где X′′, как указано выше, могут быть получены
1n-i) реакцией соединения формулы (IIIc),
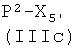 ,
,
где Р2, как указано выше, Х5' представляет
- (а4′′) -С(O)-CH(R1a-ОН)-NHR4a'
- (b4′′) -С(О)-СН2-СН(R2a-OH)-NHR4a'
где R1a выбран из А7), R2a выбран из В7) и Р2, как указано выше, с соединением формулы (IVe)
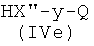
где X′′ и Q, как указано выше, y представляет радикал Y′, где Y′, как указано выше, и
1n-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 1n-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
1n-iii) необязательным снятием защитных групп с полученных на стадии 1n-i) или 1n-ii) соединений, как указано выше.
Реакцию соединения формулы (IIIc), где Р2 и Х5', как указано выше, с соединением формулы (IVe), где X′′, y, Q, как указано выше, можно проводить, как описано в 1-i-1).
Соединения формулы (IIIc), где Х5' и Р2, как указано выше, являются коммерчески доступными или могут быть получены известными из литературы методами.
Соединения формулы (Ia), где W представляет -Cl или O-Ra, X1 представляет радикал, выбранный из (а4′) или (b4′), где R1a выбран из А7), R2a выбран из В7), Y′ и Q, как указано выше, Т′′ представляет X′′, где X′′, как указано выше, могут быть получены из соответствующих кислот (Ia), где W представляет -ОН, известными в литературе методами.
1о) Соединения формулы (Ia), где W представляет -ОН, X1 представляет радикал, выбранный из (а4′) или (b4′), где R1a выбран из А7), R2a выбран из В7), Y′, Q и R4a', как указано выше, и Т′′ представляет -NR', где R', как указано выше, могут быть получены
1o-i) реакцией соединения формулы (IIIc)
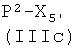
где Р2 и Х5', как указано выше, с соединением формулы (IVg)
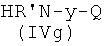
где R′ и Q, как указано выше, y представляет радикал Y′, и
1o-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 1o-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
1o-iii) необязательным снятием защитных групп с полученных на стадии 1o-i) или 1o-ii) соединений, как указано выше.
Реакцию соединения формулы (IIIc), где Р2 и Х5', как указано выше, с соединением формулы (IVg), где R′, y и Q, как указано выше, можно проводить, как описано в 1a-i).
Соединения формулы (Ia), где W представляет -Cl или O-Ra, X1 представляет радикал, выбранный из (а4′) или (b4′), где R1a выбран из А7), R2a выбран из В7) и где Y′ и Q, как указано выше, Т′′ представляет -NR′, где R′, как указано выше, могут быть получены из соответствующих кислот (Ia), где W=-ОН, известными из литературы методами.
1p) Соединения формулы (Ia), где W представляет -ОН, X1 представляет радикал, выбранный из (а4′) или (b4′), где R1a выбран из А7), R2a выбран из В7), Y′, Q и R4a', как указано выше, и Т′′ представляет -O-CH(R′)-O-C(O), где R′, как указано выше, могут быть получены
1p-i) реакцией соединения формулы (IIIc)
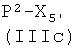
где Р2 и X5', как указано выше, с соединением формулы (IVm)
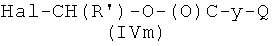
где R′ и Q, как указано выше, y представляет радикал Y′, где Y′, как указано выше, Hal представляет атом галоида и
1p-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 1p-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
1p-iii) необязательным снятием защитных групп с полученных на стадии 1p-i) или 1p-ii) соединений, как указано выше.
Реакцию соединения формулы (IIIc), где Р2 и X5', как указано выше, с соединением формулы (IVm), где R′, y, Q, Hal, как указано выше, можно проводить, как описано в 1l-1).
Соединения формулы (Ia), где W представляет -Cl или O-Ra, X1 представляет радикал, выбранный из (а4′) или (b4′), где R1a выбран из А7), R2a выбран из В7), и когда Y и Q, как указано выше, и Т′′ представляет группу -O-CH(R′)-O-C(O), где R′, как указано выше, могут быть получены из соответствующих кислот (Ia), где W представляет -ОН, известными в литературе методами.
1q) Соединения формулы (Ia), где W представляет -ОН, X1 представляет радикал, выбранный из (а4′) или (b4′), где R1a выбран из А7), R2a выбран из В7), Y′, Q и R4a', как указано выше, и Т′′ представляет -O-CH(R′)-O-C(O)-O-, где R′, как указано выше, могут быть получены
1q-i) реакцией соединения формулы (IIIc)
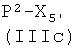
где Р2 и Х5', как указано выше, с соединением формулы (IVo)
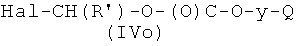
где R′ и Q, как указано выше, y представляет радикал Y′, где Y′, как указано выше, Hal представляет атом галоида и
1q-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 1q-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
1q-iii) необязательным снятием защитных групп с полученных на стадии 1q-i) или 1q-ii) соединений, как указано выше.
Реакцию соединения формулы (IIIc), где Р2 и Х5', как указано выше, с соединением формулы (IVo), где R′, y, Q, Hal, как указано выше, можно проводить, как описано в 1l-1).
Соединения формулы (Ia), где W представляет -Cl или O-Ra, X1 представляет радикал, выбранный из (а4′) или (b4′), где R1a выбран из А7), R2a выбран из В7), и когда Y и Q, как указано выше, и Т′′ представляет группу -O-CH(R′)-O-C(O)-O-, где R′, как указано выше, могут быть получены из соответствующих кислот (Ia), где W представляет -ОН, известными в литературе методами.
2) Соединения указанной выше общей формулы (I), где а равно 1, радикал Rx выбран из (а2), (а4), (а8), (b2), (b4), (b8), (c2), (e2), (f1), (g2), (h1), (i1), (l2), (m2), (n2), (o2), (p2), (q2), (r2), (s2), (t2), (u2), (v2), Z представляет -CH(R′)-O-, где R′ выбран из Н или прямого или разветвленного C1-С4алкила, могут быть получены:
2-i) реакцией соединения формулы (IIa)
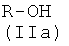
где R, как указано выше, с соединением формулы (If)
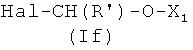
где Hal представляет атом галогена, R′ и X1, как указано выше, и
2-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 2-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
2-iii) необязательным снятием защитных групп с полученных на стадии 2-i) или 2-ii) соединений, как указано выше.
Реакцию соединения формулы (If), где X1 и R′, как указано выше, с соединением формулы (IIa), где R′, как указано выше, можно проводить, как описано в 1l-i).
Соединения формулы (If) получены реакцией соединения R′-CHO, где R′, как указано выше, с соединением формулы (Ia)
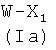
где W представляет атом хлора, X1, как указано выше, и ZnCl2 известными из литературы методами.
3) Соединения указанной выше общей формулы (I), где а равно 1, радикал Rx выбран из (а1), (а3), (а7), (b), (b3), (b7), (с1), (е1), (f2), (g1), (h2), (i2), (l1), (m1), (n1), (o1), (p1), (q1), (r1), (s1), (t1), (u1), (v1), Z представляет С(О), могут быть получены
3-i) реакцией соединения формулы
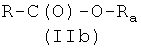
где R и Ra, как указано выше, с соединением формулы (Ig)
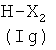
где X2 представляет радикал, имеющий следующие значения:
- (а1′) -HN-CH(R1′)-C(O)-(T-Y-Q)
- (а2′) -HN-CH(R1a-Т′′-Y'-Q)-COOR3a'
- (а7′) -HN-CH(R1a-Т′′-Y'-Q)-C(O)-(T-Y-Q)
- (b1) -HN-CH(R2′)-СН2С(О)-(T-Y-Q)
- (b3′) -HN-CH(R2a-T′′-Y'-Q)-CH2COOR3a′
- (b7′) -HN-CH(R2a-T′′-Y′-Q)-CH2-C(O)-(T-Y-Q),
где R1′, R1a, R2′, R2a, как указано выше,
R3a′ выбран из Р2, -OR5a или

где R5a, как указано выше;
- (c1′) -HN-(CH2)b-C(O)-(T-Y-Q);
- (e1′)
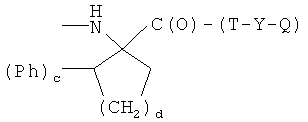
- (f2′)
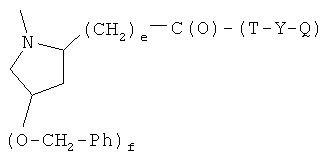
- (g1′)
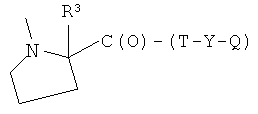
- (h2′)
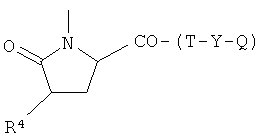
- (i2′)
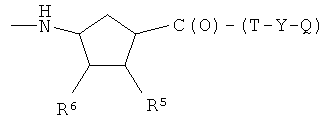
- (l1′)
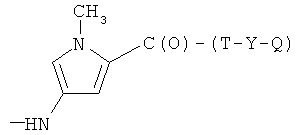
- (m1′)
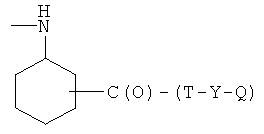
- (n1′)
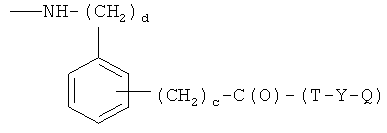
- (o1′)
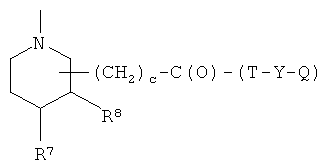
- (p1′)
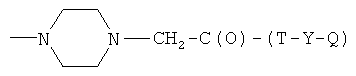
- (q1′)
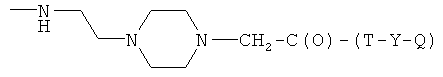
- (r1′)
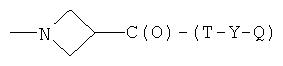
- (s1′)
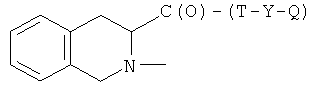
- (t1′)
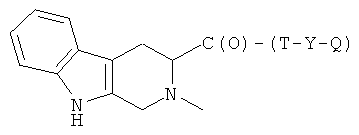
- (u1′)
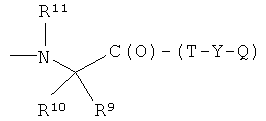
- (v1′)
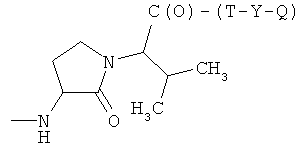
где Т, Т′′, Y и Y′, как указано выше,
3-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 3-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
3-iii) необязательным снятием защитных групп с полученных на стадии
3-i) или 3-ii) соединений, как указано выше.
Реакцию соединения формулы (IIb), где R и Ra, как указано выше, с соединением формулы (Ig), где X1, как указано выше, можно проводить, как описано в 1-i-2).
Соединения формулы 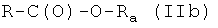 , где R и Ra, как указано выше, получают из соединения R-H (IIa) реакцией с соединением формулы Cl-C(O)-O-Ra, где Ra, как указано выше, известными из литературы методами.
, где R и Ra, как указано выше, получают из соединения R-H (IIa) реакцией с соединением формулы Cl-C(O)-O-Ra, где Ra, как указано выше, известными из литературы методами.
3а) Соединения формулы (Ig), где Х2 выбран из (а1′), (а3′), (b1′), (b3′), (с1′), (e1′), (f2′), (g1′), (h2′), (i2′), (l1′), (ml′), (n1′), (о1′), (р1′), (q1′), (r1′), (s1′), (t1′), (u1′), (v1′), где R1′ выбран из А1), А2′), A3′), А4′), R1a выбран из А7), R2a выбран из В7) и R2′ выбран из В1), В2′), В3′), В4′), Y и Y′, как указано выше, Т и Т′′ представляют X′′, где X′′, как указано выше,
могут быть получены
3а-i) реакцией соединения формулы (IIIe),
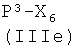
где Р3, как указано выше, Х6 представляет радикал, имеющий следующие значения:
- а1′′) -HN-CH(R1′)-С(О)-ОН
- а3′′) -HN-CH(R1a-OH)-COOR3a′
- b1′′) -HN-CH(R2′)-CH2C(О)-ОН
- (b3′′) -HN-CH(R2a-OH)-CH2COOR3a′,
где R1′ выбран из А1), А2′), A3′), А4′), R1a выбран из А7), R2a выбран из В7) и R2' выбран из B1), В2′), В3′), В4′), и R3a′, как указано выше,
-(c1′′) -HN-(CH2)b-C(O)-OH;
- (e1′′)
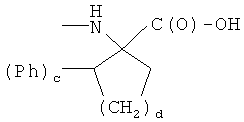
- (f2′′)
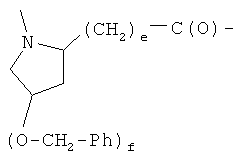
- (g1′′)
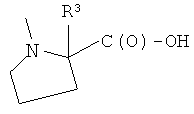
- (h2′′)
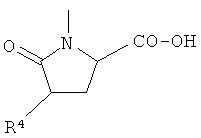
- (i2′′)
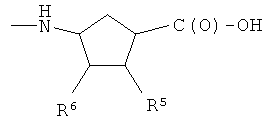
- (l1′′)
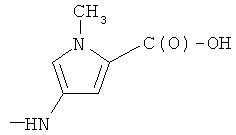
- (m1′′)
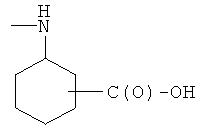
- (n1′′)
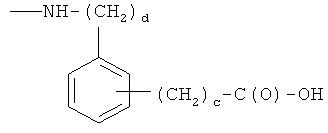
- (o1′′)
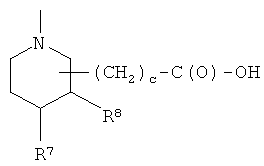
- (p1′′)
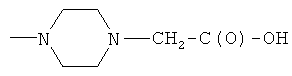
- (q1′′)
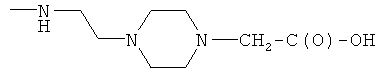
- (r1′′)
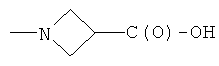
- (s1′′)
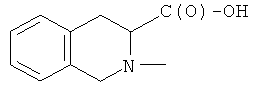
- (t1′′)
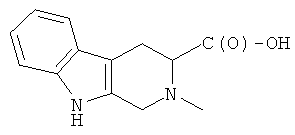
- (u1′′)
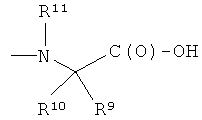
- (v1′′)
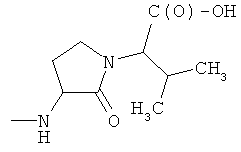
с соединением формулы (IVe)
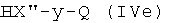
где Q и X′′, как указано выше, у представляет радикал Y, когда Х6 выбран из (а1′), (b′), (с1′), (е1′), (f2′), (g1′), (h2′), (i2′), (l1′), (m1′), (n1′), (о1′), (р1′), (q1′), (r1′), (s1′), (t1′), (u1′) и (v1′), y представляет Y′, когда Х6 выбран из (а3′) и (b3′), где Y и Y′, как указано выше, и,
3а-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 3а-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
3а-iii) необязательным снятием защитных групп с полученных на стадии 3а-i) или 3а-ii) соединений, как указано выше.
Реакцию соединения формулы (IIIe), где Р3 и Х6, как указано выше, с соединением формулы (IVe), где y, Q и X′′, как указано выше, можно проводить, как описано в 1-i-1).
Соединения формулы (IIIe) являются коммерчески доступными или могут быть получены известными из литературы методами.
3b) Соединения формулы (Ig), где Х2 выбран из (а1′), (а3′), (b1′), (b3′), (с1′), (е1′), (f2′), (g1′), (h2′), (i2′), (l1′), (m1′), (n1′), (o1′), (р1′), (q1′), (r1′), (s1′), (t1′), (u1′), (v1′), где R1′ выбран из А1), А2′), A3′), А4′), R1a выбран из А7), R2a выбран из В7) и R2′ выбран из В1), В2′), В3′), В4′), и R3a′, Y и Y′, как указано выше, Т и Т′′ представляют -NR′, где R′, как указано выше,
могут быть получены
3b-i) реакцией соединения формулы (IIIe),
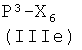
где Р3 и Х6, как указано выше, с соединением формулы
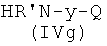
где R′ и Q, как указано выше, y представляет радикал Y, когда Х6 выбран из (а1′), (b1′), (с1′), (е1′), (f2′), (g1′), (h2′), (i2′), (l1′), (ml′), (n1′), (о1′), (р1′), (q1′), (r1′), (s1′), (t1′), (u1′) и (v1′), y представляет радикал Y′, когда Х6 выбран из (а3′) и (b3′), где Y и Y′, как указано выше, и
3b-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 3b-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
3b-iii) необязательным снятием защитных групп с полученных на стадии 3b-i) или 3b-ii) соединений, как указано выше.
Реакцию соединения формулы (IIIe), где Р3 и Х6, как указано выше, с соединением формулы (IVg), где R′, y, Q, как указано выше, можно проводить, как описано в 1a-i).
3с) Соединения формулы (Ig), где Х2 выбран из (а1′), (а3′), (b1′), (b3′), (с1′), (е1′), (f2′), (g1′), (h2′), (i2′), (l1′), (m1′), (n1′), (о1′), (р1′), (q1′), (r1′), (s1′), (t1′), (u1′), (v1′), где R1′ выбран из А1), А2′), A3′), А4′), R1a выбран из А7), R2a выбран из В7) и R2′ выбран из В1), В2′), В3′), В4′), и R3a′, Y и Y′, как указано выше, Т и Т′′ представляют -O-CH(R′)-O-C(O)-, где R′, как указано выше,
могут быть получены
3с-i) реакцией соединения формулы (IIIe),
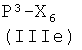
где Р3 и Х6, как указано выше, с соединением формулы (IVm)
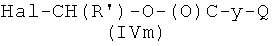
где R′ и Q, как указано выше, Hal представляет атом галоида, y представляет радикал Y, когда Х6 выбран из (а1′), (b1′), (с1′), (е1′), (f2′), (g1′), (h2′), (i2′), (l1′), (m1′), (n1′), (о1′), (р1′), (q1′), (r1′), (s1′), (t1′), (u1′) и (v1′), y представляет радикал Y′, когда Х6 выбран из (а3′) и (b3′), где Y и Y′, как указано выше, и
3с-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 3с-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
3с-iii) необязательным снятием защитных групп с полученных на стадии
3с-i) или 3с-ii) соединений, как указано выше.
Реакцию соединения формулы (IIIe), где Р3 и Х6, как указано выше, с соединением формулы (IVm), где R′, y, Q, как указано выше, можно проводить, как описано в 1l-i).
3d) Соединения формулы (Ig), где Х2 выбран из (а1′), (а3′), (b1′), (b3′), (с1′), (е1′), (f2′), (g1′), (h2′), (i2′), (l1′), (m1′), (n1′), (о1′), (р1′), (q1′), (r1′), (s1′), (t1′), (u1′), (v1′), где R1′ выбран из А1), А2′), A3′), А4′), R1a выбран из А7), R2a выбран из В7) и R2′ выбран из В1), В2′), В3′), В4′), и R3a′, Y и Y′, как указано выше, Т и Т′′ представляют -O-CH(R′)-O-C(O)O-, где R′, как указано выше,
могут быть получены
3d-i) реакцией соединения формулы (IIIe),
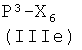
где Р3 и Х6, как указано выше, с соединением формулы (IVo)
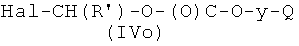
где R′ и Q, как указано выше, Hal представляет атом галоида, y представляет радикал Y, когда Х6 выбран из (а1′), (b1′), (с1′), (е1′), (f2′), (g1′), (h2′), (i2′), (l1′), (m1′), (n1′), (о1′), (р1′), (q1′), (r1′), (s1′), (t1′), (u1′) и (v1′), y представляет радикал Y1, когда Х6 выбран из (а3′) и (b3′), где Y и Y′, как указано выше, и
3d-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 3d-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
3d-iii) необязательным снятием защитных групп с полученных на стадии 3d-i) или 3d-ii) соединений, как указано выше.
Реакцию соединения формулы (IIIe), где Р3 и Х6, как указано выше, с соединением формулы (IVo), где R′, y, Q, как указано выше, можно проводить, как описано в 1l-i).
3е) Соединения формулы (Ig), где Х2 выбран из (а7′) или (b7′), где R1a выбран из А5) или А6), R1b выбран из В5) или В6), Т′′ представляет -С(O)-, Т представляет -X′′, -NR′, -O-CH(R′)-O-C(O)- или -O-CH(R′)-O-C(O)O-, где X′′ и R′, Y и Y′, как указано выше, могут быть получены
3е-i) реакцией соединения формулы (Ih)
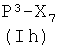
где Р3, как указано выше, и Х7 представляет радикал, имеющий следующие значения
- (а7′′) -HN-CH(R1a-H)-С(О)-(T-Y-Q)
- (b7′′) -HN-CH(R2a-H)-СН2-С(О)-(T-Y-Q)
где R1a выбран из А5) или А6), R2a выбран из В5) или В6), с соединением формулы (IVa)
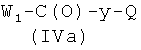
где W1 и Q, как указано выше, у представляет радикал Y′, где Y′, как указано выше, и
3е-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 3е-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
3е-iii) необязательным снятием защитных групп с полученных на стадии 3е-i) или 3е-ii) соединений, как указано выше.
Реакцию соединения формулы (Ih), где Р3 и Х7, как указано выше, с соединением формулы (IVa), где у, Q, W1, как указано выше, можно проводить, как описано в 1-i-1), 1-i-2), 1-i-3) и 1a-i).
Соединения формулы (Ih), где Р3 и Х7, как указано выше, Т представляет -X′′, получены, как описано в 3а).
Соединения формулы (Ih), где Р3 и Х7, как указано выше, Т представляет -NR′, получены, как описано в 3b).
Соединения формулы (Ih), где Р3 и Х7, как указано выше, Т представляет -O-СН(R′)-O-C(O)-, получены, как описано в 3с).
Соединения формулы (Ih), где Р3 и Х7, как указано выше, Т представляет -O-CH(R′)-O-C(O)O-, получены, как описано в 3d).
3f) Соединения формулы (Ig), где Х2 выбран из (а7′) или (b7′), где R1a выбран из А5) или А6), R1b выбран из В5) или В6), Т′′ представляет -С(O)-X′′, Т представляет -X′′, -NR1, -O-CH(R′)-O-C(O)- или -O-CH(R′)-O-C(O)O-, где X′′ и R′, Y и Y′, как указано выше, могут быть получены
3f-i) реакцией соединения формулы (Ih)
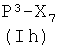
где Р3 и Х7, как указано выше, с соединениями формулы (IVd)
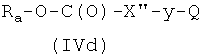
где Ra, X′′ и Q, как указано выше, y представляет радикал Y′, где Y' указано выше, и
3f-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 3f-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
3f-iii) необязательным снятием защитных групп с полученных на стадии
3f-i) или 3f-ii) соединений, как указано выше.
Реакцию соединения формулы (Ih), где Р3 и Х7, как указано выше, с соединением формулы (IVd), где y, Q, Ra, как указано выше, можно проводить, как описано в 1-i-2).
3g) Соединения формулы (Ig), где Х2 выбран из (а7′) или (b7′), где R1a выбран из А5), А6), R1b выбран из В5), В6), Т′′ представляет -C(O)-NR′, Т представляет -X′′, -NR′, -O-CH(R′)-O-C(O)- или -O-CH(R′)-O-C(O)O-, где X′′ и R′, Y и Y′, как указано выше, могут быть получены
3g-i) реакцией соединения формулы (Ih)
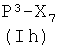
где Р3 и Х7, как указано выше, с соединениями формулы (IVf)
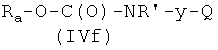
где Ra и Q, как указано выше, у представляет радикал Y′, где Y′ указано выше, и
3g-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 3g-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
3g-iii) необязательным снятием защитных групп с полученных на стадии 3g-i) или 3g-ii) соединений, как указано выше.
Реакцию соединения формулы (Ih), где Р3 и Х7, как указано выше, с соединением формулы (IVf), где y, Q, Ra и R′, как указано выше, можно проводить, как описано в 1-i-2).
Соединения формулы (Ih), где Р3 и Х7, как указано выше, Т представляет -X′′, получены, как описано в 3а).
Соединения формулы (Ih), где Р3 и Х7, как указано выше, Т представляет -NR′, получены, как описано в 3b).
Соединения формулы (Ih), где Р3 и Х7, как указано выше, Т представляет -O-СН(R′)-O-C(O)- получены, как описано в 3с).
Соединения формулы (Ih), где Р3 и Х7, как указано выше, Т представляет -O-CH(R′)-O-C(O)O-, получены, как описано в 3d).
3h) Соединения формулы (Ig), где Х2 выбран из (а7′) или (b7′), где R1a выбран из А7), R1b выбран из В7, Т′′ представляет -X′′, Т представляет -X′′, -NR′, -O-CH(R′)-O-C(O)- или -O-CH(R′)-O-C(O)O-, где X′′ и R′, Y и Y′, как указано выше, могут быть получены
3h-i) реакцией соединения формулы (Iv)
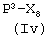
где Р3, как указано выше, и X8 представляет радикал, имеющий следующие значения
-(а7′′) -HN-CH(R1a-H)-C(O)-(T-Y-Q)
- (b7′′) -HN-CH(R2a-H)-CH2-C(O)-(T-Y-Q)
где R1a выбран из А7), R1b выбран из В7), с
соединениями формулы (IVe)

где X′′ и Q, как указано выше, у представляет радикал Y′, где Y′, как указано выше, и
3h-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 3h-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
3h-iii) необязательным снятием защитных групп с полученных на стадии 3h-i) или 3h-ii) соединений, как указано выше.
Реакцию соединения формулы (Iv), где Р3 и X8, как указано выше, с соединением формулы (IVe), где y, Q, X′′, как указано выше, можно проводить, как описано в 1-i-1), 1-i-2) и 1a-1).
Соединения формулы (Iv), где Р3 и X8, как указано выше, Т представляет -X′′, получены, как описано в 3а).
Соединения формулы (Iv), где Р3 и X8, как указано выше, Т представляет -NR′, получены, как описано в 3b).
Соединения формулы (Iv), где Р3 и X8, как указано выше, Т представляет -O-СН(R′)-O-C(O)-, получены, как описано в 3с).
Соединения формулы (Iv), где Р3 и X8, как указано выше, Т представляет -O-CH(R′)-O-C(O)O-, получены, как описано в 3d).
3i) Соединения формулы (Ig), где Х2 выбран из (а7) или (b7), где R1a выбран из А7), R1b выбран из В7), Т′′ представляет NR′, Т представляет -X′′, -NR′, -O-CH(R′)-O-C(O)- или -O-CH(R′)-O-С(O)O-, где X′′ и R′, Y и Y′, как указано выше, могут быть получены
3i-i) реакцией соединения формулы (Iv)
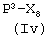
где Р3 и X8, как указано выше, с соединениями формулы (IVg)
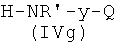
где R′ и Q, как указано выше, y представляет радикал Y′, где Y′, как указано выше, и
3i-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 3i-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
3i-iii) необязательным снятием защитных групп с полученных на стадии 3i-i) или 3i-ii) соединений, как указано выше.
Реакцию соединения формулы (Iv), где Р3 и X8, как указано выше, с соединением формулы (IVg), где Y, Q, R′, как указано выше, можно проводить, как описано в 1а-1).
3l) Соединения формулы (Ig), где Х2 выбран из (а7) или (b7), где R1a выбран из А7), R1b выбран из В7), Т′′ представляет -O-CH(R′)-O-C(O), Т представляет -X′′, -NR′, -O-CH(R′)-O-C(O)- или -O-CH(R′)-O-С(O)O-, где X′′ и R′, Y и Y′, как указано выше, могут быть получены
3l-i) реакцией соединения формулы (Iv)
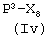
где Р3 и Х8, как указано выше, с соединениями формулы (IVm)
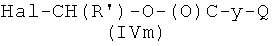
где R′ и Q, как указано выше, y представляет радикал Y′, где Y′, как указано выше, Hal представляет атом галоида, и
3l-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 3l-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
3l-iii) необязательным снятием защитных групп с полученных на стадии 3l-i) или 3l-ii) соединений, как указано выше.
Реакцию соединения формулы (Iv), где Р3 и X8, как указано выше, с соединением формулы (IVm), где y, Q, R′, как указано выше, можно проводить, как описано в 1-l-i).
3m) Соединения формулы (Ig), где Х2 выбран из (а7) или (b7), где R1a выбран из А7), R1b выбран из В7), Т′′ представляет -O-CH(R′)-O-C(O), Т представляет -X′′, -NR′, -O-CH(R′)-O-C(O)- или -O-CH(R′)-O-С(O)O-, где X′′ и R′, Y и Y′, как указано выше, могут быть получены 3m-i) реакцией соединения формулы (Iv)
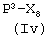
где Р3 и X8, как указано выше, с соединениями формулы (IVo)
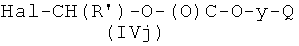
где R′ и Q, как указано выше, y представляет радикал Y′, где Y′, как указано выше, Hal представляет атом галоида, и
3m-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 3m-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
3m-iii) необязательным снятием защитных групп с полученных на стадии 3m-i) или 3m-ii) соединений, как указано выше.
Реакцию соединения формулы (Iv), где Р3 и Х8, как указано выше, с соединением формулы (IVo), где y, Q, R′, как указано выше, можно проводить, как описано в 1l-i).
3n) Соединения формулы (Ig), где Х2 выбран из (а3′) или (b3′), где R1a выбран из А5) или А6), R2a выбран из В5) или В6), Y′, как указано выше, Т′′ представляет С(O), могут быть получены
3n-i) реакцией соединения формулы (IIIf),
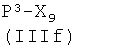
где Р3, как указано выше, Х9 представляет радикал, имеющий следующие значения
-(а3′′) -HN-CH(R1a-H)-COOR3a′
-(b3′′) -HN-CH(R2a-Н)-CH2COOR3a′
где R1a выбран из А5 или А6) и R2a выбран из В5) или В6), где R3a', как указано выше, с соединениями формулы (IVa)
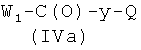
где W1 и Q, как указано выше, y представляет радикал Y′, где Y′, как указано выше, и
3n-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 3n-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
3n-iii) необязательным снятием защитных групп с полученных на стадии 3n-i) или 3n-ii) соединений, как указано выше.
Реакцию соединения формулы (IIIf), где Р3 и Х9, как указано выше, с соединением формулы (IVa), где W1, y, Q, как указано выше, можно проводить, как описано в 1-i-1), 1-i-2), 1a-1).
Соединения формулы (IIIf), где Р3 и Х9, как указано выше, являются коммерчески доступными или получены, как описано в литературе.
3о) Соединения формулы (Ig), где Х2 выбран из (а3′) или (b3′), где R1a выбран из А5) или А6), R2a выбран из В5) или В6), Y′, как указано выше, Т′′ представляет С(O)-X′′, где X′′, как указано выше, могут быть получены 3о-i) реакцией соединения формулы (IIIf),
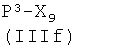
где Р3 и Х9, как указано выше, с соединениями формулы (IVd)
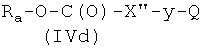
где Ra, X′′, Q, как указано выше, y представляет радикал Y′, где Y′, как указано выше, и
3о-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 3о-1), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
3о-iii) необязательным снятием защитных групп с полученных на стадии 3о-i) или 3о-ii) соединений, как указано выше.
Реакцию соединения формулы (IIIf), где Р3 и Х9, как указано выше, с соединением формулы (IVd), где Ra, X′′, y, Q, как указано выше, можно проводить, как описано в 1-i-2).
3р) Соединения формулы (Ig), где Х2 выбран из (а3′) или (b3′), где R1a выбран из А5) или А6), R2a выбран из В5) или В6), Y′, как указано выше, Т′′ представляет С(O)-NR′, где R′, как указано выше, могут быть получены
3р-i) реакцией соединения формулы (IIIf),
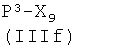
где Р3 и Х9, как указано выше, с соединениями формулы (IVf)
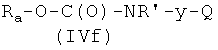
где Ra, R′, Q, как указано выше, y представляет радикал Y′, где Y′, как указано выше, и
3р-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 3р-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
3р-iii) необязательным снятием защитных групп с полученных на стадии 3р-i) или 3р-ii) соединений, как указано выше.
Реакцию соединения формулы (IIIf), где Р3 и Х9, как указано выше, с соединением формулы (IVf), где Ra, R′, y, Q, как указано выше, можно проводить, как описано в 1-i-2).
4) Соединения указанной выше общей формулы (I), где а равно 1, радикал Rx выбран из (d1), (d2), (d3), (d4), (d7), (d8), Z представляет С(O), могут быть получены
4-i) реакцией соединения формулы (IIb)
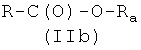
где R и Ra, как указано выше, с соединением формулы (Im)
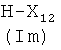
где X12 представляет радикал Rx, имеющий следующие значения
- (d1′) -HN-CH(R12′)-СН2-O-(T′′′-Y-Q)
- (d2′) -O-СН2-СН(R12')-NH-(T′-Y-Q)
- (d3′) -HN-CH(R12a-T′′-Y′-Q)-CH2OH
- (d4′) -О-СН2-СН(R12a-T′′-Y′-Q)-NHR4a
- (d7′) -HN-CH(R12a-T′′-Y′-Q)-СН2-O-(T′′′-Y-Q)
- (d8′) -O-CH2-CH(R12a-T′′-Y′-Q)-NH-(Т′-Y-Q)
где R12′ представляет
D1),
D2′) -СН2-ОР1, -СН(СН3)-ОР1, -СН2[(С6Н4)-4-ОР1], -CH2-(С6Н3)-(3,5-дииодо)-4-ОР1], -СН2-[(С6Н3)-3-нитро-4-ОР1];
D3′) -CH2-NHR′′′′, -(СН2)2-NHR′′′′, -(CH2)3-NHR′′′′, -(СН2)4-NHR′′′′,
где R′′′′, как указано выше;
D4′) -CH2-C(O)R′′′′′, -(CH2)2-C(O)R′′′′′, -(СН2)4-С(О)R′′′′′, где
R′′′′′, как указано выше;
где R12", как указано выше;
и
4-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 4-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
4-iii) необязательным снятием защитных групп с полученных на стадии 4-i) или 4-ii) соединений, как указано выше.
Реакцию соединения формулы (IIb), где R и Ra, как указано выше, с соединением формулы (Im), где Х12, как указано выше, можно проводить, как описано в 1-i-2).
4а) Соединения формулы (Im), где X12 выбран из (d1′), (d2′), (d3′) или (d4′), где R12′ выбран из D1), D2′), D3′) или D4′) и R12a выбран из D5) или D6), Y и Y′, как указано выше, Т′ и Т′′ и Т′′′ представляют С(O), могут быть получены 4a-i) реакцией соединения формулы (IIIi),
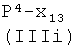
где Р4 представляет Р3 или P1, как указано выше, и Х13 представляет радикал, имеющий следующие значения
-(d1′′) -HN-CH(R12′)-CH2-OH
-(d2′′) -О-CH2-CH(R12′)-NH2
-(d3′′) -HN-CH(R12a-H)-CH2OP1
-(d4′′) -O-CH2-CH(R12a-H)-NHR4a′
где R12′ представляет D1), D2′), D3′) или D4′), R12a представляет D5) или D6), R4a′ и Р1, как указано выше, с соединением формулы (IVa)
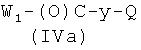
где Q и W1, как указано выше, у представляет радикал Y, когда Х13 выбран из (d1′) или (d2′), y представляет радикал Y′, когда X13 выбран из (d3′) или (d4′), где Y и Y′, как указано выше, и
4a-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 4a-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
4a-iii) необязательным снятием защитных групп с полученных на стадии 4a-i) или 4a-ii) соединений, как указано выше.
Реакцию соединения формулы (IIIi), где Х13 и Р4, как указано выше, с соединением формулы (IVa), где W1, y, Q, как указано выше, можно проводить, как описано в 1-i-1) и 1-i-2).
Соединения формулы (IIIi), где Х13 и Р4, как указано выше, являются коммерчески доступными или известными из литературы.
4b) Соединения формулы (Im), где Х12 выбран из (d1′), (d2′), (d3′) или (d4′), где R12′ выбран из D1), D2′), D3′) или D4′) и R12a выбран из D5) или D6), Y и Y′, как указано выше, Т′ и Т′′ и Т′′′ представляют С(O)-Х′′, где X′′, как указано выше, могут быть получены
4b-i) реакцией соединения формулы (IIIi),
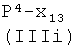
где Р4 и Х13, как указано выше, с соединением формулы (IVd)
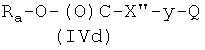
где Q, Ra и X′′, как указано выше, y представляет радикал Y, когда Х13 выбран из (d1′) или (d2′), y представляет радикал Y′, когда Х13 выбран из (d3′) или (d4′), где Y и Y′, как указано выше, и
4b-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 4b-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
4b-iii) необязательным снятием защитных групп с полученных на стадии 4b-i) или 4b-ii) соединений, как указано выше.
Реакцию соединения формулы (IIIi), где Х13 и Р4, как указано выше, с соединением формулы (IVd), где y, Q, Ra и X′′, как указано выше, можно проводить, как описано в 1-i-2).
4с) Соединения формулы (Im), где Х12 выбран из (d7′) или (d8′), где R12a выбран из D5) или D6), Y′ и Y, как указано выше, Т и Т′′ и Т′′′ представляют С(О), могут быть получены
4c-i) реакцией соединения формулы (IIIl),
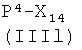
где Р4 представляет Р1 или Р3, Х14 представляет радикал, имеющий следующие значения
- (d7′′) -HN-CH(R12a-H)-CH2-ОН
- (d8′′) -О-СН2-CH(R12a-Н)-NH2
где R12a выбран из D5) или D6), с соединением формулы (IVa)
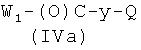
где W1 и Q, как указано выше, y представляет радикал Y′, где Y′, как указано выше, и
4c-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 4c-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
4c-iii) необязательным снятием защитных групп с полученных на стадии 4с-i) или 4c-ii) соединений, как указано выше.
Реакцию соединения формулы (IIIl), где Р4 и Х14, как указано выше, с соединением формулы (IVa), где W1 представляет ОН, у и Q, как указано выше, можно проводить, как описано в 1-i-1), используя соотношение (IIIl)/(IVa) 1:2.
Реакцию соединения формулы (IIIl), где Р4 и Х14, как указано выше, с соединением формулы (IVa), где W1 представляет ORa, y и Q, как указано выше, можно проводить, как описано в 1-i-2), используя соотношение (IIIl)/(IVa) 1:2.
Соединения формулы (IIIl), где Р4 и Х14, как описано выше, являются коммерчески доступными или известны из литературы.
4d) Соединения формулы (Im), где Х12 выбран из (d7′) или (d8′), где R12a выбран из D5) или D6), Q, Y и Y′, как указано выше, Т′, Т′′′ и Т′′ представляют С(O), могут быть получены
4d-i) реакцией соединения формулы (In)
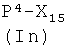
где Р4, как указано выше, и X15 представляет радикал, имеющий следующие значения
- (d7′′′) -HN-CH(R12a-H)-СН2-O-(Т′′′-Y-Q)
- (d8′′′) -О-СН2-СН(R12a-H)-NH-(T′-Y-Q)
где R12a выбран из D5) или D6), Y, Q, Т′ и Т′′′, как указано выше, с соединением формулы (IVa)
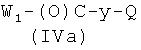
где W1, y и Q′, как указано выше, y представляет радикал Y′, где Y′, как указано выше, и
4d-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 4d-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
4d-iii) необязательным снятием защитных групп с полученных на стадии 4d-i) или 4d-ii) соединений, как указано выше.
Реакцию соединения формулы (In), где Р4 и X15, как указано выше, с соединением формулы (IVa), где W1 представляет ОН, y и Q, как указано выше, можно проводить, как описано в 1-i-1).
Реакцию соединения формулы (In), где Р4 и X15, как указано выше, с соединением формулы (IVa), где W1 представляет ORa, y и Q, как указано выше, можно проводить, как описано в 1-i-2).
Соединения формулы (In), где Р4 и X15, как указано выше, Т′ и Т′′ представляют С(O), могут быть получены, как описано в 4а).
4е) Соединения формулы (Im), где X12 выбран из (d7′) или (d8′), где R12a выбран из D5) или D6), Q, Y и Y′, как указано выше, Т′′ представляет С(O)-Х′′, где X′′, как указано выше, Т′ и Т′′ представляют С(O), могут быть получены
4e-i) реакцией соединения формулы (In)
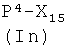
где Р4 и X15, как указано выше, с соединением формулы (IVa)
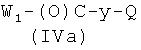
где W1, y и Q, как указано выше, y представляет радикал Y′, где Y′, как указано выше, и
4e-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 4e-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
4e-iii) необязательным снятием защитных групп с полученных на стадии 4e-i) или 4e-ii) соединений, как указано выше.
Реакцию соединения формулы (In), где Р4 и X15, как указано выше, с соединением формулы (IVa), где W1 представляет ОН, y и Q, как указано выше, можно проводить, как описано в 1-i-1).
Реакцию соединения формулы (In), где Р4 и X15, как указано выше, с соединением формулы (IVa), где W1 представляет ORa, y и Q, как указано выше, можно проводить, как описано в 1-i-2).
Соединения формулы (In), где Р4 и Х15, как указано выше, могут быть получены, как описано в 4b).
4f) Соединения формулы (Im), где X12 выбран из (d7′) или (d8′), где R12a выбран из D5) или D6), Y и Y′ имеют одинаковые указанные выше значения, Т, Т′′ и Т′′′ представляют С(O)-Х′′, где X′′, как указано выше, могут быть получены
4f-i) реакцией соединения формулы (IIIl),
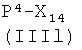
где Р4 и X14, как указано выше, с соединением формулы (IVd)
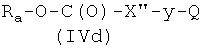
где Ra, X′′ и Q, как указано выше, y представляет радикал Y′,
где Y′, как указано выше, и
4f-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 4f-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
4f-iii) необязательным снятием защитных групп с полученных на стадии 4f-i) или 4f-ii) соединений, как указано выше.
Реакцию соединения формулы (IIIl), где Р4 и X14, как указано выше, с соединением формулы (IVd), где Ra, X′′, y и Q, как указано выше, можно проводить, как описано в 1-i-2), используя соотношение (IIIl)/(IVd) 1:2.
4g) Соединения формулы (Im), где X12 выбран из (d7′) или (d8′), где R12a выбран из D5) или D6), Q, Y и Y′, как указано выше, Т′′ представляет С(O)-Х′′, Т′ и Т′′ представляют С(O) или С(O)-Х′′, где X′′, как указано выше, могут быть получены
4g-i) реакцией соединения формулы (In)
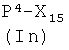
где Р4 и X15, как указано выше, с соединением формулы (IVd)
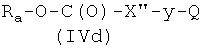
где Ra, X′′ и Q, как указано выше, y представляет радикал Y′, где Y′, как указано выше, и
4g-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 4g-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
4g-iii) необязательным снятием защитных групп с полученных на стадии 4g-i) или 4g-ii) соединений, как указано выше.
Реакцию соединения формулы (In), где Р4 и X15, как указано выше, с соединением формулы (IVd), где Ra, X′′, y и Q, как указано выше, можно проводить, как описано в 1-i-2).
Соединения формулы (In), где Т′ или Т′′′ представляют С(О), Р4 и X15, как указано выше, получены, как описано в 4a-i), 4a-ii).
Соединения формулы (In), где Т′ или Т′′′ представляют С(O)-Х′′, где Р4 и X15, как указано выше, получены, как описано в 4b-i), 4b-ii).
4h) Соединения формулы (Im), где Х12 выбран из (d7′) или (d8′), где R12a выбран из D5) или D6), Q, Y и Y', как указано выше, Т′′ представляет C(O)-NR′-, Т′ и Т′′′ представляют С(O) или С(O)-Х′′, где X′′, как указано выше, могут быть получены
4h-i) реакцией соединения формулы (In)
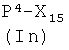
где Р4 и X15, как указано выше, с соединением формулы
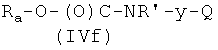
где Ra, R′ и Q, как указано выше, y представляет радикал Y′, где Y′, как указано выше, и
4h-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 4h-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
4h-iii) необязательным снятием защитных групп с полученных на стадии 4h-i) или 4h-ii) соединений, как указано выше.
Реакцию соединения формулы (In), где Р4 и X15, как указано выше, с соединением формулы (IVf), где Ra, R′, y и Q, как указано выше, можно проводить, как описано в 1-i-2).
Соединения формулы (In), где Т′ или Т′′′ представляют С(O), где Р4 и X15, как указано выше, получают, как описано в 4a-i), 4a-ii).
Соединения формулы (In), где Т′ или Т′′′ представляют С(O)-X′′, где Р4 и X15, как указано выше, получают, как описано в 4b-i), 4b-ii).
4i) Соединения формулы (Im), где X12 выбран из (d7′) или (d8′), где R12a выбран из D7), Q, Y и Y′, как указано выше, Т′′ представляет -X′′, где X′′, как указано выше, Т′ и Т′′′ представляют С(O) или С(O)-Х′′, где X′′, как указано выше, могут быть получены
4i-i) реакцией соединения формулы (Ir),
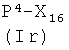
- (d7′′′′) -HN-CH(R12a-OH)-CH2-O-(T′′′′-Y-Q)
- (d8′′′′) -O-CH2-CH(R12a-OH)-NH-(T′-Y-Q)
где Р4, как указано выше, R12a выбран из D7), с соединением формулы (IVe)
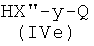
где Y′, X′′ и Q, как указано выше, y представляет радикал Y′, где Y′, как указано выше, и
4i-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 4i-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
4i-iii) необязательным снятием защитных групп с полученных на стадии 4i-i) или 4i-ii) соединений, как указано выше.
Реакцию соединения формулы (Ir), где Р4 и X16, как указано выше, с соединением формулы (IVe), где y, X′′ и Q, как указано выше, можно проводить, как описано в 1-i-1).
Соединения формулы (Ir), где Т′ или Т′′′ представляют С(O), где Р4 и X16, как указано выше, получают, как описано в 4a-i), 4a-ii).
Соединения формулы (Ir), где Т′ или Т′′′ представляют С(O)-X′′, где Р4 и X16, как указано выше, получают, как описано в 4b-i), 4b-ii).
4l) Соединения формулы (Im), где X12 выбран из (d7′) или (d8′), где R12a выбран из D7), Q, Y и Y′, как указано выше, Т′′ представляет -NR′, где R′, как указано выше, Т′ и Т′′′ представляют С(O) или С(O)-Х′′, где X′′, как указано выше, могут быть получены
4l-i) реакцией соединения формулы (Ir),
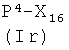
где Р4 и X16, как указано выше, и R12a выбран из D7), с соединением формулы
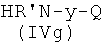
где R′ и Q, как указано выше, y представляет радикал Y′, где Y′, как указано выше, и
4l-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 4l-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
4l-iii) необязательным снятием защитных групп с полученных на стадии 4l-i) или 4l-ii) соединений, как указано выше.
Реакцию соединения формулы (Ir), где Р4 и X16, как указано выше, с соединением формулы (IVg), где R′, y, Q, как указано выше, можно проводить, как описано в 1-i-1).
4m) Соединения формулы (Im), где Х12 выбран из (d7′) или (d8′) где R12a выбран из D7), Q, Y и Y′, как указано выше, Т′′ представляет -O-CH(R′)-O-C(O)-, где R′, как указано выше, Т′ и Т′′′ представляют С(O) или С(O)-Х′′, где X′′, как указано выше, могут быть получены
4m-i) реакцией соединения формулы (Ir),
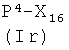
где Р4 и X16, как указано выше, и R12a выбран из D7), с соединением формулы (IVm)
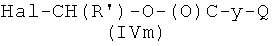
где R′ и Q, как указано выше, Hal представляет атом галоида, y представляет радикал Y′, где Y′, как указано выше, и
4m-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 4m-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
4m-iii) необязательным снятием защитных групп с полученных на стадии 4m-i) или 4m-ii) соединений, как указано выше.
Реакцию соединения формулы (Ir), где Р4 и Х16, как указано выше, с соединением формулы (IVm), где y, Q, R′, как указано выше, можно проводить, как описано в 1l-i).
4n) Соединения формулы (Im), где Х12 выбран из (d7′) или (d8′), где R12a выбран из D7), Q, Y и Y′, как указано выше, Т′′ представляет -O-CH(R′)-O-C(O)-O-, где R′, как указано выше, Т′ и Т′′′ представляют С(O) или С(O)-Х′′, где X′′, как указано выше, могут быть получены
4n-i) реакцией соединения формулы (Ir),
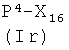
где Р4 и X16, как указано выше, и R12a выбран из D7), с соединением формулы (IVo)
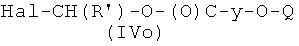
где R′ и Q, как указано выше, Hal представляет атом галоида, y представляет радикал Y′, где Y′, как указано выше, и
4n-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 4n-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
4n-iii) необязательным снятием защитных групп с полученных на стадии 4n-i) или 4n-ii) соединений, как указано выше.
Реакцию соединения формулы (Ir), где Р4 и X16, как указано выше, с соединением формулы (IVo), где y, Q, R', Hal, как указано выше, можно проводить, как описано в 1l-i).
4о) Соединения формулы (Im), где Х12 выбран из (d3′) или (d4′), где R12a выбран из D7), Y′, как указано выше, Т′′ представляет X′′, где X′′, как указано выше, могут быть получены
4o-i) реакцией соединения формулы (IIIm),
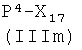
где Р4, как указано выше, и Х17 представляет радикал
- (d3′′) -HN-CH(R12a-H)-CH2-OPl
- (d4′′) -О-CH2-CH(R12a-H)-NHR4a′
где R12a выбран из D7), где Р1 и R4a', как указано выше, с соединением формулы (IVe)
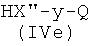
где X′′ и Q, как указано выше, у представляет радикал Y′, где Y′, как указано выше, и
4o-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 4o-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
4o-iii) необязательным снятием защитных групп с полученных на стадии 4o-i) или 4o-ii) соединений, как указано выше.
Реакцию соединения формулы (IIIm), где Р4 и Х17, как указано выше, с соединением формулы (IVe), где y, X′′ и Q, как указано выше, можно проводить, как описано в 1-i-1).
Соединения формулы (IIIm), где где Р4 и Х17, как указано выше, являются коммерчески доступными или получены известными из литературы методами.
4р) Соединения формулы (Im), где X12 выбран из (d3′) или (d4′), где R12a выбран из D7), Y′, как указано выше, Т′′ представляет NR′, где R′, как указано выше, могут быть получены
4p-i) реакцией соединения формулы (IIIm),
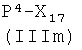
где Р4 и X17, как указано выше, где R12a выбран из D7, с соединением формулы (IVg)
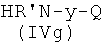
где R′ и Q, как указано выше, y представляет радикал Y′, где Y′, как указано выше, и
4p-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 4p-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
4p-iii) необязательным снятием защитных групп с полученных на стадии 4p-i) или 4p-ii) соединений, как указано выше.
Реакцию соединения формулы (IIIm), где Р4 и Х17, как указано выше, с соединением формулы (IVg), где R′, y, Q, как указано выше, можно проводить, как описано в 1a-i).
4q) Соединения формулы (Im), где Х12 выбран из (d3′) или (d4′), где R12a выбран из D7), Y′, как указано выше, Т′′ представляет -O-CH(R′)-O-C(O)-, где R′, как указано выше, могут быть получены
4q-i) реакцией соединения формулы (IIIm),
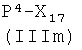
где Р4 и Х17, как указано выше, где R12a выбран из D7, с соединением формулы (IVm)
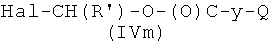
где R′ и Q, как указано выше, Hal представляет атом галогена, y представляет радикал Y′, где Y′, как указано выше, и
4q-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 4q-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
4q-iii) необязательным снятием защитных групп с полученных на стадии 4q-i) или 4q-ii) соединений, как указано выше.
Реакцию соединения формулы (IIIm), где Р4 и Х17, как указано выше, с соединением формулы (IVm), где R′, y, Q, как указано выше, можно проводить, как описано в 1l-i).
4r) Соединения формулы (Im), где X12 выбран из (d3′) или (d4′), где R12a выбран из D7), Y′, как указано выше, Т′′ представляет -O-CH(R′)-O-C(O)-O-, где R′, как указано выше, могут быть получены
4r-i) реакцией соединения формулы (IIIm),
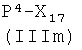
где Р4 и Х17, как указано выше, где R12a выбран из D7, с соединением формулы (IVo)
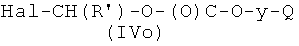
где R′ и Q, как указано выше, Hal представляет атом галоида, y представляет радикал Y′, где Y′, как указано выше, и
4r-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 4r-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
4r-iii) необязательным снятием защитных групп с полученных на стадии
4r-i) или 4r-ii) соединений, как указано выше.
Реакцию соединения формулы (IIIm), где Р4 и X17, как указано выше, с соединением формулы (IVo), где y, Q, R′, Hal, как указано выше, можно проводить, как описано в 1l-i).
5) Соединение указанной выше общей формулы (I), где а равно 0, Rx представляет радикал, выбранный из (d5), (d6), (d9) или (d10), где R12b выбран из D10), может быть получено
5-i) реакцией соединения формулы (IIa)
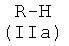
где R, как указано выше, с соединением формулы (Is)
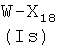
где W, как указано выше, X18 представляет радикал, имеющий следующие значения
- (d5′) -R12b-CH(NHR4a)-СН2-О-(Т′′′-Y-Q)
- (d6′) -R12b-CH(CH2OH)-NH-(T′-Y-Q)
- (d9′) -R12b-CH(NH-T′′′-Y′-Q)-CH2-O-(T′-Y-Q)
- (d10′) -R12b-CH(CH2-O-T′′′-Y′-Q)-NH-(T′-Y-Q)
где R12b выбран из D10), Т′, Т′′′, Y, Y′ и Q, как указано выше, и
5-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 5-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
5-iii) необязательным снятием защитных групп с полученных на стадии 5-i) или 5-ii) соединений, как указано выше.
Реакцию соединения формулы (IIa), где R, как указано выше, с соединением формулы (Is), где W и X18, как указано выше, можно проводить, как описано в 1).
5а) Соединения формулы (Is), где X18 представляет радикал формулы (d5′) или (d6′), где R12b выбран из D10), Т′ и Т′′′ представляют С(O), могут быть получены
5a-i) реакцией соединения формулы (IIIn),
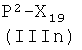
где Р2, как указано выше, X19 представляет радикал, имеющий следующие значения
- (d5′′) -R12b-CH(NHP3)-СН2-ОН
- (d6′′) -R12b-CH(CH2OP1)-NH2
где Р1 и Р3, как указано выше, и R12b выбран из D10), с соединением формулы (IVa)
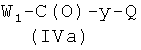
где W1, y, Q, как указано выше, у представляет радикал Y, где Y, как указано выше, и
5a-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 5a-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
5a-iii) необязательным снятием защитных групп с полученных на стадии 5a-i) или 5a-ii) соединений, как указано выше.
Реакцию соединения формулы (IIIn), где Р2 и Х19, как указано выше, с соединением формулы (IVa), W1, y и Q, как указано выше, можно проводить, как описано в 1-i-1), 1-i-2), 1-i-3) и 1a-1).
Соединения формулы (IIIn), где где Р4 и X19, как указано выше, являются коммерчески доступными или получены известными из литературы методами.
5b) Соединения формулы (Is), где X18 представляет радикал формулы (d5′) или (d6′), где R12b выбран из D10), Т′ и Т′′′ представляют С(O)-Х′′, где X′′, как указано выше, могут быть получены
5b-i) реакцией соединения формулы (IIIn),
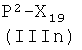
где Р2 и X19, как указано выше, с соединением формулы (IVd)

где Ra и Q, X′′, как указано выше, у представляет радикал Y, где Y, как указано выше, и
5b-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 5b-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
5b-iii) необязательным снятием защитных групп с полученных на стадии 5b-i) или 5b-ii) соединений, как указано выше.
Реакцию соединения формулы (IIIn), где Р2 и Х19, как указано выше, с соединением формулы (IVd), Ra, y, Q, X′′, как указано выше, можно проводить, как описано в 1-i-2).
5с) Соединения формулы (Is), где X18 представляет радикал формулы (d9′), где R12b выбран из D10), Y и Y′, как указано выше, Т представляет С(O)- и Т′′′ представляет С(O)- или С(O)-Х′′, где X′′, как указано выше, могут быть получены
5с-i) реакцией соединения формулы (It),
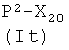
где Р2, как указано выше, и Х20 представляет радикал, имеющий следующие значения
- (d9′′) -R12b-CH(NH2)-СН2-О-(Т′′′-Y-Q)
где R12b выбран из D10), Т′′′, Y и Q, как указано выше, с соединением формулы (IVa)
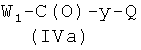
где W1 и Q, как указано выше, y представляет радикал Y′, где Y′, как указано выше,
5c-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 5c-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
5c-iii) необязательным снятием защитных групп с полученных на стадии 5c-i) или 5c-ii) соединений, как указано выше.
Реакцию соединения формулы (It), где Р2 и Х20, как указано выше, с соединением формулы (IVa), где W1, y, Q, как указано выше, можно проводить, как описано в 1-i-1), 1-i-2), 1-i-3) и 1a-1).
5d) Соединения формулы (Is), где X18 представляет радикал формулы (d9′), где R12b выбран из D10), Т′ представляет С(O)-Х′′ и Т′′′ представляет С(O)- или С(O)-Х′′, где X′′, как указано выше, могут быть получены
5d-i) реакцией соединения формулы (It′)
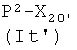
где Р2 and Х20', как указано выше, с соединением формулы (IVd)
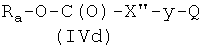
где Ra и Q, X′′, как указано выше, y представляет радикал Y′, где Y', как указано выше, и
5d-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 5d-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
5d-iii) необязательным снятием защитных групп с полученных на стадии 5d-i) или 5d-ii) соединений, как указано выше.
Реакцию соединения формулы (It′), где Р2 и Х20′, как указано выше, с соединением формулы (IVd) Ra, y, Q, X′′, как указано выше, можно проводить, как указано в 1-i-2).
5е) Соединения формулы (Is), где X18 представляет радикал формулы (d10′), где R12b выбран из D10), Y и Y′, как указано выше, Т′′′ представляет С(O)- и Т′ представляет С(O) или С(O)-Х′′, где X′′, как указано выше, могут быть получены
5e-i) реакцией соединения формулы (It),
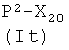
где Р2, как указано выше, и Х20 представляет радикал, имеющий следующие значения
- (d10′′) -R12b-CH(CH2-ОН)-NH-(T′-Y-Q)
где R12b выбран из D10), Т′, Y и Q, как указано выше, с соединением формулы (IVa)
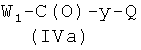
где W1 и Q, как указано выше, y представляет радикал Y′, где Y′, как указано выше, и
5e-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 5e-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
5е-iii) необязательным снятием защитных групп с полученных на стадии 5e-i) или 5e-ii) соединений, как указано выше.
Реакцию соединения формулы (It), где Р2 и Х20, как указано выше, с соединением формулы (IVa), где W1, y, Q, как указано выше, можно проводить, как описано в 1-i-1), 1-i-2), 1-i-3) и 1a-1).
5f) Соединения формулы (Is), где X18 представляет радикал формулы (d10′), где R12b выбран из D10), Т′′′ представляет С(O)-Х′′ и Т′ представляет С(O)- или С(O)-Х′′, где X′′, как указано выше, могут быть получены
5f-i) реакцией соединения формулы (If),
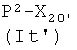
где Р2 и Х20′, как указано выше, с соединением формулы (IVd)
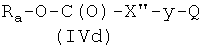
где Ra и Q, X′′, как указано выше, y представляет радикал Y′, где Y′, как указано выше, и
5f-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 5f-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
5f-iii) необязательным снятием защитных групп с полученных на стадии 5f-i) или 5f-ii) соединений, как указано выше.
Реакцию соединения формулы (If), где Р2 и Х20′, как указано выше, с соединением формулы (IVd), где Ra, y, Q, X′′, как указано выше, можно проводить, как описано в 1-i-2).
6) Соединения указанной выше общей формулы (I), где а равно 1, Rx представляет радикал, выбранный из (d5), (d6), (d9) или (d10), где R12b выбран из D10), Z представляет -CH(R′)-O-, где R′, как указано выше, могут быть получены
6-i) реакцией соединения формулы (IIa)
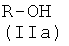
где R, как указано выше, с соединением формулы (Iu)
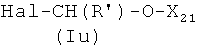
где Hal представляет атом галоида, R′, как указано выше, и X21 представляет радикал, выбранный из (d5′), (d6′), (d9′) или (d10′), где R12b выбран из D10), и
6-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 6-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
6-iii) необязательным снятием защитных групп с полученных на стадии 6-i) или 6-ii) соединений, как указано выше.
Реакцию соединения формулы (Iu), где Hal, X21 и R′, как указано выше, с соединением формулы (IIa), где R, как указано выше, можно проводить, как описано в 1l-i).
Соединения формулы (Iu) получены реакцией соединения R′-CHO, где R′, как указано выше, с соединением формулы (IIIo)
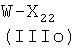
где W представляет атом хлора, Х22 представляет радикал, имеющий следующие значения
- (d5′′′) -R12b-CH(NHP3)-СН2-O-(Т′′′-Y-Q)
- (d6′′′) -R12b-CH(CH2OP1)-NH-(Т′-Y-Q)
- (d9′′′) -R12b-CH(NH-T′-Y′-Q)-СН2-O-(T′′′-Y-Q)
- (d10′′′) -R12b-CH(CH2-O-T′′′-Y'-Q)-NH-(T′′-Y-Q)
где R12b, P3, P1, T′, T′′′, Y′, Y и Q, как указано выше, и ZnCl2, как известно из литературы.
Соединения формулы (IIIo), где W и Х22, как указано выше, могут быть произведены, как описано в 5).
7) Соединения указанной выше общей формулы (I), где а равно 1, Rx представляет радикал, выбранный из (d5), (d6), (d9) или (d10), где R12b выбран из D8) или D9), Z представляет -С(O)-, могут быть получены
7-i) реакцией соединения формулы (IIb)
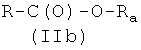
где R и Ra, как указано выше, с соединением формулы (Iv)
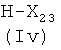
где Х23 представляет радикал, выбранный из (d5′), (d6′), (d9′) или (d10′), где
R12b выбран из D8) или D9), и
7-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 7-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
7-iii) необязательным снятием защитных групп с полученных на стадии 7-i) или 7-ii) соединений, как указано выше.
Реакцию соединения формулы (Iv), где Х23, как указано выше, с соединением формулы (IIb), где R, как указано выше, можно проводить, как описано в 1l-i).
8) Соединения указанной выше общей формулы (I), где а равно 0, Rx представляет радикал, выбранный из (а5), (а6), (а9) или (а10), (b5), (b6), (b9) или (b10), где R1b выбран из А10) и R2b выбран из В10), могут быть получены 8-i) реакцией соединения формулы (IIa)
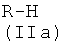
где R, как указано выше, с соединением формулы (Iz)
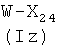
где W, как указано выше, Х24 представляет радикал Rx, имеющий следующие значения
- (а5′) -R1b-CH(NHR4a)-С(O)-(T-Y-Q)
- (а6′) -R1b-CH(СОOR3а)NH-(T′-Y-Q)
- (а9′) -R1b-CH(NH-T′-Y′-Q)-C(O)-(T-Y-Q)
- (а10′) -R1b-CH(C(O)-T′-Y′-Q)-NH-(T-Y-Q)
- (b5′) -R2b-CH(NHR4a)-CH2C(О)-(T-Y-Q)
- (b6′) -R2b-CH(CH2COOR3a)NH-(T′-Y-Q)
- (b9′) -R2b-CH(NH-T′-Y′-Q)-СН2С(О)-(T-Y-Q)
- (b10′) -R2b-CH(CH2C(О)-T′-Y′-Q)-NH-(T-Y-Q)
где R1b выбран из А10), R2b is выбран из B10), Т, Т′, Y и Q, как указано выше, и
8-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 8-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
8-iii) необязательным снятием защитных групп с полученных на стадии 8-i) или 8-ii) соединений, как указано выше.
Реакцию соединения формулы (IIa), где R, как указано выше, с соединением формулы (Iv), где W и Х24, как указано выше, можно проводить, как описано в 1).
8а) Соединения формулы (Iz), где Х24 представляет радикал формулы (а5′), (а6′), (b5′) или (b6′), где R1b выбран из А10) и R2b выбран из В10), Т и Т′′ представляют С(O), могут быть получены
8a-i) реакцией соединения формулы (IIIq),
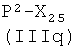
где Р2, как указано выше, Х25 представляет радикал, имеющий следующие значения
-(а5′′) -R1b-CH(NHP3)-С(O)-ОН
-(а6′′) -R1b-CH(СООР2)-NH2
-(b5′′) -R2b-CH(NHP3)-СН2С(O)-ОН
-(b6′′) -R2b-CH(CH2COOP2)NH2
где Р2 и Р3, как указано выше, и R1b выбран из А10), R2b выбран из В10), с соединением формулы (IVa)
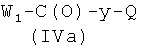
где W1 и Q, как указано выше, y представляет радикал Y, где Y, как указано выше, и
8a-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 8a-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
8a-iii) необязательным снятием защитных групп с полученных на стадии 8a-i) или 8a-ii) соединений, как указано выше.
Реакцию соединения формулы (IIIq), где Р2 и Х25, как указано выше, с соединения формулы (IVa), W1, Y, и Q, как указано выше, можно проводить, как описано в 1-i-1), 1-i-2), 1-i-3) и 1a-1).
Соединения формулы (IIIq), где Р2 и Х25, как указано выше, являются коммерчески доступными или получены известными из литературы методами.
8b) Соединения формулы (Iz), где Х24 представляет радикал формулы (а5′), (а6′), (b5′) или (b6′), где R1b выбран из А10) и R2b выбран из В 10), Т и Т′ представляют С(O)-Х′′, где X′′, как указано выше, могут быть получены 8b-i) реакцией соединения формулы (IIIq),
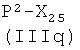
где Р2 и Х25, как указано выше, с соединением формулы (IVd)
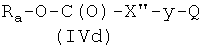
где Ra, Q и X", как указано выше, y представляет радикал Y, где Y, как указано выше, и
8b-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 8b-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
8b-iii) необязательным снятием защитных групп с полученных на стадии 8b-i) или 8b-ii) соединений, как указано выше.
Реакцию соединения формулы (IIIq), где Р2 и Х25, как указано выше, с соединением формулы (IVd), Ra, y, Q, X", как указано выше, можно проводить, как описано в 1-i-2).
8с) Соединения формулы (Iz), где Х24 представляет радикал формулы (а9′) или (b9′), где R1b выбран из А10) и R2b выбран из В10), Y и Y′, как указано выше, Т представляет С(О)- или С(O)-Х′′, где X′′, как указано выше, и Т′ представляет С(O), могут быть получены
8c-i) реакцией соединения формулы (Iy),
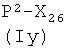
где Р2, как указано выше, и Х26 представляет радикал, имеющий следующие значения
- (а9′′) -R1b-CH(NH2)-С(О)-(T-Y-Q)
- (b9′′) -R2D-CH(NH2)-СН2С(О)-(T-Y-Q)
где R1b выбран из А10) и R2b выбран из В10),
с соединением формулы (IVa)
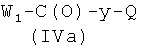
где W1 и Q, как указано выше, y представляет радикал Y′, где Y′, как указано выше, и
8c-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 8c-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
8c-iii) необязательным снятием защитных групп с полученных на стадии 8c-i) или 8c-ii) соединений, как указано выше.
Реакцию соединения формулы (Iy), где Р2 и Х26, как указано выше, с соединением формулы (IVa), где W1, y, Q, как указано выше, можно проводить, как описано в 1-i-1), 1-i-2), 1-i-3) и 1a-1).
8d) Соединения формулы (Iz), где Х24 представляет радикал формулы (а9′) или (b9′), где R1b выбран из А10), R2b выбран из В10), Y и Y′, как указано выше, Т представляет С(O)- или С(O)-Х′′, где X′′, как указано выше, и Т′ представляет С(O)-Х′′, могут быть получены
8d-i) реакцией соединения формулы (Iy),
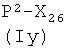
где Р2 и Х26, как указано выше, с соединением формулы (IVd)
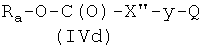
где Ra и X′′, как указано выше, y представляет радикал Y′, где Y′, как указано выше, и
8d-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 5d-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
8d-iii) необязательным снятием защитных групп с полученных на стадии 8d-i) или 8d-ii) соединений, как указано выше.
Реакцию соединения формулы (Iy), где Р2 и Х20, как указано выше, с соединением формулы (IVd), Ra, y, Q, X′′, как указано выше, можно проводить, как описано в 1-i-2).
8е) Соединения формулы (Iz), где Х24 представляет радикал формулы (а10′) или (b10′), где R1b выбран из А10), и R2b выбран из В10), Y и Y′, как указано выше, Т представляет С(O)- или С(O)-Х′′, где X′′, как указано выше, и Т′ представляет С(O), могут быть получены
8e-i) реакцией соединения формулы (Iy′),
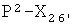
где Р2, как указано выше, и Х26 представляет радикал, имеющий следующие значения
- (а10′′) -R1b-CH(С(О)-ОН)-NH-(T-Y-Q)
- (b10′′) -R2b-CH(CH2C(О)-ОН)-NH-(T-Y-Q)
где R1b выбран из А10) и R2b представляет В10), с соединением формулы (IVa)
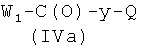
где W1 и Q, как указано выше, y представляет радикал Y′, где Y′, как указано выше, и
8e-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 8e-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
8e-iii) необязательным снятием защитных групп с полученных на стадии 8e-i) или 8e-ii) соединений, как указано выше.
Реакцию соединения формулы (Iy′), где Р2 и Х26', как указано выше, с соединением формулы (IVa), где W1, y, Q, как указано выше, можно проводить, как описано в 1-i-1), 1-i-2), 1-i-3) и 1a-1).
8f) Соединения формулы (Iz), где Х24 представляет радикал формулы (а10′) или (b10′), где R2b выбран из А10) и R2b выбран из В10), Y и Y′, как указано выше, Т представляет С(O)- или С(O)-Х′′, где X′′, как указано выше, и Т′ представляет С(O)-Х′′, могут быть получены
8f-i) реакцией соединения формулы (Iy')
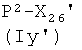
где Р2 и Х26', как указано выше, с соединением формулы (IVd)
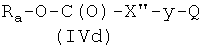
где Ra и X′′, как указано выше, y представляет радикал Y′, где Y′, как указано выше, и
8f-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 8f-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
8f-iii) необязательным снятием защитных групп с полученных на стадии 8f-i) или 8f-ii) соединений, как указано выше.
Реакцию соединения формулы (Iy′) где Р2 и Х26', как указано выше, с соединением формулы (IVd), где Ra, y, Q, X′′, как указано выше, можно проводить, как описано в 1-i-2).
9) Соединения указанной выше общей формулы (I), где а равно 1, Rx представляет радикал, выбранный из (а5), (а6), (а9) или (а10), (b5), (b6), (b9) или (b10), где R1b выбран из А8) или А9), R2b выбран из В8) или В9), Z представляет -С(O)-, могут быть получены
9-i) реакцией соединения формулы (IIb)
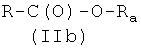
где R и Ra, как указано выше, с соединением формулы (Ix)
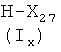
где Х27 представляет радикал, выбранный из (а5′), (а6′), (а9′), (а10′), (b5′), (b6′), (b9′) или (b10′), где R1b выбран из А8) или А9), R2b выбран из В8) или В9), и
9-ii) когда Q представляет Z2, превращением соединения, полученного на стадии 9-i), в нитропроизводное взаимодействием с источником нитрата, как описано выше, и
9i-iii) необязательным снятием защитных групп с полученных на стадии
9i-i) или 9i-ii) соединений, как указано выше.
Реакцию соединения формулы (Ix), где Х27, как указано выше, с соединением формулы (IIb), где R, как указано выше, можно проводить, как описано в 1l-i).
Пример 1
Синтез (11β,16β)-9-хлор-11,17-дигидрокси-16-метил-21-[1-оксо-((2-(4-(нитроокси)бутилоксикарбониламино)ацетил)]-прегна-1,4-диен-3,20-диона.
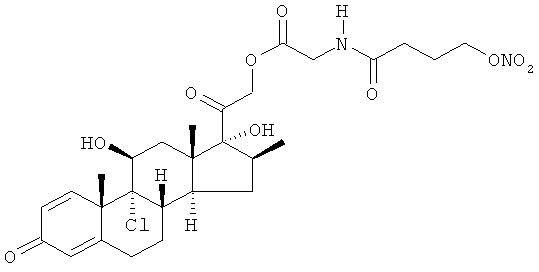
(11β,16β)-9-хлор-11,17-дигидрокси-16-метил-21-[1-оксо-((трет-бутилкарбониламино)ацетил)]-прегна-1,4-диен-3,20-дион
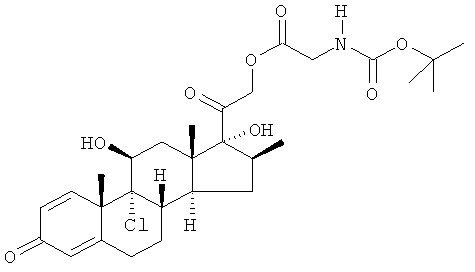
К раствору беклометазона (0,6 г, 1,46 ммоль) в ацетоне (35 мл) добавляют N-Вос-глицин (Boc - третбутилоксикарбонил) (0,334 г, 1,90 ммоль) и DMAP (4-N,N-диметиламинопиридил) (каталитическое количество). Реакционную смесь охлаждают при 0°С и добавляют EDAC (N-этил-N′-диметиламинопропил карбодиимид гидрохлорид) (0,365 г, 1,90 ммоль). Перемешивают при комнатной температуре 2 часа. Растворитель испаряют под вакуумом. Остаток обрабатывают водой (50 мл) и метиленхлоридом (50×3 мл), органический слой сушат над сульфатом натрия и концентрируют при пониженном давлении. Остаток очищают с помощью флэш-хроматографии, элюент н-гексан/этилацетат 6/4. Получают 0,8 г продукта.
(11β,16β)-9-хлор-11,17-дигидрокси-16-метил-21-[1-оксо-2-((карбониламино)ацетил)]-прегна-1,4-диен-3,20-дион гидрохлорид
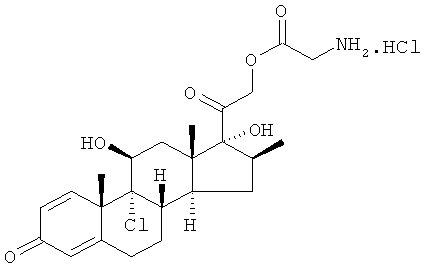
Раствор соединения А (0,8 г, 0,41 ммоль) в метиленхлориде (70 мл) перемешивают при комнатной температуре. В раствор барботируют газообразный HCl в течение 1 часа. Растворитель испаряют при пониженном давлении. Продукт используют на следующей стадии без какой-либо очистки.
(11β,16β)-9-Хлор-11,17-дигидрокси-16-метил-21-[1-оксо-(2-((4-(нитроокси)бутокси-карбониламино)ацетил)]-прегна-1,4-диен-3,20-дион
К раствору В) (0,75 г, 1,46 ммоль) в метиленхлориде (40 мл) добавляют пентафторфениловый эфир 4-нитрооксибутановой кислоты (0,41 г, 1,46 ммоль), DMAP (каталитическое количество) и триэтиламин (0,3 мл, 2,19 ммоль). Реакционную смесь перемешивают при комнатной температуре 24 часа. Раствор обрабатывают 5% раствором H3PO4 (50 мл). Органический слой сушат над сульфатом натрия и концентрируют при пониженном давлении. Остаток очищают с помощью флэш-хроматографии (Biotage System, column FLASH 40+M™ KP-Sil), элюент: градиент н-гексан/этилацетат 1/1 (130 мл) до этилацетат 100% (130 мл), этилацетат 100% (130 мл). Получают 0,62 г продукта в виде белого порошка.
1H-NMR: (ДМСО), δ: 8.42 (1Н, t); 7.30 (1Н, d); 6.22 (1H, dd); 5.98 (1H, s); 5.46 (1H, d); 5.42 (2H, s); 5.05 (1H, d); 4.84 (1H, d); 4.5 (2H, t); 4.34 (1H, sb); 3.97 (2Н, d); 2.71-2.57 (2H, m); 2.5-2.2 (6H, m); 2.0-1.7 (5H, m); 1.65-1.35 (5H, m); 1.25-0.97 (4H, m); 0.8 (3H, s).
Пример 2
Синтез (11β,16β)-9-фтор-11,17-дигидрокси-16-метил-21-[1-оксо-((2-(4-(нитроокси)бутилоксикарбониламино)ацетил)]-прегна-1,4-диен-3,20-диона.
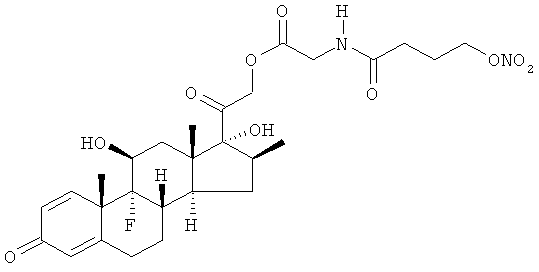
Соединение синтезировали, используя процедуру, описанную в примере 1, исходя из бетаметазона, Вос-глицина и пентафторфенилового эфира 4-нитрооксибутановой кислоты.
1H-NMR: (ДМСО), δ: 8.4 (1Н, t); 7.28 (1Н, d); 6.22 (1H, dd); 6.0 (1Н, s); 5.30 (1Н, d); 5.08 (1Н, d); 4.83 (1Н, d); 4.53 (2H, t); 4.15 (1Н, bp); 3.95 (2H, d); 2.71-2.52 (1Н, m); 2.51-2.4 (6H, m); 2.38-2.07 (2H, m); 2.03-1.75 (6H, m)/ 1.58-1.45 (4H, m), 1.11-0.8 (6H, m).
Пример 3
Синтез (11β,16β)-9-фтор-11-гидрокси-16,17-(1-метилэтилиденбис(окси))-21-[1-оксо-(2-(4-(нитроокси)бутилоксикарбониламино)ацетил)]-прегна-1,4-диен-3,20-диона.
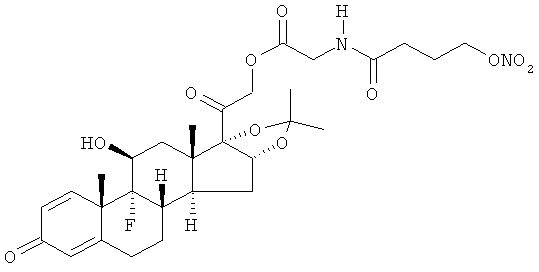
Соединение синтезировали, используя процедуру, описанную в примере 1, исходя из триамцинолон ацетонида, Вос-глицина и пентафторфенилового эфира 4-нитрооксибутановой кислоты.
1H-NMR: (ДМСО), δ: 8.43 (1Н, t); 7.27 (1Н, d); 6.21 1H-NMR: (ДМСО), δ: (1Н, dd); 6. (1Н, s); 5.46 (1Н, d); 5.18 (1Н, d); 4.87-4.83 (1Н, m); 4.74 (1Н, d); 4.50 (1Н, t); 4.18 (1Н, sb); 3.98-3.96 (2H, m); 2.71-2.31 (5H, m); 2.30-2.2 (3Н, m); 2.10-1.77 (6H, m); 1.75-1.42 (7H, m); 1.4-1.32 (4H, m); 1.12 (3Н, s); 0.85 (3Н, s).
Пример 4
Синтез (6α,11β,16α)-6,9-дифтор-11-гидрокси-16,17-(1-метилэтилиден)бис(окси))-21-[1-оксо-(2-(4-(нитроокси)бутилоксикарбониламино)ацетил)]-прегна-1,4-диен-3,20-диона.
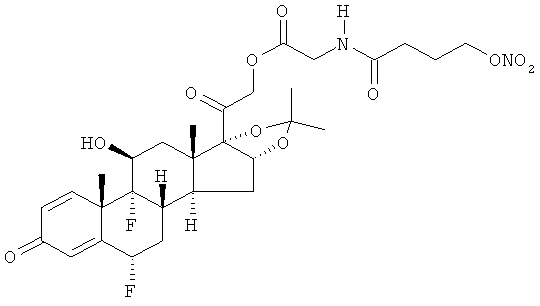
Соединение синтезировали, используя процедуру, описанную в примере 1, исходя из фторцинолон ацетонида, Вос-глицина и пентафторфенилового эфира 4-нитрооксибутановой кислоты.
1H-NMR: (ДМСО), δ: 8.43 (1Н, t); 7.25 (1Н, d); 6.28 (1H, dd); 6.09 (1H, s); 5.75-5.48 (2H, m); 5.18 (1H, d); 4.83 (1H, d); 4.78 (1H, d); 4.50 (2H, t); 4.18 (1H, sb); 3.9-3.8 (2H, m); 2.72-2.48 (4H, m); 2.25 (2H, t); 2.10-1.8 (3H, m); 1.78-1.65 (1H, m); 1.62-1.51(2H, m); 1.48 (3H, s); 1.32 (3H, s); 1.10 (3H, s); 0.8 (3H, s).
Пример 5
Синтез 4-(нитроокси)бутил 2-ацетамидо-3-(4-((2-((9R,10S,11S,13S,16R,17S)-9-фтор-11-гидрокси-16,17-((1-метилэтилиден)бис(окси))10,13-диметил-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-17-ил)-2-оксоэтокси)карбонилокси)фенил)пропаноата
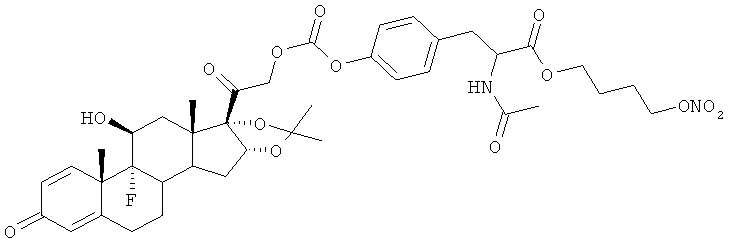
D) 4-(Нитроокси)бутил 2-(трет-бутоксикарбониламино)-3-(4-гидроксифенил)пропаноат
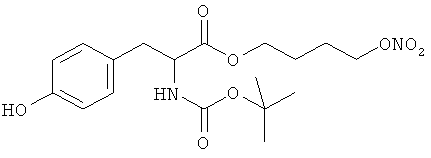
К раствору Вос-(L)-тирозина (5.0 г, 17,77 ммоль) в N,N-диметилформамиде (40 мл) добавляют карбонат цезия (5,79 г, 17,77 ммоль). Реакционную смесь охлаждают до 0°С и добавляют по каплям раствор 4-бромбутилнитрата (17,77 ммоль) в дихлорметане (20% вес./вес., 17,06 г). Реакционную смесь перемешивают при 0°С 20 минут и затем при комнатной температуре 22 часа.
Смесь вливают в 5% водный раствор NaH2PO4 и экстрагируют диэтиловым эфиром (40×4 мл), органический слой сушат над сульфатом натрия и концентрируют при пониженном давлении. Остаток очищают с помощью флэш-хроматографии (Biotage System, column FLASH 65+M™ KP-Sil), элюент: градиент н-гексан/этилацетат 9/1 (500 мл) до н-гексан/этилацетат 1/1 4000 мл, н-гексан/этилацетат 1/1 (1000 мл). Получают 3,91 г продукта.
Е) 4-(Нитроокси)бутил 2-амино-3-(4-гидроксифенил)пропаноат
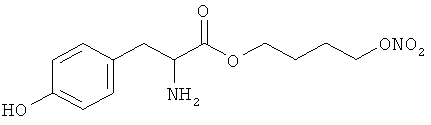
Раствор соединения D (0,96 г, 2,41 ммоль) в дихлорметане (20 мл) перемешивают при комнатной температуре. В течение 3 часов барботируют в через раствор газообразный HCl. Смесь разбавляют дихлорметаном (25 мл), промывают насыщенным водным раствором карбоната натрия. Органический слой сушат над сульфатом натрия и концентрируют при пониженном давлении. Продукт (0,71 г) используют на следующей стадии без какой-либо очистки.
F) 4-(Нитроокси)бутил 2-ацетамидо-3-(4-гидроксифенил)пропаноат
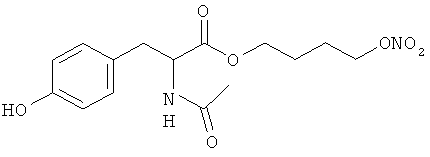
К раствору соединения Е (0,63 г, 2,25 ммоль) в дихлорметане (15 мл) добавляют триэтиламин (0,31 мл, 2,25 ммоль). Реакционную смесь охлаждают при 0°С и добавляют по каплям ацетилхлорид (0,17 мл, 2,48 ммоль). Реакционную смесь перемешивают при 0°С 10 минут и затем при комнатной температуре 16 часов. Смесь разбавляют дихлорметаном (25 мл), промывают водой. Органический слой сушат над сульфатом натрия и концентрируют при пониженном давлении. Остаток очищают с помощью флэш-хроматографии (Biotage System, column FLASH 25+M™ KP-Sil), элюент: градиент н-гексан/этилацетат 9/1 (100 мл) до н-гексан/этилацетат 2/8 (1200 мл). Получают 0,54 г продукта.
G) 4-(Нитроокси)бутил 2-ацетамидо-3-(4-((4-нитрофенокси)карбонилокси)фенил)пропаноат
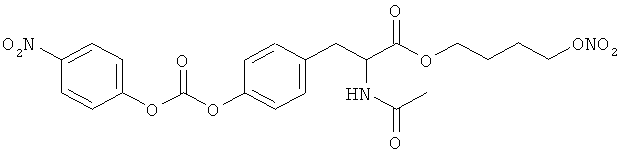
К раствору соединения F (0,54 г, 1,58 ммоль) в дихлорметане (8 мл) добавляют пиридин (0,15 мл, 1,58 ммоль). Реакционную смесь охлаждают до 0°С и добавляют п-нитрофенилхлорформиат (320 мг, 1,58 ммоль). Реакционную смесь перемешивают при 0°С 15 минут и затем при комнатной температуре 48 часов. Смесь разбавляют дихлорметаном (25 мл), промывают 1 М водным раствором HCl и затем насыщенным водным раствором карбоната натрия. Органические слои сушат над сульфатом натрия и концентрируют при пониженном давлении. Остаток очищают с помощью флэш-хроматографии (Biotage System, column FLASH 25+M™ KP-Sil), элюент: градиент н-гексан/этилацетат 9/1 (150 мл) до н-гексан/этилацетат 3/7 1200 мл, н-гексан/этилацетат 3/7 (600 мл). Получают 0,59 г продукта.
Н) 4-(Нитроокси)бутил 2-ацетамидо-3-(4-((2-((9R,10S,11S,13S,16R,17S)-9-фтор-11-гидрокси-16,17-((1-метилэтилиден)бис(окси))10,13-диметил-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-17-ил)-2-оксоэтокси)карбонилокси)фенил)пропаноат
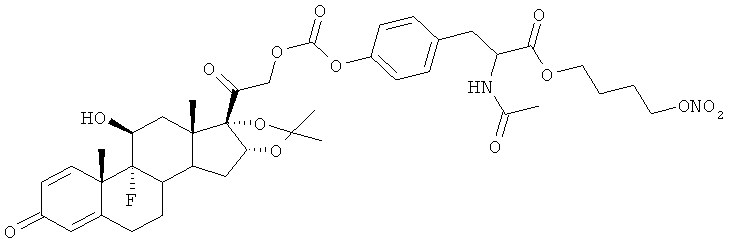
К раствору соединения G (0,55 г, 1,09 ммоль) в дихлорметане (12 мл) добавляют трифлат (трифторметансульфонат) скандия (0,05 г, 0,11 ммоль) и DMAP (0,26 г, 2,19 ммоль). Реакционную смесь охлаждают до 0°С и добавляют триамцинолон ацетонид (0,47 г, 1,09 ммоль). Реакционную смесь перемешивают при комнатной температуре 18 часов. Смесь разбавляют дихлорметаном (24 мл), промывают 5% NaH2PO4 и затем насыщенным водным раствором карбоната натрия. Органический слой сушат над сульфатом натрия и концентрируют при пониженном давлении. Остаток очищают с помощью флэш-хроматографии (Biotage System, column FLASH 25+M™ KP-Sil, элюент: градиент н-гексан/этилацетат 9/1 (150 мл) до н-гексан/этилацетат 2/8, 1200 мл, н-гексан/этилацетат 2/8 (800 мл)). Получают 0,29 г продукта.
1H-NMR: (ДМСО), δ: 8.36 (1Н, d); 7.37-7.32 (3Н, m); 7.21-7.12 (2Н, m); 6.23 (1H, dd); 6.02 (1Н. s); 5.47 (1Н, d); 5.31 (1Н, d); 4.97-4.87 (2Н, m); 4.59-4.48 (3Н, m); 4.27-4.17 (1Н, sb); 4.11-3.97 (2Н, m); 3.10- 2.90 (1Н, m); 2.71-2.29 (4H, m); 2.10-1.75 (5H, m); 1.60-1.40 (7H, m); 1.38 (3Н, s); 1.12 (3Н, s); 0.80 (3Н, s).
Пример 6
Синтез (2S)-4-(нитроокси)бутил 2-ацетамидо-3-(4-((2-((6S,9R,10S,11S,13S,16R,17S)-6,9-дифтор-11-гидрокси-16,17-((1-метилэтилиден)бис(окси))-10,13-диметил-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-17-ил)-2-оксоэтокси)карбонилокси)фенил)пропаноата

Соединение синтезировали, используя процедуру, описанную в примере 5, исходя из фторцинолон ацетонида и соединения G.
1H-NMR: (ДМСО), δ: 8.36 (1Н, d); 7.28 (3H, m); 7.09 (2H, m); 6.30 (1H, dd); 6.11 (1H, d); 5.56 (1H, d); 5.31 (1H, d); 4.91 (2H, m); 4.50 (2H, t); 4.93 (1H, m); 4.25 (1H, m); 4.02 (3H, t); 2.96 (2H, m); 2.27 (1H, m); 2.01 (3H, m); 1.90-1.25 (17H, m); 1.15 (3H, s); 0.80 (3H, s).
Пример 7
Синтез (2S)-4-(нитроокси)бутил 2-амино-3-(4-((2-((9R,10S,HS,13S,16R,17S)-9-фтор-11-гидрокси-16,17-((1-метилэтилилен)бис(окси))-10,13-диметил-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-17-ил)-2-оксоэтокси)карбонилокси)фенил)пропаноата гидрохлорида
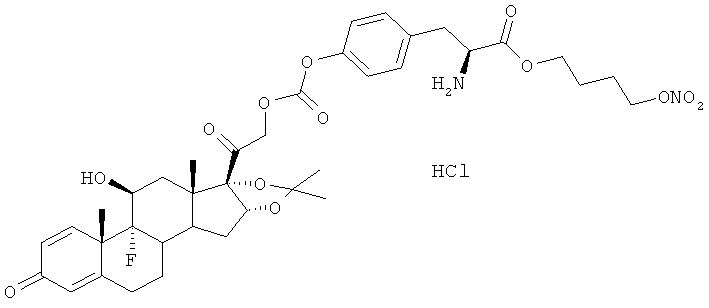
I) 4-Гидроксибутил 2-(трет-бутоксикарбониламино)-3-(4-((4-нитрофенокси)карбонилокси)фенил)пропаноат
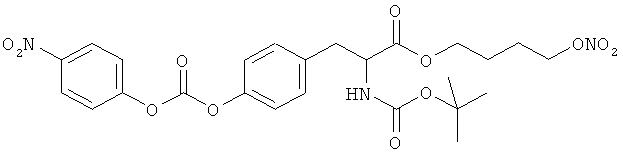
К раствору соединения D (1,97 г, 4,86 ммоль) в дихлорметане (24 мл) добавляют пиридин (0,48 мл, 4,86 ммоль). Реакционную смесь охлаждают до 0°С и добавляют р-нитрофенилхлорформиат (980 мг, 4,86 ммоль). Реакционную смесь перемешивают при 0°С 10 минут и затем при комнатной температуре 21 час. Смесь разбавляют дихлорметаном (25 мл), промывают 1 М водным раствором HCl и затем насыщенным водным раствором карбоната натрия. Органические слои сушат над сульфатом натрия и концентрируют при пониженном давлении. Остаток очищают с помощью флэш-хроматографии (Biotage System, column FLASH40+М™ KP-Sil, элюент: градиент н-гексан/этилацетат 98/2 (200 мл) до н-гексан/этилацетат 6/4 1600 мл, н-гексан/этилацетат 6/4 (300 мл)). Получают 2,19 г продукта.
J) (2S)-4-(Нитроокси)бутил 2-(трет-бутоксикарбониламино)-3-(4-((2-((9R,10S,11S,13S,16R,17S)-9-фтор-11-гидрокси-16,17-((1-метилэтилиден)бис(окси))-10,13-диметил-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-17-ил)-2-оксоэтокси)карбонилокси)фенил)пропаноат
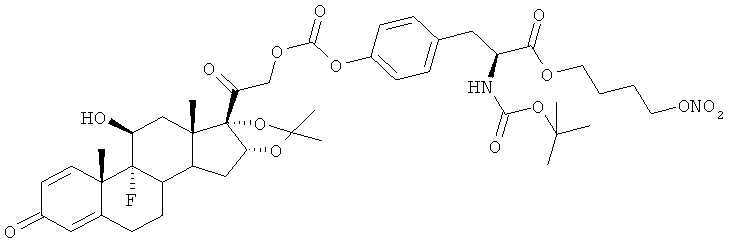
К раствору соединения I (1,35 г, 2,4 ммоль) в дихлорметане (40 мл), добавляют трифлат скандия (0,11 г, 0,24 ммоль) и DMAP (0,57 г, 4,8 ммоль). Реакционную смесь охлаждают при 0°С и добавляют триамцинолон ацетонид (1,25 г, 2,88 ммоль). Реакционную смесь перемешивают при комнатной температуре 79 часов. Растворитель испаряют при пониженном давлении. Остаток очищают с помощью флэш-хроматографии (Biotage System, column FLASH 40+M™ KP-Sil, элюент: градиент н-гексан/этил ацетат 9/1 (200 мл) до н-гексан/этил ацетат 3/7 1600 мл, н-гексан/этил ацетат 3/7 (500 мл)). Получают 0,98 г продукта.
К) (2S)-4-(Нитроокси)бутил-2-амино-3-(4-((2-((9R,10S,11S,13S,16R,17S)-9-фтор-11-гидрокси-16,17-((1-метилэтилиден)бис(окси))-10,13-диметил-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-17-ил)-2-оксоэтокси)карбонилокси)фенил)пропаноат гидрохлорид
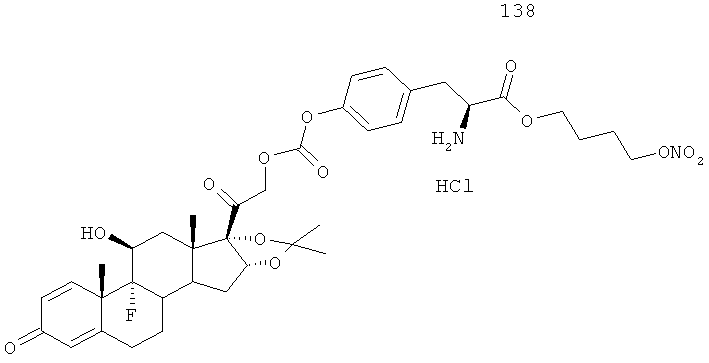
Раствор соединения J (1,42 г, 1,65 ммоль) в дихлорметане (28 мл) перемешивают при комнатной температуре. В течение 15 минут барботируют газообразный HCl. Смесь разбавляют дихлорметаном (35 мл), промывают насыщенным водным раствором карбоната натрия. Органический слой сушат над сульфатом натрия и концентрируют при пониженном давлении. Остаток очищают с помощью флэш-хроматографии с обратной фазой (Biotage System, column FLASH 40+M™ KP-Sil, элюент: градиент вода/ацетонитрил 9/1 (150 мл) до вода/ацетонитрил 2/8 1400 мл, вода/ацетонитрил 2/8 (200 мл)). Продукт М в виде свободного основания (0,67 г) обрабатывают раствором HCl в диэтиловом эфире. Отфильтровывают хлористоводородную соль соединения М и сушат под вакуумом. Получают (0,57 г) продукта.
1H-NMR: (ДМСО), δ: 8.57 (2Н, m); 7.38-7.29 (3Н, m); 7.22-7.19 (2Н, m); 6.22 (1Н, dd); 6.00 (1Н, s); 5.54 (1H, d); 5.31 (1H, d); 4.88-4.84 (2Н, m); 4.52-4.40 (2Н, m); 4.25-4.20 (1H, sb); 4.16-4.09 (3Н, m); 3.22-3.04 (1H, m); 2.71-2.29 (4Н, m); 2.10-1.75 (5Н, m); 1.60-1.34 (7Н, m); 1.13 (3Н, s); 0.82 (3Н, s).
Пример 8
Синтез (2S)-4-(нитроокси)бутил 2-амино-3-(4-((2-((6S,9R,10S,11S,13S,16R,17S)-6,9-дифтор-11-гидрокси-16,17-((1-метилэтилиден)бис(окси))-10,13-диметил-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-17-ил)-2-оксоэтокси)карбонилокси)фенил)пропаноата гидрохлорида
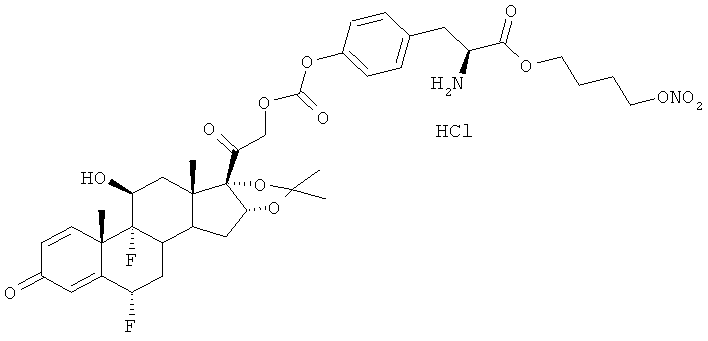
Соединение синтезируют, используя процедуру, описанную в примере 7, исходя из фторцинолон ацетонида и соединения I.
1H-NMR: (ДМСО), δ: 8.64 (2Н, s); 7.41-7.35 (3Н, m); 7.23 (2Н, d); 6.30 (1H, dd); 6.11 (1H, s); 5.80-5.50 (2Н, m); 5.40-5.27 (1H, m); 5.00-4.75 (2Н, m); 4.53-4.45 (2Н, m); 4.48-4.05 (4Н, m); 3.31-3.03 (2Н, m); 2.75-2.60 (1H, m); 2.27 (1H. sb); 2.11-1.98 (3Н, m); 1.82-1.52 (5Н, m); 1.50 (3Н, s); 1.38 (3Н, s); 1.10 (3H, s); 0.81 (3H, s).
Пример 9
Синтез 2-((8S,9R,10S,11S,13S,14S,16R,17S)-9-фтор-11-гидрокси-16,17-(1-метилэтилиденбис(окси))-10,13-диметил-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-17-ил)-2-оксоэтил-2-(5-(нитроокси)пентанамидо)ацетата
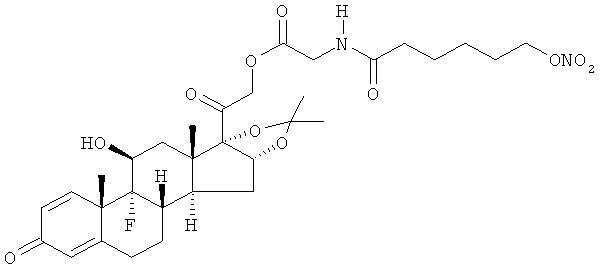
Соединение синтезируют, используя процедуру, описанную в примере 1, исходя из триамцинолон ацетонида, Вос-глицина и пентафторфенилового эфира 4-нитрооксибутановой кислоты.
1H-NMR: (ДМСО), δ: 7.29 (1Н, d); 6.23 (1H, dd); 6.02 (1H, s); 5.48 (1H, d); 5.20 (1H, d); 4.86 (1H, m); 4.78 (1H, d); 4.50 (2H, t); 4.18 (1H, sb); 3.98-3.96 (2H, m); 2.71-2.25 (2H, m); 2.30 (5H, m); 1.75-1.42 (14H, m); 1.4-1.32 (4H, m); 1.12(3H, s); 0.83 (3H, s).
Пример 10
Синтез 2-((8S,9R,10S,11S,13S,14S,16S,17R)-9-фтор-11,17-дигидрокси-10,13,16-триметил-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-17-ил)-2-оксоэтил 2-(5-(нитроокси)гексанамидоамидо)ацетата
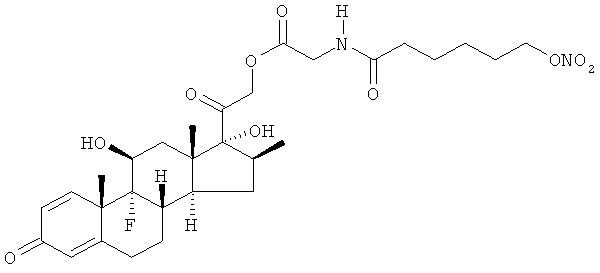
Соединение синтезируют, используя процедуру, описанную в примере 1, исходя из бетаметазона, Вос-глицина и пентафторфенолового эфира 6-нитрооксигексановой кислоты.
1H-NMR: (ДМСО), δ: 8.28 (1Н, t); 7.27 (1Н, d); 6.15 (1H, dd); 5.99 (1H, s); 5.35 (1H, s); 5.27 (1H, d); 4.99 (1H, d), 4.79 (1H, d); 4.48 (2H, t), 4.11 (1H, m); 3.91 (2H, d); 2.60 (1H, m); 2.50-2.30 (2H, m); 2.10 (4H, m); 2.00-1.80 (3Н, m); 1.70-1.30 (11H, m); 1.00 (4H, d); 0.99 (3Н, s).
Пример 11
Синтез 2-((6S,8S,9R,10S,11S,13S,14S,16R,17S)-6,9-дифтор-11-гидрокси-16,17-диметокси-10,13-диметил-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-17-ил)-2-оксоэтил 2-(6-нитрооксигексанамидо)ацетата
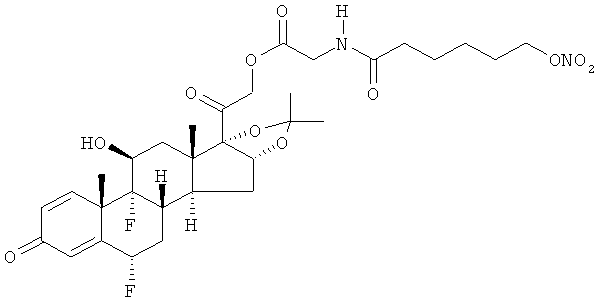
Соединение синтезируют, используя процедуру, описанную в примере 1, исходя из фторцинолон ацетамида, Вос-глицина и пентафторфенолового эфира 6-нитрооксигексановой кислоты.
1H-NMR: (ДМСО), δ: 8.32 (1Н, t); 7.25 (1H, d); 6.28 (1H, dd); 6.09 (1H, s); 5.74-5.50 (2H, m); 5.18 (1H, d); 4.85 (1H, d); 4.78 (1H, d); 4.48 (2H, t); 4.19 (1H, sb); 3.94 (2H, m); 2.63-2.48 (1H, m); 2.25 (1H, t); 2.13 (2H, t); 2.10-1.93 (2H, m); 1.73-1.40 (11H, m); 1.30 (5H, m); 1.10 (3Н, s); 0.8 (3Н, s).
Пример 12
Синтез 1-(2-((8S,9R,10S,11S,13S,14S,16R,17S)-9-фтор-11-гидрокси-16,17-((1-метилэтилиден)бис(окси))-10,13-диметил-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-17-ил)-2-оксоэтил)-1-(4-(нитроокси)бутил) 2-ацетамидо пентандиоата
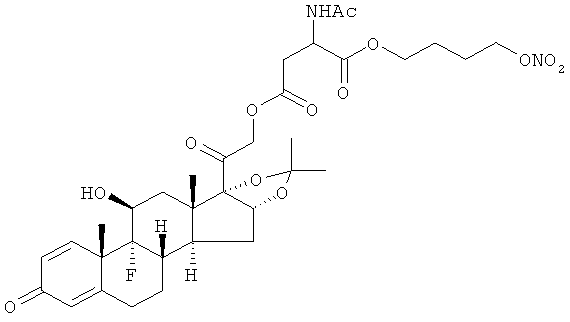
L) 2-Ацетамидо-4-(2-((8S,9R,10S,11S,13S,14S,16R,17S)-9-фтор-11-гидрокси-16,17-((1-метилэтилиден)бис(окси))-10,13-диметил-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-17-ил)-2-оксоэтокси)-4-оксобутановая кислота
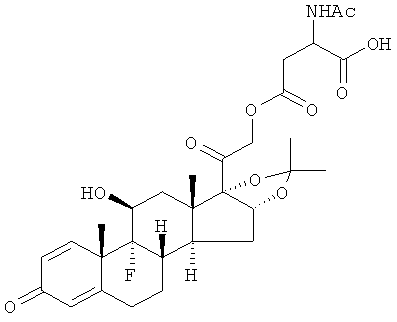
К раствору триамцинолон ацетонида (3,1 г, 7,13 ммоль) в ацетоне (100 мл) добавляют N-ацетил аспарагиновую кислоту (2,0 г, 11,42 ммоль) и DMAP (кат. количество). Реакционную смесь охлаждают при 0°С и добавляют EDAC (2,18 г, 11,42 ммоль). Реакционную смесь перемешивают при комнатной температуре 24 часа. Растворитель испаряют под вакуумом. Остаток очищают с помощью флэш-хроматографии (Biotage System, column FLASH 65+M™ KP-Sil, элюент: градиент дихлорметан/метанол 95/5 (675 мл) до дихлорметан/метанол 9/1 3600 мл, дихлорметан/метанол 9/1 (900 мл)). Получают 2,67 г продукта.
М) 1-(4-Хлорбутил)4-(2-((8S,9R,10S,11S,13S,14S,16R,17S)-9-фтор-11-гидрокси-16,17-((1-метилэтилиден)бис(окси))-10,13-диметил-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-17-ил)-2-оксоэтокси)-2-ацетамидосукцинат.
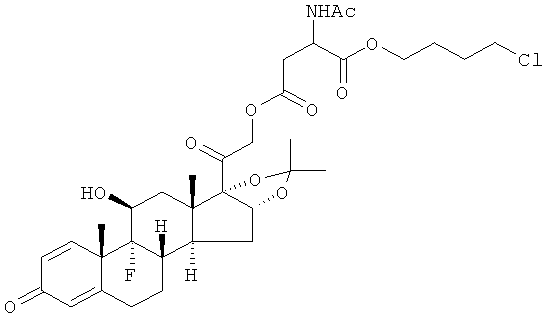
К раствору соединения L (0,6 г, 1,31 ммоль) в дихлорметане (30 мл) добавляют 4-хлорбутанол (0,13 мл, 1,31 ммоль) и DMAP (кат. количество). Реакционную смесь охлаждают при 0°С и добавляют EDAC (0,25 г, 1,31 ммоль). Смесь перемешивают при комнатной температуре 24 часа. Растворитель испаряют под вакуумом. Остаток очищают с помощью флэш-хроматографии (Biotage System, column FLASH 25+M™ KP-Sil, элюент: градиент н-гексан/ этил ацетат 6/4 (60 мл) до н-гексан/этил ацетат 2/8 600 мл до этил ацетат 60 мл, этил ацетат (180 мл)). Получают 0,65 г продукта.
N) 1-(4-Иодбутил)4-(2-((8S,9R,10S,11S,13S,14S,16R,17S)-9-фтор-11-гидрокси-16,17-((1-метилэтилиден)бис(окси))-10,13-диметил-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-17-ил)-2-оксоэтил)2-ацетамидо сукцинат
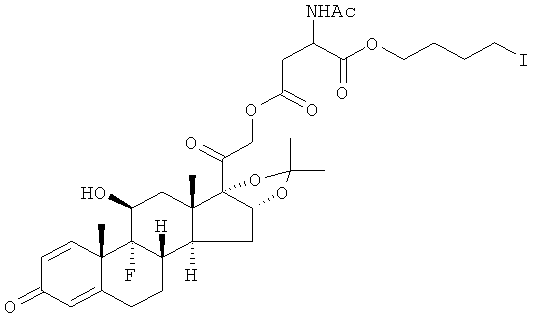
К раствору соединения М (0,55 г, 0,76 ммоль) в ацетонитриле (18 мл) добавляют иодид натрия (0,45 г, 3,06 ммоль). Реакционную смесь нагревают до 120°С 60 минут под действием микроволнового излучения. Реакционную смесь охлаждают, фильтруют и удаляют растворитель при пониженном давлении, получая твердый продукт, который используют далее без какой-либо очистки.
О) 1-(2-((8S,9R,10S,11S,13S,14S,16R,17S)-9-фтор-11-гидрокси-16,17-((1-метилэтилиден)бис(окси))-10,13-диметил-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-17-ил)-2-оксоэтил)-1-(4-(нитроокси)бутил)2-ацетамидо пентандиоат
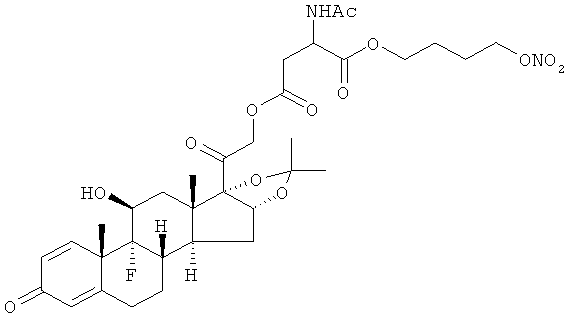
К раствору соединения N (0,60 г, 0,76 ммоль) в ацетонитриле (20 мл) добавляют нитрат серебра (0,51 г, 3,06 ммоль). Реакционную смесь нагревают до 120°С в течение 5 минут под действием микроволнового излучения. Полученную смесь охлаждают, фильтруют и удаляют растворитель при пониженном давлении. Остаток очищают с помощью флэш-хроматографии (Biotage System, column FLASH 25+M™ KP-Sil, элюент: градиент н-гексан/этил ацетат 4/6 (60 мл) до этил ацетат 100% 480 мл, этил ацетат (120 мл)). Получают 0,40 г продукта.
1H-NMR: (ДМСО): 8.45 (1Н, d); 7.26 (1Н, d); 6.22 (1H, dd); 6.00 (1H, s); 5.48 (1H, m); 5.12 (1H, dd), 4.84-4.76 (3H, m); 4.52 (2H, t); 4.20 (1H, m), 4.06 (2H, m); 2.87 (1H, dm); 2.75-2.48 (3H, m); 2.10-1.75 (4H, m); 1.82 (3H, s); 1.50-1-70 (7H, m); 1.47(3H, s); 1.33 (4H, m); 1.15 (3H, s); 0.83 (3H, s).
Пример 13
Синтез 2-((8S,9R,10S,11S,3S,14S,16S,17R)-9-фтор-11,17-дигидрокси-10,13,16-триметил-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-17-ил)-2-оксоэтил 3-(6-(нитроокси)гексанамидо) пропаноата
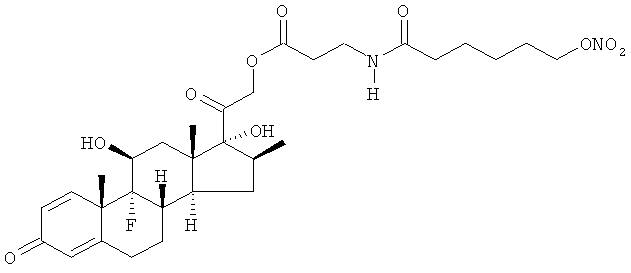
Соединение синтезируют, используя процедуру, описанную в примере 1, исходя из бетаметазона, Вос-бета-аланина и пентафторфенолового эфира 6-нитрооксигексановой кислоты.
1H-NMR: (ДМСО), δ: 7.88 (1Н, t); 7.29 (1H, d); 6.22 (1H, dd); 6.01 (1H, s); 5.36 (1H, s); 5.31 (1H, d); 5.01 (1H, d); 4.84 (1H, d); 4.50 (2H, t); 4.15 (1H, sb); 3.48-3.25 (2H, m); 2.75-2.25 (7H, m); 2.20-2.00 (4H, m); 1.99-1.75 (4H, m); 1.71-1.61 (2H, m); 1.57-1.48 (5H, m); 1.42-1.27 (2H, m); 1.01 (3H, d); 0.90 (3H, s).
Пример 14
Синтез 2-((8S,9R,10S,11S,13S,14S,16R,17S)-9-фтор-11-гидрокси-16,17-диметокси-10,13-((1-метилэтилиден)бис(окси))-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-17-ил)-2-оксоэтил-3-(6-(нитроокси)гексанамидо)пропаноата
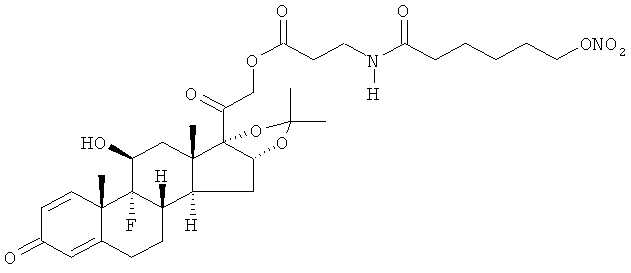
Соединение синтезируют, используя процедуру, описанную в примере 1, исходя из триамцинолон ацетонида, Вос-бета-аланина и пентафторфенолового эфира 6-нитрооксигексановой кислоты.
1H-NMR: (ДМСО), δ: 8.31 (1H, t); 7.30 (1H, d); 6.24 (1H, dd); 6.01 (1H, s); 5.49 (1H, d); 5.25 (1H, d); 4.86 (1H, d); 4.75 (1H, d); 4.50 (2H, t); 4.19 (1H, sb); 3.93 (2H, m); 2.75-2.25 (2H, m); 2.15 (2H, t); 2.10-1.75 (3H, m); 1.75-1.45 (7H, m); 1.47 (3H, s); 1.40-1.20 (6H, m); 1.17 (5H, m); 0.80 (3H, s);
Пример 15
Синтез 2-((6S,8S,9R,10S,11S,13S,14S,16R,17S)-6,9-дифтор-1-гидрокси-16,17-((1-метилэтилиден)бис(окси))-10,13-диметил-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-17-ил)-2-оксоэтил-3-(6-(нитроокси)гексанамидо)пропаноата
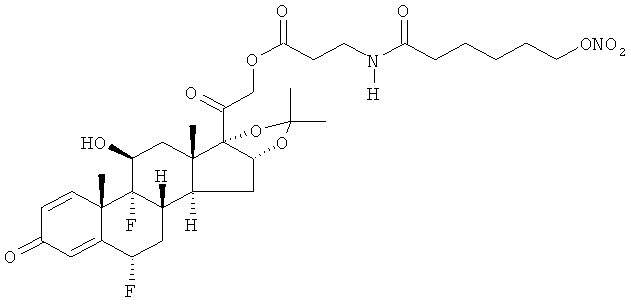
Соединение синтезируют, используя процедуру, описанную в примере 1, исходя из фторцинолон ацетонида, Вос-бета-аланина и пентафторфенолового эфира 6-нитрооксигексановой кислоты.
1H-NMR: (ДМСО), δ: 7.91 (1Н, t); 7.27 (1H, d); 6.30 (1H, dd); 6.11 (1H, s); 5.75-5.50 (2H, m) / 5.16 (1H, d); 4.85-4.90 (1H, m); 4.76 (1H, d); 4.61-4.48 (2H, t); 4.22 (1H, sb); 3.40-3.25 (3H, m) / 2.70-2.50 (4H, m); 2.40-2.30 (1H, m); 2.15-1.93 (2H, m); 1.80-1.45 (10Н, m); 1.41-1.28 (5H, m); 1.21 (3H, s); 0.82 (3H, s).
Пример 16
Синтез 4-(2-((8S,9R,10S,11S,13S,14S,16R,17S)-9-фтор-11-гидрокси-16,17-((1-метилэтилиден)бис(окси))-10,13-диметил-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-17-ил)-2-оксоэтил)-1-(4-(нитроокси)бутил)2-(6-(нитроокси)гексанамидо)сукцината
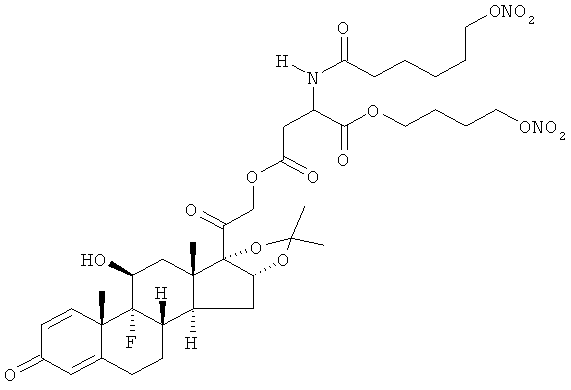
Р) 1-Аллил 4-(2-((8S,9R,10S,11S,13S,14S,16R,17S)-9-фтор-11-гидрокси-16,17-((1-метилэтилиден)бис(окси))-10,13-диметил-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-17-ил)-2-оксоэтил)2-(трет-бутоксикарбонил амино) сукцинат
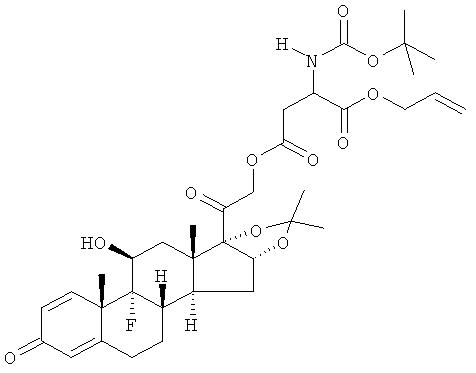
К раствору триамцинолон ацетонида (3,0 г, 6,9 ммоль) в дихлорметане (100 мл) добавляют 4-(аллилокси)-3-(трет-бутоксикарбониламино)-4-оксобутановую кислоту (1,88 г, 6,9 ммоль) и DMAP (кат. количество). Реакционную смесь охлаждают при 0°С и добавляют EDAC (1,7 г, 8,97 ммоль). Реакционную смесь перемешивают при комнатной температуре 12 часов. Растворитель испаряют под вакуумом. Остаток очищают с помощью флэш-хроматографии (Biotage System, column FLASH 40+M™ KP-Sil, элюент: градиент н-гексан/этил ацетат 8/2 (300 мл) до н-гексан/этил ацетат 4/6 900 мл, n-гексан/этил ацетат 4/6 (300 мл)). Получают 4,16 г продукта.
Q) 1-Аллил 4-(2-((8S,9R,10S,11S,13S,14S,16R,17S)-9-фтор-11-гидрокси-16,17-((1-метилэтилиден)бис(окси))-10,13-диметил-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-17-ил)-2-оксоэтил)2-(амино)сукцинат гидрохлорид
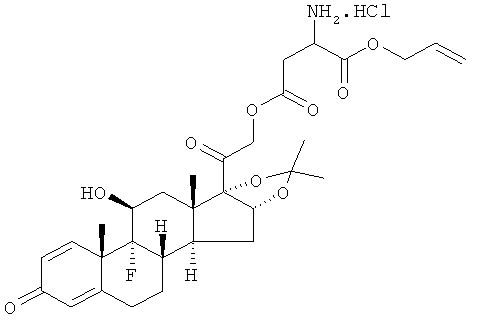
Раствор соединения Р (1,0 г, 1,45 ммоль) в дихлорметане (28 мл) перемешивают при комнатной температуре. В течение 25 минут в раствор барботируют газообразный HCl. Упаривают растворитель под вакуумом с получением твердого продукта, который используют без какой-либо очистки.
R) 1-Аллил 4-(2-((8S,9R,10S,11S,13S,14S,16R,17S)-9-фтор-11-гидрокси-16,17-((1-метилэтилиден)бис(окси))-10,13-диметил-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-17-ил)-2-оксоэтил)-2-(6-(нитроокси)гексанамидо) сукцинат
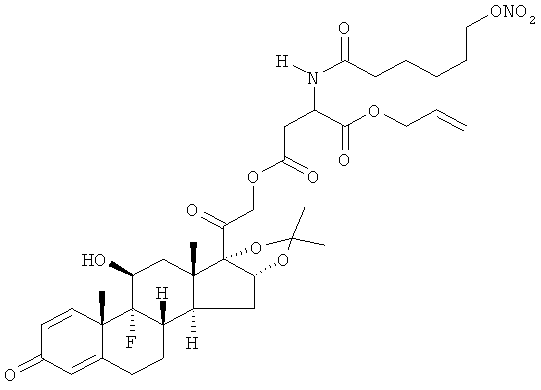
К раствору соединения Q (0,91 г, 1,45 ммоль) в дихлорметане (100 мл) добавляют DMAP (0,26 г, 2,17 ммоль) и пентафторфеноловый эфир 6-нитрооксигексановой кислоты (0,49 г, 1,45 ммоль). Реакционную смесь перемешивают при комнатной температуре 12 часов. Растворитель испаряют под вакуумом. Остаток очищают с помощью флэш-хроматографии (Biotage System, column FLASH 40+M™ KP-Sil, элюент: градиент n-гексан/этил ацетат 1/1 (150 мл) до этил ацетат 900 мл, этил ацетат (450 мл)).
Получают 0,64 г продукта.
S) 4-(2-((8S,9R,10S,11S,13S,14S,16R,17S)-9-Фтор-11-гидрокси-16,17-((1-метилэтилиден)бис(окси))-10,13-диметил-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-17-ил)-2-оксоэтил)-2-(6-(нитроокси)гексанамидо)-4-оксобутановая кислота
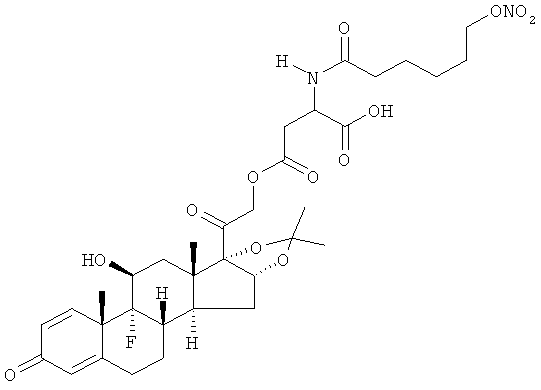
К раствору соединения R (0,58 г, 0,77 ммоль) в дихлорметане (20 мл) добавляют 5,5-диметил-1,3-циклогександион (0,13 г, 0,97 ммоль), трифенилфосфин (0,30 г, 1,16 ммоль) и тетракис(трифенилфосфин) палладия (0,045 г, 0,039 ммоль). Реакционную смесь перемешивают при комнатной температуре 12 часов. Растворитель испаряют под вакуумом. Остаток очищают с помощью флэш-хроматографии (Biotage System, column FLASH 40+M™ KP-Sil, элюент: н-гексан/ацетон/уксусная кислота 4/6/0,1%).
Получают 0,31 г продукта.
Т) 4-(2-((8S,9R,10S,11S,13S,14S,16R,17S)-9-фтор-11-гидрокси-16,17-((1-метилэтилиден)бис(окси))-10,13-диметил-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-17-ил-оксоэтил)-1-(4-(хлор)бутил) 2-(6-(нитроокси)гексанамидо) сукцинат
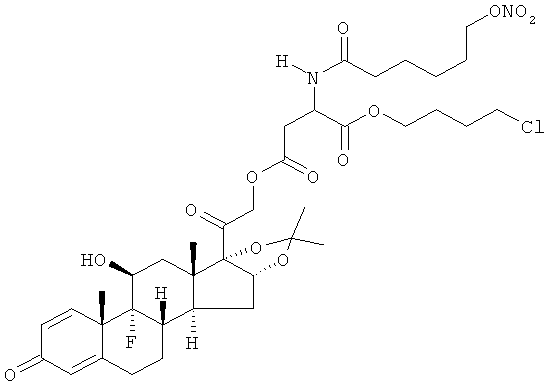
К раствору соединения S (0,33 г, 0,47 ммоль) в дихлорметане (20 мл) добавляют 4-хлорбутанол (0,06 мл, 0,61 ммоль) и DMAP (кат. количество). Реакционную смесь охлаждают при 0°С и добавляют EDAC (0,12 г, 0,62 ммоль). Реакционную смесь перемешивают при комнатной температуре 24 часа. Растворитель испаряют под вакуумом. Остаток очищают с помощью флэш-хроматографии (Biotage System, column FLASH 25+M™ KP-Sil, элюент: градиент н-гексан/этил ацетат 6/4 (60 мл) до н-гексан/этил ацетат 2/8 360 мл, н-гексан/этил ацетат 2/8 (240 мл)). Получают 0,25 г продукта.
U) 4-(2-((8S,9R,10S,11S,13S,14S,16R,17S)-9-фтор-11-гидрокси-16,17-((1-метилэтилиден)бис(окси))-10,13-диметил-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-17-ил)-2-оксоэтил)1-(4-(иод)бутил)2-(6-(нитроокси)гексанамидо)сукцинат
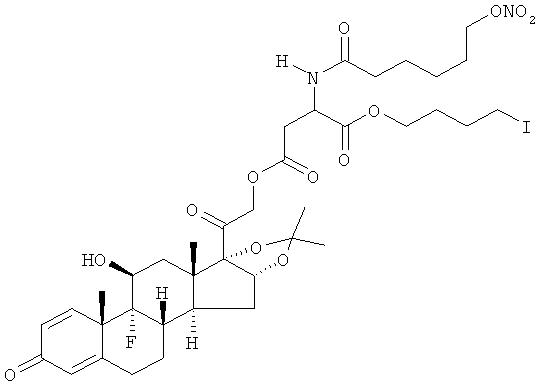
К раствору соединения Т (0,25 г, 0,31 ммоль) в ацетонитриле (10 мл) добавляют иодид натрия (0,18 г, 1,25 ммоль). Реакционную смесь нагревают до 120°С 60 минут под воздействием микроволнового излучения. Полученную смесь охлаждают, фильтруют и удаляют растворитель при пониженном давлении с получением твердого продукта, который используют далее без какой-либо очистки.
V) 4-(2-((8S,9R,10S,11S,13S,14S,16R,17S)-9-фтор-11-гидрокси-16,17-((1-метилэтилиден)бис(окси))-10,13-диметил-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-17-ил)-2-оксоэтил)-1-(4-(нитроокси)бутил) 2-(6-(нитроокси)гексанамидо) сукцинат

К раствору соединения U (0,27 г, 0,31 ммоль) в ацетонитриле (10 мл) добавляют нитрат серебра (0,21 г, 1,24 ммоль). Реакционную смесь нагревают до 120°С 5 минут под воздействием микроволнового излучения. Смесь охлаждают, фильтруют и удаляют растворитель при пониженном давлении. Остаток очищают с помощью флэш-хроматографии (Biotage System, column FLASH 25+M™ KP-Sil, элюент: градиент н-гексан/ацетон 8/2 (120 мл) до н-гексан/ацетон 55/45 480 мл, н-гексан/ацетон 55/45 (120 мл)). Получают 0,13 г продукта.
1H-NMR: (ДМСО), δ: 7.18 (1Н, d); 6.59 (1H, d); 6.32 (1H, dd); 6.13 (1H, s); 5.02-4.88 (4H, m); 4.51-4.40 (5H, m); 4.27-4.11 (2H, m) / 3.05 (1H, dd); 2.90 (1H, dd); 2.68-2.30 (4H, m); 2.27 (2H, t); 2.27-2.00 (2H, m); 1.90-1.40 (18H, m); 1.21 (3Н, s); 0.88 (3Н, s).
Пример 17
Синтез 1-(2,3-бис(нитроокси)пропил)4-(2-((9R,10S,11S,13S,16R,17S)-9-фтор-11-гидрокси-16,17-((1-метилэтилиден)бис(окси))-10,13-диметил-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-17-ил)-2-оксоэтил)-2-аминосукцината гидрохлорида
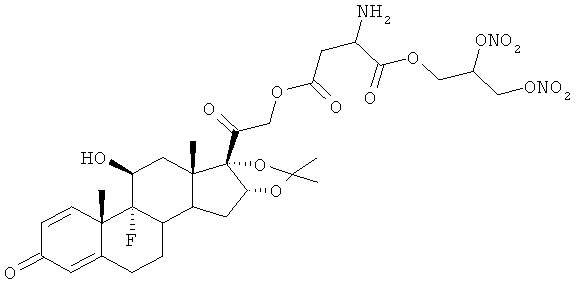
W) 1-Аллил-4-(4-нитрофенил)-2-(трет-бутоксикарбониламино)сукцинат
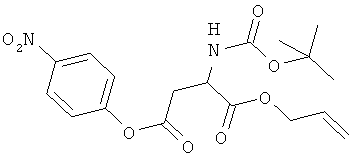
К раствору 4-(аллилокси)-3-(трет-бутоксикарбониламино)-4-оксобутановой кислоты (3,0 г, 11,0 ммоль) в дихлорметане (50 мл) добавляют 4-нитрофенол (1,4 г, 11,0 ммоль) и DMAP (кат. количество). Реакционную смесь охлаждают при 0°С и добавляют EDAC (2,85 г, 15,0 ммоль). Смесь перемешивают при комнатной температуре 12 часов. Под вакуумом испаряют растворитель. Остаток очищают флэш-хроматографией (Biotage System, column FLASH 65+M™ KP-Sil, элюент: градиент н-гексан/этилацетат 95/5 (450 мл) до н-гексан/этилацетат 6/4 4500 мл, н-гексан/этилацетат 6/4 (900 мл)). Получают 1,5 г продукта.
X) 1-(2,3-бис(нитроокси)пропил) 4-(4-нитрофенил) 2-(трет-бутоксикарбонил амино)сукцинат
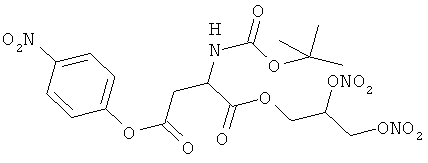
К раствору соединения W (1,5 г, 3,8 ммоль) в ацетонитриле (60 мл) добавляют нитрат серебра (0,63 г, 3,8 ммоль). Реакционную смесь охлаждают при -15°С и добавляют иод (0,96 г, 3,8 ммоль). Реакционную смесь перемешивают при 0°С 1 час. Добавляют нитрат серебра (1,27 г, 7,6 ммоль) и смесь перемешивают при 70°С 7 дней, добавляя каждый день нитрат серебра (0,96 г, 3,8 ммоль). Растворитель испаряют под вакуумом. Остаток очищают флэш-хроматографией (Biotage System, column FLASH 65+M™ KP-Sil, элюент: градиент н-гексан/этилацетат 95/5 (450 мл) до н-гексан/этилацетат 6/4 4500 мл, н-гексан/этилацетат 6/4 (900 мл)). Получают 0,54 г продукта.
Y) 1-(2,3-бис(нитроокси)пропил) 4-(2-((9R,10S,11S,13S,16R,17S)-9-фтор-11-гидрокси-16,17-((1-метилэтилиден)бис(окси))-10,13-диметил-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-17-ил)-2-оксоэтил)-2-(трет-бутоксикарбониламино)сукцинат
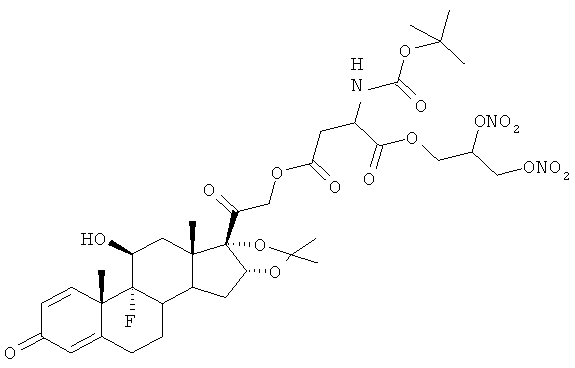
К раствору триамцинолон ацетонида (0,21 г, 0,5 ммоль) в дихлорметане (13 мл) добавляют соединение Х (0,26 г, 0,5 ммоль) и DMAP (0,06 г, 0,5 ммоль)). Реакционную смесь перемешивают при комнатной температуре 12 часов. Испаряют растворитель под вакуумом. Остаток очищают флэш-хроматографией (Biotage System, SNAP Cartridge silica 100 г, элюент: градиент н-гексан/этилацетат 88/12 (150 мл) до этилацетат 1500 мл, этилацетат (300 мл)). Получают 0,4 г продукта.
Z) 1-(2,3-бис(нитроокси)пропил) 4-(2-((9R,10S,11S,13S,16R,17S)-9-фтор-11-гидрокси-16,17-((1-метилэтилиден)бис(окси))-10,13-диметил-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3Н-циклопента[а]фенантрен-17-ил)-2-оксоэтил) 2-аминосукцинат гидрохлорид

Раствор соединения Y (0,4 г, 0,49 ммоль) в дихлорметане (8 мл) перемешивают при комнатной температуре. В течение 15 минут в раствор барботируют газообразный HCl. Под вакуумом испаряют растворитель. Остаток очищают флэш-хроматографией с обратной фазой (Biotage System, column FLASH 25+M™ KP-Sil, элюент: вода/ацетонитрил 1/1. Получают 0,13 г продукта.
1H-NMR: (ДМСО), δ: 7.30 (1Н, d); 6.23 (1H, dd); 6.02 (1H, s); 5.66 (1H, m); 5.49 (1H, m); 5.17 (1H, dd), 4.97 (1H, dd); 4.89-4.79 (3H, m); 4.48 (1H, dm); 4.38 (1H, dd), 4.20 (1H, m); 3.82 (1H, m); 2.78 (1H, dm); 2.68-2.49 (7H, m); 2.10-1.75 (3H, m); 1.54 (1H, m); 1.49 (5H, m); 1.35 (4H, m); 1.15 (3H, s); 0.83 (3H, s).
Изобретение относится к нитрооксипроизводным кортикостероидов общей формулы (I) и их фармакологически приемлемым солям или стереоизомерам, где R представляет остаток кортикостероида формулы (II), где:
R1 представляет ОН, R2 представляет СН3 или R1 и R2, взятые вместе, образуют группу формулы (III), R3 представляет Cl или F; где R1, R2, R3 и R4 могут быть присоединены к соответствующим атомам углерода стероидной структуры в положении α или β; при условии, что, когда R1 и R2 представляют группу формулы (III), тогда R3 представляет F и R4 представляет Н или F. Соединения полезны для лечения респираторных заболеваний, воспалительных заболеваний, дерматологических заболеваний и глазных заболеваний. 2 н. и 8 з.п. ф-лы.
1. 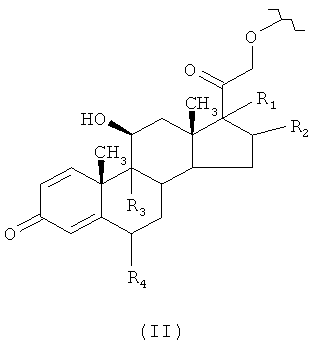
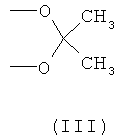
1. Соединения общей формулы (I) и их фармацевтически приемлемые соли или стереоизомеры
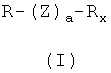
где R представляет остаток кортикостероида формулы (II):
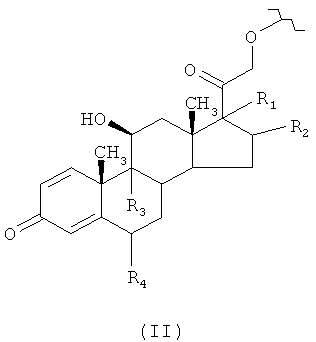
где R1 представляет ОН в положении α, R2 представляет -СН3 в положении β,
R3 представляет Cl в положении α и R4 представляет Н; или
R1 представляет ОН в положении α, R2 представляет -СН3 в положении β,
R3 представляет F в положении α и R4 представляет Н; или
R1 и R2 взятые вместе образуют группу формулы (III)
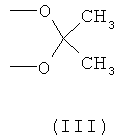
R3 представляет F и R4 представляет Н; R1, R2 и R3 находятся в положении α; или
R1 и R2 взятые вместе образуют группу формулы (III)

R3 и R4 представляют F; R1, R2, R3 и R4 находятся в положении α; а в формуле (I) представляет 0;
Rx выбран из:
(а2) -C(O)-CH(R′)-NH-(T′-Y-ONO2), где
R′ группы А1) выбран из Н, изобутила;
T′ представляет -С(О)-, -С(О)-Х′′, где X′′ представляет -S- или -О-;
или Rx выбран из
(a5) -RIb-CH(NHR4a)-C(O)-(T-Y-ONO2);
(а9) -RIb-CH(NH-T′-Y′-ONO2)-C(O)-(T-Y-ONO2) или
где RIb группы А10) выбран из -С(О)-СН2-, -С(О)-(СН2)2-, -С(О)-(СН2)4-;
R4a представляет Н или -С(О)СН3;
Т представляет -О-, -S-, -NR′- где R′ представляет Н или -СН3;
Т′ представляет -С(О)- или -С(О)-Х′′, где X′′ представляет -S- или -О-;
или Rx представляет
(b2) -C(O)-CH2-CH(R2)-NH-(T′-Y-ONO2),
где R2 группы В1) выбран из Н, СН3, изобутила, изопропила;
Т′ представляет -С(О)-, -С(О)-Х′′, где X′′ представляет -S- или -О-;
Y и Y′ каждый независимо выбран из
а)
- прямого или разветвленного C1-С10алкилена,
- прямого или разветвленного С1-С10алкилена, замещенного группой -ONO2.
2. Соединение формулы (I) и их фармацевтически приемлемые соли и стереоизомеры
где R представляет остаток кортикостероида формулы (II)

где R1 представляет ОН в положении α, R2 представляет -СН3 в положении β,
R3 представляет Cl в положении α и R4 представляет Н; или
R1 представляет ОН в положении α, R2 представляет -СН3 в положении β,
R3 представляет F в положении α и R4 представляет Н; или
R1 и R2 взятые вместе образую группу формулы (III)

R3 представляет F и R4 представляет Н; R2 и R3 находятся в положении α;
или
R1 и R2 взятые вместе образуют группу формулы (III)

R3 и R4 представляют F, R2, R3 и R4 находятся в положении α;
а представляет 1 и Z представляет -С(О)-;
Rx представляет
(a5) -RIb-CH(NHR4a)-C(O)-(T-Y-ONO2)
(а9) -RIb-CH(NH- Т′-Y′-ONO2)-C(O)-(T-Y-ONO2) или
где RIb группы А8) представляет [-(4-О)-(С6Н4)]-СН2-,
R4a представляет Н или -С(О)СН3;
Т представляет -О-, -S-, -NR′-, где R′ представляет Н или прямой или разветвленный С1-С4алкил;
Т′ представляет -С(О)- или -С(О)-Х′′, где X′′ представляет -S- или -О-;
Y и Y′ каждый независимо выбран из
а)
- прямой или разветвленный С1-С10алкилен,
- прямой или разветвленный C1-С10алкилен, замещенный -ONO2 группой.
3. Соединение формулы (I) по п.1, где
Rx представляет
(а2) -C(O)-CH(R′)-NH-(T-Y-ONO2),
где R1 представляет Н и Т′′ представляет -С(О)-.
4. Соединение формулы (I) по п.1, где
Rx представляет
(а5) -RIb-CH(NHR4a)-C(O)-(T-Y-ONO2);
(a9) -RIb-CH(NH-T′-Y′-ONO2)-C(O)-(T-Y-ONO2), где
RIb представляет -О-СН2-,
R4a представляет Н или -С(О)СН3 и
Т′ представляет -С(O)-.
5. Соединение формулы (I) по п.2,
где Т выбран из -О- и Т′′ представляет -С(О)-.
6. Соединение формулы (I) по п.1,
где Rx представляет
(b2) -C(O)-CH2-CH(R2)-NH-(T′-Y-ONO2),
где R2 представляет Н и Т′′ представляет -С(О)-.
7. Соединение формулы (I) по п.1 и его фармацевтически приемлемые соли или стереоизомеры, выбранное из группы, состоящей из:
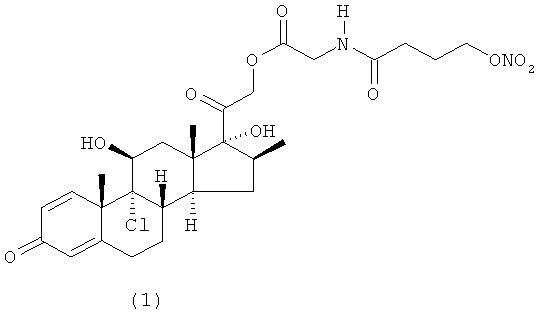
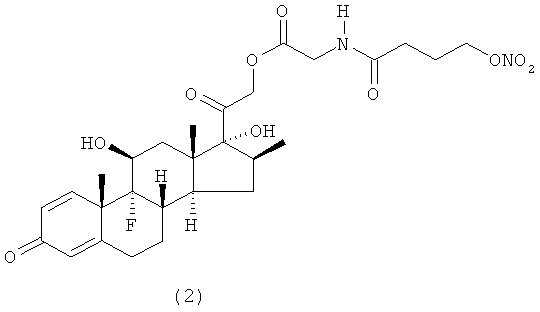
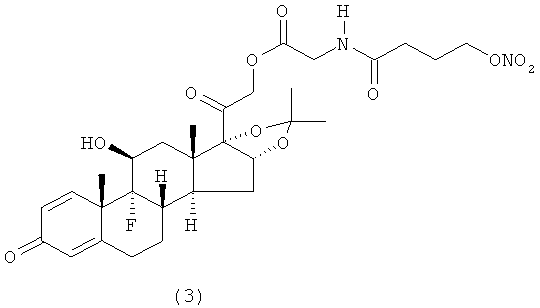
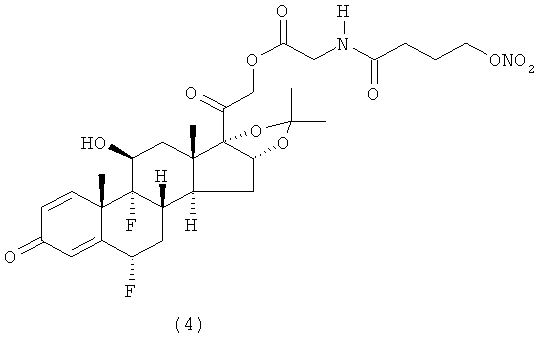
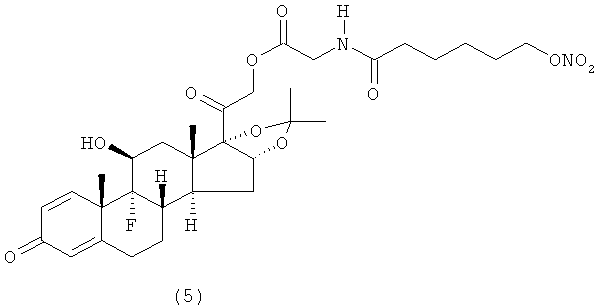
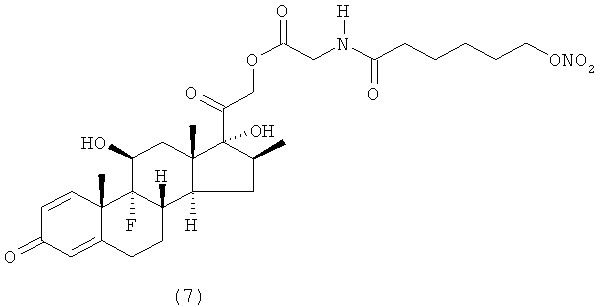
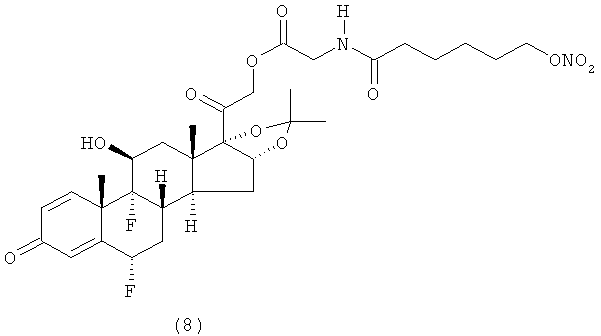
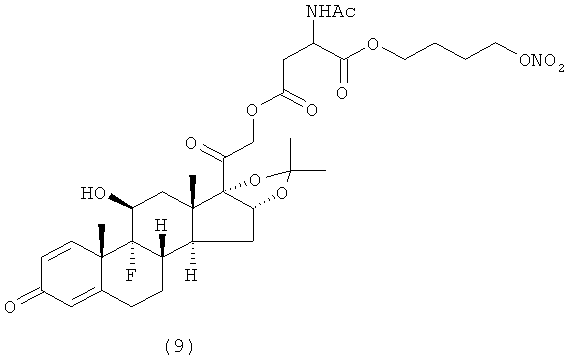
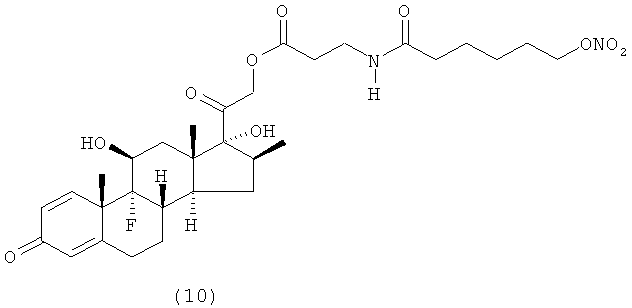
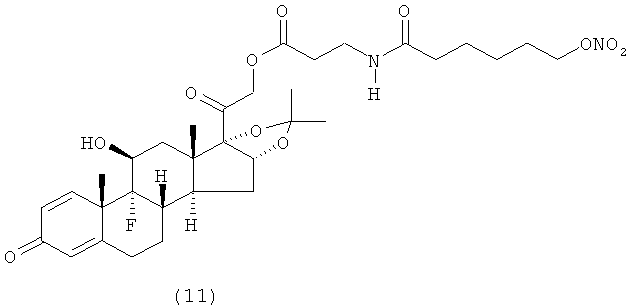

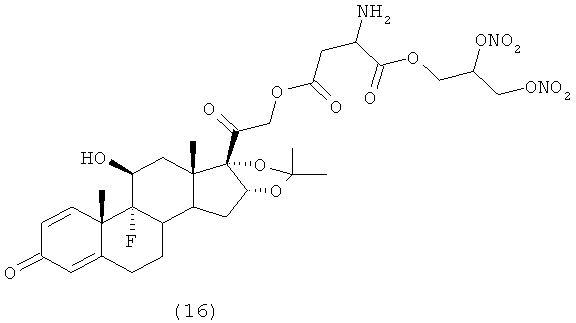
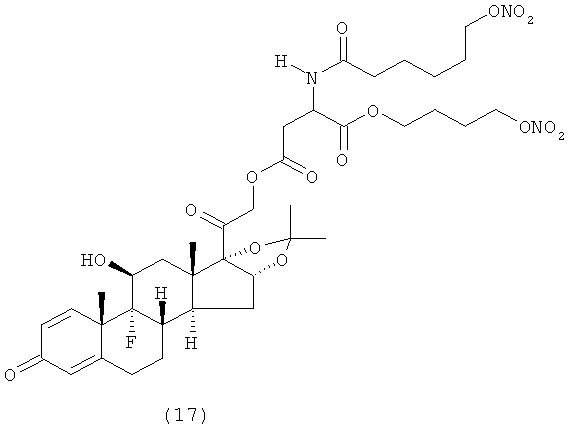
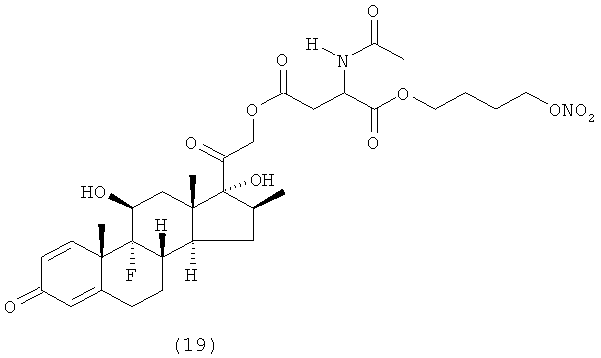
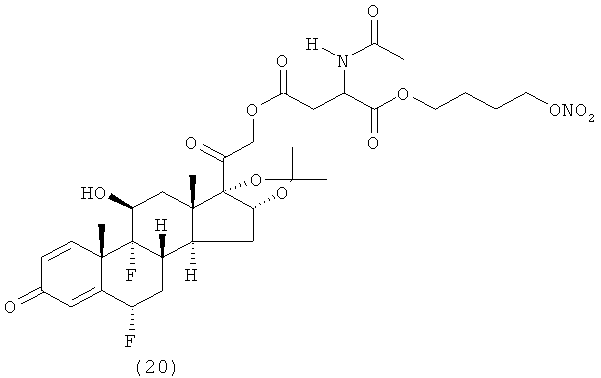
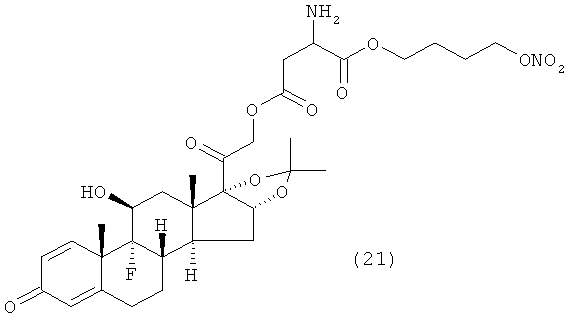
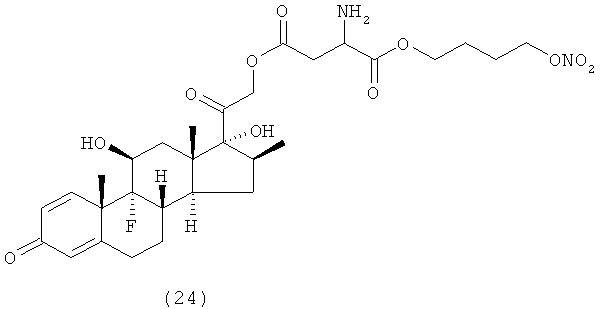
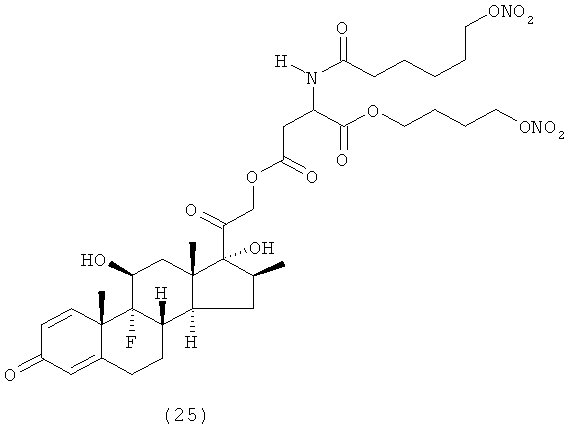
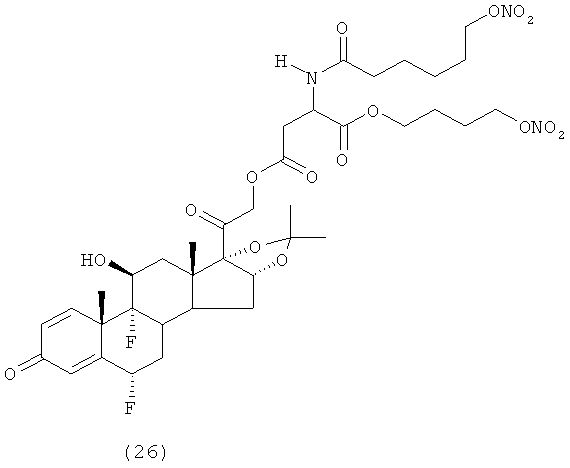
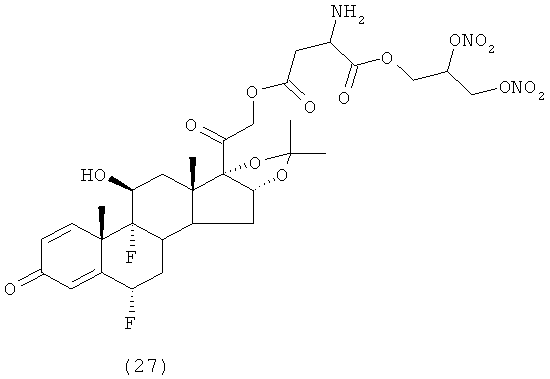
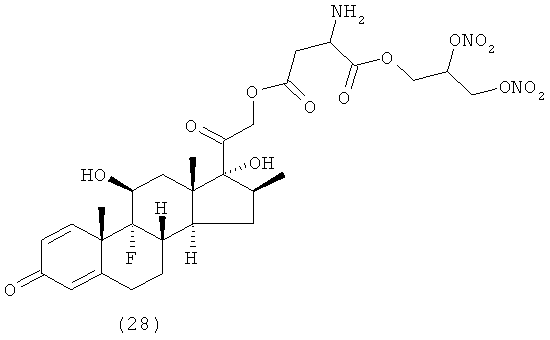
8. Соединение формулы (1) по п.2 и его фармацевтически приемлемые соли и стереоизомеры, выбранное из группы, состоящей из
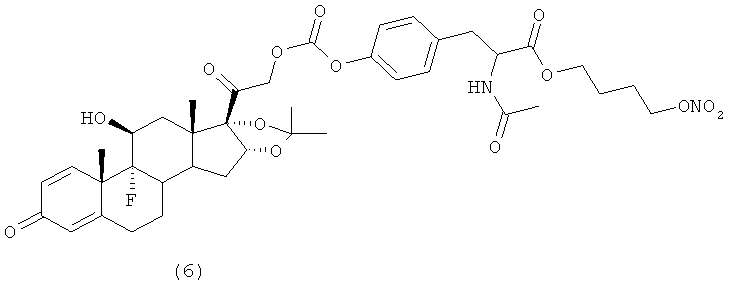

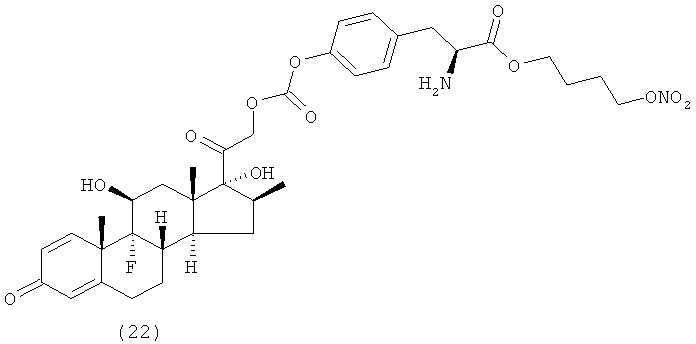
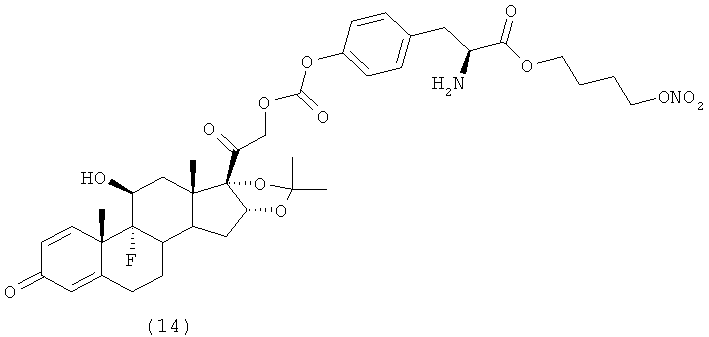
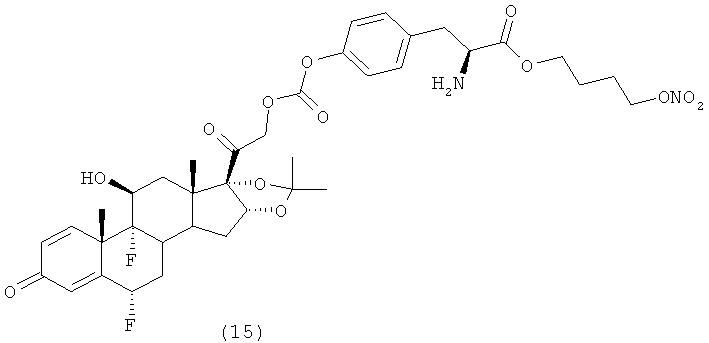
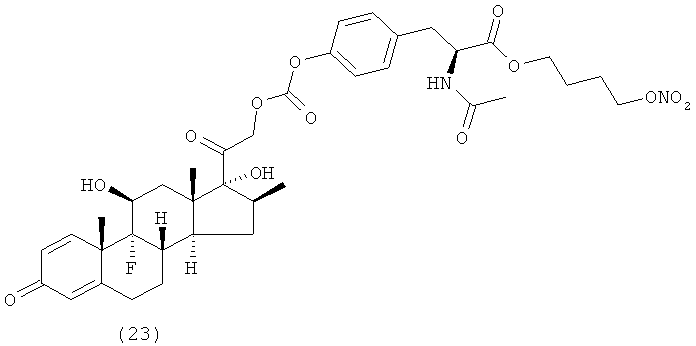
9. Соединение формулы (1) по пп.1-8 для применения для лечения глазных заболеваний.
10. Соединение по п.9 для применения для лечения глазной гипертонии, возрастной макулярной дистрофии, диабетического отека желтого пятна, диабетической ретинопатии, гипертонической ретинопатии и ретинальной васкулопатии.
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| BARALDI P.G | |||
| et al // J | |||
| Med | |||
| Chem | |||
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| WO 2000061604 А, 19.10.2000 | |||
| US 3494941 A, 10.02.1970. | |||
Авторы
Даты
2012-02-20—Публикация
2008-01-28—Подача