Область техники, к которой относится изобретение
Настоящее изобретение относится к фармацевтическим композициям и способам лечения, включающим введение больным, нуждающимся в этом, комбинации 2-алкилиденового производного 19-нор-витамина D и бисфосфоната. В частности, настоящее изобретение относится к фармацевтическим композициям и способам лечения, включающим введение больным, нуждающимся в этом, терапевтически эффективного количества 2-метилен-19-нор-20(S)-1α,25-дигидроксивитамина D3 и бисфосфоната.
Уровень техники
Витамин D представляет собой общий термин, который обозначает группу стероидных молекул. Активная форма витамина D, которая называется 1,25-дигидроксивитамин D3 (1,25-дигидроксихолекальциферол), образуется в результате биосинтеза в организме человека путем превращения 7-дегидрохолестерина в витамин D3 (холекальциферол). Указанное превращение происходит в коже человека, и для него необходимо УФ-облучение (обычно облучение солнечным светом). Затем витамин D3 метаболизирует в печени в 25-гидроксивитамин D3 (25-гидроксихолекальциферол), который далее метаболизирует в почках в активную форму витамина D - 1,25-дигидроксивитамин D3. 1,25-дигидроксивитамин D3 распределяется в организме, где он связывается с внутриклеточными рецепторами витамина D.
Активная форма витамина D представляет собой гормон, который, как известно, участвует в минеральном метаболизме и росте костей и способствует всасыванию кальция в кишечнике.
Аналоги витамина D описаны в патенте США № 5843928, выданном 1 декабря 1998 г. Описанные соединения представляют собой 2-алкилиденовые производные 19-нор-витамина D и характеризуются низкой активностью в отношении транспорта кальция в кишечнике и высокой активностью в отношении мобилизации кальция из костей по сравнению с 1,25-дигидроксивитамином D3.
Настоящее изобретение относится к способам лечения, в которых используют комбинацию 2-алкилиденового производного 19-нор-витамина D и, конкретно, соединения 2-метилен-19-нор-20(S)-1α,25-дигидроксивитамина D3 (также известного как 2MD) и бисфосфоната. Настоящее изобретение также относится к фармацевтической композиции, содержащей 2-алкилиденовое производное 19-нор-витамина D, конкретно, соединение 2-метилен-19-нор-20(S)-1α,25-дигидроксивитамин D3 (также известное как 2MD) и бисфосфонат.
Сущность изобретения
Настоящее изобретение относится к фармацевтическим композициям, включающим соединение 2-метилен-19-нор-20(S)-1α,25-дигидроксивитамин D3 и бисфосфонат. Конкретные варианты осуществления изобретения представляют собой фармацевтические композиции, включающие соединение 2-метилен-19-нор-20(S)-1α,25-дигидроксивитамин D3 и бисфосфонат, в которых бисфосфонат выбран из тилудроната, алендроната, золедроната, ибандроната, ризедроната, этидроната, клодроната или памидроната. Более конкретно, настоящее изобретение относится к фармацевтическим композициям, включающим соединение 2-метилен-19-нор-20(S)-1α,25-дигидроксивитамин D3 и алендронат или ризендронат. Настоящее изобретение также относится к способу лечения старческого остеопороза, постклимактерического остеопороза, переломов костей, трансплантатов костей, рака груди, рака простаты, ожирения, остеопении, мужского остеопороза, слабости, повреждений мышц и саркопении, способу, включающему введение больному, который нуждается в этом, терапевтически эффективного количества 2-метилен-19-нор-20(S)-1α,25-дигидроксивитамина D3 и терапевтически эффективного количества бисфосфоната. Конкретный вариант осуществления способа лечения представляет собой способ, описанный выше, в котором вводят перорально 2-метилен-19-нор-20(S)-1α,25-дигидроксивитамин D3 и бисфосфонат. Дополнительными вариантами осуществления способа лечения являются способы лечения, как описано выше, в которых 2-метилен-19-нор-20(S)-1α,25-дигидроксивитамин D3 и бисфосфонат вводят парентерально или трансдермально. Дополнительными вариантами осуществления настоящего изобретения являются способы лечения, в которых бисфосфонат выбран из тилудроната, алендроната, золедроната, ибандроната, ризедроната, этидроната, клодроната или памидроната. Конкретными вариантами осуществления настоящего изобретения являются способы лечения, в которых бисфосфонат представляет собой алендронат или ризедронат.
Подробное описание изобретения
Настоящее изобретение относится к фармацевтическим композициям и способам лечения метаболических костных заболеваний, старческого остеопороза, постклимактерического остеопороза, остеопороза, вызванного стероидами, остеопороза низкого ремоделирования кости, остеомаляции, нефрогенной остеодистрофии, псориаза, рассеянного склероза, сахарного диабета, отторжения трансплантата «хозяином», отторжения трансплантата, ревматоидного артрита, астмы, переломов костей, костного трансплантата, акнэ, аллопеции, сухости кожи, недостаточного салоотделения, морщин, гипертензии, лейкемии, рака толстой кишки, рака груди, рака простаты, ожирения, остеопении, мужского остеопороза, гипогонадизма, андропаузы, слабости, повреждения мышц, саркопении, остеосаркомы, гипокальциемической тетании, гипопаратиреоза, рахитов, дефицита витамина D, анорексии, пониженной костной массы в результате активных занятий спортом и для увеличения максимума костной массы в отрочестве и профилактики вторичного перелома костей тазобедренного сустава, с помощью комбинации 2-алкилиденового производного 19-нор-витамина D и бисфосфоната.
В предпочтительном варианте осуществления настоящее изобретение относится к способу лечения метаболических костных заболеваний, старческого остеопороза, постклимактерического остеопороза, остеопороза, вызванного стероидами, остеопороза низкого ремоделирования кости, остеомаляции, нефрогенной остеодистрофии, псориаза, рассеянного склероза, сахарного диабета, отторжения трансплантата «хозяином», отторжения трансплантата, ревматоидного артрита, астмы, переломов костей, костного трансплантата, акнэ, аллопеции, сухости кожи, недостаточного салоотделения, морщин, гипертензии, лейкемии, рака толстой кишки, рака груди, рака простаты, ожирения, остеопении, мужского остеопороза, гипогонадизма, андропаузы, слабости, повреждения мышц, саркопении, остеосаркомы, гипокальциемической тетании, гипопаратиреоза, рахитов, дефицита витамина D, анорексии, пониженной костной массы в результате активных занятий спортом, увеличения максимума костной массы в отрочестве и профилактики вторичного перелома костей тазобедренного сустава, в котором используют комбинацию 2-алкилиденового производного 19-нор-витамина D и бисфосфоната.
В предпочтительном варианте осуществления изобретения способы лечения, в которых используют указанную комбинацию, представляют собой способы лечения старческого остеопороза, постклимактерического остеопороза, переломов костей, костного трансплантата, рака груди, рака простаты, ожирения, остеопении, мужского остеопороза, слабости, повреждения мышц и саркопении.
Остеопения представляет собой утоньшение костей, но в меньшей степени, чем при остеопорозе, и является стадией, предшествующей истинному остеопорозу. Всемирная организация здравоохранения разработала диагностические категории, основанные на плотности костной массы (BMD), которые указывают, что человек имеет нормальную костную массу, что он болен или остеопенией, или остеопорозом. Нормальная плотность кости соответствует плотности кости молодого взрослого человека ± одно стандартное отклонение (+1 или -1). Остеопения (пониженная костная масса) определяется как плотность костной массы ниже значения для молодого взрослого человека на 1-2,5 стандартного отклонения (от -1 до -2,5), и остеопороз диагностируется, когда плотность костной массы ниже значения плотности для молодого взрослого человека на 2,5 стандартных отклонения (или больше) (>-2,5).
Гипогонадизм обычно определяют как неполноценную гонадную функцию, что проявляется в недостаточности гаметогенеза и/или секреции гонадных гормонов, которая может приводить к задержке половой зрелости и/или репродуктивной недостаточности. Существует три основных типа гипогонадизма: 1) первичный гипогонадизм; 2) вторичный гипогонадизм и 3) резистентный гипогонадизм. При первичном гипогонадизме повреждение клеток Лейдига уменьшает продуцирование андрогена. При вторичном гипогонадизме расстройство гипоталамуса или гипофиза уменьшает секрецию гонадотропина, а в случае резистентного гипогонадизма ответ организма на действие андрогена неадекватен.
Рахит представляет собой детское заболевание, включающее размягчение и ослабление костей, причиной рахита является прежде всего недостаток витамина D, кальция и/или фосфата.
Анорексия представляет собой заболевание, которое имеет следующие характеристики: отказ сохранять массу тела на уровне, минимально нормальном для соответствующего возраста и роста, или выше нормального (например, потеря массы, приводящая к сохранению массы, менее 85% от ожидаемой; или не достижение ожидаемого увеличения массы во время периода роста, что приводит к массе тела, составляющей менее 85% от ожидаемой); сильный страх прибавления в весе или боязнь ожирения, даже при недостаточной массе тела; и беспокойство по поводу имеющегося состояния массы или формы тела, чрезмерное влияние массы или формы тела на самооценку или отрицание серьезности имеющейся пониженной массы тела. Соединения и комбинации по настоящему изобретению можно использовать для лечения анорексии и для лечения потери костной массы, связанной с анорексией.
Еще одним состоянием, которое можно лечить с помощью соединений и комбинаций по настоящему изобретению, является потеря костной массы из-за интенсивных занятий спортом, особенно у женщин. Энергичное участие в тренировках и занятиях спортом может привести к потере костной массы, которая обычно сопровождается аменореей у женщин. У мужчин, интенсивно занимающихся спортом, также отмечается потеря костной массы.
Андропауза (также называемая мужской менопаузой или виропаузой) представляет собой естественное явление у мужчин, которое обычно имеет место в возрасте сорока-сорока пяти лет. Андропауза связана со снижением уровня гормона тестостерона. Из-за понижения уровня тестостерона у мужчин в период андропаузы могут наблюдаться различные изменения и состояния, включающие понижение энергии и силы, повышенное образование жира в организме, остеопороз, депрессию, снижение остроты ума, неспособность поддерживать мускулатуру, сердечно-сосудистые заболевания, атеросклероз, пониженное либидо, уменьшение силы оргазма, эректильные дисфункции, повышенную раздражительность и ноющие и тугоподвижные суставы, особенно суставы рук и ног. Кроме того, мужчины в период андропаузы и пережившие андропаузу могут иметь гинекомастию, липидные нарушения в сыворотке крови, включающие гиперхолестеринемию, пониженную реактивность сосудов, гипогонадизм и доброкачественную гиперплазию простаты.
Слабость характеризуется прогрессирующей и неослабевающей потерей массы скелетных мышц, что в результате приводит к повышенному риску травм при падении, трудному выздоровлению после болезней, продлению госпитализации и длительной инвалидности, при которой требуется помощь в самообслуживании. Уменьшение мышечной массы, физической силы и физической работоспособности приводит к понижению качества жизни, потере самостоятельности и смерти. Слабость обычно ассоциируется со старением, но может также происходить в результате потери массы и уменьшения физической силы, обусловленных другими факторами, такими, как вызванная болезнью кахексия, иммобилизация или саркопения, индуцированная лекарствами. Еще одним термином, используемым для обозначения слабости, является термин «саркопения», который представляет собой общее обозначение для потери массы скелетных мышц или их качества. Примеры свойств скелетных мышц, которые вносят вклад в общее их качество, включают сократительную способность, размер и тип волокон, утомляемость, восприимчивость к действию гормонов, усвояемость глюкозы/метаболизм и плотность капилляров. Ухудшение качества мышц, даже при отсутствии потери мышечной массы, может приводить к потере физической силы и снижению работоспособности.
Термин «поражение мышц» здесь используется для обозначения поражения любой мышечной ткани. Поражение мышц может быть вызвано физической травмой мышечной ткани в результате несчастных случаев, спортивных травм, эндокринных расстройств, заболеваний, ранений или хирургических операций. Способы по настоящему изобретению применимы для лечения поражений мышц.
У женщин преклонного возраста остеопороз определяют по пиковому значению костной массы, приобретенной в период от юности к зрелости, сохранению такого значения пиковой костной массы в предклимактерический период и по скорости потери костной массы в период после менопаузы. Факторы, определяющие пиковое значение костной массы включают генетические факторы, факторы, относящиеся к питанию и окружающей среде, и физические нагрузки (упражнения). Таким образом, для профилактики развития остеопороза в более поздний период жизни желательно в юности увеличивать пиковую костную массу для достижения максимальной массы скелета. Подобно этому увеличение пиковой костной массы у мужчин в зрелом возрасте также желательно.
На заболеваемость и смертность больных существенное влияние оказывают такие переломы, как перелом шейки бедра. Лишь немногие больные с переломом шейки бедра рассматривают профилактические меры, направленные на уменьшение риска переломов в дальнейшем. В настоящее время 10-13% больных пациентов позже получают и второй перелом шейки бедра. Из пациентов, перенесших второй перелом шейки бедра, лишь немногие сохраняют способность передвигаться самостоятельно, такую как после первого перелома (53 и 91%, соответственно, P<0,0005) [Pearse E.O. et al., Injury, 2003, 34(7), 518-521]. После второго перелома шейки бедра будущая самостоятельность больного в повседневной жизни больного определяется степенью его подвижности. У больных более преклонного возраста и больных, в истории болезни которых отмечались многочисленные падения, промежуток времени между переломами короче. Второй перелом шейки бедра существенным образом влияет на подвижность пациента и его самостоятельность в повседневной жизни. Следовательно, существует потребность в новых методах профилактики второго перелома шейки бедра.
Остеосаркома представляет собой относительно распространенную крайне злокачественную опухоль первичной кости, которая имеет склонность к образованию метастаз в легких. Остеосаркома чаще всего встречается у лиц от 10 до 20 лет, хотя она может появиться в любом возрасте. Приблизительно половина всех остеосарком локализуется в области колена, остеосаркома может возникнуть в любой кости. Боль и опухоль являются обычными симптомами остеосаркомы. Обычно остеосаркому лечат хирургическими методами в сочетании с химиотерапией. Для лечения остеосаркомы можно использовать химиотерапию до операции или после операции, применяя такие препараты, как метотрексан, доксорубицин, цисплатин или карбоплатин.
Гипопаратиреоз представляет собой склонность к гипокальциемии, часто связанную с хронической тетанией, возникающей из-за недостатка гормонов, и характеризуется низким содержанием кальция и высоким содержанием фосфора в сыворотке крови. Гипопаратиреоз - самостоятельность больного в повседневной жизни обычно сопровождается случайным удалением или поражением нескольких околощитовидных желез во время резекции щитовидной железы (тиреоидэктомии). Транзиторный гипопаратиреоз обычно наблюдается после субтотальной тиреоидэктомии и постоянно имеет место менее чем в 3% тиреоидэктомий, выполненных опытными специалистами.
Гипокальцемическая тетания представляет собой форму тетании, которая возникает в результате гипокальциемии. Гипокальциемия характеризуется снижением общей концентрации кальция в плазме ниже 8,8 мг/дл (миллиграммов/децилитр) при нормальной концентрации белков в плазме. Тетания может быть явной со спонтанными симптомами или латентной. Явная тетания характеризуется сенсорными симптомами, такими как парестезия губ, языка, пальцев и ступней, карпопедальный спазм, которые могут быть продолжительными и болезненными; общая мышечная боль и спазм мускулатуры лица. Для выявления латентной тетании требуются провокационные пробы, и она обычно имеет место при менее сильно пониженных концентрациях кальция в плазме, таких как 7-8 мг/дл. У животных также наблюдают гипокальцемическую тетанию по данным ветеринарной практики. Например, гипокальцемическая тетания у лошадей представляет собой редко встречающееся состояние, связанное с резким понижением содержания ионов кальция в сыворотке крови и иногда с изменениями концентраций магния и фосфата в сыворотке крови. Тетания имеет место после продолжительной физической нагрузки или транспортировки (транспортная тетания) и у лактирующих кобыл (лактационная тетания). Признаки различны и относятся к повышенной нервно-мышечной раздражительности.
Настоящее изобретение также относится к фармацевтическим композициям для лечения метаболического заболевания костей, старческого остеопороза, постклимактерического остеопороза, остеопороза, вызванного стероидами, остеопороза с низкой скоростью метаболизма, остеомаляции, нефрогенной остеодистрофии, псориаза, рассеянного склероза, сахарного диабета, отторжения трансплантата «хозяином», отторжения трансплантата, ревматоидного артрита, астмы, переломов костей, костного трансплантата, акнэ, аллопеции, сухости кожи, недостаточного салоотделения, морщин, гипертензии, лейкемии, рака толстой кишки, рака груди, рака простаты, ожирения, остеопении, мужского остеопороза, гипогонадизма, андропаузы, слабости, повреждения мышц, саркопении, остеосаркомы, гипокальциемической тетании, гипопаратиреоза, рахитов, недостатка витамина D, анорексии, пониженной костной массы в результате активных занятий спортом, для увеличения максимума костной массы в отрочестве и для профилактики вторичного перелома костей тазобедренного сустава, содержащие 2-алкилиденовое производное 19-нор-витамина D, такое как соединение формулы I, бисфосфонат и носитель, растворитель, разбавитель и т.п.
В одном из вариантов осуществления изобретения комбинации по изобретению содержат терапевтически эффективное количество первого соединения, причем указанное первое соединение представляет собой 2-алкилиденовое производное 19-нор-витамина D, такое как соединение формулы I, и терапевтически эффективное количество второго соединения, причем второе соединение представляет собой бисфосфонат.
Особенно предпочтительной комбинацией является комбинация 2-метилен-19-нор-20(S)-1α,25-дигидроксивитамина D3 и бисфосфоната.
2-Алкилиденовые производные 19-нор-витамина D, которые могут быть использованы по настоящему изобретению, описаны в патенте США № 5843928, указанные производные характеризуются общей формулой I, показанной ниже:

где Y1 и Y2, которые могут быть одинаковыми или разными, выбраны из группы, состоящей из водорода и гидроксизащитнойгруппы, R6 и R8, которые могут быть одинаковыми или разными, выбраны из группы, состоящей из водорода, алкила, гидроксиалкила и фторалкила, или взятые вместе представляют собой группу -(CH2)х-, где х обозначает целое число от 2 до 5, а группа R представляет собой любую из обычных боковых цепей, известных для соединений типа витамина D.
Более конкретно, R может представлять собой насыщенный или ненасыщенный углеводородный радикал, содержащий 1-35 атомов углерода, который может быть линейным, разветвленным или циклическим и может содержать один или несколько дополнительных заместителей, таких как гидрокси- или защищенные гидроксигруппы, фтор, карбонильные, сложноэфирные группы, эпокси-, амино- или другие группы, содержащие гетероатомы. Предпочтительные боковые цепи указанного типа представлены структурой, изображенной ниже:
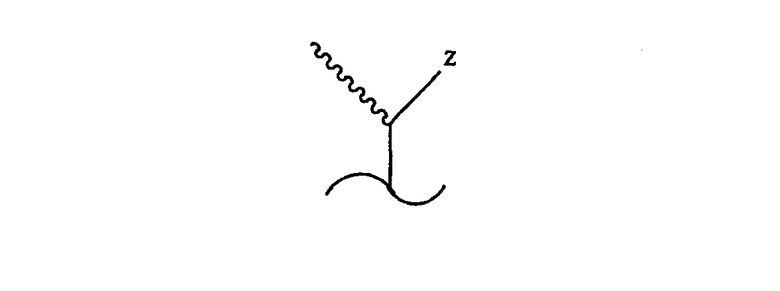
где стереохимический центр (соответствующий С-20 согласно нумерации стероидов) может иметь R- или S-конфигурацию (т.е. или природную конфигурацию у углеродного атома С-20 или 20-epi конфигурацию), и где Z выбран из Y, -OY, -CH2OY, -C≡CY и -CH=CHY, где двойная связь может иметь цис- или транс-геометрию, и где Y выбран из водорода, метила, COR5 и радикала структуры:
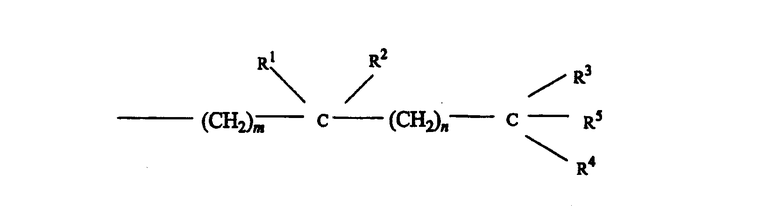
где m и n независимо представляют собой целые числа от 0 до 5, где R1 выбран из водорода, дейтерия, гидроксигруппы, защищенной гидроксигруппы, фтора, трифторметила и C1-5-алкила, который может быть линейным или разветвленным, необязательно содержит гидрокси- или защищенный гидроксизаместитель, где каждый R2, R3 и R4 независимо выбран из дейтерия, дейтероалкила, водорода, фтора, трифторметила и C1-5-алкила, который может быть линейным или разветвленным, необязательно содержит гидрокси- или защищенный гидроксизаместитель, и где R1 и R2 вместе представляют собой оксогруппу или алкилиденовую группу, =CR2R3 или группу -(CH2)p-, в которой p обозначает целое число от 2 до 5, и где R3 и R4 вместе представляют собой оксогруппу или группу -(CH2)q, в которой q обозначает целое число от 2 до 5, и где R5 представляет собой водород, гидроксигруппу, защищенную гидроксигруппу или С1-5алкил и где любая из CH-групп в положениях 20, 22 или 23 в боковой цепи может быть замещена атомом азота или где любая из групп CH(CH3)-, -CH(R3)- или -CH(R2)- в положениях 20, 22 и 23, соответственно, может быть замещена атомом кислорода или серы.
Волнистая линия к метильному заместителю при C-20 указывает, что атом углерода-20 может иметь или R-, или S-конфигурацию.
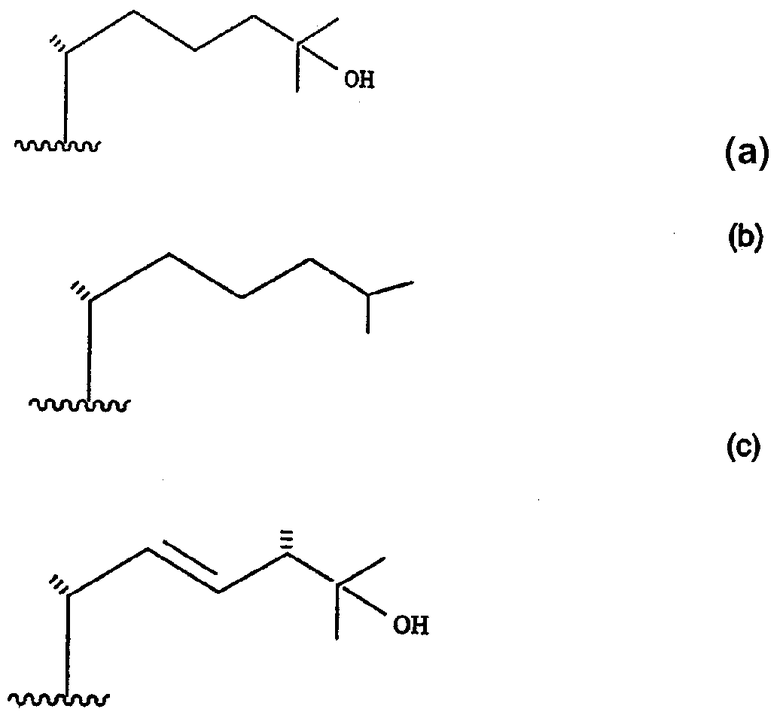
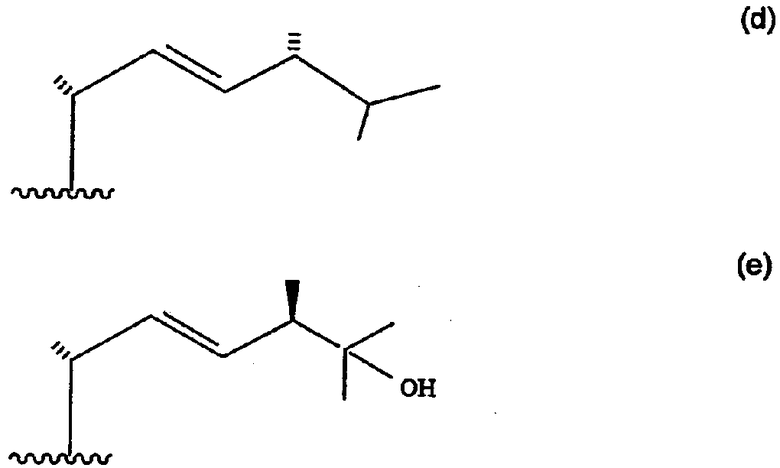
Конкретными важными примерами боковых цепей с природной 20-R-конфигурацией являются структуры, изображаемые ниже формулами (a), (b), (c), (d) и (e), т.е. такие боковые цепи, которые встречаются в 25-гидроксивитамине D3 (a); витамине D3 (b); 25-гидроксивитамине D2 (c); витамине D2 (d); и C-24 эпимере 25-гидроксивитамина D (e);
Термин "гидроксизащитная группа" здесь используют для обозначения любой группы, которую обычно применяют для временной защиты гидроксильных функциональных групп, такой, например, как алкоксикарбонильная, ацильная, алкилсилильная или алкиларилсилильная группы (которые далее называют просто «силильными» группами) и алкоксиалкильные группы. Алкоксикарбонильные защитные группы представляют собой алкил-O-CO-группы, такие как метоксикарбонил, этоксикарбонил, пропоксикарбонил, изопропоксикарбонил, бутоксикарбонил, изобутоксикарбонил, трет-бутоксикарбонил, бензилоксикарбонил или аллилоксикарбонил. Термин «ацил» обозначает алканоильную группу, содержащую 1-6 атомов углерода, во всех ее изомерных формах или карбоксиалканоильную группу, содержащую 1-6 атомов углерода, такую как оксалильная, малонильная, сукцинильная или глутарильная группа, или ароматическую ацильную группу, такую как бензоильная или галоген-, нитро- или алкилзамещенная бензоильная группа. Термин «алкил» используют в описании или формуле изобретения для обозначения линейного или разветвленного алкильного радикала, содержащего от 1 до 10 атомов углерода, во всех его изомерных формах. Алкоксиалкильные защитные группы представляют собой такие группы, как метоксиметил, этоксиметил, метоксиэтоксиметил или тетрагидрофуранил и тетрагидропиранил. Предпочтительными силильными защитными группами являются триметилсилил, триэтилсилил, трет-бутилдиметилсилил, дибутилметилсилил, дифенилметилсилил, фенилдиметилсилил, дифенил-трет-бутилсилил и аналогичные алкилированные силильные радикалы. Термином «арил», за исключением случаев, для которых указано иное, обозначают фенильную или любую алкил-, нитро- или галогензамещенную фенильную группу.
«Защищенная гидроксигруппа» представляет собой гидроксигруппу, которая преобразована или защищена любой из вышеуказанных групп, обычно используемых для временной или постоянной защиты гидроксильных функциональных групп, например, силильной, алкоксилкильной, ацильной или алкоксикарбонильной группами, как определено ранее. Термины «гидроксиалкил», «дейтероалкил» и «фторалкил» относятся к любым алкильным радикалам, замещенным одним или несколькими гидрокси-, дейтеро- или фторзаместителями, соответственно.
Следует отметить в настоящем описании, что термин «24-гомо» относится к присоединению одной метиленовой группы, а термин «24-дигомо» относится к присоединению двух метиленовых групп к углероду в положении 24 боковой цепи. Аналогично термин «тригомо» относится к присоединению трех метиленовых групп. Также термин «26,27-диметил» относится к присоединению метильной группы к углероду в положениях 26 и 27 таким образом, что, например, R3 и R4 представляют собой этильные группы. Аналогично, термин «26,27-диэтил» относится к присоединению этильной группы в положения 26 и 27 таким образом, что R3 и R4 представляют собой пропильные группы.
В приведенных ниже списках соединений следует в названии указывать конкретный алкилиденовый заместитель, присоединенный к атому углерода в положении 2. Например, если алкилиденовый заместитель представляет собой метиленовую группу, названия всех упомянутых соединений должны начинаться с термина «2-метилен». Если алкилиденовым заместителем является этиленовая группа, названия всех соединений с этиленовой группой в положении 2 должны начинаться с термина «2-этилен», и так далее. Кроме того, если метильная группа, при атоме углерода в положении 20, находится в epi или неприродной конфигурации, термин «20(S)» или «20-epi» следует включить в название каждого из поименованных соединений. Упомянутые соединения могут также быть соединениями типа витамина D2, если желательно.
Конкретными и предпочтительными примерами 2-алкилиденовых соединений структуры I с ненасыщенной боковой цепью являются
19-нор-24-гомо-1,25-дигидрокси-22-дегидровитамин D3,
19-нор-24-дигомо-1,25-дигидрокси-22-дегидровитамин D3,
19-нор-24-тригомо-1,25-дигидрокси-22-дегидровитамин D3,
19-нор-26,27-диметил-24-гомо-1,25-дигидрокси-22-дегидровитамин D3,
19-нор-26,27-диметил-24-дигомо-1,25-дигидрокси-22-дегидровитамин D3,
19-нор-26,27-диметил-24-тригомо-1,25-дигидрокси-22-дегидровитамин D3,
19-нор-26,27-диэтил-24-гомо-1,25-дигидрокси-22-дегидровитамин D3,
19-нор-26,27-диэтил-24-дигомо-1,25-дигидрокси-22-дегидровитамин D3,
19-нор-26,27-диэтил,24-тригомо-1,25-дигидрокси-22-дегидровитамин D3,
19-нор-26,27-дипропил-24-гомо-1,25-дигидрокси-22-дегидровитамин D3,
19-нор-26,27-дипропил-24-дигомо-1,25-дигидрокси-22-дегидровитамин D3 и
19-нор-26,27-дипропил-24-тригомо-1,25-дигидрокси-22-дегидровитамин D3.
Конкретными и предпочтительными примерами 2-алкилиденовых соединений структуры I с насыщенной боковой цепью являются
19-нор-24-гомо-1,25-дигидроксивитамин D3,
19-нор-24-дигомо-1,25-дигидроксивитамин D3,
19-нор-24-тригомо-1,25-дигидроксивитамин D3,
19-нор-26,26-диметил-24-гомо-1,25-дигидроксивитамин D3,
19-нор-26,27-диметил-24-дигомо-1,25-дигидроксивитамин D3,
19-нор-26,27-диметил-24-тригомо-1,25-дигидроксивитамин D3,
19-нор-26,27-диэтил-24-гомо-1,25-дигидроксивитамин D3,
19-нор-26,27-диэтил-24-дигомо-1,25-дигидроксивитамин D3,
19-нор-26,27-диэтил-24-тригомо-1,25-дигидроксивитамин D3,
19-нор-26,27-дипропил-24-гомо-1,25-дигидроксивитамин D3,
19-нор-26,27-дипропил-24-дигомо-1,25-дигидроксивитамин D3 и
19-нор-26,27-дипропил-24-тригомо-1,25-дигидроксивитамин D3.
Полифосфонаты, включающие бисфосфонаты, применимы в качестве второго соединения в композициях и способах по настоящему изобретению. Примеры полифосфонатов включают полифосфонаты типа описанных в патенте США № 3683080. Предпочтительными полифосфонатами являются геминальные дифосфонаты (называемые в настоящей заявке бисфосфонатами). Предпочтительными бисфосфонатами являются бисфосфонаты общей формулы А

где
R4 обозначает H, OH или Cl; и
R5 обозначает
(а) алкил, содержащий 1-6 атомов углерода (необязательно амино-, алкиламино-, диалкиламинозамещенный), или гетероциклил;
(b) галоген;
(с) арилтиогруппу, предпочтительно хлорзамещенную;
(d) алкиламиногруппу, содержащую 5-7 атомов углерода, или
(е) насыщенный пяти- или шестичленный азотсодержащий гетероциклил, содержащий один или два гетероатома;
или их фармацевтически приемлемая соль или пролекарство.
«Алкил» группы в «алкиламино» и «диалкиламино» группах в определении R5 для формулы А могут содержать 1-5 атомов углерода и могут быть независимо выбраны в диалкиламиногруппе. Под термином «гетероциклил», обозначаемым R5 в формуле А, подразумевают насыщенную или ненасыщенную 5-7-членную гетероциклическую группу с одним или двумя циклами и 1-3 гетероатомами, независимо выбранными из N, O и S. Термин «арил» в обозначении «арилтио» в определении R5 обозначает фенильную, фурильную, тиенильную или пиридильную группу или конденсированную циклическую систему из любых упомянутых групп, такую как нафтил. Если арильная группа в R5 является замещенной, она замещена одной или несколькими алкил-, галоген-, амино-, тиол-, нитро-, гидрокси-, ацил-, арил- или цианогруппами.
Соединения формулы А включают:
4-амино-1-гидроксибутилиден-1,1-бисфосфонат (алендронат), (3-амино-1-гидроксипропилиден)бисфосфонат (памидронат), [2-(2-пиридинил)этилиден]бисфосфонат (пиридронат), (дихлорметилен)бисфосфоновая кислота (клодроновая кислота) или ее динатриевая соль (клодронат), N,N-диметил-3-амино-1-гидроксипропилиден-1,1-бисфосфонат (милдронат, олпадронат), 1-гидрокси-3-(N-метил-N-пентиламино)пропилиден-1,1-бисфосфонат (ибандронат), 1-гидрокси-2-(3-пиридил)этилиден-1,1-бисфосфонат (ризедронат), 1-гидроксиэтилиден-1,1-бисфосфонат (этидронат), 1-гидрокси-3-(1-пирролидинил)пропилиден-1,1-бисфосфонат (ЕВ-1053), 1-гидрокси-2-(1-имидазолил)этилиден-1,1-бисфосфонат (золедронат) 1-гидрокси-2-(имидазо[1,2-a]пиридин-3-ил)этилиден-1,1-бисфосфонат (минодронат), 1-(4-хлорфенилтио)метилиден-1,1-бисфосфонат (тилудронат), 1-(циклогептиламино)метилиден-1,1-бисфосфонат (цимадронат, инкадронат), 6-амино-1-гидроксигексилиден-1,1-бисфосфонат (неридронат).
Термин «бисфосфонат» означает соединение в виде бисфосфоновой кислоты и ее фармацевтически приемлемых солей. Например, используемый в данной заявке термин «алендронат», относится к алендроновой кислоте (в виде свободной кислоты) и к ее фармацевтически приемлемым солям, таким как алендронат натрия. Подобным же образом под термином «ризедронат» подразумевают ризедроновую кислоту и ее фармацевтически приемлемые соли, такие как ризедронат натрия. В определение «бисфосфонат», используемое в данной заявке, включены также сложноэфирные формы указанных соединений, которые способны подвергаться гидролизу.
Динатрийтилудронат представляет собой особенно предпочтительный бисфосфонат. Ибандронат представляет собой особенно предпочтительный бисфосфонат. Алендронат представляет собой особенно предпочтительный бисфосфонат. Золендронат представляет собой особенно предпочтительный бисфосфонат. Другими предпочтительными бисфосфонатами являются 6-амино-1-гидроксигексилиденбисфосфонат и 1-гидрокси-3(метилпентиламино)пропилиденбисфосфонат. Полифосфонаты, включающие бисфосфонаты, можно вводить в виде кислоты или растворимой соли щелочного или щелочноземельного металла. Гидролизуемые сложные эфиры полифосфонатов также включены. Конкретные примеры включают этан-1-гидрокси-1,1-дифосфоновую кислоту, метандифосфоновую кислоту, пентан-1-гидрокси-1,1-дифосфоновую кислоту, метандихлордифосфоновую кислоту, метангидроксидифосфоновую кислоту, этан-1-амино-1,1-дифосфоновую кислоту, этан-2-амино-1,1-дифосфоновую кислоту, пропан-3-амино-1-гидрокси-1,1-дифосфоновую кислоту, пропан-N,N-диметил-3-амино-1-гидрокси-1,1-дифосфоновую кислоту, пропан-3,3-диметил-3-амино-1-гидрокси-1,1-дифосфоновую кислоту, фениламинометандифосфоновую кислоту, N,N-диметиламинометандифосфоновую кислоту, N(2-гидроксиэтил)аминометандифосфоновую кислоту, бутан-4-амино-1-гидрокси-1,1-дифосфоновую кислоту, пентан-5-амино-1-гидрокси-1,1-дифосфоновую кислоту, гексан-6-амино-1-гидрокси-1,1-дифосфоновую кислоту и их фармацевтически приемлемые сложные эфиры или соли.
Особенно предпочтительные бисфосфонаты, применяемые в композициях и способах по настоящему изобретению, включают тилудроновую кислоту, алендроновую кислоту, золендроновую кислоту, ибандроновую кислоту, розендроновую кислоту, этидроновую кислоту, клодроновую кислоту и памидроновую кислоту и их фармацевтически приемлемые соли или пролекарства или соли пролекарств.
Бисфосфонаты, используемые в композициях и способах по изобретению, известны в области техники и описаны в литературе. Тилудроновая кислота, родственные соединения и ее соли описаны в патентах США № 4134969; № 4578376; № 4621077; № 4876248; № 4980171; № 5405994 и № 5656288. В патенте США № 5405994 описаны полугидрат динатрийтилудроната и моногидрат динатрийтилудроната. В патенте США № 5656288 описан тетрагидрат динатрийтилудроната. Алендронат в виде тригидрата его мононатриевой соли, который продается под названием Fosamax®, описан в патентах США № 4621077; № 4922007; № 5019651; № 5510517 и № 5648491. Например, алендронат в виде бисфосфоновой кислоты можно получить, как описано в патенте США № 4621077, методика из которого воспроизведена ниже. Смесь 1 моль 4-аминомасляной кислоты, 1,5 моль фосфорной кислоты и 500 см3 безводного хлорбензола нагревают до 100°C. При указанной температуре прибавляют 1,5 моль трихлорида фосфора при сильном перемешивании. Смесь перемешивают при 100°C в течение 31/2 часов, пока полностью не образуется густая фаза и затем дают охладиться. Твердое вещество отфильтровывают, промывают небольшим количеством хлорбензола и растворяют в воде. Раствор нагревают до температуры кипения в течение часа, затем охлаждают и обесцвечивают активированным углем. Вещество фильтруют и продукт высаждают избытком горячего метанола. Неочищенное вещество, полученное таким образом, нагревают и кипятят с обратным холодильником в 20%-ной соляной кислоте в течение 8 часов. Соляную кислоту удаляют перегонкой и остаток перекристаллизовывают из воды. Продукт представляет собой 4-амино-1-гидроксибутан-1,1-бифосфоновую кислоту в виде белого кристаллического порошка.
Золедронат в виде моногидрата свободной кислоты, который продается под названием Zometa®, описан в патенте США № 4939130. Ибандронат описан в патенте США № 4927814. Пиридронат описан в патенте США № 4761406. Клодронат описан в патенте Бельгии № 672205 (1966) и в статье J. Org. Chem. 1967, 32, 4111. Инкандронат описан в патенте США № 4970335. Ризедронат в виде полупентагидрата его мононатриевой соли (2,5 H2O), который продается под названием Actonel®, описан в патентах США № 5583122; 5994329; 6015801; 6096342 и 6165513. Например, ризедронат может быть получен по следующей методике, которая изложена в примере 3 патента США № 5583122. Синтез 2-(2-пиридил)-1-гидроксиэтан-1,1-дифосфоновой кислоты. В 3-горлую круглодонную колбу, снабженную обратным холодильником и стержнем для магнитной мешалки, загружают 6,94 г (0,04 моль) 2-пиридинуксусной кислоты, 9,84 г (0,14 моль) фосфорной кислоты и 150 мл хлорбензола. Полученную реакционную смесь нагревают на кипящей водяной бане и прибавляют по каплям 16,5 г (0,12 моль) трихлорида фосфора при перемешивании. Реакционную смесь нагревают 21/2 часов, за это время образуется вязкое желтое масло. Реакционную смесь затем охлаждают на ледяной бане и хлорбензольный раствор сливают с затвердевшего продукта. В реакционную колбу с затвердевшим продуктом загружают 150 мл воды и нагревают на кипящей водяной бане в течение нескольких часов. Затем горячий раствор фильтруют через Celite 545® (диатомитовая земля, Mallinckrodt Baker, Inc., Phillipsburg, NJ). К теплому фильтрату прибавляют 300 мл метанола, и образуется осадок. Охлаждают льдом в течение 1 часа, затем осадок отфильтровывают и промывают смесью метанол/вода (1/1 об/об), метанолом, эфиром и сушат на воздухе. Продукт может быть перекристаллизован из горячей воды. Выход составляет приблизительно 5,9 г (52%). Образец характеризуют ЯМР P-31 и C-13.
Настоящее изобретение также относится к фармацевтическим композициям для лечения метаболического заболевания костей, старческого остеопороза, постклимактерического остеопороза, остеопороза, вызванного стероидами, остеопороза с низкой скоростью метаболизма, остеомаляции, ренальной остеодистрофии, псориаза, рассеянного склероза, сахарного диабета, отторжения трансплантата («хозяин против трансплантата»), отторжения трансплантата, ревматоидного артрита, астмы, переломов костей, костного трансплантата, акнэ, алопеции, сухости кожи, недостаточной плотности кожи, недостаточного салоотделения, морщин, гипертензии, лейкемии, рака толстой кишки, рака груди, рака простаты, ожирения, мужского остеопороза, гипогонадизма, андропаузы, слабости, поражений мышц, саркопении, остеосаркомы, гипокальциемической тетании, гипопаратиреоза, рахита, нехватки витамина D, анорексии, пониженной костной массы в результате активных занятий спортом и для увеличения максимума костной массы в юности и для профилактики вторичного перелома костей тазобедренного сустава, включающим введение больному, который нуждается в этом, комбинации 2-алкилиденового производного 19-нор-витамина D, такого как соединение формулы I, и бисфосфоната, и носителя, растворителя, разбавителя и т.п.
Отметим, что когда соединения обсуждаются здесь, предполагается, что соединения можно вводить пациенту в виде фармацевтически приемлемой соли, пролекарства или соли пролекарства. Подразумевается, что все такие варианты включены в изобретение.
Термином «больной, который нуждается в этом» обозначают человека и других животных, которые страдают перечисленными ниже заболеваниями или для них существует угроза таких заболеваний, как метаболические болезни костей, старческий остеопороз, постклимактерический остеопороз, остеопороз, вызванный стероидами, остеопороз с низкой скоростью метаболизма, остеомаляция, ренальная остеодистрофия, псориаз, рассеянный склероз, сахарный диабет, отторжение трансплантата («хозяин против трансплантата»), отторжение трансплантата, ревматоидный артрит, астма, переломы костей, трансплантатов костей, акнэ, алопеция, сухость кожи, недостаточная плотность кожи, недостаточное салоотделение, морщины, гипертензия, лейкемия, рак толстой кишки, рак груди, рак простаты, ожирение, мужской остеопороз, гипогонадизм, андропауза, слабость, поражения мышц, саркопения, остеосаркома, гипокальциемическая тетания, гипопаратиреоз, рахит, нехватка витамина D, анорексия, пониженная костная масса в результате активных занятий спортом, или они нуждаются в увеличении максимума костной массы в юности и профилактике вторичного перелома костей тазобедренного сустава.
Термины «лечение», «лечить», используемые здесь, включают превентивное (например, профилактику), паллиативное и радикальное лечение.
Выражение «фармацевтически приемлемый» используют для обозначения носителя, разбавителя, наполнителя и/или соли или пролекарства, которые должны быть совместимы с другими ингредиентами рецептуры и не должны быть вредными для больного.
Термин «пролекарство» означает соединение, которое трансформируется in vivo, с образованием соединения по изобретению. Трансформация может происходить по различным механизмам, например путем гидролиза в крови. Применение пролекарств обсуждается в указанных ниже публикациях [T. Higuchi and W. Stella "Pro-drugs as Novel Delivery Systems," Vol. 14 of the A.C.S. Symposium Series] и [Bioreversible Carriers in Drug Design, ed. Edward B. Roche, American Pharmaceutical Association and Pergamon Press, 1987].
Например, когда соединение по изобретению содержит функциональную группу кислоты (карбоксильную группу), пролекарство может включать сложный эфир, образованный в результате замещения атома водорода группы кислоты такой группой, как (C1-C8)алкил, (C2-C12)алканоилоксиметил, 1-(алканоилокси)этил, которые содержат от 4 до 9 атомов углерода, 1-метил(алканоилокси)этил, содержащей от 5 до 10 атомов углерода, алкоксикарбонилоксиметил, содержащей от 3 до 6 атомов углерода, 1-(алкоксикарбонилокси)этил, содержащей от 4 до 7 атомов углерода, 1-метил-1-(алкоксикарбонилокси)этил, содержащей от 5 до 8 атомов углерода, N-(алкоксикарбонил)аминометил, содержащей от 3 до 9 атомов углерода, 1-(N-(алкоксикарбонил)амино)этил, содержащей от 4 до 10 атомов углерода, 3-фталидил, 4-кротонолактонил, гамма-бутиролактон-4-ил, ди-N,N-(C1-C2)алкиламино(C2-C3)алкил (такой как β-диметиламиноэтил), карбамоил(C1-C2)алкил, N,N-ди(C1-C2)алкилкарбамоил(C1-C2)алкил и пиперидино-, пирролидино- или морфолино(C2-C3)алкил.
Аналогично, когда соединение по настоящему изобретению содержит спиртовую функциональную группу, пролекарство может быть образовано путем замещения атома водорода спиртовой группы такой группой, как (C1-C6)алканоилоксиметил, 1-((C1-C6)алканоилокси)этил, 1-метил-1-((C1-C6)алканоилокси)этил, (C1-C6)алкоксикарбонилоксиметил, N-(C1-C6)алкоксикарбониламинометил, сукциноил, (C1-C6)алканоил, α-амино(C1-C4)алканоил, арилацил и α-аминоацил или α-аминоацил-α-аминоацил, где каждая α-аминоацильная группа независимо выбрана из природных L-аминокислот, P(O)(OH)2, -P(O)(O(C1-C6)алкил)2 или гликозил (радикал, получающийся в результате удаления гидроксильной группы гемиацетальной формы углевода).
Когда соединение по настоящему изобретению включает функциональную аминогруппу, пролекарство может быть образовано путем замещения атома водорода в аминогруппе такой группой, как RX-карбонил, RXO-карбонил, NRХRХ'-карбонил, где RХ и RX', каждый, независимо представляют собой (C1-С10)алкил, (C3-C7)циклоалкил, бензил; или RX-карбонил представляет собой природный α-аминоацил, или природный α-аминоацил-(природный)α-аминоацил, -C(OH)C(O)OYX, где YX представляет собой H, (C1-C6)алкил или бензил), -C(OYХ0)YХ1, где YХ0 представляет собой (C1-C4)алкил и YX1 представляет собой (C1-C6)алкил, карбокси(C1-C6)алкил, амино(C1-C4)алкил или моно-N- или ди-N,N-(C1-C6)алкиламиноалкил, -C(YХ2)YХ3, где YX2 представляет собой водород или метил и YХ3 представляет собой моно-N- или ди-N,N-(C1-C6)алкиламино, морфолино, пиперидин-1-ил или пирролидин-1-ил.
Выражение «фармацевтически приемлемая соль» относится к нетоксичным анионным солям, содержащим анионы, такие как (но не ограничивается ими) хлорид, бромид, иодид, сульфат, бисульфат, фосфат, ацетат, малеат, фумарат, оксалат, лактат, тартрат, цитрат, глюконат, метансульфонат и 4-толуолсульфонат. Выражение также относится к нетоксичным катионным солям, таким как (но не ограничивается ими) соли натрия, калия, кальция, магния, аммония или протонированных бензатина (N,N'-дибензилэтилендиамина), холина, этаноламина, диэтаноламина, этилендиамина, мегламина (N-метилглюкамина), бенетамина (N-бензилфенетиламина), пиперазина или трометамина (2-амино-2-гидроксиметил-1,3-пропандиола).
Понятно, что соединения по изобретению могут существовать в виде соединений с радиоактивной меткой, т.е. указанные соединения могут содержать один или несколько атомов, имеющих атомную массу или атомный номер, отличающийся от атомной массы или атомного номера, которые обычно встречаются в природе. Радиоизотопы водорода, углерода, фосфора, фтора и хлора включают 3H, 14C, 32P. 35S, 18F и 36Cl, соответственно. Соединения по изобретению, которые содержат указанные радиоизотопы и/или радиоизотопы других атомов, охватываются объемом данного изобретения. Радиоизотопы трития, т.е. 3H, и углерода-14, т.е. 14C, особенно предпочтительны из-за легкости их получения и определения. Соединения с радиоактивной меткой по изобретению обычно получают способами, хорошо известными специалистам в данной области техники. Удобно, что такие соединения с радиоактивной меткой можно получать по методикам, описанным в настоящей заявке, за исключением замещения легко доступного реагента с радиоактивной меткой реагентом без радиоактивной метки.
Специалисту, обладающему обычными познаниями в данной области техники, должно быть понятно, что некоторые из соединений по изобретению содержат по меньшей мере один асимметрический атом углерода и, следовательно, являются энантиомерами или диастереомерами. Диастереомерные смеси можно разделить на индивидуальные диастереомеры, исходя из различий их физико-химических свойств, способами, которые по сути известны, например, хроматографией или фракционной кристаллизацией. Энантиомеры могут быть разделены превращением энантиомерной смеси в диастереомерную смесь реакцией с соответствующим оптически активным соединением (например, спиртом), разделением диастереомеров и превращением индивидуальных диастереомеров в соответствующие чистые энантиомеры (например, гидролизом, включающим как методы химического гидролиза, так и микробные методы гидролиза липазы, например, гидролиз, катализируемый ферментами). Все такие изомеры, включающие диастереомеры, энантиомеры и их смеси, рассматриваются как часть изобретения. Некоторые соединения по изобретению представляют собой атропоизомеры (например, замещенные биарилы), и их также рассматривают как часть изобретения.
Кроме того, когда соединения по изобретению, включая соединения формулы I или бисфосфонаты, образуют гидраты или сольваты, они также охватываются объемом изобретения.
Введение соединений по изобретению можно осуществлять любым способом, который позволяет доставлять соединение по изобретению системно и/или локально. Упомянутые способы включают пероральный, парентеральный и интрадуоденальный пути и т.д. Вообще, соединения по изобретению вводят перорально, но можно применять парентеральное введение (например, внутривенное, внутримышечное, трансдермальное, подкожное, ректальное или интрамедуллярное), например, в тех случаях, когда пероральное введение не подходит для намеченной цели или больной не способен глотать лекарство.
Соединения по изобретению могут также применяться местно для нанесения пациенту на место локализации в подходящем носителе или разбавителе.
2MD и другие 2-алкилиденовые производные 19-нор-витамина D по изобретению можно вводить больному человеку в дозе, составляющей от около 0,01 мкг/день до около 10 мкг/день. Предпочтительные дозы составляют от около 0,05 мкг/день до около 1 мкг/день и более предпочтительный интервал доз составляет от около 0,1 мкг/день до около 0,4 мкг/день.
Обычно дозировка бисфосфоната является такой, что однократная доза бисфосфонатного активного ингредиента, которую вводят больному, нуждающемуся в таком лечении, составляет от 0,002 мг/кг до 20 мг/кг, главным образом, от 0,01 мг/кг до 10,0 мг/кг. Термин «мг/кг» означает миллиграммы бисфосфоната на килограмм массы тела больного. Примеры серийно выпускаемых лекарственных форм бисфосфонатов включают таблетки ризедроната для перорального введения (5 мг, 30 мг и 35 мг) в виде его натриевой соли (ризедронат натрия), которые продаются под названием Actonel® и таблетки алендроната для перорального введения (5 мг, 10 мг, 35 мг, 40 мг и 70 мг) также в виде его натриевой соли (алендронат натрия), которые продаются под названием Fosamax®. Может быть приведена, например, дневная доза бисфосфоната, доза для введения два раза в неделю или один раз в неделю.
Количество и время введения будут, разумеется, зависеть от субъекта, которого лечат, от тяжести заболевания, способа введения и мнения лечащего врача. Таким образом, из-за варьирования дозы для каждого из больных дозировки, приведенные в описании, являются методическими рекомендациями, и лечащий врач может назначать такие дозы лекарств, которые он считает подходящими для больного. При рассмотрении степени необходимого лечения врач должен учитывать множество факторов, таких как возраст пациента, наличие предсуществующего заболевания, а также наличие других заболеваний. Дозу лекарства можно вводить один раз в день или более одного раза в день или вводить лекарственную форму с замедленным высвобождением или с регулируемым высвобождением. Можно также вводить комбинацию лекарственных средств с немедленным высвобождением и регулируемым высвобождением и/или замедленным высвобождением.
Введение 2MD или другого 2-алкилиденового производного 19-нор-витамина D и бисфосфоната или их комбинации можно проводить в соответствии с любой схемой непрерывного или периодического курса лечения. Неограничивающими примерами схем лечения 2MD или еще одним 2-алкилиденовым производным 19-нор-витамина D являются следующие: один раз в день, несколько раз в день, один раз в неделю, один раз в две недели, несколько раз в две недели, один раз в месяц, несколько раз в месяц, один раз в два месяца, один раз в три месяца, один раз в шесть месяцев и один раз в год.
Соединения по изобретению обычно вводят в виде фармацевтической композиции, содержащей по меньшей мере одно из соединений по изобретению вместе с фармацевтически приемлемым носителем или разбавителем. Следовательно, соединения по изобретению можно вводить в любой обычной пероральной, парентеральной, ректальной или трансдермальной лекарственной форме.
Фармацевтическая композиция для перорального введения может быть в виде растворов, суспензий, таблеток, пилюль, капсул, порошков и т.п. Таблетки, содержащие различные наполнители, такие как цитрат натрия, карбонат кальция и фосфат кальция, применяют с различными разрыхлителями, такими как крахмал, предпочтительно крахмал из картофеля или тапиоки, и некоторые сложные силикаты вместе со связывающими агентами, такими как поливинилпирролидон, сахароза, желатин и аравийская камедь.
Кроме того, смазывающие вещества, такие как стеарат магния, лаурилсульфат магния и тальк часто очень полезны для целей таблетирования. Твердые композиции аналогичного типа также применяют в качестве наполнителей в мягких и твердых желатиновых капсулах. Предпочтительные вещества в этой связи включают лактозу или молочный сахар, полиэтиленгликоли с высокой молекулярной массой. Когда для перорального введения требуются водные суспензии и/или эликсиры, соединения по изобретению могут быть объединены с различными подслащивающими агентами, веществами, исправляющими вкус, красителями, эмульгаторами и/или суспендирующими агентами, а также такими разбавителями, как вода, этанол, пропиленгликоль, глицерин и различные аналогичные комбинации указанных веществ. Один пример приемлемой рецептуры для 2MD и других 2-алкилиденовых производных 19-нор-витамина D представляет собой мягкую желатиновую капсулу, содержащую метиловый эфир бензойной кислоты, в котором растворено 2MD или другое 2-алкилиденовое производное 19-нор-витамина D. Для специалистов в данной области должны быть очевидны и другие подходящие рецептуры.
Для парентерального введения можно использовать растворы в кунжутном или арахисовом масле или в водном пропиленгликоле, а также стерильные водные растворы соответствующих растворимых в воде солей. Такие водные растворы могут быть буферированы подходящим образом, если необходимо, а жидкий разбавитель сначала делают изотоническим, используя достаточное количество физиологического раствора или глюкозы. Упомянутые водные растворы особенно подходят для внутривенных, внутримышечных, подкожных и внутрибрюшинных инъекций. В связи с этим все применяемые стерильные водные среды легко можно получить стандартными методами, хорошо известными специалистам в данной области.
Для трансдермального (например, местного) введения обычно готовят разбавленные стерильные водные или частично водные растворы (обычно их концентрация составляет от около 0,1 до 5%) по прочим параметрам аналогичные вышеупомянутым растворам для парентерального введения.
Способы получения различных фармацевтических композиций с некоторым количеством активного ингредиента известны или должны быть очевидны для специалистов в данной области техники. Примеры способов получения фармацевтических композиций даны в [см.Remington's Pharmaceutical Sciences, Mack Publishing Company, Easton, Pa., 19th Edition (1995)].
Еще одним объектом настоящего изобретения является набор, содержащий:
а. некоторое количество 2-алкилиденового производного 19-нор-витамина D, такого как соединение формулы I, и фармацевтически приемлемый носитель или разбавитель в первой стандартной лекарственной форме;
b. некоторое количество бисфосфоната и фармацевтически приемлемый носитель или разбавитель во второй стандарной лекарственной форме;
с. упаковка.
Набор содержит две отдельные фармацевтические композиции: 2-алкилиденовое производное 19-нор-витамина D, такое как соединение формулы I, и второе соединение, как описано выше. Набор содержит упаковочные средства для упаковки отдельных композиций, такие как флакон или пакет из фольги, разделенные на отделения, однако отдельные композиции могут также быть помещены в одну неразделенную упаковку. Обычно набор содержит инструкции для введения отдельных компонентов. Форма в виде набора обычно особенно выгодна, когда отдельные компоненты предпочтительно вводить в различных лекарственных формах (например, перорально и парентерально), вводить с различными интервалами или когда лечащий врач считает необходимым провести титрование отдельных компонентов комбинации.
Примером такого набора является так называемая блистерная упаковка. Блистеры широко известны в упаковочной индустрии и широко используются для упаковки фармацевтических стандартных лекарственных форм (таблетки, капсулы и тому подобные). Блистерные упаковки обычно состоят из листа относительно жесткого материала, покрытого фольгой предпочтительно из прозрачного пластичного материала. Во время процесса упаковки в пластичной фольге образуются углубления. Углубления имеют размер и форму таблетки или капсулы, которую упаковывают. Затем таблетки или капсулы помещают в углубления и лист относительно жесткого материала запаивают со стороны фольги на стороне, противоположной направлению, в котором образовались углубления. В результате таблетки или капсулы запаиваются в углублениях между фольгой из пластика и листом. Предпочтительно, если прочность листа такова, что таблетки и капсулы можно удалить из блистерной упаковки вручную, нажимая на углубления, при этом в листе на месте углубления образуется отверстие. Затем через указанное отверстие вынимают таблетку или капсулу.
Желательно обеспечить набор инструкцией-напоминанием, например, в виде номеров у таблеток или капсул, номера должны соответствовать тем дням схемы лечения, когда следует принимать указанную лекарственную форму. Еще одним примером такого напоминания является календарь, напечатанный на карточке, например, следующим образом: «первая неделя, понедельник, вторник, ...», и т.д. Другие варианты напоминания совершенно очевидны. «Дневная доза» может представлять собой одну таблетку или капсулу или несколько таблеток или капсул, которые необходимо принять в определенный день. Дневная доза соединения формулы I, его пролекарства или фармацевтически приемлемой соли указанного соединения или указанного пролекарства может состоять из одной таблетки или капсулы, тогда как дневная доза второго соединения может состоять из нескольких таблеток или капсул и наоборот. Напоминание должно отражать данную информацию.
Еще один конкретный вариант осуществления изобретения относится к дозатору, предназначенному для дозирования дневных доз. Предпочтительно, дозатор снабжен напоминанием (памяткой), для того, чтобы дополнительно способствовать соблюдению схемы лечения. Примером такого напоминания является механический счетчик, который указывает количество дневных доз, которые были выданы. Еще одним примером такого напоминания является микрочип (с питанием от батареек), соединенный с жидкокристаллическим устройством для считывания данных, или звуковым сигналом-напоминанием, сообщающим, например, что последняя дневная доза введена и/или напоминающим, когда следует ввести дневную дозу.
2-Алкилиденовое производное 19-нор-витамина D и бисфосфонат можно вводить в одной лекарственной форме или в разных лекарственных формах в одно и то же время или в разное время. Рассматриваются все варианты методов введения. Предпочтительным методом введения является введение комбинации в одной и той же лекарственной форме и в одно время. Еще один предпочтительный метод введения состоит во введении 2-алкилиденового производного 19-нор-витамина D в одной лекарственной форме, а бисфосфоната в другой, причем обе формы вводят в одно и то же время.
Получение соединений 1α-гидрокси-2-алкил-19-нор-витамина D, конкретно, соединений 1α-гидрокси-2-метил-19-нор-витамина D, имеющих базовую структуру I, можно осуществить общеизвестным общим способом, т.e. конденсацией бициклического кетона типа Виндауса-Грундманна (Windaus-Grundmann) II с аллильным фосфиноксидом III, которая приводит к образованию соответствующих аналогов 2-метилен-19-нор-витамина D IV, с последующим снятием защиты с C-1 и C-3 в образующихся соединениях:

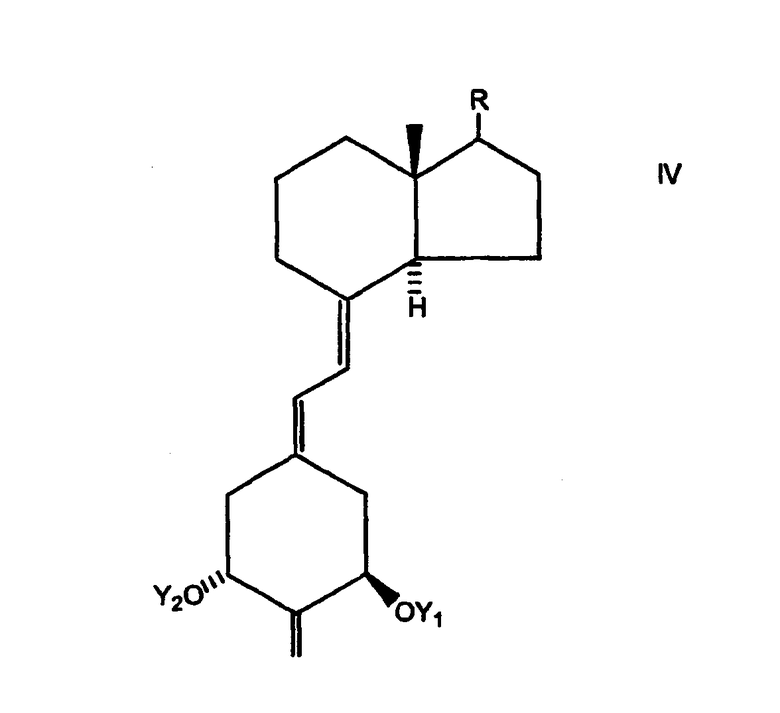
В структурах II, III и IV группы Y1 и Y2 и R представляют собой группы, определенные выше, Y1 и Y2 представляют собой предпочтительно гидроксизащитные группы, причем понятно также, что любые функциональные группы в R, которые могли бы быть уязвимы или которые могли бы препятствовать реакции, должны быть соответствующим образом защищены, что хорошо известно в данной области техники. Способ, показанный выше, представляет собой конвергентную концепцию синтеза, которая эффективно применена для получения соединений витамина D [например, Lythgoe et al., J. Chem. Soc. Perkin Trans. 1, 590 (1978); Lythgoe, Chem. Soc. Rev. 9, 449 (1983); Toh et al., J. Org. Chem. 48, 1414 (1983); Baggiolini et al., J. Org. Chem. 51, 3098 (1986); Sardina et al., J. Org. Chem. 51, 1264 (1986); J. Org. Chem. 51, 1269 (1986); DeLuca et al., U.S. Pat. No. 5,086,191; DeLuca et al., U.S. Pat. No. 5,536,713].
Гидринданоны общей структуры II известны или могут быть получены известными способами. Конкретные важные примеры таких известных бициклических кетонов представляют собой структуры с боковыми цепями (a), (b), (c) и (d), описанными выше, т.е. 25-гидроксикетон Грундманна (f) [Baggiolini et al., J. Org. Chem. 51, 3098 (1986)], кетон Грундманна (g) [Inhoffen et al., Chem. Ber. 90, 664 (1957)], 25-гидроксикетон Виндауза (h) [Baggiolini et al., J. Org. Chem. 51, 3098 (1986)] и кетон Виндауза (i) [Windaus et al., Ann., 524, 297 (1936)].

Для получения нужных фосфиноксидов общей структуры III разработан новый путь синтеза из производного метилхиниката 1, который легко получается из имеющейся в продаже (1R,3R,4S,5R)-(-)-хинной кислоты, как описано в Perlman et al., Tetrahedron Lett. 32, 7663 (1991) и DeLuca et al., U.S. Pat. No. 5,086,191. Полный способ превращения исходного метилового сложного эфира 1 в нужные синтоны с А-циклом показан на схеме I. Таким образом, вторичную 4-гидроксильную группу сложного эфира 1 окисляют RuO4 (каталитический метод с RuCl3 и NaIO4 в качестве соокислителей). Применение такого сильного окислителя необходимо для эффективного окисления указанной очень стерически затрудненной гидроксильной группы. Однако можно применять и другие чаще используемые окислители (например, дихромат пиридиния), хотя в таких случаях для завершения реакции требуется больше времени. Вторая стадия синтеза включает реакцию Виттига стерически затрудненного 4-кетосоединения 2 с илидом, полученным из бромида метилтрифенилфосфония и н-бутиллития. Другие основания (подобные трет-BuOK, NaNH2, NaH, K/HMPT, NaN(TMS)2 и т.п.) также можно использовать для получения реакционно-способного метиленфосфорана. Для получения 4-метиленового соединения 3 можно применять некоторые описанные модификации способа Виттига, например, реакцию соединения 2 с активированным метилентрифенилфосфораном [Corey et al., Tetrahedron Lett. 26, 555 (1985)]. Альтернативно, можно использовать другие способы, которые широко применяют для метиленирования нереакционно-способных кетонов, например реакцию Виттига-Хорнера с PO-илидом, полученным из метилдифенилфосфиноксида депротонированием н-бутиллитием. [Schosse et al., Chimia 30, 197 (1976)] или реакцией кетона с метилсульфинатом натрия [Corey et al., J.Org.Chem. 28, 1128 (1963)] и метилсульфинатом калия [Greene et al., Tetrahedron Lett. 3755 (1976)]. Восстановление сложного эфира 3 алюмогидридом лития или другим подходящим восстанавливающим агентом (например, DIBALH) приводит к диолу 4, который затем окисляют периодатом натрия в производное циклогексанона 5. Следующая стадия способа включает реакцию Петерсона кетона 5 с метил(триметилсилил)ацетатом. Полученный аллиловый сложный эфир 6 обрабатывают диизобутилалюмогидридом и образовавшийся аллиловый спирт 7 превращают, в свою очередь, в нужный фосфиноксид 8, содержащий цикл А. Превращение 7 в 8 включает 3 стадии, а именно, тозилирование in situн-бутиллитием и п-толуолсульфонилхлоридом с последующей реакцией с литиевой солью дифенилфосфина и окислением пероксидом водорода.
Несколько соединений 2-метилен-19-нор-витамина D общей структуры IV можно синтезировать с помощью синтона 8, содержащего А-цикл, и соответствующего кетона Виндауса-Грундманна II c боковой цепью нужной структуры. Таким образом, например, сочетанием по Виттигу-Хорнеру литийфосфиноксикарбаниона, получаемого из 8 и н-бутиллития действием кетона Грундманна 9 (с защищенным гидроксилом в 25 положении), полученного по опубликованной методике [Sicinski et al., J. Med. Chem. 37, 3730 (1994)] получают ожидаемое защищенное соединение витамина 10, которое после снятия защиты с помощью катионообменной смолы AG 50W-X4 дает 1α,25-дигидрокси-2-метилен-19-нор-витамин D3 (11).
C-20 эпимеризацию осуществляют аналогичной реакцией сочетания фосфиноксида 8 с кетоном Грундманна 13 с защищенной (20S)-25-гидроксильной группой (схема II) и получают 19-нор-витамин 14, который после гидролиза гидроксизащитных групп дает (20S)-1α,25-дигидрокси-2-метилен-19-нор-витамин D3 (15). Как указано выше, другие 2-метиленовые производные 19-нор-витамина D могут быть синтезированы описанными в описании изобретения способами. Например, 1α-гидрокси-2-метилен-19-нор-витамин D3 может быть получен из кетона Грундманна (g).
Все документы, цитируемые в описании, включая патенты и патентные заявки, включены в данную заявку в качестве ссылок. Примеры, представленные ниже, предназначены для того, чтобы иллюстрировать конкретные варианты осуществления изобретения, и они никоим образом не ограничивают изобретение, включая формулу изобретения.
Примеры
В заявке используют следующие сокращения:
Получение соединений формулы I описано в патенте США № 5843928 и изложено ниже:
В указанных примерах конкретные продукты, обозначенные арабскими цифрами (например, 1, 2, 3 и т.п.), относятся к конкретным структурам, обозначенным таким образом в предшествующем описании, в схеме I и в схеме II.
ПРИМЕР 1
Получение 1α,25-дигидрокси-2-метилен-19-нор-витамина D3 (11)
Согласно схеме I: исходное производное - метиловый эфир хинной кислоты 1 получают из имеющейся в продаже (-)-хинной кислоты, как описано ранее [Perlman et al., Tetrahedron Lett. 32, 7663 (1991) и DeLuca et al., U.S. Pat. No. 5086191].
1: Т.пл. 82-82,5°C (из гексана).
1H ЯМР (CDCl3) δ 0,098, 0,110, 0,142 и 0,159 (каждый 3Н, каждый с, 4×SiCH3), 0,896 и 0,911 (9Н и 9Н, каждый с, 2×Si-t-Bu), 1,820 (1Н, дд, J=13,1, 10,3 Гц), 2,02 (1Н, ддд, J=14,3, 4,3, 2,4 Гц), 2,09 (1Н, дд, J=14,3, 2,8 Гц), 2,19 (1Н, ддд, J=13,1, 4,4, 2,4 Гц), 2,31 (1Н, д, J=2,8 Гц, ОН), 3,42 (1Н, м; после D2O дд, J=8,6, 2,6 Гц), 3,77 (3Н, с), 4,12 (1Н, м), 4,37 (1Н, м), 4,53 (1Н, ушир.с, ОН).
(a) Окисление 4-гидроксигруппы в метиловом эфире хинной кислоты (соединение 1)
Метиловый сложный эфир (3R,5R)-3,5-бис[(трет-бутилдиметилсилил)окси]-1-гидрокси-4-оксоциклогексанкарбоновой кислоты (2). К перемешиваемому раствору гидрата хлорида рутения (III) (434 мг, 2,1 ммоль) и периодата натрия (10,8 г, 50,6 ммоль) в воде (42 мл) прибавляют раствор метилхинната 1 (6,09 г, 14 ммоль) в CCl4/CH3CN (1:1, 64 мл) и энергично перемешивают в течение 8 ч. Прибавляют несколько капель 2-пропанола, смесь выливают в воду и экстрагируют хлороформом. Органические экстракты объединяют, промывают водой, сушат (MgSO4) и упаривают, получая темный маслянистый остаток (около 5 г), который очищают флэш-хроматографией. Элюирование смесью гексан/этилацетат (8:2) дает чистый маслообразный 4-кетон 2 (3,4 г, 56%):
1H ЯМР (CDCl3) δ 0,054, 0,091, 0,127 и 0,132 (каждый 3Н, каждый с, 4×SiCH3), 0,908 и 0,913 (9Н и 9Н, каждый с, 2×Si-t-Bu), 2,22 (1Н, дд, J=13,2, 11,7 Гц), 2,28 (1Н, ˜дт J=14,9, 3,6 Гц), 2,37 (1Н, дд, J=14,9, 3,2 Гц), 2,55 (1Н, ддд, J=13,2, 6,4, 3,4 Гц), 3,79 (3Н, с), 4,41 (1Н, т, J˜3,5 Гц), 4,64 (1Н, с, ОН), 5,04 (1Н, дд, J=11,7, 6,4 Гц);
MC m/z (относительная интенсивность) M+ отсутствует, 375 (M+-t-Bu, 32), 357 (M+-t-Bu-H2O, 47), 243 (31), 225 (57), 73 (100).
(b) Реакция Виттига 4-кетона (соединение 2)
Метиловый эфир (3R,5R)-3,5-бис[(трет-бутилдиметилсилил)окси]-1-гидрокси-4-метиленциклогексанкарбоновой кислоты (3). К метилтрифенилфосфонийбромиду (2,813 г, 7,88 ммоль) в безводном ТГФ (32 мл) прибавляют по каплям n-BuLi(2,5 M в смеси гексанов, 6,0 мл, 15 ммоль) при 0°C в атмосфере аргона при перемешивании. Затем прибавляют еще одну порцию MePh3P+Br- (2,813 г, 7,88 ммоль) и раствор перемешивают при 0°C в течение 10 мин и при комнатной температуре в течение 40 мин. Оранжево-красную смесь опять охлаждают до 0°C и в реакционную колбу сифонируют раствор 4-кетона 2 (1,558 г, 3,6 ммоль) в безводном ТГФ (16+2 мл) в течение 20 мин. Реакционную смесь перемешивают при 0°C в течение 1 часа и при комнатной температуре в течение 3 ч. Затем смесь осторожно выливают в рассол, содержащий 1% HCl, и экстрагируют этилацетатом и бензолом. Объединенные органические экстракты промывают разбавленным NaHCO3 и рассолом, сушат (MgSO4), упаривают и получают оранжевый маслообразный остаток (приблизительно 2,6 г), который очищают флэш-хроматографией. Элюированием смесью гексан/этилацетат (9:1) получают чистое 4-метиленовое соединение 3 в виде бесцветного масла (368 мг, 24%):
1H ЯМР (CDCl3) δ 0,078, 0,083, 0,092, и 0,115 (каждый 3Н, каждый с, 4×SiCH3),0,889 и 0,920 (9Н и 9Н, каждый с, 2×Si-t-Bu), 1,811 (1Н, дд, J=12,6, 11,2 Гц), 2,10 (2Н, м), 2,31 (1Н, дд, J=12,6, 5,1 Гц), 3,76 (3Н, с), 4,69 (1Н, т, J=3,1 Гц), 4,78 (1Н, м), 4,96 (2Н, м; после D2O 1Н, ушир.с), 5,17 (1Н, т, J=1,9 Гц);
MC m/z (относительная интенсивность) M+ отсутствует 373 (M+-t-Bu, 57), 355 (M+-t-Bu-H2O, 13), 341 (19), 313 (25), 241 (33), 223 (37), 209 (56), 73 (100).
(c) Восстановление сложноэфирной группы в 4-метиленовом соединении 3
[(3R,5R)-3,5-бис[(трет-бутилдиметилсилил)окси]-1-гидрокси-4-метиленциклогексил]метанол (4). (i) К перемешиваемому раствору сложного эфира 3 (90 мг, 0,21 ммоль) в безводном ТГФ (8 мл) прибавляют алюмогидрид лития (60 мг, 1,6 ммоль) при 0°С в атмосфере аргона. Охлаждающую баню убирают через 1 ч и продолжают перемешивание при 6°С в течение 12 ч и при комнатной температуре в течение 6 ч. Избыток реагента разлагают насыщенным водным раствором Na2SO4 и смесь экстрагируют этилацетатом и эфиром, сушат (MgSO4) и упаривают. Флэш-хроматографией остатка смесью гексан/этилацетат (9:1) выделяют непрореагировавший субстрат (12 мг) и чистый кристаллический диол 4 (35 мг, 48% в расчете на возвращенный сложный эфир 3):
1H ЯМР (CDCl3 + D2О) δ 0,079, 0,091, 0,100, и 0,121 (каждый 3Н, каждый с, 4×SiCH3), 0,895 и 0,927 (9Н и 9Н, каждый с, 2×Si-t-Bu), 1,339 (1Н, т, J˜12 Гц), 1,510 (1Н, дд, J=14,3, 2,7 Гц), 2,10 (2Н, м), 3,29 и 3,40 (1Н и 1Н, каждый д, J=11,0 Гц) 4,66 (1Н, т, J˜2,8 Гц), 4,78 (1Н, м), 4,92 (1Н, т, J=1,7 Гц), 5,13 (1Н, т, J=2,0 Гц);
MC m/z (относительная интенсивность): M+ отсутствует, 345 (M+-t-Bu, 8), 327(M+-t-Bu-H2O, 22), 213 (28), 195 (11), 73(100).
(ii) Гидрид диизобутилалюминия (1,5 M в толуоле, 2,0 мл, 3 ммоль) прибавляют к раствору сложного эфира 3 (215 мг, 0,5 ммоль) в безводном эфире (3 мл) при -78°C в атмосфере аргона. Смесь перемешивают при -78°C в течение 3 ч и при -24°C в течение 1,5 ч, разбавляют эфиром (10 мл) и гасят медленным прибавлением 2N тартрата калия-натрия. Раствор согревают до комнатной температуры и перемешивают в течение 15 мин, выливают в рассол и экстрагируют этилацетатом и эфиром. Органические экстракты объединяют, промывают разбавленной (около 1%) HCl и рассолом, сушат (MgSO4) и упаривают. Кристаллический остаток очищают флэш-хроматографией. Элюируют смесью гексан/этилацетат (9:1) и получают кристаллический диол 4 (43 мг, 24%).
(d) Расщепление вицинального диола 4
(3R,5R)-3,5-бис[(трет-бутилдиметилсилил)окси]-4-метиленциклогексанон (5). Воду, насыщенную периодатом натрия (2,2 мл), прибавляют к раствору диола 4 (146 мг, 0,36 ммоль) в метаноле (9 мл) при 0°C. Раствор перемешивают при 0°C в течение 1 ч, выливают в рассол и экстрагируют эфиром и бензолом. Органические экстракты объединяют, промывают рассолом, сушат (MgSO4) и упаривают. Маслообразный остаток растворяют в гексане (1 мл) и наносят на картридж Sep-Pak с диоксидом кремния. Чистое производное 4-метиленциклогексанона 5 (110 мг, 82%) элюируют смесью гексан/этилацетат (95:5) в виде бесцветного масла:
1H ЯМР (CDCl3) δ 0,050 и 0,069 (6Н и 6Н, каждый с, 4×SiCH3), 0,881 (18Н, с, 2×Si-t-Bu), 2,45 (2Н, ддд, J=14,2, 6,9, 1,4 Гц), 2,64 (2Н, ддд, J=14,2, 4,6, 1,4 Гц), 4,69 (2Н, дд, J=6,9, 4,6 Гц), 5,16 (2Н, с);
MC m/z (относительная интенсивность): M+отсутствует, 355 (M+-Me, 3), 313 (M+-t-Bu, 100), 73 (76).
(e) Получение аллилового сложного эфира 6
Метиловый эфир [(3'R,5'R)-3',5'-бис[(трет-бутилдиметилсилил)окси]-4'-метиленциклогексилиден]уксусной кислоты (6). К раствору диизопропиламина (37 мкл, 0,28 ммоль) в безводном ТГФ (200 мкл) при перемешивании прибавляют n-BuLi (2,5 M в смеси гексанов, 113 мкл, 0,28 ммоль) в атмосфере аргона при -78°C, затем прибавляют метил(триметилсилил)ацетат (46 мкл, 0,28 ммоль). Через 15 мин по каплям прибавляют кетосоединение 5 (49 мг, 0,132 ммоль) в безводном ТГФ (200+80 мкл). Раствор перемешивают при -78°C в течение 2 ч, и реакционную смесь гасят насыщенным NH4Cl, выливают в рассол и экстрагируют эфиром и бензолом. Объединенные органические экстракты промывают рассолом, сушат (MgSO4) и упаривают. Остаток растворяют в гексане (1 мл) и наносят на картридж Sep-Pak с диоксидом кремния. Элюируют гексаном и смесью гексан/этилацетат (98:2) и получают чистый аллиловый эфир 6 (50 мг, 89%) в виде бесцветного масла:
1H ЯМР(CDCl3) δ 0,039, 0,064 и 0,076 (6Н, 3Н, и 3Н, каждый с, 4×SiCH3), 0,864 и 0,884 (9Н и 9Н, каждый с, 2×Si-t-Bu), 2,26 (1Н, дд, J=12,8, 7,4 Гц), 2,47 (1Н, дд, J=12,8, 4,2 Гц), 2,98 (1Н, дд, J=13,3, 4,0 Гц), 3,06 (1Н, дд, J=13,3, 6,6 Гц), 3,69 (3Н, с), 4,48 (2Н, м), 4,99 (2Н, с), 5,74 (1Н, с);
MC m/z (относительная интенсивность): M+отсутствует, 426 (M+, 2), 411 (M+-Ме, 4), 369 (M+-t-Bu, 100), 263 (69).
(f) Восстановление аллилового эфира 6
2-[(3'R,5'R)-3',5'-бис[(трет-бутилдиметилсилил)окси]-4'-метиленциклогексилиден]этанол (7). Гидрид диизобутилалюминия (1,5 M в толуоле, 1,6 мл, 2,4 ммоль) медленно прибавляют к перемешиваемому раствору аллилового сложного эфира 6 (143 мг, 0,33 ммоль) в смеси толуол/метиленхлорид (2: 1; 5,7 мл) при -78°C в атмосфере аргона. Перемешивание продолжают в течение 1 ч при -78°C и в течение 25 мин при -46°C (баня циклогексанон/сухой лед). Смесь гасят, медленно прибавляя тартрат натрия-калия (2N, 3 мл), водную HCl (2N, 3 мл) и H2O (12 мл), затем разбавляют метиленхлоридом (12 мл) и экстрагируют эфиром и бензолом. Органические экстракты объединяют, промывают разбавленной (приблизительно 1%) HCl и рассолом, сушат (MgSO4) и упаривают. Остаток очищают флэш-хроматографией. Элюируют смесью гексан/этилацетат (9:1) и получают кристаллический аллиловый спирт 7 (130 мг, 97%):
1H ЯМР(CDCl3) δ 0,038, 0,050, и 0,075 (3Н, 3Н и 6Н, каждый с, 4×SiCH3), 0,876 и 0,904 (9Н и 9Н, каждый с, 2×Si-t-Bu), 2,12 (1Н, дд, J=12,3, 8,8 Гц), 2,23 (1Н, дд, J=13,3, 2,7 Гц), 2,45 (1Н, дд, J=12,3, 4,8 Гц), 2,51 (1Н, дд, J=13,3, 5,4 Гц), 4,04 (1Н, м; после D2O дд, J=12,0, 7,0 Гц), 4,17 (1Н, м; после D2O дд, J=12,0, 7,4 Гц), 4,38 (1Н, м), 4,49 (1Н, м), 4,95 (1Н, ушир. с), 5,05 (1Н, т, J=1,7 Гц), 5,69 (1Н, ˜т, J=7,2 Гц);
MS m/z (относительная интенсивность): 398 (M+, 2), 383 (M+-Me, 2), 365(M+-Me-H20, 4), 341 (M+-t-Bu, 78), 323(M+-t-Bu-H2О, 10), 73 (100).
(g) Превращение аллилового спирта 7 в фосфиноксид 8
[2-[(3'R,5'R)-3',5'-бис[(трет-бутилдиметилсилил)окси]-4'-метиленциклогексилиден]этил]дифенилфосфиноксид (8). К аллиловому спирту 7 (105 мг, 0,263 ммоль) в безводном ТГФ (2,4 мл) прибавляют n-BuLi(2,5 M в смеси гексанов, 105 мкл, 0,263 ммоль) в атмосфере аргона при 0°С. Свежеперекристаллизованный тозилхлорид (50,4 мг, 0,264 ммоль) растворяют в безводном ТГФ (480 мкл) и прибавляют к раствору аллиловый спирт-BuLi. Смесь перемешивают при 0°C в течение 5 мин и оставляют при 0°C. В еще одной сухой колбе, в которой воздух заменен аргоном, n-BuLi (2,5 M в смеси гексанов, 210 мкл, 0,525 ммоль) прибавляют к Ph2PH (93 мкл, 0,534 ммоль в безводном ТГФ (750 мкл) при 0°C при перемешивании. Красный раствор откачивают сифоном под давлением аргона в раствор тозилата до тех пор, пока сохраняется оранжевая окраска (приблизительно до прибавления 1/2 раствора). Полученную смесь перемешивают дополнительно в течение 30 мин и гасят, прибавляя H2О (30 мкл). Растворители упаривают при пониженном давлении и остаток повторно растворяют в метиленхлориде (2,4 мл) и перемешивают с 10% H2О2 при 0°С в течение 1 ч. Органический слой отделяют, промывают холодным водным сульфитом натрия и H2O, сушат (MgSO4) и упаривают. Остаток подвергают флэш-хроматографии. Элюируют смесью бензол/этилацетат (6:4) и получают полукристаллический фосфиноксид 8 (134 мг, 87%):
1H ЯМР(CDCl3) δ 0,002, 0,011 и 0,019 (3Н, 3Н, и 6Н, каждый с, 4×SiCH3), 0,855 и 0,860 (9Н и 9Н, каждый с, 2×Si-t-Bu), 2,0-2,1 (3Н, ушир. м), 2,34 (1Н, м), 3,08 (1Н, м), 3,19 (1Н, м), 4,34 (2Н, м), 4,90 и 4,94 (1Н и 1Н, каждый с,), 5,35 (1Н, ˜кв, J=7,4 Гц), 7,46 (4Н, м), 7,52 (2н, м), 7,72 (4Н, м);
MC m/z (относительная интенсивность): M+ отсутствует,581(M+-1,1), 567 (M+-Me, 3) 525 (M+-t-Bu, 100), 450 (10), 393 (48).
(h) Сочетание по Виттигу-Хорнеру кетона Грундманна 9 с защищенной 25-гидроксигруппой с фосфиноксидом 8
1α,25-Дигидрокси-2-метилен-19-нор-витамин D3 (11). К раствору фосфиноксида 8 (33,1 мг, 56,8 мкмоль) в безводном ТГФ (450 мкл) при 0°C медленно прибавляют n-BuLi (2,5M в гексанах, 23 мкл, 57,5, мкмоль) в атмосфере аргона при перемешивании. Раствор приобретает интенсивную оранжевую окраску. Смесь охлаждают до -78°C и медленно прибавляют предварительно охлажденный (-78°C) раствор кетона 9 с защищенной гидроксигруппой (9,0 мг, 22,8 мкмоль), полученного по опубликованной методике [Sicinski et al., J. Med. Chem. 37, 3730 (1994)], в безводном ТГФ (200+100 мкл). Смесь перемешивают в атмосфере аргона при -78°C в течение 1 часа и при 0°C в течение 18 часов. Прибавляют этилацетат и органическую фазу промывают рассолом, сушат (MgSO4) и упаривают. Остаток растворяют в гексане, наносят на картридж Sep-Pak с диоксидом кремния и промывают смесью гексан/этилацетат (99:1, 20 мл), получая производное 19-нор-витамина 10 (13,5 мг, 78%). Затем картридж Sep-Pak промывают смесью гексан/этилацетат (96:4, 10 мл), чтобы возвратить некоторое количество непрореагировавшего кетона 9, содержащего C,D-циклы (2 мг), и этилацетатом (10 мл) для возвращения дифенилфосфиноксида (20 мг). Для аналитических целей образец защищенного витамина 10 с защитными группами дополнительно очищают ВЭЖХ (колонка Zorbax-Sil 6,2 мм x 25 см, 4 мл/мин), используя систему растворителей гексан/этилацетат (99,9:0,1). Чистое соединение 10 элюируют при Rν 26 мл в виде бесцветного масла: УФ (в гексане) λmax 224, 253, 263 нм;
1H ЯМР(CDCl3) δ 0,025, 0,049, 0,066, и 0,080 (каждый 3Н, каждый с, 4×SiCH3), 0,546 (3Н, с, 18-Н3), 0,565 (6Н, кв, J=7,9 Гц, 3×SiCH2), 0,864 и 0,896 (9Н и 9Н, каждый с, 2×Si-t-Bu), 0,931 (3Н, д, J=6,0 Гц, 21-Н3), 0,947 (9Н, т, J=7,9 Гц, 3×SiCH2СН3), 1,188 (6Н, с, 26- и 27-Н3), 2,00 (2Н, м), 2,18 (1Н, дд, J=12,5, 8,5 Гц, 4β-Н), 2,33 (1Н, дд, J=13,1, 2,9 Гц, 10β-Н), 2,46 (1Н, дд, J=12,5, 4,5 Гц, 4α-Н), 2,52 (1Н, дд, J=13,1, 5,8 Гц, 10α-Н), 2,82 (1Н, ушир. д, J=12 Гц, 9β-Н), 4,43 (2Н, м, 1β- и 3α-Н), 4,92 и 4,97 (1Н и 1Н, каждый с, =СН2), 5,84 и 6,22 (1Н и 1Н, каждый д, J=11,0 Гц, 7- и 6-Н);
MC m/z (относительная интенсивность): 758 (M+, 17), 729 (M+-Et, 6), 701 (M+-t-Bu, 4) 626 (100), 494 (23), 366 (50) 73 (92).
Витамин 10 с защитными группами (4,3 мг) растворяют в бензоле (150 мкл) и прибавляют смолу (AG 50W-X4, 60 мг; предварительно промытую этанолом) в метаноле (800 мкл). Смесь перемешивают при комнатной температуре в атмосфере аргона в течение 17 ч, разбавляют смесью этилацетат/эфир (1:1, 4 мл) и декантируют. Смолу промывают эфиром (8 мл) и объединенные органические фазы промывают рассолом, насыщенным NaHCO3, сушат (MgSO4) и упаривают. Остаток очищают ВЭЖХ (колонка Zorbax-Sil 62 мм Ч 25 см, 4 мл/мин), используя систему растворителей гексан/2-пропанол (9:1). Аналитически чистый 2-метилен-19-нор-витамин 11 (2,3 мг, 97%) выделяют при Rν 29 мл (1α,25-дигидроксивитамин D3 элюируют при Rν 52 мл в той же системе) в виде белого твердого вещества: УФ (в EtOH) λmax 243,5, 252; 262,5 нм;
1H ЯМР(CDCl3) δ 0,552 (3Н, с, 18-Н3), 0,941 (3Н, д, J=6,4 Гц, 21-Н3), 1,222(6Н, с,26- и 27-Н3), 2,01 (2Н, м), 2,27-2,36 (2Н, м), 2,58 (1Н, м), 2,80-2,88 (2Н, м), 4,49 (2Н, м,1β- и 3α-Н), 5,10 и 5,11 (1Н и 1Н, каждый с, =СН2), 5,89 и 6,37 (1Н и 1Н, каждый д, J=11,3 Гц, 7- и 6-Н);
MC m/z (относительная интенсивность): 416 (M+, 83), 398 (25), 384 (31), 380 (14), 351 (20), 313 (100).
ПРИМЕР 2
Получение (20S)-1α,25-дигидрокси-2-метилен-19-нор-витамина D3 (15)
На схеме II показано получение кетона Грундманна 13 с защищенной (20S)-25-гидроксигруппой, и реакция его сочетания с фосфиноксидом 8 (полученным, как описано в примере 1).
(а) Силилирование гидроксикетона 12
(20S)-25-[(Триэтилсилил)окси]-дез-A,B-холестан-8-он (13). Раствор кетона 12 (Tetrionics, Inc. Madison,WI.; 56 мг, 0,2 ммоль) и имидазола (65 мг, 0,95 ммоль) в безводном ДМФА (1,2 мл) обрабатывают триэтилсилилхлоридом (95 мкл, 0,56 ммоль) и смесь перемешивают при комнатной температуре в атмосфере аргона в течение 4 ч. Прибавляют этилацетат и воду и органический слой отделяют. Этилацетатный слой промывают водой и рассолом, сушат (MgSO4) и упаривают. Остаток пропускают через картридж Sep-Pak с диоксидом кремния в смеси гексан/этилацетат (9:1) и после упаривания очищают ВЭЖХ (колонка Zorbax-Sil 9,4 мм × 25 см, 4 мл/мин), используя систему растворителей гексан/этилацетат (9:1). Чистый кетон 13 с защищенной гидроксигруппой (55 мг, 70%) элюируют при Rν 35 мл в виде бесцветного масла.
1H ЯМР(CDCl3) δ 0,566 (6Н, кв, J=7,9 Гц, 3×SiCH2), 0,638 (3Н, с, 18-Н3), 0,859 (3Н, д, J=6,0 Гц, 21-Н3), 0,947 (9Н, т, J=7,9 Гц, 3×SiCH2СН3), 1,196 (6Н, с, 26- и 27-Н3), 2,45 (1Н, дд, J=11,4, 7,5 Гц, 14α-Н).
(b) Сочетание по Виттигу-Хорнеру кетона Грундманна соединения 13, содержащего защищенную (20S)-25-гидроксигруппу, с фосфиноксидом 8
(20S)-1α,25-Дигидрокси-2-метилен-19-нор-витамин D3 (15). К раствору фосфиноксида 8 (15,8 мг, 27,1 мкмоль) в безводном ТГФ (200 мкл) при 0°C медленно прибавляют n-BuLi (2,5M в смеси гексанов, 11 мкл, 27,5 мкмоль) в атмосфере аргона при перемешивании. Раствор приобретает интенсивную оранжевую окраску. Смесь охлаждают до -78°C и медленно прибавляют предварительно охлажденный (-78°C) раствор кетона 13 с защищенной гидроксигруппой (8,0 мг, 20,3 мкмоль) в безводном ТГФ (100 мкл). Смесь перемешивают в атмосфере аргона при -78°C в течение 1 ч и при 0°C в течение 18 ч. Прибавляют этилацетат и органическую фазу промывают рассолом, сушат (MgSO4) и упаривают. Остаток растворяют в гексане, наносят на картридж Sep-Pak с диоксидом кремния, промывают смесью гексан/этилацетат (99,5:0,5, 20 мл) и получают производное 19-нор-витамина 14 (7 мг, 45%) в виде бесцветного масла. Затем Sep-Pak картридж промывают смесью гексан/этилацетат (96:4, 10 мл), чтобы возвратить некоторое количество непрореагировавшего кетона 13, содержащего C,D-циклы (4 мг), и этилацетатом (10 мл), чтобы возвратить дифенилфосфиноксид (9 мг). Для аналитических целей образец витамина 14 с защитной группой дополнительно очищают ВЭЖХ (колонка Zorbax-Sil 6,2 мм × 25 см, 4 мл/мин), используя систему растворителей гексан/этилацетат (99,9:0,1).
14: УФ (в гексане) λmax 244, 253,5, 263 нм;
1H ЯМР(CDCl3) δ 0,026, 0,049, 0,066 и 0,080 (каждый 3Н, каждый с, 4×SiCH3), 0,541 (3Н, с, 18-Н3), 0,564 (6Н, кв, J=7,9 Гц, 3×SiCH2), 0,848 (3Н, д, J=6,5 Гц, 21-Н3), 0,864 и 0,896 (9Н и 9Н каждый с, 2×Si-t-Bu), 0,945 (9Н, т, J=7,9 Гц, 3×SiCH2СН3), 1,188 (6Н, с, 26- и 27-Н3), 2,15-2,35 (4Н, ушир. м), 2,43-2,53 (3Н, ушир. м), 2,82 (1Н, ушир. д, J=12,9 Гц, 9β-Н), 4,42 (2Н, м, 1β- и 3α-Н), 4,92 и 4,97 (1Н и 1Н каждый с, =СН2), 5,84 и 6,22 (1Н и 1Н, каждый д, J=11,1 Гц, 7- и 6-Н);
MC m/z (относительная интенсивность): 758 (M+, 33), 729 (M+-Et, 7), 701 (M+-t-Bu, 5), 626 (100), 494 (25), 366 (52), 75 (82), 73 (69).
Витамин 14 с защищенной гидроксильной группой (5,0 мг) растворяют в бензоле (160 мкл) и прибавляют смолу (AG 50W-X4, 70 мг, предварительно промытую метанолом) в метаноле (900 мкл). Смесь перемешивают при комнатной температуре в атмосфере аргона в течение 19 ч, разбавляют смесью этилацетат/эфир (1:1, 4 мл) и декантируют. Смолу промывают эфиром (8 мл) и объединенные органические фазы промывают рассолом, насыщенным раствором NaHCO3, сушат (MgSO4) и упаривают. Остаток очищают ВЭЖХ (колонка Zorbax-Sil 62 мм × 25 см, 4 мл/мин), используя систему растворителей гексан/2-пропанол (9:1). Аналитически чистый 2-метилен-19-нор-витамин 15 (2,6 мг, 95%) выделяют при Rν 28 мл, [(20R)-аналог элюируют при Rν 29 мл и 1α,25-дигидроксивитамин D3 при Rν 52 мл в той же системе] в виде белого твердого вещества: УФ (в EtOH) λmax 243,5; 252,5; 262,5 нм; 3H ЯМР(CDCl3) δ 0,551 (3Н, с, 18-Н3), 0,858 (3Н, д, J=6,6 Гц, 21-Н3), 1,215 (6Н, с, 26- и 27-Н3), 1,95-2,04 (2Н, м), 2,27-2,35 (2Н, м), 2,58 (1Н, дд, J=13,3, 3,0 Гц), 2,80-2,87 (2Н, м), (2Н, м, 1β- и 3α-Н), 5,09 и 5,11 (1Н и 1Н, каждый с, =СН2), 5,89 и 6,36 (1Н и 1Н, каждый д, J=11,3 Гц, 7- и 6-Н);
MC m/z (относительная интенсивность): 416 (M+, 100), 398 (26), 380 (13), 366 (21), 313 (31).
БИОЛОГИЧЕСКАЯ АКТИВНОСТЬ 2-МЕТИЛЕНЗАМЕЩЕННЫХ 19-НОР-1,25-(OH)2D3 СОЕДИНЕНИЙ И ИХ 20S-ИЗОМЕРОВ
Биологическая активность соединений формулы I описана в патенте США № 5843928, как изложено ниже. Введение метиленовой группы в положение 2 19-нор-1,25-(OH)2D3 или его 20S-изомера не влияет или слабо влияет на связывание со свиным интестинальным рецептором витамина D. Все соединения связываются одинаково хорошо со свиным рецептором, включая стандарт 1,25-(OH)2D3. На основании упомянутых результатов можно было бы ожидать, что все соединения будут иметь эквивалентную биологическую активность. Однако, удивительно, что в результате замещения метиленовой группой в положение 2 получаются высокоселективные аналоги с их основным воздействием на костную ткань. При введении в течение 7 дней при хронической форме наиболее сильным из испытанных соединений оказался 2-метилен-19-нор-20S-1,25-(OH)2D3 (таблица 1). При дозе 130 пмоль/день его действие на мобилизацию кальция из костей (содержание кальция в сыворотке крови) было примерно по меньшей мере в 10 и, возможно, в 100-1000 раз выше, чем действие нативного гормона. В одинаковых условиях дважды доза 1,25-(OH)2D3 давала содержание кальция в сыворотке крови 13,8 мг/100 мл сыворотки при дозе 130 пмоль. При дозе 260 пмоль/день соединение показывало поразительно высокое содержание кальция в сыворотке крови 14 мг/100 мл сыворотки за счет вымывания из кости. Проявляя избирательность, указанное соединение не приводило к значительному изменению транспорта кальция в кишечнике при дозе или 130, или 260 пмоль, хотя 1,25-(OH)2D3 давал ожидаемое повышение транспорта кальция в кишечнике при единственной испытанной дозе, т.е. 260 пмоль/день. 2-метилен-19-нор-1,25-(OH)2D3 также обладал крайне высокой мобилизацией кальция из костной ткани, как при одной, так и при другой дозе, но также не показал активности в отношении транспорта кальция в кишечнике. Активность указанного соединения в отношении мобилизации кальция из костей, вероятно, в 10-100 раз выше, чем активность 1,25-(OH)2D3. Упомянутые результаты показывают, что 2-метиленовые и 20S-2-метиленовые производные 19-нор-1,25-(OH)2D3 избирательны в отношении мобилизации кальция из костей. Таблица 2 иллюстрирует реакцию содержания кальция в кишечнике и сыворотке крови на единичную большую дозу различных соединений; подтверждая выводы, сделанные при анализе данных таблицы 1.
Результаты показывают, что 2-метилен-19-нор-20S-1,25-(OH)2D3 чрезвычайно эффективен в индуцировании дифференцировки клеток HL-60 в моноциты. 2-метилен-19-нор соединение имеет активность, близкую к активности 1,25-(OH)2D3. Указанные результаты иллюстрируют потенциал 2-метилен-19-нор-20S-1,25-(OH)2D3 и 2-метилен-19-нор-1,25-(OH)2D3 соединений в качестве противораковых средств, особенно средств против лейкемии, рака толстой кишки, рака груди и рака простаты, или средств для лечения псориаза.
Конкурентное связывание аналогов со свиным интестинальным рецептором проводят способом, описанным в работе Dame et al. (Biochemistry 25, 4523-4534,1986).
Дифференцировку HL-60 промиелоцитов в моноциты определяют, как описано в работе Ostrem et al. (J. Biol. Chem. 262, 14164-14171, 1987).
и их 20S-изомеров
в кишечнике (S/М)
в сыворотке крови
(мг/100 мл)
Крысы-самцы (детеныши) от Sprague Dawley Co. (Indianapolis, Ind.) в течение 1 недели получают рацион с недостатком витамина D и содержанием кальция 0,47% и фосфора 0,3%, затем в течение 2 недель они получают тот же рацион с содержанием кальция 0,02% и содержанием фосфора 0,3%. Во время последней недели животным вводят внутрибрюшинно инъекцию указанной дозы соединения в 0,1 мл 95% пропиленгликоля и 5% этанола в течение 7 дней. Контрольные животные получают только 0,1 мл 95% пропиленгликоля и 5% этанол.
Через 24 ч после введения последней дозы крыс умерщвляют и определяют транспорт кальция в кишечнике по методике выворачивания (мешка), как описано ранее, содержание кальция в сыворотке крови определяют атомно-абсорбционной спектрометрией на приборе Perkin Elmer 3110 (Norwalk, Conn.). В группе было 5 крыс, и приведенные величины представляют собой средние (±) SEM.
как ответ на хронические дозы 2-метиленовых производных 19-нор-1,25-(OH)2D3 и их 20S-изомеров
в кишечнике (S/М)
в сыворотке крови (мг/100 мл)
Крысы-самцы (детеныши) (Holtzman strain) от Sprague Dawley Co. (Indianapolis, Ind.) в течение 1 недели получают рацион с содержанием кальция 0,47% и фосфора 0,3%, описанный в работе Suda et al. J. Nutr. 100, 1049-1052, 1970], затем в течение следующих 2 недель они получают тот же рацион с содержанием кальция 0,02% и содержанием фосфора 0,3%. В это время животные получают одиночную внутрияремную инъекцию указанной дозы, растворенной в 0,1 мл смеси 95% пропиленгликоль/5% этанола. Контрольные животные получают только 0,1 мл 95% пропиленгликоля и 5% этанол. Через 24 ч после введения последней дозы крыс умерщвляют и определяют транспорт кальция в кишечнике и содержание кальция в сыворотке крови, как описано в таблице 1. Доза соединений составляет 650 пмоль и число животных в группе - 5. Данные представляют собой средние значения (±) SEM.
Соответственно, соединения нижеследующей формулы Ia, наряду с соединениями формулы I, также охватываются настоящим изобретением:
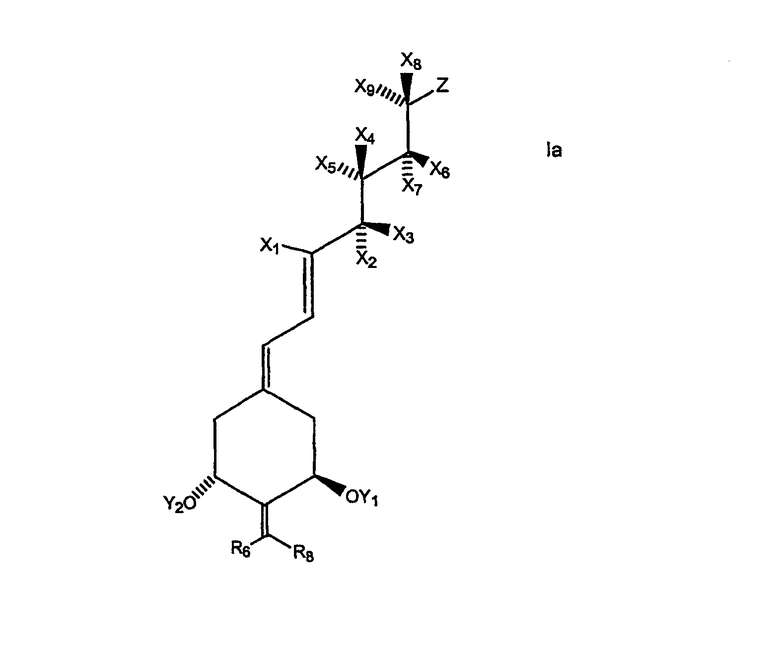
В представленной выше формуле Ia Y1, Y2, R6, R8 и Z такие, как ранее определено в данной заявке. Что касается X1, X2, X3, X4, X5, X6, X7, X8 и X9, они могут быть одинаковыми или разными и выбраны из водорода или низшего алкила, например, С1-5 алкила, такого как метил, этил или н-пропил. Кроме того, парные заместители X1 и X4, или X5, X2 или X3 и X6 или X7, X4 или X5 и X8 или X9, вместе с тремя соседними атомами углерода центральной части соединения, которые соответствуют положениям 8, 14, 13 или 14, 13, 17 или 13, 17, 20, соответственно, могут быть одинаковыми или разными и могут образовывать насыщенный или ненасыщенный, замещенный или незамещенный карбоциклический 3-, 4-, 5-, 6- или 7-членный цикл.
Предпочтительные соединения по настоящему изобретению могут быть представлены одной из следующих формул:
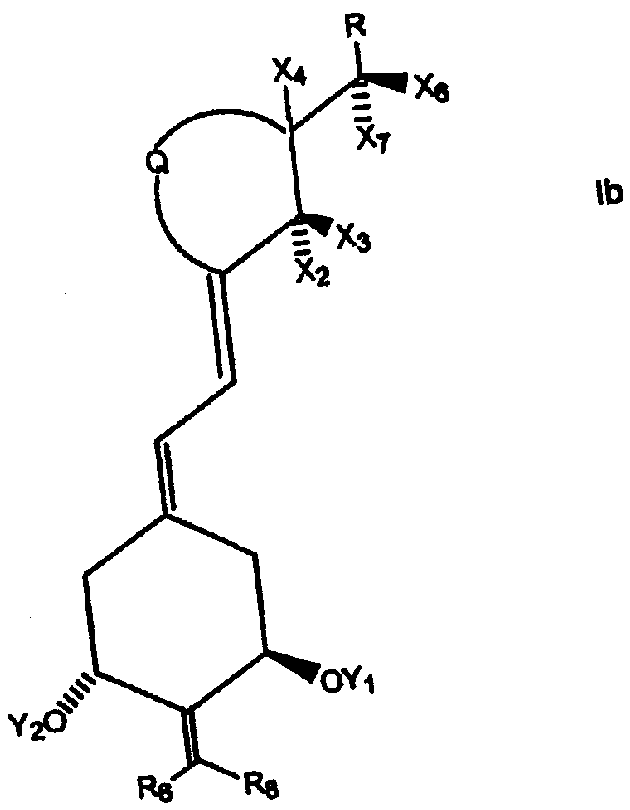
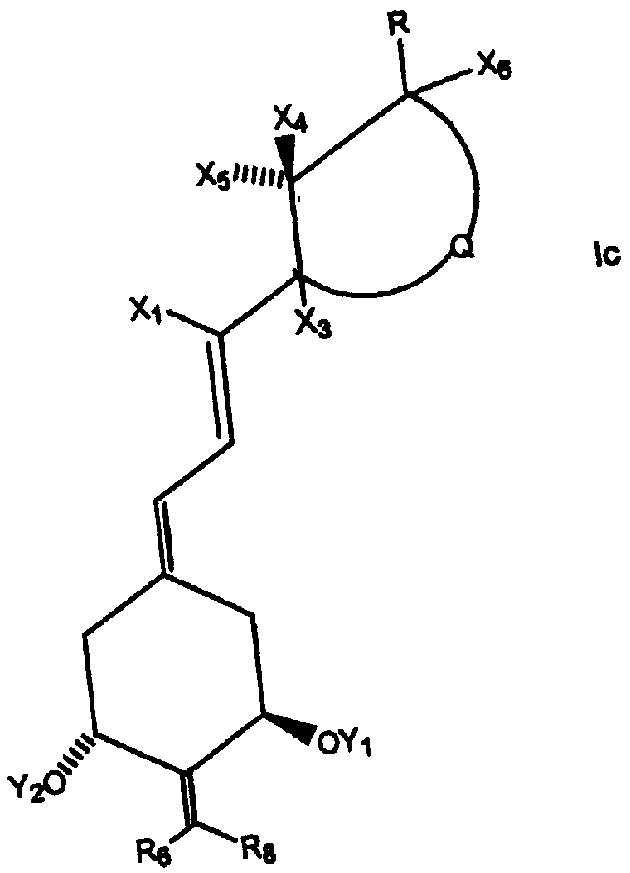
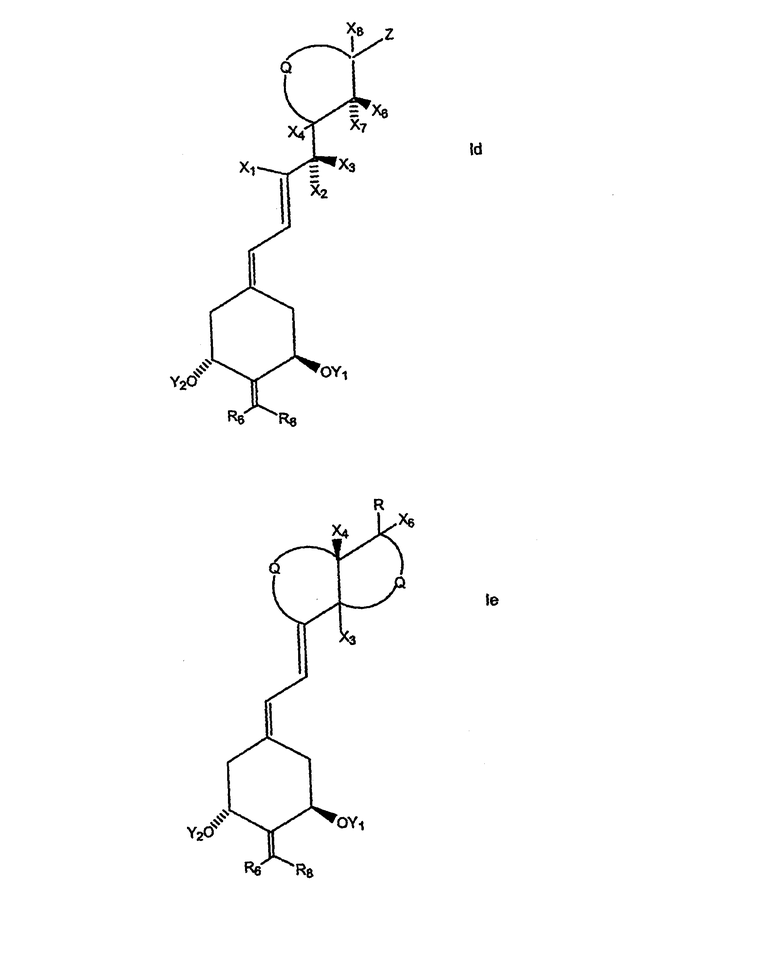

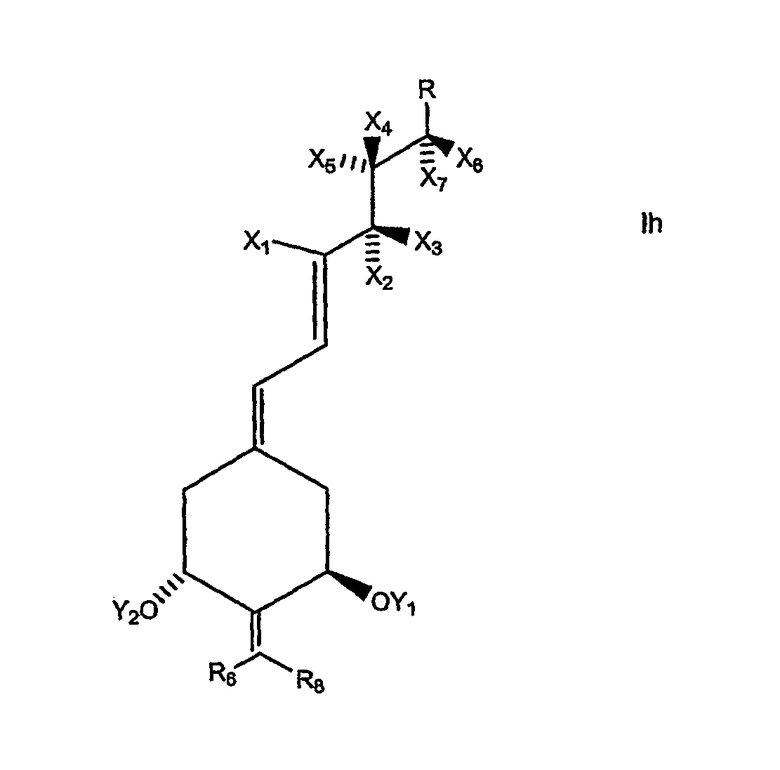
В представленных выше формулах Ib, Ic, Id, Ie, If, Ig и Ih определения Y1, Y2, R6, R8, R, Z, X1, X2, X3, X4, X5, X6, X7 и X8 такие, как ранее приведены в данной заявке. Заместитель Q обозначает насыщенную или ненасыщенную, замещенную или незамещенную углеводородную цепь, содержащую 0, 1, 2, 3 или 4 атома углерода, но предпочтительно, группу -(CH2)k-, где k представляет собой целое число, равное 2 или 3.
Способы получения соединений формул Ia-Ih известны. Конкретно, ссылаются на международную заявку номер PCT/EP94/02294, поданную 7 июля 1994 г., и опубликованную 19 января 1995 г., номер публикации международной заявки WО95/01960.
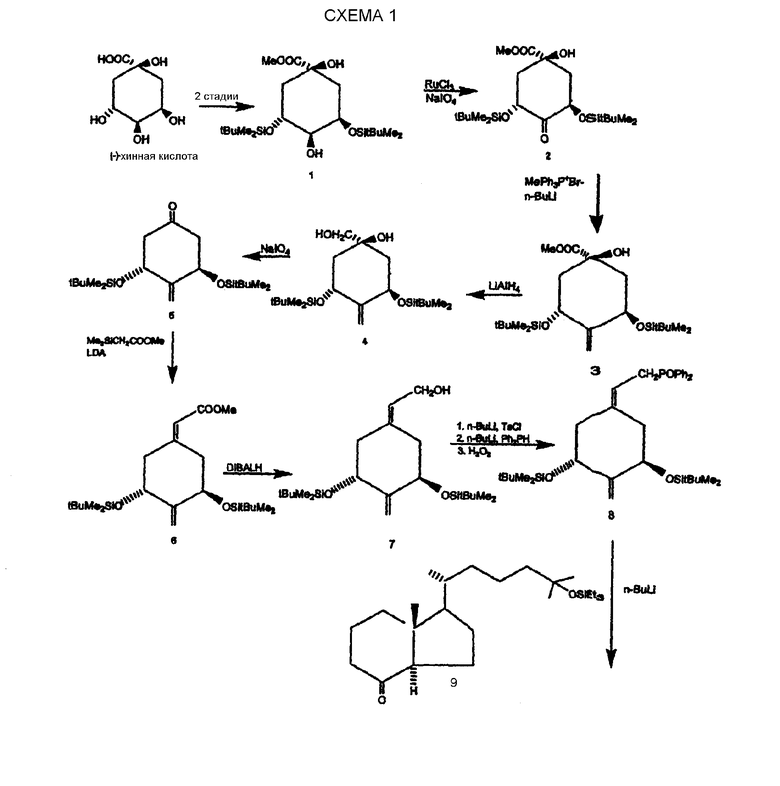
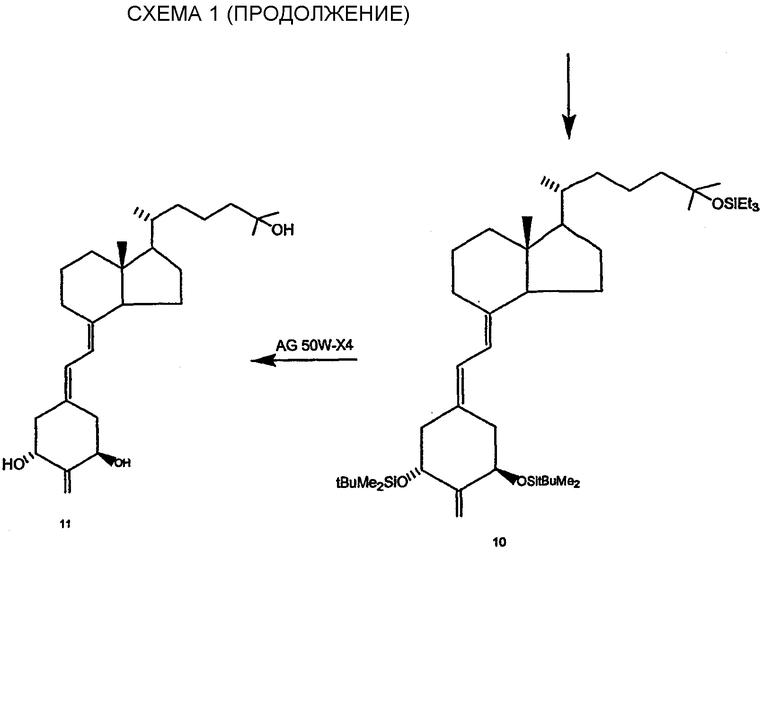

| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ 2-АЛКИЛИДЕН-19-НОР-ВИТАМИНА D ДЛЯ ЛЕЧЕНИЯ СЛАБОСТИ, ПОРАЖЕНИЯ МЫШЦ ИЛИ САРКОПЕНИИ | 2004 |
|
RU2326674C2 |
| ГОМОЛОГИ 1α - ГИДРОКСИВИТАМИНА D С НЕНАСЫЩЕННОЙ БОКОВОЙ ЦЕПЬЮ, КОМПОЗИЦИЯ, СПОСОБСТВУЮЩАЯ СТИМУЛЯЦИИ И УСИЛЕНИЮ ДИФФЕРЕНЦИАЦИИ ЗЛОКАЧЕСТВЕННЫХ КЛЕТОК ЛЕЙКЕМИИ ЧЕЛОВЕКА, СПОСОБ СТИМУЛЯЦИИ И УСИЛЕНИЯ ДИФФЕРЕНЦИАЦИИ ЗЛОКАЧЕСТВЕННЫХ КЛЕТОК ЛЕЙКЕМИИ ЧЕЛОВЕКА | 1989 |
|
RU2057117C1 |
| СПОСОБ ПОЛУЧЕНИЯ α -ГИДРОКСИ-24-ЭПИВИТАМИНА D | 1990 |
|
RU2065851C1 |
| ПРИМЕНЕНИЕ 2-МЕТИЛЕН-19-НОР-(20S)-1α,25-ДИГИДРОКСИВИТАМИНА D ДЛЯ ЛЕЧЕНИЯ ВТОРИЧНОГО ГИПЕРПАРАТИРЕОЗА | 2013 |
|
RU2666995C2 |
| СОЕДИНЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ, СПОСОБЫ ЛЕЧЕНИЯ | 2002 |
|
RU2296121C2 |
| ПРОИЗВОДНОЕ 23-ИН-ВИТАМИНА D | 2011 |
|
RU2558362C2 |
| N-(2-БЕНЗИЛ)-2-ФЕНИЛБУТАНАМИДЫ В КАЧЕСТВЕ МОДУЛЯТОРОВ РЕЦЕПТОРА АНДРОГЕНА | 2005 |
|
RU2378255C2 |
| НОВЫЕ ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ ДЛЯ СИНТЕЗА ПРОИЗВОДНЫХ ВИТАМИНА D | 2004 |
|
RU2317992C2 |
| ПРИМЕНЕНИЕ ПРОИЗВОДНЫХ ВИТАМИНОВ D В ЛЕЧЕНИИ ОСТЕОПОРОЗА И СВЯЗАННЫХ ЗАБОЛЕВАНИЙ КОСТЕЙ, А ТАКЖЕ НОВЫХ ПРОИЗВОДНЫХ ВИТАМИНА D3 | 2001 |
|
RU2253455C2 |
| ИНГИБИТОРЫ ЦИСТЕИНОВОЙ ПРОТЕАЗЫ КАТЕПСИНА | 2005 |
|
RU2399613C2 |
Настоящее изобретение относится к химико-фармацевтической промышленности и касается фармацевтической композиции и способу лечения, включающему введение больному, который нуждается в таком лечении, композиции 2-алкилиденового производного 19-нор-витамина D и бисфосфоната. Конкретно, настоящее изобретение относится к фармацевтическим композициям и способам лечения, включающим введение пациенту, который нуждается в таком лечении, 2-метилен-19-нор-20(S)-1α,25-дигидроксивитамина D3 и бисфосфоната, выбранного из тилудроната, алендроната, золедроната, ибандроната, ризедроната, этидроната, клодроната или памидроната. Заявленное изобретение позволяет повысить эффективность лечения таких заболеваний, как старческий остеопороз, постклимактерический остеопороз, перелом кости, костный трансплантат, остеопения или мужской остеопороз. 3 н. и 15 з.п. ф-лы, 2 табл.
| US 5843923 A, 01.12.1998 | |||
| US 6416737 B1, 09.07.2002 | |||
| АНАЛОГИ ВИТАМИНА D, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1993 |
|
RU2165923C2 |
Авторы
Даты
2008-06-20—Публикация
2004-09-06—Подача