Изобретение относится к медицине, в частности может быть использовано при лечении онкологических заболеваний.
Известен способ лечения злокачественных опухолей [1], заключающийся в интраоперационной терапии опухоли с применением цитостатика.
Однако недостатком данного способа является значительное повреждение окружающих здоровых тканей и органов, что служит причиной недостаточной эффективности данного способа лечения.
Известен способ лечения поверхностно расположенных опухолей [2], заключающийся в нанесении на поверхность опухоли цитостатика или салфетки, пропитанной раствором цитостатика, и последующем контактном воздействии на опухоль низкочастотным ультразвуком при частоте колебаний 45 кГц и амплитуде колебаний 40-80 мкм в течение 3-5 мин.
Однако недостатками вышеуказанного способа лечения опухолей, препятствующими получению высокого лечебного эффекта, являются:
- высокие значения амплитуды колебаний излучающего торца волновода-инструмента, контактно воздействующего на опухоль, с одной стороны, способные вызвать рассеивание опухолевых клеток из первичной опухоли вследствие процессов ее дезинтеграции и ультразвукового распыления, а с другой - ультразвуковую импрегнацию клеток дезинтегрированной опухоли в русло прилежащих кровеносных и лимфатических капилляров и сосудов;
- недостаточность времени ультразвукового воздействия на опухоль в случае наличия массивных опухолей и глубокой их инвазии в ткани;
- опасность кровотечения в зоне ультразвукового воздействия при разрушении обильно васкуляризированной опухоли.
Вышеуказанное создает опасность диссеминации клеток дезинтегрированной контактным ультразвуком опухолевой ткани по лимфатическим и кровеносным сосудам, а также образования имплантационных метастазов.
Наиболее близким по технической сущности и достигаемому результату является способ ультразвуковой интраоперационной внутриполостной химиотерапии [3], заключающийся в том, что после удаления опухоли на ткани раневой полости воздействуют низкочастотным ультразвуком, а затем цитостатиком. При этом первоначально в полость вводят интактную звукопроводящую жидкую среду и воздействуют на ткани низкочастотным ультразвуком в докавитационном режиме с помощью ультразвукового инструмента, имеющего амплитуду колебаний излучающего торца 6±1 мкм, а после эвакуации интактной жидкой среды в полость вводят цитостатик.
Однако вышеуказанный способ лечения опухолей имеет следующие недостатки, снижающие его клиническую эффективность:
- способ не обеспечивает насыщения кровеносной и лимфатической систем, а также интерстициальной среды организма и опосредовано тканей опухоли озон/NO-содержащим веществом, обладающим канцероцидным действием;
- способ не обеспечивает на интраоперационном этапе создания исходной локальной канцероцидной среды в операционной полости перед удалением опухоли;
- способ не обеспечивает после санации операционной полости возможность принудительной импрегнации цитостатика вглубь ее тканей, а также регионарных кровеносных и лимфатических сосудов, что повышает вероятность имплантационного метастазирования опухолевых клеток, оставшихся в прилежащих тканях ложа опухоли;
- малая амплитуда колебаний излучающего торца ультразвукового инструмента (6±1 мкм) не позволяет, с одной стороны, достигнуть выраженных массообменных процессов на границе раздела "интактный раствор - ткани операционной полости", а следовательно, обеспечить качественную санацию операционной полости от раневого содержимого и возможно остатков опухолевых тканей и клеток ("диссеминат"), а с другой - реализовать свой возможный цитодеструктивный потенциал за счет непосредственного воздействия на опухолевые клетки в зоне кавитационной области вблизи излучающего торца;
- способ не обеспечивает поверхностного воздействия высококонцентрированными источниками энергии и высокоактивными химическими группами веществ на опухолевые клетки, обсеменяющие в процессе резекции опухоли операционную полость, ткани стенок операционной полости и оперативного доступа, инструменты, шовный материал, марлевые салфетки, тупферы;
- применяемый в данном способе цитостатик, а именно карбоплатин, применяется в концентрациях, часто не адекватно воздействующих не только на опухолевые клетки, но и, как правило, на здоровые клетки тканей организма.
Задачей изобретения является повышение эффективности профилактики имплантационного метастазирования и улучшение результатов хирургического лечения опухолей.
Задача изобретения достигается тем, что в способе профилактики имплантационного метастазирования при хирургическом лечении опухолей, заключающемся в оперативном доступе к опухоли, удалении опухоли, ультразвуковой санации тканей послеоперационной раневой полости через промежуточную жидкую среду, эвакуации отработанной жидкости, введении в операционную полость канцероцидного вещества и ушивании полости, первоначально осуществляют создание исходной канцероцидной среды в операционной полости озон/NO-ультразвуковой обработкой путем ультразвукового напыления на ткани полости и капсулу опухоли струйно-аэрозольным факелом озон/NO-содержащего лекарственного вещества в виде озонид/NO-содержащей 30-45% масляной эмульсии типа "масло в воде", после чего удаляют опухоль с дополнительным использованием ультразвуковых режущих и коагулирующих инструментов, затем производят поверхностную фотоплазмодинамическую обработку операционной зоны путем ее обдува смесью высокоактивных газовых компонентов 1О2, О*, О2 *, О3, О2, О. с одновременным облучением тканей широкополосным УФ излучением, после этого раневую полость первоначально санируют путем промывания озон/NO-содержащим физиологическим раствором, а затем после эвакуации отработанного раствора операционную полость вновь заполняют озонид/NO-содержащей 20-30% масляной эмульсией типа "масло в воде" и проводят ее озон/NO-ультразвуковую обработку при одновременном барботировании эмульсии озон/NO-содержащей газовой смесью с концентрацией озона 3-5 мг/л, при параметрах: частота ультразвуковых колебаний - 26,5 кГц, амплитуда колебаний излучающего торца волновода-инструмента - 30-60 мкм, экспозиция ультразвуковой санации - 0,5-1 сек/см2 озвучиваемой поверхности с последующим удалением отработанного раствора, после этого, на конечном этапе, осуществляют сначала поверхностную канцероцидную фотоплазмодинамическую обработку тканей операционной полости путем их обдува смесью высокоактивных газовых компонентов 1О2, О*, O2 *, О3, O2, О. и одновременного облучения широкополосным УФ излучением, а затем послойное ушивание раны, которое осуществляют с применением последовательно проводимых: сначала послойного обдува смесью высокоактивных газовых компонентов 1О2, О*, О2 *, О3, О2, О. с одновременным облучением тканей широкополосным УФ излучением, а затем озон/NO-ультразвуковой их обработкой путем напыления струйно-аэрозольным факелом на каждый из ушиваемых слоев озонид/NO-содержащей 30-45% масляной эмульсии типа "масло в воде".
Кроме того, в процессе выполнения операции для предупреждения контактного переноса "диссемината" периодически осуществляют обработку операционных инструментов озон/NO-содержащим раствором, например озонид/NO-содержащей 30-45% масляной эмульсией типа "масло в воде", а также периодическую смену перчаток хирурга.
Проведенный анализ показывает, что при использовании известных способов профилактики имплантационного метастазирования при хирургическом лечении опухолей и технических средств для их осуществления невозможно обеспечить повышение эффективности лечения данной категории больных.
Способ основан на комплексном воздействии на опухолевую ткань, ткани операционной полости и, прежде всего, на диссеминированные опухолевые клетки ("диссеминат") озон/NO-содержащими лекарственными веществами в разных фазовых состояниях (газообразном, газожидкостном и жидком), широкополосным УФ излучением, высокоактивными газовыми компонентами 1О2, О*, O2 *, О3, О2, О., а также высокоамплитудным низкочастотным ультразвуком, которые выступают в качестве высокоэффективных канцероцидных компонентов. При этом активное диспергирующее воздействие низкочастотного ультразвука блокируется средой с большим коэффициентом вязкости - озонид/NO-содержащей 20-30% масляной эмульсией типа "масло в воде", исключающей проявление выраженной кавитации, которая, в то же время, обеспечивает выраженность акустических течений и массообменных процессов в области озвучивания, а следовательно, и качественной санации операционной полости. При этом 20-30% масляную эмульсию типа "масло в воде" применяют в случаях санации операционной полости при ее озвучивании через промежуточную озонид/NO-содержащую масляную эмульсию типа "масло в воде", а ультразвуковое напыление на ткани струйно-аэрозольным факелом и обработку операционных инструментов осуществляют 30-45% озонид/NO-содержащей масляной эмульсией типа "масло в воде".
Кроме того, в комплексе и по отдельности, они являются высокоактивными антибластиками, детоксикаторами, иммуномодуляторами, оксигенаторами, антигипоксантами, регуляторами биологически активных веществ, антипиретиками, анальгетиками, антиоксидантами, фунги-, бактери- и вирулицидами и пр. (Рокитански О. и др, 1981; Риллинг З., Фибан Р., 1985; Педдер В.В. и др., 1985, 2003; Масленников О.В., Конторщикова К.Н., 2005 и др).
Сущность изобретения на примере хирургического лечения рака легкого поясняется чертежами, где изображены:
- на Фиг.1 - блок-схема аппаратного комплекса "ФОТООНКОТОН-О3/NO" (далее - аппаратный комплекс) для озон/NO-ультразвуковой и поверхностной фотоплазмодинамической обработки биотканей, используемой для профилактики имплантационного метастазирования при хирургическом лечении опухолей;
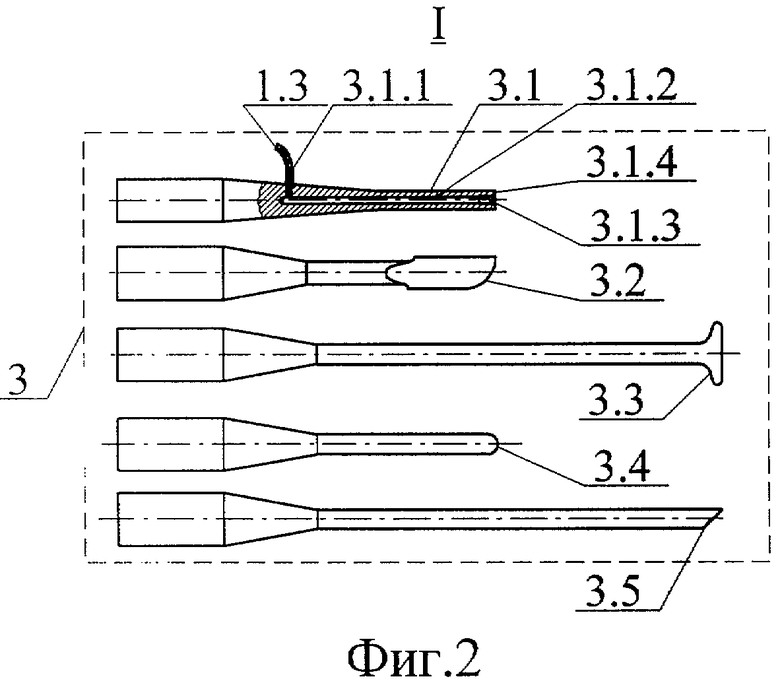
- на Фиг.2 - схематичное изображение набора ультразвуковых хирургических инструментов, используемых на различных этапах операции;
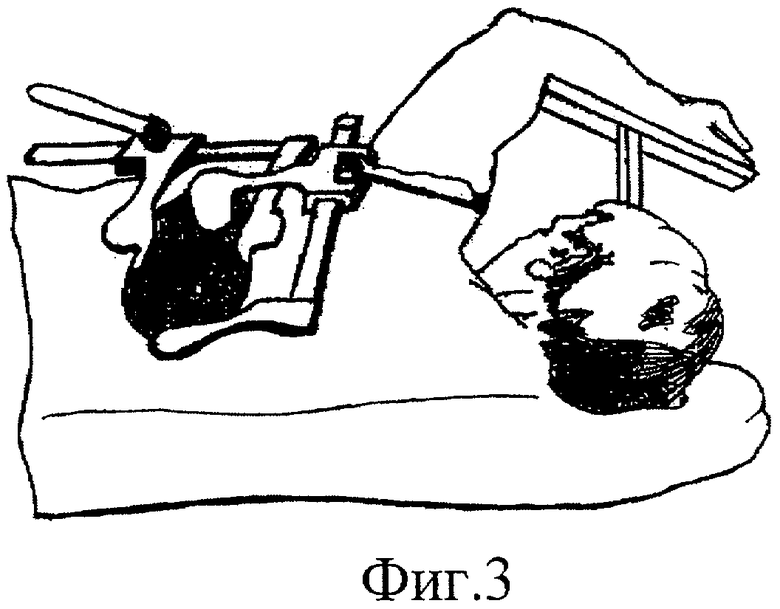
- на Фиг.3 - схематичное изображение положения пациента при торакотомии, выполненной по поводу рака легкого;
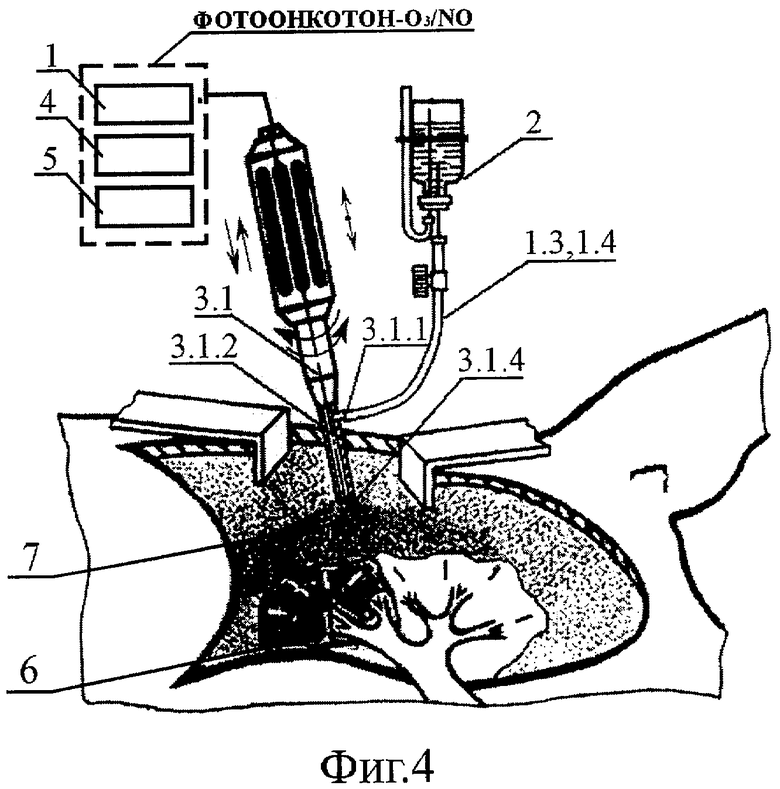
- на Фиг.4 - схема озон/NO-ультразвуковой обработки путем напыления струйно-аэрозольным факелом на ткани операционной полости и капсулу опухоли озон/NO-содержащего лекарственного вещества в виде озонид/NO-содержащей 30-45% масляной эмульсии типа "масло в воде";
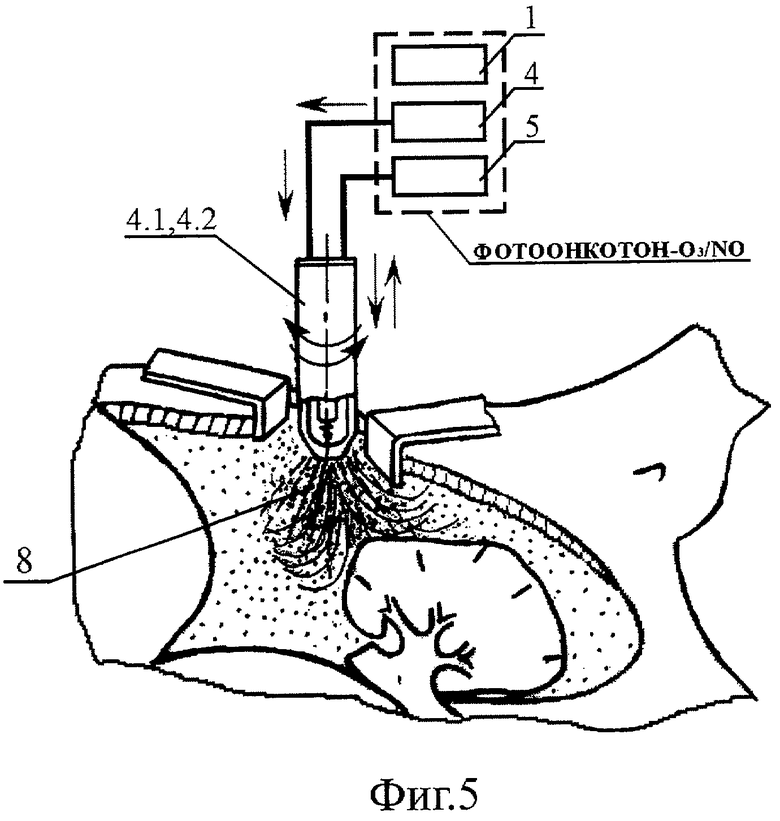
- на Фиг.5 - схема поверхностной канцероцидной фотоплазмодинамической обработки операционной полости обдувом смесью высокоактивных газовых компонентов 1О2, О*, O2 *, О3, O2, О. и облучением тканей широкополосным УФ излучением;
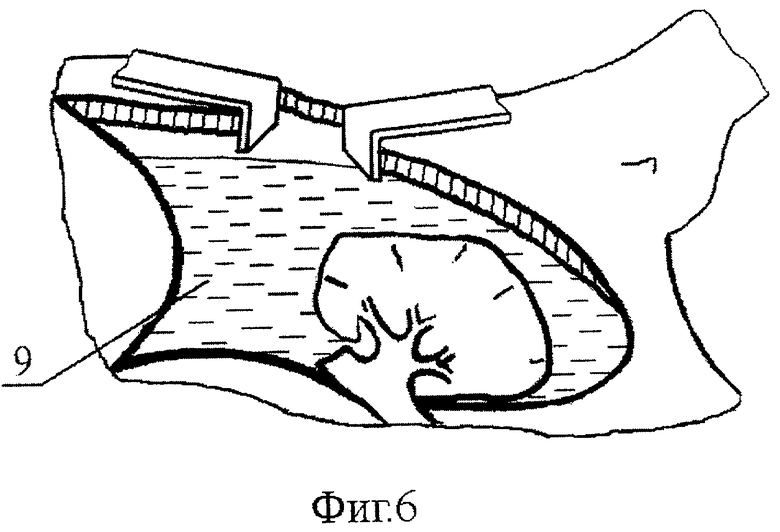
- на Фиг.6 - схема первоначальной санации операционной полости путем промывания ее озонированным физиологическим раствором;
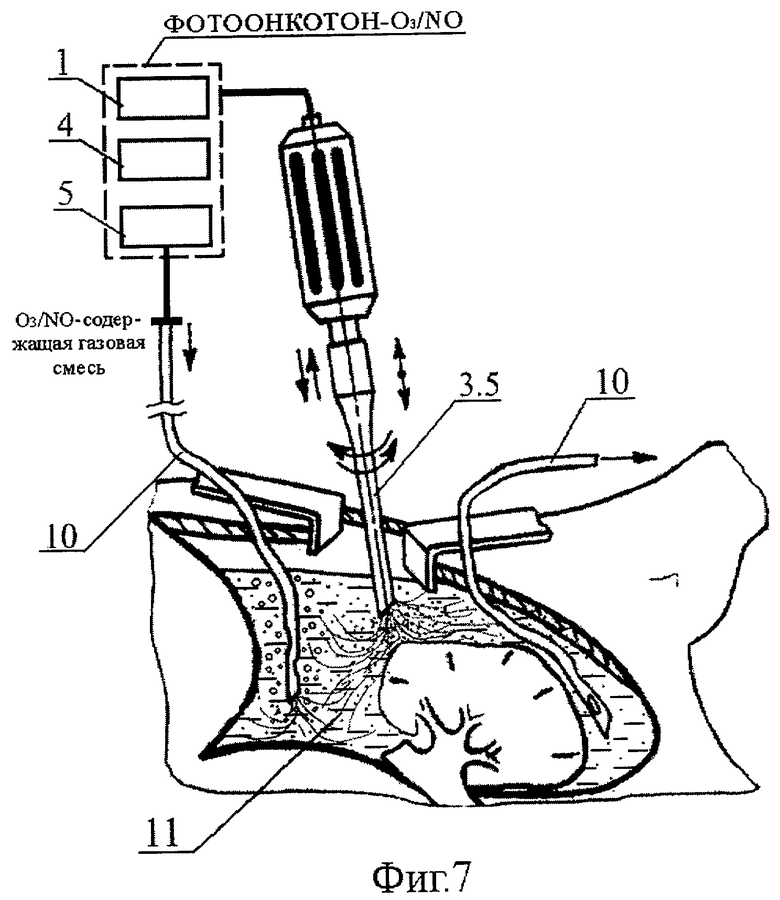
- на Фиг.7 - схема канцероцидной озон/NO-ультразвуковой обработки операционной полости путем озвучивания через промежуточный раствор озонид/NO-содержащей 20-30% масляной эмульсии типа "масло в воде";
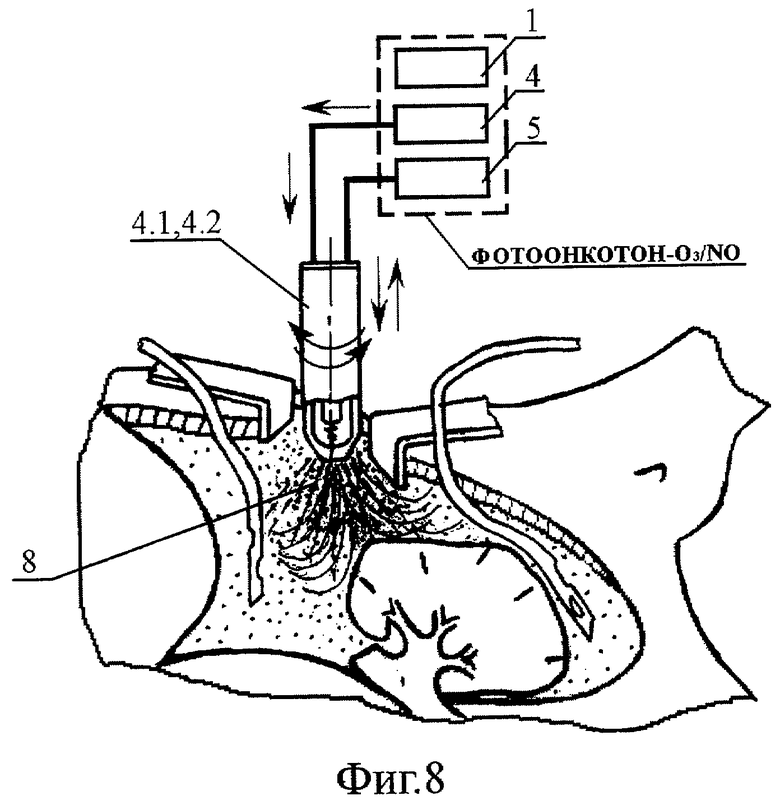
- на Фиг.8 - схема поверхностной канцероцидной фотоплазмодинамической обработки операционной полости обдувом смесью высокоактивных газовых компонентов 1О2, О*, О2 *, О3, О2, О. и облучением тканей широкополосным УФ излучением;
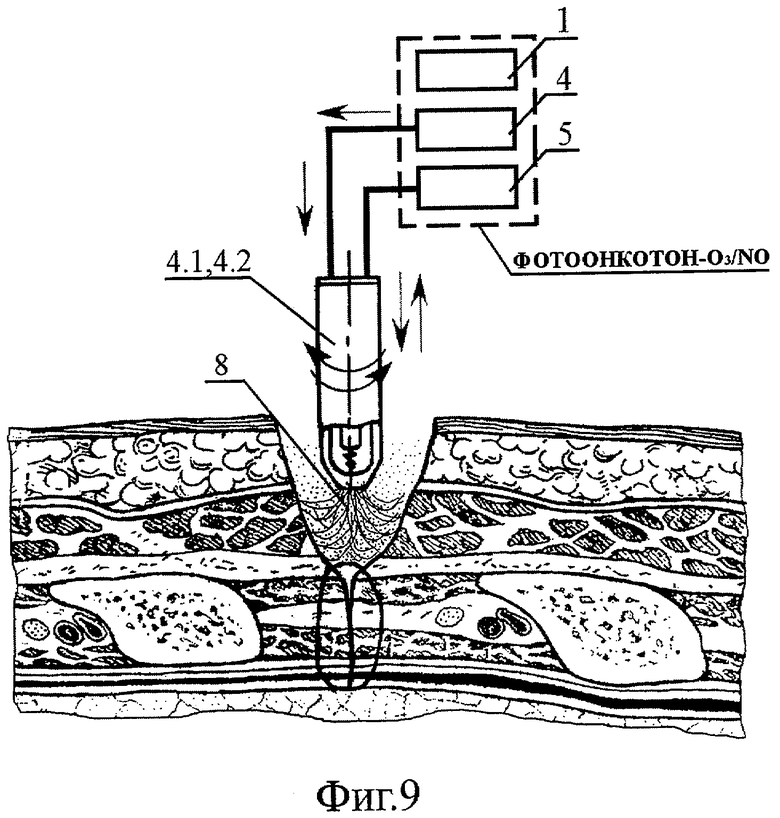
- на Фиг.9 - схема поверхностной канцероцидной фотоплазмодинамической обработки обдувом смесью высокоактивных газовых компонентов 1О2, О*, О2 *, О3, O2, О. и облучением тканей широкополосным УФ излучением послойно ушиваемых тканей оперативного доступа;
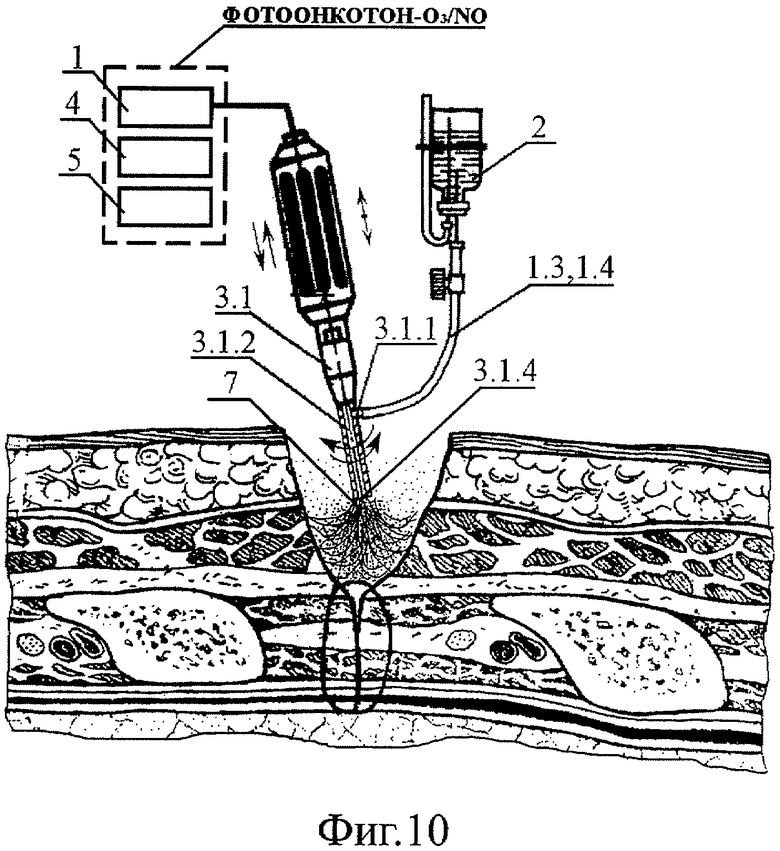
- на Фиг.10 - схема озон/NO-ультразвуковой обработки путем напыления струйно-аэрозольным факелом озонид/NO-содержащей 30-45% масляной эмульсии типа "масло в воде" на послойно ушиваемые ткани оперативного доступа.
При осуществлении способа профилактики имплантационного метастазирования при хирургическом лечении опухолей целенаправленно используют озон/NO-содержащие лекарственные вещества в виде: озон/NO-содержащей газовой смеси с концентрацией озона 3-5 мг/л, озон/NO-содержащего физиологического раствора, озонид/NO-содержащей 20-45% масляной эмульсии типа "масло в воде", как наиболее приемлемые для создания канцероцидной среды в операционной полости.
Для реализации предлагаемого способа профилактики имплантационного метастазирования при хирургическом лечении опухолей применяют аппаратный комплекс (Фиг.1), включающий генератор ультразвуковой 1 (например, выпускаемый серийно аппарат ультразвуковой хирургический "КАВИТОН", г.Омск) с присоединенными к нему акустическими узлами (АКУ) 1.1 и 1.2, которые сопряжены, соответственно, с подающими патрубками 1.3 и 1.4 и через них с емкостью 2, содержащей озон/NO-содержащие лекарственные растворы. Также аппаратный комплекс снабжен набором ультразвуковых хирургических инструментов 3 (Фиг.2), включающим в себя: волновод-инструмент "распылитель" 3.1, волновод-инструмент "скальпель" 3.2, волновод-инструмент "коагулятор чашеобразный" 3.3, волновод-инструмент "коагулятор полусферический" 3.4, волновод-инструмент "пика" 3.5. Кроме того, аппаратный комплекс содержит: генератор высоковольтных электрических импульсов 4 с присоединенными к нему высоковольтными импульсными электроразрядными узлами (ВИЭР-узлами) 4.1. и 4.2 (например, аппарат хирургический "ВИЭРТОН", г.Омск), генератор озон/NO-содержащей газовой смеси 5 с патрубками 5.1 и 5.2 для подачи озон/NO-содержащей газовой смеси соответственно к ВИЭР-узлам 4.1 и 4.2 (например, выпускаемый серийно аппарат физиотерапевтический "ОЗОТРОН", г.Омск).
При этом аппарат ультразвуковой хирургический "КАВИТОН" генерирует колебания низкочастотного диапазона - 26,5 кГц и обеспечивает амплитуду колебаний излучающих торцев волноводов-инструментов - 0-100 мкм. Аппарат физиотерапевтический "ОЗОТРОН" генерирует из атмосферного воздуха озон/NO-содержащую газовую смесь с концентрацией озона не менее 3-5 мг/л. Аппарат хирургический "ВИЭРТОН" обеспечивает генерирование смеси высокоактивных газовых компонентов 1O2, О*, O2 *, О3, О2, О., а также широкополосного УФ излучения длиной волны от 1500 до 6000 Ангестрем.
Предлагаемый способ профилактики имплантационного метастазирования при хирургическом лечении опухолей осуществляют с применением вышеуказанного аппаратного комплекса поэтапно. В процессе выполнения операции в целях предупреждения контактного переноса "диссемината" периодически осуществляют обработку операционных инструментов озон/NO-содержащим раствором, например озонид/NO-содержащей 30-45% масляной эмульсии типа "масло в воде", а также периодическую смену перчаток хирурга.
После выполнения оперативного доступа известными методами (Фиг.3) создают канцероцидную среду в операционной полости озон/NO-ультразвуковой обработкой, осуществляемой путем ультразвукового напыления на ткани полости и капсулу опухоли 6 струйно-аэрозольным факелом 7 предварительно приготовленной озонид/NO-содержащей 30-45% масляной эмульсии типа "масло в воде" (Фиг.4). Для этого из емкости 2 через один из патрубков (например, 1.3), штуцер 3.1.1, закрепленный на волноводе-инструменте ("распылитель") 3.1 и осевое отверстие 3.1.2 к соплу 3.1.3 излучающего торца 3.1.4 (Фиг.2) подают озонид/NO-содержащую 30-45% масляную эмульсию типа "масло в воде". Под действием ультразвуковых колебаний из сопла 3.1.3 генерируется струйно-аэрозольный факел озонид/NO-содержащей эмульсии типа "масло в воде", каждая аэрозольная частица которой, с одной стороны, обладает определенной кинетической энергией, а с другой - высокой энергией Гиббса по поверхности. Указанное позволяет обеспечить проникновение частиц струйно-аэрозольного факела 7 в полости сложной конфигурации и большой глубины, а также внедрение их в поверхностный слой тканей с достижением в них высокой степени канцероцидности.
Затем, в соответствии с общепринятыми приемами абластики онкохирургии, удаляют опухоль 6. Для этого включают генератор ультразвуковой 1 и, используя ультразвуковой режущий инструмент - волновод-инструмент "скальпель" 3.2 (Фиг.2), осуществляют иссечение опухоли 6 с последующим обеспечением дополнительной ультразвуковой термомеханической абластики путем коагуляции зоны резекции ультразвуковым коагулятором волноводом-инструментом "коагулятор чашеобразный" 3.3 или волноводом-инструментом "коагулятор полусферический" 3.4 (Фиг.2), снижающей опасность имплантации "диссемината" вглубь резецированных ранее тканей.
После удаления опухоли 6 и коагуляции зоны резекции осуществляют поверхностную фотоплазмодинамическую обработку операционной полости (Фиг.5). Для этого в операционную полость вводят ВИЭР-узел 4.1 или 4.2, включают генератор высоковольтных электрических импульсов 4 и генератор озон/NO-содержащей газовой смеси 5. Операционную полость обдувают смесью высокоактивных газовых компонентов 8 1О2, О*, О2 *, О3, О2, О. с одновременным облучением тканей широкополосным УФ излучением, обеспечивая при этом инактивацию и биохимическое разрушение поверхностно лежащего "диссемината" и насыщение ими поверхности тканей операционной полости.
Следующим этапом, операционную полость санируют путем заполнения ее озон/NO-содержащим физиологическим раствором 9 и последующего промывания (Фиг.6). После эвакуации отработанного озон/NO-содержащего физиологического раствора 9 и осушения полости в нее устанавливают силиконовые дренажные трубки 10 и вновь заполняют полость озонид/NO-содержащей 20-30% масляной эмульсией типа "масло в воде" 11. Затем в эмульсию 11 вводят волновод-инструмент "пика" 3.5 и проводят озон/NO-ультразвуковую обработку путем равномерного кругового озвучивания операционной полости при параметрах: частота ультразвуковых колебаний - 26,5 кГц, амплитуда колебаний излучающего торца волновода-инструмента - 30-60 мкм (в зависимости от области озвучивания: при озвучивании тканей, прилежащих к ложу опухоли и самой опухоли, а также зоны лимфодиссекции используют амплитуду порядка 30 мкм, а при озвучивании интактных тканей в операцинной полости - порядка 60 мкм), экспозиция ультразвуковой санации - 0,5-1 с/см2 озвучиваемой поверхности.
Одновременно с озвучиванием осуществляют барботирование озонид/NO-содержащей эмульсии 11 озон/NO-содержащей газовой смесью для поддержания высокой степени канцероцидности среды, в которой может иметь место циркуляция "диссемината", экстрагируемого и вымываемого в раствор при инициировании "обратного" звукокапиллярного эффекта в процессе озвучивания стенок операционной полости (В.В.Педдер, 1980). Для этого силиконовую дренажную трубку 10 подсоединяют к включенному в работу генератору озон/NO-содержащей газовой смеси 5.
После озвучивания отработанную озонид/NO-содержащую эмульсию 11 эвакуируют и осушают операционную полость. Следующим этапом, осуществляют поверхностную канцероцидную фотоплазмодинамическую обработку тканей операционной полости (Фиг.8). Для этого включают генератор высоковольтных электрических импульсов 4 и генератор озон/NO-содержащей газовой смеси 5, вводят в операционную полость ВИЭР-узел 4.1 или 4.2 и, осуществляя круговые и возвратно-поступательные перемещения ВИЭР-узла относительно операционной зоны и стенок операционной полости, проводят их обдув смесью высокоактивных газовых компонентов 8 (1O2, О*, O2 *, О3, О2, О.) с одновременным облучением тканей широкополосным УФ излучением, обеспечивая на заключительном этапе обработки операционной полости достижение гарантированной инактивации и разрушения возможно оставшегося на поверхности "диссемината".
Далее производят ушивание раны с применением сначала последовательного и послойного обдува смесью высокоактивных газовых компонентов 8 (1О2, О*, О2 *, О3, О2, О.) с одновременным облучением тканей широкополосным УФ излучением с применением ВИЭР-узла 4.1 или 4.2 (Фиг.9), а затем озон/NO-ультразвуковой обработки путем напыления на каждый из ушиваемых слоев струйно-аэрозольным факелом 7 озонид/NO-содержащей 30-45% масляной эмульсии типа "масло в воде" с применением волновода-инструмента "распылитель" 3.1 (Фиг.10).
Дальнейшее ведение пациента в послеоперационный период осуществляют общепринятыми методами.
ПРИМЕР. Больной Б, 53 года. Диагноз: Центральный рак нижней доли правого легкого. T2N1M0G2. Гистологический вариант - аденокарцинома. Диагноз поставлен на основании рентгенологических данных. Гистологическое исследование трансбронхиального биоптата - умеренно дифференцированная аденокарцинома. Рекомендовано оперативное лечение.
После премедикации и вводного наркоза больному произведена раздельная интубация с положением интубационной трубки в левом главном бронхе. После обработки операционного поля произведена боковая торакотомия в шестом межреберье. Сращения плевральной полости разделены, полость ревизована. В нижней доле правого легкого - опухолевый узел 5×5×7 см. После определения объема резекции проведено создание канцероцидной среды в операционной полости (плевральной полости) согласно предложенному способу профилактики имплантационного метастазирования при хирургическом лечении опухолей. При этом дальнейшие этапы выполнения операции, связанные с реализацией предлагаемого способа, выполнены согласно приведенному выше описанию изобретения и включали в себя:
- выполнение озон/NO-ультразвуковой обработки путем ультразвукового напыления струйно-аэрозольным факелом озонид/NO-содержащей 30-45% масляной эмульсии типа "масло в воде" на поверхность тканей операционной полости;
- выполнение резекционного этапа операции с применением как обычных, так и ультразвуковых инструментов, при этом последние использовались для выделения элементов корня легкого, резекции доли легкого, лимфодиссекции и коагуляционного гемостаза;
- выполнение поверхностной фотоплазмодинамической обработки тканей операционной полости (корня легкого, зоны лимфодиссекции, стенки плевральной полости, верхней и средней доли легкого и др.) путем обдува смесью высокоактивных газовых компонентов 1О2, О*, О2 *, О3, О2, О. с одновременным облучением широкополосным УФ излучением;
- выполнение первоначального санирования операционной полости промыванием озон/NO-содержащим физиологическим раствором с частичным расправлением оставшихся долей легкого, последующей эвакуации отработанного раствора, осушения полости и установки силиконовых дренажей;
- выполнение озон/NO-ультразвуковой обработки операционной полости путем ее заполнения озонид/NO-содержащей 20-30% масляной эмульсией типа "масло в воде" и озвучивание полости низкочастотным ультразвуком при параметрах, указанных в описании изобретения, с одновременным барботированием раствора озон/NO-содержащей газовой смесью;
- выполнение поверхностной фотоплазмодинамической обработки тканей операционной полости путем обдува смесью высокоактивных газовых компонентов 1О2, О*, О2 *, О3, О2, О. с одновременным облучением широкополосным УФ излучением;
- выполнение перемещения интубационной трубки из левого главного бронха в трахею и расправление оставшихся долей правого легкого;
- выполнение ушивания раны с применением первоначально послойного обдува смесью высокоактивных газовых компонентов 1О2, О*, О2 *, О3, О2, О. с одновременным облучением тканей широкополосным УФ излучением, а затем озон/NO-ультразвуковой обработки путем напыления струйно-аэрозольным факелом на каждый из ушиваемых слоев озонид/NO-содержащей 30-45% масляной эмульсии типа "масло в воде";
- присоединение дренажей к пневмосистеме вакуумного аспиратора;
- выполнение общепринятой обработки операционного поля с наложением асептической повязки. Окончание операции.
Послеоперационный период протекал без особенностей. Больной выписан в удовлетворительном состоянии. В течение последующих шести месяцев динамическое рентгенологическое наблюдение не выявило рецидивирования опухолевого процесса, что указывает на достаточность проведенных мероприятий по профилактике имплантационного метастазирования с применением озон/NO-ультразвукового способа лечения.
На клинической базе Омского онкологического диспансера проведена ограниченная клиническая апробация предложенного способа. Пролечено 4 человека с верифицированным диагнозом - рак легкого. В течение шести месяцев пациенты находились под динамическим диспансерным наблюдением. По истечении шести месяцев ни в одном случае не выявлено рецидива опухолевого процесса. В то же время в контрольной группе рентгенологически определены метастатические образования в области корня легкого. Этим пациентам, в установленном порядке, в дальнейшем проводилась лучевая гамма-терапия.
Предлагаемый способ профилактики имплантационного метастазирования при хирургическом лечении опухолей возможно реализовать в различных разделах онкохирургии: в абдоминальной онкохирургии, в онкоурологии и онкогинекологии, в онкохирургии головы и шеи, в онкохирургии мягких тканей, а также хрящевых и костных тканей и пр. Комплекс физико-химических и химических воздействий, реализуемый предлагаемым способом, является универсальным по отношению к различным морфологическим видам, гистологическим типам и степени дифференцировки опухолевой ткани.
Опыт ограниченной клинической апробации подтвердил то, что предлагаемый способ обеспечивает:
- качественную санацию тканей операционной полости вторичными факторами высокоамплитудного низкочастотного ультразвука, воздействующего на ткани операционной полости через промежуточную канцероцидную озонированную масляную эмульсию типа "масло в воде", снижающими вероятность имплантационного метастазирования опухолевых клеток при одновременном обеспечении при этом ультразвуковой механодеструкции и дезинтеграции опухолевой ткани в области озвучивания;
- локальное, а также общее принудительное насыщение тканей организма, интерстициальной среды и тканей опухоли озон/NO-содержащим веществом, обладающим канцероцидным действием, как перед удалением опухоли, так и после ее удаления;
- комплексное воздействие на опухоль, возможные остатки "диссемината", а также инструменты, шовный материал, марлевые салфетки и тупферы физико-химическими и химическими факторами (высокоамплитудный низкочастотный ультразвук, широкополосное УФ излучение, химически активные вещества: 1О2, О*, О2 *, О3, О2, О.;
- щадящее отношение к тканям и всему организму в целом за счет применения биосовместимых, высокоактивных озон/NO-содержащих веществ и химически активных групп веществ (1О2, О*, O2 *, О3, О2, О.), позволяющих ограничить применение широко применяемых в онкологии цитостатиков.
Источники информации
1. Патент РФ № 2074736, МПК А61К 47/00, 1997.
2. А.С. СССР № 1686726, МПК А61Н 23/00, 1994.
3. Патент РФ № 2162721, МПК А61N 7/00, 2001.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ МОЧЕВОГО ПУЗЫРЯ ВОСПАЛИТЕЛЬНОЙ ЭТИОЛОГИИ | 2005 |
|
RU2304990C2 |
| СПОСОБ ОЗОН/NO-УЛЬТРАЗВУКОВОЙ ТЕРАПИИ ЭКССУДАТИВНЫХ СИНУСИТОВ | 2006 |
|
RU2322217C2 |
| Способ комбинированного лечения хронического тонзиллита | 2023 |
|
RU2831944C1 |
| СПОСОБ ПОДАВЛЕНИЯ ВИЧ-ИНФЕКЦИИ | 1999 |
|
RU2198664C2 |
| СПОСОБ ЛИПОСАКЦИИ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2005 |
|
RU2297849C2 |
| СПОСОБ ЛЕЧЕНИЯ СИНДРОМА ДИАБЕТИЧЕСКОЙ СТОПЫ | 2004 |
|
RU2277002C1 |
| Способ коррекции уровня интоксикационного синдрома в комплексной терапии хронического гломерулонефрита | 2020 |
|
RU2778900C2 |
| АППАРАТ ДЛЯ ПЛАЗМОДИНАМИЧЕСКОЙ ОБРАБОТКИ ИНФИЦИРОВАННЫХ РАН И ПОЛОСТЕЙ ОРГАНИЗМА | 2004 |
|
RU2258545C1 |
| УСТРОЙСТВО ДЛЯ ЛЕЧЕНИЯ ЛИМФЕДЕМЫ У БОЛЬНЫХ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ | 2011 |
|
RU2479301C2 |
| СПОСОБ ЛЕЧЕНИЯ ДИСТРОФИЧЕСКИХ ЗАБОЛЕВАНИЙ СЕТЧАТКИ ГЛАЗА | 2010 |
|
RU2471454C2 |
Изобретение относится к медицине, к онкологии и может быть использовано для профилактики имплантационного метастазирования при хирургическом лечении опухолей. Для этого осуществляют ультразвуковое напыление на ткани операционной полости и капсулу опухоли струйно-аэрозольным факелом озонид/NO-содержащей 30-45% масляной эмульсии типа "масло в воде". Затем удаляют опухоль с использованием ультразвуковых режущих и коагулирующих инструментов. Операционную зону обдувают смесью высокоактивных газовых компонентов 1O2, О*, О2 *, О3, O2, О. и одновременно облучают ткани широкополосным УФ излучением. После этого раневую полость промывают озон/NO-содержащим физиологическим раствором. После эвакуации отработанного раствора операционную полость вновь заполняют озонид/NO-содержащей 20-30% масляной эмульсией и проводят ее озон/NO-ультразвуковую обработку при одновременном барботировании эмульсии озон/NO-содержащей газовой смесью с концентрацией озона 3-5 мг/л. На конечном этапе осуществляют поверхностную канцероцидную фотоплазмодинамическую обработку, послойное ушивание раны, послойный обдув высокоактивными газовыми компонентами, УФ облучение, напыление озонид/NO-содержащей 30-45% масляной эмульсии на каждый из ушиваемых слоев. Проведение такой тактики позволяет повысить качество санации тканей операционной полости и снизить вероятность метастазирования опухолевых клеток. 1 з.п. ф-лы, 10 ил.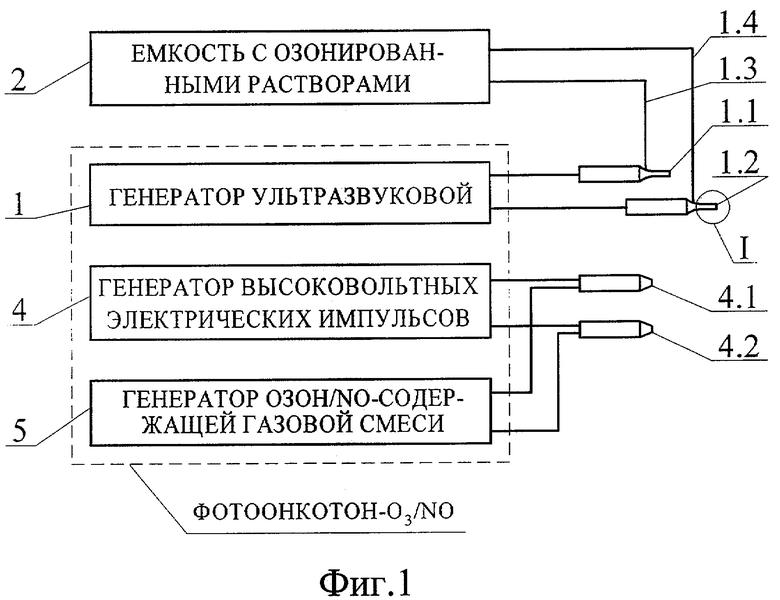
| СПОСОБ ЛЕЧЕНИЯ ПОВЕРХНОСТНО РАСПОЛОЖЕННЫХ ОПУХОЛЕЙ | 1987 |
|
SU1686726A1 |
| СПОСОБ УЛЬТРАЗВУКОВОЙ ИНТРАОПЕРАЦИОННОЙ ВНУТРИПОЛОСТНОЙ ХИМИОТЕРАПИИ | 1999 |
|
RU2162721C2 |
| Дефибриллятор | 1986 |
|
SU1470299A1 |
| Столяров В.И | |||
| Особенности метастазирования, пути профилактики и лечения метастазов рака пищевода | |||
| // Хирургическое и комбинированное лечение опухолей | |||
| Предохранительное устройство для паровых котлов, работающих на нефти | 1922 |
|
SU1996A1 |
| Yusuf U | |||
| et al | |||
| Survival with combined modality therapy after intracerebral recurrence of pleuropulmonary blastoma | |||
| // Med | |||
| Pediatr Oncol | |||
| Способ и аппарат для получения гидразобензола или его гомологов | 1922 |
|
SU1998A1 |
Авторы
Даты
2007-06-10—Публикация
2005-11-09—Подача