Настоящая заявка является частичным продолжением заявки US 09/944524, поданной августа 31, 2001, которая включена в данное описание во всей полноте в качестве ссылки.
1. Область изобретения
Изобретение касается индено[1,2-c]изохинолиновых соединений; композиций, включающих индено[1,2-c]изохинолиновые соединения; и способов лечения или профилактики воспалительного заболевания или реперфузионного нарушения.
2. Предпосылки изобретения
Воспалительные заболевания, такие как артрит, колит и аутоиммунный диабет, обычно имеют очевидные признаки нарушений, отличных от заболеваний, вызванных реперфузионными нарушениями, напримерударом и сердечным приступом, и могут клинически проявляться как особые формы. Однако в основе этих двух типов нарушений могут лежать общие механизмы. В частности, воспалительное заболевание и реперфузионное нарушение могут индуцировать синтез провоспалительных цитокинов и хемокинов, который может, в свою очередь, приводить к продуцированию цитотоксических свободных радикалов, таких как оксид азота (V) и супероксид. NO и супероксид могут взаимодействовать с образованием пероксинитрита (ONOO-) (Szaby et al., Shock 6:79-88, 1996).
Клеточный некроз, индуцированныйONOO-,наблюдаемый привоспалительном заболевании и реперфузионном нарушении, включаетактивацию нуклеарного фермента поли(ADP-рибоза)синтетазы (PARS). Считается, что активация PARS является важной ступенью в клеточном некрозе, наблюдаемом привоспалительном и реперфузионном нарушении (Szaby et al., Trends Pharmacol. Sci. 19:287-98, 1998).
В данной области описан ряд ингибиторов PARS. См., например, Banasik et al., J. Biol. Chem., 267:1569-75, 1992 и Banasik et al., Mol. Cell. Biochem., 138:185-97,1994; WO 00/39104; WO 00/39070; WO 99/59975; WO 99/59973; WO 99/11649; WO 99/11645; WO 99/11644; WO 99/11628; WO 99/11623; WO 99/11311; WO 00/42040; Zhang et al., Biochem. Biophys. Res. Commun., 278:590-98, 2000; White et al., J. Med. Chem., 43:4084-4097, 2000; Griffin et al., J. Med. Chem., 41:5247-5256, 1998; Shinkwin et al., Bioorg. Med. Chem., 7:297-308, 1999 и Soriano et al., Nature Medicine, 7:108-113, 2001. Побочные эффекты, связанные с введением ингибиторов PARS, обсуждаются в Milan et al., Science, 223:589-591, 1984.
Производные индено[1,2-c]изохинолина ранее были описаны в данной области. Например, о цитотоксических ингибиторах некамптотехиновой топоизомеразы Iсообщается у Cushman et al., J. Med. Chem., 43:3688-3698, 2000 и Cushman et al., J. Med. Chem. 42:446-57, 1999; о индено[1,2-c]изохинолинах сообщается в качестве антинеопластических агентову Cushman et al., WO 00/21537 и в качестве ингибиторов неоплазмов у Hrbata et al, WO 93/05023.
Сообщается о синтезах производных индено[1,2-c]изохинолина. Например, см. Wawzonek et al., Org. Prep. Proc. Int. 14:163-8, 1982; Wawzonek et al., Can. J. Chem. 59:2833, 1981; Andoi et al., Bull. Chem. Soc. Japan, 47:1014-17, 1974; Dusemund et al., Arch. Pharm (Weinheim, Ger.), 3 17:381-2, 1984 и Lal et al., Indian J. Chem., Sect. B, 38B:33-39, 1999.
Однако в данной области сохраняется потребность в соединениях, полезных для лечения или профилактики воспалительных заболеваний или реперфузионных нарушений.
Использование какой-либо ссылки в разделе 2 данной заявки не является признанием того, что ссылка относится к предшествующему уровню техники.
3. Краткое описание изобретения
Изобретение отчасти основано на открытии новых замещенных тетрациклических производных бензамида и оказываемых указанными производными действиями при лечении воспаления, некроза клеток и лечении удара и реперфузионных нарушений.
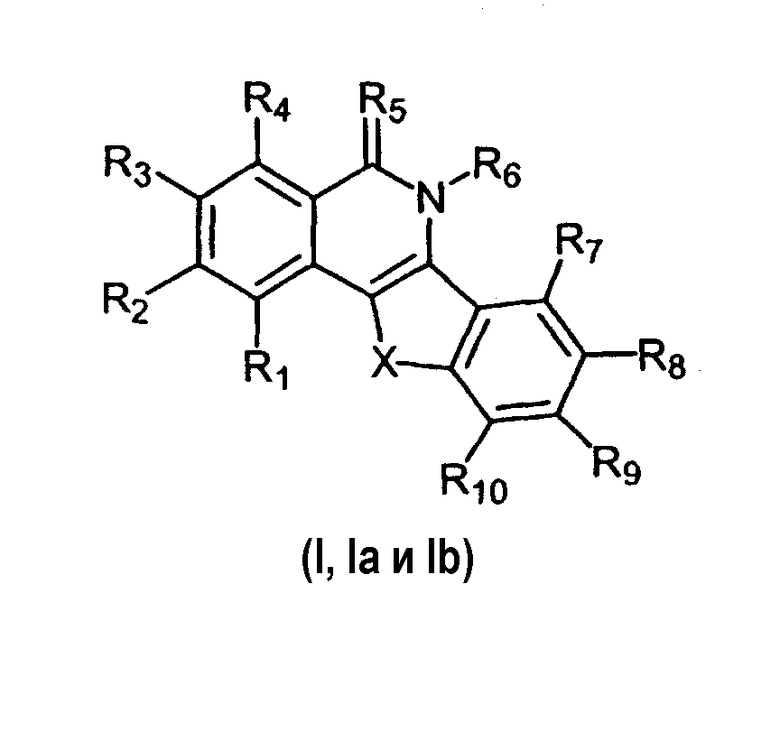
Следовательно, по одному из аспектов, изобретение охватывает соединение формулы I, формулы Ia, формулы Ib, формулы II или формулы III, или фармацевтически приемлемую соль, или гидрат указанного соединения (индено[1,2-c]изохинолиновое соединение), как изложено ниже в подробном описании изобретения.
Изобретением также представлен способ терапевтического или профилактического лечения воспалительного заболевания или реперфузионного нарушения у пациента, включающий введение нуждающемуся в таком терапевтическом или профилактическом лечении субъекту эффективного количества индено[1,2-c]изохинолинового соединения.
Согласно другому аспекту изобретение включает также способ получения индено[1,2-c]изохинолинового соединения.
Индено[1,2-c]изохинолиновые соединения могут быть использованы для лечения или профилактики различных состояний или заболеваний, включающих, но не в порядке ограничения, воспалительное заболевание или реперфузионное нарушение.
Изобретение охватывает также фармацевтические композиции, включающие эффективное количество индено[1,2-c]изохинолинового соединения и фармацевтически приемлемый носитель. Композиции полезны для терапевтического или профилактического лечения воспалительного заболевания или реперфузионного нарушения. Изобретение включает также индено[1,2-c]изохинолиновое соединение, представленное в виде фармацевтически приемлемого пролекарства, гидратированной соли, такой как фармацевтически приемлемая соль, либо их смеси.
Подробно изобретение изложено в приведенном ниже описании. В данном описании представлены иллюстративные способы и соединения, хотя при практической реализации или проверке настоящего изобретения могут быть использованы любые способы и соединения, подобные или равноценные описанным. Другие особенности, объекты и преимущества настоящего изобретения станут очевидны из описания и приложенной формулы изобретения. В описании и приложенной формуле изобретения формы единственного числа также включают формы множественного числа, если это явно не противоречит контексту. За исключением особо указанных случаев, все используемые в данном описании технические и научные термины имеют те же значения, что и общепринятые у специалистов в данной области, на которых и рассчитано изобретение. Все приведенные в данном описании патенты и публикации включены в данное описание в качестве ссылок.
4. Подробное описание изобретения
Настоящее изобретение касается нового класса индено[1,2-c]изохинолиновых соединений, отвечающих формуле I, формуле Ia, формуле Ib, формуле II и формуле III, представленным ниже:

и их фармацевтически приемлемых солей и гидратов, где:
R5 означает O, NH или S;
R6 означает -H или C1-C4алкил;
X означает -C(O)-, -CH2-, -CH(галоген)-, -CH(OH)(CH2)n-, -CH(OH)-арилен-, -O-, -NH-, -S- или -CH(NR11R12)-, где n равно целому числу в пределах 0-5;
R11 и R12 независимо означают водород или -C1-C9алкил, либо N, R11 и R12, взятые вместе, образуют гетероциклический амин;
R1, R2, R3, R4, R7, R8, R9 и R10 независимо означают водород, галоген, гидрокси, -O-(C1-C5алкил), -C1-C10алкил, -алкилгалоген, -C2-C10алкенил, -C3-C8карбоцикл, арил, -NH2, -алкиламино, -C(O)OH, -C(O)O(C1-C5алкил), -OC(O)(C1-C5алкил), NO2 или -A-B;
где A означает -SO2-, -SO2NH-, -NHCO-, -NHCONH-, -O-, -CO-, -OC(O)-, -C(O)O-, -CONH-, -CON(C1-C4алкил)-, -NH-, -CH2, -S- или -C(S)-;
B означает -C1-C10алкил, -C2-C10алкенил, гетероцикл, -C3-C8карбоцикл, арил, -NZ1Z2, -алкиламино, -аминодиалкил, -акилгетероцикл, -ариламидо, -C(O)OH, -C(O)O-(C1-C5алкил) или -C(O)O-фенил, любой из которых является незамещенным или замещен одной или более группами, включающими -O-(C1-C5алкил), галоген, -алкилгалоген, алканол, -алкиламино, гидрокси, -NO2, -NH2, -аминоалкил, -аминодиалкил, гетероциклический амин, -C1-C10алкил, -C2-C10алкенил, -C2-C10алкинил, арил, бензил, -алкиламидо, алкилкарбокси, -C1-C5алкилен-C(O)O-C1-C5алкил или -C1-C5алкилен-OC(O)-C1-C5алкил; и
Z1 и Z2 независимо означают -H или -C1-C10алкил, который является незамещенным или замещен одной или более группами, включающими галоген, -OH или -N(Z3)(Z4), где Z3 и Z4 независимо означают -H или -C1-C5алкил, который является незамещенным или замещен одной или более группами, включающими галоген, гидрокси или -NH2; либо N, Z3 и Z4, взятые вместе, образуют незамещенный или замещенный гетероциклический амин; либо N, Z1 и Z2, взятые вместе, образуют гетероциклический амин.
Изобретение также касается соединений формулы Ia:
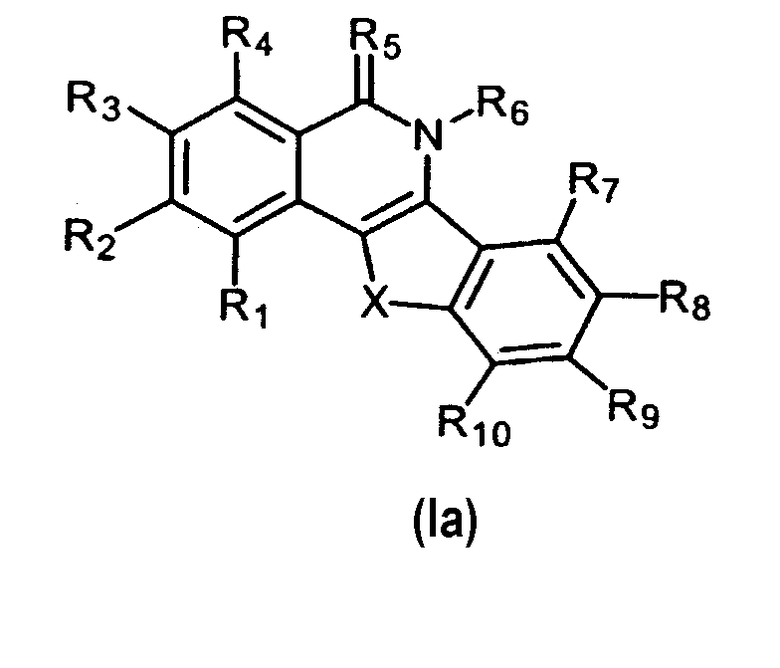
и их фармацевтически приемлемых солей и гидратов, где:
R5 означает NH или S;
R6 означает -H или C1-C4алкил;
X означает -C(O)-, -CH2-, -CH(галоген)-, -CH(OH)(CH2)n-, -CH(OH)-арилен-, -O-, -NH-, -S- или -CH(NR11R12)-, где n равно целому числу в пределах 0-5;
R11 и R12 независимо означают водород или -C1-C9алкил, либо N, R11 и R12, взятые вместе, образуют гетероциклический амин;
R1, R2, R3, R4, R7, R8, R9 и R10 независимо означают водород, галоген, гидрокси, -O-(C1-C5алкил), -C1-C10алкил, -алкилгалоген, -C2-C10алкенил, -C3-C8карбоцикл, арил, -NH2, -алкиламино, -C(O)OH, -C(O)O(C1-C5алкил), -OC(O)(C1-C5алкил), NO2 или -A-B;
где A означает -SO2-, -SO2NH-, -NHCO-, -NHCONH-, -O-, -CO-, -OC(O)-, -C(O)O-, -CONH-, -CON(C1-C4алкил)-, -NH-, -CH2, -S- или -C(S)-;
B означает -C1-C10алкил, -C2-C10алкенил, гетероцикл, -C3-C8карбоцикл, арил, -NZ1Z2, -алкиламино, -аминодиалкил, -алкилгетероцикл, -ариламидо, -C(O)OH, -C(O)O-(C1-C5алкил) или -C(O)O-фенил, любой из которых является незамещенным или замещен одной или более группами, включающими -O-(C1-C5алкил), галоген, -алкилгалоген, алканол, -алкиламино, гидрокси, -NO2, -NH2, -аминоалкил, -аминодиалкил, гетероциклический амин, -C1-C10алкил, -C2-C10алкенил, -C2-C10алкинил, арил, бензил, -алкиламидо, алкилкарбокси, -C1-C5алкилен-C(O)O-C1-C5алкил или -C1-C5алкилен-OC(O)-C1-C5алкил; и
Z1 и Z2 независимо означают -H или -C1-C10алкил, который является незамещенным или замещен одной или более группами, включающими галоген, -OH или -N(Z3)(Z4), где Z3 и Z4 независимо означают -H или -C1-C5алкил, который является незамещенным или замещен одной или более группами, включающими галоген, гидрокси или -NH2; либо N, Z3 и Z4, взятые вместе, образуют незамещенный или замещенный гетероциклический амин; либо N, Z1 и Z2, взятые вместе, образуют гетероциклический амин.
В одном из вариантов изобретения A означает -SO2-.
Еще в одном варианте изобретения R1, R2, R3, R4, R7, R8, R9 и Rl0 независимо означают арилалкил.
В других иллюстративных вариантах изобретения R5 и X в соединении формулы Ia принимают приведенные ниже значения:
Изобретение также касается соединений формулы Ib:
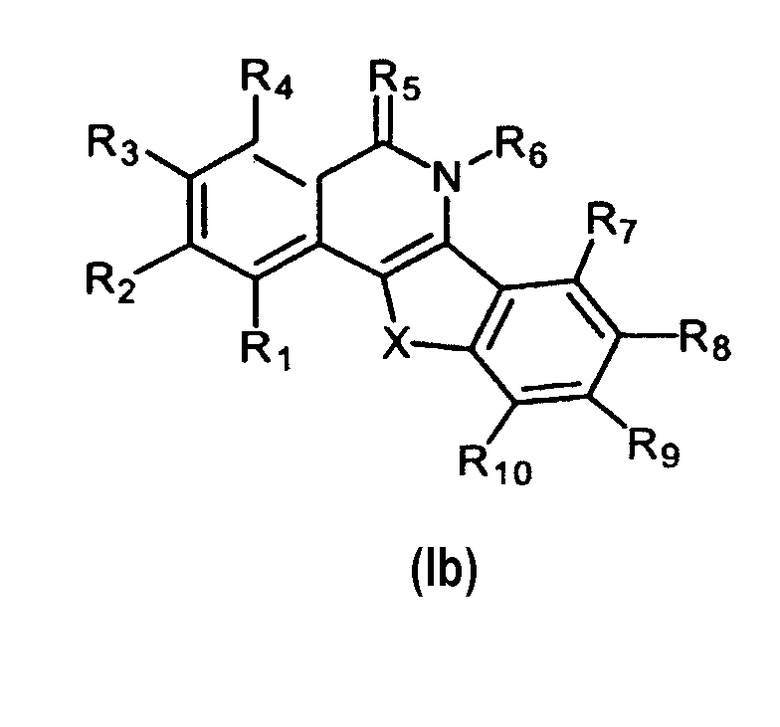
и их фармацевтически приемлемых солей и гидратов, где:
R5 означает О, NH или S;
R6 означает -H или C1-C4алкил;
X означает -CH2-, -CH(галоген)-, -CH(OH)(CH2)n-, -CH(OH)-арилен-, -O-, -NH-, -S- или -CH(NR11R12)-, где n равно целому числу в пределах 0-5;
R11 и R12 независимо означают водород или -C1-C9алкил, либо N, R11 и R12, взятые вместе, образуют гетероциклический амин;
R1, R2, R3, R4, R7, R8, R9 и R10 независимо означают водород, галоген, гидрокси, -O-(C1-C5алкил), -C1-C10алкил, -алкилгалоген, C2-C10алкенил, -C3-C8карбоцикл, арил, -NH2, -алкиламино, -C(O)OH, -C(O)O(C1-C5алкил), -OC(O)(C1-C5алкил), NO2 или -A-B;
где A означает -SO2-, -SO2NH-, -NHCO-, -NHCONH-, -O-, -CO-, -OC(O)-, -C(O)O-, -CONH-, -CON(C1-C4алкил)-, -NH-, -CH2, -S- или -C(S)-;
B означает -C1-C10алкил, -C2-C10алкенил, гетероцикл, -C3-C8карбоцикл, арил, -NZ1Z2, -алкиламино, -аминодиалкил, -алкилгетероцикл, -ариламидо, -C(O)OH, -C(O)O-(C1-C5алкил) или -C(O)O-фенил, любой из которых является незамещенным или замещен одной или более группами, включающими -O-(C1-C5алкил), галоген, -алкилгалоген, алканол, -алкиламино, гидрокси, -NO2, -NH2, -аминоалкил, -аминодиалкил, гетероциклический амин, -C1-C10алкил, -C2-C10алкенил, -C2-C10алкинил, арил, бензил, -алкиламидо, алкилкарбокси, -C1-C5алкилен-C(O)O-C1-C5алкил или -C1-C5алкилен-OC(O)-C1-C5алкил; и
Z1 и Z2 независимо означают -H или -C1-C10алкил, который является незамещенным или замещен одной или более группами, включающими галоген, -OH или -N(Z3)(Z4), где Z3 и Z4 независимо означают -H или -C1-C5алкил, который является незамещенным или замещен одной или более группами, включающими галоген, гидрокси или -NH2; либо N, Z3 и Z4, взятые вместе, образуют незамещенный или замещенный гетероциклический амин; либо N, Z1 и Z2, взятые вместе, образуют гетероциклический амин.
В одном из вариантов изобретения A означает -SO2-.
Еще в одном варианте изобретения R1, R2, R3, R4, R7, R8, R9 и Rl0 независимо означают арилалкил.
В иллюстративных вариантах изобретения R5 и X в соединении формулы Ib принимают приведенные ниже значения:
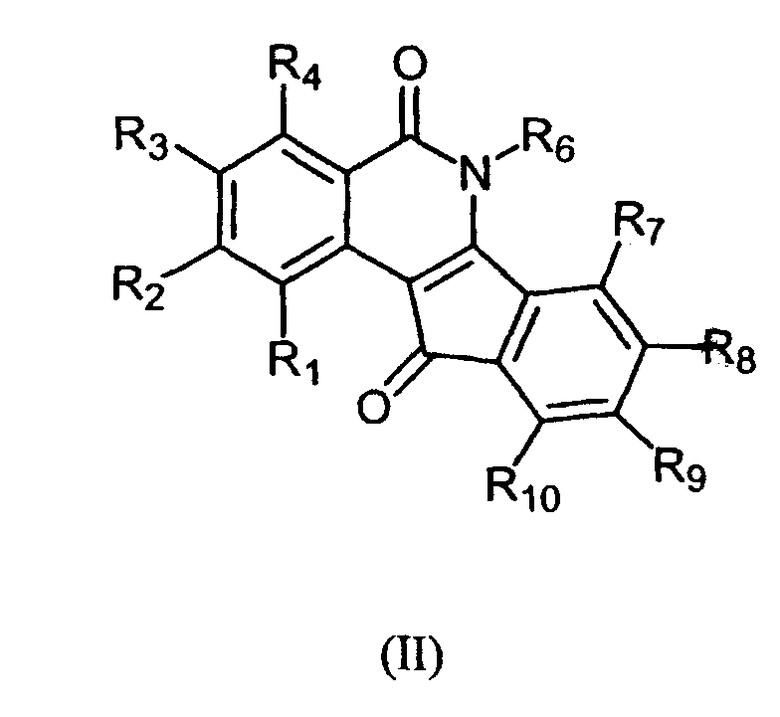
Изобретение также касается соединений формулы II:
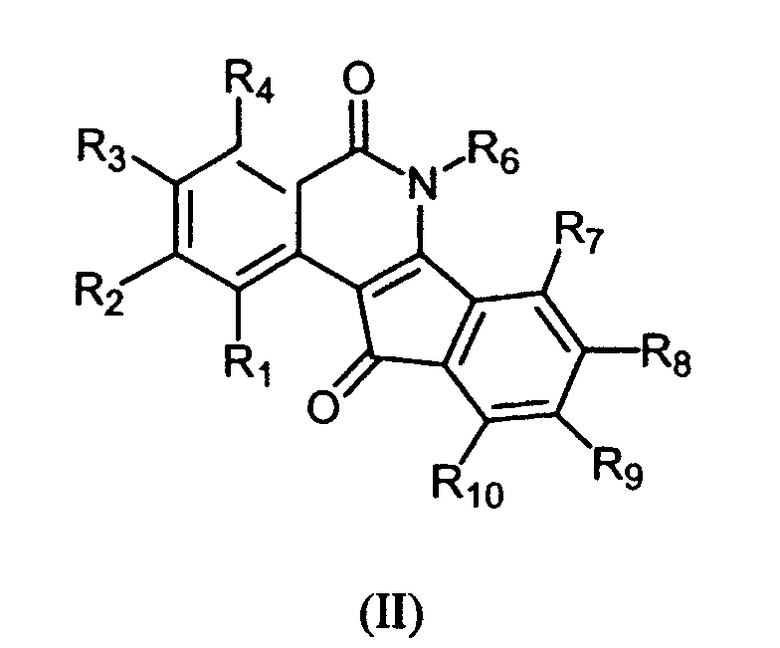
и их фармацевтически приемлемых солей и гидратов,
где:
R6 означает -H или C1-C4алкил;
R1, R2, R3, R4, R7, R8, R9 и R10 независимо означают водород, галоген, гидрокси, -O-(C1-C5алкил), -C1-C10алкил, -алкилгалоген, -C2-C10алкенил, -C3-C8карбоцикл, арил, -NH2, -алкиламино, -C(O)OH, -C(O)O(C1-C5алкил), -OC(O)(C1-C5алкил), NO2 или -A-B; где, по меньшей мере, один из R1, R4 и R10 отличен от водорода;
A означает -SO2-, -SO2NH-, -NHCO-, -NHCONH-, -O-, -CO-, -OC(O)-, -C(O)O-, -CONH-, -CON(C1-C4алкил)-, -NH-, -CH2, -S- или -C(S)-;
B означает -C1-C10алкил, -C2-C10алкенил, гетероцикл, -C3-C8карбоцикл, арил, -NH2, -алкиламино, -аминодиалкил, -алкилгетероцикл, -ариламидо, -C(O)OH, -C(O)O-(C1-C5алкил), -C(O)O-фенил или NZ1Z2 и
Z1 и Z2 независимо означают -H или -C1-C10алкил, который является незамещенным или замещен одной или более группами, включающими галоген, -OH или -N(Z3)(Z4), где Z3 и Z4 независимо означают -H или -C1-C5алкил, который является незамещенным или замещен одной или более группами, включающими галоген, гидрокси или -NH2; либо N, Z3 и Z4, взятые вместе, образуют незамещенный или замещенный гетероциклический амин; либо N, Z1 и Z2, взятые вместе, образуют гетероциклический амин.
В одном из вариантов изобретения B означает гетероциклический амин.
В другом варианте изобретения B означает арилалкил.
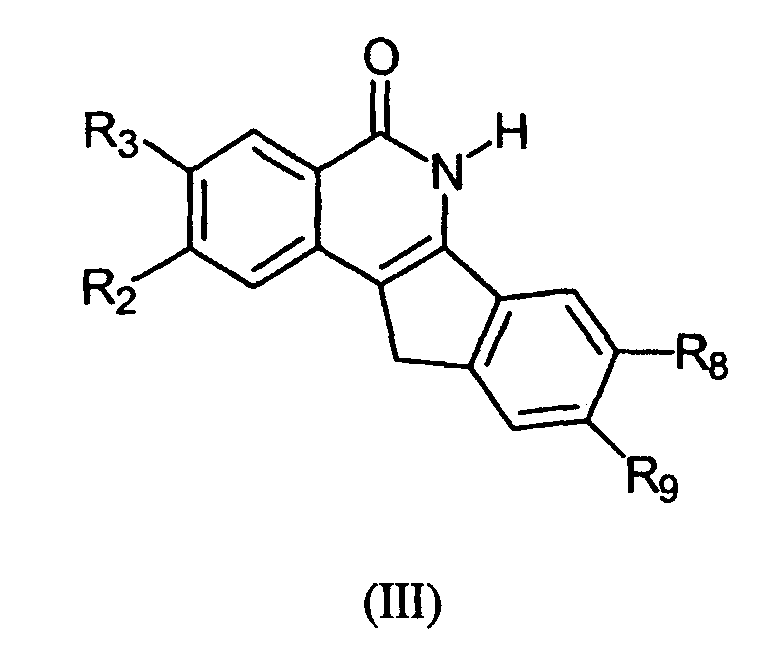
Изобретение также касается соединений формулы III:
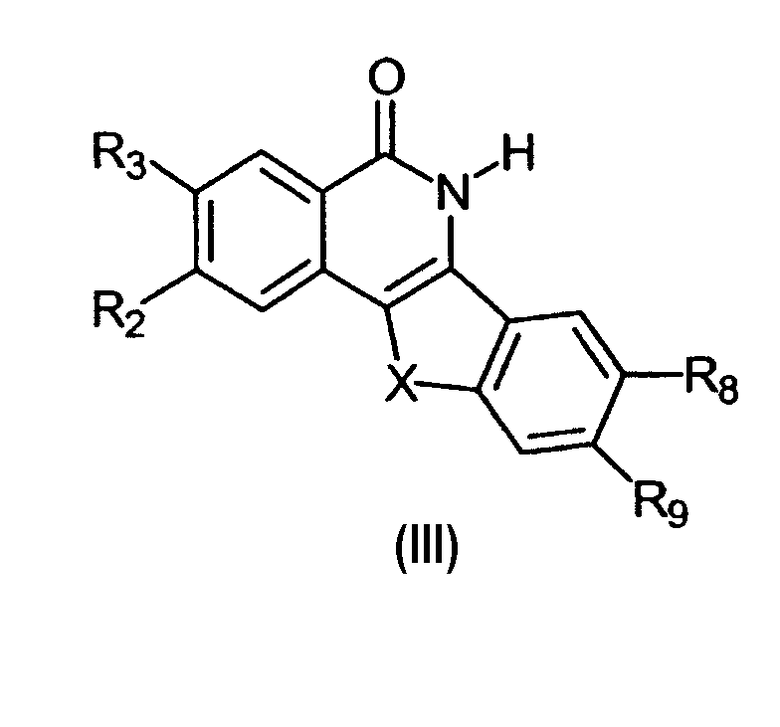
и их фармацевтически приемлемых солей и гидратов,
где:
X означает -CH2- или -O-;
R2 и R3 независимо означают водород, галоген, -алкилгалоген, гидрокси, -O-(C1-C5алкил), -C1-C3алкил, -NO2, -NH2, -CONH2, -C(O)OH, -OC(O)-C1-C5алкил или -C(O)O-C1-C5алкил;
R8 и R9 независимо означают водород и -A-B;
A означает -SO2-, -SO2NH- или -NHCO- и
B означает -C1-C3алкил, -NZ1Z2, гетероцикл или -алкиламино, каждый является незамещенным или замещен одной или более группами, включающими алканол, -алкиламино, -аминоалкил, -аинодиалкил или гетероцикл, каждый является незамещенным или замещен группой -C1-C10алкил или алканол; и
Z1 и Z2 независимо означают водород или -C1-C8алкил, который является незамещенным или замещен одной или более группами, включающими гидрокси или -NZ3Z4, где Z3 и Z4 независимо означают H или -C1-C3алкил, который является незамещенным или замещен одной или более группами, включающими гидрокси или -NH2; либо N, Z3 и Z4, взятые вместе, образуют гетероциклический амин; либо N, Z1 и Z2, взятые вместе, образуют гетероциклический амин.
В одном из вариантов изобретения -X- означает -CH2-.
В другом варианте изобретения -X- означает -O-.
В одном варианте изобретения R8 означает водород и R9 означает -A-B.
Еще в одном варианте изобретения R8 означает -A-B и R9 означает водород.
В одном из вариантов изобретения, либо R8 означает водород и R9 означает -A-B, либо R8 означает -A-B и R9 означает водород.
В одном из вариантов изобретения, R3, R8 и R9 означают водород и R2 означает -A-B, где A означает -NHC(O)-.
Еще в одном варианте изобретения R2, R8 и R9 означают водород и R3 означает -A-B, где A означает -NHC(O)-.
Еще в одном варианте изобретения R2, R3 и R8 означают водород и R9 означает -A-B, где A означает -SO2- или -SO2NH-.
4.1 Определения
"C1-C3алкил" означает линейный или разветвленный насыщенный углеводород, содержащий 1-3атома углерода. Примеры C1-C3алкильной группы включают, но не в порядке ограничения, метил, этил, пропил и изопропил.
"C1-C4алкил" означает линейный или разветвленный насыщенный углеводород, содержащий 1-4атома углерода. Примеры C1-C4алкильной группы включают, но не в порядке ограничения, метил, этил, пропил, бутил, изопропил, изобутил, втор-бутил и трет-бутил.
"C1-C5алкил" означает линейный или разветвленный насыщенный углеводород, содержащий 1-5атома углерода. Примеры C1-C5алкильной группы включают, но не в порядке ограничения, метил, этил, пропил, бутил, пентил, изопропил, изобутил, втор-бутил и трет-бутил, изопентил и неопентил.
"C1-C8алкил" означает линейный или разветвленный насыщенный углеводород, содержащий 1-8атомов углерода. Примеры C1-C8алкильной группы включают, но не в порядке ограничения, метил, этил, пропил, бутил, пентил, гексил, гептил, октил, изопропил, изобутил, втор-бутил и трет-бутил, изопентил, неопентил, изогексил, изогептил и изооктил.
"C1-C9алкил" означает линейный или разветвленный насыщенный углеводород, содержащий 1-9атомов углерода. Примеры C1-C9алкильной группы включают, но не в порядке ограничения, метил, этил, пропил, бутил, пентил, гексил, гептил, октил, нонил, изопропил, изобутил, втор-бутил и трет-бутил, изопентил, неопентил, изогексил, изогептил, изооктил и изононил.
"C1-C10алкил" означает линейный или разветвленный насыщенный углеводород, содержащий 1-10атомов углерода. Примеры C1-C10алкильной группы включают, но не в порядке ограничения, метил, этил, пропил, бутил, пентил, гексил, гептил, октил, нонил, децил, изопропил, изобутил, втор-бутил и трет-бутил, изопентил, неопентил, изогексил, изогептил, изооктил, изононил и изодецил.
"C2-C10алкенил" означает линейный или разветвленный ненасыщенный углеводород, содержащий 2-10 атомов углерода. Примеры C2-C10алкенильной группы включают, но не в порядке ограничения, этилен, пропилен, 1-бутилен, 2-бутилен, изобутилен, втор-бутилен, 1-пентен, 2-пентен, изопентен, 1-гексен, 2-гексен, 3-гексен, изогексен, 1-гептен, 2-гептен, 3-гептен, 1-октен, 2-отен, 3-октен, 4-октен, 1-нонен, 2-нонен, 3-нонен, 4-нонен, 1-децен, 2-децен, 3-децен, 4-децен и 5-децен.
"C2-C10алкинил" означает линейный или разветвленный ненасыщенный углеводород, содержащий 2-10 атомов углерода и, по меньшей мере, одну тройную связь. Примеры C2-C10алкинильной группы включают, но не в порядке ограничения, ацетилен, пропин, 1-бутин, 2-бутин, изобутин, втор-бутин, 1-пентин, 2-пентин, изопентин, 1-гексин, 2-гексин, 3-гексин, изогексин, 1-гептин, 2-гептин, 3-гептин, 1-октин, 2-октин, 3-октин, 4-октин, 1-нонин, 2-нонин, 3-нонин, 4-нонин, 1-децин, 2-децин, 3-децин, 4-децин и 5-децин.
"C1-C4алкилен" означает C1-C4алкильную группу, в которой один из атомов водорода C1-C4алкильной группы заменен химической связью. Примеры C1-C4алкилена включают -CH2-, -CH2CH2-, -CH2CH2CH2- и -CH2CH2CH2CH2-.
"C1-C5алкилен" означает C1-C5алкильную группу, в которой один из атомов водорода C1-C5алкильной группы заменен химической связью. Примеры C1-C5алкилена включают -CH2-, -CH2CH2-, -CH2CH2CH2-, -CH2CH2CH2CH2- и -CH2CH2CH2CH2CH2-.
"Алкилгалоген" означает указанную выше C1-C5алкильную группу, где один или более атомов водорода C1-C5алкильной группы заменены -F, -Cl, -Br или -I. Характерные примеры -алкилгалогеновой группы включают, но не в порядке ограничения, -CH2F, -CCl3, -CF3, -CH2Cl, -CH2CH2Br, -CH2CH2I, -CH2CH2CH2F, -CH2CH2CH2Cl, -CH2CH2CH2CH2Br, -CH2CH2CH2CH2I, -CH2CH2CH2CH2CH2Br, -CH2CH2CH2CH2CH2I, -CH2CH(Br)CH3 -CH2CH(Cl)CH2CH3 -CH(F)CH2CH3 и -C(CH3)2(CH2Cl).
"Алкиламино" означает указанную выше C1-C4алкильную группу, где один или более атомов водорода C1-C4алкильной группы заменены -NH2. Характерные примеры алкиламиногруппы включают, но не в порядке ограничения, -CH2NH2, -CH2CH2NH2, -CH2CH2CH2NH2, -CH2CH2CH2CH2NH2, -CH2CH(NH2)CH3, -CH2CH(NH2)CH2CH3, -CH(NH2)CH2CH3 и -C(CH3)2(CH2NH2).
"Аминоалкил" означает группу -NH, где атом азота указанной группы соединен с указанной выше C1-C4алкильной группой. Характерные примеры аминоалкильной группы включают, но не в порядке ограничения, -NHCH3, -NHCH2CH3, -NHCH2CH2CH3, -NHCH2CH2CH2CH3, -NHCH(CH3)2, -NHCH2CH(CH3)2, -NHCH(CH3)CH2CH3 и -NH-C(CH3)3.
"Аминодиалкил" означает атом азота, соединенный с двумя вышеуказанными C1-C4алкильными группами. Характерные примеры аминодиалкильной группы включают, но не в порядке ограничения, -N(CH3)2, -N(CH2CH3)(CH3), -N(CH2CH3)2, -N(CH2CH2CH3)2, -N(CH2CH2CH2CH3)2, -N(CH(CH3)2)2, -N(CH(CH3)2)(CH3), -N(CH2CH(CH3)2)2, -NH(CH(CH3)CH2CH3)2, -N(C(CH3)3)2 и -N(C(CH3)3)(CH3).
"Арил" означает фенильную или пиридильную группу. Примеры арильной группы включают, но не в порядке ограничения, фенил, N-пиридил, 2-пиридил, 3-пиридил и 4-пиридил. Арильная группа может быть незамещенной или замещена одной или более группами, выбираемыми из следующей группы: -C1-C5алкил, галоген, -акилгалоген, гидрокси, -O-C1-C5алкил, -NH2, -аминоалкил, -аинодиалкил, -COOH, -C(O)O-(C1-C5алкил), -OC(O)-(C1-C5алкил), -N-амидоалкил, -C(O)NH2, -карбоксамидоалкил или -NO2.
"Арилалкил" означает указанную выше арильную группу, где один из атомов водорода арильной группы заменен указанной выше C1-C5алкильной группой. Характерные примеры арилалкильной группы включают, но не в порядке ограничения, 2-метилфенил, 3-метилфенил, 4-метилфенил, 2-этилфенил, 3-этилфенил, 4-этилфенил, 2-пропилфенил, 3-пропилфенил, 4-пропилфенил, 2-бтилфенил, 3-бутилфенил, 4-бутилфенил, 2-пентилфенил, 3-пентилфенил, 4-пентилфенил, 2-изопропилфенил, 3-иопропилфенил, 4-изопропилфенил, 2-изобутилфенил, 3-изобутилфенил, 4-изобутилфенил, 2-втор-бутилфенил, 3-втор-бутилфенил, 4-втор-бутилфенил, 2-трет-бутилфенил, 3-трет-бутилфенил и 4-трет-бутилфенил.
"Ариламидо" означает указанную выше арильную группу, где один из атомов водорода арильной группы заменен одной или более группами -C(O)NH2. Характерные примеры ариламидогруппы включают, но не в порядке ограничения, 2-C(O)NH2-фенил, 3-C(O)NH2-фенил, 4-C(O)NH2-фенил, 2-C(O)NH2-пиридил, 3-C(O)NH2-пиридил и 4-C(O)NH2-пиридил.
"Алкилгетероцикл" означает указанную выше C1-C5алкильную группу, где один или более атомов водорода C1-C5алкильной группы заменены гетероциклом. Характерные примеры алкилгетероциклической группы включают, но не в порядке ограничения, -CH2CH2-морфолин, -CH2CH2-пиперидин, -CH2CH2CH2-морфолин и -CH2CH2CH2-имидазол.
"Алкиламидо" означает указанную выше C1-C5алкильную группу, где один из атомов водорода C1-C5алкильной группы заменен группой -C(O)NH2. Характерные примеры алкиламидогруппы включают, но не в порядке ограничения, -CH2C(O)NH2, -CH2CH2C(O)NH2, -CH2CH2CH2C(O)NH2, -CH2CH2CH2CH2C(O)NH2, -CH2CH2CH2CH2CH2C(O)NH2, -CH2CH(C(O)NH2)CH3, -CH2CH(C(O)NH2)CH2CH3, -CH(C(O)NH2)CH2CH3 и -C(CH3)2CH2C(O)NH2.
"Алканол" означает указанную выше C1-C5алкильную группу, где один из атомов водорода C1-C5алкильной группы заменен гидроксильной группой. Характерные примеры алканольной группы включают, но не в порядке ограничения, -CH2OH, -CH2CH2OH, -CH2CH2CH2OH, -CH2CH2CH2CH2OH, -CH2CH2CH2CH2CH2OH, -CH2CH(OH)CH3 -CH2CH(OH)CH2CH3, -CH(OH)CH2CH3 и -C(CH3)2CH2OH.
"Алкилкарбокси" означает указанную выше C1-C5алкильную группу, где один из атомов водорода C1-C5алкильной группы заменен группой -COOH. Характерные примеры алкилкарбоксильной группы включают, но не в порядке ограничения, -CH2COOH, -CH2CH2COOH, -CH2CH2CH2COOH, -CH2CH2CH2CH2COOH, -CH2CH(COOH)CH3, -CH2CH2CH2CH2CH2COOH, -CH2CH(COOH)CH2CH3, -CH(COOH)CH2CH3 и -C(CH3)2CH2COOH.
"N-Амидоалкил" означает группу -NHC(O)-, где карбонильный атом углерода указанной группы соединен с указанной выше C1-C5алкильной группой. Характерные примеры N-аидоалкильной группы включают, но не в порядке ограничения, -NHC(O)CH3, -NHC(O)CH2CH3, -NHC(O)CH2CH2CH3, -NHC(O)CH2CH2CH2CH3, -NHC(O)CH2CH2CH2CH2CH3, -NHC(O)CH(CH3)2, -NHC(O)CH2CH(CH3)2, -NHC(O)CH(CH3)CH2CH3, -NHC(O)-C(CH3)3 и -NHC(O)CH2C(CH3)3.
"Карбоксамидоалкил" означает группу -C(O)NH-, где атом азота указанной группы соединен с указанной выше C1-C5алкильной группой. Характерные примеры карбоксамидоалкильной группы включают, но не в порядке ограничения, -C(O)NHCH3, -C(O)NHCH2CH3, -C(O)NHCH2CH2CH3, -C(O)NHCH2CH2CH2CH3, -C(O)NHCH2CH2CH2CH2CH3, -C(O)NHCH(CH3)2, -C(O)NHCH2CH(CH3)2, -C(O)NHCH(CH3)CH2CH3, -C(O)NH-C(CH3)3 и -C(O)NHCH2C(CH3)3.
Группа "арилен" означает фенильную группу, в которой один из атомов водорода фенильной группы заменен химической связью. Ариленовая группа может быть в орто-, мета- или пара- конфигурации и может быть незамещенной или независимо замещена одной или более группами, выбираемыми из следующей группы: -C1-C5алкил, галоген, -алкилгалоген, гидрокси, -O-C1-C5алкил, -NH2, -аминоалкил, -аминодиалкил, -COOH, -C(O)O-(C1-C5алкил), -OC(O)-(C1-C5алкил), -N-амидоалкил, -C(O)NH2, карбоксамидоалкил или -NO2.
"C3-C8карбоцикл" означает неароматическое, насыщенное углеводородное кольцо, содержащее 3-8 атомов углерода. Характерные примеры C3-C8карбоцикла включают, но не в порядке ограничения, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил. C3-C8карбоцикл может быть незамещенным или необязательно замещен одной или более группами, выбираемыми из следующей группы: -C1-C5алкил, галоген, -алкилгалоген, гидрокси, -O-C1-C5алкил, -NH2, -аминоалкил, -аминодиалкил, -COOH, -C(O)O-(C1-C5алкил), -OC(O)-(C1-C5алкил), -N-аидоалкил, -C(O)NH2, -карбоксиамидоалкил или -NO2.
"Гетероцикл" означает 5-10-членный ароматический или неароматический карбоцикл, в котором 1-4 атома углерода кольца независимо заменены атомом N, O или S. Характерные примеры гетероциклической группы включают, но не в порядке ограничения, пиперидинил, пиперазинил, морфолинил, пирролил, оксазинил, тиазинил, диазинил, триазинил, тетразинил, имидазолил, бензимидазолил, тетразолил, индолил, изохинолинил, хинолинил, хиназолинил, пирролидинил, пуринил, изоксазолил, бензизоксазолил, фуранил, фуразанил, пиридинил, оксазолил, бензоксазолил, тиазолил, бензтиазолил, тиофенил, пиразолил, триазолил, бензодиазолил, бензотриазолил, пиримидинил, изоиндолил и индазолил. Гетероциклическая группа может быть незамещенной или независимо замещена одной или более группами, выбираемыми из следующей группы: -C1-C5алкил, галоген, -акилгалоген, гидрокси, -O-C1-C5алкил, -NH2, -аминоалкил, -аинодиалкил, -COOH, -C(O)O-(C1-C5алкил), -OC(O)-(C1-C5алкил), -N-амидоалкил, -C(O)NH2, -карбоксамидоалкил или -NO2.
"Гетероциклический амин" означает указанный выше гетероцикл с 1-4 атомами азота в кольце. Характерные примеры гетероциклических аминов включают, но не в порядке ограничения, пиперидинил, пиперазинил, пирролил, оксазинил, тиазинил, диазинил, триазинил, тетразинил, имидазолил, бензимидазолил, тетразолил, индолил, изохинолинил, хинолинил, хиназолинил, пирролидинил, пуринил, изоксазолил, бензизоксазолил, пиридинил, оксазолил, бензоксазолил, тиазолил, бензтиазолил, пиразолил, триазолил, бензодиазолил, бензотриазолил, пиримидинил, изоиндолил, индазолил и морфолинил; каждый из которых может быть незамещенным или замещен одним или более заместителями, включающими: -N-(C1-C5алкил), -C(O)-(C1-C5алкил), -N-C(O)(C1-C4алкил), -O-(C1-C5алкил), галоген, -алкилгалоген, алканол, -акиламино, гидрокси, -NO2, -NH2, -аминоалкил, -аминодиалкил, гетероциклический амин, -C1-C10алкил, -C2-C10алкенил, -C2-C10алкинил, арил, бензил, -алкиламидо, алкилкарбокси, -COOH, -C1-C5алкилен-OC(O)-C1-C5алкил, -C1-C5алкилен-C(O)O-C1-C5алкил, либо гетероцикл или C3-C8карбоцикл, который может быть незамещенным или замещен одним или более заместителями, включающими: -C1-C10алкил, -O-(C1-C5алкил), галоген, -акилгалоген, алканол, -алкиламино, гидрокси, -NO2 или -NH2.
"Галоген" означает -F, -Cl, -Br или -I.
"Субъект" означает млекопитающее, напримерчеловека, мышь, крысу, морскую свинку, собаку, кошку, лошадь, корову, свинью или не принадлежащего к человеческому роду примата.
Изобретение также включает фармацевтические композиции, содержащие индено[1,2-c]изохинолиновое соединение и фармацевтически приемлемый носитель. Изобретение включает индено[1,2-c]изохинолиновое соединение, представленное в форме фармацевтически приемлемого пролекарства, гидратированной соли, такой как фармацевтически приемлемая соль, либо их смеси.
Характерные примеры "фармацевтически приемлемых солей" включают, например,водорастворимые или водонерастворимые соли, такие как ацетат, амсонат (4,4-диаминостильбен-2,2-дисульфонат), бензолсульфонат, бензонат, бикарбонат, бисульфат, битартрат, борат, бромид, бутират, кальцийэдетат, камзилат, карбонат, хлорид, цитрат, клавулариат, дигидрохлорид, эдетат, эдизилат, эстолят, эзилат, fiunarate, глуцептат, глюконат, глутамат, гликоллиларсанилат, гексафторфосфат, гексилрезорцинат, гидрабамин, гидробромид, гидрохлорид, гидроксинафтоат, иодид, изотионат, лактат, лактобионат, лаурат, малат, малеат, манделат, мезилат, метилбромид, метилнитрат, метилсульфат, мукат, напзилат, нитрат, N-метилглюкаминаммониевая соль, 3-гидрокси-2-нафтоат, олеат, оксалат, пальмитат, памоат (1,1-метен-бис-2-гидрокси-3-нафтоат, эйнбонат), пантотенат, фосфат/дифосфат, пикрат, полигалактуронат, пропионат, п-толуолсульфонат, салицилат, стеарат, субацетат, сукцинат, сульфат, сульфосалицилат, сурамат, таннат, тартрат, теоклат, тозилат, триэтиодид и валерат.
"Эффективное количество", когда используется в связи с индено[1,2-c]изохинолиновым соединением, означает количество, эффективное для лечения или профилактики воспалительного заболевания или реперфузионного нарушения.
В описании используются следующие сокращения, имеющие указанные значения: AcOH означает уксусную кислоту, CLP означает слепокишечную перевязку и прокол, DMEM означает среду игла, модифицированную по Дульбекко, ДМФА означает N,N-диметилформамид, ДМСО означает диметилсульфоксид, EtOAc означает этилацетат, EtOH означает этанол, HEPES означает 4-(2-гидроксиэтил)-1-пиперазинэтансульфоновую кислоту, LPS означает липополисахарид, MeOH означает метанол, МС означает масс-спектрометрию, ЯМР означает ядерный магнитный резонанс, PBS означает забуференный фосфатом физиологический раствор (pH 7,4), PARS означает поли(ADP-рибоза)синтетазу, Py означает пиридин, SDS означает додецилсульфат (натриевую соль), STZ означает стрептозотоцин, ТХУ означает трихлоруксусную кислоту, ТФУ означает трифторуксусную кислоту, ТСХ означает тонкослойную хроматографию, TNF означает фактор некроза опухоли и TRIS означает трис(гидроксиметил)аминометан.
Способы применения индено[1,2-c]изохинолиновых соединений
Изобретение также включает способы ингибирования PARS в клетке. PARS, известный также как поли(ADP-рибоза)синтетаза, PARP ((поли(ADP-рибоза)полимераза, EC2.4.99) и ADP-рибозилтрансфераза (ADPRT, EC 2.4.2.30), является нуклеарным ферментом, катализирующим перенос группы ADP-рибозы от NAD+ к акцепторному белку.
В одном из вариантов изобретения способ включает контактирование клетки с индено[1,2-c]изохинолиновым соединением в количестве, достаточном для ингибирования PARS в клетке. Обычно может быть использована любая клетка, обладающая или способная обладать PARS-активностью или способная к экспрессии PARS. Клетка может быть представлена в любой форме. Например, клетка может быть обеспечена in vitro, ex vivo или in vivo. PARS-активность может быть измерена любым известным в данной области способом, например, способами, описанными у Banasik et al., J. Biol. Chem. 267:1569-75 (1991). Иллюстративные примеры клеток, способных к экспрессии PARS, включают, но не в порядке ограничения, клетки мышцы, костей, десны, нервные, головного мозга, печени, почек, поджелудочной железы, легкого, сердца, мочевого пузыря, желудка, ободочной кишки, прямой кишки, тонкой кишки, кожи, пищевода, глаз, гортани, матки, яичника, предстательной железы, сухожилия, костного мозга, крови, лимфы, тестикулярные, вагинальные и опухолевые клетки.
Кроме того, настоящим изобретением представлен способ блокирования, профилактики или лечения воспаления или воспалительного заболевания у субъекта. Воспаление может быть обусловлено воспалительным заболеванием. Воспалительные заболевания могут возникать там, где существует воспаление ткани организма. Воспалительные заболевания включают местные воспалительные реакции и системное воспаление. Примеры таких заболеваний включают: отторжение трансплантированного органа; нарушение реоксигенации, являющееся результатом трансплантации органов (см., Grupp et al. J. Mol. Cell Cardiol. 31:297-303 (1999)), включающей, но не в порядке ограничения, трансплантацию следующих органов: сердца, легкого, печени и почки; хронические воспалительные заболевания суставов, включающие артрит, ревматоидный артрит, остеоартрит и костные заболевания, вызванные повышенным разрежением костей; воспалительные заболевания кишечника, такие как илеит, неспецифический язвенный колит, синдром Беррета и болезнь Крона; воспалительное заболевание легких, такое как астма, синдром расстройства дыхания у взрослых и хроническое обструктивное заболевание дыхательных путей; воспалительные глазные заболевания, включающие дистрофию роговицы, трахому, онхоцеркоз, увеит, симпатическую офтальмиюиэндофтальмит; хронические воспалительные заболевания десен, включающие гингивит и периодонтит; туберкулез; лепру; воспалительные заболевания почек, включающие уремические осложнения, гломерулонефрит и нефроз; воспалительные заболевания кожи, включающие склеродерматит, псориаз и экзему; воспалительные заболевания центральной нервной системы, включающие хроническое демиелинизирующее заболевание нервной системы, рассеянный склероз, вызванную СПИДом нейродегенерацию и болезнь Альцгеймера, инфекционный менингит, энцефаломиелит, болезнь Паркинсона, болезнь Хантингтона, боковой амиотрофический склерози вирусный или аутоиммунный энцефалит; аутоиммунные заболевания, включающие сахарный диабет типа I и типа II; диабетические осложнения, включающие, но не в порядке ограничения, диабетическую катаракту, глаукому, ретинопатию, нефропатию, такую какмикроалюминурияи прогрессирующая диабетическая нефропатия, полиневропатия, гангрена стоп, атеросклеротическое поражение коронарной артерии, периферическое артериальное поражение, некетотическая гипергликемическая-гиперосмолярная кома, мононевропатия, автономная невропатия, язвы стоп, проблемы суставов иосложнение кожи или слизистой оболочки, такое как инфекция, пятна голени, кандидозная инфекция или липоидный диабетический некроз; иммуно-комплексный васкулит, системная красная волчанка(SLE);воспалительные заболевания сердца, такие как кардиомиопатия, ишемическая болезнь сердца,гиперхолестеринемияи атеросклероз, а также различные другие заболевания, несущие существенные воспалительные компоненты, включающиепреэклампсию; хроническую печеночную недостаточность, травму головного и спинного мозгаи раковую опухоль. Воспалительные заболевания могут также быть системным воспалением организма, характерными примерами которых являютсяграмположительный или грамотрицательный шок, геморрагический шок, анафилактический шок или шок, вызываемый противораковой химиотерапиейв ответ на провоспалительные цитокины,например, шок, вызванный противовоспалительными цитокинами. Такой шок может быть вызван, например, химиотерапевтическим средством, принимаемым при лечении рака.
В одном из вариантов изобретения нарушение реоксигенации, являющееся результатом трансплантации органов, происходит во время трансплантации органов.
Изобретение также включает способы лечения, предупреждения или иным способом подавления реперфузионного нарушения у субъекта, нуждающегося в таком лечении, предупреждении или блокировании. Способ включает введение индено[1,2-c]изохинолинового соединения в количестве, достаточном для лечения, предупреждения или блокирования реперфузионного нарушения у субъекта. Реперфузия означает процесс, посредством которого восстанавливается кровоток в кровеносных сосудах после ишемии, такой как возникает после сужения или закупорки сосуда. Реперфузионное нарушение может возникать в результате естественного приступа, такого как инфаркт миокарда, удар, или во время хирургического вмешательства, когда ток крови в сосудах умышленно или неумышленно прекращается.
В некоторых вариантах изобретения субъекту вводят эффективное количество индено[1,2-c]изохинолинового соединения.
Изобретение также включает фармацевтические композиции, полезные для лечения или профилактики воспалительного заболевания или реперфузионного нарушения, или для ингибирования PARS-активности, либо более чем одной из указанных активностей. Композиции могут быть подходящими для внутреннего применения и включать эффективное количество индено[1,2-c]изохинолинового соединения и фармацевтически приемлемого носителя. Индено[1,2-c]изохинолиновые соединения в особенности полезны потому, что проявляют очень низкую периферическую токсичность, либо не обладают периферической токсичностью.
Индено[1,2-c]изохинолиновые соединения могут быть введены в количествах, достаточных для лечения или профилактики воспалительного заболевания или реперфузионного нарушения и/или для остановки развития указанных нарушений у субъекта.
Введение индено[1,2-c]изохинолиновых соединений может быть выполнено любым способом введения терапевтических средств. Такие способы включают системное и локальное введение, такое как введение пероральным, назальным, парентеральным, трансдермальным, подкожным, вагинальным, буккальным, ректальным или местным способами.
В зависимости от предлагаемого способа введения композиции могут быть в твердой, полутвердой или жидкой лекарственной форме, такой как, например, инъекции, таблетки, суппозитории, пилюли, капсулы замедленного высвобождения, эликсиры, настойки, эмульсии, сиропы, порошки, жидкости, суспензии или тому подобное, предпочтительно в виде стандартных лекарственных доз в соответствии с общепринятой фармацевтической практикой. Кроме того, указанные композиции могут также быть введены во внутривенной (как болюсы, так и вливание), внутрибрюшинной, подкожной или внутримышечной форме, все используемые формы хорошо известны специалистам в области фармацевтики.
Иллюстративными примерами фармацевтических композиций являются таблетки и желатиновые капсулы, содержащие индено[1,2-c]изохинолиновое соединение вместе с фармацевтически приемлемым носителем, таким как a) разбавитель, например,лактоза, декстроза, сахароза, маннит, сорбит, целлюлоза, натриевая соль, сахарин, глюкоза и/или глицин; b) смазывающее вещество, например, диоксид кремния, тальк, стеариновая кислота, соль магния или кальция и стеариновой кислоты, олеат натрия, стеарат натрия, стеарат магния, бензоат натрия, ацетат натрия, хлорид натрия и/или полиэтиленгликоль; для таблеток также c) связующее вещество, например, магнийалюминийсиликат, крахмальный клейстер, желатин, трагакантовая камедь, метилцеллюлоза, натрийкарбоксиметилцеллюлоза, карбонат магния, природные сахара, такие как глюкоза или бета-лактоза, кукурузные подсластители, природные и синтетические камеди, такие как аравийская камедь, трагакант, или альгинат натрия, воски и/или поливинилпирролидон; при необходимости, d) дезинтегрирующее средство, например,крахмалы, агар, метилцеллюлоза, бентонит, ксантановая камедь, альгиновая кислота или натриевая соль указанной кислоты, либо шипучие смеси и/или e) абсорбент, краситель, корригент и подсластитель.
Жидкие, в частности, предназначенные для инъекции, композиции могут, например, быть получены путем растворения, дисперсии и т.д. Например, индено[1,2-c]изохинолиновое соединение растворяют в фармацевтически приемлемом растворителе или смешивают с указанным растворителем, таким как, например, вода, физиологический раствор, водная декстроза, глицерин, этанол и тому подобное, получая таким образом изотонический раствор или суспензию, пригодные для инъекции.
Индено[1,2-c]изохинолиновые соединения могут также быть сформулированы в виде суппозитория, который может быть получен из жировых эмульсий или суспензий при использовании полиалкиленгликолей, таких как пропиленгликоль, в качестве носителя.
Индено[1,2-c]изохинолиновые соединения могут также быть введены в форме липосомных систем доставки, таких как небольшие моноламеллярные везикулы, крупные моноламеллярные везикулы и мультиламеллярные везикулы. Липосомы могут быть образованы разнообразными фосфолипидами, содержащими холестерин, стеариламин или фосфатидилхолины. В некоторых вариантах изобретения, пленку липидных компонентов гидратируют водным раствором лекарственного средства, получая липидный слой, инкапсулирующий лекарственное средство, как описано в патенте Соединенных Штатов № 5262564.
Индено[1,2-c]изохинолиновые соединения могут также доставляться с использованием моноклональных антител в качестве индивидуальных носителей, с которыми связаны молекулы индено[1,2-c]изохинолиновых соединений. Индено[1,2-c]изохинолиновые соединения могут также быть связаны с растворимыми полимерами в качестве прицельных лекарственных носителей. Такие полимеры могут включать поливинилпирролидон, сополимер пирана, полигидроксипропилметакриламидофенол, полигидроксиэтиласпанамидофенол или полиэтиленоксидполилизин, замещенный пальмитоиловыми остатками. Кроме того, индено[1,2-c]изохинолиновые соединения могут быть связаны с классом биоразлагаемых полимеров, полезных для достижения регулируемого высвобождения лекарственного средства, например, с полимолочной кислотой, полиэпсилонкапролактоном, полигидроксимасляной кислотой, сложными полиортоэфирами, полиацеталями, полигидропиранами, полицианоакрилатами и сшитыми или амфифильными блоксополимерами гидрогелей.
Парентеральное инъекционное введение обычно используют в случае подкожных, внутримышечных или внутривенных инъекций и инфузий. Инъецируемые препараты могут быть получены в общепринятых формах, либо в виде жидких растворов или суспензий, либо в твердых формах, подходящих для растворения в жидкости перед инъекцией.
В одном из вариантов парентерального введения используют имплантацию системы медленного высвобождения или замедленного высвобождения, согласно патенту US 3710795, включенному в данное описание в качестве ссылки.
Композиции могут быть стерильными или содержать нетоксичные количества вспомогательных веществ, таких как консерванты, стабилизаторы, увлажнители или эмульгаторы, промоторы растворения, соли для регулирования осмотического давления, регулирующие pH буферные средства и другие вещества, включающие, но не в порядке ограничения, ацетат натрия или триэтаноламинолеат. Кроме того, указанные композиции могут также содержать другие терапевтически значимые вещества.
Композиции могут быть получены согласно общепринятым способам смешивания, гранулирования или нанесения защитной оболочки, соответственно, и рассматриваемые фармацевтические композиции могут содержать приблизительно от 0,1% до 99%, от 1% до 70% индено[1,2-c]изохинолинового соединения по массе или объему.
Схему приема индено[1,2-c]изохинолинового соединения выбирают в соответствии с различными факторами, включающими вид, возраст, массу, пол и состояние пациента; тяжесть излечиваемого заболевания; способ введения; почечную или печеночную функцию пациента и конкретное используемое индено[1,2-c]изохинолиновое соединение. Специалист в данной области, лечащий врач или ветеринар, легко может определить и прописать эффективное количество лекарственного средства, требуемое для предупреждения, противодействия прогрессированию или остановки прогрессирования состояния.
Эффективные количества лекарственного средства по настоящему изобретению, при употреблении в целях указанных воздействий, составляют приблизительно в пределах от 0,05 до 1000 мг индено[1,2-c]изохинолинового соединения в день. Композиции могут содержать приблизительно 0,5, 1,0, 2,5, 5,0, 10,0, 15,0, 25,0, 50,0, 100,0, 250,0, 500,0 или 1000,0 мг индено[1,2-c]изохинолинового соединения. В одном из вариантов изобретения композиции представлены в форме таблеток, которые разделены насечками. Эффективные уровни в плазме индено[1,2-c]изохинолиновых соединений могут составлять приблизительно в пределах от 0,002 мг до 50 мг на кг массы тела в день.
Индено[1,2-c]изохинолиновые соединения могут быть введены в однократной суточной дозе, либо общая суточная доза может быть представлена в виде разделенной суточной дозы, вводимой два, три или четыре раза в день. Кроме того, индено[1,2-c]изохинолиновые соединения могут быть введены в интраназальной форме путем местного применения подходящих интраназальных носителей, или трансдермальными способами, путем использования соответствующих форм трансдермальных пластырей для кожи, хорошо известных специалистам в данной области. При введении в форме трансдермальной системы доставки режим введения лекарства в соответствии со схемой приема может быть скорее непрерывным, чем периодическим. Другие иллюстративные примеры местных препаратов включают кремы, мази, лосьоны, аэрозольные спреи и гели, где концентрация индено[1,2-c]изохинолинового соединения может изменяться в пределах приблизительно от 0,1% до 15%, мас./мас. или мас./об.
Способы получения индено[1,2-c]изохинолиновых соединений
Примеры способов синтеза, полезных для получения индено[1,2-c]изохинолиновых соединений, представлены в приведенных ниже примерах и обобщены схемами 1 и 2.
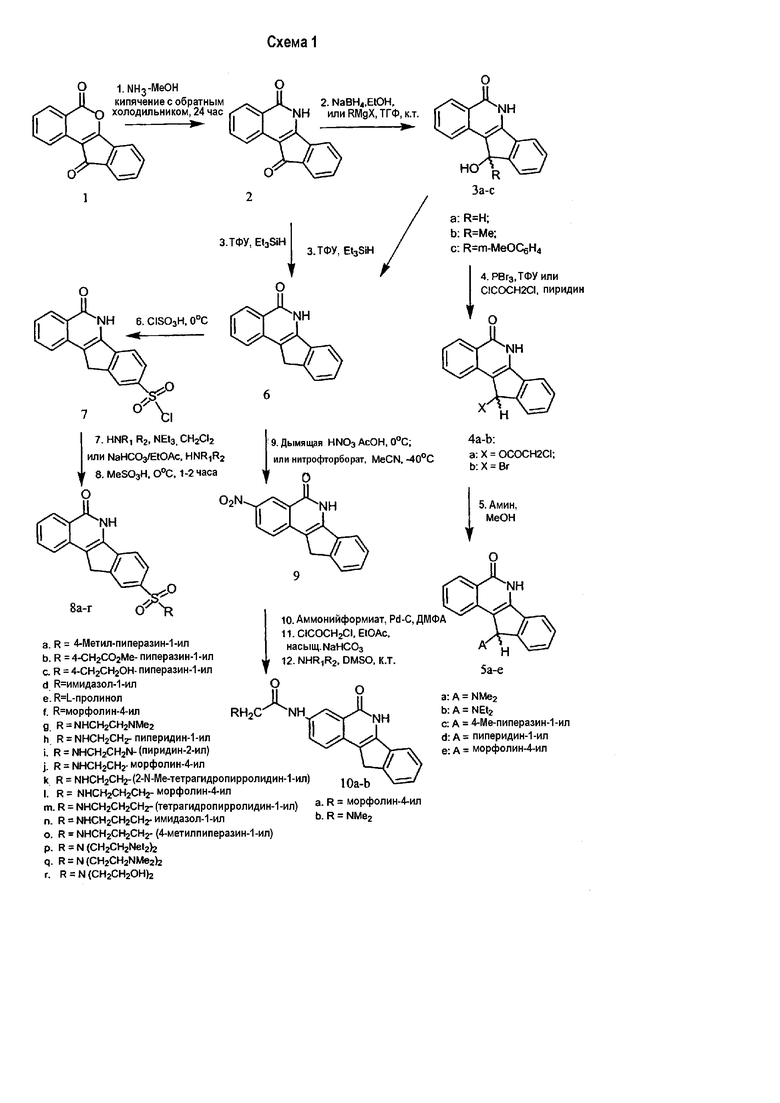
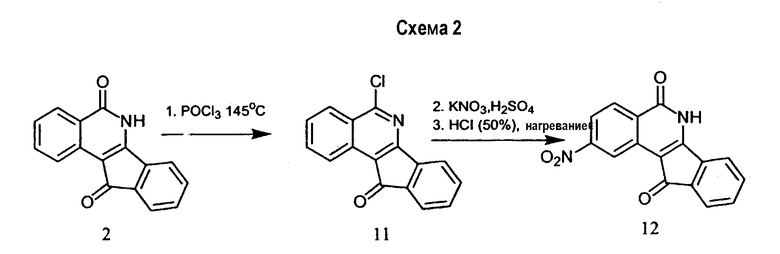
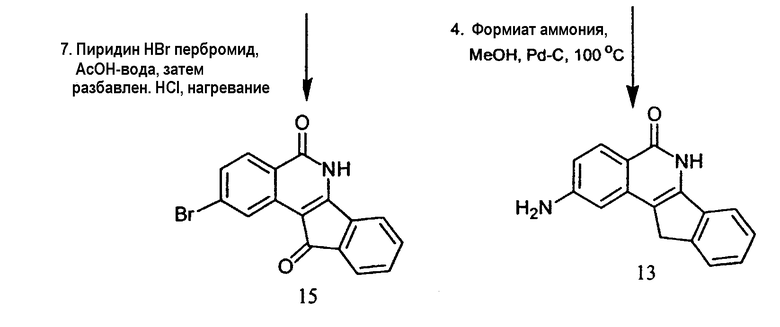

5,6-Дигидро-5,11-дикето-11Н-индено[1,2-c]изохинолин получают взаимодействием соединения 1 (Aldrich Chemical, Milwaukee, WI) с аммиаком в метаноле.
(±)11-Гидрокси-5,6-дигидро-5-оксо-11H-индено[1,2-c]изохинолин (3a) получают взаимодействием 2 с NaBH4 в этаноле.
(±)11-Гидрокси-11-метил-5,6-дигидро-5-оксо-11H-индено[1,2-c]изохинолин (3b) получают взаимодействием 2 с MeMgI.
(±)11-Гидрокси-11-(м-метоксифенил)-5,6-дигидро-5-оксо-11H-индено[1,2-c]изохинолин (3c) получают из 2, используя м-MeO-C6H4MgI.
(±)11-N,N-Диметиламино-5,6-дигидро-5-оксо-11H-индено[1,2-c]изохинолин (5a) получают из 3a, используя хлорацетилхлорид, при последующем взаимодействии с диметиламином. Подобным образом получают:
(±)11-N,N-диэтиламино-5,6-дигидро-5-оксо-11H-индено[1,2-c]изохинолин (5b),
(±)11-N-(пиперидино-1-ил)-5,6-дигидро-5-оксо-11H-индено[1,2-c]изохинолин (5d),
(±)11-N-(4-метилпиперазино-1-ил)-5,6-дигидро-5-оксо-11H-индено[1,2-c]изохинолин (5c),
(±)11-N-(морфолино-4-ил)-5,6-дигидро-5-оксо-11H-индено[1,2-c]изохинолин (5e).
(±) 11-N-(Морфолино-4-ил)-5,6-дигидро-5-оксо-11H-индено[1,2-c]изохинолин (5e) также получают из (±)11-бром-5,6-дигидро-5-оксо-11H-индено[1,2-c]изохинолина (4b).
5,6-Дигидро-5-оксо-11Н-индено[1,2-c]изохинолин(6) получают восстановлением 5,6-дигидро-5,11-дикето-11Н-индено[1,2-c]изохинолина (2) или (±)11-гидрокси-5,6-дигидро-5-оксо-11H-индено[1,2-c]изохинолина (3a), используя CF3COOH/триэтилсилан. 9-Хорсульфонил-5,6-дигидро-5-оксо-11H-индено[1,2-c]изохинолин (7) получают хлорсульфонированием 5,6-дигидро-5-оксо-11H-индено[1,2-c]изохинолина (6). 9-[N-(4-Метилпиперазин-1-ил)сульфонил]-5,6-дигидро-5-оксо-11H-ндено[1,2-c]изохинолин (8a) получают из 9-хлорсульфонил-5,6-дигидро-5-оксо-11H-ндено[1,2-c]изохинолина (7) и N-метилпиперазина. Подобным образом получают:
9-[N-(4-карбометоксиметиленпиперазино-1-ил)сульфонил]-5,6-дигидро-5-оксо-11H-ндено[1,2-c]изохинолин(8b),
9-[N-4-(2-гидроксиэтилпиперазино-1-ил)сульфонил]-5,6-дигидро-5-оксо-11H-ндено[1,2-c]изохинолин (8c),
9-[N-(имидазоло-1-ил)сульфонил]-5,6-дигидро-5-оксо-11H-индено[1,2-c]изохинолин (8d),
9-[N-(2-гидроксипролинил)сульфонил]-5,6-дигидро-5-оксо-11H-индено[1,2-c]изохинолин (8e),
9-[N-морфолинсульфонил]-5,6-дигидро-5-оксо-11H-ндено[1,2-c]изохинолин(8f),
9-[N-(2-[N,N-диметиламино]этил)аминосульфонил]-5,6-дигидро-5-оксо-11H-индено[1,2-c]изохинолин (8g),
9-[N-(2-[пиперидино-1-ил]этил)аминосульфонил]-5,6-дигидро-5-оксо-11H-индено[1,2-c]изохинолин (8h),
9-[N-(2-(пиридино-2-ил)этил)аминосульфонил]-5,6-дигидро-5-оксо-11H-индено[1,2-c]изохинолин (8i),
9-[N-(2-[морфолино-4-ил]этил)аминосульфонил]-5,6-дигидро-5-оксо-11H-индено[l,2-c]изохинолин (8j),
9-[N-(2-[N-метилтетрагидропирролидино-1-ил]этил)аминосульфонил]-5,6-дигидро-5-оксо-11H-ндено[1,2-c]изохинолин(8k),
9-[N-(3-[морфолино-4-ил]пропил)аминосульфонил]-5,6-дигидро-5-оксо-11H-ндено[1,2-c]изохинолин (8l),
9-[N-(3-[тетрагидропирролидино-1-ил]пропил)аминосульфонил]-5,6-дигидро-5-оксо-11H-ндено[1,2-c]изохинолин(8m),
9-[N-(3-[имидазоло-1-ил]пропил)аминосульфонил]-5,6-дигидро-5-оксо-11H-ндено[1,2-c]изохинолин (8n),
9-[N-[3-(4-метилпиперазино-1-ил]пропил)аминосульфонил]-5,6-дигидро-5-оксо-11H-ндено[1,2-c]изохинолин (8o),
9-[N,N-ди-(2-[N,N-диэтиламино]этил)аминосульфонил]-5,6-дигидро-5-оксо-11H-ндено[1,2-c]изохинолин(8p),
9-[N,N-ди-(2-[N,N-диметиламино]этил)аминосульфонил]-5,6-дигидро-5-оксо-11H-ндено[1,2-c]изохинолин(8q) и
9-[N,N-ди-(2-[N,N-дигидроксиэтиламино]этил)аминосульфонил]-5,6-дигидро-5-оксо-11H-ндено[1,2-c]изохинолин (8r).
Амидные производные, 3-морфолин-4-ил-N-(5-оксо-5,11-дигидро-6Н-индено[1,2-c]изохинолин-3-ил)ацетамид(10a), 3-диметиламино-N-(5-оксо-5,11-дигидро-6Н-индено[1,2-c]изохинолин-3-ил)ацетамид (10b)и 2-диметиламино-N-(5-оксо-5,11-дигидро-6Н-индено[1,2-c]изохинолин-2-ил)ацетамид(14) получают из 5,6-дигидро-5-оксо-11H-индено[1,2-c]изохинолина (6) и 5-хлор-11H-индено[1,2-c]изохинолина(11), используя нитрование, затем восстановление и последующее аминирование хлорацетамидного промежуточного соединения. 2-Бром-5,6-дигидро-5-оксо-11H-индено[1,2-c]изохинолин(15) получают бромированием хлорамидата 11.
Далее изобретение описывается следующими примерами, которые не ограничивают объем изобретения, определяемый приложенной формулой изобретения. Следующие примеры иллюстрируют синтез характерных индено[1,2-c]изохинолиновых соединений в соответствии с изобретением и демонстрируют полезность указанных соединений при лечении или профилактике воспалительного заболевания или реперфузионного нарушения.
5. ПРИМЕРЫ
Пример 1
Синтез иллюстративных индено[1,2-c]изохинолиновых соединений
a) Общие способы
Протонный ЯМР-спектр получают, используя спектрофотометр Varian 300 МГц и величины химических сдвигов (δ) представляют в миллионных долях (м.д.). ТСХ выполняют, используя пластины для ТСХ с предварительно нанесенным слоем силикагеля 60 F-254, а препаративную ТСХ осуществляют, используя пластины для ТСХ с фильтрующим слоем Whatman 60A. Все промежуточные и конечные соединения характеризуются данными 1H-ЯМР и МС.
b) Синтез 5,6-дигидро-5,H-дикето-11Н-индено[1,2-c]изохинолина (2):
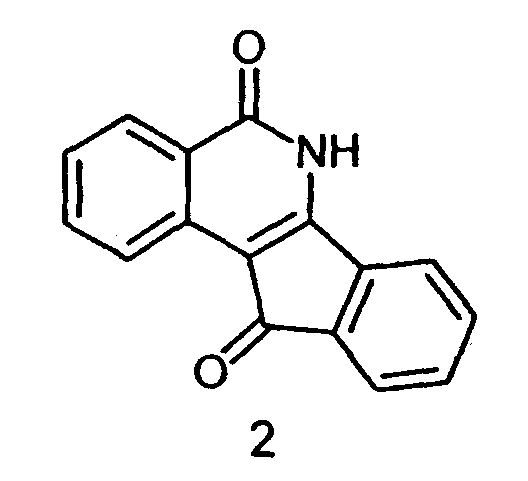
Перемешиваемую суспензию соединения 1 (55 г, 0,22 моль) в NH3/MeOH (7,0н, 700 мл) кипятят с обратным холодильником в течение 24 ч. Затем реакционную смесь оставляют охлаждаться до комнатной температуры, отфильтровывают и тщательно промывают MeOH, получая 46 г указанного в заголовке продукта оранжевого цвета с выходом 84%.
1Н ЯМР (ДМСО-d6) δ: 7,48-7,61 (м, 4H), 7,80-7,88 (м, 1H), 7,86 (д, J=8,7 Гц, 1H), 8,22 (д, J=8,4 Гц, 1H), 8,44 (д, J=7,5 Гц, 1H), 13,05 (c, 1H); 13C ЯМР (ДМСО-d6): δ106,33, 121,63, 122,94, 123,27, 124,80, 128,45, 132,17, 133,60, 134,03, 134,68, 134,68, 134,81, 137,09, 156,41, 163,76, 190,57; MC (ES-): m/z 246,2 (М-1); Анализ. Вычислено для С16Н9NO2: С, 77,72; H, 3,67; N, 5,67; Найдено: С, 77,54; H, 3,69, N, 5,69.
c) Синтез (±)11-гидрокси-5,6-дигидро-5-оксо-11H-индено[1,2-c]изохинолина (3a):
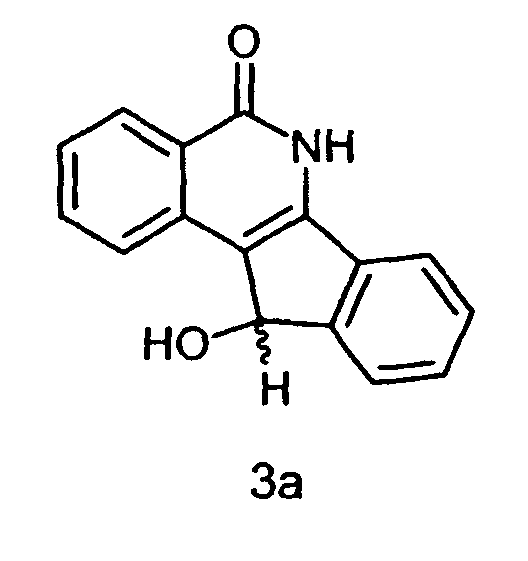
К перемешиваемой суспензии соединения 2 (2,5 г, 0,01 моль) в EtOH (25 мл) при комнатной температуре небольшими порциями за 30 мин добавляют NaBH4 (3,75г, 0,1моль). Реакционную смесь перемешивают еще 2 ч и затем охлаждают до 0°C, после чего растирают c разбавленной HCl (10% раствор). Выпавший в результате осадок твердого вещества отфильтровывают и промывают водой и MeOH, получая соединение 3a (2,326 г, 92%).
1Н ЯМР (ДМСО-d6) δ: 5,58 (д, J=8,1 Гц, 1H), 5,78 (д, J=8,7 Гц, 1H), 7,33-7,89 (м, 6H), 7,95 (д, J=7,8 Гц, 1Н), 8,22 (д, J=7,8 Гц, 1H), 12,29 (c, 1H); 13C ЯМР (ДМСО-d6): δ 77,44, 118,81, 120,15, 124,28, 125,04, 125,67, 126,34, 128,46, 128,64, 128,95, 133,27, 135,62, 136,12, 139,93, 148,55, 163,69; MC (ES+): m/z 250,1 (М+1); Анализ. Вычислено для С16Н11NO2: С, 77,10; Н, 4,45; N, 5,62. Найдено: С, 77,01; Н, 4,57, N, 5,59.
Подобным образом, взаимодействием соединения 2 с MeMgI и м-MeO-C6H4MgBr, соответственно, получают соединения: (±)11-гидрокси-11-метил-5,6-дигидро-5-оксо-11Н-индено[1,2-c]изохинолин (3b) и (±)11-гидрокси-11-(м-метоксифенил)-5,6-дигидро-5-оксо-11H-индено[1,2-c]изохинолин (3c).
d) Синтез 11-замещенных 5,6-дигидро-5-оксо-11Н-индено[1,2-c]изохинолинов (5a-e):
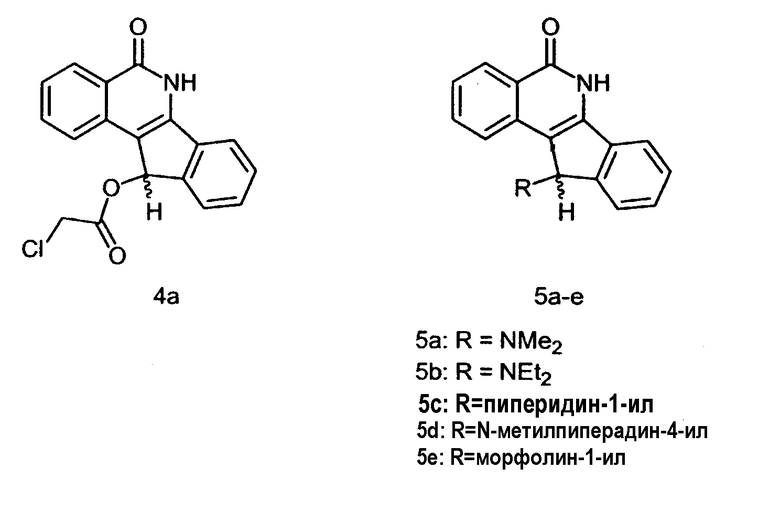
К перемешиваемой суспензии соединения 3a (0,5г, 0,002 моль) в пиридине (10 мл) добавляют хлорацетилхлорид (0,81 г, 0,006 моль) при 0°C. Реакционной смеси дают нагреться до комнатной температуры и перемешивают в течение 24 ч. Затем реакционную смесь выливают на лед и экстрагируют EtOAc. Органический слой отделяют, сушат и концентрируют, получая неочищенное соединение 4a, которое в дальнейшем обрабатывают диметиламином и перемешивают при комнатной температуре в течение 24 ч. Реакционную смесь выливают на лед и обрабатывают 10% HCl. Затем полученную смесь подщелачивают насыщенным водным NaHCO3, и полученное в результате твердое вещество отфильтровывают, получая требуемый продукт 5a.
1Н ЯМР (ДМСО-d6) δ: 2,31 (c, 6H), 5,00 (c, 1H), 7,28-7,45 (м, 3H), 7,68-7,73 (м, 2H), 7,95 (д, J=6,9 Гц, 1H), 8,10 (д, J=7,8 Гц, 1H), 8,21 (д, J=8,1 Гц, 1H), 12,26 (c, 1H); 13C ЯМР (ДМСО-d6) δ: 68,09, 116,28, 120,52, 124,58, 125,74, 126,27, 126,34, 127,68, 128,64, 133,02, 136,27, 144,45, 163,80; MC (ES+): m/z 277,2 (М+1).
Следующие соединения также получают взаимодействием указанного выше соединения 4a с диэтиламином, пиперидином, N-мтилпиперидином и морфолином, соответственно:
(±)11-диэтиламино-5,6-дигидро-5-оксо-11H-индено[1,2-c]изохинолин (5b)
(±)11-пиперидино-5,6-дигидро-5-оксо-11H-индено[1,2-c]изохинолин (5c)
(±)11-(м-метилпиперазино)-5,6-дигидро-5-оксо-11H-индено[1,2-c]изохинолин (5d)
(±)11-морфолино-5,6-дигидро-5-оксо-11H-индено[1,2-c]изохинолин (5e).
e) Синтез (±)11-морфолино-5,6-дигидро-5-оксо-11H-индено[1,2-c]изохинолинов (5e) из 4b
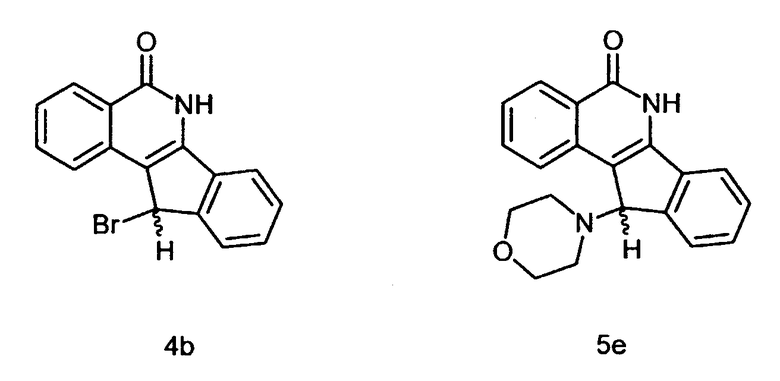
К перемешиваемой суспензии соединения 3a (0,6г, 2,4 ммоль) в трифторуксусной кислоте (5мл) добавляют трибромид фосфора (1,0 M раствор в CH2Cl2, 3 мл) при комнатной температуре и реакционную смесь перемешивают в течение 8 ч. Реакционную смесь выливают на лед и полученное в результате твердое вещество отфильтровывают, получая бромированное соединение 4b (0,61 г, 76%).
1Н ЯМР (ДМСО-d6) δ: 7,35-7,50 (м, 3H), 7,61 (д, J=6,6 Гц, 1H), 7,73-7,82 (м, 211), 7,94 (д, J=6,6 Гц, 1H), 8,23 (д, J=7,8 Гц, 1Н), 12,41 (c, 1H); 13C ЯМР (ДМСО-d6) δ: 52,06, 79,35, 114,43, 120,56, 123,58, 125,27, 125,50, 126,68, 128,55, 128,86, 129,66, 133,73, 135,91, 136,61, 141,39, 143,95, 163,74.
Соединение 4b (0,5 г) суспендируют в MeOH (10мл), обрабатывают избытком морфолина (˜10 экв.) при комнатной температуре и перемешивают при 60°C в течение 3 ч. Реакционную смесь выливают на лед и разбавляют этилацетатом (40 мл). Органический слой отделяют и экстрагируют разбавленной HCl (10% раствор), затем водный слой подщелачивают насыщенным водным NaHCO3 и выпавший в результате осадок твердого вещества отфильтровывают и сушат, получая соединение 5e (0,46 г, 90%).
1Н ЯМР (ДМСО-d6) δ: 2,56 (м, 4H), 3,49 (м, 4H), 5,04 (c, 1H), 7,31-7,45 (м, 3H), 7,65-7,76 (м, 2H), 7,96 (д, J=7,2Гц, 1H), 8,20-8,24 (м, 2H), 12,29 (c, 1H); 13C ЯМР (ДМСО-d6) δ: 49,36, 67,62, 68,11, 115,20, 120,60, 124,47, 125,84, 126,34, 126,41, 127,76, 128,30, 128,72, 133,09, 136,30, 136,96, 140,35, 144,44, 163,67.
f)Синтез 5,6-дигидро-5-оксо-11H-индено[1,2-c]изохинолина (6):
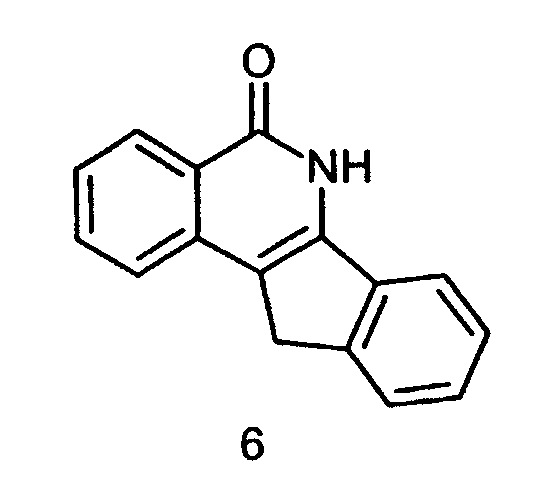
Способ I: к перемешиваемому раствору спирта 3a (0,35 г, 1,4 ммоль) в трифторуксусной кислоте (10 мл) добавляют при комнатной температуре триэтилсилан (0,812 г, 7 ммоль) и реакционную смесь перемешивают в течение 24 ч. Трифторуксусную кислоту выпаривают в вакууме и к полученному неочищенному продукту добавляют EtOAc. Полученное твердое вещество отфильтровывают и промывают H2O и EtOAc, что дает указанное в приведенном выше заголовке соединение 6 (0,285 г, 87%).
1Н ЯМР (ДМСО-d6) δ: 3,89 (c, 2H), 7,30-7,47 (м, 3H), 7,59 (д, J=6,9 Гц, 1H), 7,72-7,74 (м, 2H), 7,98 (д, J=7,8 Гц, 1H), 8,23 (д, J=8,4 Гц, 1H), 12,31 (c, 1H); 13C ЯМР (ДМСО-d6) δ: 33,51, 116,50, 120,19, 124,01, 125,51, 125,55, 126,42, 127,50, 127,68, 128,56, 133,45, 136,39, 137,53, 140,18, 143,80, 163,46; MC (ES-): m/z 232,1 (М-1); Анализ. Вычислено для С16Н11NO: С, 82,38; Н, 4,75; N, 6,00. Найдено: С, 81,79; Н, 4,45, N, 5,99.
Способ II: К перемешиваемой суспензии соединения 2 (40 г, 0,16 моль) в трифторуксусной кислоте (2,5 л) небольшими порциями при комнатной температуре добавляют триэтилсилан (94 г, 0,8 моль) и реакционную смесь перемешивают в течение 96 ч, в течение указанного периода времени протекание реакции контролируют с помощью ТСХ (элюент - 5% MeOH/CH2Cl2). Реакционную смесь медленно выливают на лед, отфильтровывают, промывают большим количеством H2O и MeOH и сушат в вакууме, получая указанное в приведенном выше заголовке соединение 6 (33,1 г, 88%), спектральные данные для которого идентичны спектральным данным, соответствующим образцу соединения 6, полученного, применяя способ I.
g) Синтез 9-хлорсульфонил-5,6-дигидро-5-оксо-11H-индено[1,2-c]изохинолина(7):
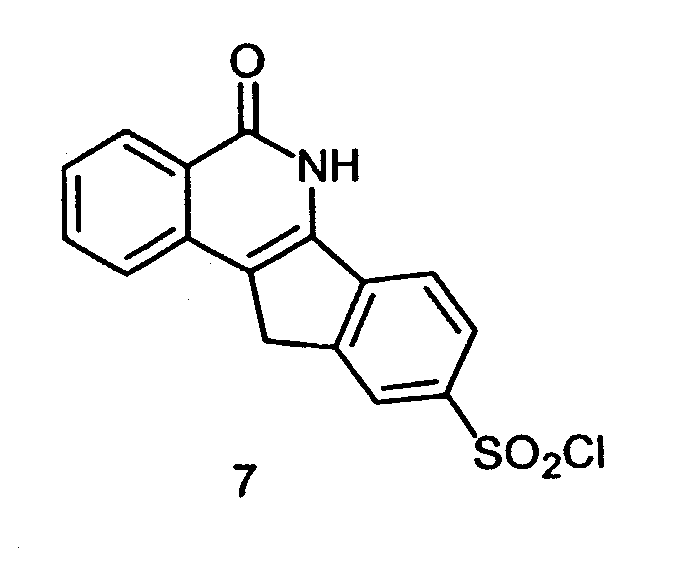
Соединение 6 (40г, 0,17моль) добавляют небольшими порциями к хлорсульфонилхлориду (112 мл, 1,71 моль) при 0°C, реакционной смеси дают нагреться до комнатной температуры и перемешивают в течение 2 ч. Реакционную смесь медленно выливают на лед и полученное в результате желтое твердое вещество отфильтровывают, тщательно промывают водой и EtOAc и сушат в вакууме, получая указанный в приведенном выше заголовке продукт 7 (52 г, 92%).
1Н ЯМР (ДМСО-d6) δ: 3,91 (c, 2H), 7,43-7,48 (м, 1H), 7,60 (д, J=7,2 Гц, 1H), 7,7-7,76 (м, 2H), 7,79 (c, 1H), 7,90 (д, J=7,5 Гц, 1H), 8,23 (д, J=7,8 Гц, 1H). Анализ. Вычислено для С16Н12ClNO4S: C, 54,94; H, 3,46; N, 4,00. Найдено: C, 55,28; H, 3,43, N, 3,68. Карл-Фишер, 2,95.
h) Синтез 9-сульфонамидо-производных 5,6-дигидро-5-оксо-11Н-индено[1,2-c]изохинолинов (8a-r) из 7:
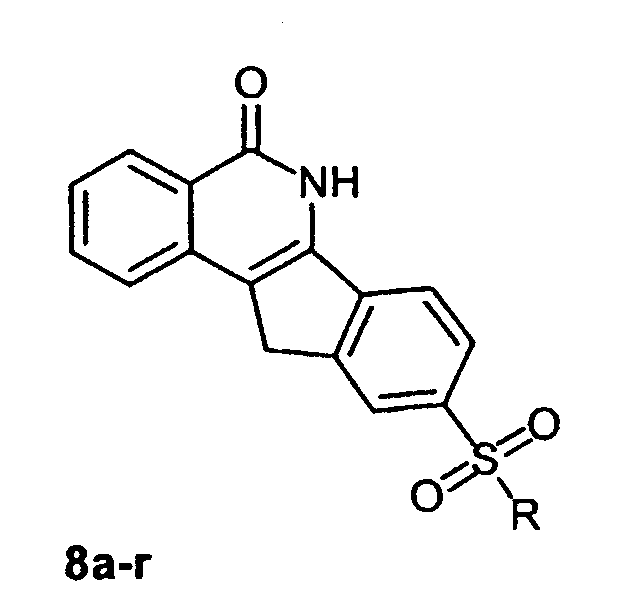
a. R=-N-(4-Метилпиперазин-1-ил)
b. R=-N-(4-CH2CO2Me)-пиперазин-1-ил
c. R=-N-(4-CH2CH2OH)-пиперазин-1-ил
d. R=-N-имидазол-1-ил
e. R=-N-L-пролинил
f. R=-N-морфолин-4-ил
g. R=-NHCH2CH2NMe2
h. R=-NHCH2CH2-пиперидин-1-ил
i. R=-NHCH2CH2-(пиридин-2-ил)
j. R=-NHCH2CH2-морфолин-4-ил
k. R=-NHCH2CH2-(2-N-Me-тетрагидропирролидин-1-ил)
l. R=-NHCH2CH2CH2-морфолин-4-ил
m. R=-NHCH2CH2CH2-(тетрагидропирролидин-1-ил)
n. R=-NHCH2CH2CH2-имидазол-1-ил
o. R=-NHCH2CH2CH2-(4-метилпиперазин-1-ил)
p. R=-N(CH2CH2Net2)2
q. R=-N(CH2CH2NMe2)2
r. R=-N(CH2CH2OH)2
Способ I: к перемешиваемой суспензии 3-(4-морфолино)-1-пропиламина (17,28 г, 0,12 моль) в EtOAc добавляют насыщенный водный. NaHCO3 (300 мл) и смесь оставляют перемешиваться на 15 мин. Затем вносят небольшими порциями при комнатной температуре соединение 7 (4,0 г, 0,012 моль). Реакционную смесь перемешивают в течение 24 ч; отфильтровывают и промывают H2O, EtOAc и MeOH; кипятят в MeOH с обратным холодильником в течение 30 мин; отфильтровывают смесь в нагретом состоянии и промывают MeOH, получая указанный в приведенном выше заголовке продукт 8l в виде свободного основания (2,330 г, 44%).
1Н ЯМР (ДМСО-d6) δ: 1,47-1,52 (м, 2H), 2,16-2,21 (м, 4H), 2,47-2,48 (м, 2H), 3,44-3,48 (м, 2H), 3,23 (м, 4H), 4,02 (c, 2H), 7,49-7,58 (м, 1H), 7,78-7,82 (м, 3Н), 7,97 (c, 1H), 8,14 (д, J=7,8 Гц, 1H), 8,26 (д, J=7,8 Гц, 1H), 9,59 (c, 1H), 12,42 (c, 1H).
Свободные основания 8d, 8g, 8h, 8j, 8l, 8m-8rтакже получают способом I, но заменяя 3-(4-морфолино)-1-пропиламин имидазолом, 2-диметиламиноэтиламином,
2-(N-пиперидинил)этиламином, 2-(N-морфолинил)этиламином,
3-(N-морфолинил)пропиламином,
3-(N-тетрагидропирролидинил)пропиламином,
3-(N-имидазолил)пропиламином,
3-(N-(4-метилпиперазинил)пропиламином,
ди-(2-(диэтиламино)этил)амином, ди-(2-(диметиламино)этил)амином
и ди-(2-гидроксиэтил)амином, соответственно.
9-(N-Сульфонилимидазол)-5,6-дигидро-5-оксо-11Н-индено[1,2-c]изохинолины (8a-r):
Способ II: к перемешиваемой суспензии 3-(4-морфолино)-1-пропиламина (4,250 г) в CH2Cl2 (100 мл) добавляют соединение 7 (1,950 г, 5,89 ммоль) и полученную смесь перемешивают в течение 5 минут. Потом добавляют триэтиламин (3 мл) и реакционную смесь перемешивают в течение 24 час при комнатной температуре. По прошествии указанного времени осадок отделяют и промывают MeOH (2×100 мл) и неочищенное твердое вещество переносят в круглодонную колбу. Указанное вещество разбавляют MeOH (200 мл), кипятят с обратным холодильником в течение 30 мин и смесь отфильтровывают в нагретом состоянии. Полученный плотный осадок на фильтре промывают MeOH (200 мл), что дает требуемый продукт в виде свободного основания 8l (1,460 г, 56%).
Свободные основания соединений 8a-r получают, применяяспособII, но заменяя 3-(4-морфолино)-1-пропиламин имидазолом, 2-диметиламиноэтиламином, 2-(N-пиперидинил)этиламином,
2-(N-морфолинил)этиламином, 3-(N-морфолинил)пропиламином,
3-(N-тетрагидропирролидинил)пропиламином,
3-(N-имидазолил)пропиламином,
3-(N-(4-метилпиперазинил)пропиламином,
ди-(2-(диэтиламино)этил)амином, ди-(2-(диметиламино)этил)амином
и ди-(2-гидроксиэтил)амином, соответственно.
i) Общий способ получения мезилатных солей 8a-r:
Свободное основание 8l добавляют к метансульфоновой кислоте при 0°C, полученной смеси дают нагреться до комнатной температуры и перемешивают в течение 2 ч. Затем реакционную смесь выливают в охлажденный MeOH (в пределах от -10°C до 0°C) и выпавшее в осадок твердое вещество отфильтровывают, промывают MeOH (100 мл) и сушат в вакууме. Затем сухое твердое вещество растворяют в воде (˜200 мл) и лиофилизуют, получая метансульфонатмоногидратную соль соединения 8l (1,020 г, 84%).
1Н ЯМР (ДМСО-d6) δ: 1,75-1,85 (м, 2H), 2,35 (c, 3H), 2,78-2,84 (м, 2H), 2,96-3,12 (м, 4H), 3,36 (д, J=12,3 Гц, 2H), 3,61 (т, J=11,4 Гц, 2H), 3,94 (д, J=12,9 Гц, 2H), 4,03 (c, 2H), 7,49-7,55 (м, 1H), 7,76-7,84 (м, 3H), 7,99 (д, J=0,9 Гц, 1H), 8,15 (д, J=8,4 Гц, 1H), 8,25 (д, J=8,4 Гц, 1H), 9,59 (c, 1H), 12,42 (c, 1H); 13C ЯМР (ДМСО-d6) δ: 24,27, 33,86, 51,89, 54,51, 64,02, 119,70, 120,39, 123,53, 126,09, 126,45, 128,63, 133,66, 135,80, 138,71, 141,21, 144,57, 163,29; Анализ. Вычислено для С24Н31N3O8S2: С, 52,06; Н, 5,46; N, 7,59. Карл-Фишер, 3,36. Найдено: С, 51,85; Н, 5,35, N, 7,30, Карл-Фишер 4,32.
Подобным образом получают соли 8l с HCl, H2SO4, CH3COOH, и янтарной кислотой, заменяя метансульфоновую кислоту HCl, H2SO4 и CH3COOH, соответственно.
Пример 2
Влияние иллюстративных индено[1,2-c]изохинолиновых соединений на активность PARS в культивированных макрофагах, использование анализа на основе цельных клеток и анализ на очищенный фермент
Демонстрацию способности иллюстративных индено[1,2-c]изохинолиновых соединений ингибировать PARS и предотвращать вызываемую пероксинитритом цитотоксичность осуществляют, используя способы, описанные у Virag et al., Br J Pharmacol. 1999, 126(3):769-77 и Immunology 1998, 94(3):345-55. Макрофаги RAW-мышей культивируют в среде DMEM с высоким содержанием глюкозы, дополненной 10% околоплодной сывороткой теленка. Клетки используют при 80% слиянии в 12-луночных планшетах. Клетки предварительно обрабатывают различными концентрациями (100 нМ - 1 мкМ) индено[1,2-c]изохинолинового соединения в течение 10 мин. Пероксинитрит, прототипический оксидант, индуцирующий разрушение отдельных нитей ДНК, используют для индуцирования PARS-активации. Пероксинитрит разводят забуференным фосфатном физиологическим раствором (PBS) (pH 11,0) и добавляют к клеткам в болюсах на 50 мкл. Затем клетки инкубируют в течение 20 мин. Используемый в качестве контроля пероксинитрит разлагают, выдерживая в течение 30 мин при pH 7,0, при этом пероксинитрит теряет способность влиять на исследуемые параметры. После 20 мин инкубации клетки центрифугируют, среду отсасывают и клетки ресуспендируют в 0,5 мл буфера для анализа (56 мМ HEPES pH 7,5, 28 мМ KCl, 28 мМ NaCl, 2 мМ MgCl2, 0,01% мас./об. дигитонин и 0,125 мкМ NAD+ и 0,5 мкКи/мл 3H-NAD+). После инкубации в буфере для анализа (10 мин при 37°C) активность PARS измеряют следующим образом: добавляют 200 мкл охлажденного льдом 50% мас./об. ТХУ и пробы инкубируют в течение 4 часов при 4°C. Затем пробы центрифугируют (10 мин при 10000 g) и осадки в пробирке после центрифугирования дважды промывают охлажденным льдом 5% мас./об. ТХУ солюбилизируют в течение ночи в 250 мкл 2% мас./об. SDS/0,1н NaOH при 37°C. Содержимое пробирок добавляют к 6,5мл сцинтилляционной жидкости ScintiSafe Plus (Fisher Scientific) и измеряют радиоактивность, используя жидкостной сцинтилляционный счетчик (Wallac, Gaithersburg, MD). Результаты, приведенные в таблице 1, демонстрируют, что иллюстративные индено[1,2-c]изохинолиновые соединения существенно и дозозависимо ингибируют активацию PARS при анализе на микрофагах.
Ингибирующее действие различных новых замещенных индено[1,2-c]изохинолинов на PARS-активацию в культивированных макрофагах мышей
Затем определяют эффективность ингибирования очищенного фермента PARS для отобранных индено[1,2-c]изохинолиновых соединений и эффективность сравнивают с соответствующей эффективностью 3-аминобензамида, прототипического эталонного ингибитора PARS. Испытание осуществляют в 96-луночных планшетах ТИФА согласно инструкциям, прилагаемым к промышленно выпускаемому набору для анализа на ингибирование PARS (Trevigen, Gaithersburg, MD). Кратко, лунки, покрытые 1 мг/мл гистоном (50 мкл/лунка), оставляют на ночь при 4°C. Затем планшеты промывают четыре раза PBS и блокируют, добавляя 50 мкл Strep-Diluent (поставляемый в комплекте с набором). После инкубации (1 час, комнатная температура) планшеты промывают четыре раза PBS. Соответственно разведенные растворы ингибиторов PARS объединяют с 2x PARS коктейлем(1,95 мМ NAD+, 50 мкМ биотинилированного NAD+ в 50 мМ TRIS pH 8,0, 25 мМ MgCl2) и ферментом PARS высокой специфической активности (оба поставляются в комплекте с набором) в объеме 50 мкл. Взаимодействию позволяют протекать в течение 30 мин при комнатной температуре. После 4 промывок в PBS объединенный биотин определяют с помощью конъюгированного с пероксидазой стрептавидина (разведение 1:500) и TACS Sapphire субстрата. Анализ подтверждает результаты исследования PARS на основе макрофагов. Например, ингибитор PARS соединение 8l вызывает 50% ингибирование активности PARS в данном испытании при 3 нМ, и, таким образом, является приблизительно в 50000 раз эффективнее эталонного соединения, 3-аминобензамида.
Пример 3
Влияния иллюстративных индено[1,2-c]изохинолиновых соединений на различные модели воспалительного заболевания и реперфузионного нарушения
a:Влияния иллюстративных индено[1,2-c]изохинолиновых соединений на клеточные модели заболеванияin vitro
В дополнительных исследованиях на изолированных тимоцитах in vitro клетки подвергают действию пероксинитрита или пероксида водорода (токсические оксиданты) для индуцирования цитотоксичности. В такой системе токсичность, по меньшей мере частично, связана с активацией нуклеарного фермента PARS. При таком анализе на стимулированные оксидантами тимоциты (описанном подробно у Virag et al., Immunology 94(3):345-55, 1998), исследуемые соединения предотвращают вызванное оксидантом угнетение жизнеспособности клеток и ведут себя таким образом в низкой наномолярной области концентраций. Пример подобного реагирования (соединение 8l) показан в таблице 2. Такое испытание представляет модель in vitro клеток, погибающих по причине воздействия прооксидантов, как это наблюдается при реперфузии ишемизированных органов.
Снижение индуцируемой пероксинитритом цитотоксичности под действием 30 нМ - 3 мкМ индено[1,2-c]изохинолинового соединения 8l
30 нМ
100 нМ
300 нМ
1 мкМ
3 мкМ
b:Влияние иллюстративных индено[1,2-c]изохинолиновых соединений на модели воспалительных заболеваний in vivo
С целью доказательства эффективности соединений при воспалительных заболеваниях демонстрируется влияние иллюстративных индено[1,2-c]изохинолиновых соединений на модели системного воспаления, вызываемого бактериальным липополисахаридом (LPS), который, как сообщается, отвечает за возникновение реперфузионных нарушений и воспалительных заболеваний, таких как септический шок и синдром системной воспалительной реакции у животных (см., Parrillo, N. Engl. J. Med., 328:1471-1478 (1993) и Lamping, J. Clin. Invest. 101:2065-2071 (1998)). В серии экспериментов мышам предварительно интраперитонеально вводят 0,1 и 1 мг/кг соединений 8l, 8pи 8j, вводят и.п. LPS при 10 мг/кг и измеряют TNF-альфа в плазме через 90 мин. Как показано в таблице 3, все соединения существенно снижают продуцирование TNF, что указывает на противовоспалительную активность соединений.
Снижение вызванного LPS продуцирования TNF, при интраперитонеальной инъекции 0,1-1 мг/кг ингибирующих PARS соединений 8l, 8Р и 8J, у мышей in vivo
(0,1 мг/кг)
(1,0 мг/кг)
(0,1 мг/кг)
(1,0 мг/кг)
(0,1 мг/кг)
(1,0
мг/кг)
±385,2
±377,1
±184,4
±203,7
±300,9
±311,5
±904,4
Все соединения заметно подавляют индуцируемое LPS продуцирование TNF по сравнению с контролем.
При высоких дозах LPS вызывает множественную дисфункцию органов, похожую на септический шок, и, в конечном счете, гибель (отчасти вследствие первоначального высвобождения TNF-альфа). Подобным образом, на модели, индуцируемой слепокишечной перевязкой и проколом (CLP), живые бактерии кишечной флоры индуцируют системное воспаление и шок. Агенты, которые ингибируют продуцирование медиатора воспаления, активацию PARS и клеточный некроз на данной модели, предотвращают летальность, вызываемую LPS или CLP. В экспериментах на мышах Balb/c, интраперитонеальное введение 100 мг/кг LPS вызывает гибель у 50% животных за 24 ч, тогда как обработка животных 3 мг/кг/день соединением 8l снижает вызываемую эндотоксином летальность до 10% в тех же самых экспериментальных условиях. В ответ на CLP-индуцированный шок, соединение 8l (3 мг/кг/день) вызывает снижение летальности от 100% гибели до 60% гибели за 24 часа.
Данные, демонстрирующие снижение продуцирования TNF с помощью иллюстративных индено[1,2-c]изохинолиновых соединений, используемых на моделях воспаления у животных, в связи с тем фактом, что продуцирование TNF является важным фактором, играющим роль пускового механизма воспаления при различных воспалительных заболеваниях (таких как, например, колит, артрит и нейровоспаление и шок), показывают, что индено[1,2-c]изохинолиновые соединения оказывают терапевтические действия при различных системных и местных воспалительных заболеваниях, включающих отторжение трансплантированных органов, в которое вовлечены как компонент воспалительного заболевания, так и компонент реперфузионного нарушения, и, следовательно, полезны для лечения или профилактики воспалительного заболевания или реперфузионного нарушения.
c:Влияние иллюстративных индено[1,2-c]изохинолиновых соединений на модели реперфузионных нарушений in vivo
С целью доказательства эффективности индено[1,2-c]изохинолиновых соединений при состояниях ишемия/реперфузия исследуют влияние иллюстративных индено[1,2-c]изохинолиновых соединений на модели ишемической и реперфузионной кишки у мышей. Пережимают верхнюю мезентериальную артерию в течение 45 мин, после чего следует реперфузия в течение 1 ч. После окончания реперфузии проницаемость кишки измеряют методом FD4 в выравнившихся мешках кишки (Liaudet et al; Shock 2000, 14(2): 134-41). Ишемия-реперфузия снижает проницаемость кишки от 11±4 до 216±27 мл/мин/см2, что свидетельствует о серьезном нарушении подвергшейся реперфузии кишки. Обработка соединением 8l (3 мг/кг в.в., вводимым за 10 мин до инициации реперфузии) доводит рост проницаемости приблизительно до 73%, что свидетельствует о явном сохранении функции кишки. Исследования ишемия-реперфузия в кишке сопровождаются 80% летальностью за 12 часов, тогда как только 15% летальность отмечается у животных, обработанных соединением 8l.
В другой серии экспериментов исследуют влияние соединения 8l на модели окклюзии/реперфузии срединной церебральной артерии у крыс, как описано у Abdelkarim et al., Int J Mol Med. 2001, 7(3):255-60. Окклюзия длится в течение 2 часов с последующей реперфузией в течение 24 часов. Размер инфаркта определяют количественно с помощью окрашивания тетразолием. Соединение 8l вводят при 3 мг/кг/день в виде 3 разделенных интраперитонеальных инъекций, первую дозу начинают вводить за 10 мин до инициации реперфузии. Наблюдается приблизительно 80% снижение степени кортикального некроза и гибели нейронов у животных, получавших соединение 8l, по сравнению с контролями, обработанными растворителем. Такая защита также приносит функциональную пользу, выраженную в неврологических улучшениях в группе, получающей ингибитор PARS.
Приведенные данные показывают, что индено[1,2-c]изохинолиновые соединения оказывают терапевтические действия на различные системные и местные состояния реперфузионных нарушений, включающих отторжение трансплантированных органов, в которое вовлечены как компонент воспалительного заболевания, так и компонент реперфузионного нарушения, и, следовательно, полезны для лечения или профилактики воспалительного заболевания или реперфузионного нарушения.
d:Влияние иллюстративных индено[1,2-c]изохинолиновых соединений на модель диабета
Известно, что ингибиторы PARS и дефицит PARS ослабляют развитие диабета и снижают частоту диабетических осложнений (Mabley et al., Br J Pharmacol. 2001, 133(6):909-9 и Soriano et al., Nat Med. 2001, 7(1):108-13). С целью доказательства эффективности индено[1,2-c]изохинолиновых соединений исследование на модели диабета, вызываемого разовой высокой дозой стрептозотоцина, проводят как описано выше. Кратко, 160 мг/кг стрептозотоцина вводят мышам, обработанным носителем или иллюстративными индено[1,2-c]изохинолиновыми соединениями интраперитонеально (3мг/кг), и спустя 3 дня определяют уровни сахара в крови, используя измеритель глюкозы в крови. Приведенные в таблице 4 данные демонстрируют, что иллюстративные индено[1,2-c]изохинолиновые соединения ослабляют проявление вызванного стрептозотоцином диабета, поскольку указанные соединения снижают повышенное содержание глюкозы в крови.
Снижение вызванной стрептозотоцином (STZ) гипергликемии при интраперитонеальной инъекции 3 мг/кг ингибирующих PARS соединений 8l, 8p и 8j у мышей in vivo
Следовательно, индено[1,2-c]изохинолиновые соединения полезны для лечения или профилактики диабета или диабетических осложнений.
Настоящее изобретение не ограничивается объемом конкретных вариантов выполнения, описанных в примерах, которые предназначены для иллюстрации некоторых аспектов изобретения, и любые функционально эквивалентные варианты входят в объем настоящего изобретения и приложенной формулы изобретения. Безусловно, различные модификации изобретения, в дополнение к тем, что приведены и описаны в данном описании, являются очевидными для специалиста в данной области и считаются входящими в объем приложенной формулы изобретения.
Был приведен ряд ссылок, содержание которых включено в описание во всей полноте.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЗАМЕЩЕННЫЕ 1,2-ДИГИДРО-3Н-ПИРАЗОЛО[3,4-D]ПИРИМИДИН-3-ОНЫ | 2019 |
|
RU2812726C2 |
| ЗАМЕЩЕННЫЕ ИЗОХИНОЛИНОВЫЕ И ИЗОХИНОЛИНОНОВЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ Rho-КИНАЗЫ | 2007 |
|
RU2455302C2 |
| 6-[X-(2-ГИДРОКСИЭТИЛ)АМИНОАЛКИЛ]-5,11-ДИОКСО-5,6-ДИГИДРО-11H-ИНДЕ- НО/1,2-С/ИЗОХИНОЛИНЫ ИЛИ ИХ СОЛИ С НЕОРГАНИЧЕСКИМИ И ОРГАНИЧЕСКИМИ КИСЛОТАМИ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1992 |
|
RU2120939C1 |
| ПРОИЗВОДНЫЕ ЦИКЛИЧЕСКОГО ИМИНОПИРИМИДИНА В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗ | 2018 |
|
RU2801302C2 |
| ПРОИЗВОДНЫЕ НОСКАПИНА (ВАРИАНТЫ), КОМБИНАТОРНАЯ И ФОКУСИРОВАННАЯ БИБЛИОТЕКИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) И ПРИМЕНЕНИЯ | 2006 |
|
RU2304584C1 |
| КОМПОЗИЦИИ И СПОСОБЫ ЛЕЧЕНИЯ КОЛИТА | 2010 |
|
RU2518416C2 |
| ТРИЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2020 |
|
RU2833354C1 |
| ТРИЦИКЛИЧЕСКИЕ КОНДЕНСИРОВАННЫЕ ПРОИЗВОДНЫЕ ПИРИДИН-2-ОНА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ BRD4 | 2016 |
|
RU2734959C2 |
| ПОЛИЦИКЛИЧЕСКИЕ СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ РЕСПИРАТОРНО-СИНЦИТИАЛЬНЫХ ВИРУСНЫХ ИНФЕКЦИЙ | 2004 |
|
RU2422444C2 |
| ЗАМЕЩЕННЫЕ ЦИКЛОАЛКИЛАМИНОМ ПРОИЗВОДНЫЕ ИЗОХИНОЛОНА | 2007 |
|
RU2457203C2 |
Изобретение относится к химии гетероциклических соединений. Описывается соединение формулы
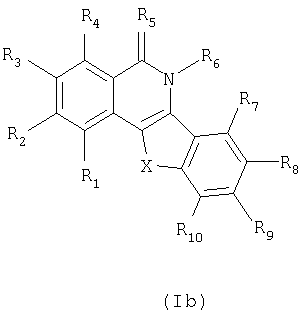
или фармацевтически приемлемые гидрат или соль указанного соединения, где: R5 означает О; R6 означает -Н; Х означает -CH2-, -СН(ОН)(СН2)n- или -CH(NR11R12)-, где n равно 0; R11 и R12 независимо означают водород или -С1-C9алкил, либо N, R11 и R12, взятые вместе, образуют 5-10-членный ароматический или неароматический карбоцикл, в котором 1-4 атома углерода кольца независимо заменены атомом N, О или S, по меньшей мере один из которых является атомом азота; R1, R2, R3, R4, R7, R8, R9 и R10 независимо означают водород или -А-В; где А означает -SO2-; В означает -NZ1Z2, 5-10-членный ароматический или неароматический карбоцикл, в котором 1-4 атома углерода кольца независимо заменены атомом N, О или S, любой из которых является незамещенным или замещен одной или более группами, включающими -C1-С10алкил, -С1-С5алкилен-ОС(O)-С1-С5алкил; и Z1 и Z2 независимо означают -Н или -C1-С10алкил, который является незамещенным или замещен одной или более группами -N(Z3)(Z4), где Z3 и Z4 независимо означают -Н или -С1-С5алкил, который является незамещенным или замещен одной или более гидроксигруппами; либо N, Z3 и Z4, взятые вместе, образуют незамещенный или замещенный 5-10-членный ароматический или неароматический карбоцикл, в котором 1-4 атома углерода кольца независимо заменены атомом N, О или S, по меньшей мере один из которых является атомом азота. 24 н. и 18 з.п. ф-лы, 4 табл.
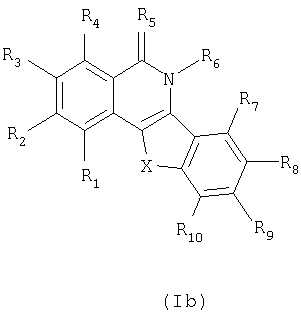
или фармацевтически приемлемые гидрат или соль указанного соединения,
где R5 означает О;
R6 означает -Н;
Х означает -СН2; -СН(ОН)(СН2)n- или -CH(NR11R12)-, где n равно 0;
R11 и R12 независимо означают водород или -С1-С9алкил, либо N, R11 и R12, взятые вместе, образуют 5-10-членный ароматический или неароматический карбоцикл, в котором 1-4 атома углерода кольца независимо заменены атомом N, О или S, по меньшей мере один из которых является атомом азота;
R1, R2, R3, R4, R7, R8, R9 и R10 независимо означают водород или -А-В;
где А означает -SO2-;
В означает -NZ1Z2, 5-10-членный ароматический или неароматический карбоцикл, в котором 1-4 атома углерода кольца независимо заменены атомом N, О или S, любой из которых является незамещенным или замещен одной или более группами, включающими -C1-С10алкил, -C1-С5алкилен-ОС(O)-С1-С5алкил; и
Z1 и Z2 независимо означают -Н или -C1-С10алкил, который является незамещенным или замещен одной или более группами -N(Z3)(Z4), где Z3 и Z4 независимо означают -Н или -C1-C5алкил, который является незамещенным или замещен одной или более гидроксигруппами; либо N, Z3 и Z4, взятые вместе, образуют незамещенный или замещенный 5-10-членный ароматический или неароматический карбоцикл, в котором 1-4 атома углерода кольца независимо заменены атомом N, О или S, по меньшей мере один из которых является атомом азота.
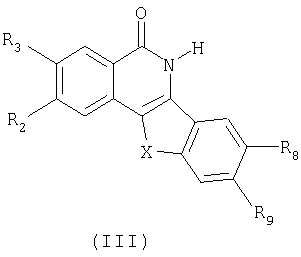
или фармацевтически приемлемые гидрат или соль указанного соединения,
где Х означает -СН2-;
R2 и R3 каждый означает водород;
R8 означает водород;
R9 означает -А-В;
А означает -SO2- или -SO3NH; и
В означает -C1-С3алкил, -NZ1Z2, -алкиламино или 5-10-членный ароматический или неароматический карбоцикл, в котором 1-4 атома углерода кольца независимо заменены атомом N, О или S, где алкиламино или 5-10-членный ароматический или неароматический карбоцикл является незамещенным или замещен одной или более группами, включающими алканол, -алкиламино, -аминоалкил, -аминодиалкил или 5-10-членный ароматический или неароматический карбоцикл, в котором 1-4 атома углерода кольца независимо заменены атомом N, О или S, где алканол, -алкиламино, -аминоалкил, -аминодиалкил или 5-10-членный ароматический или неароматический карбоцикл являются незамещенными или замещенными -C1-С8алкилом или алканолом; и
Z1 и Z2 независимо означают водород или -С1-С8алкил, который является незамещенным или замещен одной или более группами, включающими гидрокси или -NZ3Z4, где Z3 и Z4, независимо означают Н или -C1-С3алкил, который является незамещенным или замещен одной или более группами, включающими гидрокси или -NH2; либо N, Z3 и Z4, взятые вместе, образуют 5-10-членный ароматический или неароматический карбоцикл, в котором 1-4 атома углерода кольца независимо заменены атомом N, О или S, по меньшей мере один из которых является атомом азота; либо N, Z1 и Z2, взятые вместе, образуют 5-10-членный ароматический или неароматический карбоцикл, в котором 1-4 атома углерода кольца независимо заменены атомом N, О или S, по меньшей мере один из которых является атомом азота.
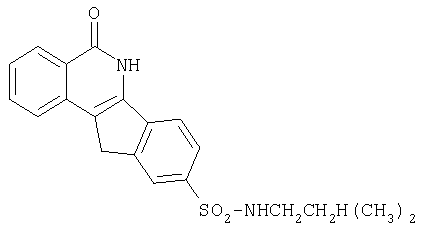
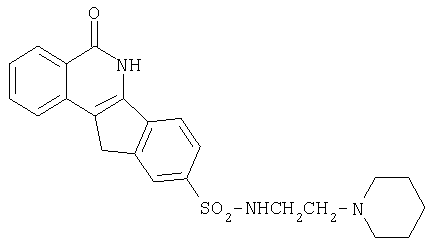

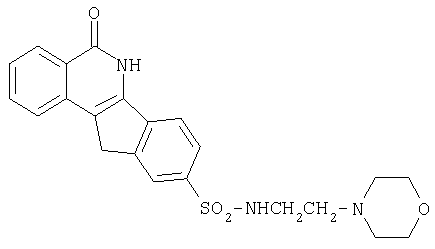
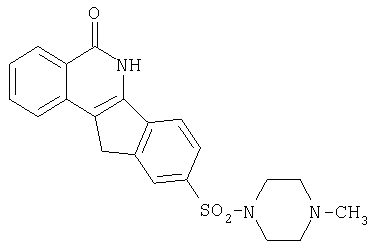
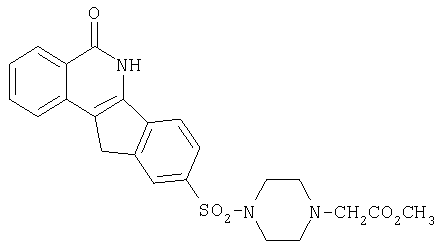
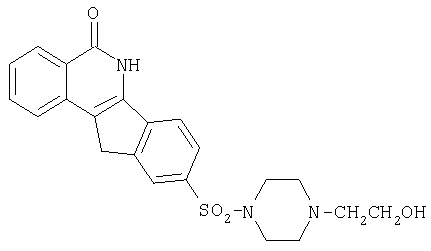
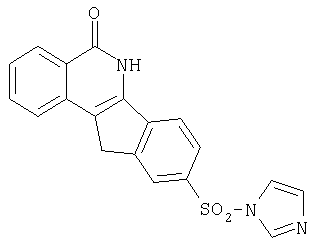
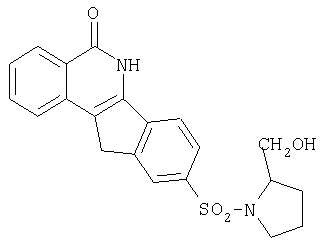
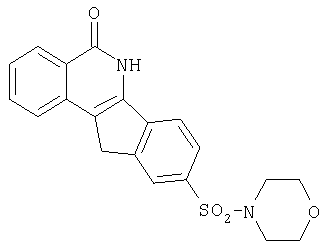
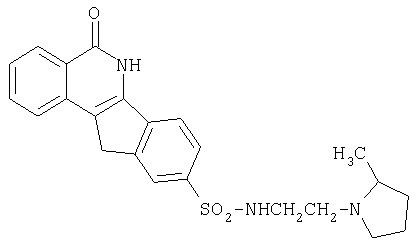
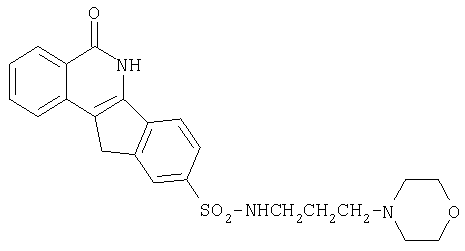
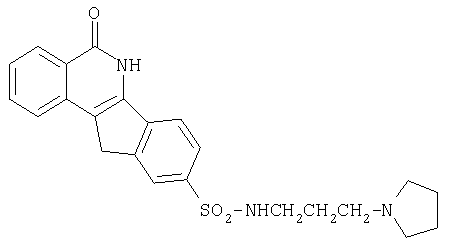
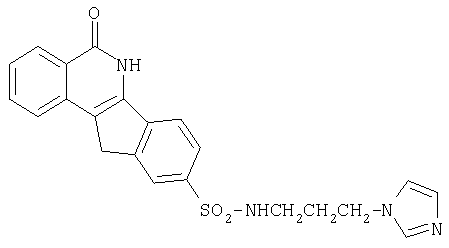
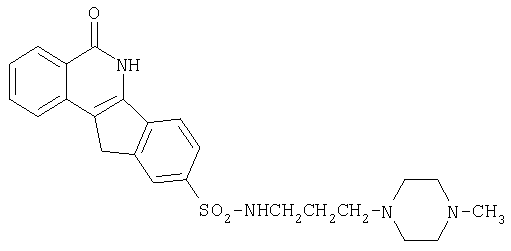
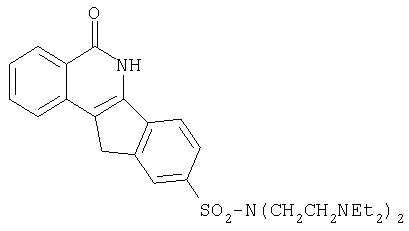
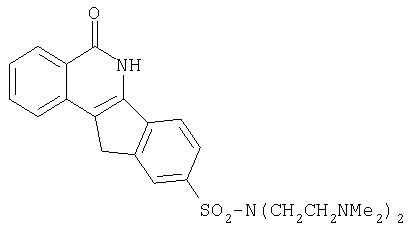
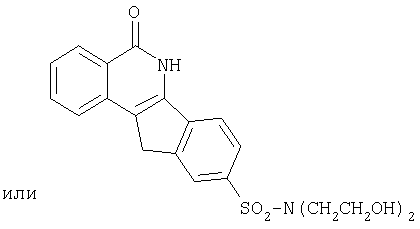
или фармацевтически приемлемые гидрат или соль указанного соединения.
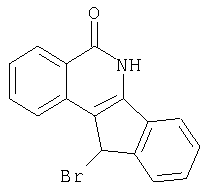
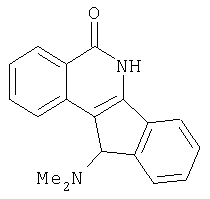
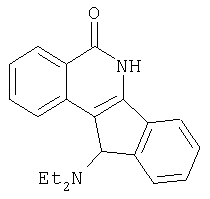
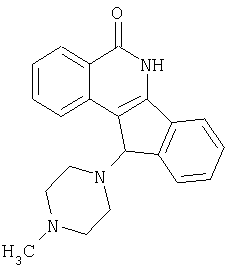
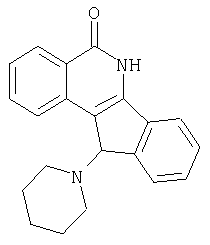
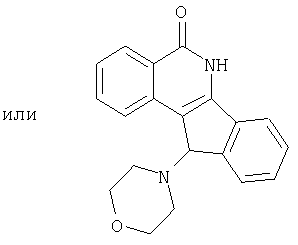
или фармацевтически приемлемые гидрат или соль указанного соединения.
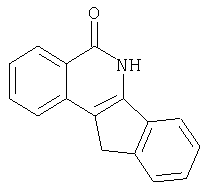
или фармацевтически приемлемого гидрата или соли соединения в количестве, достаточном для лечения воспалительного заболевания, где указанным воспалительным заболеванием является воспалительное заболевание сустава, хроническое воспалительное заболевание десны, воспалительное заболевание кишки, воспалительное заболевание легкого, воспалительное заболевание центральной нервной системы или воспалительное заболевание глаза.

или фармацевтически приемлемого гидрата или соли соединения в количестве, достаточном для лечения или профилактики реперфузионного нарушения, где реперфузионным нарушением является инфаркт миокарда или удар.

или фармацевтически приемлемого гидрата или соли соединения в количестве, достаточном для лечения диабета.

или фармацевтически приемлемого гидрата или соли соединения в количестве, достаточном для лечения нарушения реоксигенации, возникающего при трансплантации органов.
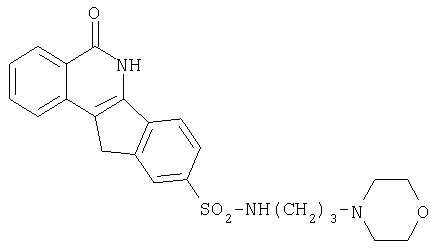
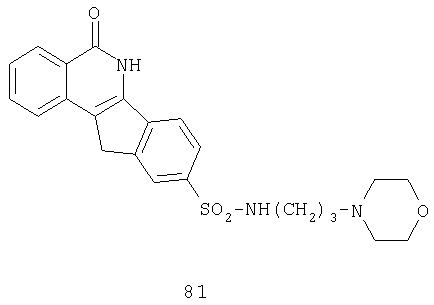
в указанном способе
(i) соединение 13а
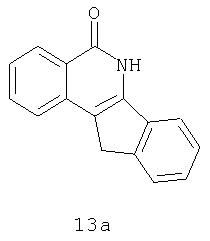
вводят в реакцию с хлорсульфоновой кислотой в условиях, достаточных для получения соединения 7
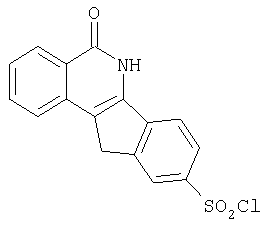
(ii) соединение 7 вводят в реакцию с соединением формулы
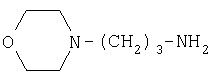
в присутствии триэтиламина или карбоната натрия в условиях, достаточных для получения соединения 81.
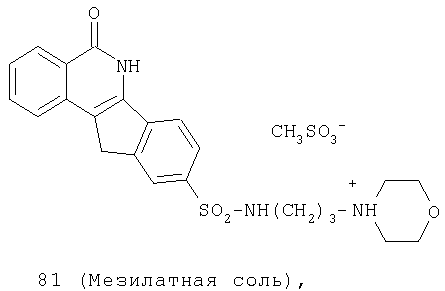
в указанном способе соединение 81
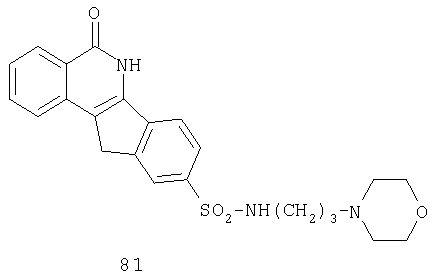
вводят в реакцию с метансульфоновой кислотой в условиях, достаточных для получения мезилатной соли соединения 81.
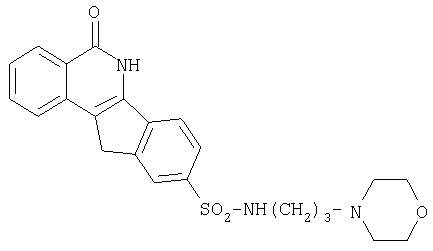
или фармацевтически приемлемые гидрат или соль указанного соединения.
| 6-[X-(2-ГИДРОКСИЭТИЛ)АМИНОАЛКИЛ]-5,11-ДИОКСО-5,6-ДИГИДРО-11H-ИНДЕ- НО/1,2-С/ИЗОХИНОЛИНЫ ИЛИ ИХ СОЛИ С НЕОРГАНИЧЕСКИМИ И ОРГАНИЧЕСКИМИ КИСЛОТАМИ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1992 |
|
RU2120939C1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
Авторы
Даты
2007-06-10—Публикация
2002-08-30—Подача