Изобретение относится к биологии, токсикологической и санитарной химии, а именно к способам определения N-(бензимидазолил-2)-O-метилкарбамата в биологическом материале, и может быть использовано в практике санэпидстанций, химико-токсикологических и ветеринарных лабораторий. Способ относится к числу массовых.
Известен способ определения органических веществ в биологическом материале, заключающийся в измельчении биологического объекта, неоднократном настаивании с этанолом (каждый раз в течение суток), объединении вытяжек, сгущении объединенного извлечения, осаждении в нем белков абсолютным этанолом, фильтровании, упаривании фильтрата до густоты сиропа и разбавлении его водой с последующей экстракцией анализируемых соединений сначала из кислого, а затем из щелочного раствора (Швайкова М.Д. Токсикологическая химия. - М.: Медицина, 1975, - с.119-123).
Способ трудоемок, требует значительных затрат времени на его осуществление, характеризуется низкой степенью извлечения N-(бензимидазолил-2)-O-метилкарбамата.
Известен способ определения производных карбаминовой кислоты (1-нафтил-N-метилкарбамата) в биологических объектах путем измельчения биологической ткани, ее обработки гексаном в присутствии безводного сульфата натрия в течение 2-3 часов, отделения гексанового извлечения, упаривания до сухого остатка, растворения остатка в смеси вода-метанол, взятых в объемном соотношении 3:2, прибавления к водно-метанольному раствору хлорида натрия, экстракции раствора хлороформом, отделения хлороформного экстракта, упаривания до сухого остатка, растворения остатка в гексане с последующим хроматографированием в тонком слое силикагеля на пластинах «Силуфол» с использованием подвижной фазы гексан-ацетон (3:1) и проявлением хроматограмм путем последовательной обработки водно-этанольным раствором гидроксида калия и раствором соли диазония (Лабораторные исследования в ветеринарии. Химико-токсикологические методы. / Под ред. Б.И.Антонова. - М.: Агропромиздат, 1989. - С.160-162).
Способ характеризуется недостаточно высокой степенью извлечения N-(бензимидазолил-2)-O-метилкарбамата, относительно низкими точностью и чувствительностью определения.
Наиболее близким является способ определения N-(бензимидазолил-2)-O-метилкарбамата в биологическом материале, заключающийся в том, что биологическую пробу измельчают, троекратно настаивают с этилацетатом, этилацетатные извлечения объединяют, фильтруют, анализируемое вещество из этилацетата экстрагируют 0,1 н. раствором хлороводородной кислоты, полученный экстракт промывают гексаном, подщелачивают 4 н. раствором гидроксида натрия до рН 10, экстрагируют этилацетатом, экстракт обезвоживают, экстрагент испаряют, сухой остаток растворяют в ацетоне, хроматографируют в тонком слое силикагеля на пластинах «Силуфол» с использованием подвижной фазы этилацетат-хлороформ-уксусная кислота (50:50:10), хроматограммы проявляют в УФ-свете и определяют анализируемое вещество визуально по интенсивности окраски и размеру пятна на хроматограмме (Методы определения микроколичеств пестицидов в продуктах питания, кормах и внешней среде. / Под ред. М.А.Клисенко. - Т.1. - М.: ВО «Колос», 1992. - С.477-480).
Способ характеризуется относительно низкой степенью извлечения анализируемого соединения, недостаточно высокими точностью и чувствительностью.
Задачей настоящего изобретения является повышение степени извлечения, а также точности и чувствительности определения N-(бензимидазолил-2)-O-метилкарбамата.
Поставленная задача достигается с помощью предлагаемого способа, который заключается в том, что биологическую ткань измельчают, трехкратно настаивают с органическим экстрагентом, в качестве которого используется смесь растворителей этилацетат-дихлорэтан-муравьиная кислота, взятых в соотношении 5:5:1 (по объему), каждый раз в течение 15 минут. Полученные извлечения объединяют, объединенное извлечение фильтруют, фильтрат экстрагируют 0,1 н. раствором хлороводородной кислоты, полученный кислотный экстракт промывают гидрофобным органическим растворителем, которым является этилацетат, этилацетатный слой отбрасывают, водный слой подщелачивают 10% раствором гидроксида натрия до рН 8-9, экстрагируют этилацетатом, полученный экстракт отделяют, обезвоживают, экстрагент испаряют, остаток растворяют в органическом растворителе (ледяной уксусной кислоте), хроматографируют в тонком слое силикагеля, обработанного вазелиновым маслом, с использованием подвижной фазы ацетонитрил-вода (6:4), хроматограммы проявляют в УФ-свете, анализируемое вещество элюируют из сорбента смесью растворителей этилацетат-дихлорэтан-муравьиная кислота (5:5:1) и определяют оптическую плотность элюата при длине волны 282 нм.
Способ осуществляется следующим образом: биологическую ткань, содержащую N-(бензимидазолил-2)-O-метилкарбамат, измельчают, трижды настаивают с органическим экстрагентом, в качестве которого используется смесь растворителей этилацетат-дихлорэтан-муравьиная кислота, взятых в соотношении 5:5:1 (по объему), каждый раз в течение 15 минут, полученные извлечения отделяют от твердых частиц биоматериала, объединяют, объединенное извлечение фильтруют, фильтрат экстрагируют 0,1 н. раствором хлороводородной кислоты, полученный кислотный экстракт промывают гидрофобным органическим растворителем, которым является этилацетат, этилацетатный слой отбрасывают, водный слой подщелачивают 10% раствором гидроксида натрия до рН 8-9, экстрагируют этилацетатом, полученный экстракт отделяют, обезвоживают, экстрагент испаряют, остаток растворяют в органическом растворителе (ледяной уксусной кислоте), хроматографируют в тонком слое силикагеля, обработанного вазелиновым маслом, с использованием подвижной фазы ацетонитрил-вода (6:4), хроматограммы проявляют в УФ-свете, анализируемое вещество элюируют из сорбента смесью растворителей этилацетат-дихлорэтан-муравьиная кислота (5:5:1) и определяют оптическую плотность элюата при длине волны 282 нм.
Пример 1
Определение N-(бензимидазолил-2)-O-метилкарбамата в ткани печени
К 10 г мелкоизмельченной ткани печени прибавляют 5 мг N-(бензимидазолил-2)-O-метилкарбамата, тщательно перемешивают биологическую ткань с веществом и оставляют на сутки при температуре 18-20°С. По истечении указанного времени биологический объект, содержащий анализируемое вещество, заливают 20 мл органического экстрагента, в качестве которого используется смесь растворителей этилацетат-дихлорэтан-муравьиная кислота (5:5:1) (по объему) и выдерживают 15 минут при перемешивании. Извлечение отделяют, операцию настаивания повторяют еще дважды в указанных условиях. Отдельные вытяжки объединяют, фильтруют через бумажный фильтр, фильтрат экстрагируют 0,1 н. раствором хлороводородной кислоты дважды порциями по 60 мл каждая. Кислотные экстракты объединяют, экстрагируют 120 мл гидрофобного органического растворителя, которым является этилацетат, этилацетатный слой отбрасывают, водный слой подщелачивают 10% раствором гидроксида натрия до рН 8-9, экстрагируют дважды порциями этилацетата по 150 мл каждая. Этилацетатные извлечения объединяют, пропускают через стеклянный фильтр с 10 г безводного сульфата натрия, фильтр промывают 20 мл этилацетата. Отдельные фильтраты объединяют, растворитель испаряют в токе воздуха при комнатной температуре, остаток растворяют в 6-8 мл оранического растворителя (ледяной уксусной кислоты), количественно переносят раствор в мерную колбу вместимостью 10 мл и доводят объем содержимого в колбе до метки ледяной уксусной кислотой. 0,2 мл полученного раствора наносят на линию старта хроматографической пластины типа «Силуфол» UV-254, предварительно обработанной 10% раствором вазелинового масла в гексане. Хроматографирование осуществляют, используя в качестве подвижной фазы систему растворителей ацетонитрил-вода (6:4) в присутствии вещества-свидетеля. Хроматограмму проявляют в УФ-свете. Анализируемое вещество обнаруживается на хроматограмме в виде темного пятна с Rf=0,54±0,02. Участок пластины с пятном вещества вырезают и элюируют вещество из сорбента 10 мл смеси растворителей этилацетат-дихлорэтан-муравьиная кислота (5:5:1) (по объему). Оптическую плотность полученного элюата измеряют на спектрофотометре СФ-46 при длине волны 282 нм в кюветах с толщиной рабочего слоя 10 мм. Измерения проводят на фоне раствора, полученного в контрольном опыте. Количественное содержание N-(бензимидазолил-2)-O-метилкарбамата определяют, используя уравнение калибровочного графика, и пересчитывают на навеску анализируемого вещества, внесенную в биологический материал.
Построение калибровочного графика
На линию старта хроматографической пластины типа «Силуфол» UV-254, предварительно обработанной 10% раствором вазелинового масла в гексане, наносят 0,05, 0,1, 0,2, 0,4, 1,0, 2,0, 4,5 мл 0,004% раствора N-(бензимидазолил-2)-O-метилкарбамата в органическом растворителе (ледяной уксусной кислоте) и осуществляют хроматографирование, используя подвижную фазу ацетонитрил-вода (6:4). N-(бензимидазолил-2)-O-метилкарбамат обнаруживается на хроматограмме в виде темных пятен с Rf=0,54±0,02. Участки пластины с находящимися на них пятнами вещества вырезают и элюируют каждое пятно 10 мл смеси растворителей этилацетат-дихлорэтан-муравьиная кислота (5:5:1). Элюаты фотометрируют при длине волны 282 нм на спектрофотометре СФ-46 в кювете с толщиной рабочего слоя 10 мм. Раствор сравнения - элюат, полученный при проведении контрольного опыта. По результатам измерений строят график зависимости оптической плотности раствора от концентрации определяемого вещества. Методом наименьших квадратов рассчитывают уравнение калибровочного графика, которое в данном случае имеет вид:
D=0,0756·C+0,0018,
где D - оптическая плотность; С - концентрация определяемого вещества в фотометрируемом растворе, мкг/мл.
Результаты определения N-(бензимидазолил-2)-O-метилкарбамата в ткани печени представлены в таблице 1.
Пример 2
Определение N-(бензимидазолил-2)-O-метилкарбамата в ткани яблок
К 10 г мелкоизмельченной ткани яблок прибавляют 5 мг N-(бензимидазолил-2)-O-метилкарбамата, тщательно перемешивают биологическую ткань с веществом и оставляют на сутки при температуре 18-20°С. По истечении указанного времени биологический объект, содержащий анализируемое вещество, заливают 20 мл органического экстрагента, в качестве которого используется смесь растворителей этилацетат-дихлорэтан-муравьиная кислота (5:5:1) (по объему), и выдерживают 15 минут при перемешивании. Извлечение отделяют, операцию настаивания повторяют еще дважды в указанных условиях. Отдельные вытяжки объединяют, фильтруют через бумажный фильтр, фильтрат экстрагируют 0,1 н. раствором хлороводородной кислоты дважды порциями по 60 мл каждая. Кислотные экстракты объединяют, экстрагируют 120 мл гидрофобного органического растворителя, которым является этилацетат, этилацетатный слой отбрасывают, водный слой подщелачивают 10% раствором гидроксида натрия до рН 8-9, экстрагируют дважды порциями этилацетата по 150 мл каждая. Этилацетатные извлечения объединяют, пропускают через стеклянный фильтр с 10 г безводного сульфата натрия, фильтр промывают 20 мл этилацетата. Отдельные фильтраты объединяют, растворитель испаряют в токе воздуха при комнатной температуре, остаток растворяют в 6-8 мл органического растворителя (ледяной уксусной кислоты), количественно переносят раствор в мерную колбу вместимостью 10 мл и доводят объем содержимого в колбе до метки ледяной уксусной кислотой. 0,2 мл полученного раствора наносят на линию старта хроматографической пластины типа «Силуфол» UV-254, предварительно обработанной 10% раствором вазелинового масла в гексане. Хроматографирование осуществляют, используя в качестве подвижной фазы систему растворителей ацетонитрил-вода (6:4) в присутствии вещества-свидетеля. Хроматограмму проявляют в УФ-свете. Анализируемое вещество обнаруживается на хроматограмме в виде темного пятна с Rf=0,54±0,02. Участок пластины с пятном вещества вырезают и элюируют вещество из сорбента 10 мл смеси растворителей этилацетат-дихлорэтан-муравьиная кислота (5:5:1) (по объему). Оптическую плотность полученного элюата измеряют на спектрофотометре СФ-46 при длине волны 282 нм в кюветах с толщиной рабочего слоя 10 мм. Измерения проводят на фоне раствора, полученного в контрольном опыте. Количественное содержание N-(бензимидазолил-2)-O-метилкарбамата определяют, используя уравнение калибровочного графика, и пересчитывают на навеску анализируемого вещества, внесенную в биологический материал.
Построение калибровочного графика и его уравнение приводятся в примере 1.
Результаты количественного определения N-(бензимидазолил-2)-O-метилкарбамата в ткани яблок представлены в таблице 2.
Предлагаемый способ по сравнению с прототипом в два раза увеличивает степень извлечения N-(бензимидазолил-2)-O-метилкарбамата из биологического материала (с 40,09 до 84,79%), в три раза повышает точность определения (относительная ошибка среднего результата уменьшается с ±10,56 до ±2,98%), характеризуется более высокой чувствительностью (открываемый минимум снижается с 0,03 до 0,015 мг в 100 г биологической ткани).
Сравнительная характеристика предлагаемого и известного способов представлена в таблице 3.
Результаты определения Н-(бензимидазолил-2)-O-метилкарбамата в ткани печени (n=5; Р=0,95)
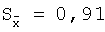


Результаты определения N-(бензимидазолил-2)-O-метилкарбамата в ткани яблок (n=5; Р=0,95)


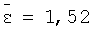
Сравнительная характеристика предлагаемого и известного способов (на примере исследования ткани печени)
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения N-(бензимидазолил-2)-О-метилкарбамата в биологическом материале | 2018 |
|
RU2692127C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ O-(2,3-ДИГИДРО-2,2-ДИМЕТИЛ-7-БЕНЗОФУРАНИЛ)-N-МЕТИЛКАРБАМАТА В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2004 |
|
RU2269780C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ОКСИБЕНЗОЛА И ЕГО МОНОМЕТИЛЬНЫХ ПРОИЗВОДНЫХ В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2004 |
|
RU2269137C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ТЕТРАМЕТИЛТИУРАМДИСУЛЬФИДА В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2009 |
|
RU2415425C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ 2,6-БИС-[БИС-(БЕТА-ОКСИЭТИЛ)-АМИНО]-4,8-ДИ-N-ПИПЕРИДИНО-ПИРИМИДО(5,4-D)ПИРИМИДИНА В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2006 |
|
RU2322674C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГЕТЕРОЦИКЛИЧЕСКИХ НИТРОСОЕДИНЕНИЙ В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 1996 |
|
RU2100808C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГИДРОКСИБЕНЗОЛА И ЕГО МОНОМЕТИЛЬНЫХ ЗАМЕЩЕННЫХ В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2014 |
|
RU2550953C1 |
| Способ определения 2,6-бис-[бис-(бета-оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина в биологическом материале | 2016 |
|
RU2617176C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СЛОЖНОГО НИТРОФЕНОЛЬНОГО ПРЕПАРАТА "НИТРАФЕН" В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 1999 |
|
RU2153169C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ О-(2,3-ДИГИДРО-2,2-ДИМЕТИЛ-7-БЕНЗОФУРАНИЛ)-N-МЕТИЛКАРБАМАТА В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2014 |
|
RU2548742C1 |
Изобретение относится к биологии, токсикологической и ветеринарной химии, а именно к способам определения N-(бензимидазолил-2)-O-метилкарбамата в биологическом материале, и может быть использовано в практике санэпидстанций, химико-токсикологических и ветеринарных лабораторий. Биологическую ткань измельчают, троекратно настаивают с органическим экстрагентом, в качестве которого используется смесь растворителей этилацетат-дихлорэтан-муравьиная кислота, взятых в соотношении 5:5:1 (по объему), каждый раз в течение 15 минут, полученные извлечения отделяют от твердых частиц биоматериала, объединяют, объединенное извлечение фильтруют, фильтрат экстрагируют 0,1 н. раствором хлороводородной кислоты, полученный кислотный экстракт промывают гидрофобным органическим растворителем, которым является этилацетат, этилацетатный слой отбрасывают, водный слой подщелачивают 10% раствором гидроксида натрия до рН 8-9, экстрагируют этилацетатом, полученный экстракт отделяют, обезвоживают, экстрагент испаряют, остаток растворяют в органическом растворителе (ледяной уксусной кислоте), хроматографируют в тонком слое силикагеля, обработанного вазелиновым маслом, с использованием подвижной фазы ацетонитрил-вода (6:4), хроматограммы проявляют в УФ-свете, анализируемое вещество элюируют из сорбента смесью растворителей этилацетат-дихлорэтан-муравьиная кислота (5:5:1) и определяют оптическую плотность элюата при длине волны 282 нм. Достигается увеличение степени извлечения, точности и чувствительности определения. 3 табл.
Способ определения N-(бензимидазолил-2)-O-метилкарбамата в биологическом материале, заключающийся в том, что анализируемую пробу измельчают, троекратно настаивают с органическим экстрагентом, полученные органические извлечения объединяют, объединенное извлечение фильтруют, анализируемое вещество экстрагируют из фильтрата 0,1 н. раствором хлороводородной кислоты, полученный кислотный экстракт промывают гидрофобным органическим растворителем и подщелачивают раствором гидроксида натрия, анализируемое вещество экстрагируют этилацетатом, полученный экстракт отделяют и обезвоживают, экстрагент испаряют, сухой остаток растворяют в органическом растворителе, хроматографируют в тонком слое сорбента - силикагеля с использованием подвижной фазы, хроматограмму проявляют в УФ-свете с последующим определением анализируемого вещества, отличающийся тем, что анализируемую пробу настаивают с использованием в качестве органического экстрагента смеси растворителей этилацетат-дихлорэтан-муравьиная кислота, взятых в соотношении 5:5:1 по объему, в качестве гидрофобного органического растворителя при промывке кислотного экстракта используют этилацетат, промытый кислотный экстракт подщелачивают до рН 8-9, сухой остаток растворяют с использованием в качестве органического растворителя ледяной уксусной кислоты, при хроматографировании в качестве сорбента используют силикагель, обработанный вазелиновым маслом, а в качестве подвижной фазы используют систему растворителей ацетонитрил-вода в соотношении 6:4 по объему, после проявления хроматограммы в УФ-свете анализируемое вещество элюируют из сорбента смесью растворителей этилацетат-дихлорэтан-муравьиная кислота, взятых в соотношении 5:5:1 по объему, а определение анализируемого вещества осуществляют измерением оптической плотности элюата при длине волны 282 нм с использованием калибровочного графика.
| КЛИСЕНКО М.А | |||
| Методы определения микроколичеств пестицидов в продуктах питания, кормах и внешней среде | |||
| - M.: ВО "Колос", 1992, т.1, с.477-480 | |||
| Способ раздельного определения диалкилдитиокарбаматов щелочных металлов и диалкилдитиокарбаминовых кислот в их смеси | 1984 |
|
SU1182391A1 |
| ПОЛЮДЕК-ФАБИНИ Р., БЕЙРИХ Т | |||
| Органический анализ | |||
| - Л.: Химия, 1981, с.217-220, 564 | |||
| ГУБЕН-ВЕЙЛЬ | |||
| Методы органической химии, т.2 | |||
| Методы анализа | |||
| - M.: Химия, 1967, с.559. | |||
Авторы
Даты
2007-06-10—Публикация
2005-10-25—Подача