Изобретение относится к биологии и токсикологической химии, а именно к способам определения 2,6-бис-[бис-(бета-оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина в биологическом материале, и может быть использовано в практике санэпидстанций, химико-токсикологических, экспертно-криминалистических и ветеринарных лабораторий. Способ относится к числу массовых.
Известен способ определения 2,6-бис-[бис-(β-оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-е)пиримидина в биологических объектах путем измельчения биологической ткани, двукратного настаивания с водой, подкисленной щавелевой кислотой, отделения извлечений, их объединения, фильтрования объединенного извлечения, экстракции анализируемого соединения хлороформом после подщелачивания раствора, отделения хлороформного экстракта, испарения хлороформа до сухого остатка, растворения остатка в разбавленном растворе хлороводородной кислоты и измерения оптической плотности полученного раствора (Муравьева Г.М., Дмитриченко М.И. Судебно-химическое определение курантила и верапамила // Судебно-медицинская экспертиза. - 1995. - Т. 38, N 1. - С. 21-23).
Способ характеризуется недостаточно высокой степенью извлечения 2,6-бис-[бис-(β-оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина, относительно низкими точностью и чувствительностью определения.
Известен способ определения 2,6-бис-[бис-(β-оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина в биологическом материале, заключающийся в том, что биологическую пробу измельчают, трижды настаивают с этанолом (первый раз в течение 24 часов, второй и третий - в течение 1 часа), извлечения отделяют центрифугированием, отдельные центрифугаты объединяют, смешивают с разбавленным раствором хлороводородной кислоты, доводят pH среды полученной водно-этанольной смеси до 2,0, промывают эфиром, доводят pH среды до 9,0, экстрагируют хлороформом, хлороформное извлечение подкисляют раствором хлороводородной кислоты до pH 4,0-5,0, растворитель испаряют и определяют анализируемое вещество в остатке экстракционно-фотометрическим методом на основе реакции с метиловым оранжевым в сочетании с электрофорезом на бумаге с использованием в качестве электролита буферной смеси Бриттона-Робинсона с pH 2,0 (Зимнухов В.В., Бахарева Н.А., Травенко Е.Н., Удалов А.В.. Смертельные отравления дипиридамолом // Судебно-медицинская экспертиза. - 1999. - Т. 42, N 3. - С. 34).
Способ характеризуется значительными затратами времени на осуществление анализа, относительно низкой степенью извлечения анализируемого соединения, недостаточно высокой точностью и чувствительностью определения.
Наиболее близким является способ определения 2,6-бис-[бис-(β-оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина в биологическом материале, заключающийся в том, что биологический объект двукратно настаивают с ацетоном, каждый раз в течение 30 минут, полученные извлечения объединяют, объединенное извлечение фильтруют, фильтрат испаряют до получения сухого остатка, остаток растворяют в хлороформе, экстрагируют 0,1 н. раствором хлороводородной кислоты, хлороформный слой отбрасывают, полученный кислотный экстракт промывают органическим растворителем, которым является эфир, слой органического растворителя отбрасывают, водный слой подщелачивают 10% раствором гидроксида натрия до pH 8-10, насыщают хлоридом натрия, экстрагируют этилацетатом, полученный экстракт отделяют, обезвоживают, экстрагент испаряют, остаток растворяют в смеси ацетонитрила и 1 н. раствора серной кислоты, взятых в соотношении 8:2 по объему, хроматографируют в макроколонке с сорбентом «Силасорб С-18» с размером частиц 30 мкм, используя подвижную фазу, включающую ацетонитрил и 1 н. раствор серной кислоты в соотношении 8:2 по объему, фракции элюата, содержащие анализируемое вещество, объединяют и определяют анализируемое вещество физико-химическим методом, которым является спектрофотометрия, измеряя оптическую плотность элюата при длине волны 286 нм (Патент 2322674 Российская Федерация, МПК G01N 33/15; G01N 33/49; G01N 33/48 / Способ определения 2,6-бис-[бис(-бета-оксэтил)-амино]-4,8-ди-N-пипиридинопиримидо(5,3-d)пиримидина в биологическом материале / Шорманов В.К., Квачахия Л.Л., Сипливая Л.Е.; заявители и патентообладатели: Шорманов В.К., Квачахия Л.Л., Сипливая Л.Е. (RU). - №2006135873/15; Заяв. 10.10.2006; Опуб. 20.04.2008 // Изобретения (Заявки и патенты). - 2008. - №11. -6 с).
Способ характеризуется недостаточно высокой чувствительностью определения.
Техническим результатом настоящего изобретения является повышение чувствительности определения.
Технический результат достигается тем, что биологический объект двукратно настаивают с ацетоном, каждый раз в течение 30 минут, полученные извлечения объединяют, объединенное извлечение фильтруют, фильтрат испаряют до получения сухого остатка, остаток неоднократно обрабатывают ацетоном, ацетоновые извлечения отделяют, объединяют, растворитель из объединенного извлечения испаряют, остаток растворяют в хлороформе, экстрагируют 0,1 н. раствором хлороводородной кислоты, хлороформный слой отбрасывают, полученный кислотный экстракт промывают органическим растворителем, которым является смесь эфира и гексана в соотношении 1:1 по объему, слой органического растворителя отбрасывают, водный слой подщелачивают 10% раствором гидроксида натрия до pH 8-10, насыщают хлоридом натрия, экстрагируют этилацетатом, полученный экстракт отделяют, обезвоживают, экстрагент испаряют, остаток растворяют в смеси ацетонитрила и 1 н. раствора серной кислоты, взятых в соотношении 9:1 по объему, хроматографируют в макроколонке с сорбентом «Силасорб С-18» с размером частиц 15 мкм, используя подвижную фазу, включающую ацетонитрил и 1 н. раствор серной кислоты в соотношении 9:1 по объему, фракции элюата, содержащие анализируемое вещество, объединяют и определяют анализируемое вещество физико-химическим методом, которым является ВЭЖХ, хроматографируя элюат в колонке сорбента Zorbax SB С8, термостатируемой при 40°C, с использованием подвижной фазы ацетонитрил - 0,025 М раствор дигидрофосфата калия в соотношении 3:2 по объему и детектора на основе фотодиодной матрицы.
Способ осуществляется следующим образом: биологический материал, содержащий 2,6-бис-[бис-(β-оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидин, двукратно настаивают с ацетоном, каждый раз в течение 30 минут, полученные извлечения объединяют, объединенное извлечение фильтруют, фильтрат испаряют до получения сухого остатка, остаток неоднократно обрабатывают ацетоном, ацетоновые извлечения отделяют, объединяют, растворитель из объединенного извлечения испаряют, остаток растворяют в хлороформе, экстрагируют 0,1 н. раствором хлороводородной кислоты, хлороформный слой отбрасывают, полученный кислотный экстракт промывают органическим растворителем, которым является смесь эфира и гексана в соотношении 1:1 по объему, слой органического растворителя отбрасывают, водный слой подщелачивают 10% раствором гидроксида натрия до pH 8-10, насыщают хлоридом натрия, экстрагируют этилацетатом, полученный экстракт отделяют, обезвоживают, экстрагент испаряют, остаток растворяют в смеси ацетонитрила и 1 н. раствора серной кислоты, взятых в соотношении 9:1 по объему, хроматографируют в макроколонке с сорбентом «Силасорб С-18» с размером частиц 15 мкм, используя подвижную фазу, включающую ацетонитрил и 1 н. раствор серной кислоты в соотношении 9:1 по объему, фракции элюата, содержащие анализируемое вещество, объединяют и определяют анализируемое вещество физико-химическим методом, которым является ВЭЖХ, хроматографируя элюат в колонке сорбента Zorbax SB С8, термостатируемой при 40°C, с использованием подвижной фазы ацетонитрил - 0,025 М раствор дигидрофосфата калия в соотношении 3:2 по объему и детектора на основе фотодиодной матрицы.
Способ иллюстрируется следующими примерами.
Пример 1
Определение 2,6-бис-[бис-(β-оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина в ткани печени
К 25 г мелкоизмельченной (до размеров частиц 0,2-0,5 см) ткани печени прибавляют 10 мг 2,6-бис-[бис-(β-оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина, тщательно перемешивают биологическую ткань с веществом и оставляют на сутки при температуре 18-20°C.
По истечении указанного времени биологический объект, содержащий анализируемое вещество, заливают 50 мл ацетона и настаивают 30 минут при перемешивании. Извлечение отделяют, операцию настаивания повторяют еще раз в указанных условиях. Отдельные извлечения объединяют, фильтруют через стеклянный фильтр диаметром 3 см с 10 г безводного сульфата натрия. Через слой сульфата натрия дополнительно пропускают 25 мл ацетона. Отдельные фильтраты объединяют в фарфоровой чашке, растворитель испаряют в токе воздуха при комнатной температуре до получения сухого остатка.
Остаток неоднократно (трижды по 3 минуты) обрабатывают при энергичном перемешивании порциями (по 25 г каждая) ацетона, ацетоновые извлечения отделяют, объединяют, растворитель из объединенного извлечения испаряют в токе воздуха при температуре 18-20°C.
Остаток растворяют в 10 мл хлороформа, экстрагируют дважды порциями 0,1 н. раствора хлороводородной кислоты по 20 мл каждая, отдельные извлечения отделяют, объединяют, хлороформный слой отбрасывают, полученный объединенный кислотный экстракт промывают органическим растворителем, которым является смесь эфира и гексана в соотношении 1:1 по объему, встряхивая в делительной воронке в течение 3 минут, слой органического растворителя отбрасывают, водный слой подщелачивают 10%-ным раствором гидроксида натрия до pH 8-10, насыщают хлоридом натрия, вводя его в количестве 3,6 г, и экстрагируют дважды этилацетатом, порциями по 40 мл каждая. Отдельные экстракты отделяют, объединяют, полученный объединенный экстракт обезвоживают путем фильтрования через двухслойный бумажный фильтр, фильтр промывают 10 мл этилацетата. Фильтрат и промывную жидкость объединяют в фарфоровой чашке, экстрагент испаряют в токе воздуха при температуре 18-20°C до получения сухого остатка.
Остаток растворяют в 2-3 мл смеси ацетонитрила и 1 н. раствора серной кислоты, взятых в соотношении 9:1 по объему, и вводят полученный раствор в макроколонку размерами 490×11 мм, заполненную 7,5 г сорбента «Силасорб С-18» с размером частиц 15 мкм. После полного вхождения раствора в сорбент хроматографируют в макроколонке с сорбентом «Силасорб С-18» с размером частиц 15 мкм, используя подвижную фазу, включающую ацетонитрил и 1 н. раствор серной кислоты в соотношении 9:1 по объему.
Элюат собирают фракциями по 1 мл каждая. Фракции элюата №6-7, содержащие анализируемое вещество, которым является 2,6-бис-[бис-(β-оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидин, объединяют в мерной колбе вместимостью 10 мл и доводят содержимое колбы до метки смесью ацетонитрила и 1 н. раствора серной кислоты в соотношении 9:1 по объему.
10 мкл полученного раствора вводят в хроматограф «Waters Alliance 2695» с диодно-матричным детектором модели 2996 и определяют анализируемое вещество физико-химическим методом, которым является ВЭЖХ.
Хроматографирование осуществляют в колонке размером 150×4,6 мм с предколонкой размером 12,5×4,6 мм, заполненных обращеннофазовым сорбентом Zorbax SB С8 с размером частиц 3,5 мкм, используя подвижную фазу ацетонитрил-0,025 М раствор дигидрофосфата калия в соотношении 3:2 по объему и детектор на основе фотодиодной матрицы. Скорость подачи элюента составляет 1 мл/мин при температуре термостатирования колонки 40°C. Оптическую плотность регистрируют при длине волны 285 нм. Пик на хроматограмме с временем удерживания 1,775 мин (объемом удерживания 1775 мкл) соответствует 2,6-бис-[бис-(β-оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидину.
Количественное содержание 2,6-бис-[бис-(β-оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина определяют, исходя из площади хроматографического пика, по уравнению градуировочного графика и пересчитывают на навеску вещества, внесенную в биологический материал.
Построение градуировочного графика
В ряд мерных колб вместимостью 25 мл вносят 0,25, 0,5, 1,0, 1,5, 3,0, 5,0, 7,5 и 12,5 мл 0,08% раствора 2,6-бис-[бис-(β-оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина в смеси ацетонитрила и 1 н. раствора серной кислоты в соотношении 9:1 по объему и доводят содержимое каждой колбы данной смесью растворителей до метки. 10 мкл каждого из полученных растворов вводят в хроматограф.
Хроматографирование осуществляют в колонке размером 150×4,6 мм с предколонкой размером 12,5×4,6 мм, заполненных обращеннофазовым сорбентом Zorbax SB С8 с размером частиц 3,5 мкм, используя подвижную фазу ацетонитрил-0,025 М раствор дигидрофосфата калия в соотношении 3:2 по объему и детектор на основе фотодиодной матрицы. Скорость подачи элюента составляет 1 мл/мин при температуре термостатирования колонки 40°C. Оптическую плотность регистрируют при длине волны 285 нм.
По результатам измерений на хроматографе строят график зависимости площади хроматографического пика от концентрации определяемого вещества в хроматографируемой пробе. График линеен в интервале концентраций 0,08-4,0 мкг.
Методом наименьших квадратов рассчитывают уравнение градуировочного графика, которое в данном случае имеет вид:
S=759560⋅C+13504,
где S - площадь хроматографического пика, С - концентрация определяемого вещества в хроматографируемой пробе, мкг.
Результаты определения 2,6-бис-[бис-(β-оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина в ткани печени представлены в таблице 1.
Пример 2
Определение 2,6-бис-[бис-(β-оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина в крови
К 25 мл крови прибавляют 10 мг 2,6-бис-[бис-(β-оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина, тщательно перемешивают биологическую жидкость с веществом и оставляют на сутки при температуре 18-20°C.
По истечении указанного времени биологический объект, содержащий анализируемое вещество, заливают 50 мл ацетона и настаивают 30 минут при перемешивании. Извлечение отделяют, операцию настаивания повторяют еще раз в указанных условиях. Отдельные извлечения объединяют, фильтруют через стеклянный фильтр диаметром 3 см с 10 г безводного сульфата натрия. Через слой сульфата натрия дополнительно пропускают 25 мл ацетона. Отдельные фильтраты объединяют в фарфоровой чашке, растворитель испаряют в токе воздуха при комнатной температуре до получения сухого остатка.
Остаток неоднократно (трижды по 3 минуты) обрабатывают при энергичном перемешивании порциями (по 25 г каждая) ацетона, ацетоновые извлечения отделяют, объединяют, растворитель из объединенного извлечения испаряют в токе воздуха при температуре 18-20°C.
Остаток растворяют в 10 мл хлороформа, экстрагируют дважды порциями 0,1 н. раствора хлороводородной кислоты по 20 мл каждая, отдельные извлечения отделяют, объединяют, хлороформный слой отбрасывают, полученный объединенный кислотный экстракт промывают органическим растворителем, которым является смесь эфира и гексана в соотношении 1:1 по объему, встряхивая в делительной воронке в течение 3 минут, слой органического растворителя отбрасывают, водный слой подщелачивают 10%-ным раствором гидроксида натрия до pH 8-10, насыщают хлоридом натрия, вводя его в количестве 3,6 г, и экстрагируют дважды этилацетатом, порциями по 40 мл каждая. Отдельные экстракты отделяют, объединяют, полученный объединенный экстракт обезвоживают путем фильтрования через двухслойный бумажный фильтр, фильтр промывают 10 мл этилацетата. Фильтрат и промывную жидкость объединяют в фарфоровой чашке, экстрагент испаряют в токе воздуха при температуре 18-20°C до получения сухого остатка.
Остаток растворяют в 2-3 мл смеси ацетонитрила и 1 н. раствора серной кислоты, взятых в соотношении 9:1 по объему, и вводят полученный раствор в макроколонку размерами 490×11 мм, заполненную 7,5 г сорбента «Силасорб С-18» с размером частиц 15 мкм. После полного вхождения раствора в сорбент хроматографируют в макроколонке с сорбентом «Силасорб С-18» с размером частиц 15 мкм, используя подвижную фазу, включающую ацетонитрил и н. раствор серной кислоты в соотношении 9:1 по объему.
Элюат собирают фракциями по 1 мл каждая. Фракции элюата №6-7, содержащие анализируемое вещество, которым является 2,6-бис-[бис-(β-оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидин, объединяют в мерной колбе вместимостью 10 мл и доводят содержимое колбы до метки смесью ацетонитрила и 1 н. раствора серной кислоты в соотношении 9:1 по объему.
10 мкл полученного раствора вводят в хроматограф «Waters Alliance 2695» с диодно-матричным детектором модели 2996 и определяют анализируемое вещество физико-химическим методом, которым является ВЭЖХ.
Хроматографирование осуществляют в колонке размером 150×4,6 мм с предколонкой размером 12,5×4,6 мм, заполненных обращеннофазовым сорбентом Zorbax SB С8 с размером частиц 3,5 мкм, используя подвижную фазу ацетонитрил-0,025 М раствор дигидрофосфата калия в соотношении 3:2 по объему и детектор на основе фотодиодной матрицы. Скорость подачи элюента составляет 1 мл/мин при температуре термостатирования колонки 40°C. Оптическую плотность регистрируют при длине волны 285 нм. Пик на хроматограмме с временем удерживания 1,775 мин (объемом удерживания 1775 мкл) соответствует 2,6-бис-[бис-(β-оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидину.
Количественное содержание 2,6-бис-[бис-β-оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина определяют, исходя из площади хроматографического пика, по уравнению градуировочного графика и пересчитывают на навеску вещества, внесенную в биологический материал.
Построение градуировочного графика
Построение градуировочного графика и его уравнение приводятся в примере 1.
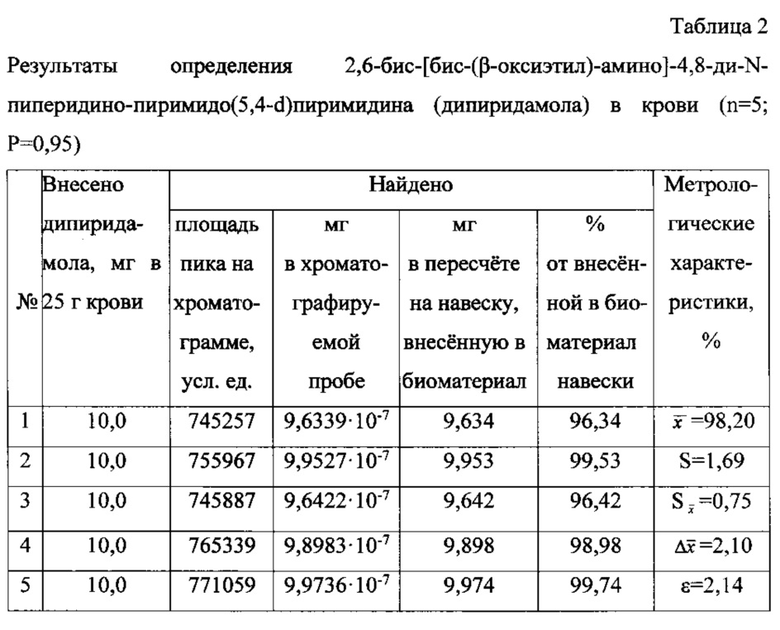
Результаты определения 2,6-бис-[бис-(β-оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина в крови представлены в таблице 2.
Предлагаемый способ по сравнению с прототипом в 40 раз повышает чувствительность определения в анализируемой пробе и в 5 раз - в биологическом материале.
Сравнительные характеристики предлагаемого и известного способов представлены в таблице 3.


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ 2,6-БИС-[БИС-(БЕТА-ОКСИЭТИЛ)-АМИНО]-4,8-ДИ-N-ПИПЕРИДИНО-ПИРИМИДО(5,4-D)ПИРИМИДИНА В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2006 |
|
RU2322674C1 |
| Способ определения N-(бензимидазолил-2)-О-метилкарбамата в биологическом материале | 2018 |
|
RU2692127C1 |
| Способ определения нифедипина в биологическом материале | 2018 |
|
RU2686741C1 |
| Способ получения производныхпиримидо (5,4- )пиримидина | 1973 |
|
SU509227A3 |
| Способ определения нифедипина в биологическом материале | 2023 |
|
RU2812598C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ 1,1'-ЭТИЛЕН-2,2'-ДИПИРИДИЛИЙДИБРОМИДА В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2010 |
|
RU2425368C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ОКСИБЕНЗОЛА И ЕГО МОНОМЕТИЛЬНЫХ ПРОИЗВОДНЫХ В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2004 |
|
RU2269137C1 |
| Способ определения 2-диметиламино-1,3-бис-(фенил-сульфонилтио)пропана в биологическом материале | 2017 |
|
RU2647477C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ Н-БУТИЛОВОГО ЭФИРА 2-[4-(5-ТРИФТОРМЕТИЛПИРИДИЛ-2-ОКСИ)ФЕНОКСИ]ПРОПИОНОВОЙ КИСЛОТЫ В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2011 |
|
RU2477479C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ 2-МЕТОКСИ-4-АЛЛИЛГИДРОКСИБЕНЗОЛА В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2011 |
|
RU2456597C1 |
Изобретение относится к биологии и токсикологической химии, а именно к способам определения 2,6-бис-[бис-(бета-оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина в биологическом материале, и может быть использовано в практике санэпидстанций, химико-токсикологических, экспертно-криминалистических и ветеринарных лабораторий. Способ осуществляется следующим образом: биологический материал, содержащий 2,6-бис-[бис-(β-оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидин, двукратно настаивают с ацетоном, каждый раз в течение 30 минут, полученные извлечения объединяют, объединенное извлечение фильтруют. Затем фильтрат испаряют до получения сухого остатка, остаток неоднократно обрабатывают ацетоном, ацетоновые извлечения отделяют и объединяют. Далее растворитель из объединенного извлечения испаряют, остаток растворяют в хлороформе, экстрагируют 0,1 н. раствором хлороводородной кислоты, хлороформный слой отбрасывают, полученный кислотный экстракт промывают органическим растворителем, которым является смесь эфира и гексана в соотношении 1:1 по объему, слой органического растворителя отбрасывают и водный слой подщелачивают 10% раствором гидроксида натрия до рН 8-10, насыщают хлоридом натрия. Затем экстрагируют этилацетатом, полученный экстракт отделяют, обезвоживают, экстрагент испаряют, остаток растворяют в смеси ацетонитрила и 1 н. раствора серной кислоты, взятых в соотношении 9:1 по объему, хроматографируют в макроколонке с сорбентом «Силасорб С-18» с размером частиц 15 мкм, используя подвижную фазу, включающую ацетонитрил и 1 н. раствор серной кислоты в соотношении 9:1 по объему, фракции элюата, содержащие анализируемое вещество, объединяют и определяют анализируемое вещество физико-химическим методом, которым является ВЭЖХ. Далее хроматографируют элюат в колонке сорбента Zorbax SB С8, термостатируемой при 40°C, с использованием подвижной фазы ацетонитрил - 0,025 М раствор дигидрофосфата калия в соотношении 3:2 по объему и детектора на основе фотодиодной матрицы. Техническим результатом является повышение чувствительности. 3 табл., 2 пр.
Способ определения 2,6-бис-[бис-(β-оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина в биологическом материале, заключающийся в том, что биологический объект двукратно настаивают с ацетоном, каждый раз в течение 30 минут, полученные извлечения объединяют, объединенное извлечение фильтруют, фильтрат испаряют до получения сухого остатка, остаток растворяют в хлороформе, экстрагируют 0,1 н. раствором хлороводородной кислоты, хлороформный слой отбрасывают, полученный кислотный экстракт промывают органическим растворителем, слой органического растворителя отбрасывают, водный слой подщелачивают 10% раствором гидроксида натрия до рН 8-10, насыщают хлоридом натрия, экстрагируют этилацетатом, полученный экстракт отделяют, обезвоживают, экстрагент испаряют, остаток растворяют в смеси ацетонитрила и 1 н. раствора серной кислоты, хроматографируют в макроколонке с сорбентом «Силасорб С-18», используя подвижную фазу, включающую ацетонитрил и 1 н. раствор серной кислоты, фракции элюата, содержащие анализируемое вещество, объединяют и определяют анализируемое вещество физико-химическим методом, отличающийся тем, что перед растворением остатка в хлороформе его неоднократно обрабатывают ацетоном, ацетоновые извлечения отделяют, объединяют, растворитель из объединенного извлечения испаряют, органическим растворителем для промывания кислотного экстракта является смесь эфира и гексана в соотношении 1:1 по объему, соотношение ацетонитрила и 1 н. раствора серной кислоты в смеси для растворения остатка перед хроматографированием в макроколонке составляет 9:1 по объему, при хроматографировании в макроколонке применяют сорбент «Силасорб С-18» с размером частиц 15 мкм, соотношение ацетонитрила и 1 н. раствора серной кислоты в подвижной фазе составляет 9:1 по объему, физико-химическим методом для определения анализируемого вещества является ВЭЖХ, хроматографируют в колонке сорбента Zorbax SB С8, термостатируемой при 40°C, с использованием подвижной фазы ацетонитрил - 0,025 М раствор дигидрофосфата калия в соотношении 3:2 по объему и детектора на основе фотодиодной матрицы.
| СПОСОБ ОПРЕДЕЛЕНИЯ 2,6-БИС-[БИС-(БЕТА-ОКСИЭТИЛ)-АМИНО]-4,8-ДИ-N-ПИПЕРИДИНО-ПИРИМИДО(5,4-D)ПИРИМИДИНА В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2006 |
|
RU2322674C1 |
| ЗИМНУХОВ В.В | |||
| и др, Смертельные отравления дипиридамолом, Судебно-медицинская экспертиза, т.42, N3, стр | |||
| Нивелир для отсчетов без перемещения наблюдателя при нивелировании из средины | 1921 |
|
SU34A1 |
| WO 2006090428 A 31.08.2006 | |||
| ШВАЙКОВА М.Д | |||
| Токсикологическая химия | |||
| - М.: Медицина, стр | |||
| Способ получения камфоры | 1921 |
|
SU119A1 |
| Сплав для отливки колец для сальниковых набивок | 1922 |
|
SU1975A1 |
Авторы
Даты
2017-04-21—Публикация
2016-03-10—Подача