Изобретение относится к области цветной металлургии, в частности к получению катодного никеля из сульфидного медно-никелевого сырья.
Известен способ получения электролитного никеля [Ю.В.Баймаков А.И.Журин. Электролиз в гидрометаллургии. - М.: Металлургия, 1977, с.201], состоящий из флотационного разделения файнштейна на никелевый и медный концентраты, окислительного обжига никелевого концентрата, восстановлении закиси никеля, электроплавки восстановленной закиси никеля на анодный металл, электролитического получения катодного никеля с растворимыми анодами и очисткой сульфат-хлоридного электролита содержащего 30-42 г/л хлоридов и 110-130 г/л сульфатов от примесей.
В данном способе получение электролита происходит в процессе электрохимического растворения анодного металла. Электролит последовательно очищают от железа с нейтрализацией раствора карбонатом никеля до рН 3.8-4.1, очистка от меди никелевым порошком с предварительным подкислением электролита серной кислотой до рН 2.8-3,3, очистка от кобальта проводится с нейтрализацией электролита до рН 3,9-4,1.
Перед подачей очищенного электролита в катодную ячейку его подкисляют серной кислотой до значений рН 2.1-2.7. В процессах очистки электролита и подготовке его к электролизу применяют серную кислоту, производимую из технологических газов процесса обжига никелевого концентрата.
Однако известный способ имеет следующие недостатки: высокие эксплуатационные затраты на плавку восстановленной закиси никеля; высокие потери металлов при данном процессе; высокие эксплуатационные затраты при электролизе с растворимыми анодами; большой объем оборотных продуктов. Кроме того, процесс характеризуется большими затратами реагентов на очистку электролита и его подготовку к электролизу.
Известен способ получения катодного никеля [Патент РФ №2141010, С25С 1/08, С22В 23/00, опубл. 10.11.99, бюл. №31], включающий флотационное разделение файнштейна на медный и никелевый концентраты, окислительный обжиг никелевого концентрата, восстановление закиси никеля, электроэкстракцию никеля из сульфатного никелевого электролита, полученного путем растворения в отработанном электролите восстановленной закиси никеля с активностью не менее 60%. Данный способ характеризуется медленной кинетикой растворения восстановленной закиси никеля в отработанном электролите, а низкая активность материала приводит к образованию больших объемов нерастворимого осадка, возвращаемого на повторное восстановление. Процесс электроэкстракции никеля из сульфатных растворов осуществляется при плотностях тока 180-230 А/м2, что не позволяет достигнуть высокой производительности процесса производства никеля. Использование чисто сульфатного электролита при электроэкстракции никеля требует создания отдельного производства для реализации заявленной технологической схемы.
Наиболее близким техническим решением является способ получения катодного никеля [Патент РФ №2191850, С25С 1/08, опубл. 27.10.2002, бюл.30], в котором никелевый концентрат, полученный путем флотационного разделения файнштейна, подвергают окислительному обжигу, восстановлению продуктов обжига, растворению хлором восстановленной закиси никеля и обработке остатка выщелачивания соляной кислотой, а далее - получение никеля электроэкстракцией из хлоридных растворов.
Недостатком данного способа является то, что электроэкстракция никеля из чисто хлоридных растворов требует создания отдельного производства для реализации технологии. Известный способ предполагает использование в технологии очистки электролита только хлора и соляной кислоты и ограничивает использование серной кислоты, производимой из технологических газов в процессе обжига никелевого концентрата. Организация процесса очистки растворов от меди с использованием чисто хлоридного электролита затруднена.
Настоящее изобретение направлено на снижение материальных затрат при производстве электролитного никеля за счет организации процесса электроэкстракции всего объема или части никеля из смешанного сульфат-хлоридного электролита с использованием выделяющегося в процессе электролиза хлора для хлоридного выщелачивания восстановленной закиси никеля, а также использование кислого анолита электроэкстракции никеля для очистки электролита и подготовки его к использованию в процессе электроэкстракции или рафинирования никеля.
Предлагаемый способ получения электролитного никеля включает флотационное разделение файнштейна на медный и никелевый концентраты, окислительный обжиг никелевого концентрата, восстановление закиси никеля, очистку растворов выщелачивания последовательно от железа, меди, кобальта и электроэкстракцию никеля.
В отличие от известного решения в предлагаемом способе электроэкстракцию никеля осуществляют из никелевого электролита, содержащего 40-85 г/л сульфата и не менее 45 г/л хлорида в электролизных ваннах с анодными ячейками. Образующуюся в анодных ячейках газожидкостную смесь удаляют и затем разделяют на газовую фазу и кислый анолит. Электрохимические реакции, происходящие на аноде, в основном описываются реакциями
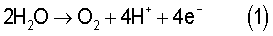
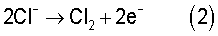
Газовую фазу, содержащую преимущественно хлор, используют для хлоридного выщелачивания восстановленной закиси никеля.
Одну часть кислого анолита, полученного после отделения хлора и содержащего более низкую концентрацию хлоридов, чем электролит, подаваемый в ванны электроэкстракции, используют для разбавления электролита перед проведением операции очистки от меди до необходимой концентрации хлоридов и кислоты, что обеспечивает необходимое качество очистки. Вторую часть кислого анолита подают в схему хлоридного выщелачивания и используют для приготовления электролита католита, подаваемого в ванны электроэкстракции или рафинирования никеля.
При осуществлении электроэкстракции никеля из смешанного электролита, содержащего сульфаты и хлориды, с ростом концентрации сульфатов происходит снижение выхода по току хлора, образующегося по реакции (2), и увеличение выхода по току кислорода по реакции (1), пример 1. Наиболее существенное снижение выхода по току хлора начинается при концентрациях сульфатов в электролите более 85 г/л.
Аналогичные процессы происходят и при снижении концентрации хлоридов ниже 45 г/л. Снижение выхода по току хлора приводит к уменьшению количества образующегося в анодных ячейках хлора реакция (2) и росту кислотности анолита.
Процесс выщелачивания восстановленной закиси никеля в этом случае существенно затруднен вследствие существенного различия скоростей растворения закиси никеля по хлоридному механизму и окислительному кислотному механизму. Длительность процесса выщелачивания восстановленной закиси никеля в хлоридных растворах ограничивается 30 минутами, в то время как процесс растворения в серной кислоте с окислением кислородом - около 5 часов.
Кроме того, при низком выходе по току хлора количество кислоты, образующейся в анолите, превышает объемы, необходимые для процессов приготовления электролита и организации процесса очистки от меди. Это приводит к необходимости увеличения объемов анолита, подаваемого на операцию выщелачивания закиси никеля, что в свою очередь приводит к увеличению затрат на операцию выщелачивания и очистку от железа.
При организации процесса электроэкстракции никеля из преимущественно хлоридных растворов с концентрацией сульфатов ниже 40 г/л выход по току хлора возрастает до 98% и реакция (1), приводящая к образованию кислоты в анолите, практически блокируется. В этом случае количество кислоты, образующейся в анолите, недостаточно для приготовления электролита необходимой кислотности и осуществления подкисления растворов перед очисткой от меди. Для осуществления данных операций необходимо применение соляной кислоты, что приводит к росту затрат на производство никеля.
Очистка растворов выщелачивания, содержащих высокую концентрацию хлоридов, от меди может быть осуществлена только с помощью многократного избытка восстановленной закиси никеля, что существенно усложняет процесс очистки, пример 2. При этом остаточное содержание меди в очищаемых растворах не позволяет обеспечить требуемые качественные показатели электролитного никеля.
Организация процесса очистки от меди с предварительным разбавлением очищенных от железа растворов выщелачивания восстановленной закиси никеля анолитом с низкой концентрацией хлоридов позволяет осуществить очистку растворов от меди до концентрации менее 5 мг/л, что достаточно для производства электролитного никеля требуемых марок.
Технологическая схема процесса получения электролитного никеля изображена на фиг.1. По данной схеме восстановленную закись никеля, полученную в результате флотационного разделения медно-никелевого файнштейна на медный и никелевые концентраты, окислительного обжига никелевого концентрата и восстановления известными способами, имеющую следующий типичный состав: никель 90%, медь 3,5%, железо 3% и кобальт 2,1%, выщелачивают газовой смесью, полученной из анодной ячейки электроэкстракции никеля. Для процесса выщелачивания закиси никеля используется незначительная часть анолита электроэкстракции никеля, который обычно содержит 55-70 г/л никеля.
Выщелачивание восстановленной закиси никеля проводят при температуре в диапазоне 60-108°С. Обычное время выщелачивания составляет 20-40 минут.
Процесс выщелачивания осуществляется по следующим основным реакциям

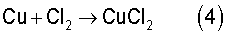
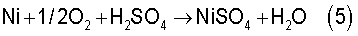
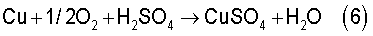
Процесс электроэкстракции никеля организован таким образом, что обеспечивает выход по току хлора 93-95%, при котором выщелачивание осуществляется преимущественно по реакциям (3, 4), что обеспечивает высокую скорость выщелачивания материала.
Раствор хлоридного выщелачивания с суммарной концентрацией никеля, меди, железа и кобальта до 200-280 г/л и концентрацией хлоридов до 270 г/л, после отделения нерастворимого остатка направляется на очистку от железа, которая осуществляется путем окисления железа воздухом и нейтрализацией полученной пульпы карбонатом никеля.
При организации операции очистки от меди цементацией из растворов с высокой концентрацией хлоридов не удается достигнуть остаточного содержания меди менее 20 мг/л, что не позволяет обеспечить требуемые качественные показатели электролитного никеля.
Для достижения требуемого качества очистки растворов от меди их смешивают с анолитом электроэкстракции никеля, обеспечив тем самым снижение концентрации хлоридов до концентрации 55-80 г/л и одновременно подкисление кислотой, содержащейся в анолите.
Очистка от меди осуществляется восстановленной закисью никеля в количестве, составляющем 1,1-1,2 от количества меди в очищаемом растворе, в две стадии с противоточным движением раствора и восстановленной закиси никеля. Такая организация процесса позволяет обеспечить очистку растворов от меди до остаточной концентрации меди 5 мг/л при содержании хлоридов в растворе до 65 г/л.
При более высоких содержаниях хлоридов в растворе в диапазоне, указанном выше, на очистку от меди подается 1,5 - 3-кратный избыток восстановленной закиси никеля по отношению к количеству меди в очищаемом растворе. При этом часть продукта очистки второй стадии очистки направляется на операцию хлоридного выщелачивания совместно с основным объемом закиси никеля, а часть в количестве, необходимом для вывода балансовой меди, на первую стадию очистки. Полученный на первой стадии медный продукт, содержащий обычно до 90% меди и 3-6% никеля направляется на переработку в медное производство.
Очистка от кобальта, свинца и марганца осуществляется обычным образом с окислением данных металлов хлором и нейтрализацией карбонатом никеля.
Очищенный от примесей раствор, содержащий 80-90 г/л никеля, используют для приготовления электролита электроэкстракции никеля, для чего его смешивают с частью анолита электроэкстракции для получения раствора с содержанием никеля 60-70 г/л с рН 2,4-2,6.
Электроэкстракцию никеля осуществляют в электролизных ваннах с анодными ячейками, оснащенными титановыми анодами с каталитическим покрытием, при плотности тока 250-350 А/м2, при температуре 55-60°. Аноды изготовлены из титановой сетки или титановых пластин с покрытием из оксидов иридия, рутения или их смеси с добавкой оксидов титана или тантала.
Смесь анолита и газов, выделяющихся в процессе электроэкстракции никеля, удаляют из анодных ячеек и используют в процессе производства электролитного никеля, как указывалось ранее.
Избыток католита, вытекающий из электролизных ванн, практически не содержащий свободного хлора и кислоты, используют для приготовления карбоната никеля, применяемого в операциях очистки.
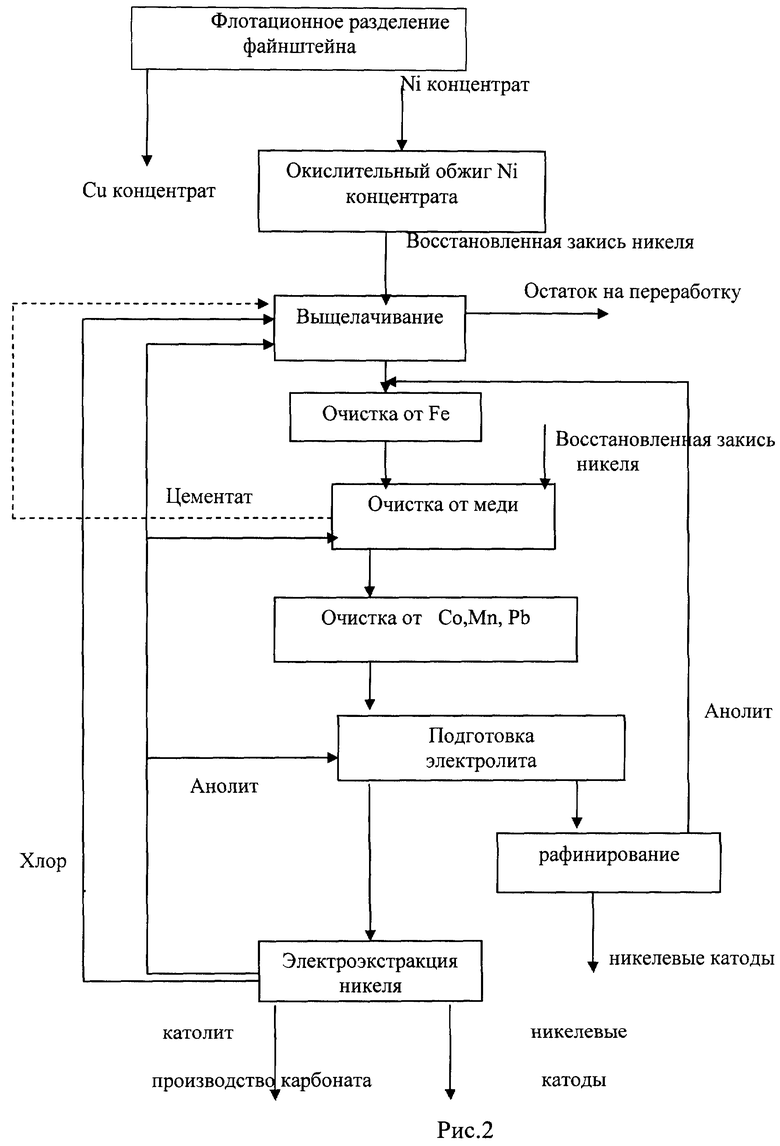
На фиг.2 изображен вариант технологической схемы, в которой только часть восстановленной закиси никеля подвергается выщелачиванию хлором, а вторая часть используется для производства анодов.
По данной схеме соответствующие доли никеля производятся способами электроэкстракции никеля и рафинирования анодов. При одновременном производстве электролитного никеля как способом электроэкстракции, так и рафинирования анодов, электролит для подачи в электролизные ванны готовится для обоих процессов путем смешения очищенного от примесей никелевого раствора и части анолита электроэкстракции никеля.
Анолит, получаемый в процессе рафинирования никелевых анодов, направляется на операцию очистки от железа совместно с растворами хлоридного выщелачивания восстановленной закиси никеля.
Такая организация процесса позволит осуществить процесс электроэкстракции для части производимого никеля, сохраняя технологию рафинирования никелевых анодов для оставшейся части никеля с использованием общей схемы очистки электролита, что очень важно для крупных предприятий, для которых полное изменение технологической схемы осложняется большими капитальными затратами.
Совокупность предлагаемых признаков изобретения обеспечивает достижение требуемого технического результата, т.е. достигается значительная экономия материальных энергетических ресурсов.
Пример 1.
По заявляемому изобретению электроэкстракция никеля проводится из смешанного сульфат-хлоридного электролита в лабораторном электролизере с анодными ячейками. Подача электролита осуществляется в катодное пространство. Из анодного пространства обеспечивается принудительное удаление смеси хлора и анолита.
Применяются два типа анодов: аноды из просечного титана и сплошных титановых пластин. Аноды имеют покрытие из смеси окислов иридия и рутения а так же окиси титана.
В качестве катодов применяются никелевые пластины или титановые матрицы. Во всех опытах электролиз проводится при катодной плотности тока 250 А/м2. Электролит для питания электролизера приготовлен из восстановленной закиси никеля, используемой для производства никелевых анодов.
Закись никеля производят из медно-никелевого файнштейна следующего состава: никель 46%, медь 28%, кобальт 1,6%, железо 3%, сера 22%.
Файнштейн измельчают преимущественно до 45 мк и подвергают флотационному разделению на медный концентрат состава: медь 68%, никель 4,5%, кобальт 0,25%, железо 4%, и никелевый концентрат состава: никель 68%, медь 2,5%, кобальт 1,6%, железо 3,5%. Никелевый концентрат обжигают в печи кипящего слоя при температуре 1100-1200° для удаления серы, а затем восстанавливают в трубчатой печи с использованием в качестве восстановителя кокса. Полученная таким образом восстановленная закись никеля со степенью металлизации не ниже 90%, состава: никель 90%, медь 3,5% кобальт 2,1%, железо 3,5% используется для выщелачивания.
Выщелачивание восстановленной закиси никеля проводят путем распульповки в электролите действующего никелевого производства, имеющего состав: никель 90 г/л, сульфат 120 г/л, хлорид 40 г/л и воде в соотношении 1:1, и подаче хлора в течение 20-40 минут при температуре 70-96°С и рН 1,0-1,5.
После отделения нерастворимого остатка получают раствор состава: никель 225 г/л, медь 7 г/л, железо 7 г/л, кобальт 4,2 г/л.
Раствор очищают от железа путем окисления воздухом в течение 2 часов при температуре 65-70°С при рН-3,5 путем нейтрализации карбонатом никеля.
Для проведения очистки от меди полученный раствор разбавляют электролитом с низкой концентрацией хлоридов. Очистка от меди проводится цементацией 3-5-кратным избытком восстановленной закиси никеля.
Полученный таким образом раствор дополнительно очищают от кобальта путем его окисления хлором до Co3+ и осаждения гидроокиси кобальта нейтрализацией раствора карбонатом никеля.
Очищенные от примесей растворы, содержащие различные концентрации хлоридов и сульфатов никеля, используются для питания лабораторного электролизера в опытах 1-5. В опыте 6 проведена дополнительная очистка электролита от сульфата путем введения в него раствора хлорида бария.
Параметры процесса электроэкстракции никеля приведены в таблице 1.
При проведении процесса электроэкстракции никеля из электролита с высокой концентрацией сульфата, выше 85 г/л, процесс электроэкстракции никеля осуществляется с низким выходом по току хлора и существенным ростом кислотности анолита.
Аналогично при снижении концентрации хлоридов в подаваемом на электроэкстракцию электролите ниже 45 г/л происходит снижение выхода по току хлора и увеличение кислотности анолита.
Электроэкстракция никеля из электролита с низким содержанием сульфата приводит к росту выхода по току хлора до 97%, при этом количество выделяющейся в анодной ячейке кислоты недостаточно для осуществления процесса приготовления электролита и подкисления растворов выщелачивания перед операцией очистки от меди.
Пример 2. По заявляемому изобретению очистка растворов выщелачивания от меди осуществляется цементацией восстановленной закисью никеля.
В таблице 2 приведены данные лабораторных опытов по цементации меди, восстановленной закисью никеля из растворов выщелачивания, полученных в соответствии с примером 1.
Варьирование концентрации хлорида осуществляется путем разбавления очищенного от железа раствора выщелачивания анолитом электроэкстракции никеля. Кроме того, в опытах 1-4 в раствор дополнительно вводится хлорид меди.
Опыты проводятся в лабораторных ректорах при температуре 80-85°. Продолжительность цементации 2 часа. Для обеспечения глубины очистки подается избыток восстановленной закиси по отношению к осаждаемой меди.
При высоких концентрациях хлоридов в очищаемом растворе остаточное содержание меди в очищаемом растворе не позволяет в дальнейшем осуществить производство катодного никеля без организации дополнительных операций очистки. При этом необходимо существенное превышение количества восстановленной закиси никеля по отношению к количеству осаждаемой меди.
При осуществлении операции очистки раствора выщелачивания с предварительным разбавлением анолитом электроэкстракции никеля остаточное содержание меди в растворе 5 мг/л, что соответствует требованиям для производства электролитного никеля.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ КАТОДНОГО НИКЕЛЯ | 1999 |
|
RU2141010C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАТОДНОГО НИКЕЛЯ | 2001 |
|
RU2191850C1 |
| СПОСОБ ПОЛУЧЕНИЯ НИКЕЛЯ И КОНЦЕНТРАТА ДРАГОЦЕННЫХ МЕТАЛЛОВ ИЗ МЕДНО-НИКЕЛЕВОГО ФАЙНШТЕЙНА | 2009 |
|
RU2415956C1 |
| Способ осаждения меди из растворов автоклавного и атмосферного выщелачивания медно-никелевых файнштейнов и штейнов | 2024 |
|
RU2827187C1 |
| СПОСОБ ПОЛУЧЕНИЯ НИКЕЛЯ ИЗ РУДНОГО СУЛЬФИДНОГО СЫРЬЯ | 2012 |
|
RU2492253C1 |
| СПОСОБ ПЕРЕРАБОТКИ МЕДНОГО КОНЦЕНТРАТА ОТ ФЛОТАЦИОННОГО РАЗДЕЛЕНИЯ ФАЙНШТЕЙНА | 2007 |
|
RU2341573C1 |
| СПОСОБ ПРОИЗВОДСТВА КОНЦЕНТРАТА ДРАГОЦЕННЫХ МЕТАЛЛОВ ИЗ СУЛЬФИДНОГО МЕДНО-НИКЕЛЕВОГО СЫРЬЯ | 2010 |
|
RU2444573C2 |
| СПОСОБ ПЕРЕРАБОТКИ МЕДНО-НИКЕЛЕВЫХ СУЛЬФИДНЫХ МАТЕРИАЛОВ | 2001 |
|
RU2175995C1 |
| Способ переработки медно-никелевых сульфидных материалов | 2019 |
|
RU2706400C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОБАЛЬТА И ЕГО СОЕДИНЕНИЙ | 2010 |
|
RU2444574C1 |
Изобретение относится к области цветной металлургии, в частности к получению катодного никеля из сульфидного медно-никелевого сырья. Способ включает флотационное разделение файнштейна на медный и никелевый концентраты, окислительный обжиг никелевого концентрата, восстановление закиси никеля, выщелачивание восстановленной закиси никеля, очистку растворов выщелачивания последовательно от железа, меди, кобальта, электроэкстракцию никеля. Для получения электролитного никеля требуемых марок и экономии материальных энергетических ресурсов электроэкстракцию никеля осуществляют в электролизных ваннах с анодными ячейками из никелевого электролита, содержащего 40-85 г/л сульфата и не менее 45 г/л хлорида, образующуюся газожидкостную смесь удаляют из анодной ячейки, затем разделяют на газовую фазу, содержащую преимущественно хлор, который используют для хлоридного выщелачивания восстановленной закиси никеля, и кислый анолит, который используют для разбавления раствора выщелачивания перед очисткой от меди. 1 з.п. ф-лы, 2 ил., 2 табл.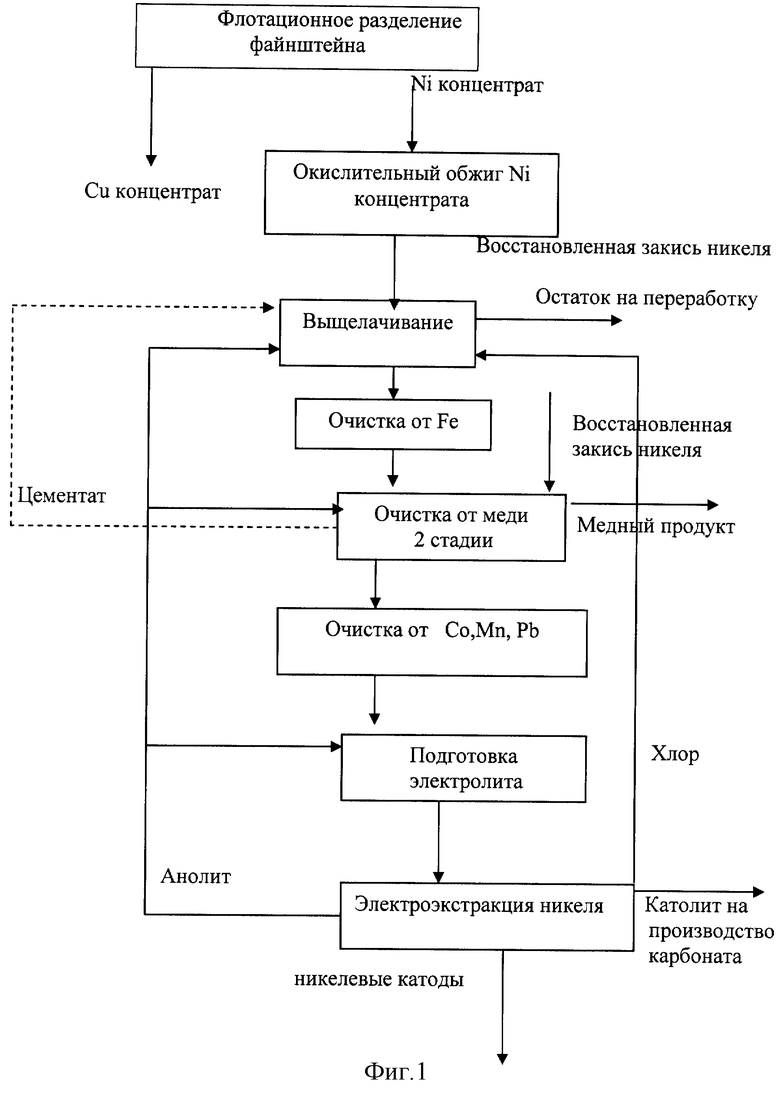
| СПОСОБ ПОЛУЧЕНИЯ КАТОДНОГО НИКЕЛЯ | 2001 |
|
RU2191850C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАТОДНОГО НИКЕЛЯ | 1999 |
|
RU2141010C1 |
| ЭЛЕКТРОХИМИЧЕСКИЙ СПОСОБ ПЕРЕРАБОТКИ МЕДНО-НИКЕЛЕВОГО ФАЙНШТЕЙНАИИ I til I ни-It At: ;БИБЛИО"С;':А | 0 |
|
SU280858A1 |
| Способ электроэкстракции никеля из сульфатно-хлоридного электролита | 1989 |
|
SU1633023A1 |
| Цифровой фильтр | 1986 |
|
SU1385263A1 |
| US 4201648 A, 06.05.1980. | |||
Авторы
Даты
2007-07-20—Публикация
2005-08-11—Подача