Настоящее изобретение относится к новым соединениям, эффективным для профилактики и лечения различных заболеваний, связанных с аномальным ангиогенезом, и к медицинским композициям, таким как ингибиторы ангиогенеза и противоопухолевые агенты, содержащие новые соединения.
Ангиогенез является существенным биологическим феноменом для формирования сосудов плода и морфологического и функционального развития органов. Формирование новых кровеносных сосудов складывается из нескольких процессов, включая миграцию клеток эндотелия, пролиферацию и образование трубки, и, как показано, тучные клетки, лимфоциты, интерстициальные клетки и другие клетки играют важную роль в данном процессе (J. Biol. Chem., 267, 10931, 1992).
Идентифицировано множество факторов, стимулирующих ангиогенез in vivo, в частности фактор роста эндотелия сосудов (сокращаемый здесь далее как VEGF) и фактор роста фибробластов (сокращаемый здесь далее как FGF), как сообщается, усиливают ангиогенез (Endocrinology, 133, 848, 1993, and Biochem. Biophys. Res. Commun., 147, 876, 1987).
Хотя физиологический ангиогенез происходит во время заживления раны или в женском эстральном цикле у взрослых индивидуумов, известно, что патологическое усиление ангиогенеза у взрослых индивидуумов вовлечено в возникновение или прогрессию различных заболеваний. Конкретные болезни, связанные с аномальным ангиогенезом, включают рак, ревматоидный артрит, атеросклероз, диабетическую ретинопатию, ангиому, псориаз и тому подобное (N. Engl. J. Med., 333, 1757, 1995). В частности, в литературе указывается на зависимость роста солидных опухолей от ангиогенеза, и ингибиторы ангиогенеза являются, следовательно, перспективными в качестве новых терапевтических агентов для воздействия на солидные опухоли (J. Natl. Cancer Inst., 82, 4, 1990).
Патентная литература (WO 02/16348 и WO 02/32872) предлагается как иллюстрация предшествующего уровня техники в отношении 6-членных азотсодержащих ароматических производных, связанных с замещенным индолом.
Хотя WO 02/16348 описывает производные индола, которые подавляют стимулированный VEGF ангиогенез благодаря селективному ингибированию тирозинкиназы, результаты фармакологических тестов их ингибирующего действия не раскрыты. Несмотря на то, что WO 02/32872 описывает производные пиридина, связанные с индольным кольцом через атом кислорода в 4 положении, ни соединение по настоящему изобретению, ни его ингибирующее действие на ангиогенез, стимулированный FGF, не раскрыты.
Описание изобретения
Задачей настоящего изобретения является исследование и раскрытие соединений, ингибирующих ангиогенез, которые (1) проявляют противоопухолевую активность путем существенного подавления ангиогенеза, индуцируемого как VEGF, так и FGF, которые являются главными факторами ангиогенеза in vivo, (2) и являются пригодными в качестве лекарственных средств в плане их свойств, биокинетики и безопасности, и (3) пригодны для облегчения, предотвращения и лечения различных заболеваний, связанных с аномальным усилением ангиогенеза.
В результате очень упорных исследований изобретатели настоящего изобретения успешно синтезировали новые пиридиновые производные и пиримидиновые производные, представленные следующей общей формулой (I), их соли или гидраты. Показано, что данные соединения, их соли или гидраты оказывают прекрасный ингибирующий ангиогенез эффект.
Конкретно в настоящем изобретении предлагается следующее:
<1> соединение (за исключением N1-циклопропил-5-((2-(((2-хлорэтиламино)карбонил)амино)-4-пиридил)окси)-1H-1-индолкарбоксамида),
представленное общей формулой
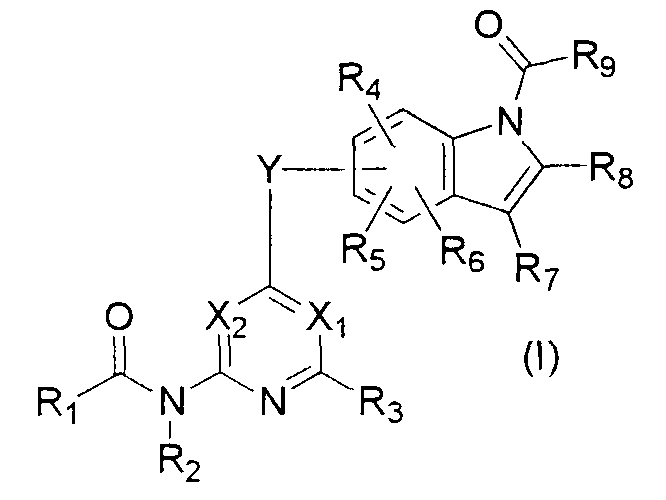
где X1 представляет собой атом азота или группу, представленную формулой -CR10=, X2 представляет собой атом азота или группу, представленную формулой -CR11= и X1 и X2 не представляют собой атом азота одновременно;
Y представляет собой атом кислорода, атом серы, сульфинильную группу, сульфонильную группу или группу, представленную формулой -NRY- (где RY представляет собой атом водорода или С1-6алкильную группу);
R1 представляет собой необязательно замещенную С1-6алкоксигруппу, необязательно замещенную С6-10арилоксигруппу, группу, представленную формулой -NR12aR12b, группу, представленную формулой
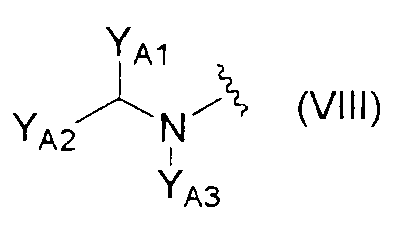
(где YA1 и YA2 каждый независимо представляет собой группу, представленную формулой -A10-A11-A12 (где A10 представляет собой простую связь или необязательно замещенный С1-6алкилен; A11 представляет собой простую связь, атом кислорода, карбонильную группу или сульфонильную группу и A12 представляет собой атом водорода, С1-6алкильную группу, С2-6алкенильную группу, С2-6алкинильную группу, С3-8циклоалкильную группу, С6-10арильную группу, 5-10-членную гетероарильную группу, группу, представленную формулой -NRA10RA11, группу, представленную формулой -ORA12 (где RA10, RA11 и RA12 каждый независимо представляет собой атом водорода, С1-6алкильную группу или С3-8циклоалкильную группу) или группу, представленную формулой
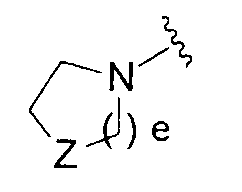
(где e равно 1 или 2; Z представляет собой атом кислорода, группу, представленную формулой -CRX7RX8-, или группу, представленную формулой -NRX9-; RX7, RX8 и RX9 каждый независимо представляет собой атом водорода, гидроксильную группу или С1-6алкильную группу)); YA3 представляет собой атом водорода или необязательно замещенную С1-6алкильную группу) или группу, представленную формулой
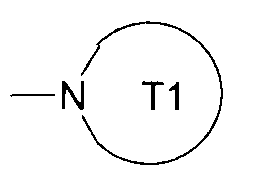
(где T1 представляет собой необязательно замещенный 5-10-членный ароматический гетероцикл, который может иметь X в кольце, или необязательно замещенный 3-10-членный гетероцикл, который может иметь X в кольце);
R3, R4, R5, R6, R7, R8, R10 и R11 каждый независимо представляет собой атом водорода, атом галогена, цианогруппу, необязательно замещенную С1-6алкильную группу, необязательно замещенную С2-6алкенильную группу, необязательно замещенную С2-6алкинильную группу, необязательно замещенную С3-8циклоалкильную группу, группу, представленную формулой -CO-R13, группу, представленную формулой -NR14-CO-R13, группу, представленную формулой -SO2-R15, группу, представленную формулой -NR14-SO2-R15, или группу, представленную формулой -NR16aR16b; R9 представляет собой группу, представленную формулой -NR16aR16b, или группу, представленную формулой
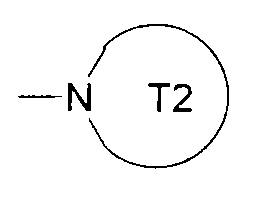
(где T2 представляет собой необязательно замещенный 5-10-членный ароматический гетероцикл или необязательно замещенный 3-10-членный гетероцикл);
R12a и R12b каждый независимо представляет собой атом водорода, необязательно замещенную С1-6алкильную группу, необязательно замещенную С3-6алкенильную группу, необязательно замещенную С3-6алкинильную группу, необязательно замещенную С3-8циклоалкильную группу, необязательно замещенную 3-10-членную гетероциклическую группу или необязательно замещенную С1-6алкоксигруппу;
R13 представляет собой атом водорода, необязательно замещенную С1-6алкильную группу, необязательно замещенную С2-6алкенильную группу, необязательно замещенную С2-6алкинильную группу, необязательно замещенную С3-8циклоалкильную группу, необязательно замещенную С6-10арильную группу, необязательно замещенную 5-10-членную гетероарильную группу, необязательно замещенную 3-10-членную гетероциклическую группу, необязательно замещенную С1-6алкоксигруппу, необязательно замещенную С6-10арилоксигруппу, группу, представленную формулой -NR12aR12b, или группу, представленную формулой
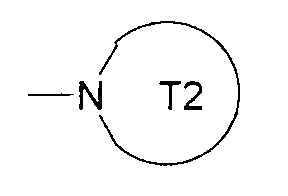
(где T2 представляет собой необязательно замещенный 5-10-членный ароматический гетероцикл или необязательно замещенный 3-10-членный гетероцикл);
R2 и R14 каждый независимо представляет собой атом водорода, необязательно замещенную С1-6алкильную группу, необязательно замещенную С2-6алкенильную группу, необязательно замещенную С2-6алкинильную группу, необязательно замещенную С3-8циклоалкильную группу или группу, представленную формулой -CO-R13;
R15 представляет собой необязательно замещенную С1-6алкильную группу, необязательно замещенную С2-6алкенильную группу, необязательно замещенную С2-6алкинильную группу, необязательно замещенную С3-8циклоалкильную группу, необязательно замещенную С6-10арильную группу, необязательно замещенную 5-10-членную гетероарильную группу, или необязательно замещенную 3-10-членную гетероциклическую группу;
R16a и R16b каждый независимо представляет собой атом водорода, необязательно замещенную С1-6алкильную группу, необязательно замещенную С3-6алкенильную группу, необязательно замещенную С3-6алкинильную группу, необязательно замещенную С3-8циклоалкильную группу, необязательно замещенную С6-10арильную группу, необязательно замещенную 5-10-членную гетероарильную группу, необязательно замещенную 3-10-членную гетероциклическую группу или необязательно замещенную С1-6алкоксигруппу и
X представляет собой атом кислорода, атом серы, карбонильную группу, сульфонильную группу, группу, представленную формулой -CRX1RX2-, или группу, представленную формулой -NRX3- (где RX1,RX2 и RX3 каждый независимо представляет собой атом водорода или группу, представленную формулой -A1-A2-A3 (где A1 и A2 каждый независимо представляет собой простую связь, необязательно замещенную С1-6алкиленовую группу или карбонильную группу и A3 представляет собой атом водорода, С3-8циклоалкильную группу, группу, представленную формулой -NRA1RA2, или формулой -ORA3 (где RA1,RA2 и RA3 каждый независимо представляет собой атом водорода или С1-6алкильную группу), или необязательно замещенную группу, представленную формулой

(где a равно 1 или 2))),
его соль или гидрат;
<2> соединение (за исключением N1-циклопропил-5-((2-(((2-хлорэтиламино)карбонил)амино)-4-пиридил)окси)-1H-1-индолкарбоксамида), представленное общей формулой
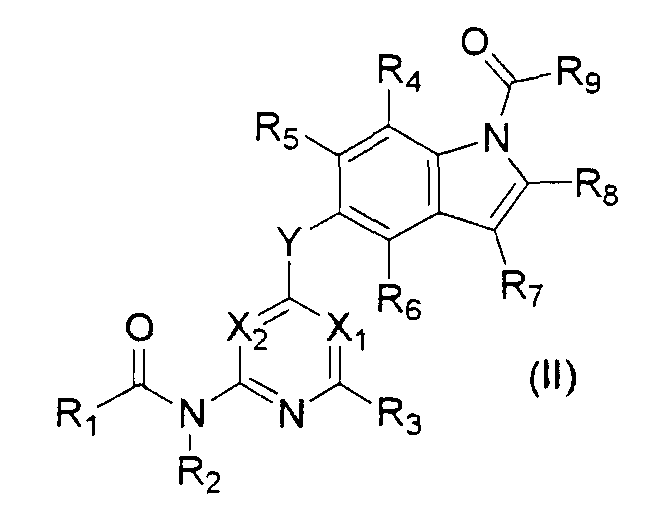
где X1, X2, Y, R1, R2, R3, R4, R5, R6, R7, R8 и R9 имеют те же самые значения, что и X1, X2, Y, R1, R2, R3, R4, R5, R6, R7, R8 и R9 в<1> соответственно, его соль или гидрат;
<3> соединение по <1> или <2>, соль соединения или гидрат, где Y представляет собой атом кислорода, группу, представленную формулой -NH-, или группу, представленную формулой -N(CH3)-;
<4> соединение по <1> или <2>, соль соединения или гидрат, где Y представляет собой атом кислорода;
<5> соединение по любому из <1>-<4>, соль соединения или гидрат, где один из X1 и X2 представляет собой группу, представленную формулой -CH=, а другой представляет собой атом азота;
<6> соединение по любому из <1>-<4>, соль соединения или гидрат, где оба X1 и X2 представляют собой группу, представленную формулой -CH=;
<7> соединение по любому из <1>-<6>, соль соединения или гидрат, где R3, R4, R5, R6 и R8 каждый представляют собой атом водорода и R7 представляет собой атом водорода, атом галогена или необязательно замещенную С1-6алкильную группу;
<8> соединение по любому из <1>-<7>, соль соединения или гидрат, где R9 представляет собой группу, представленную формулой -NHR17 (где R17 представляет собой необязательно замещенную С1-6алкильную группу, С3-6алкинильную группу, С3-8циклоалкильную группу, необязательно замещенную С6-10арильную группу или необязательно замещенную 5-10-членную гетероарильную группу);
<9> соединение по любому из <1>-<7>, соль соединения или гидрат, где R9 представляет собой группу, представленную формулой -NR18aR18b (где R18a и R18b каждый независимо представляет собой С1-6алкильную группу);
<10> соединение по любому из <1>-<7>, соль соединения или гидрат, где R9 представляет собой группу, представленную формулой
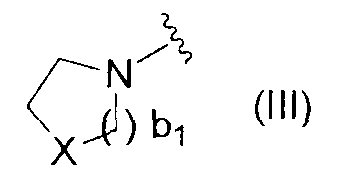
(где b1 равен 1 или 2; X имеет то же определение, что и X в<1>);
<11> соединение по любому из <1>-<7>, соль соединения или гидрат, где R9 представляет собой группу, представленную формулой -NHR19 (где R19 представляет собой С1-6алкильную группу, С3-6алкинильную группу, С3-8циклоалкильную группу или С6-10арильную группу);
<12> соединение по любому из <1>-<11>, соль соединения или гидрат, где R3, R4, R5, R6, R7 и R8, каждый представляет собой атом водорода;
<13> соединение по любому из <1>-<12>, соль соединения или гидрат, где R2 представляет собой атом водорода;
<14> соединение по любому из <1>-<13>, соль соединения или гидрат, где R9 представляет собой группу, представленную формулой -NHR20 (где R20 представляет собой метильную группу, этильную группу или циклопропильную группу);
<15> соединение по любому из <1>-<13>, соль соединения или гидрат, где R9 представляет собой группу, представленную формулой -NH(CH3);
<16> соединение по любому из <1>-<15>, соль соединения или гидрат, где R1 представляет собой дополнительно необязательно замещенную группу, представленную формулой
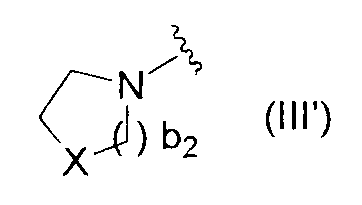
(где b2 равен 0, 1 или 2; X имеет то же определение, что и X в<1>);
<17> соединение по любому из <1>-<16>, соль соединения или гидрат, где R1 представляет собой группу, представленную формулой
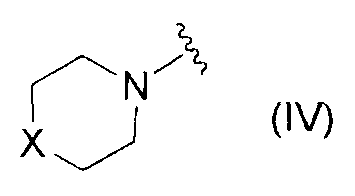
(где X имеет то же определение, что и X в <1>);
<18> соединение по <17>, соль соединения или гидрат, где X в формуле (IV) представляет собой атом кислорода;
<19> соединение по <17>, соль соединения или гидрат, где X в формуле (IV) представляет собой группу, представленную формулой

(где RX4 представляет собой атом водорода или группу, представленную формулой -A4-A5-A6 (где A4 и A5 каждый независимо представляет собой простую связь, необязательно замещенную С1-6алкиленовую или карбонильную группу и A6 представляет собой атом водорода, С3-8циклоалкильную группу или группу, представленную формулой -NRA4RA5 или формулой -ORA6 (где RA4,RA5 и RA6 каждый независимо представляет собой атом водорода или С1-6алкильную группу)));
<20> соединение по <17>, соль соединения или гидрат, где X в формуле (IV) представляет собой группу, представленную формулой
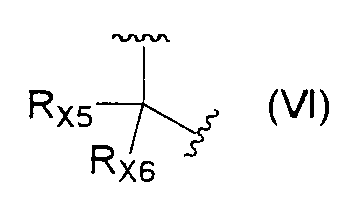
(где RX5 и RX6 каждый независимо представляет собой атом водорода или группу, представленную формулой -A7-A8-A9 (где A7 и A8 каждый независимо представляет собой простую связь, необязательно замещенную С1-6алкиленовую группу или карбонильную группу и A9 представляет собой атом водорода, С3-8циклоалкильную группу, группу, представленную формулой -NRA7RA8 или формулой -ORA9 (где RA7,RA8 и RA9 каждый независимо представляет собой атом водорода или С1-6алкильную группу) или группу, представленную формулой
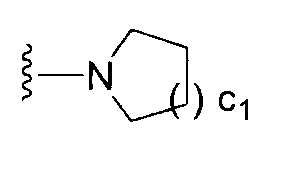
(где c1 равен 0, 1 или 2)));
<21> соединение по <20>, соль соединения или гидрат, где один из RX5 и RX6 в формуле (VI) представляет собой гидроксильную группу, а другой представляет собой атом водорода или С1-6алкильную группу;
<22> соединение по <20>, соль соединения или гидрат, где один из RX5 и RX6 в формуле (VI) представляет собой атом водорода, а другой представляет собой группу, представленную формулой

(где c2 равен 1 или 2);
<23> соединение по любому из <1>-<16>, соль соединения или гидрат, где R1 представляет собой группу, представленную формулой
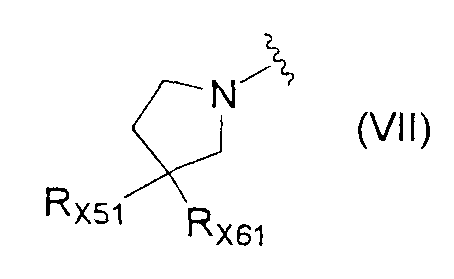
(где RX51 и RX61 каждый независимо представляет собой атом водорода или группу, представленную формулой -A71-A81-A91 (где A71 и A81 каждый независимо представляет собой простую связь, необязательно замещенную С1-6алкиленовую группу или карбонильную группу и A91 представляет собой атом водорода, С3-8циклоалкильную группу, группу, представленную формулой -NRA71RA81, или формулой -ORA91 (где RA71,RA81 и RA91 каждый независимо представляет собой атом водорода или С1-6алкильную группу) или группу, представленную формулой
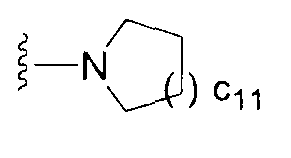
(где c11 равен 0, 1 или 2)));
<24> соединение по любому из <1>-<15>, соль соединения или гидрат, где R1 представляет собой группу, представленную формулой
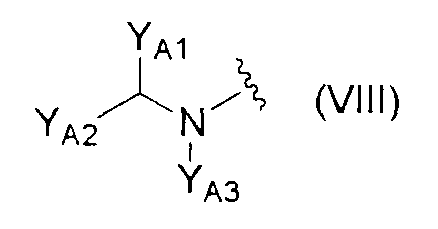
(где YA1 и YA2 каждый независимо представляет собой группу, представленную формулой -A10-A11-A12 (где A10 представляет собой простую связь или необязательно замещенную С1-6алкиленовую группу; A11 представляет собой простую связь, атом кислорода, карбонильную группу или сульфонильную группу и A12 представляет собой атом водорода, С1-6алкильную группу, С2-6алкенильную группу, С2-6алкинильную группу, С3-8циклоалкильную группу, С6-10арильную группу, 5-10-членную гетероарильную группу, группу, представленную формулой -NRA10RA11 или формулой -ORA12 (где RA10,RA11 и RA12 каждый независимо представляет собой атом водорода, С1-6алкильную группу или С3-8циклоалкильную группу) или группу, представленную формулой

(где e равен 1 или 2, а Z представляет собой атом кислорода или группу, представленную формулой -CRX7RX8 или формулой -NRX9- (где RX7,RX8 и RX9 каждый независимо представляет собой атом водорода, гидроксильную группу или С1-6алкильную группу))), и YA3 представляет собой атом водорода или необязательно замещенную С1-6алкильную группу);
<25> соединение по <24>, соль соединения или гидрат, где один из YA1 и YA2 в формуле (VIII) представляет собой атом водорода, а другой представляет собой группу, представленную формулой -(CH2)2-A13-A14 (где A13 представляет собой простую связь, карбонильную группу или сульфонильную группу и A14 представляет собой С1-6алкильную группу, группу, представленную формулой -NRA13RA14 (где RA13 и RA14 каждый независимо представляет собой атом водорода, С1-6алкильную группу или С3-8циклоалкильную группу) или группу, представленную формулой
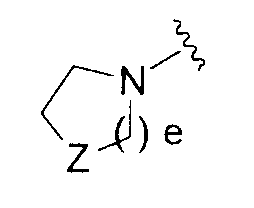
(где e и Z имеют то же значение, что и e и Z в <24> соответственно), и YA3 в формуле (VIII) представляет собой атом водорода;
<26> соединение по любому из <1>-<15>, соль соединения или гидрат, где R1 представляет собой группу, представленную формулами
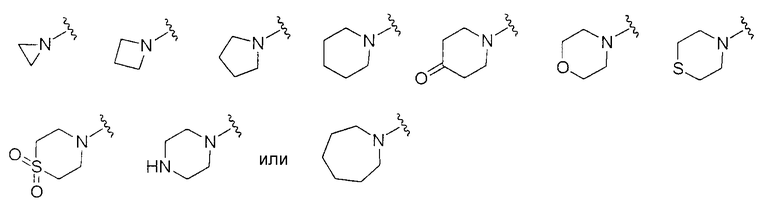
(причем каждый из указанных выше членов необязательно замещен группой, выбранной из группы заместителей альфа,
где группа заместителей альфа представляет собой группу, состоящую из атома галогена, гидроксильной группы, тиоловой группы, нитрогруппы, цианогруппы, карбоксильной группы, аминогруппы, С1-6алкильной группы, С3-8циклоалкильной группы и группы, представленной формулами
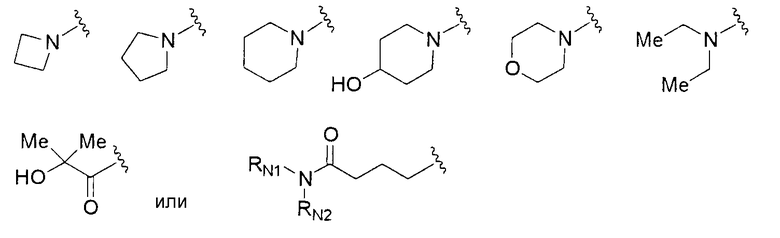
(где RN1 и RN2 каждый независимо представляет собой атом водорода или С1-6алкильную группу);
<27> соединение по любому из<1>-<15>, соль соединения или гидрат, где R1 представляет собой группу, представленную формулами
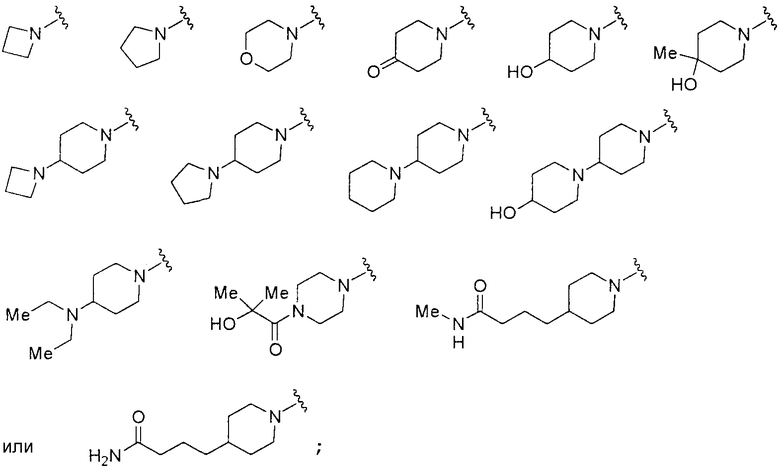
<28> соединение по любому из <1>-<15>, соль соединения или гидрат, где R1 представляет собой группу, представленную формулами
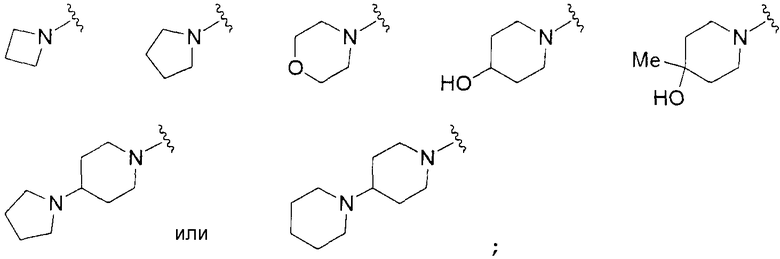
<29> соединение по любому из <1>-<15>, соль соединения или гидрат, где R1 представляет собой группу, представленную формулами
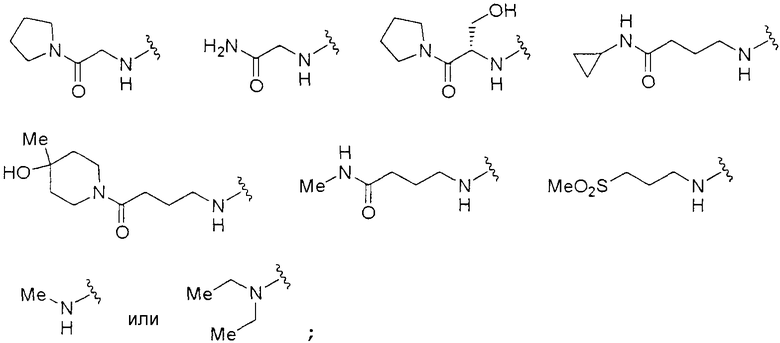
<30> соединение по <1> или <2>, соль соединения или гидрат, где соединение представлено общей формулой
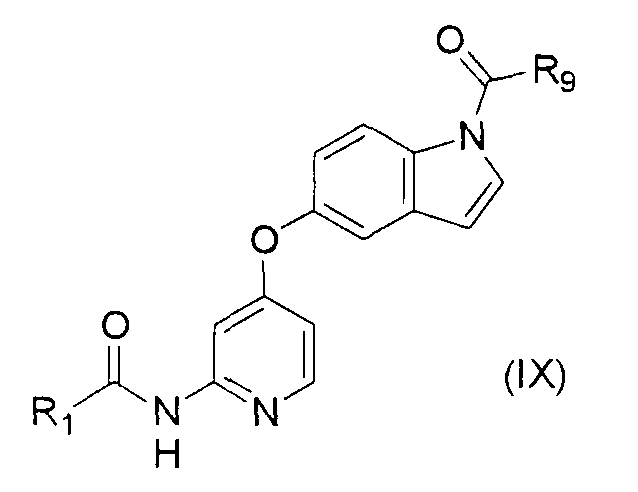
(где R1 представляет собой группу, представленную формулами
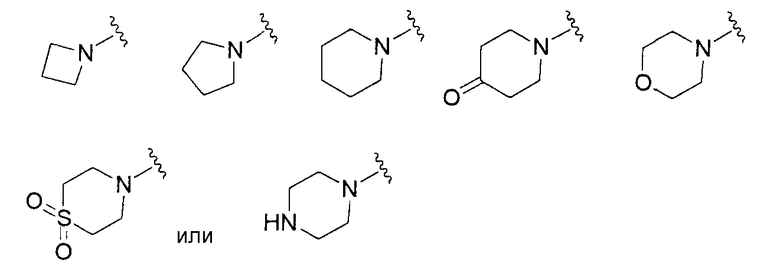
(причем каждый из указанных выше членов необязательно замещен группой, выбранной из группы заместителей бета,
где группа заместителей бета представляет собой группу, состоящую из гидроксильной группы, С1-6алкильной группы, С3-8циклоалкильной группы и группы, представленной формулами
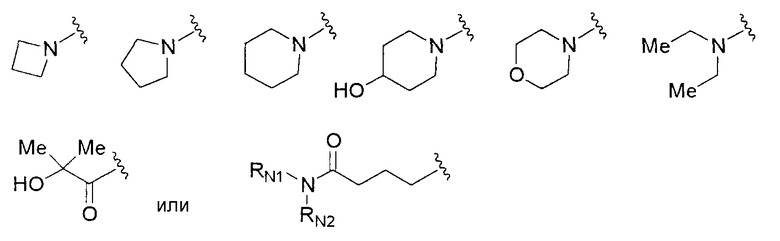
(где RN1 и RN2 каждый независимо представляет собой атом водорода или С1-6алкильную группу)); R9 представляет собой группу, представленную формулой -NHR20 (где R20 представляет собой метильную группу, этильную группу или циклопропильную группу));
<31> соединение по <1>, соль соединения или гидрат, где соединение представляет собой соединение, выбранное из группы, включающей
(1) N1-этил-5-(2-((метоксиламино)карбонил)амино-4-пиримидил)окси-1H-индолкарбоксамид,
(2) метиламид 5-(6-(3-(3-диэтиламинопропиламино)уреидо)пиримидин-4-илокси)-1H-индол-1-карбоновой кислоты,
(3) метиламид 5-(6-(((4-гидроксипиперидин-1-ил)карбонил)амино)пиримидин-4-илокси)-1H-индол-1-карбоновой кислоты,
(4) метиламид 5-(6-((4-пирролидин-1-ил)пиперидин-1-ил)карбониламино)пиримидин-4-илокси)-1H-индол-1-карбоновой кислоты,
(5) метиламид 5-(2-(3-((1R)-1-карбамоил-2-фенилэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(6) метиламид 5-(2-(3-((1S)-1-карбамоил-2-фенилэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(7) метиламид 5-(2-(3-(2-оксо-2-(пирролидин-1-ил)этил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(8) метиламид 5-(2-(3-(2-(4-гидрокси-4-метилпиперидин-1-ил)-2-оксоэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(9) метиламид 5-(2-(3-((1S)-1-карбамоилэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(10) метиламид 5-(2-(3-((1S)-1-карбамоил-3-метилбутил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(11) метиламид 5-(2-(3-карбамоилметилуреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(12) метиламид 5-(2-(3-циклопропилкарбамоилметилуреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(13) метиламид 5-(2-(3-((1S)-1-карбамоил-2-гидроксиэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(14) метиламид 5-(2-(3-((1R)-1-карбамоил-2-гидроксиэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(15) диамид (2S)-2-(3-(4-(1-метилкарбамоил-1H-индол-5-илокси)пиридин-2-ил)уреидо)-1,5-пентандикарбоновой кислоты,
(16) (2S)-2-(3-(4-(1-метилкарбамоил-1H-индол-5-илокси)пиридин-2-ил)уреидо)сукцинамид,
(17) метиламид 5-(2-(3-((1S)-1-циклопропилкарбамоил-2-гидроксиэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(18) метиламид 5-(2-(3-((1S)-1-гидроксиметил-2-оксо-2-пирролидин-1-илэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(19) метиламид 5-(2-(3-((1R)-1-гидроксиметил-2-оксо-2-пирролидин-1-илэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(20) метиламид 5-(2-(3-((1S)-1-гидроксиметил-2-оксо-2-пиперидин-1-илэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(21) метиламид 5-(2-(3-((1R)-1-гидроксиметил-2-оксо-2-пиперидин-1-илэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(22) метиламид 5-(2-(3-((1S)-1-гидроксиметил-2-(4-гидроксипиперидин-1-ил)-2-оксоэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(23) метиламид 5-(2-(3-((1S)-1-гидроксиметил-2-(морфолин-4-ил)-2-оксоэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(24) метиламид 5-(2-(3-(2-циклопропилкарбамоилэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(25) метиламид 5-(2-(3-(3-оксо-3-(пирролидин-1-ил)пропил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(26) метиламид 5-(2-(3-(3-(4-гидрокси-4-метилпиперидин-1-ил)-3-оксопропил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(27) N1-этил-5-(2-(((2-этоксиэтил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(28) N1-метил-5-(2-((4-(2-гидрокси-2-метилпропионил)пиперазин-1-ил)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(29) N1-метил-5-(2-((3-(диэтиламино)пропиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(30) N1-метил-5-(2-(((3-(4-гидроксипиперидин)пропил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(31) N1-метил-5-(2-(((3-(4-метилпиперазин-1-ил)пропил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(32) метиламид 5-(2-(3-(4-оксо-4-(пирролидин-1-ил)бутил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(33) метиламид 5-(2-(3-(3-(циклопропилкарбамоил)пропил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(34) метиламид 5-(2-(3-(4-(4-гидрокси-4-метилпиперидин-1-ил)-4-оксобутил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(35) метиламид 5-(2-(3-(3-(диэтилкарбамоил)пропил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(36) метиламид 5-(2-(3-(3-(метилкарбамоил)пропил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(37) N1-метил-5-(2-(пирролидин-1-илкарбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(38) N1-метил-5-(2-(пиперидин-1-илкарбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(39) N1-метил-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(40) N1-метил-5-(2-(4-оксопиперидин-1-илкарбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(41) метиламид 5-(2-(((4-гидрокси-4-метилпиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(42) N1-метил-5-(2-((4-(1-гидрокси-1-метилэтил)пиперидин)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(43) метиламид 5-(2-(((4-(3-метилкарбамоилпропил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(44) метиламид 5-(2-(((4-(3-карбамоилпропил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(45) метиламид 5-(2-((4-((пирролидин-1-ил)карбонил)пиперидин-1-ил)карбониламино)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(46) N1-метил-5-(2-(((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид,
(47) N1-метил-5-(2-(((4-(пиперидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид,
(48) N1-метил-5-(2-((4-этилпиперазин-1-ил)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(49) N1-метил-5-(2-((4-(2-гидроксиэтил)пиперазин-1-ил)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(50) N1-метил-5-(2-((3-метилсульфонилпропиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(51) N1-метил-5-(2-((4-(2-диметиламиноацетил)пиперазин-1-ил)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(52) N1-метил-5-(2-((4-циклогексилпиперазин-1-ил)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(53) N4-(4-(1-(метиламино)карбонил-1H-5-индолил)окси-2-пиридил)-4-морфолинкарбоксамид,
(54) N1-метил-5-(2-((1,1-диоксотиоморфолин-4-илкарбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид,
(55) этиламид 5-(2-(3-((1R)-1-гидроксиметил-2-оксо-2-пирролидин-1-илэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(56)этиламид 5-(2-(3-((1S)-1-гидроксиметил-2-оксо-2-пирролидин-1-илэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(57) этиламид 5-(2-(3-((1R)-1-гидроксиметил-2-оксо-2-пиперидин-1-илэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(58) этиламид 5-(2-(3-((1S)-1-гидроксиметил-2-оксо-2-пиперидин-1-илэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(59) этиламид 5-(2-(3-(2-(4-гидрокси-4-метилпиперидин-1-ил)-2-оксоэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(60) N1-этил-5-(2-((((1-метил-4-пиперидил)метил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(61) N1-этил-5-(2-(((2-(диэтиламино)этил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(62) N1-этил-5-(2-(((2-(морфолин-4-ил)этил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(63) N1-этил-5-(2-(((2-(4-гидроксипиперидин)этил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(64) N1-метил-5-(2-(((2-(4-гидроксипиперидин)этил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(65) N1-этил-5-(2-((3-(диэтиламино)пропиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(66) N1-этил-5-(2-(((3-(морфолин-4-ил)пропил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(67) N1-этил-5-(2-(((3-(4-метилпиперазин-1-ил)пропил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(68) N1-циклопропил-5-(2-(((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид,
(69) циклопропиламид 5-(2-(3-((1R)-1-гидроксиметил-2-оксо-2-пирролидин-1-илэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(70) циклопропиламид 5-(2-(3-((1S)-1-гидроксиметил-2-оксо-2-пирролидин-1-илэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(71) циклопропиламид 5-(2-(3-(2-оксо-2-(пирролидин-1-ил)этил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(72) циклопропиламид 5-(2-(3-(3-оксо-3-(пирролидин-1-ил)пропил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(73) циклопропиламид 5-(2-(3-((1R)-1-гидроксиметил-2-оксо-2-пиперидин-1-илэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(74) циклопропиламид 5-(2-(3-((1S)-1-гидроксиметил-2-оксо-2-пиперидин-1-илэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(75) N1-фенил-5-(2-(((3-(диэтиламино)пропил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(76) N1-фенил-5-(2-(((3-(4-метилпиперазин-1-ил)пропил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(77) N1-этил-5-(2-(((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид,
(78) этиламид 5-(2-(((4-гидрокси-4-метилпиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(79) N1-этил-5-(2-((4-гидроксипиперидин-1-ил)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(80) N1-этил-5-(2-(пиперидин-1-илкарбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(81) N1-этил-5-((2-((пирролидин-1-илкарбонил)амино)-4-пиридил)окси)-1H-1-индолкарбоксамид,
(82) N4-(4-((1-(этиламино)карбонил-1H-5-индолил)окси)-2-пиридил)-4-морфолинкарбоксамид,
(83) N1-этил-5-(2-((1,1-диоксотиоморфолин-4-илкарбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид,
(84) N1-этил-5-(2-((метоксиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(85) N1-циклопропил-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(86) N1-циклопропил-5-(2-(((4-гидрокси-4-метилпиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид,
(87) N4-(4-(1-(циклопропиламино)карбонил-1H-5-индолил)окси-2-пиридил)-4-морфолинкарбоксамид,
(88) N1-циклопропил-5-(2-((пирролидин-1-илкарбонил)амино)-4-пиридил)окси-1H-1-индолкарбоксамид,
(89) N1-циклопропил-5-(2-(пиперидин-1-илкарбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(90) N4-(4-(1-(циклопентиламино)карбонил-1H-5-индолил)окси-2-пиридил)-4-морфолинкарбоксамид,
(91) циклопентиламид 5-(2-(((4-гидроксипиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(92) N1-циклопентил-5-(2-((4-(пирролидин-1-ил)пиперидин-1-илкарбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид,
(93) N1-(3-метилбутил)-5-(2-(((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид,
(94) N1-(3-метилбутил)-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(95) N4-(4-(1-((3-метилбутил)амино)карбонил-1H-5-индолил)окси-2-пиридил)-4-морфолинкарбоксамид,
(96) N1-(1-этилпропил)-5-(2-(((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид,
(97) N1-(1-этилпропил)-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(98) N4-(4-(1-((1-этилпропил)амино)карбонил-1H-5-индолил)окси-2-пиридил)-4-морфолинкарбоксамид,
(99) N4-(4-(1-((1-пентил)амино)карбонил-1H-5-индолил)окси-2-пиридил)-4-морфолинкарбоксамид,
(100) N1-(1-пентил)-5-(2-(((4-гидроксипиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид,
(101) N1-(1-пентил)-5-(2-((4-(пирролидин-1-ил)пиперидин-1-илкарбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид,
(102) N1-метил-3-хлор-5-(2-(((3-(диэтиламино)пропил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(103) N1-метил-3-хлор-5-(2-((4-(пирролидин-1-ил)пиперидин)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(104) N1-метил-3-хлор-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(105) N1-метил-3-хлор-5-(2-(((3-(4-гидроксипиперидин)пропил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(106) N1-метил-3-хлор-5-(2-((4-(2-гидроксиэтил)пиперазин-1-ил)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(107) N4-(4-(3-хлор-1-(метиламино)карбонил-1H-5-индолил)окси-2-пиридил)-4-морфолинкарбоксамид,
(108) N1-метил-3-хлор-5-(2-((4-этилпиперазин-1-ил)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(109) N1-этил-3-хлор-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(110) N1-этил-3-хлор-5-(2-(((3-(4-гидроксипиперидин)пропил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(111) N1-этил-3-хлор-5-(2-(((3-(диэтиламино)пропил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(112) N1,3-диметил-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(113) N1,3-диметил-5-(2-((4-(пирролидин-1-ил)пиперидин)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(114) N1-циклопропил-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-3-метил-1H-1-индолкарбоксамид,
(115) N1-циклопропил-5-(2-((4-(2-гидроксиэтил)пиперазин-1-ил)карбонил)амино-4-пиридил)окси-3-метил-1H-1-индолкарбоксамид,
(116) N1-метил-5-(2-((метиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(117) N1-метил-5-(2-((диэтиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(118) N1-(2-пропинил)-5-(2-((пирролидин-1-ил)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид;
(119) N1-метил-5-(2-(азетидин-1-илкарбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(120) N1-этил-5-(2-(азетидин-1-илкарбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(121) N1-циклопропил-5-(2-(азетидин-1-илкарбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(122) N1-метил-5-(2-(((4-(морфолин-4-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид,
(123) N1-метил-5-(2-(((4-(азетидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид,
(124) N1-метил-5-(2-(((4-(диэтиламино)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид,
(125) N1-метил-5-(2-(((4-(4-гидроксипиперидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид и
(126) N1-пропил-5-(2-(пирролидин-1-илкарбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид;
<32> соединение по <1>, соль соединения или гидрат, где соединение представляет собой соединение, выбранное из группы, включающей
(1) метиламид 5-(2-(3-(2-оксо-2-(пирролидин-1-ил)этил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(2) метиламид 5-(2-(3-карбамоилметилуреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(3) метиламид 5-(2-(3-((1S)-1-гидроксиметил-2-оксо-2-пирролидин-1-илэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(4) N1-метил-5-(2-((4-(2-гидрокси-2-метилпропионил)пиперазин-1-ил)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(5) метиламид 5-(2-(3-(4-оксо-4-(пирролидин-1-ил)бутил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(6) метиламид 5-(2-(3-(3-(циклопропилкарбамоил)пропил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(7) метиламид 5-(2-(3-(4-(4-гидрокси-4-метилпиперидин-1-ил)-4-оксобутил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(8) метиламид 5-(2-(3-(3-(метилкарбамоил)пропил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(9) N1-метил-5-(2-(пирролидин-1-илкарбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(10) N1-метил-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(11) N1-метил-5-(2-(4-оксопиперидин-1-илкарбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(12) метиламид 5-(2-(((4-гидрокси-4-метилпиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(13) метиламид 5-(2-(((4-(3-метилкарбамоилпропил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(14) метиламид 5-(2-(((4-(3-карбамоилпропил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(15) N1-метил-5-(2-(((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид,
(16) N1-метил-5-(2-(((4-(пиперидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид,
(17) N1-метил-5-(2-((3-метилсульфонилпропиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(18) N4-(4-(1-(метиламино)карбонил-1H-5-индолил)окси-2-пиридил)-4-морфолинкарбоксамид,
(19) N1-циклопропил-5-(2-(((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид,
(20) этиламид 5-(2-(((4-гидрокси-4-метилпиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(21) N1-этил-5-(2-((4-гидроксипиперидин-1-ил)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(22) N1-этил-5-((2-((пирролидин-1-илкарбонил)амино)-4-пиридил)окси)-1H-1-индолкарбоксамид,
(23) N4-(4-((1-(этиламино)карбонил-1H-5-индолил)окси)-2-пиридил)-4-морфолинкарбоксамид,
(24) N1-циклопропил-5-(2-((пирролидин-1-илкарбонил)амино)-4-пиридил)окси-1H-1-индолкарбоксамид,
(25) N1-метил-3-хлор-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(26) N1-метил-5-(2-((метиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(27) N1-метил-5-(2-((диэтиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(28) N1-(2-пропинил)-5-(2-((пирролидин-1-ил)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(29) N1-метил-5-(2-(азетидин-1-илкарбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(30) N1-этил-5-(2-(азетидин-1-илкарбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(31) N1-циклопропил-5-(2-(азетидин-1-илкарбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(32) N1-метил-5-(2-(((4-(морфолин-4-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид,
(33) N1-метил-5-(2-(((4-(азетидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид,
(34) N1-метил-5-(2-(((4-(диэтиламино)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид,
(35) N1-метил-5-(2-(((4-(4-гидроксипиперидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид и
(36) N1-пропил-5-(2-(пирролидин-1-илкарбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид;
<33> соединение по <1>, соль соединения или гидрат, где соединение представляет собой соединение, выбранное из группы, включающей
(1) метиламид 5-(2-(((4-гидрокси-4-метилпиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(2) N1-метил-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид,
(3) N1-метил-5-(2-(((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид,
(4) N1-метил-5-(2-(((4-(пиперидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид и
(5) N4-(4-(1-(метиламино)карбонил-1H-5-индолил)окси-2-пиридил)-4-морфолинкарбоксамид;
<34> фармацевтическая композиция, включающая соединение по любому из <1>-<33>, и фармацевтически приемлемый адъювант;
<35> агент для профилактики или лечения заболевания, при котором эффективно ингибирование ангиогенеза, включающий в качестве активного ингредиента соединение по любому из <1>-<33>, его соль или гидрат;
<36> ингибитор ангиогенеза, включающий в качестве активного ингредиента соединение по любому из <1>-<33>, его соль или гидрат;
<37> противоопухолевый агент, включающий в качестве активного ингредиента соединение по любому из <1>-<33>, его соль или гидрат;
<38> противоопухолевый агент по <37>, где опухоль представляет собой рак поджелудочной железы, рак желудка, рак ободочной кишки, рак молочной железы, рак простаты, рак легких, рак почки, рак мозга, рак крови или рак яичников;
<39> терапевтический агент для лечения гемангиомы, включающий в качестве активного ингредиента соединение по любому из <1>-<33>, его соль или гидрат;
<40> ингибитор метастазов рака, включающий в качестве активного ингредиента соединение по любому из <1>-<33>, его соль или гидрат;
<41> терапевтический агент для лечения неоваскуляризации сетчатки или диабетической ретинопатии, включающий в качестве активного ингредиента соединение по любому из <1>-<33>, его соль или гидрат;
<42> терапевтический агент для лечения воспалительного заболевания, включающий в качестве активного ингредиента соединение по любому из <1>-<33>, его соль или гидрат;
<43> терапевтический агент для лечения воспалительного заболевания по <42>, где воспалительное заболевание представляет собой деформирующий артрит, ревматоидный артрит, псориаз или реакцию гиперчувствительности отставленного типа;
<44> терапевтический агент для лечения атеросклероза, включающий в качестве активного ингредиента соединение по любому из <1>-<33>, его соль или гидрат;
<45> противоопухолевый агент, ингибирующий ангиогенез, включающий в качестве активного ингредиента соединение по любому из <1>-<33>, его соль или гидрат;
<46> способ профилактики или лечения заболевания, при котором эффективным является ингибирование ангиогенеза, включающий введение больному фармакологически эффективной дозы соединения по любому из <1>-<33>, его соли или гидрата и
<47> применение соединения по любому из <1>-<33>, его соли или гидрата для получения профилактического или терапевтического агента для лечения заболевания, при котором эффективным является торможение ангиогенеза.
Лучший вариант осуществления изобретения
Ниже описываются значения терминов, символов или тому подобного, применяемых в описании, и подробно описывается настоящее изобретение.
Следует отметить, что хотя в данном описании структурная формула соединения может указывать для удобства на определенный изомер, настоящее изобретение включает все геометрические изомеры, возможные для структур заявленных соединений, изомеры, такие как оптические изомеры на основе асимметричного атома углерода, стереоизомеры и таутомеры, и смеси изомеров, которые для удобства не ограничиваются описаниями формул, могут быть включены любые из изомеров или смесей. Следовательно, могут существовать оптически активные соединения и рацемические соединения, когда в молекуле имеется асимметричные атомы углерода, однако, настоящее изобретение ими не ограничивается, и в объем настоящего изобретения могут быть включены любые случаи. Кроме того, хотя существует множество кристаллических морфизмов, это тоже сходно не ограничивается. Конкретно, может быть включена любая из отдельных кристаллических форм или смесей, кроме того, могут быть включены ангидриды, гидраты или сольваты.
Кроме того, соединения по настоящему изобретению также включают соединения, которые все еще проявляют желаемую активность после того, как они подверглись в организме метаболизму, такому как окисление, восстановление, гидролиз и конъюгация, и в объем настоящего изобретения также включаются соединения, из которых получаются соединения по настоящему изобретению после того, как они подвергаются метаболизму, такому как окисление, восстановление и гидролиз.
Термин "C1-6алкильная группа", указанный в описании, представляет собой линейную или разветвленную алкильную группу, содержащую от 1 до 6 атомов углерода, которая представляет собой одновалентную группу, полученную в результате удаления атома водорода из алифатического углеводорода, содержащего от 1 до 6 атомов углерода. В качестве конкретных примеров могут быть упомянуты метильная группа, этильная группа, н-пропильная группа, изопропильная группа, н-бутильная группа, изобутильная группа, втор-бутильная группа, трет-бутильная группа, н-пентильная группа, изопентильная группа, втор-пентильная группа, неопентильная группа, 1-метилбутильная группа, 2-метилбутильная группа, 1,1-диметилпропильная группа, 1,2-диметилпропильная группа, н-гексильная группа, изогексильная группа, 1-метилпентильная группа, 2-метилпентильная группа, 3-метилпентильная группа, 1,1-диметилбутильная группа, 1,2-диметилбутильная группа, 2,2-диметилбутильная группа, 1,3-диметилбутильная группа, 2,3-диметилбутильная группа, 3,3-диметилбутильная группа, 1-этилбутильная группа, 2-этилбутильная группа, 1,1,2-триметилпропильная группа, 1,2,2-триметилпропильная группа, 1-этил-1-метилпропильная группа, 1-этил-2-метилпропильная группа или тому подобное, и предпочтительно метильная группа, этильная группа, н-пропильная группа, изопропильная группа, н-бутильная группа, изобутильная группа, втор-бутильная группа и трет-бутильная группа.
Термин "C2-6алкенильная группа", указанный в описании, представляет собой линейную или разветвленную алкенильную группу, содержащую от 2 до 6 атомов углерода, которая может содержать от 1 до 2 двойных связей. В качестве конкретных примеров здесь может быть отмечена этенильная группа, 1-пропенильная группа, 2-пропенильная группа, 1-бутенильная группа, 2-бутенильная группа, 3-бутенильная группа, 2-метил-1-пропенильная группа, пентенильная группа, гексенильная группа, гександиенильная группа или тому подобное, предпочтительно этенильная группа, 1-пропенильная группа, 2-пропенильная группа, 1-бутенильная группа, 2-бутенильная группа, 3-бутенильная группа и 2-метил-1-пропенильная группа.
Термин "C3-6алкенильная группа", указанный в описании, представляет собой линейную или разветвленную алкенильную группу, содержащую от 3 до 6 атомов углерода, которая может содержать от 1 до 2 двойных связей. В качестве конкретных примеров здесь может быть отмечена 1-пропенильная группа, 2-пропенильная группа, 1-бутенильная группа, 2-бутенильная группа, 3-бутенильная группа, 2-метил-1-пропенильная группа, пентенильная группа, гексенильная группа, гександиенильная группа или тому подобное, предпочтительно 1-пропенильная группа, 2-пропенильная группа, 1-бутенильная группа, 2-бутенильная группа, 3-бутенильная группа и 2-метил-1-пропенильная группа.
Термин "C2-6алкинильная группа", указанный в описании, представляет собой линейную или разветвленную алкинильную группу, содержащую от 2 до 6 атомов углерода, которая может содержать от 1 до 2 тройных связей. В качестве конкретных примеров здесь может быть отмечена этинильная группа, 1-пропинильная группа, 2-пропинильная группа, 1-бутинильная группа, 2-бутинильная группа, 3-бутинильная группа, пентинильная группа, гексинильная группа, гександиинильная группа или тому подобное, предпочтительно этинильная группа, 1-пропинильная группа, 2-пропинильная группа, 1-бутинильная группа, 2-бутинильная группа и 3-бутинильная группа.
Термин "C3-6алкинильная группа", указанный в описании, представляет собой линейную или разветвленную алкинильную группу, содержащую от 3 до 6 атомов углерода, которая может содержать от 1 до 2 тройных связей. В качестве конкретных примеров здесь может быть отмечена 1-пропинильная группа, 2-пропинильная группа, 1-бутинильная группа, 2-бутинильная группа, 3-бутинильная группа, пентинильная группа, гексинильная группа, гександиинильная группа или тому подобное, предпочтительно 1-пропинильная группа, 2-пропинильная группа, 1-бутинильная группа, 2-бутинильная группа и 3-бутинильная группа.
Термин "C3-8циклоалкильная группа", указанный в описании, представляет собой циклическую алифатическую углеводородную группу, содержащую от 3 до 8 атомов углерода, и в качестве конкретных примеров здесь может быть отмечена циклопропильная группа, циклобутильная группа, циклопентильная группа, циклогексильная группа, циклогептильная группа, циклооктильная группа или тому подобное, и предпочтительно циклопропильная группа, циклобутильная группа и циклопентильная группа.
Термин "C1-6алкиленовая группа", указанный в описании, представляет собой двухвалентную группу, получаемую в результате дополнительного удаления атома водорода из указанного ранее определения C1-6алкильной группы. В качестве конкретных примеров здесь может быть отмечена метиленовая группа, этиленовая группа, метилэтиленовая группа, пропиленовая группа, этилэтиленовая группа, 1,1-диметилэтиленовая группа, 1,2-диметилэтиленовая группа, тетраметиленовая группа, пентаметиленовая группа, гексаметиленовая группа или тому подобное, предпочтительно метиленовая группа и этиленовая группа.
Термин "C1-6алкоксигруппа", указанный в описании, представляет собой оксигруппу, связанную с указанным ранее определением "C1-6алкильной группы." В качестве конкретных примеров здесь может быть отмечена метоксигруппа, этоксигруппа, н-пропоксигруппа, изопропоксигруппа, н-бутоксигруппа, изобутоксигруппа, втор-бутоксигруппа, трет-бутоксигруппа, н-пентилоксигруппа, изопентилоксигруппа, втор-пентилоксигруппа, неопентилоксигруппа, 1-метилбутоксигруппа, 2-метилбутоксигруппа, 1,1-диметилпропоксигруппа, 1,2-диметилпропоксигруппа, н-гексилоксигруппа, изогексилоксигруппа, 1-метилпентилоксигруппа, 2-метилпентилоксигруппа, 3-метилпентилоксигруппа, 1,1-диметилбутоксигруппа, 1,2-диметилбутоксигруппа, 2,2-диметилбутоксигруппа, 1,3-диметилбутоксигруппа, 2,3-диметилбутоксигруппа, 3,3-диметилбутоксигруппа, 1-этилбутоксигруппа, 2-этилбутоксигруппа, 1,1,2-триметилпропоксигруппа, 1,2,2-триметилпропоксигруппа, 1-этил-1-метилпропоксигруппа, 1-этил-2-метилпропоксигруппа или тому подобное, предпочтительно метоксигруппа, этоксигруппа, н-пропоксигруппа, изопропоксигруппа, н-бутоксигруппа, изобутоксигруппа, втор-бутоксигруппа и трет-бутоксигруппа.
Термин "C1-6алкилтиогруппа", указанный в описании, представляет собой тиогруппу, связанную с указанным ранее определением C1-6алкильной группы. В качестве конкретных примеров здесь может быть отмечена метилтиогруппа, этилтиогруппа, н-пропилтиогруппа, изопропилтиогруппа, н-бутилтиогруппа, изобутилтиогруппа, втор-бутилтиогруппа, трет-бутилтиогруппа, н-пентилтиогруппа, изопентилтиогруппа, втор-пентилтиогруппа, неопентилтиогруппа, 1-метилбутилтиогруппа, 2-метилбутилтиогруппа, 1,1-диметилпропилтиогруппа, 1,2-диметилпропилтиогруппа, н-гексилтиогруппа, изогексилтиогруппа, 1-метилпентилтиогруппа, 2-метилпентилтиогруппа, 3-метилпентилтиогруппа, 1,1-диметилбутилтиогруппа, 1,2-диметилбутилтиогруппа, 2,2-диметилбутилтиогруппа, 1,3-диметилбутилтиогруппа, 2,3-диметилбутилтиогруппа, 3,3-диметилбутилтиогруппа, 1-этилбутилтиогруппа, 2-этилбутилтиогруппа, 1,1,2-триметилпропилтиогруппа, 1,2,2-триметилпропилтиогруппа, 1-этил-1-метилпропилтиогруппа, 1-этил-2-метилпропилтиогруппа или тому подобное, предпочтительно метилтиогруппа, этилтиогруппа, н-пропилтиогруппа, изопропилтиогруппа, н-бутилтиогруппа, изобутилтиогруппа, втор-бутилтиогруппа и трет-бутилтиогруппа.
Термин "C6-10арильная группа", указанный в описании, представляет собой ароматическую углеводородную кольцевую группу, содержащую от 6 до 10 атомов углерода. В качестве конкретных примеров здесь может быть отмечена фенильная группа, 1-нафтильная группа, 2-нафтильная группа, инденильная группа, азуленильная группа, гепталенильная группа или тому подобное, предпочтительно фенильная группа, 1-нафтильная группа и 2-нафтильная группа.
Термин "C6-10арилоксигруппа", указанный в описании, представляет собой оксигруппу, связанную с указанным ранее определением C1-6алкильной группы. В качестве конкретных примеров здесь может быть отмечена феноксигруппа, 1-нафтилоксигруппа, 2-нафтилоксигруппа, инденилоксигруппа, азуленилоксигруппа, гепталенилоксигруппа или тому подобное, предпочтительно феноксигруппа, 1-нафтилоксигруппа и 2-нафтилоксигруппа.
Термин "атом галогена", указанный в описании, представляет собой атом фтора, атом хлора, атом брома или атом иода и предпочтительно атом фтора, атом хлора и атом брома.
Термин "гетероатом", указанный в описании, представляет собой атом азота, атом серы или атом кислорода.
Термин "5-10-членный ароматический гетероцикл", указанный в описании, представляет собой ароматическое кольцо, в котором число атомов, образующих кольцо, составляет от 5 до 10, и от 1 до нескольких гетероатомов входят в состав атомов, образующих кольцо. Конкретные примеры представляют собой пиррольное кольцо, пиридиновое кольцо, пиридазиновое кольцо, пиримидиновое кольцо, пиразиновое кольцо, пиразольное кольцо, имидазольное кольцо, триазольное кольцо, тетразольное кольцо, индольное кольцо, изоиндольное кольцо, индазольное кольцо, хинолиновое кольцо, изохинолиновое кольцо, циннолиновое кольцо, хиназолиновое кольцо, хиноксалиновое кольцо, нафтиридиновое кольцо, фталазиновое кольцо, карбазольное кольцо, пуриновое кольцо, фурановое кольцо, тиофеновое кольцо, бензимидазольное кольцо, имидазопиридиновое кольцо, имидазотриазиновое кольцо, пирролопиридиновое кольцо, пирролопиримидиновое кольцо, пиридопиримидиновое кольцо, оксазольное кольцо, изоксазольное кольцо, тиазольное кольцо, изотиазольное кольцо, феноксазиновое кольцо, фенотиазиновое кольцо, фуропиррольное кольцо, имидазотиазольное кольцо, бензоксазольное кольцо, бензтиазольное кольцо, пиразолоксазольное кольцо, пиридоксазиновое кольцо, бензофурановое кольцо, бензотиофеновое кольцо или тому подобное, предпочтительно фурановое кольцо, тиофеновое кольцо и тиазольное кольцо.
Термин "5-10-членная гетероарильная группа", указанный в описании, представляет собой одновалентную группу, получаемую при удалении атома водорода из определения 5-10-членного ароматического гетероцикла.
Термин "3-10-членный гетероцикл", указанный в описании, представляет собой
(1) моноциклическое или бициклическое неароматическое кольцо,
(2) имеющее от 3 до 10 атомов в кольце,
(3) содержащее от 1 до 2 гетероатомов среди атомов кольца,
(4) необязательно включающее от 1 до 2 двойных связей в кольце и
(5) необязательно включающее от 1 до 3 карбонильных групп или от 1 до 3 сульфонильных групп в кольце.
Конкретные примеры представляют собой азиридиновое кольцо, азетидиновое кольцо, пирролидиновое кольцо, пиперидиновое кольцо, 4-оксопиперидиновое кольцо, гомопиперидиновое кольцо, пиперазиновое кольцо, гомопиперазиновое кольцо, морфолиновое кольцо, тиоморфолиновое кольцо, 1,1-диоксотиоморфолиновое кольцо, пиридоновое кольцо, фталимидное кольцо, сукцинимидное кольцо или тому подобное, предпочтительно азетидиновое кольцо, пирролидиновое кольцо, пиперидиновое кольцо, пиперазиновое кольцо, морфолиновое кольцо и тиоморфолиновое кольцо.
Термин "3-10-членная гетероциклическая группа", указанный в описании, представляет собой одновалентную группу, получаемую при удалении атома водорода из определения 3-10-членного гетероцикла.
Термин "необязательно замещенный", указанный в описании, эквивалентен по значению термину "который может иметь 1 или множество заместителей при произвольном их сочетании в замещаемых положениях". В качестве конкретных примеров таких заместителей здесь могут быть отмечены следующие:
(1) атом галогена,
(2) гидроксильная группа,
(3) тиоловая группа,
(4) нитрогруппа,
(5) цианогруппа,
(6) азидогруппа,
(7) формильная группа,
(8) карбоксильная группа,
(9) аминогруппа,
(10) оксогруппа или
(11) группа, представленная формулой -T1-T2-T3, где T1 представляет собой простую связь или C1-6алкиленовую группу; T2 представляет собой простую связь, C1-6алкиленовую группу, атом кислорода, атом серы, сульфинильную группу, сульфонильную группу, карбонильную группу или группу, представленную формулой -O-CO-, формулой -CO-O-, формулой -NRT1-, формулой -CO-NRT1-, формулой -NRT1-CO-, формулой -SO2-NRT1- или формулой -NRT1-SO2-; T3 представляет собой атом водорода, C1-6алкильную группу, C2-6алкенильную группу, C2-6алкинильную группу, C3-8циклоалкильную группу, C6-10арильную группу, 5-10-членную гетероарильную группу, 3-10-членную гетероциклическую группу или группу, представленную формулой -N(RT2)(RT3); RT1, RT2 или RT3 каждый независимо представляет собой атом водорода или C1-6алкильную группу, где C1-6алкильная группа, C2-6алкенильная группа, C2-6алкинильная группа, C3-8циклоалкильная группа, C6-10арильная группа, 5-10-членная гетероарильная группа и 3-10-членная гетероциклическая группа в T3 каждая независимо может иметьот 1 до 3 групп, выбранных из группы, указанной ниже группы заместителей.
<Группа заместителей>
Атом галогена, гидроксильная группа, тиоловая группа, нитрогруппа, цианогруппа, C1-6алкильная группа, C3-8циклоалкильная группа, C2-6алкенильная группа, C2-6алкинильная группа, C6-10арильная группа, 5-10-членная гетероарильная группа, 3-10-членная гетероциклическая группа, C1-6алкоксигруппа и C1-6алкилтиогруппа.
Термин "уходящая группа", указанный в описании, может представлять собой любую группу, обычно известную как уходящая группа в органическом синтезе, без специальных ограничений, и в качестве конкретных примеров здесь может быть отмечен атом галогена, такой как атом хлора, атом брома, атом иода; нитрогруппа; алкилтиогруппа, такая как метилтиогруппа, этилтиогруппа и пропилтиогруппа; арилтиогруппа, такая как фенилтиогруппа, толуилтиогруппа и 2-пиридилтиогруппа; алкилсульфонилоксигруппа, такая как метансульфонилоксигруппа, трифторметансульфонилоксигруппа, этансульфонилоксигруппа, пропансульфонилоксигруппа; арилсульфонилоксигруппа, такая как бензолсульфонилоксигруппа, п-толуолсульфонилоксигруппа; алканоилоксигруппа, такая как ацетоксигруппа и трифторацетоксигруппа; алкоксигруппа, такая как метоксигруппа, этоксигруппа и пропоксигруппа; алкиламиногруппа, такая как метиламиногруппа, этиламиногруппа, пропиламиногруппа и бутиламиногруппа; диалкиламиногруппа, такая как диметиламиногруппа, диэтиламиногруппа, дипропиламиногруппа, метилэтиламиногруппа, этилпропиламиногруппа и метилпропиламиногруппа; замещенная фосфорилоксигруппа, такая как дифеноксифосфорилоксигруппа или тому подобное, предпочтительно атом галогена, такой как атом хлора, атом брома и атом иода, трифторметансульфонильная группа или тому подобное.
В качестве "соли", указанной в описании, здесь может быть отмечена, например, соль с неорганической кислотой, соль с органической кислотой, соль с неорганическим основанием, соль с органическим основанием, соль с кислой или основной аминокислотой или тому подобное, предпочтительно фармакологически приемлемая соль. Соль образуется в подходящем соотношении от 0,1 до 5 молекул кислоты или основания на одну молекулу соединения.
В качестве предпочтительных примеров соли с неорганической кислотой здесь может быть отмечена, например, соль с хлористоводородной кислотой, бромистоводородной кислотой, серной кислотой, азотной кислотой, фосфорной кислотой или тому подобное, и в качестве предпочтительных примеров соли с органической кислотой здесь может быть отмечена, например, соль с уксусной кислотой, янтарной кислотой, фумаровой кислотой, малеиновой кислотой, винной кислотой, лимонной кислотой, молочной кислотой, стеариновой кислотой, бензойной кислотой, метансульфокислотой, п-толуолсульфокислотой или тому подобное.
В качестве предпочтительных примеров соли с неорганическим основанием здесь может быть отмечена, например, соль щелочных металлов, такая как соль натрия и соль калия, соль щелочноземельных металлов, такая как соль кальция и соль магния, соль алюминия, соль аммония или тому подобное. В качестве предпочтительных примеров соли с органическим основанием здесь может быть отмечена, например, соль с диэтиламином, диэтаноламином, меглумином, N,N'-дибензилэтилендиамином или тому подобное.
В качестве предпочтительных примеров соли с кислыми аминокислотами здесь может быть отмечена, например, соль с аспарагиновой кислотой, глутаминовой кислотой или тому подобное и в качестве предпочтительных примеров соли с основными аминокислотами здесь может быть отмечена, например, соль с аргинином, лизином, орнитином или тому подобное.
В качестве "адъюванта", указанного в описании, здесь может быть отмечен, например, наполнитель, связующий агент, разрыхлитель, смазывающий агент, окрашивающий агент, агент, корректирующий покрытие, стабилизатор, эмульгатор, усилитель поглощения, поверхностно-активное вещество, агент, доводящий рН, консервант, антиоксидант или тому подобное.
Далее раскрыты способы получения соединений изобретения. Для получения соединений изобретения, представленных общими формулами (I) и (II), могут рассматриваться различные способы синтеза, осуществляемого обычными способами органического синтеза, и последующее является иллюстративными примерами способов их получения.
Общий способ синтеза
Способ получения 1
Обычный способ получения соединения, представленного формулой (Ia)
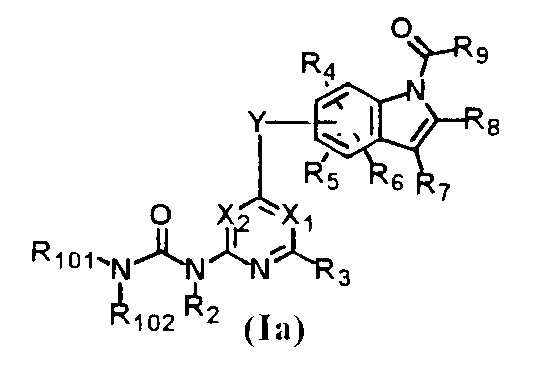
где R101, R102 могут представлять собой то же самое определение, что и R12a, R12b формулы (R12a и R12b определены выше) соответственно, или R101 и R102 образуют цикл, и формула -NR101R102 может представлять собой формулу
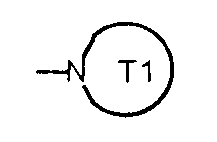
(где T1 определен выше); другие обозначения определены выше.
Способ получения 1-A
Обычный способ получения соединения (1e), которое представляет собой соединение, представленное формулой (Ia), где Y представляет собой атом кислорода, атом серы или группу, представленную формулой -NRY- (RY представляет собой атом водорода или C1-6алкильную группу)
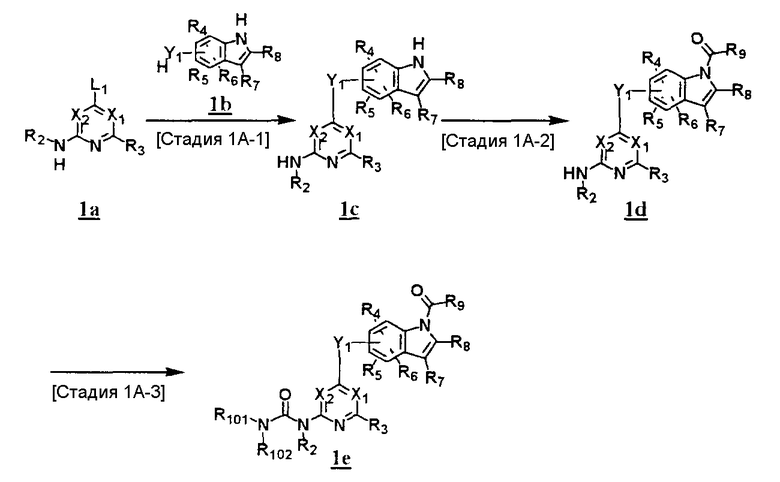
где Y1 представляет собой атом кислорода, атом серы или группу, представленную формулой -NRY1- (RY1 представляет собой атом водорода или C1-6алкильную группу); L1 представляет собой уходящую группу; другие обозначения указаны выше.
<Стадия 1A-1>
Данная стадия предназначена для получения соединения (1 с) путем конденсации пиримидинового или пиридинового производного (1а), содержащего уходящую группу (L1) в положении 4, с производным индола (1b). В качестве растворителя в реакции может быть использован N-метилпирролидон, N,N-диметилформамид, диметилсульфоксид, 2-этоксиэтанол, хлорбензол или тому подобное. В реакционную смесь может быть добавлено основание или кислота, конкретно могут быть использованы органическое основание, такое как диизопропилэтиламин, неорганическое основание, такое как карбонат калия, карбонат цезия и гидрид натрия, и кислота, такая как пиридингидрохлорид и хлористоводородная кислота. Реакцию можно проводить при температуре, варьирующей от комнатной температуры до температуры кипения с обратным холодильником в течение времени, варьирующего от 10 минут до 30 часов. Кроме того, в качестве исходного вещества может быть использовано соединение, в котором атом галогена, который не является уходящей группой, присоединен к пиримидиновому или пиридиновому кольцу, и после данной стадии атом галогена может быть восстановлен посредством каталитического восстановления или подобного ему.
<Стадия 1A-2>
Данная стадия предназначена для получения соединения (1d) путем карбоксамидирования положения 1 индола в соединении (1с). В качестве реагента может быть использовано производное карбамата, производное изоцианата, галогенизированное карбамоильное производное или тому подобное. В качестве растворителя для реакции может быть использован хлороформ, толуол, N-метилпирролидон, N,N-диметилформамид, диметилсульфоксид, хлорбензол. В реакционную среду может быть добавлено основание, например органическое основание, такое как пиридин, триэтиламин и диизопропилэтиламин, неорганическое основание, такое как карбонат калия, карбонат цезия и гидрид натрия. Реакцию можно проводить в течение времени от 10 минут до 30 часов при температуре от 0°С до температуры кипения с обратным холодильником.
<Стадия 1A-3>
Данная стадия предназначена для превращения соединения (1d) в производное мочевины (1e). Сложноэфирное производное карбамата получают с использованием, например, фенилхлоркарбоната или тому подобного. После выделения данного промежуточного соединения или без его выделения промежуточное соединение вводят в реакцию с амином, в результате чего может быть получено производное мочевины. Альтернативно, путем взаимодействия карбаматного производного или изоцианатного производного в качестве реагента оно может быть превращено в соответствующее производное мочевины. В качестве растворителя для реакции может быть использован хлороформ, толуол, N-метилпирролидон, N,N-диметилформамид, диметилсульфоксид, хлорбензол или тому подобное. В реакцию может быть добавлено основание, например, органическое основание, такое как пиридин, триэтиламин и диизопропилэтиламин, неорганическое основание, такое как карбонат калия, карбонат цезия и гидрид натрия. Реакцию можно проводить в течение времени от 10 минут до 30 часов при температуре от 0°C до температуры кипения с обратным холодильником.
Следует отметить, что превращение заместителя в R2, R101, R102 может быть также осуществлено с помощью подходящей реакции окисления, реакции восстановления, реакции восстановительного аминирования, реакции образования сложного эфира, реакции образования амида, реакции введения защитной группы, реакции снятия защиты, реакции гидролиза или тому подобного, которые обычно применяют до и/или после каждого процесса. Конкретно, например, в случае, когда R2 представляет собой атом водорода в соединениях (1a), (1c) и (1d), пригодны следующие способы при указанных выше превращениях заместителя, а именно способ превращения R2 в С1-6алкильную группу путем проведения реакции восстановительного аминирования с альдегидом или кетоном, способ, в котором после получения соответствующего производного мочевины, как указано на <стадии 1A-3>, из соединения (1 с) и кетона или альдегида, содержащего амин, аминную боковую цепь вводят в R101, R102 путем дальнейшего проведения реакции восстановительного аминирования с амином или тому подобным. В данных случаях в качестве восстанавливающего агента могут быть использованы цианоборогидрид натрия, триметоксиборогидрид натрия, триацетоксиборогидрид натрия или тому подобное и в качестве растворителя для реакции могут быть использованы метанол, тетрагидрофуран, дихлорметан, дихлорэтан или тому подобное. Кроме того, пригоден способ, при котором получают производное бензотриазола и производное восстанавливают борогидридом натрия, как сообщалось в Tetrahedron 47, 2683 (1991), или тому подобное. Альтернативно, соответствующую мочевину получают, как раскрыто на <стадии 1A-3> из соединения (1 с) и сложного эфира, содержащего амин. После гидролиза сложного эфира с помощью оснований, таких как гидроксид лития, гидроксид натрия или гидроксид калия, в водном этаноле амидное производное может быть также получено с помощью конденсирующего агента. В данном случае в качестве растворителя для реакции может быть использован N,N-диметилформамид, тетрагидрофуран или тому подобное и в качестве конденсирующего агента может быть использован 1-этил-3-(3-диметиламинопропил)карбодиимида гидрохлорид, (1H-1,2,3-бензотриазол-1-илокси)(три(диметиламино))фосфония гексафторфосфат. Реакцию можно проводить в течение времени от 10 минут до 30 часов при температуре от 0°С до температуры кипения с обратным холодильником.
Способ получения 1-B
Способ получения соединения (1g), которое представляет собой соединение, представленное формулой (Ia), где Y представляет собой сульфинильную группу или сульфонильную группу
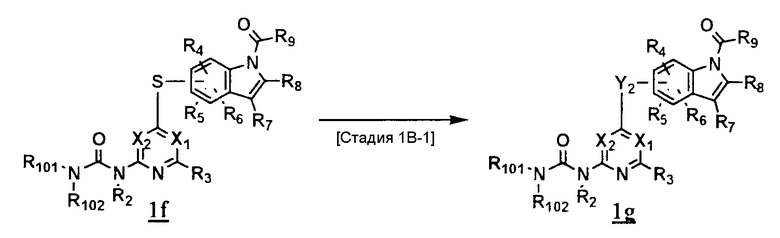
где Y2 представляет собой сульфинильную группу или сульфонильную группу; другие обозначения представляют собой то же самое, что и указанное выше.
<Стадия 1B-1>
Данная стадия представляет собой окисление соединения (1f) до соединения (1g). В качестве окисляющего агента могут быть использованы перекись водорода, надуксусная кислота, метапериодат, 3-хлорнадбензойная кислота или тому подобное. В качестве растворителя могут быть использованы метанол, вода, дихлорметан, хлороформ или тому подобное. Реакцию можно проводить в течение времени от 10 минут до 30 часов при температуре от 0°C до температуры кипения с обратным холодильником.
Способ получения 2
Другой способ получения соединения (2c), которое представляет собой соединение (1c), содержащее атом галогена, формильную группу или цианогруппу в качестве заместителя в положении 3 индольного кольца
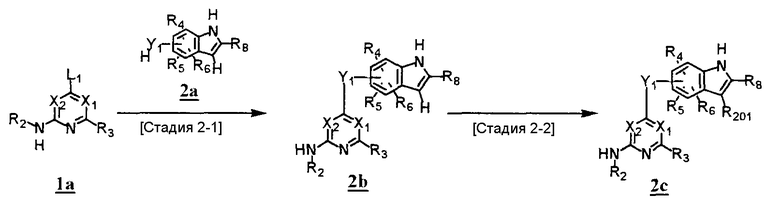
где R201 представляет собой атом галогена, формильную группу или цианогрупу; другие обозначения представляют собой то же самое, что и указанное выше.
<Стадия 2-1>
Данная стадия предназначена для получения соединения (2b) путем конденсации пиримидинового или пиридинового производного (1a) и производного индола (2a), не содержащего заместителя в положении 3. Соединение (2b) может быть получено в тех же условиях, что и на <стадии 1A-1>.
<Стадия 2-2>
Данная стадия предназначена для введения заместителя в положение 3 индола в соединении (2b) с получением соединения, замещенного в положении 3 индола (2c). Соединение (2c), замещенное атомом галогена, формильной группой или аминогруппой, или тому подобное в качестве заместителя в положении 3, может быть получено путем взаимодействия соединения (2b) с галогенизирующими агентами, такими как N-хлорсукцинимид, N-бромсукцинимид или смешанный реагент, состоящий из оксихлоргидрида фосфора или хлорида тионила, с N,N-диметилформамидом, или после превращения соединения в N-хлорсульфонилкарбамоильное производное путем взаимодействия хлорсульфонилизоцианата с соединением с последующим взаимодействием триэтиламина с производным или тому подобное, как сообщалось в Tetrahedron 50, 6549 (1994). В качестве растворителя для реакции может быть использован 2-пропанол, N,N-диметилформамид, тетрагидрофуран, ацетонитрил или тому подобное, и реакцию можно проводить в течение времени от 10 минут до 30 часов при температуре от 0°С до температуры кипения с обратным холодильником.
Способ получения 3
Другой способ получения соединения (1d) через соединения (3c), (3d), (3g) или (3h)
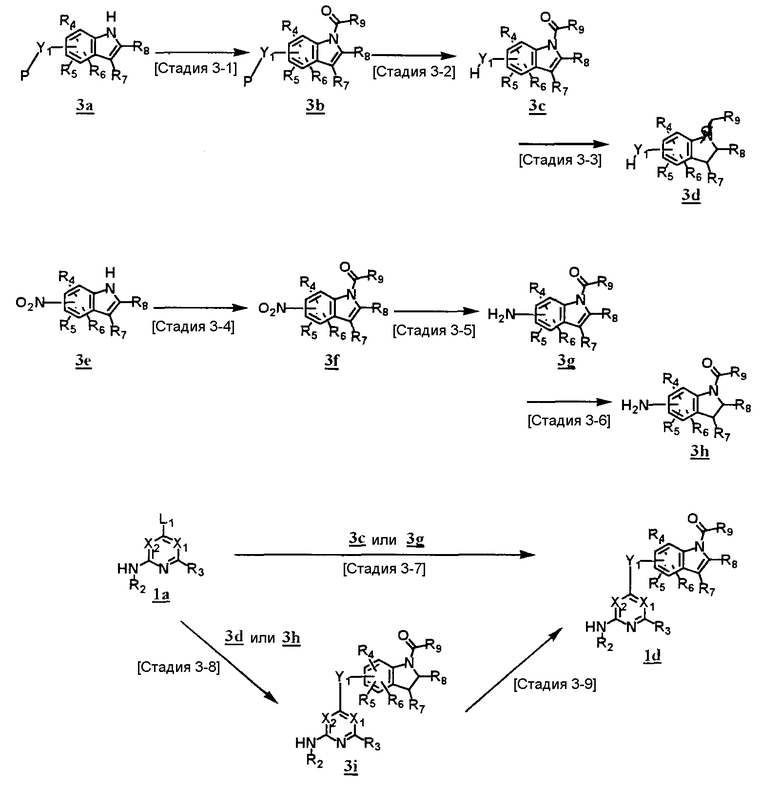
где P представляет собой защитную группу; другие обозначения представляют собой то же самое, что и указанное выше.
<Стадия 3-1> <Стадия 3-2> <Стадия 3-3>
Данные стадии предназначены для получения производного индола (3с) или производного индолина (3d), причем в оба вводят карбоксамидную группу в положение 1 через соединение (3b) из производного индола (3a).
<Стадия 3-1> представляет собой стадию, предназначенную для осуществления карбоксамидирования положения 1 производного индола (3a) с получением соединения (3b), и может быть осуществлена способом, аналогичным<стадии 1A-2>. В качестве защитной группы могут быть использованы, например, метильная группа, бензильная группа, замещенная бензильная группа, бензилоксикарбонильная группа.
<Стадия 3-2> представляет собой стадию, предназначенную для получения соединения (3c) путем снятия защиты производного индола (3b). Конкретно, например, в случае, когда Y1 представляет собой атом кислорода, могут быть использованы способы, обычно применяемые для снятия защиты, такие как деметилирование с помощью боронтрибромида, дебензилирование с помощью смеси трифторуксусная кислота-тиоанизол, дебензилирование или дебензилоксикарбонилирование с помощью каталитического восстановления.
<Стадия 3-3> представляет собой стадию, предназначенную для восстановления производного индола (3c) с получением производного индолина (3d). Может быть применена реакция каталитического гидрирования в присутствии палладиевого катализатора при обычном давлении или при повышенном давлении или тому подобное. В качестве растворителя в реакции может быть использован метанол, N,N-диметилформамид, тетрагидрофуран или тому подобное, и реакцию можно проводить в течение времени от 10 минут до 30 часов при температуре от 0°С до температуры кипения с обратным холодильником.
<Стадия 3-4> <Стадия 3-5> <Стадия 3-6>
Данные стадии предназначены для получения производного аминоиндола (3g) или производного аминоиндолина (3h), содержащего карбоксамидную группу в положении 1, через соединение (3f) из производного нитроиндола (3e).
<Стадия 3-4> представляет собой стадию проведения карбоксамидирования положения 1 производного индола (3e) с получением соединения (3f) и может быть осуществлена аналогично <стадии 1A-2>.
<Стадия 3-5> представляет собой стадию, предназначенную для восстановления производного нитроиндола (3f) до производного аминоиндола (3g). Могут быть использованы обычно применяемые условия для реакции восстановления нитрогруппы до аминогруппы, конкретно, например, восстановление с помощью железо-аммониевого хлорида или железо-уксусной кислоты или тому подобное, каталитическое восстановление с помощью гидроксида палладия-водорода или тому подобное. В качестве растворителя в реакции может быть использован метанол, этанол, вода, N,N-диметилформамид, тетрагидрофуран или тому подобное, и реакцию можно проводить при температуре от комнатной температуры до температуры кипения с обратным холодильником в течение от 10 минут до 30 часов.
<Стадия 3-6> представляет собой стадию, предназначенную для восстановления производного индола (3g) до производного индолина (3h) и может быть осуществлена аналогично <стадии 3-3>.
<Стадия 3-7> <Стадия 3-8>
Данные стадии предназначены для конденсации производного индола (3c или 3g) или производного индолина (3d или 3h) и соединения (1a) с получением производного индола (1d) или производного индолина (3i) и могут быть осуществлены аналогично <стадии 1A-1>.
<Стадия 3-9>
Данная стадия предназначена для окисления производного индолина (3i) до производного индола (1d). Например, в качестве окисляющего агента может быть использован 2,3-дихлор-5,6-дициано-1,4-бензохинон (DDQ) или тому подобное и в качестве растворителя может быть использован 1,4-диоксан, толуол, бензол или тому подобное. Альтернативно, может быть использован способ, в котором в качестве окисляющего агента используется ацетат марганца(III) или тому подобное, как сообщалось в Tetrahedron Lett. 29, 2151 (1988).
Кроме того, в случае, когда Y1 представляет собой формулу -NRY1- и RY1 представляет собой атом водорода в соединениях (3g), (3h), (3c) или (3d), соединение (1d), где Y1 представляет собой формулу -NRY1- и RY1 представляет собой С1-6алкильную группу, также может быть получено путем превращения атома водорода в С1-6алкильную группу путем реакции восстановительного аминирования с альдегидом или кетоном и с использованием их для соответствующих последующих реакций. Кроме того, в случае, когда Y1 представляет собой формулу -NRY1- и RY1 представляет собой атом водорода в соединениях (3i) или (1d), соединения могут быть аналогично превращены в соединения (3i) или (1d), в которых Y1 представляет собой формулу -NRY1- и RY1 представляет собой С1-6алкильную группу. В данном случае в качестве восстанавливающего агента могут быть использованы цианоборогидрид натрия, триметоксиборогидрид натрия, триацетоксиборогидрид натрия или тому подобное, и в качестве растворителя в реакции могут быть использованы метанол, тетрагидрофуран, дихлорметан, дихлорэтан или тому подобное. Кроме того, может быть использован способ, при котором получают производное бензотриазола с его восстановлением борогидридом натрия, как сообщалось в Tetrahedron 47, 2683 (1991), или тому подобное.
Способ получения 4
Другой способ получения соединения (1e)
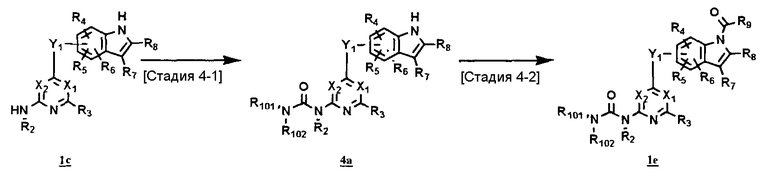
где каждое обозначение определено выше.
<Стадия 4-1>
Данная стадия предназначена для превращения соединения (1c) в соединение (4a) и может быть осуществлена аналогично <стадии 1A-3>.
<Стадия 4-2>
Данная стадия предназначена для проведения карбоксамидирования положения 1 индола в соединении (4a) с получением соединения (1e), и может быть осуществлена аналогично <стадии 1A-2>.
Следует отметить, что, как описано в [способе получения 1-A], превращение заместителя может быть также осуществлено в R2, R9, R101 и R102 путем подходящим образом проводимой реакции окисления, реакции восстановления, реакции восстановительного аминирования, реакции образования сложного эфира, реакции образования амида, реакции введения защитной группы, реакции снятия защиты, реакции гидролиза или тому подобного, которые обычно применяют после данных стадий.
Способ получения 5
Другой способ получения соединения (1e)
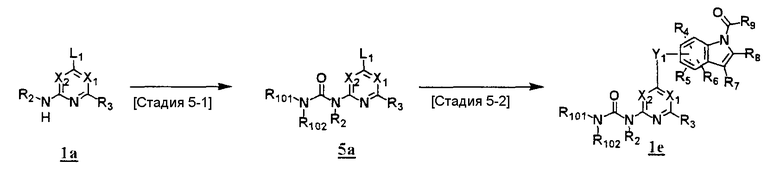
где каждое обозначение определено выше.
<Стадия 5-1>
Данная стадия предназначена для превращения производного пиримидина или пиридина (1a) в соответствующее производное мочевины (5a) и может быть осуществлена аналогично<стадии 1A-3>.
<Стадия 5-2>
Данная стадия предназначена для получения соединения (1e) из производного пиримидина или пиридина (5a), содержащего мочевину. Может быть использован способ, в котором последовательно выполняются те же операции, что и на <стадии 1A-1> и <стадии 1A-2>, способ, в котором последовательно выполняются те же операции, что и на <стадии 2-1>, <стадии 2-2> и <стадии 1A-2>, способ как на <стадии 3-7>, способ, в котором последовательно выполняются те же операции, что и на <стадии 3-8> и <стадии 3-9> или тому подобное.
Следует отметить, что, как описано в [способе получения 1-A], превращение заместителя может быть также осуществлено в R2, R9, R101 и R102 путем подходящим образом проводимой реакции окисления, реакции восстановления, реакции восстановительного аминирования, реакции образования сложного эфира, реакции образования амида, реакции введения защитной группы, реакции снятия защиты, реакции гидролиза или тому подобного, которые обычно применяют после данных стадий.
Способ получения 6
Другой способ получения соединений (1c), (1d), (3i)
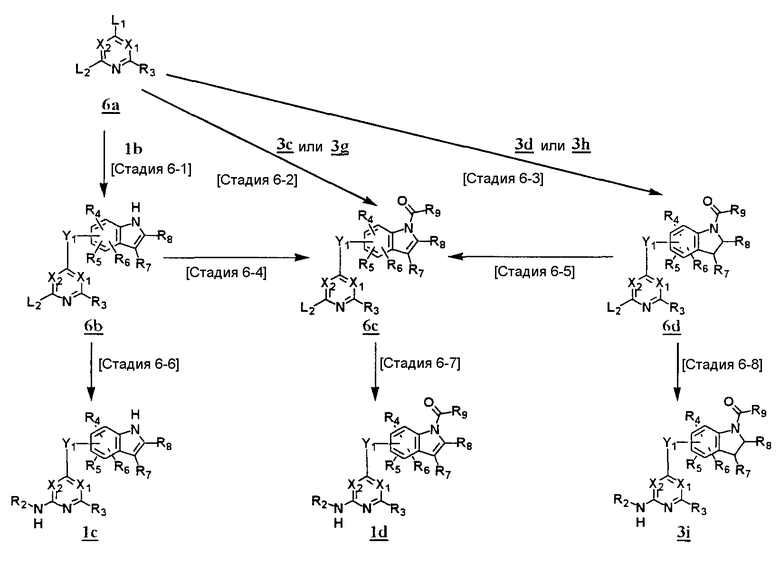
где L2 представляет собой уходящую группу; каждое обозначение определено выше.
<Стадия 6-1> <Стадия 6-2> <Стадия 6-3>
Данные стадии предназначены для конденсации производного пиримидина или пиридина, имеющего уходящие группы L1 и L2, и производного индола или индолина. В данных стадиях предпочтительно, чтобы L1 представлял собой заместитель, имеющий более высокую реакционную способность, чем таковая L2. Конкретно, например, сочетание L1, представляющего собой нитрогруппу, и L2, представляющего собой атом хлора или тому подобное, входит в данную категорию. Используя производное индола (1b), производные индола (3c), (3g), имеющие карбоксамидную группу в положении 1, производные индола (3d), (3h), имеющие карбоксамидную группу в положении 1, может быть получено каждое из соединений (6b), (6c) и (6d) с применением тех же условий, что и на <стадии 1A-1>.
<Стадия 6-4>
Данная стадия предназначена для проведения карбоксамидирования в положении 1 индола в соединении (6b) для получения соединения (6c) и может быть осуществлена аналогично<стадии 1A-2>.
<Стадия 6-5>
Данная стадия предназначена для окисления производного индола (6d) до производного индола (6c). Может быть использован тот же способ, что и на <стадии 3-9>.
<Стадия 6-6> <Стадия 6-7> <Стадия 6-8>
Это стадии, в которых уходящую группу L2 производных пиримидина или пиридина (6b), (6c) или (6d) превращают в группу, представленную формулой -NHR2, где R2 определен выше, для получения соединений (1c), (1d) или (3i) соответственно. Например, применяют аммиачно-этаноловый раствор или соответствующий первичный амин и реакцию осуществляют в запаянной пробирке в течение от 10 минут до 100 часов при температуре от 60°C до температуры кипения с обратным холодильником.
Способ получения 7
Другой способ получения соединения (7j), которое представляет собой соединение, представленное формулой (Ia), где Y представляет собой атом кислорода и в обоих положениях 2 и 3 индола (R8, R7) находятся атомы водорода.
Способ получения 7a
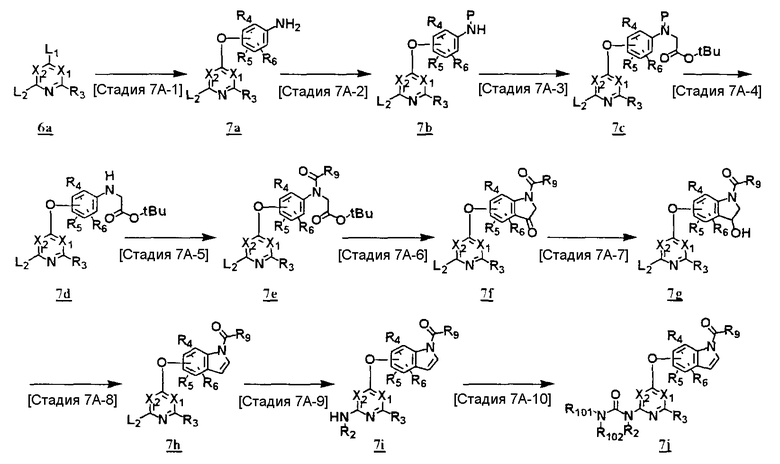
где каждое обозначение определено выше.
<Стадия 7A-1>
Данная стадия предназначена для получения соединения (7a) путем введения аминофеноксигруппы в соединение (6a). Предпочтительно, чтобы в соединении (6a) L1 представлял собой заместитель, имеющий более высокую реакционную способность, чем таковая L2. Конкретно, например, сочетание L1, представляющего собой нитрогруппу, и L2, представляющего собой атом хлора, входит в данную категорию. Соединение (7a) может быть получено с использованием соединения (6a) и производного аминофенола аналогично <стадии 1A-1>. Кроме того, далее данные соединения подвергают конденсации, используя производное нитрофенола способом, аналогичным способу на <стадии 1A-1>, с последующим восстановлением нитрогруппы с помощью реакции каталитического гидрирования в присутствии палладиевого катализатора или тому подобное или реакции восстановления металла с использованием железо-аммониевого хлорида, железо-уксусной кислоты или тому подобное. В качестве растворителя для реакции восстановления нитрогруппы может быть использован метанол, этанол, тетрагидрофуран, N,N-диметилформамид или тому подобное, и реакцию каталитического гидрирования можно проводить при нормальном давлении или при повышенном давлении. Реакцию можно проводить при температуре от комнатной температуры до температуры кипения с обратным холодильником в течение от 10 минут до 30 часов.
<Стадия 7A-2>
Данная стадия предназначена для защиты аминогруппы соединения (7a) с получением соединения (7b). В качестве защитной группы может быть введена, например, бензилоксикарбонильная группа или тому подобное с использованием соответствующего хлоркарбонатного эфира.
<Стадия 7A-3>
Это способ получения соединения (7c) из соединения (7b). Могут быть использованы трет-бутилбромацетат в качестве реагента, гидрид натрия или тому подобное в качестве основания, N,N-диметилформамид, тетрагидрофуран, диметилсульфоксид или тому подобное в качестве растворителя для реакции. Реакцию можно проводить при температуре от комнатной температуры до температуры кипения с обратным холодильником в течение от 10 минут до 30 часов.
<Стадия 7A-4>
Данная стадия предназначена для снятия защиты аминогруппы соединения (7c) с получением соединения (7d). Следует отметить, что, например, может быть применена реакция снятия защиты путем реакции каталитического гидрирования бензилоксикарбонильной группы или тому подобное.
<Стадия 7A-5>
Данная стадия предназначена для получения соединения (7e) путем введения карбоксамидной группы в соединение (7d). В качестве реагента может быть использовано изоцианатное производное, карбаматное производное или тому подобное. В качестве растворителя для реакции может быть использован N,N-диметилформамид, тетрагидрофуран, диметилсульфоксид, толуол или тому подобное, и туда могут быть добавлены органические основания, такие как триэтиламин или пиридин, сколько требуется. Реакцию можно проводить в течение от 10 минут до 30 часов при температуре от 0°С до температуры кипения с обратным холодильником.
<Стадия 7A-6>
Данная стадия предназначена для получения соединения (7f) из соединения (7e) с помощью реакции циклизации. Реакцию осуществляют в кислых условиях, конкретно, например, в смеси трифторуксусная кислота-трифторуксусный ангидрид или тому подобное. Реакцию можно проводить в течение от 10 минут до 30 часов при температуре от 0°С до температуры кипения с обратным холодильником.
<Стадия 7A-7> <Стадия 7A-8>
Данные стадии служат для превращения производного оксоиндолина (7f) в производное индола (7h) через соединение (7g). Производное 3-гидроксииндолина (7g) получают путем восстановления карбонильной группы с использованием борогидрида натрия в качестве реагента в тетрагидрофуране, метаноле, этаноле или тому подобном в качестве растворителя для реакции, после этого соединение (7h) может быть получено путем осуществления дегидрирования с использованием камфорсульфокислоты или тому подобного в качестве реагента и толуола, дихлорэтана или тому подобного в качестве растворителя для реакции.
<Стадия 7A-9> <Стадия 7A-10>
Далее проводят стадию, в которой соединение (7j) получают в тех же условиях в каждой из<стадии 6-6>, <стадии 1A-3>
Способ получения 7-B
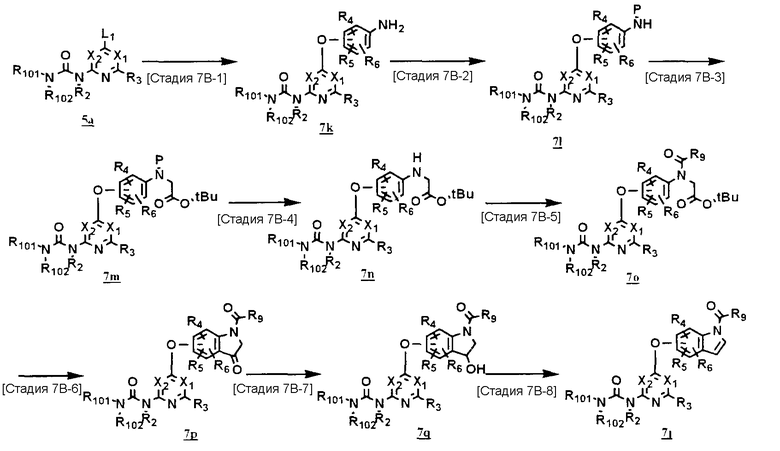
где каждое обозначение определено выше.
<Стадия 7B-1>
Данная стадия предназначена для получения соединения (7k) из соединения (5a) и она может быть осуществлена аналогично <стадии 7A-1>.
<Стадия 7B-2>
Данная стадия предназначена для защиты аминогруппы соединения (7k) для получения соединения (7l) и она может быть осуществлена аналогично<стадии 7A-2>.
<Стадия 7B-3>
Это способ получения соединения (7m) из соединения (7l) и он может быть осуществлен аналогично <стадии 7A-3>.
<Стадия 7B-4>
Данная стадия предназначена для снятия защиты у соединения (7m) для получения соединения (7n) и она может быть осуществлена аналогично <стадии 7A-4>.
<Стадия 7B-5>
Данная стадия предназначена для введения карбоксамидной группы в соединение (7n) для получения соединения (7o) и она может быть осуществлена аналогично <стадии 7A-5>.
<Стадия 7B-6>
Данная стадия предназначена для получения циклического соединения (7p) из соединения (7o) и она может быть осуществлена аналогично <стадии 7A-6>.
<Стадия 7B-7> <Стадия 7B-8>
Данные стадии предназначены для превращения в производное индола (7j) через соединение (7g) из производного 3-оксоиндолина (7p) и они могут быть осуществлены аналогично <стадии 7A-7> <стадии 7A-8>.
Способ получения 8
Другой способ получения соединения (8g), которое представляет собой соединение, представленное формулой (Ia), где в обоих положениях 2 и 3 индола (R8, R7) находятся атомы водорода.
Способ получения 8a
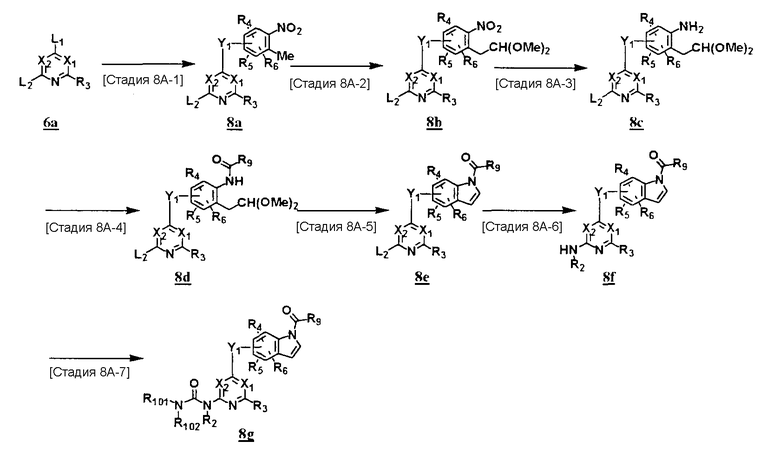
где каждое обозначение определено выше.
<Стадия 8A-1>
Это реакция присоединения соединения (6a) к производному нитробензола. Соединение (8a) может быть получено в тех же условиях, что и на <стадии 1A-1>.
<Стадия 8A-2>
Данная стадия предназначена для получения соединения (8b) из соединения (8a). Реакция может быть проведена в условиях, описанных в Tetrahedron Lett. 39, 71 (1998). Конкретно, диметилацетатное соединение может быть дериватизировано путем конденсации производного нитротолуола и диметилацеталя диметилформамида в N,N-диметилформамиде при температуре от комнатной температуры до температуры кипения с обратным холодильником в течение от 10 минут до 30 часов и путем последующего осуществления реакции соединения в метаноле в кислых условиях при температуре от комнатной температуры до температуры кипения с обратным холодильником в течение от 10 минут до 30 часов.
<Стадия 8A-3>
Данная стадия предназначена для восстановления соединения (8b) до соединения (8c). Может быть использовано восстановление с помощью железо-аммониевого хлорида или железо-уксусной кислоты или тому подобного. В качестве растворителя для реакции может быть использован метанол, этанол, тетрагидрофуран, N,N-диметилформамид или тому подобное. Реакцию можно проводить при температуре от комнатной температуры до температуры кипения с обратным холодильником в течение от 10 минут до 30 часов.
<Стадия 8A-4>
Данная стадия предназначена для превращения соединения (8c) в производное мочевины для получения соединения (8d) и может быть проведена тем же образом, что и <стадия 7A-5>. Альтернативно, в качестве растворителя реакции используют тетрагидрофуран или N,N-диметилформамид, например, после получения карбаматного производного с использованием фенилхлоркарбоната или тому подобного, и мочевина также может быть введена путем взаимодействия производного с амином при температуре от комнатной температуры до температуры кипения с обратным холодильником в течение от 10 минут до 30 часов, при этом в качестве растворителя применяют N,N-диметилформамид, диметилсульфоксид.
<Стадия 8A-5>
Данная стадия предназначена для циклизации соединения (8d) с получением соединения (8e). Реакция может быть проведена при условиях, описанных в Tetrahedron Lett. 39, 71 (1998). Конкретно, может быть упомянут способ, при котором кипячение с обратным холодильником проводят в растворителях, таких как бензол, в присутствии каталитических количеств камфорсульфокислоты и хинолина.
<Стадия 8A-6>
Данная стадия предназначена для получения соединения (8f) из соединения (8e) и может быть проведена аналогично <стадии 6-6>.
<Стадия 8A-7>
Данная стадия предназначена для получения соединения (8g) из соединения (8f) и может быть проведена аналогично <стадии 7A-10>.
Способ получения 8-B
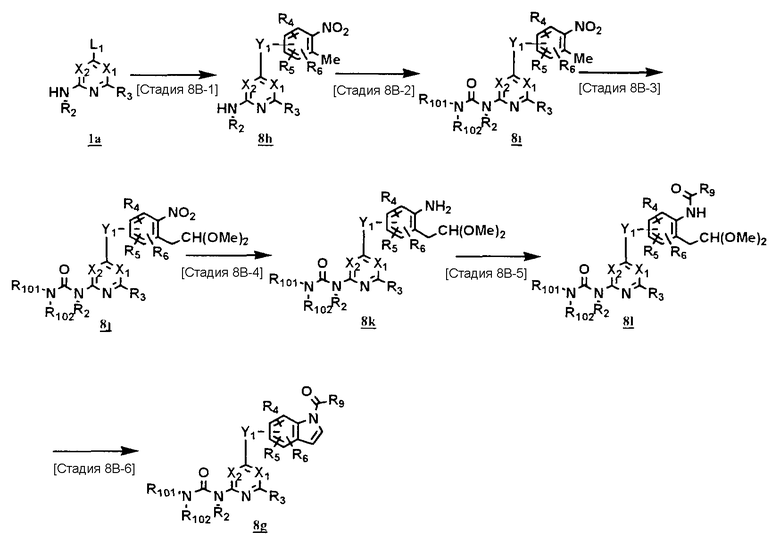
где каждое обозначение определено выше.
<Стадия 8B-1>
Данная стадия предназначена для получения соединения (8h) путем проведения реакции присоединения соединения (1a) к производному нитробензола и может быть проведена аналогично<стадии 1A-1>.
<Стадия 8B-2>
Данная стадия предназначена для введения мочевины в соединение (8h) с получением соединения (8i) и может быть проведена аналогично <стадии 1A-3>.
<Стадия 8B-3>
Данная стадия предназначена для конденсации производного нитротолуола (8i) и диметилацеталя диметилформамида последовательно с превращением соединения в диметилацетальное соединение (8j). Стадия может быть проведена аналогично <стадии 8A-2>.
<Стадия 8B-4>
Данная стадия предназначена для восстановления нитрогруппы соединения (8j) с получением соединения (8k) и может быть проведена аналогично <стадии 8A-3>.
<Стадия 8B-5>
Данная стадия предназначена для получения соединения (8l) из соединения (8k) путем введения мочевины и может быть проведена аналогично <стадии 8A-4>.
<Стадия 8B-6>
Данная стадия предназначена для циклизации соединения (8l) с получением соединения (8g) и может быть проведена аналогично <стадии 8A-5>.
Способ получения 9
Другой способ получения соединения (7j)
Способ получения 9-A
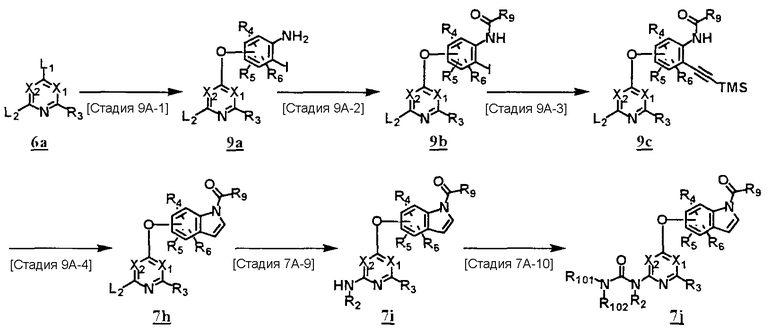
где каждое обозначение определено выше.
<Стадия 9A-1>
Данная стадия предназначена для получения соединения (9a) путем присоединения соединения (6a) к производному фенола. Конкретно, например, соответствующее конденсированное соединение может быть получено при тех же условиях, что и на <стадии 1A-1>, с использованием 4-амино-3-иодфенола, полученного из трет-бутил (2-иод-4-((триизопропилсилил)окси)фенил)карбамата, полученного способом, описанным в J. Org. Chem., 62, 6507 (1997), путем взаимодействия с ним фторида н-бутиламмония или тому подобного.
<Стадия 9A-2>
Данная стадия предназначена для превращения соединения (9a) в производное мочевины с получением соединения (9b) и может быть проведена аналогично <стадии 8A-4>.
<Стадия 9A-3>
Данная стадия предназначена для получения ацетиленового производного (9c) из иодсодержащего соединения (9b) с использованием триметилсилилацетилена. Конденсация может быть проведена в присутствии тетракис(трифенилфосфин)палладия или дихлорбис(трифенилфосфин)палладия, иодида меди. В качестве растворителя реакции может быть использован N,N-диметилформамид или тому подобное, и реакцию можно проводить при температуре от комнатной температуры до температуры кипения с обратным холодильником в течение от 10 минут до 30 часов.
<Стадия 9A-4>
Данная стадия предназначена для проведения циклизации путем нагревания ацетиленового производного (9c) в присутствии иодида меди с получением производного индола (7h). В качестве растворителя реакции может быть использован N,N-диметилформамид или тому подобное, и реакцию можно проводить при температуре от 80°С до температуры кипения с обратным холодильником в течение от 5 минут до 10 часов.
Затем соединение (7h) может быть превращено в соединение (7j), как описано в <стадии 7A-9>, <стадии 7A-10>.
Способ получения 9-B
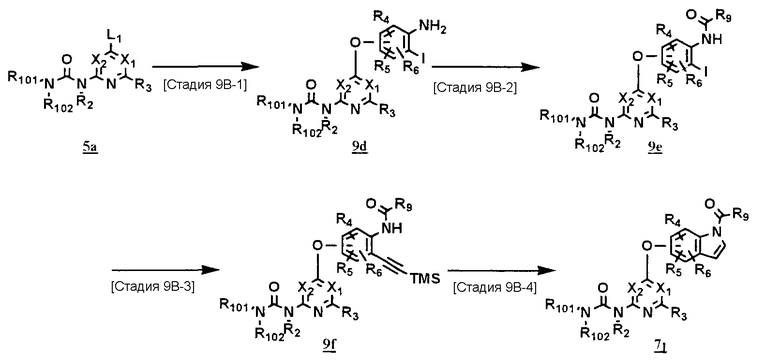
где каждое обозначение определено выше.
<Стадия 9B-1>
Данная стадия предназначена для присоединения соединения (5a) к производному фенола с получением соединения (9d) и может быть проведена аналогично <стадии 9A-1>.
<Стадия 9B-2>
Данная стадия предназначена для превращения соединения (9d) в производное мочевины с получением соединения (9e) и может быть проведена аналогично <стадии 7A-5>.
<Стадия 9B-3>
Данная стадия предназначена для получения ацетиленового производного (9f) из иодсодержащего соединения (9e) с использованием триметилсилилацетилена и может быть проведена аналогично <стадии 9A-3>.
<Стадия 9B-4>
Данная стадия предназначена для циклизации ацетиленового производного (9f) путем нагревания в присутствии иодида меди с получением производного индола (7j). Могут быть применены те же условия, что на <стадии 9A-4>.
Способ получения 10
Типичный способ получения соединения (10g), которое является соединением, представленным формулой (Ia), где Y представляет собой атом кислорода, атом серы или группу, представленную формулой -NRY- (где RY представляет собой атом водорода или С1-6алкильную группу), X1 представляет собой группу, представленную формулой -C(CN)=, X2 представляет собой группу, представленную формулой -CH=, R2 представляет собой атом водорода, R3 представляет собой атом водорода, необязательно замещенный С1-6алкильной группой или необязательно замещенный С3-8циклоалкильной группой.
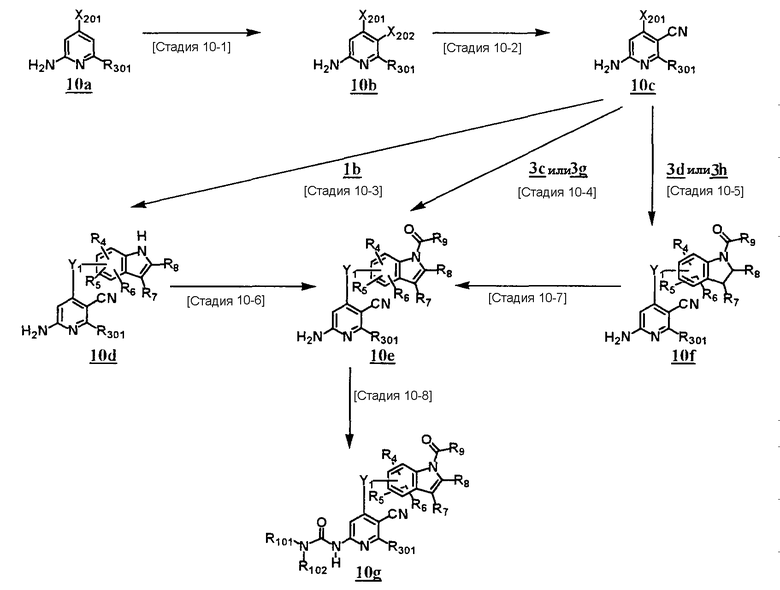
где X201 представляет собой атом хлора или атом брома, X202 представляет собой атом брома или атом иода; R301 представляет собой атом водорода, необязательно замещенный С1-6алкильной группой или необязательно замещенный С3-8циклоалкильной группой; предпочтительно, чтобы в сочетании X201 и X202 X202 представлял собой атом иода или атом брома, если X201 представляет собой атом хлора, X202 представлял собой атом иода, если X201 представляет собой атом брома; другие обозначения определены выше.
<Стадия 10-1>
Данная стадия предназначена для бромирования или иодирования положения 5 2-аминопиридинового производного (10a), содержащего атом хлора или атом брома в положении 4, с получением соединения (10b). Например, могут быть использованы галогенизирующие агенты, такие как иод, N-бромсукцинимид, бром, N-иодсукцинимид. В качестве растворителя для реакции может быть использован, например, N,N-диметилформамид, диметилсульфоксид, метиленхлорид и ацетонитрил. Реакцию можно проводить при температуре от 0°С до температуры кипения с обратным холодильником в течение от 10 минут до 48 часов.
<Стадия 10-2>
Данная стадия предназначена для превращения X202 соединения (10b) в цианогруппу с получением соединения (10c).
Например, от 0,5 до 0,6 эквивалентов цианида цинка, от 1,0 до 1,2 эквивалентов цианида калия или триметилсилилцианида вводят в реакцию с соединением (10b) в присутствии палладиевого катализатора, такого как тетракис(трифенилфосфин)палладий или дихлорбис(трифенилфосфин)палладий. В качестве растворителя для реакции может быть использован, например, N,N-диметилформамид, диоксан и тетрагидрофуран. Реакцию можно проводить при температуре от комнатной температуры до температуры кипения с обратным холодильником в течение от 10 минут до 10 часов.
<Стадия 10-3> <Стадия 10-4> <Стадия 10-5>
Данные стадии предназначены для конденсации пиридинового производного (10c) и производного индола или индолина. Соединения (10d), (10e) и (10f) могут быть получены соответственно при использовании производного индола (1b), производных индола (3c), (3g), содержащих карбоксамидную группу в положении 1, и производных индолина (3d), (3h), содержащих карбоксамидную группу в положении 1, при тех же условиях, что и на <стадии 1A-1>.
<Стадия 10-6>
Данная стадия предназначена для проведения карбоксамидирования положения 1 индола соединения (10d) с получением соединения (10e) и может быть проведена аналогично <стадии 1A-2>.
<Стадия 10-7>
Данная стадия предназначена для окисления производного индолина (10f) до производного индола (10e) и может быть проведена аналогично <стадии 3-9>.
<Стадия 10-8>
Данная стадия предназначена для превращения соединения (10e) в соединение (10g) и может быть проведена аналогично <стадии 1A-3>.
Способ получения 11
Другой способ получения соединения (10g)
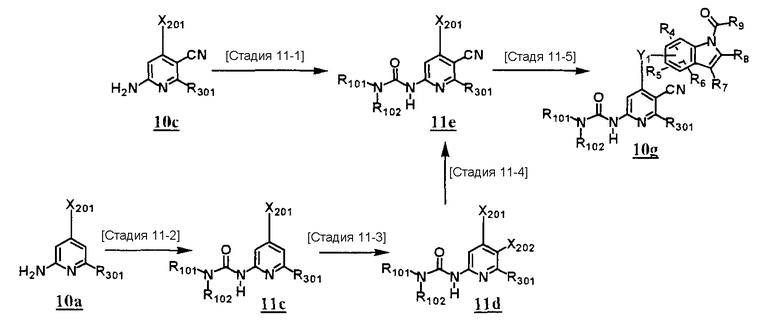
где каждое обозначение определено выше.
<Стадия 11-1> <Стадия 11-2>
Данные стадии предназначены для превращения аминопиридиновых производных (10c), (10a) в соответствующие производные мочевины (11e), (11c) соответственно и могут быть проведены аналогично <стадии 1A-3>.
<Стадия 11-3>
Данная стадия предназначена для иодирования или бромирования положения 5 2-уреидопиридинового производного (11c) содержащего атом хлора или атом брома в положении 4, с получением соединения (11d) и может быть проведена аналогично <стадии 10-1>.
<Стадия 11-4>
Данная стадия предназначена для превращения X202 соединения (11d) в цианогруппу с получением соединения (11e) и может быть проведена аналогично <стадии 10-2>.
<Стадия 11-5>
Данная стадия предназначена для получения соединения (10g) из пиридинового производного (11e), содержащего мочевину, и может быть проведена аналогично <стадии 5-2>.
Способ получения 12
Способ получения соединения (12b), которое является соединением, представленным формулой (Ia), где Y представляет собой сульфинильную группу или сульфонильную группу, X1 представляет собой группу, представленную формулой -C(CN)=, и R2 представляет собой атом водорода
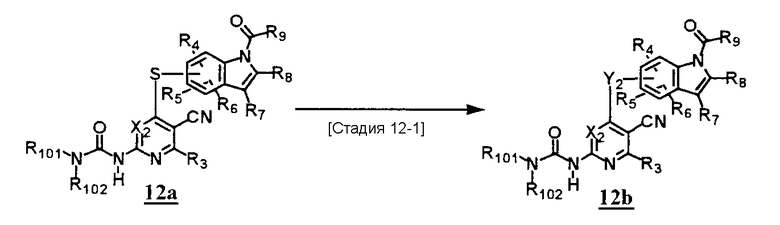
где другие обозначения определены выше.
<Стадия 12-1>
Данная стадия предназначена для окисления соединения (12a) до соединения (12b) и может быть проведена аналогично <стадии 1B-1>.
Способ получения 13
Способ получения соединения (13l), которое является соединением, представленным формулой (Ia), где Y представляет атом кислорода, атом серы или формулу -NRY- (где RY представляет собой водород или алкильную группу от C1 до С6) и X1 представляет собой группу, представленную формулой -C(CN)=
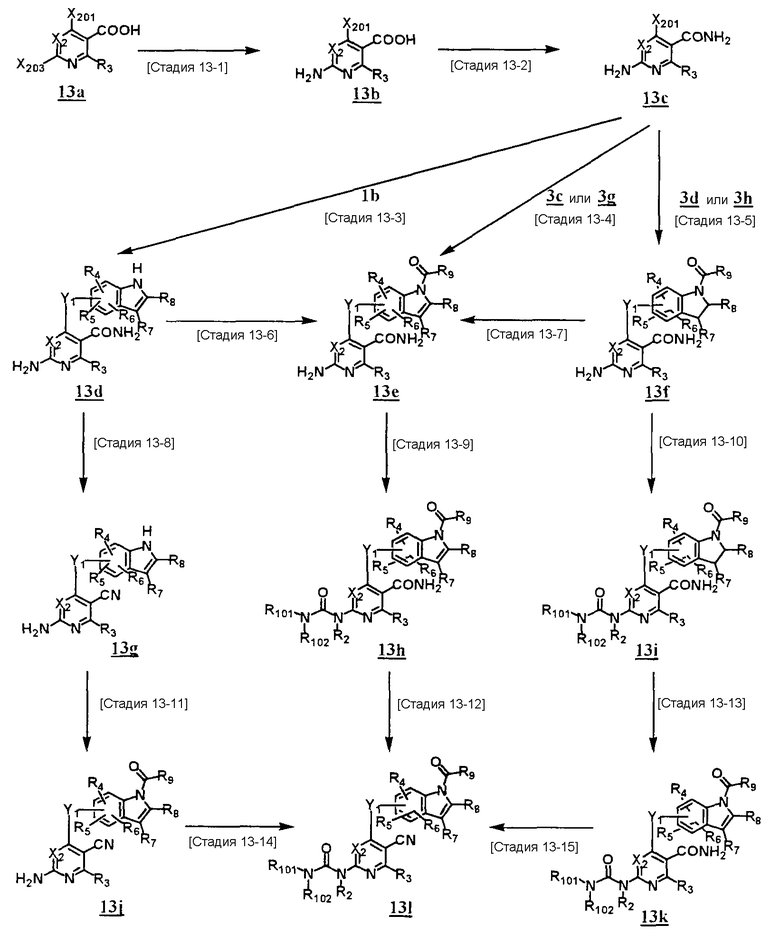
где X203 представляет собой атом хлора, атом брома или атом иода; другие обозначения определены выше.
<Стадия 13-1>
Данная стадия предназначена для превращения X203 4,6-дигалогенизированной никотиновой кислоты или ее аналогичного соединения (13a), такого как 4,6-дихлорникотиновая кислота, как сообщалось в Acad. Nauk Ukr. SSSR, 1986, page 36, в аминогруппу с получением соединения (13b). Реакцию можно проводить при температуре от 0°C до температуры кипения с обратным холодильником в течение от 10 минут до 100 часов c использованием, например, раствора аммиак-этанол или тому подобного.
<Стадия 13-2>
Данная стадия предназначена для получения соединения (13c) путем превращения карбоксильной группы соединения (13b) в карбамоильную группу. Например, может быть использован способ, при котором после взаимодействия оксалилхлорида или тионилхлорида с соединением при температуре от 0°С до температуры кипения с обратным холодильником в течение от 10 минут до 24 часов соединение вводят во взаимодействие с аммиаком, или способ, при котором используют диэтилцианофосфат, хлорид аммония, триэтиламин, как раскрыто в Synthesis [SYNTBF], 1998, 1467-1475 или тому подобное.
<Стадия 13-3> <Стадия 13-4> <Стадия 13-5>
Данные стадии предназначены для конденсации пиридинового или пиримидинового производного (13c) и производного индола или индолина. Соединения (13d), (13e), (13f) могут быть получены соответственно при использовании производного индола (1b), производных индола (3c), (3g), содержащих карбоксамидную группу в положении 1, или производных индолина (3d), (3h), содержащих карбоксамидную группу в положении 1, при тех же условиях, что и на <стадии 1A-1>.
<Стадия 13-6> <Стадия 13-11>
Данные стадии предназначены для проведения карбоксамидирования положения 1 индола соединений (13d), (13g) с получением соединения (13e), (13j) и могут быть осуществлены аналогично <стадии 1A-2>.
<Стадия 13-8> <Стадия 13-12> <Стадия 13-15>
Данные стадии предназначены для превращения карбамоильной группы соединений (13d), (13h), (13k) в цианогруппу с получением соединений (13g), (13l). Например, может быть использован способ, при котором оксихлорид фосфора, тионилхлорид, ангидрид трифторуксусной кислоты вводят во взаимодействие с соединениями при температуре от 0°С до температуры кипения с обратным холодильником в течение от 10 минут до 24 часов.
<Стадия 13-9> <Стадия 13-10> <Стадия 13-14>
Данные стадии предназначены для превращения аминопиридиновых или аминопиримидиновых производных (13e), (13f), (13j) в соответствующие производные мочевины (13h), (13i), (13l) и могут быть проведены аналогично <стадии 1A-3>.
<Стадия 13-7> <Стадия 13-13>
Данные стадии предназначены для окисления производных индолина (13f), (13i) с получением производных индола (13e), (13k) и могут быть проведены аналогично <стадии 3-9>.
Способ получения 14
Типичный способ получения соединений (14d), (14e), (14f) путем галогенизации соединений (14a), (14b), (14c)
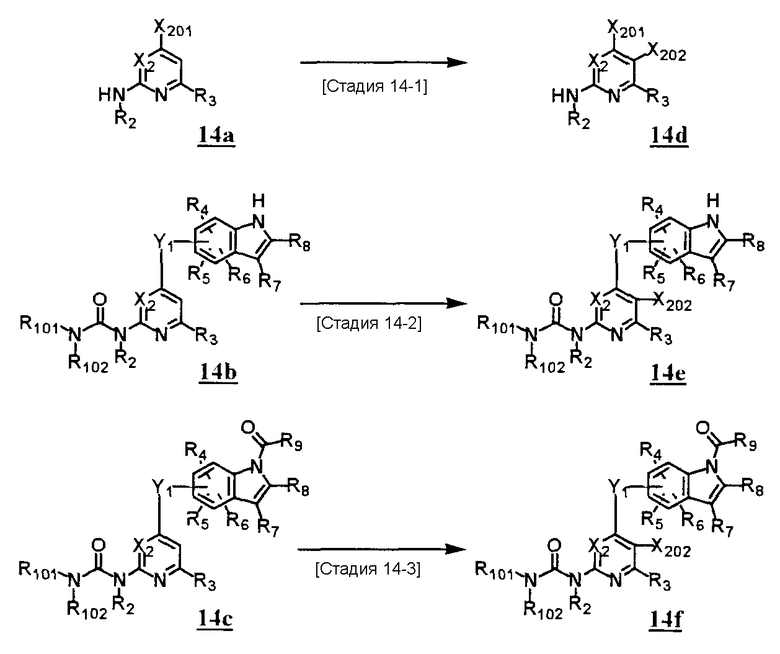
где каждое обозначение определено выше.
<Стадия 14-1> <Стадия 14-2> <Стадия 14-3>
Данные стадии предназначены для замещения заместителя в 6-членном гетероцикле атома водорода на атом галогена. Соединение может быть получено из соответствующего соединения: соединение (14d) из соединения (14a), соединение (14e) из соединения (14b) и соединение (14f) из соединения (14c), как на <стадии 10-1>.
Способ получения 15
Типичный способ получения соединений (15a), (15b), (15c) путем замещения атома галогена в 6-членном гетероцикле соединений (14d), (14e), (14f) цианогруппой
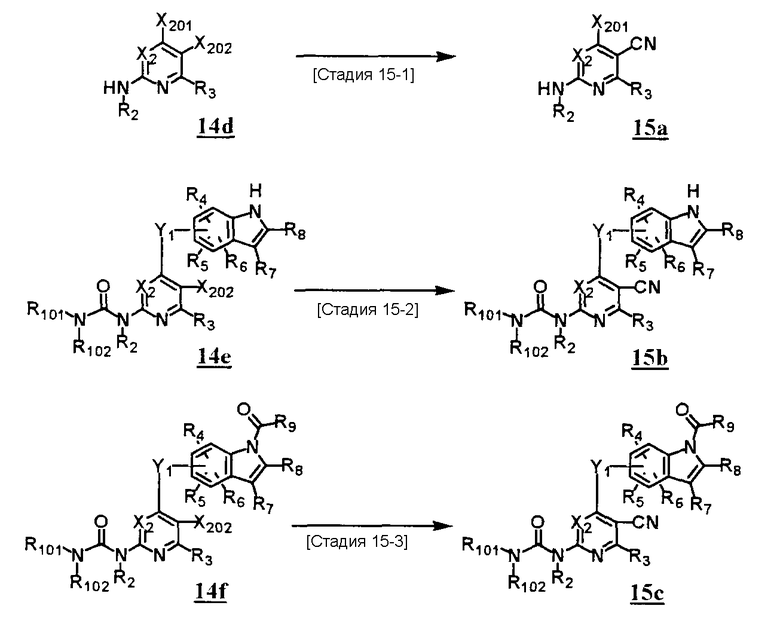
где каждое обозначение определено выше.
<Стадия 15-1> <Стадия 15-2> <Стадия 15-3>
Данные стадии предназначены для получения соединения из соответствующего соединения: соединения (15a) из соединения (14d), соединения (15b) из соединения (14e) и соединения (15c) из соединения (14f) путем замены заместителя в 6-членном гетероцикле вместо атома галогена цианогруппой. Может быть использовано от 0,5 до 2,0 эквивалентов цианида цинка или от 1,0 до 3,0 эквивалентов цианида меди(I), цианида калия, цианида натрия, триметилсилилцианида или тому подобного для соединений (14d), (14e) и (14f). Для ускорения реакции в качестве катализатора может быть использован, например, палладиевый катализатор, такой как тетракис(трифенилфосфин)палладий или дихлорбис(трифенилфосфин)палладий, иодид меди(I), медь(0) или тому подобное. В качестве растворителя для реакции может быть использован, например, N,N-диметилформамид, N-метилпирролидон, диметилсульфоксид, диоксан, тетрагидрофуран или тому подобное. Реакцию можно проводить при температуре от комнатной температуры до температуры кипения с обратным холодильником в течение от 10 минут до 2 дней.
После завершения указанных выше реакций полученные соединения могут быть подвергнуты очистке с помощью традиционного способа обработки, например колоночной хроматографии с использованием силикагеля или адсорбирующих смол или тому подобного, или перекристаллизации из подходящего растворителя.
Соединения изобретения, их соли или гидраты могут входить в состав рецептур в виде таблеток, порошков, тонко измельченных частиц, гранул, таблеток, покрытых оболочкой, капсул, сиропов, пастилок, ингалируемых агентов, суппозиториев, агентов для инъекций, мазей, мазей для глаз, глазных капель, капель в нос, ушных капель, паст, лосьонов и тому подобного, с помощью обычных способов. В составе могут быть использованы любые обычно применяемые наполнители, связующие агенты, смазывающие агенты, окрашивающие агенты, агенты, корректирующие покрытие, и, если это необходимо, стабилизаторы, эмульгаторы, усилители поглощения, поверхностно-активные вещества, агенты, доводящие рН, консерванты, антиоксиданты или тому подобное, в сочетании с различными компонентами, которые обычно применяются в качестве сырьевых материалов для фармацевтических составов. Например, пероральный состав может быть приготовлен путем объединения соединения изобретения или его фармацевтически приемлемой соли с носителем, если это необходимо, с добавлением связующего агента, разрыхляющего агента, смазывающего агента, окрашивающего агента, агента, корректирующего покрытие, или тому подобного, и составления порошка, тонко измельченных частиц, гранул, таблеток, таблеток, покрытых оболочкой, капсул и т.п.с помощью обычного способа. Могут быть отмечены такие компоненты, как животные и растительные масла, такие как соевое масло, говяжий жир и синтетические глицериды; углеводороды, такие как жидкий парафин, сквалан и твердый парафин; сложноэфирные масла, такие как октилдодецилмиристат и изопропилмиристат; высшие спирты, такие как цетостеариловый спирт и бегениловый спирт; кремнийорганические смолы; кремнийорганические масла; поверхностно-активные вещества, такие как сложные эфиры полиоксиэтилена и жирных кислот, сложные эфиры сорбитана и жирных кислот, сложные эфиры глицерина и жирных кислот, сложные эфиры полиоксиэтиленсорбитана и жирных кислот, полиоксиэтиленовое гидрогенизированное касторовое масло и полиоксиэтилен-полиоксипропилен блок-сополимер; растворимые в воде полимеры, такие как гидроксиэтилцеллюлоза, полиакриловая кислота, карбоксивиниловый полимер, полиэтиленгликоль, поливинилпирролидон и метилцеллюлоза; низшие спирты, такие как этанол и изопропанол; многоатомные спирты, такие как глицерин, пропиленгликоль, дипропиленгликоль и сорбит; сахара, такие как глюкоза и сахароза; неорганические порошки, такие как кремниевый ангидрид, силикат магния-алюминия и силикат алюминия, очищенная вода и тому подобное. Примеры наполнителей, которые могут быть использованы, включают лактозу, кукурузный крахмал, белый мягкий сахар, глюкозу, маннит, сорбит, кристаллическую целлюлозу и диоксид кремния, примеры связующих агентов, которые могут быть использованы, включают поливиниловый спирт, поливиниловый эфир, метилцеллюлозу, этилцеллюлозу, аравийскую камедь, трагакант, желатин, шеллак, гидроксипропилметилцеллюлозу, гидроксипропилцеллюлозу, поливинилпирролидон, полипропиленгликоль-полиоксиэтилен блок-сополимер и меглумин, примеры разрыхляющих агентов, которые могут быть использованы, включают крахмал, агар, желатиновый порошок, кристаллическую целлюлозу, карбонат кальция, бикарбонат натрия, цитрат кальция, декстрин, пектин и кальциевую соль карбоксиметилцеллюлозы, примеры смазывающих агентов, которые могут быть использованы, включают стеарат магния, тальк, полиэтиленгликоль, диоксид кремния и гидрогенизированные растительные масла, примеры окрашивающих агентов, которые могут быть использованы, включают те, которые разрешены для лекарств, и примеры агентов, корректирующих покрытие, которые могут быть использованы, включают порошок какао, ментол, ароматические порошки, мятное масло, борнеол и порошковую корицу. Таблетки или гранулы могут быть также покрыты сахарозой или обеспечены другим типом подходящего покрытия, если это необходимо. Для получения жидкого состава, такого как сироп или состав для инъекций, может быть использован обычный способ получения состава соединения изобретения или его фармацевтически приемлемой соли с агентом, доводящим рН, солюбилизатором, агентом, придающим изотоничность, или тому подобным, а также агентом для поддержания растворимости, стабилизатором и т.д., если необходимо. Не существует особых ограничений способа получения внешнего агента, и может быть использован любой способ. Это значит, что он может быть получен с использованием в качестве основных материалов любых из различных сырых материалов, которые обычно применяют в лекарствах, квазилекарствах, косметике и тому подобном. В качестве примеров конкретных основных материалов здесь могут быть отмечены такие сырые материалы, как животные и растительные масла, минеральные масла, сложноэфирные масла, парафины, высшие спирты, жирные кислоты, силиконовые масла, поверхностно-активные вещества, фосфолипиды, спирты, многоатомные спирты, водорастворимые полимеры, глинистые минералы, очищенная вода и тому подобное, и, если это необходимо, могут быть также добавлены агенты, доводящие рН, антиоксиданты, хелатирующие агенты, антисептики и фунгициды, окрашивающие агенты, ароматизаторы и тому подобное, хотя основные материалы для внешних агентов по изобретению не ограничиваются этим. Если необходимо, туда могут быть также включены такие компоненты, как ингредиенты, обладающие активностью, индуцирующей дифференциацию, усилители циркуляции, бактерициды, противовоспалительные агенты, активаторы клеток, витамины, аминокислоты, увлажнители, кератолитические агенты и тому подобное. Количества указанных выше основных материалов могут составлять концентрации, установленные для получения обычных внешних агентов.
При введении не существует особых ограничений на соединение изобретения, его соль или его гидрат, и может быть осуществлено либо пероральное, либо парентеральное введение в соответствии с обычными способами. Например, оно может быть изготовлено и введено в форме таблетки, порошка, гранулы, капсулы, сиропа, пастилки, средства для ингаляции, суппозитория, агента для инъекции, мази, мази для глаз, глазных капель, капель в нос, ушных капель, паст, лосьона или тому подобного.
Хотя дозировка лекарства по изобретению должна различаться в зависимости от тяжести симптомов, возраста, пола, массы тела, формы введения, типа заболевания и т.п., она должна составлять 100 мкг - 10 г в день для взрослого, и такие дозы могут быть введены за один раз или разделены на несколько введений.
Форма введения лекарства по настоящему изобретению особенно не ограничивается, и это может быть пероральное введение или парентеральное введение с помощью обычно применяемого способа.
Биохимическая активность и действие, и эффекты (активность в отношении торможения ангиогенеза, противоопухолевая активность или тому подобное) в качестве лекарства соединений по настоящему изобретению могут быть оценены с помощью следующих способов.
Далее следует перечень сокращений, применяемых в примерах фармакологических тестов, описанных ниже.
<Перечень сокращений>
ДНК (дезоксирибонуклеиновая кислота)
VEGFR2 (рецептор 2 фактора роста эндотелия сосудов)
Hepes (N-[2-гидроксиэтил]пиперазин-N'-[2-этансульфокислота], HEPES (буферный раствор))
MgCl2 (хлорид магния)
MnCl2 (хлорид марганца)
Na3VO4 (ортованадат(V) натрия)
АТФ (аденозин 5'-трифосфат)
ЭДТА (этилендиаминтетрауксусная кислота)
HTRF (гомогенная флуоресценция с разрешением во времени)
FGFR1 (рецептор 1 фактора роста фибробластов)
PDGFRβ (рецептор β фактора роста тромбоцитов)
HGFR (рецептор фактора роста гепатоцитов)
EGFR (рецептор эпидермального фактора роста)
Трис (Трис (гидроксиметил)аминометан, Трис (буферный раствор))
NaCl (хлорид натрия)
БСА (бычий сывороточный альбумин)
HRP (пероксидаза хрена)
ЭГТА (этиленгликоль-бис(2-аминоэтиловый эфир)-N,N,N',N'-тетрауксусная кислота)
ДДС-Na (додецилсульфат натрия)
NP-40 (Nonidet P-40)
ПЦР: полимеразная цепная реакция
ОТ-ПЦР: полимеразная цепная реакция с обратной транскрипцией
РНК: рибонуклеиновая кислота
кДНК: комплементарная ДНК
кРНК: комплементарная РНК
dNTP: смесь, состоящая из dATP, dCTP, dGTP и dTTP
UTP: уридин-5'-трифосфат
CTP: цитидин-5'-трифосфат
dATP: 2'-дезоксиаденозин 5'-трифосфат
dCTP: 2'-дезоксицитидин 5'-трифосфат
dGTP: 2'-дезоксигуанозин 5'-трифосфат
dUTP: 2'-дезоксиуридин 5'-трифосфат
GAPDH: глицеральдегид-3-фосфатдегидрогеназа
FBS: сыворотка плодов телят
ЗФР: забуференный фосфатом физиологический раствор
MTT: (3-[4,5-диметилтиозол-2-ил]-2,5-дифенилтетразолия бромид; тиазолиловый синий)
ДМСО: диметилсульфоксид
PDGF: фактор роста тромбоцитов
EGF: эпидермальный фактор роста
FGF2: фактор 2 роста фибробластов
VEGF: фактор роста эндотелия сосудов
HGF: фактор роста гепатоцитов
TNF-α: фактор некроза опухолей альфа
FCS: сыворотка плодов телят
EGM-2: ростовая среда 2 для эндотелиальных клеток
Пример 1 фармакологического теста: ингибирование образования многослойной трубки эндотелиальными клетками сосуда в ответ на стимуляцию ангиогенным фактором
Эндотелиальные клетки пупочной вены человека (HUVEC) выделяли в соответствии с сообщенным методом (Shinseikagaku Jikken Koza [New Biochemistry Experiment Lectures], "Saibo Baiyo Gijutsu" [Cell Culturing Techniques], p.197-202) и культивировали в инкубаторе с 5% CO2 (37°С) с использованием среды EGM-2 (приобретенной у Clonetics Corp.) до достижения клетками конфлюэнтности.
Охлажденную на льду смесь коллаген : 5x RPMI 1640 : буфер для реконституции (все приобретено у Nitta Gelatin, Inc.) в отношении 7:2:1 разносили по 0,4 мл в каждую лунку 24-луночного планшета. После образования из раствора геля в результате нахождения в течение 40 минут в инкубаторе с 5% CO2 (37°С) в каждую лунку добавляли по 0,4 мл суспензии клеток HUVEC (используя от 1 до 1,2·105 клеток, хотя количество клеток немного отличалось в зависимости от лота HUVEC), причем суспензия клеток HUVEC находилась в бессывороточной среде для эндотелиальных клеток человека (SFM, приобретенной у GIBCO BRL), содержащей добавленные ангиогенные факторы [20 нг/мл FGF2 (приобретенного у GIBCO BRL) и 10 нг/мл EGF (приобретенного у GIBCO BRL), или 25 нг/мл VEGF (приобретенного у Wako Pure Chemical Industries Co., Ltd.) и 10 нг/мл EGF или 30 нг/мл HGF (приобретенного у R&D Co.) и 10 нг/мл EGF], и культивировали в течение ночи в инкубаторе с 5% CO2 (37°С). На следующий день среду с верхнего слоя отсасывали и затем 0,4 мл охлажденной на льду смеси коллаген : 5x RPMI 1640 : буфер для реконституции (все приобретено у Nitta Gelatin, Inc.) в отношении 7:2:1 вносили в каждую лунку перед помещением на 4 часа в инкубатор с 5% CO2 (37°С) для образования геля. После добавления на верхний слой 1,5 мл SFM, содержащей каждый из указанных выше ангиогенных факторов, и разведенного тестируемого вещества проводили культивирование в инкубаторе с 5% CO2 (37°С). После отсасывания культурального супернатанта из каждой лунки на 4-й день после добавления тестируемого вещества в каждую лунку добавляли 0,4 мл 3,3 мг/мл раствора MTT, растворенного в ЗФР (приобретенного у Sigma Corp.), и культивировали в течение приблизительно 2 часов в инкубаторе с 5% CO2 (37°С). Образовавшиеся в коллагеновом геле каждой лунки трубки окрашивали MTT, изображения трубок переносили на компьютер (Macintosh) и определяли общую длину трубок с помощью компьютерной программы анализа изображений "MacScope" (приобретенной у Mitani Corp.). Отношение общей длины трубок, образованных в лунке, содержащей тестируемое вещество, к общей длине трубок, образованных в лунке, не содержащей тестируемое вещество, выражали в процентах и из величины отношения определяли концентрацию каждого тестируемого вещества, требуемую для 50% ингибирования образования (IC50). Результаты представлены в таблице 1.
IC50 (нМ)
IC50 (нМ)
Пример 2 фармакологического теста: измерение ингибирования активности рецепторных тирозинкиназ
Данный тест применяют для определения ингибирования тестируемым веществом активности тирозинкиназ. ДНК, кодирующую цитоплазматический домен VEGFR2, получают с помощью синтеза суммарной кДНК (Edwards M., International Biotechnology Lab 5(3), 19-25, 1987) или путем клонирования. При экспрессии в подходящей экспрессионной системе можно получить полипептид с тирозинкиназной активностью. Цитоплазматический домен VEGFR2, полученный экспрессией рекомбинантного белка, например, в клетках насекомых, как было показано, проявляет присущую ему тирозинкиназную активность. Для VEGFR2 (GenBank Accession No. L04947), фрагмент ДНК в 1,7 т.п.н., описанный Terman et al. (Oncogene, 6(9), 1677-1683, 1991), кодирующего цитоплазматический домен, начинающийся с лизина 791 и включающий кодон терминации, был выделен из библиотеки плацентарной кДНК человека (приобретено у Clontech Laboratories, Inc.) и клонирован в бакуловирусном экспрессионном векторе (pFastBacHis, приобретено у GIBCO BRL). Рекомбинантный конструкт трансфицировали в клетки насекомых (Spondoptea frugiperda 9 (Sf9)) для получения рекомбинантного бакуловируса. (Инструкции по получению и применению рекомбинантного бакуловируса могут быть найдены в стандартных текстах, таких как "Bac-To-Bac Baculovirus Expression System" (GIBCO BRL).) Цитоплазматический фрагмент, начинающийся с лизина 398 (FGFR1, GenBank Accession No. X52833), цитоплазматический фрагмент, начинающийся с лизина 558 (PDGFRβ, GenBank Accession No. M21616), или цитоплазматический фрагмент, начинающийся с лизина 974 (HGFR, GenBank Accession No. J02958), могут быть клонированы и экспрессированы с помощью того же способа для применения в тестах на другие тирозинкиназы. EGFR приобретали у Sigma Co. (Product No. E-2645).
Для экспрессии тирозинкиназы VEGFR2 клетки Sf9 инфицировали VEGFR2 рекомбинантным вирусом и собирали через 48 часов. Собранные клетки промывали охлажденным на льду забуференным фосфатом физиологическим раствором (ЗФР) и затем ресуспендировали с применением 20 мл охлажденного на льду буфера для лизиса (50 мМ Трис-HCl (pH 8,5), 5 мМ 2-меркаптоэтанол, 100 мМ KCl, 1 мМ фенилметилсульфонилфторид, 1% (об./об.) NP-40) на 1,5·108 клеток. Суспензию центрифугировали при 12000 об/мин в течение 30 минут при 4°С и получали супернатант.Супернатант добавляли к колонке агарозы Ni-NTA (3 мл, приобретенной у Qiagen), уравновешенной буфером А {20 мМ Трис-HCl (pH 8,5), 5 мМ 2-меркаптоэтанол, 500 мМ KCl, 20 мМ имидазол, 10% (об./об.) глицерин}. Колонку промывали 30 мл буфера A и затем 6 мл буфера B {20 мМ Трис-HCl (pH 8,5), 5 мМ 2-меркаптоэтанол, 1 М KCl, 10% (об./об.) глицерин} и, наконец, 6 мл буфера A. После промывания его элюировали 6 мл буфера C {20 мМ Трис-HCl (pH 8,5), 5 мМ 2-меркаптоэтанол, 100 мМ KCl, 100 мМ имидазол, 10% (об./об.) глицерин}. Элюат помещали в диализную пленку (приобретенную у Spectrum Laboratories) и диализовали буфером для диализа (20 мМ Трис-HCl (pH 7,5), 10% (об./об.) глицерин, 1 мМ дитиотреитол, 0,1 мМ Na3VO4, 0,1 мМ ЭГТА}. После диализа его подвергали электрофорезу с ДДС-Na и рекомбинантный белок (His6-VEGFR2, цитоплазматический домен VEGFR2, гибридизованный с 6 остатками гистидина на N-конце), определяемый по молекулярной массе, равной приблизительно 100 кДа, тестировали с помощью окрашивания кумасси синим с применением БСА (бычий сывороточный альбумин, приобретенный у Sigma Co.) в качестве вещества-стандарта и хранили при - 80°С до использования. Применение того же способа для цитоплазматических доменов FGFR1, PDGFRβ и HGFR дало соответствующие рекомбинантные белки, гибридизованные на N-конце с 6 остатками гистидина (His6-FGFR1, His6-PDGFRβ или His6-HGFR).
Тирозинкиназную реакцию проводили следующим образом. В случае VEGFR2, например, 10 мкл раствора для киназной реакции {200 мМ Hepes (pH 7,4), 80 мМ MgCl2, 16 мМ MnCl2, 2 мМ Na3VO4}, 250 нг связанного с биотином поли(Glu4:Tyr1) (биотин-поли(GT), приобретенный у CIS Diagnostics Co.) (6 мкл 15-кратного разведения дистиллированной водой), 15 нг His6-VEGFR2 (10 мкл 240-кратного разведения 0,4% раствором БСА) и тестируемое вещество, растворенное в диметилсульфоксиде (4 мкл 100-кратного разведения 0,1% раствором БСА) добавляли в каждую лунку 96-луночного планшета с круглодонными лунками (NUNC Co., Product No. 163320) до суммарного объема 30 мкл. Затем добавляли 10 мкл 4 мкМ АТФ (разведенного дистиллированной водой) перед инкубацией при 30°С в течение 10 минут и затем добавляли 10 мкл 500 мМ ЭДТА (рН 8,0).
Фосфорилированный по тирозину биотин-поли(GT) измеряли с помощью метода гомогенной флуоресценции с разрешением во времени (HTRF) (Analytical Biochemistry, 269, 94-104, 1999). Конкретно, раствор для киназной реакции переносили в 96-луночный черный полупланшет (Product No. 3694, Coster, Inc.), туда добавляли 7,5 нг антител против фосфотирозина, меченных криптатом европия (Eu(K)-PY20, приобретенных у CIS Diagnostics Co.) (25 мкл 250-кратного разведения 20 мМ Hepes (pH 7,0), 0,5 М KF, 0,1% раствор БСА) и туда добавляли 250 нг меченного XL665 стрептавидина (XL665-SA, приобретенного у CIS Diagnostics Co.) (25 мкл 62,5-кратного разведения 20 мМ Hepes (pH 7,0), 0,5 М KF и 0,1% раствор БСА), смеси давали постоять при комнатной температуре в течение 30 минут и затем измеряли интенсивность флуоресценции при 665 нм и 620 нм при длине волны возбуждающего излучения 337 нм с применением анализатора Discovery HTRF Microplate Analyzer (Packard Co.). Скорость фосфорилирования тирозина биотин-поли(GT) выражали как величину дельта F(%), как описано CIS Diagnostics Co в HTRF Standard Experiment Methods text. Величину дельта F(%) в присутствии тестируемого вещества определяли как отношение (%) к величине дельта F(%) при добавлении His6-VEGFR2 в отсутствие тестируемого вещества, принятой за 100%, и величину дельта F(%) при отсутствии как тестируемого вещества, так и His6-VEGFR2 принимали за 0%. Данное отношение (%) применяли для расчета концентрации тестируемого вещества, требуемой для 50% ингибирования киназной активности VEGFR2 (IC50).
Измерение ингибирования киназной активности FGFR1, EGFR и HGFR проводили с применением 15 нг His6-FGFR1, 23 нг EGFR и 30 нг His6-HGFR соответственно, в соответствии с тирозинкиназной реакцией и методом HTRF, описанными выше. Измерение ингибирования киназной активности PDGFRβ проводили с применением 50 нг His6-PDGFRβ в соответствии с тирозинкиназной реакцией, описанной выше, с последующим определением фосфорилированного по тирозину биотин-поли(GT) с помощью следующего метода. Конкретно, раствор для киназной реакции добавляли к 96-луночному планшету с покрытыми стрептавидином лунками (Product No. 15129, Pierce Chemical) и инкубировали при комнатной температуре в течение 30 минут.После 3-кратного промывания 150 мкл промывающего раствора {20 мМ Трис-HCl (pH 7,6), 137 мМ NaCl, 0,05% Твин-20, 0,1% БСА}, туда добавляли 70 мкл конъюгата (PY20)-HRP против фосфотирозина (Product No. P-11625, Transduction Laboratories) {2000-кратное разведение 20 мМ Трис-HCl (pH 7,6), 137 мМ NaCl, 0,05% Твин-20, 1% БСА} и инкубацию осуществляли при комнатной температуре в течение 1 часа. После инкубации его промывали 3 раза 150 мкл промывающего раствора и добавляли 100 мкл TMB, субстрата пероксидазы мембран (Product No. 50-5077-03, Funakoshi Co., Ltd.), для инициации реакции. После инкубации при комнатной температуре в течение 10 минут добавляли 100 мкл 1 М фосфорной кислоты для прекращения реакции и измеряли поглощение при 450 нм с помощью микропланшетного ридера (BIO KINETICS READER EL304, Bio-Tek Instruments). Коэффициент поглощения в присутствии тестируемого вещества определяли по отношению к 100%, за которое принимали поглощение при добавлении His6-PDGFRβ без тестируемого вещества, и 0% как поглощения без добавления как тестируемого вещества, так и His6-PDGFRβ. Данный коэффициент поглощения применяли для расчета концентрации тестируемого вещества, требуемой для 50% ингибирования киназной активности PDGFRβ (IC50). Результаты представлены в таблице 2.
Пример 3 фармакологического теста: оценка in vivo активности по индукции ангиогенеза с применением модели дорсального воздушного мешка мыши
(1) Конструкция экспрессионного вектора VEGF (фактора роста эндотелия сосудов)
ПЦР проводили с применением библиотеки кДНК плаценты человека (Toyobo Co., Ltd.) в качестве матрицы и SEQ ID NO:1 (5'CCGGATCCATGAACTTTCTGCTG3') и SEQ ID NO:2 (5'GTGAATTCTGTATCGATCGTT3') VEGF в качестве праймеров. После завершения реакции ПЦР 5'-концы фосфорилировали и полосу из приблизительно 600 п.н. ДНК выделяли с помощью гель-электрофореза в 1,2% агарозе. После полимеризации путем самолигирования кДНК разрезали с помощью EcoRI и BamHI и вставляли в сайты EcoRI и BamHI вектора pUC19. Его использовали для трансформации E.coli JM83, и в трансформированных клонах открывали плазмиды. Фрагмент кДНК VEGF вырезали из плазмид с помощью HindIII и EcoRI и затем вставляли в вектор pIRES2-rsGFP для получения pIRES2-rsGFP/VEGF для экспрессии белка.
(2) Получение штамма с высокой экспрессией VEGF
После культивирования в течение ночи клеток KP-1 рака поджелудочной железы человека (3·106 клеток) в среде RPMI 1640, содержащей 10% FCS, применяли набор Effectene Transfection Reagent Kit (Qiagen) для введения 3 мкг pIRES2-rsGFP/VEGF в клетки KP-1. После культивирования в среде RPMI 1640, содержащей 10% FCS и содержащей 600 мкг/мл генетицина, отбирали клетки, устойчивые к лекарству. Далее клетки с высокой экспрессией GFP собирали с помощью клеточного сортера (Becton Dickinson) как клетки KP-1 с высокой экспрессией VEGF (KP-1/VEGF).
(3) Измерение уровня VEGF в культуральном супернатанте
Клетки KP-1/VEGF разводили до 5·105 клеток/мл и 0,5 мл этого вносили в каждую лунку 24-луночного планшета и культивировали при 37°С в течение 24 часов. Культуральные супернатанты собирали и в них измеряли уровни VEGF с применением набора для измерения VEGF (IBL Co., Ltd.) для подтверждения высокой экспрессии.
(4) Оценка in vivo индуцирующей ангиогенез активности с применением модели дорсального воздушного мешка мыши
Миллипоровые кольца (Nihon Millipore) спаивали с 0,45 мкм мембранами для фильтрации Durapore (Nihon Millipore) для создания камер. Клетки рака поджелудочной железы человека KP-1/VEGF (3·106), суспендированные в 0,17 мл коллагенового геля, вводили в каждую камеру через отверстие для инъекции и камеры запаивали. Затем вводили приблизительно 10 мл воздуха в дорсальную кожу 6-недельных самок мышей C57BL/6N под анестезией для получения мешков и туда трансплантировали полученные камеры. Приблизительно через 6 часов после завершения трансплантации тестируемое вещество, суспендированное в 0,5% метилцеллюлозе, вводили перорально (0,1 мл/10 г массы тела) и так продолжали по одному разу в день в течение последующих 4 дней.
На 4-й день после трансплантации камер 0,2 мл меченных 51Cr (Amersham Pharmacia) эритроцитов мыши (2,5·106 имп/мин/мл) вводили через хвостовые вены каждой из мышей с трансплантированными камерами. После заданного периода кожу, находившуюся в контакте с камерой, удаляли и замораживали, участок, находящийся в прямом контакте с камерой точно вырезали и измеряли радиоактивность с помощью γ-счетчика. Объем крови рассчитывали, исходя из радиоактивности, и применяли в качестве индекса активности, индуцирующей ангиогенез in vivo. Объем ангиогенеза записывали как данный измеренный объем крови минус объем крови, полученный при трансплантации камеры, содержащей только коллагеновый гель. Эксперимент проводили с применением 10 мышей в контрольной группе (введение растворителя) и 5 мышей в каждой группе с введением соединений. Отношения (%) уровня ангиогенеза после введения тестируемого вещества к таковому у контроля представлены в таблице 3.
Пример 4 фармакологического теста: оценка противоопухолевой активности на клетках KP-1/VEGF на моделях подкожных ксенотрансплантатов
Клетки рака поджелудочной железы, высоко экспрессирующие VEGF (KP-1/VEGF), суспендированные в ЗФР в концентрации 1·107 клеток/мл, трансплантировали под кожу правого бока 6-недельных самок мышей Balb/c (nu/nu) в объеме 0,1 мл. Когда объем опухоли достигал приблизительно 100 мм3, вводили перорально тестируемое вещество дважды в день в течение 2 недель по схеме 5 дней в неделю. Тестируемое вещество суспендировали в 0,5% метилцеллюлозе до вводимого объема 0,1 мл/10 г массы тела. Размер опухоли измеряли дважды в неделю с применением микрометрического штангенциркуля. Объем опухоли определяли с помощью измерения длинного и короткого диаметров опухоли микрометрическим штангенциркулем и расчета 1/2 x (длинный диаметр x короткий диаметр). Эксперимент проводили с применением 10 мышей в контрольной группе (введение растворителя) и 5 мышей в каждой группе с введением тестируемых соединений. Отношения (%) объема опухолей после введения тестируемого вещества к таковым у контроля представлены в таблице 4.
Пример 5 фармакологического теста: оценка ингибирующей ангиогенез активности на модели ангиогенеза мыши с применением Matrigel
Эксперимент проводили в соответствии с методом, как уже описывалось в методе (Lab. Invest., 67(4), 519-528, 1992). Конкретно, 10 мкг/мл рекомбинантного FGF-2 (приобретенного у Invitrogen Corporation), растворенного в ЗФР, добавляли к Matrigel Matrix (приобретенного у BD Biosciences) для получения 1 мкг/мл. После этого 300 мкл данной смеси Matrigel Matrix и рекомбинантного FGF-2 вводили под кожу ткани средней линии живота 6-недельной мыши Balb/c (nu/nu).
Затем тестируемое вещество, суспендированное в 0,5% метилцеллюлозе или тому подобном, вводили перорально в виде суспензии один раз в день или два раза в день в течение 7 дней.
Через 7 дней имплантированный Matrigel вынимали, туда добавляли 300 мкл воды и нарезали на куски ножницами. Полученное вещество оставляли на холоду в темном месте на ночь. После полной экстракции гемоглобина из Matrigel 100 мкл супернатанта, полученного центрифугированием, и 100 мкг раствора Драбкина (приобретенного у Sigma Chemical Co., Ltd) давали взаимодействовать при комнатной температуре в темном месте в течение 1 часа. После этого измеряли поглощение реакционного раствора при длине волны 550 нм и референтной длине волны 660 нм. Количество гемоглобина (г/мл) в Matrigel рассчитывали по калибровочной кривой, полученной при применении гемоглобина в качестве стандарта.
Эксперимент проводили с применением 8 мышей в контроле (введение растворителя) и 6 мышей в каждой группе с введением соединения.
Примеры
Соединения по настоящему изобретению могут быть получены с помощью способов, описанных, например, в последующих примерах. Они являются, однако, иллюстративными, и соединения по настоящему изобретению в любых случаях не ограничиваются конкретными примерами, указанными ниже.
Пример 1
N1-Этил-5-(2-((метоксиамино)карбонил)амино-4-пиримидил)окси-1H-1-индолкарбоксамид
Так же как и в примере получения 27-2, сырой продукт фенил N-(4-(1-(этиламино)карбонил-1H-5-индолил)окси-2-пиримидил)карбамат (546 мг, 1,31 ммоль, 56,3%) получали в виде бледно-коричневого порошка из N1-этил-5-(2-амино-4-пиримидил)окси-1H-1-индолкарбоксамида (691 мг, 2,32 ммоль) и фенилхлоркарбоната. Сырой карбаматный продукт (273 мг, 0,65 ммоль) растворяли в тетрагидрофуране (7,0 мл) и к нему добавляли триэтиламин (0,91 мл, 6,53 ммоль) и метоксиамина гидрохлорид (273 мг, 3,27 ммоль) при перемешивании при комнатной температуре. После перемешивания реакционной смеси в течение ночи реакционную смесь подвергали распределению между этилацетатом и водой. Органический слой промывали водой и насыщенным раствором соли и сушили над безводным сульфатом натрия. Растворитель отгоняли и остаток очищали с помощью колоночной хроматографии на силикагеле (элюент: смесь этилацетат:гексан=1:1). Кристаллы осаждали из смеси этилацетат:гексан (1:10), отфильтровывали и сушили при аэрировании с получением указанного в заголовке соединения (52,5 мг, 0,14 ммоль, 21,7%) в виде белых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,17 (3H, т, J=7,2 Гц), 3,20-3,40 (2H, м), 3,68 (3H, с), 6,45 (1H, д, J=5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 7,09 (1H, дд, J=2,4, 8,8 Гц), 7,43 (1H, д, J=2,4 Гц), 7,54 (1H, д, J=5,6 Гц), 7,89 (1H, д, J=3,6 Гц), 8,21 (1H, м), 8,26 (1H, д, J=8,8 Гц), 8,34 (1H, д, J=5,6 Гц), 9,31 (1H, д, J=10,0 Гц).
Исходные вещества синтезировали следующими способами.
Пример получения 1-1
4-Хлор-6-(1H-5-индолилокси)-2-пиримидинамин
Гидрид натрия (1,0 г, 25 ммоль) суспендировали в диметилсульфоксиде (40 мл) в атмосфере азота и постепенно добавляли 5-гидроксииндол (3,33 г, 25 ммоль) при перемешивании смеси при комнатной температуре. Через 20 минут добавляли 2-амино-4,6-дихлорпиримидин (3,28 г, 20 ммоль). Реакционную смесь нагревали при 100°С и перемешивали в течение 3 часов. После охлаждения реакционной смеси до комнатной температуры реакционную смесь подвергали распределению между этилацетатом и 10% водным раствором аммиака. Органический слой промывали водой и насыщенным раствором соли и сушили над безводным сульфатом натрия. После отгонки растворителя остаток очищали с помощью NH-колоночной хроматографии на силикагеле (элюент: смесь этилацетат:гексан=2:1). Кристаллы осаждали из этилацетата, отфильтровывали и сушили при аэрировании с получением указанного в заголовке соединения (1,15 г, 4,41 ммоль, 22,0%) в виде белых кристаллов.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 5,09 (2H, уш.с), 6,07 (1H, с), 6,57 (1H, м), 6,95 (1H, дд, J=2,4, 8,8 Гц), 7,29 (1H, м), 7,37 (1H, м), 7,41 (1H, д, J=8,8 Гц), 8,28 (1H, уш.с).
Пример получения 1-2
4-(1H-5-Индолилокси)-2-пиримидинамин
4-Хлор-6-(1H-5-индолилокси)-2-пиримидинамин (1,15 г, 4,41 ммоль) растворяли в тетрагидрофуране (50 мл) - триэтиламине (3,07 мл), добавляли 10% палладий-на-угле (50% влажность, 500 мг) и реакционную смесь перемешивали в течение ночи в атмосфере водорода при атмосферном давлении.
Реакционную смесь промывали азотом. После добавления метанола (50 мл) и перемешивания катализатор отфильтровывали. Полученный раствор концентрировали при пониженном давлении с получением в результате указанного в заголовке соединения (826 мг, 3,65 ммоль, 82,8%) в виде бледно-серого порошка.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 4,96 (2H, уш.с), 6,06 (1H, д, J=5,6 Гц), 6,56 (1H, м), 6,97 (1H, дд, J=2,4, 8,8 Гц), 7,26-7,28 (1H, м), 7,38-7,42 (2H, м), 8,08 (1H, д, J=8,8 Гц), 8,29 (1H, уш.с).
Пример получения 1-3
N1-Этил-5-(2-амино-4-пиримидил)окси-1H-1-индолкарбоксамид
Гидрид натрия (157 мг, 3,93 ммоль) суспендировали в N,N-диметилформамиде (10 мл) в атмосфере азота и постепенно добавляли 4-(1H-5-индолилокси)-2-пиримидинамин (826 мг, 3,65 ммоль) при перемешивании реакционной смеси при комнатной температуре. Через 10 минут реакционную смесь охлаждали с помощью водно-ледяной бани, добавляли фенил N-этилкарбамат (633 мг, 3,83 ммоль), реакционную смесь нагревали до комнатной температуры и раствор перемешивали в течение 4 часов. Реакционную смесь подвергали распределению между этилацетатом и водой. Органический слой промывали водой и насыщенным раствором соли и сушили над безводным сульфатом натрия. Растворитель отгоняли и остаток очищали хроматографией на силикагеле (элюент: смесь этилацетат:гексан=3:1) с получением указанного в заголовке соединения (691 мг, 2,32 ммоль, 63,7%) в виде белого порошка.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 1,32 (3H, т, J=7,2 Гц), 3,54 (2H, м), 4,94 (2H, уш.с), 5,50 (1H, уш.с), 6,11 (1H, дд, J=2,4, 5,6 Гц), 6,62 (1H, д, J=3,6 Гц), 7,09 (1H, дд, J=2,4, 8,8 Гц), 7,34 (1H, д, J=2,4 Гц), 7,46 (1H, д, J=3,6 Гц), 8,11 (1H, д, J=5,6 Гц), 8,15 (1H, д, J=8,8 Гц).
Пример 2
Метиламид 5-(6-(3-(3-диэтиламинопропиламино)уреидо)пиримидин-4-илокси)-1H-индол-1-карбоновой кислоты
Фенил-(6-(1-метилкарбамоил-1H-индол-5-илокси)пиримидин-4-ил)карбамат (161 мг, 0,400 ммоль) растворяли в N,N-диметилформамиде (1,0 мл) и добавляли 3-(диэтиламино)пропиламин (130 мг, 1,00 ммоль) при перемешивании реакционной смеси при комнатной температуре. После перемешивания реакционной смеси в течение ночи реакционную смесь подвергали распределению между этилацетатом и водой. Органический слой промывали водой и насыщенным раствором соли и сушили над безводным сульфатом натрия. Растворитель отгоняли и остаток очищали с помощью NH колоночной хроматографии на силикагеле (элюент: смесь этилацетат:метанол=50:1). Кристаллы осаждали из смеси этилацетат-гексан, отфильтровывали и сушили при аэрировании с получением указанного в заголовке соединения (123 мг, 0,280 ммоль, 70%) в виде белых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,93 (6H, т, J=7,0 Гц), 1,52 (2H, м), 2,32-2,46 (6H, м), 2,84 (3H, д, J=3,6 Гц), 3,12 (2H, м), 6,69 (1H, д, J=3,6 Гц), 6,98 (1H, с), 7,06 (1H, дд, J=2,2, 8,8 Гц), 7,37-7,46 (2H, м), 7,88 (1H, д, J=3,6 Гц), 8,18 (1H, м), 8,27 (1H, д, J=8,8 Гц), 8,37 (1H, с), 9,49 (1H, уш.с).
Исходные вещества синтезировали следующими способами.
Пример получения 2-1
Фенил-N-метилкарбамат
Метиламина гидрохлорид (16,9 г, 250 ммоль) растворяли в N,N-диметилформамиде (250 мл), к нему добавляли пиридин (44 мл, 275 ммоль) и реакционную смесь перемешивали. Реакционную смесь охлаждали с помощью льда, к ней по каплям добавляли фенилхлорформиат (35 мл, 275 ммоль) и реакционную смесь затем перемешивали при комнатной температуре в течение 24 часов. Реакционную смесь подвергали распределению между этилацетатом и водой. Органический слой промывали насыщенным раствором соли и сушили над безводным сульфатом магния, растворитель отгоняли при пониженном давлении. Полученные кристаллы суспендировали в диэтиловом эфире, разбавленном гексаном, отфильтровывали, промывали смесью диэтиловый эфир:гексан=1:1 и сушили вакуумированием с получением указанного в заголовке соединения (22,3 г, 147 ммоль, 59,1%) в виде бесцветных кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,64 (3H, д, J=3,6 Гц), 7,07 (2H, д, J=8,0 Гц), 7,17 (1H, т, J=8,4 Гц), 7,35 (2H, дд, J=8,0 Гц, 8,4 Гц), 7,58 (1H, д, J=3,6 Гц).
Пример получения 2-2
6-(1H-Индол-5-илокси)пиримидин-4-иламин
Гидрид натрия (400 мг, 10,0 ммоль) суспендировали в диметилсульфоксиде (20 мл) в атмосфере азота и постепенно добавляли 5-гидроксииндол (1,33 г, 10,0 ммоль) при перемешивании реакционной смеси при комнатной температуре. Через 20 минут туда добавляли 6-хлорпиримидин-4-иламин (1,04 г, 8,00 ммоль), реакционную смесь нагревали при 100°С и перемешивали в течение 1 часа. После естественного охлаждения реакционной смеси до комнатной температуры реакционную смесь подвергали распределению между этилацетатом и водой. Органический слой промывали водой и насыщенным раствором соли и сушили над безводным сульфатом магния. Растворитель отгоняли и остаток очищали колоночной хроматографией на силикагеле (элюент: смесь этилацетат:гексан=3:1) с получением указанного в заголовке соединения (1,07 г, 4,73 ммоль, 59%) в виде коричневого масла.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 5,54 (1H, с), 6,43 (1H, м), 6,71 (2H, уш.с), 6,85 (1H, дд, J=2,4, 8,8 Гц), 7,29 (1H, д, J=2,4 Гц), 7,40-7,45 (2H, м), 8,06 (1H, с), 11,20 (1Н, уш.с).
Пример получения 2-3
Метиламид 5-(6-аминопиримидин-4-илокси)-1H-индол-1-карбоновой кислоты
Гидрид натрия (199 мг, 4,97 ммоль) суспендировали в N,N-диметилформамиде (10 мл) в атмосфере азота, постепенно добавляли синтезированный в примере получения 2-2 6-(1H-индол-5-илокси)пиримидин-4-иламин (1,07 г, 4,73 ммоль) при перемешивании реакционной смеси при комнатной температуре. Через 30 минут реакционную смесь охлаждали с помощью водно-ледяной бани, после чего добавляли синтезированный в примере получения 2-1 фенил-N-метилкарбамат (751 мг, 4,97 ммоль). Реакционную смесь нагревали до комнатной температуры и перемешивали в течение 1 часа. Реакционную смесь подвергали распределению между этилацетатом и водой. Органический слой промывали водой и насыщенным раствором соли и сушили над безводным сульфатом магния. После отгонки растворителя остаток очищали колоночной хроматографией на силикагеле (элюент: этилацетат) с получением указанного в заголовке соединения (847 мг, 2,99 ммоль, 63%) в виде белых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,85 (3H, д, J=4,0 Гц), 5,62 (1H, с), 6,68 (1H, д, J=3,6 Гц), 6,77 (2H, уш.с), 7,04 (1H, дд, J=2,4, 9,2 Гц), 7,36 (1H, д, J=2,4 Гц), 7,87 (1H, д, J=3,6 Гц), 8,07 (1H, с), 8,15 (1H, кв, J=4,0 Гц), 8,27 (1H, д, J=9,2 Гц).
Пример получения 2-4
Фенил-(6-(1-метилкарбамоил)-1H-индол-5-илокси)пиримидин-4-ил)карбамат
Метиламид 5-(6-аминопиримидин-4-илокси)-1H-индол-1-карбоновой кислоты (847 мг, 2,99 ммоль), синтезированный в примере получения 2-3, растворяли в N,N-диметилформамиде (10 мл) в атмосфере азота. К нему последовательно по каплям добавляли пиридин (0,290 мл, 11,5 ммоль) и фенилхлоркарбамат (0,394 мл, 3,15 ммоль) при охлаждении с помощью водно-ледяной бани. После перемешивания реакционной смеси в течение 30 минут добавляли триэтиламин (0,417 мл, 2,99 ммоль) и реакционную смесь нагревали до комнатной температуры при перемешивании. Через 30 минут реакционную смесь подвергали распределению между этилацетатом и водой. Органический слой промывали водой и насыщенным раствором соли и сушили над безводным сульфатом магния. Растворитель отгоняли и остаток затем очищали колоночной хроматографией на силикагеле (элюент: смесь этилацетат:гексан=3:1). Кристаллы осаждали из смеси этилацетат-гексан, отфильтровывали и сушили при аэрировании с получением указанного в заголовке соединения (504 мг, 1,25 ммоль, 42%) в виде белых кристаллов.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 3,05 (3H, д, J=4,8 Гц), 5,53 (1H, кв, J=4,8 Гц), 6,58 (1H, д, J=4,0 Гц), 7,08 (1H, дд, J=2,4, 8,8 Гц), 7,13-7,19 (2H, м), 7,23-7,29 (1H, м), 7,34 (1H, д, J=2,4 Гц), 7,36-7,44 (3H, м), 7,52 (1H, с), 8,14 (1H, д, J=8,8 Гц), 8,59 (1H, с), 9,99 (1H, уш.с).
Пример 3
Метиламид 5-(6-(((4-гидроксипиперидин-1-ил)карбонил)амино)пиримидин-4-илокси)-1H-индол-1-карбоновой кислоты
Аналогично примеру 2 указанное в заголовке соединение (100 мг, 0,231 ммоль, 58%) получали в виде белого порошка из фенил-(6-(1-метилкарбамоил)-1H-индол-5-илокси)пиримидин-4-ил)карбамата (161 мг, 0,400 ммоль) и 4-гидроксипиперидина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,24-1,34 (2H, м), 1,64-1,73 (2H, м), 2,85 (3H, д, J=4,0 Гц), 3,02-3,12 (2H, м), 3,64 (1H, м), 3,72-3,80 (2H, м), 4,69 (1H, д, J=4,0 Гц), 6,68 (1H, д, J=3,6 Гц), 7,06 (1H, дд, J=2,4, 8,8 Гц), 7,20 (1H, с), 7,40 (1H, д, J=2,4 Гц), 7,88 (1H, д, J=3,6 Гц), 8,17 (1H, кв, J=4,0 Гц), 8,27 (1H, д, J=8,8 Гц), 8,40 (1H, с), 9,72 (1H, уш.с).
Пример 4
Метиламид 5-(6-((4-пирролидин-1-ил)пиперидин-1-ил)карбониламино)пиримидин-4-илокси)-1H-индол-1-карбоновой кислоты
Аналогично примеру 2 указанное в заголовке соединение (141 мг, 0,304 ммоль, 76%) получали в виде белых кристаллов из фенил-(6-(1-метилкарбамоил)-1H-индол-5-илокси)пиримидин-4-ил)карбамата (161 мг, 0,400 ммоль) и 4-(1-пирролидинил)пиперидина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,23-1,36 (2H, м), 1,63-1,70 (4H, м), 1,74-1,84 (2H, м), 2,08-2,18 (1H, м), 2,42-2,50 (4H, м), 2,82-2,95 (5H, м), 3,90-3,98 (2H, м), 6,68 (1H, д, J=3,6 Гц), 7,06 (1H, дд, J=2,4, 8,8 Гц), 7,20 (1H, с), 7,40 (1H, д, J=2,4 Гц), 7,88 (1H, д, J=3,6 Гц), 8,17 (1H, кв, J=4,0 Гц), 8,27 (1H, д, J=8,8 Гц), 8,40 (1H, с), 9,71 (1H, уш.с).
Пример 5
Метиламид 5-(2-(3-((1R)-1-карбамоил-2-фенилэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамат (104 мг, 0,200 ммоль) и триэтиламин (1 мл) растворяли в N,N-диметилформамиде (3 мл), добавляли (2R)-2-амино-3-фенилпропионамида гидрохлорид (201 мг, 1,00 ммоль) и реакционную смесь перемешивали в течение 18 часов. Реакционную смесь подвергали распределению между этилацетатом и насыщенным водным раствором хлорида аммония. Органический слой промывали водой и насыщенным раствором соли и сушили над безводным сульфатом магния. Растворитель отгоняли и остаток очищали колоночной хроматографией на силикагеле (элюент: смесь этилацетат:метанол=50:1). Кристаллы осаждали из смеси растворителей этилацетат-гексан, отфильтровывали и сушили при аэрировании с получением указанного в заголовке соединения (77,2 мг, 0,152 ммоль, 76%) в виде белых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,81 (1H, дд, J=8,0, 13,2 Гц), 2,84 (3H, д, J=4,4 Гц), 3,01 (1H, дд, J=4,8, 13,2 Гц), 4,38 (1H, м), 6,52 (1H, дд, J=2,4, 6,0 Гц), 6,69 (1H, д, J=3,2 Гц), 6,86 (1H, с), 7,01-7,07 (2H, м), 7,15-7,30 (5H, м), 7,37 (1H, д, J=2,4 Гц), 7,50 (1H, с), 7,88 (1H, д, J=3,2 Гц), 8,02 (1H, д, J=6,0 Гц), 8,18 (1H, кв, J=4,4 Гц), 8,22-8,34 (2H, м), 9,11 (1H, с).
Исходное вещество, фенил-N-(4-(1-(метиламино)карбонил-1H-индол-5-илокси)пиридин-2-ил)-N-(феноксикарбонил)карбамат, синтезировали следующим образом.
Пример получения 5-1
N1-Метил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамид
Гидрид натрия (430 мг, 10,75 ммоль) суспендировали в N,N-диметилформамиде (25 мл) в атмосфере азота и постепенно добавляли 4-(1H-5-индолилокси)-2-пиридинамин (2,253 г, 10,00 ммоль, CAS No. 417722-11-3), описанный в WO 02/32872, при перемешивании при комнатной температуре. Через 10 минут реакционную смесь охлаждали с помощью водно-ледяной бани, после чего добавляли фенил-N-метилкарбамат (1,587 г, 10,50 ммоль). Реакционную смесь нагревали до комнатной температуры и перемешивали в течение 2 часов. Реакционную смесь подвергали распределению между этилацетатом и водой. Органический слой промывали водой и насыщенным раствором соли и сушили над безводным сульфатом натрия. Растворитель удаляли отгонкой. Кристаллы осаждали из этилацетата, отфильтровывали и сушили при аэрировании с получением указанного в заголовке соединения (2,163 г, 7,66 ммоль, 76,6%) в виде бледно-коричневых кристаллов.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 3,09 (3H, д, J=4,8 Гц), 4,36 (2H, м), 5,49 (1H, м), 5,92 (1H, д, J=2,0 Гц), 6,30 (1H, дд, J=2,0, 6,0 Гц), 6,61 (1H, д, J=3,6 Гц), 7,07 (1H, дд, J=2,4, 8,8 Гц), 7,30 (1H, д, J=2,4 Гц), 7,45 (1H, д, J=3,6 Гц), 7,92 (1H, д, J=6,0 Гц), 8,17 (1H, д, J=8,8 Гц).
Пример получения 5-2
Фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамат
N1-Метил-5-(2-аминопиридил)окси-1H-1-индолкарбоксамид (2,0 г, 7,1 ммоль) суспендировали в тетрагидрофуране (140 мл) и N,N-диметилформамиде (1,4 мл) при комнатной температуре и при перемешивании добавляли триэтиламин (2,2 мл, 16 ммоль). Реакционную смесь охлаждали с помощью льда, добавляли фенилхлорформиат (1,8 мл, 15 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 1,5 часов. Дополнительно добавляли фенилхлорформиат (0,5 мл) и реакционную смесь перемешивали при комнатной температуре в течение 0,5 часов. К реакционной смеси добавляли насыщенный раствор соли и это подвергали экстракции этилацетатом, промывке насыщенным раствором соли, сушке над безводным сульфатом магния и концентрированию при пониженном давлении. К остатку добавляли диэтиловый эфир, после чего выпавшие кристаллы отфильтровывали, промывали диэтиловым эфиром и сушили при аэрировании с получением указанного в заголовке соединения (3,3 г, 6,3 ммоль, 89%) в виде бледно-коричневых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 3,30 (3H, д, J=4,4 Гц), 6,66 (1H, д, J=3,6 Гц), 6,95 (1H, дд, J=2,4, 6,0 Гц), 7,10 (1H, дд, J=2,4, 8,8 Гц), 7,15-7,18 (4H, м), 7,27-7,31 (2H, м), 7,40-7,45 (5H, м), 7,52 (1H, д, J=2,4 Гц), 7,88 (1H, д, J=3,6 Гц), 8,17 (1H, кв, J=4,4 Гц), 8,31 (1H, д, J=8,8 Гц), 8,41 (1H, д, J=6,0 Гц).
N1-Метил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамид, описанный в примере получения 5-1, может быть синтезирован следующим образом.
N1-Метил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамид
Метиламид 5-(2-аминопиридин-4-илокси)-2,3-дигидро-1H-индол-1-карбоновой кислоты (40 мг, 0,14 ммоль) растворяли в уксусной кислоте (0,9 мл), к нему добавляли ацетат марганца(III) (29 мг, 0,17 ммоль) и реакционную смесь перемешивали при 70°С в течение 3,5 часов. Дополнительно добавляли ацетат марганца(III) (29 мг, 0,17 ммоль) и реакционную смесь дополнительно перемешивали при 70°С в течение 0,5 часов. После естественного охлаждения до комнатной температуры реакционную смесь подвергали распределению между этилацетатом и насыщенным водным раствором бикарбоната натрия. Органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Полученные кристаллы суспендировали в смеси диэтиловый эфир:ацетон=3:1, отфильтровывали, промывали диэтиловым эфиром и сушили при аэрировании с получением указанного в заголовке соединения (24 мг, 0,085 ммоль, 61%) в виде бесцветных кристаллов.
Исходное вещество, метиламид 5-(2-аминопиридин-4-илокси)-2,3-дигидро-1H-индол-1-карбоновой кислоты, синтезировали следующим образом.
Пример получения 5-3
Метиламид 5-бензилокси-1H-индол-1-карбоновой кислоты
Гидрид натрия (2,212 г, 55,30 ммоль, 60% в масле) суспендировали в N,N-диметилформамиде (100 мл), к нему добавляли 5-бензилоксииндол (10,29 г, 46,09 ммоль) при перемешивали при комнатной температуре и реакционную смесь перемешивали при комнатной температуре в течение 40 минут. Реакционную смесь охлаждали с помощью водно-ледяной бани и добавляли фенил-N-метилкарбамат (8,360 г, 55,30 ммоль). После перемешивания реакционной смеси в течение 30 минут раствор перемешивали при комнатной температуре в течение 2,5 часов. После добавления к реакционной смеси воды и перемешивания реакционной смеси при комнатной температуре в течение 1 часа полученные кристаллы отфильтровывали, после чего данные кристаллы последовательно промывали водой и диэтиловым эфиром и сушили при аэрировании с получением указанного в заголовке соединения (12,07 г, 43,06 ммоль, 93,41%) в виде бледно-желтых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,80 (3H, д, J=4,4 Гц), 5,10 (2H, с), 6,56 (1H, д, J=3,8 Гц), 6,93 (1H, дд, J=2,4, 9,0 Гц), 7,16 (1H, д, J=2,4 Гц), 7,30 (1H, т, J=7,2 Гц), 7,37 (2H, т, J=7,2 Гц), 7,45 (2H, д, J=7,2 Гц), 7,74 (1H, д, J=3,8 Гц), 8,00 (1H, м), 8,11 (1H, д, J=9,0 Гц).
Пример получения 5-4
Метиламид 5-гидрокси-2,3-дигидро-1H-индол-1-карбоновой кислоты
Метиламид 5-бензилокси-1H-индол-1-карбоновой кислоты (10,00 г, 35,67 ммоль) растворяли в метаноле (200 мл) и тетрагидрофуране (150 мл), добавляли 10% палладий-на-угле (0,9 г) и реакционную смесь перемешивали при комнатной температуре в атмосфере водорода в течение 9 часов. После удаления катализатора фильтрованием растворитель отгоняли при пониженном давлении. Остаток растворяли в этаноле (400 мл), добавляли 10% палладий-на-угле (0,9 г), после чего реакционную смесь перемешивали при комнатной температуре в атмосфере водорода в течение 26 часов. После удаления катализатора фильтрованием растворитель отгоняли при пониженном давлении. Полученные кристаллы суспендировали в диэтиловом эфире, отфильтровывали, промывали диэтиловым эфиром и сушили при аэрировании с получением указанного в заголовке соединения (6,522 г, 33,93 ммоль, 95,12%) в виде сероватых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,61 (3H, д, J=4,4 Гц), 2,99 (2H, т, J=8,6 Гц), 3,76 (2H, т, J=8,6 Гц), 6,33 (1H, д, J=4,4 Гц), 6,43 (1H, дд, J=2,4, 8,4 Гц), 6,54 (1H, д, J=2,4 Гц), 7,58 (1H, д, J=8,4 Гц), 8,82 (1H, с).
Пример получения 5-5
Метиламид 5-(2-аминопиридин-4-илокси)-2,3-дигидро-1H-индол-1-карбоновой кислоты
Гидрид натрия (202 мг, 3,89 ммоль, 60% в масле) суспендировали в диметилсульфоксиде (5,0 мл), после чего добавляли метиламид 5-гидрокси-2,3-дигидро-1H-индол-1-карбоновой кислоты (971 мг, 5,06 ммоль) и 2-амино-4-хлорпиридин (500 мг, 3,89 ммоль) при комнатной температуре в атмосфере азота, реакционную смесь нагревали и перемешивали при 160°С в течение 12 часов в атмосфере азота. После естественного охлаждения до комнатной температуры реакционную смесь подвергали распределению между этилацетатом и водой. Органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia BW-300; элюент: этилацетат, смесь этилацетат:метанол=85:10 в данном порядке). Фракции, содержащие желаемое соединение, концентрировали и остаток дополнительно очищали колоночной хроматографией на силикагеле (Fuji Silysia NH, элюент: от этилацетата до смеси этилацетат:метанол=90:10). Полученные кристаллы суспендировали в смеси диэтиловый эфир:ацетон=3:1, отфильтровывали, промывали диэтиловым эфиром и сушили при аэрировании с получением указанного в заголовке соединения (51 мг, 0,18 ммоль, 4,6%) в виде бледно-зеленых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,65 (3H, д, J=4,4 Гц), 3,09 (2H, т, J=8,6 Гц), 3,86 (2H, т, J=8,6 Гц), 5,75 (1Н, д, J=2,0 Гц), 5,85 (2H, уш.с), 6,07 (1H, дд, J=2,0, 6,0 Гц), 6,56 (1H, д, J=4,4 Гц), 6,81 (1H, дд, J=2,4, 8,4 Гц), 6,90 (1H, д, J=2,4 Гц), 7,73 (1H, д, J=6,0 Гц), 7,83 (1H, д, J=8,4 Гц).
Пример 6
Метиламид 5-(2-(3-((1S)-1-карбамоил-2-фенилэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
N1-Метил-5-((2-амино-4-пиридил)окси-1H-1-индолкарбоксамид (100 мг, 0,354 ммоль), синтезированный в примере получения 5-1, и триэтиламин (0,3 мл) растворяли в N,N-диметилформамиде (3 мл). Туда по каплям добавляли фенилхлоркарбонат (0,0888 мл, 0,708 ммоль) при комнатной температуре и реакционную смесь перемешивали в течение 30 минут. Добавляли (2S)-2-амино-3-фенилпропионамид (290 мг, 1,77 ммоль) и реакционную смесь перемешивали в течение 3 дней. Реакционную смесь подвергали распределению между смесью растворителей этилацетат-тетрагидрофуран и вода. Органический слой промывали водой и насыщенным раствором соли, сушили над безводным сульфатом магния. Растворитель отгоняли и остаток очищали с помощью колоночной хроматографии на силикагеле (элюент: смесь этилацетат:метанол=20:1). Кристаллы осаждали из смеси растворителей этилацетат-гексан, отфильтровывали и сушили при аэрировании с получением указанного в заголовке соединения (69,4 мг, 0,147 ммоль, 41%) в виде белых кристаллов.
Пример 7
Метиламид 5-(2-(3-(2-оксо-2-(пирролидин-1-ил)этил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
трет-Бутоксикарбониламиноуксусную кислоту (876 мг, 5,00 ммоль) и N-метилморфолин (506 мг, 5,00 ммоль) растворяли в тетрагидрофуране (20 мл). После добавления по каплям изобутилхлорформиата (683 мг, 5,00 ммоль) при температуре ниже -15°С и перемешивания к реакционной смеси в течение 30 минут добавляли пирролидин (782 мг, 11,0 ммоль) при температуре ниже -15°С и реакционную смесь дополнительно перемешивали при 0°С в течение 30 минут. Реакционную смесь подвергали распределению между этилацетатом и 1 н. водным раствором гидроксида натрия. Органический слой промывали 1 н. хлористоводородной кислотой, насыщенным водным раствором бикарбоната натрия и насыщенным раствором соли и сушили над безводным сульфатом магния. Растворитель отгоняли и остаток растворяли в смеси растворителей этилацетат (10 мл) - тетрагидрофуран (5 мл). Добавляли 4 н. раствор хлористоводородной кислоты в этилацетате (5 мл) и реакционную смесь перемешивали при комнатной температуре в течение 18 часов. После отгонки растворителя к сырому продукту добавляли этилацетат для осаждения кристаллов; кристаллы отфильтровывали и сушили при аэрировании с получением 2-амино-1-(пирролидин-1-ил)этанона гидрохлорида (573 мг, 4,16 ммоль, 84%) в виде белых кристаллов.
Указанное в заголовке соединение (74,7 мг, 0,171 ммоль, 86%) получали в виде белых кристаллов из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (104 мг, 0,200 ммоль), синтезированного в примере получения 5-2, и ранее полученного 2-амино-1-(пирролидин-1-ил)этанона гидрохлорида (165 мг, 1,00 ммоль), аналогично примеру 5.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,71-1,81 (2H, м), 1,83-1,93 (2H, м), 2,85 (3H, д, J=4,0 Гц), 3,26-3,40 (4H, м), 3,90 (2H, д, J=4,4 Гц), 6,55 (1H, дд, J=2,0, 6,0 Гц), 6,69 (1H, д, J=3,4 Гц), 6,94 (1H, д, J=2,0 Гц), 7,06 (1H, дд, J=2,0, 9,0 Гц), 7,38 (1H, д, J=2,0 Гц), 7,89 (1H, д, J=3,4 Гц), 8,05 (1H, д, J=6,0 Гц), 8,12-8,26 (2H, м), 8,30 (1H, д, J=9,0 Гц), 9,28 (1H, с).
Пример 8
Метиламид 5-(2-(3-(2-(4-гидрокси-4-метилпиперидин-1-ил)-2-оксоэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
4-Гидрокси-4-метилпиперидина гидрохлорид (113 мг, 0,745 ммоль) суспендировали в N,N-диметилформамиде (3 мл), затем добавляли триэтиламин (1 мл), туда добавляли бензотриазол-1-изоокситрис(диметиламино)фосфония гексафторфосфат (201 мг, 0,454 ммоль) и ((4-(1-метилкарбамоил-1H-индол-5-илокси)пиридин-2-ил)аминокарбониламино)уксусную кислоту (145 мг, 0,378 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 2 часов. После добавления воды к реакционной смеси производили экстракцию смесью этилацетат-тетрагидрофуран. Органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (Fuji Silysia NH силикагель; этилацетат, смесь этилацетат:метанол=20:1, 10:1, в данном порядке). После концентрирования при пониженном давлении продукт переводили в твердое состояние с помощью диэтилового эфира, суспендировали, отфильтровывали, промывали диэтиловым эфиром и сушили при аэрировании с получением указанного в заголовке соединения (137 мг, 0,285 ммоль, 75,4%) в виде бесцветного аморфного твердого вещества.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,10 (3H, с), 1,38-1,44 (4H, м), 2,83 (3H, д, J=3,6 Гц), 3,02 (2H, м), 3,90 (2H, м), 3,96 (2H, д, J=4,0 Гц), 4,37 (1H, с), 6,52 (1H, д, J=5,6 Гц), 6,67 (1H, д, J=3,2 Гц), 6,91 (1H, с), 7,04 (1H, д, J=9,0 Гц), 7,36 (1H, с), 7,87 (1H, д, J=3,2 Гц), 8,03 (1H, д, J=5,6 Гц), 8,17 (2H, м), 8,28 (1H, д, J=9,0 Гц), 9,27 (1H, с).
Исходные вещества синтезировали следующим образом.
Пример получения 8-1
((4-(1-Метилкарбамоил-1H-индол-5-илокси)пиридин-2-ил)аминокарбониламино)уксусная кислота
Метиламиноацетата гидрохлорид (300 мг, 2,3 ммоль) растворяли в N,N-диметилформамиде (4 мл) и затем добавляли триэтиламин (1 мл). Туда добавляли фенил N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамат (250 мг, 0,48 ммоль), синтезированный в примере получения 5-2. Реакционную смесь перемешивали при комнатной температуре в течение 22 часов. После добавления воды к реакционной смеси производили экстракцию смесью растворителей этилацетат-тетрагидрофуран. Органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали с помощью колоночной хроматографии на силикагеле (Fuji Silysia BW-300, этилацетат). Полученное бледно-желтое масло растворяли в смеси растворителей тетрагидрофуран (2 мл) - метанол (1 мл), после чего добавляли 4 н. водный раствор гидроксида лития (0,48 мл) и реакционную смесь перемешивали при комнатной температуре в течение 1 часа. После этого добавляли 1 н. хлористоводородную кислоту (2 мл) и содержимое подвергали экстракции смесью этилацетат-тетрагидрофуран. Органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния и концентрировали при пониженном давлении с получением указанного в заголовке соединения (145 мг, 0,38 ммоль, 79%) в виде бесцветных кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,83 (3H, д, J=3,6 Гц), 3,81 (2H, д, J=5,6 Гц), 6,57 (1H, м), 6,68 (1H, д, J=3,6 Гц), 6,84 (1H, с), 7,05 (1H, дд, J=2,0, 9,2 Гц), 7,38 (1H, д, J=2,0 Гц), 7,88 (1H, д, J=3,6 Гц), 8,05 (1H, д, J=5,6 Гц), 8,16-8,30 (3H, м), 9,33 (1H, уш.с).
Пример получения 8-2
Бензил-(4-гидрокси-4-метилпиперидин-1-ил)карбоксилат
Бензил-(4-оксопиперидин-1-ил)карбоксилат (4,7 г, 20 ммоль) растворяли в тетрагидрофуране (200 мл), туда по каплям добавляли раствор метиллитий-диэтиловый эфир (9,0 мл (1,02 М)+11,6 мл (1,14 М), суммарно 22 ммоль) (внутренняя температура -60°С или ниже) при перемешивании при -78°С в атмосфере азота и затем реакционную смесь перемешивали в течение 1,5 часов в данных условиях. С другой стороны сходную реакцию проводили с применением пиперидин-4-он-1-карбоксилата (1,1 г, 5,0 ммоль) в другой емкости. После добавления к каждой реакционной смеси насыщенного водного раствора хлорида аммония две реакционные смеси объединяли. Экстракцию проводили с помощью этилацетата, промывали насыщенным раствором соли, сушили над безводным сульфатом магния, концентрировали при пониженном давлении и очищали колоночной хроматографией на силикагеле (Fuji Silysia BW-300, система: гексан-этилацетат) с получением указанного в заголовке соединения (4,5 г, 18 ммоль, 73%) в виде бесцветных кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,10 (3H, с), 1,32-1,44 (4H, м), 3,17 (2H, м), 3,61 (2H, дт, J=3,6, 9,2 Гц), 4,34 (1H, с), 5,04 (2H, с), 7,27-7,37 (5H, м).
Пример получения 8-3
4-Гидрокси-4-метилпиперидина моногидрохлорид
Бензил-(4-гидрокси-4-метилпиперидин-1-ил)карбоксилат (4,5 г, 18 ммоль) растворяли в метаноле (90 мл), добавляли 10% палладий-на-порошке угля (0,60 г) и реакционную смесь перемешивали при комнатной температуре в атмосфере водорода в течение ночи. Катализатор удаляли фильтрацией и полученный раствор концентрировали при пониженном давлении с получением сырого продукта 4-гидрокси-4-метилпиперидина в виде бледно-желтого масла (2,1 г). После растворения продукта в метаноле добавляли 1 н. хлористоводородную кислоту (17,5 мл) и растворитель отгоняли при пониженном давлении. Полученные кристаллы суспендировали в ацетоне, кристаллы отфильтровывали, промывали ацетоном и сушили при аэрировании с получением указанного в заголовке соединения (2,1 г, 14 ммоль, 77%) в виде бесцветных кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,14 (3H, с), 1,55-1,69 (4H, м), 3,00 (4H, м), 4,68, (1H, уш.с), 8,77 (1H, уш.с), 8,89 (1H, уш.с).
Пример 9
Метиламид 5-(2-(3-((1S)-1-карбамоилэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
N1-Метил-5-((2-амино-4-пиридил)окси-1H-1-индолкарбоксамид (100 мг, 0,354 ммоль), синтезированный в примере получения 5-1, и триэтиламин (1 мл) растворяли в тетрагидрофуране (3 мл), затем по каплям добавляли фенилхлоркарбонат (0,0888 мл, 0,708 ммоль) при комнатной температуре и реакционную смесь перемешивали в течение 2 часов. После отгонки растворителя при пониженном давлении остаток растворяли в N,N-диметилформамиде (3 мл). Добавляли (2S)-2-аминопропионамида гидрохлорид (220 мг, 1,77 ммоль) и триэтиламин (1 мл) и реакционную смесь перемешивали в течение 18 часов. Реакционную смесь подвергали распределению между этилацетатом и насыщенным водным раствором хлорида аммония. Органический слой промывали насыщенным раствором соли и сушили над безводным сульфатом магния. Растворитель отгоняли и остаток очищали с помощью колоночной хроматографии на силикагеле (элюент: смесь этилацетат:метанол=20:1). Кристаллы осаждали из смеси растворителей этилацетат-гексан, отфильтровывали и сушили при аэрировании с получением указанного в заголовке соединения (38,5 мг, 0,0971 ммоль, 27%) в виде белых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,21 (3H, д, J=6,8 Гц), 2,85 (3H, д, J=4,0 Гц), 4,17 (1H, м), 6,55 (1H, д, J=5,2 Гц), 6,70 (1H, д, J=3,6 Гц), 6,93 (1H, с), 7,02 (1H, с), 7,06 (1H, дд, J=2,0, 8,8 Гц), 7,39 (1H, д, J=2,0 Гц), 7,46 (1H, с), 7,90 (1H, д, J=3,6 Гц), 8,06 (1H, д, J=5,2 Гц) 8,11 (1H, уш.с), 8,20 (1H, кв, J=4,0 Гц), 8,30 (1H, д, J=8,8 Гц), 9,21 (1H, уш.с).
Пример 10
Метиламид 5-(2-(3-((1S)-1-карбамоил-3-метилбутил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Аналогично примеру 9 указанное в заголовке соединение (59,5 мг, 0,135 ммоль, 38%) получали в виде белых кристаллов из N1-метил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамида (100 мг, 0,354 ммоль), синтезированного в примере получения 5-1, и (2S)-2-амино-4-метилпентанамида гидрохлорида (295 мг, 1,77 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,83-0,91 (6H, м), 1,35-1,50 (2H, м), 1,58 (1H, м), 2,85 (3H, д, J=4,4 Гц), 4,17 (1H, м), 6,53 (1H, дд, J=2,4, 6,0 Гц), 6,69 (1H, д, J=3,8 Гц), 6,92-7,01 (2H,м), 7,06 (1H, дд, J=2,4, 8,8 Гц), 7,38 (1H, д, J=2,4 Гц), 7,48 (1H, с), 7,89 (1H, д, J=3,8 Гц) 7,98-8,12 (2H, м), 8,19 (1H, кв, J=4,4 Гц), 8,30 (1H, д, J=8,8 Гц), 9,09 (1H, с).
Пример 11
Метиламид 5-(2-(3-карбамоилметилуреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (52,8 мг, 0,138 ммоль, 69%) получали в виде белых кристаллов из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (104 мг, 0,200 ммоль), синтезированного в примере получения 5-2, и глицинамида гидрохлорида (111 мг, 1,00 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,85 (3H, д, J=4,0 Гц), 3,70 (2H, д, J=5,2 Гц), 6,53 (1H, дд, J=2,4, 5,8 Гц), 6,69 (1H, д, J=3,4 Гц), 6,92 (1H, д, J=2,4 Гц), 7,01 (1H, с), 7,06 (1H, дд, J=2,4, 9,2 Гц), 7,34-7,42 (2H, м), 7,89 (1H, д, J=3,4 Гц), 8,05 (1H, д, J=5,8 Гц), 8,14-8,26 (2H, м), 8,30 (1H, д, J=9,2 Гц), 9,21 (1H, с).
Пример 12
Метиламид 5-(2-(3-циклопропилкарбамоилметилуреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (50,7 мг, 0,120 ммоль, 60%) получали в виде белого порошка из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (104 мг, 0,200 ммоль), синтезированного в примере получения 5-2, и 2-амино-N-циклопропилацетамида гидрохлорида (151 мг, 1,00 ммоль), полученного из трет-бутоксикарбониламиноуксусной кислоты и циклопропиламина способом, сходным с примером 7.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,36-0,42 (2H, м), 0,57-0,63 (2H, м), 2,60 (1H, м), 2,85 (3H, д, J=4,4 Гц), 3,68 (2H, д, J=5,2 Гц), 6,53 (1H, дд, J=2,0, 6,0 Гц), 6,69 (1H, д, J=3,6 Гц), 6,91 (1H, д, J=2,0 Гц), 7,06 (1H, дд, J=2,4, 9,0 Гц), 7,38 (1H, д, J=2,4 Гц), 7,89 (1H, д, J=3,6 Гц), 8,00 (1H, д, J=4,0 Гц), 8,06 (1H, д, J=6,0 Гц) 8,14-8,26 (2H, м), 8,30 (1H, д, J=9,0 Гц), 9,21 (1H, с).
Пример 13
Метиламид 5-(2-(3-((1S)-1-карбамоил-2-гидроксиэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Аналогично примеру 9 указанное в заголовке соединение (52,1 мг, 0,126 ммоль, 36%) получали в виде белых кристаллов из N1-метил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамида (100 мг, 0,354 ммоль), синтезированного в примере получения 5-1, и (2S)-2-амино-3-гидроксипропионамида гидрохлорида (249 мг, 1,77 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,85 (3H, д, J=4,4 Гц), 3,52 (1H, дд, J=4,8, 6,4 Гц), 3,62 (1H, дд, J=4,8, 6,4 Гц), 4,13 (1H, м), 4,94 (1H, уш.с), 6,53 (1H, дд, J=2,4, 6,0 Гц), 6,69 (1H, д, J=3,6 Гц), 6,99 (1H, с), 7,02-7,10 (2H, м), 7,35 (1H, с), 7,38 (1H, д, J=2,4 Гц), 7,89 (1H, д, J=3,6 Гц), 8,05 (1H, д, J=6,0 Гц), 8,10-8,26 (2H, м), 8,30 (1H, д, J=8,8 Гц), 9,22 (1H, с).
Пример 14
Метиламид 5-(2-(3-((1R)-1-карбамоил-2-гидроксиэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Аналогично примеру 9 указанное в заголовке соединение (56,0 мг, 0,136 ммоль, 68%) получали в виде белых кристаллов из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (104 мг, 0,200 ммоль), синтезированного в примере получения 5-2, и (2R)-2-амино-3-гидроксипропионамида гидрохлорида (167 мг, 1,00 ммоль), полученного из (2R)-2-(трет-бутоксикарбониламино)-3-гидроксипропионовой кислоты и водного аммиака способом, сходным с примером 7.
Пример 15
Диамид (2S)-2-(3-(4-(1-метилкарбамоил-1H-индол-5-илокси)пиридин-2-ил)уреидо)-1,5-пентандикарбоновой кислоты
Аналогично примеру 6 указанное в заголовке соединение (82,5 мг, 0,189 ммоль, 51%) получали в виде белого порошка из N1-метил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамида (100 мг, 0,354 ммоль), синтезированного в примере получения 5-1, и диамида (2S)-2-амино-1,5-пентандикарбоновой кислоты гидрохлорида (321 мг, 1,77 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,66-2,28 (4H, м), 2,85 (3H, д, J=4,4 Гц), 4,17 (1H, м), 6,53 (1H, дд, J=2,4, 6,0 Гц), 6,69 (1H, д, J=3,6 Гц), 6,72 (1H, с), 6,97 (1H, с), 7,01-7,10 (2H, м), 7,30 (1H, с), 7,38 (1H, д, J=2,4 Гц), 7,49 (1H, с), 7,76 (1H, с) 7,89 (1H, д, J=3,6 Гц), 8,06 (1H, д, J=6,0 Гц), 8,18 (1H, кв, J=4,4 Гц), 8,30 (1H, д, J=8,8 Гц), 9,13 (1H, с).
Пример 16
(2S)-2-(3-(4-(1-Метилкарбамоил-1H-индол-5-илокси)пиридин-2-ил)уреидо)сукцинамид
Аналогично примеру 6 указанное в заголовке соединение (65,7 мг, 0,150 ммоль, 42%) получали в виде белых кристаллов из N1-метил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамида (100 мг, 0,354 ммоль), синтезированного в примере получения 5-1, и (2S)-2-аминосукцинамида гидрохлорида (297 мг, 1,77 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,45 (2H, д, J=6,8 Гц), 2,85 (3H, д, J=3,6 Гц), 4,40 (1H, м), 6,53 (1H, дд, J=2,4, 6,0 Гц), 6,69 (1H, д, J=3,6 Гц), 6,88 (1H, с), 6,95 (1H, с), 7,00 (1H, д, J=2,4 Гц), 7,06 (1Н, дд, J=2,4, 9,2 Гц), 7,28 (1H, с), 7,35 (1H, с), 7,38 (1H, д, J=2,4 Гц), 7,89 (1H, д, J=3,6 Гц), 8,04 (1H, д, J=6,0 Гц), 8,18 (1H, кв, J=4,0 Гц), 8,26 (1H, уш.с), 8,30 (1H, д, J=9,2 Гц), 9,19 (1H, с).
Пример 17
Метиламид 5-(2-(3-((1S)-1-циклопропилкарбамоил-2-гидроксиэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (72,0 мг, 0,159 ммоль, 80%) получали в виде белого порошка из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (104 мг, 0,200 ммоль), синтезированного в примере получения 5-2, и (2S)-2-амино-N-циклопропил-3-гидроксипропионамида гидрохлорида (181 мг, 1,00 ммоль), полученного из (2S)-2-(трет-бутоксикарбониламино)-3-гидроксипропионовой кислоты и циклопропиламина способом, сходным с примером 7.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,35-0,44 (2H, м), 0,54-0,63 (2H, м), 2,62 (1H, м), 2,85 (3H, д, J=4,0 Гц), 3,45-3,58 (2H, м), 4,09 (1H, м), 4,91 (1H, т, J=5,2 Гц), 6,53 (1H, дд, J=2,0, 6,0 Гц), 6,69 (1H, д, J=3,6 Гц), 6,99 (1H, д, J=2,0 Гц), 7,04 (1H, дд, J=2,4, 8,8 Гц), 7,38 (1H, д, J=2,4 Гц), 7,89 (1H, д, J=3,6 Гц), 7,98 (1H, д, J=4,4 Гц), 8,05 (1H, д, J=6,0 Гц), 8,09-8,24 (2H, м), 8,30 (1H, д, J=8,8 Гц), 9,18 (1H, с).
Пример 18
Метиламид 5-(2-(3-((1S)-1-гидроксиметил-2-оксо-2-пирролидин-1-илэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (67,6 мг, 0,145 ммоль, 73%) получали в виде белого порошка из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (104 мг, 0,200 ммоль), синтезированного в примере получения 5-2, и (2S)-2-амино-3-гидрокси-1-(пирролидин-1-ил)пропан-1-она гидрохлорида (165 мг, 0,848 ммоль), полученного из (2S)-2-(трет-бутоксикарбониламино)-3-гидроксипропионовой кислоты и пирролидина способом, сходным с примером 7.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,72-1,81 (2H, м), 1,81-1,90 (2H, м), 2,85 (3H, д, J=4,4 Гц), 3,22-3,36 (2H, м), 3,46-3,60 (4H, м), 4,54 (1H, м), 4,98 (1H, уш.с), 6,54 (1H, дд, J=2,0, 5,6 Гц), 6,69 (1H, д, J=3,6 Гц), 6,97 (1H, д, J=2,0 Гц), 7,05 (1H, дд, J=2,4, 8,8 Гц), 7,38 (1H, д, J=2,4 Гц), 7,89 (1H, д, J=3,6 Гц), 8,05 (1H, д, J=5,6 Гц), 8,13-8,23 (2H, м), 8,30 (1H, д, J=8,8 Гц), 9,18 (1H, с).
Пример 19
Метиламид 5-(2-(3-((1R)-1-гидроксиметил-2-оксо-2-пирролидин-1-илэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (305 мг, 0,654 ммоль, 93%) получали в виде белого порошка из фенил N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (366 мг, 0,700 ммоль), синтезированного в примере получения 5-2, и (2R)-2-амино-3-гидрокси-1-(пирролидин-1-ил)пропан-1-она гидрохлорида, полученного из (2R)-2-(трет-бутоксикарбониламино)-3-гидроксипропионовой кислоты и пирролидина способом, сходным с примером 7.
Пример 20
Метиламид 5-(2-(3-((1S)-1-гидроксиметил-2-оксо-2-пиперидин-1-илэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (124 мг, 0,258 ммоль, 86%) получали в виде белых кристаллов из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (157 мг, 0,300 ммоль), синтезированного в примере получения 5-2, и (2S)-2-амино-3-гидрокси-1-(пиперидин-1-ил)пропан-1-она гидрохлорида (312 мг, 1,50 ммоль), полученного из (2S)-2-(трет-бутоксикарбониламино)-3-гидроксипропионовой кислоты и пиперидина способом, сходным с примером 7.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,36-1,61 (6H, м), 2,85 (3Н, д, J=4,4 Гц), 3,40-3,53 (6H, м), 4,76 (1H, м), 4,92 (1H, уш.с), 6,54 (1H, дд, J=2,4, 6,0 Гц), 6,69 (1H, д, J=3,6 Гц), 6,97 (1H, д, J=2,4 Гц), 7,06 (1H, дд, J=2,4, 9,0 Гц), 7,38 (1H, д, J=2,4 Гц), 7,89 (1H, д, J=3,6 Гц), 8,05 (1H, д, J=6,0 Гц), 8,10-8,26 (2H, м), 8,30 (1H, д, J=9,0 Гц), 9,21 (1H, с).
Пример 21
Метиламид 5-(2-(3-((1R)-1-гидроксиметил-2-оксо-2-пиперидин-1-илэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
(2R)-2-Бензилоксикарбониламино-3-гидроксипропионовую кислоту (1,91 г, 8,00 ммоль) и N-метоксиморфолин (809 мг, 8,00 ммоль) растворяли в тетрагидрофуране (20 мл). После добавления по каплям изобутилхлорформиата (1,09 г, 8,00 ммоль) при -15°С или ниже реакционную смесь перемешивали в течение 30 минут. Затем добавляли пирролидин (1,13 г, 16,0 ммоль) при -15°С или ниже и реакционную смесь дополнительно перемешивали при 0°С в течение 30 минут. Реакционную смесь подвергали распределению между этилацетатом и водой. Органический слой промывали 1 н. хлористоводородной кислотой, 1 н. водным раствором гидроксида натрия, насыщенным водным раствором бикарбоната натрия и насыщенным раствором соли и сушили над безводным сульфатом магния. Растворитель отгоняли и полученный остаток растворяли в смеси метанол (15 мл) - тетрагидрофуран (15 мл). Затем добавляли 10% палладий-на-угле (сырой) (300 мг) и реакционную смесь перемешивали при комнатной температуре под струей водорода в течение 90 минут. После удаления катализатора фильтрованием растворитель фильтрата отгоняли при пониженном давлении с получением (2R)-2-амино-3-гидрокси-1-(пиперидин-1-ил)пропан-1-она (684 мг, 3,97 ммоль, 50%) в виде бесцветного масла. Аналогично примеру 5 указанное в заголовке соединение (107 мг, 0,223 ммоль, 74%) получали в виде белых кристаллов из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (157 мг, 0,300 ммоль), синтезированного в примере получения 5-2, и ранее полученного (2R)-2-амино-3-гидрокси-1-(пиперидин-1-ил)пропан-1-она (228 мг, 1,32 ммоль).
Пример 22
Метиламид 5-(2-(3-((1S)-1-гидроксиметил-2-(4-гидроксипиперидин-1-ил)-2-оксоэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (118 мг, 0,238 ммоль, 69%) получали в виде белого порошка из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (179 мг, 0,343 ммоль), синтезированного в примере получения 5-2, и (2S)-2-амино-3-гидрокси-1-(4-гидроксипиперидин-1-ил)пропан-1-она гидрохлорида (385 мг, 1,71 ммоль), полученного из (2S)-2-(трет-бутоксикарбониламино)-3-гидроксипропионовой кислоты и 4-гидроксипиперидина способом, сходным с примером 7.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,16-1,40 (2H, м), 1,61-1,80 (2H, м), 2,85 (3H, д, J=4,0 Гц), 2,98-3,50 (5H, м), 3,63-3,95 (3H, м), 4,76 (1H, м), 4,92 (1H, уш.с), 6,55 (1H, дд, J=2,0, 6,0 Гц), 6,69 (1H, д, J=3,6 Гц), 6,96 (1H, д, J=2,0 Гц), 7,06 (1H, дд, J=2,4, 8,8 Гц), 7,38 (1H, д, J=2,4 Гц), 7,90 (1H, д, J=3,6 Гц), 8,05 (1H, д, J=6,0 Гц), 8,08-8,26 (2H, м), 8,30 (1H, д, J=8,8 Гц), 9,26 (1H, с).
Пример 23
Метиламид 5-(2-(3-((1S)-1-гидроксиметил-2-(морфолин-4-ил)-2-оксоэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (121 мг, 0,251 ммоль, 84%) получали в виде белых кристаллов из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (157 мг, 0,300 ммоль), синтезированного в примере получения 5-2, и (2S)-2-амино-3-гидрокси-1-(морфолин-4-ил)пропан-1-она гидрохлорида (316 мг, 1,50 ммоль), полученного из (2S)-2-(трет-бутоксикарбониламино)-3-гидроксипропионовой кислоты и морфолина способом, сходным с примером 7.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,85 (3H, д, J=4,4 Гц), 3,36-3,62 (10H, м), 4,74 (1H, м), 4,92 (1H, уш.с), 6,54 (1H, дд, J=2,4, 6,0 Гц), 6,69 (1H, д, J=3,6 Гц), 6,96 (1H, д, J=2,4 Гц), 7,06 (1H, дд, J=2,4, 8,8 Гц), 7,38 (1H, д, J=2,4 Гц), 7,89 (1H, д, J=3,6 Гц), 8,05 (1H, д, J=6,0 Гц), 8,14-8,28 (2H, м), 8,30 (1H, д, J=8,8 Гц), 9,25 (1H, с).
Пример 24
Метиламид 5-(2-(3-(2-циклопропилкарбамоилэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (117 мг, 0,268 ммоль, 89%) получали в виде белых кристаллов из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (157 мг, 0,300 ммоль), синтезированного в примере получения 5-2, и 3-амино-N-циклопропилпропионамида гидрохлорида (247 мг, 1,50 ммоль), полученного из 3-(трет-бутоксикарбониламино)пропионовой кислоты и циклопропиламина способом, сходным с примером 7.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,32-0,38 (2H, м), 0,54-0,60 (2H, м), 2,19 (2H, т, J=6,4 Гц), 2,60 (1H, м), 2,85 (3H, д, J=4,4 Гц), 3,25-3,33 (2H, м), 6,53 (1H, дд, J=2,0, 6,0 Гц), 6,69 (1H, д, J=3,6 Гц), 6,90 (1H, д, J=2,0 Гц), 7,05 (1H, дд, J=2,4, 9,0 Гц), 7,38 (1Н, д J=2,4 Гц), 7,89 (1H, д, J=3,6 Гц), 7,93 (1H, д, J=4,0 Гц), 7,96-8,06 (2H, м), 8,18 (1H, кв, J=4,4 Гц), 8,30 (1H, д, J=9,0 Гц), 9,08 (1H, с).
Пример 25
Метиламид 5-(2-(3-(3-оксо-3-(пирролидин-1-ил)пропил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (122 мг, 0,270 ммоль, 90%) получали в виде белых кристаллов из фенил- N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (157 мг, 0,300 ммоль), синтезированного в примере получения 5-2, и 3-амино-1-пирролидин-1-ил)пропан-1-она гидрохлорида (268 мг, 1,50 ммоль), полученного из 3-(трет-бутоксикарбониламино)пропионовой кислоты и пирролидина способом, сходным с примером 7.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,70-1,78 (2H, м), 1,80-1,88 (2H, м), 2,40 (2H, т, J=6,2 Гц), 2,85 (3H, д, J=4,4 Гц), 3,24-3,38 (6H, м), 6,52 (1H, дд, J=2,0, 5,6 Гц), 6,69 (1H, д, J=3,6 Гц), 6,92 (1H, д, J=2,0 Гц), 7,05 (1H, дд, J=2,4, 9,0 Гц), 7,38 (1H, д, J=2,4 Гц), 7,89 (1H, д, J=3,6 Гц), 7,98-8,10 (2H, м), 8,18 (1H, кв, J=4,4 Гц), 8,30 (1H, д, J=9,0 Гц), 9,10 (1H, с).
Пример 26
Метиламид 5-(2-(3-(3-(4-гидрокси-4-метилпиперидин-1-ил)-3-оксопропил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Указанное в заголовке соединение (177 мг, 0,358 ммоль, 71,1%) получали в виде бесцветных кристаллов путем проведения реакции аналогично примеру 8 с применением 3-(3-(4-(1-метилкарбамоил-1H-индол-5-илокси)пиридин-2-ил)уреидо)пропионовой кислоты (200 мг, 0,503 ммоль) и 4-гидрокси-4-метилпиперидина моногидрохлорида (114 мг, 0,755 ммоль, способ получения 8-3).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,07 (3H, с), 1,23-1,41 (4H, м), 2,44 (2H, д, J=4,8 Гц), 2,83 (3H, д, J=4,4 Гц), 2,98 (1H, м), 3,23-3,30 (3H, м), 3,46 (1H, м), 3,93 (1H, м), 4,32 (1H, с), 6,49 (1H, дд, J=2,0, 6,0 Гц), 6,67 (1H, д, J=3,4 Гц), 6,90 (1H, с), 7,03 (1H, дд, J=2,0, 8,8 Гц), 7,35 (1H, д, J=2,0 Гц), 7,87 (1H, д, J=3,4 Гц), 8,00 (2H, м), 8,15 (1H, д, J=4,4 Гц), 8,28 (1H, д, J=8,8 Гц), 9,06 (1Н, с).
Исходное вещество синтезировали следующими способами.
Пример получения 26-1
3-(3-(4-(1-Метилкарбамоил-1H-индол-5-илокси)пиридин-2-ил)уреидо)пропионовая кислота
Этил-4-аминопропионата гидрохлорид (588 мг, 3,8 ммоль) суспендировали в N,N-диметилформамиде (3,0 мл), затем добавляли 5 н. водный раствор гидроксида натрия (0,77 мл, 3,8 ммоль) и реакционную смесь перемешивали при комнатной температуре. Туда добавляли фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамат (400 мг, 0,77 ммоль, пример получения 5-2) и реакционную смесь перемешивали при комнатной температуре в течение 0,75 часа. К реакционной смеси добавляли воду и содержимое подвергали экстракции смесью этилацетата-тетрагидрофурана, сушке над безводным сульфатом магния и концентрированию при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia BW-300, этилацетат) с получением бледно-коричневого масла. Данное масло растворяли в тетрагидрофуране (4,0 мл) и метаноле (2,0 мл), добавляли 4 н. водный раствор гидроксида лития (0,77 мл) при комнатной температуре и реакционную смесь перемешивали при комнатной температуре в течение 1,5 часов. К реакционной смеси добавляли 1 н. хлористоводородную кислоту (3,1 мл) при перемешивании при комнатной температуре; содержимое подвергали экстракции смесью этилацетат-тетрагидрофуран, промывали насыщенным раствором соли, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. К полученному аморфному твердому веществу добавляли небольшое количество ацетона и данный раствор разбавляли диэтиловым эфиром. Кристаллы отфильтровывали, промывали диэтиловым эфиром и сушили при аэрировании с получением указанного в заголовке соединения (200 мг, 0,50 ммоль, 66%) в виде бесцветных кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,39 (2H, т, J=6,2 Гц), 2,84 (3H, д, J=4,0 Гц), 3,30 (2H, м), 6,51 (1H, д, J=5,8 Гц), 6,68 (1H, д, J=3,2 Гц), 6,87 (1H, с), 7,05 (1H, д, J=9,0 Гц), 7,37 (1H, с), 7,88 (1H, д, J=3,2 Гц), 8,01 (1H, д, J=5,8 Гц), 8,16 (1H, м), 8,17 (1H, д, J=4,0 Гц), 8,29 (1H, д, J=9,0 Гц), 9,10 (1H, с), 12,24 (1H, с).
Пример 27
N1-Этил-5-(2-(((2-этоксиэтил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Фенил-N-(4-(1-(этиламино)карбонил-1H-5-индолил)окси-2-пиридил)карбамат (100 мг, 0,24 ммоль) растворяли в N,N-диметилформамиде (1,0 мл) и добавляли 2-этоксиэтиламин (0,063 мл, 0,6 ммоль) при перемешивании при комнатной температуре. Через 1 час реакционную смесь подвергали распределению между этилацетатом и водой. Органический слой промывали водой и насыщенным раствором соли и сушили над безводным сульфатом натрия. После отгонки растворителя кристаллы осаждали из смеси этилацетат-гексан (1:5), отфильтровывали и сушили при аэрировании с получением указанного в заголовке соединения (100 мг, 0,24 ммоль, количественный выход) в виде белых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,09 (3H, т, J=7,2 Гц), 1,17 (3H, т, J=7,2 Гц), 3,21-3,45 (8H, м), 6,50 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 6,87 (1H, уш.с), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,36 (1H, д, J=2,4 Гц), 7,91 (1H, д, J=3,6 Гц), 8,01 (1H, д, J=5,6 Гц), 8,12 (1H, м), 8,22 (1H, т, J=4,8 Гц), 8,28 (1H, д, J=8,8 Гц), 9,08 (1H, с).
Исходные вещества синтезировали следующими способами.
Пример получения 27-1
N1-Этил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамид
Гидрид натрия (573 мг, 14,32 ммоль) суспендировали в N,N-диметилформамиде (30 мл) в атмосфере азота. К нему постепенно добавляли 4-(1H-5-индолилокси)-2-пиримидинамин (3,00 г, 13,32 ммоль, CAS No. 417722-11-3), описанный в WO 02/32872, при перемешивании при комнатной температуре. Через 10 минут реакционную смесь охлаждали с помощью водно-ледяной бани и добавляли фенил-N-этилкарбамат (2,31 г, 13,98 ммоль). Реакционную смесь нагревали до комнатной температуры и перемешивали в течение 2 часов. Реакционную смесь подвергали распределению между этилацетатом и водой.
Органический слой промывали водой и насыщенным раствором соли и сушили над безводным сульфатом натрия. Растворитель отгоняли, после чего кристаллы осаждали из этилацетата, отфильтровывали и сушили при аэрировании с получением указанного в заголовке соединения (3,168 г, 10,69 ммоль, 80,3%) в виде бледно-коричневых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,32 (3H, т, J=7,2 Гц), 2,40-2,50 (2H, м), 5,74 (1H, д, J=2,4 Гц), 5,83 (2H, уш.с), 6,12 (1H, дд, J=2,4, 5,6 Гц), 6,66 (1Н, д, J=3,6 Гц), 7,01 (1H, дд, J=2,4, 8,8 Гц), 7,32 (1H, д, J=2,4 Гц), 7,75 (1H, д, J=5,6 Гц), 7,88 (1H, д, J=3,6 Гц), 8,19 (1H, т, J=5,6 Гц), 8,26 (1H, д, J=8,8 Гц).
Пример получения 27-2
Фенил-N-(4-(1-(этиламино)карбонил-1H-5-индолил)окси-2-пиридил)карбамат
N1-Этил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамид (3,168 г, 10,69 ммоль), синтезированный в примере получения 27-1, растворяли в N,N-диметилформамиде (30 мл) в атмосфере азота. Последовательно по каплям добавляли пиридин (1,25 мл, 15,40 ммоль) и фенилхлоркарбонат (1,61 мл, 12,83 ммоль) при охлаждении с помощью водно-ледяной бани. Реакционную смесь нагревали до комнатной температуры при перемешивании. Через 1 час реакционную смесь подвергали распределению между этилацетатом и водой. Органический слой промывали водой и насыщенным раствором соли и сушили над безводным сульфатом натрия. Растворитель отгоняли и кристаллы осаждали из этилацетата, отфильтровывали и сушили при аэрировании с получением указанного в заголовке соединения (1,530 г, 3,67 ммоль, 34,4%) в виде белых кристаллов.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 1,32 (3H, т, J=7,2 Гц), 3,53 (2H, м), 5,48 (1H, м), 6,58 (1H, д, J=4,0 Гц), 6,62 (1H, дд, J=2,4, 5,6 Гц), 7,06 (1H, дд, J=2,4, 8,8 Гц), 7,15 (2H, м), 7,20-7,27 (1H, м), 7,30 (1H, д, J=2,4 Гц), 7,37 (2H, м), 7,45 (1H, д, J=4,0 Гц), 7,52 (1H, д, J=2,4 Гц), 8,10-8,15 (3H, м).
Пример 28
N1-Метил-5-(2-((4-(2-гидрокси-2-метилпропионил)пиперазин-1-ил)карбонил)амино-4-пиридил)окси-1H-индолкарбоксамид
N1-Метил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамид (150 мг, 0,53 ммоль), синтезированный в примере получения 5-1, растворяли в тетрагидрофуране (3 мл). Последовательно по каплям добавляли триэтиламин (0,37 мл, 2,66 ммоль) и фенилхлоркарбонат (0,15 мл, 1,2 ммоль) при комнатной температуре и реакционную смесь перемешивали в течение 30 минут. Добавляли 1-(2-гидрокси-2-метилпропионил)пиперазин (412 мг, 2,39 ммоль) и N,N-диметилформамид (3 мл) и реакционную смесь перемешивали в течение 3 дней. Реакционную смесь подвергали распределению между этилацетатом и водой. Органический слой промывали водой и насыщенным раствором соли и сушили над безводным сульфатом натрия. Растворитель отгоняли и остаток очищали колоночной хроматографией на силикагеле (элюент: смесь этилацетат:метанол=95:5). Кристаллы осаждали из смеси диэтиловый эфир-гексан (1:2), отфильтровывали и сушили при аэрировании с получением указанного в заголовке соединения (189,4 мг, 0,39 ммоль, 74,2%) в виде белых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,28 (6H, с), 2,83 (3H, д, J=4,0 Гц), 3,10-3,50 (8H, м), 5,43 (1H, с), 6,56 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,30 (1H, д, J=2,4 Гц), 7,36 (1H, д, J=2,4 Гц), 7,87 (1H, д, J=3,6 Гц), 8,08 (1H, д, J=5,6 Гц), 8,16 (1H, кв, J=4,0 Гц), 8,28 (1H, д, J=8,8 Гц), 9,21 (1H, с).
1-(2-Гидрокси-2-метилпропионил)пиперазин синтезировали следующими способами.
Пример получения 28-1
Бензил-4-(2-гидрокси-2-метилпропионил)пиперазин-1-карбоксилат
Бензилпиперазин-1-карбамат (2,203 г, 10,0 ммоль) растворяли в тетрагидрофуране (50 мл), добавляли 2-гидрокси-2-метилпропионовую кислоту (1,25 г, 12,0 ммоль), 1-этил-3-(3-диметиламинопропил)карбодиимида гидрохлорид (2,30 г, 12,0 ммоль), 1-гидрокси-1H-бензотриазола моногидрат (1,84 г, 12,0 ммоль) и триэтиламин (3,35 мл, 24,0 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 7 часов. Реакционную смесь подвергали распределению между этилацетатом и 1 н. хлористоводородной кислотой. Органический слой промывали водой, насыщенным водным раствором бикарбоната натрия и насыщенным раствором соли и сушили над безводным сульфатом натрия. Растворитель отгоняли и сушили при пониженном давлении с получением указанного в заголовке соединения (2,823 г, 9,21 ммоль, 92,1%) в виде бесцветного масла.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 1,50 (6H, с), 3,52-3,55 (4H, м), 3,60-3,70 (4H, м), 3,93 (1H, с), 5,16 (2H, с), 7,34-7,38 (5H, м).
Пример получения 28-2
1-(2-Гидрокси-2-метилпропионил)пиперазин
Бензил-4-(2-гидрокси-2-метилпропионил)пиперазин-1-карбамат (2,82 г, 9,20 ммоль), синтезированный в примере получения 28-1, растворяли в метаноле (100 мл) в атмосфере азота, туда добавляли 10% палладий-на-угле (50% влажность, 1,96 г), реакционную систему продували водородом при атмосферном давлении и реакционную смесь перемешивали в течение ночи. После продувания реакционной системы азотом катализатор отфильтровывали и промывали метанолом, после чего растворитель вместе с фильтратом и промывающим раствором отгоняли. Остаток сушили при пониженном давлении с получением указанного в заголовке соединения (1,58 г, 9,20 ммоль, количественный выход) в виде бесцветного масла.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 1,49 (6H, с), 2,84-2,94 (4H, м), 3,49 (1H, с), 3,62-3,70 (4H, м).
Пример 29
N1-Метил-5-(2-((3-диэтиламино)пропиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 27 указанное в заголовке соединение (96,4 мг, 0,22 ммоль, 73,3%) получали в виде белых кристаллов из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолил)окси)-2-пиридил)карбамата (121 мг, 0,30 ммоль) и 3-(диэтиламино)пропиламина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,91 (6H, т, J=7,2 Гц), 1,50 (2H, м), 2,30-2,44 (6H, м), 2,83 (3H, д, J=4,4 Гц), 3,23 (2H, м), 6,50 (1H, дд, J=2,4, 6,0 Гц), 6,68 (1H, д, J=3,6 Гц), 6,82 (1H, с), 7,04 (1H, дд, J=2,4, 8,8 Гц), 7,37 (1H, д, J=2,4 Гц), 7,87 (1H, д, J=3,6 Гц), 8,01 (1H, д, J=6,0 Гц), 8,10-8,17 (2H, м), 8,29 (1H, д, J=8,8 Гц), 9,04 (1H, с).
Исходное вещество синтезировали следующим образом.
Пример получения 29-1
Фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолил)окси)-2-пиридил)карбамат
N1-Метил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамид (2,163 г, 7,66 ммоль), синтезированный в примере получения 5-1, растворяли в N,N-диметилформамиде (50 мл) в атмосфере азота, последовательно по каплям добавляли пиридин (0,93 мл, 11,5 ммоль), триэтиламин (2,4 мл, 17,24 ммоль) и фенилхлоркарбонат (1,44 мл, 11,5 ммоль) при охлаждении с помощью водно-ледяной бани и реакционную смесь нагревали до комнатной температуры при перемешивании. Через 1 час реакционную смесь подвергали распределению между этилацетатом и водой. Органический слой промывали водой и насыщенным раствором соли и сушили над безводным сульфатом натрия. Растворитель отгоняли, после чего остаток очищали колоночной хроматографией на силикагеле (элюент: этилацетат), осаждали из смеси этилацетат-гексан (1:10), отфильтровывали и сушили при аэрировании с получением указанного в заголовке соединения (2,731 г, 6,79 ммоль, 88,6%) в виде белых кристаллов.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 3,09 (3H, д, J=4,8 Гц), 5,52 (1H, м), 6,62 (1H, д, J=3,6 Гц), 6,98 (1H, дд, J=2,4, 5,6 Гц), 7,01 (1H, д, J=2,4 Гц), 7,11 (1H, дд, J=2,4, 8,8 Гц), 7,14-7,40 (7H, м), 7,47 (1H, д, J=3,6 Гц), 8,24 (1H, д, J=8,8 Гц), 8,41 (1H, д, J=5,6 Гц).
Пример 30
N1-Метил-5-(2-(((3-(-4-гидроксипиперидин)пропил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 27 указанное в заголовке соединение (51,3 мг, 0,11 ммоль, 29,5%) получали в виде белых кристаллов из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолил)окси-2-пиридил)карбамата (150 мг, 0,37 ммоль, пример получения 29-1)) и 1-(3-аминопропил)-4-гидроксипиперидина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,29-1,38 (2H, м), 1,50-1,55 (2H, м), 1,64-1,68 (2H, м), 1,88-1,92 (2H, м), 2,20-2,24 (2H, м), 2,62-2,66 (2H, м), 2,83 (3H, д, J=4,4 Гц), 3,06-3,12 (2H, м), 3,39 (1H, м), 4,49 (1H, д, J=4,0 Гц), 6,50 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 6,84 (1H, с), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,36 (1H, с), 7,87 (1H, д, J=3,6 Гц), 8,01 (1H, д, J=5,6 Гц), 8,05 (1H, м), 8,16 (1H, кв, J=4,4 Гц), 8,28 (1H, д, J=8,8 Гц), 9,02 (1H, с).
Пример 31
N1-Метил-5-(2-(((3-(4-метилпиперазин-1-ил)пропил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 27 указанное в заголовке соединение (133,2 мг, 0,29 ммоль, 76,8%) получали в виде белых кристаллов из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолил)окси-2-пиридил)карбамата (150 мг, 0,37 ммоль, пример получения 29-1) и 1-(3-аминопропил)-4-метилпиперазина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,53 (2H, м), 2,11 (3H, с), 2,11-2,40 (10H, м), 2,83 (3H, д, J=4,0 Гц), 3,09 (2H, м), 6,50 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 6,84 (1H, с), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,36 (1H, д, J=2,4 Гц), 7,87 (1H, д, J=3,6 Гц), 8,01, (1H, д, J=5,6 Гц), 8,05 (1H, м), 8,16 (1H, кв, J=4,0 Гц), 8,28 (1H, д, J=8,8 Гц), 9,01 (1H, с).
Пример 32
Метиламид 5-(2-(3-(4-оксо-4-(пирролидин-1-ил)бутил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Указанное в заголовке соединение (113 мг, 0,24 ммоль, 77%) получали в виде бесцветных кристаллов путем проведения реакции, сходной с примером 8, с применением 4-((4-(1-метилкарбамоил-1H-индол-5-илокси)пиридин-2-ил)аминокарбониламино)масляной кислоты (130 мг, 0,31 ммоль) и пирролидина (0,053 мл, 0,63 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,64 (2H, м), 1,71 (2H, м), 1,82 (2H, м), 2,20 (2H, т, J=6,8 Гц), 2,83 (3H, д, J=4,0 Гц), 3,09 (2H, кв, J=6,8 Гц), 3,22 (2H, т, J=6,8 Гц), 3,33 (2H, м), 6,50 (1H, дд, J=2,4, 5,8 Гц), 6,67 (1H, д, J=3,6 Гц), 6,86 (1H, д, J=2,4 Гц), 7,03 (1H, дд, J=2,4, 9,0 Гц), 7,36 (1H, д, J=2,4 Гц), 7,87 (1H, д, J=3,6 Гц), 8,00 (1H, м), 8,03 (1H, д, J=5,8 Гц), 8,16 (1H, м), 8,28 (1H, д, J=9,0 Гц), 9,00 (1H, с).
Исходное вещество синтезировали следующими способами.
Пример получения 32-1
4-((4-(1-Метилкарбамоил-1H-индол-5-илокси)пиридин-2-ил)аминокарбониламино)масляная кислота
Этил-4-аминобутирата гидрохлорид (1,0 г, 6,0 ммоль) суспендировали в N,N-диметилформамиде (6,7 мл), добавляли 5 н. водный раствор гидроксида натрия (1,2 мл, 6,0 ммоль) и реакционную смесь перемешивали при комнатной температуре. Туда добавляли фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамат (700 мг, 1,3 ммоль, пример получения 5-2) и реакционную смесь перемешивали при комнатной температуре в течение 1,2 часов. Реакционную смесь подвергали распределению между этилацетатом и водой. Органический слой сушили над безводным сульфатом магния, концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia BW-300, этилацетат) с получением бледно-желтого масла. Данное масло растворяли в тетрагидрофуране (6,0 мл) и метаноле (3,0 мл), туда добавляли 4 н. гидроксид лития (1,1 мл) при комнатной температуре и реакционную смесь перемешивали при комнатной температуре в течение 3,5 часов. Затем туда добавляли 1 н. хлористоводородную кислоту (4,4 мл) и воду (2 мл) при перемешивании при комнатной температуре и содержимое подвергали экстракции этилацетатом, промывали насыщенным раствором соли, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. После суспендирования выпавших кристаллов в смеси диэтиловый эфир:гексан=1:1 кристаллы отфильтровывали, промывали диэтиловым эфиром и сушили при аэрировании с получением указанного в заголовке соединения (411 мг, 1,0 ммоль, 75%) в виде бесцветных кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,63 (2H, м), 2,20 (2H, т, J=7,4 Гц), 2,83 (3H, д, J=4,0 Гц), 3,10 (2H, м), 6,52 (1H, д, J=5,4 Гц), 6,68 (1H, д, J=3,6 Гц), 6,87 (1H, с), 7,04 (1H, дд, J=2,4, 9,0 Гц), 7,37 (1H, д, J=2,4 Гц), 7,88 (1H, д, J=3,6 Гц), 8,03 (2H, м), 8,17 (1H, д, J=4,0 Гц), 8,29 (1H, д, J=9,0 Гц), 9,03 (1H, с), 12,05 (1H, с).
Пример 33
Метиламид 5-(2-(3-(3-(циклопропилкарбонил)пропил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Указанное в заголовке соединение (166 мг, 0,37 ммоль, 76%) получали в виде бесцветных кристаллов путем проведения реакции, сходной с примером 8, с применением 4-((4-(1-метилкарбамоил-1H-индол-5-илокси)пиридин-2-ил)аминокарбониламино)масляной кислоты (200 мг, 0,49 ммоль, пример получения 32-1) и циклопропиламина (0,028 мл, 0,58 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,33-0,37 (2H, м), 0,54-0,59 (2H, м), 1,62 (2H, м), 2,02 (2H, т, J=7,4 Гц), 2,58 (1H, м), 2,85 (3H, м), 3,08 (2H, м), 6,53 (1H, дд, J=2,4, 6,0 Гц), 6,70 (1H, д, J=3,6 Гц), 6,88 (1H, д, J=2,4 Гц), 7,06 (1H, дд, J=2,4, 8,8 Гц), 7,39 (1H, д, J=2,4 Гц), 7,86 (1H, д, J=3,6 Гц), 7,90 (1H, д, J=3,6 Гц), 8,04 (1H, м), 8,05 (1H, д, J=6,0 Гц), 8,19 (1H, д, J=4,2 Гц), 8,31 (1H, д, J=8,8 Гц), 9,04 (1H, с).
Пример 34
Метиламид 5-(2-(3-(4-(4-гидрокси-4-метилпиперидин-1-ил)-4-оксобутил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Указанное в заголовке соединение (195 мг, 0,383 ммоль, 78,9%) получали в виде бесцветных кристаллов путем проведения реакции, сходной с примером 8, с применением 4-((4-(1-метилкарбамоил-1H-индол-5-илокси)пиридин-2-ил)аминокарбониламино)масляной кислоты (200 мг, 0,486 ммоль, пример получения 32-1) и 4-гидрокси-4-метилпиперидина моногидрохлорида (110 мг, 0,729 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,08 (3H, с), 1,22-1,44 (4H, м), 1,62 (2H, м), 2,27 (2H, т, J=7,4 Гц), 2,83 (3H, д, J=4,0 Гц), 2,97 (1H, м), 3,08 (2H, м), 3,29 (1H, м), 3,47 (1H, м), 3,89 (1H, м), 4,33 (1H, с), 6,50 (1H, д, J=6,0 Гц), 6,67 (1H, д, J=3,6 Гц), 6,87 (1H, с), 7,04 (1H, д, J=9,2 Гц), 7,36 (1H, с), 7,87 (1H, д, J=3,6 Гц), 8,01 (1H, м), 8,02 (1H, д, J=6,0 Гц), 8,16 (1H, м), 8,28 (1H, д, J=9,2 Гц), 9,00 (1H, м).
Пример 35
Метиламид 5-(2-(3-(3-(диэтилкарбамоил)пропил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Указанное в заголовке соединение (94 мг, 0,20 ммоль, 64%) получали в виде бесцветных кристаллов путем проведения реакции, сходной с примером 8, с применением 4-((4-(1-метилкарбамоил-1H-индол-5-илокси)пиридин-2-ил)аминокарбониламино)масляной кислоты (130 мг, 0,31 ммоль, пример получения 32-1) и диэтиламина (0,066 мл, 0,63 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,96 (3H, т, J=7,2 Гц), 1,04 (3H, т, J=7,2 Гц), 1,63 (2H, м), 2,25 (2H, т, J=7,2 Гц), 2,83 (3H, д, J=4,4 Гц), 3,09 (2H, м), 3,22 (4H, м), 6,51 (1H, дд, J=2,0, 5,6 Гц), 6,67 (1H, д, J=3,4 Гц), 6,86 (1H, д, J=2,0 Гц), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,36 (1H, д, J=2,4 Гц), 7,87 (1H, д, J=3,4 Гц), 8,02 (2H, м), 8,16 (1H, д, J=4,4 Гц), 8,29 (1H, д, J=8,8 Гц), 9,00 (1H, с).
Пример 36
Метиламид 5-(2-(3-(3-(метилкарбамоил)пропил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Указанное в заголовке соединение (107 мг, 0,25 ммоль, 69%) получали в виде бесцветных кристаллов путем проведения реакции, сходной с примером 8, с применением 4-((4-(1-метилкарбамоил-1H-индол-5-илокси)пиридин-2-ил)аминокарбониламино)масляной кислоты (150 мг, 0,36 ммоль, пример получения 32-1) и метиламина гидрохлорида (49 мг, 0,73 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,61 (2H, м), 2,03 (2H, т, J=7,6 Гц), 2,51 (3H, д, J=4,4 Гц), 2,83 (3H, д, J=4,0 Гц), 3,06 (2H, кв, J=6,4 Гц), 6,50 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 6,86 (1H, д, J=2,4 Гц), 7,03 (1H, дд, J=2,4, 9,2 Гц), 7,36 (1H, д, J=2,4 Гц), 7,71 (1H, м), 7,87 (1H, д, J=3,6 Гц), 8,03 (2H, м), 8,16 (1H, д, J=4,4 Гц), 8,28 (1H, д, J=9,2 Гц), 9,01 (1H, с).
Пример 37
N1-Метил-5-(2-(пирролидин-1-илкарбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 5 указанное в заголовке соединение (265 мг, 0,70 ммоль, 69%) получали в виде белых кристаллов из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (532 мг, 1,02 ммоль), синтезированного в примере получения 5-2, и пирролидина (0,42 мл, 5,0 ммоль).
МС-спектр (ESI): 380 (M+1), 759 (2M+1).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,78-1,84 (4H, м), 2,83 (3H, д, J=4,5 Гц), 3,22-3,36 (4H, м), 6,54 (1H, дд, J=2,3, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 7,03 (1H, дд, J=2,3, 8,7 Гц), 7,35 (1H, д, J=2,3 Гц), 7,41 (1H, д, J=2,3 Гц), 7,87 (1H, д, J=3,6 Гц), 8,04 (1H, д, J=5,6 Гц), 8,16 (1H, м), 8,28 (1H, т, J=8,7 Гц), 8,59 (1H, с).
Пример 38
N1-Метил-5-(2-(пиперидин-1-илкарбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 5 указанное в заголовке соединение (265 мг, 0,674 ммоль, 76%) получали в виде белых кристаллов из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (463 мг, 0,885 ммоль), синтезированного в примере получения 5-2, и пиперидина (0,44 мл, 4,4 ммоль).
МС-спектр (ESI): 394 (M+1), 787 (2M+1).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,37-1,57 (6H, м), 2,83 (3H, д, J=4,4 Гц), 3,26-3,45 (4H, м), 6,54 (1H, дд, J=2,4, 5,4 Гц), 6,67 (1H, д, J=3,4 Гц), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,30 (1H, д, J=2,4 Гц), 7,36 (1H, д, J=2,4 Гц), 7,87 (1H, д, J=3,4 Гц), 8,05 (1H, д, J=5,4 Гц), 8,16 (1H, м), 8,28 (1H, т, J=8,8 Гц), 9,05 (1H, с).
Пример 39
N1-Метил-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 27 указанное в заголовке соединение (86,7 мг, 0,21 ммоль, 21,2%) получали в виде белого порошка из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)карбамата (402 мг, 1,0 ммоль), синтезированного в примере получения 29-1, и 4-гидроксипиперидина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,60-1,70 (2H, м), 1,75 (1H, м), 2,83 (3H, д, J=4,4 Гц), 2,95-3,01 (2H, м), 3,55-3,65 (2H, м), 3,71-3,76 (2H, м), 4,64 (1H, д, J=4,0 Гц), 6,53 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,32 (1H, д, J=2,4 Гц), 7,36 (1H, д, J=2,4 Гц), 7,87 (1H, д, J=3,6 Гц), 8,06 (1H, д, J=5,6 Гц), 8,16 (1H, кв, J=4,4 Гц), 8,28 (1H, д, J=8,8 Гц), 9,10 (1H, с).
Пример 40
N1-Метил-5-(2-(4-оксопиперидин-1-илкарбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамат (440 мг, 0,841 ммоль), синтезированный в примере получения 5-2, растворяли в N,N-диметилформамиде (5 мл), туда добавляли триэтиламин (0,543 мл, 3,90 ммоль) и 4-пиперидона гидрохлорида моногидрат (0,530 г, 3,93 ммоль) и реакционную смесь перемешивали в течение 2 часов. Реакционную смесь подвергали распределению между этилацетатом и водой. Органический слой концентрировали с получением указанного в заголовке соединения (0,202 г, 0,496 ммоль, 59%) в виде бесцветного аморфного твердого вещества.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,32 (4H, т, J=4,9 Гц), 2,82 (3H, д, J=4,3 Гц), 3,68 (4H, т, J=4, 9 Гц), 6,55 (1H, дд, J=2,3, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 7,03 (1H, дд, J=2,3, 8,6 Гц), 7,37 (2H, с), 7,87 (1H, д, J=3,6 Гц), 8,09 (1H, д, J=5,6 Гц), 8,17 (1H, с), 8,28 (1H, т, J=8,6 Гц), 9,37 (1H, с).
Пример 41
Метиламид 5-(2-(((4-гидрокси-4-метилпиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индол-1-карбоновой кислоты
4-Гидрокси-4-метилпиперидина моногидрохлорид (508 мг, 3,83 ммоль, пример получения 8-3) растворяли в N,N-диметилформамиде (8 мл), добавляли триэтиламин (2 мл) и реакционную смесь перемешивали при комнатной температуре. Добавляли фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамат (500 мг, 0,957 ммоль, пример получения 5-2) и реакционную смесь перемешивали при комнатной температуре в течение 8 часов. Реакционную смесь подвергали распределению между этилацетатом и водой. Органический слой сушили над безводным сульфатом магния и концентрировали при пониженном давлении; остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia BW-300, этилацетат, смесь этилацетат:метанол=20:1, затем 10:1). Полученное аморфное твердое вещество кристаллизовали добавлением смеси диэтиловый эфир:ацетон=2:1. Полученные таким образом кристаллы отфильтровывали, промывали диэтиловым эфиром и сушили при аэрировании с получением указанного в заголовке соединения (385 мг, 0,909 ммоль, 95,0%).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,08 (3H, с), 1,33-1,40 (4H, м), 2,83 (3H, д, J=4,4 Гц), 3,14 (2H, м), 3,63 (2H, м), 4,27 (1H, с), 6,53 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,4 Гц), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,32 (1H, д, J=2,4 Гц), 7,35 (1H, д, J=2,4 Гц), 7,87 (1H, д, J=3,4 Гц), 8,06 (1H, д, J=5,6 Гц), 8,16 (1H, м), 8,28 (1H, д, J=8,8 Гц), 9,04 (1H, с).
Пример 42
N1-Метил-5-(2-((4-(1-гидрокси-1-метилэтил)пиперидин)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (71,1 мг, 0,16 ммоль, 29,7%) получали в виде белых кристаллов из N1-этил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамида (150 мг, 0,53 ммоль), синтезированного в примере получения 5-1, и 4-(1-гидрокси-1-метилэтил)пиперидина (342 мг, 2,39 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,99 (6H, с), 1,03-1,09 (2H, м), 1,30 (1H, м), 1,60-1,64 (2H, м), 2,54-2,61 (2H, м), 2,83 (3H, д, J=4,4 Гц), 4,08 (1H, с), 4,10-4,15 (2H, м), 6,53 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,32 (1H, д, J=2,4 Гц), 7,36 (1H, д, J=2,4 Гц), 7,87 (1H, д, J=3,6 Гц), 8,06 (1H, д, J=5,6 Гц), 8,16 (1H, кв, J=4,0 Гц), 8,27 (1H, д, J=8,8 Гц), 9,04 (1H, с).
4-(1-Гидрокси-1-метилэтил)пиперидин синтезировали следующими способами.
Пример получения 42-1
Бензил-4-этоксикарбонилпиперидин-1-карбоксилат
4-Этоксикарбонилпиперидин (1,572 г, 10,0 ммоль) растворяли в тетрагидрофуране (50 мл), по каплям при охлаждении с помощью водно-ледяной бани добавляли триэтиламин (2,79 мл, 20,0 ммоль) и бензилхлоркарбонат (1,71 мл, 12,0 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение ночи. Реакционную смесь подвергали распределению между этилацетатом и насыщенным водным раствором бикарбоната натрия. Органический слой промывали насыщенным раствором соли и сушили над безводным сульфатом натрия. Растворитель отгоняли и остаток очищали с помощью колоночной хроматографии на силикагеле (элюент: смесь этилацетат:гексан=1:3) с получением указанного в заголовке соединения (2,315 г, 7,95 ммоль, 79,5%) в виде бесцветного масла.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 1,26 (3H, т, J=7,2 Гц), 1,60-1,70 (2H, м), 1,80-2,00 (2H, м), 2,46 (1H, м), 2,80-3,00 (2H, м), 4,00-4,20 (2H, м), 4,15 (2H, кв, J=7,2 Гц), 5,13 (2H, с), 7,29-7,38 (5H, м).
Пример получения 42-2
Бензил-4-(1-гидрокси-1-метилэтил)пиперидин-1-карбоксилат
Бензил-4-этоксикарбонилпиперидин-1-карбоксилат (2,315 г, 7,95 ммоль), синтезированный в примере получения 42-1, растворяли в тетрагидрофуране (25 мл) в атмосфере азота, по каплям при охлаждении с помощью водно-ледяной бани добавляли бромметилмагний (0,93 М) в тетрагидрофуране (32,5 мл, 30,2 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение ночи. Реакционную смесь подвергали распределению между этилацетатом и насыщенным водным раствором хлорида аммония. Органический слой промывали насыщенным раствором соли и сушили над безводным сульфатом натрия. Растворитель отгоняли и остаток очищали колоночной хроматографией на силикагеле (элюент: смесь этилацетат:гексан=1:1) с получением указанного в заголовке соединения (1,786 г, 6,44 ммоль, 81%) в виде бесцветного масла.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 1,18 (6H, с), 1,18-1,27 (2H, м), 1,40-1,48 (1H, м), 1,74-1,78 (2H, м), 2,60-2,80 (2H, м), 4,20-4,40 (2H, м), 5,13 (2H, с), 7,27-7,37 (5H, м).
Пример получения 42-3
4-(1-Гидрокси-1-метилэтил)пиперидин
Бензил-4-(1-гидрокси-1-метилэтил)пиперидин-1-карбоксилат (1,786 г, 6,44 ммоль), синтезированный в примере получения 42-2, растворяли в метаноле (100 мл) в атмосфере азота, добавляли 10% палладий-на-угле (50% влажность, 1,37 г), реакционную систему продували водородом при атмосферном давлении и реакционную смесь перемешивали в течение ночи. После продувания реакционной системы азотом катализатор отфильтровывали и промывали метанолом, растворитель вместе с фильтратом и промывочным раствором отгоняли и остаток сушили при пониженном давлении с получением указанного в заголовке соединения (922 мг, 6,44 ммоль, количественный выход) в виде бледно-серых кристаллов.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 1,18 (6Н, с), 1,26-1,42 (3Н, м), 1,74-1,80 (2Н, м), 2,57-2,64 (2Н, м), 3,14-3,22 (2Н, м), 3,48 (1Н, с).
Пример 43
Метиламид 5-(2-(((4-(3-метилкарбамоилпропил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
4-(1-((4-(1-Метилкарбамоил-1H-индол-5-илокси)пиридин-2-ил)аминокарбонил)пиперидин-4-ил)масляную кислоту (170 мг, 0,35 ммоль) растворяли в N,N-диметилформамиде (7,0 мл), туда добавляли метиламина гидрохлорид (48 мг, 0,71 ммоль), бензотриазол-1-илокси-трис(диметиламино)фосфония гексафторфосфат (314 мг, 0,71 ммоль) и триэтиламин (0,35 мл) и реакционную смесь перемешивали при комнатной температуре в течение 2 часов. Реакционную смесь подвергали распределению между этилацетатом и водой. Органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia NH силикагель, система гексан-этилацетат-метанол). После добавления к полученному аморфному твердому веществу небольшого количества ацетона и этилацетата данный раствор разбавляли диэтиловым эфиром, твердую часть отфильтровывали, промывали диэтиловым эфиром и сушили при аэрировании с получением указанного в заголовке соединения (30 мг, 0,061 ммоль, 17%) в виде бесцветного аморфного твердого вещества.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,87-1,00 (2H, м), 1,13 (2H, м), 1,33 (1H, м), 1,46 (2H, м), 1,57 (2H, м), 1,99 (2H, т, J=7,4 Гц), 2,52 (3H, д, J=4,4 Гц), 2,65 (2H, м), 2,83 (3H, д, J=4,0 Гц), 4,03 (2H, м), 6,53 (1H, д, J=6,0 Гц), 6,67 (1H, д, J=3,4 Гц), 7,03 (1H, д, J=9,0 Гц), 7,31 (1H, с), 7,35 (1H, с), 7,66 (1H, м), 7,87 (1H, д, J=3,4 Гц), 8,06 (1H, д, J=4,0 Гц), 8,16 (1H, д, J=4,0 Гц), 8,27 (1H, д, J=9,0 Гц), 9,05 (1H, с).
Исходные вещества синтезировали следующими способами.
Пример получения 43-1
трет-Бутил-4-(3-этоксикарбонилпропил)пиперидин-1-карбоксилат
трет-Бутил-4-(2-(толуол-4-сульфонилокси)этил)пиперидин-1-карбоксилат (7,55 г, 19,7 ммоль, CAS No. 89151-45-1), как описано в WO 02/32872, растворяли в этаноле, добавляли диэтилмалонат (3,3 мл, 21,3 ммоль) и этоксид натрия (1,45 г, 21,3 ммоль) и реакционную смесь нагревали до кипения с обратным холодильником в атмосфере азота в течение 2,5 часов. После естественного остывания до комнатной температуры добавляли насыщенный водный раствор хлорида аммония, содержимое подвергали экстракции этилацетатом, промывали насыщенным раствором соли, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. После растворения остатка в диметилсульфоксиде (20 мл) добавляли хлорид лития (1,7 г, 40 ммоль) и воду (0,36 мл, 20 ммоль) и реакционную смесь перемешивали при 185°С в течение 1,5 часов и дополнительно перемешивали при 195°С в течение 2 часов. После естественного остывания до комнатной температуры реакционную смесь подвергали распределению между этилацетатом и насыщенным раствором соли. Органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia BW-300, система гексан-этилацетат) с получением указанного в заголовке соединения (2,60 г, 8,7 ммоль, 43%) в виде бледно-желтого масла.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 1,02-1,13 (2H, м), 1,23-1,29 (5H, м), 1,39 (1H, м), 1,45 (9H, с), 1,62-1,69 (4H, м), 2,29 (2H, т, J=7,4 Гц), 2,67 (2H, м), 4,07 (2H, м), 4,13 (2H, кв, J=7,2 Гц).
Пример получения 43-2
Этил-4-(пиперидин-4-ил)бутират
трет-Бутил-4-(3-этоксикарбонилпропил)пиперидин-1-карбоксилат (1,2 г, 4,0 ммоль, пример получения 43-1) растворяли в трифторуксусной кислоте (30 мл) и реакционную смесь перемешивали при комнатной температуре в течение 20 минут.Содержимое концентрировали при пониженном давлении и затем азеотропно отгоняли с толуолом. Полученный остаток подвергали распределению между этилацетатом и насыщенным водным раствором бикарбоната натрия. Органический слой сушили над безводным сульфатом магния. Кроме того, водный слой концентрировали при пониженном давлении досуха, полученное твердое вещество суспендировали в тетрагидрофуране, нерастворимую часть отфильтровывали и данный раствор добавляли к ранее полученному органическому слою. Содержимое очищали колоночной хроматографией на силикагеле (Fuji Silysia NH, система гексан-этилацетат-метанол) с получением указанного в заголовке соединения (1,15 г, количественный выход) в виде желтого масла.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 1,26 (3H, м), 1,28-1,37 (2H, м), 1,40-1,52 (3H, м), 1,64 (2H, м), 1,86 (2H, м), 2,29 (2H, т, J=7,4 Гц), 2,82 (2H, м), 3,35 (2H, м), 4,13 (2H, м).
Пример получения 43-3
Метиламид 5-(2-(((4-(3-этоксикарбамоилпропил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Этил-4-(пиперидин-4-ил)бутират (650 мг, 2,0 ммоль, пример получения 43-2) суспендировали в N,N-диметилформамиде (3,35 мл), добавляли фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамат (350 мг, 0,67 ммоль, пример получения 5-2) и реакционную смесь перемешивали при комнатной температуре в течение 1 часа. Реакционную смесь подвергали распределению между этилацетатом и водой. Органический слой сушили над безводным сульфатом магния, концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia BW-300, система гексан-этилацетат-метанол) с получением указанного в заголовке соединения (271 мг, 0,54 ммоль, 80%) в виде бледно-желтого масла.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 1,05-1,16 (2H, м), 1,22-1,28 (5H, м), 1,43 (1H, м), 1,62 (2H, м), 1,71 (2H, м), 2,27 (2H, т, J=7,4 Гц), 2,80 (2H, м), 2,95 (3H, д, J=4,4 Гц), 3,99 (2H, м), 4,12 (2H, кв, J=7,2 Гц), 6,09 (1H, д, J=4,4 Гц), 6,46 (1H, д, J=3,4 Гц), 6,58 (1H, дд, J=2,0, 5,6 Гц), 7,04 (1H, дд, J=2,0, 8,8 Гц), 7,24 (1H, с), 7,28 (1H, д, J=2,0 Гц), 7,32 (1H, д, J=3,4 Гц), 7,54 (1H, д, J=2,0 Гц), 8,03 (1H, д, J=5,6 Гц), 8,20 (1H, д, J=8,8 Гц).
Пример получения 43-4
4-(1-((4-(1-Метилкарбамоил-1H-индол-5-илокси)пиридин-2-ил)аминокарбонил)пиперидин-4-ил)масляная кислота
Метиламид 5-(2-(((4-(3-этоксикарбамоилпропил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты (271 мг, 0,54 ммоль, пример получения 43-3) растворяли в тетрагидрофуране (3,0 мл) и метаноле (1,5 мл), добавляли 4 н. гидроксид лития (0,54 мл) и реакционную смесь перемешивали при комнатной температуре в течение 3,5 часов. Туда добавляли 1 н. хлористоводородную кислоту (2,2 мл) при перемешивании при комнатной температуре. После отфильтровывания выпавших кристаллов кристаллы промывали последовательно водой и диэтиловым эфиром и сушили при аэрировании с получением указанного в заголовке соединения (170 мг, 0,35 ммоль, 66%) в виде бесцветных кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,93 (2H, м), 1,16 (2H, м), 1,36 (1H, м), 1,47 (2H, м), 1,58 (2H, м), 2,15 (2H, т, J=7,4 Гц), 2,66 (2H, м), 2,83 (3H, д, J=4,2 Гц), 4,02 (2H, м), 6,53 (1H, д, J=6,0 Гц), 6,67 (1H, д, J=3,4 Гц), 7,03 (1H, д, J=9,2 Гц), 7,31 (1H, с), 7,35 (1H, с), 7,86 (1H, д, J=3,4 Гц), 8,05 (1H, д, J=6,0 Гц), 8,15 (1H, д, J=4,2 Гц), 8,27 (1H, д, J=9,2 Гц), 9,02 (1H, с).
Пример 44
Метиламид 5-(2-(((4-(3-карбамоилпропил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
4-(Пиперидин-4-ил)бутанамид (547 мг, 1,41 ммоль) растворяли в N,N-диметилформамиде (3 мл), туда добавляли фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамат (210 мг, 0,402 ммоль, продукт примера получения 5-2) и реакционную смесь перемешивали при комнатной температуре в течение 1,5 часов. Реакционную смесь подвергали распределению между этилацетатом и водой, органический слой сушили над безводным сульфатом магния и концентрировали при пониженном давлении; остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia NH, система этилацетат-метанол). Полученное аморфное твердое вещество кристаллизовали добавлением диэтилового эфира. После добавления небольшого количества этанола для получения суспензии содержимое разбавляли гексаном. После разделения фильтрацией для получения кристаллов кристаллы промывали диэтиловым эфиром и сушили при аэрировании. Таким образом было получено указанное в заголовке соединение в виде бесцветных кристаллов (157 мг, 0,328 ммоль, 81,7%).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,87-1,00 (2H, м), 1,10-1,16 (2H, м), 1,35 (1H, м), 1,42-1,50 (2H, м), 1,58 (2H, м), 1,98 (2H, т, J=7,4 Гц), 2,65 (2H, м), 2,83 (3H, д, J=4,0 Гц), 4,03 (2H, м), 6,53 (1H, дд, J=2,0, 5,6 Гц), 6,67 (2H, м), 7,03 (1H, дд, J=2,0, 9,0 Гц), 7,20 (1H, с), 7,31 (1H, д, J=2,0 Гц), 7,35 (1H, д, J=2,0 Гц), 7,87 (1H, д, J=3,2 Гц), 8,06 (1H, д, J=5,6 Гц), 8,16(1H, м), 8,28 (1H, д, J=9,0 Гц), 9,05 (1H, с).
Исходные вещества синтезировали следующим образом.
Пример получения 44-1
трет-Бутил-4-(3-карбамоилпропил)пиперидин-1-карбоксилат
трет-Бутил-4-(3-этоксикарбонилпропил)пиперидин-1-карбоксилат (0,60 г, 2,0 ммоль, продукт примера получения 43-1) и формамид (0,27 мл, 6,7 ммоль) растворяли в N,N-диметилформамиде (1,0 мл), туда добавляли этоксид натрия (0,095 г, 1,4 ммоль) при перемешивании и нагревании при 100°С; реакционную смесь перемешивали в течение 2 часов в атмосфере азота. После охлаждения до комнатной температуры реакционную смесь подвергали распределению между водой и этилацетатом. Органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния и затем растворитель отгоняли при пониженном давлении. Остаток очищали хроматографией на силикагеле (элюент: смесь гексан-этилацетат=от 95:5 до 85:15). Указанное в заголовке соединение получали в виде бесцветного масла (0,38 г, 1,4 ммоль, 70%).
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 1,03-1,14 (2H, м), 1,26-1,31 (2H, м), 1,35-1,45 (1H, м), 1,46 (9H, с), 1,63-1,71 (4H, м), 2,22 (2H, т, J=7,6 Гц), 2,67 (2H, м), 4,07 (2H, уш.с), 5,30 (1H, уш.с), 5,39 (1H, уш.с).
Пример получения 44-2
4-(Пиперидин-4-ил)бутанамид
трет-Бутил-4-(3-карбамоилпропил)пиперидин-1-карбоксилат (0,38 г, 1,4 ммоль, пример получения 44-1) растворяли в трифторуксусной кислоте (2 мл) и реакционную смесь перемешивали при комнатной температуре в течение 20 минут. Реакционную смесь концентрировали при пониженном давлении и затем азеотропно отгоняли с толуолом. Остаток подвергали распределению между тетрагидрофураном и насыщенным водным раствором бикарбоната натрия; органический слой сушили над безводным сульфатом магния и концентрировали при пониженном давлении и остаток очищали хроматографией на силикагеле (Fuji Silysia NH, система этилацетат-метанол) с получением указанного в заголовке соединения (0,55 г, количественный выход) в виде бледно-желтого масла.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,90-1,01 (2H, м), 1,09-1,15 (2H, м), 1,26 (1H, м), 1,45 (2H, м), 1,55 (2H, м), 1,98 (2H, т, J=7,4 Гц), 2 43 (2H, м), 2,91 (2H, м), 6,65 (1H, с), 7,20 (1H, с).
Пример 45
Метиламид 5-(2-((4-пирролидин-1-ил)карбонил)пиперидин-1-ил)карбониламино)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (134 мг, 0,273 ммоль, 91%) получали в виде белых кристаллов из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (157 мг, 0,300 ммоль), синтезированного в примере получения 5-2, и (пиперидин-4-ил)-(пирролидин-1-ил)метанона (328 мг, 1,50 ммоль), полученного из N-бензилоксикарбонилизонипекотовой кислоты и пирролидина способом, сходным с примером 21.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,35-1,48 (2H, м), 1,56-1,65 (2H, м), 1,71-1,80 (2H, м), 1,82-1,91 (2H, м), 2,61 (1H, м), 2,73-2,84 (2H, м), 2,85 (3H, д, J=4,4 Гц), 3,22-3,28 (2H, м), 3,44-3,50 (2H, м), 4,04-4,12 (2H, м), 6,56 (1H, д, J=6,0 Гц), 6,69 (1H, д, J=3,6 Гц), 7,06 (1H, дд, J=2,4, 9,2 Гц), 7,34 (1H, с), 7,38 (1H, д, J=2,4 Гц), 7,89 (1H, д, J=3,6 Гц), 8,09 (1H, д, J=6,0 Гц) 8,18 (1H, кв, J=4,4 Гц), 8,30 (1H, д, J=9,2 Гц), 9,16 (1H, с).
Пример 46
N1-Метил-5-(2-(((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид
Аналогично примеру 27 указанное в заголовке соединение (88,5 мг, 0,19 ммоль, 63,8%) получали в виде белых кристаллов из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолил)окси)-2-пиридил)карбамата (121 мг, 0,30 ммоль, пример получения 29-1) и 4-(1-пирролидинил)пиперидина.
Фенил-N1-метил-5-(2-(((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид может быть синтезирован следующими способами.
Фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамат (12,1 г, 23,2 ммоль), синтезированный в примере получения 5-2, растворяли в диметилформамиде (150 мл), туда добавляли 4-(1-пирролидинил)пиперидин (14,4 г, 93,3 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 16 часов. Реакционную смесь подвергали распределению между этилацетатом и водой. Органический слой промывали насыщенным раствором соли и концентрировали до приблизительно 100 мл. Остаток оставляли охлаждаться при 5°С в течение ночи для выпадения кристаллов. Кристаллы отфильтровывали, промывали этилацетатом с получением указанного в заголовке соединения (7,8 г, 16,9 ммоль, 73%) в виде белых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,20-1,33 (2H, м), 1,60-1,70 (4H, м), 1,70-1,80 (2H, м), 2,40-2,60 (5H, м), 2,77-2,84 (5H, м), 3,90-4,00 (2H, м), 6,54 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц) 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,31 (1H, с), 7,35 (1H, д, J=2,4 Гц), 7,87 (1Н, д, J=3,6 Гц), 8,06 (1H, д, J=5,6 Гц), 8,16 (1H, м), 8,28 (1H, д, J=8,8 Гц), 9,11 (1H, с).
Пример 47
N1-Метил-5-(2-(((4-(пиперидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид
Аналогично примеру 27 указанное в заголовке соединение (94,6 мг, 0,20 ммоль, 66,2%) получали в виде белых кристаллов из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолил)окси-2-пиридил)карбамата (121 мг, 0,30 ммоль, пример получения 29-1) и 4-пиперидинпиперидина.
N1-метил-5-(2-(((4-(пиперидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид может быть получен следующими способами.
Фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамат (15,5 г, 29,7 ммоль), синтезированный в примере получения 5-2, растворяли в диметилформамиде (180 мл), туда добавляли 4-пиперидинпиперидин (20,0 г, 119 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 9 часов. Реакционную смесь подвергали распределению между этилацетатом и водой. Органический слой промывали насыщенным раствором соли и концентрировали до приблизительно 100 мл. Остаток оставляли охлаждаться при 5°С в течение ночи для выпадения кристаллов. Кристаллы отфильтровывали и промывали этилацетатом с получением указанного в заголовке соединения (4,0 г, 8,4 ммоль, 28%) в виде белых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,20-1,65 (10H, м), 2,31-2,40 (5H, м), 2,66 (2H, м), 2,83 (3H, д, J=4,4 Гц), 4,08 (2H, м), 6,53 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,31 (1H, д, J=2,4 Гц), 7,35 (1H, д, J=2,4 Гц), 7,87 (1H, д, J=3,6 Гц), 8,06 (1H, д, J=5,6 Гц), 8,16 (1H, кв, J=4,4 Гц), 8,28 (1H, д, J=8,8 Гц), 9,09 (1H, с).
Пример 48
N1-Метил-5-(2-((4-этилпиперазин-1-ил)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 27 указанное в заголовке соединение (73,2 мг, 0,17 ммоль, 57,8%) получали в виде белого порошка из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолил)окси-2-пиридил)карбамата (121 мг, 0,30 ммоль, пример получения 29-1) и 1-этилпиперазина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,97 (3H, т, J=7,2 Гц), 2,25-2,32 (6H, м), 2,83 (3H, д, J=4,0 Гц), 3,20-3,40 (4H, м), 6,55 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 7,04 (1H, дд, J=2,4, 8,8 Гц), 7,31 (1H, д, J=2,4 Гц), 7,36 (1H, д, J=2,4 Гц), 7,87 (1H, д, J=3,6 Гц), 8,07 (1H, д, J=5,6 Гц), 8,16 (1H, кв, J=4,0 Гц), 8,28 (1Н, д, J=8,8 Гц), 9,13 (1H, с).
Пример 49
N1-Метил-5-(2-((4-(2-гидроксиэтил)пиперазин-1-ил)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 27 указанное в заголовке соединение (97,6 мг, 0,22 ммоль, 59,7%) получали в виде бледно-розового порошка из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолил)окси-2-пиридил)карбамата (150 мг, 0,37 ммоль, пример получения 29-1) и 1-(2-гидроксиэтил)пиперазина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,30-2,40 (6H, м), 2,83 (3H, д, J=4,0 Гц), 3,20-3,40 (4H, м), 3,46 (2H, м), 4,39 (1H, т, J=5,6 Гц), 6,55 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,31 (1H, д, J=2,4 Гц), 7,35 (1H, д, J=2,4 Гц), 7,87 (1H, д, J=3,6 Гц), 8,06 (1H, д, J=5,6 Гц), 8,16 (1H, кв, J=4,0 Гц), 8,27 (1H, д, J=8,8 Гц), 9,12 (1H, с).
Пример 50
N1-Метил-5-(2-((3-метилсульфонилпропиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (166,8 мг, 0,37 ммоль, 70,5%) получали в виде белых кристаллов из N1-метил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамида (150 мг, 0,53 ммоль, пример получения 5-1) и 3-метилсульфонилпропиламина гидрохлорида (410 мг, 2,36 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,70-1,90 (2H, м), 2,83 (3H, д, J=4,4 Гц), 2,94 (3H, с), 3,04-3,09 (2H, м), 3,17-3,24 (2H, м), 6,52 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 6,86 (1H, с), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,36 (1H, с), 7,87 (1H, д, J=3,6 Гц), 8,03 (1H, д, J=5,6 Гц), 8,10-8,17 (2H, м), 8,28 (1H, д, J=8,8 Гц), 9,07 (1H, с).
Пример 51
N1-Метил-5-(2-((4-(2-диметиламиноацетил)пиперазин-1-ил)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (189,8 мг, 0,40 ммоль, 74,5%) получали в виде белого порошка из N1-метил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамида (150 мг, 0,53 ммоль, пример получения 5-1) и 1-(2-диметиламиноацетил)пиперазина (500 мг, 2,92 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,14 (6H, с), 3,04 (3H, д, J=4,0 Гц), 3,29 (2H, с), 3,20-3,49 (8H, м), 6,56 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 7,03 (1H, дд, J=2,4, 8,8 Гц) 7,30 (1H, д, J=2,4 Гц), 7,36 (1H, д, J=2,4 Гц), 7,87 (1H, д, J=3,6 Гц), 8,08 (1H, д, J=5,6 Гц), 8,16 (1H, кв, J=4,0 Гц), 8,28 (1H, д, J=8,8 Гц), 9,24 (1H, с).
1-(2-Диметиламиноацетил)пиперазин получали следующими способами.
Пример получения 51-1
Бензил-4-(2-диметиламиноацетил)пиперазин-1-карбоксилат
Бензилпиперазин-1-карбамат (2,203 г, 10,0 ммоль) растворяли в тетрагидрофуране (50 мл), туда добавляли диметиламиноуксусную кислоту (1,24 г, 12,0 ммоль), 1-этил-3-(3-диметиламинопропил)карбодиимида гидрохлорид (2,30 г, 12,0 ммоль), 1-гидрокси-1H-бензотриазола моногидрат (1,84 г, 12,0 ммоль) и триэтиламин (3,35 мл, 24,0 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 7 часов. Реакционную смесь подвергали распределению между этилацетатом и насыщенным водным раствором бикарбоната натрия. Органический слой промывали насыщенным водным раствором бикарбоната натрия, водой и насыщенным раствором соли, сушили над безводным сульфатом натрия и остаток очищали колоночной хроматографией на силикагеле NH (элюент: смесь этилацетат:гексан=3:1) с получением указанного в заголовке соединения (954 мг, 3,12 ммоль, 31,2%) в виде бесцветного масла.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 2,26 (6H, с), 3,11 (2H, с), 3,45-3,65 (8H, м), 5,15 (2H, с), 7,32-7,38 (5H, м).
Пример получения 51-2
1-(2-Диметиламиноацетил)пиперазин
Бензил-4-(2-диметиламиноацетил)пиперазин-1-карбоксилат (954 мг, 3,12 ммоль), синтезированный в примере получения 51-1, растворяли в метаноле (50 мл) в атмосфере азота, туда добавляли 10% палладий-на-угле (50% влажность, 665 мг), реакционную систему продували водородом при атмосферном давлении и реакционную смесь перемешивали в течение ночи. После продувания реакционной системы азотом катализатор отфильтровывали и промывали метанолом. Растворитель вместе с фильтратом и промывочным раствором отгоняли и остаток сушили при пониженном давлении с получением указанного в заголовке соединения (508 мг, 2,97 ммоль, 95,0%) в виде бесцветного масла.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 2,28 (6H, с), 2,80-2,88 (4H, м), 3,11 (2H, с), 3,52-3,62 (4H, м).
Пример 52
N1-Метил-5-(2-((4-(циклогексилпиперазин-1-ил)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 27 указанное в заголовке соединение (121,3 мг, 0,25 ммоль, 68,2%) получали в виде белых кристаллов из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолил)окси-2-пиридил)карбамата (150 мг, 0,37 ммоль, пример получения 29-1) и 1-циклогексилпиперазина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,00-1,20 (6H, м), 1,53 (2H, м), 1,60-1,80 (4H, м), 2,19 (2H, м), 2,30-2,45 (5H, м), 2,83 (3H, д, J=4,0 Гц), 6,54 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,31 (1H, д, J=2,4 Гц), 7,35 (1H, д, J=2,4 Гц), 7,87 (1H, д, J=3,6 Гц), 8,06 (1H, д, J=5,6 Гц), 8,16 (1H, кв, J=4,0 Гц), 8,27 (1H, д, J=8,8 Гц), 9,09 (1H, с).
Пример 53
N4-(4-(1-(Метиламино)карбонил)-1H-5-индолил)окси-2-пиридил)-4-морфолинкарбоксамид
Аналогично примеру 27 указанное в заголовке соединение (58,6 мг, 0,15 ммоль, 49,4%) получали в виде белого порошка из фенил-N-(4-((1-((метиламино)карбонил)-1H-5-индолил)окси-2-пиридил)карбамата (121 мг, 0,30 ммоль, пример получения 29-1) и морфолина.
N4-(4-((1-(Метиламино)карбонил-1H-5-индолил)окси-2-пиридил)-4-морфолинкарбоксамид может быть получен следующими способами.
Фенил-N-(4-(1-(метиламино)карбонил-1Н-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамат (20 г, 38 ммоль), синтезированный в примере получения 5-2, растворяли в N,N-диметилформамиде (190 мл), туда добавляли морфолин (13,3 мг, 153 ммоль) и реакционную систему перемешивали при комнатной температуре в течение 9 часов. Реакционную смесь подвергали распределению между этилацетатом и водой; органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Полученный остаток растворяли в этилацетате и небольшом количестве тетрагидрофурана, данную суспензию фильтровали через силикагель и через гель пропускали этилацетат и три разных соотношения смеси растворителей этилацетат:метанол=20:1, 10:1 и 5:1. Фильтрат концентрировали при пониженном давлении. Остаток растворяли в диэтиловом эфире (40 мл), туда добавляли гексан (200 мл), выпавшую в осадок нерастворимую сиропную часть удаляли из раствора и полученный раствор вновь концентрировали при пониженном давлении. Остаток растворяли в этилацетате (300 мл) и его оставляли при комнатной температуре. После выпадения кристаллов кристаллы отфильтровывали, промывали этилацетатом и сушили с получением сырых кристаллов указанного в заголовке соединения (10,3 г). 9 г данных сырых кристаллов суспендировали в смеси тетрагидрофурана (3 мл) и N,N-диметилформамида (3 мл), данную суспензию разбавляли этанолом (60 мл), кристаллы отфильтровывали, промывали этанолом и сушили с получением указанного в заголовке соединения в виде бесцветных кристаллов (7,70 г, 19 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,83 (3H, д, J=4,4 Гц), 3,34-3,38 (4H, м), 3,50-3,53 (4H, м), 6,56 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 7,04 (1H, дд, J=2,4, 8,8 Гц), 7,31 (1H, д, J=2,4 Гц), 7,36 (1H, д, J=2,4 Гц), 7,87 (1H, д, J=3,6 Гц), 8,08 (1H, д, J=5,6 Гц), 8,17 (1H, кв, J=4,4 Гц), 8,28 (1H, д, J=8,8 Гц), 9,19 (1H, с).
Пример 54
N1-Метил-5-(2-((1,1-диоксотиоморфолин-4-илкарбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид
Фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамат (150 мг, 0,278 ммоль, пример получения 5-2) растворяли в N,N-диметилформамиде (1,5 мл), туда добавляли 5 н. водный раствор гидроксида натрия (0,29 мл) и 1,1-диоксотиоморфолина гидрохлорид (246 мг, 1,44 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 5 часов. Реакционную смесь подвергали распределению между этилацетатом и водой. Органический слой сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia BW-300, этилацетат). К содержимому добавляли диэтиловый эфир для обеспечения кристаллизации; кристаллы отфильтровывали, промывали диэтиловым эфиром и сушили при аэрировании с получением указанного в заголовке соединения в виде бесцветных кристаллов (100 мг, 0,226 ммоль, 78,5%).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,83 (3H, д, J=3,6 Гц), 3,10 (4H, м), 3,81 (4H, м), 6,57 (1H, дд, J=1,2, 5,6 Гц), 6,67 (1H, д, J=3,2 Гц), 7,03 (1H, дд, J=2,0, 9,2 Гц), 7,32 (1H, м), 7,36 (1H, д, J=2,0 Гц), 7,87 (1H, д, J=3,2 Гц), 8,09 (1H, д, J=5,6 Гц), 8,16 (1H, д, J=3,6 Гц), 8,28 (1H, д, J=9,2 Гц), 9,54 (1H, с).
Исходное вещество синтезировали следующими способами.
Пример получения 54-1
трет-Бутилтиоморфолин-4-карбоксилат
Тиоморфолин (5,0 мл, 53 ммоль) растворяли в тетрагидрофуране (200 мл), туда добавляли триэтиламин (8,1 мл, 58 ммоль) и реакционную смесь перемешивали при комнатной температуре. Туда добавляли трет-бутоксикарбонила бикарбонат (13,3 мл, 58 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 10 часов. Реакционную смесь концентрировали при пониженном давлении и остаток очищали на колонке силикагеля (элюент: смесь гексан:этилацетат=от 80:20, 75:25 до 70:30) с получением указанного в заголовке соединения в виде бесцветных кристаллов (10,4 г, 51 ммоль).
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 1,46 (9H, с), 2,57 (4H, м), 3,69 (4H, м).
Пример получения 54-2
трет-Бутил-1,1-диоксотиоморфолин-4-карбоксилат
трет-Бутилтиоморфолин-4-карбоксилат (1,91 г, 9,42 ммоль) растворяли в дихлорметане (50 мл), постепенно, при охлаждении в ледяной бане, перемешивании и в атмосфере азота добавляли м-хлорнадбензойную кислоту (5,0 г, 19 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 12 часов. После добавления насыщенного водного раствора тиосульфата натрия реакционную смесь оставляли перемешиваться на некоторое время и содержимое подвергали экстракции этилацетатом, промывали насыщенным раствором соли, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. К полученным кристаллам добавляли триэтиламин (8,1 мл, 58 ммоль) и реакционную смесь перемешивали при комнатной температуре. Туда добавляли трет-бутоксикарбонила бикарбонат (13,3 мл, 58 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 10 часов. Реакционную смесь концентрировали при пониженном давлении и полученные кристаллы суспендировали смесью растворителей диэтиловый эфир:этанол 10:1, отфильтровывали, промывали диэтиловым эфиром и сушили при аэрировании с получением указанного в заголовке соединения в виде бесцветных кристаллов (2,03 г, 8,63 ммоль, 91,6%).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,40 (9H, с), 3,09 (4H, т, J=5,2 Гц), 3,72 (4H, т, J=5,2 Гц).
Пример получения 54-3
Тиоморфолин-1,1-диоксида моногидрохлорид
трет-Бутил-1,1-диоксотиоморфолин-4-карбоксилат (2,03 г, 8,63 ммоль) растворяли в смеси хлористоводородная кислота-метанол 10 (20 мл, полученной от Tokyo Kasei Kogyo Co., Ltd) и тетрагидрофурана (20 мл), туда при перемешивании при комнатной температуре добавляли хлористоводородную кислоту (4,0 мл) и реакционную смесь перемешивали при комнатной температуре в течение 3 часов. Реакционную смесь концентрировали и к полученным кристаллам добавляли метанол (20 мл), тетрагидрофуран (20 мл) и хлористоводородную кислоту (4,0 мл). Далее к данному раствору добавляли воду (10 мл) для полного растворения кристаллов и данный раствор перемешивали при комнатной температуре в течение 1 часа. Растворитель концентрировали при пониженном давлении и полученные кристаллы суспендировали в метаноле, отфильтровывали, промывали метанолом и сушили при аэрировании с получением указанного в заголовке соединения в виде бесцветных кристаллов (1,49 г, 8,65 ммоль, количественный выход).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 3,54 (8H, м), 9,83 (2H, уш.с).
Пример 55
Этиламид 5-(2-(3-((1R)-1-гидроксиметил-2-оксо-2-пирролидин-1-илэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (118 мг, 0,246 ммоль, 82%) получали в виде белых кристаллов из фенил-N-(4-(1-(этиламино)карбонил-1H-5-индолилокси-2-пиридил)-N-(феноксикарбонил)карбамата (161 мг, 0,300 ммоль) и (2R)-2-амино-3-гидрокси-1-(пирролидин-1-ил)пропан-1-она (265 мг, 1,67 ммоль), полученного способом, сходным с примером 21, из (2R)-2-бензилоксикарбониламино-3-гидроксипропионовой кислоты и пирролидина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,19 (3H, т, J=7,2 Гц), 1,70-1,90 (4H, м), 3,20-3,60 (8H, м), 4,54 (1H, м), 4,98 (1H, уш.с), 6,55 (1H, д, J=6,0 Гц), 6,69 (1H, д, J=3,6 Гц), 6,97 (1H, с), 7,05 (1H, дд, J=2,4, 8,8 Гц), 7,39 (1H, д, J=2,4 Гц), 7,92 (1H, д, J=3,6 Гц), 8,05 (1H, д, J=6,0 Гц), 8,08-8,28 (2H, м), 8,30 (1H, д, J=8,8 Гц), 9,21 (1H, с).
Исходное вещество синтезировали следующим образом.
Пример получения 55-1
Фенил-N-(4-(1-(этиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамат
Проводили реакцию, сходную с примером получения 5-2, с применением N1-этил-5-(2-аминопиридин-4-илокси)-1H-индолкарбоксамида (2,9 г, 9,9 ммоль, пример получения 27-1), тетрагидрофурана, триэтиламина и фенилхлорформиата; проводили экстракцию и промывку, полученный остаток кристаллизовали добавлением смеси растворителей диэтиловый эфир:гексан=1:1 и полученные кристаллы отфильтровывали, промывали диэтиловым эфиром и сушили при аэрировании с получением указанного в заголовке соединения в виде бледно-розовых кристаллов (3,7 г, 6,9 ммоль, 70%).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,17 (3H, т, J=7,2 Гц), 3,29 (2H, м), 6,66 (1H, д, J=3,4 Гц), 6,96 (1H, дд, J=2,0, 5,8 Гц), 7,09 (1H, дд, J=2,0, 8,0 Гц), 7,17 (4H, д, J=8,0 Гц), 7,29 (2H, д, J=8,0 Гц), 7,41-7,44 (5H, м), 7,51 (1H, д, J=2,0 Гц), 7,92 (1H, д, J=3,4 Гц), 8,22 (1H, м), 8,31 (1H, д, J=8,8 Гц), 8,42 (1H, д, J=5,8 Гц).
Пример 56
Этиламид-5-(2-(3-((1S)-1-гидроксиметил-2-оксо-2-пирролидин-1-илэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (132 мг, 0,275 ммоль, 92%) получали в виде белых кристаллов из фенил-N-(4-(1-(этиламино)карбонил-1H-5-индолилокси-2-пиридил)-N-(феноксикарбонил)карбамата (161 мг, 0,300 ммоль), синтезированного в примере получения 55-1, и (2S)-2-амино-3-гидрокси-1-(пирролидин-1-ил)пропан-1-она гидрохлорида (синтезированного в качестве промежуточного соединения в примере 18).
Пример 57
Этиламид 5-(2-(3-((1R)-1-гидроксиметил-2-оксо-2-пиперидин-1-илэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (127 мг, 0,257 ммоль, 86%) получали в виде белых кристаллов из фенил-N-(4-(1-(этиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (161 мг, 0,300 ммоль) и (2R)-2-амино-3-гидрокси-1-(пиперидин-1-ил)пропан-1-она (228 мг, 1,32 ммоль, синтезированного в качестве промежуточного соединения в примере 21).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,19 (3H, т, J=7,2 Гц), 1,38-1,61 (6H, м), 3,25-3,53 (8H, м), 4,75 (1H, м), 4,92 (1H, уш.с), 6,54 (1H, дд, J=2,4, 6,0 Гц), 6,69 (1H, д, J=3,6 Гц), 6,97 (1H, д, J=2,4 Гц), 7,05 (1H, дд, J=2,4, 9,0 Гц), 7,38 (1H, д, J=2,4 Гц), 7,92 (1H, д, J=3,6 Гц), 8,05 (1H, д, J=6,0 Гц), 8,08-8,27 (2H, м), 8,30 (1H, д, J=9,0 Гц), 9,21 (1H, с).
Пример 58
Этиламид 5-(2-(3-((1S)-1-гидроксиметил-2-оксо-2-пиперидин-1-илэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (54,4 мг, 0,110 ммоль, 73%) получали в виде белых кристаллов из фенил N-(4-(1-(этиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (80,1 мг, 0,150 ммоль), синтезированного в примере получения 55-1, и (2S)-2-амино-3-гидрокси-1-(пиперидин-1-ил)пропан-1-она гидрохлорида (156 мг, 0,748 ммоль, синтезированного в качестве промежуточного соединения в примере 20).
Пример 59
Этиламид 5-(2-(3-(2-(4-гидрокси-4-метилпиперидин-1-ил)-2-оксоэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Реакцию, сходную с примером 5, проводили с применением ((4-(1-этилкарбамоил-1H-индол-5-илокси)пиридин-2-ил)аминокарбониламино)уксусной кислоты (149 мг, 0,37 ммоль) и 4-гидрокси-4-метилпиперидина моногидрохлорида (68 мг, 0,45 ммоль, пример получения 8-3); очистку проводили колоночной хроматографией на силикагеле (Fuji Silysia BW-300, элюент: смесь этилацетат:метанол=9:1; Fuji Silysia NH, элюент: смесь этилацетат:метанол=10:1 и вновь Fuji Silysia BW-300, элюент: система этилацетат-метанол) и полученные кристаллы суспендировали в диэтиловом эфире, отфильтровывали, промывали диэтиловым эфиром и сушили при аэрировании с получением указанного в заголовке соединения в виде бесцветных кристаллов (40 мг, 0,081 ммоль, 22%).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,10 (3H, с), 1,16 (3H, т, J=7,2 Гц), 1,43 (4H, м), 3,01 (2H, м), 3,36 (2H, м), 3,89 (2H, м), 3,96 (2H, д, J=4,4 Гц), 4,37 (1H, с), 6,52 (1H, д, J=5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 6,91 (1H, с), 7,03 (1H, д, J=9,0 Гц), 7,37 (1H, с), 7,90 (1H, д, J=3,6 Гц), 8,03 (1H, д, J=5,6 Гц), 8,17 (1H, м), 8,22 (1H, м), 8,28 (1H, д, J=9,0 Гц), 9,27 (1H, с).
Исходное вещество синтезировали следующим способом.
Пример получения 59-1
((4-(1-Этилкарбамоил-1H-индол-5-илокси)пиридин-2-ил)аминокарбониламино)уксусная кислота
Метиламиноацетата гидрохлорид (292 мг, 2,33 ммоль) суспендировали в смеси растворителей N,N-диметилформамида (4 мл) и триэтиламина (1 мл), туда добавляли фенил-N-(4-(1-(этиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамат (250 мг, 0,466 ммоль, пример получения 55-1) и реакционную смесь перемешивали при комнатной температуре в течение 2 дней. Реакционную смесь подвергали распределению между этилацетатом и водой и органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Полученный остаток растворяли в смеси растворителей тетрагидрофурана (2 мл) и метанола (1 мл); туда при перемешивании при комнатной температуре добавляли 4 н. водный раствор гидроксида натрия и реакционную смесь перемешивали в течение 1,5 часов при комнатной температуре. После добавления 1 н. хлористоводородной кислоты производили экстракцию смесью этилацетат-тетрагидрофуран, промывали насыщенным раствором соли, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Полученные кристаллы суспендировали в диэтиловом эфире, отфильтровывали, промывали диметиловым эфиром и сушили при аэрировании с получением указанного в заголовке соединения в виде бесцветных кристаллов (149 мг, 0,375 ммоль, 80,5%).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,17 (3H, т, J=7,0 Гц), 3,36 (2H, д, J=7,0 Гц), 3,81 (2H, д, J=5,2 Гц), 6,54 (1H, д, J=5,6 Гц), 6,67 (1H, д, J=3,4 Гц), 6,85 (1H, с), 7,04 (1H, дд, J=2,0, 8,8 Гц), 7,37 (1H, д, J=2,0 Гц), 7,90 (1H, д, J=3,4 Гц), 8,05 (1H, д, J=5,6 Гц), 8,20-8,30 (3H, м), 9,27 (1H, с), 12,55 (1H, с).
Пример 60
N1-Этил-5-(2-((((1-метил-4-пиперидил)метил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 27 сырой продукт трет-бутил 4-(((((4-((1-(этиламино)карбонил-1H-5-индолил)окси)-2-пиридил)амино)карбонил)амино)метил)пиперидин-1-карбоксилат получали из фенил-N-(4-(1-(этиламино)карбонил)-1H-5-индолил)окси)-2-пиридил)карбамата (150 мг, 0,36 ммоль, пример получения 27-2) и трет-бутил-4-аминометил-1-пиперидина карбоксилата. К содержимому добавляли трифторуксусную кислоту при комнатной температуре, раствор перемешивали в течение 30 минут; трифторуксусную кислоту отгоняли, к остатку для нейтрализации добавляли смесь триэтиламина-метанола и растворитель вновь отгоняли при пониженном давлении. Остаток растворяли в смеси тетрагидрофуран (4,0 мл) - метанол (4,0 мл), добавляли при комнатной температуре уксусную кислоту (0,1 мл), 37% водный раствор формальдегида (0,5 мл) и цианоборогидрид натрия (90,5 мг, 1,44 ммоль) и реакционную смесь перемешивали в течение 1 часа. Реакционную смесь подвергали распределению между этилацетатом и водой и органический слой промывали водой и насыщенным раствором соли, сушили над безводным сульфатом натрия. Растворитель отгоняли и остаток очищали колоночной хроматографией на NH-силикагеле (элюент: смесь этилацетат:метанол=98:2). Кристаллы осаждали из диэтилового эфира, отфильтровывали и сушили при аэрировании с получением указанного в заголовке соединения в виде белых кристаллов (197,0 мг, 0,44 ммоль, 60,7%).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,08-1,19 (5H, м), 1,30 (1H, м), 1,54 (2H, м), 1,75 (2H, м), 2,09 (3H, м), 2,70 (2H, м), 2,98 (2H, м), 3,20-3,40 (2H, м), 6,49 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 6,85 (1H, с), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,36 (1H, д, J=3,6 Гц), 7,90 (1H, д, J=2,4 Гц), 8,02 (1H, д, J=5,6 Гц), 8,08 (1H, м), 8,22 (1H, м), 8,28 (1H, д, J=8,8 Гц), 9,00 (1H, с).
Пример 61
N1-Этил-5-(2-(((2-(диэтиламино)этил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 27 указанное в заголовке соединение (140,9 мг, 0,32 ммоль, 89,2%) получали в виде белых кристаллов из фенил-N-(4-(1-(этиламино)карбонил-1H-5-индолил)окси-2-пиридил)карбамата (150 мг, 0,36 ммоль, пример получения 27-2) и 2-(диэтиламино)этиламина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,93 (6H, т, J=7,2 Гц), 1,17 (3H, т, J=7,2 Гц), 2,40-2,49 (6H, м), 3,13 (2H, м), 3,20-3,40 (2H, м), 6,49 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 6,82 (1H, с), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,36 (1H, д, J=2,4 Гц), 7,90 (1H, д, J=3,6 Гц), 8,00 (1H, д, J=5,6 Гц), 8,20-8,25 (2H, м), 8,28 (1H, д, J=8,8 Гц), 9,11 (1H, с).
Пример 62
N1-Этил-5-(2-(((2-(морфолин-4-ил)этил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 27 указанное в заголовке соединение (155,0 мг, 0,34 ммоль, 95,1%) получали в виде белых кристаллов из фенил-N-(4-(1-(этиламино)карбонил-1H-5-индолил)окси-2-пиридил)карбамата (150 мг, 0,36 ммоль, пример получения 27-2) и 4-(2-аминоэтил)морфолина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,67 (3H, т, J=7,2 Гц), 2,30-2,40 (6H, м), 3,20 (2H, м), 3,20-3,40 (2H, м), 3,54-3,57 (4H, м), 6,50 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 6,84 (1H, с), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,36 (1H, д, J=3,6 Гц), 7,90 (1H, д, J=2,4 Гц), 8,02 (1H, д, J=5,6 Гц), 8,10-8,25 (2H, м), 8,28 (1H, д, J=8,8 Гц), 9,11 (1H, с).
Пример 63
N1-Этил-5-(2-(((2-(4-гидроксипиперидин)этил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 27 указанное в заголовке соединение (49,1 мг, 0,11 ммоль, 35,1%) получали в виде белых кристаллов из фенил-N-(4-(1-(этиламино)карбонил-1H-5-индолил)окси-2-пиридил)карбамата (125 мг, 0,30 ммоль, пример получения 27-2) и 1-(2-аминоэтил)-4-гидроксипиперидина дигидрохлорида.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,17 (3H, т, J=7,2 Гц), 1,36 (2H, м), 1,66-1,70 (2H, м), 2,00 (2H, м), 2,32 (2H, м), 2,65-2,69 (2H, м), 3,16 (2H, м), 3,20-3,40 (2H, м), 3,40 (1H, м), 4,53 (1H, д, J=4,0 Гц), 6,50 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 6,83 (1H, с), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,36 (1H, д, J=2,4 Гц), 7,90 (1H, д, J=3,6 Гц), 8,01 (1H, д, J=5,6 Гц), 8,10-8,23 (2H, м), 8,28 (1H, д, J=8,8 Гц), 9,11 (1H, с).
Пример 64
N1-Метил-5-(2-(((2-(4-гидроксипиперидин)этил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 27 указанное в заголовке соединение (114,3 мг, 0,25 ммоль, 25,3%) получали в виде белых кристаллов из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолил)окси-2-пиридил)карбамата (402 мг, 1,0 ммоль, пример получения 29-1) и 1-(2-аминоэтил)-4-гидроксипиперидина дигидрохлорида.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,32-1,38 (2H, м), 1,60-1,70 (2H, м), 1,96-2,03 (2H, м), 2,31-2,34 (2H, м), 2,60-2,70 (2H, м), 2,83 (3H, д, J=4,4 Гц), 3,15-3,18 (2H, м), 3,42 (1H, м), 4,53 (1H, д, J=4,0 Гц), 6,51 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 6,84 (1Н, с), 7,04 (1H, дд, J=2,4, 8,8 Гц), 7,36 (1H, д, J=2,4 Гц), 7,87 (1H, д, J=3,6 Гц), 8,01 (1H, д, J=5,6 Гц), 8,14-8,16 (2H, м), 8,28 (1H, д, J=8,8 Гц), 9,11 (1H, с).
Пример 65
N1-Этил-5-(2-((3-(диэтиламино)пропиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 27 указанное в заголовке соединение (159,9 мг, 0,35 ммоль, 98,1%) получали в виде белых кристаллов из фенил-N-(4-(1-(этиламино)карбонил-1H-5-индолил)окси-2-пиридил)карбамата (150 мг, 0,36 ммоль, пример получения 27-2) и 3-(диэтиламино)пропиламина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,91 (6H, т, J=7,2 Гц), 1,17 (3H, т, J=7,2 Гц), 1,50 (2H, м), 2,32-2,41 (6H, м), 3,10 (2H, м), 3,20-3,40 (2H, м), 6,50 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 6,81 (1H, с), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,36 (1H, д, J=3,6 Гц), 7,90 (1H, д, J=2,4 Гц), 8,00 (1H, д, J=5,6 Гц), 8,12 (1H, м), 8,22 (1H, т, J=5,2 Гц), 8,28 (1H, д, J=8,8 Гц), 9,03 (1H, с).
Пример 66
N1-Этил-5-(2-(((3-(морфолин-4-ил)пропил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 27 указанное в заголовке соединение (135,0 мг, 0,29 ммоль, 96,4%) получали в виде белых кристаллов из фенил N-(4-(1-(этиламино)карбонил-1H-5-индолил)окси-2-пиридил)карбамата (125 мг, 0,30 ммоль, пример получения 27-2) и 4-(3-аминопропил)морфолина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,17 (3H, т, J=7,2 Гц), 1,55 (2H, м), 2,20-2,40 (6H, м), 3,11 (2H, м), 3,20-3,40 (2H, м), 3,51-3,55 (4H, м), 6,50 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 6,84 (1H, с), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,36 (1H, д, J=2,4 Гц), 7,90 (1H, д, J=3,6 Гц), 8,01 (1H, д, J=5,6 Гц), 8,04 (1H, м), 8,21 (1H, т, J=5,6 Гц), 8,28 (1H, д, J=8,8 Гц), 9,02 (1H, с).
Пример 67
N1-Этил-5-(2-(((3-(4-метилпиперазин-1-ил)пропил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 27 указанное в заголовке соединение (141,9 мг, 0,30 ммоль, 98,6%) получали в виде белых кристаллов из фенил-N-(4-(1-(этиламино)карбонил-1H-5-индолил)окси-2-пиридил)карбамата (125 мг, 0,30 ммоль, пример получения 27-2) и 1-(3-аминопропил)-4-метилпиперазина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,17 (3H, т, J=7,2 Гц), 1,54 (2H, м), 2,11 (3H, с), 2,11-2,40 (10H, м), 3,08 (2H, м), 3,20-3,40 (2H, м), 6,50 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 6,84 (1H, с), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,36 (1H, д, J=2,4 Гц), 7,90 (1H, д, J=3,6 Гц), 8,01 (1H, д, J=5,6 Гц), 8,04 (1H, м), 8,22 (1H, т, J=5,6 Гц), 8,28 (1H, д, J=8,8 Гц), 9,01 (1H, с).
Пример 68
N1-Циклопропил-5-(2-(((4-(пирролидин-1-ил)пиперидин-1-ил) карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид
Тетрагидрофуран (30 мл) и триэтиламин (3,87 мл, 27,8 ммоль) добавляли к N1-циклопропил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамиду (2,85 г, 9,25 ммоль, CAS No. 417722-12-4), который был описан в WO 02/32872; туда добавляли фенилхлорформиат (2,57 мл, 20,4 ммоль) при 0°С при перемешивании и реакционную смесь перемешивали при комнатной температуре в течение 2 часов. Реакционную смесь подвергали распределению между этилацетатом и водой и органический слой концентрировали с получением 3,30 г смеси фенил-N-(4-(1-(циклопропиламино)карбонил-1H-5-индолил)окси-2-пиридил)карбамата и фенил-N-(4-(1-(циклопропиламинокарбонил-1H-5-индолил)окси-2-пиридил)-N-(феноксикарбонил)карбамата. Часть смеси в количестве 0,524 г растворяли в N,N-диметилформамиде (5 мл), туда добавляли 4-(1-пирролидинил)пиперидин (0,736 г, 4,80 ммоль), реакционную смесь перемешивали в течение 5 часов, реакционную смесь подвергали распределению между этилацетатом и водой и органический слой концентрировали с получением указанного в заголовке соединения в виде белых кристаллов (280 мг, 0,57 ммоль).
МС-спектр (ESI): 489 (M+1).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,57-0,75 (4H, м), 1,18-1,30 (2H, м), 1,58-1,80 (6H, м), 2,03-2,12 (1H, м), 2,38-2,48 (4H, м), 2,72-2,87 (3H, м), 3,88-3,96 (2H, м), 6,53 (1H, дд, J=2,7, 6,1 Гц), 6,64 (1H, д, J=3,4 Гц), 7,03 (1H, дд, J=2,7, 8,9 Гц), 7,30 (1H, д, J=2,7 Гц), 7,35 (1H, д, J=2,7 Гц), 7,86 (1H, д, J=3,4 Гц), 8,06 (1H, д, J=6,1 Гц), 8,24-8,29 (2H, м), 9,08 (1H, с).
Пример 69
Циклопропиламид 5-(2-(3-((1R)-1-гидроксиметил-2-оксо-2-пирролидин-1-илэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (113 мг, 0,229 ммоль) получали в виде белых кристаллов из смеси (165 мг) фенил-N-(4-(1-циклопропиламинокарбонил-1H-5-индолил)окси-2-пиридил)-N-(феноксикарбонил)карбамата и фенил-N-(4-(1-циклопропиламинокарбонил-1H-5-индолил)окси-2-пиридил)карбамата, промежуточных соединений примера 68, и (2R)-2-амино-3-гидрокси-1-(пирролидин-1-ил)пропан-1-она (265 мг, 1,67 ммоль, синтезированного в качестве промежуточного соединения в примере 55).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,58-0,66 (2H, м), 0,70-0,78 (2H, м), 1,72-1,90 (4H, м), 2,78 (1H, м), 3,20-3,60 (6H, м), 4,54 (1H, м), 4,98 (1H, т, J=5,6 Гц), 6,53 (1H, дд, J=2,0, 6,0 Гц), 6,67 (1H, д, J=3,6 Гц) 6,97 (1H, д, J=2,0 Гц), 7,06 (1H, дд, J=2,4, 8,8 Гц), 7,37 (1H, д, J=2,4 Гц), 7,88 (1H, д, J=3,6 Гц), 8,05 (1H, д, J=6,0 Гц), 8,16 (1H, уш.с), 8,25-8,34 (2H, м), 9,18 (1H, с).
Пример 70
Циклопропиламид 5-(2-(3-((1S)-1-гидроксиметил-2-оксо-2-пирролидин-1-илэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (117 мг, 0,237 ммоль) получали в виде белых кристаллов из смеси (165 мг) фенил-N-(4-(1-циклопропиламинокарбонил-1H-5-индолил)окси-2-пиридил)-N-(феноксикарбонил)карбамата и фенил-N-(4-(1-циклопропиламинокарбонил-1H-5-индолил)окси-2-пиридил)карбамата, промежуточных соединений примера 68, и (2S)-2-амино-3-гидрокси-1-(пирролидин-1-ил)пропан-1-она гидрохлорида (синтезированного в качестве промежуточного соединения в примере 18).
Пример 71
Циклопропиламид 5-(2-(3-(2-оксо-2-(пирролидин-1-ил)этил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (90,9 мг, 0,197 ммоль) получали в виде белых кристаллов из смеси (165 мг) фенил-N-(4-(1-циклопропиламинокарбонил-1H-5-индолил)окси-2-пиридил)-N-(феноксикарбонил)карбамата и фенил-N-(4-(1-циклопропиламинокарбонил-1H-5-индолил)окси-2-пиридил)карбамата, промежуточных соединений примера 68, и 2-амино-1-(пирролидин-1-ил)этанона гидрохлорида (247 мг, 1,50 ммоль, синтезированного в качестве промежуточного соединения в примере 7).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,58-0,66 (2H, м), 0,71-0,79 (2H, м), 1,72-1,80 (2H, м), 1,83-1,91 (2H, м), 2,78 (1H, м), 3,28-3,40 (4H, м), 3,89 (2H, д, J=4,4 Гц), 6,54 (1H, дд, J=2,0, 6,0 Гц), 6,67 (1H, д, J=3,6 Гц), 6,94 (1H, д, J=2,0 Гц), 7,06 (1H, дд, J=2,4, 8,8 Гц), 7,38 (1H, д, J=2,4 Гц), 7,88 (1H, д, J=3,6 Гц), 8,05 (1H, д, J=6,0 Гц), 8,17 (1H, уш.с), 8,26-8,35 (2H, м), 9,28 (1H, с).
Пример 72
Циклопропиламид 5-(2-(3-(3-оксо-3-(пирролидин-1-ил)пропил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (113 мг, 0,227 ммоль) получали в виде белых кристаллов из смеси (165 мг) фенил-N-(4-(1-циклопропиламинокарбонил-1H-5-индолил)окси-2-пиридил)-N-(феноксикарбонил)карбамата и фенил-N-(4-(1-циклопропиламинокарбонил-1H-5-индолил)окси-2-пиридил)карбамата, промежуточных соединений примера 68, и 3-амино-1-(пирролидин-1-ил)пропан-1-она гидрохлорида (268 мг, 1,50 ммоль, синтезированного в качестве промежуточного соединения в примере 25).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,58-0,66 (2H, м), 0,71-0,79 (2H, м), 1,70-1,79 (2H, м), 1,79-1,88 (2H, м), 2,40 (2H, т, J=6,4 Гц), 2,78 (1H, м), 3,24-3,38 (6H, м), 6,51 (1H, дд, J=2,0, 6,0 Гц), 6,67 (1H, д, J=3,8 Гц), 6,93 (1H, д, J=2,0 Гц), 7,05 (1H, дд, J=2,4, 8,8 Гц), 7,37 (1H, д, J=2,4 Гц), 7,88 (1H, д, J=3,8 Гц), 7,98-8,10 (2H, м), 8,26-8,34 (2H, м), 9,09 (1H, с).
Пример 73
Циклопропиламид 5-(2-(3-((1R)-1-гидроксиметил-2-оксо-2-пиперидин-1-илэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (106 мг, 0,209 ммоль) получали в виде белых кристаллов из смеси (165 мг) фенил-N-(4-(1-циклопропиламинокарбонил-1H-5-индолил)окси-2-пиридил)-N-(феноксикарбонил)карбамата и фенил-N-(4-(1-циклопропиламинокарбонил-1H-5-индолил)окси-2-пиридил)карбамата, промежуточных соединений примера 68, и (2R)-2-амино-3-гидрокси-1-(пиперидин-1-ил)пропан-1-она (228 мг, 1,32 ммоль, синтезированного в качестве промежуточного соединения в примере 57).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,58-0,66 (2H, м), 0,70-0,78 (2H, м), 1,38-1,62 (6H, м), 2,79 (1H, м), 3,38-3,53 (6H, м), 4,75 (1H, м), 4,93 (1H, т, J=5,8 Гц), 6,54 (1H, дд, J=2,0, 6,0 Гц), 6,67 (1H, д, J=3,6 Гц), 6,97 (1H, д, J=2,0 Гц), 7,06 (1H, дд, J=2,4, 8,8 Гц), 7,37 (1H, д, J=2,4 Гц), 7,88 (1H, д, J=3,6 Гц), 8,05 (1H, д, J=6,0 Гц), 8,10-8,34 (3H, м), 9,20 (1H, с).
Пример 74
Циклопропиламид 5-(2-(3-((1S)-1-гидроксиметил-2-оксо-2-пиперидин-1-илэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (66,8 мг, 0,132 ммоль) получали в виде белых кристаллов из смеси (82,3 мг) фенил-N-(4-(1-циклопропиламинокарбонил-1H-5-индолил)окси-2-пиридил)-N-(феноксикарбонил)карбамата и фенил-N-(4-(1-циклопропиламинокарбонил-1H-5-индолил)окси-2-пиридил)карбамата, промежуточных соединений примера 68, и (2S)-2-амино-3-гидрокси-1-(пиперидин-1-ил)пропан-1-она гидрохлорида (156 мг, 0,748 ммоль, синтезированного в качестве промежуточного соединения в примере 20).
Пример 75
N1-Фенил-5-(2-(((3-(диэтиламино)пропил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Указанное в заголовке соединение получали из N1-фенил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамида (CAS No. 417721-87-0), который был описан в описании WO 02/32872, и 3-диэтиламинопропиламина с применением процедуры, аналогичной описанной в примере 28.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,91 (6H, т, J=7,2 Гц), 1,47-1,53 (2H, м), 2,30-2,44 (6H, м), 3,05-3,14 (2H, м), 6,52 (1H, дд, J=6,0, 2,0 Гц), 6,76 (1H, д, J=3,6 Гц), 6,84 (1H, д, J=2,0 H), 7,09 (1H, дд, J=9,2, 2,4 Гц), 7,13 (1H, т, J=7,6 Гц), 7,38 (2H, дд, J=7,6, 7,6 Гц), 7,42 (1H, д, J=2,4 Гц), 7,64 (2H, д, J=7,6 Гц), 8,02 (1H, д, J=6,0 Гц), 8,10-8,14 (2H, м), 8,27 (1H, д, J=9,2 Гц), 9,05 (1H, уш.с), 10,10 (1H, уш.с).
Пример 76
N1-Фенил-5-(2-(((3-(4-метилпиперазин-1-ил)пропил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение получали из N1-фенил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамида (CAS No. 417721-87-0), который был описан в WO 02/32872, и 1-(3-аминопропил)-4-метилпиперазина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,52-1,59 (2H, м), 2,13 (3H, с), 2,15-2,45 (10H, м), 3,08-3,15 (2H, м), 6,54 (1H, дд, J=6,0, 2,0 Гц), 6,79 (1H, д, J=3,6 Гц), 6,89 (1H, уш.с), 7,10 (1H, дд, J=2,4, 9,2 Гц), 7,15 (1H, т, J=7,6 Гц), 7,40 (2H, т, J=7,6 Гц), 7,44 (1H, д, J=2,4 Гц), 7,66 (2H, д, J=7,6 Гц), 8,03-8,07 (2H, м), 8,14 (1H, д, J=3,6 Гц), 8,29 (1H, д, J=9,2 Гц), 9,05 (1H, уш.с), 10,10 (1H, уш.с).
Пример 77
N1-Этил-5-(2-(((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид
Тетрагидрофуран (20 мл) и триэтиламин (2,70 мл, 19,4 ммоль) добавляли к N1-этил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамиду (1,91 г, 6,45 ммоль, пример получения 27-1), туда при 0°С при перемешивании добавляли фенилхлорформиат (1,79 мл, 14,2 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 2 часов. Реакционную смесь подвергали распределению между этилацетатом и водой, органический слой концентрировали с получением смеси (2,95 г) фенил-N-(4-(1-(этиламино)карбонил-1H-5-индолил)окси-2-пиридил)карбамата и фенил-N-(4-(1-(этиламино)карбонил-1H-5-индолил)окси-2-пиридил)-N-(феноксикарбонил)карбамата. Часть смеси в количестве 0,454 г растворяли в N,N-диметилформамиде (5 мл), добавляли 4-(1-пирролидинил)пиперидин (0,522 г, 3,39 ммоль) и реакционную смесь перемешивали в течение 5 часов. Реакционную смесь подвергали распределению между этилацетатом и водой; органический слой концентрировали с получением твердого вещества; полученное твердое вещество промывали смесью гексан:диэтиловый эфир=1:1 с получением указанного в заголовке соединения в виде кристаллов (205 мг, 0,43 ммоль).
МС-спектр (ESI): 477 (M+1), 953 (2M+1).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,12-1,22 (5H, м), 1,57-1,81 (6H, м), 2,05-2,15 (1H, м), 2,38-2,50 (4H, м), 2,77-2,78 (2H, м), 3,28-3,37 (2H, м), 3,87-3,97 (2H, м), 6,53 (1Н, дд, J=2,5, 5,4 Гц), 6,66 (1H, д, J=3,5 Гц), 7,02 (1H, дд, J=2,5, 8,9 Гц), 7,30 (1H, д, J=2,5 Гц), 7,36 (1H, д, J=2,5 Гц), 7,89 (1H, д, J=3,5 Гц), 8,05 (1H, д, J=5,4 Гц), 8,20 (1H, м), 8,27 (1H, т, J=8,9 Гц), 9,08 (1H, с).
Пример 78
Этиламид 5-(2-(((4-гидрокси-4-метилпиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Аналогично примеру 41 указанное в заголовке соединение получали в виде бесцветных кристаллов (124 мг, 0,283 ммоль, 89,4%) из 4-гидрокси-4-метилпиперидина моногидрохлорида (216 мг, 1,42 ммоль, пример получения 8-3) и фенил-N-(4-(1-(этиламино)карбонил-1H-5-индолилокси-2-пиридил)-N-(феноксикарбонил)карбамата (170 мг, 0,317 ммоль, пример получения 55-1).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,08 (3H, с), 1,17 (3H, т, J=7,2 Гц), 1,38-1,44 (4H, м), 3,13 (2H, м), 3,30 (2H, м), 3,63 (2H, м), 4,27 (1H, с), 6,53 (1H, дд, J=2,4, 6,0 Гц), 6,67 (1H, д, J=3,6 Гц), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,32 (1H, д, J=2,4 Гц), 7,35 (1H, д, J=2,4 Гц), 7,90 (1H, д, J=3,0 Гц), 8,05 (1H, д, J=6,0 Гц), 8,21 (1H, т, J=5,4 Гц), 8,27 (1H, д, J=8,8 Гц), 9,04 (1H, с).
Пример 79
N1-Этил-5-(2-((4-гидроксипиперидин-1-ил)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 27 указанное в заголовке соединение получали в виде белого порошка (18,7 мг, 0,044 ммоль, 14,7%) из фенил N-(4-(1-(этиламино)карбонил-1H-5-индолил)окси-2-пиридил)карбамата (125 мг, 0,30 ммоль, пример получения 27-2) и 4-гидроксипиперидина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,13-1,27 (5H, м), 1,63-1,67 (2H, м), 2,98 (2H, м), 3,20-3,40 (2H, м), 3,60 (1H, м), 3,74 (2H, м), 4,64 (1H, д, J=4,4 Гц), 6,53 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,31 (1H, д, J=2,4 Гц), 7,35 (1H, д, J=2,4 Гц), 7,90 (1H, д, J=3,6 Гц), 8,06 (1H, д, J=5,6 Гц), 8,21 (1H, т, J=5,2 Гц), 8,27 (1H, д, J=8,8 Гц), 9,09 (1H, с).
Пример 80
N1-Этил-5-(2-(пиперидин-1-илкарбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
К смеси (0,336 г) фенил-N-(4-(1-(этиламино)карбонил-1H-5-индолил)окси-2-пиридил)карбамата и фенил-N-(4-(1-(этиламино)карбонил-1H-5-индолил)окси-2-пиридил)-N-(феноксикарбонил)карбамата, полученной в примере 77, добавляли N,N-диметилформамид (4 мл) и пиперидин (0,31 мл, 3,13 ммоль), реакционную смесь перемешивали в течение ночи, реакционную смесь подвергали распределению между этилацетатом и водой и органический слой концентрировали с получением указанного в заголовке соединения в виде кристаллов (182 мг, 0,45 ммоль).
МС-спектр (ESI): 408 (M+1), 815 (2M+1).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,18 (3H, т, J=7,6 Гц), 1,35-1,57 (6H, м), 3,23-3,33 (6H, м), 6,52 (1H, дд, J=2,4, 5,4 Гц), 6,67 (1H, д, J=3,4 Гц), 7,03 (1H, дд, J=2,4, 8,7 Гц), 7,30 (1H, д, J=2,4 Гц), 7,36 (1H, д, J=2,4 Гц), 7,90 (1H, д, J=3,4 Гц), 8,06 (1H, д, J=5,5 Гц), 8,21 (1H, т, J=5,5 Гц), 8,27 (1H, д, J=8,7 Гц), 9,05 (1H, с).
Пример 81
N1-Этил-5-((2-((пирролидин-1-илкарбонил)амино)-4-пиридил)окси)-1H-1-индолкарбоксамид
К смеси (0,461 г) фенил-N-(4-(1-(этиламино)карбонил)-1H-5-индолил)окси-2-пиридил)карбамата и фенил-N-(4-(1-(этиламино)карбонил-1H-5-индолил)окси)-2-пиридил)-N-(феноксикарбонил)карбамата, полученной в примере 77, добавляли N,N-диметилформамид (5 мл) и пирролидин (0,36 мл, 4,3 ммоль), реакционную смесь перемешивали в течение ночи, реакционную смесь подвергали распределению между этилацетатом и водой и органический слой концентрировали с получением указанного в заголовке соединения в виде кристаллов (245 мг, 0,623 ммоль).
МС-спектр (ESI): 394 (M+1), 787 (2M+1).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,16 (3H, т, J=7,6 Гц), 1,70-1,82 (4H, м), 3,22-3,40 (6H, м), 6,54 (1H, дд, J=2,4, 5,5 Гц), 6,67 (1H, д, J=3,4 Гц), 7,03 (1H, дд, J=2,4, 8,7 Гц), 7,35 (1H, д, J=2,4 Гц), 7,41 (1H, д, J=2,4 Гц), 7,90 (1H, д, J=3,4 Гц), 8,06 (1H, д, J=5,5 Гц), 8,21 (1H, т, J=5,5 Гц), 8,27 (1H, д, J=8,7 Гц), 8,59 (1H, с).
Пример 82
N4-(4-((1-Этиламино)карбонил-1H-5-индолил)окси)-2-пиридил)-4-морфолинкарбоксамид
К смеси (0,401 г) фенил-N-(4-(1-(этиламино)карбонил)-1H-5-индолил)окси-2-пиридил)карбамата и фенил-N-(4-(1-(этиламино)карбонил-1H-5-индолил)окси)-2-пиридил)-N-(феноксикарбонил)карбамата, полученной в примере 77, добавляли N,N-диметилформамид (5 мл) и морфолин (0,326 мл, 3,73 ммоль), реакционную смесь перемешивали в течение ночи, реакционную смесь подвергали распределению между этилацетатом и водой, органический слой концентрировали и полученное твердое вещество промывали смесью растворителей гексан:диэтиловый эфир=1:1 с получением указанного в заголовке соединения (255 мг, 0,62 ммоль).
МС-спектр (ESI): 410 (M+1), 819 (2M+1).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,17 (3H, т, J=7,7 Гц), 3,25-3,42 (6H, м), 3,48-3,53 (4H, м), 6,55 (1H, дд, J=2,6, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 7,02 (1H, дд, J=2,6, 8,7 Гц), 7,29 (1H, д, J=2,6 Гц), 7,35 (1H, д, J=2,4 Гц), 7,90 (1H, д, J=3,6 Гц), 8,08 (1H, д, J=5,6 Гц), 8,20 (1H, т, J=5,6 Гц), 8,28 (1H, т, J=5,6 Гц), 9,19 (1H, с).
Пример 83
N1-Этил-5-(2-((1,1-диоксотиоморфолин-4-илкарбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид
Аналогично примеру 54 указанное в заголовке соединение получали в виде бесцветных кристаллов (116 мг, 0,253 ммоль, 80,0%) из 1,1-диоксотиоморфолина гидрохлорида (248 мг, 1,42 ммоль, пример получения 54-3) и фенил-N-(4-(1-(этиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (170 мг, 0,317 ммоль, пример получения 55-1).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,17 (3H, т, J=7,2 Гц), 3,10 (4H, м), 3,29 (2H, м), 3,80 (4H, м), 6,58 (1H, дд, J=2,0, 5,6 Гц), 6,67 (1H, д, J=3,4 Гц), 7,03 (1H, дд, J=2,0, 9,0 Гц), 7,31 (1H, д, J=2,0 Гц), 7,36 (1H, д, J=2,0 Гц), 7,90 (1H, д, J=3,4 Гц), 8,10 (1H, д, J=5,6 Гц), 8,22 (1H, т, J=5,4 Гц), 8,28 (1H, д, J=9,0 Гц), 9,54 (1H, с).
Пример 84
N1-Этил-5-(2-((метоксиамино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 27 указанное в заголовке соединение получали в виде белых кристаллов (94,3 мг, 0,26 ммоль, 70,9%) из фенил-N-(4-(1-(этиламино)карбонил-1H-5-индолил)окси-2-пиридинил)карбамата (150 мг, 0,36 ммоль, пример получения 27-2) и метоксиламина гидрохлорида.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,17 (3H, т, J=7,2 Гц), 3,20-3,40 (2H, м), 3,59 (3H, с), 6,57 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 7,05 (1H, дд, J=2,4, 8,8 Гц), 7,16 (1H, с), 7,38 (1H, д, J=2,4 Гц), 7,90 (1H, д, J=3,6 Гц), 8,08 (1H, д, J=5,6 Гц), 8,21 (1H, м), 8,28 (1H, д, J=8,8 Гц), 8,95 (1H, с), 10,15 (1H, с).
Пример 85
N1-Циклопропил-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
К смеси (470 мг) фенил-N-(4-(1-циклопропиламинокарбонил-1H-5-индолил)окси-2-пиридил)-N-(феноксикарбонил)карбамата и фенил-N-(4-(1-циклопропиламинокарбонил-1H-5-индолил)окси-2-пиридил)карбамата, полученной в примере 68, добавляли N,N-диметилформамид (5 мл) и 4-гидроксипиперидин (433 мг, 4,29 ммоль), реакционную смесь перемешивали в течение ночи, реакционную смесь подвергали распределению между этилацетатом и водой и органический слой концентрировали с получением указанного в заголовке соединения в виде кристаллов (220 мг, 0,51 ммоль, 39%).
МС-спектр (ESI): 436 (M+1), 871 (2M+1).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,58-0,63 (2H, м), 0,69-0,76 (2Н, м), 1,18-1,30 (2Н, м), 1,60-1,70 (2Н, м), 2,70-2,80 (1Н, м), 2,93-3,02 (2H, м), 3,55-3,64 (1H, м), 3,69-3,77 (2H, м), 4,63 (1H, д, J=4,4 Гц), 6,53 (1H, дд, J=2,4, 5,8 Гц), 6,64 (1H, д, J=3,6 Гц), 7,04 (1H, дд, J=2,4, 8,5 Гц), 7,31 (1H, д, J=2,4 Гц), 7,35 (1H, д, J=2,4 Гц), 7,86 (1H, д, J=3,6 Гц), 8,06 (1H, д, J=5,8 Гц), 8,24-8,29 (2H, м), 9,08 (1H, с).
Пример 86
N1-Циклопропил-5-(2-(((4-гидрокси-4-метилпиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид
Аналогично примеру 41 указанное в заголовке соединение получали в виде бесцветных кристаллов (109 мг, 0,242 ммоль) из 4-гидрокси-4-метилпиперидина моногидрохлорида (221 мг, 1,46 ммоль, пример получения 8-3) и смеси (200 мг, промежуточный продукт примера 68) фенил-N-(4-(1-циклопропиламинокарбонил-1H-5-индолил)окси-2-пиридил)-N-(феноксикарбонил)карбамата и фенил-N-(4-(1-циклопропиламинокарбонил-1H-5-индолил)окси-2-пиридил)карбамата.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,61 (2H, м), 0,73 (2H, м), 1,08 (3H, с), 1,30-1,41 (4H, м), 2,76 (1H, м), 3,14 (2H, м), 3,63 (2H, м), 4,27 (1H, с), 6,53 (1H, д, J=5,4 Гц), 6,65 (1H, д, J=3,4 Гц), 7,03 (1H, д, J=8,8 Гц), 7,32 (1H, с), 7,35 (1H, с), 7,86 (1H, д, J=3,4 Гц) 8,06 (1H, д, J=5,4 Гц), 8,27 (2H, м), 9,04 (1H, с).
Пример 87
N4-(4-(1-(Циклопропиламино)карбонил)-1H-5-индолил)окси)-2-пиридил)-4-морфолинкарбоксамид
К смеси (0,470 мг) фенил-N-(4-(1-циклопропиламинокарбонил-1H-5-индолил)окси)-2-пиридил)-N-(феноксикарбонил)карбамата и фенил-N-(4-(1-циклопропиламинокарбонил)-1H-5-индолил)окси-2-пиридил)карбамата, полученной в примере 68, добавляли N,N-диметилформамид (5 мл) и морфолин (0,373 мл, 4,28 ммоль), реакционную смесь перемешивали в течение ночи, реакционную смесь подвергали распределению между этилацетатом и водой, органический слой концентрировали и полученное твердое вещество промывали смесью растворителей гексан:диэтиловый эфир=1:1 с получением указанного в заголовке соединения (255 мг, 0,58 ммоль, 95%).
МС-спектр (ESI): 422 (M+1), 843 (2M+1).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,58-0,75 (4H, м), 2,72-2,81 (1H, м), 3,26-3,40 (4H, м), 3,50 (4H, т, J=4,8 Гц), 6,56 (1H, дд, J=2,5, 5,6 Гц), 6,65 (1H, д, J=3,4 Гц), 7,04 (1H, дд, J=2,5, 8,8 Гц), 7,30 (1H, д, J=2,5 Гц), 7,36 (1H, д, J=2,5 Гц), 7,86 (1H, д, J=3,4 Гц), 8,08 (1H, д, J=5,5 Гц), 8,24-8,30 (2H, м), 9,18 (1H, с).
Пример 88
N1-Циклопропил-5-(2-((пирролидин-1-илкарбонил)амино)-4-пиридил)окси)-1H-1-индолкарбоксамид
К смеси (0,470 мг) фенил-N-(4-(1-циклопропиламинокарбонил-1H-5-индолил)окси)-2-пиридил)-N-(феноксикарбонил)карбамата и фенил-N-(4-(1-циклопропиламинокарбонил)-1H-5-индолил)окси-2-пиридил)карбамата, полученной в примере 68, добавляли N,N-диметилформамид (5 мл) и пирролидин (0,35 мл, 4,2 ммоль), реакционную смесь перемешивали в течение ночи, реакционную смесь подвергали распределению между этилацетатом и водой и органический слой концентрировали с получением указанного в заголовке соединения в виде белых кристаллов (200 мг, 0,49 ммоль).
МС-спектр (ESI): 406 (M+1), 811 (2M+1).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,58-0,78 (4H, м), 1,70-1,83 (4H, м), 2,73-2,81 (1H, м), 3,23-3,45 (4H, м), 6,55 (1H, дд, J=2,2, 5,7 Гц), 6,65 (1H, д, J=3,5 Гц), 7,03 (1H, дд, J=2,2, 8,7 Гц), 7,36 (1H, д, J=2,2 Гц), 7,41 (1H, д, J=2,2 Гц), 7,86 (1H, д, J=3,5 Гц), 8,06 (1H, д, J=5,7 Гц), 8,16-8,30 (2H, м), 8,59 (1H, с).
Пример 89
N1-Циклопропил-5-(2-(пиперидин-1-илкарбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
К смеси (0,467 мг) фенил-N-(4-(1-циклопропиламинокарбонил-1H-5-индолил)окси-2-пиридил)-N-(феноксикарбонил)карбамата и фенил-N-(4-(1-циклопропиламинокарбонил-1H-5-индолил)окси-2-пиридил)карбамата, полученной в примере 68, добавляли N,N-диметилформамид (5 мл) и пиперидин (0,42 мл, 4,2 ммоль); реакционную смесь перемешивали в течение ночи; реакционную смесь подвергали распределению между этилацетатом и водой; органический слой концентрировали; полученное твердое вещество промывали смесью растворителей гексан:диэтиловый эфир=1:1 с получением указанного в заголовке соединения в виде кристаллов (241 мг, 0,57 ммоль).
МС-спектр (ESI): 420 (M+1), 839 (2M+1).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,58-0,77 (4H, м), 1,34-1,55 (6H, м), 2,72-2,81 (1H, м), 3,27-3,40 (4H, м), 6,52 (1H, дд, J=2,6, 5,6 Гц), 6,64 (1H, д, J=3,6 Гц), 7,03 (1H, дд, J=2,6, 8,7 Гц), 7,30 (1H, д, J=2,6 Гц), 7,35 (1H, д, J=2,6 Гц), 7,87 (1H, д, J=3,6 Гц), 8,06 (1H, д, J=5,6 Гц), 8,23-8,30 (2H, м), 9,03 (1H, с).
Пример 90
N4-(4-(1-(Циклопентиламино)карбонил)-1H-5-индолил)окси-2-пиридил)-4-морфолинкарбоксамид
Фенил-N-(4-(1-циклопентиламинокарбонил-1H-индол-5-илокси)-2-пиридил)-N-(феноксикарбонил)карбамат (200 мг, 0,35 ммоль) растворяли в N,N-диметилформамиде (1,5 мл) и морфолине (0,15 мл, 1,73 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение ночи. Реакционную смесь подвергали распределению между этилацетатом и водой, органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia BW-300; этилацетат, смесь этилацетат:метанол=10:1 в данном порядке); полученное бесцветное масло кристаллизовали добавлением диэтилового эфира, кристаллы отфильтровывали, промывали диэтиловым эфиром и сушили при аэрировании с получением указанного в заголовке соединения в виде бесцветных кристаллов (140 мг, 0,31 ммоль, 90%).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,48-1,64 (4H, м), 1,66-1,76 (2H, м), 1,88-1,98 (2H, м), 3,35 (4H, м), 3,51 (4H, м), 4,14 (1H, м), 6,56 (1H, д, J=6,0 Гц), 6,65 (1H, д, J=3,6 Гц), 7,02 (1H, д, J=8,8 Гц), 7,30 (1H, с), 7,35 (1H, с), 7,96 (1H, д, J=3,6 Гц), 8,00 (1H, д, J=6,8 Гц), 8,08 (1H, д, J=6,0 Гц), 8,25 (1H, д, J=8,8 Гц), 9,18 (1H, с).
Исходные вещества синтезировали следующим образом.
Пример получения 90-1
Фенил-N-циклопентилкарбамат
Циклопентиламин (9,9 мл, 100 ммоль) растворяли в тетрагидрофуране (400 мл); туда добавляли пиридин (8,9 мл, 110 ммоль) и реакционную смесь перемешивали. Реакционную смесь охлаждали с помощью льда; по каплям в течение 5 минут при перемешивании добавляли фенилхлорформиат (13,8 мл, 110 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 24,5 часов. Реакционную смесь подвергали распределению между этилацетатом и водой; органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Полученные кристаллы суспендировали в смеси растворителей гексан:этилацетат=5:1, отфильтровывали, промывали гексаном и сушили при аэрировании с получением указанного в заголовке соединения в виде бесцветных кристаллов (16,6 г, 81 ммоль, 81%).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,47 (4H, м), 1,63 (2H, м), 1,81 (2H, м), 3,81 (1H, м), 7,07 (2H, д, J=7,6 Гц), 7,17 (1H, т, J=7,6 Гц), 7,35 (2H, т, J=7,6 Гц), 7,75 (1H, д, J=6,8 Гц).
Пример получения 90-2
N1-Циклопентил-5-(2-аминопиридин-4-илокси)-1H-1-индолкарбоксамид
4-(1H-5-Индолилокси)-2-пиридинамин (2,50 г, 11,1 ммоль, CAS No. 417722-11-3), который был описан в WO 02/32872, растворяли в N,N-диметилформамиде (30 мл); туда добавляли гидрид натрия (0,530 г, 13,3 ммоль) при комнатной температуре и реакционную смесь перемешивали в течение 30 минут. Туда при комнатной температуре при перемешивании добавляли фенил-N-циклопентилкарбамат (2,50 г, 12,2 ммоль) и реакционную смесь перемешивали в течение 30 минут. К реакционной смеси добавляли воду и выпавшие кристаллы отфильтровывали и промывали водой. Данные кристаллы растворяли в метаноле и очищали колоночной хроматографией на силикагеле (Fuji Silysia NH; смесь гексан:этилацетат=1:1, этилацетат, смесь этилацетат:метанол=98:2 в данном порядке). Полученные кристаллы суспендировали в смеси гексан:этанол=10:1, отфильтровывали, промывали гексаном и сушили при аэрировании с получением указанного в заголовке соединения в виде бесцветных кристаллов (2,08 г, 6,18 ммоль, 55,7%).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,56 (4H, м), 1,71 (2H, м), 1,92 (2H, м), 4,14 (1H, м), 5,74 (1H, д, J=2,0 Гц), 5,83 (2H, с), 6,12 (1H, дд, J=2,0, 5,6 Гц), 6,64 (1H, д, J=3,4 Гц), 7,00 (1H, дд, J=2,0, 8,8 Гц), 7,32 (1H, д, J=2,0 Гц), 7,75 (1H, д, J=5,6 Гц), 7,94 (1H, д, J=3,4 Гц), 7,97 (1H, д, J=6,4 Гц), 8,23 (1H, д, J=8,8 Гц).
Пример получения 90-3
Фенил-N-(4-(1-циклопентиламинокарбонил-1H-индол-5-илокси)-2-пиридил)-N-(феноксикарбонил)карбамат
N1-Циклопентил-5-(2-аминопиридин-4-илокси)-1H-1-индолкарбоксамид (1,55 г, 4,58 ммоль) растворяли в тетрагидрофуране (90 мл); туда добавляли триэтиламин (1,43 мл, 10,31 ммоль) и пиридин (0,56 мл, 6,88 ммоль) и реакционную смесь перемешивали. Реакционную смесь охлаждали с помощью льда; по каплям добавляли фенилхлорформиат (1,44 мл, 11,45 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 2,5 часов. Реакционную смесь подвергали распределению между этилацетатом и водой, органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia BW-300; смесь гексан:этилацетат=1:1, 1:3, в данном порядке) с получением указанного в заголовке соединения в виде бесцветного аморфного твердого вещества (2,516 г, 4,36 ммоль, 95,2%).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,50-1,63 (4H, м), 1,66-1,74 (2H, м), 1,88-1,98 (2H, м), 4,15 (1H, м), 6,65 (1H, д, J=3,8 Гц), 6,95 (1H, дд, J=2,4, 5,6 Гц), 7,09 (1H, дд, J=2,4, 8,8 Гц), 7,16 (4H, д, J=7,6 Гц), 7,29 (2H, д, J=7,6 Гц), 7,42 (4H, д, J=7,6 Гц), 7,44 (1H, д, J=2,4 Гц), 7,51 (1H, д, J=2,4 Гц), 7,98 (1H, д, J=3,8 Гц), 8,01 (1H, д, J=6,8 Гц), 8,28 (1H, д, J=8,8 Гц), 8,42 (1H, д, J=5,6 Гц).
Пример 91
Циклопентиламид 5-(2-(((4-гидроксипиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты
Аналогично примеру 90 указанное в заголовке соединение получали в виде бесцветных кристаллов (129 мг, 0,278 ммоль, 80,2%) из фенил-N-(4-(1-циклопентиламинокарбонил-1H-индол-5-илокси)-2-пиридил)-N-(феноксикарбонил)карбамата (200 мг, 0,346 ммоль, пример получения 90-3) и 4-гидроксипиперидина (175 мг, 1,73 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,23 (2H, м), 1,48-1,77 (8H, м), 1,92 (2H, м), 2,98 (2H, м), 3,59 (1H, м), 3,73 (2H, м), 4,15 (1H, м), 4,64 (1H, д, J=4,4 Гц), 6,53 (1H, дд, J=2,0, 5,6 Гц), 6,65 (1H, д, J=3,6 Гц), 7,02 (1H, дд, J=2,0, 9,0 Гц), 7,31 (1H, д, J=2,0 Гц), 7,35 (1H, д, J=2,0 Гц), 7,96 (1H, д, J=3,6 Гц), 7,99 (1H, д, J=6,8 Гц), 8,06 (1H, д, J=5,6 Гц), 8,24 (1H, д, J=9,0 Гц), 9,09 (1H, с).
Пример 92
N1-Циклопентил-5-(2-((4-пирролидин-1-ил)пиперидин-1-илкарбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид
Аналогично примеру 90 указанное в заголовке соединение получали в виде бесцветных кристаллов (83 мг, 0,161 ммоль, 46,3%) из фенил-N-(4-(1-циклопентиламинокарбонил-1H-индол-5-илокси)-2-пиридил)-N-(феноксикарбонил)карбамата (200 мг, 0,346 ммоль, пример получения 90-3) и 4-(1-пирролидинил)пиперидина (268 мг, 1,73 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,18-1,30 (2H, м), 1,50-1,80 (12H, м), 1,87-1,98 (2H, м), 2,08 (1H, м), 2,43 (4H, м), 2,81 (2H, м), 3,91 (2H, м), 4,15 (1H, м), 6,53 (1H, дд, J=2,0, 5,6 Гц), 6,65 (1H, д, J=3,6 Гц), 7,02 (1H, дд, J=2,0, 9,0 Гц), 7,31 (1H, д, J=2,0 Гц), 7,35 (1H, д, J=2,0 Гц), 7,96 (1H, д, J=3,6 Гц), 7,99 (1H, д, J=6,8 Гц), 8,06 (1H, д, J=5,6 Гц), 8,25 (1H, д, J=9,0 Гц), 9,08 (1H, с).
Пример 93
N1-(3-Метилбутил)-5-(2-(((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид
К N1-(3-метилбутил)-5-((2-амино-4-пиридил)окси)-1H-1-индолкарбоксамиду (1,45 г, 4,29 ммоль) добавляли N,N-диметилформамид (30 мл), пиридин (0,52 мл, 6,4 ммоль) и триэтиламин (1,35 мл, 9,69 ммоль), при 0°С при перемешивании добавляли фенилхлорформиат (0,81 мл, 6,4 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 1 часа. Реакционную смесь подвергали распределению между этилацетатом и водой и органический слой концентрировали и подвергали колоночной хроматографии на силикагеле с получением смеси (2,0 г) фенил-N-(4-(1-((3-метилбутил)амино)карбонил-1H-5-индолил)окси-2-пиридил)карбамата и фенил-N-(4-(1-((3-метилбутил)амино)карбонил-1H-5-индолил)окси-2-пиридил)-N-(феноксикарбонил)карбамата. Часть смеси в количестве 0,4 г растворяли в N,N-диметилформамиде (4 мл); туда добавляли 4-(1-пирролидинил)пиперидин (0,43 г, 2,8 ммоль) и реакционную смесь перемешивали в течение 2 часов. Реакционную смесь подвергали распределению между этилацетатом и водой; органический слой концентрировали и остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia NH; смесь этилацетат:метанол=10:1) с получением указанного в заголовке соединения в виде белых кристаллов (275 мг, 0,53 ммоль).
МС-спектр (ESI): 519 (M+1).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,91 (6H, д, J=7,6 Гц), 1,18-1,30 (3H, м), 1,47 (2H, кв, J=7,6 Гц), 1,57-1,80 (6H, м), 2,03-2,22 (1H, м), 2,37-2,48 (4H, м), 2,76-2,85 (2H, м), 3,25-3,36 (2H, м), 3,88-3,97 (2H, м), 6,53 (1H, дд, J=2,4, 5,4 Гц), 6,66 (1H, д, J=3,6 Гц), 7,02 (1H, дд, J=2,4, 8,7 Гц), 7,31 (1H, д, J=2,4 Гц), 7,35 (1H, д, J=2,4 Гц), 7,90 (1H, д, J=3,6 Гц), 8,06 (1H, д, J=5,4 Гц), 8,16 (1H, т, J=5,4 Гц), 8,27 (1H, д, J=8,7 Гц), 9,08 (1H, с).
Исходные вещества синтезировали следующим образом.
Пример получения 93-1
N1-(3-Метилбутил)-5-((2-амино-4-пиридил)окси)-1H-1-индолкарбоксамид
4-(1H-5-Индолилокси)-2-пиридинамин (2,0 г, 8,9 ммоль, CAS No. 417722-11-3), который был описан в WO 02/32872, растворяли в N,N-диметилформамиде (20 мл) и туда при комнатной температуре при перемешивании добавляли гидрид натрия (426 мг, 10,7 ммоль). Через 30 минут реакционную смесь охлаждали в ледяной бане; туда добавляли фенил N-(3-метоксибутил)карбамат (2,02 г, 9,75 ммоль) и реакционную смесь перемешивали в течение 3 часов при комнатной температуре. Реакционную смесь подвергали распределению между этилацетатом и водой; органический слой промывали водой и насыщенным раствором соли, сушили над безводным сульфатом натрия и концентрировали; остаток очищали колоночной хроматографией на NH-силикагеле (смесь гексан:этилацетат=3:1) с получением указанного в заголовке соединения в виде кристаллов (1,45 г, 4,3 ммоль, 48%).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,89-0,93 (6H, м), 1,40-1,70 (3H, м), 3,25-3,40 (2H, м), 5,72-5,75 (1H, м), 5,83 (2H, с), 6,10-6,40 (1H, м), 6,64-6,68 (1H, м), 6,98-7,02 (1H, м), 7,30-7,34 (1H, м), 7,75 (1H, дд, J=1,5, 6,0 Гц), 7,86-7,90 (1H, м), 8,14 (1H, т, J=4,5 Гц), 8,25 (1H, д, J=9,0 Гц).
Пример получения 93-2
Фенил-N-(3-метоксибутил)карбамат
Фенилхлорформиат (14,8 мл, 0,117 моль) растворяли в тетрагидрофуране (200 мл); туда при комнатной температуре при перемешивании добавляли триэтиламин (18,0 мл, 0,129 моль) и изоамиламин (15,0 мл, 0,129 моль) и реакционную смесь перемешивали в течение ночи. Реакционную смесь подвергали распределению между этилацетатом и водой; органический слой концентрировали и сушили при пониженном давлении с получением указанного в заголовке соединения в виде кристаллов (14 г, 0,068 моль, 58%).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,89 (6H, д, J=7,9 Гц), 1,36 (2H, кв, J=7,9 Гц), 1,55-1,69 (1H, м), 3,05 (2H, кв, J=7,9 Гц), 7,03-7,09 (2H, м), 7,14-7,19 (1H, м), 7,31-7,38 (2H, м), 7,68 (1H, т, J=4,8 Гц).
Пример 94
N1-(3-Метилбутил)-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
К смеси (243 мг) фенил-N-(4-(1-((3-метилбутил)амино)карбонил-1H-5-индолил)окси-2-пиридил)карбамата и фенил-N-(4-(1-((3-метилбутил)амино)карбонил-1H-5-индолил)окси-2-пиридил)-N-(феноксикарбонил)карбамата, синтезированной в примере 93, добавляли N,N-диметилформамид (2,5 мл) и 4-гидроксипиперидин (213 мг, 2,11 ммоль) и реакционную смесь перемешивали в течение 2 часов. Реакционную смесь подвергали распределению между этилацетатом и водой; органический слой концентрировали и остаток очищали колоночной хроматографией на NH-силикагеле (смесь этилацетат:метанол=10:1) с получением указанного в заголовке соединения в виде белых кристаллов (150 мг, 0,322 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,91 (6H, д, J=7,2 Гц), 1,18-1,30 (2H, м), 1,46 (2H, кв, J=7,2 Гц), 1,60-1,70 (3H, м), 2,97 (2H, м), 3,25-3,35 (2H, м), 3,55-3,64 (1H, м), 3,69-3,80 (2H, м), 4,63 (1H, д, J=3,4 Гц), 6,53 (1H, дд, J=2,3, 5,8 Гц), 6,66 (1H, д, J=3,5 Гц), 7,02 (1H, дд, J=2,3, 8,6 Гц), 7,31 (1H, д, J=2,3 Гц), 7,35 (1H, д, J=2,3 Гц), 7,90 (1H, д, J=3,5 Гц), 8,06 (1H, д, J=5,8 Гц), 8,16 (1H, т, J=5,8 Гц), 8,26 (1H, т, J=8,6 Гц), 9,08 (1H, с).
Пример 95
N4-(4-(1-((Метилбутил)амино)карбонил)-1H-5-индолил)окси)-2-пиридил)-4-морфолинкарбоксамид
К смеси (0,6 г) фенил-N-(4-(1-((3-метилбутил)амино)карбонил-1H-5-индолил)окси-2-пиридил)карбамата и фенил-N-(4-(1-((3-метилбутил)амино)карбонил-1H-5-индолил)окси-2-пиридил)-N-(феноксикарбонил)карбамата, синтезированной в примере 93, добавляли N,N-диметилформамид (5 мл) и морфолин (0,163 мл, 1,87 ммоль); реакционную смесь перемешивали в течение 2 часов. Реакционную смесь подвергали распределению между этилацетатом и водой; органический слой концентрировали и остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia NH, смесь этилацетат:метанол=10:1) с получением указанного в заголовке соединения в виде белых кристаллов (0,202 г, 0,447 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,92 (6H, дд, J=1,7, 7,3 Гц), 1,47 (2H, кв, J=7,3 Гц), 1,58-1,70 (1H, м), 3,25-3,60 (10H, м), 6,55-6,59 (1H, м), 6,65-6,70 (1H, м), 7,00-7,07 (1H, м), 7,32 (1H, с), 7,37 (1H, м), 7,90 (1H, м), 8,07 (1H, м), 8,17 (1H, т, J=5,2 Гц), 8,27 (1H, д, J=8,3 Гц), 9,18 (1H, с).
Пример 96
N1-(1-Этилпропил)-5-(2-(((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид
К N1-(1-этилпропил)-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамиду (1,45 г, 4,29 ммоль) добавляли тетрагидрофуран (20 мл) и триэтиламин (1,73 мл, 12,4 ммоль); туда добавляли при 0°С фенилхлорформиат (1,15 мл, 9,1 ммоль) при перемешивании; и реакционную смесь перемешивали при комнатной температуре в течение 1 часа. Реакционную смесь подвергали распределению между этилацетатом и водой; и органический слой концентрировали и подвергали колоночной хроматографии на силикагеле с получением смеси (1,8 г) фенил N-(4-(1-((1-этилпропил)амино)карбонил-1H-5-индолил)окси-2-пиридил)карбамата и фенил N-(4-(1-((1-этилпропил)амино)карбонил-1H-5-индолил)окси-2-пиридил)-N-(феноксикарбонил)карбамата. Часть смеси в количестве 0,6 г растворяли в N,N-диметилформамиде (5 мл); туда добавляли 4-(1-пирролидинил)пиперидин (0,7 г, 4,7 ммоль) и перемешивали в течение 2 часов; реакционную смесь подвергали распределению между этилацетатом и водой; органический слой концентрировали; и остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia NH, смесь этилацетат:метанол=10:1) с получением белых кристаллов (202 мг, 0,391 ммоль).
МС спектр (ESI): 519 (M+1).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,90 (6H, т, J=7,5 Гц), 1,20-1,30 (3H, м), 1,47-1,80 (9H, м), 2,03-2,12 (1H, м), 2,40-2,47 (4H, м), 2,77-2,86 (2H, м), 3,62-3,72 (1H, м), 3,88-3,95 (2H, м), 6,53 (1H, дд, J=2,4, 5,9 Гц), 6,66 (1H, д, J=3,5 Гц), 7,02 (1H, дд, J=2,4, 8,8 Гц), 7,11 (1H, д, J=2,4 Гц), 7,35 (1H, д, J=2,4 Гц), 7,78 (1H, д, J=8,8 Гц), 7,99 (1H, д, J=3,5 Гц), 8,06 (1H, д, J=5,9 Гц), 8,25 (1H, т, J=8,8 Гц), 9,08 (1H, с).
Исходные вещества синтезировали следующими способами.
Пример получения 96-1
N1-(1-Этилпропил)-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамид
4-(1H-5-Индолилокси)-2-пиридинамин (1,85 г, 8,2 ммоль, CAS No. 417722-11-3), который был описан в WO 02/32872, растворяли в N,N-диметилформамиде (20 мл); и туда добавляли гидрид натрия (394 мг, 9,84 ммоль) при перемешивании при комнатной температуре. Реакционную смесь охлаждали в ледяной бане через 30 минут; добавляли фенил N-(1-этилпропил)карбамат (1,87 г, 9,03 ммоль); и реакционную смесь перемешивали при комнатной температуре в течение 3 часов. Реакционную смесь подвергали распределению между этилацетатом и водой; органический слой промывали водой и насыщенным раствором соли, сушили над безводным сульфатом натрия, концентрировали; и остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia NH; смесь гексан:этилацетат=3:1) с получением указанного в заголовке соединения в виде кристаллов (1,95 г, 5,8 ммоль, 71%).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,89 (6H, т, J=7,5 Гц), 1,44-1,63 (4H, м), 3,60-3,72 (1H, м), 5,73 (1H, д, J=2,6 Гц), 5,80 (2H, с), 6,12 (1H, дд, J=2,6, 6,0 Гц), 6,67 (1H, д, J=4,3 Гц), 7,00 (1H, дд, J=2,6, 8,6 Гц), 7,32 (1H, д, J=2,6 Гц), 7,75 (1H, д, J=6,0 Гц), 7,98 (1H, д, J=4,3 Гц), 8,23 (1H, д, J=8,6 Гц), 9,30 (1H, с).
Пример получения 96-2
Фенил N-(1-этилпропил)карбамат
1-Этилпропиламин (11,6 мл, 100 ммоль) растворяли в тетрагидрофуране (400 мл); туда добавляли пиридин (8,9 мл, 110 ммоль) при комнатной температуре; и реакционную смесь перемешивали. Реакционную смесь охлаждали в ледяной бане; по каплям добавляли фенилхлорформиат (13,8 мл, 110 ммоль); и реакционную смесь перемешивали при комнатной температуре в течение 24 часов. К реакционной смеси добавляли воду; реакционную смесь подвергали распределению между этилацетатом и водой; и органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом натрия, и растворитель отгоняли при пониженном давлении. Полученные кристаллы промывали смесью диэтиловый эфир:гексан=1:5 с получением указанного в заголовке соединения в виде кристаллов (22,3 г, 147 ммоль, 59,1%).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,87 (6H, т, J=7,5 Гц), 1,30-1,56 (4H, м), 3,20-3,34 (1H, м), 7,03-7,08 (2H, м), 7,14-7,19 (1H, м), 7,32-7,38 (2H, м), 7,51 (1H, д, J=8,7 Гц).
Пример 97
N1-(1-Этилпропил)-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
К смеси (456 мг) фенил-N-(4-(1-((1-этилпропил)амино)карбонил-1H-5-индолил)окси-2-пиридил)карбамата и фенил-N-(4-(1-((1-этилпропил)амино)карбонил-1H-5-индолил)окси-2-пиридил)-N-(феноксикарбонил)карбамата, синтезированной в примере 96, добавляли N,N-диметилформамид (4 мл) и 4-гидроксипиперидин (380 мг, 3,56 ммоль) и реакционную смесь перемешивали в течение 2 часов. Реакционную смесь подвергали распределению между этилацетатом и водой; органический слой концентрировали и остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia NH; смесь этилацетат:метанол=10:1) с получением указанного в заголовке соединения в виде белых кристаллов (1,37 мг, 0,294 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,90 (6H, т, J=7,5 Гц), 1,18-1,30 (3H, м), 1,45-1,70 (6H, м), 2,92-3,02 (2H, м), 3,55-3,80 (3H, м), 4,63 (1H, д, J=5,1 Гц), 6,53 (1H, м), 6,66 (1H, д, J=3,5 Гц), 7,02 (1H, дд, J=2,5, 8,8 Гц), 7,31 (1H, д, J=2,5 Гц), 7,36 (1H, д, J=2,5 Гц), 7,78 (1H, д, J=8,8 Гц), 7,98 (1H, д, J=3,5 Гц), 8,06 (1H, д, J=5,7 Гц), 8,24 (1H, т, J=8,8 Гц), 9,08 (1H, с).
Пример 98
N4-(4-(1-((1-Этилпропил)амино)карбонил-1H-5-индолил)окси-2-пиридил)-4-морфолинкарбоксамид
К смеси (0,324 г) фенил-N-(4-(1-((1-этилпропил)амино)карбонил-1H-5-индолил)окси-2-пиридил)карбамата и фенил-N-(4-(1-((1-этилпропил)амино)карбонил-1H-5-индолил)окси-2-пиридил)-N-(феноксикарбонил)карбамата, синтезированной в примере 96, добавляли N,N-диметилформамид (3 мл) и морфолин (0,22 мл, 2,5 ммоль) и реакционную смесь перемешивали в течение 2 часов. Реакционную смесь подвергали распределению между этилацетатом и водой; органический слой концентрировали и остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia NH, смесь этилацетат:метанол=10:1) с получением указанного в заголовке соединения в виде белых кристаллов (95 мг, 0,21 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,91 (6H, т, J=7,5 Гц), 1,45-1,65 (4H, м), 3,37-3,40 (4H, м), 3,48-3,58 (4H, м), 3,62-3,72 (1H, м), 6,56 (1H, дд, J=2,6, 5,8 Гц), 6,68 (1H, д, J=3,5 Гц), 7,02 (1H, дд, J=2,6, 8,8 Гц), 7,31 (1H, д, J=2,6 Гц), 7,36 (1H, д, J=2,6 Гц), 7,80 (1H, д, J=9,1 Гц), 8,00 (1H, д, J=3,5 Гц), 8,08 (1H, д, J=5,8 Гц), 8,26 (1H, д, J=8,8 Гц), 9,18 (1H, с).
Пример 99
N4-(4-(1-((1-Пентил)амино)карбонил-1H-5-индолил)окси-2-пиридил)-4-морфолинкарбоксамид
Аналогично примеру 90 указанное в заголовке соединение получали в виде бесцветных кристаллов (131 мг, 0,29 ммоль, 84%) из фенил-N-(4-(1-(1-пентиламино)карбонил-1H-индол-5-илокси)-2-пиридил)-N-(феноксикарбонил)карбамата (200 мг, 0,35 ммоль) и морфолина (0,15 мл, 1,7 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,88 (3H, т, J=6,0 Гц), 1,31 (4H, м), 1,56 (2H, м), 3,26 (2H, м), 3,35 (4H, м), 3,51 (4H, м), 6,56 (1H, д, J=5,6 Гц), 6,67 (1H, д, J=3,0 Гц), 7,03 (1H, д, J=8,0 Гц), 7,31 (1H, с), 7,36 (1H, с), 7,91 (1H, д, J=3,0 Гц), 8,08 (1H, д, J=5,6 Гц), 8,20 (1H, т, J=5,6 Гц), 8,26 (1H, д, J=8,0 Гц), 9,18 (1H, с).
Исходные вещества синтезировали следующими способами.
Пример получения 99-1
Фенил-N-(1-пентил)карбамат
Аналогично примеру 90-1 указанное в заголовке соединение получали в виде бледно-желтых кристаллов (20,5 г, 99 ммоль, 99%) из 1-пентиламина (11,6 мл, 100 ммоль), пиридина (8,9 мл, 110 ммоль) и фенилхлорформиата (13,8 мл, 110 ммоль).
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 0,92 (3H, т, J=6,8 Гц), 1,36 (4H, м), 1,58 (2H, м), 3,26 (2H, кв, J=6,8 Гц), 5,00 (1H, уш.с), 7,13 (2H, д, J=7,6 Гц), 7,19 (1H, т, J=7,6 Гц), 7,35 (2H, т, J=7,6 Гц).
Пример получения 99-2
N1-(1-Пентил)-5-(2-аминопиридин-4-илокси)-1H-1-индолкарбоксамид
4-(1H-5-Индолилокси)-2-пиридинамин (5,0 г, 22 ммоль, CAS No. 417722-11-3), который был описан в WO 02/32872, растворяли в N,N-диметилформамиде (60 мл); туда добавляли гидрид натрия (1,06 г, 27 ммоль) при комнатной температуре и реакционную смесь перемешивали в течение 30 минут. Туда при перемешивании при комнатной температуре добавляли фенил-N-н-пентилкарбамат (5,06 г, 24 ммоль) и реакционную смесь перемешивали в течение 30 минут. Реакционную смесь подвергали распределению между водой и этилацетатом (нерастворимые части полностью растворялись при добавлении небольшого количества метанола); органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом натрия, концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia NH; смесь гексан:этилацетат=1:1, этилацетат, смесь этилацетат:метанол=95:5 в данном порядке). Полученные кристаллы суспендировали в смеси гексан:этанол=10:1, отфильтровывали, промывали гексаном и сушили при аэрировании с получением указанного в заголовке соединения в виде бесцветных кристаллов (1,55 г, 4,58 ммоль, 21%).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,87 (3Н, т, J=6,6 Гц), 1,31 (4H, м), 1,56 (2H, м), 3,25 (2H, м), 5,74 (1H, д, J=2,8 Гц), 5,83 (2H, с), 6,12 (1H, дд, J=2,8, 5,8 Гц), 6,65 (1H, д, J=3,6 Гц), 7,00 (1H, дд, J=2,0, 8,8 Гц), 7,32 (1H, д, J=2,0 Гц), 7,75 (1H, д, J=5,8 Гц), 7,89 (1H, д, J=3,6 Гц), 8,17 (1H, т, J=5,4 Гц), 8,25 (1H, д, J=8,8 Гц).
Пример получения 99-3
Фенил-N-(4-((1-пентил)аминокарбонил-1H-индол-5-илокси)-2-пиридил)-N-(феноксикарбонил)карбамат
Аналогично примеру 90-3 указанное в заголовке соединение получали в виде бесцветного аморфного твердого вещества (2,39 г, 4,13 ммоль, 90,1%) из N1-(1-пентил)-5-(2-аминопиридин-4-илокси)-1H-1-индолкарбоксамида (1,55 г, 4,58 ммоль), триэтиламина (1,43 мл, 10,31 ммоль), пиридина (0,56 мл, 6,88 ммоль) и фенилхлорформиата (1,44 мл, 11,45 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,87 (3H, т, J=6,4 Гц), 1,31 (4H, м), 1,56 (2H, м), 3,27 (2H, м), 6,56 (1H, д, J=3,6 Гц), 6,96 (1H, дд, J=2,4, 5,4 Гц), 7,09 (1H, дд, J=2,4, 9,0 Гц), 7,16 (4H, д, J=7,6 Гц), 7,29 (2H, т, J=7,6 Гц), 7,43 (5H, м), 7,51 (1H, д, J=2,4 Гц), 7,93 (1H, д, J=2,4 Гц), 8,21 (1H, т, J=5,6 Гц), 8,31 (1H, д, J=9,0 Гц), 8,42 (1H, д, J=5,4 Гц).
Пример 100
N1-(1-Пентил)-5-(2-(((4-гидроксипиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид
Аналогично примеру 90 указанное в заголовке соединение получали в виде бесцветных кристаллов (149 мг, 0,320 ммоль, 92,6%) из фенил-N-(4-(1-(1-пентил)аминокарбонил-1H-индол-5-илокси)-2-пиридил)-N-(феноксикарбонил)карбамата (200 мг, 0,346 ммоль, пример получения 99-3) и 4-гидроксипиперидина (174 мг, 1,73 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,87 (3H, м), 1,15-1,40 (6H, м), 1,50-1,70 (4H, м), 2,98 (2H, м), 3,36 (2H, м), 3,59 (1H, м), 3,74 (2H, м), 4,64 (1H, д, J=4,0 Гц), 6,53 (1H, д, J=5,2 Гц), 6,70 (1H, д, J=3,6 Гц), 7,03 (1H, д, J=8,6 Гц), 7,31 (1H, с), 7,35 (1H, с), 7,91 (1H, д, J=3,6 Гц), 8,06 (1H, д, J=5,2 Гц), 8,19 (1H, м), 8,26 (1H, д, J=8,6 Гц), 9,09 (1H, с).
Пример 101
N1-(1-Пентил)-5-(2-((4-(пирролидин-1-ил)пиперидин-1-илкарбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид
Аналогично примеру 90 указанное в заголовке соединение получали в виде бесцветных кристаллов (124 мг, 0,239 ммоль, 69,2%) из фенил-N-(4-(1-(1-пентил)аминокарбонил-1H-индол-5-илокси)-2-пиридил)-N-(феноксикарбонил)карбамата (200 мг, 0,346 ммоль, пример получения 99-3) и 4-(1-пирролидинил)пиперидина (267 мг, 1,73 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,87 (3H, т, J=6,8 Гц), 1,20-1,35 (6H, м), 1,52-1,67 (6H, м), 1,74 (2H, м), 2,08 (1H, м), 2,43 (2H, м), 2,81 (2H, т, J=7,6 Гц), 3,23-3,29 (4H, м), 3,92 (2H, м), 6,53 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,8 Гц), 7,03 (1H, дд, J=2,4, 9,2 Гц), 7,31 (1H, д, J=2,4 Гц), 7,35 (1H, д, J=2,4 Гц), 7,91 (1H, т, J=3,8 Гц), 8,06 (1H, д, J=5,6 Гц), 8,19 (1H, д, J=5,4 Гц), 8,26 (1H, д, J=9,2 Гц), 9,09 (1H, с).
Пример 102
N1-Метил-3-хлор-5-(2-(((3-(диэтиламино)пропил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Фенил-N-(4-(3-хлор-1-(метиламино)карбонил-1H-5-индолил)окси-2-пиридил)карбамат (160 мг), 3-(диэтиламино)пропиламин (120 мг), N,N-диметилформамид (5 мл) смешивали и перемешивали при комнатной температуре в течение 10 минут. После добавления водного бикарбоната натрия производили экстракцию этилацетатом. Очистка колоночной хроматографией на силикагеле (Fuji Silysia NH, этилацетат и затем смесь этилацетат: метанол=10:1) дала указанное в заголовке соединение в виде белого твердого вещества (86 мг).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,90 (6H, т, J=7,2 Гц), 1,46-1,56 (2H, м), 2,32-2,46 (6H, м), 2,83 (3H, д, J=4,4 Гц), 3,08-3,15 (2H, м), 6,52 (1H, дд, J=5,6, 2,4 Гц), 6,84 (1H, д, J=2,4 Гц), 7,16 (1H, дд, J=8,8, 2,4 Гц), 7,28 (1H, д, J=2,4 Гц), 8,02 (1H, д, J=5,6 Гц), 8,09 (2H, с), 8,21 (1H, кв, J=4,4 Гц), 8,33 (1H, д, J=8,8 Гц), 9,04 (1H, с).
Исходные вещества синтезировали следующим образом.
Пример получения 102-1
N1-Метил-5-(2-амино-4-пиридил)окси-3-хлор-1H-индолкарбоксамид
5-((2-Амино-4-пиридил)окси)-3-хлор-1H-1-индол (4,0 г, 15 ммоль, CAS No. 417721-98-3), описанный в WO 02/32872, растворяли в N,N-диметилформамиде (20 мл); туда добавляли гидрид натрия (0,68 г, 60% в масле) и фенил-N-метилкарбамат (2,6 г, продукт примера получения 2-1) и реакционную смесь перемешивали при комнатной температуре в течение 1 часа. Реакционную смесь подвергали распределению между этилацетатом и водой; органический слой концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia NH; смесь гексан:этилацетат=1:2) с получением указанного в заголовке соединения в виде бесцветного аморфного твердого вещества (1,5 г).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,83 (3H, д, J=4,0 Гц), 5,78 (1H, д, J=2,0 Гц), 5,88 (2H, уш.с), 6,14 (1H, дд, J=2,0, 5,8 Гц), 7,14 (1H, дд, J=2,4, 9,0 Гц), 7,23 (1H, д, J=2,4 Гц), 7,78 (1H, д, J=5,8 Гц), 8,08 (1H, с), 8,19 (1H, м), 8,32 (1H, д, J=9,0 Гц).
Пример получения 102-2
Фенил-N-(4-(3-хлор-1-(метиламино)карбонил-1H-5-индолил)окси-2-пиридил)карбамат
К охлажденной с помощью льда смеси N1-метил-5-(2-амино-4-пиридил)окси-3-хлор-1H-1-индолкарбоксамида (850 мг, пример получения 102-1), триэтиламина (0,37 мл), пиридина (320 мг) и N,N-диметилформамида (10 мл) по каплям добавляли хлорид натрия, фенилхлорформиат (630 мг). После перемешивания в течение 20 минут туда добавляли водный раствор бикарбоната натрия; производили экстракцию этилацетатом и производили очистку колоночной хроматографией на силикагеле (этилацетат). Выпавшие в осадок при добавлении этилацетата кристаллы отфильтровывали с получением указанного в заголовке соединения в виде белых кристаллов (160 мг).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,80 (3H, д, J=4,4 Гц), 6,70 (1H, дд, J=5,6, 2,4 Гц), 7,10-7,25 (4H, м), 7,26-7,40 (4H, м), 8,07 (1H, с), 8,18 (2H, м), 8,31 (1H, д, J=8,8 Гц), 10,77 (1H, с).
Пример 103
N1-Метил-3-хлор-5-(2-((4-(пирролидин-1-ил)пиперидин)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Смесь N1-метил-5-(2-амино-4-пиридил)окси-3-хлор-1H-1-индолкарбоксамида (278 мг, пример получения 102-1), триэтиламина (0,37 мл), тетрагидрофурана (5 мл) охлаждали на льду и перемешивали; к смеси по каплям добавляли фенилхлорформиат (0,33 мл) и реакционную смесь дополнительно перемешивали в течение 10 минут. Туда добавляли воду; производили экстракцию этилацетатом и производили очистку колоночной хроматографией на силикагеле с получением 373 мг остатка. Часть остатка в количестве 245 мг растворяли в N,N-диметилформамиде (2 мл); туда добавляли 4-(1-пирролидинил)пиперидин (345 мг) и реакционную смесь перемешивали при комнатной температуре в течение 30 минут. Производили экстракцию этилацетатом после добавления воды; органический слой промывали водой и насыщенным раствором соли, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia NH) с получением указанного в заголовке соединения (154 мг).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,19-1,30 (2H, м), 1,58-1,68 (4H, м), 1,70-1,78 (2H, м), 2,03-2,13 (1H, м), 2,36-2,46 (4H, м), 2,77-2,87 (5H, м), 3,88-3,97 (2H, м), 6,55 (1H, д, J=5,6 Гц), 7,16 (1H, дд, J=9,2, 2,4 Гц), 7,27 (1H, д, J=2,4 Гц), 7,32 (1H, с), 8,08 (1H, д, J=5,6 Гц), 8,10 (1H, с), 8,19-8,22 (1H, м), 8,33 (1H, д, J=9,2 Гц), 9,13 (1H, уш.с).
Пример 104
N1-Метил-3-хлор-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Смесь N1-метил-5-(2-амино-4-пиридил)окси-3-хлор-1H-1-индолкарбоксамида (480 мг, пример получения 102-1), триэтиламина (0,63 мл), тетрагидрофурана (15 мл) охлаждали на льду и перемешивали; к смеси по каплям добавляли фенилхлорформиат (710 мг) и реакционную смесь дополнительно перемешивали в течение 10 минут. Производили экстракцию этилацетатом после добавления воды и производили очистку колоночной хроматографией на силикагеле (смесь гексан:этилацетат=1:1). Полученный остаток растворяли в N,N-диметилформамиде (5 мл); туда добавляли 4-гидроксипиперидин (450 мг) и реакционную смесь перемешивали при комнатной температуре в течение ночи. К реакционной смеси добавляли воду; производили экстракцию этилацетатом и производили очистку колоночной хроматографией на силикагеле (Fuji Silysia NH, смесь этилацетат:метанол=40:1) с получением указанного в заголовке соединения в виде бесцветного порошка (78 мг).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,20-1,30 (2H, м), 1,61-1,79 (2H, м), 2,82 (3H, д, J=4,4 Гц), 2,94-3,03 (2H, м), 3,56-3,63 (1H, м), 3,70-3,78 (2H, м), 4,64 (1H, д, J=4,0 Гц), 6,55 (1H, дд, J=5,6, 2,4 Гц), 7,16 (1H, дд, J=8,8, 2,4 Гц), 7,27 (1H, д, J=2,4 Гц), 7,32 (1H, д, J=2,4 Гц), 8,08 (1H, д, J=5,6 Гц), 8,09 (1H, с), 8,21 (1H, кв, J=4,4 Гц), 8,32 (1H, д, J=8,8 Гц), 9,13 (1H, с).
Пример 105
N1-Метил-3-хлор-5-(2-(((3-(4-гидроксипиперидин)пропил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 103 указанное в заголовке соединение получали в виде белых кристаллов из 1-(3-аминопропил)-4-гидроксипиперидина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,25-1,38 (2H, м), 1,48-1,58 (2H, м), 1,62-1,70 (2H, м), 1,86-1,97 (2H, м), 2,18-2,25 (2H, м), 2,60-2,68 (2H, м), 2,83 (3H, д, J=3,6 Гц), 3,02-3,13 (2H, м), 3,34-3,42 (1H, м), 4,49 (1H, д, J=4,0 Гц), 6,52 (1H, дд, J=6,0, 2,4 Гц), 6,84-6,86 (1H, м), 7,17 (1H, дд, J=8,8, 2,4 Гц), 7,28 (1H, д, J=2,4 Гц), 8,01-8,05 (2H, м), 8,10 (1H, с), 8,19-8,24 (1H, м), 8,33 (1H, д, J=8,8 Гц), 9,04 (1H, уш.с).
Исходные вещества синтезировали следующим образом.
Пример получения 105-1
2-(3-(4-Гидроксипиперидин)пропил)изоиндолин-1,3-дион
N-(3-Бромпропил)фталимид (26,8 г), 4-гидроксипиперидин (15,0 г) и карбонат калия (27,6 г) добавляли к N,N-диметилформамиду; реакционную смесь перемешивали при комнатной температуре в течение ночи. После добавления воды производили экстракцию этилацетатом; органический слой промывали водой и насыщенным раствором соли, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении с получением указанного в заголовке соединения (13,9 г).
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 1,40-2,05 (6H, м), 2,10-2,60 (4H, м), 2,70-2,90 (2H, м), 3,60-3,85 (3H, м), 7,70-7,75 (2H, м), 7,82-7,87 (2H, м).
Пример получения 105-2
Бензил-N-(3-(4-гидроксипиперидин)пропил)карбамат
К 2-(3-(4-гидроксипиперидин)пропил)изоиндолин-1,3-диону (4,5 г) добавляли этанол (100 мл) и гидразингидрат (1,5 г); реакционную смесь нагревали до кипения с обратным холодильником в течение 2,5 часов и полученные кристаллы отфильтровывали. К фильтрату добавляли N-метилморфолин (2,5 мл) и N-(бензилоксикарбонилокси)сукцинимид (5,2 г) и реакционную смесь перемешивали при комнатной температуре в течение ночи. К реакционной смеси добавляли водный раствор бикарбоната натрия; производили экстракцию этилацетатом; органический слой промывали водой и насыщенным раствором соли, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле с получением указанного в заголовке соединения (2,96 г).
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 1,52-2,10 (6H, м), 2,10-2,60 (4H, м), 2,78-2,90 (2H, м), 3,24-3,33 (2H, м), 3,53-3,86 (1H, м), 5,09 (2H, с), 5,88-5,96 (1H, м), 7,28-7,38 (5H, м).
Пример получения 105-3
1-(3-Аминопропил)-4-гидроксипиперидин
К бензил-N-(3-(4-гидроксипиперидин)пропил)карбамату (2,96 г) добавляли этанол (200 мл) и палладий-на-угле (2,5 г) и реакционную смесь интенсивно перемешивали в атмосфере водорода в течение ночи. Палладий-на-угле удаляли фильтрацией и фильтрат концентрировали с получением указанного в заголовке соединения (1,5 г).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,25-1,38 (2H, м), 1,41-1,49 (2H, м), 1,61-1,69 (2H, м), 1,84-1,95 (2H, м), 2,18-2,25 (2H, м), 2,49-2,57 (2H, м), 2,58-2,69 (2H, м), 3,30-3,42 (1H, м).
Пример 106
N1-Метил-3-хлор-5-(2-((4-(2-гидроксиэтил)пиперазин-1-ил)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 104 указанное в заголовке соединение получали из 4-(2-гидроксиэтил)пиперазина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,30-2,48 (6H, м), 2,82 (3H, д, J=4,4 Гц), 3,30-3,40 (4H, м), 3,46 (2H, кв, J=5,6 Гц), 4,38 (1H, т, J=5,6 Гц), 6,57 (1H, дд, J=5,6, 2,4 Гц), 7,16 (1H, дд, J=8,8, 2,4 Гц), 7,29 (1H, д, J=2,4 Гц), 7,32 (1H, д, J=2,4 Гц), 8,07-8,13 (2H, м), 8,21 (1H, кв, J=4,4 Гц), 8,32 (1H, д, J=8,8 Гц), 9,15 (1H, с).
Пример 107
N4-(4-(3-хлор-1-(метиламино)карбонил-1H-5-индолил)окси-2-пиридил)-4-морфолинкарбоксамид
Аналогично примеру 104 указанное в заголовке соединение получали из морфолина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,82 (3H, д, J=4,4 Гц), 3,33-3,40 (4H, м), 3,49-3,56 (4H, м), 6,58 (1H, дд, J=5,6, 2,4 Гц), 7,16 (1H, дд, J=8,8, 2,4 Гц), 7,27 (1H, д, J=2,4 Гц), 7,32 (1H, д, J=2,4 Гц), 8,06-8,13 (2H, м), 8,21 (1H, кв, J=4,4 Гц), 8,32 (1H, д, J=8,8 Гц), 9,22 (1H, с).
Пример 108
N1-Метил-3-хлор-5-(2-((4-этилпиперазин-1-ил)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 103 указанное в заголовке соединение получали из N-этилпиперазина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,96 (3H, т, J=7,2 Гц), 2,24-2,32 (6H, м), 2,82 (3H, д, J=4,0 Гц), 3,34-3,39 (4H, м), 6,57 (1H, дд, J=6,0, 2,4 Гц), 7,17 (1H, дд, J=9,2, 2,4 Гц), 7,27 (1H, д, J=2,4 Гц), 7,32 (1H, д, J=2,4 Гц), 8,07-8,10 (2H, м), 8,18-8,25 (1H, м), 8,33 (1H, д, J=9,2 Гц), 9,17 (1H, уш.с).
Пример 109
N1-Этил-3-хлор-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 104 указанное в заголовке соединение получали в виде бесцветного аморфного твердого вещества из N1-этил-5-(2-амино-4-пиридил)окси-3-хлор-1H-1-индолкарбоксамида.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,15 (2H, м), 1,61 (3H, т, J=7,2 Гц), 1,60-1,70 (2H, м), 2,94-3,02 (2H, м), 3,26-3,36 (2H, м), 3,56-3,63 (1H, м), 3,70-3,78 (2H, м), 4,64 (1H, д, J=4,4 Гц), 6,55 (1H, дд, J=5,6, 2,4 Гц), 7,16 (1H, дд, J=8,8, 2,4 Гц), 7,27 (1H, д, J=2,4 Гц), 7,32 (1H, д, J=2,4 Гц), 8,08 (1H, д, J=5,6 Гц), 8,13 (1H, с), 8,22-8,27 (1H, м), 8,32 (1H, д, J=8,8 Гц), 9,12 (1H, с).
Исходное вещество получали следующим образом.
Пример получения 109-1
N1-Этил-5-(2-амино-4-пиридил)окси-3-хлор-1H-1-индолкарбоксамид
Фенил-N-этилкарбамат добавляли к раствору 5-(2-амино-4-пиридил)окси-3-хлор-1H-1-индола (1,35 г, CAS No. 417721-98-3), который был описан в WO 02/32872, гидрида натрия (210 мг) и N,N-диметилформамида; реакционную смесь перемешивали в течение 1 часа. К реакционной смеси добавляли водный раствор хлорида аммония; производили экстракцию этилацетатом и производили очистку колоночной хроматографией на силикагеле (Fuji Silysia NH, смесь гексан:этилацетат=1:2) с получением указанного в заголовке соединения в виде бесцветного масла (1,07 г).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,15 (3H, т, J=7,2 Гц), 3,25-3,35 (2H, м), 5,76 (1H, д, J=2,4 Гц), 5,87 (2H, с), 6,14 (1H, дд, J=5,6, 2,4 Гц), 7,13 (1H, дд, J=8,8, 2,4 Гц), 7,23 (1H, д, J=2,4 Гц), 7,77 (1H, д, J=5,6 Гц), 8,11 (1H, с), 8,20-8,25 (1H, м), 8,31 (1H, д, J=8,8 Гц).
Пример 110
N1-Этил-3-хлор-5-(2-(((3-(4-гидроксипиперидин)пропил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 103 указанное в заголовке соединение получали в виде белых кристаллов из N1-этил-5-(2-амино-4-пиридил)окси-3-хлор-1H-1-индолкарбоксамида и 1-(3-аминопропил)-4-гидроксипиперидина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,16 (3H, т, J=7,2 Гц), 1,26-1,38 (2H, м), 1,48-1,57 (2H, м), 1,63-1,70 (2H, м), 1,86-1,97 (2H, м), 2,18-2,25 (2H, м), 2,60-2,68 (2H, м), 3,05-3,13 (2H, м), 3,26-3,34 (2H, м), 3,34-3,42 (1H, м), 4,49 (1H, д, J=4,0 Гц), 6,52 (1H, дд, J=6,0, 2,4 Гц), 6,84-6,86 (1H, м), 7,16 (1H, дд, J=8,8, 2,4 Гц), 7,28 (1H, д, J=2,4 Гц), 7,98-8,05 (2H, м), 8,14 (1H, с), 8,22-8,28 (1H, м), 8,33 (1H, д, J=8,8 Гц), 9,03 (1H, уш.с).
Пример 111
N1-Этил-3-хлор-5-(2-(((3-(диэтиламино)пропил)амино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 104 указанное в заголовке соединение получали из N1-этил-5-(2-амино-4-пиридил)окси-3-хлор-1H-1-индолкарбоксамида и 3-(диэтиламино)пропиламина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,90 (6H, т, J=7,2 Гц), 1,16 (3H, т, J=7,2 Гц), 1,46-1,54 (2H, м), 2,33-2,44 (6H, м), 3,07-3,14 (2H, м), 3,26-3,34 (2H, м), 6,52 (1H, дд, J=5,6, 2,4 Гц), 6,83 (1H, с), 7,16 (1H, дд, J=8,8, 2,4 Гц), 7,28 (1H, д, J=2,4 Гц), 8,02 (1H, д, J=5,6 Гц), 8,04-8,13 (1H, уш.с), 8,14 (1H, с), 8,23-8,27 (1H, м), 8,33 (1H, д, J=8,8 Гц), 9,04 (1H, с).
Пример 112
N1,3-Диметил-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 104 указанное в заголовке соединение получали в виде бесцветного аморфного твердого вещества из N1,3-диметил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамида.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,17-1,30 (2H, м), 1,61-1,70 (2H, м), 2,19 (3H, с), 2,80 (3H, д, J=4,0 Гц), 2,94-3,03 (2H, м), 3,56-3,64 (1H, м), 3,70-3,78 (2H, м), 4,64 (1H, д, J=4,0 Гц), 6,52 (1H, дд, J=5,6, 2,4 Гц), 7,02 (1Н, дд, J=8,8, 2,4 Гц), 7,29-7,33 (2H, м), 7,66 (1H, с), 8,00 (1H, кв, J=4,0 Гц), 8,05 (1H, д, J=5,6 Гц), 8,25 (1H, д, J=8,8 Гц), 9,08 (1H, с).
Исходные вещества синтезировали следующим образом.
Пример получения 112-1
4-(3-Метил-1H-5-индолил)окси-2-пиридинамин
Смесь 5-гидрокси-3-метилиндола (4,7 г), 2-амино-4-хлорпиридина (4,1 г), гидрида натрия (1,3 г) и диметилсульфоксида (40 мл) перемешивали при 160°С в течение 15 часов. Туда добавляли воду; проводили экстракцию этилацетатом и проводили очистку колоночной хроматографией на силикагеле (этилацетат, затем смесь этилацетат:метанол=20:1). Растворитель отгоняли с получением указанного в заголовке соединения в виде коричневого твердого вещества (1,6 г).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,29 (3H, с), 5,70 (1H, д, J=2,4 Гц), 5,77 (2H, с), 6,10 (1H, дд, J=5,6, 2,4 Гц), 6,80 (1H, дд, J=8,8, 2,4 Гц), 7,15 (1H, с), 7,17 (1H, д, J=2,4 Гц), 7,35 (1H, д, J=8,8 Гц), 7,72 (1H, д, J=5,6 Гц), 10,83 (1H, с).
Пример получения 112-2
N1,3-Диметил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамид
Фенил-N-метилкарбамат (350 мг, пример получения 2-1) добавляли к раствору 4-(3-метил-1H-5-индолил)окси-2-пиридинамина (500 мг), гидрида натрия (93 мг) и N,N-диметилформамида (5 мл) при комнатной температуре и реакционную смесь перемешивали в течение 2 часов и 45 минут. К реакционной смеси добавляли воду; проводили экстракцию этилацетатом и проводили очистку колоночной хроматографией на NH-силикагеле (Fuji Silysia, смесь гексан:этилацетат=1:2, затем этилацетат) с получением указанного в заголовке соединения в виде бледно-желтого аморфного твердого вещества (365 мг).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,19 (3H, с), 2,80 (3H, д, J=4,0 Гц), 5,73 (1H, д, J=2,4 Гц), 5,83 (2H, с), 6,12 (1H, дд, J=5,6, 2,4 Гц), 7,00 (1H, дд, J=8,8, 2,4 Гц), 7,27 (1H, д, J=2,4 Гц), 7,64 (1H, с), 7,75 (1H, д, J=5,6 Гц), 7,98 (1H, кв, J=4,0 Гц), 8,24 (1H, д, J=8,8 Гц).
Пример 113
N1,3-Диметил-5-(2-((4-(пирролидин-1-ил)пиперидин)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 104 указанное в заголовке соединение получали в виде бесцветного аморфного твердого вещества из N1,3-диметил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамида и 4-(1-пирролидинил)пиперидина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,17-1,79 (2H, м), 1,60-1,67 (4H, м), 1,70-1,79 (2H, м), 2,03-2,13 (1H, м), 2,19 (3H, с), 2,40-2,57 (4H, м), 2,77-2,86 (5H, м), 3,88-3,96 (2H, м), 6,52 (1H, дд, J=5,6, 2,4 Гц), 7,02 (1H, дд, J=8,8, 2,4 Гц), 7,28-7,85 (2H, м), 7,66 (1H, с), 8,00 (1H, кв, J=4,0 Гц), 8,05 (1H, д, J=5,6 Гц), 8,25 (1H, д, J=8,8 Гц), 9,08 (1H, с).
Пример 114
N1-Циклопропил-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-3-метил-1H-1-индолкарбоксамид
Аналогично примеру 104 указанное в заголовке соединение получали в виде бесцветного аморфного твердого вещества из N1-циклопропил-5-(2-амино-4-пиридил)окси-3-метил-1H-1-индолкарбоксамида.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,56-0,60 (2H, м), 2,67-2,73 (2H, м), 1,19-1,29 (2H, м), 1,61-1,70 (2H, м), 2,18 (3H, с), 2,72-2,78 (1H, м), 2,94-3,03 (2H, м), 3,56-3,63 (1H, м), 3,70-3,77 (2H, м), 4,64 (1H, д, J=4,0 Гц), 6,51 (1H, дд, J=5,6, 2,4 Гц), 7,02 (1H, дд, J=8,8, 2,4 Гц), 7,28-7,32 (2H, м), 7,65 (1H, с), 8,05 (1H, д, J=5,6 Гц), 8,11 (1H, д, J=2,4 Гц), 8,24 (1H, д, J=8,8 Гц), 9,08 (1H, с).
Исходное вещество синтезировали следующим образом.
Пример получения 114-1
N1-Циклопропил-5-(2-амино-4-пиридил)окси-3-метил-1H-1-индолкарбоксамид
Аналогично примеру получения 112-2 указанное в заголовке соединение получали в виде бесцветного аморфного твердого вещества из фенил-N-циклопропилкарбамата.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,55-0,60 (2H, м), 0,68-0,73 (2H, м), 2,18 (3H, с), 2,70-2,79 (1H, м), 5,73 (1H, д, J=2,4 Гц), 5,83 (2H, с), 6,12 (1H, дд, J=5,6, 2,4 Гц), 7,00 (1H, дд, J=8,8, 2,4 Гц), 7,26 (1H, д, J=2,4 Гц), 7,63 (1H, с), 7,75 (1H, д, J=5,6 Гц), 8,09 (1H, д, J=2,4 Гц), 8,23 (1H, д, J=8,8 Гц).
Пример 115
N1-Циклопропил-5-(2-((4-(2-гидроксиэтил)пиперазин-1-ил)карбонил)амино-4-пиридил)окси-3-метил-1H-1-индолкарбоксамид
Аналогично примеру 104 указанное в заголовке соединение получали в виде бесцветного аморфного твердого вещества из N1-циклопропил-5-(2-амино-4-пиридил)окси-3-метил-1H-1-индолкарбоксамида и 1-(2-гидроксиэтил)пиперазина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,57-0,60 (2H, м), 0,67-0,74 (2H, м), 2,18 (3H, с), 2,30-2,37 (6H, м), 2,70-2,78 (1H, м), 3,30-3,38 (4H, м), 3,46 (2H, кв, J=6,4 Гц), 4,38 (1H, т, J=6,4 Гц), 6,53 (1H, дд, J=5,6, 2,4 Гц), 7,02 (1H, дд, J=8,8, 2,4 Гц), 7,28-7,32 (2H, м), 7,65 (1H, с), 8,06 (1H, д, J=5,6 Гц), 8,11 (1H, д, J=2,4 Гц), 8,24 (1H, д, J=8,8 Гц), 9,10 (1H, с).
Пример 116
N1-Метил-5-(2-((метиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 5 указанное в заголовке соединение получали в виде белых кристаллов (19,5 мг, 0,058 ммоль, 58%) из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (52 мг, 0,1 ммоль), синтезированного в примере получения 5-2, и 40% метиламина в метаноле.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,64 (3H, д, J=4,4 Гц), 2,83 (3H, д, J=4,4 Гц), 6,50 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 6,82 (1H, д, J=2,4 Гц), 7,04 (1H, дд, J=2,4, 8,8 Гц), 7,36 (1H, д, J=2,4 Гц), 7,87 (1H, д, J=3,6 Гц), 7,95 (1H, м), 8,02 (1H, д, J=5,6 Гц), 8,16 (1H, м), 8,28 (1H, д, J=8,8 Гц), 9,07 (1H, с).
Пример 117
N1-Метил-5-(2-((этиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 5 указанное в заголовке соединение получали в виде белых кристаллов (15,0 мг, 0,042 ммоль, 42%) из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (52 мг, 0,1 ммоль), синтезированного в примере получения 5-2, и 2,0 M этиламина в тетрагидрофуране.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,02 (3H, т, J=7,2 Гц), 2,83 (3H, д, J=4,0 Гц), 3,10 (2H, м), 6,50 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 6,86 (1H, д, J=2,4 Гц), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,36 (1H, д, J=2,4 Гц), 7,87 (1H, д, J=3,6 Гц), 7,96 (1H, м), 8,02 (1H, д, J=5,6 Гц), 8,17 (1H, м), 8,28 (1H, д, J=8,8 Гц), 8,99 (1H, с).
Пример 118
N1-Метил-5-(2-((циклопропиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 5 указанное в заголовке соединение получали в виде белых кристаллов из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (52 мг, 0,1 ммоль), синтезированного в примере получения 5-2, и циклопропиламина.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 0,58-0,62 (2H, м), 0,71-0,79 (2H, м), 2,70 (1H, м), 3,07 (3H, д, J=4,8 Гц), 5,64 (1H, м), 6,26 (1H, м), 6,41 (1H, м), 6,58 (1H, д, J=3,6 Гц), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,20-7,30 (2H, м), 7,42-7,53 (2H, м), 7,90 (1H, д, J=5,6 Гц), 8,19 (1H, д, J=8,8 Гц).
Пример 119
N1-Метил-5-(2-((диэтиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 5 указанное в заголовке соединение получали в виде белых кристаллов (24,7 мг, 0,065 ммоль, 65%) из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (52 мг, 0,1 ммоль), синтезированного в примере получения 5-2, и диэтиламина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,01 (6H, т, J=7,2 Гц), 2,82 (3H, д, J=4,4 Гц), 3,20-3,50 (4H, м), 6,54 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 7,04 (1H, дд, J=2,4, 8,8 Гц), 7,36 (1H, д, J=2,4 Гц), 7,40 (1H, д, J=2,4 Гц), 7,78 (1H, д, J=3,6 Гц), 8,06 (1H, д, J=5,6 Гц), 8,16 (1H, м), 8,28 (1H, д, J=8,8 Гц), 8,59 (1H, с).
Пример 120
N1-Метил-5-(2-((1-пропиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 5 указанное в заголовке соединение (28,0 мг, 0,076 ммоль, 76%) получали в виде белых кристаллов из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (52 мг, 0,1 ммоль), синтезированного в примере получения 5-2, и 1-пропиламина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,83 (3H, т, J=7,2 Гц), 1,40 (2H, м), 2,83 (3H, д, J=4,4 Гц), 3,04 (2H, м), 6,49 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 6,86 (1H, с), 7,04 (1H, дд, J=2,4, 8,8 Гц), 7,36 (1H, д, J=2,4 Гц), 7,87 (1H, д, J=3,6 Гц), 8,01-8,03 (2H, м), 8,16 (1H, м), 8,28 (1H, д, J=8,8 Гц), 9,00 (1H, с).
Пример 121
N1-Метил-5-(2-((2-пропиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 5 указанное в заголовке соединение (20,7 мг, 0,056 ммоль, 56%) получали в виде белых кристаллов из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (52 мг, 0,1 ммоль), синтезированного в примере получения 5-2, и 2-пропиламина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,06 (6H, д, J=6,8 Гц), 2,83 (3H, д, J=4,4 Гц), 3,74 (1H, м), 6,49 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 6,89 (1H, д, J=2,4 Гц), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,36 (1H, д, J=2,4 Гц), 7,81 (1H, м), 7,87 (1H, д, J=3,6 Гц), 8,02 (1H, д, J=5,6 Гц), 8,16 (1H, м), 8,28 (1H, д, J=8,8 Гц), 8,90 (1H, с).
Пример 122
N1-Метил-5-(2-((циклопентиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 5 указанное в заголовке соединение (30,7 мг, 0,078 ммоль, 78%) получали в виде белых кристаллов из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (52 мг, 0,1 ммоль), синтезированного в примере получения 5-2, и циклопентиламина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,10-1,90 (8H, м), 2,83 (3H, д, J=4,4 Гц), 3,89 (1H, м), 6,50 (1H, д, J=2,4, 5,6 Гц), 6,68 (1H, д, J=3,6 Гц), 6,90 (1H, д, J=2,4 Гц), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,36 (1H, д, J=2,4 Гц), 7,87 (1H, м), 7,93 (1H, д, J=3,6 Гц), 8,00 (1H, д, J=5,6 Гц), 8,15 (1H, м), 8,28 (1H, д, J=8,8 Гц), 8,89 (1H, с).
Пример 123
N1-Метил-5-(2-((циклогексиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 5 указанное в заголовке соединение (32,5 мг, 0,080 ммоль, 80%) получали в виде белых кристаллов из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (52 мг, 0,1 ммоль), синтезированного в примере получения 5-2, и циклогексиламина.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 1,00-2,00 (8H, м), 2,83 (3H, д, J=4,4 Гц), 3,40-3,60 (2H, м), 3,75 (1H, м), 6,11 (1H, с), 6,43 (1H, м), 6,60 (1H, д, J=3,6 Гц), 6,95 (1H, м), 7,04 (1H, м), 7,20-7,30 (2H, м), 7,44 (1H, д, J=3,6 Гц), 7,95 (1H, д, J=5,6 Гц), 8,20 (1H, д, J=8,8 Гц), 9,20 (1H, м).
Пример 124
N1-Метил-5-(2-((2-пропениламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 5 указанное в заголовке соединение (18,5 мг, 0,051 ммоль, 51%) получали в виде белых кристаллов из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (52 мг, 0,1 ммоль), синтезированного в примере получения 5-2, и аллиламина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,85 (3H, д, J=4,8 Гц), 3,75 (2H, м), 5,06 (1H, дд, J=1,6, 10,4 Гц), 5,14 (1H, дд, J=1,6, 17,2 Гц), 5,87 (1H, м), 6,54 (1H, дд, J=2,4, 5,6 Гц), 6,69 (1H, д, J=3,6 Гц), 6,87 (1H, д, J=2,4 Гц), 7,06 (1H, дд, J=2,4, 8,8 Гц), 7,39 (1H, д, J=2,4 Гц), 7,89 (1H, д, J=3,6 Гц), 8,05 (1H, д, J=5,6 Гц), 8,16-8,19 (2H, м), 8,30 (1H, д, J=8,8 Гц), 9,13 (1H, с).
Пример 125
N1-Метил-5-(2-((2-пропиниламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 5 указанное в заголовке соединение (16,8 мг, 0,046 ммоль, 46%) получали в виде белых кристаллов из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (52 мг, 0,1 ммоль), синтезированного в примере получения 5-2, и пропаргиламина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,85 (3H, д, J=4,4 Гц), 3,12 (1Н, м), 3,92 (2H, м), 6,56 (1H, дд, J=2,4, 5,6 Гц), 6,70 (1H, д, J=3,6 Гц), 6,87 (1H, д, J=2,4 Гц), 7,06 (1H, дд, J=2,4, 8,8 Гц), 7,39 (1H, д, J=2,4 Гц), 7,89 (1H, д, J=3,6 Гц), 8,07 (1H, д, J=5,6 Гц), 8,18 (1H, м), 8,29-8,31 (2H, м), 9,21 (1H, с).
Пример 126
N1-Метил-5-(2-((бензиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 5 указанное в заголовке соединение (26,1 мг, 0,063 ммоль, 63%) получали в виде белых кристаллов из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (52 мг, 0,1 ммоль), синтезированного в примере получения 5-2, и бензиламина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,85 (3H, д, J=4,4 Гц), 4,34 (2H, д, J=5,6 Гц), 6,53 (1H, дд, J=2,4, 5,6 Гц), 6,69 (1H, д, J=3,6 Гц), 6,90 (1Н, д, J=2,4 Гц), 7,06 (1H, дд, J=2,4, 8,8 Гц), 7,20-7,35 (5H, м), 7,39 (1H, д, J=2,4 Гц), 7,89 (1H, д, J=3,6 Гц), 8,04 (1H, д, J=5,6 Гц), 8,17 (1H, м), 8,30 (1H, д, J=8,8 Гц), 8,51 (1H, м), 9,17 (1H, с).
Пример 127
N1-Метил-5-(2-((фурфуриламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 5 указанное в заголовке соединение (9,1 мг, 0,022 ммоль, 22%) получали в виде белого порошка из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (52 мг, 0,1 ммоль), синтезированного в примере получения 5-2, и фурфуриламина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,85 (3H, д, J=4,4 Гц), 4,32 (2H, д, J=5,2 Гц), 6,24 (1H, с), 6,38 (1H, с), 6,54 (1H, м), 6,69 (1H, д, J=3,6 Гц), 6,90 (1H, с), 7,06 (1H, м), 7,39 (1H, с), 7,57 (1H, с), 7,89 (1H, д, J=2,4 Гц), 8,05 (1H, д, J=5,6 Гц), 8,18 (1H, м), 8,31 (1H, д, J=8,8 Гц), 8,38 (1H, м), 9,15 (1H, с).
Пример 128
N1-Метил-5-(2-((тиофен-2-илметиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 5 указанное в заголовке соединение (22,6 мг, 0,054 ммоль, 54%) получали в виде белого порошка из фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (52 мг, 0,1 ммоль), синтезированного в примере получения 5-2, и 2-тиофенметиламина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,85 (3H, д, J=4,4 Гц), 4,50 (2H, д, J=5,6 Гц), 6,54 (1H, дд, J=2,4, 5,6 Гц), 6,69 (1H, д, J=3,6 Гц), 6,88-6,98 (3H, м), 7,06 (1H, дд, J=2,4, 8,8 Гц), 7,35-7,39 (2H, м), 7,89 (1H, д, J=3,6 Гц), 8,04 (1H, д, J=5,6 Гц), 8,18 (1H, м), 8,30 (1H, д, J=8,8 Гц), 8,55 (1H, м), 9,18 (1H, с).
Пример 129
N1-Этил-5-(2-((этиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 27 указанное в заголовке соединение (23,1 мг, 0,063 ммоль, 63%) получали в виде белых кристаллов из фенил-N-(4-(1-(этиламино)карбонил-1H-5-индолил)окси-2-пиридил)карбамата (42 мг, 0,1 ммоль), синтезированного в примере получения 27-2, и 2,0 M этиламина в тетрагидрофуране.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,04 (3H, т, J=7,2 Гц), 1,18 (3H, т, J=7,2 Гц), 3,12 (2H, м), 3,31 (2H, м), 6,52 (1H, дд, J=2,4, 5,6 Гц), 6,69 (1H, д, J=3,6 Гц), 6,88 (1H, д, J=2,4 Гц), 7,05 (1H, дд, J=2,4, 8,8 Гц), 7,38 (1H, д, J=2,4 Гц), 7,92 (1H, д, J=3,6 Гц), 7,97 (1H, м), 8,04 (1H, д, J=5,6 Гц), 8,23 (1H, м), 8,30 (1H, д, J=8,8 Гц), 9,01 (1H, с).
Пример 130
N1-Этил-5-(2-((диэтиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 27 указанное в заголовке соединение (25,8 мг, 0,065 ммоль, 65%) получали в виде белых кристаллов из фенил-N-(4-(1-(этиламино)карбонил-1H-5-индолил)окси-2-пиридил)карбамата (42 мг, 0,1 ммоль), синтезированного в примере получения 27-2, и диэтиламина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,03 (6H, т, J=7,2 Гц), 1,19 (3H, т, J=7,2 Гц), 3,20-3,40 (6H, м), 6,55 (1H, дд, J=2,4, 5,6 Гц), 6,69 (1H, д, J=3,6 Гц), 7,05 (1H, дд, J=2,4, 8,8 Гц), 7,38 (1H, с), 7,43 (1H, д, J=2,4 Гц), 7,92 (1H, д, J=3,6 Гц), 8,08 (1H, д, J=5,6 Гц), 8,23 (1H, м), 8,30 (1H, д, J=8,8 Гц), 8,62 (1H, с).
Пример 131
N1-Диметил-5-(2-((метиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (17,5 мг, 0,05 ммоль, 35%) получали в виде белого порошка из N1-диметил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамида (42 мг, 0,14 ммоль) и 40% метиламина в метаноле.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,67 (3H, д, J=4,4 Гц), 3,05 (6H, с), 6,53 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 6,83 (1H, д, J=2,4 Гц), 7,04 (1H, дд, J=2,4, 8,8 Гц), 7,40 (1H, д, J=2,4 Гц), 7,68-7,71 (2H, м), 8,00-8,05 (2H, м), 9,10 (1H, с).
Исходные вещества синтезировали с помощью следующих методов.
Пример получения 131-1
Фенил-N,N-диметилкарбамат
Аналогично примеру получения 2-1 указанное в заголовке соединение (6,27 г, 0,038 моль, 38%) получали в виде бесцветного масла из 2,0 M диэтиламина в тетрагидрофуране (50 мл, 0,1 моль), фенилхлорформиата (13,8 мл, 0,11 моль) и пиридина (8,9 мл, 0,11 моль).
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 3,02 (3H, с), 3,11 (3H, с), 7,09-7,39 (5H, м).
Пример получения 131-2
N1-Диметил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру получения 1-3 указанное в заголовке соединение (128 мг, 0,43 ммоль, 43%) получали в виде белых кристаллов из 4-(1H-5-индолилокси)-2-пиридинамина (225 мг, 1,0 ммоль) и фенил-N,N-диметилкарбамата.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 3,13 (6H, с), 4,36 (2H, уш.с), 5,92 (1H, д, J=2,4 Гц), 6,31 (1H, дд, J=2,4, 5,6 Гц), 6,59 (1H, д, J=3,6 Гц), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,30 (1H, д, J=2,4 Гц), 7,37 (1H, д, J=3,6 Гц), 7,70 (1H, д, J=8,8 Гц), 7,91 (1H, д, J=5,6 Гц).
Пример 132
N1-Диметил-5-(2-((этиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (21,4 мг, 0,058 ммоль, 41%) получали в виде белого порошка из N1-диметил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамида (42 мг, 0,14 ммоль) и 2,0 M этиламина в тетрагидрофуране.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,05 (3H, т, J=7,2 Гц), 3,05 (6H, с), 3,13 (2H, м), 6,52 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 6,87 (1H, д, J=2,4 Гц), 7,04 (1H, дд, J=2,4, 8,8 Гц), 7,40 (1H, д, J=2,4 Гц), 7,68-7,71 (2H, м), 8,00-8,05 (2H, м), 9,02 (1H, с).
Пример 133
N1-Диметил-5-(2-((диметиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (15,1 мг, 0,041 ммоль, 29%) получали в виде белого порошка из N1-диметил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамида (42 мг, 0,14 ммоль) и 2,0 M диметиламина в тетрагидрофуране.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,85 (6H, с), 3,03 (6H, с), 6,54 (1H, д, J=5,6 Гц), 6,65 (1H, д, J=3,6 Гц), 7,02 (1H, д, J=8,8 Гц), 7,30-7,50 (2H, м), 7,60-7,69 (2H, м), 8,06 (1H, д, J=5,6 Гц), 8,81 (1H, с).
Пример 134
N1-Бензил-5-(2-((метиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (12,5 мг, 0,030 ммоль, 24%) получали в виде белого порошка из N1-бензил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамида (45 мг, 0,13 ммоль) и 40% метиламина в метаноле.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,66 (3H, д, J=4,4 Гц), 4,51 (2H, д, J=5,6 Гц), 6,52 (1H, дд, J=2,4, 5,6 Гц), 6,72 (1H, д, J=3,6 Гц), 6,84 (1H, д, J=2,4 Гц), 7,06 (1H, дд, J=2,4, 8,8 Гц), 7,20-7,44 (6H, м), 7,96 (1H, м), 8,00-8,05 (2H, м), 8,31 (1H, д, J=8,8 Гц), 8,83 (1H, т, J=5,6 Гц), 9,09 (1H, с).
Исходное вещество синтезировали с помощью следующих методов.
Пример получения 134-1
N1-Бензил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру получения 1-3 указанное в заголовке соединение (45 мг, 0,13 ммоль, 13%) получали в виде белого порошка из 4-(1H-5-индолилокси)-2-пиридинамина (225 мг, 1,0 ммоль) и фенил-N-бензилкарбамата.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 4,38 (2H, уш.с), 4,68 (2H, д, J=4,0 Гц), 5,82 (1H, м), 5,92 (1H, м), 6,30 (1H, м), 6,61 (1H, д, J=3,6 Гц), 7,07 (1H, дд, J=2,4, 8,8 Гц), 7,26-7,47 (7H, м), 7,91 (1H, д, J=5,6 Гц), 8,19 (1H, д, J=8,8 Гц).
Пример 135
Пирролидин-1-иламид 5-(2-((метиламино)карбонил)амино-4-пиридил)окси-1H-1-индол-1-карбоновой кислоты
Аналогично примеру 28 указанное в заголовке соединение (21,1 мг, 0,056 ммоль, 27%) получали в виде белого порошка из пирролидин-1-иламида 5-(2-амино-4-пиридил)окси-1H-1-индол-1-карбоновой кислоты (67 мг, 0,21 ммоль) и 40% метиламина в метаноле.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,80-2,00 (4H, м), 2,67 (3H, д, J=4,4 Гц), 3,40-3,60 (4H, м), 6,53 (1H, дд, J=2,4, 5,6 Гц), 6,66 (1H, д, J=3,6 Гц), 6,85 (1H, д, J=2,4 Гц), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,39 (1H, д, J=2,4 Гц), 7,80 (1H, д, J=3,6 Гц), 7,83 (1H, д, J=8,8 Гц), 8,00 (1H, м), 8,04 (1H, д, J=5,6 Гц), 9,10 (1H, с).
Исходные вещества синтезировали с помощью следующих методов.
Пример получения 135-1
Фенилпирролидин-1-илкарбоксилат
Аналогично примеру получения 2-1 указанное в заголовке соединение (2,68 г, 0,014 моль, 14%) получали в виде белых кристаллов из пирролидина (8,3 мл, 0,1 моль), фенилхлорформиата (13,8 мл, 0,11 моль) и пиридина (8,9 мл, 0,11 моль).
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 1,90-1,99 (4H, м), 3,46-3,59 (4H, м), 7,20-7,37 (5H, м).
Пример получения 135-2
Пирролидин-1-иламид 5-(2-амино-4-пиридил)окси-1H-1-индол-1-карбоновой кислоты
Аналогично примеру получения 1-3 указанное в заголовке соединение (146 мг, 0,45 ммоль, 60%) получали в виде белого порошка из 4-(1H-5-индолилокси)-2-пиридинамина (170 мг, 0,76 ммоль) и фенилпирролидин-1-илкарбоксилата.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 1,96-2,02 (4H, м), 3,60-3,67 (4H, м), 4,35 (2H, уш.с), 5,91 (1H, д, J=2,4 Гц), 6,31 (1H, дд, J=2,4, 5,6 Гц), 6,57 (1H, д, J=3,6 Гц), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,29 (1H, д, J=2,4 Гц), 7,43 (1H, д, J=3,6 Гц), 7,88 (1H, д, J=8,8 Гц), 7,91 (1H, д, J=5,6 Гц).
Пример 136
Пирролидин-1-иламид 5-(2-((пирролидин-1-иламино)карбонил)амино-4-пиридил)окси-1H-1-индол-1-карбоновой кислоты
Аналогично примеру 28 указанное в заголовке соединение (6,2 мг, 0,015 ммоль, 9,2%) получали в виде белого порошка из пирролидин-1-иламида 5-(2-амино-4-пиридил)окси-1H-1-индол-1-карбоновой кислоты (52 мг, 0,16 ммоль) и пирролидина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,70-1,90 (8H, м), 3,20-3,40 (4H, м), 3,50-3,70 (4H, м), 6,56 (1H, дд, J=2,4, 5,6 Гц), 6,66 (1H, д, J=3,6 Гц), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,38 (1H, д, J=2,4 Гц), 7,45 (1H, д, J=2,4 Гц), 7,80 (1H, д, J=3,6 Гц), 7,84 (1H, д, J=8,8 Гц), 8,08 (1H, д, J=5,6 Гц), 8,61 (1H, с).
Пример 137
N1-(2-Пропинил)-5-(2-((этиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (16,5 мг, 0,044 ммоль, 25%) получали в виде белых кристаллов из N1-(2-пропинил)-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамида (54 мг, 0,18 ммоль) и 2,0 M этиламина в тетрагидрофуране.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,04 (3H, т, J=7,2 Гц), 3,12 (2H, м), 3,23 (1H, м), 4,10 (2H, м), 6,52 (1H, дд, J=2,4, 5,6 Гц), 6,53 (1H, д, J=3,6 Гц), 6,88 (1H, д, J=2,4 Гц), 7,08 (1H, дд, J=2,4, 8,8 Гц), 7,40 (1H, д, J=2,4 Гц), 7,92 (1H, д, J=3,6 Гц), 8,00 (1H, м), 8,04 (1H, д, J=5,6 Гц), 8,31 (1H, д, J=8,8 Гц), 8,73 (1H, м), 9,02 (1H, с).
Исходные вещества синтезировали с помощью следующих методов.
Пример получения 137-1
Фенил-N-(2-пропинил)карбамат
Аналогично примеру получения 2-1 указанное в заголовке соединение (7,64 г, 0,044 моль, 87%) получали в виде белых кристаллов из 2-пропиниламина (3,43 мл, 0,05 моль), фенилхлорформиата (6,9 мл, 0,055 моль) и пиридина (4,45 мл, 0,055 моль).
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 2,30 (1H, т, J=2,8 Гц), 4,05-4,15 (2H, м), 5,22 (1H, уш.с), 7,10-7,40 (5H, м).
Пример получения 137-2
N1-(2-Пропинил)-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру получения 1-3 указанное в заголовке соединение (169 мг, 0,55 ммоль, 28%) получали в виде белых кристаллов из 4-(1H-5-индолилокси)-2-пиридинамина (450 мг, 2,0 ммоль) и фенил-N-(2-пропинил)карбамата.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 2,35 (1H, м), 4,20-4,40 (4H, м), 5,72 (1H, уш.с), 5,92 (1H, д, J=2,4 Гц), 6,30 (1H, дд, J=2,4, 5,6 Гц), 6,63 (1H, д, J=3,6 Гц), 7,08 (1Н, дд, J=2,4, 8,8 Гц), 7,30 (1H, д, J=2,4 Гц), 7,46 (1H, д, J=3,6 Гц), 7,92 (1H, д, J=5,6 Гц), 8,20 (1H, д, J=8,8 Гц).
Пример 138
N1-(2-Пропинил)-5-(2-((диэтиламино)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (27,9 мг, 0,069 ммоль, 39%) получали в виде белых кристаллов из N1-(2-пропинил)-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамида (54 мг, 0,18 ммоль) и N,N-диэтиламина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,03 (6H, т, J=7,2 Гц), 3,23 (1H, м), 3,25-3,40 (4H, м), 4,01 (2H, м), 6,56 (1H, дд, J=2,4, 5,6 Гц), 6,72 (1H, д, J=3,6 Гц), 7,08 (1H, дд, J=2,4, 8,8 Гц), 7,39 (1H, д, J=2,4 Гц), 7,43 (1H, д, J=2,4 Гц), 7,92 (1H, д, J=3,6 Гц), 8,08 (1H, д, J=5,6 Гц), 8,31 (1H, д, J=8,8 Гц), 8,63 (1H, с), 8,73 (1H, м).
Пример 139
N1-(2-Пропинил)-5-(2-((пирролидин-1-ил)карбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (25,1 мг, 0,062 ммоль, 35%) получали в виде белых кристаллов из N1-(2-пропинил)-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамида (54 мг, 0,18 ммоль) и пирролидина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,70-1,90 (4H, м), 3,22 (1H, м), 3,25-3,40 (4H, м), 4,10 (2H, м), 6,56 (1H, дд, J=2,4, 5,6 Гц), 6,71 (1H, д, J=3,6 Гц), 7,07 (1H, дд, J=2,4, 8,8 Гц), 7,39 (1H, д, J=2,4 Гц), 7,44 (1H, д, J=2,4 Гц), 7,92 (1H, д, J=5,6 Гц), 8,08 (1H, д, J=5,6 Гц), 8,30 (1H, д, J=8,8 Гц), 8,62 (1H, с), 8,72 (1H, м).
Пример 140
N1-Метил-5-(6-((морфолин-4-ил)карбонил)аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (12,5 мг, 0,032 ммоль, 12%) получали в виде бледно-желтого порошка из N1-метил-5-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамида (73 мг, 0,26 ммоль) и морфолина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,83 (3H, д, J=3,6 Гц), 3,43-3,45 (4H, м), 3,55-3,58 (4H, м), 6,63 (1H, д, J=3,6 Гц), 7,26 (1H, с), 7,32 (1H, д, J=8,8 Гц), 7,77 (1H, д, J=3,6 Гц), 7,90 (1H, с), 8,05 (1H, м), 8,14 (1H, д, J=8,8 Гц), 8,29 (1H, с), 9,21 (1H, с), 9,34 (1H, с).
Исходные вещества синтезировали с помощью следующих методов.
Пример получения 140-1
6-Хлор-4-(1H-5-индолиламино)пиримидин
4,6-Дихлорпиримидин (5,89 г, 40 ммоль), 5-аминоиндол (6,27 г, 47 ммоль) и N,N-диизопропилэтиламин (20,6 мл, 0,12 моль) растворяли в N-метилпирролидоне (80 мл) и реакционную смесь перемешивали при 50°С в течение 2,5 часов. Реакционную смесь подвергали распределению между этилацетатом и водой; водный слой подвергали повторной экстракции этилацетатом; объединенный органический слой промывали насыщенным раствором соли и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении; к остатку добавляли небольшое количество этилацетата для кристаллизации; кристаллы отфильтровывали, промывали диэтиловым эфиром и сушили при аэрировании с получением указанного в заголовке соединения (3,70 г, 15 ммоль, 38%) в виде белых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 6,42 (1H, м), 6,62 (1H, уш.с), 7,11 (1H, д, J=8,0 Гц), 7,35-7,40 (2H, м), 7,72 (1H, уш.с), 8,38 (1H, с), 9,68 (1H, с), 11,11 (1H, с).
Пример получения 140-2
6-Амино-4-(1H-5-индолиламино)пиримидин
7 н. аммиак в метаноле (60 мл) добавляли к 6-хлор-4-(1H-5-индолиламино)пиримидину (2,455 г, 10 ммоль) и реакционную смесь нагревали в запаянной пробирке при 130°С в течение 90 часов. Растворитель отгоняли при пониженном давлении; остаток очищали колоночной хроматографией на силикагеле (элюент: смесь этилацетат:тетрагидрофуран=1:1); добавляли диэтиловый эфир для кристаллизации и кристаллы отфильтровывали, промывали диэтиловым эфиром и сушили при аэрировании с получением указанного в заголовке соединения (1,563 г, 6,9 ммоль, 69%) в виде бледно-коричневых кристаллов.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 4,50 (2H, уш.с), 5,66 (1H, м), 6,55 (1H, м), 6,68 (1H, уш.с), 7,07 (1H, дд, J=2,4, 8,8 Гц), 7,25-7,28 (1H, м), 7,40 (1H, д, J=8,8 Гц), 7,52 (1H, д, J=2,4 Гц), 8,19 (1H, с), 8,29 (1H, уш.с).
Пример получения 140-3
N1-Метил-5-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру получения 2-3 указанное в заголовке соединение (295 мг, 1,05 ммоль, 52%) получали в виде белых кристаллов из 6-амино-4-(1H-5-индолиламино)пиримидина (450,5 мг, 2,0 ммоль) и фенил-N-метилкарбамата.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 3,09 (3H, д, J=4,0 Гц), 4,56 (2H, уш.с), 5,52 (1H, м), 5,73 (1H, м), 6,61 (1H, д, J=3,6 Гц), 6,66 (1H, уш.с), 7,19 (1H, дд, J=2,4, 8,8 Гц), 7,43 (1H, д, J=3,6 Гц), 7,48 (1H, д, J=2,4 Гц), 8,13 (1Н, д, J=2,4 Гц), 8,21 (1H, с).
Пример 141
N1-Метил-5-(6-((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (20,6 мг, 0,045 ммоль, 17%) получали в виде белых кристаллов из N1-метил-5-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамида (73 мг, 0,26 ммоль) и 4-(пирролидин-1-ил)пиперидина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,20-1,36 (2H, м), 1,60-1,70 (4H, м), 1,70-1,85 (2H, м), 2,40-2,60 (5H, м), 2,83 (3H, д, J=4,4 Гц), 2,85-2,95 (2H, м), 3,95-4,05 (2H, м), 6,63 (1H, д, J=3,6 Гц), 7,24 (1H, с), 7,31 (1H, дд, J=2,4, 8,8 Гц), 7,77 (1H, д, J=3,6 Гц), 7,90 (1H, с), 8,05 (1H, м), 8,14 (1H, д, J=8,8 Гц), 8,28 (1H, с), 9,14 (1H, с), 9,31 (1H, с).
Пример 142
N1-Этил-5-(6-((этиламино)карбонил)аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Гидрид натрия (69 мг, 1,73 ммоль) суспендировали в N,N-диметилформамиде (3 мл); туда добавляли при комнатной температуре под струей азота 6-амино-4-(1H-5-индолиламино)пиримидин (311 мг, 1,38 ммоль); реакционную смесь перемешивали в течение 30 минут; туда добавляли фенил-N-этилкарбамат (286 мг, 1,73 ммоль) и реакционную смесь перемешивали в течение ночи. Реакционную смесь подвергали распределению между смесью растворителей этилацетат-тетрагидрофуран (1:1) и насыщенным водным раствором бикарбоната натрия; органический слой промывали водой и насыщенным раствором соли и сушили над безводным сульфатом натрия; растворитель отгоняли; остаток очищали колоночной хроматографией на силикагеле (элюент: смесь этилацетат:тетрагидрофуран=1:1); фракции элюата концентрировали; к остатку добавляли этилацетат для кристаллизации; кристаллы отфильтровывали и сушили при аэрировании с получением указанного в заголовке соединения (14,3 мг, 0,039 ммоль, 2,8%) в виде белых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,07 (3H, т, J=7,2 Гц), 1,18 (3H, т, J=7,2 Гц), 3,11-3,40 (4H, м), 6,64 (1H, д, J=3,6 Гц), 6,87 (1H, с), 7,29 (1H, дд, J=2,4, 8,8 Гц), 7,62 (1H, м), 7,80 (1H, д, J=3,6 Гц), 7,86 (1H, с), 8,09-8,17 (2H, м), 8,27 (1H, с), 9,06 (1H, с), 9,35 (1H, с).
Далее, полученные при указанной выше хроматографии фракции элюата концентрировали; остаток очищали опять колоночной хроматографией на силикагеле (элюент: смесь этилацетат:метанол=95:5); фракции элюата концентрировали; к остатку добавляли этилацетат для кристаллизации; кристаллы отфильтровывали и сушили при аэрировании с получением N1-этил-5-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамида (210 мг, 0,71 ммоль, 51%) в виде белых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,18 (3H, т, J=7,2 Гц), 3,20-3,40 (2H, м), 5,72 (1H, м), 6,24 (2H, уш.с), 6,61 (1H, д, J=3,6 Гц), 7,21 (1H, дд, J=2,4, 8,8 Гц), 7,76 (1H, с), 7,79 (1H, д, J=3,6 Гц), 8,01 (1H, с), 8,07-8,14 (2H, м), 8,74 (1H, с).
Пример 143
N1-Этил-5-(6-((диэтиламино)карбонил)аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (24,5 мг, 0,062 ммоль, 26%) получали в виде белых кристаллов из N1-этил-5-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамида (70 мг, 0,24 ммоль) и диэтиламина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,07 (6H, т, J=7,2 Гц), 1,18 (3H, т, J=7,2 Гц), 3,20-3,50 (6H, м), 6,63 (1H, д, J=3,6 Гц), 7,31-7,33 (2H, м), 7,80 (1H, д, J=3,6 Гц), 7,91 (1H, с), 8,09-8,15 (2H, м), 8,28 (1H, с), 8,66 (1H, с), 9,33 (1H, с).
Пример 144
N1-Этил-5-(6-((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (43,3 мг, 0,091 ммоль, 39%) получали в виде белых кристаллов из N1-этил-5-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамида (70 мг, 0,24 ммоль) и 4-(пирролидин-1-ил)пиперидина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,18 (3H, т, J=7,2 Гц), 1,20-1,36 (2H, м), 1,60-1,70 (4H, м), 1,70-1,85 (2H, м), 2,40-2,60 (5H, м), 2,85-2,95 (2H, м), 3,20-3,50 (2H, м), 3,95-4,05 (2H, м), 6,63 (1H, д, J=3,6 Гц), 7,24 (1H, с), 7,31 (1H, д, J=8,0 Гц), 7,80 (1H, д, J=3,6 Гц), 7,90 (1H, с), 8,10-8,15 (2H, м), 8,28 (1H, с), 9,14 (1H, с), 9,31 (1H, с).
Пример 145
N1-Этил-5-(6-((2-(N,N-диэтиламино)этиламино)карбонил)аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (43,0 мг, 0,098 ммоль, 42%) получали в виде белых кристаллов из N1-этил-5-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамида (70 мг, 0,24 ммоль) и 2-(N,N-диэтиламино)этиламина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,96 (6H, т, J=7,2 Гц), 1,18 (3H, т, J=7,2 Гц), 2,30-2,60 (6H, м), 3,10-3,40 (4H, м), 6,64 (1H, д, J=3,6 Гц), 6,87 (1H, с), 7,29 (1H, д, J=8,8 Гц), 7,71 (1H, м), 7,80 (1H, д, J=3,6 Гц), 7,88 (1H, с), 8,09-8,20 (2H, м), 8,25 (1H, с), 9,21 (1H, с), 9,34 (1H, с).
Пример 146
N1-Фенил-5-(6-((диэтиламино)карбонил)аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (27,5 мг, 0,062 ммоль, 27%) получали в виде белых кристаллов из N1-фенил-5-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамида (80 мг, 0,23 ммоль) и диэтиламина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,08 (6H, т, J=7,2 Гц), 3,20-3,40 (4H, м), 6,74 (1H, д, J=3,6 Гц), 7,13 (1H, дд, J=2,4, 8,8 Гц), 7,33-7,42 (4H, м), 7,64-7,67 (2H, м), 7,98-8,03 (2H, м), 8,13 (1H, д, J=8,8 Гц), 8,31 (1H, с), 8,69 (1H, с), 9,39 (1H, с), 10,00 (1H, с).
Исходное вещество синтезировали путем следующего метода.
Пример получения 146-1
N1-Фенил-5-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру получения 2-3 указанное в заголовке соединение (160 мг, 0,46 ммоль, 35%) получали в виде бледно-коричневого порошка из 6-амино-4-(1H-5-индолиламино)пиримидина (300 мг, 1,33 ммоль) и фенилизоцианата.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 4,61 (2H, уш.с), 5,76 (1H, м), 6,68 (1H, д, J=3,6 Гц), 6,77 (1H, с), 7,22-7,25 (2H, м), 7,35-7,45 (3H, м), 7,50-7,60 (4H, м), 8,16 (1H, д, J=8,8 Гц), 8,22 (1H, с).
Пример 147
N1-Фенил-5-(6-((3-(N,N-диэтиламино)пропиламино)карбонил)аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (56,2 мг, 0,11 ммоль, 48%) получали в виде белого порошка из N1-фенил-5-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамида (80 мг, 0,23 ммоль) и 3-(N,N-диэтиламино)пропиламина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,80-1,00 (6H, м), 1,40-1,65 (2H, м), 2,20-2,60 (6H, м), 3,00-3,40 (2H, м), 6,70-6,88 (2H, м), 7,10-7,17 (1H, м), 7,30-7,49 (3H, м), 7,60-7,80 (3H, м), 7,90-8,40 (4H, м), 9,10-9,40 (2H, м), 10,00-10,14 (1H, м).
Пример 148
N1-Циклопропил-5-(6-((4-(пиперидин-1-ил)пиперидин-1-ил)карбонил)аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру получения 2-3 сырой продукт N1-циклопропил-5-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамида (132 мг) получали в виде белого порошка из 6-амино-4-(1H-5-индолиламино)пиримидина (300 мг, 1,33 ммоль) и фенил-N-циклопропилкарбамата.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,60-0,63 (2H, м), 0,70-0,74 (2H, м), 2,76 (1H, м), 5,73 (1H, с), 6,24 (2H, уш.с), 6,59 (1H, д, J=3,6 Гц), 7,02 (1H, дд, J=2,4, 8,8 Гц), 7,74-7,76 (2H, м), 8,01 (1H, с), 8,12 (1H, д, J=8,8 Гц), 8,15 (1H, д, J=2,4 Гц), 8,75 (1H, с).
Аналогично примеру 28 указанное в заголовке соединение (20,6 мг, 0,041 ммоль, 3,1% в 2 процессах) получали в виде белых кристаллов из сырого продукта.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,59-0,63 (2H, м), 0,70-0,76 (2H, м), 1,20-1,60 (8H, м), 1,60-1,80 (2H, м), 2,30-2,80 (8H, м), 4,05-4,20 (2H, м), 6,61 (1H, д, J=3,6 Гц), 7,24 (1H, с), 7,32 (1H, дд, J=2,4, 8,8 Гц), 7,76 (1H, д, J=3,6 Гц), 7,90 (1H, с), 8,13 (1H, д, J=8,8 Гц), 8,17 (1H, д, J=2,4 Гц), 8,28 (1H, с), 9,15 (1H, с), 9,32 (1H, с).
Пример 149
N1-Диметил-5-(6-((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (19,2 мг, 0,040 ммоль, 21%) получали в виде белого порошка из N1-диметил-5-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамида (56 мг, 0,19 ммоль) и 4-(пирролидин-1-ил)пиперидина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,20-1,36 (2H, м), 1,60-1,70 (4H, м), 1,70-1,85 (2H, м), 2,40-2,60 (5H, м), 2,85-2,95 (2H, м), 3,00 (6H, с), 3,95-4,05 (2H, м), 6,60 (1H, д, J=3,2 Гц), 7,22 (1H, д, J=1,2 Гц), 7,30 (1H, дд, J=2,0, 8,8 Гц), 7,50-7,55 (2H, м), 7,88 (1H, уш.с), 8,26 (1H, д, J=1,2 Гц), 9,13 (1H, с), 9,29 (1H, с).
Исходное вещество синтезировали с помощью следующего метода.
Пример получения 149-1
N1-Диметил-5-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру получения 2-3 указанное в заголовке соединение (101 мг, 0,34 ммоль, 34%) получали в виде белых кристаллов из 6-амино-4-(1H-5-индолиламино)пиримидина (225,3 мг, 1,0 ммоль) и фенил-N,N-диметилкарбамата.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 3,02 (6H, с), 5,71 (1Н, с), 6,23 (2H, уш.с), 6,60 (1H, д, J=3,6 Гц), 7,22 (1H, дд, J=2,0, 8,8 Гц), 7,50-7,55 (2H, м), 7,74 (1H, д, J=2,0 Гц), 8,00 (1H, с), 8,73 (1H, с).
Пример 150
N1-Диметил-5-(6-((3-диэтиламинопропил)карбонил)аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (55,3 мг, 0,12 ммоль, 66%) получали в виде белых кристаллов из N1-диметил-5-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамида (55 мг, 0,19 ммоль) и 3-диэтиламинопропиламина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,92 (6H, т, J=7,2 Гц), 1,50-1,55 (2H, м), 2,30-2,45 (6H, м), 3,00 (6H, с), 3,10-3,15 (2H, м), 6,60 (1H, дд, J=0,8, 3,6 Гц), 6,82 (1H, уш.с), 7,28 (1H, дд, J=2,0, 8,8 Гц), 7,50-7,55 (2H, м), 7,71 (1H, м), 7,84 (1H, уш.с), 8,23 (1H, д, J=0,8 Гц), 9,08 (1H, с), 9,32 (1H, с).
Пример 151
Пирролидин-1-иламид 5-(6-((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)амино-4-пиримидил)амино-1H-1-индол-1-карбоновой кислоты
Аналогично примеру 28 указанное в заголовке соединение (13,1 мг, 0,026 ммоль, 14%) получали в виде белых кристаллов из пирролидин-1-иламида 5-(6-амино-4-пиримидил)амино-1H-1-индол-1-карбоновой кислоты (61 мг, 0,19 ммоль) и 4-(пирролидин-1-ил)пиперидина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,20-1,36 (2H, м), 1,60-1,70 (4H, м), 1,70-1,90 (6H, м), 2,40-2,60 (5H, м), 2,85-2,95 (2H, м), 3,40-3,60 (4H, м), 3,95-4,05 (2H, м), 6,59 (1H, д, J=3,2 Гц), 7,22 (1H, уш.с), 7,28 (1H, дд, J=2,0, 8,8 Гц), 7,60-7,70 (2H, м), 7,87 (1H, м), 8,26 (1H, д, J=1,2 Гц), 9,12 (1H, с), 9,28 (1H, с).
Исходное вещество синтезировали с помощью следующего метода.
Пример получения 151-1
Пирролидин-1-иламид 5-(6-амино-4-пиримидил)амино-1H-1-индол-1-карбоновой кислоты
Аналогично примеру получения 2-3 указанное в заголовке соединение (122 мг, 0,38 ммоль, 38%) получали в виде белых кристаллов из 6-амино-4-(1H-5-индолиламино)пиримидина (225,3 мг, 1,0 ммоль) и фенилпирролидин-1-илкарбоксилата.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,80-1,95 (4H, м), 3,50-3,60 (4H, м), 5,71 (1H, с), 6,23 (2H, уш.с), 6,59 (1H, д, J=3,6 Гц), 7,20 (1H, дд, J=2,0, 8,8 Гц), 7,64-7,69 (2H, м), 7,74 (1H, д, J=2,0 Гц), 8,00 (1H, с), 8,73 (1H, с).
Пример 152
Пирролидин-1-иламид 5-(6-((морфолин-4-ил)карбонил)амино-4-пиримидил)амино-1H-1-индол-1-карбоновой кислоты
Аналогично примеру 28 указанное в заголовке соединение (30,3 мг, 0,070 ммоль, 37%) получали в виде белого порошка из пирролидин-1-иламида 5-(6-амино-4-пиримидил)амино-1H-1-индол-1-карбоновой кислоты (61 мг, 0,19 ммоль) и морфолина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,80-1,90 (4H, м), 3,40-3,50 (4H, м), 3,50-3,60 (8H, м), 6,59 (1H, д, J=2,8 Гц), 7,24 (1H, д, J=2,0 Гц), 7,28 (1H, дд, J=2,0, 8,8 Гц), 7,63-7,69 (2H, м), 7,88 (1H, уш.с), 8,27 (1H, д, J=2,8 Гц), 9,19 (1H, с), 9,31 (1H, с).
Пример 153
N1-(2-Пропил)-5-(6-((2-пропиламино)карбонил)аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Гидрид натрия (48 мг, 1,2 ммоль) суспендировали в N,N-диметилформамиде (2,5 мл); туда добавляли при комнатной температуре под струей азота 6-амино-4-(1H-5-индолиламино)пиримидин (225,3 мг, 1,0 ммоль); реакционную смесь перемешивали в течение 30 минут; туда добавляли фенил-N-(2-пропил)карбамат (215 мг, 1,2 ммоль) и реакционную смесь перемешивали в течение ночи. Реакционную смесь подвергали распределению между смесью растворителей этилацетат-тетрагидрофуран (1:1) и насыщенным водным раствором бикарбоната натрия; органический слой промывали водой и насыщенным раствором соли и сушили над безводным сульфатом натрия. После отгонки растворителя остаток очищали колоночной хроматографией на силикагеле (элюент: этилацетат); фракции элюата концентрировали; к остатку добавляли этилацетат для кристаллизации; кристаллы отфильтровывали и сушили при аэрировании с получением указанного в заголовке соединения (31,3 мг, 0,079 ммоль, 7,9%) в виде белых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,09 (6H, д, J=6,8 Гц), 1,20 (6H, д, J=6,8 Гц), 3,75 (1H, м), 4,00 (1H, м), 6,60 (1H, д, J=3,6 Гц), 6,89 (1H, с), 7,27 (1H, дд, J=2,0, 8,8 Гц), 7,45 (1H, м), 7,80-7,90 (3H, м), 8,11 (1H, д, J=8,8 Гц), 8,24 (1H, с), 8,91 (1H, с), 9,31 (1H, с).
Указанную выше хроматографию далее проводили с помощью элюирования смесью этилацетат:метанол=95:5; фракции элюата концентрировали; к остатку добавляли смесь этилацетат-гексан (1:5) для кристаллизации; кристаллы отфильтровывали и сушили при аэрировании с получением N1-(2-пропил)-5-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамида (77,8 мг, 0,25 ммоль, 25%) в виде белых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,29 (6H, д, J=6,8 Гц), 3,98 (1H, м), 5,70 (1H, с), 6,21 (2H, уш.с), 6,57 (1H, д, J=2,8 Гц), 7,18 (1H, д, J=8,8 Гц), 7,72 (1H, с), 7,79-7,82 (2H, м), 7,98 (1H, с), 8,08 (1H, д, J=8,8 Гц), 8,72 (1H, с).
Пример 154
N1-(2-Пропил)-5-(6-((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (36,3 мг, 0,074 ммоль, 60%) получали в виде белого порошка из N1-(2-пропил)-5-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамида (38 мг, 0,12 ммоль) и 4-(пирролидин-1-ил)пиперидина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,20 (6H, д, J=6,8 Гц), 1,20-1,36 (2H, м), 1,60-1,70 (4H, м), 1,70-1,85 (2H, м), 2,40-2,60 (5H, м), 2,85-2,95 (2H, м), 3,90-4,10 (3H, м), 6,60 (1H, д, J=3,6 Гц), 7,22 (1H, с), 7,29 (1H, д, J=8,0 Гц), 7,80-8,00 (3H, м), 8,10 (1H, д, J=8,0 Гц), 8,26 (1H, с), 9,13 (1H, с), 9,29 (1H, с).
Пример 155
N1-(2-Пропил)-5-(6-((3-диэтиламинопропил)карбонил)аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (27,3 мг, 0,059 ммоль, 48%) получали в виде белых кристаллов из N1-(2-пропил)-5-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамида (38 мг, 0,12 ммоль) и 3-диэтиламинопропиламина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,91 (6H, т, J=6,8 Гц), 1,20 (6H, д, J=6,8 Гц), 1,40-1,60 (2H, м), 2,20-2,50 (6H, м), 3,10-3,20 (2H, м), 4,00 (1H, м), 6,60 (1H, д, J=3,6 Гц), 6,82 (1H, с), 7,26 (1H, д, J=8,8 Гц), 7,70 (1H, м), 7,80-7,85 (3H, м), 8,11 (1H, д, J=8,8 Гц), 8,24 (1H, с), 9,08 (1H, с), 9,32 (1H, с).
Пример 156
N1-Метил-4-(6-((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (21,0 мг, 0,045 ммоль, 31%) получали в виде белого порошка из N1-метил-4-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамида (41 мг, 0,15 ммоль) и 4-(пирролидин-1-ил)пиперидина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,20-1,40 (2H, м), 1,60-1,70 (4H, м), 1,70-1,85 (2H, м), 2,40-2,60 (5H, м), 2,81 (3H, д, J=4,4 Гц), 2,85-2,95 (2H, м), 3,90-4,10 (2H, м), 6,85 (1H, м), 7,18 (1H, т, J=8,0 Гц), 7,35 (1H, д, J=4,0 Гц), 7,55 (1H, д, J=8,0 Гц), 7,64 (1H, д, J=8,0 Гц), 7,70 (1H, д, J=4,0 Гц), 7,93 (1H, д, J=8,0 Гц), 8,08 (1H, м), 8,26 (1H, с), 9,19 (1H, с).
Исходные вещества синтезировали с помощью следующих методов.
Пример получения 156-1
6-Хлор-4-(1H-4-индолиламино)пиримидин
4,6-Дихлорпиримидин (1,01 г, 6,6 ммоль), 4-аминоиндол (900 мг, 6,6 ммоль) и N,N-диизопропилэтиламин (3,14 мл, 18 ммоль) растворяли в N,N-диметилформамиде (20 мл) и реакционную смесь перемешивали при 80°С в течение 6 часов. Реакционную смесь подвергали распределению между этилацетатом и водой; водный слой подвергали повторной экстракции этилацетатом и объединенный органический слой промывали насыщенным раствором соли и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и к остатку добавляли небольшое количество метанола для кристаллизации; кристаллы отфильтровывали, промывали метанолом и этилацетатом и сушили при аэрировании с получением указанного в заголовке соединения (599 мг, 2,5 ммоль, 37%) в виде бледно-коричневых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 6,49 (1H, уш.с), 6,75 (1H, уш.с), 7,10 (1H, м), 7,25 (1H, д, J=8,0 Гц), 7,33-7,40 (2H, м), 8,42 (1H, с), 9,71 (1H, уш.с), 11,24 (1H, уш.с).
Пример получения 156-2
6-Амино-4-(1H-4-индолиламино)пиримидин
7 н. раствор аммиака в метаноле (50 мл) и тетрагидрофуран (20 мл) добавляли к 6-хлор-4-(1H-4-индолиламино)пиримидину (599 мг, 2,5 ммоль) и реакционную смесь нагревали в запаянной пробирке при 130°С в течение 137 часов. Растворитель отгоняли при пониженном давлении; остаток очищали колоночной хроматографией на силикагеле (элюент: смесь этилацетат:тетрагидрофуран=1:1); к остатку добавляли диэтиловый эфир для кристаллизации; кристаллы отфильтровывали, промывали диэтиловым эфиром и сушили при аэрировании с получением указанного в заголовке соединения (454 мг, 2,0 ммоль, 82%) в виде бледно-коричневых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 5,74 (1H, с), 6,20 (2H, уш.с), 6,50 (1H, м), 7,00 (1H, т, J=8,0 Гц), 7,09 (1H, д, J=8,0 Гц), 7,15-7,30 (2H, м), 7,98 (1H, с), 8,55 (1H, с), 11,06 (1H, уш.с).
Пример получения 156-3
N1-Метил-4-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру получения 2-3 указанное в заголовке соединение (124,7 мг, 0,44 ммоль, 44%) получали в виде бледно-коричневых кристаллов из 6-амино-4-(1H-5-индолиламино)пиримидина (225,3 мг, 1,0 ммоль) и фенил-N-метилкарбамата.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,81 (3H, д, J=4,0 Гц), 5,75 (1H, с), 6,27 (2H, уш.с), 6,76 (1H, д, J=4,0 Гц), 7,17 (1H, т, J=8,0 Гц), 7,43 (1H, д, J=8,0 Гц), 7,70 (1H, д, J=4,0 Гц), 7,92 (1H, д, J=8,0 Гц), 8,00 (1H, с), 8,06 (1H, м), 8,70 (1H, с).
Пример 157
N1-Метил-4-(6-((4-(пиперидин-1-ил)пиперидин-1-ил)карбонил)аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (7,7 мг, 0,016 ммоль, 11%) получали в виде белого порошка из N1-метил-4-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамида (41 мг, 0,15 ммоль) и 4-(пиперидин-1-ил)пиперидина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,20-1,60 (8H, м), 1,60-1,80 (2H, м), 2,30-2,80 (7H, м), 2,81 (3H, д, J=4,4 Гц), 4,05-4,20 (2H, м), 6,85 (1H, м), 7,18 (1H, т, J=8,0 Гц), 7,35 (1H, д, J=4,0 Гц), 7,55 (1H, д, J=8,0 Гц), 7,65-7,70 (2H, м), 7,92 (1H, д, J=8,0 Гц), 8,06 (1H, м), 8,26 (1H, с), 9,18 (1H, с).
Пример 158
N1-Метил-4-(6-((3-диэтиламинопропиламино)карбонил)аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (23,3 мг, 0,053 ммоль, 37%) получали в виде белых кристаллов из N1-метил-4-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамида (41 мг, 0,15 ммоль) и 3-диэтиламинопропиламина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,92 (6H, т, J=6,8 Гц), 1,40-1,60 (2H, м), 2,20-2,50 (6H, м), 2,82 (3H, д, J=4,4 Гц), 3,10-3,20 (2H, м), 6,80 (1H, м), 6,93 (1H, д, J=6,8 Гц), 7,19 (1H, т, J=8,0 Гц), 7,55 (1H, д, J=8,0 Гц), 7,60-7,70 (2H, м), 7,95 (1H, д, J=8,0 Гц), 8,08 (1H, м), 8,23 (1H, с), 9,11 (1H, с), 9,26 (1H, с).
Пример 159
N1-(4-Фторфенил)-4-(6-((3-диэтиламинопропиламино)карбонил)аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (28,6 мг, 0,055 ммоль, 40%) получали в виде белого порошка из N1-(4-фторфенил)-4-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамида (50 мг, 0,14 ммоль) и 3-диэтиламинопропиламина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,93 (6H, т, J=6,8 Гц), 1,40-1,60 (2H, м), 2,30-2,50 (6H, м), 3,10-3,15 (2H, м), 6,90 (1H, д, J=3,6 Гц), 6,97 (1H, м), 7,18-7,26 (3H, м), 7,60-7,70 (4H, м), 7,90-8,00 (2H, м), 8,25 (1Н, с), 9,13 (1H, с), 9,32 (1H, с), 10,09 (1H, уш.с).
Исходное вещество синтезировали с помощью следующего метода.
Пример получения 159-1
N1-(4-Фторфенил)-4-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру получения 2-3 указанное в заголовке соединение (109 мг, 0,30 ммоль, 30%) получали в виде бледно-желтого порошка из 6-амино-4-(1H-4-индолиламино)пиримидина (225,3 мг, 1,0 ммоль) и фенил-N-(4-фторфенил)карбамата.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 5,78 (1H, с), 6,29 (2H, уш.с), 6,86 (1H, д, J=3,6 Гц), 7,15-7,30 (3H, м), 7,51 (1H, д, J=8,0 Гц), 7,60-7,70 (2H, м), 7,89 (1H, д, J=8,0 Гц), 7,92 (1H, д, J=3,6 Гц), 8,01 (1H, с), 8,76 (1H, с), 10,07 (1H, с).
Пример 160
N1-(4-Фторфенил)-4-(6-((2-диэтиламиноэтиламино)карбонил)аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (36,1 мг, 0,072 ммоль, 52%) получали в виде белых кристаллов из N1-(4-фторфенил)-4-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамида (50 мг, 0,14 ммоль) и 2-диэтиламиноэтиламина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,95 (6H, т, J=6,8 Гц), 2,30-2,50 (6H, м), 3,10-3,20 (2H, м), 6,91 (1H, д, J=3,6 Гц), 6,99 (1H, м), 7,18-7,26 (3H, м), 7,60-7,75 (4H, м), 7,90-8,00 (2H, м), 8,25 (1H, с), 9,24 (1H, с), 9,31 (1H, с), 10,09 (1H, уш.с).
Пример 161
N1-Метил-6-(6-((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (35,6 мг, 0,077 ммоль, 43%) получали в виде белых кристаллов из N1-метил-6-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамида (51 мг, 0,18 ммоль) и 4-(пирролидин-1-ил)пиперидина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,20-1,40 (2H, м), 1,60-1,70 (4H, м), 1,70-1,85 (2H, м), 2,40-2,60 (5H, м), 2,81 (3H, д, J=4,0 Гц), 2,85-2,95 (2H, м), 3,90-4,10 (2H, м), 6,57 (1H, д, J=3,6 Гц), 7,23 (1H, с), 7,39-7,50 (2H, м), 7,68 (1H, д, J=3,6 Гц), 8,02 (1H, м), 8,26 (1H, с), 8,51 (1H, с), 9,13 (1H, с), 9,40 (1H, с).
Исходные вещества синтезировали с помощью следующих методов.
Пример получения 161-1
6-Хлор-4-(1H-6-индолиламино)пиримидин
Указанное в заголовке соединение (1,229 г, 5,0 ммоль, 46%) получали в виде бледно-желтых кристаллов из 4,6-дихлорпиримидина (1,69 г, 11 ммоль), 6-аминоиндола и N,N-диизопропилэтиламина способом, сходным с синтезом 6-хлор-4-(1H-5-индолиламино)пиримидина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 6,39 (1H, с), 6,74 (1H, с), 7,02 (1H, дд, J=2,8, 8,8 Гц), 7,30 (1H, т, J=2,8 Гц), 7,50 (1H, д, J=8,8 Гц), 7,83 (1H, м), 8,43 (1H, с), 9,78 (1H, с), 11,07 (1H, уш.с).
Пример получения 161-2
6-Амино-4-(1H-6-индолиламино)пиримидин
7 н. раствор аммиака в метаноле (75 мл) добавляли к 6-хлор-4-(1H-6-индолиламино)пиримидину (1,229 г, 5,0 ммоль) и реакционную смесь нагревали в запаянной пробирке при 130°С в течение 6 дней. Растворитель отгоняли при пониженном давлении; остаток очищали колоночной хроматографией на силикагеле (элюент: смесь этилацетат:тетрагидрофуран=1:1); к остатку добавляли диэтиловый эфир для кристаллизации; кристаллы отфильтровывали, промывали диэтиловым эфиром и сушили при аэрировании с получением указанного в заголовке соединения (883 мг, 3,9 ммоль, 78%) в виде бледно-желтых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 5,71 (1H, с), 6,19 (2H, уш.с), 6,32 (1H, с), 6,92 (1H, дд, J=1,2, 8,0 Гц), 7,20 (1H, м), 7,40 (1H, д, J=8,0 Гц), 7,65 (1H, с), 7,98 (1H, с), 8,65 (1H, с), 10,91 (1H, с).
Пример получения 161-3
N1-Метил-6-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру получения 2-3 указанное в заголовке соединение (105 мг, 0,37 ммоль, 48%) получали в виде бледно-коричневых кристаллов из 6-амино-4-(1H-6-индолиламино)пиримидина (175 мг, 0,78 ммоль) и фенил-N-метилкарбамата.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,80 (3H, д, J=4,4 Гц), 5,73 (1H, с), 6,24 (2H, уш.с), 6,56 (1H, д, J=2,8 Гц), 7,33 (1H, д, J=8,4 Гц), 7,44 (1H, д, J=8,4 Гц), 7,66 (1H, д, J=2,8 Гц), 7,90-8,10 (2H, м), 8,33 (1H, с), 8,84 (1H, с).
Пример 162
N1-Метил-6-(6-((3-диэтиламинопропиламино)карбонил)аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (37,3 мг, 0,085 ммоль, 47%) получали в виде белых кристаллов из N1-метил-6-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамида (51 мг, 0,18 ммоль) и 3-диэтиламинопропиламина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,92 (6H, т, J=6,8 Гц), 1,40-1,60 (2H, м), 2,20-2,40 (6H, м), 2,81 (3H, д, J=4,0 Гц), 3,05-3,20 (2H, м), 6,58 (1H, д, J=4,0 Гц), 6,83 (1H, с), 7,38 (1H, д, J=8,0 Гц), 7,46 (1H, д, J=8,0 Гц), 7,60-7,80 (2H, м), 8,03 (1H, м), 8,23 (1H, с), 8,46 (1H, с), 9,10 (1H, с), 9,43 (1H, с).
Пример 163
N1-(2-Пропил)-6-(6-((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (40,4 мг, 0,082 ммоль, 54%) получали в виде белых кристаллов из N1-(2-пропил)-6-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамида (47 мг, 0,15 ммоль) и 4-(пирролидин-1-ил)пиперидина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,20 (6H, д, J=6,8 Гц), 1,20-1,36 (2H, м), 1,60-1,70 (4H, м), 1,70-1,85 (2H, м), 2,40-2,60 (5H, м), 2,80-3,00 (2H, м), 3,90-4,10 (3H, м), 6,56 (1H, д, J=3,6 Гц), 7,24 (1H, с), 7,30-7,50 (2H, м), 7,74 (1H, д, J=3,6 Гц), 7,81 (1H, д, J=8,8 Гц), 8,26 (1H, с), 8,50 (1H, с), 9,13 (1H, с), 9,39 (1H, с).
Исходное вещество синтезировали с помощью следующего метода.
Пример получения 163-1
N1-(2-Пропил)-6-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру получения 2-3 указанное в заголовке соединение (95,3 мг, 0,31 ммоль, 40%) получали в виде бледно-коричневых кристаллов из 6-амино-4-(1H-6-индолиламино)пиримидина (175 мг, 0,78 ммоль) и фенил-N-(2-пропил)карбамата.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,20 (6H, д, J=6,4 Гц), 4,00 (1H, м), 5,73 (1H, с), 6,24 (2H, уш.с), 6,55 (1H, д, J=3,6 Гц), 7,33 (1H, дд, J=2,0, 8,0 Гц), 7,44 (1H, д, J=8,0 Гц), 7,73 (1H, д, J=3,6 Гц), 7,80 (1H, д, J=8,0 Гц), 7,98 (1H, с), 8,33 (1H, с), 8,84 (1H, с).
Пример 164
N1-(2-Пропил)-6-(6-((3-диэтиламинопропиламино)карбонил)аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (40,1 мг, 0,086 ммоль, 57%) получали в виде белых кристаллов из N1-(2-пропил)-6-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамида (47 мг, 0,15 ммоль) и 3-диэтиламинопропиламина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,92 (6Н, т, J=6,8 Гц), 1,20 (6H, д, J=6,4 Гц), 1,40-1,60 (2H, м), 2,20-2,50 (6H, м), 3,05-3,20 (2H, м), 4,00 (1H, м), 6,57 (1H, д, J=3,6 Гц), 6,84 (1H, с), 7,36 (1H, дд, J=8,0 Гц), 7,46 (1H, д, J=8,0 Гц), 7,12 (1H, м), 7,76 (1H, д, J=3,6 Гц), 7,82 (1H, д, J=8,0 Гц), 8,23 (1H, с), 8,44 (1H, с), 9,10 (1H, с), 9,43 (1H, с).
Пример 165
N1-(4-Фторфенил)-6-(6-((3-диэтиламинопропиламино)карбонил)аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (22,9 мг, 0,044 ммоль, 24%) получали в виде белых кристаллов из N1-(4-фторфенил)-6-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамида (67 мг, 0,19 ммоль) и 3-диэтиламинопропиламина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,92 (6H, т, J=6,8 Гц), 1,40-1,60 (2H, м), 2,20-2,40 (6H, м), 3,05-3,20 (2H, м), 6,68 (1H, д, J=3,6 Гц), 6,87 (1H, с), 7,24 (2H, т, J=8,8 Гц), 7,43 (1H, дд, J=2,0, 8,4 Гц), 7,52 (1H, д, J=8,4 Гц), 7,60-7,80 (4H, м), 7,89 (1H, д, J=3,6 Гц), 8,23 (1Н, с), 8,48 (1H, с), 9,11 (1H, с), 9,45 (1H, с).
Исходное вещество синтезировали с помощью следующего метода.
Пример получения 165-1
N1-(4-Фторфенил)-6-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру получения 2-3 указанное в заголовке соединение (137 мг, 0,38 ммоль, 49%) получали в виде бледно-коричневых кристаллов из 6-амино-4-(1H-6-индолиламино)пиримидина (175 мг, 0,78 ммоль) и фенил-N-(4-фторфенил)карбамата.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 5,75 (1H, с), 6,26 (2H, уш.с), 6,66 (1H, д, J=3,6 Гц), 7,22 (2H, т, J=8,8 Гц), 7,39 (1H, дд, J=2,0, 8,4 Гц), 7,49 (1H, д, J=8,4 Гц), 7,60-7,70 (2H, м), 7,87 (1H, д, J=3,6 Гц), 7,99 (1H, с), 8,36 (1H, с), 8,91 (1H, с), 10,01 (1H, с).
Пример 166
N1-(4-Фторфенил)-6-(6-((2-диэтиламиноэтиламино)карбонил)аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (11,1 мг, 0,022 ммоль, 12%) получали в виде белых кристаллов из N1-(4-фторфенил)-6-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамида (67 мг, 0,19 ммоль) и 2-диэтиламиноэтиламина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,80-1,00 (6H, м), 2,20-2,50 (6H, м), 3,00-3,20 (2H, м), 6,74 (1H, с), 6,84 (1H, д, J=3,6 Гц), 7,03 (1H, д, J=8,0 Гц), 7,20 (2H, т, J=8,8 Гц), 7,50-7,70 (3H, м), 7,70 (1H, д, J=8,0 Гц), 8,00 (1H, с), 8,12 (1H, д, J=3,6 Гц), 8,37 (1H, с), 9,23 (1H, с), 9,41 (1H, с), 10,12 (1H, с).
Пример 167
N1-Диметил-6-(6-((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (16,1 мг, 0,034 ммоль, 17%) получали в виде бледно-желтого порошка из N1-диметил-6-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамида (58 мг, 0,20 ммоль) и 4-(пирролидин-1-ил)пиперидина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,20-1,36 (2H, м), 1,60-1,70 (4H, м), 1,70-1,85 (2H, м), 2,40-2,60 (5H, м), 2,80-3,00 (2H, м), 3,02 (6H, с), 3,90-4,10 (2H, м), 6,55 (1H, с), 7,26 (1H, с), 7,30 (1H, д, J=8,0 Гц), 7,40-7,50 (2H, м), 8,01 (1H, с), 8,29 (1H, с), 9,16 (1H, с), 9,41 (1H, с).
Исходное вещество синтезировали с помощью следующего метода.
Пример получения 167-1
N1-Диметил-6-(6-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру получения 2-3 указанное в заголовке соединение (58,3 мг, 0,20 ммоль, 25%) получали в виде бледно-коричневых кристаллов из 6-амино-4-(1H-6-индолиламино)пиримидина (175 мг, 0,78 ммоль) и фенил-N,N-диметилкарбамата.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 3,01 (6H, с), 5,72 (1H, с), 6,26 (2H, уш.с), 6,54 (1H, д, J=3,6 Гц), 7,24 (1H, дд, J=2,0, 8,0 Гц), 7,40-7,50 (2H, м), 7,84 (1H, с), 8,01 (1H, с), 8,86 (1H, с).
Пример 168
N1-Диэтил-5-(2-((пирролидин-1-иламино)карбонил)аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (91,0 мг, 0,22 ммоль, 38%) получали в виде бледно-желтого порошка из N1-диэтил-5-(2-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамида (186 мг, 0,57 ммоль) и пирролидина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,15 (6H, т, J=6,8 Гц), 1,60-1,90 (4H, м), 3,20-3,50 (8H, м), 6,28 (1H, д, J=6,0 Гц), 6,52 (1H, д, J=3,6 Гц), 7,40-7,50 (3H, м), 7,96 (1H, д, J=6,0 Гц), 8,24 (1H, уш.с), 8,67 (1H, с), 9,35 (1H, с).
Исходные вещества синтезировали с помощью следующих методов.
Пример получения 168-1
2-Амино-4-(1H-5-индолиламино)пиримидин
Смесь 2-амино-4,6-дихлорпиримидина (1,64 г, 10 ммоль), 5-аминоиндола (1,32 г, 10 ммоль), диизопропилэтиламина (5,23 мл, 30 ммоль) и N,N-диметилформамида (30 мл) нагревали при 60°С и перемешивали в течение ночи в атмосфере азота. Реакционную смесь после остывания до комнатной температуры подвергали распределению между этилацетатом и водой; органический слой промывали водой и насыщенным раствором соли и сушили над безводным сульфатом натрия. Растворитель отгоняли; полученный остаток растворяли в тетрагидрофуране (100 мл); туда добавляли в атмосфере азота 10% палладий-на-угле (50% влажность, 1,0 г) и реакционную смесь перемешивали в течение 4 дней в атмосфере водорода при атмосферном давлении. Реакционную систему продували азотом; катализатор отфильтровывали; фильтрат концентрировали при пониженном давлении; остаток очищали колоночной хроматографией на NH-силикагеле (элюент: смесь этилацетат:метанол=95:5); к остатку добавляли диэтиловый эфир для кристаллизации и кристаллы отфильтровывали и сушили при аэрировании с получением указанного в заголовке соединения (852 мг, 3,8 ммоль, 38%) в виде бледно-коричневых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 5,89 (1H, д, J=5,6 Гц), 5,99 (2H, уш.с), 6,34 (1H, с), 7,12 (1H, д, J=8,4 Гц), 7,20-7,40 (2H, м), 7,70 (1H, д, J=5,6 Гц), 7,79 (1H, с), 8,73 (1H, с), 10,95 (1H, с).
Пример получения 168-2
N1-Диэтил-5-(2-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру получения 2-3 указанное в заголовке соединение (1,22 г, 3,8 ммоль, количественно) получали в виде бледно-коричневого порошка из 2-амино-4-(1H-5-индолиламино)пиримидина (852 мг, 3,8 ммоль) и диэтилкарбамилхлорида.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 1,26 (6H, т, J=7,2 Гц), 3,49 (4H, кв, J=7,2 Гц), 4,78 (2H, уш.с), 6,03 (1H, д, J=5,6 Гц), 6,57 (1H, д, J=3,6 Гц), 6,66 (1H, с), 7,16 (1H, дд, J=2,0, 8,8 Гц), 7,31 (1H, д, J=3,6 Гц), 7,53 (1H, д, J=2,0 Гц), 7,65 (1H, д, J=8,8 Гц), 7,88 (1H, д, J=5,6 Гц).
Пример 169
N1-Диэтил-5-(5-иод-2-((пирролидин-1-иламино)карбонил)аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (37,3 мг, 0,068 ммоль, 26%) получали в виде белого порошка из N1-диэтил-5-(2-амино-5-иодпиримидин-4-ил)амино-1H-1-индолкарбоксамида (117 мг, 0,26 ммоль) и пирролидина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,15 (6H, т, J=6,8 Гц), 1,60-1,80 (4H, м), 3,30-3,50 (8H, м), 6,54 (1H, с), 7,30-7,60 (3H, м), 8,09 (1H, с), 8,15 (1H, с), 8,33 (1H, с), 8,82 (1H, с).
Исходное вещество синтезировали с помощью следующего метода.
Пример получения 169-1
N1-Диэтил-5-(2-амино-5-иодпиримидин-4-ил)амино-1H-1-индолкарбоксамид
N1-Диэтил-5-(2-аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид (1,06 г, 3,27 ммоль) растворяли в N,N-диметилформамиде (10 мл) в атмосфере азота; туда добавляли N-иодсукцинимид (920 мг, 4,08 ммоль) при охлаждении в водно-ледяной бане и реакционную смесь перемешивали при комнатной температуре в течение ночи. Реакционную смесь подвергали распределению между этилацетатом и водой; органический слой промывали водой и насыщенным раствором соли и сушили над безводным сульфатом натрия. Растворитель отгоняли; остаток очищали колоночной хроматографией на силикагеле (элюент: этилацетат) с получением указанного в заголовке соединения (1,00 г, 2,33 ммоль, 68%) в виде желтого порошка.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 1,26 (6H, т, J=7,2 Гц), 3,49 (4H, кв, J=7,2 Гц), 4,84 (2H, уш.с), 6,58 (1H, д, J=3,6 Гц), 6,95 (1H, с), 7,27-7,40 (2H, м), 7,63 (1H, д, J=8,8 Гц), 7,82 (1H, с), 8,16 (1H, с).
Пример 170
N1-Диэтил-5-(5-циано-2-((пирролидин-1-иламино)карбонил)аминопиримидин-4-ил)амино-1H-1-индолкарбоксамид
Аналогично примеру 28 указанное в заголовке соединение (35,3 мг, 0,079 ммоль, 28%) получали в виде белых кристаллов из N1-диэтил-5-(2-амино-5-цианопиримидин-4-ил)амино-1H-1-индолкарбоксамида (100 мг, 0,29 ммоль) и пирролидина.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,15 (6H, т, J=6,8 Гц), 1,60-1,80 (4H, м), 3,20-3,50 (8H, м), 6,56 (1H, с), 7,40-7,60 (3H, м), 8,03 (1H, с), 8,49 (1H, с), 9,43 (1H, с), 9,50 (1H, с).
Исходное вещество синтезировали следующим образом.
Пример получения 170-1
N1-Диэтил-5-(2-амино-5-цианопиримидин-4-ил)амино-1H-1-индолкарбоксамид
N1-Диэтил-5-(2-амино-5-иодпиримидин-4-ил)амино-1H-1-индолкарбоксамид (882 мг, 1,96 ммоль) растворяли в N,N-диметилформамиде (10 мл) в атмосфере азота; туда добавляли цианид цинка (253 мг, 2,15 ммоль) и тетракис(трифенилфосфин)палладий (226 мг, 0,2 ммоль); реакционную смесь перемешивали при 100°С в течение 2 часов. Реакционную смесь подвергали распределению между этилацетатом и водой; органический слой промывали водой и насыщенным раствором соли и сушили над безводным сульфатом натрия. Растворитель отгоняли и остаток очищали колоночной хроматографией на силикагеле (элюент: этилацетат) с получением указанного в заголовке соединения (493 мг, 1,41 ммоль, 72%) в виде белых кристаллов.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 1,26 (6H, т, J=7,2 Гц), 3,49 (4H, кв, J=7,2 Гц), 5,26 (2H, уш.с), 6,59 (1H, д, J=3,6 Гц), 7,05 (1H, с), 7,27-7,35 (2H, м), 7,66 (1H, д, J=8,8 Гц), 7,78 (1H, м), 8,27 (1H, с).
Пример 171
(2-Диэтиламиноэтил)амид 5-(2-(3-этилуреидо)пиридин-4-илокси)индол-1-карбоновой кислоты
Аналогично примеру получения 5-1 сырой продукт (2-диэтиламиноэтил)амид 5-(2-аминопиридин-4-илокси)индол-1-карбоновой кислоты (81 мг) получали в виде бледно-желтого масла из 4-(1H-5-индолилокси)-2-пиридинамина (225 мг, 1,00 ммоль, WO 02/32872), гидрида натрия (80 мг, 2,00 ммоль, 60% в масле) и фенил-N-(2-диэтиламиноэтил)карбамата (314 мг, 1,50 ммоль). Аналогично примеру получения 5-2 смесь фенил(4-(1-(2-диэтиламиноэтил)карбамоил-1H-индол-5-илокси)пиридин-2-ил)-N-(феноксикарбонил)карбамата и фенил(4-(1-(2-диэтиламиноэтил)карбамоил-1H-индол-5-илокси)пиридин-2-ил)карбамата (32 мг) получали в виде бледно-желтого масла из сырого продукта, полученного выше, фенилхлорформиата (0,041 мл, 0,33 ммоль) и триэтиламина (0,049 мл, 0,35 ммоль). Аналогично примеру 5 указанное в заголовке соединение (11 мг, 0,025 ммоль, 12%) получали в виде бледно-желтых кристаллов из полученной выше смеси этиламингидрохлорида (30 мг, 0,26 ммоль) и триэтиламина (0,5 мл).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,97 (6H, т, J=7,0 Гц), 1,02 (3H, т, J=7,0 Гц), 2,44-2,60 (8H, м), 3,10 (2H, м), 6,50 (1H, дд, J=1,6, 6,0 Гц), 6,68 (1H, д, J=3,6 Гц), 6,86 (1H, д, J=1,6 Гц), 7,03 (1H, дд, J=2,0, 8,8 Гц), 7,36 (1H, д, J=2,0 Гц), 7,89 (1H, д, J=3,6 Гц), 7,97 (1H, м), 8,02 (1H, д, J=6,0 Гц), 8,17 (1H, м), 8,28 (1H, д, J=8,8 Гц), 9,00 (1H, с).
ESI-МС: 439,30 (M+H).
Исходное вещество синтезировали следующим образом.
Пример получения 171-1
Фенил-N-(2-диэтиламиноэтил)карбамат
Аналогично примеру получения 2-1 сырой продукт получали из 2-диэтиламиноэтиламина (7,3 мл, 50 ммоль) и фенилхлорформиата (6,9 мл, 55 ммоль). Сырой продукт очищали колоночной хроматографией на силикагеле (Fuji Silysia NH, этилацетат) и дополнительно очищали колоночной хроматографией на силикагеле (Fuji Silysia NH; смесь гексан:этилацетат=3:1, 1:1, этилацетат в данном порядке) с получением указанного в заголовке соединения (1,3 г, 6,4 ммоль, 13%) в виде бесцветного масла.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 1,04 (6H, т, J=7,2 Гц), 2,52-2,62 (6H, м), 3,31 (2H, кв, J=5,6 Гц), 5,62 (1H, уш.с), 7,13 (2H, д, J=7,6 Гц), 7,18 (1H, т, J=7,6 Гц), 7,35 (2H, т, J=7,6 Гц).
Пример 172
(2-Этоксиэтил)амид 5-(2-(3,3-диэтилуреидо)пиридин-4-илокси)индол-1-карбоновой кислоты
Аналогично примеру получения 5-2 смесь фенил(4-(1-(2-этоксиэтил)карбамоил-1H-индол-5-илокси)пиридин-2-ил)-N-(феноксикарбонил)карбамата и фенил(4-(1-(2-этоксиэтил)карбамоил-1H-индол-5-илокси)пиридин-2-ил)карбамата (3,42 г) получали в виде бледно-желтого масла из (2-этоксиэтил)амида 5-(2-аминопиридин-4-илокси)индол-1-карбоновой кислоты (1,86 г, 5,46 ммоль), фенилхлорформиата (1,51 мл, 12,0 ммоль) и триэтиламина (1,90 мл, 13,7 ммоль). Аналогично примеру 5 указанное в заголовке соединение получали в виде бледно-розовых кристаллов (84 мг, 0,19 ммоль) из данных промежуточных веществ (174 мг) и диэтиламина (0,16 мл, 1,5 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,01 (6H, т, J=7,2 Гц), 1,11 (3H, т, J=7,2 Гц), 3,26-3,31 (4H, м), 3,42-3,50 (4H, м), 3,53 (2H, м), 6,54 (1H, дд, J=2,4, 5,6 Гц), 6,68 (1H, д, J=3,6 Гц), 7,04 (1H, дд, J=2,4, 9,0 Гц), 7,36 (1H, д, J=2,4 Гц), 7,41 (1H, д, J=2,4 Гц), 7,93 (1H, д, J=3,6 Гц), 8,06 (1H, д, J=5,6 Гц), 8,28 (1H, д, J=9,0 Гц), 8,31 (1H, м), 8,60 (1H, с).
ESI-МС: 440,47 (M+H).
Исходные вещества синтезировали следующим образом.
Пример получения 172-1
Фенил-N-(2-этоксиэтил)карбамат
Аналогично примеру 5 сырой продукт получали из 2-этоксиэтиламина (5,2 мл, 50 ммоль), фенилхлорформиата (6,9 мл, 55 ммоль) и пиридина (4,5 мл, 55 ммоль). Полученный сырой продукт очищали колоночной хроматографией на силикагеле (Fuji Silysia BW-300, смесь гексан:этилацетат=85:15-50:50) с получением указанного в заголовке соединения (8,38 г, 40,4 ммоль, 80,9%) в виде бледно-желтого масла.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 1,23 (3H, т, J=7,0 Гц), 3,44-3,48 (2H, м), 3,52-3,58 (4H, м), 5,41 (1H, уш.с), 7,13 (2H, д, J=7,6 Гц), 7,19 (1H, т, J=7,6 Гц), 7,35 (2H, т, J=7,6 Гц).
Пример получения 172-2
(2-Этоксиэтил)амид 5-(2-аминопиридин-4-илокси)индол-1-карбоновой кислоты
Аналогично примеру получения 5-1 указанное в заголовке соединение (1,86 г, 5,46 ммоль, 61,5%) получали в виде бледно-коричневого масла из 4-(1H-5-индолилокси)-2-пиридинамина (2,00 г, 8,88 ммоль, WO 02/32872), гидрида натрия (462 мг, 11,5 ммоль, 60% в масле) и фенил-N-(2-этоксиэтил)карбамата (2,23 г, 10,7 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,11 (3H, т, J=7,2 Гц), 3,42 (2H, м), 3,47 (2H, кв, J=7,2 Гц), 3,53 (2H, т, J=6,0 Гц), 5,74 (1H, д, J=2,0 Гц), 5,84 (2H, м), 6,12 (1H, дд, J=2,0, 6,0 Гц), 6,67 (1H, д, J=3,8 Гц), 7,01 (1H, дд, J=2,0, 8,8 Гц), 7,33 (1H, д, J=2,0 Гц), 7,75 (1H, д, J=6,0 Гц), 7,91 (1H, д, J=6,0 Гц), 8,26 (1H, д, J=8,8 Гц), 8,28 (1H, м).
Пример 173
(2-Этоксиэтил)амид 5-(2-(3-этилуреидо)пиридин-4-илокси)индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение получали в виде бесцветных кристаллов (84 мг, 0,204 ммоль) из смеси (174 мг) фенил(4-(1-(2-этоксиэтил)карбамоил-1H-индол-5-илокси)пиридин-2-ил)-N-(феноксикарбонил)карбамата и фенил(4-(1-(2-этоксиэтил)карбамоил-1H-индол-5-илокси)пиридин-2-ил)карбамата, который получали в виде промежуточного вещества в примере 172, этиламина гидрохлорида (122 мг, 1,50 ммоль) и триэтиламина (0,5 мл).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,02 (3H, т, J=7,0 Гц), 1,12 (3H, т, J=7,0 Гц), 3,10 (2H, м), 3,40-3,49 (4H, м), 3,53 (2H, т, J=5,8 Гц), 6,50 (1H, дд, J=2,4, 5,8 Гц), 6,68 (1H, д, J=3,6 Гц), 6,86 (1H, д, J=2,4 Гц), 7,04 (1H, дд, J=2,4, 8,8 Гц), 7,37 (1H, д, J=2,4 Гц), 7,93 (1H, д, J=3,6 Гц), 7,96 (1H, м), 8,02 (1H, д, J=5,8 Гц), 8,28 (1H, д, J=8,8 Гц), 8,31 (1H, м), 9,00 (1H, с).
ESI-МС: 412,18 (M+H).
Пример 174
(3-Этоксипропил)амид 5-(2-(3-этилуреидо)пиридин-4-илокси)индол-1-карбоновой кислоты
Сходно с получением примера 5-2 смесь фенил(4-(1-(3-этоксипропил)карбамоил-1H-индол-5-илокси)пиридин-2-ил)-N-(феноксикарбонил)карбамата и фенил(4-(1-(3-этоксипропил)карбамоил-1H-индол-5-илокси)пиридин-2-ил)карбамата получали в виде бледно-коричневого масла (720 мг) из (3-этоксипропил)амида 5-(2-аминопиридин-4-илокси)индол-1-карбоновой кислоты (900 мг, 2,54 ммоль), фенилхлорформиата (0,669 мл, 5,33 ммоль) и триэтиламина (0,885 мл, 6,35 ммоль). Аналогично примеру 5 указанное в заголовке соединение получали в виде бледно-розовых кристаллов (41 мг, 0,096 ммоль) из данного промежуточного вещества (100 мг), этиламина гидрохлорида (64 мг, 0,841 ммоль) и триэтиламина (0,5 мл).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,02 (3H, т, J=7,2 Гц), 1,10 (3H, т, J=7,2 Гц), 1,79 (2H, м), 3,10 (2H, м), 3,34 (2H, м), 3,42 (4H, м), 6,50 (1H, дд, J=2,4, 5,8 Гц), 6,67 (1H, д, J=3,8 Гц), 6,86 (1H, д, J=2,4 Гц), 7,03 (1H, дд, J=2,4, 9,2 Гц), 7,36 (1H, д, J=2,4 Гц), 7,90 (1H, д, J=3,8 Гц), 7,95 (1H, м), 8,02 (1H, д, J=5,8 Гц), 8,20 (1H, м), 8,28 (1H, м), 8,99 (1H, с).
ESI-МС: 426,39 (M+H).
Исходное вещество синтезировали следующим образом.
Пример получения 174-1
(3-Этоксипропил)амид 5-(2-аминопиридин-4-илокси)индол-1-карбоновой кислоты
Аналогично примеру получения 5-1 указанное в заголовке соединение (900 мг, 2,54 ммоль, 57,2%) получали в виде бледно-коричневого масла из 4-(1H-5-индолилокси)-2-пиридинамина (1,00 г, 4,44 ммоль, WO 02/32872), гидрида натрия (213 мг, 5,33 ммоль, 60% в масле) и фенил-N-(3-этоксипропил)карбамата (1,19 г, 5,33 ммоль, WO 02/32872).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,07-1,13 (3H, м), 1,81 (2H, м), 3,33-3,47 (6H, м), 5,76 (1H, д, J=2,4 Гц), 5,85 (2H, с), 6,14 (1H, дд, J=2,4, 6,0 Гц), 6,68 (1H, д, J=3,6 Гц), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,34 (1H, д, J=2,4 Гц), 7,77 (1H, д, J=6,0 Гц), 7,90 (1H, д, J=3,6 Гц), 8,20 (1H, м), 8,27 (1H, д, J=8,8 Гц).
Пример 175
(3-Метилсульфанилпропил)амид 5-(2-(3-этилуреидо)пиридин-4-илокси)индол-1-карбоновой кислоты
Аналогично примеру получения 5-1 сырой продукт (3-метилсульфанилпропил)амида 5-(2-аминопиридин-4-илокси)индол-1-карбоновой кислоты (105 мг) получали в виде бледно-желтого масла из 4-(1H-5-индолилокси)-2-пиридинамина (125 мг, 0,555 ммоль, WO 02/32872), гидрида натрия (28 мг, 0,694 ммоль, 60% в масле) и фенил-N-(3-метилсульфанилпропил)карбамата (156 мг, 0,694 ммоль, WO 02/32872). Аналогично примеру получения 5-2 смесь фенил(4-(1-(3-метилсульфанилпропил)карбамоил-1H-индол-5-илокси)пиридин-2-ил)-N-(феноксикарбонил)карбамата и фенил(4-(1-(3-метилсульфанилпропил)карбамоил-1H-индол-5-илокси)пиридин-2-ил)карбамата получали в виде бледно-желтого масла из сырого продукта, полученного выше, фенилхлорформиата (0,10 мл, 0,76 ммоль) и триэтиламина (0,12 мл, 0,83 ммоль). Аналогично примеру 5 указанное в заголовке соединение (17 мг, 0,040 ммоль) получали в виде бесцветных кристаллов из смеси, полученной выше, этиламина гидрохлорида (141 мг, 1,73 ммоль) и триэтиламина (0,5 мл).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,02 (3H, т, J=7,2 Гц), 1,83 (2H, м), 2,05 (3H, с), 2,52 (2H, т, J=7,6 Гц), 3,10 (2H, м), 3,35 (2H, м), 6,50 (1H, д, J=5,6 Гц), 6,68 (1H, д, J=3,4 Гц), 6,86 (1H, с), 7,03 (1H, д, J=9,2 Гц), 7,36 (1H, с), 7,91 (1H, д, J=3,4 Гц), 7,94 (1H, м), 8,02 (1H, д, J=5,6 Гц), 8,24 (1H, м), 8,27 (1H, д, J=9,2 Гц), 8,99 (1H, с).
Пример 176
Тиазол-2-иламид 5-(2-(3,3-диэтилуреидо)пиридин-4-илокси)индол-1-карбоновой кислоты
Аналогично примеру получения 5-2 смесь (267 мг) фенил(4-(1-(тиазол-2-ил)карбамоил-1H-индол-5-илокси)пиридин-2-ил)-N-(феноксикарбонил)карбамата и фенил(4-(1-(тиазол-2-ил)карбамоил-1H-индол-5-илокси)пиридин-2-ил)карбамата получали в виде бледно-желтого масла из тиазол-2-иламида 5-(2-аминопиридин-4-илокси)индол-1-карбоновой кислоты (145 мг, 0,413 ммоль), фенилхлорформиата (0,110 мл, 0,909 ммоль) и триэтиламина (0,140 мл, 1,03 ммоль). Аналогично примеру 5 указанное в заголовке соединение (74 мг, 0,16 ммоль) получали в виде бледно-розовых кристаллов из промежуточного вещества, полученного выше (131 мг), и диэтиламина (0,120 мл, 1,11 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,01 (6H, т, J=6,8 Гц), 3,28 (4H, м), 6,56 (1H, дд, J=2,0, 5,6 Гц), 6,66 (1H, м), 7,06 (2H, м), 7,37 (1H, д, J=2,0 Гц), 7,43 (1H, с), 7,47 (1H, д, J=4,4 Гц), 8,05 (1H, м), 8,07 (1H, д, J=5,6 Гц), 8,60 (2H, м).
ESI-МС: 451,15 (M+H).
Исходное вещество синтезировали следующим образом.
Пример получения 176-1
Тиазол-2-иламид 5-(2-аминопиридин-4-илокси)индол-1-карбоновой кислоты
Аналогично примеру получения 5-1 указанное в заголовке соединение (145 мг, 0,413 ммоль, 57,2%) получали в виде бледно-коричневого масла из 4-(1H-5-индолилокси)-2-пиридинамина (225 мг, 1,00 ммоль, WO 02/32872), гидрида натрия (120 мг, 3,00 ммоль, 60% в масле) и фенил-N-(тиазол-2-ил)карбамата (286 мг, 1,30 ммоль, WO 02/32872).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 5,77 (1H, д, J=2,4 Гц), 5,87 (2H, уш.с), 6,15 (1H, дд, J=2,4, 5,6 Гц), 6,65 (1H, д, J=3,6 Гц), 7,03 (1H, дд, J=2,4, 9,0 Гц), 7,07 (1H, д, J=4,6 Гц), 7,34 (1H, д, J=2,4 Гц), 7,46 (1H, д, J=4,6 Гц), 7,77 (1H, д, J=5,6 Гц), 8,04 (1H, д, J=3,6 Гц), 8,58 (1H, д, J=9,0 Гц).
Пример 177
Тиазол-2-иламид 5-(2-(3-этилуреидо)пиридин-4-илокси)индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (71 мг, 0,168 ммоль) получали в виде бесцветных кристаллов из смеси (135 мг) фенил(4-(1-(тиазол-2-ил)карбамоил-1H-индол-5-илокси)пиридин-2-ил)-N-(феноксикарбонил)карбамата и фенил(4-(1-(тиазол-2-ил)карбамоил-1H-индол-5-илокси)пиридин-2-ил)карбамата, полученных в примере 176, этиламина гидрохлорида (91 мг, 1,1 ммоль) и триэтиламина (0,5 мл).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,07 (3H, т, J=7,2 Гц), 3,07-3,14 (2H, м), 6,51 (1H, дд, J=2,0, 6,0 Гц), 6,61 (1H, с), 7,01 (2H, м), 7,35 (1H, с), 7,41 (1H, м), 8,01-8,06 (3H, м), 8,05 (1H, м), 8,62 (1H, д, J=9,2 Гц), 9,00 (1H, с).
ESI-МС: 423,23 (M+H).
Пример 178
1-Этил-3-(4-(1-((4-метилпиперазин-1-ил)карбонил)-1H-индол-5-илокси)пиридин-2-ил)мочевина
Аналогично примеру получения 5-2 смесь (1,09 г) фенил(4-(1-((4-метилпиперазин-1-ил)карбонил)-1H-индол-5-илокси)пиридин-2-ил)-(N-феноксикарбонил)карбамата и фенил(4-(1-((4-метилпиперазин-1-ил)карбонил)-1H-индол-5-илокси)пиридин-2-ил)карбамата получали в виде бесцветного аморфного твердого вещества из (5-(2-аминопиридин-4-илокси)индол-1-ил)-(4-метилпиперазин-1-ил)метанона (0,66 г, 1,9 ммоль), фенилхлорформиата (0,52 мл, 4,2 ммоль) и триэтиламина (0,66 мл, 4,8 ммоль). Аналогично примеру 5 указанное в заголовке соединение (41 мг, 0,097 ммоль) получали в виде бесцветных кристаллов из промежуточного вещества, полученного выше (177 мг), этиламина гидрохлорида (0,122 г, 1,50 ммоль) и триэтиламина (0,5 мл).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,03 (3H, т, J=6,0 Гц), 2,21 (3H, с), 2,39 (4H, м), 3,12 (2H, м), 3,51 (4H, м), 6,51 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,4 Гц), 6,86 (1H, д, J=2,4 Гц), 7,04 (1H, дд, J=2,4, 8,8 Гц), 7,39 (1H, д, J=2,4 Гц), 7,61 (1H, д, J=3,4 Гц), 7,70 (1H, д, J=8,8 Гц), 8,02 (1H, м), 8,03 (1H, д, J=8,8 Гц), 9,00 (1H, с).
ESI-МС: 423,27 (M+H).
Исходные вещества синтезировали следующим образом.
Пример получения 178-1
Фенил(4-метилпиперазин-1-ил)карбоксилат
Аналогично примеру получения 2-1 кристаллы получали из 1-метилпиперазина (5,5 мл, 50 ммоль), фенилхлорформиата (6,9 мл, 55 ммоль) и пиридина (4,5 мл, 55 ммоль). Полученные кристаллы суспендировали в смеси диэтиловый эфир:гексан=2:1, отфильтровывали, промывали гексаном и сушили с получением указанного в заголовке соединения (9,7 г, 44 ммоль, 88%) в виде масла бледно-оранжевого цвета.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,20 (3H, с), 2,34 (4H, м), 3,40 (2H, м), 3,56 (2H, м), 7,09 (2H, д, J=7,6 Гц), 7,20 (1H, т, J=7,6 Гц), 7,36 (2H, т, J=7,6 Гц).
Пример получения 178-2
(5-(2-Аминопиридин-4-илокси)индол-1-ил)-(4-метилпиперазин-1-ил)метанон
Аналогично примеру получения 5-1 сырой продукт получали из 4-(1H-5-индолилокси)-2-пиридинамина (2,00 г, 8,88 ммоль, WO 02/32872), гидрида натрия (462 мг, 11,5 ммоль, 60% в масле) и фенил(4-метилпиперазин-1-ил)карбоксилата (2,35 г, 10,7 ммоль). Полученный сырой продукт очищали колоночной хроматографией на силикагеле (Fuji Silysia NH; смесь гексан:этилацетат=3:7, этилацетат, смесь этилацетат:метанол=9:1 в данном порядке) с получением указанного в заголовке соединения (0,66 г, 1,9 ммоль, 21%) в виде бесцветного аморфного твердого вещества.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,20 (3H, с), 2,39 (4H, м), 3,51 (4H, м), 5,75 (1H, д, J=2,0 Гц), 5,84 (2H, м), 6,13 (1H, дд, J=2,0, 6,0 Гц), 6,66 (1H, д, J=3,2 Гц), 7,02 (1H, дд, J=2,4, 8,8 Гц), 7,36 (1H, д, J=2,4 Гц), 7,59 (1H, д, J=3,2 Гц), 7,68 (1H, д, J=8,8 Гц), 7,76 (1H, д, J=6,0 Гц).
Пример 179
1-Этил-3-(4-(1-(морфолин-4-илкарбонил)-1H-индол-5-илокси)пиридин-2-ил)мочевина
Аналогично примеру получения 5-2 сырой продукт получали из 5-(2-аминопиридин-4-илокси)индол-1-ил)-(морфолин-4-ил)метанона (0,60 г, 1,8 ммоль), фенилхлорформиата (0,49 мл, 3,9 ммоль) и триэтиламина (0,62 мл, 4,4 ммоль). Полученный сырой продукт фильтровали через силикагель (Fuji Silysia BW-300, этилацетат) и концентрировали при пониженном давлении с получением смеси (1,11 г) фенил(4-(1-(морфолин-4-илкарбонил)-1H-индол-5-илокси)пиридин-2-ил)-N-(феноксикарбонил)карбамата и фенил(4-(1-(морфолин-4-илкарбонил)-1H-индол-5-илокси)пиридин-2-ил)карбамата в виде бледно-желтого масла. Аналогично примеру 5 указанное в заголовке соединение (73 мг, 0,178 ммоль) получали в виде бесцветных кристаллов из промежуточного вещества, полученного выше (173 мг), этиламина гидрохлорида (122 мг, 1,50 ммоль) и триэтиламина (0,5 мл).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,03 (3H, т, J=7,2 Гц), 3,07-3,14 (2H, м), 3,52 (4H, м), 3,68 (4H, м), 6,50 (1H, дд, J=2,4, 6,0 Гц), 6,68 (1H, д, J=3,2 Гц), 6,87 (1H, д, J=2,4 Гц), 7,05 (1H, дд, J=2,4, 8,8 Гц), 7,40 (1H, д, J=2,4 Гц), 7,64 (1H, д, J=3,2 Гц), 7,73 (1H, д, J=8,8 Гц), 8,00 (1H, м), 8,03 (1H, д, J=6,0 Гц), 9,01 (1H, с).
ESI-МС: 410,57 (M+H).
Исходные вещества синтезировали следующим образом.
Пример получения 179-1
Фенил(морфолин-4-ил)карбоксилат
Аналогично примеру получения 2-1 сырой продукт получали из морфолина (4,4 мл, 50 ммоль), фенилхлорформиата (6,9 мл, 55 ммоль) и пиридина (4,5 мл, 55 ммоль). Полученный сырой продукт очищали колоночной хроматографией на силикагеле (Fuji Silysia BW-300; смесь гексан:этилацетат=85:15, 60:40 в данном порядке) с получением указанного в заголовке соединения (8,9 г, 43 ммоль, 86%) в виде бесцветных кристаллов.
Спектр 1H-ЯМР (CDCl3) δ (м.д.): 3,57 (2H, уш.с), 3,68 (2H, уш.с), 3,75 (4H, м), 7,11 (2H, д, J=7,6 Гц), 7,21 (1H, т, J=7,6 Гц), 7,37 (2H, т, J=7,6 Гц).
Пример получения 179-2
(5-(2-Аминопиридин-4-илокси)индол-1-ил)-(морфолин-4-ил)метанон
Аналогично примеру получения 5-1 сырой продукт получали из 4-(1H-5-индолилокси)-2-пиридинамина (2,00 г, 8,88 ммоль, WO 02/32872), гидрида натрия (462 мг, 11,5 ммоль, 60% в масле) и фенил(морфолин-4-ил)карбоксилата (2,21 г, 10,7 ммоль). Полученный сырой продукт очищали колоночной хроматографией на силикагеле (Fuji Silysia NH, смесь гексан:этилацетат=2:3 или этилацетат) и дополнительно очищали колоночной хроматографией на силикагеле (Fuji Silysia BW-300, смесь гексан:этилацетат=2:3, этилацетат или смесь этилацетат:метанол=9:1) с получением указанного в заголовке соединения (0,60 г, 1,8 ммоль, 20%) в виде бесцветных кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 3,52 (4H, м), 3,68 (4H, м), 5,77 (1H, д, J=2,4 Гц), 5,83 (2H, уш.с), 6,13 (1H, дд, J=2,4, 5,6 Гц), 6,67 (1H, д, J=3,2 Гц), 7,02 (1H, дд, J=2,4, 8,8 Гц), 7,36 (1H, д, J=2,4 Гц), 7,61 (1H, д, J=3,2 Гц), 7,71 (1H, д, J=8,8 Гц), 7,76 (1H, д, J=5,6 Гц).
Пример 180
1,1-Диэтил-3-(4-(1-(морфолин-4-илкарбонил)-1H-индол-5-илокси)пиридин-2-ил)мочевина
Аналогично примеру 5 указанное в заголовке соединение (85 мг, 0,194 ммоль) получали в виде бесцветных кристаллов из смеси (173 мг) фенил(4-(1-(морфолин-4-илкарбонил)-1H-индол-5-илокси)пиридин-2-ил)-N-(феноксикарбонил)карбамата и фенил(4-(1-(морфолин-4-илкарбонил)-1H-индол-5-илокси)пиридин-2-ил)карбамата, синтезированного в виде промежуточного вещества в примере 179, и диэтиламина (0,16 мл, 1,50 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,01 (6H, т, J=6,8 Гц), 3,30 (4H, м), 3,53 (4H, м), 3,68 (4H, м), 6,54 (1H, д, J=6,0 Гц), 6,68 (1H, д, J=3,4 Гц), 7,05 (1H, дд, J=2,0, 8,8 Гц), 7,39 (1H, д, J=2,0 Гц), 7,43 (1H, с), 7,64 (1H, д, J=3,4 Гц), 7,73 (1H, д, J=8,8 Гц), 8,07 (1H, д, J=6,0 Гц), 8,62 (1H, с).
ESI-МС: 438,25 (M+H).
Пример 181
Пиперидин-4-иламид 5-(2-(3-этилуреидо)пиридин-4-илокси)индол-1-карбоновой кислоты
Аналогично примеру получения 5-1 сырой продукт трет-бутил-4-((5-(2-аминопиридин-4-илокси)индол-1-карбонил)амино)пиперидин-1-карбоксилат получали из 4-(1H-5-индолилокси)-2-пиридинамина (144 мг, 0,639 ммоль, WO 02/32872), гидрида натрия (29 мг, 0,735 ммоль, 60% в масле) и трет-бутил(4-феноксикарбониламинопиперидин-1-ил)карбоксилата (215 мг, 0,671 ммоль). Реакцию, сходную с примером получения 5-2, проводили с применением действительного количества данного сырого продукта, фенилхлорформиата (0,20 мл, 1,6 ммоль) и триэтиламина (0,22 мл); растворитель отгоняли при пониженном давлении после завершения реакции. Реакцию, сходную с примером 5, проводили с применением действительного количества остатка, этиламина гидрохлорида (260 мг, 3,92 ммоль) и триэтиламина (0,5 мл); органический слой подвергали распределению между этилацетатом и водой, промывали насыщенным раствором соли и сушили над безводным сульфатом натрия; растворитель отгоняли при пониженном давлении. Остаток растворяли в трифторацетате (3,0 мл); реакционную смесь перемешивали при комнатной температуре в течение 15 минут и концентрировали; остаток подвергали распределению между этилацетатом и водой. Органический слой промывали насыщенным раствором соли и сушили над безводным сульфатом натрия; растворитель отгоняли при пониженном давлении; остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia NH, смесь этилацетат:метанол=с 98:2 до 75:25). Полученные кристаллы суспендировали в диэтиловом эфире и отфильтровывали, промывали диэтиловым эфиром и сушили с получением указанного в заголовке соединения (43 мг, 0,10 ммоль, 16%) в виде бесцветных кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,02 (3H, т, J=7,2 Гц), 1,37-1,49 (2H, м), 1,80 (2H, м), 2,48 (2H, м), 2,95 (2H, м), 3,10 (2H, м), 3,71 (1H, м), 6,50 (1H, дд, J=2,4, 6,0 Гц), 6,66 (1H, д, J=3,4 Гц), 6,86 (1H, д, J=2,4 Гц), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,36 (1H, д, J=2,4 Гц), 7,90-8,01 (3H, м), 8,02 (1H, д, J=6,0 Гц), 8,26 (1H, д, J=8,8 Гц), 8,99 (1H, с).
ESI-МС: 423,26 (M+H).
Исходное вещество синтезировали следующим образом.
Пример получения 181-1
трет-Бутил(4-феноксикарбониламинопиперидин-1-ил)карбоксилат
Реакция аналогична реакции в примере получения 2-1 с применением трет-бутил-4-аминопиперидин-1-илкарбоксилата (328 мг, 1,64 ммоль), фенилхлорформиата (0,226 мл, 1,80 ммоль) и пиридина (0,146 мл, 1,80 ммоль); полученные кристаллы суспендировали в смеси гексан:этилацетат=4:1, отфильтровывали и фильтрат очищали колоночной хроматографией на силикагеле (Fuji Silysia BW-300, смесь гексан:этилацетат=4:1-1:1). Очищенные кристаллы затем суспендировали в смеси гексан:этилацетат=4:1 и отфильтровывали. Указанное в заголовке соединение (215 мг, 0,617 ммоль, 40,9%) получали в виде бесцветных кристаллов совместно с полученными ранее кристаллами.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,22-1,34 (2H, м), 1,38 (9H, с), 1,77 (2H, м), 2,83 (2H, м), 3,51 (1H, м), 3,84 (2H, м), 7,08 (2H, д, J=7,6 Гц), 7,18 (1H, т, J=7,6 Гц), 7,35 (2H, т, J=7,6 Гц), 7,78 (1H, д, J=8,0 Гц).
ESI-МС: 343,15 (M+Na).
Пример 182
(1-Метилпиперидин-4-ил)амид 5-(2-(3-этилуреидо)пиридин-4-илокси)индол-1-карбоновой кислоты
Пиперидин-4-иламид 5-(2-(3-этилуреидо)пиридин-4-илокси)индол-1-карбоновой кислоты (36 мг, 0,085 ммоль, пример 181) растворяли в тетрагидрофуране (2,0 мл) и метаноле (1,0 мл); туда добавляли 37% водный раствор формальдегида (0,036 мл, 0,43 ммоль) и уксусную кислоту (0,0098 мл, 0,17 ммоль). При перемешивании при комнатной температуре добавляли триацетоксиборогидрид натрия (27 мг, 0,13 ммоль) и реакционную смесь перемешивали в течение 30 минут. Реакционную смесь подвергали распределению между этилацетатом и насыщенным водным раствором бикарбоната натрия; органический слой промывали насыщенным раствором соли и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении; полученные кристаллы суспендировали в диэтиловом эфире, отфильтровывали, промывали диэтиловым эфиром и сушили с получением указанного в заголовке соединения (25 мг, 0,057 ммоль, 67%) в виде бесцветных кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,02 (3H, т, J=7,2 Гц), 1,54-1,68 (2H, м), 1,83 (2H, м), 1,96 (2H, м), 2,16 (3H, с), 2,78 (2H, м), 3,10 (2H, м), 3,64 (1H, м), 6,50 (1H, дд, J=2,4, 6,0 Гц), 6,66 (1H, д, J=3,6 Гц), 6,86 (1H, д, J=2,4 Гц), 7,03 (1H, дд, J=2,4, 8,8 Гц), 7,36 (1H, д, J=2,4 Гц), 7,95 (1H, д, J=3,6 Гц), 7,97 (2H, м), 8,02 (1H, д, J=6,0 Гц), 8,25 (1H, д, J=8,8 Гц), 8,99 (1H, м).
ESI-МС: 437,37 (M+H).
Пример 183
Метиламид 5-(2-(N-метил-(4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)индол-1-карбоновой кислоты
Метиламид 5-(2-(метиламино)пиридин-4-илокси)индол-1-карбоновой кислоты (70 мг, 0,24 ммоль) растворяли в тетрагидрофуране (7,0 мл); туда добавляли друг за другом триэтиламин (0,039 мл) и 4-нитрофенилхлорформиат (57 мг, 0,28 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 2 часов. Реакционную смесь подвергали распределению между этилацетатом и водой; органический слой промывали насыщенным водным раствором бикарбоната натрия и насыщенным раствором соли, затем сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток растворяли в N,N-диметилформамиде (2,0 мл); туда добавляли 4-(пирролидин-1-ил)пиперидин (43 мг, 0,28 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 24 часов. Реакционную смесь подвергали распределению между этилацетатом и водой и органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia NH, система гексан-этилацетат-метанол); отверждение полученного масла вызывали гексаном; полученное твердое вещество затем суспендировали в гексане, отфильтровывали, промывали гексаном и сушили с получением указанного в заголовке соединения (51 мг, 0,11 ммоль, 45%) в виде бледно-желтых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,13-1,30 (2H, м), 1,65 (6H, м), 2,02 (1H, м), 2,42 (4H, м), 2,72 (2H, м), 2,83 (3H, д, J=4,0 Гц), 3,08 (3H, с), 3,53 (2H, м), 6,23 (1H, с), 6,51 (1H, д, J=6,0 Гц), 6,66 (1H, д, J=3,4 Гц), 7,04 (1H, д, J=9,0 Гц), 7,36 (1H, с), 7,87 (1H, д, J=3,4 Гц), 8,11 (1H, д, J=6,0 Гц), 8,15 (1H, м), 8,29 (1H, д, J=9,0 Гц).
ESI-МС: 477,38 (M+H).
Исходное вещество синтезировали следующим образом.
Пример получения 183-1
Метиламид 5-(2-(метиламино)пиридин-4-илокси)индол-1-карбоновой кислоты
N1-Метил-5-(2-аминопиридин-4-ил)окси-1H-1-индолкарбоксамид (5,00 г, 17,7 ммоль, пример получения 5-1) растворяли в этаноле (170 мл) и N,N-диметилформамиде (40 мл); туда добавляли 1H-бензотриазол-1-метанол (2,64 г, 17,7 ммоль) и реакционную смесь нагревали до температуры кипения с обратным холодильником в течение 2 часов. После остывания до комнатной температуры к реакционной смеси добавляли борогидрид натрия (1,49 г, 35,4 ммоль); реакционную смесь перемешивали при комнатной температуре в течение 2 часов. Реакционную смесь подвергали распределению между этилацетатом и водой; органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia BW-300, система гексан-этилацетат-метанол). Полученные кристаллы суспендировали в смеси ацетон:диэтиловый эфир=1:3, отфильтровывали, промывали гексаном и сушили с получением указанного в заголовке соединения (1,05 г, 3,55 ммоль, 20,1%) в виде бледно-желтых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,66 (3H, д, J=4,8 Гц), 2,82 (3H, д, J=4,0 Гц), 5,76 (1H, д, J=2,0 Гц), 6,10 (1H, дд, J=2,0, 6,0 Гц), 6,36 (1H, м), 6,65 (1H, д, J=4,0 Гц), 7,00 (1H, дд, J=2,4, 8,8 Гц), 7,31 (1H, д, J=2,4 Гц), 7,83 (2H, м), 8,13 (1H, м), 8,26 (1H, д, J=8,8 Гц).
Пример 184
Метиламид 5-(2-(1-метилуреидо)пиридин-4-илокси)индол-1-карбоновой кислоты
4-Нитрофенил-N-метил-(4-(1-метилкарбамоилиндол-5-илокси)пиридин-2-ил)карбамат (105 мг, 0,228 ммоль) растворяли в N,N-диметилформамиде (2,5 мл); туда добавляли водный аммиак (0,5 мл, 28,0%); реакционную смесь перемешивали при комнатной температуре в течение 10,5 часов. Реакционную смесь подвергали распределению между этилацетатом и водой; органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Полученные кристаллы суспендировали в смеси этанол:диэтиловый эфир=1:1 (6 мл), отфильтровывали, промывали диэтиловым эфиром и сушили с получением указанного в заголовке соединения (37 мг, 0,11 ммоль, 48%) в виде бледно-желтых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,83 (3H, д, J=4,0 Гц), 3,19 (3H, с), 6,51 (1H, д, J=5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 6,84 (1H, с), 7,07 (1H, д, J=9,0 Гц), 7,39 (1H, с), 7,87 (1H, д, J=3,6 Гц), 8,14 (2H, м), 8,29 (1H, д, J=9,0 Гц).
ESI-МС: 340,07 (M+H).
Исходное вещество синтезировали следующим образом.
Пример получения 184-1
4-Нитрофенил-N-метил-(4-(1-метилкарбамоилиндол-5-илокси)пиридин-2-ил)карбамат
Метиламид 5-(2-(метиламино)пиридин-4-илокси)индол-1-карбоновой кислоты (200 мг, 0,675 ммоль), синтезированный в примере получения 183-1, растворяли в тетрагидрофуране (20 мл); туда добавляли друг за другом триэтиламин (0,100 мл, 0,742 ммоль) и 4-нитрофенилхлорформиат (150 мг, 0,742 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 2 часов. Реакционную смесь подвергали распределению между этилацетатом и водой; органический слой промывали насыщенным водным раствором бикарбоната натрия и насыщенным раствором соли, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia BW-300, система гексан-этилацетат) с получением указанного в заголовке соединения (210 мг, 0,455 ммоль, 67,4%) в виде бледно-желтого масла.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,82 (3H, д, J=4,4 Гц), 3,46 (3H, с), 6,62 (1H, д, J=3,6 Гц), 6,83 (1H, дд, J=2,0, 5,6 Гц), 7,03 (1H, дд, J=2,0, 8,4 Гц), 7,24 (1H, д, J=2,0 Гц), 7,37 (1H, д, J=2,0 Гц), 7,41 (2H, д, J=9,2 Гц), 7,85 (1H, д, J=3,6 Гц), 8,14 (1H, м), 8,22 (2H, д, J=9,2 Гц), 8,23 (1H, д, J=8,4 Гц), 8,32 (1H, д, J=5,6 Гц).
Пример 185
Метиламид 5-(2-(3,3-диэтил-1-метилуреидо)пиридин-4-илокси)индол-1-карбоновой кислоты
Аналогично примеру 184 указанное в заголовке соединение (14 мг, 0,035 ммоль, 16%) получали в виде бесцветного аморфного твердого вещества из 4-нитрофенил-N-метил-(4-(1-метилкарбамоилиндол-5-илокси)пиридин-2-ил)карбамата (105 мг, 0,228 ммоль, пример получения 184-1) и диэтиламина (0,028 мл, 0,27 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,80 (6H, т, J=6,4 Гц), 2,83 (3H, д, J=3,2 Гц), 3,03 (3H, с), 3,07 (4H, м), 6,11 (1H, с), 6,49 (1H, м), 6,66 (1H, с), 7,02 (1H, д, J=9,0 Гц), 7,35 (1H, с), 7,86 (1H, с), 8,09 (1H, д, J=5,6 Гц), 8,15 (1H, м), 8,28 (1H, д, J=9,0 Гц).
ESI-МС: 396,18 (M+H).
Пример 186
Метиламид 5-(2-(3-этил-1-метилуреидо)пиридин-4-илокси)индол-1-карбоновой кислоты
Аналогично примеру получения 27-2 фенил N-метил-(4-(1-метилкарбамоилиндол-5-илокси)пиридин-2-ил)карбамат (324 мг, 0,778 ммоль) получали в виде бесцветного аморфного твердого вещества из метиламида 5-(2-(метиламино)пиридин-4-илокси)индол-1-карбоновой кислоты (500 мг, 1,69 ммоль), фенилхлорформиата (0,23 мл, 1,9 ммоль) и триэтиламина (0,26 мл, 1,9 ммоль). Данное промежуточное вещество (125 мг, 0,300 ммоль) растворяли в N,N-диметилформамиде (2,5 мл) - триэтиламине (0,5 мл); туда добавляли этиламина гидрохлорид (122 мг, 1,50 ммоль); реакционную смесь перемешивали при комнатной температуре в течение ночи и затем перемешивали при 80°С в течение 1,5 часов. Туда добавляли этиламина гидрохлорид (122 мг, 1,50 ммоль); реакционную смесь перемешивали при 80°С в течение 2 часов; туда дополнительно добавляли этиламина гидрохлорид (122 мг, 1,50 ммоль) и триэтиламин (0,5 мл); реакционную смесь перемешивали при 80°С в течение 0,5 часов и затем перемешивали при комнатной температуре в течение 2 дней. Реакционную смесь подвергали распределению между этилацетатом (100 мл) и водой (50 мл); органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia BW-300, смесь гексан:этилацетат=3:2, затем этилацетат); полученные кристаллы суспендировали в смеси диэтиловый эфир (10 мл) - гексан (50 мл), отфильтровывали и сушили с получением указанного в заголовке соединения (41 мг, 0,11 ммоль) в виде бесцветных кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,04 (3H, т, J=7,2 Гц), 2,83 (3H, д, J=4,4 Гц), 3,15 (2H, м), 3,19 (3H, с), 6,51 (1H, дд, J=2,4, 6,6 Гц), 6,67 (1H, д, J=4,0 Гц), 6,77 (1H, д, J=2,4 Гц), 7,07 (1H, дд, J=2,4, 8,8 Гц), 7,39 (1H, д, J=2,4 Гц), 7,87 (1H, д, J=4,0 Гц), 8,15 (1H, д, J=6,0 Гц), 8,16 (1H, м), 8,29 (1H, д, J=8,8 Гц), 9,27 (1H, м).
ESI-МС: 368,13 (M+H).
Пример 187
Метиламид 6-(2-(3-этилуреидо)пиридин-4-илокси)индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (54 мг, 0,15 ммоль, 80%) получали в виде бесцветных кристаллов из фенил(4-(1-метилкарбамоил-1H-индол-6-илокси)пиридин-2-ил)-N-(феноксикарбонил)карбамата (100 мг, 0,19 ммоль), этиламина гидрохлорида (78 мг, 0,96 ммоль) и триэтиламина (0,5 мл).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,03 (3H, т, J=7,2 Гц), 2,79 (3H, д, J=4,4 Гц), 3,07-3,14 (2H, м), 6,52 (1H, дд, J=2,4, 5,8 Гц), 6,71 (1H, д, J=3,6 Гц), 6,88 (1H, д, J=2,4 Гц), 6,99 (1H, дд, J=2,4, 8,4 Гц), 7,65 (1H, д, J=8,4 Гц), 7,84 (1H, д, J=3,6 Гц), 7,96 (2H, м), 8,04 (1H, д, J=5,8 Гц), 8,16 (1H, м), 9,02 (1H, с).
ESI-МС: 354,15 (M+H), 376,16 (M+Na).
Исходные вещества синтезировали следующим образом.
Пример получения 187-1
4-(1H-Индол-6-илокси)пиридин-2-иламин
Гидрид натрия (1,04 г, 26,0 ммоль, 60% в масле) суспендировали в диметилсульфоксиде (2,5 мл); туда последовательно добавляли при комнатной температуре под струей азота 6-гидроксииндол (3,46 г, 26,0 ммоль) и 2-амино-4-хлорпиридин (2,57 г, 20,0 ммоль, WO 02/332872) и реакционную смесь перемешивали при 160°С в течение 8,5 часов. После остывания до комнатной температуры реакционную смесь подвергали распределению между этилацетатом (150 мл) и смесью растворителей - водный аммиак:вода=1:1 (50 мл); органический слой промывали смесью растворителей - водный аммиак:вода=1:1 и насыщенным раствором соли, сушили над безводным сульфатом натрия и концентрировали. Остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia BW-300, этилацетат или смесь этилацетат:метанол=93:7); полученные кристаллы суспендировали в диэтиловом эфире, отфильтровывали, промывали диэтиловым эфиром и сушили с получением указанного в заголовке соединения (477 мг, 2,12 ммоль, 10,6%) в виде бледно-желтых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 5,76 (1H, с), 5,82 (2H, уш.с), 6,13 (1H, д, J=6,0 Гц), 6,44 (1H, с), 6,75 (1H, д, J=8,4 Гц), 7,10 (1H, с), 7,34 (1H, с), 7,56 (1H, д, J=8,4 Гц), 7,75 (1H, д, J=6,0 Гц), 11,12 (1H, уш.с).
Пример получения 187-2
Метиламид 6-(2-аминопиридин-4-илокси)индол-1-карбоновой кислоты
Аналогично примеру получения 5-1 указанное в заголовке соединение (315 мг, 1,12 ммоль, 87,9%) получали в виде бесцветных кристаллов из 4-(1H-индол-6-илокси)пиридин-2-иламина (285 мг, 1,27 ммоль), гидрида натрия (63 мг, 1,58 ммоль, 60% в масле) и фенил-N-метилкарбамата (239 мг, 1,58 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,80 (3H, д, J=4,4 Гц), 5,77 (1H, д, J=2,0 Гц), 5,85 (2H, м), 6,14 (1H, дд, J=2,0, 5,6 Гц), 6,69 (1H, д, J=3,6 Гц), 6,96 (1H, дд, J=2,0, 8,4 Гц), 7,63 (1H, д, J=8,4 Гц), 7,77 (1H, д, J=5,6 Гц), 7,81 (1H, д, J=3,6 Гц), 7,94 (1H, д, J=2,0 Гц), 8,13 (1H, д, J=4,4 Гц).
Пример получения 187-3
Фенил-(4-(1-метилкарбамоил-1H-индол-6-илокси)пиридин-2-ил)-N-(феноксикарбонил)карбамат
Аналогично примеру получения 5-2 указанное в заголовке соединение (404 мг, 0,77 ммоль, 69%) получали в виде бледно-розовых кристаллов из метиламида 6-(2-аминопиридин-4-илокси)индол-1-карбоновой кислоты (315 мг, 1,12 ммоль), триэтиламина (0,51 мл, 3,7 ммоль) и фенилхлорформиата (0,42 мл, 3,4 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,78 (3H, д, J=4,4 Гц), 6,74 (1H, д, J=3,6 Гц), 7,02 (1H, дд, J=2,4, 5,6 Гц), 7,05 (1H, дд, J=2,4, 8,4 Гц), 7,16 (4H, д, J=7,8 Гц), 7,29 (2H, т, J=7,8 Гц), 7,42 (4H, т, J=7,8 Гц), 7,52 (1H, м), 7,69 (1H, д, J=8,4 Гц), 7,86 (1H, д, J=3,6 Гц), 8,04 (1H, д, J=2,4 Гц), 8,15 (1H, м), 8,44 (1H, д, J=5,6 Гц).
Пример 188
Метиламид 6-(2-(3,3-диэтилуреидо)пиридин-4-илокси)индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (55 мг, 0,14 ммоль, 76%) получали в виде бесцветных кристаллов из фенил(4-(1-метилкарбамоил-1H-индол-6-илокси)пиридин-2-ил)-N-(феноксикарбонил)карбамата (100 мг, 0,19 ммоль) и диэтиламина (0,10 мл, 0,96 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,01 (6H, т, J=7,2 Гц), 2,79 (3H, д, J=4,4 Гц), 3,26-3,32 (4H, м), 6,56 (1H, дд, J=2,0, 5,6 Гц), 6,71 (1H, д, J=3,6 Гц), 6,99 (1H, дд, J=2,0, 8,8 Гц), 7,42 (1H, д, J=2,0 Гц), 7,65 (1H, д, J=8,8 Гц), 7,84 (1H, д, J=3,6 Гц), 7,96 (1H, д, J=2,0 Гц), 8,08 (1H, д, J=5,6 Гц), 8,15 (1H, м), 8,63 (1H, с).
ESI-МС: 382,21 (M+H).
Пример 189
Метиламид 6-(2-(3-(2-диэтиламиноэтил)уреидо)пиридин-4-илокси)индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (51 мг, 0,12 ммоль, 63%) получали в виде бледно-желтых кристаллов из фенил(4-(1-метилкарбамоил-1H-индол-6-илокси)пиридин-2-ил)-N-(феноксикарбонил)карбамата (100 мг, 0,19 ммоль) и 2-диэтиламиноэтиламина (0,14 мл, 0,96 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,93 (6H, т, J=7,6 Гц), 2,41-2,49 (6H, м), 2,79 (3H, д, J=4,0 Гц), 3,14 (2H, м), 6,51 (1H, дд, J=2,4, 6,0 Гц), 6,71 (1H, д, J=3,6 Гц), 6,84 (1H, д, J=2,4 Гц), 6,99 (1H, дд, J=2,4, 8,2 Гц), 7,65 (1H, д, J=8,2 Гц), 7,84 (1H, д, J=3,6 Гц), 7,96 (1H, д, J=2,4 Гц), 8,02 (1H, д, J=6,0 Гц), 8,16 (2H, м), 9,13 (1H, с).
ESI-МС: 425,29 (M+H).
Пример 190
Метиламид 6-(2-(((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (72 мг, 0,16 ммоль, 82%) получали в виде бесцветных кристаллов из фенил(4-(1-метилкарбамоил-1H-индол-6-илокси)пиридин-2-ил)-N-(феноксикарбонил)карбамата (100 мг, 0,19 ммоль) и 4-(пирролидин-1-ил)пиперидина (148 мг, 0,96 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,19-1,31 (2H, м), 1,63 (4H, м), 1,76 (2H, м), 2,09 (1H, м), 2,44 (4H, м), 2,79 (3H, д, J=4,0 Гц), 2,82 (2H, м), 3,92 (2H, м), 6,55 (1H, дд, J=2,4, 5,6 Гц), 6,71 (1H, д, J=3,8 Гц), 6,98 (1H, дд, J=2,4, 8,8 Гц), 7,32 (1H, д, J=2,4 Гц), 7,65 (1H, д, J=8,8 Гц), 7,84 (1H, д, J=3,8 Гц), 7,96 (1H, д, J=2,4 Гц), 8,08 (1H, д, J=5,6 Гц), 8,15 (1H, м), 9,12 (1H, с).
ESI-МС: 436,32 (M+H).
Пример 191
Метиламид 6-(6-(3-этилуреидо)пиримидин-4-илокси)индол-1-карбоновой кислоты
Аналогично примеру получения 5-2 промежуточное вещество, фенил(4-(1-метилкарбамоил-1H-индол-6-илокси)пиримидин-6-ил)-N-(феноксикарбонил)карбамат, получали в виде бледно-желтых кристаллов (597 мг) из метиламида 6-(6-аминопиримидин-4-илокси)индол-1-карбоновой кислоты (245 мг, 0,865 ммоль), триэтиламина (0,40 мл, 2,9 ммоль) и фенилхлорформиата (0,33 мл, 2,6 ммоль). Аналогично примеру 5 указанное в заголовке соединение (43 мг, 0,12 ммоль) получали в виде бесцветных кристаллов из данного промежуточного вещества (143 мг), этиламина гидрохлорида (88 мг, 1,1 ммоль) и триэтиламина (0,5 мл).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,03 (3H, т, J=6,8 Гц), 2,80 (3H, с), 3,10 (2H, м), 6,71 (1H, с), 6,99 (1H, д, J=8,4 Гц), 7,01 (1H, с), 7,04 (1H, м), 7,62 (1H, д, J=8,4 Гц), 7,84 (1H, с), 7,98 (1H, с), 8,16 (1H, м), 8,36 (1H, с), 9,45 (1H, с).
ESI-МС: 355,27 (M+H), 377,26 (M+Na).
Исходное вещество синтезировали следующим образом.
Пример получения 191-1
6-(1H-Индол-6-илокси)пиримидин-4-иламин
Гидрид натрия (200 мг, 5,00 ммоль) суспендировали в диметилсульфоксиде (8 мл); при перемешивании при комнатной температуре туда добавляли друг за другом 6-гидроксииндол (666 мг, 5,00 ммоль) и 6-амино-4-хлорпиримидин (518 мг, 4,00 ммоль); реакционную смесь перемешивали при 60°С в течение 2 часов, при 80°С в течение 1 часа и при 100°С в течение 1,5 часов. После остывания до комнатной температуры реакционную смесь подвергали распределению между этилацетатом и водой; органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом натрия и концентрировали. Остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia BW-300, смесь гексан:этилацетат=1:1, этилацетат, затем смесь этилацетат:метанол=98:2); полученные кристаллы суспендировали в этилацетате (50 мл) и перемешивали при комнатной температуре в течение ночи, отфильтровывали, промывали диэтиловым эфиром и сушили с получением указанного в заголовке соединения (322 мг, 1,42 ммоль, 35,6%) в виде бледно-желтых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 5,56 (1H, с), 6,44 (1H, с), 6,72 (2H, с), 6,76 (1H, д, J=8,4 Гц), 7,12 (1H, с), 7,34 (1H, с), 7,55 (1H, д, J=8,4 Гц), 8,05 (1H, с), 11,13 (1H, уш.с).
Пример получения 191-2
Метиламид 6-(6-аминопиримидин-4-илокси)индол-1-карбоновой кислоты
Аналогично примеру получения 5-1 указанное в заголовке соединение (245 мг, 0,865 ммоль, 61,3%) получали в виде бесцветных кристаллов из 6-(1H-индол-6-илокси)пиримидин-4-иламина (320 мг, 1,41 ммоль), гидрида натрия (68 мг, 1,7 ммоль, 60% в масле) и фенил-N-метилкарбамата (257 мг, 1,70 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,80 (3H, д, J=4,4 Гц), 5,64 (1H, с), 6,69 (1H, д, J=3,6 Гц), 6,77 (2H, с), 6,96 (1H, дд, J=2,0, 8,4 Гц), 7,61 (1H, д, J=8,4 Гц), 7,81 (1H, д, J=3,6 Гц), 7,94 (1H, д, J=2,0 Гц), 8,05 (1H, с), 8,12 (1H, м).
Пример 192
Метиламид 6-(6-(3,3-диэтилуреидо)пиримидин-4-илокси)индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (63 мг, 0,16 ммоль) получали в виде молочно-белых кристаллов из промежуточного вещества, полученного в примере 191 (149 мг), и диэтиламина (0,11 мл, 1,1 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,03 (6H, т, J=7,2 Гц), 2,80 (3H, д, J=4,4 Гц), 3,33 (4H, кв, J=7,2 Гц), 6,71 (1H, д, J=3,8 Гц), 7,00 (1H, дд, J=2,0, 8,4 Гц), 7,31 (1H, с), 7,62 (1H, д, J=8,4 Гц), 7,83 (1H, д, J=3,8 Гц), 7,98 (1H, д, J=2,0 Гц), 8,15 (1H, м), 8,38 (1H, с), 9,31 (1H, с).
ESI-МС: 383,23 (M+H), 405,26 (M+Na).
Пример 193
Метиламид 6-(6-(3-(2-диэтиламиноэтил)уреидо)пиримидин-4-илокси)индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (63 мг, 0,15 ммоль) получали в виде серовато-белых кристаллов из промежуточного вещества, полученного в примере 191 (164 мг), и 2-диэтиламиноэтиламина (0,15 мл, 1,1 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,93 (6H, т, J=7,0 Гц), 2,44 (6H, м), 2,80 (3H, д, J=4,0 Гц), 3,13 (2H, м), 6,70 (1H, д, J=3,6 Гц), 6,90 (2H, м), 7,43 (1H, уш.с), 7,62 (1H, д, J=8,4 Гц), 7,83 (1H, д, J=3,6 Гц), 7,98 (1H, д, J=1,6 Гц), 8,15 (1H, м), 8,34 (1H, с), 9,63 (1H, с).
ESI-МС: 426,31 (M+H).
Пример 194
Метиламид 6-(6-(((4-пирролидин-1-ил)пиперидин-1-илкарбонил)амино)пиримидин-4-илокси)индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (59 мг, 0,13 ммоль) получали в виде бесцветных кристаллов из промежуточного вещества, полученного в примере 191 (141 мг), и 4-(пирролидин-1-ил)пиперидина (167 мг, 1,08 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,22-1,34 (2H, м), 1,64 (4H, м), 1,78 (2H, м), 2,12 (1H, м), 2,44 (4H, м), 2,80 (3H, д, J=4,0 Гц), 2,88 (2H, м), 3,93 (2H, м), 6,70 (1H, д, J=3,6 Гц), 6,99 (1H, дд, J=2,0, 8,4 Гц), 7,20 (1H, с), 7,62 (1H, д, J=8,4 Гц), 7,83 (1H, д, J=3,6 Гц), 7,97 (1H, д, J=2,0 Гц), 8,15 (1H, м), 8,38 (1H, с), 9,73 (1H, с).
ESI-МС: 464,36 (M+H).
Пример 195
Метиламид 4-(6-(3-этилуреидо)пиримидин-4-илокси)индол-1-карбоновой кислоты
Аналогично примеру получения 5-2 промежуточное вещество (смесь фенил(4-(1-метилкарбамоил-1H-индол-4-илокси)пиримидин-6-ил)-N-(феноксикарбонил)карбамата и фенил(4-(1-метилкарбамоил-1H-индол-4-илокси)пиримидин-6-ил)карбамата, 379 мг) получали в виде бледно-желтых кристаллов из метиламида 4-(6-аминопиримидин-4-илокси)индол-1-карбоновой кислоты (245 мг, 0,865 ммоль), триэтиламина (0,40 мл, 2,9 ммоль) и фенилхлорформиата (0,33 мл, 2,6 ммоль). Аналогично примеру 5 указанное в заголовке соединение (41 мг, 0,12 ммоль) получали в виде бесцветного кристалла из данного промежуточного вещества (94 мг), этиламина гидрохлорида (78 мг, 0,96 ммоль) и триэтиламина (0,5 мл).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,03 (3H, т, J=7,4 Гц), 2,82 (3H, д, J=4,0 Гц), 3,12 (2H, м), 6,40 (1H, д, J=3,8 Гц), 6,98 (1H, д, J=8,0 Гц), 7,05 (1H, с), 7,28 (1H, т, J=8,0 Гц), 7,31 (1H, м), 7,76 (1H, д, J=3,8 Гц), 8,14 (1H, д, J=8,0 Гц), 8,17 (1H, м), 8,33 (1H, м), 9,48 (1H, с).
ESI-МС: 355,20 (M+H), 377,25 (M+Na).
Исходные вещества синтезировали следующим образом.
Пример получения 195-1
6-(1H-Индол-4-илокси)пиримидин-4-иламин
Указанное в заголовке соединение (568 мг, 2,51 ммоль, 41,8%) получали в виде серовато-белых кристаллов путем проведения реакции, аналогичной реакции в примере получения 191-1, с применением 6-амино-4-хлорпиримидина (777 мг, 6,00 ммоль), 4-гидроксииндола (999 мг, 7,50 ммоль) и гидрида натрия (300 мг, 7,50 ммоль) при 100°С в течение 6 часов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 5,56 (1H, с), 6,13 (1H, м), 6,70 (2H, уш.с), 6,74 (1H, д, J=8,0 Гц), 7,09 (1H, т, J=8,0 Гц), 7,29 (2H, м), 8,05 (1H, с), 11,28 (1H, с).
Пример получения 195-2
Метиламид 4-(6-аминопиримидин-4-илокси)индол-1-карбоновой кислоты
Аналогично примеру получения 5-1 указанное в заголовке соединение (279 мг, 0,985 ммоль, 74,0%) получали в виде бесцветных кристаллов из 6-(1H-индол-4-илокси)пиримидин-4-иламина (300 мг, 1,33 ммоль), гидрида натрия (83 мг, 2,1 ммоль, 60% в масле) и фенил-N-метилкарбамата (314 мг, 2,07 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,82 (3H, д, J=4,4 Гц), 5,64 (1H, с), 6,39 (1H, д, J=3,6 Гц), 6,77 (2H, уш.с), 6,94 (1H, д, J=8,0 Гц), 7,27 (1H, т, J=8,0 Гц), 7,75 (1H, д, J=3,6 Гц), 8,04 (1H, с), 8,12 (1H, д, J=8,0 Гц), 8,15 (1H, м).
Пример 196
Метиламид 4-(6-(3,3-диэтилуреидо)пиримидин-4-илокси)индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (54 мг, 0,14 ммоль) получали в виде бесцветных кристаллов из промежуточного вещества, полученного в примере 195 (94 мг), и диэтиламина (0,10 мл, 0,96 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,04 (6H, т, J=6,8 Гц), 2,82 (3H, д, J=4,0 Гц), 3,34 (4H, кв, J=6,8 Гц), 6,41 (1H, д, J=3,8 Гц), 6,98 (1H, д, J=8,0 Гц), 7,28 (1H, т, J=8,0 Гц), 7,36 (1H, с), 7,76 (1H, д, J=3,8 Гц), 8,14 (1H, д, J=8,0 Гц), 8,17 (1H, м), 8,35 (1H, с), 9,34 (1H, с).
ESI-МС: 383,31 (M+H), 405,22 (M+Na).
Пример 197
Метиламид 4-(6-(3-(2-диэтиламиноэтил)уреидо)пиримидин-4-илокси)индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (49 мг, 0,12 ммоль) получали в виде бесцветных кристаллов из промежуточного вещества, полученного в примере 195 (94 мг), и 2-диэтиламиноэтиламина (0,14 мл, 0,96 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,93 (6H, т, J=7,0 Гц), 2,45 (6H, м), 2,82 (3H, д, J=4,0 Гц), 3,14 (2H, м), 6,40 (1H, д, J=3,4 Гц), 6,98 (1H, д, J=8,0 Гц), 7,04 (1H, с), 7,28 (1H, т, J=8,0 Гц), 7,45 (1H, м), 7,76 (1H, д, J=3,4 Гц), 8,14 (1H, д, J=8,0 Гц), 8,17 (1H, м), 8,32 (1H, с), 8,65 (1H, уш.с).
ESI-МС: 426,27 (M+H).
Пример 198
Метиламид 4-(6-(((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)амино)пиримидин-4-илокси)индол-1-карбоновой кислоты
Аналогично примеру 5 указанное в заголовке соединение (57 мг, 0,12 ммоль) получали в виде бесцветных кристаллов из промежуточного вещества, полученного в примере 195 (94 мг), и 4-(пирролидин-1-ил)пиперидина (148 мг, 0,96 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,22-1,35 (2H, м), 1,64 (4H, м), 1,78 (2H, м), 2,13 (1H, м), 2,45 (4H, м), 2,82 (3H, д, J=3,2 Гц), 2,89 (2H, м), 3,94 (2H, м), 6,40 (1H, м), 6,98 (1H, д, J=8,0 Гц), 7,26 (1H, с), 7,28 (1H, т, J=8,0 Гц), 7,76 (1H, м), 8,13 (1H, д, J=8,0 Гц), 8,16 (1H, м), 8,35 (1H, с), 9,35 (1H, с).
ESI-МС: 464,35 (M+H).
Пример 199
Метиламид 5-(2-(3-(3-диэтиламинопропил)уреидо)пиридин-4-иламино)индол-1-карбоновой кислоты
1-(4-Хлорпиридин-2-ил)-3-(3-диэтиламинопропил)мочевину (30 мг, 0,11 ммоль) растворяли в этоксиэтаноле (1,1 мл); туда добавляли пиридингидрохлорид (24 мг, 0,22 ммоль) и метиламид 5-аминоиндол-1-карбоновой кислоты (22 мг, 0,12 ммоль, пример получения 218-2) и реакционную смесь перемешивали при 130°С в течение 2 часов. После остывания до комнатной температуры реакционную смесь подвергали распределению между насыщенным водным раствором бикарбоната натрия и этилацетатом; органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia NH, смесь гексан:этилацетат=1:3, этилацетат, смесь этилацетат:метанол=93:7 в данном порядке) с получением указанного в заголовке соединения (8 мг, 0,018 ммоль, 17%) в виде бледно-желтого порошка.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,94 (6H, т, J=6,8 Гц), 1,54 (2H, м), 2,37-2,46 (6H, м), 2,83 (3H, д, J=3,6 Гц), 3,16 (2H, м), 6,42 (1H, д, J=5,8 Гц), 6,63 (1H, д, J=3,2 Гц), 6,73 (1H, с), 7,07 (1H, д, J=8,8 Гц), 7,37 (1H, с), 7,76 (1H, д, J=5,8 Гц), 7,80 (1H, м), 8,08 (1H, м), 8,19 (1H, д, J=8,8 Гц), 8,66 (1H, с), 8,81 (1H, м), 8,86 (1H, с).
ESI-MS: 438,36 (M+H).
Исходные вещества синтезировали следующим образом.
Пример получения 199-1
Фенил(4-хлорпиридин-2-ил)-N-(феноксикарбонил)карбамат
2-Амино-4-хлорпиридин (5,00 г, 38,9 ммоль, WO 02/32872) растворяли в тетрагидрофуране (200 мл) и туда добавляли триэтиламин (17,9 мл, 128 ммоль). При перемешивании в водяной бане туда по каплям добавляли фенилхлорформиат (14,6 мл, 117 ммоль); реакционную смесь перемешивали при комнатной температуре в течение 1,5 часов. Реакционную смесь подвергали распределению между водой и этилацетатом; органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Полученный остаток фильтровали через силикагель; кристаллы, полученные после концентрирования, суспендировали в диэтиловом эфире, отфильтровывали, промывали диэтиловым эфиром и сушили с получением указанного в заголовке соединения (3,77 г, 10,2 ммоль, 26,3%) в виде бледно-желтых кристаллов. Маточную жидкость концентрировали при пониженном давлении, затем обрабатывали сходными способами с получением указанного в заголовке соединения (3,98 г, 10,5 ммоль, 27,1%) в виде бледно-желтых кристаллов (вторичные кристаллы).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 7,20 (4H, д, J=7,6 Гц), 7,30 (2H, т, J=7,6 Гц), 7,44 (4H, т, J=7,6 Гц), 7,68 (1H, дд, J=1,6, 5,2 Гц), 8,21 (1H, д, J=1,6 Гц), 8,60 (1H, д, J=5,2 Гц).
Пример получения 199-2
1-(4-Хлорпиридин-2-ил)-3-(3-диэтиламинопропил)мочевина
Фенил(4-хлорпиридин-2-ил)-N-(феноксикарбонил)карбамат (738 мг, 2,00 ммоль) растворяли в N,N-диметилформамиде (8,0 мл); туда добавляли N,N-диэтил-1,3-диаминопропан (1,57 мл, 10,0 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 1 часа. Реакционную смесь подвергали распределению между водой и этилацетатом; органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia NH, система гексан-этилацетат-метанол) с получением указанного в заголовке соединения (309 мг, 1,09 ммоль, 54,3%) в виде бледно-коричневого масла.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,92 (6H, т, J=7,0 Гц), 1,54 (2H, м), 2,35-2,44 (6H, м), 3,16 (2H, м), 7,02 (1H, д, J=5,6 Гц), 7,54 (1H, с), 7,73 (1H, уш.с), 8,13 (1H, д, J=5,6 Гц), 9,31 (1H, м).
Пример 200
Метиламид 5-(N-(2-(3-(3-диэтиламинопропил)уреидо)пиридин-4-ил)-N-метиламино)индол-1-карбоновой кислоты
Аналогично примеру 199 указанное в заголовке соединение (6 мг, 0,013 ммоль, 12%) получали в виде бледно-желтого порошка из метиламида 5-(N-метиламино)индол-1-карбоновой кислоты (22 мг, 0,11 ммоль), 1-(4-хлорпиридин-2-ил)-3-(3-диэтиламинопропил)мочевины (30 мг, 0,11 ммоль, пример получения 199-2) и пиридина гидрохлорида (25 мг, 0,22 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,91 (6H, т, J=7,0 Гц), 1,51 (2H, м), 2,34-2,43 (6H, м), 2,83 (3H, д, J=4,0 Гц), 3,13 (2H, м), 3,23 (3H, с), 6,11 (1H, д, J=6,0 Гц), 6,40 (1H, с), 6,70 (1H, д, J=3,6 Гц), 7,10 (1H, д, J=8,6 Гц), 7,44 (1H, с), 7,69 (1H, д, J=6,0 Гц), 7,84 (1H, д, J=3,6 Гц), 8,14 (1H, м), 8,27 (1H, д, J=8,6 Гц), 8,76 (1H, с), 8,78 (1H, уш.с).
ESI-МС: 452,38 (M+H).
Исходное вещество синтезировали следующим образом.
Пример получения 200-1
Метиламид 5-(N-метиламино)индол-1-карбоновой кислоты
Метиламид 5-аминоиндол-1-карбоновой кислоты (22 мг, 0,11 ммоль, пример получения 218-2) растворяли в метаноле (5,5 мл) и туда добавляли бензотриазол-1-илметанол (434 мг, 2,91 ммоль). Поскольку кристаллы выпадали немедленно, для растворения осадка добавляли метанол (5,5 мл) и реакционную смесь перемешивали при комнатной температуре в течение 1,25 часа. Затем реакционную смесь нагревали и перемешивали при 60°C в течение часа. После охлаждения до комнатной температуры выпавшие кристаллы отфильтровывали, промывали метанолом и сушили с получением бесцветных кристаллов (421 мг). Кристаллы растворяли в смеси растворителей N,N-диметилформамида (4,2 мл) и метанола (21 мл); борогидрид натрия (99 мг, 2,63 ммоль) добавляли при перемешивании при комнатной температуре и реакционную смесь перемешивали в течение 1,5 часов. Туда дополнительно добавляли борогидрид натрия (99 мг, 2,63 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 12 часов. Сходную реакцию проводили с применением остатка, полученного концентрированием при пониженном давлении маточного раствора ранее полученных кристаллов, и борогидрида натрия (342 мг, 9,02 ммоль). Обе упомянутые выше реакционные смеси подвергали распределению между насыщенным водным раствором бикарбоната натрия и этилацетатом; два органических слоя объединяли, промывали насыщенным водным раствором бикарбоната натрия, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia BW-300, система гексан-этилацетат-метанол). Полученные кристаллы суспендировали в этилацетате, отфильтровывали, промывали этилацетатом и сушили с получением указанного в заголовке соединения (255 мг, 1,25 ммоль, 43,1%) в виде бледно-розовых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,66 (3H, с), 2,78 (3H, д, J=4,4 Гц), 5,32 (1H, уш.с), 6,42 (1H, д, J=3,6 Гц), 6,56 (1H, д, 2,4 Гц), 6,57 (1H, дд, J=2,4, 9,0 Гц), 7,61 (1H, д, J=3,6 Гц), 7,84 (1H, д, J=4,4 Гц), 7,93 (1H, д, J=9,0 Гц).
Пример 201
Фениламид 5-(2-(3,3-диэтилуреидо)пиридин-4-иламино)индол-1-карбоновой кислоты
Фениламид 5-(2-аминопиридин-4-иламино)индол-1-карбоновой кислоты (69 мг, 0,20 ммоль) растворяли в тетрагидрофуране (14 мл); туда добавляли триэтиламин (0,055 мл, 0,40 ммоль) и туда добавляли при охлаждении на льду и перемешивании фенилхлорформиат (0,038 мл, 0,30 ммоль). Часть реакционной смеси в количестве 7,0 мл переносили в другой сосуд и концентрировали при пониженном давлении. После растворения остатка в N,N-диметилформамиде (1,0 мл) проводили реакцию, аналогичную реакции в примере 27, с применением диэтиламина (0,031 мл, 0,30 ммоль). Полученный сырой продукт очищали на пластине для ТСХ (Fuji Silysia NH, растворитель для разделения: этилацетат) с получением указанного в заголовке соединения (2,0 мг, 0,005 ммоль) в виде бледно-желтых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,07 (6H, т, J=7,0 Гц), 3,33 (4H, м), 6,52 (1H, м), 6,72 (1H, м), 7,14 (2H, м), 7,40 (3H, м), 7,52 (1H, с), 7,66 (2H, д, J=7,6 Гц), 7,83 (1H, д, J=6,4 Гц), 8,04 (1H, д, J=2,8 Гц), 8,18 (2H, м), 8,65 (1H, с), 10,03 (1H, с).
ESI-МС: 443,28 (M+H).
Исходные вещества синтезировали следующим образом.
Пример получения 201-1
Фениламид 5-нитроиндол-1-карбоновой кислоты
Гидрид натрия (802 мг, 20,0 ммоль, 60% в масле) суспендировали в N,N-диметилформамиде (40 мл); туда добавляли 5-нитроиндол (2,50 г, 15,4 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 30 минут. Туда добавляли фенилизоцианат (2,01 мл, 1,23 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 1,5 часов. К реакционной смеси добавляли воду (80 мл); реакционную смесь перемешивали при комнатной температуре в течение 30 минут; выпавшие кристаллы отфильтровывали, промывали последовательно водой и диэтиловым эфиром и сушили отсасыванием с получением указанного в заголовке соединения (3,53 г, 12,3 ммоль, 79,8%) в виде бледно-желтых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 7,00 (1H, д, J=3,6 Гц), 7,16 (1H, т, J=8,0 Гц), 7,40 (2H, т, J=8,0 Гц), 7,65 (2H, д, J=8,0 Гц), 8,17 (1H, дд, J=2,4, 9,2 Гц), 8,25 (1H, д, J=3,6 Гц), 8,36 (1H, д, J=9,2 Гц), 8,62 (1H, д, J=2,4 Гц), 10,30 (1H, с).
Пример получения 201-2
Фениламид 5-аминоиндол-1-карбоновой кислоты
Фениламид 5-нитроиндол-1-карбоновой кислоты (3,53 г, 12,3 ммоль) растворяли в этаноле (250 мл); туда добавляли воду (50 мл), электролитический порошок железа (2,75 г, 49,2 ммоль), хлорид аммония (5,26 г, 98,4 ммоль), реакционную смесь нагревали и перемешивали при 80°С в течение 2 часов. После охлаждения до комнатной температуры реакционную смесь отфильтровывали; нерастворимые части промывали этилацетатом и фильтрат концентрировали при пониженном давлении. Остаток подвергали распределению между водой и смесью растворителей этилацетата и тетрагидрофурана; органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток переводили в твердое состояние с помощью диэтилового эфира; кристаллы суспендировали в диэтиловом эфире, отфильтровывали, промывали диэтиловым эфиром и сушили с получением указанного в заголовке соединения в виде бледно-красного порошка (681 мг, 2,71 ммоль, 22,0%). Маточный раствор концентрировали при пониженном давлении, который затем обрабатывали сходными способами с получением указанного в заголовке соединения (590 мг, 2,35 ммоль, 19,1%) в виде бледно-красных кристаллов (вторичные кристаллы).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 4,80 (2H, с), 6,48 (1H, д, J=3,4 Гц), 6,59 (1H, дд, J=2,4, 8,8 Гц), 6,71 (1H, д, J=2,4 Гц), 7,09 (1H, т, J=7,6 Гц), 7,34 (2H, т, J=7,6 Гц), 7,61 (2H, д, J=7,6 Гц), 7,84 (1H, д, J=3,4 Гц), 7,88 (1H, д, J=8,8 Гц), 9,79 (1H, с).
Пример получения 201-3
Фениламид 5-(2-аминопиридин-4-иламино)индол-1-карбоновой кислоты
2-Амино-4-хлорпиридин (500 мг, 0,446 ммоль) растворяли в N-метилпирролидоне (5,0 мл); туда добавляли пиридина гидрохлорид (750 мг) и фениламид 5-аминоиндол-1-карбоновой кислоты (408 мг, 1,62 ммоль); реакционную смесь перемешивали при 100°C в течение 6,5 часов. После охлаждения до комнатной температуры реакционную смесь подвергали распределению между насыщенным водным раствором бикарбоната натрия и этилацетатом; органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia NH, система гексан-этилацетат-метанол). Полученное бледно-желтое масло переводили в твердое состояние с помощью диэтилового эфира; кристаллы суспендировали в диэтиловом эфире, отфильтровывали, промывали диэтиловым эфиром и сушили с получением указанного в заголовке соединения (188 мг, 0,464 ммоль, 35,7%) в виде бледно-желтых кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 5,45 (2H, м), 5,99 (1H, д, J=2,0 Гц), 6,10 (1H, дд, J=2,0, 6,0 Гц), 6,69 (1H, д, J=3,6 Гц), 7,07 (1H, дд, J=2,0, 8,6 Гц), 7,12 (1H, т, J=7,6 Гц), 7,37 (3H, м), 7,56 (1H, д, J=6,0 Гц), 7,63 (2H, д, J=7,6 Гц), 8,00 (1H, д, J=3,6 Гц), 8,14 (1H, д, J=8,6 Гц), 8,26 (1H, с), 9,98 (1H, с).
Пример 202
Фениламид 5-(2-(3-(3-диэтиламинопропил)уреидо)пиридин-4-иламино)индол-1-карбоновой кислоты
Фениламид 5-(2-аминопиридин-4-иламино)индол-1-карбоновой кислоты (69 мг, 0,20 ммоль, пример получения 201-3) растворяли в тетрагидрофуране (14 мл); туда добавляли триэтиламин (0,055 мл, 0,40 ммоль) и при перемешивании и охлаждении на льду добавляли фенилхлорформиат (0,038 мл, 0,30 ммоль). Часть данной реакционной смеси в количестве 7,0 мл переносили в другой сосуд, а оставшуюся часть реакционной смеси концентрировали при пониженном давлении. Остаток растворяли в N,N-диметилформамиде (1,0 мл); проводили реакцию, аналогичную реакции в примере 201, с применением N,N-диэтил-1,3-диаминопропана (0,047 мл, 0,30 ммоль); полученный сырой продукт очищали с помощью пластины для ТСХ (Fuji Silysia NH, растворитель для разделения: смесь этилацетат/этанол=10/1); полученные кристаллы суспендировали в этилацетате, отфильтровывали и сушили с получением указанного в заголовке соединения (3 мг, 0,006 ммоль) в виде бесцветных кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,93 (6H, т, J=7,0 Гц), 1,53 (2H, м), 2,42 (6H, м), 3,18 (2H, м), 6,43 (1H, д, J=5,6 Гц), 6,70 (1H, с), 6,75 (1H, с), 7,12 (2H, м), 7,38 (3H, м), 7,64 (2H, д, J=8,0 Гц), 7,76 (1H, д, J=5,6 Гц), 8,03 (1H, с), 8,16 (1H, д, J=9,2 Гц), 8,70 (1H, с), 8,78 (1H, м), 8,86 (1H, с), 10,01 (1H, с).
ESI-МС: 500,54 (M+H).
Пример 203
Фениламид 5-(5-циано-2-(3-(2-диэтиламиноэтил)уреидо)пиридин-4-иламино)индол-1-карбоновой кислоты
Реакцию, сходную с примером получения 5-2, проводили с применением фениламида 5-(2-амино-5-цианопиридин-4-иламино)индол-1-карбоновой кислоты (60 мг, 0,16 ммоль), триэтиламина (0,056 мл, 0,41 ммоль) и фенилхлорформиата (0,082 мл, 0,66 ммоль); растворитель концентрировали при пониженном давлении. Аналогично примеру 5 указанное в заголовке соединение (63 мг, 0,12 ммоль, 76%) получали в виде бледно-желтых кристаллов из остатка, полученного выше, и 2-диэтиламиноэтиламина (0,115 мл, 0,81 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,92 (6H, т, J=7,0 Гц), 2,38-2,46 (6H, м), 3,09 (2H, м), 6,75 (1H, д, J=3,8 Гц), 7,03 (1H, уш.с), 7,13 (1H, дд, J=6,8, 7,6 Гц), 7,18 (1H, дд, J=2,0, 8,8 Гц), 7,38 (2H, т, J=7,6 Гц), 7,48 (1H, д, J=2,0 Гц), 7,65 (3H, м), 8,07 (1H, д, J=3,8 Гц), 8,21 (1H, д, J=8,8 Гц), 8,25 (1H, с), 8,87 (1H, с), 9,21 (1H, уш.с), 10,06 (1H, с).
ESI-МС: 511,53 (M+H).
Исходное вещество синтезировали следующим образом.
Пример получения 203-1
Фениламид 5-(2-амино-5-цианопиридин-4-иламино)индол-1-карбоновой кислоты
2-Амино-4-хлор-5-цианопиридин (200 мг, 1,30 ммоль, пример получения 215-3) растворяли в этоксиэтаноле (13,0 мл); туда добавляли фениламид 5-аминоиндол-1-карбоновой кислоты (408 мг, 1,62 ммоль, пример получения 201-2) и пиридина гидрохлорид (315 мг, 2,73 ммоль) и реакционную смесь нагревали и перемешивали при 130°С в течение 4 часов. После охлаждения до комнатной температуры реакционную смесь подвергали распределению между насыщенным водным раствором бикарбоната натрия и этилацетатом; органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia NH, смесь гексан:этилацетат=2:3, этилацетат, смесь этилацетат:метанол=95:5, в данном порядке). Полученное бледно-желтое масло переводили в твердое состояние с помощью диэтилового эфира; кристаллы суспендировали в диэтиловом эфире, отфильтровывали, промывали диэтиловым эфиром и сушили с получением указанного в заголовке соединения (171 мг, 0,464 ммоль, 35,7%) в виде бесцветных кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 5,77 (1H, с), 6,40 (2H, уш.с), 6,74 (1H, д, J=3,6 Гц), 7,13 (1H, т, J=7,6 Гц), 7,17 (1H, дд, J=2,4, 8,8 Гц), 7,38 (2H, т, J=7,6 Гц), 7,46 (1H, д, J=2,4 Гц), 7,64 (2H, д, J=7,6 Гц), 8,04 (1H, с), 8,05 (1H, д, J=3,6 Гц), 8,20 (1H, д, J=8,8 Гц), 8,35 (1H, с), 10,04 (1H, с).
Пример 204
Фениламид 5-(5-циано-2-(((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-иламино)индол-1-карбоновой кислоты
Аналогично примеру 203 указанное в заголовке соединение (73 мг, 0,13 ммоль, 82%) получали в виде бесцветных кристаллов из фениламида 5-(2-амино-5-цианопиридин-4-иламино)индол-1-карбоновой кислоты (60 мг, 0,16 ммоль, пример получения 203-1), триэтиламина (0,056 мл, 0,41 ммоль), фенилхлорформиата (0,082 мл, 0,66 ммоль) и 4-(пирролидин-1-ил)пиперидина (126 мг, 0,81 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,17-1,28 (2H, м), 1,62 (4H, м), 1,73 (2H, м), 2,07 (1H, м), 2,42 (4H, м), 2,80 (2H, м), 3,87 (2H, м), 6,75 (1H, д, J=3,6 Гц), 7,13 (1H, т, J=7,6 Гц), 7,18 (1H, д, J=8,8 Гц), 7,38 (3H, м), 7,48 (1H, с), 7,64 (2H, д, J=7,6 Гц), 8,07 (1H, д, J=3,6 Гц), 8,20 (1H, д, J=8,8 Гц), 8,30 (1H, с), 8,87 (1H, с), 9,20 (1H, уш.с), 10,06 (1H, с).
ESI-МС: 549,48 (M+H).
Пример 205
Метиламид 5-(N-(2-(3-(3-диэтиламинопропил)уреидо)-5-цианопиридин-4-ил)-N-метиламино)индол-1-карбоновой кислоты
Аналогично примеру 203 указанное в заголовке соединение (13 мг, 0,027 ммоль, 67%) получали в виде бесцветных кристаллов из метиламида 5-(N-(2-амино-5-цианопиридин-4-ил)-N-метиламино)индол-1-карбоновой кислоты (13 мг, 0,041 ммоль), фенилхлорформиата (0,011 мл, 0,089 ммоль), триэтиламина (0,014 мл, 0,10 ммоль) и N,N-диэтил-1,3-диаминопропана (0,032 мл, 0,21 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,92 (6H, т, J=7,0 Гц), 1,53 (2H, м), 2,41 (6H, м), 2,82 (3H, д, J=4,0 Гц), 3,14 (2H, м), 3,29 (3H, с), 6,65 (1H, д, J=3,6 Гц), 7,09 (1H, с), 7,13 (1H, дд, J=2,0, 8,8 Гц), 7,45 (1H, д, J=2,0 Гц), 7,74 (1H, уш.с), 7,84 (1H, д, J=3,6 Гц), 8,10 (1H, с), 8,15 (1H, м), 8,23 (1H, д, J=8,8 Гц), 9,27 (1H, с).
ESI-МС: 477,40 (M+H).
Исходное вещество синтезировали следующим образом.
Пример получения 205-1
Метиламид 5-(N-(2-амино-5-цианопиридин-4-ил)-N-метиламино)индол-1-карбоновой кислоты
Аналогично примеру получения 203 указанное в заголовке соединение (13 мг, 0,041 ммоль, 35,7%) получали в виде бесцветных кристаллов из 2-амино-4-хлор-5-цианопиридина (27 мг, 0,18 ммоль, пример получения 215-3), метиламида 5-(N-метиламино)индол-1-карбоновой кислоты (30 мг, 0,15 ммоль) и пиридина гидрохлорида (38 мг, 0,38 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 5,77 (1H, с), 6,40 (2H, уш.с), 6,74 (1H, д, J=3,6 Гц), 7,13 (1H, т, J=7,6 Гц), 7,17 (1H, дд, J=2,4, 8,8 Гц), 7,38 (2H, т, J=7,6 Гц), 7,46 (1H, д, J=2,4 Гц), 7,64 (2H, д, J=7,6 Гц), 8,04 (1H, с), 8,05 (1H, д, J=3,6 Гц), 8,20 (1H, д, J=8,8 Гц), 8,35 (1H, с), 10,04 (1H, с).
Пример 206
N1-Метил-5-(2-(азетидин-1-илкарбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Азетидина гидрохлорид (104 мг, 1,11 ммоль) и триэтиламин (0,155 мл, 1,11 ммоль) добавляли к раствору фенил-N-(4-(1-(метиламино)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (116 мг, 0,222 ммоль), синтезированного в примере получения 5-2, в диметилформамиде (1 мл) и реакционную смесь перемешивали в течение ночи при комнатной температуре. Реакционную смесь подвергали распределению между этилацетатом и водой; органический слой сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток промывали смесью растворителей эфир-гексан=1:1 и полученное твердое вещество отфильтровывали с получением указанного в заголовке соединения (50 мг) в виде кристаллов.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,03-2,13 (2H, м), 2,83 (3H, д, J=6,2 Гц), 3,99 (4H, т, J=7,9 Гц), 6,54 (1H, дд, J=2,2, 6,7 Гц), 6,68 (1H, д, J=3,9 Гц), 7,03 (1H, дд, J=2,2, 8,3 Гц), 7,35 (1H, д, J=2,2 Гц), 7,41 (1H, д, J=2,2 Гц), 7,87 (1H, д, J=3,9 Гц), 8,04 (1H, д, J=6,7 Гц), 8,03-8,20 (1H, м), 8,28 (1H, т, J=8,3 Гц), 8,88 (1H, с).
Пример 207
N1-Этил-5-(2-(азетидин-1-илкарбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 206 указанное в заголовке соединение (50 мг) получали в виде белых кристаллов из фенил-N-(4-(1-(этиламин)карбонил-1H-5-индолилокси)-2-пиридил)-N-(феноксикарбонил)карбамата (120 мг, 0,224 ммоль), синтезированного в примере получения 55-1, диметилформамида (1 мл), азетидина гидрохлорида (105 мг, 1,12 ммоль) и триэтиламина (0,156 мл, 1,12 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,19 (3H, т, J=7,9 Гц), 2,04-2,13 (2H, м), 3,27-3,36 (2H, м), 3,90 (4H, т, J=7,0 Гц), 6,52 (1H, дд, J=1,9, 6,5 Гц), 6,67 (1H, д, J=3,9 Гц), 7,02 (1H, дд, J=1,9, 8,4 Гц), 7,34 (1H, д, J=1,9 Гц), 7,42 (1H, д, J=1,9 Гц), 7,90 (1H, д, J=3,9 Гц), 8,05 (1H, д, J=6,5 Гц), 8,21 (1H, т, J=6,5 Гц), 8,28 (1H, д, J=8,4 Гц), 8,88 (1H, с).
Пример 208
N1-Циклопропил-5-(2-(азетидин-1-илкарбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру 206 указанное в заголовке соединение (80 мг) получали в виде белых кристаллов из смеси (228 мг) фенил-N-(4-(1-циклопропиламинокарбонил-1H-5-индолил)окси-2-пиридил)-N-(феноксикарбонил)карбамата и фенил-N-(4-(1-циклопропиламинокарбонил-1H-5-индолил)окси-2-пиридил)карбамата, полученной способом, аналогичным способу примера 68, с применением N,N-диметилформамида (2 мл), азетидина гидрохлорида (194 мг, 2,07 ммоль) и триэтиламина (0,29 мл, 2,08 ммоль).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,59-0,65 (2H, м), 0,70-0,78 (2H, м), 2,03-2,13 (2H, м), 2,73-2,82 (1H, м), 3,89 (4H, т, J=7,1 Гц), 6,52 (1H, дд, J=2,0, 6,6 Гц), 6,64 (1H, д, J=3,9 Гц), 7,02 (1H, дд, J=2,0, 8,5 Гц), 7,34 (1H, д, J=2,0 Гц), 7,41 (1H, д, J=2,0 Гц), 7,87 (1H, д, J=3,9 Гц), 8,05 (1H, д, J=6,6 Гц), 8,23-8,30 (2H, м), 8,87 (1H, с).
Пример 209
N1-Метил-5-(2-(((4-(морфолин-4-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид
Морфолин (228 мг, 1,64 ммоль), триацетоксиборогидрид натрия (372 мг, 1,76 ммоль) и уксусную кислоту (0,134 мл, 2,34 ммоль) добавляли к раствору N1-метил-5-(2-(4-оксопиперидин-1-илкарбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамида (476 мг), синтезированного в примере 40, в дихлорметане (3,5 мл) и перемешивали в течение ночи при комнатной температуре. Реакционную смесь подвергали распределению между этилацетатом и водой и органический слой сушили над безводным сульфатом натрия. Раствор концентрировали при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia NH, система этилацетат-метанол). Полученное промывали смесью растворителей эфир-гексан=1:1 и твердое вещество отфильтровывали с получением указанного в заголовке соединения (110 мг) в виде кристаллов.
Спектр МС (ESI): 479 (M+1), 958 (2M+1).
Пример 210
N1-Метил-5-(2-(((4-(азетидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид
Азетидина гидрохлорид (179 мг, 2,00 ммоль) и триацетоксиборогидрид натрия (434 мг, 2,05 ммоль) добавляли к раствору N1-метил-5-(2-(4-оксопиперидин-1-илкарбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамида (555 мг, 1,36 ммоль), синтезированного в примере 40, в дихлорметане (3,7 мл) и перемешивали в течение ночи при комнатной температуре. Реакционную смесь подвергали распределению между этилацетатом и водой и органический слой сушили над безводным сульфатом натрия. Раствор концентрировали при пониженном давлении и остаток очищали с помощью колоночной хроматографии на силикагеле (Fuji Silysia NH, система этилацетат-метанол). Полученное промывали смесью растворителей эфир-гексан=1:1 и твердое вещество отфильтровывали с получением кристаллов указанного в заголовке соединения (5 мг) и смеси (410 мг), включающей указанное в заголовке соединение.
Спектр МС (ESI): 449 (M+1), 897 (2M+1).
Пример 211
N1-Метил-5-(2-(((4-(диэтиламин)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид
Аналогично примеру 209 указанное в заголовке соединение (20 мг) получали в виде кристаллов из раствора N1-метил-5-(2-(4-оксопиперидин-1-илкарбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамида (558 мг), синтезированного в примере 40, в дихлорметане (4 мл), диэтиламина (0,199 мл, 1,92 ммоль), триацетоксиборогидрида натрия (436 мг, 2,06 ммоль) и уксусной кислоты (0,157 мл, 2,74 ммоль). Была также получена смесь (180 мг), включающая указанное в заголовке соединение.
Спектр МС (ESI): 465 (M+1).
Пример 212
N1-Метил-5-(2-(((4-(4-гидроксипиперидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1H-1-индолкарбоксамид
Аналогично примеру 209 указанное в заголовке соединение (100 мг) получали в виде кристаллов из раствора N1-метил-5-(2-(4-оксопиперидин-1-илкарбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамида (500 мг), синтезированного в примере 40, в дихлорметане (3,5 мл), 4-гидроксипиперидина (174 мг, 1,72 ммоль), триацетоксиборогидрида натрия (389 мг, 1,84 ммоль) и уксусной кислоты (0,141 мг, 2,46 ммоль).
Спектр МС (ESI): 493 (M+1), 985(2M+1).
Пример 213
N1-Пропил-5-(2-(пирролидин-1-илкарбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
N1-Пропил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамид (477 мг, 1,54 ммоль) суспендировали в тетрагидрофуране (5 мл) при комнатной температуре; туда добавляли при перемешивании триэтиламин (0,536 мг, 3,08 ммоль) и фенилхлорформиат (0,389 мл, 3,85 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 2 часов. К реакционной смеси добавляли воду; содержимое подвергали экстракции этилацетатом, промывали насыщенным раствором соли, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. К остатку добавляли N,N-диметилформамид (3 мл) и пирролидин (0,27 мл, 3,23 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение ночи. Реакционную смесь подвергали распределению между этилацетатом и водой и органический слой сушили над безводным сульфатом натрия. Раствор концентрировали при пониженном давлении; остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia NH, смесь этилацетат-метанол). Полученное промывали смесью растворителей эфир:гексан=1:1 и твердое вещество отфильтровывали с получением кристаллов (40 мг) указанного в заголовке соединения.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,93 (3H, т, J=7,1 Гц), 1,52-1,65 (2H, м), 1,74-1,82 (4H, м), 3,20-3,40 (6H, м), 6,56 (1H, дд, J=2,7, 6,3 Гц), 6,68 (1H, д, J=3,6 Гц), 7,04 (1H, дд, J=2,7, 7,6 Гц), 7,37 (1H, д, J=2,7 Гц), 7,44 (1H, д, J=2,7 Гц), 7,94 (1H, д, J=3,6 Гц), 8,08 (1H, д, J=6,3 Гц), 8,23 (1H, т, J=7,1 Гц), 8,28 (1H, д, J=7,6 Гц), 8,61 (1H, с).
Исходные вещества синтезировали следующим образом.
Пример получения 213-1
N1-Пропил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамид
Гидрид натрия (60% в масле, 104 мг, 2,6 ммоль) добавляли постепенно при комнатной температуре в атмосфере азота к раствору 4-(1H-5-индолилокси)-2-пиридинамина (487 мг, 2,16 ммоль, CAS No.417722-11-3), который был описан в WO 02/32872, в N,N-диметилформамиде (7 мл). После перемешивания реакционной смеси в течение 2 часов туда добавляли фенил-N-пропилкарбамат (465 мг, 2,6 ммоль) и реакционную смесь перемешивали в течение 4 часов. Реакционную смесь подвергали распределению между этилацетатом и водой и органический слой промывали водой и насыщенным раствором соли, сушили над безводным сульфатом натрия. Раствор концентрировали при пониженном давлении и остаток фильтровали колоночной хроматографией на силикагеле (Fuji Silysia NH, смесь этилацетат-метанол) с получением смеси (500 мг), включающей указанное в заголовке соединение.
Спектр МС (ESI): 311 (M+1).
Пример 214
N1-Изопропил-5-(2-(пирролидин-1-илкарбонил)амино-4-пиридил)окси-1H-1-индолкарбоксамид
N1-Изопропил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамид (90 мг, 0,29 ммоль) суспендировали в тетрагидрофуране (2 мл) при комнатной температуре; туда добавляли при перемешивании триэтиламин (0,121 мг, 0,868 ммоль) и фенилхлорформиат (0,08 мл, 0,633 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 2 часов. К реакционной смеси добавляли воду; содержимое подвергали экстракции этилацетатом, промывали насыщенным раствором соли, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. К остатку добавляли N,N-диметилформамид (1 мл) и пирролидин (0,2 мл, 2,39 ммоль) и перемешивали при комнатной температуре в течение ночи. Реакционную смесь подвергали распределению между этилацетатом и водой; органический слой сушили над безводным сульфатом натрия. Данный раствор концентрировали при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia NH, смесь этилацетат-метанол). Полученное промывали смесью растворителей (эфир:гексан=1:1) и твердое вещество отфильтровывали с получением указанного в заголовке соединения в виде кристаллов (65 мг).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,23 (6H, д, J=6,8 Гц), 1,75-1,82 (4H, м), 3,28-3,46 (4H, м), 3,98-4,09 (1H, м), 6,56 (1Н, дд, J=2,4, 6,0 Гц), 6,68 (1Н, д, J=3,6 Гц), 7,04 (1H, дд, J=2,4, 8,8 Гц), 7,37 (1H, д, J=2,4 Гц), 7,42 (1H, д, J=2,4 Гц), 7,84-8,00 (2H, м), 8,08 (1H, д, J=6,0 Гц), 8,28 (1H, д, J=8,8 Гц), 8,61 (1H, с).
Исходные вещества синтезировали следующим образом.
Пример получения 214-1
N1-Изопропил-5-(2-амино-4-пиридил)окси-1H-1-индолкарбоксамид
Аналогично примеру получения 213-1 указанное в заголовке соединение получали в виде кристаллов (220 мг) из 4-(1H-5-индолилокси)-2-пиридинамина (482 мг, 2,16 ммоль, CAS No.417722-11-3), который был описан в WO 02/32872, N,N-диметилформамида (7 мл), гидрида натрия (60% в масле, 94 мг, 2,57 ммоль) и фенил-N-изопропилкарбамата (460 мг, 2,57 ммоль) в атмосфере азота.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,22 (6H, д, J=6,8 Гц), 3,97-4,08 (1H, м), 5,76 (1H, д, J=2,0 Гц), 5,85 (2H, с), 6,14 (1H, дд, J=2,0, 5,6 Гц), 6,67 (1H, д, J=3,6 Гц), 7,02 (1H, дд, J=2,0, 8,8 Гц), 7,34 (1H, д, J=2,4 Гц), 7,77 (1H, д, J=6,0 Гц), 7,94-7,96 (2H, м), 8,27 (1H, д, J=8,8 Гц).
Пример 215
N1-Метил-5-(2-(метиламинокарбонил)амино-5-циано-4-пиридил)окси-1H-1-индолкарбоксамид
Пример получения 215-1
N1-Метил-5-(2-амино-5-циано-4-пиридил)окси-1H-1-индолкарбоксамид
6-Амино-4-(1H-5-индолилокси)никотинонитрил (63 мг, 0,252 ммоль) растворяли в N,N-диметилформамиде (1 мл) и туда постепенно добавляли гидрид натрия (60% в масле, 11,6 мг, 0,29 ммоль) при перемешивании при комнатной температуре. После перемешивания реакционной смеси в течение 30 минут туда добавляли фенил-N-пропилкарбамат (49,5 мг, 0,277 ммоль) и реакционную смесь перемешивали в течение 3 часов. Туда добавляли насыщенный водный раствор хлорида аммония; содержимое подвергали экстракции этилацетатом и сушили над безводным сульфатом натрия. Данный раствор концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia NH, смесь этилацетат-метанол) с получением указанного в заголовке соединения (12 мг) и N1-метил-5-(2-амино-5-циано-4-пиридил)окси-1H-1-индолкарбоксамида (17 мг).
N1-Метил-5-(2-(метиламинокарбонил)амино-5-циано-4-пиридил)окси-1H-1-индолкарбоксамид
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,58 (3H, д, J=4,6 Гц), 2,86 (3H, д, J=4,6 Гц), 7,15 (1H, дд, J=2,0, 8,3 Гц), 7,20-7,28 (1H, м), 7,51 (1H, д, J=2,0 Гц), 7,93 (1H, д, J=3,0 Гц), 8,22 (1H, кв, J=4,6 Гц), 8,34 (3H, д, J=8,3 Гц), 8,59 (1H, с), 9,51 (1H, с).
N1-Метил-5-(2-амино-5-циано-4-пиридил)окси-1H-1-индолкарбоксамид
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,85 (3H, д, J=4,9 Гц), 5,59 (1H, с), 6,72 (1H, д, J=2,6 Гц), 6,87 (2H, уш.с), 7,13 (1H, дд, J=1,6, 8,5 Гц), 7,49 (1H, д, J=1,6 Гц), 7,92 (1H, д, J=2,6 Гц), 8,21 (1H, кв, J=4,9 Гц), 8,28 (1H, с), 8,34 (1H, д, J=8,5 Гц).
Пример получения 215-2
2-Амино-4-хлор-5-иодпиридин
N,N-Диметилформамид (47 мл) и N-иодсукцинимид (10,7 г, 47,6 ммоль) добавляли к 2-амино-4-хлорпиридину (4,72 г, 36,7 ммоль) и реакционную смесь перемешивали в течение ночи. Туда добавляли водный раствор тиосульфата натрия и этилацетат; органический слой отделяли, концентрировали и сушили над безводным сульфатом натрия. Содержимое концентрировали при пониженном давлении; к остатку добавляли смесь растворителей (эфир:гексан=1:1) и твердое вещество отфильтровывали с получением указанного в заголовке соединения (7,0 г, 27,5 ммоль).
Спектр 1H-ЯМР (CDCl3) (м.д.): 4,56 (2H, уш.с), 6,68 (1Н, с), 8,32 (1H, с).
Пример получения 215-3
2-Амино-4-хлор-5-цианопиридин
1-Метил-2-пирролидон (20 мл), цианид цинка (0,49 г, 4,17 ммоль) и тетракис(трифенилфосфин)палладий (1,3 г, 1,12 ммоль) добавляли к 2-амино-4-хлор-5-иодпиридину (1,93 г, 7,58 ммоль), синтезированному в примере получения 215-2, и реакционную смесь перемешивали при 130-135°С в течение 5 часов. К реакционной смеси добавляли приблизительно 0,28% водный аммиак (100 мл) и этилацетат; органический слой отделяли, промывали насыщенным раствором соли и сушили над безводным сульфатом натрия. Содержимое концентрировали при пониженном давлении и остаток фильтровали колоночной хроматографией на силикагеле (Fuji Silysia NH, этилацетат). После концентрирования при пониженном давлении к остатку добавляли смесь растворителей (эфир:гексан=1:1) и перемешивали; твердое вещество отфильтровывали с получением указанного в заголовке соединения в виде кристаллов (680 мг).
Спектр 1H-ЯМР (CDCl3) (м.д.): 5,03 (2H, уш.с), 6,58 (1Н, с), 8,32 (1H, с).
МС спектр (EI): 153 (M).
Пример получения 215-4
6-Амино-4-(1H-5-индолилокси)никотинонитрил
5-Гидроксииндол (313 мг, 2,35 ммоль) растворяли в диметилсульфоксиде (3 мл) и туда при перемешивании при комнатной температуре постепенно добавляли гидрид натрия (90 мг, 2,25 ммоль). После перемешивания реакционной смеси в течение 1 часа туда добавляли 2-амино-4-хлор-5-цианопиридин (300 мг, 1,96 ммоль), синтезированный в примере получения 215-3, и реакционную смесь нагревали и перемешивали при 120°С в течение 4 часов. После остывания до комнатной температуры реакционную смесь подвергали распределению между этилацетатом и водой; органический слой промывали водой и насыщенным раствором соли и сушили над безводным сульфатом натрия. Растворитель отгоняли; остаток подвергали колоночной хроматографии на силикагеле (Fuji Silysia NH, смесь этилацетат-метанол); фракции, содержащие желаемое соединение, концентрировали при пониженном давлении; туда добавляли эфир; твердое вещество отфильтровывали и сушили при пониженном давлении с получением указанного в заголовке соединения (95 мг, 0,38 ммоль, 59%).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 5,59 (1H, с), 6,48 (1H, с), 6,82 (2H, с), 6,92 (1H, дд, J=2,0, 9,0 Гц), 7,40 (1H, д, J=2,0 Гц), 7,46 (1H, т, J=2,0 Гц), 7,50 (1H, д, J=9,0 Гц), 8,26 (1H, с), 11,30 (1H, с).
Пример 216
N1-Метил-5-(2-(пирролидин-1-илкарбонил)амино-5-циано-4-пиридил)окси-1H-1-индолкарбоксамид
N1-Метил-5-(2-амино-5-циано-4-пиридил)окси-1H-1-индолкарбоксамид (20 мг), синтезированный в примере 215, суспендировали в тетрагидрофуране (0,5 мл) при комнатной температуре; туда добавляли при перемешивании триэтиламин (0,121 мл, 0,868 ммоль) и фенилхлорформиат (0,08 мл, 0,633 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 2 часов. К реакционной смеси добавляли воду; содержимое подвергали экстракции этилацетатом, промывали насыщенным раствором соли, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. К части остатка (14 мг) добавляли N,N-диметилформамид и пирролидин (0,013 мл) и реакционную смесь перемешивали в течение ночи. Реакционную смесь подвергали распределению между этилацетатом и водой; органический слой сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia NH, смесь этилацетат-метанол). Полученное промывали смесью растворителей (эфир:гексан=1:1) с получением указанного в заголовке соединения в виде кристаллов (6 мг).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,74 (4H, уш.с), 2,85 (3H, д, J=4,4 Гц), 3,15-3,40 (4H, м), 6,72 (1H, д, J=4,7 Гц), 7,15 (1H, дд, J=1,9, 8,4 Гц), 7,37 (1H, с), 7,50 (1H, д, J=1,9 Гц), 7,93 (1H, д, J=4,7 Гц), 8,20-8,26 (1H, м), 8,33 (1H, д, J=8,4 Гц), 8,63 (1H, с), 9,28 (1H, уш.с).
Пример 217
N1-Метил-5-(2-((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)амино-5-циано-4-пиридил)окси-1H-1-индолкарбоксамид
N1-Метил-5-(2-амино-5-циано-4-пиридил)окси-1H-1-индолкарбоксамид (15 мг, 0,049 ммоль), синтезированный в примере 215, суспендировали в тетрагидрофуране (0,5 мл) при комнатной температуре; туда добавляли при перемешивании триэтиламин (17 мкл, 0,122 ммоль) и фенилхлорформиат (14 мкл, 0,072 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 2 часов. К реакционной смеси добавляли воду, содержимое подвергали экстракции этилацетатом, промывали насыщенным раствором соли, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. К части остатка (14 мг) добавляли N,N-диметилформамид (0,5 мл) и 4-(1-пирролидинил)пиперидин (28 мг, 0,18 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение ночи. Реакционную смесь подвергали распределению между этилацетатом и водой и органический слой сушили над безводным сульфатом натрия. Содержимое концентрировали при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia NH, смесь этилацетат-метанол). Полученное промывали смесью растворителей (эфир:гексан=1:1) и твердое вещество отфильтровывали с получением указанного в заголовке соединения в виде кристаллов (6 мг).
МС-спектр (ESI): 488 (M+1), 975 (2M+1).
Пример 218
N1-Метил-5-(2-((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)амино-5-циано-4-пиридил)амино-1H-1-индолкарбоксамид
N1-Метил-5-(2-амино-5-циано-4-пиридил)амино-1H-1-индолкарбоксамид (50 мг, 0,16 ммоль) суспендировали в тетрагидрофуране (1 мл) при комнатной температуре; туда добавляли при перемешивании триэтиламин (0,057 мл, 0,41 ммоль) и фенилхлорформиат (0,041 мл, 0,325 ммоль); реакционную смесь перемешивали при комнатной температуре в течение 2 часов. К реакционной смеси добавляли воду; содержимое подвергали экстракции этилацетатом, промывали насыщенным раствором соли, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. К остатку добавляли N,N-диметилформамид (0,5 мл) и 4-(1-пирролидинил)пиперидин (100 мг, 0,648 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение ночи. Реакционную смесь подвергали распределению между этилацетатом и водой и органический слой сушили над безводным сульфатом натрия. Содержимое концентрировали при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia NH, смесь этилацетат-метанол) с получением указанного в заголовке соединения (65 мг, 0,134 ммоль).
МС-спектр (ESI): 487 (M+1).
Исходные вещества синтезировали следующим образом.
Пример получения 218-1
N1-Метил-5-нитро-1H-1-индолкарбоксамид
К раствору 5-нитроиндола (0,841 г, 5,19 ммоль) в N,N-диметилформамиде (0,5 мл) постепенно при перемешивании при комнатной температуре добавляли гидрид натрия (60% в масле, 228 мг, 5,7 ммоль); туда добавляли фенил-N-метилкарбамат (1,02 г, 6,74 ммоль) и реакционную смесь перемешивали в течение ночи. Реакционную смесь подвергали распределению между этилацетатом и водой; органический слой промывали водой и насыщенным раствором соли, сушили над безводным сульфатом натрия. Содержимое концентрировали при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (смесь гексан-этилацетат, затем этилацетат) с получением указанного в заголовке соединения (600 мг).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,88 (3H, д, J=4,4 Гц), 6,94 (1H, д, J=3,6 Гц), 8,03 (1H, д, J=3,6 Гц), 8,15 (1H, дд, J=2,4, 9,2 Гц), 8,35-8,43 (2H, м), 8,59 (1H, д, J=2,4 Гц).
Пример получения 218-2
N1-Метил-5-амино-1H-1-индолкарбоксамид
К N1-метил-5-нитро-1H-1-индолкарбоксамиду (0,32 г, 1,46 ммоль), синтезированному в примере получения 218-1, добавляли метанол (6 мл), воду (2 мл), железо (0,32 г) и хлорид аммония (0,64 г) и реакционную смесь нагревали до температуры кипения с обратным холодильником в течение 2 часов. Реакционную смесь подвергали распределению между этилацетатом и водой; органический слой промывали водой и насыщенным раствором соли и сушили над безводным сульфатом натрия. Остаток фильтровали через целит и концентрировали при пониженном давлении с получением указанного в заголовке соединения (210 мг).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,79 (3H, д, J=4,4 Гц), 4,73 (2H, уш.с), 6,48 (1H, д, J=3,6 Гц), 6,56 (1H, дд, J=2,4, 8,8 Гц), 6,68 (1H, д, J=l,6 Гц), 7,60 (1H, д, J=3,6 Гц), 7,80-7,88 (1H, м), 7,89 (1H, д, J=8,8 Гц).
Пример получения 218-3
N1-Метил-5-(2-амино-5-циано-4-пиридил)амино-1H-1-индолкарбоксамид
2-Амино-4-хлор-5-цианопиридин (123 мг, 0,80 ммоль), синтезированный в примере получения 215-3, этоксиэтанол (3 мл) и пиридина гидрохлорид (186 мг, 1,60 ммоль) добавляли к N1-метил-5-амино-1H-1-индолкарбоксамиду (198 мг, 1,05 ммоль), синтезированному в примере получения 218-2, и реакционную смесь перемешивали при 130°С в течение 3 часов. После остывания до комнатной температуры реакционную смесь подвергали распределению между насыщенным водным раствором бикарбоната натрия и этилацетатом; органический слой промывали водой и насыщенным раствором соли, сушили над безводным сульфатом натрия. Растворитель отгоняли и остаток очищали колоночной хроматографией на силикагеле (смесь гексан-этилацетат, этилацетат, в данном порядке) с получением указанного в заголовке соединения (110 мг, 0,359 ммоль).
МС-спектр (ESI): 307 (M+1).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,84 (3H, д, J=4,4 Гц), 5,75 (1H, с), 6,39 (2H, с), 6,66 (1H, д, J=3,2 Гц), 7,13 (1H, дд, J=2,0, 8,8 Гц), 7,42 (1H, д, J=2,0 Гц), 7,82 (1H, д, J=3,2 Гц), 8,04 (1H, с), 8,08-8,14 (1H, м), 8,23 (1H, д, J=8,8 Гц), 8,30 (1H, с).
Пример 219
N1-Метил-5-(2-(3-(2-диэтиламиноэтил)уреидо)амино-5-циано-4-пиридил)амино-1H-1-индолкарбоксамид
N1-Метил-5-(2-амино-5-циано-4-пиридил)амино-1H-1-индолкарбоксамид (36 мг, 0,12 ммоль), синтезированный в примере получения 218-3, суспендировали в тетрагидрофуране (2 мл) при комнатной температуре; туда добавляли при перемешивании триэтиламин (0,1 мл, 0,72 ммоль) и фенилхлорформиат (0,037 мл, 0,29 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 2 часов. К реакционной смеси добавляли воду; содержимое подвергали экстракции этилацетатом, промывали насыщенным раствором соли, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. К остатку добавляли N,N-диметилформамид (0,5 мл) и N,N-диэтиламиноэтиламин (0,1 мл) и реакционную смесь перемешивали при комнатной температуре в течение ночи. Реакционную смесь подвергали распределению между этилацетатом и водой; органический слой промывали насыщенным раствором соли, сушили над безводным сульфатом натрия. Содержимое концентрировали при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia NH, смесь этилацетат-метанол) с получением указанного в заголовке соединения (25 мг, 0,056 ммоль).
МС-спектр (ESI): 449 (M+1).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,93 (6H, т, J=6,8 Гц), 2,37-2,50 (6H, м), 2,84 (3H, д, J=4,4 Гц), 3,10 (2H, кв, J=6,8 Гц), 6,68 (1H, д, J=3,2 Гц), 7,05 (1H, с), 7,15 (1H, дд, J=2,4, 8,8 Гц), 7,44 (1H, д, J=3,2 Гц), 7,70 (1H, уш.с), 7,84 (1H, д, J=4,0 Гц), 8,14 (1H, д, J=4,4 Гц), 8,24 (1H, д, J=8,8 Гц), 8,25 (1H, с), 8,84 (1H, с), 9,21 (1H, с).
Пример 220
N1-Диэтил-2-метил-5-(2-((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)амино-5-циано-4-пиридил)амино-1H-1-индолкарбоксамид
N1-Диэтил-2-метил-5-(2-амино-5-циано-4-пиридил)амино-1H-1-индолкарбоксамид (84 мг, 0,249 ммоль) суспендировали в тетрагидрофуране (1 мл) при комнатной температуре; туда добавляли при перемешивании триэтиламин (0,2 мл, 1,43 ммоль) и фенилхлорформиат (0,079 мл, 0,626 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 2 часов. К реакционной смеси добавляли воду и содержимое подвергали экстракции этилацетатом, промывали насыщенным раствором соли, сушили над безводным сульфатом натрия и концентрировали при пониженном давлении. К части (80 мг) полученного остатка (120 мг) добавляли N,N-диметилформамид (0,5 мл) и 4-(1-пирролидинил)пиперидин (173 мг, 0,111 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение ночи. Реакционную смесь подвергали распределению между этилацетатом и водой и органический слой сушили над безводным сульфатом натрия. Содержимое концентрировали при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia NH, система этилацетат-метанол) с получением указанного в заголовке соединения (45 мг, 0,083 ммоль).
МС-спектр (ESI): 543,5 (M+1).
Исходные вещества синтезировали следующим образом.
Пример получения 220-1
N1-Диэтил-2-метил-5-нитро-1H-1-индолкарбоксамид
К раствору 2-метил-5-нитроиндола (0,841 г, 5,19 ммоль) в N,N-диметилформамиде (0,5 мл) постепенно добавляли при перемешивании при комнатной температуре гидрид натрия (60% в масле, 94 мг); туда добавляли диэтилкарбамоилхлорид (0,341 мл) и реакционную смесь нагревали и перемешивали при 70°С в течение 4 часов. После охлаждения до комнатной температуры реакционную смесь подвергали распределению между этилацетатом и водой; органический слой промывали водой и насыщенным раствором соли и сушили над безводным сульфатом натрия. Содержимое концентрировали при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (Fuji Silysia NH; смесь гексан-этилацетат, этилацетат, в данном порядке) с получением указанного в заголовке соединения (420 мг).
МС-спектр (ESI): 330 (M+55).
Пример получения 220-2
N1-Диэтил-2-метил-5-амино-1H-1-индолкарбоксамид
К N1-метил-5-нитро-1H-1-индолкарбоксамиду (415 г, 1,46 ммоль), синтезированному в примере получения 220-1, добавляли метанол (8 мл), воду (2 мл), порошок железа (0,42 г) и хлорид аммония (0,84 г) и реакционную смесь нагревали до температуры кипения с обратным холодильником в течение 2 часов. Реакционную смесь подвергали распределению между этилацетатом и водой; органический слой промывали водой и насыщенным раствором соли и сушили над безводным сульфатом натрия. Фильтрация через целит и концентрирование при пониженном давлении дали указанное в заголовке соединение (322 мг).
МС-спектр (ESI): 246 (M+1).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,10 (6H, т, J=7,2 Гц), 2,28 (3H, с), 3,25-3,40 (4H, м), 4,92 (2H, уш.с), 6,10 (1H, т, J=0,8 Гц), 6,51 (1H, дд, J=2,4, 8,4 Гц), 6,64 (1H, д, J=2,4 Гц), 6,89 (1H, д, J=8,4 Гц).
Пример получения 220-3
N1-Диэтил-2-метил-5-(2-амино-5-циано-4-пиридил)амино-1H-1-индолкарбоксамид
2-Амино-4-хлор-5-цианопиридин (140 мг, 0,92 ммоль), синтезированный в примере получения 215-3, этоксиэтанол (2,5 мл) и пиридина гидрохлорид (223 мг, 1,92 ммоль) добавляли к N1-диэтил-2-метил-5-амино-1H-1-индолкарбоксамиду (320 мг, 1,31 ммоль), синтезированному в примере получения 220-2, и реакционную смесь перемешивали при 130°С в течение 3 часов. После охлаждения до комнатной температуры реакционную смесь подвергали распределению между насыщенным водным раствором бикарбоната натрия и этилацетатом; органический слой промывали водой и насыщенным раствором соли и сушили над безводным сульфатом натрия. Растворитель отгоняли и остаток очищали колоночной хроматографией на силикагеле (смесь гексан-этилацетат, затем этилацетат) с получением указанного в заголовке соединения (110 мг, 0,359 ммоль).
МС-спектр (ESI): 363 (M+1).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 1,05-1,20 (6H, м), 2,36 (3H, с), 3,25-3,40 (4H, м), 5,68 (1H, с), 6,35-6,37 (3H, м), 7,02 (1H, дд, J=2,0, 8,4 Гц), 7,19 (1H, д, J=8,4 Гц), 7,30 (1H, д, J=2,0 Гц), 8,01 (1H, с), 8,22 (1H, с).
Пример 221
Метиламид 5-(5-иод-2-(3-метилуреидо)пиримидин-4-илокси)-1H-индол-1-карбоновой кислоты
Фенил-N-(5-иод-4-(1-метиламинокарбонил-1H-индол-5-илокси)пиримидин-2-ил)-N-(феноксикарбонил)карбамат (597 мг, 0,919 ммоль) растворяли в диметилформамиде (3,0 мл); добавляли при перемешивании при 0°С 40% раствор метиламина в метаноле (1,0 мл) и реакционную смесь дополнительно перемешивали в течение 30 минут при поддержании температуры. После завершения реакции к реакционной смеси добавляли воду (10 мл); выпавшие кристаллы отфильтровывали, промывали водой, метанолом и диэтиловым эфиром и сушили при теплом аэрировании с получением указанного в заголовке соединения в виде белых кристаллов (367 мг, 0,787 ммоль, 86%).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,04 (3H, д, J=4,8 Гц), 2,85 (3H, д, J=4,0 Гц), 6,73 (1H, д, J=3,6 Гц), 7,16 (1H, дд, J=2,4, 8,8 Гц), 7,52 (1H, д, J=2,4 Гц), 7,61 (1H, м), 7,92 (1H, д, J=3,6 Гц), 8,20 (1H, м), 8,35 (1H, д, J=8,8 Гц), 8,69 (1H, с), 9,78 (1H, уш.с).
Исходные вещества синтезировали следующим образом.
Пример получения 221-1
N1-Метил-5-(2-амино-4-пиримидил)окси-1H-1-индолкарбоксамид
Аналогично примеру получения 1-3 указанное в заголовке соединение получали в виде белого порошка из 4-(1H-5-индолилокси)-2-пиримидинамина (413 мг, 1,83 ммоль), синтезированного в примере получения 1-2, и фенил-N-метилкарбамата (332 мг, 2,20 ммоль), синтезированного в примере получения 2-1.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,84 (3H, д, J=4,0 Гц), 6,06 (1H, д, J=5,6 Гц), 6,57 (2H, уш.с), 6,67 (1H, д, J=3,6 Гц), 7,04 (1H, дд, J=2,4, 8,8 Гц), 7,36 (1H, д, J=2,4 Гц), 7,85 (1H, д, J=3,6 Гц), 8,08 (1H, д, J=5,6 Гц), 8,14 (1H, м), 8,25 (1H, д, J=8,8 Гц).
Пример получения 221-2
N1-Метил-5-(2-амино-5-иод-4-пиримидил)окси-1H-1-индолкарбоксамид
N1-Метил-5-(2-амино-4-пиримидил)окси-1H-1-индолкарбоксамид (302 мг, 1,07 ммоль) и N-иодсукцинимид (301 мг, 1,34 ммоль) растворяли в N,N-диметилформамиде (3,0 мл) и реакционную смесь перемешивали при комнатной температуре в течение 1 часа. Реакционную смесь подвергали распределению между этилацетатом и водой; органический слой промывали водой и насыщенным раствором соли и сушили над безводным сульфатом магния. Растворитель отгоняли и остаток очищали колоночной хроматографией на силикагеле (элюент: смесь этилацетат:гексан=2:1) с получением указанного в заголовке соединения в виде желтых кристаллов (224 мг, 0,547 ммоль, 51%).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 2,84 (3H, д, J=4,4 Гц), 6,67 (1H, д, J=3,6 Гц), 6,72 (2H, уш.с), 7,04 (1H, дд, J=2,4, 8,8 Гц), 7,36 (1H, д, J=2,4 Гц), 7,85 (1H, д, J=3,6 Гц), 8,15 (1H, м), 8,24 (1H, д, J=8,8 Гц), 8,33 (1H, с).
Пример получения 221-3
Фенил-N-(5-иод-4-(1-метиламинокарбонил-1H-индол-5-илокси)пиримидин-2-ил)-N-(феноксикарбонил)карбамат
N1-Метил-5-(2-амино-5-иод-4-пиримидил)окси-1H-1-индолкарбоксамид (205 мг, 0,500 ммоль) суспендировали в тетрагидрофуране (5,0 мл); туда добавляли при перемешивании триэтиламин (0,209 мл, 1,50 ммоль). Суспензию охлаждали с помощью льда; туда добавляли фенилхлорформиат (0,188 мл, 1,50 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 3 часов. Реакционную смесь подвергали распределению между этилацетатом и насыщенным водным раствором бикарбоната натрия; органический слой промывали насыщенным водным раствором бикарбоната натрия и насыщенным раствором соли и сушили над безводным сульфатом магния. После отгонки растворителя полученный сырой продукт кристаллизовали из смеси этилацетат-гексан; кристаллы отфильтровывали и сушили при аэрировании с получением указанного в заголовке соединения в виде белых кристаллов (207 мг, 0,319 ммоль, 64%).
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 3,09 (3H, д, J=4,8 Гц), 5,56 (1H, м), 6,56 (1H, д, J=3,6 Гц), 6,98-7,14 (4H, м), 7,17-7,34 (6H, м), 7,36-7,42 (2H, м), 7,68 (1H, с), 8,12 (1H, д, J=8,8 Гц), 8,74 (1H, с).
Контрольный пример 1
N1-Циклопропил-5-((2-(((2-хлорэтиламино)карбонил)амино)-4-пиридил)окси)-1H-1-индолкарбоксамид
N1-Циклопропил-5-((2-амино-4-пиридил)окси)-1H-1-индолкарбоксамид (400 мг, CAS No. 417722-12-4), описанный в WO 02/32872, 2-хлорэтилизоцианат (150 мг) и тетрагидрофуран (5 мл) перемешивали при 80°С в течение 1,5 часов. Смесь охлаждали до комнатной температуры, добавляли силикагель и растворитель отгоняли при пониженном давлении. Силикагель наносили на сухую колонку, набитую силикагелем, и проводили очистку колоночной хроматографией (смесь гексан:этилацетат=1:1, затем этилацетат) с получением 280 мг бесцветного порошка.
Спектр 1H-ЯМР (ДМСО-d6) δ (м.д.): 0,57-0,63 (2H, м), 0,70-0,75 (2H, м), 2,73-2,80 (1H, м), 3,42 (2H, кв, J=6,0 Гц), 3,61 (2H, т, J=6,0 Гц), 6,52 (1H, дд, J=5,6 Гц, 2,4 Гц), 6,65 (1H, д, J=3,6 Гц), 6,85 (1H, д, J=2,4 Гц), 7,04 (1H, дд, J=8,8 Гц, 2,4 Гц), 7,35 (1H, д, J=2,4 Гц), 7,86 (1H, д, J=3,6 Гц), 8,04 (1H, д, J=5,6 Гц), 8,27 (1H, с), 8,28 (1H, д, J=8,8 Гц), 8,34 (1H, уш.с), 9,19 (1H, с).
Структурные формулы соединений, полученных в примерах получения, примерах и контрольном примере, приведенных выше, показаны ниже в таблицах с 5 по 17.
Таблица 5
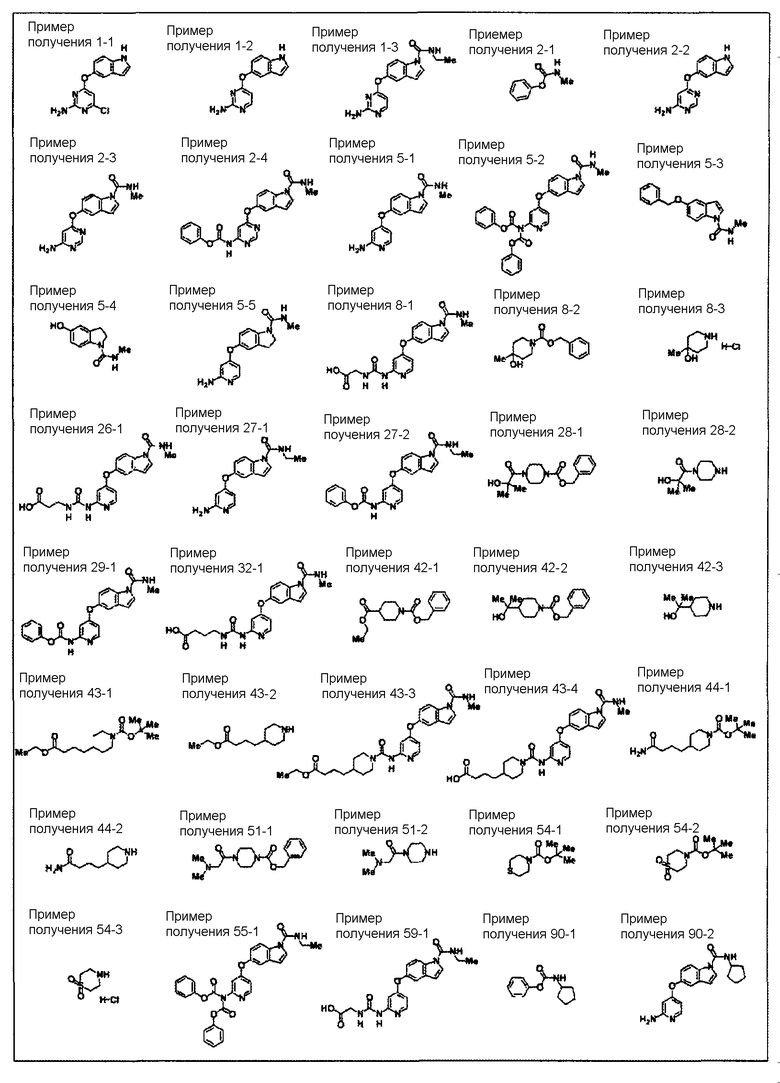
Таблица 6
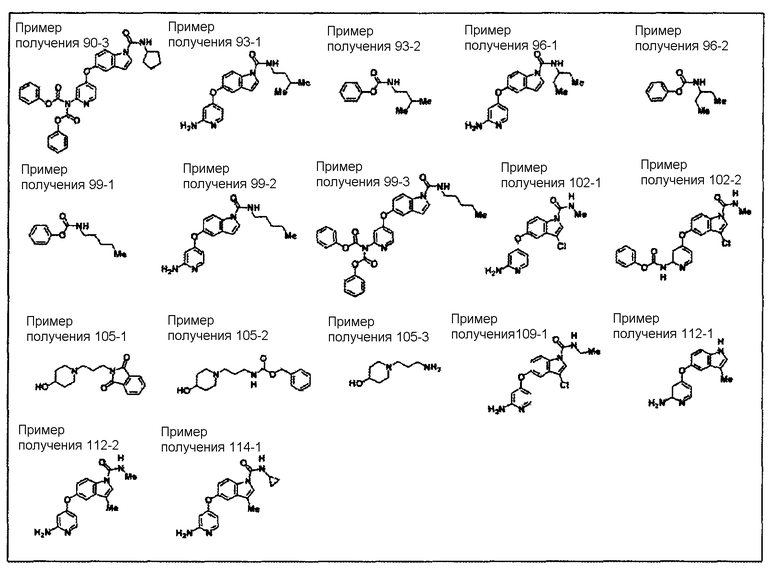
Таблица 7
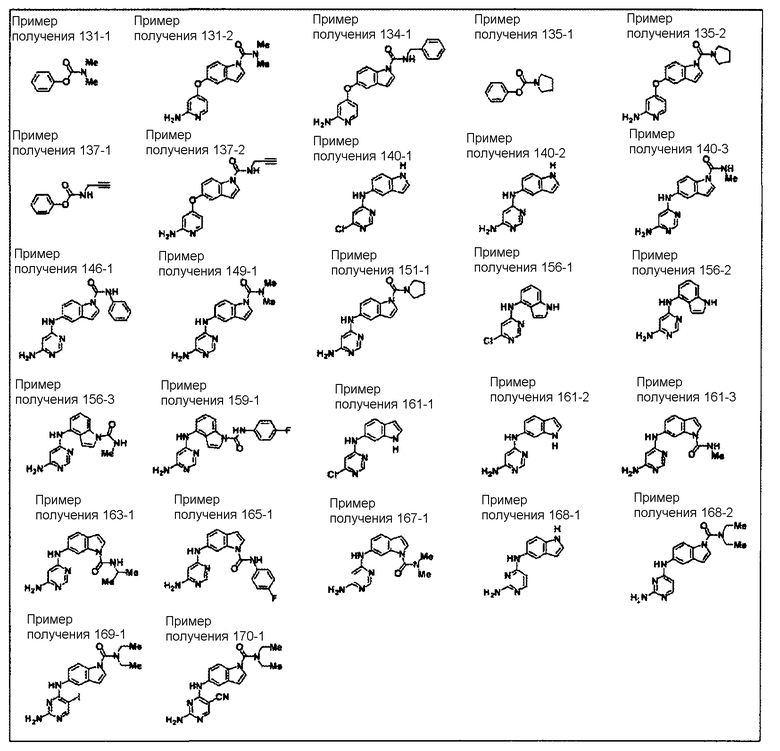
Таблица 8
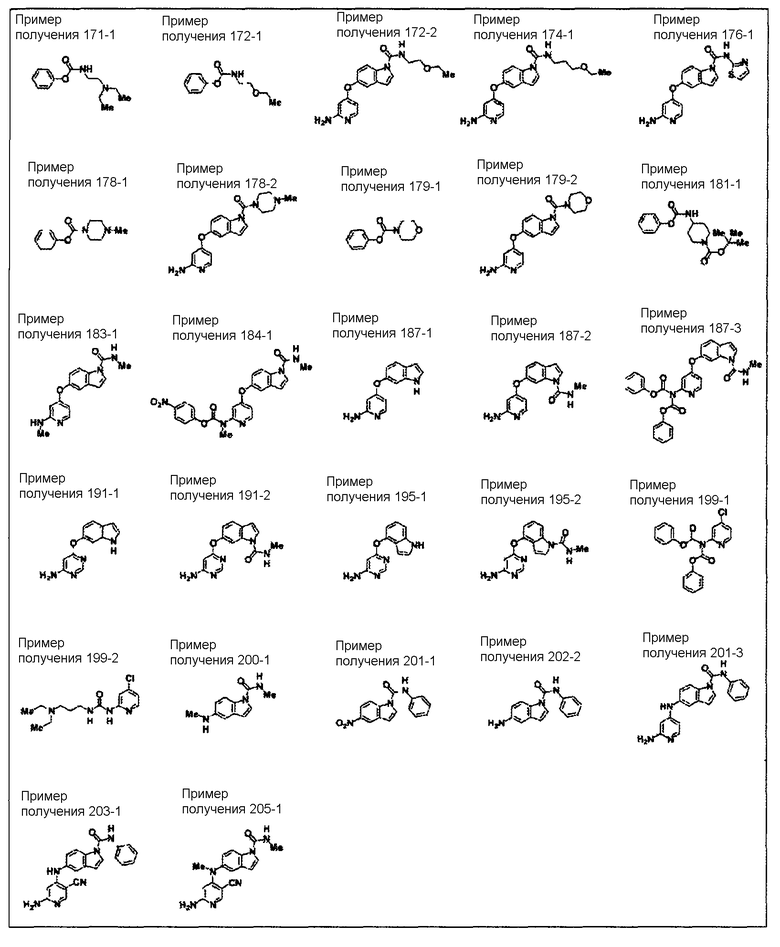
Таблица 9
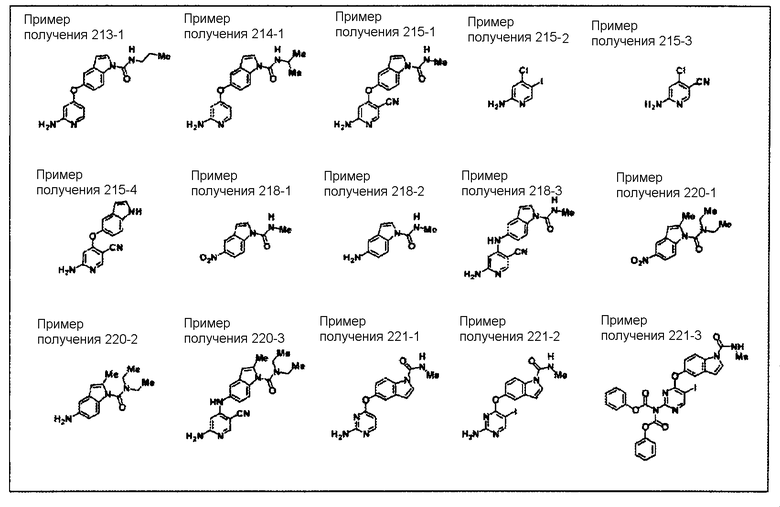
Таблица 10
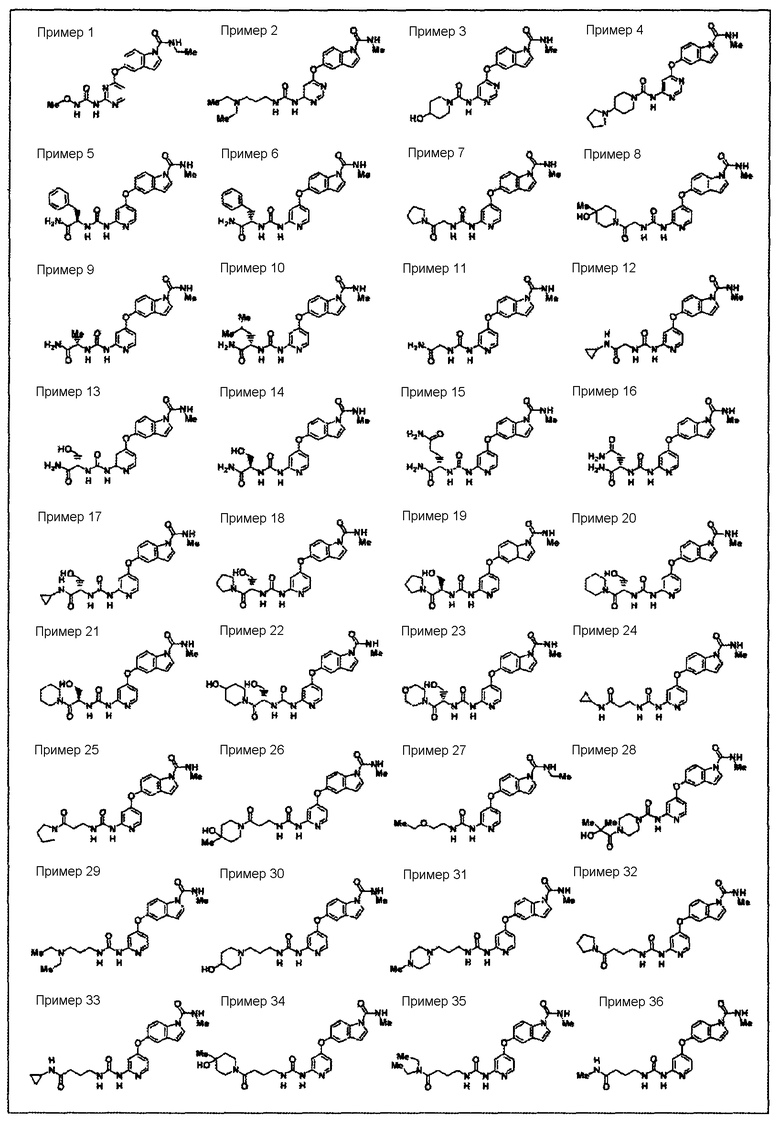
Таблица 11
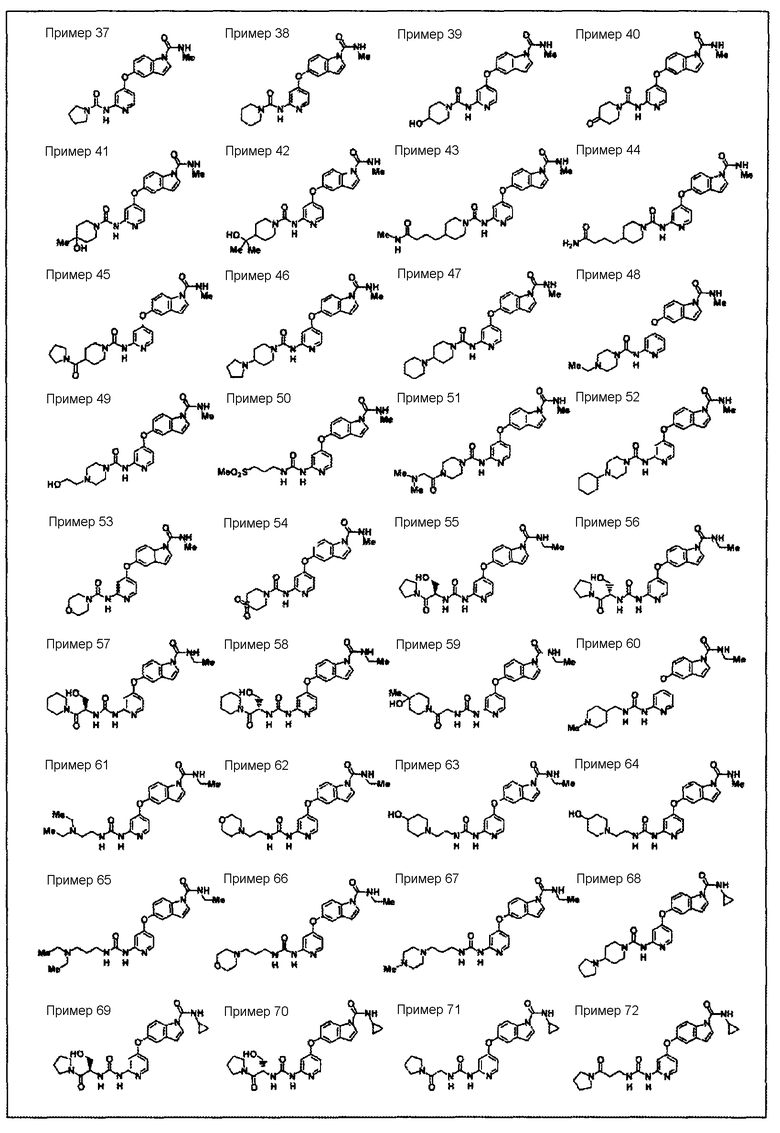
Таблица 12
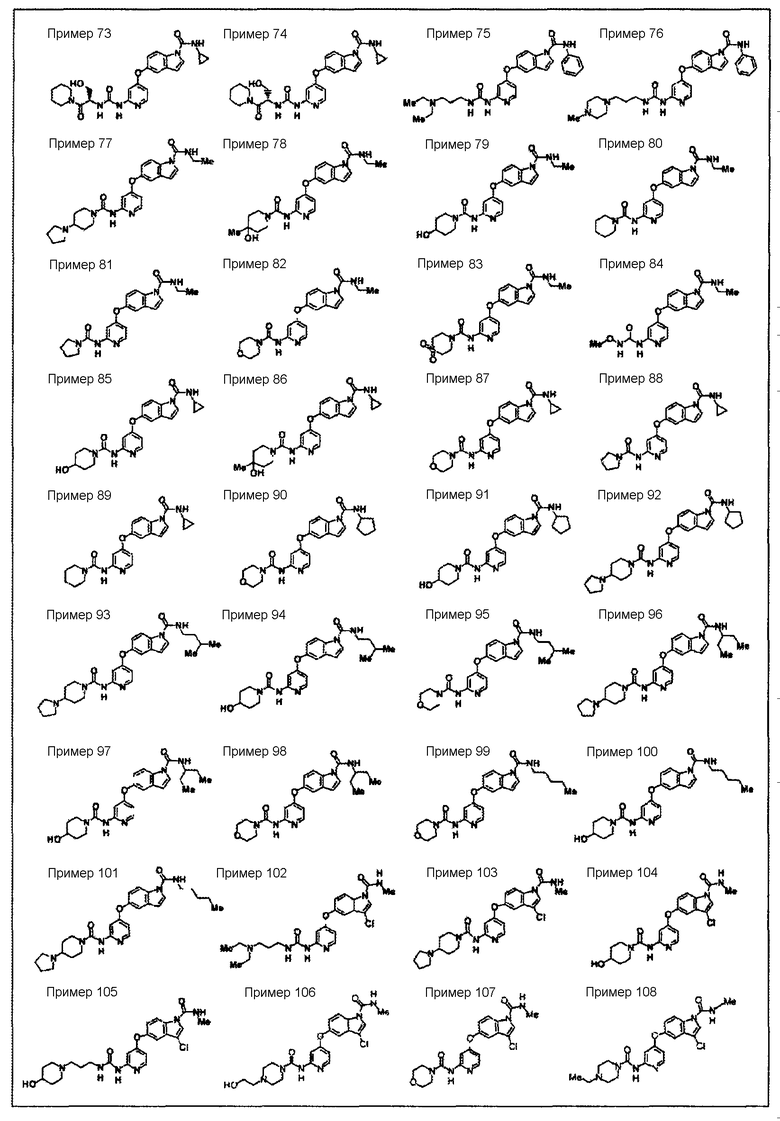
Таблица 13
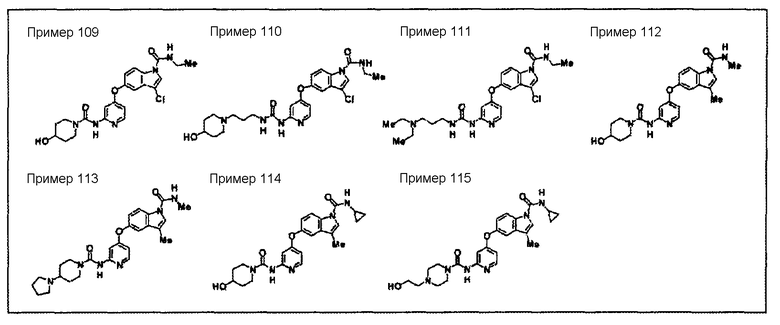
Таблица 14
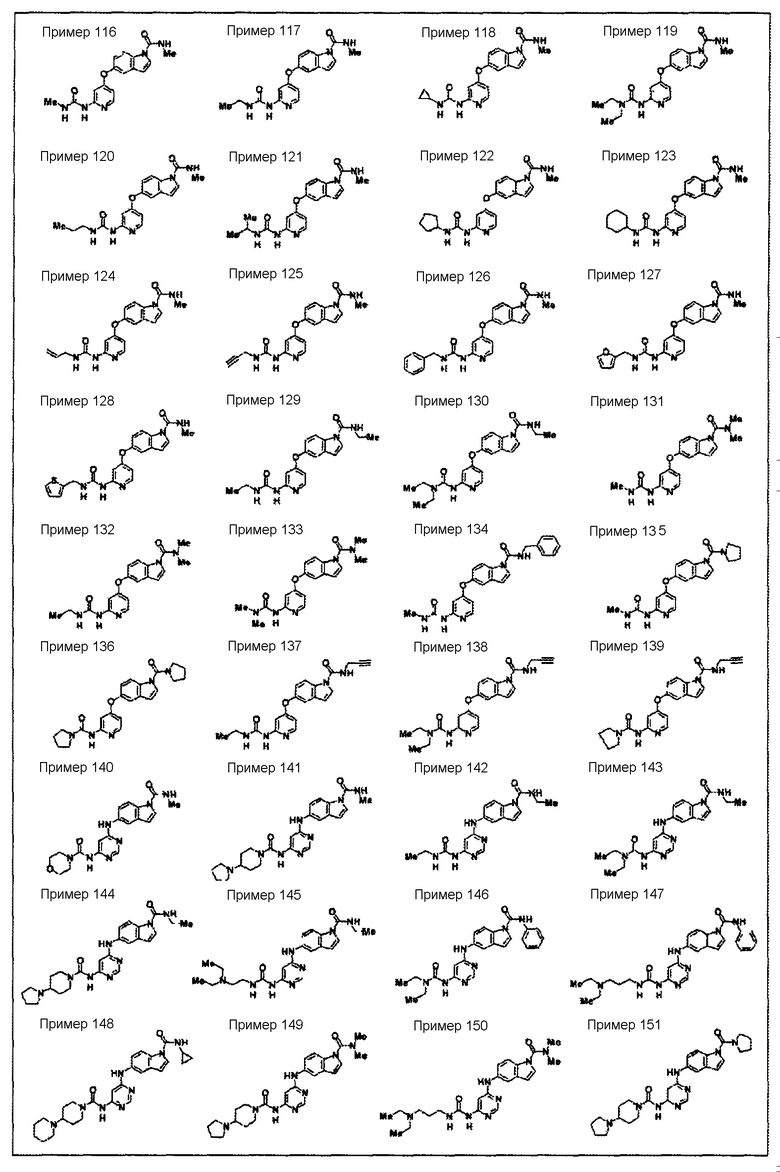
Таблица 15
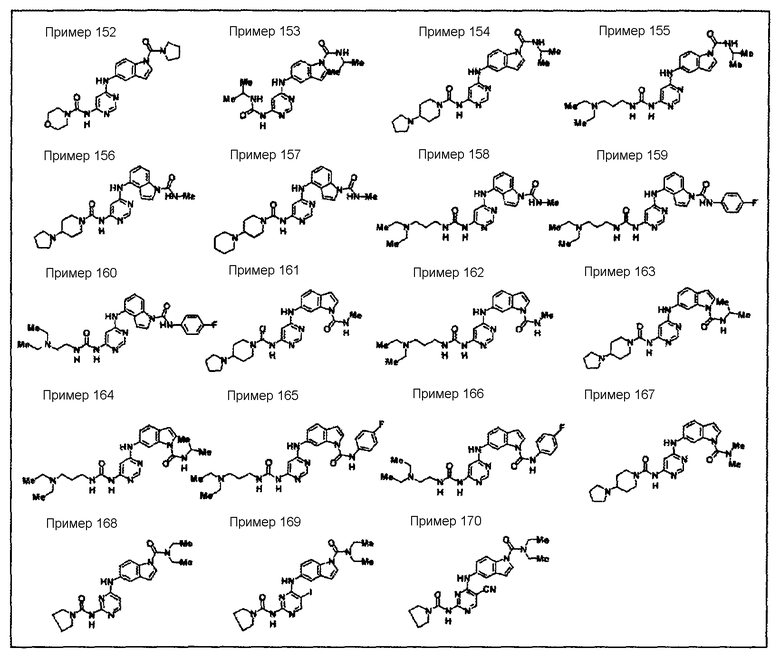
Таблица 16
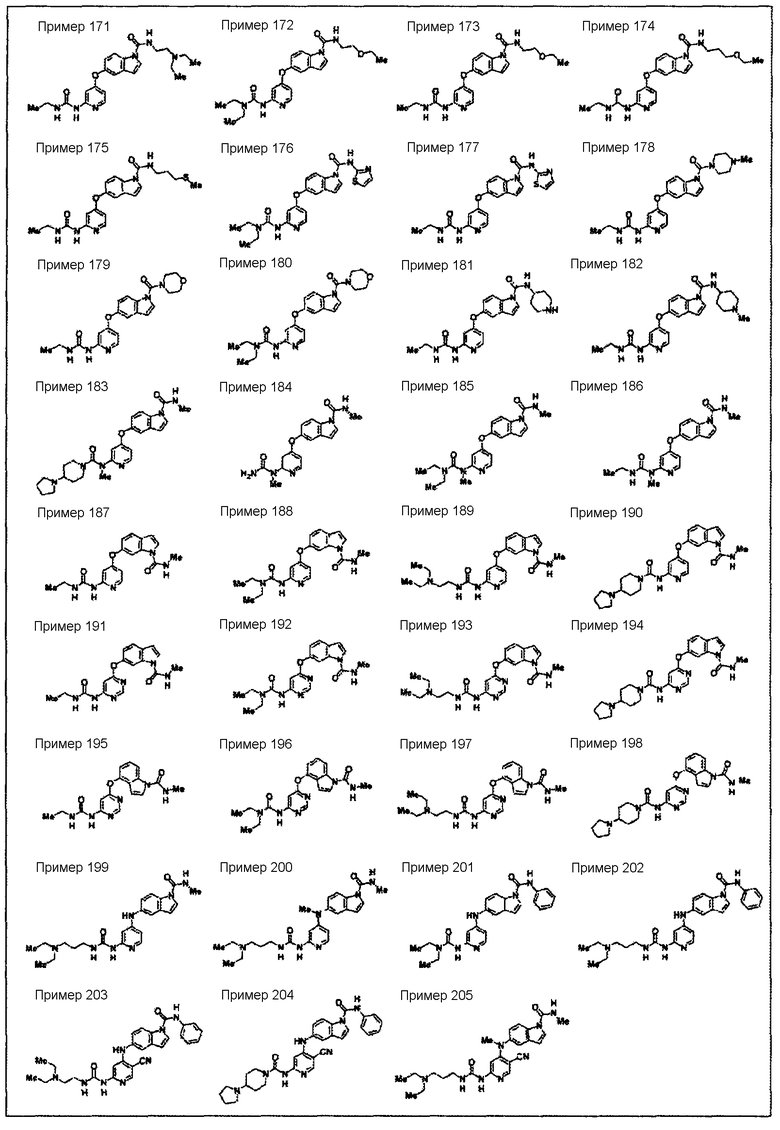
Таблица 17
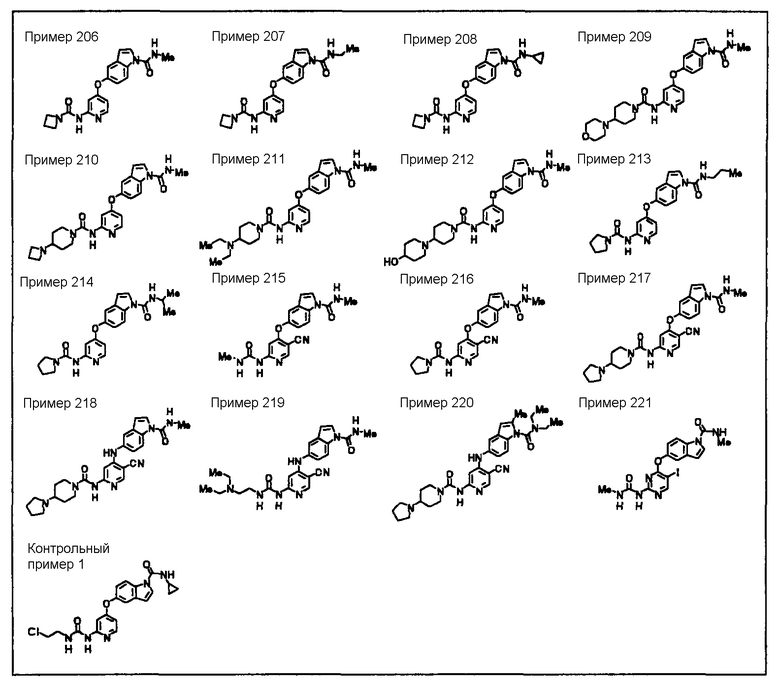
Промышленное применение
Настоящее изобретение позволяет получить новые соединения, которые проявляют (1) мощное ингибирующее действие в отношении формирования трубок клетками эндотелия сосудов под действием VEGF или FGF и (2) мощное ингибирующее действие в отношении рецепторных киназ для VEGF или FGF и которые пригодны в качестве высокоэффективных лекарственных средств.
Следует отметить, что формирование трубок клетками эндотелия сосудов является важным процессом в ангиогенезе, и поэтому соединения, обладающие ингибирующим данный процесс действием, обладают ингибирующим ангиогенез действием. Кроме того, известно, что в организме ангиогенез усиливается аддитивным/синергическим действием множества ангиогенных факторов, представленных VEGF и FGF (Koolwijk P, van Erck MGM, de Vree WJA, Vermeer MA, Weich HA, Hance maaijer R, van Hinsbergh VWM. Cooperative effect of TNF-alpha, bFGF and VEGF on the formation of tubular structures of human microvascular endothelial cells in a fibrin matrix. Role of urokinase activity. J. Cell Biol., 132 P. 1177-1188, (1996)).
Таким образом, ожидается, что соединения изобретения, которые ингибируют формирование трубок, индуцированное VEGF или FGF, продуцированных раковыми клетками и тому подобным, должны оказывать мощное ингибирующее действие на ангиогенез in vivo и должны быть высокоэффективными в качестве ингибиторов ангиогенеза. Более того, соединения изобретения являются высокоэффективными ингибиторами ангиогенеза, и также пригодны в качестве профилактических и терапевтических агентов при заболеваниях, в отношении которых ингибирование ангиогенеза является эффективным, ингибиторов ангиогенеза, противоопухолевых агентов, терапевтических агентов в отношении ангиомы, ингибиторов метастазирования рака, терапевтических агентов в отношении неоваскуляризации сетчатки, терапевтических агентов в отношении диабетической ретинопатии, терапевтических агентов в отношении воспалительного заболевания, терапевтических агентов в отношении воспалительного заболевания, выбранного из деформирующего артрита, ревматоидного артрита, псориаза или отставленной реакции гиперчувствительности, терапевтических агентов в отношении атеросклероза и противоопухолевых агентов на основе ингибирования ангиогенеза.
Кроме того, при применении соединений изобретения в качестве противоопухолевых агентов опухоли включают, например, рак поджелудочной железы, рак желудка, рак ободочной кишки, рак молочной железы, рак предстательной железы, рак легких, рак почек, рак головного мозга, рак крови и рак яичников; опухолями, подходящими для направленного применения, являются рак желудка, рак ободочной кишки, рак предстательной железы или рак почек.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНГИБИТОРЫ БРОМДОМЕНА | 2012 |
|
RU2671571C1 |
| НОВОЕ ПРОИЗВОДНОЕ КУМАРИНА, ОБЛАДАЮЩЕЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2007 |
|
RU2428420C2 |
| ИНГИБИТОРЫ БРОМДОМЕНА | 2012 |
|
RU2647592C2 |
| АЗААДАМАНТАНОВЫЕ ПРОИЗВОДНЫЕ И СПОСОБЫ ПРИМЕНЕНИЯ | 2007 |
|
RU2450002C2 |
| НОВЫЕ ПИРИДИНОВОЕ ПРОИЗВОДНОЕ И ПИРИМИДИНОВОЕ ПРОИЗВОДНОЕ (1) | 2005 |
|
RU2330021C2 |
| БИЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ ИМИДАЗОЛА В КАЧЕСТВЕ СРЕДСТВА ПРОТИВ ВИРУСОВ СЕМЕЙСТВА FLAVIVIRIDAE | 2004 |
|
RU2355687C2 |
| КОНДЕНСИРОВАННОЕ 4-ОКСОПИРИМИДИНОВОЕ ПРОИЗВОДНОЕ | 2005 |
|
RU2358969C2 |
| НОВЫЕ СОЕДИНЕНИЯ И ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ | 2018 |
|
RU2785126C2 |
| СУЛЬФОНАМИДНОЕ ПРОИЗВОДНОЕ И ЕГО МЕДИЦИНСКОЕ ПРИМЕНЕНИЕ | 2013 |
|
RU2607081C2 |
| ИНГИБИТОРЫ ПРОТЕИНКИНАЗ ДЛЯ УСИЛЕНИЯ РЕГЕНЕРАЦИИ ПЕЧЕНИ ИЛИ СНИЖЕНИЯ ИЛИ ПРЕДОТВРАЩЕНИЯ ГИБЕЛИ ГЕПАТОЦИТОВ | 2019 |
|
RU2822216C2 |
Описываются новые азотсодержащие ароматические производные общей формулы I
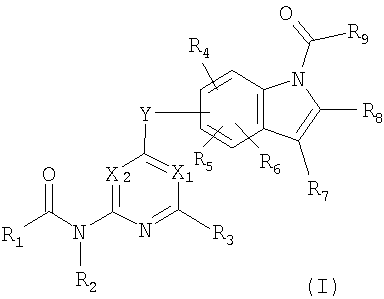
где X1 - N или -CR10=, где R10 - Н, галоид или CN; X2 - N или -CR11= причем X1 и Х2 не могут означать N одновременно;
Y - О или -NRY-, где RY - атом водорода или C1-6 алкильная группа;
R1 - феноксигруппа;
группа -NR12aR12b;
группа
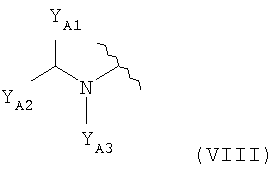 ,
,
группа 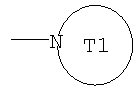 и другие значения;
и другие значения;
R3, R4, R5, R6, и R11 каждый означает водород;
R7 - водород, галоген или С1-6алкильная группа;
R8 - водород или C1-6алкильная группа;
R10 - водород, галоген или циано;
R9 - NR16aR16b или группа формулы
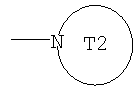 ,
,
где Т2 - пирролидиновое, пиперазиновое кольцо, возможно замещенное C1-6алкильной группой, или морфолиновое кольцо;
R12a и R12b - независимо водород, C1-6алкил, С1-6алкокси;
R2 - водород или C1-6алкил;
R16a - водород или C1-6алкил и
R16в - C1-6алкил, возможно замещенный фенилом, С1-6алкокси, C1-6алкилтио или диC1-6алкиламиногруппой, С3-6алкинил, С3-8циклоалкил, фенил, возможно замещенный галогеном, тиазолил или пиперидинил, возможно замещенный C1-6алкилом,
их соли или гидраты; также описываются фармацевтическая композиция, способ лечения или профилактики опухолевых заболеваний и применение новых соединений для получения средства, пригодного для лечения указанных выше заболеваний. 5 н. и 21 з.п. ф-лы, 17 табл.
(57) 1. Азотсодержащие ароматические производные общей формулы I:
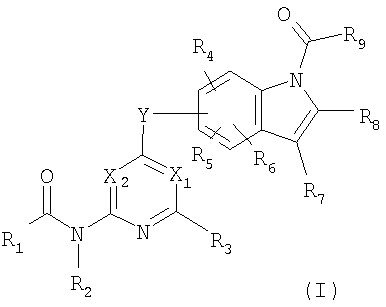
где X1 представляет собой атом азота или группу, представленную формулой -CR10=,
X2 представляет собой атом азота или группу, представленную формулой -CR11= и X1 и Х2 не представляют собой атом азота одновременно;
Y представляет собой атом кислорода или группу, представленную формулой -NRY, где RY представляет собой атом водорода или C1-6алкильную группу;
R1 представляет собой феноксигруппу; группу, представленную формулой -NR12aR12b; группу, представленную формулой
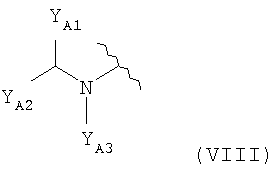
где YA1 и YA2 каждый независимо представляет собой группу, представленную формулой -A10-A11-A12, где А10 представляет собой простую связь или C1-6алкилен; А11 представляет собой простую связь, карбонильную группу или сульфонильную группу; и A12 представляет собой атом водорода, С1-6алкильную группу, С3-8циклоалкильную группу, фенильную группу или группу, представленную формулой -NRA10RA11 группу, представленную формулой -ORA12, где RA10, RA11 и RA11 каждый независимо представляет собой атом водорода, С1-6алкильную группу или С3-8циклоалкильную группу, группу, представленную формулой
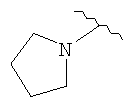
группу, представленную формулой
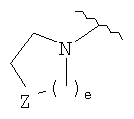 ,
,
где е=2; Z представляет кислород, группу, представленную -CRX7RX8 или группу, представленную формулой -NRX9-; каждый RX7, RX8 и RX9 независимо представляет водород, гидроксил или С1-6алкил; и YA3 представляет водород или С1-6алкил; или R1
представляет группу формулы
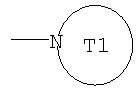 ,
,
где Т1 представляет собой 4-6-членный гетероцикл, выбранный из азетидинового кольца; пирролидинового кольца; пиперидинового кольца, которое может иметь один или более заместителей, выбранных из группы, включающей гидроксильную группу, C1-6алкильную группу и группу, представленную формулой -Т1-Т2-Т3-, где Т1 представляет простую связь или C1-6алкиленовую группу;
Т2 представляет простую связь или С1-6алкиленовую группу или карбонильную группу;
Т3 представляет атом водорода или C1-6алкильную группу, которая может быть замещена гидроксильной группой, С3-8циклоалкильную группу, 4-6-членный гетероцикл, выбранный из азетидиновой группы, пирролидинильной группы, пиперидинильной группы, которая может быть замещена гидроксильной группой, и морфолинильной группы, или группу -N(RT2)(RT3), где RT2 или RT3 каждый независимо представляет атом водорода или С1-6алкильную группу; 4-оксопиперидинового кольца; пиперазинового кольца, которое может иметь один или более заместителей, выбранных из группы, включающей гидроксильную группу, C1-6алкильную группу и группу, представленную формулой -Т1-Т2-Т3-, где Т1 представляет простую связь или С1-6алкиленовую группу; Т2 представляет простую связь или C1-6алкиленовую группу или карбонильную группу; Т3 представляет атом водорода или C1-6алкильную группу, которая может быть замещена гидроксильной группой, С3-8циклоалкильную группу, 4-6-членный гетероцикл, выбранный из азетидиновой группы, пирролидинильной группы, пиперидинильной группы, которая может быть замещена гидроксильной группой, и морфолинильной группы, или группу -N(RT2)(RT3), где RT2 или RT3 каждый независимо представляет атом водорода или С1-6алкильную группу; морфолинового кольца и 1,1-диоксотиоморфолинового кольца;
R3, R4, R5, R6 и R11 каждый независимо представляет собой атом водорода;
R7 представляет атом водорода, галогена или С1-6алкильную группу;
R8 представляет атом водорода или C1-6алкильную группу;
R10 представляет атом водорода, галогена или цианогруппу;
R9 представляет собой группу, представленную формулой -NR16aR16b, или группу, представленную формулой
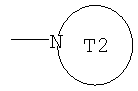 ,
,
где Т2 представляет собой 5-6-членный гетероцикл, выбранный из пирролидинового кольца, пиперазинового кольца, которое может быть замещено C1-6алкильной группой, и морфолинового кольца;
R12a и R12b каждый независимо представляет собой атом водорода, C1-6алкильную группу, С1-6алкоксигруппу;
R2 представляет собой атом водорода или С1-6алкильную группу;
R16a представляет собой атом водорода или С1-6алкильную группу; и
R16b представляет собой С1-6алкильную группу, которая может иметь один или более заместителей, выбранных из фенильной группы, С1-6алкоксигруппы, С1-6алкилтиогруппы и диС1-6алкиламиновую группы, С3-6алкинильную группу, С3-8циклоалкильную группу, фенильную группу, которая может быть замещена атомом галогена, тиазолильную группу или пиперидинильную группу, которая может быть замещена С1-6алкильной группой; или
их соль или гидрат.
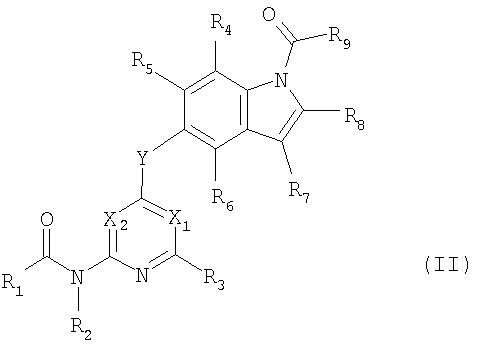
где X1, X2, Y, R1, R2, R3, R4, R5, R6, R7, R8 и R9 имеют значения, указанные в п.1, его соль или гидрат.
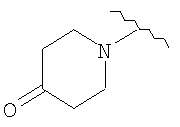
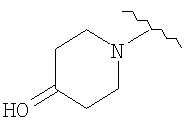
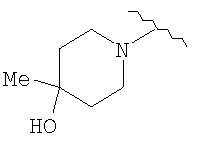
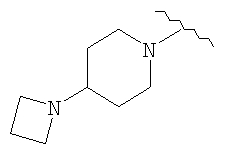
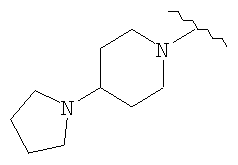
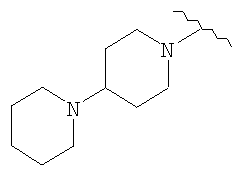
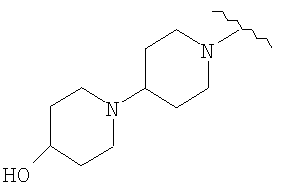
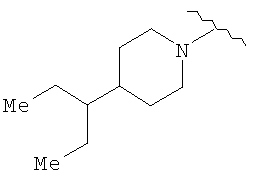
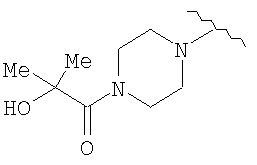
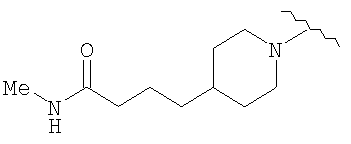
или 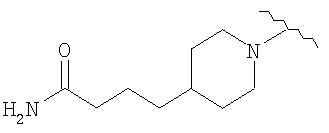





 или
или 
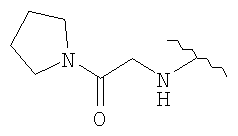
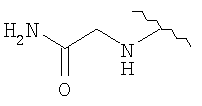
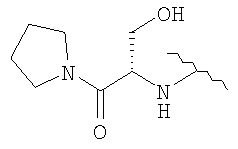
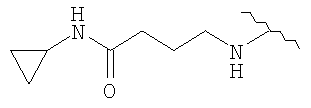
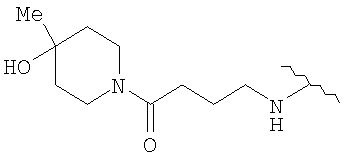
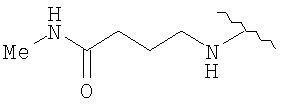
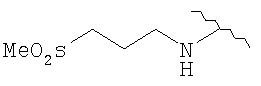
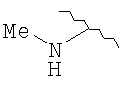 или
или 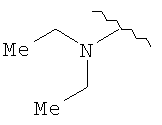
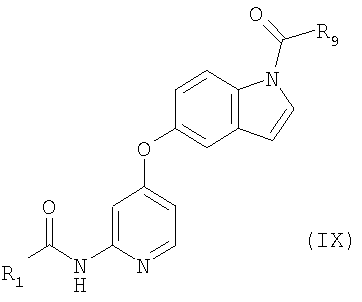 ,
,
где R1 представляет собой группу, представленную формулами:



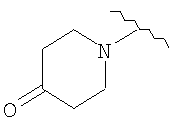









или 
и R9 представляет собой группу, представленную формулой -NHR20, где R20 представляет собой метильную группу, этильную группу или циклопропильную группу.
(1) N1-этил-5-(2-((метоксиламино)карбонил)амино-4-пиримидил)окси-1Н-индолкарбоксамид,
(2) метиламид 5-(6-(3-(3-диэтиламинопропиламино)уреидо) пиримидин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(3) метиламид 5-(6-(((4-гидроксипиперидин-1-ил)карбонил)амино)-пиримидин-4-илокси)-1 Н-индол-1 -карбоновой кислоты,
(4) метиламид 5-(6-((4-пирролидин-1-ил)пиперидин-1-ил) карбониламино)пиримидин-4-илокси)-1 Н-индол-1-карбоновой кислоты,
(5) метиламид 5-(2-(3-((1R)-1-карбамоил-2-фенилэтил)уреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(6) метиламид 5-(2-(3-((1S)-1-карбамоил-2-фенилэтил)уреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(7) метиламид 5-(2-(3-(2-оксо-2-(пирролидин-1-ил)этил)уреидо) пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(8) метиламид 5-(2-(3-(2-(4-гидрокси-4-метилпиперидин-1-ил)-2-оксоэтил)уреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(9) метиламид 5-(2-(3-((1S)-1-карбамоилэтил)уреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(10) метиламид 5-(2-(3-((1S)-1-карбамоил-3-метилбутил)уреидо) пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(11) метиламид 5-(2-(3-карбамоилметилуреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(12) метиламид 5-(2-(3-циклопропилкарбамоилметилуреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(13) метиламид 5-(2-(3-((1S)-1-карбамоил-2-гидроксиэтил)уреидо) пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(14) метиламид 5-(2-(3-((1R)-1-карбамоил-2-гидроксиэтил)уреидо) пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(15) диамид (28)-2-(3-(4-(1-метилкарбамоил-1Н-индол-5-илокси) пиридин-2-ил)уреидо)-1,5-пентандикарбоновой кислоты,
(16) (2S)-2-(3-(4-(1-метилкарбамоил-1Н-индол-5-илокси)пиридин-2-ил)уреидо)сукцинамид,
(17) метиламид 5-(2-(3-((1S)-1-циклопропилкарбамоил-2-гидроксиэтил) уреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(18) метиламид 5-(2-(3-((1S)-1-гидроксиметил-2-оксо-2-пирролидин-1-илэтил)уреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(19) метиламид 5-(2-(3-((1R)-1-гидроксиметил-2-оксо-2-пирролидин-1-илэтил)уреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(20) метиламид 5-(2-(3-((1S)-1-гидроксиметил-2-оксо-2-пиперидин-1 -илэтил)уреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(21) метиламид 5-(2-(3-((1R)-1-гидроксиметил-2-оксо-2-пиперидин-1-илэтил)уреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(22) метиламид 5-(2-(3-((1S)-1-гидроксиметил-2-(4-гидроксипиперидин-1-ил)-2-оксоэтил)уреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(23) метиламид 5-(2-(3-((1S)-1-гидроксиметил-2-(морфолин-4-ил)-2-оксоэтил)уреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(24) метиламид 5-(2-(3-(2-циклопропилкарбамоилэтил)уреидо) пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(25) метиламид 5-(2-(3-(3-оксо-3-(пирролидин-1-ил)пропил)уреидо) пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(26) метиламид 5-(2-(3-(3-(4-гидрокси-4-метилпиперидин-1-ил)-3-оксопропил)уреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(27) N1-этил-5-(2-(((2-этоксиэтил)амино)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(28) N1-метил-5-(2-((4-(2-гидрокси-2-метилпропионил)пиперазин-1-ил)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(29) N1-метил-5-(2-((3-(диэтиламино)пропиламино)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(30) N1-метил-5-(2-(((3-(4-гидроксипиперидин)пропил)амино) карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(31) N1-метил-5-(2-(((3-(4-метилпиперазин-1-ил)пропил)амино) карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(32) метиламид 5-(2-(3-(4-оксо-4-(пирролидин-1-ил)бутил)уреидо) пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(33) метиламид 5-(2-(3-(3-(циклопропилкарбамоил)пропил)уреидо) пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(34) метиламид 5-(2-(3-(4-(4-гидрокси-4-метилпиперидин-1-ил)-4-оксобутил)уреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(35) метиламид 5-(2-(3-(3-(диэтилкарбамоил)пропил)уреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(36) метиламид 5-(2-(3-(3-(метилкарбамоил)пропил)уреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(37) N1-метил-5-(2-(пирролидин-1-илкарбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(38) N1-метил-5-(2-(пиперидин-1-илкарбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(39) N1-метил-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(40) N1-метил-5-(2-(4-оксопиперидин-1-илкарбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(41) метиламид 5-(2-(((4-гидрокси-4-метилпиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(42) N1-метил-5-(2-((4-(1-гидрокси-1-метилэтил)пиперидин)карбонил) амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(43) метиламид 5-(2-(((4-(3-метилкарбамоилпропил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(44) метиламид 5-(2-(((4-(3-карбамоилпропил)пиперидин-1-ил) карбонил)амино)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(45) метиламид 5-(2-((4-((пирролидин-1-ил)карбонил)пиперидин-1-ил)карбониламино)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(46) N1-метил-5-(2-(((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1Н-1-индолкарбоксамид,
(47) N1-метил-5-(2-(((4-(пиперидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1Н-1-индолкарбоксамид,
(48) N1-метил-5-(2-((4-этилпиперазин-1-ил)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(49) N1-метил-5-(2-((4-(2-гидроксиэтил)пиперазин-1-ил)карбонил) амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(50) N1-метил-5-(2-((3-метилсульфонилпропиламино)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(51) N1-метил-5-(2-((4-(2-диметиламиноацетил)пиперазин-1-ил) карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(52) N1-метил-5-(2-((4-циклогексилпиперазин-1-ил)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(53) N4-(4-(1-(метиламино)карбонил-1Н-5-индолил)окси-2-пиридил)-4-морфолинкарбоксамид,
(54) N1-метил-5-(2-((1,1-диоксотиоморфолин-4-илкарбонил)амино) пиридин-4-илокси)-1Н-1-индолкарбоксамид,
(55) этиламид 5-(2-(3-((1R)-1-гидроксиметил-2-оксо-2-пирролидин-1-илэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(56)этиламид 5-(2-(3-((1S)-1-гидроксиметил-2-оксо-2-пирролидин-1-илэтил)уреидо)пиридин-4-илокси)-1H-индол-1-карбоновой кислоты,
(57) этиламид 5-(2-(3-((1R)-1-гидроксиметил-2-оксо-2-пиперидин-1-илэтил)уреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(58) этиламид 5-(2-(3-((1S)-1-гидроксиметил-2-оксо-2-пиперидин-1-илэтил)уреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(59) этиламид 5-(2-(3-(2-(4-гидрокси-4-метилпиперидин-1-ил)-2-оксоэтил)уреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(60) N1-этил-5-(2-((((1-метил-4-пиперидил)метил)амино)карбонил) амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(61) N1-этил-5-(2-(((2-(диэтиламино)этил)амино)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(62) N1-этил-5-(2-(((2-(морфолин-4-ил)этил)амино)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(63) N1-этил-5-(2-(((2-(4-гидроксипиперидин)этил)амино)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(64) N1-метил-5-(2-(((2-(4-гидроксипиперидин)этил)амино)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(65) N1-этил-5-(2-((3-(диэтиламино)пропиламино)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(66) N1-этил-5-(2-(((3-(морфолин-4-ил)пропил)амино)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(67) N1-этил-5-(2-(((3-(4-метилпиперазин-1-ил)пропил)амино) карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(68) N1-циклопропил-5-(2-(((4-(пирролидин-1-ил)пиперидин-1-ил) карбонил)амино)пиридин-4-илокси)-1Н-1-индолкарбоксамид,
(69) циклопропиламид 5-(2-(3-((1R)-1-гидроксиметил-2-оксо-2-пирролидин-1-илэтил)уреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(70) циклопропиламид 5-(2-(3-((18)-1-гидроксиметил-2-оксо-2-пирролидин-1-илэтил)уреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(71) циклопропиламид 5-(2-(3-(2-оксо-2-(пирролидин-1-ил)этил) уреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(72) циклопропиламид 5-(2-(3-(3-оксо-3-(пирролидин-1-ил)пропил) уреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(73) циклопропиламид 5-(2-(3-((1R)-1-гидроксиметил-2-оксо-2-пиперидин-1-илэтил)уреидо)пиридин-4-илокси)-1 Н-индол-1 -карбоновой кислоты,
(74) циклопропиламид 5-(2-(3-((1S)-1-гидроксиметил-2-оксо-2-пиперидин-1-илэтил)уреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(75) N1-фенил-5-(2-(((3-(диэтиламино)пропил)амино)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(76) N1-фенил-5-(2-(((3-(4-метилпиперазин-1-ил)пропил)амино) карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(77) N1-этил-5-(2-(((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1Н-1-индолкарбоксамид,
(78) этиламид 5-(2-(((4-гидрокси-4-метилпиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(79) N1-этил-5-(2-((4-гидроксипиперидин-1-ил)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(80) N1-этил-5-(2-(пиперидин-1-илкарбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(81) N1-этил-5-((2-((пирролидин-1-илкарбонил)амино)-4-пиридил)окси)-1Н-1-индолкарбоксамид,
(82) N4-(4-((1-(этиламино)карбонил-1Н-5-индолил)окси)-2-пиридил)-4-морфолинкарбоксамид,
(83) N1-этил-5-(2-((1,1-диоксотиоморфолин-4-илкарбонил)амино)пиридин-4-илокси)-1Н-1-индолкарбоксамид,
(84) N1-этил-5-(2-((метоксиламино)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(85) N1-циклопропил-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(86) N1-циклопропил-5-(2-(((4-гидрокси-4-метилпиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1Н-1-индолкарбоксамид,
(87) N4-(4-(1-(циклопропиламино)карбонил-1Н-5-индолил)окси-2-пиридил)-4-морфолинкарбоксамид,
(88) N1-циклопропил-5-(2-((пирролидин-1-илкарбонил)амино)-4-пиридил)окси-1Н-1-индолкарбоксамид,
(89) N1-циклопропил-5-(2-(пиперидин-1-илкарбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(90) N4-(4-(1-(циклопентиламино)карбонил-1Н-5-индолил)окси-2-пиридил)-4-морфолинкарбоксамид,
(91) циклопентиламид 5-(2-(((4-гидроксипиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(92) N1-циклопентил-5-(2-((4-(пирролидин-1-ил)пиперидин-1-илкарбонил)амино)пиридин-4-илокси)-1 Н-1 -индолкарбоксамид,
(93) N1-(3-метилбутил)-5-(2-(((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1Н-1-индолкарбоксамид,
(94) N1-(3-метилбутил)-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(95) N4-(4-(1-((3-метилбутил)амино)карбонил-1Н-5-индолил)окси-2-пиридил)-4-морфолинкарбоксамид,
(96) N1-(1-этилпропил)-5-(2-(((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1Н-1-индолкарбоксамид,
(97) N1-(1-этилпропил)-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(98) N4-(4-(1-((1-этилпропил)амино)карбонил-1Н-5-индолил)окси-2-пиридил)-4-морфолинкарбоксамид,
(99) N4-(4-(1-((1-пентил)амино)карбонил-1Н-5-индолил)окси-2-пиридил)-4-морфолинкарбоксамид,
(100) N1-(1-пентил)-5-(2-(((4-гидроксипиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1Н-1-индолкарбоксамид,
(101) N1-(1-пентил)-5-(2-((4-(пирролидин-1-ил)пиперидин-1-илкарбонил)амино)пиридин-4-илокси)-1Н-1-индолкарбоксамид,
(102) N1-метил-3-хлор-5-(2-(((3-(диэтиламино)пропил)амино) карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(103) N1-метил-3-хлор-5-(2-((4-(пирролидин-1-ил)пиперидин) карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(104) 1Н-метил-3-хлор-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(105) N1-метил-3-хлор-5-(2-(((3-(4-гидроксипиперидин)пропил)амино)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(106) N1-метил-3-хлор-5-(2-((4-(2-гидроксиэтил)пиперазин-1-ил)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(107) N4-(4-(3-хлор-1-(метиламино)карбонил-1Н-5-индолил)окси-2-пиридил)-4-морфолинкарбоксамид,
(108) N1-метил-3-хлор-5-(2-((4-этилпиперазин-1-ил)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(109) N1-этил-3-хлор-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(110) N1-этил-3-хлор-5-(2-(((3-(4-гидроксипиперидин)пропил)амино)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(111) N1-этил-3-хлор-5-(2-(((3-(диэтиламино)пропил)амино)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(112) N1,3-диметил-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(113) N1,3-диметил-5-(2-((4-(пирролидин-1-ил)пиперидин)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(114) N1-циклопропил-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-3-метил-1Н-1-индолкарбоксамид,
(115) N1-циклопропил-5-(2-((4-(2-гидроксиэтил)пиперазин-1-ил)карбонил)амино-4-пиридил)окси-3-метил-1Н-1-индолкарбоксамид,
(116) N1-метил-5-(2-((метиламино)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(117) N1-метил-5-(2-((диэтиламино)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(118) N1-(2-пропинил)-5-(2-((пирролидин-1-ил)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(119) N1-метил-5-(2-(азетидин-1-илкарбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(120) N1-этил-5-(2-(азетидин-1-илкарбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(121) N1-циклопропил-5-(2-(азетидин-1-илкарбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(122) N1-метил-5-(2-(((4-(морфолин-4-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1Н-1-индолкарбоксамид,
(123) N1-метил-5-(2-(((4-(азетидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1Н-1-индолкарбоксамид,
(124) N1-метил-5-(2-(((4-(диэтиламино)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1Н-1-индолкарбоксамид,
(125) N1-метил-5-(2-(((4-(4-гидроксипиперидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1Н-1-индолкарбоксамид, и
(126) N1-пропил-5-(2-(пирролидин-1-илкарбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид.
(1) метиламид 5-(2-(3-(2-оксо-2-(пирролидин-1-ил)этил)уреидо)
пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(2) метиламид 5-(2-(3-карбамоилметилуреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(3) метиламид 5-(2-(3-((1S)-1-гидроксиметил-2-оксо-2-пирролидин-1-илэтил)уреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(4) N1-метил-5-(2-((4-(2-гидрокси-2-метилпропионил)пиперазин-1-ил)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(5) метиламид 5-(2-(3-(4-оксо-4-(пирролидин-1-ил)бутил)уреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(6) метиламид 5-(2-(3-(3-(циклопропилкарбамоил)пропил)уреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(7) метиламид 5-(2-(3-(4-(4-гидрокси-4-метилпиперидин-1-ил)-4-оксобутил)уреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(8) метиламид 5-(2-(3-(3-(метилкарбамоил)пропил)уреидо)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(9) Н1-метил-5-(2-(пирролидин-1-илкарбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(10) N1-метил-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(11) N1-метил-5-(2-(4-оксопиперидин-1-илкарбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(12) метиламид 5-(2-(((4-гидрокси-4-метилпиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1Н-индол-1 -карбоновой кислоты,
(13) метиламид 5-(2-(((4-(3-метилкарбамоилпропил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(14) метиламид 5-(2-(((4-(3-карбамоилпропил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(15) N1-метил-5-(2-(((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1Н-1-индолкарбоксамид,
(16) N1-метил-5-(2-(((4-(пиперидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1Н-1-индолкарбоксамид,
(17) N1-метил-5-(2-((3-метилсульфонилпропиламино)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(18) N4-(4-(1-(метиламино)карбонил-1Н-5-индолил)окси-2-пиридил)-4-морфолинкарбоксамид,
(19) N1-циклопропил-5-(2-(((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1Н-1-индолкарбоксамид,
(20) этиламид 5-(2-(((4-гидрокси-4-метилпиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(21) N1-этил-5-(2-((4-гидроксипиперидин-1-ил)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(22) N1-этил-5-((2-((пирролидин-1-илкарбонил)амино)-4-пиридил)окси)-1Н-1-индолкарбоксамид,
(23) N4-(4-((1-(этиламино)карбонил-1Н-5-индолил)окси)-2-пиридил)-4-морфолинкарбоксамид,
(24) N1-циклопропил-5-(2-((пирролидин-1-илкарбонил)амино)-4-пиридил)окси-1Н-1-индолкарбоксамид,
(25) N1-метил-3-хлор-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(26) N1-метил-5-(2-((метиламино)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(27) N1-метил-5-(2-((диэтиламино)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(28) N1-(2-пропинил)-5-(2-((пирролидин-1-ил)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(29) N1-метил-5-(2-(азетидин-1-илкарбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(30) N1-этил-5-(2-(азетидин-1-илкарбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(31) N1-циклопропил-5-(2-(азетидин-1-илкарбонил)амино-4-пиридил) окси-1Н-1-индолкарбоксамид,
(32) N1-метил-5-(2-(((4-(морфолин-4-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1Н-1-индолкарбоксамид,
(33) N1-метил-5-(2-(((4-(азетидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1Н-1-индолкарбоксамид,
(34) N1-метил-5-(2-(((4-(диэтиламино)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1Н-1-индолкарбоксамид,
(35) N1-метил-5-(2-(((4-(4-гидроксипиперидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1Н-1-индолкарбоксамид, и
(36) N1-пропил-5-(2-(пирролидин-1-илкарбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид.
(1) метиламид 5-(2-(((4-гидрокси-4-метилпиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1Н-индол-1-карбоновой кислоты,
(2) N1-метил-5-(2-((4-гидроксипиперидин)карбонил)амино-4-пиридил)окси-1Н-1-индолкарбоксамид,
(3) N1-метил-5-(2-(((4-(пирролидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1Н-1-индолкарбоксамид,
(4) N1-метил-5-(2-(((4-(пиперидин-1-ил)пиперидин-1-ил)карбонил)амино)пиридин-4-илокси)-1Н-1-индолкарбоксамид, и
(5) N4-(4-(1-(метиламино)карбонил-1H-индолил)окси-2-пиридил)-морфолинкарбоксамид.
Приоритет по пунктам:
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| ПРОИЗВОДНЫЕ ИНДОЛА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ПРОЯВЛЯЮЩАЯ СВЯЗЫВАЮЩУЮ СЕЛЕКТИВНОСТЬ ПО ОТНОШЕНИЮ К РЕЦЕПТОРАМ 5-НТ И ВАЗОКОНСТРИКТОРНОЕ ДЕЙСТВИЕ, СВЯЗАННОЕ С АГОНИЗМОМ РЕЦЕПТОРОВ 5 НТ, И СПОСОБ СЕЛЕКТИВНОГО СВЯЗЫВАНИЯ 5-НТ-РЕЦЕПТОРОВ ИЛИ АГОНИСТИЧЕСКОГО ДЕЙСТВИЯ НА 5-НТ-РЕЦЕПТОРЫ | 1993 |
|
RU2117667C1 |
| ПРОИЗВОДНЫЕ ИНДОЛ-3-ИЛА | 2001 |
|
RU2257380C2 |
Авторы
Даты
2007-11-20—Публикация
2003-08-28—Подача