Область изобретения
Настоящее изобретение относится к производным индануксусной кислоты и их использованию в фармацевтических композициях для лечения заболеваний, таких как диабет, ожирение, гиперлипидемия и атеросклеротическое заболевание. Настоящее изобретение также относится к промежуточным продуктам, пригодным для использования при получении производных индануксусной кислоты, и к способам получения.
Предшествующий уровень
Диабет типа II является самой распространенной формой диабета и у 90 - 95% пациентов, страдающих гипергликемией, обнаруживается эта форма заболевания. При диабете типа II, по-видимому, происходит уменьшение массы β-клеток поджелудочной железы, наблюдается несколько отдельных дефектов секреции инсулина и снижение чувствительности ткани к инсулину. Симптомы и последствия этой формы диабета включают усталость, частое мочеиспускание, жажду, пелену перед глазами, частые инфекции и медленное заживление ран, вызванные диабетом неврологические поражения, ретинопатию, микро- и макроскопические поражения кровеносных сосудов и заболевания сердца и почек.
Резистентность к метаболическим воздействиям инсулина является одной из основных особенностей диабета типа II. Резистентность к инсулину характеризуется нарушениями поглощения и использования глюкозы в чувствительных к инсулину органах-мишенях, например, в адипоцитах и скелетных мышцах, и нарушениями ингибирования процесса выведения глюкозы печенью. Функциональная инсулиновая недостаточность, резистентность к инсулину на периферии и неспособность инсулина подавлять процесс выведения глюкозы печенью приводят к гипергликемии натощак. β-Клетки поджелудочной железы компенсируют резистентность к инсулину, вырабатывая инсулин в повышенных уровнях. Однако β-клетки неспособны поддерживать такую значительную выработку инсулина и в конечном счете индуцированная глюкозой выработка инсулина снижается, что приводит к нарушению гомеостаза глюкозы и последующему развитию явного диабета. Гиперинсулинемия также связана с резистентностью к инсулину, гипертриглицеридемией, низким уровнем липопротеинов высокой плотности (ЛВП) холестерина и повышенным содержанием липопротеинов низкой плотности (ЛНП) в плазме. Сочетание резистентности к инсулину и гиперинсулинемии с этими нарушениями метаболизма называют "синдромом X" и он тесно связан с повышением опасности гипертензии и ишемической болезни сердца.
Ожирение является избыточным накоплением жировой ткани. Избыток жировой ткани приводит к развитию тяжелых патологических состояний, например, диабета типа II, гипертензии, заболевания коронарной артерии, гиперлипидемии, ожирения и некоторых злокачественных образований. Адипоциты также могут влиять на гомеостаз глюкозы посредством продуцирования фактора некроза опухолевых клеток a (TNFa) и других молекул.
Известно, что атеросклеротическое заболевание вызывается целым рядом факторов, например, гипертензией, низкими уровнями ЛВП и высокими уровнями ЛНП. Связанные с атеросклерозом заболевания включают сердечно-сосудистые заболевания, ишемическую болезнь сердца (ИБС), цереброваскулярные заболевания и заболевания периферических сосудов. Ишемическая болезнь сердца включает смерть от ИБС, инфаркт миокарда и коронарную реваскуляризацию. Цереброваскулярные заболевания включают ишемический или гемморрагический удар и преходящие ишемические приступы.
В соответствии с этим, несмотря на наличие некоторых фармацевтических препаратов, которые используются для лечения этих заболеваний, сохраняется потребность в новых фармацевтических препаратах, которые одновременно являются безопасными и эффективными средствами лечения этих заболеваний, а также в эффективных способах их получения.
Настоящее изобретение относится к соединениям, которые пригодны для использования при лечении диабета и родственных заболеваний, таких как синдром X, нарушение переносимости глюкозы, нарушение уровня глюкозы в крови натощак и гиперинсулинемия, ожирение, атеросклеротическое заболевание, дислипидемия и родственные заболевания, такие как гипертриглицеридемия, низкое содержание ЛВП холестерина и гиперхолестеринемия, сердечно-сосудистые заболевания и цереброваскулярные заболевания.
Описание изобретения
Настоящее изобретение охватывает соединения формулы I,
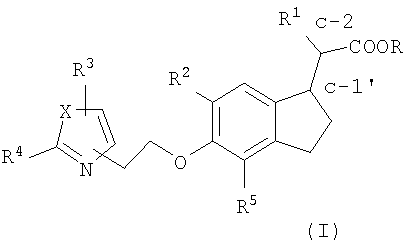
где R означает Н или C1-C6 алкил;
R1 означает Н, COOR, С3-С8циклоалкил или C1-С6 алкил, С2-С6алкенил или C1-C6 алкоксил, каждый из которых может быть незамещенным или содержать в качестве заместителей фтор, метилендиоксифенил или фенил, который может быть незамещенным или содержать в качестве заместителей R6;
R2 означает Н, галоген или C1-C6 алкил, который может быть незамещенным или содержать в качестве заместителей C1-С6алкоксил, оксогруппу, фтор,
или
R2 означает фенил, фурил, тиенил, пирролил, оксазолил, тиазолил, имидазолил, пиразолил, изоксазолил, изотиазолил, триазолил, оксадиазолил, тиадиазолил, тет-разолил, пиридил, пирролидинил, пиперидинил, тетрагидропиранил, тетрагидротиопиранил, пиперазинил или морфолинил, каждый из которых может быть незамещенным или содержать в качестве заместителей R6;
R3 означает Н, C1-C6 алкил или фенил, который может быть незамещенным или содержать в качестве заместителей R6;
Х означает О или S;
R4 означает C1-C6алкил или С3-С8циклоалкил, каждый из которых может быть незамещенным или содержать в качестве заместителей фтор, оксогруппу или С1-С6алкоксил, который может быть незамещенным или содержать в качестве заместителей С1-С6алкоксил или фенил, необязательно содержащий в качестве заместителя R6, каждый из которых может содержать в качестве заместителя фенил, нафтил, фурил, тиенил, пирролил, тетрагидрофурил, пирролидинил, пирролинил, тет-рагидротиенил, оксазолил, тиазолил, имидазолил, пиразолил, изоксазолил, изотиазолил, триазолил, оксадиазолил, тиадиазолил, тетразолил, пиридил, пиперидинил, тетрагидропиранил, тетрагидротиопиранил, пиримидинил, пиразинил, пиридазинил, пиперазинил, морфолинил, бензофурил, дигидробензофурил, бензотиенил, дигидробензотиенил, индолил, индолинил, индазолил, бензоксазолил, бензотиазолил, бензимидазолил, бензизоксазолил, бензизотиазолил, бензодиоксолил, хинолил, изохинолил, хиназолинил, хиноксазолинил, дигидробензопиранил, дигидробензотиопиранил или 1,4-бензодиоксанил, каждый из которых может быть незамещенным или содержать в качестве заместителей R6,
или
C1-С6алкил также может содержать в качестве заместителя С3-С8 циклоалкил или феноксил, который может быть незамещенным или содержать в качестве заместителей R6 или фенил, нафтил, фурил, тиенил, пирролил, тетрагидрофурил, пирролидинил, пирролинил, тетрагидротиенил, оксазолил, тиазолил, имидазолил, пиразолил, изоксазолил, изотиазолил, триазолил, оксадиазолил, тиадиазолил, тетразолил, пиридил, пиперидинил, тетрагидропиранил, тетрагидротиопиранил, пиримидинил, пиразинил, пиридазинил, пиперазинил, морфолинил, бензофурил, дигидробензофурил, бензотиенил, дигидробензотиенил, индолил, индолинил, индазолил, бензоксазолил, бензотиазолил, бензимидазолил, бензизоксазолил, бензизотиазолил, бензодиоксолил, хинолил, изохинолил, хиназолинил, хиноксазолинил, дигидробензопиранил, дигидробензотиопиранил или 1,4-бензодиоксанил, каждый из которых может быть незамещенным или содержать в качестве заместителей R6,
или
R4 означает фенил, нафтил, фурил, тиенил, пирролил, тетрагидрофурил, пирролидинил, пирролинил, тетрагидротиенил, оксазолил, тиазолил, имидазолил, пиразолил, изоксазолил, изотиазолил, триазолил, оксадиазолил, тиадиазолил, тетразолил, пиридил, пиперидинил, тетрагидропиранил, тетрагидротиопиранил, пиримидинил, пиразинил, пиридазинил, пиперазинил, морфолинил, бензофурил, дигидробен-зофурил, бензотиенил, дигидробензотиенил, индолил, индолинил, индазолил, бензоксазолил, бензотиазолил, бензимидазолил, бензизоксазолил, бензизотиазолил, бензодиоксолил, хинолил, изохинолил, хиназолинил, хиноксазолинил, дигидробензопиранил, дигидробензотиопиранил или 1,4-бензодиоксанил, каждый из которых может быть незамещенным или содержать в качестве заместителей R6 или фенил, фурил, тиенил, пирролил, оксазолил, тиазолил, имидазолил, пиразолил, изоксазолил, изотиазолил, триазолил, оксадиазолил, тиадиазолил, тетразолил, пиридил, пирролидинил, пиперидинил, тетрагидропиранил, тетрагидротиопиранил, пиперазинил, морфолинил, бензодиоксолил, дигидробензофуранил, индолил, пиримидинил или феноксил, каждый из которых может быть незамещенным или содержать в качестве заместителей R6;
R5 означает Н, галоген или C1-C6алкил, необязательно содержащий в качестве заместителя оксогруппу;
R6 означает галоген, CF3, C1-C6алкил, необязательно содержащий в качестве заместителя оксогруппу или гидроксил, или C1-C6алкоксил, необязательно содержащий в качестве заместителя фтор;
и их фармацевтически приемлемые соли и сложные эфиры. Определенные ниже термины во всем изобретении означают следующее:
"C1-C6алкил" означает линейные или разветвленные цепочечные алкильные группы, содержащие от одного до примерно шести атомов углерода. Такие группы включают метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, неопентил, 2-пентил, н-гексил, 2-гексил, 3-гексил, 2,3-диметилбутил и т.п.
"С2-С6алкенил" означает линейные или разветвленные цепочечные алкенильные группы, содержащие от двух до примерно шести атомов углерода и содержащие одну или большее количество двойных связей. Такие группы включают этенил, пропенил, изопропенил, 2-изобутенил, 4-пентенил, 5-гексенил и т.п.
"С3-С8 циклоалкил" означает насыщенные моноциклические алкильные группы, содержащие от 3 до примерно 9 атомов углерода и включает такие группы, как циклопропил, циклопентил, циклогексил и т.п.
"C1-C6 алкоксил" означает линейные или разветвленные цепочечные алкоксильные группы, содержащие от одного до примерно шести атомов углерода и включает такие группы, как метоксил, этоксил, н-пропоксил, изопропоксил, н-бутоксил, изобутоксил, втор-бутоксил, трет-бутоксил и т.п.
"Галоген" означает фтор, хлор, бром или йод.
Если указано, что алкильная, циклоалкильная, алкенильная или алкоксильная группа содержит в качестве заместителя фтор, она может содержать в качестве заместителей один или большее количество атомов фтора при любом доступном атоме углерода вплоть до перфторирования.
Если указано, что алкильный заместитель содержит в качестве заместителя оксо-группу, это означает замещение атомом кислорода с двойной связью, который совместно с атомом углерода, к которому он присоединен, образует карбонильную группу -(С=O)-.
Если указано, что какой-либо фрагмент является замещенным, то он может содержать один или большее количество указанных заместителей, которые могут располагаться в любом доступном положении этого фрагмента. Если у какого-либо фрагмента имеется два или большее количество заместителей, то каждый заместитель может быть определен независимо от любого другого заместителя и в соответствии с этим они могут быть одинаковыми или разными.
Термин "необязательно содержащий заместители" означает, что модифицированный таким образом фрагмент может быть незамещенными или содержать указанный заместитель (заместители).
R3 может быть присоединен к гетероциклическому фрагменту соединения формулы 1 в положении 4 или 5 (т.е. к любому доступному атому углерода) и, соответственно, оставшаяся часть молекулы будет присоединена к оставшемуся доступному атому углерода.
Примеры соединений формулы I, которые иллюстрируют настоящее изобретение, но никоим образом его не ограничивают, приведены в таблице 1.
Таблица 1.
Иллюстративные примеры соединений Формулы I
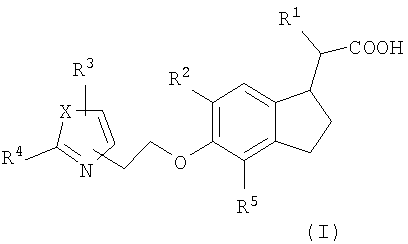
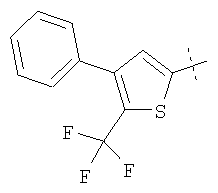
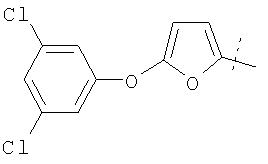



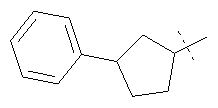
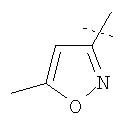
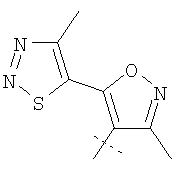
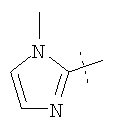
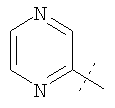

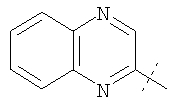

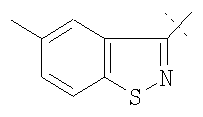
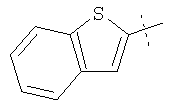

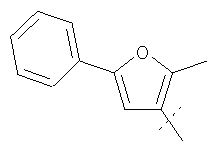
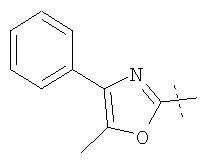

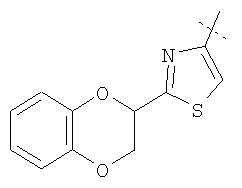
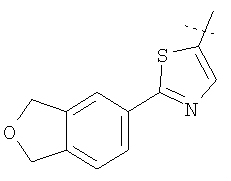
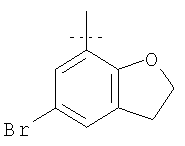
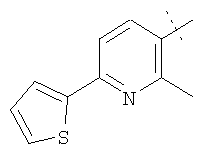

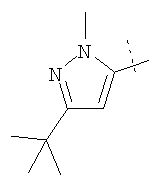




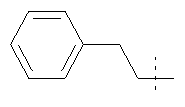
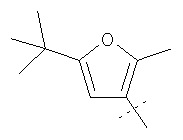


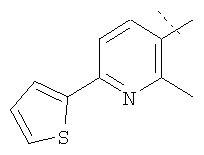

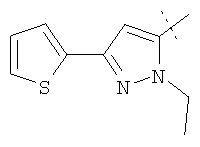
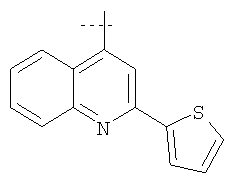




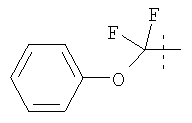


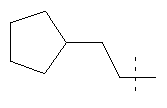
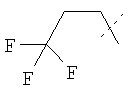

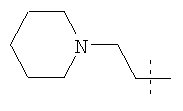
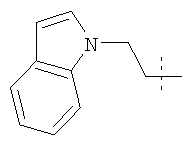


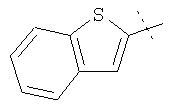


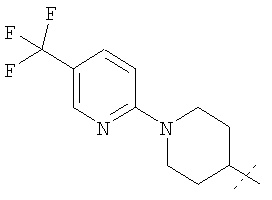
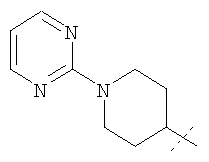

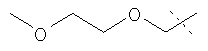

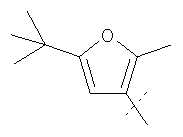
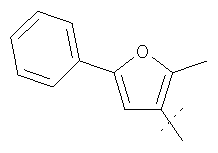

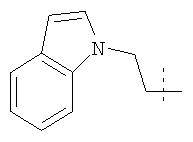
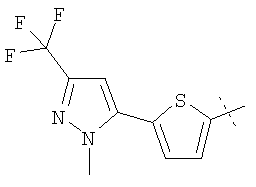
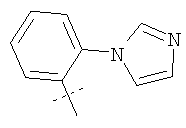
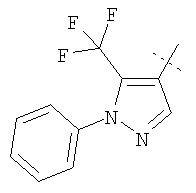
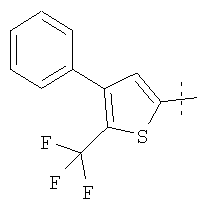


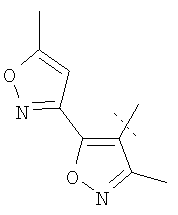
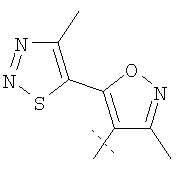
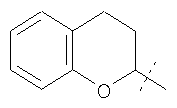
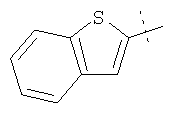
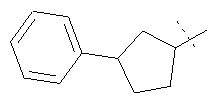


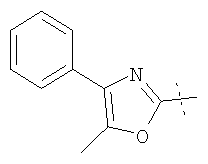
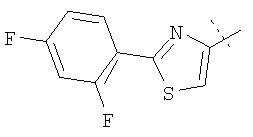
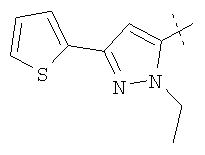



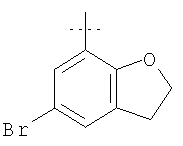




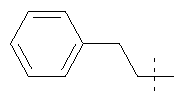




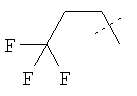












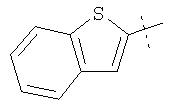



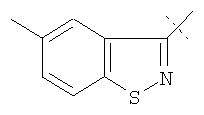
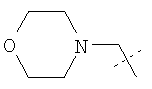
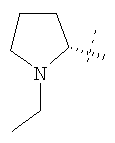






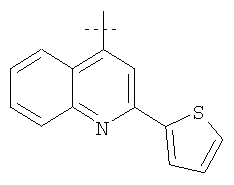


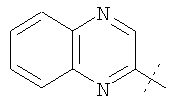

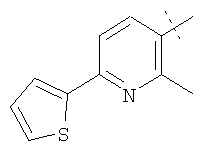
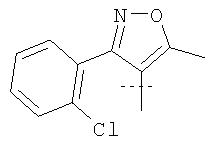
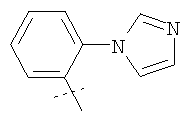
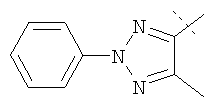
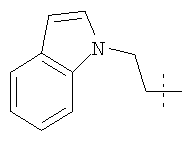
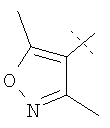

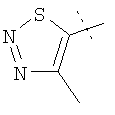

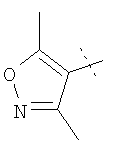

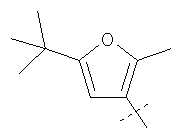
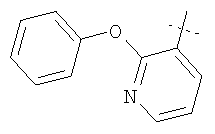
Соль соединения формулы I можно получить in situ во время окончательного выделения и очистки соединения или путем введения очищенного соединения, использующегося в виде свободного основания, в реакцию с подходящей органической или неорганической кислотой и выделения полученной таким образом соли. Аналогичным образом, когда соединение формулы I содержит карбоксильный фрагмент (например, R=H), соль указанного соединения формулы I можно получить путем его отдельного введения в реакцию с подходящей органической или неорганической кислотой и выделения полученной таким образом соли.
Термин "фармацевтически приемлемая соль" означает относительно нетоксичную молекулярную соль с неорганической или органической кислотой соединения, соответствующего настоящему изобретению (см., например, Berge et al., J. Pharm. Sci. 66:1-19, 1977).
Типичные соли соединения формулы I включают обычные нетоксичные соли и четвертичные соли аммония, которые получают, например, из неорганических или органических кислот или оснований способами, хорошо известными в данной области техники. Например, такие молекулярные соли кислот включают ацетат, адипат, альгинат, аскорбат, аспартат, бензоат, бензолсульфонат, бисульфат, бутират, цитрат, камфорат, камфорсульфонат, циннамат, циклопентанпропионат, глюконат, додецилсульфат, этансульфонат, фумарат, глюкогептаноат, глицерофосфат, гемисульфат, гептаноат, гексаноат, гидрохлорид, гидробромид, гидройодид, 2-гидроксиэтансульфонат, итаконат, лактат, малеат, манделат, метансульфонат, 2-нафталинсульфонат, никотинат, нитрат, оксалат, пальмоат, пектинат, персульфат, 3-фенилпропионат, пикрат, пивалат, пропионат, сукцинат, сульфонат, тартрат, тиоцианат, тозилат, ундеканоат и т.п.
Основные соли включают, например, соли щелочных металлов, такие как соли калия и натрия, щелочноземельных металлов, такие как соли кальция и магния, и соли аммония с органическими основаниями, такими как дициклогексиламин и N-метил-D-глюкамин. Кроме того, содержащие азот основные группы в сопряженном основании можно превратить в четвертичные соединения с помощью таких реагентов, как низшие алкилгалогениды, такие как метил-, этил-, пропил- и бутилхлориды, -бромиды и -йодиды; диалкилсульфаты, такие как диметил-, диэтил- и дибутилсульфаты, и диамилсульфаты, галогениды с длинными цепями, такие какдецил-, лаурил-, миристил- и стеарилхлориды, -бромиды и -йодиды, арилалкилгалогениды, такие как бензил- и фенетилбромиды, и т.п.
Сложные эфиры формулы I в настоящем изобретении представляют собой нетоксичные, фармацевтически приемлемые сложные эфиры, например, алкильные сложные эфиры, такие как метиловые, этиловые, пропиловые, изопропиловые, бутиловые, изобутиловые или пентиловые сложные эфиры. Можно использовать дополнительные сложные эфиры, например метиловый сложный эфир или фенил-C1-С5-алкил. Соединения формулы I можно этерифицировать с помощью множества различных методик, включая введение подходящего ангидрида, карбоновой кислоты или хлорангидрида кислоты со спиртовой группой соединения формулы I. Для облегчения ацилирования подходящий ангидрид можно ввести в реакцию со спиртом в присутствии основания, такого как 1,8-бис[диметиламино]-нафталин или N,N-диметиламинопиридин. Подходящую карбоновую кислоту можно ввести в реакцию со спиртом в присутствии дегидратирующего реагента, такого как дициклогексил-карбодиимид, 1-[3-диметиламинопропил]-3-этилкарбодиимид или с другими растворимыми в воде дегидратирующими реагентами, которые используются для проведения реакции путем удаления воды, и, необязательно, в присутствии катализатора ацилирования. Этерификацию также можно осуществить с использованием подходящей карбоновой кислоты в присутствии трифторуксусного ангидрида и, необязательно, пиридина, или в присутствии N,N-карбодиимидазола с пиридином. Реакцию хлорангидрида кислоты со спиртом можно провести с использованием катализатора ацилирования, такого как 4-DMAP или пиридин.
Специалист в данной области техники должен хорошо знать, как успешно осуществить эти, а также другие способы этерификации спиртов.
Кроме того, во время осуществления любого из указанных выше способов получения сложных эфиров к чувствительным или реакционноспособным группам соединения формулы I может потребоваться присоединить или от них удалить защитные группы. Обычно защитные группы можно присоединять или удалять обычными способами, хорошо известными в данной области техники (см., например, Т.W. Greene and P.G.M. Wuts, Protective Groups in Organic Synthesis; Wiley: New York, (1999)).
В зависимости от положения и природы различных необходимых заместителей соединения формулы I могут содержать один или большее количество асимметрических центров. Асимметрические атомы углерода могут находиться в (R)- или (S)-конфигурации. Предпочтительными являются изомеры с такой абсолютной конфигурацией, которые дают соединения формулы I, обладающие более желательной биологической активностью. В некоторых случаях асимметрия может возникать вследствие заторможенного вращения вокруг данной связи, например центральной связи, соединяющей два ароматических кольца заданных соединений.
Заместители у кольца могут находиться в цис- или транс-форме, а заместители у двойной связи могут находиться в Z- или Е-форме.
Предполагается, что в объем настоящего изобретения включены все изомеры (включая энантиомеры и диастереоизомеры), наличие которых обусловлено природой асимметрических центров или заторможенным вращением, как описано выше, в виде разделенных, чистых или частично очищенных изомеров или их рацемических смесей. Очистка указанных изомеров и разделение указанных смесей изомеров могут быть выполнены по стандартным методикам, известным в данной области техники.
Конкретный способ, применяющийся для получения соединений, соответствующих настоящему изобретению, зависит от конкретного необходимого соединения. Все такие факторы, как выбор конкретного фрагмента Х и конкретных заместителей, возможных для различных положений в молекуле, играют роль в схеме получения конкретных соединений, соответствующих настоящему изобретению. Эти факторы легко устанавливаются специалистом с общей подготовкой в данной области техники.
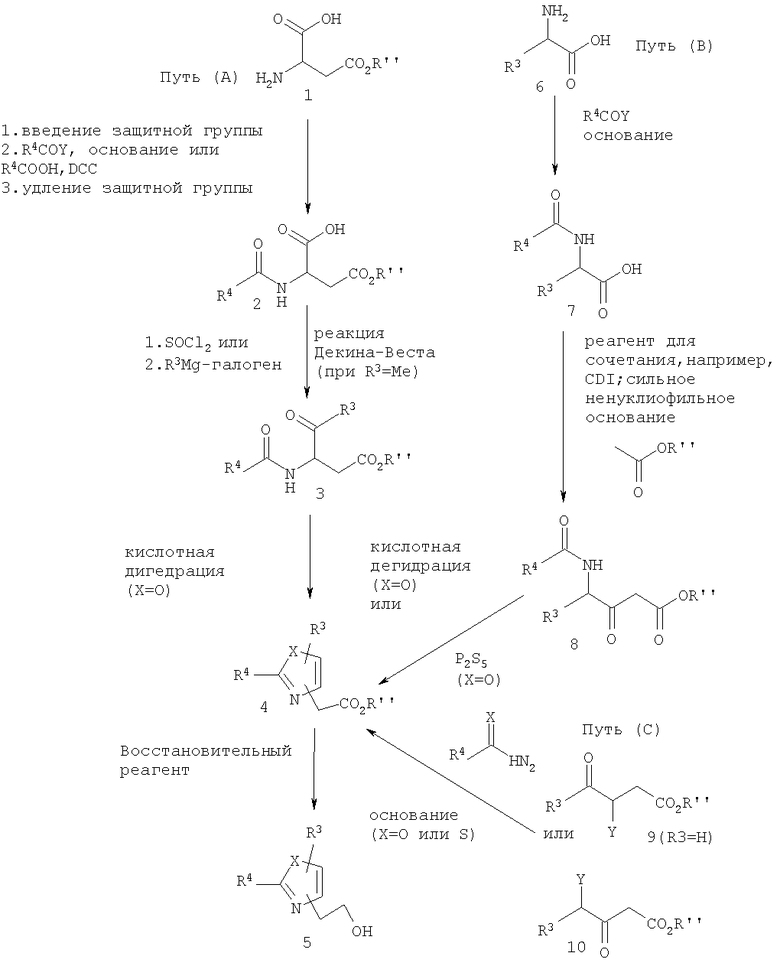
Обычно соединения, соответствующие настоящему изобретению, можно получить с помощью стандартных методик, известных в данной области техники, и с помощью аналогичных им способов. Соединения формулы I обычно можно синтезировать по Схемам реакций 1, 2 и 3. Схемы реакций 1 и 2 показывают, как получить промежуточные продукты, которые с помощью сочетания, показанного на Схеме реакций 3, приводят к соединениям формулы I.
Путь (А) на Схеме реакций 1 представляет собой способ получения соединений 4 и 5, в которых R'' означает C1-C6 низший алкил или бензил, R3 означает не водород и Х означает О. На первой стадии показана защита кислотной группы продажного производного аспартата 1 с помощью способа, хорошо известного в данной области техники, такого как, например, получение силилового сложного эфира с последующим N-ацилированием соответствующим производным R4-кислоты, R4COY, где Y означает отщепляющуюся группу, такую как галогенидная. В заключение у соединения удаляют защитную группу с помощью способа, хорошо известного в данной области техники, такого как, например, в случае силилового сложного эфира, обработка водой с получением соединения 2. Альтернативно, конденсация защищенной формы соединения 1 со свободной карбоновой кислотой, такой как R4COOH, в присутствии дегидратирующего реагента, такого как DCC или EDCl, также дает соединение 2. После этого соединение 2 несколькими способами можно превратить в соединение 3, в котором R3 является таким, как определено для соединений формулы I. Например, один такой способ, когда R3=Me, представляет собой хорошо известную реакцию Дэкина-Веста, которую обычно проводят с использованием уксусного ангидрида и пиридина. Если R3 означает не водород, соединение 2 можно превратить в хлорангидрид кислоты с помощью реагента, такого как тионилхлорид, и ввести в реакцию с реагентом Гриньяра, таким как R3Mg-галоген, и получить соединение 3. Можно использовать другие способы получения кетонов соединения 3 из кислот и производных кислот, например, путем использования амидов Вейнреба, которые известны специалистам в данной области техники. Затем соединение 3 циклизуют в кислой среде в условиях дегидратации с использованием, например, оксихлорида фосфора или смеси серной кислоты с уксусным ангидридом, обычно при нагревании, и получают соединение 3, в котором Х означает О и группа R3 присоединена в положении 5.
Специалисты в данной области техники должны понимать, что соединение 4 и тем самым соединение 5 могут существовать в двух региоизомерных формах в зависимости от места присоединения групп R3, CH2CO2R'' и CH2CH2OH. С использованием пути (В) можно получить соединение 4, в котором R3 присоединен в положении 4 и карбоксиметильная боковая цепь присоединена в положении 5, т.е. по сравнению с путем (А) группы поменялись местами. С помощью пути (В) продажную аминокислоту, соединение 6, можно ацилировать в щелочной среде, например, с использованием водного раствора гидроксида натрия, с помощью подходящего производного R4-кислоты (например, R4COY), где Y означает отщепляющуюся группу, такую как хлоридную, и получить N-ацилированный продукт 7. Соединение 7 затем можно ввести в реакцию сочетания со сложным эфиром уксусной кислоты в присутствии сильного ненуклеофильного основания и получить сложный кетоэфир 8, в котором R'' означает C1-C6алкил или бензил. Циклизация соединения 8 с использованием дегидратирующего реагента, такого как POCl3, дает соединение 4, в котором Х=О и R3 присоединен в положении 4. Реакция соединения 8 с нуклеофильным серосодержащим реагентом, таким как P2S5, в растворителях, таких как пиридин или ацетонитрил/триэтиламин, при необходимости с нагреванием, дает соединение 4, в котором Х=S и R3 присоединен в положении 4.
Путь (С) Схемы реакций 1 представляет собой получение соединения 4 из сложных кетоэфиров 9 или 10, где Y означает отщепляющуюся группу, такую как галогенидная, и R'' означает C1-C6алкил или бензил. Соединение 9 или 10 можно выбрать в качестве исходного вещества в зависимости от того, означает ли группа R3 в искомом конечном продукте водород или же она присоединена в положение 4 или 5. В соответствии с этим соединение 9 или 10 можно ввести в реакцию с амидом или тиоамидом, где Х означает О или S, и получить соединение 4. Сложные кетоэфиры 9 или 10 имеются в продаже или их можно получить способами, хорошо известными в данной области техники, такими как бромированием продажных кетоэфиров 9 или 10, в которых Y означает водород. Амиды (R4C(=X)NH2), где Х означает О, могут быть продажными амидами карбоновых кислот или их можно получить из соответствующих продажных кислот или хлорангидридов кислот хорошо известными способами. Тиоамиды (R4C(=X)NH2), где Х означает S, могут быть продажными тиоамидами или их можно получить из соответствующих продажных амидов известными способами, такими как способом с использованием реагента Лавессона. Реакция сложного кетоэфира 9 с амидом или тиоамидом в присутствии основания дает соединение 4, т.е. оксазол или тиазол соответственно, где R3 означает не водород и расположен в положении 4. Реакция сложного кетоэфира 10 с амидом или тиоамидом в присутствии основания дает соединение 4, т.е. оксазол или тиазол соответственно, где R3 расположен в положении 5.
Все пути (А), (В) и (С) приводят к соединению 4, в котором R3 и R4 являются такими, как определено для соединений формулы I, и в котором R'' означает низший алкил или бензил. Затем соединение 4 можно восстановить в соединение 5 с использованием восстановительного реагента, такого как алюмогидрид лития, борогидрид лития или другие подходящие доноры водорода, в условиях, хорошо известных в данной области техники.
Схема реакции 1
На Схеме реакций 2 представлено превращение продажного гидроксикетона 11 в производное с защитной группой 12 по реакции с R7-Y в присутствии основания, где R7 означает C1-C6алкил, необязательно содержащий в качестве заместителя фенил или оксогруппу, С1-С6триалкилсилил, арилалкилсилил или COR8; и R8 означает C1-C6 алкил или фенил, необязательно содержащий в качестве заместителя С1-С6алкил, галоген или нитрогруппу; и Y означает отщепляющуюся группу. "C1-C6триалкилсилил" означает три независимо выбранные линейные или разветвленные цепочечные алкильные группы, содержащие от 1 до примерно 6 атомов углерода, каждая из которых связана с кремнием, и включает такие группы, как триметилсилильная, трет-бутилдиметилсилильная и т.п. "Арилалкилсилил" означает хотя бы одну фенильную или замещенную фенильную группу, связанную с кремнием, с соответствующим количеством независимо выбранных линейных или разветвленных цепочечных алкильных групп, содержащих от 1 до примерно 6 атомов углерода, каждая из которых связана с кремнием, и включает такие группы, как трет-бутилдифенилсилил, метилдифенилсилил, диметилпентафторфенилсилил и т.п. "Отщепляющаяся группа" включает галогенидные, такие как I, Br и Cl; карбоксилаты, такие как ацетаты и трифторацетаты, и арил- и алкилсульфонаты, такие как метансульфонаты (мезилаты) и п-толуолсульфонаты (тозилаты) и т.п.
В соединение 12 заместители R2 (как показано в формуле I) вводят, например, с помощью реакции с источником электрофильного галогена или реакции Фриделя-Крафтса в присутствии кислоты Льюиса и R2-Y, где Y является таким, как описано выше, с получением замещенного кетона 13. Альтернативно, галогенированные соединения, полученные таким образом (например, содержащие бром или йод в качестве заместителей), можно ввести в реакцию сочетания с самыми различными компонентами при катализе соединениями металлов с использованием комплексов и соединений элементов, таких как палладий и никель, хорошо известных специалистам в данной области техники, с получением замещенного кетона 13. Примеры таких катализаторов включают тетракис(трифенилфосфин)-палладий(O) и [1,1'-бис(дифенилфосфино)-ферроцен]-дихлорпалладий(И) и аналогичные соединения никеля(О) и никеля(II); и примеры компонентов для реакции сочетания включают бороновые кислоты и сложные эфиры (хорошо известное сочетание Судзуки, проводимое в растворителях, таких как толуол, в присутствии основания, такого как карбонат калия), и металлоорганические соединения, такие как реагенты Гриньяра, цинкорганические соединения (сочетание Негиши) и оловоорганические производные (сочетание Стилле), и условия проведения таких реакций хорошо известны. Кроме того, такие галогенированные соединения можно ввести в реакцию сочетания со вторичными аминами, такими как пиперидин, с использованием аналогичных палладиевых или никелевых катализаторов (сочетание Гартвига или Бухвальда) с получением других замещенных кетонов 13.
Последующая реакция соединения 13 с источником галогена или R5-Y (где R5 является таким, как описано для формулы I) при аналогичных условиях дает дизамещенное соединение 14. Реакцию Виттига или модификацию Хорнера-Эммонса-Вадсворта, известные в данной области техники, можно использовать для превращения 14 в соединение 15. Например, реакция соединения 14 с триалкилфосфоно-ацетатом, где R'' означает низший алкил и R является таким, как описано для формулы I, в присутствии сильного основания, такого как гидрид натрия, дает соединение 15. Аналогичным образом соединение 13 можно превратить в соединение 15, где R5 означает Н.
Независимо оттого, какая смесь изомеров соединения 15 получается, любой изомер (E или Z) или смесь их обоих можно превратить в соединение 17 путем каталитического гидрирования или восстановления гидридным реагентом, способным к 1,4-присоединению (сопряженному), которое известно специалистам в данной области техники. Этот путь является особенно подходящим для получения соединения 17, в котором R1 означает водород.
Соединение 17, в котором R1 означает COOR, можно получить с помощью стандартных реакций конденсации, например, с помощью хорошо известной реакции Кневенагеля. В таких случаях кетон 13 или 14 можно ввести в реакцию с подходящим компонентом реакции сочетания, содержащим активный водород, при воздействии кислотных реагентов, таких как тетрахлорид титана, или основных реагентов, таких как пиперидин, в подходящих растворителях. Продукт 15b (соединение 15, в котором R1 означает COOR) можно восстановить в 17b (соединение 17, в котором R1 означает COOR), которое можно дополнительно алкилировать другой группой R1 в присутствии основания, гидролизовать и декарбоксилировать с получением 17d (соединение 17, в котором R1 означает не СООН и R означает Н).
Переэтерификация 17d и удаление защитной группы R7 дает 17с. Переэтерификацию можно проводить при стандартных условиях с помощью хорошо известной этерификации Фишера путем обработки кислотой и спиртом или по реакции с диазоалкильными реагентами или с электрофильными реагентами, такими как, например, метилйодид или диметилсульфат. Соединение 17, в котором R1 означает алкоксил, можно получить аналогичной реакцией конденсации кетона 13 или 14 с силилированным сложным эфиром енола формулы R1СН=С(OR'')O-алкилсилил, в котором R1 означает алкоксил, при воздействии кислотных реагентов, таких как тетрахлорид титана, и восстановлением промежуточного соединения 15, в котором R1 означает алкоксил, в присутствии водорода и катализатора, как это описано выше.
Общая реакция сочетания соединения 13 или 14 по реакции Реформатского дает соединение 16 (формула II), в котором R1 означает алкил или соединение 15а, в котором R1 означает Н. Кетон конденсируют с подходящим цинкорганическим соединением, полученным in situ из Zn и R1CHYCO2R, в котором Y означает галоген. Альфа-галогензамещенные сложные эфиры формулы R1CHYCO2R или являются продажными реагентами, или их получают галогенированием продажных соединений R1CH2CO2R способами, хорошо известными специалистам в данной области техники.
Превращение 16 в 17 можно осуществить в стандартных условиях гидрирования, например, с помощью Pd/C и водорода; и удаление защитной группы соединения 17, в котором R7 означает защитную группу с получением соединения 17с, в котором R7 означает водород, можно осуществить стандартными средствами. Например, если группа R7 означает алкил (например, метил), то соединение 17а можно получить нуклеофильным расщеплением с помощью реагента, такого как тиолат щелочного металла. Альтернативно, соединение 17, в котором R7 означает метил, можно превратить в соединение 17с по реакции с кислотой Льюиса, такой как бром-боран. Если R7 означает бензил, то соединение 17 можно превратить в 17с в условиях гидрирования, обычно проводимого с использованием катализатора, такого как палладий. Другие условия для удаления защитной группы R7 от соединения 17, в котором R7 означает не водород, приводящие к получению гидроксисоединения 17с, зависят от конкретной защитной группы, выбранной из числа хорошо известных специалистам в данной области техники.
Схема реакций 2
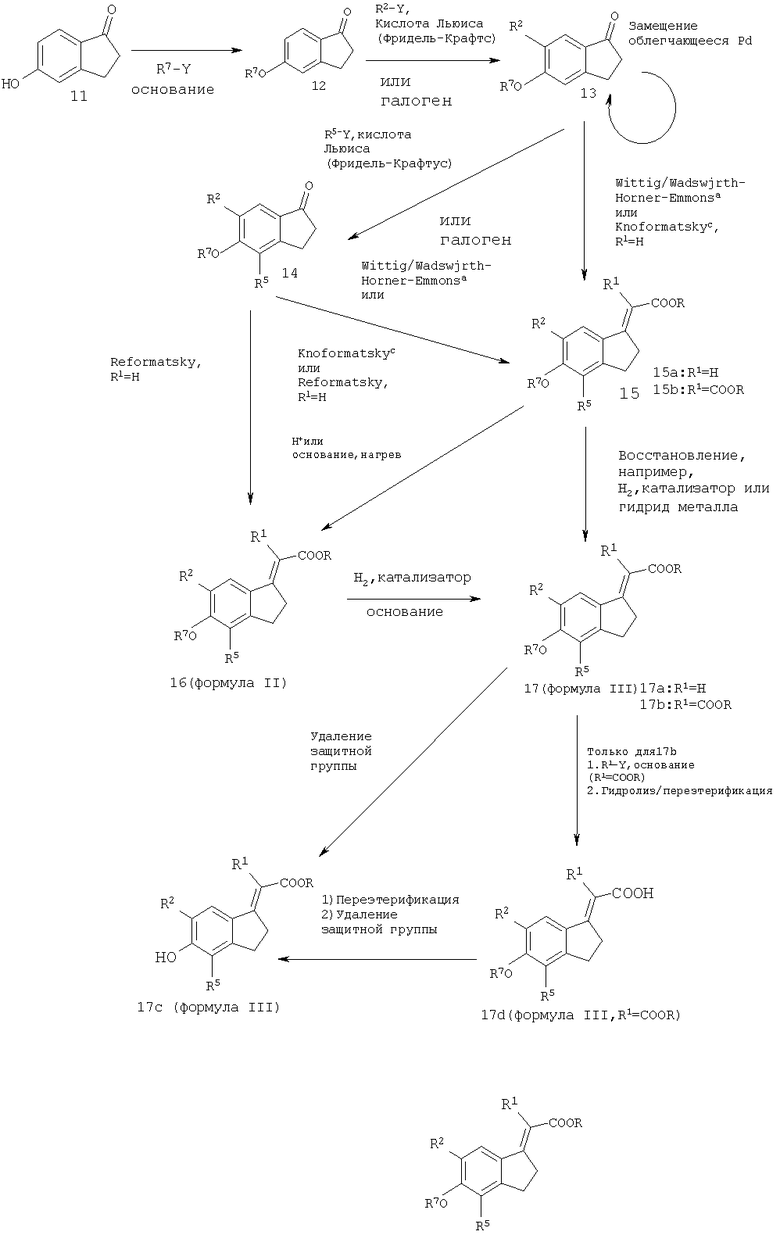
Примечания:
а. (R''O)2P(=O)CHR1COOR, где R1=Н, сильное основание.
b. R1CH2COOR, где R1=COOR, кислотный или основной катализатор.
с. R1CHBrCO2OR, Zn.
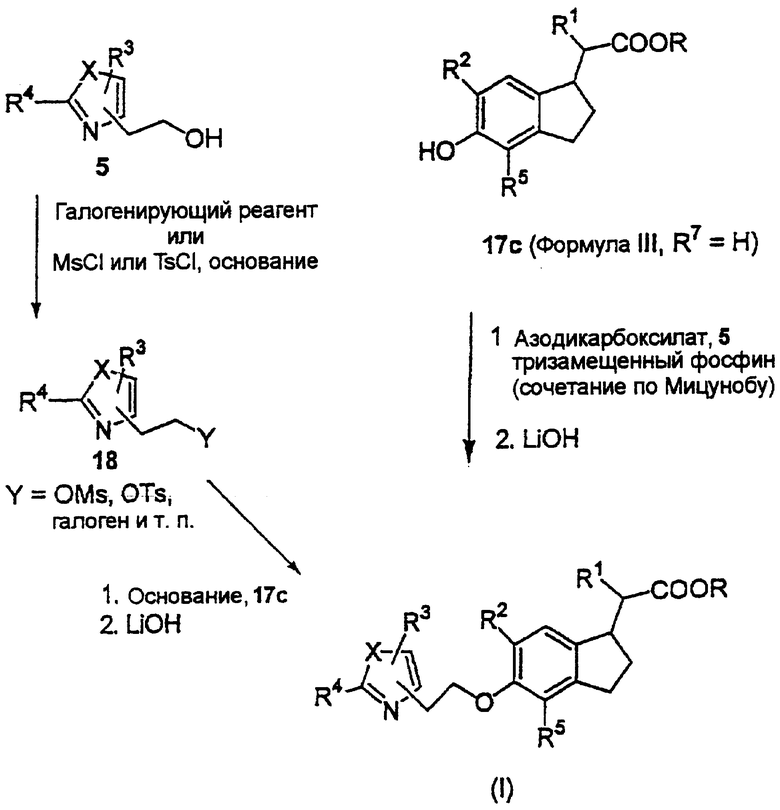
Конечная стадия получения соединений формулы I приведена на Схеме реакций 3. Спирт 5 (из Схемы реакций 1) вводят в реакцию сочетания с гидроксиинданом 17с (из Схемы реакций 2) по реакции сочетания Мицунобу, протеканию которой способствуют азодикарбоксилатный реагент, такой как DEAD, и фосфин, такой как трифенилфосфин, и получают соединения формулы I. Альтернативно, гидроксигруппу соединения 5 превращают в отщепляющуюся группу, такую как галогенид, тозилат (OTs) или мезилат (OMs), по реакции с галогенирующим реагентом, таким как тио-нилхлорид или CCl4/трифенилфосфин; или по реакции с соединением Y-галоген, в котором Y означает тозил (Ts) или мезил (Ms), в присутствии основания и получают соединение 18. Соединение 18 можно ввести в реакцию с соединением 17с в присутствии основания и получить соединения формулы I.
Соединения формулы I, в которых R означает алкил, можно превратить в соединения формулы I, в которых R означает Н путем обработки основанием (например, КОН) в подходящем растворителе (например, метаноле, THF или воде или их смесях) при нагревании. Альтернативно, это превращение можно осуществить по реакции с нуклеофилом, таким как йодид или цианид, в подходящем растворителе, таком как пиридин. Кроме того, если R означает бензил, то расщепление с образованием соединений формулы I, в которых R означает Н можно осуществить путем гидрогенолиза с помощью способов, хорошо известных в данной области техники.
Схема реакций 3
Альтернативный путь получения соединений формулы I, применяющийся, когда Х=S и группа R4 содержит один или большее количество заместителей R6, неустойчивых при условиях проведения реакций по Схеме 1 или 2, приведен на Схеме реакций 3а.
Схема реакций 3а
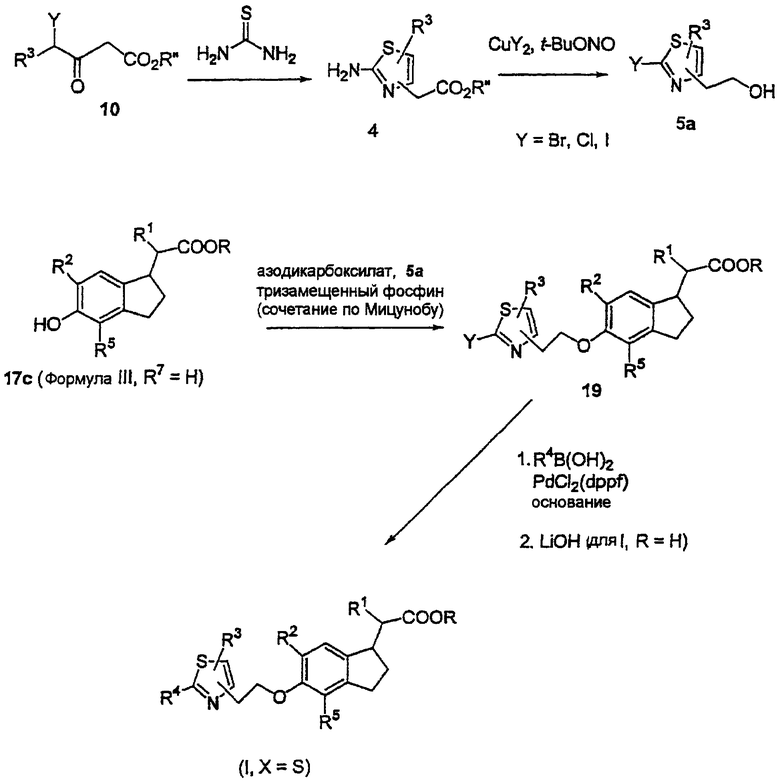
По Схеме 3а 2-аминотиазол 4 можно получить с использованием тиомочевины (аналогично пути С, Схема реакций 1) и превратить в 2-галогентиазол 5а, как показано выше (Erienmeyer et al., Helv. Chim. Acta 28:362-363,1945). Затем осуществляется сочетание 5а по Мицунобу способом, аналогичным Схеме реакций 3, и для введения заместителя R4 продукт 19 дополнительно вводят в перекрестную реакцию сочетания, катализируемую палладием. Гидролиз, проводимый так, как это показано на Схеме реакций 3, дает соединения формулы I, в которых R=Н.
Приведенные выше схемы реакций дополнительно иллюстрируются конкретными Примерами, описанными в настоящем изобретении.
Соли и сложные эфиры, соответствующие настоящему изобретению, легко можно получить с помощью обычных химических методик, описанных выше в настоящем изобретении.
Настоящее изобретение также относится к новым соединениям формулы II (соединение 16) и формулы III (соединения 17, включая соединения 17a-d), показанным на Схеме реакций 2. Эти соединения применимы для получения соединений формулы I и дополнительно описаны ниже.
Настоящее соединение охватывает соединения формулы II и формулы III,
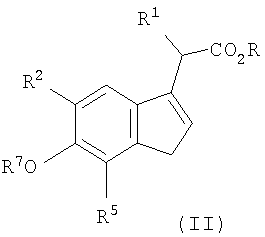
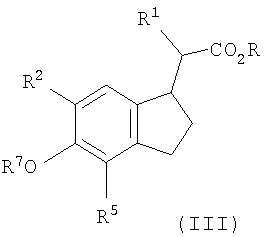
где
R, R1, R2, R3, R4, R5, R6 и Х являются такими, как определено выше для формулы I; и R7 означает Н, C1-C6алкил, необязательно содержащий в качестве заместителя фенил или оксогруппу, C1-С6триалкилсилил, арилалкилсилил, COR8, COOR8, или
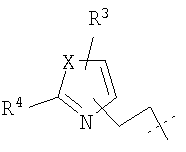 ;
;
R8 означает C1-C6алкил или фенил, необязательно содержащий в качестве заместителя C1-C6алкил, галоген или нитрогруппу; и их соли.
C1-C6триалкилсилил означает три независимо выбранные линейные или разветвленные цепочечные алкильные группы, содержащие от 1 до примерно 6 атомов углерода, каждая из которых связана с кремнием, и включает такие группы, как три-метилсилильная, трет-бутилдиметилсилильная и т.п.
Арилалкилсилил означает хотя бы одну фенильную или замещенную фенильную группу, связанную с кремнием, с соответствующим количеством независимо выбранных линейных или разветвленных цепочечных алкильных групп, содержащих от 1 до примерно 6 атомов углерода, каждая из которых связана с кремнием, и включает такие группы, как трет-бутилдифенилсилил, метилдифенилсилил, диметилпентафторфенилсилил и т.п.
Соли, соответствующие настоящему изобретению, легко можно получить с помощью обычных химических методик, описанных выше в настоящем изобретении.
В зависимости от положения и природы различных необходимых заместителей соединения формулы II и формулы III могут содержать один или большее количество асимметрических центров. Асимметрические атомы углерода могут находиться в (R)- или (S)-конфигурации. Предпочтительными являются изомеры с такой абсолютной конфигурацией, которые дают соединения формулы II или формулы III, которые будут пригодны для получения соединений формулы I, обладающих более желательной биологической активностью. В некоторых случаях асимметрия может возникать вследствие заторможенного вращения вокруг данной связи, например, центральной связи, соединяющей два ароматических кольца заданных соединений.
Заместители у кольца могут находиться в цис- или транс-форме, а заместители у двойной связи могут находиться в Z- или Е-форме.
Предполагается, что в объем настоящего изобретения включены все изомеры (включая энантиомеры и диастереоизомеры), наличие которых обусловлено природой асимметрических центров или заторможенным вращением, как описано выше, в виде разделенных, чистых или частично очищенных изомеров или их рацемических смесей. Очистка указанных изомеров и разделение указанных смесей изомеров может быть выполнена по стандартным методикам, известным в данной области техники, а также с помощью новых средств, описанных в настоящем изобретении.
Например, соединения формулы II могут содержать асимметрический центр (отмеченный, как С-2), а соединения формулы III могут содержать два асимметрических центра (отмеченных, как С-2 и С-1'), что приводит к энантиомерам и стереоизомерам. Примеры этих и других соединений формулы II и формулы III, которые иллюстрируют настоящее изобретение, приведены в таблице 2.
Таблица 2
Иллюстративные примеры соединений II и III

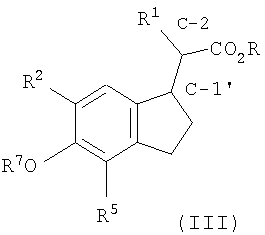
Другим вариантом осуществления настоящего изобретения является улучшенный способ получения соединений, обладающих специальной конфигурацией изомеров, когда эта специальная конфигурация желательна для необходимого конечного продукта формулы I. Улучшенный способ дает эти промежуточные соединения с намного более значительным избытком диастереоизомера, чем было возможно ранее.
В частности, ранее, при отсутствии стереоконтроля на стадии гидрирования Схемы реакций 2, гидрирование соединения формулы II, в котором R1 означает алкил, могло приводить к смеси неодинаковых количеств продуктов формулы III, в которой одна пара энантиомеров содержится в большем количестве вследствие асимметричной природы исходного вещества. Разделение таких соединений можно осуществить путем ступенчатого разделения пар энантиомеров с последующим выделением каждого энантиомера с помощью перекристаллизации или хиральной ВЭЖХ. Предварительное разделение исходного вещества на отдельные энантиомеры приводит к смесям, обогащенным одним энантиомером, которые, вероятно, можно разделить.
Однако, когда необходимо соединение одной заданной относительной конфигурации, а именно, син-форма (определенная ниже), выход является низким, когда R1 означает алкил, поскольку условия проведения стадии гидрирования, описанные в данной области техники, могут благоприятствовать образованию других диастереоизомеров (т.е. анти-формы).
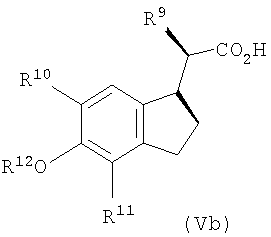
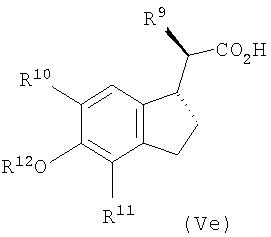
Желательные изомерные конфигурации, получающиеся с помощью этого улучшенного способа, представляют собой син-форму, когда, например, в соединениях формул Va и Vb (приведенные на Схемах реакций 4 и 5) и группа R9, и метиленовый атом углерода в положении 2' циклопентанового кольца оба находятся или под, или над плоскостью. Анти-диастереоизомеры представляют собой такие соединения, в которых, например, R9 находится над плоскостью, а метиленовый атом углерода в положении 2' находится под плоскостью. Примеры таких систем приведены ниже на фиг.1 и 2, на которых зачерненные клинообразные связи используются для обозначения расположения связей над плоскостью, а штриховые клинообразные связи используются для обозначения расположения связей под плоскостью.
Фиг.1. Син-диастереоизомеры формулы V
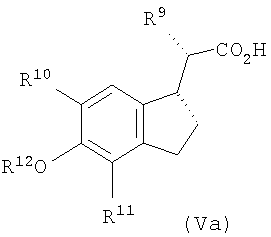
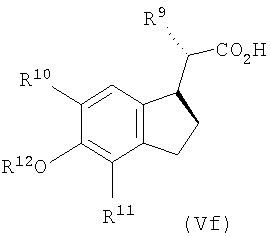
Фиг.2. Анти-диастереоизомеры формулы V
Улучшенный способ, соответствующий настоящему изобретению, дает соединения в син-форме (формулы Va и Vb, приведенные на фиг.1 и Схемах реакций 4 и 5) с намного более значительным избытком диастереоизомера, чем обычно было возможно.
Промежуточные соединения, использующиеся в качестве исходных веществ для этого способа (соединение IV на Схемах реакций 4 и 5) родственны соединениям формулы II (соединение 15) на Схеме реакций 2 и могут быть получены такими же или аналогичными способами. Эти промежуточные соединения при некоторых условиях можно ввести в реакции и получить соединения формулы V, которые родственны соединениям формулы III (соединения 17 и 17а на Схеме реакций 2), или непосредственно получить соединения формулы I. Однако, вследствие ограничений улучшенного способа для завершения этого способа пригодны только некоторые заместители.
Соответственно, настоящее изобретение относится к улучшенному способу получения существенно обогащенного син-формой соединения формулы V,
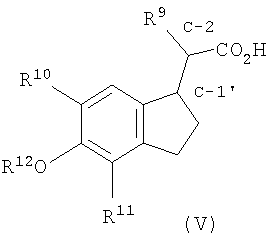
где R9 означает метоксил, необязательно содержащий фтор в качестве заместителя, С2-С6алкоксил, C1-C6алкил или С4-С8циклоалкил, каждый из которых необязательно содержит в качестве заместителя фтор, метилендиоксифенил или фенил, необязательно содержащий в качестве заместителя R13;
R10 означает водород, фтор, метил, необязательно содержащий в качестве заместителя фтор, оксогруппу или С2-С6алкил, который может быть незамещенным или содержать в качестве заместителей C1-C6алкоксил, оксогруппу, фтор или фенил, фурил, тиенил, пирролил, оксазолил, тиазолил, имидазолил, пиразолил, изоксазолил, изотиазолил, триазолил, оксадиазолил, тиадиазолил, тетразолил, пиридил, пирролидинил, пиперидинил, тетрагидропиранил, тетрагидротиопиранил, пиперазинил или морфолинил, каждый из которых может быть незамещенным или содержать в качестве заместителей R13,
или
R10 означает фенил, фурил, тиенил, пирролил, оксазолил, тиазолил, имидазолил, пиразолил, изоксазолил, изотиазолил, триазолил, оксадиазолил, тиадиазолил, тетразолил, пиридил, пирролидинил, пиперидинил, тетрагидропиранил, тетрагидротиопиранил, пиперазинил или морфолинил, каждый из которых может быть незамещенным или содержать в качестве заместителей R13;
R11 означает галоген или C1-C6алкил, необязательно содержащий в качестве заместителя оксогруппу;
R12 означает водород, метил, необязательно содержащий в качестве заместителя фтор или оксогруппу, С2-С6алкил, необязательно содержащий в качестве заместителя фенил, фтор или оксогруппу, C1-C6триалкилсилил, арилалкилсилил, COR14, COOR14 или

R13 означает фтор, CF3, C1-C6алкил, необязательно содержащий в качестве заместителя оксогруппу или С1-С6алкоксил, необязательно содержащий в качестве заместителя фтор;
R14 означает С1-С6алкил или фенил, необязательно содержащий в качестве заместителя C1-C6алкил или фтор;
R15 означает водород, C1-C6алкил или фенил, содержащий в качестве заместителя R13;
R16 означает метил, необязательно содержащий в качестве заместителя фтор, оксогруппу или фенил, нафтил, фурил, тиенил, пирролил, тетрагидрофурил, пирролидинил, пирролинил, тетрагидротиенил, оксазолил, тиазолил, имидазолил, пиразолил, изоксазолил, изотиазолил, триазолил, оксадиазолил, тиадиазолил, тетразолил, пиридил, пиперидинил, тетрагидропиранил, тетрагидротиопиранил, пиримидинил, пиразинил, пиридазинил, пиперазинил, морфолинил, бензофурил, дигидробензофурил, бензотиенил, дигидробензотиенил, индолил, индолинил, индазолил, бензоксазолил, бензотиазолил, бензимидазолил, бензизоксазолил, бензизотиазолил, бензодиоксолил, хинолил, изохинолил, хиназолинил, хиноксазолинил, дигидробензопиранил, дигидробензотиопиранил или 1,4-бензодиоксанил, каждый из которых может быть незамещенным или содержать в качестве заместителей R13 или С4-С8циклоалкил или С2-С6алкил, каждый из которых может быть незамещенным или содержать в качестве заместителей фтор, метоксил, C1-C6алкоксил, необязательно содержащий в качестве заместителя фенил или C1-C6алкоксил, оксогруппу или фенил, нафтил, фурил, тиенил, пирролил, тетрагидрофурил, пирролидинил, пирролинил, тетрагидротиенил, оксазолил, тиазолил, имидазолил, пиразолил, изоксазолил, изотиазолил, триазолил, оксадиазолил, тиадиазолил, тетразолил, пиридил, пиперидинил, тетрагидропиранил, тетрагидротиопиранил, пиримидинил, пиразинил, пиридазинил, пиперазинил, морфолинил, бензофурил, дигидробензофурил, бензотиенил, дигидробензотиенил, индолил, индолинил, индазолил, бензоксазолил, бензотиазолил, бензимидазолил, бензизоксазолил, бензизотиазолил, бензодиоксолил, хинолил, изохинолил, хиназолинил, хиноксазолинил, дигидробензопиранил, дигидробензотиопиранил или 1,4-бензодиоксанил, каждый из которых может быть незамещенным или содержать в качестве заместителей R13,
или
С2-С6алкил, который также может содержать в качестве заместителя С4-С8циклоалкил или феноксил, который может быть незамещенным или содержать в качестве заместителей R6 или фенил, нафтил, фурил, тиенил, пирролил, тетрагидрофурил, пирролидинил, пирролинил, тетрагидротиенил, оксазолил, тиазолил, имидазолил, пиразолил, изоксазолил, изотиазолил, триазолил, оксадиазолил, тиадиазолил, тет-разолил, пиридил, пиперидинил, тетрагидропиранил, тетрагидротиопиранил, пиримидинил, пиразинил, пиридазинил, пиперазинил, морфолинил, бензофурил, дигидробензофурил, бензотиенил, дигидробензотиенил, индолил, индолинил, индазолил, бензоксазолил, бензотиазолил, бензимидазолил, бензизоксазолил, бензизотиазолил, бензодиоксолил, хинолил, изохинолил, хиназолинил, хиноксазолинил, дигидробензопиранил, дигидробензотиопиранил или 1,4-бензодиоксанил, каждый из которых может быть незамещенным или содержать в качестве заместителей R13,
или
R16 означает фенил, нафтил, фурил, тиенил, пирролил, тетрагидрофурил, пирролидинил, пирролинил, тетрагидротиенил, оксазолил, тиазолил, имидазолил, пиразолил, изоксазолил, изотиазолил, триазолил, оксадиазолил, тиадиазолил, тетразолил, пиридил, пиперидинил, тетрагидропиранил, тетрагидротиопиранил, пиримидинил, пиразинил, пиридазинил, пиперазинил, морфолинил, бензофурил, дигидробензофурил, бензотиенил, дигидробензотиенил, индолил, индолинил, индазолил, бензоксазолил, бензотиазолил, бензимидазолил, бензизоксазолил, бензизотиазолил, бензодиоксолил, хинолил, изохинолил, хиназолинил, хиноксазолинил, дигидробензопиранил, дигидробензотиопиранил или 1,4-бензодиоксанил, каждый из которых может быть незамещенным или содержать в качестве заместителей R13 или фенил, фурил, тиенил, пирролил, оксазолил, тиазолил, имидазолил, пиразолил, изоксазолил, изотиазолил, триазолил, оксадиазолил, тиадиазолил, тетразолил, пиридил, пирролидинил, пиперидинил, тетрагидропиранил, тетрагидротиопиранил, пиперазинил, морфолинил, пиримидинил или феноксил, каждый из которых может быть незамещенным или содержать в качестве заместителей R13, и Х означает О или S;
включающий гидрирование рацемической смеси или выделенного оптического изомера соединения формулы IV,
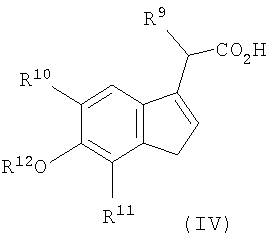
где заместители являются такими, как определено выше, в присутствии источника водорода, катализатора, необязательно в присутствии основания.
Существенно обогащенная син-форма означает, что примерно семьдесят процентов (70%) или более одного или обоих соединений конфигурации Va или Vb. Это эквивалентно не менее примерно 40% de (избытка диастереоизомера) син-диастереоизомера. Избыток син-диастереоизомера рассчитывается по следующей формуле:

в которой % de (син) означает избыток син-диастереоизомера,
[син] означает концентрацию син-диастереоизомера,
[анти] означает концентрацию анти-диастереоизомера,
и в которой %син+%анти=100%.
Таким образом, для смеси 70% син-диастереоизомера и 30% анти-диастереоизомера по расчету получается 40% de син-диастереоизомера:
40% de (син)=70% син-диастереоизомера - 30% анти-диастереоизомера.
Катализатор означает один из катализаторов на основе переходного металла, хорошо известных в данной области техники и использующихся для проведения реакций гидрирования (Р.А. Chaloner, Handbook of Co-ordination Catalysis in Organic Chemistry, Butterworth, 1986), и включает гомогенные катализаторы гидрирования. Гомогенным катализатором является катализатор, который хотя бы частично растворим в реакционной среде и который влияет на восстановление двойной связи в присутствии водорода. Такие катализаторы включают, например, ClRh[Р(Ph)3]3 (катализатор Уилкинсона), (1,5-циклооктадиен)-трициклогексилфосфинпиридиноиридий(I)-гексафторфосфат(1,5-циклооктадиен)бис(метилдифенилфосфин)иридий(I)-гексафторфосфат(катализаторы Грэбтри), и т.п.
Основание означает соединение, обладающее значением pKb, достаточным для образования /л situ соли с карбоновой кислотой (см., например, Advanced Organic Chemistry, 3rd Ed., Jerry March, pp 220-222). Основание, которое используется в этой реакции, может являться неорганическим или органическим основанием и может быть растворимо в реакционной среде. Такие основания включают, например, моно-, ди- и три-(С1-С6алкил)амины, такие как изопропиламин, диизопропиламин, три-этиламин и т.п., дополнительные первичные амины, такие как, например, циклогексанметиламин и этаноламин, дополнительные вторичные амины, такие как, например, морфолин и пимеридин, и дополнительные третичные амины, такие как, например, 1,8-диазабицикло[5.4.0]ундец-7-ен и 1,5-диазабицикло[4.3.0]нон-5-ен, а также неорганические основания, такие как гидроксиды, карбонаты, бикарбонаты щелочных металлов и щелочноземельных металлов, и оптически активные основания, такие как хинин, цинхонин и (+)- и (-)-альфа-метилбензиламин.
Такие основания также включают, например, хиральные основания, указанные ниже, которые применимы для разделения.
Источник водорода означает любое средство выделения водорода в реакционную среду и включает использование газообразного водорода. Гидрирование можно проводить в широком диапазоне давлений водорода, т.е., например, от приблизительно атмосферного давления до примерно 1000 фунтов/дюйм2, предпочтительно - от примерно 20 до примерно 100 фунтов/дюйм2. Подходящие для гидрирования растворители включают (без наложения ограничений) протонные растворители, такие как этанол, метанол, воду, 2-пропанол, трет-бутанол, метилэтоксиэтанол и т.п., и их смеси, или, необязательно, их смеси со смешивающимися с ними апротонными растворителями, такими как ТНР, такие, чтобы в них хотя бы частично растворялись катализатор гидрирования, основание и исходное вещество.
Разделение исходных производных инденуксусной кислоты формулы IV или производных инденуксусной кислоты формулы V можно осуществить способами, хорошо известными в данной области техники, например, путем использования в качестве разделяющих реагентов оптически активных оснований, таких как, например, легко доступное основание, такое как хинин, цинхонин или (+)- или (-)-альфа-метилбензиламин. Выбор основания будет зависеть от характеристик растворимости образовавшейся соли, так чтобы легко можно было осуществить разделение с помощью дифференциальной перекристаллизации. Разделение соли каждого энантиомера можно осуществить, выбрав основания с противоположной абсолютной конфигурацией. Например, в варианте осуществления, представленном на Схеме реакций 4, искомый энантиомер IVc или IVd можно отделить, а ненужный изомер можно регенерировать в исходное вещество формулы IV путем рацемизации в щелочной среде.
Растворителями, подходящими для перекристаллизации, являются такие растворители, в которых одна диастереоизомерная соль смеси растворима лучше, чем другая, что позволяет отделить ее с помощью перекристаллизации. Такие растворители включают, например, ацетонитрил, ацетон, трет-бутанол, 2-пропанол, этанол, метанол и т.п.и их смеси.
Водные растворы неорганических кислот включают, например, растворы обычно использующихся неорганических кислот, таких как хлористоводородная и серная и т.п.
Способ можно осуществить, используя в качестве исходного вещества рацемат формулы IV (см. Схему реакций 4) или соединение формулы V с конфигурацией по асимметрическому атому углерода, которая соответствует необходимой для конечного продукта (см. Схему реакций 5). Предпочтительно в качестве исходного использовать вещество, содержащее в основном одну конфигурацию, хотя любой способ приведет к необходимой конфигурации конечного продукта (V), в основном обогащенной син-формой.
Один вариант осуществления этого способа представлен в примере Схемы реакций 4 и включает стадии:
(1) получения диастереоизомерных солей IVc и IVd путем обработки IV подходящим основным разделяющим реагентом,
(2) разделения диастереоизомерных солей IVc и IVd с помощью перекристаллизации в подходящем растворителе для перекристаллизации,
(3) необязательного выделения индивидуальных антиподов IVa и IVb из разделенных солей путем обработки водным раствором неорганической кислоты, и
(4) восстановления или разделенных диастереоизомерных солей IVc и Vd, или индивидуальных антиподов IVa и IVb посредством гидрирования в присутствии гомогенного катализатора гидрирования, подходящего растворителя и основания, где М+ означает катион, выбранный из группы, включающей катион щелочного металла, щелочноземельного металла, аммония и моно-, ди- или четвертичный алкиламмоний и арилалкиламмоний, и R9-R12 являются такими, как определено выше.
Энантиомерная чистота продукта Va и Vb будет соответствовать энантиомерной чистоте использующегося изомера IVa или IVb соответственно, но продукт не будет включать значительного количества другого (анти)диастереоизомера.
Схема реакций 4
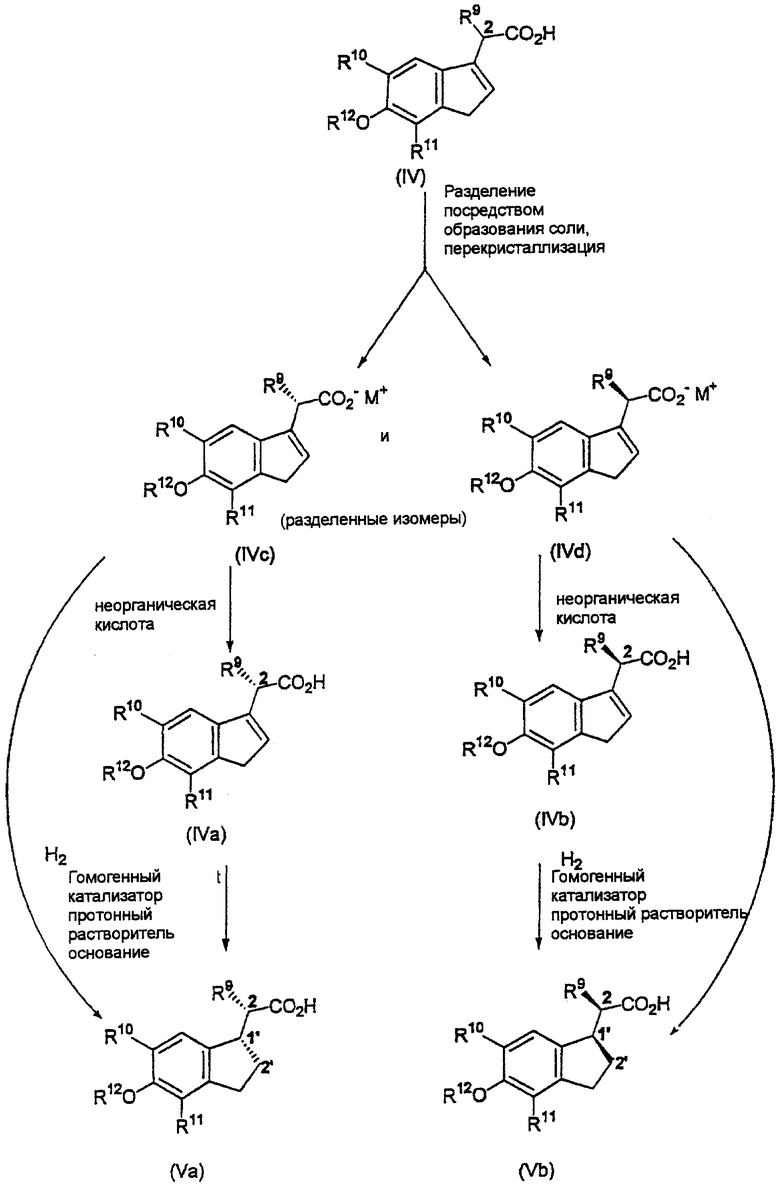
Второй вариант осуществления этого способа представлен на Схеме реакций 5 и включает стадии:
(1) восстановления индеркарбоновой кислоты формулы IV посредством гидрирования в присутствии гомогенного катализатора гидрирования, подходящего растворителя и основания,
(2) получения диастереоизомерных солей Vc и Vd путем обработки V подходящим основным разделяющим реагентом,
(3) разделения диастереоизомерных солей Vc и Vd с помощью перекристаллизации в подходящем растворителе для перекристаллизации, и
(4) выделения индивидуальных антиподов Va и Vb из разделенных солей путем обработки водным раствором неорганической кислоты.
Схема реакций 5

Разделение рацематов соединений формулы IV или формулы V можно выполнить способами, хорошо известными в данной области техники, такими как хиральная ВЭЖХ, перекристаллизация хиральных солей, хиральных сложных эфиров и т.п.
Определение абсолютной хиральности IVa, IVb, IVc, IVd, Va и Vb можно провести различными способами, известными специалистам в данной области техники. При некоторых строго определенных условиях такую информацию могут дать рентгенографические кристаллографические способы. Например, такое определение можно провести в присутствии кристаллографической элементарной ячейки другого компонента с известной хиральностью, такого как хиральный разделяющий реагент или вспомогательное соединение в виде соли, комплекса или группы, присоединенной с помощью ковалентной связи. Другой способ, известный в данной области техники, рассеяние тяжелым атомом, можно использовать, когда исследуемое соединение содержит атом, обладающий достаточной массой (например, атом брома или йода). Также можно использовать другие способы, базирующиеся на оптических характеристиках, и использующие плоскополяризованный свет. В частности, специалист в данной области техники поймет, что для данной структуры или структурного класса могут быть использованы такие методы, как круговой дихроизм.
Конкретные примеры промежуточных продуктов, которые можно получить способом, соответствующим настоящему изобретению, приведены ниже в качестве примеров, а не для наложения ограничения и их можно использовать для получения соединений формулы I, обладающих такой же абсолютной конфигурацией.

Соединения формулы III, в которых R1=Н, также можно получить по схеме получения оптически активных соединений с помощью способов, сводка которых представлена на Схеме реакций 6. Выделение рацемического сложного эфира 17а (формулы III, в которой R1 означает Н) можно осуществить путем селективного ферментативного гидролиза с использованием липазы PS (Amano) и получить 17f. Альтернативно, 17е, который можно получить гидролизом 17а, можно выделить перекристаллизацией диастереоизомерных солей, образованных с оптически активным амином, например, с (S)-(-)-α-метилбензиламином, с последующей регенерацией карбоновой кислоты путем обработки соли неорганической кислотой. Последующее превращение 17f в промежуточные продукты 17g и 17h можно осуществить способами, аналогичными описанным для получения 17с в Схеме реакций 2: переэтерификацией и удалением защитной группы R7.
Схема реакций 6
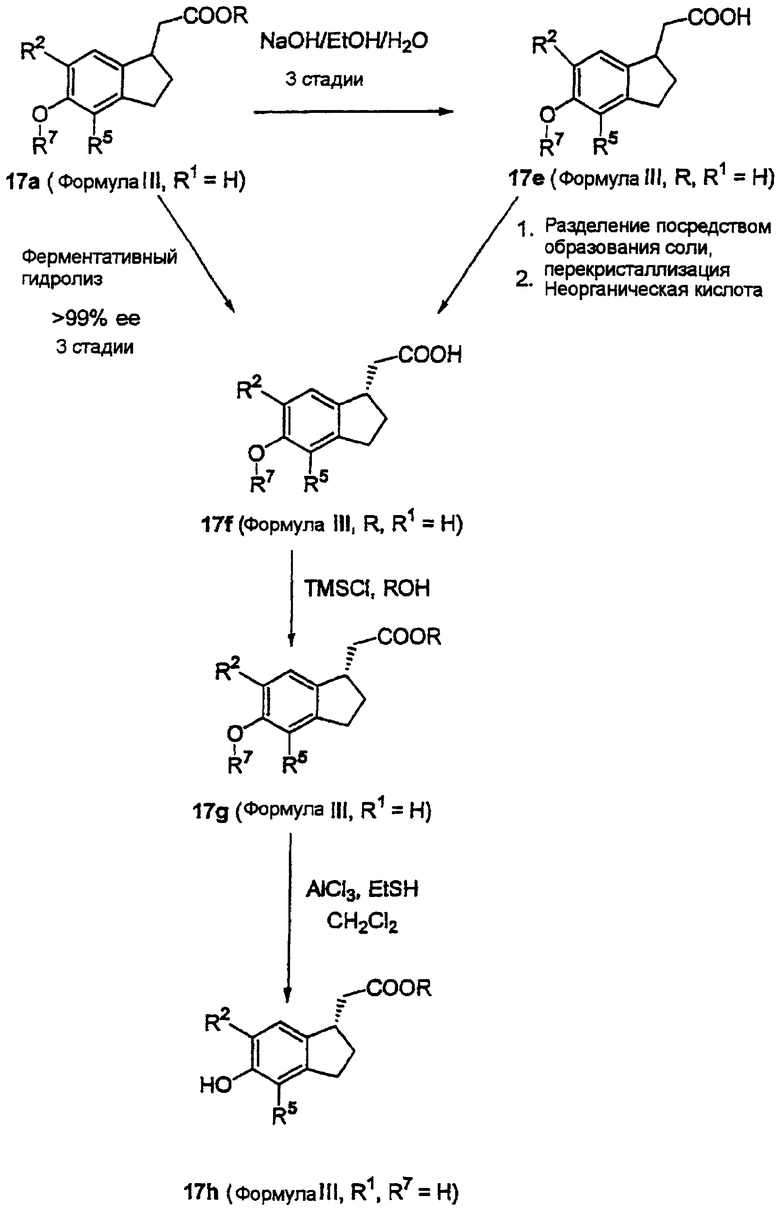
Соединения формулы I эффективны при лечении сахарного диабета типа II (включая сопутствующую диабетическую дислипидемию и другие осложнения диабета), а также для ряда других применений в фармацевтике, таких как при гипергликемии, гиперинсулинемии, нарушении переносимости глюкозы, нарушении уровня глюкозы в крови натощак, дислипидемии, гипертриглицеридемии, синдроме Х и резистентности к инсулину. Кроме того, соединения соответствующие настоящему изобретению, также эффективны для регулирования аппетита и потребления пищи при таких заболеваниях, как ожирение, и для лечения атеросклеротического заболевания, гиперлипидемии, гиперхолестеринемии, низких уровней ЛВП, гипертензии, сердечно-сосудистых заболеваний (включая атеросклероз, ишемическую болезнь сердца, заболевание коронарной артерии и гипертензию), цереброваскулярные заболевания и заболевания периферических сосудов; и для лечения волчанки, синдрома поликистоза яичников, канцерогенеза и гиперплазии. Соединения формулы I также применимы для лечения физиологических заболеваний, связанных, например, с дифференциацией клеток для продуцирования аккумулирующих липиды клеток, регуляцией чувствительности к инсулину и уровням глюкозы в крови, которые участвуют, например, в аномальной функции бета-клеток поджелудочной железы, секретирующих инсулин опухолях и/или аутоимунной гипогликемии вследствие наличия аутоантител к инсулину, аутоантител к рецептору инсулина или аутоантител, которые стимулируют бета-клетки поджелудочной железы, с дифференциацией макрофагов, которая приводит к образованию атеросклеротических бляшек, воспалительной реакцией, канцерогенезом, гиперплазией, экспрессией гена адипоцитов, дифференциацией адипоцитов, снижением массы β-клеток поджелудочной железы, секрецией инсулина, чувствительностью тканей к инсулину, ростом клеток липосаркомы, синдромом поликистоза яичников, хронической ановуляцией, гиперандрогенизмом, продуцированном прогестерона, стероидогенезом, окислительно-восстановительным потенциалом и окислительным стрессом в клетках, синтазой оксида азота (СОА), каталазой, триглицеридами плазмы, уровнями ЛВП и ЛНП холестерина и т.п.
Особенно полезными соединениями формулы I, соответствующими настоящему изобретению, являются такие, которые эффективны для снижения концентрации глюкозы в крови и уровней триглицеридов в плазме и для повышения уровней ЛВП холестерина в плазме.
Поэтому предполагается, что соединения формулы I, соответствующие настоящему изобретению, будут полезными в качестве лекарственных препаратов. В соответствии с этим вариант осуществления настоящего изобретения включает способ лечения различных патологических состояний, указанных выше, у пациента (включая млекопитающих), который включает введение указанному пациенту композиции, содержащей количество соединения формулы I, которое эффективно при лечении соответствующего патологического состояния.
Как указано выше, соединение формулы I можно вводить отдельно или в комбинации с одним или большим количеством гипогликемических агентов. Комбинированная терапия включает введение одной фармацевтической дозировочной композиции, которая содержит соединение формулы I и один или большее количество гипогликемических агентов, а также введение соединения формулы I и каждого дополнительного гипогликемического агента в своей собственной фармацевтической дозировочной композиции. Например, соединение формулы I и гипогликемический агент могут вводиться пациенту совместно в одной пероральной дозировочной композиции, такой как таблетка или капсула, или каждый агент может вводиться в отдельных пероральных дозировочных композициях.
Если используются отдельные дозировочные композиции, то соединение формулы I и один или большее количество дополнительных гипогликемических агентов можно вводить практически в одно и то же время (например, одновременно) или по отдельности в разное время (т.е. последовательно).
Например, соединение формулы I можно вводить в комбинации с одним или большим количеством следующих дополнительных гипогликемических агентов: инсулином; бигуанидинами, такими как метформин или буформин; сульфонилмочевинами, такими как ацетоксамид, хлорпропамид, толазамид, толбутамид, глиборид, глипизид, гликпарид; или с любым другим агентом для усиления секреции инсулина, таким как, например, репаглинид и натеглинид; ингибиторами α-гликозидазы, такими как укарбоза, воглибоза или миглитол; или с агонистами (β3-адренорецептора, такими как CL-316,243).
Соединения формулы I также можно использовать в виде чистой основы или в композициях, а также при исследованиях и для диагностики или в качестве аналитических эталонных стандартов и т.п., что хорошо известно в данной области техники. Поэтому настоящее изобретение включает композиции, которые содержат инертный носитель и эффективное количество соединения формулы I или его соли или сложного эфира. Инертным носителем является любое вещество, которое не взаимодействует с соединением, носителем которого оно является, и которое для соединения, носителем которого оно является, выступает в качестве удерживающего средства, средства доставки, придания объема, метки, позволяющей проследить за соединением, и т.п. Эффективным количеством соединения является такое количество, которое приводит к результату или оказывает влияние на конкретную проводимую процедуру.
Настоящее изобретение также относится к способу лечения патологического состояния пациента, при котором заболевание связано с физиологически вредным уровнем инсулина, глюкозы, свободных жирных кислот (СЖК), холестерина или триглицеридов в крови, включающему введение пациенту терапевтически эффективного количества соединения формулы I. В еще одном варианте осуществления настоящее изобретение относится к способу лечения патологического состояния пациента, при котором заболевание связано с физиологически вредным уровнем инсулина, глюкозы, свободных жирных кислот (СЖК), холестерина или триглицеридов в крови, включающему введение пациенту терапевтически эффективного количества соединения формулы I и также введение терапевтически эффективного количества дополнительного гипогликемического агента, такого как, например, инсулин, бигуанидиновое соединение и т.п.
Поскольку известно, что сульфонилмочевины и другие агенты для усиления секреции инсулина способны стимулировать выработку инсулина, но неспособны влиять на резистентность к инсулину, а соединения формулы I способны влиять на резистентность к инсулину, предполагается, что комбинацию этих лекарственных препаратов можно использовать в качестве средства лечения патологических состояний, связанных и с дефицитом секреции инсулина, и с резистентностью к инсулину. Поэтому настоящее изобретение также относится к способу лечения сахарного диабета типа II у пациента, включающему введение терапевтически эффективного количества соединения формулы I и одного или большего количества дополнительных гипогликемических агентов, таких как, например, сульфонилмочевины, бигуанидины, антагонисты β-адренорецептора, ингибиторы α-гликозидазы и инсулин. Кроме того, соединения формулы I можно использовать в комбинации с ингибиторами HMG Со-А редуктазы (статинами), связывающими желчные кислоты смолами или производными фибриновой кислоты для улучшения липидного профиля пациентов, страдающих дислипидемией и резистентностью к инсулину. Соединения формулы I также можно использовать в комбинации с агентами, которые регулируют гипертензию (например, с ингибиторами ангиотензин-конвертирующего фермента (АКФ), β-блокаторами, блокаторами кальциевых каналов) и массу тела пациентов, страдающих резистентностью к инсулину или диабетом типа II.
Приведенные ниже конкретные примеры представлены для иллюстрации описанного здесь изобретения, но их не следует рассматривать, в качестве каким-либо образом ограничивающих объем настоящего изобретения.
Примеры
ВЭЖХ-масс-спектроскопию с электрораспылением (ВЭЖХ ЭР-МС) проводят с использованием прибора Hewlett-Packard 1100 ВЭЖХ, снабженного четверным насосом, детектором с переменной длиной волны, колонкой YMC Pro C182,0 мм×23 мм и масс-спектрометром с ионной ловушкой и ионизацией электрораспылением модели Finnigan LCQ. При ВЭЖХ используют элюирование в градиентном режиме от 90% А до 95% В в течение 4 мин. Буферный раствор А содержит 98% воды, 2% ацетонитрила и 0,02% TFA, а буферный раствор В содержит 98% ацетонитрила, 2% воды и 0,018% TFA. Спектры сканируют в диапазоне 140-1200 атомных единиц массы с переменным временем пролета ионов в соответствии с количеством ионов в источнике.
Протонные 1Н) спектры ядерного магнитного резонанса (ЯМР) снимают на спектрометре General Electric GN-Omega 300 (300 МГц) с использованием в качестве стандарта Me4Si (δ 0,00) или остаточного протонированного растворителя (CHCl3 δ 7,26; МеОН δ 3,30; ДМСО δ 2,49). Углеродные (13С) спектры ЯМР снимают на спектрометре General Electric GN-Omega 300 (75 МГц) с использованием в качестве стандарта растворителя (CDCl3 δ 77,0; d3-MeOD; δ 49,0; d6-ДМСО δ 39,5).
Хиральное разделение проводят с использованием коммерчески доступной колонки Chiracel® AD ВЭЖХ, элюируя в градиентном режиме раствором изопропанола в гексане (от 1% до 15%) с прибавлением 0,1% трифторуксусной кислоты.
Аббревиатуры и сокращения
При использовании в настоящем изобретении приведенные ниже аббревиатуры обладают следующими значениями:
Ac2O - уксусный ангидрид
ADDP - 1,1'-(азодикарбонил)-дипиперидин
ВОС - трет-бутоксикарбонил
n-BuOH - н-бутанол
f-BuOH - трет-бутанол
f-BuOK - трет-бутоксид калия
CDl - карбонилдиимидазол
CD3OD - метанол-d4
Celite® - фильтрующий реагент диатомовая земля, ®Celite Corp.
СН2Cl2 - метиленхлорид
ХИ-МС (МС (ХИ)) - масс-спектроскопия с химической ионизацией
DCC - дициклогексилкарбодиимид
DCM - дихлорметан
de - избыток диастереоизомера
DEAD - диэтилазодикарбоксилат
DIA - диизопропиламин
DIBAL-H - диизобутилалюминийгидроксид
DMAP - 4-(N,N-диметиламино)-пиридин
DME - диметоксиэтан
DMF - N,N-диметилформамид
ДМСО - диметилсульфоксид
EDCl - 1-(3-диметиламинопропил)-3-этилкарбодиимидгидрохлорид
ее - избыток энантиомера
ИДСР - испарительный детектор по светорассеянию
ЭР-МС - масс-спектроскопия с электрораспылением
EtOAc - ацетилацетат
EtOH - этанол (100%)
EtSH - этантиол
Et2O - диэтиловый эфир
Et3N - триэтиламин
ГХ-МС - газовая хроматография - масс-спектроскопия
ВЭЖХ - высокоэффективная жидкостная хроматография
IPA - изопропиламин
LAH - алюмогидрид лития
ЖХ-МС - жидкостная хроматография - масс-спекроскопия
LDA - диизопропиламид лития
m/z - отношение массы к заряду
MeCN - ацетонитрил
NMM - 4-метилморфолин
Ph3Р - трифенилфосфин
Pd(dppf)Cl2 - [1,1'-бис(дифенилфосфино)-ферроцен]-дихлорпалладий(II)
Pd(PPh3)4 - тетракис(трифенилфосфин)-палладий(0)
Pd(OAc)2 - ацетат палладия
Р(O)Cl3 - оксихлорид фосфора
Rf - коэффициент удерживания (ТСХ)
ВУ - время удерживания (ВЭЖХ)
TEA - триэтиламин
THF - тетрагидрофуран
TFA - трифторуксусная кислота
ТСХ - тонкослойная хроматография
TMAD - N,N,N',N'-тетраметилэтилендиамин
TMSCI - триметилсилилхлорид
Обозначения в спектрах ЯМР: s - синглет, d - дублет, t - триплет, q - квадруплет, m - мультиплет, br - широкий.
Пример 1
Получение метил-2-(6-метокси-1H-инден-3-ил)-бутаноата

К высушенной в сушильном шкафу 5-литровой четырехгорлой колбе присоединяют термометр, холодильник, капельную воронку и механическую мешалку. В атмосфере Ar при 60°С (температура внутри колбы) перемешивают суспензию 5-метокси-1-инданона (80,0 г, 494 ммоль), порошкообразного Zn (Lancaster, 56,2 г, 865 ммоль) в 2 л безводного THF и через капельную воронку медленно прибавляют раствор метилбромбутирата (134,1 г, 741 ммоль) в 400 мл безводного THF. После завершения прибавления реакционную смесь перемешивают при 60°С (температура внутри колбы) в течение 1 ч. За протеканием реакции следят, проводя анализы аликвот, с помощью ТСХ после обработки 1 н. водным раствором HCl. После завершения реакции реакционную смесь охлаждают в бане из воды со льдом, а затем медленно прибавляют 3 л 1 н. раствора HCl. Температуру колбы поддерживают ниже 20°С. Затем смесь экстрагируют с помощью 1 л EtOAc. Органический слой промывают водой до рН 6,0-7,0, затем насыщенным раствором NaCl и сушат над Na2SO4. Продукт (127 г, >99%), желтое масло, получают после удаления растворителя и сушки в вакууме. 1H ЯМР (ДМСО-d6) δ 7,28 (d, 1Н), 7,05 (d, 1Н), 6,82 (dd, 1Н), 6,22 (s, 1Н), 3,72 (s, 3Н), 3,60 (m, 1Н), 3,58 (s, 3Н), 3,28 (s, 2H), 1,95 (m, 1Н), 1,80 (m, 1Н), 0,88 (t, 3H).
Пример 2а
Получение 2-(6-метокси-1Н-инден-3-ил)-бутановой кислоты
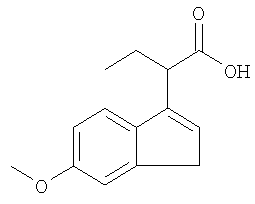
К раствору сложного эфира, полученного в Примере 1 (14,0 г, 58,9 ммоль), в 140 мл МеОН прибавляют раствор КОН (6,4 г, 113,8 ммоль) в 5 мл воды. Реакционную смесь перемешивают при 60°С (температура в колбе) в течение 2 ч. ТСХ свидетельствует о конверсии, равной 70%. Затем в колбу медленно прибавляют раствор КОН (3,0 г, 53,6 ммоль) в 100 мл воды. Через 1 ч реакция завершается. После охлаждения до комнатной температуры растворители удаляют при пониженном давлении. Остаток растворяют в 500 мл воды и затем промывают с помощью EtOAc. Водный слой охлаждают в бане из воды со льдом и затем подкисляют концентрированной HCl до рН<3,0. Продукт экстрагируют с помощью 300 мл CH2Cl2, промывают водой (2×100 мл), затем сушат над Na2SO4. После отфильтровывания Na2SO4 раствор в CH2Cl2 перемешивают с 3,0 г угля в течение 2 ч. Уголь удаляют фильтрованием через слой Celite®. Искомый продукт (12,5 г, 95%) получают в виде светло-коричневого твердого вещества после удаления растворителя и сушки в вакууме. 1H ЯМР (ДМСО-d6) δ 12,20 (b, 1H), 7,30 (d, 1H), 7,06 (d, 1H), 6,82 (dd, 1H), 6,22 (s, 1Н), 3,75 (s, 3Н), 3,45 (t, 1Н), 3,30 (s, 2Н), 1,90 (m, 1Н), 1,78 (m, 1Н), 0,90 (t, 3H).
Пример 2b
Получение 2-(6-метокси-1Н-инден-3-ил)-пропановой кислоты
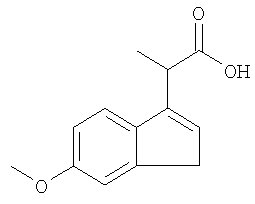
Это вещество получают с помощью тех же методик, что и описанные в Примерах 1 и 2а, исходя из 5-метоксил-1-инданона и метил-2-бромпропионата. Выход: 68%. 1H ЯМР (CD2Cl2) δ 7,34 (d, J=9, 1Н), 7,07 (d, J=2, 1Н), 6,85 (dd, J=9, J=2, 1Н), 6,32 (m, 1Н), 3,82 (m, 4H), 3,36 (m, 2H), 1,56 (d, J=7, 3Н).
Пример 3
Получение (2S)-2-(6-метокси-1Н-инден-3-ил)-бутановой кислоты
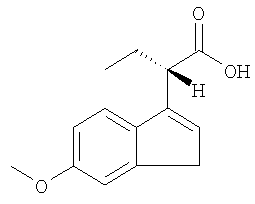
К раствору рацемической инденовой кислоты, полученной в Примере 2а (300 г, 1,29 моль), в 4,5 л CH3CN при комнатной температуре прибавляют хинин (324 г, 1,0 моль). Смесь перемешивают в течение 1 ч и получают раствор. Небольшое количество нерастворимых частиц удаляют путем фильтрования в вакууме через фильтр из микроволокон. Затем фильтрат механически перемешивают в атмосфере Ar в течение ночи. Через 24 ч небольшой образец твердого вещества отбирают и анализируют и в результате получают 76,2% ее. Еще через 2 суток перемешивание прекращают. Суспензию фильтруют. Осадок на фильтре промывают с помощью СН3CN (3×200 мл) и затем сушат в вакууме при 40°С в течение 3 ч. Это твердое вещество перемешивают с 4,5 л CH3CN при 70°С, пока все твердое вещество не перейдет в раствор. Раствору дают медленно охладиться до комнатной температуры. Полученную суспензию перемешивают при комнатной температуре в течение 24 ч. Суспензию фильтруют. Осадок на фильтре промывают с помощью СН3CN (3×250 мл) и затем сушат в вакууме при 40°С в течение 24 ч. Эту соль хинина собирают в виде белого твердого вещества (254,6 г, выход 35,4%, 96,8% ее).
Соль хинина (544,3 г, 0,98 моль) растворяют в 4,0 л CH2Cl2 и получают прозрачный раствор. Его энергично перемешивают с 4,0 л 2 н. раствора HCl в 22-литровой круглодонной колбе с нижним краном. Через 30 мин смеси дают отстояться. Нижний слой отделяют и верхний водный слой экстрагируют с помощью 1 л CH2Cl2. Объединенные слои с CH2Cl2 промывают водой (3×2,0 л) до рН 5,0-6,0 и затем сушат над Na2SO4. Продукт (230,8 г, 99%, 96,8% ее) получают в виде почти белого твердого вещества после удаления растворителя и сушки в вакууме. 1H ЯМР совпадает с таковым для рацемического вещества, описанного в Примере 2а.
Проведенная аналогичным образом обработка маточного раствора дает (R)-изомер. Альтернативно, для осуществления рацемизации и извлечения исходного рацемического вещества маточный раствор можно обработать водным раствором основания.
Пример 4
Получение (2S)-2-[(1S)-5-метокси-2,3-дигидро-1Н-инден-1-ил]-бутановой кислоты
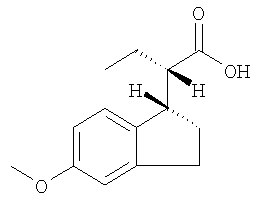
Раствор продукта, полученного в Примере 3 (105 г, 453 ммоль), ClRh(PPh3)3 (21,0 г, 5% экв.) и триэтиламин (68,8 г, 679,5 ммоль) в EtOH (945 мл) и THF (105 мл), встряхивают в 2-литровом автоклаве при давлении Н2, равном 60 фунт-сила/дюйм2, в течение 16 ч. Растворители удаляют при пониженном давлении. Полученную смесь перемешивают в 1,5 л 1 н. раствора HCl и 1,5 л CH2Cl2. Водный слой экстрагируют с помощью CH2Cl2 (2×250 мл). Объединенные СН2Cl2 слои промывают с помощью 1 л 1 н. раствора HCl и перемешивают с 1 л 1 н. раствора NaOH. Органический слой экстрагируют с помощью 1 N раствора NaOH (2×0,5 л). Объединенные водные слои промывают с помощью CH2Cl2 (2×250 мл) и подкисляют (до рН 2,0-3,0) путем медленного прибавления концентрированного раствора HCl при температуре ниже 15°С. Кислую смесь экстрагируют с помощью CH2Cl2 (2×1,5 л) и промывают водой (2×0,5 л) до рН 5,0-6,0. После промывки рассолом и сушки над безводным Na2SO4 растворитель выпаривают при пониженном давлении. Продукт (101,0 г, выход 95%, 96,8% ее) получают в виде светло-желтого масла. 1Н ЯМР (ДМСО-d6) δ 12,20 (s, 1Н), 7,04 (d, 1H), 6,78 (d, 1H), 6,66 (dd, 1H), 3,70 (s, 3Н), 3,28 (m, 1H), 2,72 (m, 2H), 2,32 (m, 1H), 2,06 (m, 1H), 1,80 (m, 1H), 1,50 (m, 1H), 1,36 (m, 1H), 0,82 (t, 3Н).
Пример 5а
Получение син-2-[5-метокси-2,3-дигидро-1Н-инден-1-ил]-бутановой кислоты
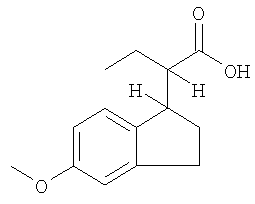
Суспензию рацемической инденовой кислоты (Пример 2, 980 мг, 4,2 ммоль), ClRh(PPh3)3 (139 мг, 0,15 ммоль), NaHCO3 (378 мг, 4,5 ммоль) в EtOH (20 мл) и H2O (10 мл) встряхивают в автоклаве объемом 500 мл при давлении Н2, равном 60 фунт-сила/дюйм2, в течение 30 ч. К реакционной смеси прибавляют дополнительное количество ClRh(PPh3)3 (300 мг, 0,33 ммоль) и гидрирование продолжают в течение еще 3 суток. После этого EtOH удаляют при пониженном давлении и остаток разбавляют с помощью 200 мл воды. Черное твердое вещество удаляют фильтрованием и фильтрат промывают с помощью EtOAc (2×200 мл). Водный раствор затем подкисляют концентрированной HCl и экстрагируют с помощью CH2Cl2 (2×100 мл). Объединенные слои, содержащие CH2Cl2, промывают рассолом и сушат над Na2SO4. Удаление растворителя в вакууме дает индановую кислоту в виде светло-желтого масла (600 мг, 60%). Смесь продуктов приводит к смеси диастереоизомеров (87:13) с преобладанием син-изомеров, о чем свидетельствуют данные анализа с помощью ЯМР с использованием отношения интегрирования пиков ЯМР, равного δ 7,11 (d, 1Н) для анти- и δ 7,03 (d, 1Н) для син-изомеров.
Разделение продукта на оптические изомеры можно осуществить следующим образом: при перемешивании механической мешалкой к раствору син-индануксусной кислоты [(2R,1R) и (2S,1S), 14,69 г, 62,7 ммоль] в ацетонитриле (290 мл) при комнатной температуре одной порцией прибавляют (Р)-(+)-α-метилбензиламин (8,49 мл, 65,9 ммоль). Полученную смесь перемешивают в течение ночи. Происходит образование небольшого количества твердого вещества. Реакционную смесь концентрируют досуха и остаток при нагревании повторно растворяют в ацетонитриле (200 мл). Для стимулирования осаждения проводят перемешивание магнитной мешалкой. Смесь перемешивают в течение ночи. Твердые вещества собирают путем фильтрования и трижды промывают небольшим количеством холодного ацетонитрила. Твердые вещества затем сушат в вакууме в течение 1,5 ч (8,1 г, 86% ее). Немного влажные твердые вещества перекристаллизовывают в ацетонитриле (120 мл) и получают 6,03 г (R)-α-метилбензиламиновой соли (2S)-2-[(1S)-5-метокси-2,3-дигидро-1Н-инден-1-ил]-бутановой кислоты (94,4% ее). Вторую порцию собирают из различных фильтратов (0,89 г, 97,6% ее). Суммарный выход разделения составляет 31% (62% в расчете на максимальное содержание (2S,1R)-кислоты в рацемате). Вещество идентично полученному в Примере 4.
Оптическую чистоту для этого Примера и Примера 4 можно определить путем анализа с помощью хиральной ВЭЖХ; Колонка: Chiracel AD, 4,6 (внутренний диаметр)×250 мм; подвижная фаза, А:0,1% TFA (трифторуксусная кислота) в гексанах, В:0,1% TFA в IPA (изопропиловый спирт); Методика, изократическая 95% А (5% В), 20 мин; скорость потока, 1,5 мл/мин; Детектор (УФ), 284 нм. Времена удерживания для четырех возможных диастереоизомеров равны 5,163 мин (2S,1R), 6,255 мин (2R,1S), 10,262 мин (2R,1R) 14,399 мин (2S,1S). Первый указатель (2S или 2R) показывает абсолютную конфигурацию атома углерода, соседнего с карбоксильной группой (положение 2); второй указатель (1S или 1R) показывает абсолютную конфигурацию атома углерода инданового цикла (его положение 1).
Стереохимическое отнесение каждого пика было проведено путем анализа с помощью хиральной ВЭЖХ рацемической диастереоизомерной смеси соединения 5 с неодинаковым содержанием син/анти-изомеров, что привело к четырем пикам, разрешенным относительно базовой линии. По данным интегрирования УФ-полос пики 3 и 4, а также пики 1 и 2 относятся к парам энантиомеров. По данным рентгеноструктурного анализа абсолютная конфигурация соединения, соответствующего пику 4, представляет собой 2S,1S. Соединению, соответствующему пику 3, соответствующему энантиомеру, с определенностью приписана конфигурация 2R,1R. Пик 1 приписан (2S,1R-диастереоизомеру (время удерживания: 5,363 мин, примерно 0,97% площади) на основании сопоставления с содержащимся в небольшом количестве продуктом, полученным восстановлением хиральной кислоты (Пример 3) в соответствии с описанием в Примере 4. Оставшийся пик 2 с определенностью можно приписать соединению с конфигурацией 2R,1S.
Пример 5b
Получение син-2-[5-метокси-2,3-дигидро-1Н-инден-1-ил]-пропановой кислоты

Соединение получено с выходом 71% и >99% de с использованием той же методики, что и описанная в Примере 4, исходя из (рацемического) продукта Примера 2b: 1H ЯМР (ДМСО-d6) δ 12,18 (s, 1Н), 7,03 (d, J=8, 1H), 6,75 (d, J=2, 1Н), 6,67 (dd, J1=8, J2=2, 1Н), 3,68 (s, 3Н), 3,37 (m, 1Н), 2,72 (m, 3H), 2,03 (m, 1Н), 1,75 (m, 1Н), 0,89 (d, J=7, 3Н); 13С ЯМР (CD2Cl2) δ 12,626, 28,228, 31,950, 43,300, 46,445, 55,607, 110,054, 112,510, 124,552, 136,702, 146,411, 159,464, 182,330.
Пример 6
Получение метил-(2S)-2-[(1S)-5-метокси-2,3-дигидро-1Н-инден-1-ил]-бутаноата
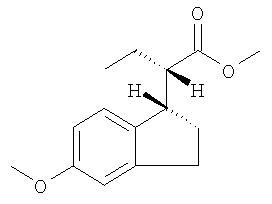
Суспензию кислоты, полученной в Примере 4 (220,0 г, 0,94 моль), NaHCO3 (237,0 г, 2,82 моль), СН3l (200 г, 1,41 моль) в 2,0 л DMF, перемешивают в атмосфере Ar при комнатной температуре в течение 18 ч. Проведенный с помощью ЯМР анализ показывает, что реакция прошла на 95%. Прибавление СН3l (100 г) и перемешивание в течение еще 24 ч при комнатной температуре приводит к завершению реакции. Реакционную смесь выливают в 4,0 л воды и экстрагируют с помощью EtOAc (2×2 л). Органический слой последовательно промывают водой (2×1 л), 1 л 1 н. раствора NaOH, водой (2×1 л) и 500 мл рассола и сушат над Na2SO4. Продукт (233 г, 99%) получают в виде светло-желтого масла после удаления растворителя и сушки в вакууме. 1H ЯМР (ДМСО-d6) δ 6,90 (d, 1H), 6,78 (d, 1H), 6,66 (dd, 1H), 3,70 (s, 3H), 3,60 (s, 3H), 3,20 (m, 1 Н), 2,80 (m, 2Н), 2,40 (m, 1Н), 2,08 (m, 1Н), 1,80 (m, 1Н), 1,58 (m, 1H), 1,40(m, 1H), 0,80 (t, 3H).
Пример 7
Получение метил-(2S)-2-[(1S)-5-гидрокси-2,3-дигидро-1Н-инден-1-ил]-бутаноата
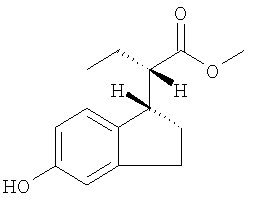
К холодному раствору (баня из воды со льдом) соединения, полученного в Примере 6 (233 г, 0,94 моль) в 2,5 л CH2Cl2 медленно прибавляют AlCl3 (630 г, 4,7 моль) в атмосфере Ar. Температуру в колбе поддерживают ниже 20°С и цвет реакционной смеси переходит в пурпурный. С помощью капельной воронки в реакционной смеси медленно прибавляют EtSH (345 мл, 4,7 моль) и температуру в колбе поддерживают ниже 15°С. Через 2 ч перемешивания при температуре ниже 20°С по данным анализа с помощью ЯМР реакция завершается. Смесь из колбы при энергичном перемешивании медленно выливают в 2,5 л воды со льдом. Органический слой отделяют и водный слой экстрагируют с помощью 1 л CH2Cl2. Объединенные слои, содержащие CH2Cl2, промывают водой (4×1 л) до рН 6,0-7,0, и затем сушат над Na2SO4. Продукт (216 г, 98%) получают в виде белого твердого вещества после удаления растворителя и сушки в вакууме. 1Н ЯМР (ДМСО-d6) δ 9,10 (s, 1H), 6,78 (d, 1H), 6,58 (d, 1H), 6,50 (dd, 1H), 3,60 (s, 3H), 3,20 (q, 1H), 2,70 (m, 2H), 2,40 (m, 1H), 2,08 (m, 1H), 1,80 (m, 1H), 1,50 (m, 2H), 0,80 (t, 3H).
Пример 8
Получение метил-3-[(4-метилбензоил)-амино]-4-оксопентаноата
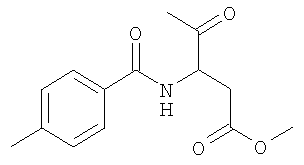
К суспензии гидрохлорида (3-метилового эфира L-аспарагиновой кислоты (250 г, 1,36 моль) в охлаждаемом (<5°С) СН2Cl2 (4 л) равномерным потоком прибавляют Et3N (440 г, 4,35 моль), а затем медленно прибавляют Ме3SiCi (324 г, 2,99 моль). Смесь нагревают до 25°С и перемешивают в течение 1 ч, повторно охлаждают (<10°С) и по каплям прибавляют п-толуолилхлорид (205 г, 1,36 моль). При перемешивании в течение 16 ч смеси дают медленно нагреться до комнатной температуры. Затем реакционную смесь разбавляют с помощью СН2Cl2 (500 мл) и промывают с помощью 1 н. HCl (500 мл), рассола (500 мл) и сушат над Na2SO4. Образовавшийся амин (310 г, 91%), белое твердое вещество, получают после удаления растворителя и сушки в вакууме. Затем его растворяют в пиридине (1,25 л) и прибавляют DMAP (5 г). Медленно прибавляют уксусный ангидрид (840 мл) и затем реакционную смесь нагревают при 90°С в течение 2 ч. Охлажденный раствор выливают в 7 л воды со льдом и экстрагируют с помощью 6 л EtOAc. Органический слой промывают с помощью 2 н. HCl (3×1 л) и 1 н. NaOH (1 л), сушат над MgSO4 и концентрируют и получают искомое соединение в виде белого твердого вещества (301 г, 93%).
Пример 9
Получение метил-[5чиетил-2-(4-метилфенил)-1,3-оксазол-4-ил]-ацетата
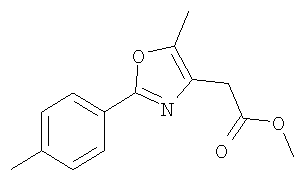
Промежуточный продукт, полученный в Примере 8 (280 г, 1,06 моль), растворяют в уксусном ангидриде (650 мл), затем медленно прибавляют концентрированную H2SO4 (60 мл). Температура в колбе повышается до 80°С. Затем реакционную смесь выдерживают при 85°С в течение 1 ч, охлаждают и уксусный ангидрид удаляют в вакууме. Остаток выливают в воду со льдом (2 л) и экстрагируют с помощью EtOAc (всего 4 л). Затем органический слой перемешивают с 1 н. NaOH (500 мл) в течение 1 ч, отделяют, затем сушат над MgSO4 и концентрируют и получают искомый сложный эфир в виде прозрачного масла (223 г, 87%), которое медленно затвердевает в белое твердое вещество.
Пример 10
Получение 2-[5-метил-2-(4-метилфенил)-1,3-оксазол-4-ил]-этанола
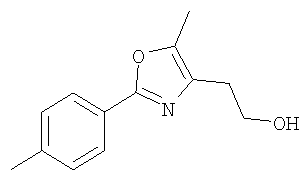
Сложный эфир оксазола, полученный в Примере 9 (300 г, 1,22 моль), растворяют в THF (2,7 л) и порциями по 5 г прибавляют твердый LiBH4 (26,6 г, 1,22 моль), поддерживая температуру ниже 45°С. Реакция завершается в течение часа после прибавления. Количество растворителя уменьшают вдвое и затем остаток выливают в воду со льдом (3 л). Затем смесь подкисляют, медленно прибавляя 1 н. HCl (1 л). Образуется белый осадок и его собирают путем фильтрования и сушат в сушильном шкафу над P2O5 и получают искомый сложный эфир оксазола (214 г, 83%).
Пример 11
Получение метил-(2S)-2((1S)-5-{2-[5-метил-2-(4-метилфенил)-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1Н-инден-1-ил)-бутаноата
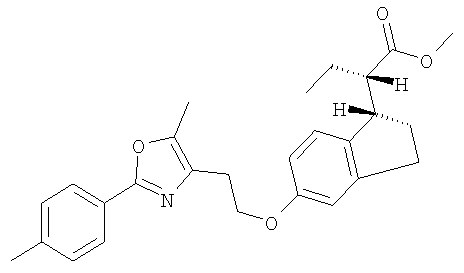
Суспензию гидроксиинданкарбоксилата, полученного в Примере 7 (208 г, 889 ммоль), оксазолового спирта, полученного в Примере 10 (212 г, 977 ммоль), ADDP (335 г, 1,33 моль), Ph3Р (348 г, 1,33 моль) в 6,0 л безводного THF, перемешивают при комнатной температуре в атмосфере Ar. За протеканием реакции следят с помощью 1H ЯМР. Через 2 дня дальнейшее протекание реакции не наблюдается. После удаления твердых веществ с помощью фильтрования THF удаляют при пониженном давлении. Оставшуюся смесь перемешивают в 3 л смеси 50/50 EtOAc/гексан в течение 10 мин, образуется дополнительное количество твердых веществ и их удаляют с помощью фильтрования. Фильтрат концентрируют и обрабатывают по той же методике с помощью смеси 25/75 EtOAc/гексан. После удаления растворителей полученную маслообразную смесь очищают на колонке с силикагелем (3,0 кг) с использованием CH2Cl2 (10,0 л) и 20% СН3CN/CH2Cl2 (10,0 л) в качестве растворителя. Фракции, содержащие продукт, собирают и затем концентрируют. Неочищенную смесь растворяют в 4,0 л CH2Cl2 непрореагировавшее гид-роксисоединение удаляют путем промывки с помощью 1 н. NaOH (3×1 л). Слой, содержащий CH2Cl2, сушат над Na2SO4. Продукт (358 г, 93%) получают в виде светло-желтого масла после удаления растворителя и сушки в вакууме. 1H ЯМР (ДМСО-d6) δ 7,78 (d, 2Н), 7,30 (d, 2H), 6,90 (d, 1Н), 6,75 (d, 1H), 6,65 (dd, 1Н), 4,15 (t, 2H), 3,60 (s, 3Н), 3,25 (q, 1H), 2,90 (t, 2H), 2,75 (m, 2H), 2,40 (m, 1H), 2,35 (s, 3Н), 2,32 (s, 3Н), 2,05 (m, 1H), 1,80 (m, 1H), 1,50 (m, 2H), 0,80 (t, 3Н).
Пример 12
Получение (2S)-2-f(1S)-5-{2-[5-метил-2-(4-метилфенил)-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-бутановой кислоты
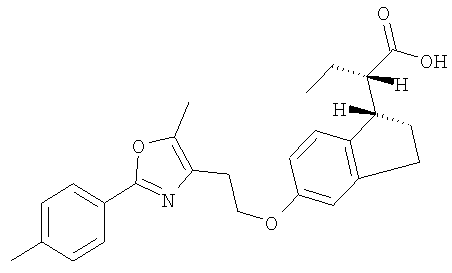
К раствору LiOH (90,4 г, 3,76 моль) в 1,3 л воды и 1,3 л МеОН прибавляют раствор сложного эфира, полученного в Примере 11 (325 г, 0,75 моль), в 3,9 л THF при комнатной температуре. Раствор становится мутным. Эту смесь нагревают при 60°С (температура в колбе) в течение 4 ч и анализ с помощью ТСХ (50% EtOAc/гексан) показывает, что реакция протекала примерно на 50%. К реакционной смеси прибавляют раствор LiOH (30,1 г, 1,25 моль) в воде (200 мл). Через 2 ч анализ с помощью ТСХ показывает, что реакция протекала примерно на 85%. К реакционной смеси повторно прибавляют раствор LiOH (30,1 г, 1,25 моль) в воде (200 мл). Через 2 ч анализ с помощью ТСХ показывает, что осталось очень мало исходного сложного эфира. Затем реакционную смесь охлаждают до комнатной температуры, THF и МеОН удаляют при пониженном давлении. Остаток разбавляют водой, пока не растворятся твердые вещества (используют всего 60 л воды). К этому водному раствору медленно прибавляют концентрированный раствор HCl до рН 2,0-3,0. Твердое вещество собирают путем фильтрования и сушат с помощью лабораторной вакуумной линии в течение ночи. Это твердое вещество в течение 30 мин перемешивают с 15 л EtOAc и 2 л 1 н. раствора HCl. Слой, содержащий EtOAc, отделяют и промывают с помощью 1 N раствора HCl (2×1 л). Затем органическую фазу промывают водой (4×2 л) до рН 5,0-6,0. В атмосфере Ar объем раствора в EtOAc уменьшают до 2,5 л путем отгонки при нормальном давлении, затем охлаждают до комнатной температуры без перемешивания. Осаждается белое твердое вещество. После дополнительного охлаждения в бане из воды со льдом в течение 2 ч твердое вещество отфильтровывают и промывают с помощью 500 мл холодного EtOAc. После сушки в высоком вакууме при 35°С до постоянной массы конечный продукт (266 г, 81%, 98% ее) собирают в виде белых кристаллов.1H ЯМР (CDCl3) δ 7,82 (d, 2H), 7,20 (d, 2Н), 7,05 (d, 1H), 6,75 (d, 1Н), 6,70 (dd, 1H), 4,20 (t, 2H), 3,42 (q, 1H), 2,95 (t, 2H), 2,80 (m, 2H), 2,50 (m, 1Н), 2,35 (s, 3Н), 2,32 (s, 3Н), 2,20 (m, 1Н), 1,90 (m, 1Н), 1,65 (m, 1Н), 1,45 (m, 1H), 0,90 (t, 3Н). Хиральная чистота 99% ее, [α]D=+16,11 (CHCl3), Температура плавления 149,5-150,5°С.
Пример 13
Получение 2-{5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}-бутановой кислоты
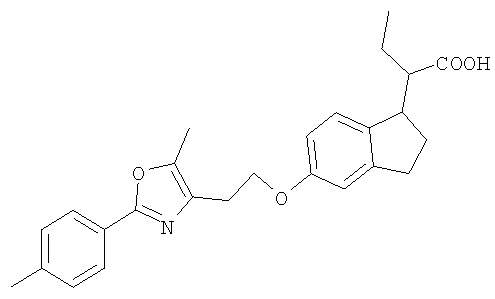
Стадия 1. К раствору 5-метокси-инданона (10 г) в толуоле (150 мл) прибавляют Aids (15 г). Смесь кипятят с обратным холодильником в течение 4 ч, пока не выпадет осадок. Полученную смесь охлаждают и выливают в воду со льдом (150 мл). Осадок фильтруют и промывают водой, затем сушат на воздухе и получают искомый продукт (8,5 г, 90%).
Стадия 2. Бензилбромид (17 г), 5-гидроксиинданон (15 г), К2СО3 (20 г) и 200 мл ацетона перемешивают в круглодонной колбе (500 мл). Смесь кипятят с обратным холодильником в течение 1 ч. К2СО3 отфильтровывают и фильтрат выпаривают. Полученный остаток перекристаллизовывают из EtOAc и получают 18 г продукта (75%).
Стадия 3. Раствор 5-бензилоксилинданона (1,14 г, 4,79 ммоль) и диэтилмалоната (0,844 г, 5,29 ммоль) в THF (20 мл) охлаждают до 0°С в атмосфере аргона и по каплям прибавляют TiCl4 (10 мл, 1 М в CH2Cl2). В конце прибавляют пиридин (2 мл). Полученную смесь перемешивают в течение ночи при комнатной температуре. После фильтрования в фильтрат прибавляют EtOAc (30 мл). Органический слой промывают рассолом (20 мл×3), сушат над Na2SO4 и выпаривают. Остаток разделяют с помощью хроматографии на силикагеле и получают 800 мг продукта (50%).
Стадия 4. Продукт, полученный на стадии 3 (1,7 г), растворяют в МеОН (25 мл) и в виде взвеси Pd-C (300 мг) прибавляют к МеОН и помещают при давлении Н2, равном 60 фунт-сила/дюйм2, в аппарат Парра для встряхивания на 6 ч. После фильтрования и концентрирования получают 1,2 г продукта (92%).
Стадия 5. Р(Ph)3 (420 мг) и ADDP (420 мг) растворяют в THF (5 мл) при 0°С и перемешивают в течение 10 мин. В колбу прибавляют раствор оксазола (300 мг) и фенола (430 мг) в THF. Полученную смесь перемешивают в течение 24 ч и фильтруют. Фильтрат выпаривают и полученный остаток разделяют с помощью хроматографии на силикагеле и получают продукт (320 мг, 45%).
Стадия 6. Промежуточный продукт, полученный на стадии 5 (160 мг), растворяют в THF (5 мл) и к раствору прибавляют йодэтан (0,5 мл) и t-BuOK (50 мг) и перемешивают в течение ночи. После фильтрования продукт отделяют с помощью ТСХ, получая 100 мг (65%).
Стадия 7. Промежуточный продукт, полученный на стадии 6 (30 мг), растворяют в ДМСО (1 мл). В колбу прибавляют LiCl (160 мг). Смесь кипятят с обратным холодильником в течение 5 ч. Из полученной смеси продукт отделяют с помощью ТСХ, получая 13 мг (52%).
Стадия 8. Промежуточный продукт, полученный на стадии 7, подвергают гидролизу в водном растворе КОН, как это описано в Примере 2 и получают продукт: ЖХ-МС, ВУ 3,57 мин, М+1 406; 1H ЯМР (CD2Cl2): δ 0,93 (t, 3Н), 1,40-1,70 (m, 2H), 1,80-2,20 (m, 2Н), 2,30 (s, 3Н), 2,40 (m, 1Н), 2,60-2,80 (m, 2H), 2,90 (t, 2H), 3,20-3,40 (m, 1Н), 4,10 (t, 2H), 6,60 (dd, 1Н), 6,70 (d, 1H), 7,00 (d, 1H), 7,30 (m, 3Н), 7,90 (m, 2H).
С использованием методик из Примеров 1-13, в некоторых случаях совместно со способом разделения с помощью хиральной ВЭЖХ, описанным в общем разделе, и с использованием подходящих исходных веществ, следующие вещества получают и характеризуют аналогичным образом:
Пример 14
2-(5-{2-[5-Метил-2-(4-метилфенил)-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1Н-инден-1-ил)-бутановая кислота

ЖХ-МС, ВУ 3,70 мин, М+1 420; 1H ЯМР (CD2Cl2): δ 0,93 (t, 3Н), 1,40-1,70 (m, 2H), 1,80-2,20 (m, 2H), 2,30 (s, 3H),2,35 (s, 3Н), 2,40 (m, 1H), 2,60-2,80 (m, 2H), 2,90 (t, 2H), 3,20-3,40 (m, 1H), 4,10 (t, 2H), 6,60 (dd, 1H), 6,70 (d, 1H), 7,00 (d, 1H), 7,20 (m, 3Н), 7,80 (m, 2H).
Пример 15
(2S)-2-{(1S)-5-[2-(5-Метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}-бутановая кислота
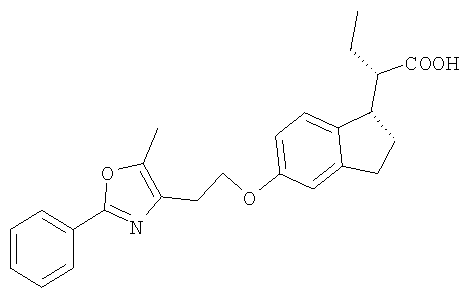
Энантиомер выделяют с помощью хиральной ВЭЖХ. ЖХ-МС, ВУ 3,57 мин, М+1 406; 1H ЯМР (CD2Cl2): δ 0,93 (t, 3Н), 1,48 (ddq, 1Н), 1,68 (ddq, 1H), 1,93 (dddd, 1H), 2,18 (dddd, 1H), 2,34 (s, 3Н), 2,50 (ddd, 1H), 2,77 (ddd, 1H), 2,87 (ddd, 1H), 2,96 (t, 2H), 3,42 (ddd, 1H), 4,19 (t, 2H), 6,68 (dd, 1H) 6,77 (d, 1H), 7,08 (d, 1H), 7,42 (m, 2H), 7,44 (m, 1Н), 7,97 (dd, 2H). 13С ЯМР: 510,4, 12,4, 22,4, 26,6, 29,5, 31,8, 46,5, 51,8, 67,2, 110,9, 113,0, 124,7, 126,2, 128,1, 129,1, 130,2, 133,2, 137,1, 145,6, 146,3, 158,7, 159,7, 180,4.
Пример 16
(2S)-2-{(1R)-5-[2-(5-Метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}-бутановая кислота

Энантиомер выделяют с помощью хиральной ВЭЖХ. ЖХ-МС, ВУ 3,57 мин, М+1 406; 1H ЯМР(CD2Cl2):δ 0,93 (t, 3H), 1,61 (ddq, 1H), 1,69 (ddq, 1H), 1,99 (dddd, 1H),2,19 (dddd, 1H), 2,47 (s, 3Н), 2,52 (ddd, 1H), 2,73 (ddd, 1H), 2,89 (ddd, 1H), 3,11 (t, 2H), 3,31 (ddd, 1H), 4,21 (t, 2H), 6,66 (dd, 1H) 6,74 (d, 1H), 7,13 (d, 1H), 7,55 (m, 2H), 7,61 (m, 1H), 8,05 (dd, 2H). 13C ЯМР: δ 10,5, 12,2, 23,8, 24,8, 30,3, 31,5, 46,4, 50,9, 66,1, 110,8, 112,6, 125,9, 127,4, 123,6, 129,8, 133,3, 129,7, 137,0, 148,4, 146,5, 158,2, 160,5, 181,0.
Пример 17
(2R)-2-{(1R)-5-[2-(5-Метил-2-[4-метилфенил]-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}-бутановая кислота

Энантиомер выделяют с помощью хиральной ВЭЖХ. ЖХ-МС, ВУ 3,70 мин, М+1 420; 1Н ЯМР (CD2Cl2): δ 0,95 (t, 3Н), 1,40 (m, 1Н), 1,70 (m, 1Н), 1,90 (m, 1Н), 2,20 (m, 1Н), 2,30 (s, 3H), 2,35 (s, 3H), 2,50 (m, 1H), 2,60-2,80 (m, 2H), 2,90 (t, 2H), 3,40 (dd, 1H), 4,20 (t, 2H), 6,60 (dd, 1H), 6,70 (d, 1H), 7,10 (d, 1H), 7,20 (m, 3H), 7,80 (m, 2H).
Пример 18
2-(5-{2-[5-Метил-2-фенил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1Н-инден-1-ил)-пропановая кислота
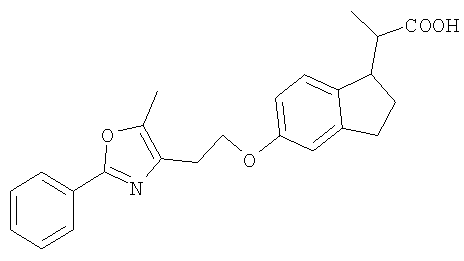
ЖХ-МС, ВУ 3,41 мин, М+1 392; 1H ЯМР (CD2Cl2): δ 1,10 (d, 3Н), 1,90 (m, 2H), 2,20 (m, 1H), 2,40 (s, 3Н), 2,70-3,00 (m, 2H), 2,95 (t, 2H), 3,45 (m, 1H), 4,20 (t, 2H), 6,70 (dd, 1H), 6,80 (d, 1H), 7,10 (d, 1H), 7,45 (m, 3Н), 8,00 (m, 2H).
Пример 19
2-{5-[2-(5-Метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}-малоновая кислота
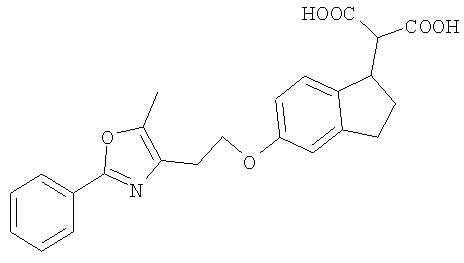
ЖХ-МС, ВУ 3,00 мин, М+1 422; 1H ЯМР (CD2Cl2): δ 1,90 (m, 2H), 2,40 (t, 3H), 2,60-3,00 (m, 3H), 3,40 (t, 2H), 3,70 (m, 1H), 4,20 (t, 2H), 6,60 (dd, 1H), 6,80 (d, 1H), 7,10 (d, 1H), 7,50 (m, 3H), 7,95 (m, 2H).
Пример 20
3-Этокси-2-{5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}-3-оксопропановая кислота
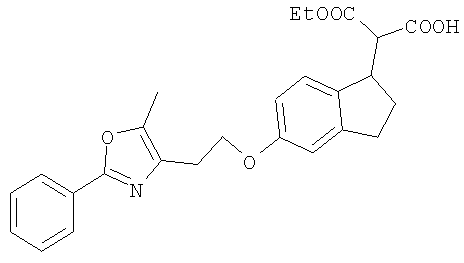
ЖХ-МС, ВУ 3,39 мин, М+1 450; 1H ЯМР (CD2Cl2): δ 1,20 (t, 3H), 2,00 (m, 1H), 2,30 (m, 1Н), 2,40 (s, 3H), 2,90 (m, 2Н), 3,10 (t, 2Н), 3,80 (m, 1H), 4,20 (t и q, 4H), 6,70 (dd, 1H), 6,80 (d,1H), 7,10 (d, 1H), 7,50 (m, 3H), 8,00 (m, 2H).
Пример 21
2-{5-[2-(5-Метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил]-5-фенилпентановая кислота

ЖХ-МС, ВУ 3,98 мин, М+1 396; 1H ЯМР (CD2Cl2): δ 1,40-1,80 (m, 4H), 1,90-2,20 (m, 2H), 2,35 (s, 3H), 2,40-3,00 (m, 5H), 2,90 (t, 2H), 3,35 (m, 1H), 4,10 (t, 2H), 6,60 (dd, 1H), 6,70 (d, 1H), 6,90-7,20 (m, 6H), 7,30 (m, 3H), 7,95 (m, 2H).
Пример 22
2-(5-{2-[5-Метил-2-(4-метилфенил)-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1Н-инден-1-ил)-пропановая кислота
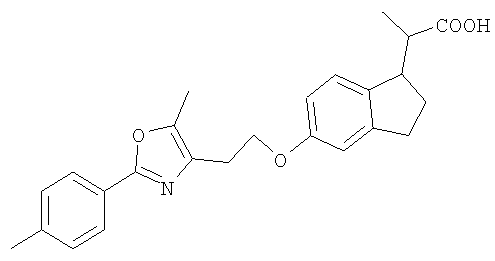
ЖХ-МС, ВУ 3,52 мин, М+1 406; 1H ЯМР (CD2Cl2): δ 1,10 (d, 3H), 1,90 (m, 2H), 2,20 (m, 1H), 2,30 (s, 3H), 2,31 (s, 3H), 2,70-3,00 (m, 2H), 2,95 (t, 2H), 3,40 (m, 1H), 4,10 (t, 2H), 6,60 (dd, 1H), 6,70 (d, 1H), 7,00 (d, 1H), 7,20 (d, 2H), 7,80 (d, 2H).
Пример 23
2-(5-{2-[5-Метил-2-(4-метил-фенил)-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1Н-инден-1-ил)-гексановая кислота
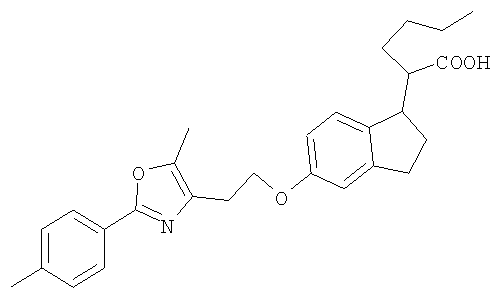
ЖХ-МС, ВУ 3,92 мин, М+1 448; 1H ЯМР (CD2Cl3): δ 0,93 (t, 3Н), 1,10-1,30 (m, 4H), 1,40-1,70 (m, 2H), 1,80-2,20 (m, 2H), 2,30 (s, 3Н), 2,31 (s, 3Н), 2,40 (m, 1H), 2,60-2,80 (m, 2H), 2,90 (t, 2H), 3,20-3,40 (m, 1H), 4,10 (t, 2H), 6,60 (dd, 1H), 6,70 (d, 1H), 7,00 (d, 1H), 7,20 (d, 2H), 7,80 (d, 2H).
Пример 24
4-Метил-2-(5-{2-[5-метил-2-(4-метилфенил)-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1Н-инден-1-ил)-пентановая кислота
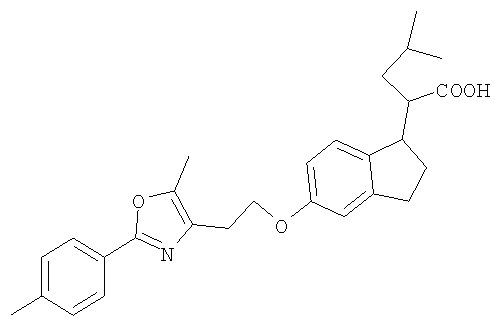
ЖХ-МС, ВУ 4,00 мин, М+1 448; 1H ЯМР (CD2Cl2): δ 0,93 (m, 6H), 1,20 (m, 1H), 1,40-1,70 (m, 2H), 1,80-2,20 (m, 2H), 2,30 (s, 3Н), 2,31 (s, 3Н), 2,40 (m, 1H), 2,60-2,80 (m, 2H), 2,90 (t, 2H), 3,20-3,40 (m, 1H), 4,10 (t, 2H), 6,60 (dd, 1H), 6,70 (d, 1H), 7,00 (d, 1H), 7,40 (d, 2H), 8,40 (d, 2H).
Пример 25
4-Метил-2-(5-{2-[5-метил-2-(4-метил-фенил)-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1Н-инден-1-ил)-пентеновая кислота
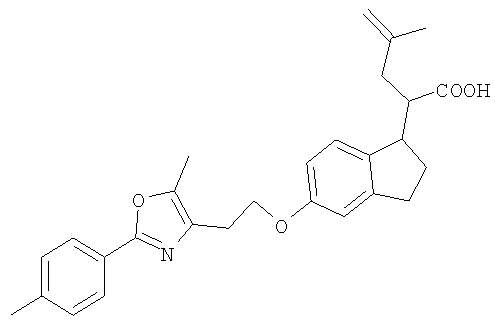
ЖХ-МС, ВУ 3.74 мин, М+1 446; 1H ЯМР (CD2Cl2): δ 1,60 (s, 3Н), 1,70 (m, 2H), 1,80-2,20 (m, 2H), 2,30 (s, 3Н), 2,31 (s, 3Н), 2,40 (m, 1H), 2,60-2,80 (m, 2H), 2,90 (t, 2H), 3,20-3,40 (m, 1H), 4,10 (t, 2H), 5,60 (m, 2H), 6,60 (dd, 1H), 6,70 (d, 1H), 7,00 (d, 1H), 7,20 (d, 2H), 7,80 (d, 2H).
Пример 26
Получение 2-{6-хлор-5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}-бутановой кислоты через 2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этилметансульфонат и метил-2-(6-хлор-5-гидрокси-2,3-дигидро-1Н-инден-1-ил)-бутаноат
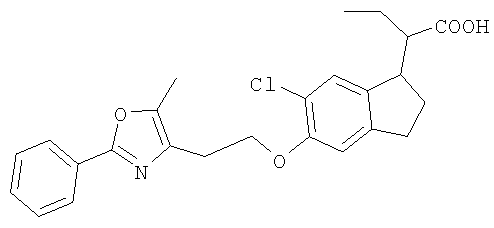
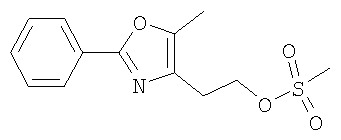
Стадия 1. К раствору 2-фенил-4-метил-5-гидроксиэтилоксазола (500 мг, 2,5 ммоль) в 12,5 мл THF прибавляют метансульфонилхлорид (0,21 мл, 2,75 ммоль) и триэтиламин (0,42 мл, 3 ммоль). Раствор реакционной смеси перемешивают при комнатной температуре в атмосфере аргона в течение 2 ч, затем концентрируют в вакууме. Полученный остаток растворяют в этилацетате, промывают 1% водным раствором хлористоводородной кислоты (трижды) и рассолом. Затем его сушат над сульфатом натрия, фильтруют и концентрируют в вакууме и получают (617 мг, 88%): ЭР-МС т/г 282 ((М+Н)+); ВЭЖХ ВУ 2,67; 1H ЯМР (d6-ДМСО) δ 2,33 (s, 3Н), 2,89 (t, 2H), 3,13 (s, 3Н), 4,41 (t, 2H), 7,47-7,51 (m, 3Н), 7,88-7,91 (m, 2H).

Стадия 2. Сульфурилхлорид (0,035 мл, 0,43 ммоль) прибавляют к раствору метил-5-гидрокси-2,3-дигидро-1-(2-бутаноата) (100 мг, 0,43 ммоль) в 2,15 мл уксусной кислоты. Раствор реакционной смеси перемешивают при комнатной температуре в течение 30 мин, затем концентрируют в вакууме. Полученный остаток растворяют в этилацетате и промывают водой, насыщенным водным раствором бикарбоната натрия и рассолом. Затем его сушат над сульфатом натрия, фильтруют и концентрируют в вакууме и получают 63 мг искомого промежуточного продукта в виде неочищенного желтого масла, которое используют без дополнительной очистки: ГХ-МС 269, ((М+Н)+); ГХ ВУ (мин) 8,71; 1H ЯМР (d6-ДМСО) δ 0,81 (t, 3Н), 1,40-1,63 (m, 2H), 1,77-1,88 (m, 1H), 2,00-2,15 (m, 1H), 2,40-2,80 (m, 3Н), 3,15-3,22 (m, 1H), 3,50 (s, 3Н), 6,76 (s, 1H), 7,13 (s, 1H), 9,84 (s, 1H).
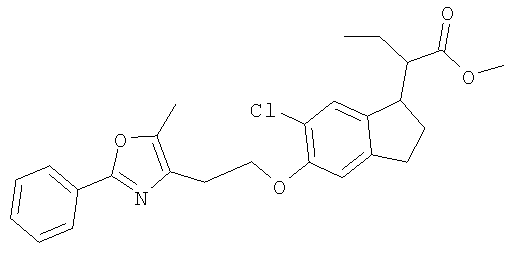
Стадия 3. Раствор продукта, полученного на стадии 2 (30,5 мг, 0,12 ммоль), в 0,6 мл DMF охлаждают до 0°С в бане со льдом. Затем прибавляют 60% дисперсию гидрида натрия в масле (5,2 мг, 0,13 ммоль) и баню со льдом удаляют. После перемешивания реакционной смеси в течение 1 ч при комнатной температуре прибавляют мезилат, полученный на стадии 1 (34 мг, 0,12 ммоль). Реакционную смесь нагревают при 50°С в течение 24 ч, затем охлаждают до 0°С. Прибавляют еще 9,6 мг NaH (60% дисперсия в масле) прибавляют и нагревание продолжают в течение еще 2 ч, после чего реакционную смесь охлаждают до комнатной температуры и перемешивают в течение 48 ч. В этот момент прибавляют этилацетат и органический раствор промывают водой и рассолом (трижды), сушат над сульфатом натрия, фильтруют и концентрируют в вакууме. Полученный остаток очищают с помощью флэш-хроматографии на силикагеле с использованием смеси 5:1 гексан:этилацетат в качестве элюента и получают продукт (19 мг, 35%) в виде смеси диастереоизомеров (3:1): ЭР-МС m/z 454 (М+Н)+; ВЭЖХ ВУ (мин) 4,21; 1H ЯМР (d6-ДМСО) δ 0,80 (t, 3Н), 1,38-1,63 (m, 2H), 1,79-1,90 (m, 1Н), 2,02-2,14 (m, 1H), 2,34 (s, 3H), 2,51-2,57 (m, 1H), 2,63-2,84 (m, 2H), 2,91 (t, 2H), 3,19-3,25 (m, 1H), 3,49 (s, 2,3H), 3,58 (s, 0,7H), 4,22 (t, 2H), 7,00 (s, 1H), 7,21 (s, 1H), 7,43-7,51 (m, 3Н), 7,85-7,90 (m, 2H).

Стадия 4. При стандартных условиях гидролиза сложный эфир, полученный на стадии 3, превращают в кислоту (смесь диастереоизомеров 3:2): ЭР-МС m/z 440 (М+Н)+; ВЭЖХ ВУ (мин) 3,69; 1H ЯМР (d6-ДМСО) δ 0,83 (t, 3Н), 2,34 (s, 3Н), 2,92 (t, 2H), 4,21 (t, 2H), 7,00-7,02 (d, 1H), 7,12 (s, 0,24H), 7,21 (s, 0,37H), 7,47-7,48 (m, 3H), 7,87-7,90 (m, 2H).
Пример 27
Получение этил-2-{5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}-пентаноата
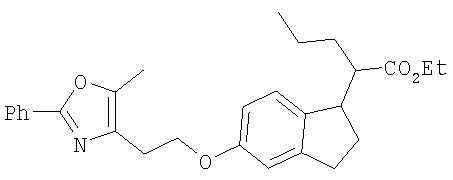
Высушенную в сушильном шкафу круглодонную колбу объемом 15 мл и стержень для перемешивания охлаждают в токе Ar (газообразного) и в нее помещают этил-2-{5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1 Н-инден-1-ил}-ацетат (0,070 г, 0,17 ммоль), а затем прибавляют 0,2 мл THF. Затем раствор при перемешивании охлаждают до -78°С, а после этого по каплям прибавляют литий-бис(триметилсилил)-амид (1,0 М раствор в гексане, 0,86 мл, 0,86 ммоль). После завершения прибавления основания раствор перемешивают при -78°С в течение 1 ч, затем с помощью шприца прибавляют йодпропан (0,142 г, 0,86 ммоль). Затем содержимое медленно нагревают до комнатной температуры и выдерживают в течение 1 ч. Содержимое колбы выливают в 5 мл NH4Cl (водный раствор), затем экстрагируют с помощью этилацетата (3×10 мл). Органические слои объединяют и сушат над Na2SO4 и концентрируют в вакууме, получая 3,0 мг (выход 4,0%) бесцветной пленки. Характеристики продукта: 1H ЯМР (300 МГц, d6-ацетон) δ 7,96 (dd, 8,1, 1,5 Гц, 2Н), 7,48 (m, 3Н), 6,99 (d, 8,4 Гц, 1Н), 6,79 (d, 2,7 Гц, 1Н), 6,70 (dd, 8,1, 2,7 Гц, 1Н), 4,22 (t, 6,9 Гц, 2Н), 4,11 (q, 7,2 Гц, 2Н), 3,33 (q, 6,6 Гц, 1Н), 2,94 (t, 6,9 Гц, 2Н), 2,78 (m, 3Н), 2,54 (m, 1Н), 2,39 (s, 3Н), 2,14 (m, 2Н), 1,91 (m, 1H), 1,63 (qt, 10, 2, 3,9 Гц, 2Н), 1,21 (t, 7,2 Гц, 3Н), 0,852 (t, 7,5 Гц, 3Н); масс-спектроскопия дает МН+=448,2 (рассчитанная молекулярная масса С28Н33NO4=447,57).
Пример 28
Получение 2-{5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}-пентановой кислоты
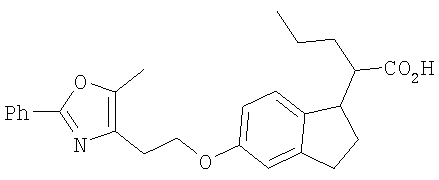
Гидролиз продукта, полученного в Примере 27, способом, описанным выше в Примере 2, дает продукт со следующими характеристиками. 1H ЯМР (300 МГц, d6-ацетон); δ 7,96 (dd, 8,1, 1,5 Гц, 2Н), 7,48 (m, 3Н), 7,10 (d, 8,4 Гц, 1H), 6,79 (d, 2,7 Гц, 1H), 6,71 (dd, 8,1, 2,7 Гц, 1H), 4,22 (t, 6,9 Гц, 2Н), 3,40 (m, 1H), 2,91 (t, 6,9 Гц, 2Н), 2,74 (m, 1Н), 2,58 (m, 1Н), 2,39 (s, 3Н), 2,26 (m, 1Н), 2,11 (m, 1Н), 1,95 (m, 2H), 1,84 (m, 1Н), 1,62 (m, 2H), 0,859 (td, 6,9, 1,5 Гц, 3Н); масс-спектроскопия дает MH+=420,1 (рассчитанная молекулярная масса С26Н29NO4=419,51).
Пример 29
Получение 2-{6-бром-5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}-бутановой кислоты через метил-2-(6-бром-5-гидрокси-2,3-дигидро-1Н-инден-1-ил)-бутаноат
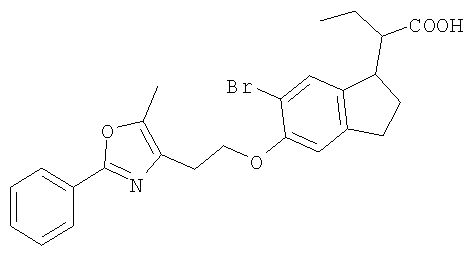
 и
и 
Стадия 1. Раствор брома (0,032 мл, 0,60 ммоль) в диоксане (3 мл) охлаждают до 0°С в течение 15 мин, после чего прибавляют раствор метилового эфира 2-(5-гидроксииндан-1-ил)-масляной кислоты (141 мг, 0,60 ммоль) в диоксане (3 мл). Через 5 мин баню со льдом удаляют и реакционную смесь перемешивают при комнатной температуре в течение 4 ч. Растворитель удаляют на роторном испарителе. Остаток очищают с помощью хроматографии на колонке (8% EtOAc в гексане) и получают монобромированный промежуточный продукт (А) (145 мг, 77%) и дибромированный промежуточный продукт (В) (20 мг) в виде бесцветного масла. A:Rf=0,46 (4:1 гексан:EtOAc); ГХ-МС (+Cl): m/z=313 (М+); 1H ЯМР (ДМСО-d6}: δ 0,840 (m, 3H), 1,511 (m, 2Н), 1,905 (m, 1Н), 2,091 (m, 1H), 2,410-2,793 (m, 3Н), 3,212 (m, 1H), 3,505 и 3,512 (s, 3Н), 6,713 и 6,753 (s, 1H), 7,034 и 7,274 (s, 1H), 9,932 и 9,934 (s, ОН).
В:Rf=0,30 (4:1 гексан:EtOAc); ГХ-МС(+Cl): m/z=393 (M+); 1H ЯМР (ДМСО-d6): δ 0,817 (m, 3Н), 1,459-1,596 (m, 2H), 1,910 (m, 1H), 2,101 (m, 1H), 2,433-2,768 (m, 3Н), 3,371 (m, 1H), 3,400 и 3,596 (s, 3Н), 7,168 и 7,357 (s, 1H), 9,535 и 9,542 (s, ОН).
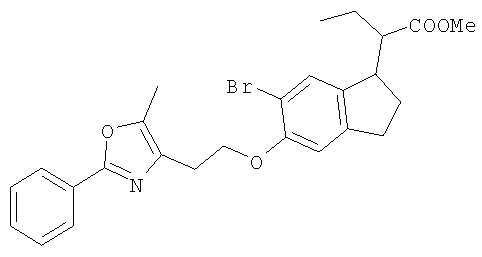
Стадия 2. К раствору (А), полученному на стадии 1 выше (118 мг, 0,38 ммоль), в DMF (3,8 мл) при 0°С прибавляют NaH (60% в минеральном масле, 30 мг). Через 1 ч прибавляют мезилат, полученный на стадии 1, Пример 26. Смесь нагревают до 50°С в течение 30 ч. Раствор разбавляют водой и затем трижды экстрагируют этилацетатом. Объединенные органические слои промывают водой и рассолом, затем сушат (Na2SO4) и концентрируют. Остаток очищают с помощью хроматографии на колонке (10% этилацетат в гексане) и получают продукт (63 мг, 34%); Rf=0,46 (2:1 гексан:EtOAc); ЭР ЖХ-МС: m/z=498 (МН+); 1H ЯМР (ДМСО-d6): δ 0,847 (m, 3H), 1,468 (m, 2H), 1,812 (m, 1H), 2,146 (m, 1H), 2,340 (s, 3H), 2,525-2,788 (m, 3H), 2,902 (m, 2H), 3,236 (m, 1H), 3,481 и 3,586 (s, 3H), 4,211 (m, 2H), 6,969 (s, 1H), 7,347 и 7,386 (s, 1H), 7,452 (m, 3H), 7,833 (m, 2H).

Стадия 3. К раствору продукта, полученного на стадии 2 (5,6 мг), в метаноле прибавляют 3 н. КОН (1 мл), а затем прибавляют THF, пока мутный раствор не станет прозрачным. Смесь кипятят с обратным холодильником в течение ночи. Для установления значения рН, равного 2, прибавляют концентрированную HCl, затем трижды экстрагируют этилацетатом. Органические слои объединяют, сушат и концентрируют и получают белое твердое вещество (4 мг). Rf=0,18 (2:1 гексан:EtOAc); ЭР ЖХ-МС: m/z=484 (МН+); 1H ЯМР (ДМСО-d6): δ 0,832 (m, 3H), 1,468 (m, 2H), 1,812 (m, 1H), 2,146 (m, 1H), 2,405 (m, 1H), 2,788 (m, 2H), 2,904 (m, 2H), 3,015 (m, 1H), 3,136 и 3,138 (s, 3H), 4,209 (m, 2H), 6,987 и 7,344 (s, 1H), 6,972 и 7,251 (s, 1H), 7,487 (m, 3H), 7,882 (m, 2H).
Пример 30
Получение 2-{5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-6-фенил-2,3-дигидро-1Н-инден-1-ил}-бутановой кислоты через метил-2-{5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-6-фенил-2,3-дигидро-1Н-инден-1-ил}-бутаноат
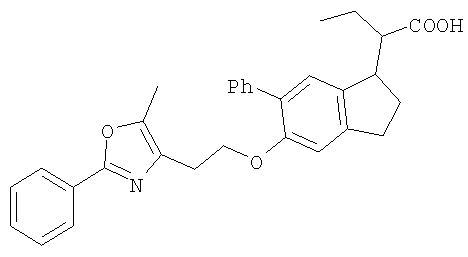
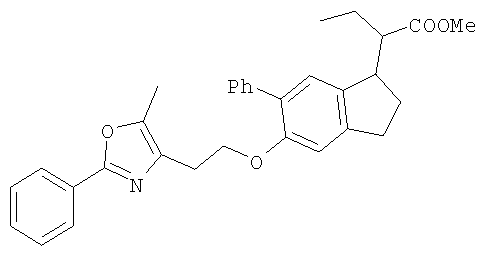
Стадия 1. Смесь продукта, полученного на стадии 2, Пример 29, и Pd(PPh3)4 в THF (1,5 мл) перемешивают при комнатной температуре в течение 30 мин. К раствору затем прибавляют фенилбороновую кислоту (13,2 мг, 0,108 ммоль) и 2 н. NaOH. Смесь кипятят с обратным холодильником в течение 14 ч. Раствору дают охладиться, разбавляют водой и трижды экстрагируют этилацетатом. Объединенные органические слои промывают рассолом и сушат над сульфатом натрия. Неочищенный продукт очищают с помощью хроматографии на колонке, элюируя 5% этилацетатом в гексане, и получают искомый продукт (8,6 мг). Rf=0,48 (2:1 гексан:EtOAc); ЭР ЖХ-МС: m/z=496 (MH+); 1H ЯМР (ДМСО-d6): δ 0,804 (m, 3H), 1,541 (m, 2H), 1,880 (m, 1H), 1,987 (m, 1H), 2,090 (s, 3H), 2,247-2,698 (m, 3H), 2,791 (m, 2H), 3,199 (m, 1H), 3,524 и 3,537 (s, 3H), 4,190 (m, 2H), 6,970 (s, 1H), 7,062 (s, 1H), 7,275 (m, 5H), 7,472 (m, 3H), 7,868 (m, 2H).

Стадия 2. Сложный эфир гидролизуют по методикам, описанным выше, и получают продукт: Rf=0,16 (2:1 гексан:EtOAc); ЭР ЖХ-МС: m/z=482 (МН+); 1H ЯМР (ДМСО-d6): δ 0,923 (m, 3H), 1,504 (m, 2H), 1,812 (m, 1H), 2,146 (m, 1H), 2,188 (s, 3H), 2,334 (m, 2H), 2,432 (m, 2H), 2,539 (m, 1H), 2,625 (m, 1H), 4,287 (m, 2H), 7,059 (s, 1H), 7,160 (s, 1H), 7,351 (m, 5H), 7,544 (m, 3H), 7,971 (m, 2H).
Пример 31
Получение метил-2-{6-(4-хлорфенил)-5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}-бутаноата
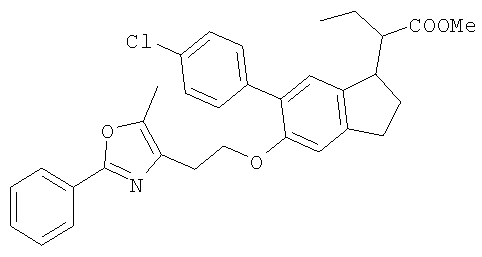
Смесь продукта, полученного на стадии 2, Пример 29 (71,4 мг, 0,14 ммоль), NaHCO3 (14,3 мг, 0,17 ммоль), 4-хлорфенилбороновой кислоты (26,8 мг, 0,17 ммоль) в диметиловом эфире этиленгликоля (1,5 мл) и воде (0,4 мл) дегазируют в течение 20 мин.
Затем к раствору прибавляют Pd(dppf)Cl2. Смесь кипятят с обратным холодильником в течение 2 суток. Затем смесь концентрируют и очищают с помощью хроматографии на колонке (10% EtOAc в гексане) и получают искомый продукт (25 мг). Rf=0,51 (2:1 гексан:EtOAc); ЭР ЖХ-МС: m/z=530 (MH+); 1H ЯМР (ДМСО-d6): δ 0,841 (m, 3H), 1,557 (m, 2H), 1,888 (m, 1H), 1,987 (m, 1H), 2,146 (s, 3H), 2,247-2,698 (m, 3H), 2,791 (m, 2H), 3,214 (m, 1H), 3,487 и 3,5538 (s, 3H), 4,189 (m, 2Н), 6,993 (s, 1H), 7,080 (s, 1H), 7,308 (s, 4H), 7,493 (m, 3H), 7,868 (m, 2H).
Путем использования методик, описанных в Примерах 26-31, с применением других подходящих исходных веществ получают и характеризуют следующие вещества:
Пример 32
2-{6-(4-Хлорфенил)-5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}бутановая кислота
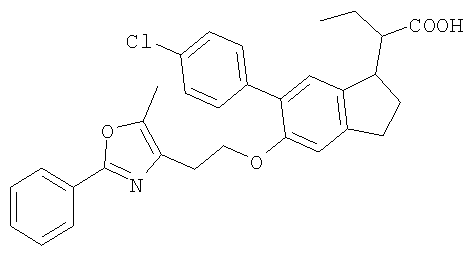
ЭР ЖХ-МС: m/z=516 (МН+); 1Н ЯМР (ДМСО - d6): δ 0,847 (m, 3H), 1,557 (m, 2H), 1,888 (m, 1H), 1,987 (m, 1H), 2,137 (s, 3H), 2,247-2,687 (m, 3H), 2,819 (m, 2H), 3,234 (m, 1H), 4,187 (m, 2H), 6,994 (s, 1H), 7,089 (s, 1H), 7,298 и 7,308 (m, 4H), 7,484 (m, 3H), 7,869 (m, 2H).
Пример 33
Метил-2-{6-метил-5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}-бутаноат
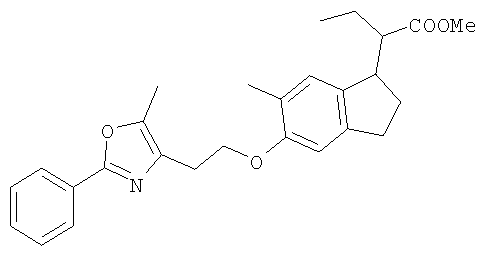
Rf=0,23 (2:1 гексан:EtOAc); ЭР ЖХ-МС: m/z=434 (МН+); 1H ЯМР (ДМСО-d6): δ 0,804 (m, 3H), 1,522 (m, 2H), 1,830 (m, 1H), 1,987 (m, 1H), 2,037 (s, 3H), 2,335 (s, 3H), 2,410 - 2,550 (m, 3H), 2,901 (m, 2H), 3,146 (m, 1H), 3,507 (s, 3H), 4,163 (m, 2H), 6,777 (s, 1H), 6,939 (s, 1H), 7,483 (m, 3H), 7,875 (m, 2H).
Пример 34
2-{6-Метил-5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}-бутановая кислота
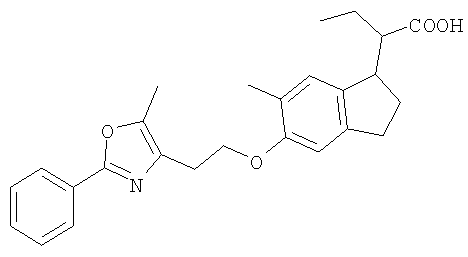
Rf=0,31 (2:1 гексан:EtOAc); ЭР ЖХ-МС: m/z=420 (MH+); 1H ЯМР (ДМСО-d6): δ 0,827 (m, 3Н), 1,508 (m, 2H), 1,828 (m, 1Н), 1,987 (m, 1H), 2,017 (s, 3Н), 2,333 (s, 3H), 2,410-2,550 (m, 3Н), 2,894 (m, 2H), 3,146 (m, 1H), 4,116 (m, 2H), 6,773 (s, 1H), 6,942 (s, 1H), 7,467 (m, 3Н), 7,880 (m, 2H).
Пример 35
Метил-2-[5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-6-(2-тиенил)-2,3-дигидро-1Н-инден-1-ил]-бутаноат

Rf=0,60 (2:1 гексан:EtOAc); ЭР ЖХ-МС: m/z=502 (МН+); 1H ЯМР (ДМСО-d6): δ 0,801 (m, 3Н), 1,535 (m, 2H), 1,891 (m, 1H), 1,987 (m, 1H), 2,299 (s, 3H), 2,410-2,550 (m, 3Н), 2,988 (m, 2H), 3,146 (m, 1H), 3,506 (s, 3Н), 4,337 (m, 2H), 7,011-7,041 (m, 2H), 7,405-7,493 (m, 5H), 7,884 (m, 2H).
Пример 36
2-[5-[2-(5-Метил-2-фенил-1,3-оксазол-4-ил)-этокси]-6-(2-тиенил)-2,3-дигидро-1Н-инден-1-ил]-бутановая кислота
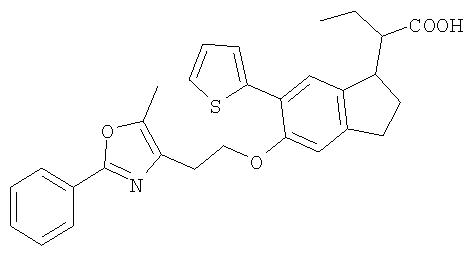
Rf=0,18 (2:1 гексан:EtOAc); ЭР ЖХ-МС: m/z=488 (МН+); 1H ЯМР (ДМСО-d6): δ 0,801 (m, 3Н), 1,535 (m, 2H), 1,891 (m, 1H), 1,987 (m, 1H), 2,299 (s, 3H), 2,410-2,550 (m, 3Н), 2,988 (m, 2H), 3,146 (m, 1H), 4,337 (m, 2H), 7,078 (m, 2H), 7,472 (m, 5H), 7,896 (m, 2H).
Пример 37
Метил-2-{4,6-дибром-5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}-бутаноат
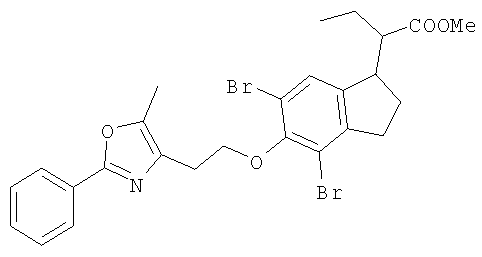
Rf=0,35 (4:1 гексан:EtOAc); ЭР ЖХ-МС: m/z=578 (MH+); 1H ЯМР (ДМСО-d6): δ 0,847 (m, 3Н), 1,468 (m, 2H), 1,812 (m, 1Н), 2,146 (m, 1H), 2,350 (s, 3H), 2,407-2,788 (m, 3Н), 2,982 (m, 2H), 3,225 (m, 1H), 3,480 и 3,588 (s, 3Н), 4,145 (m, 2H), 7,276 (s, 1H), 7,458 (m, 3Н), 7,866 (m, 2H).
Пример 38
2-[4,6-Дибром-5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил]-бутановая кислота
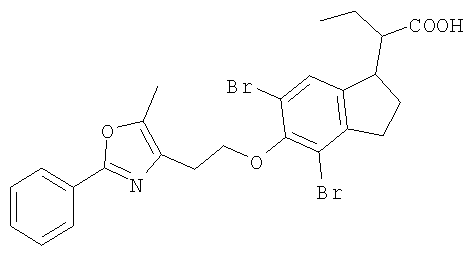
Rf=0,17 (2:1 гексан:EtOAc); ЭР ЖХ-МС: m/z=564 (МН+); 1H ЯМР (ДМСО-d6): δ 0,847 (m, 3Н), 1,468 (m, 2H), 1,812 (m, 1H), 2,146 (m, 1H), 2,361 (s, 3H), 2,414-2,781 (m, 3Н), 2,995 (m, 2H), 3,123 (m, 1H), 4,125 (m, 2H), 7,345 (s, 1H), 7,437 (m, 3H), 7,886 (m, 2H).
Пример 39
Получение 2-{6-ацетил-5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил}-этокси]-2,3-дигидро-1Н-инден-1-ил}-бутановой кислоты через метил-2-(6-ацетил-5-метокси-2,3-дигидро-1Н-инден-1-ил)-бутаноат
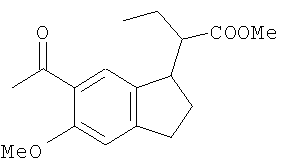
Стадия 1. К раствору Aids (103 мг, 0,78 ммоль) в метиленхлориде (2,5 мл) при 0°С прибавляют ацетилхлорид (0,044 мл, 0,63 ммоль), а затем по каплям прибавляют раствор метил-5-метокси-2,3-дигидро-1Н-инден-1-илбутаноата (130 мг, 0,52 ммоль) в метиленхлориде (2,7 мл). Смесь перемешивают при 0°С в течение 15 мин. Баню со льдом удаляют и смесь перемешивают при комнатной температуре в течение 16 ч. Смесь выливают на лед и прибавляют 4 капли концентрированной HCl. Эту смесь дважды экстрагируют метиленхлоридом. Объединенные органические слои промывают водой, 0,05 н. NaOH и водой. Органический слой сушат, концентрируют и очищают с помощью хроматографии с использованием 10% EtOAc: гексан и получают искомый продукт (103 мг, 68%). Rf=0,28 (4:1 гексан:EtOAc); ГХ-МС (+Cl): m/z=291 (М+); 1H ЯМР (ДМСО-d6): δ 0,840 (m, 3Н), 1,536 (m, 2H), 1,876 (m, 1H), 2,108 (m, 1H), 2,505 (s, 3Н), 2,521 (m, 1H), 2,760-2,889 (m, 2H), 3,236 (m, 1H), 3,511 и 3,589 (s, 3Н), 3,836 (s, 3Н), 7,012 и 7,253 (s, 1H), 7,440 (s, 1H).
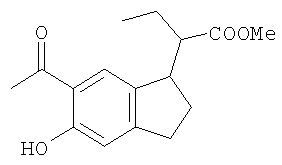
Стадия 2. К раствору AlCl3 (238 мг, 1,77 ммоль) в СН2Cl2 (1 мл) прибавляют продукт, полученный на стадии 1 (103 мг, 0,35 ммоль), в CH2Cl2 (2 мл). Смесь охлаждают до 0°С в течение 5 мин, затем медленно прибавляют EtSH (0,13 мл, 1,77 ммоль). Смесь перемешивают при этой температуре в течение 4,5 ч. Затем смесь выливают в воду со льдом, перемешивают в течение 10 мин и дважды экстрагируют с помощью CH2Cl2. Объединенные органические слои промывают водой, сушат над сульфатом натрия и концентрируют и получают продукт (86 мг, 89%). Rf=0,51 (4:1 гексан:EtOAc); ГХ-МС (+Cl): m/z=276 (M+); 1H ЯМР (ДМСО-d6): δ 0,841 (m, 3Н), 1,574 (m, 2H), 1,888 (m, 1H), 2,094 (m, 1H), 2,585 (s, 3Н), 2,639 (m, 1H), 2,729-2,847 (m, 2H), 3,244 (m, 1H), 3,513 и 3,628 (s, 3Н), 6,774 и 7,503 (s, 1H), 6,792 и 7,715 (s, 1H), 12,117 и 12,143 (s, 1H).

Стадия 3. Сочетание сложного эфира гидроксиинденуксусной кислоты, полученного на стадии 2, с мезилатом, полученным на стадии 2, Пример 26. ЭР ЖХ-МС: m/z=462 (МН+);
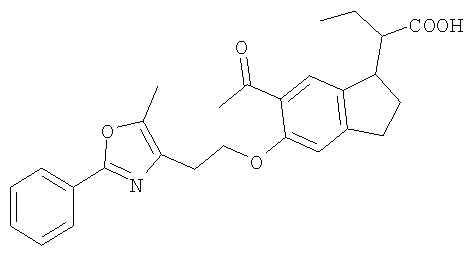
Стадия 4. Гидролиз продукта, полученного на стадии 3, проводят способом, аналогичным описанному выше, и получают продукт: Rf=0,08 (2:1 гексан:EtOAc); ЭР ЖХ-МС: m/z=448 (MH+); 1H ЯМР (ДМСО-d6): δ 0,848 (m, 3Н), 1,468 (m, 2H), 1,812 (m, 1H), 2,146 (m, 1H), 2,305 (s, 3Н), 2,368 (s, 3Н), 2,405 (m, 1H), 2,788 (m, 2H), 2,971 (m, 2H), 3,015 (m, 1H), 4,332 (m, 2H), 7,039 и 7,441 (s, 1H), 7,446 (s, 1H), 7,465 (m, 3Н), 7,875 (m, 2H).
С использованием комбинации описанных выше методик и с применением других подходящих исходных веществ получают множество описанных ниже соединений.
Пример 40
Метил-2-{5-[2-(2,5-дифенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}-бутаноат
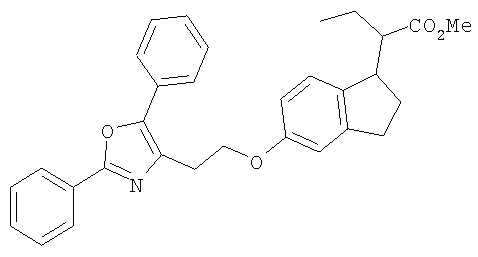
Выход: 0,09 г, 46%; 1H ЯМР (CDCl3, 400 МГц) δ 0,83-0,93 (t, 3Н), 1,55-1,78 (m, 2Н), 1,87-1,97 (m, 1Н), 2,10-2,22 (m, 1Н), 2,44-2,52 (m, 1Н), 2,67-2,80 (m, 1Н), 2,81-2,93 (m, 1Н), 3,21-3,29 (m, 1Н), 3,23-3,33 (t, 2Н), 3,62 (s, 3Н), 4,34-4,43 (t, 2Н), 6,66-6,72 (m, 1Н), 6,76 (s, 1Н), 7,05-7,14 (d, 1Н), 7,33-7,39 (t, 1Н), 7,43-7,51 (m, 5Н), 7,78-7,84 (d, 2H), 8,06-8,12 (m, 2H).
Пример 41
2-{5-[2-(2,5-дифенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}-бутановая кислота

Выход: 0,07 г, 70%; 1H ЯМР (CDCl3, 400 МГц) δ 0,85-0,98 (m, 3Н), 1,23-1,47 (m, 1Н), 1,57-1,78 (m, 1Н), 1,88-2,07 (m, 1Н), 2,12-2,27 (m, 1Н), 2,43-2,56 (m, 1Н), 2,68-2,97 (m, 2Н), 3,27-3,35 (t, 2Н), 3,42-3,50 (m, 1Н), 4,34-4,41 (t, 2Н), 6,66-6,73 (d, 1Н), 6,77 (s, 1Н), 7,02-7,16 (d, 1Н), 7,34-7,40 (t, 1Н), 7,43-7,52 (m, 5Н), 7,78-7,83 (d, 2Н), 8,05-8,12 (m, 2Н).
Пример 42
Метил-2-{5-[2-(5-изопропил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}-бутаноат
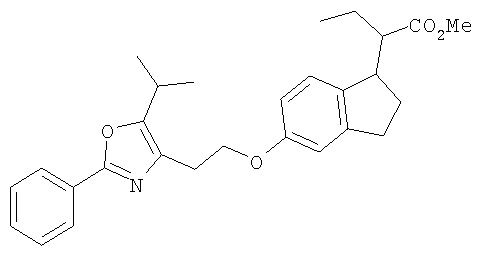
Выход: 0,09 г, 45%; 1H ЯМР (CDCl3, 400 МГц) δ 0,78-0,96 (t, 3Н), 1,26-1,32 (d, 6Н), 1,51-1,62 (m, 1Н), 1,64-1,75 (m, 1Н), 1,81-1,93 (m, 1Н), 2,07-2,21 (m, 1Н), 2,40-2,51 (m, 1Н), 2,65-2,75 (m, 1Н), 2,77-2,98 (m, 1Н), 2,91-2,98 (t, 2Н), 3,09-3,16 (m, 1Н), 3,21-3,28 (m, 1Н), 3,62 (s, 3Н), 4,10-4,17 (t, 2Н), 6,60-6,68 (d, 1Н), 6,72 (s, 1Н), 7,01-7,13 (d, 1Н), 7,33-7,45 (m, 3Н), 7,94-8,00 (d, 2Н).
Пример 43
2-{5-[2-(5-Изопропил-2-Фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}-бутановая кислота
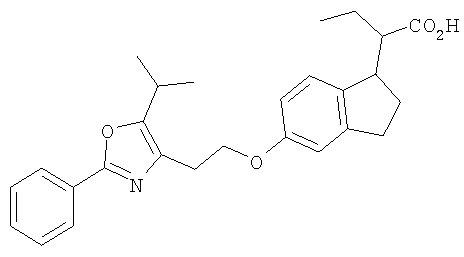
Выход: 0,08 г, 97%; 1H ЯМР (CDCl3, 400 МГц) δ 0,91-0,98 (t, 3Н), 1,30-1,36 (d, 6Н), 1,58-1,79 (m, 2Н), 1,89-2,05 (m, 1Н), 2,12-2,27 (m, 1Н), 2,44-2,57 (m, 1Н), 2,69-2,80 (m, 1Н), 2,83-2,96 (m, 1Н), 2,97-3,02 (t, 2Н), 3,10-3,21 (m, 1Н), 3,24-3,32 (m, 1Н), 4,14-4,21 (t, 2Н), 6,63-6,71 (d, 1Н), 6,75 (s, 1Н), 7,04-7,16 (d, 1Н), 7,36-7,45 (m, 3Н), 7,94-8,00 (d, 2Н).
Пример 44
Метил-2-{5-[2-(5-этил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инденил}-бутаноат
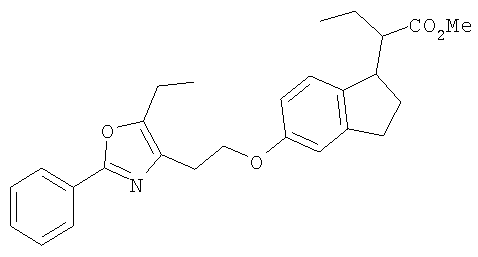
Выход: 0,14 г, 60%; 1H ЯМР (CDCl3, 400 МГц) δ 0,85-0,91 (t, 3Н), 1,25-1,35 (t, 3Н), 1,58-1,77 (m, 2Н), 1,85-1,97 (m, 1Н), 2,10-2,22 (m, 1Н), 2,44-2,64 (m, 2Н), 2,68-2,80 (q, 2Н), 2,82-2,93 (m, 1Н), 2,95-3,01 (t, 2Н), 3,25-3,34 (m, 1Н), 3,62 (s, 3Н), 4,16-4,25 (t, 2Н), 6,66-6,71 (d, 1Н), 6,75 (s, 1Н), 7,08-7,14 (d, 1Н), 7,38-7,46 (m, 3Н), 7,95-8,01 (m, 2Н).
Пример 45
2-{5-[2-(5-Этил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}-бутановая кислота
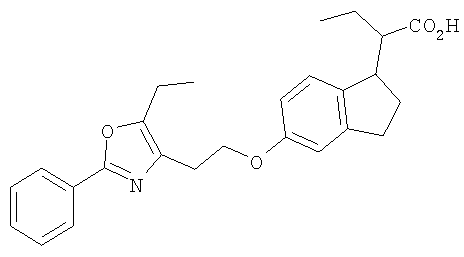
Выход: 0,05 г, 60%; 1H ЯМР (CDCl3, 400 МГц) δ 0,85-0,98 (m, 3Н), 1,21-1,33 (m, 3Н), 1,37-1,54 (m, 1Н), 1,56-1,78 (m, 2Н), 1,87-2,29 (m, 2Н), 2,45-2,60 (m, 1Н), 2,69-2,79 (q, 2Н), 2,85-2,95 (m, 1Н), 2,96-3,01 (t, 2Н), 3,27-3,49 (m, 1Н), 4,14-4,23 (t, 2Н), 6,65-6,71 (d, 1Н), 6,75 (s, 1Н), 7,03-7,17 (d, 1Н), 7,38-7,46 (m, 3Н), 7,95-8,01 (d, 2Н).
Пример 46
Метил-2-{5-[2-(2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инденил}-бутаноат
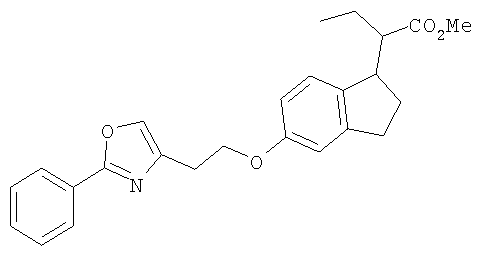
Выход: 0,18 г, 80%; 1H ЯМР (CDCl3, 400 МГц) δ 0,82-0,92 (t, 3Н), 1,56-1,66 (m, 1Н), 1,67-1,77 (m, 1Н), 1,88-1,99 (m, 1Н), 2,12-2,23 (m, 1Н), 2,43-2,52 (m, 1Н), 2,68-2,81 (m, 1Н), 2,84-2,97 (m, 1Н), 3,02-3,11 (t, 2Н), 3,25-3,33 (m, 1Н), 3,63 (s, 3Н), 4,21-4,30 (t, 2Н), 6,69-6,74 (d, 1Н), 6,79 (s, 1Н), 7,11-7,16 (d, 1Н), 7,41-7,47 (m, 3Н), 7,55-7,58 (m, 1Н), 7,99-8,05 (m, 2Н).
Пример 47
2-{5-[2-(2-Фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}бутановая кислота
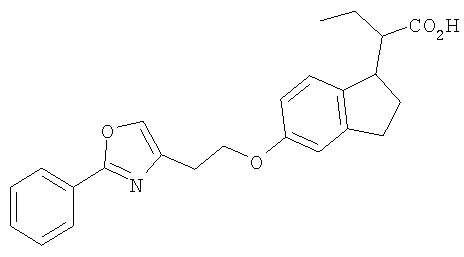
Выход: 0,07 г, 46%; 1H ЯМР (CDCl3, 400 МГц) δ 0,84-1,01 (m, 3Н), 1,36-1,51 (m, 1Н), 1,59-1,81 (m, 1Н), 1,88-2,00 (m, 1Н), 2,11-2,29 (m, 1Н), 2 43-2,64 (m, 1Н), 2,68-2,81 (m, 1Н), 2,82-3,00 (m, 2Н), 3,02-3,11 (t, 2Н), 3,23-3,37 (m, 1Н), 4,17-4,28 (t, 2Н), 6,66-6,74 (d, 1Н), 6,78 (s, 1Н), 7,04-7,19 (m, 1Н), 7,39-7,47 (m, 2Н), 7,55 (s, 1Н), 7,98-8,05 (m, 2Н).
Пример 48
Метил-2-(5-[2-[2-(2,3-дигидро-1-бензофуран-6-ил)-5-метил-1,3-оксазол-4-ил]-этокси]-2,3-дигидро-1Н-инден-1-ил)-бутаноат

Выход: 0,17 г, 58%; 1H ЯМР (CDCl3, 400 МГц) δ 0,86-0,97 (t, 3Н), 1,41-1,53 (m, 1Н), 1,61-1,77 (m, 1Н), 1,92-2,01 (m, 1Н), 2,04-2,20 (m, 1Н), 2,40 (s, 3Н), 2,49-2,56 (m, 1Н), 2,71-2,92 (m, 2Н), 3,93-3,00 (t, 2Н), 3,21-3,32 (t, 2Н), 3,34-3,49 (m, 1Н), 3,75 (s, 3Н), 4,18-4,24 (t, 2Н), 4,54-4,70 (t, 2Н), 6,70-6,76 (d, 1Н), 6,79 (s, 1Н), 6,82-6,89 (d, 1Н), 6,92-7,01 (d, 1Н), 7,75-7,80 (d, 1Н), 7,87 (s, 1Н).
Пример 49
2-(5-[2-[2-(2,3-Дигидро-1-бензофуран-6-ил)-5-метил-1,3-оксазол-4-ил]-этокси]-2,3-дигидро-1Н-инден-1-ил)бутановая кислота
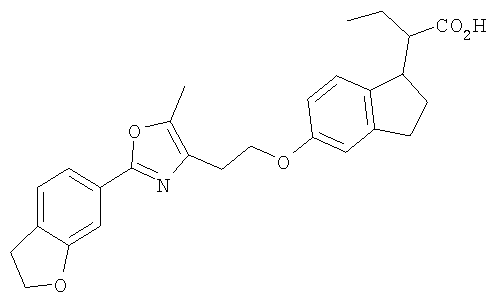
Выход: 0,10 г, 99%; 1H ЯМР (CDCI3, 400 МГц) δ 0,90-1,04 (t, 3Н), 1,41-1,54 (m, 1Н), 1,60-1,76 (m, 1Н), 1,83-1,97 (m, 1Н), 2,12-2,23 (m, 1Н), 2,35 (s, 3Н), 2,48-2,60 (m, 1Н), 2,69-2,90 (m, 2Н), 2,92-3,01 (t, 2Н), 3,18-3,28 (t, 2Н), 3,39-3,50 (m, 1Н), 4,08-4,12 (t, 2Н), 4,46-4,64 (t, 2Н), 6,76-6,71 (d, 1Н), 6,73 (s, 1Н), 6,77-6,84 (d, 1Н), 7,01-7,09 (d, 1Н), 7,71-7,78 (d, 1Н), 7,83 (s, 1Н).
Пример 50
Получение этокси-{5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}-уксусной кислоты через этил-[5-(бензилокси)-2,3-дигидро-1Н-инден-1-илиден](этокси)-этаноат
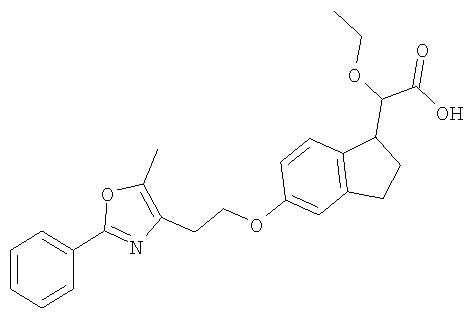
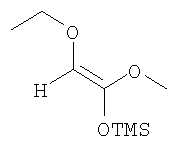
Стадия 1. LDA (полученный из 11 ммоль DIA и 11 ммоль BuLi) прибавляют к метил-2-этоксиацетату (10 ммоль) в 50 мл THF при -78°С, перемешивают в течение 1 ч, затем прибавляют TMSCI (30 ммоль). Смесь концентрируют в вакууме и непосредственно используют на следующей стадии без очистки.
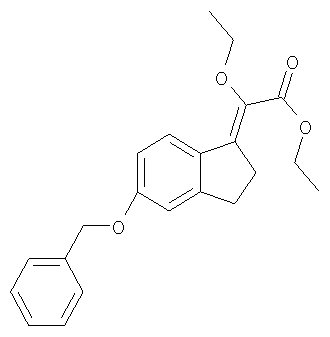
Стадия 2. 5-Бензилокси-1-инданон в CH2Cl2 мл медленно прибавляют к TiCl4 в CH2Cl2 (10 мл) при -78°С, перемешивают при -60°С в течение 10 мин и охлаждают до -78°С. Продукт, полученный на стадии 1, в CH2Cl2 (5 мл) медленно прибавляют и перемешивают в течение 10 мин. Реакцию останавливают с помощью насыщенного раствора К2СО3, фильтруют, экстрагируют этилацетатом и сушат над сульфатом натрия. Хроматография на колонке дает продукт в виде бесцветного масла. ЖХ-МС МН+=353,1, ВУ=4,00 мин; ЯМР (CDCl3, 400 МГц) δ 7,9 (1Н, d), 7,25 (5Н, m), 6,78 (2H, m), 4,93 (2Н, s), 4,15 (2Н, q), 3,75 (2Н, q), 3,05 (2Н, m), 2,85 (2Н, m), 1,22 (6Н, m)
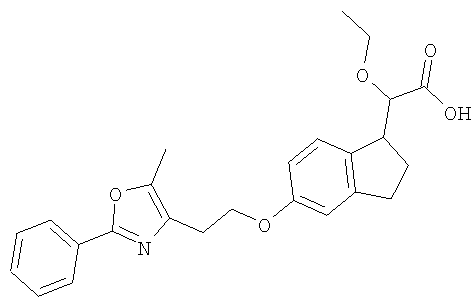
Стадия 3. С использованием в качестве исходного вещества продукта, полученного на стадии 2, и методик, аналогичных описанным в Примере 13, стадии 4-8, получают и характеризуют искомый конечный продукт: ЖХ-МС [МН+]=422,2, ВУ=3,25 мин; ЯМР (CDCl3, 400 МГц) δ 8,26 (1Н, d), 7,55 (2Н, m), 7,16 (2Н, d), 6,70 (3Н, m), 4,16 (2Н, q), 3,63 (2Н, t) 3,5 (2Н, m), 3,30 (1Н, m), 3,20 (1Н, m), 2,50 (3Н, s), 1,10 (3Н, m).
Пример 51
Получение 2-{5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1H-инден-1-ил}-бутановой кислоты через 2-(4-метил-2-фенил-1,3-оксазол-5-ил)-этанол
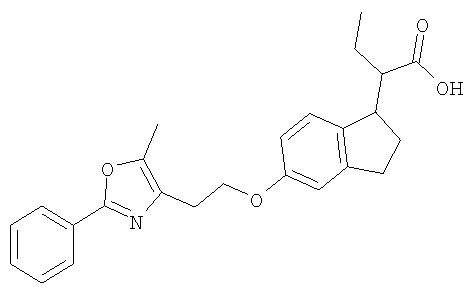
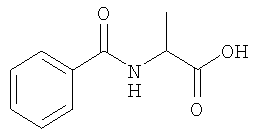
Стадия 1. К раствору гидроксида натрия (8,98 г, 224,49 ммоль) в воде (112,25 мл) прибавляют при комнатной температуре DL-аланин (10 г, 112,25 ммоль). Полученный раствор нагревают при 75°С и медленно прибавляют бензоилхлорид (15,77 г, 112,25 ммоль). Реакционную смесь нагревают в течение 30 мин, и охлаждают до 0°С в бане со льдом. Для доведения рН прибавляют концентрированную HCl, затем белое твердое вещество отфильтровывают на воронке со стеклянным пористым фильтром и сушат в вакууме над P2O5 в течение ночи. Очистка не требуется. Эта процедура дает N-бензоилаланин (19,6 г, выход 90,4%) в виде белого твердого вещества. 1H ЯМР (ДМСО-d6) δ 12,61 (s br, 1H), 8,64 (d, 1Н), 7,87-7,85 (m, 2H), 7,52-7,43 (m, 3H), 4,40 (q, 1Н), 1,39 (d, 3H).
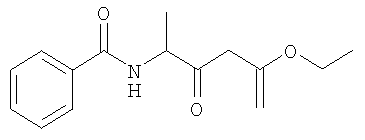
Стадия 2. В первой колбе N-бензоилаланин (2 г, 10,35 ммоль) растворяют в THF (20 мл) и прибавляют карбонилдиимидазол (CDI) (1,84 г, 11,39 ммоль). Полученную смесь перемешивают 1 ч при комнатной температуре и охлаждают до -78°С. Во второй колбе этилацетат (3,83 г, 43,48 ммоль) в THF (40 мл) охлаждают до -78°С и прибавляют LDA (24,3 мл, 48,51 ммоль, 2 М в THF), предварительно охлажденный до -78°С. Полученный раствор перемешивают 30 мин при -78°С и в первую колбу через канюлю прибавляют полученный енолят лития. Полученную белую взвесь перемешивают 30 мин при -78°С и нагревают до -10°С. Реакцию останавливают с помощью насыщенного водного раствора NH4Cl. Фазы разделяют и органическую фазу сушат над MgSO4 и растворители удаляют при пониженном давлении. Неочищенный продукт используют на следующей стадии без очистки. Это дает этил-4-(бензоиламино)-3-оксопентаноат (2,6 г, выход 95,5%) в виде белого твердого вещества. ЭР-МС m/z 263,4 (МН)+; ВЭЖХ ВУ (мин) 1,53; 1H ЯМР (ацетон-d6) δ 8,13 (s br, 1H), 7,93-7,91 (m, 2H), 7,58-7,43 (m, 3H), 4,72 (m, 1H), 4,19-4,01 (q, 2H), 3,67 (s, 2H), 1,47 (d, 3H), 1,15 (t, 3H).
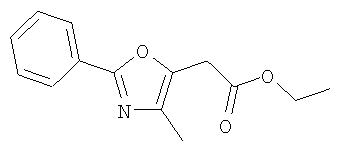
Стадия 3. К неочищенной смеси этил-4-(бензоиламино)-3-оксопентаноата (0,6 г, 2,28 ммоль) в DMF (4 мл) при комнатной температуре прибавляют POCl3 (1,04 г, 6,84 ммоль). Полученный раствор нагревают при 90°С в течение 1 ч, затем охлаждают до комнатной температуры и выливают на лед на 30 мин. Водный раствор осторожно прибавляют к насыщенному водному раствору NaHCO3. Фазы разделяют с помощью EtOAc и объединенные органические экстракты сушат над MgSO4 и растворитель удаляют при пониженном давлении. Неочищенный материал очищают на небольшой колонке Biotage с использованием градиента растворителя EtOAc/гексан от 0 до 50%. Это дает этил-(4-метил-2-фенил-1,3-оксазол-5-ил)-ацетат (0,269 г, выход 48%) в виде желтоватого масла. ЭР-МС m/z 246,2 (МН)+; ВЭЖХ ВУ (мин) 2,77; 1H ЯМР (COCl3) δ 8,01-7,98 (m, 2H), 7,45-7,41 (m, 3H), 4,20 (q, 2Н), 3,71 (s, 2H), 2,21 (s, 3H), 1,28 (t, 3H).
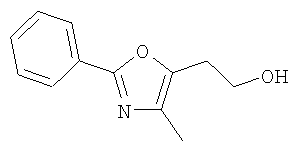
Стадия 4. К этил-(4-метил-2-фенил-1,3-оксазол-5-ил)-ацетату (0,922 г, 3,76 ммоль) в THF (6 мл) при комнатной температуре прибавляют LiBH4 2M/THF (9,41 мл, 4,70 ммоль). Реакционную смесь перемешивают в течение ночи при комнатной температуре, затем обрабатывают с помощью 2 н. HCl до рН 7. Растворитель THF удаляют при пониженном давлении, прибавляют EtOAc и разделяют фазы. Объединенные органические экстракты сушат над MgSO4 и растворитель концентрируют в вакууме. Неочищенный материал очищают на колонке Biotage с использованием градиента смеси растворителей EtOAc/гексан от 10 до 100%. Это дает 2-(4-метил-2-фенил-1,3-оксазол-5-ил)-этанол (0,193 г, выход 25%) в виде бесцветного масла. ЭР-МС m/z 204,2 (МН)+; ВЭЖХ ВУ (мин) 2,02; 1H ЯМР (ацетон-d6) δ 7,98-7,95 (m, 2H), 7,52-7,42 (m, 3H), 3,95 (s br, 1H), 3,82 (t, 2H) m, 2,90 (t, 2H), 2,13 (s, 3H).
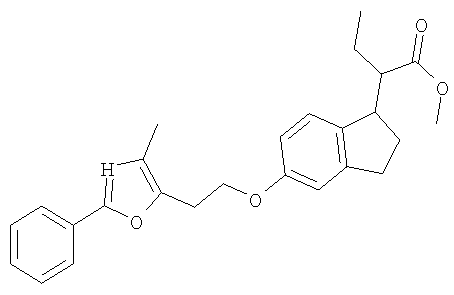
Стадия 5. DEAD (0,84 мл, 5,28 ммоль) в THF (1,5 мл) медленно прибавляют к раствору продукта, полученного на стадии 3 (4,95 ммоль), метил-5-гидрокси-2,3-дигидроинден-1-ил-2-бутаноату (0,78 г, 3,3 ммоль), PPh3 (1,4 г, 5,28 ммоль) в THF (13 мл). Смесь перемешивают при комнатной температуре в течение ночи. Смесь фильтруют, промывают водой, рассолом, сушат над сульфатом натрия и концентрируют. Хроматография на колонке дает продукт в виде бесцветного масла. ЖХ-МС [С26Н29NO4Н]+=420,4, ВУ=4,00 мин; 1H ЯМР (CDCl3): δ 7,9 (2H, d), 7,45 (2H, dd), 7,1 (d), 6,6-6,8 (3Н, m), 4,2 (2Н, t), 3,62 (3Н, s), 3,3 (1Н, m), 3,15 (2Н, t), 2,6-3,0 (2Н, m), 2,5 (1Н, m), 2,21 (3Н, s), 1,95 (1Н, m), 1,56-1,6 (3Н, br, m), 0,88 (3Н, t).
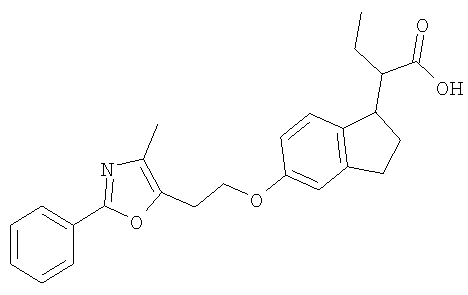
Стадия 6. КОН (0,5 мл, 3 N) прибавляют к раствору продукта, полученного на стадии 4 (42 мг, 0,1 ммоль), в THF/MeOH (1 мл, THF:МеОН 8:2). Смесь перемешивают при 70°С в течение 6 ч, затем охлаждают. Значение рН доводят до 4 с помощью 1 н. HCl. Смесь экстрагируют этилацетатом (3×2 мл). Объединенные органические слои сушат над сульфатом натрия и концентрируют в вакууме. Хроматография на колонке (2:8 гексан:этилацетат) дает продукт в виде белого твердого вещества (33 мг, 81%). ЖХ-МС [C25H27NO4H]+=406,3, ВУ=3,37 мин; 1H ЯМР (CDCl3): δ 8,0 (2Н, d), 7,45 (2Н, dd), 7,15 (1Н, d), 6,7-6,8 (3Н, m), 4,2 (2Н, t), 3,3 (1Н, m), 3,15 (2Н, t), 2,6-3,0 (2Н, m), 2,5 (1Н, m), 2,21 (3Н, s), 1,95 (1Н, m), 1,56-1,6 (3Н, br, m), 0,88 (3Н, t)
Путем использования методики, описанной выше в Примере 51, с применением других подходящих исходных веществ получают и характеризуют следующие вещества:
Пример 52
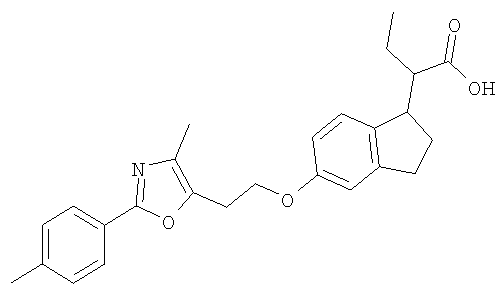
ЖХ-МС [C26H29NO4H]+=420,3, ВУ=3,52 мин; 1H ЯМР (CDCl3): δ 7,87 (2Н, d), 7,25 (2Н, dd), 7,1 (1Н, d), 6,6-6,8 (3Н, m), 4,2 (2Н, t), 3,45 (1Н, m), 3,30 (1Н, m), 3,15 (2Н, t), 2,7-3,0 (2Н, m, br), 2,5 (1Н, m), 2,4 (3Н, s) 1,95 (1Н, m), 1,56-1,60 (3Н, br, m), 0,88 (3Н, t)
Пример 53
2-{5-[2-(4-Метил-2-пропил-1,3-оксазол-5-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}-бутановая кислота
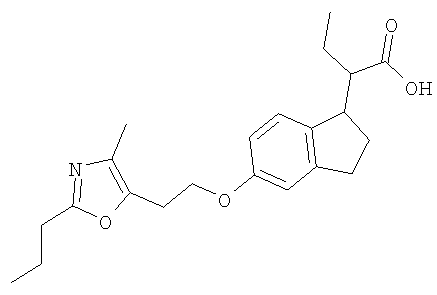
ЖХ-МС [C22H29NO4H]+=372,3, ВУ=3,16 мин; 1H ЯМР (CDCl3): δ 7,1 (1Н, d), 6,6 (2Н, d), 4,2 (2Н, t), 3,3 (1Н, m), 3,3 (1Н, m), 2,8 (2Н, t), 2,7 (1Н, m), 2,6 (2Н, t), 2,4 (2Н, m), 2,2 (3Н, s), 2,0-1,8 (2Н, br, m), 0,88 (3Н, t).
Путем использования методик, описанных выше в Примерах 1-53, с применением других подходящих исходных веществ аналогичным образом получают соединения формулы Ia, приведенные в таблице 3.
Таблица 3
Примеры получения соединений формулы (Ia)
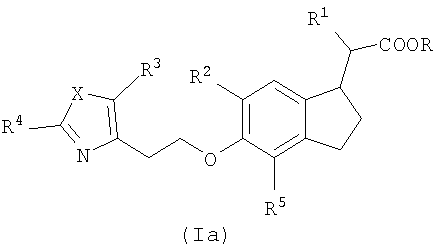

Пример 129
Получение этил-(5-метокси-2,3-дигидро-1Н-инден-1-илиден)-этаноата
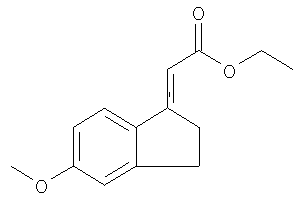
К раствору 5-метоксиинданона (150 г, 0,91 моль) в безводном тетрагидрофуране (4,5 л) прибавляют цинк (30 меш, 103,64 г, 1,59 моль) и хлорид меди(I) (4,53 г, 0,045 моль). Суспензию перемешивают в атмосфере Ar и кипятят с обратным холодильником в течение 15 мин; к кипящей с обратным холодильником смеси медленно по каплям прибавляют примерно 25% порции этилбромацетата (133 мл, 1,18 моль). После того, как смеси дают охладиться и ее перемешивают в течение ночи при комнатной температуре, ТСХ показывает наличие искомого продукта, указывая на образование реакционноспособного соединения цинка. По каплям прибавляют остальной этилбромацетат; наблюдают выделение тепла (температура в колбе повышается до 35°С). Через 4 ч ТСХ указывает на завершение реакции. После оседания твердого вещества на дно колбы жидкость сливают сифоном, оставив небольшое ее количество, закрывающее твердое вещество. В колбу повторно помещают 5-метоксиинданон (157,6 г, всего 1,86 моль), безводный тетрагидрофуран (4,5 л) и цинк (80,92 г, всего 2,73 моль). По каплям прибавляют этилбромацетат (140 мл, всего 2,36 моль). Наблюдают выделение тепла (температура в колбе повышается до 35°С). Когда перемешиваемая смесь охлаждается до комнатной температуры, ТСХ указывает на завершение реакции. Твердому веществу дают отстояться и жидкость сливают сифоном. Объединенные реакционные смеси концентрируют в вакууме до объема, равного ˜2 л. Жидкость выливают в количество 1 N водного раствора хлористоводородной кислоты (охлажденного водой со льдом), достаточное для доведения значения рН до 1. Продукт экстрагируют с помощью этилацетата (2×1 л, 1×500 мл). Объединенные экстракты промывают водой, рассолом (по 1 л каждого), сушат над сульфатом натрия, фильтруют и концентрируют в вакууме и получают темно-красное масло, которое постепенно затвердевает (438,3 г; теоретический выход = 432 г). 1H ЯМР (CDCl3): δ 7,5 (d, 1H), 6,8 (m, 2H), 6,2 (t, 1Н), 4,2 (q, 2H), 3,8 (s, 3Н), 3,3 (m, 2H), 3,0 (t, 2H), 1,3 (t, 3Н). МС (ХИ) m/z 233 [М+Н]+.
Пример 130
Получение этил-(5-метокси-2,3-дигидро-1Н-инден-1-ил]-ацетата

Неочищенный продукт, полученный в Примере 129, растворяют в абсолютном этаноле (2,6 л) и гидрируют при давлении водорода, равном 40 фунт-сила/дюйм2, над 10% палладием на угле (21,6 г). Фильтрование через целит и концентрирование фильтрата дает 433,3 г коричневого масла (выход 99% для 2 стадий).1H ЯМР (CDCl3): δ 7,1 (dd, 1H), 6,8 (d, 1Н), 6,7 (dd, 1H), 4,2 (q, 2Н), 3,8 (s, 3H), 3,5 (m, 1H), 2,9 (m, 2H), 2,7 (dd, 1H), 2,4 (m, 2H), 1,7 (m, 1H), 1,3 (t, 3H). МС (ХИ) m/z 235 [M+H]+.
Пример 131
Получение (5-метокси-2,3-дигидро-1Н-инден-1-ил)-уксусной кислоты

К раствору неочищенного сложного эфира (416 г, 1,77 моль), полученного в Примере 130, в 1 л EtOH прибавляют раствор NaOH (142 г, 3,54 моль) в 1,5 л воды. Мутную реакционную смесь кипятят с обратным холодильником и во время этой процедуры окраска переходит в темно-красную и реакционная смесь становится гомогенной. Через 1 ч реакционную смесь охлаждают до комнатной температуры и EtOH удаляют при пониженном давлении. Щелочной водный слой промывают с помощью Et2O (3×500 мл), затем подкисляют концентрированной HCl до рН ˜4, после чего образуется осадок масла. Смесь экстрагируют с помощью Et2O (4×500 мл). Объединенные экстракты промывают водой (2×300 мл), рассолом, затем сушат над Na2SO4. Фильтрование и выпаривание растворителя при пониженном давлении с последующей сушкой в вакууме в течение ночи дает искомое соединение (305 г, 83%) в виде желтого твердого вещества. 1Н ЯМР (CDCl3) δ 7,34 (d, 1Н), 6,71 (s, 1Н), 6,65 (dd, 1H), 3,71 (s, 3H), 3,47 (m, 1H), 2,80 (m, 3H), 2,35 (m, 2H), 1,71 (m, 1H). МС (ХИ) m/z 207 [М+Н]+.
Пример 132
Получение [(1S)-5-метокси-2,3-дигидро-1Н-инден-1-ил]-уксусной кислоты
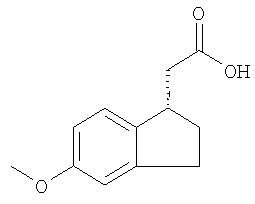
К раствору кислоты (341,0 г, 1,65 моль), полученной в Примере 131, в 8,2 л химически чистого ацетона при перемешивании при комнатной температуре по каплям прибавляют (S)-(-)-α-метилбензиламин (223,8 мл, 1,74 моль). Во время прибавления образуется густой белый осадок. Прибавляют еще 500 мл ацетона и перемешивание продолжают в течение 1 ч. Твердое вещество собирают путем фильтрования, промывают с помощью 300 мл ацетона и сушат при отсасывании. Затем твердое вещество суспендируют в ацетоне (8,2 л) и кипятят с обратным холодильником до полного растворения твердого вещества. Раствор медленно охлаждают в течение ночи, и за это время образуется белый осадок. Суспензию охлаждают до 0°С, затем фильтруют и твердое вещество промывают с помощью 500 мл ацетона. После сушки при отсасывании анализ образца с помощью ВЭЖХ приводит к 95% ее. Процедуру перекристаллизации повторяют так, как указано выше, с использованием 6,7 л ацетона. Анализ с помощью ВЭЖХ приводит к 99% ее. После сушки при отсасывании получают 192 г соли. Соль суспендируют в 2 л EtOAc и 1 л 1 N раствора HCl и встряхивают в делительной воронке, при этом соль растворяется. Органический слой отделяют, промывают с помощью 1 N HCl (500 мл), воды (2×300 мл) и рассола, затем сушат над Na2SO4. Растворитель выпаривают при пониженном давлении, получая масло, которое вскоре затвердевает. После вакуумной сушки получают искомый продукт (120,5 г, 35%) в виде почти белого твердого вещества. 1H ЯМР (CDCl3) δ 7,10 (d, 1H), 6,79 (d, 1Н), 6,73 (dd, 1H), 3,79 (s, 3H), 3,55 (m, 1H), 2,89 (m, 2H), 2,79 (dd, 1H), 2,46 (dd, 1H), 2,43 (m, 1H), 1,80 (m, 1H). MC (ESI) m/z 207 [M+H]+
Пример 133
Получение [(1S)-5-метокси-2,3-дигидро-1Н-инден-1-ил]уксусной кислоты

В качестве альтернативы Примеру 132 искомое соединение также можно получить с помощью ферментативного процесса. Так, мутную смесь неочищенного сложного эфира (500,0 г, 2,13 моль; чистота 87% по данным ВЭЖХ), полученного в Примере 130, в 1 л химически чистого ацетона, 2,5 л фосфатного буферного раствора (рН 7,0, 0,05 M) и 2,5 л деионизированной воды обрабатывают одной порцией липазы PS (Amano) (150 г) и смесь энергично перемешивают при комнатной температуре в течение ночи. Анализ аликвоты с помощью ВЭЖХ (гомогенная аликвота получена растворением аликвоты в IPA с последующим фильтрованием) приводит к одному пику, соответствующему непрореагировавшему R-сложному эфиру, и другому пику, соответствующему искомой S-кислоте. Отмечено наличие следовых количеств S-сложного эфира и R-кислоты. 2 н. HCl (500 мл, обеспечивают рН ˜2) одной порцией прибавляют к реакционной смеси и перемешивают в течение 20 мин. Смесь фильтруют и твердые вещества промывают с помощью EtOAc (2×500 мл), а затем воды (500 мл). Объединенные фильтраты дополнительно разбавляют с помощью 1 л EtOAc и слои совместно энергично перемешивают. Перемешивание прекращают и слоям дают разделиться. Обнаруживаются эмульсии, но их легко можно разрушить путем прибавления твердого NaCl и перемешивания. Водный слой удаляют, затем таким же образом экстрагируют с помощью EtOAc (3×1 л). Объединенные органические экстракты промывают водой (4×500 мл), затем рассолом. Полученный органический слой экстрагируют с помощью 5% раствора Na2CO3 (8×500 мл). Проведенный с помощью ВЭЖХ анализ органического слоя показывает, что слой не содержит S-энантиомера кислоты. Объединенные экстракты, содержащие Na2CO3, промывают с помощью EtOAc (2×1 л), затем подкисляют до рН ˜2 путем прибавления 2 н. HCl. Осаждается белое твердое вещество, что сопровождается выделением CO2. Смесь экстрагируют с помощью EtOAc (3×1 л). Объединенные экстракты промывают водой (2×1 л) и рассолом, затем сушат над Na2SO4. Проведенный с помощью ВЭЖХ анализ этого раствора показывает, что это вещество характеризуется 98% ее. Растворитель выпаривают при пониженном давлении, получая масло, которое вскоре затвердевает. Искомый продукт (172,9 г) после вакуумной сушки получают в виде не совсем белого твердого вещества. Этот материал перекристаллизовывают из кипящих гексанов (8,8 л). После охлаждения в течение ночи светло-желтые иглы собирают с помощью фильтрования, промывают гексанами (200 мл) и сушат при отсасывании. После вакуумной сушки искомый продукт (146,9 г, 38% в расчете на неочищенный исходный сложный эфир) получают в виде светло-желтых игл. 1Н ЯМР приводит к таким же результатам, как и выше.
Пример 134
Получение этил-[(1S)-5-метокси-2,3-дигидро-1Н-инден-1-ил]-ацетата
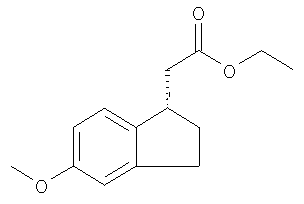
К раствору кислоты (305 г, 1,48 моль), полученной или в Примере 132 или 133, в 4,8 л абсолютного EtOH при комнатной температуре в атмосфере аргона по каплям прибавляют хлортриметилсилан (413 мл, 3,25 моль). Во время прибавления обнаруживается повышение температуры, составляющее примерно 5°С. Реакционную смесь перемешивают в течение ночи. EtOH выпаривают при пониженном давлении и получают двухфазную жидкую смесь. Ее разбавляют с помощью 500 мл воды со льдом, затем экстрагируют с помощью EtOAc (2×750 мл). Объединенные экстракты промывают водой (3×300 мл), затем насыщенным раствором NaHCO3 (200 мл). Органические вещества еще один раз промывают водой (300 мл), затем рассолом и сушат над Na2SO4. После удаления растворителя и сушки в вакууме искомое соединение (354 г, 102%) получают в виде светло-желтого масла. 1Н ЯМР (CDCl3) δ 7,07 (d, 1H), 6,78 (d, 1Н), 6,71 (dd, 1H), 4,18 (q, 2Н), 3,78 (s, 3H), 3,52 (m, 1H), 2,89 (m, 2H), 2,72 (dd, 1H), 2,37 (о, 2Н), 1,74 (m, 1H), 1,28 (t, 3H). MC (ХИ) m/z 235 [M+H]+.
Пример 135
Получение этил-[(1S)-5-гидрокси-2,3-дигидро-1H-инденил]-ацетата
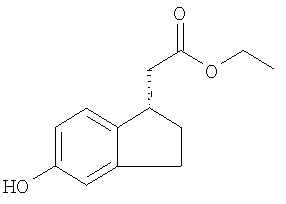
К холодному раствору (баня из воды со льдом) соединения (346 г, 1,48 моль), полученного в Примере 134, в 4,2 л СН2Cl2 порциями в атмосфере Ar прибавляют AlCl3 (984,6 г, 7,38 моль), так чтобы температура реакционной смеси сохранялась ниже 10°С. Светло-коричневую суспензию перемешивают 10 мин, затем по каплям прибавляют EtSH (546 мл, 7,38 моль) с такой скоростью, чтобы температура реакционной смеси сохранялась ниже 5°С. Через 2,5 ч перемешивания при температуре ниже 10°С реакционную смесь при энергичном перемешивании медленно выливают в 6 л воды со льдом. Органический слой отделяют и водный слой экстрагируют с помощью CH2Cl2 (3×1 л). Объединенные слои, содержащие CH2Cl2, промывают водой (2×1 л), затем сушат над Na2SO4. Растворитель удаляют при пониженном давлении, получая коричневое масло, которое фильтруют через слой силикагеля (элюируя с помощью 0-10% EtOAc/гексаны). Фракции собирают и после удаления растворителя и сушки в вакууме искомое соединение (314 г, 96%) получают в виде густого желтого масла. 1H ЯМР (CDCl3) 56,92 (d, 1H), 6,62 (d, 1H), 6,55 (dd, 1H), 4,10 (q, 2H), 3,43 (q, 1H), 2,75 (m, 2H), 2,64 (dd, 1H), 2,31 (dd, 1H), 2,29 (m, 1H), 1,67 (m, 1Н), 1,20 (t, 3H). MC (ХИ) m/z 221 [M+H]+.
Пример 136
Получение этил-2-((1S)-5-{2-[5-метил-2-(4-метилфенил](1,3-оксазол-4-ил)-этокси}-инданил)-ацетата
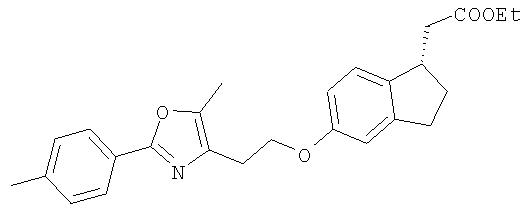
Суспензию этил-[(1S)-5-гидрокси-2,3-дигидро-1Н-инден-1-ил]-ацетата, полученного в Примере 135 (507,5 мг, 2,30 ммоль), и 2-[5-метил-2-(4-метилфенил)-1,3-оксазол-4-ил]-этанола, полученного в Примере 10 (500 мг, 2,30 ммоль), TMAD (792,6 мг, 4,60 ммоль) и (1,21 г, 4,60 ммоль) в 15 мл безводного DCM перемешивают при комнатной температуре в атмосфере Ar в течение 12 ч. DCM удаляют при пониженном давлении. Флэш-хроматография остатка на силикагеле с использованием 1% СН3CN/CH2Cl2 дает этил-2-((1S)-5-{2-[5-метил-2-(4-метилфенил)(1,3-оксазол-4-ил)]-этокси}-инданил)-ацетат (776,3 мг, 1,85 ммоль, 80,5%). ВЭЖХ/МС (М+Н)+ m/z 420,5.
Пример 137
Получение 2-((1S)-5-{2-[5-метил-2-(4-метилфенил)-(1,3-оксазол-4-ил]-этокси}-инданил)-уксусной кислоты
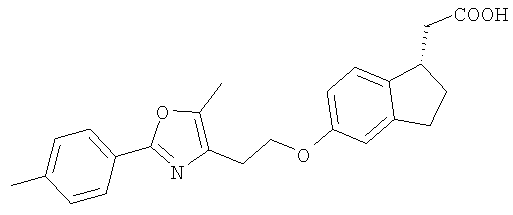
Этил-2-((1S)-5-{2-[5-метил-2-(4-метилфенил)(1,3-оксазол-4-ил)]-этокси}-инданил)-ацетат (Пример 136, 776,3 мг, 1,85 ммоль) в THF (4,0 мл) прибавляют к смеси водного раствора LiOH (2 М, 3,7 мл, 7,4 ммоль), воды (2,0 мл) и EtOH (4,0 мл) при комнатной температуре. Полученная смесь становится мутной. Эту смесь нагревают при 40°С (температура масляной бани). Реакция завершается через 1,5 ч. После охлаждения до комнатной температуры к смеси до рН 4,0 медленно прибавляют 1 N раствор HCl. Соединение экстрагируют с помощью EtOAc (3×20 мл). Объединенные слои, содержащие EtOAc, сушат (Na2SO4) и выпаривают. Флэш-хроматография остатка дает 2-((1S)-5-{2-[5-метил-2-(4-метилфенил)(1,3-оксазол-4-ил)]-этокси}-инданил)уксусную кислоту (616,8 мг, 1,57 ммоль, 85%) в виде белого твердого вещества. 1Н ЯМР (CDCl3) δ 7,83 (d, 2H), 7,21 (d, 2H), 7,03 (d, 1H), 6,74 (d, 1Н), 6,69 (dd, 1H), 4,19 (t, 2H), 3,45 (q, 1H), 2,93 (t, 2H), 2,78 (m, 2H), 2,51 (m, 2H), 2,30 (s, 3Н), 2,25 (s, 3Н), 1,53 (m, 2H).
Путем использования методик, описанных выше в Примерах 129-137, с применением других подходящих исходных веществ аналогичным образом получают соединения формулы 1а, приведенные в таблице 4.
Таблица 4
Примеры получения соединений формулы (Ia)


Пример 170
Получение метил-4-бром-3-оксопентаноата
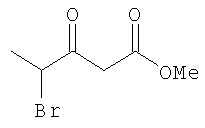
В сухую трехгорлую колбу в атмосфере Ar помещают раствор метилпропионилацетата (20 г, 154 ммоль) в CHCl3 (100 мл). С помощью капельной воронки в течение 2 ч при 0°С по каплям прибавляют бром (7,9 мл, 24,6 г, 154 ммоль). Затем реакционной смеси дают медленно нагреться до комнатной температуры и реакционную смесь перемешивают в течение ночи. Медленно прибавляют насыщенный раствор Na2CO3 (40 мл) и после перемешивания реакционной смеси в течение еще 15 мин слои растворителей разделяют и водный слой экстрагируют с помощью СН2Cl2 (50 мл). Объединенные органические слои сушат (Na2SO4), фильтруют и концентрируют при пониженном давлении. Затем остаток очищают с помощью флэш-хроматографии на силикагеле (10:1 гексаны/EtOAc) и получают искомый бромид в виде светло-желтого масла (25 г, 78%).1H ЯМР (CDCl3): δ 1,80 (d, 3H), 3,64-3,92 (m, 2Н), 3,78 (s, 3H), 4,61 (q, 1H).
Пример 171
Получение метил-(2-амино-5-метил-1,3-тиазол-4-ил)-ацетата
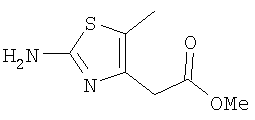
К раствору бромида, полученного в Примере 170 (18 г, 86 ммоль), в толуоле (100 мл) прибавляют тиомочевину (10,5 г, 138 ммоль). Реакционную смесь нагревают до 100°С в течение 1 ч, охлаждают до комнатной температуры и растворитель удаляют при пониженном давлении. Остаток растворяют в CH2Cl2 (100 мл), прибавляют насыщенный раствор NaHCO3 (75 мл) и смесь энергично перемешивают в течение 10 мин. Органический слой отделяют, сушат (Na2SO4), фильтруют и концентрируют при пониженном давлении. Затем остаток перекристаллизовывают из СН2Cl2/гексаны и получают продукт (10 г, 63%) в виде белого твердого вещества. (C7H10N2O2S): ЖХ-МС, ВУ 0,76 мин, М+Н 187,0; 1H ЯМР (CDCl3): δ 2,23 (s, 3H), 3,70 (s, 2Н), 3,75 (s, 3H), 4,83-4,95 (широкий s, 2Н).
Пример 172
Получение метил-(2-бром-5-метил-1,3-тиазол-4-ил)-ацетата
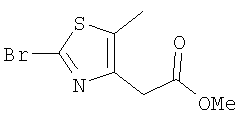
К раствору CuBr2 (4,03 г, 18,1 ммоль) и трет-бутилнитрита (2,82 мл, 23,8 ммоль) в MeCN (210 мл) при -20°С прибавляют соединение, полученное в Примере 170 (2,95 г, 15,9 ммоль). Реакционную смесь медленно нагревают до 15°С и при этой температуре наблюдается выделение N2. После перемешивания в течение еще 2 ч при 15°С реакционную смесь разбавляют с помощью Et2O (400 мл) и промывают с помощью 10% раствора HCl (200 мл). Слои растворителей разделяют, водный слой повторно экстрагируют с помощью Et2O (2×300 мл) и объединенные органические слои сушат (MgSO4), фильтруют и концентрируют при пониженном давлении. Затем остаток очищают с помощью флэш-хроматографии на силикагеле (98:2, гексаны/EtOAc) и получают бромид, полученный в Примере 172 (1,6 г, 40%), в виде бесцветного масла, которое при выдерживании затвердевает. (C7H8BrNO2S): ЖХ-МС, ВУ 2,56 мин, М+Н 250,3; 1H ЯМР (CDCl3): δ 2,26 (s, 3H), 3,60 (s, 2H), 3,61 (s, 3H).
Пример 173
Получение 2-(2-бром-5-метил-1,3-тиазол-4-ил)-этанола
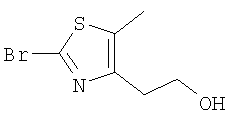
К раствору сложного эфира, полученного в Примере 172 (3,80 г, 15,2 ммоль), в CH2Cl2 (100 мл), прибавляют DIBAL-H (33,4 мл, 33,4 ммоль 1,0 М раствора в толуоле) при -78°С. Через 15 мин раствор нагревают до 0°С и перемешивают еще 90 мин. После этого для удаления избытка DIBAL-H по каплям прибавляют 2 N водный раствор HCl (50 мл). Слои растворителей разделяют и водный слой экстрагируют с помощью CH2Cl2 (2×200 мл). Объединенные органические слои сушат (MgSO4), фильтруют и концентрируют при пониженном давлении. Остаток очищают с помощью флэш-хроматографии на силикагеле (5:2 гексаны/EtOAc) и получают продукт (2,5 г, 74%) в виде желтоватого масла, которое при выдерживании затвердевает. (С6Н8BrNOS) ЖХ-МС, ВУ 1,38 мин, М+Н 221,0; 1Н ЯМР (CDCl3): δ 2,31 (s, 3H), 2,82 (t, 2Н), 2,90-3,00 (широкий s, 1Н), 3,89 (t, 2H).
Пример 174
Получение этил-{(1S)-5-[2-(2-бром-5-метил-1,3-тиазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}-ацетата
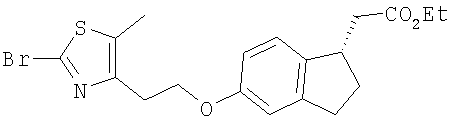
Стадия 1. К раствору соединения, полученного в Примере 173 (975 мг, 4,39 ммоль), и этил-[(1S)-5-гидрокси-2,3-дигидро-1Н-инден-1-ил]-ацетата (1,06 г, 4,83 ммоль) в THF (20 мл), прибавляют Ph3Р (1,88 г, 7,46 ммоль) и ADDP (1,96 г, 7,46 ммоль). Смесь энергично перемешивают при комнатной температуре в течение 72 ч, растворитель удаляют при пониженном давлении, и остаток очищают с помощью флэш-хроматографии на силикагеле (6:1 гексаны/EtOAc), получая продукт (1,4 г, 76%) в виде бесцветного масла, которое при выдерживании затвердевает. (C19H22BrNO3S) ЖХ-МС, ВУ 3,92 мин, М+Н 424,5; 1H ЯМР (CDCl3): δ 1,26 (t, 3H), 1,65-1,81 (m, 1Н), 2,28-2,45 (m, 2H), 2,37 (s, 3H), 2,69 (dd, 1H), 2,75-2,93 (m, 2H), 3,07 (t, 2H), 3,44-3,56 (m, 1H), 4,15 (t, 2H), 4,18 (q, 2H), 6,67 (dd, 1H), 6,73 (d, 1H), 7,03 (d, 1H).
Получение этил-((1S)-5-{2-[2-(4-изопропил-фенил)-5-метил-1,3-тиазол-4-ил-1-этокси]-2,3-дигидро-1Н-инден-1-ил}-ацетата
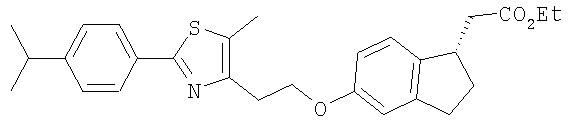
Стадия 2. К смеси толуола (15 мл) и 1,4-диоксана (3 мл) прибавляют соединение, полученное на стадии 1 (300 мг, 0,708 ммоль), 4-изопропилбензолбороновую кислоту (464 мг, 2,83 ммоль) и PdCl2(dppf).CH2Cl2 (52 мг, 0,071 ммоль). Через смесь в течение 30 мин пропускают поток Ar, затем прибавляют 2 N раствор Na2CO3 (3,7 мл, 7,08 ммоль) и реакционную смесь нагревают при 75°С в течение 18 ч. Затем реакционную смесь охлаждают до комнатной температуры, разбавляют с помощью EtOAc (200 мл) и промывают насыщенным раствором NaHCO4 (50 мл). Органический слой сушат (Na2SO4), фильтруют и концентрируют при пониженном давлении. Остаток очищают с помощью флэш-хроматографии на силикагеле (8:1 гексаны/EtOAc), и получают продукт (305 мг, 93%) в виде бесцветного масла. (С28Н33NO3S): ЖХ-МС, ВУ 5,17 мин, М+Н 464,5; 1H ЯМР (CDCl3): δ 1,17-1,31 (m, 3H), 1,26 (s, 3H), 1,27 (s, 3H), 1,65-1,82 (m, 1H), 2,30-2,43 (m, 2H), 2,46 (s, 3H), 2,72 (dd, 1Н), 2,78-3,00 (m, 3H), 3,17 (t, 2H), 3,46-3,57 (m, 1H), 4,17 (q, 2H), 4,27 (t, 2H), 6,71 (d, 1H), 6,78 (s, 1H), 7,04 (d, 1H), 7,55 (квартет АВ, 4Н).
Пример 175
Получение ((1S)-5-{2-[2-(4-изопропил-фенил)-5-метил-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1Н-инден-1-ил)-уксусной кислоты
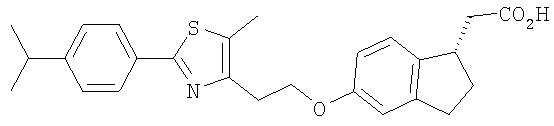
К раствору соединения, полученного в Примере 174 (305 мг, 0,657 ммоль), в смеси THF (8 мл), воды (8 мл) и EtOH (4 мл), прибавляют LiOH (63 мг, 2,63 ммоль). Реакционную смесь энергично перемешивают в течение 24 ч, разбавляют водой (20 мл), и промывают с помощью Et2O (10 мл). Затем водную фазу подкисляют до рН ˜ 1 с помощью 1 N HCl и после этого экстрагируют с помощью CH2Cl2 (4×50 мл). Объединенные органические слои сушат (Na2SO4), фильтруют и концентрируют при пониженном давлении. Затем остаток очищают с помощью флэш-хроматографии на силикагеле (95:5 CH2Cl2/MeOH) и получают продукт(189 мг, 66%) в виде белого твердого вещества. (С26Н29NO3S): ЖХ-МС, ВУ 3,95 мин, М+Н 436,4; 1H ЯМР (CDCl3): δ 1,25 (s, 3H), 1,28 (s, 3H), 1,70-1,82 (m, 1H), 2,32-2,43 (m, 2H), 2,45 (s, 3H), 2,74-2,98 (m, 4H), 3,18 (t, 2H), 3,47-3,54 (m, 1H), 4,28 (t, 2H), 6,72 (dd, 1H), 6,78 (s, 1H), 7,08 (d, 1Н), 7,51 (квартет АВ, 4H).
Пример 176
Получение метил-[5-метил-2-(4-метил-фенил)-1,3-тиазол-4-ил]ацетата
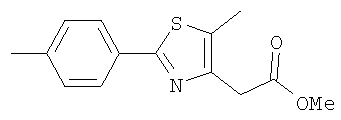
К раствору бромида, полученного в Примере 170 (1,15 г, 5,52 ммоль), в толуоле (20 мл), прибавляют 4-метилтиобензамид (1,0 г, 6,6 ммоль). Реакционную смесь кипятят с обратным холодильником в течение 15 ч, охлаждают до комнатной температуры, разбавляют с помощью EtOAc (150 мл) и промывают насыщенным раствором NaHCO3 (50 мл), а затем насыщенным раствором NH4Cl (50 мл). Органический слой сушат (Na2SO4), фильтруют и концентрируют при пониженном давлении. Затем остаток очищают с помощью флэш-хроматографии на силикагеле (9:1 гексаны/EtOAc) и получают продукт в виде розоватого масла, которое при выдерживании затвердевает (1,14 г, 62%). 1H ЯМР (CDCl3): δ 2,38 (s, 3H), 3,45 (s, 3Н), 3,74 (s, 3H), 3,80 (s, 2Н), 7,49 (квартет АВ, 4Н); Rf (0,4, элюент 9:1 гексаны/EtOAc).
Пример 177
Получение 2-[5-метил-2-(4-метилфенил)-1,3-тиазол-4-ил]-этанола

К раствору тиазола, полученного в Примере 176 (1,14 г, 4,37 ммоль), в THF (60 мл) при 0°С порциями прибавляют LiAIH4 (663 мг, 17,5 ммоль). Через 30 мин реакционную смесь нагревают до комнатной температуры и перемешивают в течение еще 60 мин. Затем реакционную смесь охлаждают до 0°С и избыток LiAIH4 удаляют, по каплям последовательно прибавляя воду (5 мл), 1 N NaOH (10 мл) и воду (5 мл). Затем смесь разбавляют с помощью насыщенного раствора соли Рошелле и экстрагируют с помощью EtOAc (4×75 мл). Объединенные органические фазы сушат (Na2SO4), фильтруют и концентрируют при пониженном давлении. Остаток очищают с помощью флэш-хроматографии на силикагеле (3:2 гексаны/EtOAc) и получают продукт в виде белого твердого вещества (830 мг, 82%). (C13H15NOS): ЖХ-МС, ВУ 2,50 мин, М+Н 234,2; 1H ЯМР (CDCl3): S 2,34 (s, 3H), 2,37 (s, 3H), 2,83 (t, 2H), 3,92-4,01 (широкий t, 2H), 4,04-4,15 (широкий s, 1H), 7,45 (квартет АВ, 4Н).
Приведенные ниже соединения синтезируют с помощью одной из двух методик, описанных в представленных выше Примерах 170-177.
Пример 178
{(1S)-5-[2-(5-Метил-2-фенил-1,3-тиазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}уксусная кислота
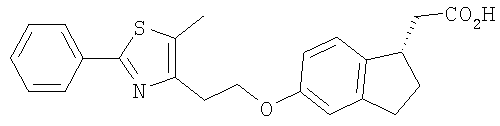
(С23Н23NO3S): ЖХ-МС ВУ 3,56 мин, М+Н 394,2; 1H ЯМР (CDCl3): δ 1,61-1,78 (m, 1H), 2,19-2,50 (m, 2H), 2,30 (s, 3Н), 2,62-2,91 (m, 3Н), 3,12 (t, 2H), 3,17-3,26 (m, 1H), 4,12 (t, 2Н), 6,70 (d, 1H), 6,79 (s, 1H), 6,98 (d, 1H), 7,21-7,40 (m, ЗН), 7,74-7,83 (m, 2H).
Пример 179
((1S)-5-{2-[5-Метил-2-(4-метил-фенил)-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1Н-инден-1-ил)-уксусная кислота
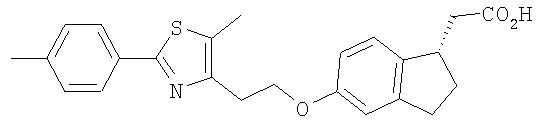
(C24H25NO3S): ЖХ-МС, ВУ 3,57 мин, М+Н 408,5; 1Н ЯМР (CDCl3): S 1,61-1,68 (m, 1H), 2,29 (s, 3Н), 2,36 (s, 3Н), 2,25-2,37 [скрытый] (m, 2H), 2,63-2,79 (m, 3Н), 3,09 (t, 2H), 3,35-3,47 (m, 1H), 4,18 (t, 2H), 6,60 (dd, 1H), 6,68 (s, 1H), 6,97 (d, 1H). 7,42 (квартет АВ, 4Н), 7,81-8,30 (br, 1H).
Пример 180
((1S)-5-{2-[2-(1,3-Бензодиоксол-5-ил)-5-метил-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1Н-инден-1-ил)уксусная кислота
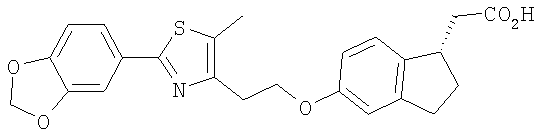
(С24Н23NO5S): ЖХ-МС, ВУ 4,04 мин, М+Н 438,5; 1H ЯМР (CDCl3): δ 1,71-1,83 (m, 1H), 2,36-2,51 (m, 2H), 2,45 (s, 3Н), 2,76-2,96 (m, 3Н), 3,15 (t, 2H), 3,48-3,58 (m, 1H), 4,29 (t, 2H), 6,00 (s, 2H), 6,72 (dd, 1H), 6,78 (s, 1H), 6,82 (d, 1H), 7,07 (d, 1H), 7,32-7,40 (m, 2H).
Пример 181
((1S)-5-[2-[2-(4-Метокси-фенил)-5-метил-1,3-тиазол-4-ил]-этокси]-2,3-дигидро-1Н-инден-1-ил)уксусная кислота
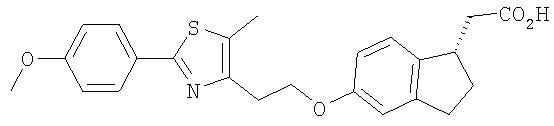
(C24H25NO4S): ЖХ-МС, ВУ 4,01 мин, М+Н 424,5; 1H ЯМР (CDCl3): δ 1,67-1,82 (m, 1H), 2,43 (s, 3Н), 2,34-2,47 (m, 2Н), 2,72-2,95 (m, ЗН), 3,09 (t, 2H), 3,42-3,57 (m, 1H), 3,84 (s, 3Н), 4,13 (t, 2H), 6,72 (d, 1H), 6,79 (s, 1H), 7,12 (d, 1H), 7,37 (квартет АВ, 4Н).
Пример 182
[(1S)-5-(2-{5-Метил-2-[4-(трифторметил)-фенил]-1,3-тиазол-4-ил}-этокси)-2,3-дигидро-1Н-инден-1-ил]-уксусная кислота

(С24Н22F3NO3S): ЖХ-МС, ВУ 4,47 мин, М+Н 462,4; 1H ЯМР (ДМСО-d6): δ 1,63-1,81 (m, 1H), 2,28-2,43 (m, 2H), 2,50 (s, 3Н), 2,69 (dd, 1H), 2,74-2,95 (m, 2H), 3,19 (t, 2H), 3,31-3,36 (m, 1H), 4,31 (t, 2H), 6,71 (dd, 1H), 6,78 (s, 1H), 7,08 (d, 1H), 7,87 (квартет АВ, 4Н).
Пример 183
((1S)-5-{2-[2-(4-Цианофенил)-5-метил-1,3-тиазол-4-ил]-этокси}-2.3-дигидро-1Н-инден-1-ил)уксусная кислота

(С24Н22F3NO3S): ЖХ-МС, ВУ 3,43 мин, М+Н 419,6; 1H ЯМР (CDCl3): δ 1,68-1,85 (m, 1H), 2,31-2,49 (m, 2H), 2,51 (s, ЗН), 2,77 (dd, 1H), 2,83-2,94 (m, 2H), 3,18 (t, 2H), 3,43-3,56 (m, 1H), 4,31 (t, 2H), 6,71 (dd, 1H), 6,79 (s, 1H), 7,10 (d, 1H), 7,86 (квартет АВ, 4Н).
Пример 184
((1S)-5-[2-[2-(4-Изопропилфенил)-5-метил-1,3-тиазол-4-ил]-этокси]-2,3-дигидро-1Н-инден-1-ил)-уксусная кислота
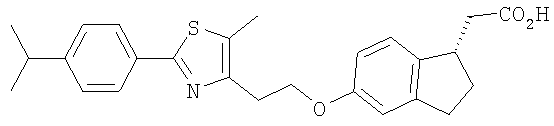
(С26Н29NO3S): ЖХ-МС, ВУ 3,95 мин, М+Н 436,4; 1H ЯМР (CDCl3): δ 1,25 (s, 3Н), 1,28 (s, 3Н), 1,70-1,82 (m, 1H), 2,32-2,43 (m, 2H), 2,45 (s, 3Н), 2,74-2,98 (m, 4H), 3,18 (t, 2Н), 3,47-3,54 (m, 1H), 4,28 (t, 2H), 6,72 (dd, 1H), 6,78 (s, 1H), 7,08 (d, 1H), 7,51 (квартет АВ, 4Н).
Пример 185
((1S)-5-{2-[2-(3-Хлор-4-фторфенил)-5-метил-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1Н-инден-1-ил)уксусная кислота
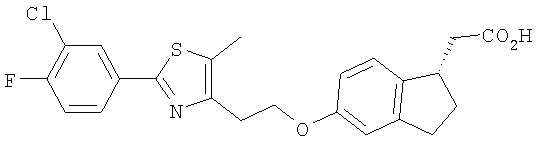
(С23Н21ClFNO3S): ЖХ-МС, ВУ 3,89 мин, М+Н 446,4; 1H ЯМР (CDCl3): δ 1,68-1,86 (m, 1H), 2,32-2,46 (m, 2H), 2,50 (s, 3Н), 2,80 (dd, 1H), 2,84-2,96 (m, 2H), 3,18 (t, 2H), 3,47-3,59 (m, 1H), 4,32 (t, 2H), 6,72 (d, 1H), 6,82 (s, 1H), 7,12 (d, 1H), 7,23 (t, 1H), 7,72-7,82 (m, 1H), 7,97-8,04 (m, 1H).
Пример 186
((1S)-5-[2-[2-(3,4-Дихлорфенил)-5-метил-1,3-тиазол-4-ил]-этокси]-2,3-дигидро-1Н-инден-1-ил)-уксусная кислота

(С23Н21Cl2NO3S): ЖХ-МС, ВУ 4,12 мин, М+Н 462,0; 1H ЯМР (CDCl3): δ 1,74-1,88 (m, 1H), 2,36-2,48 (m, 2H), 2,50 (s, 3Н), 2,73-2,93 (m, 3Н), 3,19 (t, 2H), 3,48-3,55 (m, 1H), 4,30 (t, 2H), 6,71 (d, 1H), 6,79 (s, 1H), 7,09 (d, 1H), 7,52 (d, 1H), 7,61 (dd, 1H), 8,02 (d, 1H).
Пример 187
((1S)-5-{2-[2-(4-Фторфенил)-5-метил-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1Н-инден-1-ил)уксусная кислота
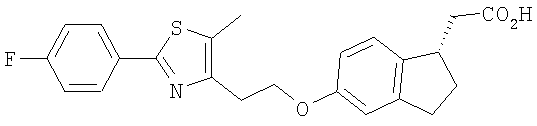
(С23Н22FNO3S): ЖХ-МС, ВУ 3,58 мин, М+Н 412,4; 1H ЯМР (CDCl3): δ 1,70-1,77 (m, 1H), 2,37-2,45 (m, 1H), 2,44 (s, 3Н), 2,70-2,90 (m, 4H), 3,16 (t, 2H), 3,47-3,52 (m, 1H), 4,27 (t, 2H), 6,70 (d, 1H), 6,76 (s, 1H), 7,00-7,10 (m, 3Н), 7,82-7,87 (m, 2H).
Пример 188
((1S)-5-(2-[2-(3,4-Диметилфенил)-5-метил-1,3-тиазол-4-ил]-этокси)-2,3-дигидро-1Н-инден-1-ил)уксусная кислота
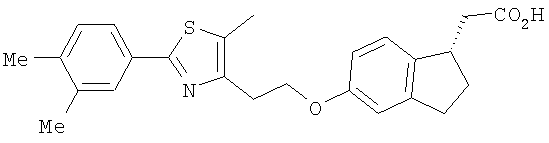
(С25Н27NO3S): ЖХ-МС, ВУ 4,39 мин, М+Н 422,3; 1H ЯМР (CDCl3): δ 1,70-1,83 (m, 1H), 2,29 (s, 3Н), 2,32 (s, 3Н), 2,37-2,50 [скрытый] (m, 2Н), 2,46 (s, 3H), 2,70,-2,90 (m, 3Н), 3,32 (t, 2Н), 3,45-3,60 (m, 1H), 4,30 (t, 2H), 6,73 (d, 1H), 6,79 (s, 1H), 7,07 (d, 1H), 7,17 (d, 1H), 7,59 (d,1H), 7,68 (s,1H).
Пример 189
((1S)-5-{2-[2-(4-Ацетилфенил)-5-метил-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1Н-инден-1-ил)уксусная кислота
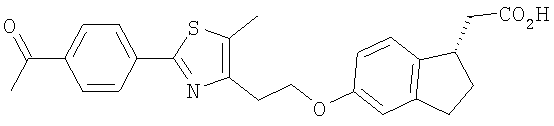
(C25H25NO4S): ЖХ-МС, ВУ 4,01 мин, М+Н 436,3; 1H ЯМР (CDCl3): δ 1,70-1,82 (m, 1H), 2,37-2,49 (m, 2H), 2,50 (s, 3Н), 2,63 (s, 3Н), 2,70-2,90 (m, 3Н), 3,20 (t, 2H), 3,45-3,60 (m, 1H), 4,30 (t, 2H), 6,72 (d, 1H), 6,78 (s, 1H), 7,08 (d, 1H), 7,95-8,03 (m, 4H).
Пример 190
[(1S)-5-(2-[2-[4-Диметиламино)-фенил]-5-метил-1,3-тиазол-4-ил]-этокси)-2,3-дигидро-1H-инден-1-ил]-уксусная кислота
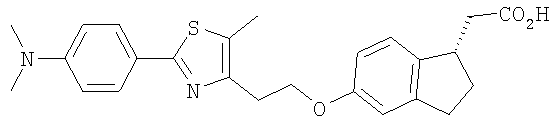
(С25Н28N2O3S): ЖХ-МС, ВУ 2,95 мин, М+Н 437,2; 1H ЯМР (ДМСО-d6): δ 1,53-1,65 (m, 1H), 2,12-2,24 (m, 2H), 2,36 (s, 3Н), 2,63-2,84 (m, 3Н), 2,94 (s, 6H), 3,03 (t, 2H), 3,27-3,38 (m, 1H), 4,18 (t, 2H), 6,65 (d, 1H), 6,75 (s, 1H), 7,08 (d, 1H), 7,17 (квартет АВ, 4H).
Пример 191
((1S)-5-{2-[2-(3-Амино-4-метилфенил)-5-метил-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1Н-инден-1-ил)уксусная кислота
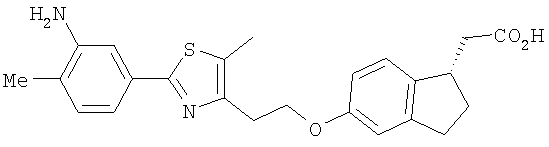
С24Н26N2O3S.С2F3O2): ЖХ-МС, ВУ 3,5 мин, М+Н 423,3; 1H ЯМР (CD3OD): δ 1,67-1,82 (m, 1H), 2,25-2,37 (m, 2H), 2,38 (s, 3H), 2,50 (s, 3Н), 2,67-2,90 (m, 3H), 3,20 (t, 2H), 3,41-3,56 (m, 1H), 4,32 (t, 2H), 6,71 (d, 1H), 6,79 (s, 1H), 7,09 (d, 1H), 7,42 (d, 1H), 7,69 (dd, 1H), 7,77 (d, 1H).
Пример 192
((1S)-5-{2-[2-(2-Фторфенил)-5-метил-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1Н-инден-1-ил)-уксусная кислота

(С23Н22FNO3S): ЖХ-МС, ВУ 4,25 мин, М+Н 412,2; 1H ЯМР (CDCl3): δ 1,70-1,82 (m, 1H), 2,37-2,48 (m, 2H), 2,49 (s, 3H), 2,74-2,94 (m, 3H), 3,21 (t, 2H), 3,42-3,60 (m, 1H), 4,31 (t, 2H), 6,72 (d, 1H), 6,79 (s, 1H), 7,06-7,35 (m, 4H), 8,21 (t, 1H).
Пример 193
((1S)-5-(2-[2-(4-Хлорфенил)-5-метил-1,3-тиазол-4-ил]-этокси)-2,3-дигидро-1Н-инден-1-ил)уксусная кислота
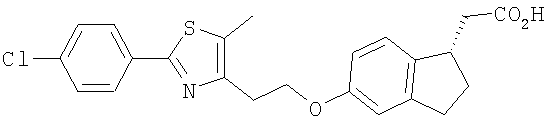
(С23Н22ClNO3S): ЖХ-МС, ВУ 4,44 мин, М+Н 428,2; 1Н ЯМР (CDCl3): S 1,70-1,81 (m, 1H), 2,35-2,45 (m, 2H), 2,46 (s, 3H), 2,74-2,89 (m, 3H), 3,17 (t, 2H), 3,42-3,60 (m, 1H), 4.28 (t, 2H), 6,71 (d, 1H), 6,77 (s, 1H), 7,07 (d, 1H), 7,36 (d, 2H), 7,79 (d, 2H).
Пример 194
((1S)-5-{2-[2-(4-Этоксифенил)-5-метил-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1Н-инден-1-ил)уксусная кислота
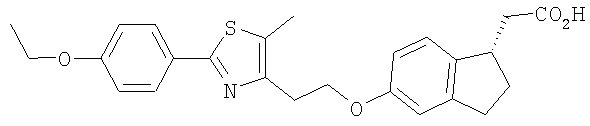
(C25H27NO4S): ЖХ-МС, ВУ 3,55 мин, М+Н 438,5; 1H ЯМР (CDCl3): δ 1,40 (t, 3H), 1,70-1,82 (m, 1H), 2,35-2,47 (m, 2Н), 2,45 (s, 3H), 2,74-2,89 (m, 3H), 3,20 (t, 2Н), 3,42-3,59 (m, 1H), 4,07 (q, 2H), 4,29 (t, 2Н), 6,71 (d, 1H), 6,76 (s, 1H), 6,91 (d, 1H), 7,06 (d, 2H), 7,82 (d, 2H).
Пример 195
((1S)-5-{2-[2-(3,4-диметоксифенил)-5-метид-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1Н-инден-1-ил)уксусная кислота

(C25H27NO5S): ЖХ-МС, ВУ 3,86 мин, М+Н 454,2; 1H ЯМР (CDCl3): δ 1,67-1,82 (m, 1H), 2,37-2,48 (m, 2H), 2,49 (s, 3H), 2,71-2,87 (m, 3H), 3,27 (t, 2H), 3,42-3,57 (m, 1H), 3,93 (s, 3H), 3,96 (s, 3H), 4,29 (t, 2H), 6,35-6,64 (широкий s, 1H), 6,67 (d, 1H), 6,75 (s, 1H), 6,89 (d, 1H), 7,05 (d, 1H), 7,39 (d, 1H), 7,56 (s, 1H).
Пример 196
((1S)-5-{2-[5-Метил-2-(3-метилфенил)-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1Н-инден-1-ил)уксусная кислота
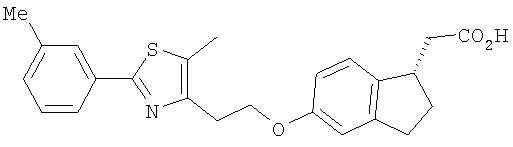
(С24Н25N3S): ЖХ-МС, ВУ 3,71 мин, М+Н 408,2; 1H ЯМР (CDCl3): δ 1,70-1,82 (m, 1H), 2,38-2,52 (m, 2H), 2,40 (s, 3H), 2,47 (s, 3H), 2,75-2,87 (m, 3H), 3,19 (t, 2H), 3,45-3,60 (m, 1H), 4,29 (t, 2H), 6,72 (d, 1H), 6,78 (s, 1H), 7,07 (d, 1H), 7,19 (d, 1H), 7,30 (t, 1H), 7,64 (d, 1H), 7,75 (s, 1H).
Пример 197
[(1S)-5-(2-{5-Метил-2-[3-(трифторметил)-фенил]-1,3-тиазол-4-ил}-этокси)-2,3-дигидро-1Н-инден-1-ил]-уксусная кислота
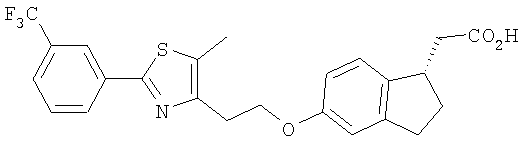
(С24Н22F3NO3S): ЖХ-МС, ВУ 3,90 мин, М+Н 462,1; 1H ЯМР (CDCl3): S 1,70-1,82 (m, 1Н), 2,38-2,48 (m, 2Н), 2,49 (s, 3Н), 2,75-2,87 (m, 3Н), 3,19 (t, 2Н), 3,44-3,59 (m, 1H), 4,30 (t, 2Н), 6,72 (d, 1H), 6,79 (s, 1H), 7,07 (d, 1H), 7,52 (t, 1H), 7,61 (d, 1H), 8,01 (d, 1H), 8,13 (s, 1H).
Пример 198
((1S)-5-{2-[2-(3-Фторфенил)-5-метил-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1Н-инден-1-ил)уксусная кислота
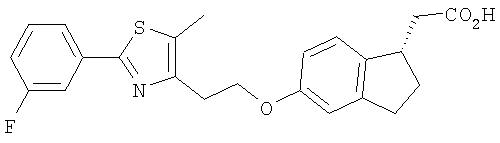
(С23Н22FNO3S): ЖХ-МС, ВУ 3,66 мин, М+Н 412,1; 1H ЯМР (CDCl3): δ 1,70-1,82 (m, 1H), 2,39-2,47 (m, 2H), 2,48 (s, 3Н), 2,76-2,87 (m, 3Н), 3,18 (t, 2H), 3,45-3,60 (m, 1H), 4,30 (t, 2H), 6,72 (d, 1H), 6,78 (s, 1H), 7,04-7,09 (m, 2H), 7,36-7,42 (m, 1H), 7,58-7,62 (m, 2H).
Пример 199
((1S)-5-(2-[2-(3,5-Диметилфенил)-5-метил-1,3-тиазол-4-ил]-этокси)-2,3-дигидро-1Н-инден-1-ил)уксусная кислота
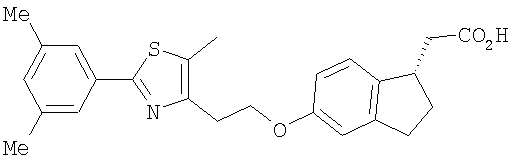
(С25Н27NO3S): ЖХ-МС, ВУ 3,88 мин, М+Н 422,2; 1H ЯМР (CDCl3): δ 1,72-1,84 (m, 1H), 2,36 (s, 6H), 2,37-2,45 (m, 2H), 2,46 (s, 3Н), 2,75-2,87 (m, 3Н), 3,19 (t, 2H), 3,45-3,60 (m, 1H), 4,28 (t, 2H), 6,72 (d, 1H), 6,79 (s, 1H), 7,01 (s, 1H), 7,07 (d, 1H), 7,48 (s, 2H).
Пример 200
[(1S)-5-(2-{5-Метил-2-[4-(трифторметокси)-фенил]-1,3-тиазол-4-ил}-этокси)-2,3-дигидро-1Н-инден-1-ил]-уксусная кислота
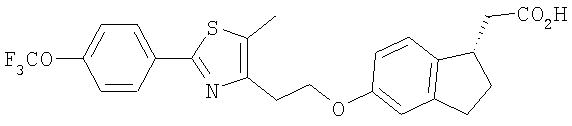
(С24Н22F3NO4S): ЖХ-МС, ВУ 3,95 мин, М+Н 478,1; 1H ЯМР (CDCl3): δ 1,72-1,84 (m, 1Н), 2,38-2,46 (m, 2Н), 2,47 (s, 3Н), 2,75-2,87 (m, 3Н), 3,18 (t, 2Н), 3,45-3,60 (m, 1H), 4,29 (t, 2Н), 6,72 (d, 1H), 6,77 (s, 1H), 7,07 (d, 1H), 7,24 (d, 2H), 7,88 (d, 2H).
Пример 201
((1S)-5-(2-[2-(3-Метоксифенил)-5-метил-1,3-тиазол-4-ил]-этокси)-2,3-дигидро-1Н-инден-1-ил)уксусная кислота
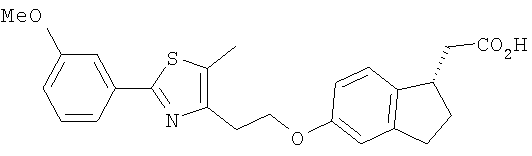
(C24H25NO4S): ЖХ-МС, ВУ 3,56 мин, М+Н 424,2; 1H ЯМР (CDCl3): 61,70-1,82 (m, 1H), 2,37-2,52 (m, 2H), 2,49 (s, 3Н), 2,75-2,87 (m, 3Н), 3,19 (t, 2H), 3,45-3,57 (m, 1H), 3,87 (s, 3Н), 4,30 (t, 2H), 6,72 (d, 1H), 6,79 (s, 1H), 6,95 (d, 1H), 7,10 (d, 1H), 7,32 (t, 1H), 7,40-7,45 (m, 2H).
Пример 202
((1S)-5-{2-[2-(1,1'-Бифенил-4-ил)-5-метил-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1Н-инден-1-ил)уксусная кислота
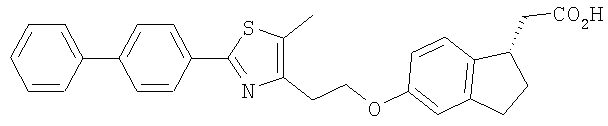
(С29Н27NO3S): ЖХ-МС, ВУ 3,96 мин, М+Н 470,3; 1H ЯМР (CDCl3): δ 1,70-1,81 (m, 1H), 2,38-2,48 (m, 2H), 2,49 (s, 3Н), 2,75-2,87 (m, 3Н), 3,20 (t, 2H), 3,43-3,59 (m, 1H), 4,31 (t, 2H), 6,72 (d, 1H), 6,79 (s, 1H), 7,08 (d, 1H), 7,36 (t, 1H), 7,45 (t, 2H), 7,61-7,65 (m, 4H), 7,93 (d, 2H).
Пример 203
Получение этил-{(1S)-5-[2-(4-метил-2-Фенил-1,3-оксазол-5-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}-ацетата
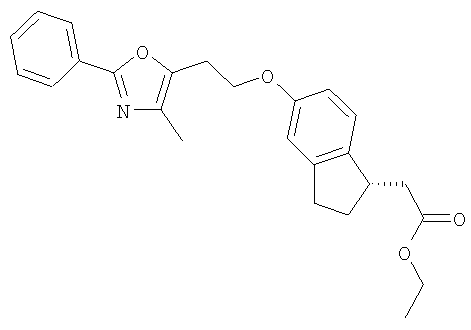
ADDP (0,205 г, 0,81 ммоль) прибавляют к смеси PPh3 (0,212 г, 0,81 ммоль), этил-[(1S)-5-гидрокси-2,3-дигидро-1Н-инден-1-ил]-ацетата (0,107 г, 0,49 ммоль) и 2-(4-метил-2-фенил-1,3-оксазол-5-ил)-этанола (стадия 4, Пример 51, 0,110 г, 0,54 ммоль) в THF (5 мл). Реакционную смесь перемешивают в течение ночи при комнатной температуре и дополнительно прибавляют ADDP (0,136 г, 0,54 ммоль) и PPh3 (0,141 г, 0,54 ммоль) с CH2Cl2 (5 мл). Раствор перемешивают в течение 24 ч при комнатной температуре и фильтруют. Фильтрат выпаривают и полученную смесь очищают на колонке Biotage с использованием градиента растворителя EtOAc/гексан от 0 до 50%. Получают этил-{(1S)-5-[2-(4-метил-2-фенил-1,3-оксазол-5-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}-ацетат (0,145 г, выход 66%) в виде желтоватого масла. ЭР-МС m/z 406,2 ((МН)+; ВЭЖХ ВУ (мин) 3,89; 1H ЯМР (ацетон-d6) δ 7,85-7,82 (m, 2H), 7,36-7,30 (m, 3Н), 6,94 (d, 1H), 6,65 (s, 1Н), 6,60-6,55 (m, 1H), 4,10 (t, 2H), 3,98 (q, 2H), 3,31-3,27 (m, 1H), 3,03 (t, 2H), 3,27-2,51 (m, 3Н), 2,24-2,14 (m, 2H), 2,18 (s, 3Н), 1,58-1,53 (m, 1H), 1,08 (t, 3H).
Пример 204
Получение {(1S)-5-[2-(4-метил-2-фенил-1,3-оксазол-5-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}-уксусной кислоты
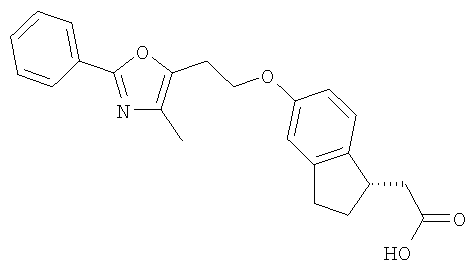
Этил-{(1S)-5-[2-(4-метил-2-фенил-1,3-оксазол-5-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}-ацетат (0,135 г, 0,33 ммоль) растворяют в EtOH (6 мл) и прибавляют LiOH (0,024 г, 1,0 ммоль). Прибавляют воду (3 мл) и THF, пока мутный раствор не станет прозрачным. Полученную смесь перемешивают в течение ночи при комнатной температуре. Прибавляют HCl (2 н.), пока значение рН не станет равным 2, затем трижды экстрагируют этилацетатом. Органические слои объединяют, сушат и концентрируют и получают {(1S)-5-[2-(4-метил-2-фенил-1,3-оксазол-5-ил)-этокси]-2,3-дигидро-1H-инден-1-ил}уксусную кислоту (0,039 г, выход 30,6%) в виде бесцветного масла. ЭР-МС m/z 378,2 (МН)+; ВЭЖХ ВУ (мин) 3,22; 1H ЯМР (ацетон-d6) S 8,1 (s br 1H) 8,0-7,95 (m, 2Н), 7,52-7,43 (m, 3Н), 7,15 (d, 1H), 6,81 (s, 1H), 6,73 (d, 1H), 4,27 (t, 2H) 3,47-3,40 (m, 1H), 3,18 (t, 2H), 2,90-2,68 (m, 3H), 2,41-2,29 (m, 2H), 2,18 (s, 3H), 1,77-1,68 (m, 1H).
Путем использования методик, описанных выше в Примерах 51, 203 и 204, с применением других подходящих исходных веществ получают и характеризуют следующие соединения:
Пример 205
Получение N-(4-метилбензоил)-аланина
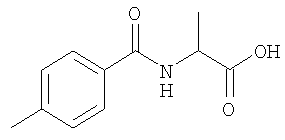
1H ЯМР (ДМСО-d6) δ 12,60 (s br, 1H), 8,57 (d, 1H), 7,81 (d, 2H), 7,28 (d, 2H), 4,38 (q, 1H), 2,35 ( s, 3H), 1,38 (d, 3H).
Пример 206
Получение N-(3-фтор-4-метилбензоил)-аланина

1H ЯМР (ДМСО-d6) δ 12,54 (s br, 1H), 8,67 (d, 1H), 7,65-7,62 (m, 2H), 7,39 (t, 1H), 4,38 (q, 1H), 2,27 (s, 3H), 1,38 (d, 3H).
Пример 207
Получение N-[4-(трифторметил)-бензоил]-аланина
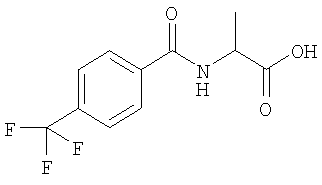
1H ЯМР (DMCO-d6) δ 12,64 (s br, 1H), 8,91 (d, 1H), 8,08 (d, 2H), 7,85 (d, 2H), 4,42 (q, 1H), 1,40 (d, 3H).
Пример 208
Получение этил-4-[(4-метилбензоил)-амино]-3-оксопентаноата
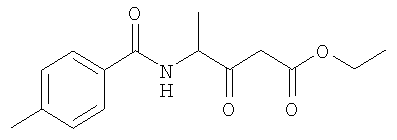
ЭР-МС m/z 278,38 ((МН)+); ВЭЖХ ВУ (мин) 2,04. 1H ЯМР (ацетон-d6) δ 8,08 (s br, 1Н), 7,90 (d, 2H), 7,28 (d, 2Н), 4,72-4,67 (m, 1H), 4,13 (q, 2Н), 3,66 (s, 2H), 2,40 (s, 3Н), 1,41 (d, 3H), 1,12 (t, 3H).
Пример 209
Получение этил-4-[(3-фтор-4-метилбензоил)-амино]-3-оксопентаноата

ЭР-МС m/z 296,4 ((МН)+); ВЭЖХ ВУ (мин) 2,26. 1H ЯМР (ацетон-d6) δ 7,75-7,60 (m, 2H), 7,38 (t, 1H), 4,20 (q, 2H), 3,65 (s, 2H), 2,23 (s, 3Н), 1,45 (d, 3Н), 1,20 (t, 3Н).
Пример 210
Получение этил-3-оксо-4-{[4-(трифторметил)-бензоил]-амино}-пентаноата
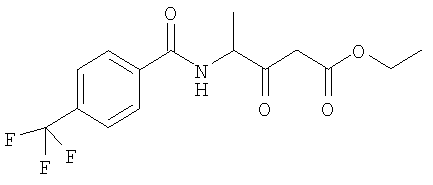
ЭР-МС m/z 332,4 ((МН)+); ВЭЖХ ВУ (мин) 2,45. 1H ЯМР (ацетон-d6) δ 8,14 (d, 2H), 7,84 (d, 2H), 4,80-4,74 (m, 2H), 4,20 (q, 2H), 3,70 (s, 2H), 1,48 (d, 3Н), 1,21 (t, 3Н).
Пример 211
Получение этил-[4-метил-2-(4-метилфенил)-1,3-оксазол-5-ил]-ацетата
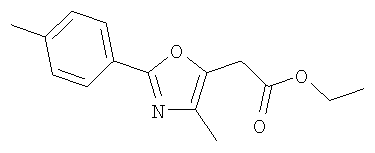
ЭР-МС m/z 260,2 ((МН)+); ВЭЖХ ВУ (мин) 2,96.1Н ЯМР (ацетон-d6) δ 7,86 (d, 2H), 7,30 (d, 2H), 4,15 (q, 2H), 3,81 (s, 2H), 2,37 (s, 3Н), 2,14 (s, 3Н), 1,24 (t, 3Н).
Пример 212
Получение этил-[2-(3-фтор-4-метилфенил)-4-метил-1,3-оксазол-5-ил]-ацетата
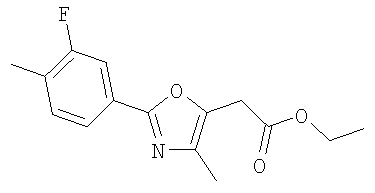
ЭР-МС m/z 278,3 ((МН)+); ВЭЖХ ВУ (мин) 2,89. 1Н ЯМР (ацетон-d6) δ 7,69 (d, 1Н), 7,60 (d, 1H), 7,37 (t, 1H), 4,15 (q, 2H), 3,83 (s, 2H), 2,31 (s, 3H), 2,15 (s, 3H), 1,23 (t, 3Н).
Пример 213
Получение этил-{4-метил-2-[4-(трифторметил)-фенил]-1,3-оксазол-5-ил}-ацетата
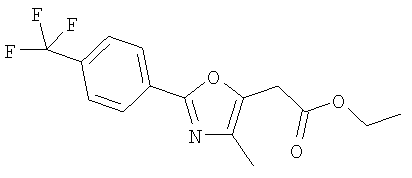
ЭР-МС m/z 314,3 ((МН)+); ВЭЖХ ВУ (мин) 3,27. 1Н ЯМР (ацетон-d6) δ 8,18 (d, 2H), 7,84 (d, 2H), 4,17 (q, 2H), 3,88 (s, 2H), 2,20 (s, 3H), 1,23 (t, 3H).
Пример 214
Получение 2-[4-метил-2-(4-метилфенил)-1,3-оксазол-5-ил]-этанола
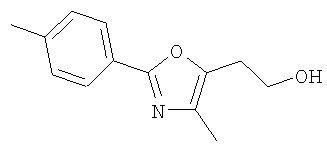
ЭР-МС m/z 218,2 ((МН)+); ВЭЖХ ВУ (мин) 2,35. 1Н ЯМР (ацетон-d6) δ 7,85 (d, 2H), 7,27 (d, 2H), 3,99 (s br, 1H), 3,83 (t, 2H), 2,90 (t, 2H), 2,37 (s, 3Н), 2,12 (s, 3Н).
Пример 215
Получение 2-[2-(3-фтор-4-метилфенил)-4-метил-1,3-оксазол-5-ил]-этанола
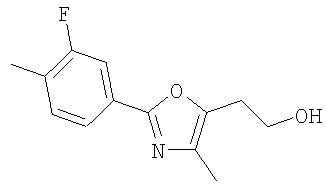
ЭР-МС m/z 236,2 ((МН)+); ВЭЖХ ВУ (мин) 2,46. 1Н ЯМР (CDCl3) δ 7,54 (d, 1 Н), 7,43 (d, 1H), 7,17 (t, 1H), 3,91 (d, 2H), 3,09 (s, 1H), 2,88 (t, 2H), 2,29 (s, 3Н), 2,13 (s, 3H).
Пример 216
Получение 2-{4-метил-2-[4-(трифторметил)-фенил]-1,3-оксазол-5-ил}-этанола

ЭР-МС m/z 272,2 ((МН)+); ВЭЖХ ВУ (мин) 2,71. 1H ЯМР (CDCl3) δ 8,03 (2, 2Н), 7,66 (d, 2H), 3,95 (t, 2Н), 2,96 (t, 2H), 2,21 (s, 3Н), 1,97 (s br, 1H).
Пример 217
Получение этил-[(1S)-5-(2-{4-метил-2-[4-(трифторметил)-фенил]-1,3-оксазол-5-ил}-этокси)-2,3-дигидро-1Н-инден-1-ил]-ацетата
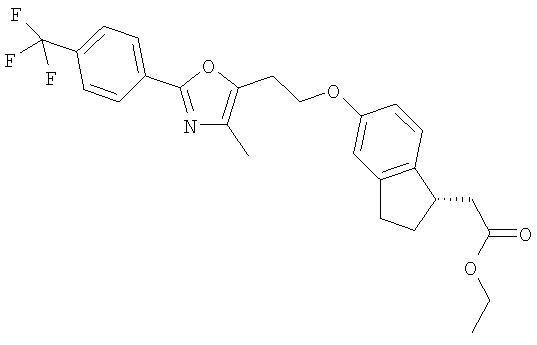
ЭР-МС m/z 474,5 ((МН)+); ВЭЖХ ВУ (мин) 4,10. 1Н ЯМР (ацетон-d6) δ 8,16 (d, 2H), 7,83 (d, 2H), 7,09 (d, 1H), 6,80 (s, 1H), 6,72 (dd, 1H), 4,28 (t, 2H), 4,12 (q, 2H), 3,46-3,41 (m, 1H), 3,21 (t, 2H), 2,86-2,65 (m, 3H), 2,39-2,26 (m, 2H), 2,20 (s, 3Н), 1,75-1,63 (m, 1H), 1,22 (t, 3H).
Пример 218
Получение этил-((1S)-5-{2-[4-метил-2-(4-метилфенил)-1,3-оксазол-5-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-ацетата
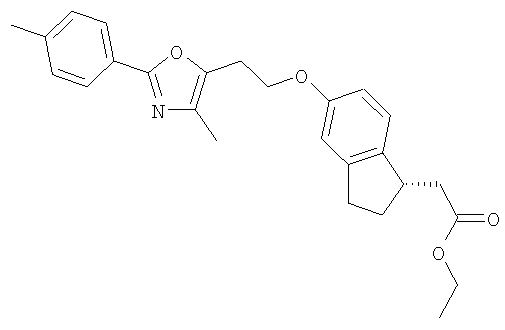
ТСХ Rf=0,22 гексан/EtOAc 4:1.
Пример 219
Получение этил-((1S)-5-{2-[2-(3-фтор-4-метилфенил)-4-метил-1,3-оксазол-5-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-ацетата
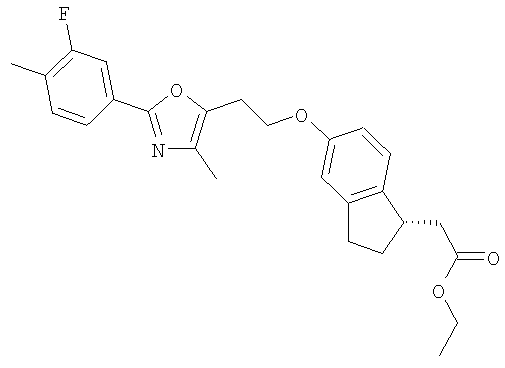
ЭР-МС m/z 438,2 ((МН)+); ВЭЖХ ВУ (мин) 4,18. 1Н ЯМР (ацетон-d6) δ 6,67 (dd, 1H), 7,59 (dd, 1H), 7,37 (t, 1H), 7,08 (d, 1H), 6,80 (s, 1H), 6,72 (dd, 1H), 4,26 (t, 2H), 4,12 (q, 2Н), 3,46-3,38 (m, 1H), 3,17 (t, 2H), 2,89-2,65 (m, 3Н), 2,39-2,23 (m, 5H), 2,17 (s, 3Н), 1,75-1,63 (m, 1H), 1,23 (t, 3H).
Пример 220
Получение ((1S)-5-{2-[4-метил-2-(4-метилфенил-3-оксазол-5-ил]-этокси}-2,3-дигидро-1Н-инден-1-ил)-уксусной кислоты
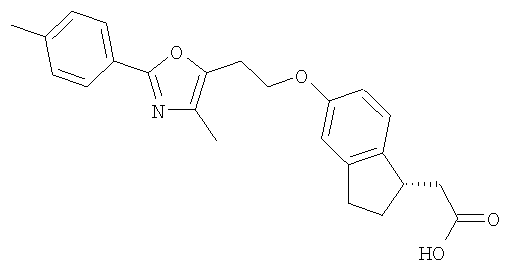
ЭР-МС m/z 392,2 ((МН)+); ВЭЖХ ВУ (мин) 3,36. 1H ЯМР (ацетон-d6) δ 7,72 (d, 2H), 7,15 (d, 2H), 6,99 (d, 1H), 6,67 (s, 1H), 6,59 (dd, 1H), 4,12 (t, 2H), 3,33-3,28 (m, 1H), 3,03 (t, 2H), 2,73-2,54 (m, 3Н), 2,27-2,21 (m, 5H), 2,02 (s, 3Н), 1,64-1,54 (m, 1H).
Пример 221
Получение ((1S)-5-{2-[2-(3-фтор-4-метилфенил)-метил-1,3-оксазол-5-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)уксусной кислоты
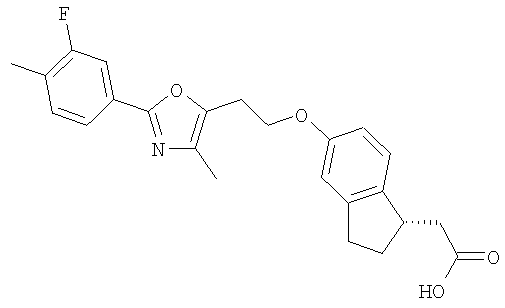
ЭР-МС m/z 410,2 ((МН)+); ВЭЖХ ВУ (мин) 3,49. 1H ЯМР (ацетон-d6) δ 7,68 (dd, 1H), 7,59 (dd, 1H), 7,36 (t, 1H), 7,12 (d, 1H), 6,80 (s, 1H), 6,72 (dd, 1H), 4,26 (t, 2H), 3,47-3,41 (m, 1H), 3,18 (t, 2H), 2,86-2,67 (m, 3H), 2,40-2,28 (m, 5H), 2,17 (s, 3H), 1,18-1,65 (m, 1H).
Пример 222
Получение [(1S)-5-(2-{4-метил-2-[4-(трифторметил)-фенил]-1,3-оксазол-5-ил}-этокси)-2,3-дигидро-1H-инден-1-ил]уксусной кислоты
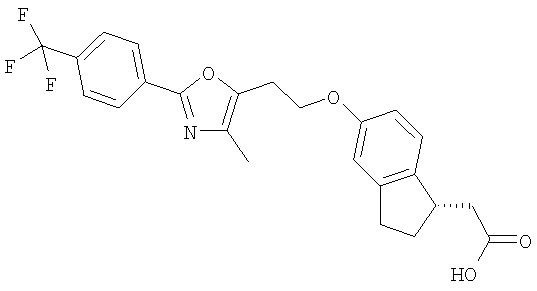
ЭР-МС m/z 446,5 ((МН)+); ВЭЖХ ВУ (мин) 3,47. 1H ЯМР (ацетон-d6) δ 8,17 (d, 2H), 7,84 (d, 2H), 7,13 (s, 1H), 6,80 (s, 1H), 6,72 (dd, 1H), 4,28 (t, 2H), 3,46-3,41 (m, 1H), 3,21 (t, 2H), 2,86-2,67 (m, 3H), 2,40-2,28 (m, 2H), 2,20 (s, 3H), 1,77-1,67 (m, 1H).
Пример 223
Получение (2S)-2{(1S)-5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил)-пропановой кислоты и (2R)-2-{(1H)-5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1H-инден-1-ил}-пропановой кислоты
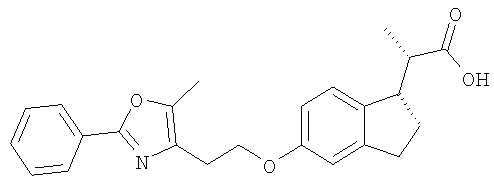 и
и 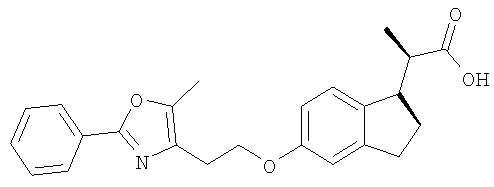
Стадия 1. Получение (2S)-2-[(1S)-5-метокси-2,3-дигидро-1Н-инден-1-ил]-пропановой кислоты и (2R)-2-[(1R)-5-метокси-2,3-дигидро-1Н-инден-1-ил]пропановой кислоты
 и
и 
Исходную кислоту (Пример 2b) вводят в реакцию по методике, аналогичной описанной в Примере 4, при давлении Н2, равном 60 фунт-сила/дюйм2, и с использованием 4,5 г исходного вещества, 1,04 г катализатора и 4,5 мл триэтиламина в 45 мл этанола и 5 мл THF. Стандартная методика экстракции дает 3,22 г продукта. Время удерживания ЖХ/МС равно 2,41 мин, ЯМР (DMCO-d6): 0,87 (d, 3H, α-метил), 1,75 (m, 1H), 2,04 (m, 1H), 3,66 (s, 3H, метоксил), 6,65 (m, 1H, арил), 6,76 (s, 1H, арил), 7,04 (d, 1H, арил), 12,18 (bs, 1H, кислота.)
Стадия 2. Получение метил-(2S)-2-[(1S)-5-метокси-2,3-дигидро-1Н-инден-1-ил]-пропаноата и метил-(2R)-2-[(1R)-5-метокси-2,3-дигидро-1Н-инден-1-ил]-пропаноата
 и
и 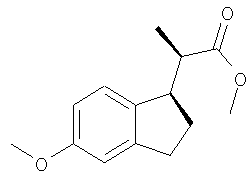
Соединение получают по реакции из 1,5 г исходной кислоты, 0,93 мл йодметана и 1,75 г бикарбоната натрия в 10 мл метанола при стандартных условиях этерификации, описанных в Примере 6. Обработка дает 1,53 г, 96%. (ЯМР (CD2Cl2): 1,05 (d, 3H, α-метил), 1,88 (m, 1H), 2,19 (m, 1H), 3,44 (m, 1H), 3,68 (s, 3H, метоксил), 3,77 (s, 3H, сложный эфир).
Стадия 3. Получение: метил-(2S)-2-[(1S)-5-гидрокси-2,3-дигидро-1Н-инден-1-ил]-пропаноата и метил-(2R)-2-[(1R)-5-гидрокси-2,3-дигидро-1Н-инден-1-ил]-пропаноата
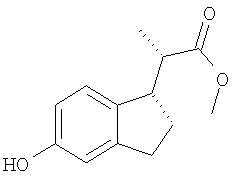 и
и 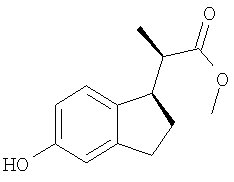
В условиях деметилирования, описанных в Примере 7 (1,53 г исходного вещества, 4,35 г AlCl3 и 2,4 мл этантриола в 20 мл дихлорметана), получают 1,21 г продукта (84%). (ЯМР (CD2Cl2): 1,05 (d, 3Н, α-метил), 1,88 (m, 1Н), 2,18 (m, 1Н), 3,45 (m, 1H), 3,67 (s, 3Н, сложный эфир), 6,60 (m, 1H, арил), 6,69 (s, 1H, арил), 6,93 (d, 1H, арил).
Стадия 4: Получение метил-(2S)-2-{(1S)-5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}-пропаноата и метил-(2R)-2-[(1R)-[5-метил-2-фенил-1,3-оксазол-4-ил-этокси]-2,3-дигидро-1Н-инден-1-ил]-пропаноата
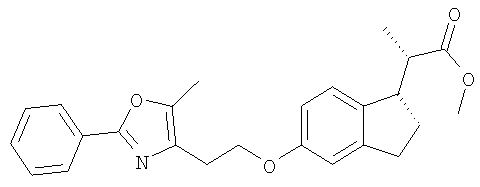 и
и 
С помощью стандартной методики сочетания Мицунобу, описанной в Примере 11 (0,100 г исходного фенола, 0,110 г оксазолилэтанола, 0,143 г трифенилфосфина и 0,137 г ADDP в 2 мл дихлорметана), после хроматографии в 15% EtOAc/гексан получают 0,107 г (58%) продукта. ЯМР (CD2Cl2): 1,62-1,87 (m, 4H), 2,40 (s, 3Н, метильная группа оксазола), 2,98 (t, 2H, метилен), 3,23 (m, 1H), 3,63 (s, 3Н, сложный эфир), 6,60 (s, 1H, арил), 6,64 (m, 1H, арил), 7,42 (m, 3Н, арил), 8,00 (m, 2H, арил).
Стадия 5. (2S)-2-{(1S)-5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}-пропановая кислота и (2R)-2-{(1R)-5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1Н-инден-1-ил}пропановая кислота
 и
и 
Для 0,090 г исходного сложного эфира используют условия гидролиза с помощью LiOH и получают 0,082 г (95%) продукта. ЯМР (CD3OD): 0,4-0,75 (m, 4H), 1,18 (s, 3Н), 1,75 (t, 2H, метилен), 2,00 (m, 1H), 2,99 (t, 2H, метилен), 5,39 (s, 1H, арил), 5,48 (m, 1H, арил), 5,83 (d, 1H, арил), 6,27 (m, 3Н, арил), 6,76 (m, 2H, арил).
С использованием методик, описанных выше, и подходящих исходных веществ дополнительные (2S,1S) и (2R,1R) соединения получают аналогичным образом в виде смесей диастереоизомеров (т.е. син-{(2S,1S)/(2R,1R)} и или анти-{(2S,1S)/(2S,1R)}) смесей или в виде индивидуальных энантиомеров. Эти соединения приведены в таблице 5.
Таблица 5
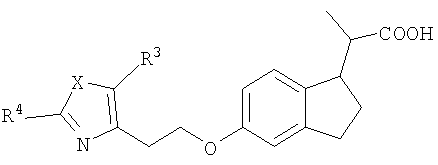
Пример 248
Получение этил-[(1S)-5-(2-{2-[4'-(5-ацетил-2-тиенил)-1.1'-бифенил-4-ил]-5-метил-1,3-оксазол-4-ил}-этокси)-2,3-дигидро-1Н-инден-1-ил]-ацетата
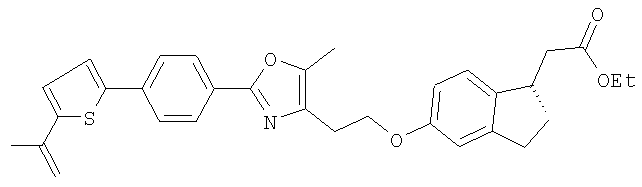
К раствору, содержащему этил-((1S)-5-{2-[2-(4-бромфенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1Н-инден-1-ил)-ацетат (0,100 г, 0,21 ммоль) [полученному из 2-[5-метил-2-(4-бромфенил)-1,3-оксазол-4-ил]-этанола и этил-[(1S)-5-гидрокси-2,3-дигидро-1Н-инден-1-ил]-ацетата (Пример 135)], 1,1'-бис(дифенилфосфино)-ферроцен]-дихлорпалладий(II) (16,9 мг, 0,02 ммоль) и 5-ацетил-2-тиенилбороновую кислоту (0,062 г, 0,41 ммоль) в дегазированных толуоле и диоксане (4:1, 2 мл), прибавляют 2 М водный раствор карбоната натрия (0,5 мл). Смесь нагревают при 85°С в течение 16 ч. Растворители выпаривают в вакууме и остаток растворяют в метаноле и ацетонитриле и фильтруют через экстракционный катридж с обращенной фазой С8. Растворители выпаривают и остаток растворяют в ацетонитриле и очищают с помощью ВЭЖХ, получая этил-[(1S)-5-(2-{2-[4'-(5-ацетил-2-тиенил)-1,1'-бифенил-4-ил]-5-метил-1,3-оксазол-4-ил}-этокси)-2,3-дигидро-1Н-инден-1-ил]-ацетат с выходом 46% (50 мг, 0,09 ммоль) МС (электрораспыление) 530,4 (М+Н)+, 1Н ЯМР (CDCl3) δ 1,24 (t, 3Н), 1,71 (m, 1H), 2,37 (m, 5Н), 2,57 (s, 3H), 2,68 (m, 1H), 2,83 (m, 2H), 3,03 (m, 2Н), 3,48 (m, 1H), 4,17 (m, 4H), 6,67 (m, 2H), 7,02 (d, 1H), 7,39 (d, 1H), 7,67 (d, 1H), 7,73 (d, 2H), 8,01 (d, 2H).
Другие соединения, полученные с использованием аналогичных исходных веществ и методики, описанной в Примере 248, в сочетании с гидролизом, описанным в Примере 11, приведены ниже в таблице 6.
Таблица 6.

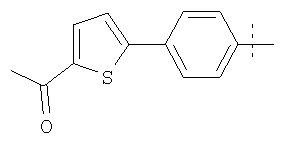
ОЦЕНКА СОЕДИНЕНИЙ
Продемонстрировать активность соединений, соответствующих настоящему изобретению можно с помощью исследований, выполняющихся in vitro, ex vivo и in vivo, хорошо известных в данной области техники. Например, чтобы продемонстрировать эффективность фармацевтического препарата для лечения диабета и родственных заболеваний, таких как синдром X, нарушение переносимости глюкозы, нарушение уровня глюкозы в крови натощак и гиперинсулинемия или атеросклеротическое заболевание и родственные заболевания, такие как гипертриглицеридемия и гиперхолестеринемия, можно выполнить следующие исследования.
Связывание инсулина рецепторами в клетках 3T3-L1, обработанных соединениями
Клетки 3T3-L1 высевают по 9300 клеток в лунку в планшеты Costar TC с плоским дном и инкубируют в течение 1 недели, прекращая инкубацию через 2 суток после слияния (например, когда клетки достигнут максимальной плотности). Затем клетки в течение 2 суток обрабатывают дифференцирующей средой (средой Игла, модифицированной по способу Дульбекко (DMEM),100 мкг/мл пенициллина/стрептомицина, 2 ммоль L-глутамина, 10% фетальной бычьей сыворотки), содержащей 0,5 мкмоль инсулиноподобного фактора роста человека (IGF-1) и исследуемые соединения. После обработки среда заменяется дифференцирующей средой и клетки инкубируют в течение 4 суток. Затем анализируют активность рецептора инсулина. После промывки клеток буферным раствором их инкубируют с помощью 0,1 нмоль 125|-инсулина и (+/-) 100 нмоль немеченого инсулина и инкубацию проводят при комнатной температуре в течение 1 ч. Затем клетки трижды промывают буферным раствором, растворяют в 1 н. NaOH и проводят подсчет с помощью счетчика гамма-излучения. Если достигнуто плато, то определяют значение ЕС50 и оценивают максимальную стимуляцию в процентах.
Анализы In Vivo
Методика измерения концентраций глюкозы в крови
У мышей db/db (полученных из Jackson Laboratories, Bar Harbor, ME) берут кровь (из глазной или хвостовой вены) и их разделяют на группы в соответствии с эквивалентными средними концентрациями глюкозы в крови. В течение 14 дней один раз в день им перорально вводят (путем принудительного кормления в фармацевтически приемлемом растворителе) исследуемое соединение. Затем у животных повторно берут кровь из глазной или хвостовой вены и с помощью сахариметра Glucometer Elite XL (Bayer Corporation, Elkhart, IN) определяют концентрации глюкозы.
Методика измерения концентраций триглицеридов
У мышей hApoA1 (полученных из Jackson Laboratories, Bar Harbor, ME) берут кровь (из глазной или хвостовой вены) и их разделяют на группы в соответствии с эквивалентными средними концентрациями триглицеридов в сыворотке. В течение 8 дней один раз в день им перорально вводят (путем принудительного кормления в фармацевтически приемлемом растворителе) исследуемое соединение. Затем у животных повторно берут кровь из глазной или хвостовой вены и определяют концентрации триглицеридов в сыворотке. Во всех случаях концентрации триглицеридов определяют с помощью прибора Technicon Axon Autoanalyzer (Bayer Corporation, Tarrytown, NY).
Методика измерения концентраций ЛВП-холестерина
Для определения концентраций ЛВП-холестерина в плазме у мышей hApoA1 берут кровь и их разделяют на группы в соответствии с эквивалентными средними концентрациями ЛВП-холестерина в плазме. В течение 7 дней один раз в день мышам перорально вводят растворитель или исследуемое соединение. Концентрации ЛВП-холестерина в плазме определяют с помощью прибора Synchron Clinical System (CX4) (Beckman Coulter, Fullerton, CA)
Методика измерения концентраций общего холестерина, ЛВП-холестерина, триглицеридов и глюкозы
В другом исследовании in vivo у страдающих ожирением обезьян берут кровь, а затем в течение 4 недель один раз в день им перорально вводят растворитель или исследуемое соединение и затем повторно берут кровь. В сыворотке определяют концентрации общего холестерина, ЛВП-холестерина, триглицеридов и глюкозы с использованием прибора Synchron Clinical System (CX4) (Beckman Coulter, Fullerton, CA). Анализ подклассов липопротеинов проводят с помощью спектроскопии ЯМР в соответствии с описанием в работе Oliver et al. (Proc. Natl. Acad. Sci. USA 98:5306-5311,2001).
Методика изучения влияния на сердечно-сосудистые параметры
Также определяют сердечно-сосудистые параметры (например, частоту сердечных сокращений и артериальное давление). Крысам SHR в течение 2 недель один раз в день перорально вводят растворитель или исследуемое соединение. Артериальное давление и частоту сердечных сокращений определяют с помощью методики манжеты для хвоста в соответствии с описанием в работе Grinsell et al. (Am. J. Hypertens. 13:370-375, 2000). У обезьян артериальное давление и частоту сердечных сокращений определяют в соответствии с описанием в работе Shen et al. (J. Pharmacol. Exp. Therap. 278:1435-1443, 1996).
Соединения, соответствующие настоящему изобретению, исследованы с помощью указанных выше способов анализа и по данным профилей активности обнаружено, что они оказывают влияние на уровень глюкозы в крови и уровень триглицеридов в сыворотке и поэтому они обладают потенциальной применимостью для лечения диабета и родственных заболеваний, таких как синдром X, нарушение переносимости глюкозы, нарушение уровня глюкозы в крови натощак и гиперинсулинемия, или сердечно-сосудистых заболеваний и родственных заболеваний, таких как гипертриглицеридемия и гиперхолестеринемия.
Фармацевтические композиции
На основании указанных выше тестов или других известных методик анализа, использующихся для определения эффективности лечения указанных выше патологических состояний млекопитающих, и путем сопоставления этих результатов с результатами для известных лекарственных препаратов, которые используются для лечения этих патологических состояний, можно легко определить эффективную дозировку соединений, соответствующих настоящему изобретению, для лечения в каждом необходимом случае. Количество активного компонента, которое следует вводить при лечении одного из этих патологических состояний, может значительно меняться в зависимости от таких факторов, как конкретное использующееся соединение и разовая доза, способ введения, продолжительность лечения, возраст и пол подвергающегося лечению пациента и природа и тяжесть подвергающегося лечению патологического состояния.
Полное количество подлежащего введению активного компонента обычно может меняться от около 0,0001 до около 200 мг/кг, а предпочтительно - от около 0,01 до около 200 мг/(кг массы тела)/сутки. Разовая доза может содержать от около 0,05 до около 1500 мг активного компонента и может вводиться один или большее количество раз в сутки. Суточная доза для введения путем инъекции, включая внутривенную, внутримышечную, подкожную и парентеральную инъекции, и при использовании методики вливания может составлять от около 0,01 до около 200 мг/(кг полной массы тела)/сутки. Чрескожная концентрация может быть такой, для которой требуется поддержание суточной дозы, составляющей от 0,01 до 200 мг/кг.
Разумеется, для каждого пациента конкретный начальный и продолжающийся дозировочный режим будет меняться в соответствии с природой и тяжестью патологического состояния, определяемого лечащим врачом, ставящим диагноз, времени введения, пути введения, скорости выведения лекарственного препарата, комбинаций лекарственных препаратов и т.п. Предпочтительный режим лечения и количество доз соединения, соответствующего настоящему изобретению, или его фармацевтически приемлемой соли могут быть определены специалистами в данной области техники с использованием обычных тестов по лечению.
Соединения, соответствующие настоящему изобретению, можно использовать для достижения необходимого фармакологического эффекта путем введения нуждающемуся в нем пациенту соответствующим образом составленной фармацевтической композиции. Для задач настоящего изобретения пациентом является млекопитающее, включая человека, нуждающееся в лечении конкретного патологического состояния или заболевания. Поэтому настоящее изобретение включает фармацевтические композиции, которые содержат фармацевтически приемлемый носитель и фармацевтически эффективное количество соединения, идентифицированного способами, описанными в настоящем изобретении, или его фармацевтически приемлемой соли или сложного эфира. Фармацевтически приемлемый носитель представляет собой любой носитель, который является относительно нетоксичным и безвредным для пациента при концентрациях, согласующихся с эффективной активностью активного компонента, так чтобы любые побочные эффекты, приписываемые носителю, не ослабляли полезные воздействия активного компонента. Фармацевтически эффективное количество соединения представляет собой такое количество, которое приводит к результату или оказывает воздействие на конкретное патологическое состояние, подвергающееся лечению. Соединения, идентифицированные способами, описанными в настоящем изобретении, могут вводиться совместно с фармацевтически приемлемым носителем с использованием любых эффективных стандартных разовых дозированных форм, включая, например, препараты немедленного или замедленного выделения, пероральные, парентеральные, местные и т.п.
Для перорального введения соединения можно включить в твердые или жидкие препараты, такие как, например, капсулы, пилюли, таблетки, пастилки, лепешки, плавкие препараты, порошки, растворы, суспензии или эмульсии и их можно приготовить в соответствии со способами, известными в области приготовления фармацевтических композиций. Твердые разовые дозировочные формы могут представлять собой капсулу, которая может являться обычной капсулой из твердого или мягкого желатина, содержащей, например, поверхностно-активные вещества, смазки и инертные наполнители, такие как лактоза, сахароза, фосфат кальция и кукурузный крахмал.
В другом варианте осуществления соединения, соответствующие настоящему изобретению, можно сформовать в таблетки с помощью обычных основ для таблеток, таких как лактоза, сахароза и кукурузный крахмал, в комбинации со связующими, такими как камедь акации, кукурузный крахмал или желатин; веществами, обеспечивающими распадаемость, предназначенными для содействия разрушению и растворению таблетки после введения, такими как картофельный крахмал, альгиновая кислота, кукурузный крахмал и гуаровая камедь; смазками, предназначенными для улучшения сыпучести таблеток и для предотвращения прилипания материала таблеток к поверхности матриц и пуансонов для формования таблеток, например талька, стеариновой кислоты или стеарата магния, кальция или цинка; красителями, окрашивающими веществами и вкусовыми добавками, предназначенными для улучшения эстетических характеристик таблеток и для того, чтобы сделать их более приемлемыми для пациента. Подходящие наполнители, предназначенные для использования в жидких пероральных дозировочных формах, включают разбавители, такие как вода и спирты, например, этанол, бензиловый спирт и полиэтиленовые спирты с прибавлением или без прибавления фармацевтически приемлемого поверхностно-активного вещества, суспендирующего реагента или эмульгирующего реагента. Различные другие вещества могут содержаться в качестве покрытий или средств для иного изменения физических характеристик дозировочной формы. Например, таблетки, пилюли или капсулы могут быть покрыты шеллаком, сахаром или обоими этими веществами.
Диспергируемые порошки и гранулы пригодны для приготовления водных суспензий. Они содержат активный компонент в смеси с диспергирующим или смачивающим веществом, суспендирующим веществом и одним или большим количеством консервантов. Примерами подходящих диспергирующих или смачивающих веществ являются вещества, уже указанные выше. Также могут содержаться дополнительные наполнители, например, подсластители, вкусовые добавки и окрашивающие вещества, описанные выше.
Фармацевтические композиции, соответствующие настоящему изобретению, также могут находиться в форме эмульсий масло-в-воде. Масляной фазой может быть растительное масло, такое как жидкий парафин или смесь растительных масел. Подходящими эмульгирующими веществами могут быть (1) природные камеди, такие как камедь акации и трагакантовая камедь, (2) природные фосфатиды, такие как соя и лецитин, (3) сложные эфиры или частичные сложные эфиры, полученные из жидких кислот и ангидридов гексита, например сорбитанмоноолеат, и (4) продукты конденсации указанных частичных сложных эфиров с этиленоксидом, например полиоксиэтиленсорбитанмоноолеат. Эмульсии могут содержать подсластители и вкусовые добавки.
Масляные суспензии можно получить путем суспендирования активного вещества в растительном масле, таком как, например, арахисовое масло, оливковое масло, кунжутное масло или кокосовое масло, или в минеральном масле, таком как жидкий парафин. Масляные суспензии могут содержать загущающее вещество, такое как, например, пчелиный воск, твердый парафин или цетиловый спирт. Суспензии также могут содержать один или большее количество консервантов, например, этил- или н-пропил-п-гидроксибензоат; одно или большее количество окрашивающих веществ; одну или большее количество вкусовых добавок и один или большее количество подсластителей, таких как сахароза или сахарин.
Сиропы и эликсиры могут быть составлены с включением подсластителей, таких как, например, глицерин, пропиленгликоль, сорбит или сахароза. Такие композиции также могут содержать средство, устраняющее раздражение, и консервант, вкусовые добавки и окрашивающие вещества.
Соединения, соответствующие настоящему изобретению, также можно вводить парентерально, т.е. подкожно, внутривенно, внутримышечно или внутрибрюшинно в виде вводимых путем инъекции доз соединения в физиологически приемлемом разбавителе с фармацевтическим носителем, которые могут представлять собой стерильную жидкость или смесь жидкостей, таких как вода, физиологический раствор, водный раствор декстрозы и растворы аналогичных сахаров; спирт, такой как этанол, изопропанол или гексадециловый спирт, гликоли, такие как пропиленгликоль и полиэтиленгликоль; кетали глицерина, такие как 2,2-диметил-1,1-диоксолан-4-метанол, простые эфиры, такие как полиэтиленгликоль 400; масло; жирную кислоту, сложный эфир или глицерид жирной кислоты или ацетилированный глицерид жирной кислоты, с прибавлением или без прибавления фармацевтически приемлемого поверхностно-активного вещества, такого как мыло или моющее средство, суспендирующего вещества, такого как пектин, карбомеры, метилцеллюлоза, гидроксипропилметилцеллюлоза или карбоксиметилцеллюлоза, или эмульгирующее вещество и другие вспомогательные фармацевтические вещества.
Примерами масел, которые можно использовать в парентеральных композициях, соответствующих настоящему изобретению, являются масла нефтяного, животного, растительного или синтетического происхождения, например, арахисовое масло, соевое масло, кунжутное масло, хлопковое масло, кукурузное масло, оливковое масло, вазелин и минеральное масло. Подходящие жирные кислоты включают олеиновую кислоту, стеариновую кислоту и изостеариновую кислоту. Подходящими сложными эфирами жирных кислот являются, например, этилолеат и изопропилмиристат. Подходящие мыла включают соли щелочных металлов, аммония и триэтаноламина жирных кислот и подходящие моющие средства включают катионогенные моющие средства, например, диметилдиалкиламмонийгалогениды, алкилпиридинийгалогениды и алкиламинацетаты; анионогенные моющие средства, например, алкил-, арил- и олефинсульфонаты, алкил-, олефин- и эфир- и моноглицеридсульфаты и сульфосукцинаты; неионогенные моющие средства, например, жирные аминоксиды, алканоламиды жирных кислот и сополимеры полиоксиэтиленполипропилена; и амфотерные моющие средства, например, алкил-бета-аминопропионаты и четвертичные аммониевые соли 2-алкилимидазолина, а также смеси.
Парентеральные композиции, соответствующие настоящему изобретению, могут содержать в растворе от около 0,5 до около 25 мас.% активного компонента. С успехом также можно использовать консерванты и буферные растворы. Для сведения к минимуму или исключения раздражения на месте инъекции такие композиции могут содержать неионогенные поверхностно-активные вещества, обладающие показателем гидрофильно-липофильного баланса (ГЛБ), равным от около 12 до около 17. Количество поверхностно-активного вещества, содержащегося в такой композиции, составляет от около 5 до около 15 мас.%. Поверхностно-активное вещество может быть однокомпонентым, обладающим указанным выше показателем ГЛБ, или может являться смесью двух или большего количества компонентов, обладающей необходимым показателем ГЛБ.
Иллюстративными примерами поверхностно-активных веществ, использующихся в парентеральных композициях, является класс полиэтиленсорбитановых сложных эфиров жирных кислот, например, сорбитанмоноолеат и высокомолекулярные продукты присоединения этиленоксида к гидрофобному основанию, получающиеся путем конденсации пропиленоксида с пропиленгликолем.
Фармацевтические композиции могут находиться в форме стерильных водных суспензий для инъекции. Такие суспензии можно составить в соответствии с известными способами с использованием подходящих диспергирующих или смачивающих веществ и суспендирующих веществ, таких как, например, натриевая соль карбоксиметилцеллюлозы, метилцеллюлоза, гидроксипропилметилцеллюлоза, альгинат натрия, поливинилпирролидон, трагакантовая камедь и камедь акации, диспергирующих или смачивающих веществ, которыми могут являться натуральные фосфатиды, такие как лецитин, продукт конденсации этиленоксида с жирной кислотой, например, полиоксиэтиленстеарат, продукт конденсации этиленоксида с алифатическим спиртом, обладающим длинной цепью, например, гептадекаэтиленоксицетанол, продукт конденсации этиленоксида с частичными сложными эфирами, полученными из жирных кислот и ангидрида гексита, например, полиоксиэтиленсорбитанмоноолеат.
Стерильный препарат для инъекции также может представлять собой стерильный раствор или суспензию для инъекции в нетоксичном приемлемом для парентерального введения разбавителе или растворителе. Разбавителями и растворителями, которые можно использовать, являются, например, вода, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, в качестве растворителей или суспендирующих средств обычно используют стерильные нелетучие масла. Для этой цели можно использовать любое смешанное нелетучее масло, включая синтетические моно- и диглицериды. Кроме того, при изготовлении препаратов для инъекций можно использовать жирные кислоты, такие как олеиновую кислоту.
Композицию, соответствующую настоящему изобретению, также можно вводить в форме суппозиториев для ректального введения лекарственного препарата. Эти композиции можно приготовить путем смешивания лекарственного препарата с подходящим не оказывающим раздражающего воздействия наполнителем, который является твердым при обычных температурах, но жидким при температуре в прямой кишке и поэтому будет плавиться в прямой кишке с высвобождением лекарственного препарата. Такими веществами являются, например масло какао и полиэтиленгликоль.
Для другой композиции, использующейся в способах, соответствующих настоящему изобретению, применяются чрескожные устройства доставки (пластыри). Такие чрескожные пластыри можно использовать для обеспечения непрерывной или прерывистой инфузии соединений, соответствующих настоящему изобретению, осуществляющейся регулируемым образом. Устройство и применение чрескожных пластырей для доставки фармацевтических препаратов хорошо известно в данной области техники (см., например, патент США №5023252, который включен в настоящее изобретение для ссылки). Такие пластыри можно изготовить для непрерывной, периодической или осуществляющейся при необходимости доставки фармацевтических препаратов.
Может быть желательно или необходимо вводить пациенту фармацевтическую композицию с помощью механического подающего устройства. Конструкция и применение механических подающих устройств для доставки фармацевтических препаратов хорошо известна в данной области техники. Например, прямые методики введения лекарственного препарата непосредственно в головной мозг обычно включают введение подающего лекарственный препарат катетера в желудочковую систему пациента, чтобы обойти гематоэнцефалический барьер. Одна такая имплантируемая подающая система, использующаяся для подачи препаратов в конкретные анатомические области организма, описана в патенте США №5011472, который включен в настоящее изобретение для ссылки.
Композиции, соответствующие настоящему изобретению, при необходимости или желании также могут содержать другие фармацевтически приемлемые предназначенные для смешивания компоненты, обычно называемые носителями или разбавителями. Любые композиции, соответствующие настоящему изобретению, можно сохранять путем прибавления антиоксидантов, таких как аскорбиновая кислота, или с помощью других подходящих консервантов. Можно использовать обычные методики приготовления таких композиций в соответствующих дозировочных формах.
Обычно использующиеся фармацевтические компоненты, которые можно применять в качестве подходящих для составления композиций, предназначенных для конкретного пути введения, включают: подкисляющие вещества, например (без наложения ограничений), уксусную кислоту, лимонную кислоту, фумаровую кислоту, хлористоводородную кислоту, азотную кислоту; и подщелачивающие вещества, такие как (без наложения ограничений), раствор аммиака, карбонат аммония, диэтаноламин, моноэтаноламин, гидроксид калия, борат натрия, карбонат натрия, гидроксид натрия, триэтаноламин, троламин.
Другие фармацевтические компоненты включают, например (без наложения ограничений), адсорбенты (например, порошкообразную целлюлозу и активированный уголь); пропелленты для аэрозолей (например, диоксид углерода, CCl2F2, F2ClC-CClF2 и CClF2); замещающие воздух вещества (например, азот и аргон); противогрибковые консерванты (например, бензойную кислоту, бутилпарабен, этилпарабен, метилпарабен, пропилпарабен, бензоат натрия); противомикробные консерванты (например, бензалконийхлорид, бензетонийхлорид, бензиловый спирт, цетилпиридинийхлорид, хлорбутанол, фенол, фенетиловый спирт, фенилмеркурнитрат и тимеросал); антиоксиданты (например, аскорбиновую кислоту, аскорбилпальмитат, бутилированный гидроксианизол, бутилированный гидрокситолуол, гипофосфорную кислоту, монотиоглицерин, пропилгаллат, аскорбат натрия, бисульфит натрия, формальдегидсульфоксилат натрия, метабисульфит натрия); связующие вещества (например, блок-полимеры, натуральный и синтетические каучуки, полиакрилаты, полиуретаны, силиконы и стирол-бутадиеновые сополимеры); буферные вещества (например, метафосфат калия, однозамещенный фосфат калия, ацетат натрия, безводный цитрат натрия и дигидрат цитрата натрия); вещества-носители (например, сироп камеди акации, ароматический сироп, ароматический эликсир, вишневый сироп, сироп какао, апельсиновый сироп, сироп, кукурузное масло, минеральное масло, арахисовое масло, кунжутное масло, бактериостатический хлорид натрия для инъекций и бактериостатическую воду для инъекций); хелатные реагенты (например, динатриевую соль этилендиаминтетрауксусной кислоты и этилендиаминтетрауксусную кислоту); красители (например, FD&C Red №3, FD&C Red №20, FD&C Yellow №6, FD&C Blue №2, D&C Green №5, D&C Orange №5, D&C Red №8, жженый сахар и красный оксид железа(III)); осветляющие вещества (например, бентонит); эмульгирующие вещества (без наложения ограничений - камедь акации, цетомакрогол, цетиловый спирт, глицерилмоностеарат, лецитин, сорбитан-моноолеат, полиэтилен 50 стеарат); капсулирующие вещества (например, желатин и ацетилфталатцеллюлозу); вкусовые добавки (например, анисовое масло, коричное масло, какао, ментол, апельсиновое масло, мятное масло и ванилин), влагоудерживающие вещества (например, глицерин, пропиленгликоль и сорбит); отмучивающие вещества (например, минеральное масло и глицерин), масла (например, арахисовое масло, минеральное масло, оливковое масло, арахисовое масло, кунжутное масло и растительное масло); основы для мазей (например, ланолин, гидрофильная мазь, полиэтиленгликолевая мазь, вазелин, гидрофильный вазелин, белая мазь, желтая мазь и мазь с розовой водой); вещества, увеличивающие проницаемость (чрескожную подачу) (например, моногидрокси- или полигидроксиспирты, насыщенные или ненасыщенные жирные спирты, сложные эфиры насыщенных или ненасыщенных жирных кислот, насыщенные или ненасыщенные дикарбоновые кислоты, эфирные масла, фосфатидильные производные, цефалин, терпены, амиды, простые эфиры, кетоны и мочевины); пластификаторы (например, диэтилфталат и глицерин); растворители (например, спирт, кукурузное масло, хлопковое масло, глицерин, изопропиловый спирт, минеральное масло, олеиновую кислоту, арахисовое масло, очищенную воду, воду для инъекций, стерильную воду для инъекций и стерильную воду для промывания); загустители (например, цетиловый спирт, цетилэфирный воск, микрокристаллический воск, парафин, стеариловый спирт, белый воск и желтый воск); основы для суппозиториев (например, масло какао и полиэтиленгликоли (смеси)); поверхностно-активные вещества (например, бензалконий-хлорид, ноноксинол 10, окстоксинол 19, полисорбат 80, лаурилсульфат натрия и сорбитанмонопальмитат); суспендирующие вещества (например, агар, бентонит, карбомеры, натриевую соль карбоксиметилцеллюлозы, гидроксиэтилцеллюлозу, гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу, каолин, метилцеллюлозу, трагакантовую камедь и вигум); подсластители (например, аспартам, декстрозу, глицерин, маннит, пропиленгликоль, натриевую соль сахарина, сорбит и сахарозу), вещества, препятствующие слипанию таблеток (например, стеарат магния и тальк); связующие для таблеток (например, камедь акации, альгиновую кислоту, натриевую соль карбоксиметилцеллюлозы, прессующийся сахар, этилцеллюлозу, желатин, жидкую глюкозу, метил целлюлозу, повидон и предварительно желатинизированный крахмал); разбавители для таблеток и капсул (например, двузамещенный фосфат кальция, каолин, лактозу, маннит, микрокристаллическую целлюлозу, порошкообразную целлюлозу, осажденный карбонат кальция, карбонат натрия, фосфат натрия, сорбит и крахмал); вещества для образования покрытий на таблетках (например, жидкую глюкозу, гидроксиэтилцеллюлозу, гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу, метилцеллюлозу, этилцеллюлозу, ацетилфталатцеллюлозу и шеллак); наполнители для прямого прессования таблеток (например, двузамещенный фосфат кальция); вещества, обеспечивающие распадаемость таблеток (например, альгиновую кислоту, кальциевую соль карбоксиметилцеллюлозы, микрокристаллическую целлюлозу, кальциевую соль полакриллина, альгинат натрия, натриевую соль гликолята крахмала и крахмал); вещества, придающие таблеткам скользкость (например, коллоидный диоксид кремния, кукурузный крахмал и тальк); смазывающие вещества для таблеток (например, стеарат кальция, стеарат магния, минеральное масло, стеариновую кислоту и стеарат цинка); вещества, придающие таблеткам/капсулам непрозрачность (например, диоксид титана);
вещества, полирующие таблетки (например, карнаубский воск и белый воск); загу-щающие вещества (например, пчелиный воск, цетиловый спирт и парафин); тонизирующие вещества (например, декстрозу и хлорид натрия); вещества, повышающие вязкость (например, альгиновую кислоту, бентонит, карбомеры, натриевую соль карбоксиметилцеллюлозы, метилцеллюлозу, повидон, альгинат натрия и трагакантовую камедь); и смачивающие вещества (например, гептадекаэтиленоксицетанол, лецитины, полиэтиленсорбитолмоноолеат, полиоксиэтиленсорбитолмоно-олеат и полиоксиэтиленстеарат).
Соединения, идентифицированные способами, описанными в настоящем изобретении, можно вводить в виде одного фармацевтического препарата или в комбинации с одним или большим количеством других фармацевтических препаратов, если эта комбинация не приводит к неприемлемым побочным эффектам. Например, соединения, соответствующие настоящему изобретению, можно комбинировать с известными препаратами против ожирения или с известными противодиабетическими препаратами или другими показанными препаратами и т.п., а также с их смесями и комбинациями.
Соединения, идентифицированные способами, описанными в настоящем изобретении, также можно использовать в виде чистой основы или в композициях, а также при исследованиях и для диагностики или в качестве аналитических эталонных стандартов и т.п. Поэтому настоящее изобретение включает композиции, которые содержат инертный носитель и эффективное количество соединения, идентифицированного способами, описанными в настоящем изобретении, или его соли или сложного эфира. Инертным носителем является любое вещество, которое не взаимодействует с соединением, носителем которого оно является, и которое для соединения, носителем которого оно является, выступает в качестве удерживающего средства, средства доставки, придания объема, метки, позволяющей проследить за соединением, и т.п. Эффективным количеством соединения является такое количество, которое приводит к результату или оказывает влияние на конкретную проводимую процедуру.
Составы, пригодные для подкожного, внутривенного, внутримышечного и т.п. введения; подходящие фармацевтические носители и методики составления и введения могут быть составлены любым из способов, хорошо известных в данной области техники (см., например, Remington's Pharmaceutical Sciences, Mack Publishing Co., Easton, Pa., 20th edition, 2000).
Приведенные ниже примеры представлены для иллюстрации описанного здесь изобретения, но их не следует рассматривать, в качестве каким-либо образом ограничивающих объем настоящего изобретения.
Состав для капсулы
Состав для капсулы изготавливают из:
Соединение по настоящему изобретению 40 мг
Крахмал 109 мг
Стеарат магния 1 мг
Компоненты смешивают, пропускают через сито с подходящим размером ячеек и помещают в капсулы из твердого желатина.
Состав для таблетки
Таблетку изготавливают из:
Соединение по настоящему изобретению 25 мг
Микрокристаллическая целлюлоза 200 мг
Коллоидный диоксид кремния 10 мг
Стеариновая кислота 5,0 мг
Компоненты смешивают и прессуют в таблетки. Для улучшения вкуса, улучшения внешнего вида и стабильности или замедления всасывания можно нанести подходящие покрытия на водной и неводной основе.
Стерильный раствор для внутривенного введения
Раствор необходимого соединения, соответствующего настоящему изобретению, концентрации 5 мг/мл готовят с использованием стерильной воды для инъекций и при необходимости регулируют значение рН. Для введения раствор разбавляют до концентрации, равной 1-2 мг/мл, с помощью стерильной 5% декстрозы и вводят в виде внутривенного вливания в течение 60 мин.
Суспензия для внутримышечного введения
Готовят следующую суспензию для внутримышечного введения:
Соединение по настоящему изобретению 50 мг/мл
Натриевая соль карбоксиметилцеллюлозы 5 мг/мл
TWEEN 804 мг/мл
Хлорид натрия 9 мг/мл
Бензоловый спирт 9 мг/мл
Эту суспензию вводят внутримышечно.
Капсулы с твердой оболочкой
Большое количество капсул с разовыми дозами готовят путем заполнения каждой стандартной двухкомпонентной капсулы из твердого желатина с помощью 100 мг порошкообразного активного компонента, 150 мг лактозы, 50 мг целлюлозы и 6 мг стеарата магния.
Капсулы из мягкого желатина
Смесь активного компонента с пищевым маслом, таким как соевое масло, хлопковое масло или оливковое масло готовят и с помощью поршневого насоса вводят в расплавленный желатин с получением капсулы из мягкого желатина, содержащей 100 мг активного компонента. Капсулы промывают и высушивают. Для получения смешивающейся с водой смеси лекарственного препарата активный компонент можно растворить в смеси полиэтиленгликоля, глицерина и сорбита.
Таблетки/капсулы непосредственного выделения
Они представляют собой твердые пероральные дозировочные формы, изготавливающиеся с помощью обычных и новых способов. Эти лекарственные формы принимают перорально без воды, и они предназначены для непосредственного растворения и выделения лекарственного препарата. Активный компонент смешан с жидкостью, содержащей компоненты, такие как сахар, желатин, пектин и подсластители. Эти жидкости отверждают с получением твердых таблеток или овальных таблеток с покрытием с использованием методик лиофильной сушки и твердофазной экстракции. Лекарственные препараты можно спрессовать совместно с вязкоупругими и термоупругими сахарами и полимерами или компонентами, применяющимися для изготовления шипучих форм, и получить пористые матрицы, которые предназначены для непосредственного выделения без использования воды.
Специалисту с общей подготовкой в данной области техники должно быть понятно, что без отклонения от сущности и объема описанного здесь изобретения в настоящее изобретение можно внести изменения и модификации.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНДАЗОЛИЛИЗОКСАЗОЛЬНЫЕ ПРОИЗВОДНЫЕ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, ТАКИХ КАК ЗЛОКАЧЕСТВЕННОЕ НОВООБРАЗОВАНИЕ | 2020 |
|
RU2836662C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ИНГИБИРОВАНИЯ ПУТИ JAK | 2011 |
|
RU2672100C2 |
| ПОЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ И СПОСОБЫ ЦЕЛЕНАПРАВЛЕННОЙ ДЕГРАДАЦИИ ПОЛИПЕПТИДОВ БЫСТРО УСКОРЕННОЙ ФИБРОСАРКОМЫ | 2019 |
|
RU2830173C2 |
| СОЕДИНЕНИЯ, ПРИГОДНЫЕ В КАЧЕСТВЕ МОДУЛЯТОРОВ TRPM8 | 2011 |
|
RU2608109C2 |
| 4-(ИМИДАЗО[1,2-а]ПИРИДИН-3-ИЛ)-ПИРИМИДИНОВЫЕ ПРОИЗВОДНЫЕ | 2020 |
|
RU2822388C2 |
| НОВЫЕ СОЕДИНЕНИЯ КОНДЕНСИРОВАННЫХ ГЕТЕРОЦИКЛИЛ-КАРБОНОГИДРАЗОНОИЛДИЦИАНИДОВ И ИХ ПРИМЕНЕНИЕ | 2021 |
|
RU2826002C1 |
| ПРОИЗВОДНЫЕ 2,3-ДИГИДРО-1Н-ИНДЕН-1-ИЛ-2,7-ДИАЗАСПИРО[3.5]НОНАНА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ АНТАГОНИСТОВ ИЛИ ОБРАТНЫХ АГОНИСТОВ ГРЕЛИНОВОГО РЕЦЕПТОРА | 2011 |
|
RU2524341C2 |
| 6,7-ДИГИДРО-5H-ПИРИДО[2,3-C]ПИРИДАЗИНОВЫЕ ПРОИЗВОДНЫЕ И РОДСТВЕННЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ БЕЛКОВ BCLXL И ПРОАПОПТОТИЧЕСКИХ СРЕДСТВ ДЛЯ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ | 2020 |
|
RU2832191C2 |
| 2, 5-ДИОКСОИМИДАЗОЛИДИН-4-ИЛ-МЕТИЛКАРБОНИЛЬНЫЕ СОЕДИНЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ, СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ИХ ПРИМЕНЕНИЕ В ИЗГОТОВЛЕНИИ ЛЕКАРСТВЕННОГО СРЕДСТВА | 2003 |
|
RU2326117C2 |
| ПРОИЗВОДНЫЕ БЕНЗОТИАЗИНОВ, ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛЕКАРСТВ | 2010 |
|
RU2523791C2 |
Изобретение относится к новым соединениям формулы (I) и их фармацевтически приемлемым солям и сложным эфирам. Соединения настоящего изобретения влияют на уровень глюкозы в крови и уровень триглицеридов в сыворотке и могут найти применение для лечения таких заболеваний, как диабет, ожирение, гиперлипидемия и атеросклеротическое заболевание. В общей формуле (I)

Х обозначает О или S; R означает Н или C1-С6 алкил; R1 означает Н, COOR, С3-C8 циклоалкил или C1-С6 алкил, С2-С6 алкенил или C1-С6 алкоксил, каждый из которых может быть незамещенным или содержать заместители; значения радикалов R2, R3, R4, R5, R6 указаны в формуле изобретения. Изобретение также относится к фармкомпозиции на основе соединений общей формулы (I) и к промежуточным продуктам общей формулы (II) и (III), которые используют для получения производных индануксусной кислоты.
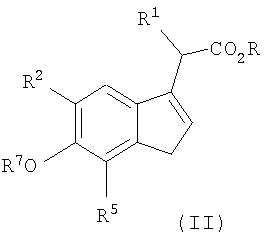
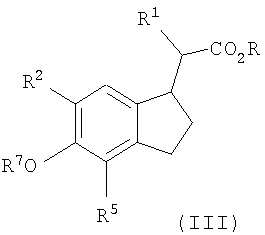
13 н. и 15 з.п. ф-лы, 6 табл.

где R означает Н или C1-С6алкил;
R1 означает Н, COOR, С3-C8 циклоалкил или C1-С6 алкил, С2-С6 алкенил или C1-С6 алкоксил, каждый из которых может быть незамещенным или содержать в качестве заместителей фтор или фенил, который может быть незамещенным или содержать в качестве заместителей R6;
R2 означает Н, галоген или C1-С6 алкил, который может быть незамещенным или содержать в качестве заместителей C1-С6 алкоксил, оксогруппу, фтор, или R2 означает фенил, фурил, тиенил, пиридил, каждый из которых может быть незамещенным или содержать в качестве заместителей R6;
R3 означает Н, C1-С6 алкил или фенил, который может быть незамещенным или содержать в качестве заместителей R6;
Х означает О или S;
R4 означает C1-С6 алкил или С3-C8 циклоалкил, каждый из которых может быть незамещенным или содержать в качестве заместителей фтор, оксогруппу или C1-С6 алкоксил, который может быть незамещенным или содержать в качестве заместителей C1-С6 алкоксил или фенил, необязательно содержащий в качестве заместителя R6, или
C1-С6 алкил также может содержать в качестве заместителя С3-C8 циклоалкил или феноксил, который может быть незамещенным или содержать в качестве заместителей R6 или фенил, который может быть незамещенным или содержать в качестве заместителей R6, или
R4 означает фенил, нафтил, фурил, тиенил, оксазолил, тиазолил, изоксазолил, пиридил, пиперидинил, бензофурил, дигидробензофурил, бензотиенил, дигидробензотиенил, бензодиоксолил, каждый из которых может быть незамещенным или содержать в качестве заместителей R6 или фенил, тиенил, индолил, каждый из которых может быть незамещенным или содержать в качестве заместителей R6;
R5 означает Н, галоген или C1-С6 алкил, необязательно содержащий в качестве заместителя оксогруппу;
R6 означает галоген, CF3, C1-С6 алкил, необязательно содержащий в качестве заместителя оксогруппу, или гидроксил, или C1-С6 алкоксил, необязательно содержащий в качестве заместителя фтор;
и их фармацевтически приемлемые соли и сложные эфиры.
R означает Н или C1-С6 алкил;
R1 означает Н, COOR, C3-С8 циклоалкил или C1-С6 алкил, C2-С6 алкенил или C1-С6 алкоксил, каждый из которых может быть незамещенным или содержать в качестве заместителей фтор или фенил, который может быть незамещенным или содержать в качестве заместителей R6;
R2 означает Н, галоген или C1-С6 алкил, который может быть незамещенным или содержать в качестве заместителей C1-С6 алкоксил, оксогруппу, фтор, или R2 означает фенил, фурил, тиенил, пиридил, каждый из которых может быть незамещенным или содержать в качестве заместителей R;
R3 означает Н, C1-С6 алкил или фенил, который может быть незамещенным или содержать в качестве заместителей R6;
Х означает О;
R4 означает C1-С6 алкил или C3-С8 циклоалкил, каждый из которых может быть незамещенным или содержать в качестве заместителей фтор, оксогруппу или C1-С6 алкоксил, который может быть незамещенным или содержать в качестве заместителей C1-С6 алкоксил или фенил, необязательно содержащий в качестве заместителя R6,
или
C1-С6 алкил также может содержать в качестве заместителя С3-C8 циклоалкил или феноксил, который может быть незамещенным или содержать в качестве заместителей R6 или фенил, который может быть незамещенным или содержать в качестве заместителей R6,
или R4 означает фенил, нафтил, фурил, тиенил, оксазолил, тиазолил, изоксазолил, пиридил, пиперидинил бензофурил, дигидробензофурил, бензотиенил, дигидробензотиенил, бензодиоксолил, каждый из которых может быть незамещенным или содержать в качестве заместителей R6 или фенил, тиенил, индолил, каждый из которых может быть незамещенным или содержать в качестве заместителей R6;
R5 означает Н, галоген или C1-С6 алкил, необязательно содержащий в качестве заместителя оксогруппу;
R6 означает галоген, CF3, C1-С6 алкил, необязательно содержащий в качестве заместителя оксогруппу или гидроксил или C1-С6 алкоксил, необязательно содержащий в качестве заместителя фтор;
и их фармацевтически приемлемые соли и сложные эфиры.
R означает Н или C1-С6алкил;
R1 означает Н, COOR, C3-С8 циклоалкил или C1-С6 алкил, C1-С6 алкенил или C1-С6 алкоксил, каждый из которых может быть незамещенным или содержать в качестве заместителей фтор, или фенил, который может быть незамещенным или содержать в качестве заместителей R6;
R2 означает Н, галоген или C1-С6алкил, который может быть незамещенным или содержать в качестве заместителей C1-С6алкоксил, оксогруппу, фтор,
или
R2 означает фенил, фурил, тиенил, пиридил, каждый из которых может быть незамещенным или содержать в качестве заместителей R6;
R3 означает Н, C1-С6 алкил или фенил, который может быть незамещенным или содержать в качестве заместителей R6;
Х означает S;
R4 означает C1-С6 алкил или C1-С6 циклоалкил, каждый из которых может быть незамещенным или содержать в качестве заместителей фтор, оксогруппу или C1-С6 алкоксил, который может быть незамещенным или содержать в качестве заместителей C1-С6 алкоксил или фенил, необязательно содержащий в качестве заместителя R6,
или C1-С6 алкил также может содержать в качестве заместителя C3-С8 циклоалкил или феноксил, который может быть незамещенным или содержать в качестве заместителей R6 или фенил, который может быть незамещенным или содержать в качестве заместителей R6,
или R4 означает фенил, нафтил, фурил, тиенил, оксазолил, тиазолил, изоксазолил, пиридил, пиперидинил, бензофурил, дигидробензофурил, бензотиенил, дигидробензотиенил, бензодиоксолил, каждый из которых может быть незамещенным или содержать в качестве заместителей R6 или фенил, тиенил, индолил, каждый из которых может быть незамещенным или содержать в качестве заместителей R6;
R5 означает Н, галоген или C1-С6 алкил, необязательно содержащий в качестве заместителя оксогруппу;
R6 означает галоген, CF3, C1-С6 алкил, необязательно содержащий в качестве заместителя оксогруппу или гидроксил или C1-С6алкоксил, необязательно содержащий в качестве заместителя фтор;
и их фармацевтически приемлемые соли и сложные эфиры.
R означает Н;
R1 означает Н, COOR, C3-С8 циклоалкил или C1-С6 алкил, C2-С6 алкенил или C1-С6 алкоксил, каждый из которых может быть незамещенным или содержать в качестве заместителей фтор или фенил, который может быть незамещенным или содержать в качестве заместителей R6;
R2 означает Н, галоген или C1-С6 алкил, который может быть незамещенным или содержать в качестве заместителей C1-С6 алкоксил, оксогруппу, фтор;
R3 означает Н или C1-С6 алкил или фенил, который может быть незамещенным или содержать в качестве заместителей R6;
Х означает S;
R4 означает фенил, нафтил, фурил, тиенил оксазолил, тиазолил, изоксазолил, пиридил, пиперидинил, бензофурил, дигидробензофурил, бензотиенил, дигидробензотиенил, бензодиоксолил, каждый из которых может быть незамещенным или содержать в качестве заместителей R6 или фенил, тиенил, индолил, каждый из которых может быть незамещенным или содержать в качестве заместителей R6;
R5 означает Н, галоген или C1-С6 алкил, необязательно содержащий в качестве заместителя оксогруппу;
R6 означает галоген, CF3, C1-С6 алкил, необязательно содержащий в качестве заместителя оксогруппу, или гидроксил, или C1-С6 алкоксил, необязательно содержащий в качестве заместителя фтор;
и их фармацевтически приемлемые соли и сложные эфиры.
R означает Н;
R1 означает Н, COOR, C3-С8 циклоалкил или C1-С6 алкил, C2-С6 алкенил или C1-С6 алкоксил, каждый из которых может быть незамещенным или содержать в качестве заместителей фтор, или фенил, который может быть незамещенным или содержать в качестве заместителей R6;
R2 означает Н, галоген или C1-С6 алкил, который может быть незамещенным или содержать в качестве заместителей C1-С6 алкоксил, оксогруппу, фтор;
R3 означает Н, или C1-С6 алкил или фенил, который может быть незамещенным или содержать в качестве заместителей R6;
Х означает О;
R4 означает фенил, нафтил, фурил, тиенил, оксазолил, тиазолил, изоксазолил, пиридил, пиперидинил, бензофурил, дигидробензофурил, бензотиенил, дигидробензотиенил, бензодиоксолил, каждый из которых может быть незамещенным или содержать в качестве заместителей R6 или фенил, тиенил, индолил, каждый из которых может быть незамещенным или содержать в качестве заместителей R6;
R5 означает Н, галоген или C1-С6 алкил, необязательно содержащий в качестве заместителя оксогруппу;
R6 означает галоген, CF3, C1-С6 алкил, необязательно содержащий в качестве заместителя оксогруппу или гидроксил или C1-С6 алкоксил, необязательно содержащий в качестве заместителя фтор;
и их фармацевтически приемлемые соли и сложные эфиры.
R означает Н;
R1 означает Н, COOR, C3-С8 циклоалкил или C1-С6 алкил, C2-С6 алкенил или C1-С6 алкоксил, каждый из которых может быть незамещенным или содержать в качестве заместителей фтор или фенил, который может быть незамещенным или содержать в качестве заместителей R6;
R2 означает фенил, фурил, тиенил, пиридил, каждый из которых может быть незамещенным или содержать в качестве заместителей R;
R3 означает Н, C1-С6 алкил или фенил, который может быть незамещенным или содержать в качестве заместителей R6;
Х означает О;
R4 означает C1-С6 алкил или C3-С8 циклоалкил, каждый из которых может быть незамещенным или содержать в качестве заместителей фтор, оксогруппу или C1-С6 алкоксил, который может быть незамещенным или содержать в качестве заместителей C1-С6 алкоксил или фенил, необязательно содержащий в качестве заместителя R6,
или C1-С6 алкил также может содержать в качестве заместителя C3-С8 циклоалкил или феноксил, который может быть незамещенным или содержать в качестве заместителей R6 или фенил, который может быть незамещенным или содержать в качестве заместителей R6,
или R4 означает фенил, нафтил, фурил, тиенил, оксазолил, тиазолил, изоксазолил, пиридил, пиперидинил, бензофурил, дигидробензофурил, бензотиенил, дигидробензотиенил, бензодиоксолил, каждый из которых может быть незамещенным или содержать в качестве заместителей R6 или фенил, тиенил, индолил, каждый из которых может быть незамещенным или содержать в качестве заместителей R6;
R5 означает Н, галоген или C1-С6 алкил, необязательно содержащий в качестве заместителя оксогруппу;
R6 означает галоген, CF3, C1-С6 алкил, необязательно содержащий в качестве заместителя оксогруппу или гидроксил или C1-С6 алкоксил, необязательно содержащий в качестве заместителя фтор;
и их фармацевтически приемлемые соли и сложные эфиры.
5-{2-[2-(4-этилфенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-(2-{5-метил-2-[4-(трифторметил)-фенил]-1,3-оксазол-4-ил}-этокси)-2,3-дигидро-1Я-инден-1-илуксусную кислоту;
5-{2-[5-метил-2-(2-нафтил)-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(4-трет-бутилфенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(4-бутилфенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(3,4-диметилфенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(1-бензотиен-2-ил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(4-изопропилфенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-[2-(2-циклопентил-5-метил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(3-фтор-4-метилфенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту; и
5-{2-[2-(4-фторфенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту.
2-(5-{2-[2-(4-этилфенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-пропановую кислоту;
2-(5-{2-[2-(3,4-дихлорфенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-пропановую кислоту;
2-(5-(2-{5-метил-2-[4-(трифторметил)-фенил]-1,3-оксазол-4-ил}-этокси)-2,3-дигидро-1H-инден-1-ил)-пропановую кислоту;
2-(5-{2-[2-(4-метоксифенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-пропановую кислоту; и
2-(5-{2-[2-(3,4-диметилфенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-пропановую кислоту.
5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-[2-(5-метил-2-фенил-1,3-тиазол-4-ил)-этокси]-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(4-метоксифенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(3-метоксифенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(1,3-бензодиоксол-5-ил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[5-метил-2-(4-метилфенил)-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(3-фторфенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(4-фтор-3-метилфенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-[2-(5-этил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(3,4-дихлорфенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(1,1'-бифенил-4-ил)-5-метил-1,3-оксазол-4-ил]-этокси }-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(1,3-бензодиоксол-5-ил)-5-метил-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(4-метоксифенил)-5-метил-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-(2-{5-метил-2-[4-(трифторметил)-фенил]-1,3-тиазол-4-ил}-этокси)-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(4-цианофенил)-5-метил-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(4-изопропилфенил)-5-метил-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(3-хлорфенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(4-цианофенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(3-цианофенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(4-хлорфенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-(2-{5-метил-2-[3-(трифторметил)-фенил]-1,3-оксазол-4-ил}-этокси)-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(3-хлор-4-фторфенил)-5-метил-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(3,4-дихлорфенил)-5-метил-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(4-фторфенил)-5-метил-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(3,4-диметилфенил)-5-метил-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(4-ацетилфенил)-5-метил-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
трифторацетат 5-{2-[2-(3-амино-4-метилфенил)-5-метил-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусной кислоты;
5-{2-[2-(2-фторфенил)-5-метил-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(4-хлорфенил)-5-метил-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(4-этоксифенил)-5-метил-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(3,4-диметоксифенил)-5-метил-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[5-метил-2-(3-метилфенил)-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-(2-{5-метил-2-[3-(трифторметил)-фенил]-1,3-тиазол-4-ил}-этокси)-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(3-фторфенил)-5-метил-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(3,5-диметилфенил)-5-метил-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-(2-{5-метил-2-[4-(трифторметокси)-фенил]-1,3-тиазол-4-ил}-этокси)-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(3-метоксифенил)-5-метил-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[2-(1,1'-бифенил-4-ил)-5-метил-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[5-этил-2-(4-этилфенил)-1,3-оксазол-4-ил]-этокси }-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[5-этил-2-(4-метилфенил)-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-{2-[5-этил-2-(4-метоксифенил)-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-(2-{2-[4'-(гидроксиметил)-1,1'-бифенил-4-ил]-5-метил-1,3-оксазол-4-ил}-этокси)-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-(2-{2-[4-(5-ацетил-2-тиенил)-фенил]-5-метил-1,3-оксазол-4-ил}-этокси)-2,3-дигидро-1H-инден-1-илуксусную кислоту;
5-(2-{2-[3-(1H-индол-5-ил)-фенил]-5-метил-1,3-оксазол-4-ил}-этокси)-2,3-дигидро-1H-инден-1-илуксусную кислоту;
(5-{2-[2-(3-фтор-4-метилфенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-уксусную кислоту; и
(5-{2-[5-метил-2-(3-метилфенил)-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-уксусную кислоту.
2-{5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1H-инден-1-ил}-бутановую кислоту;
3-этокси-2-{5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1H-инден-1-ил}-3-оксо-пропановую кислоту;
2-(5-{2-[5-метил-2-(4-метилфенил)-1,3-оксазол-4-ил]-этокси }-2,3-дигидро-1H-инден-1-ил)-пропановую кислоту;
2-(5-{2-[5-метил-2-(4-метилфенил)-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-Ш-инден-1-ил)-бутановую кислоту;
4-метил-2-(5-{2-[5-метил-2-(4-метилфенил)-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-пентановую кислоту;
2-{5-[2-(5-этил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1H-инден-1-ил}-бутановую кислоту;
2-(5-{2-[2-(4-хлорфенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-бутановую кислоту;
2-(5-{2-[5-метил-2-(3-метилфенил)-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-бутановую кислоту;
2-(5-{2-[2-(4-метоксифенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-бутановую кислоту;
2-(5-{2-[2-(3,4-дихлорфенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-бутановую кислоту;
2-(5-{2-[5-метил-2-(2-нафтил)-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-бутановую кислоту;
2-(5-{2-[5-метил-2-(1-нафтил)-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-бутановую кислоту;
2-(5-{2-[2-(4-фторфенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-бутановую кислоту;
2-(5-{2-[2-(3-хлорфенил)-5-метил-1,3-тиазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-бутановую кислоту;
2-(5-{2-[2-циклопентил-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-бутановую кислоту;
2-(5-{2-[2-циклогексил-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-бутановую кислоту;
2-(5-{2-[2-(3-метоксифенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-бутановую кислоту;
2-(5-{2-[2-(4-этилфенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-бутановую кислоту;
2-(5-{2-[2-(1-бензотиен-2-ил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-бутановую кислоту;
2-[5-(2-{5-метил-2-[3-(трифторметил)-фенил]-1,3-оксазол-4-ил}-этокси)-2,3-дигидро-1H-инден-1-ил]-бутановую кислоту;
2-(5-{2-[2-(4-трет-бутилфенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-бутановую кислоту;
2-(5-{2-[2-(3-фторфенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-бутановую кислоту;
2-(5-{2-[2-(4-изопропилфенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-бутановую кислоту;
2-(5-{2-[2-(1,3-бензодиоксол-5-ил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-бутановую кислоту;
2-{5-[2-(2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1H-инден-1-ил}-бутановую кислоту;
2-(5-{2-[2-(3,4-дифторфенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-бутановую кислоту;
2-[5-(2-{5-метил-2-[4-(трифторметил)-фенил]-1,3-оксазол-4-ил}-этокси)-2,3-дигидро-1H-инден-1-ил]-бутановую кислоту;
2-(5-{2-[5-метил-2-(феноксиметил)-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-бутановую кислоту;
2-(5-{2-[2-(4-фтор-3-метилфенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-бутановую кислоту;
2-(5-{2-[2-(3-фтор-4-метилфенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-бутановую кислоту;
2-(5-{2-[2-(4-бутилфенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-бутановую кислоту;
2-(5-{2-[2-(3,4-диметилфенил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-бутановую кислоту;
2-(5-{2-[5-метил-2-(4-хлорфеноксиметил)-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-бутановую кислоту;
2-{6-хлор-5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1H-нден-1-ил}-бутановую кислоту;
2-{5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-6-фенил-2,3-дигидро-1H-инден-1-ил}-бутановую кислоту;
2-{6-(4-хлорфенил)-5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1H-инден-1-ил}-бутановую кислоту;
2-{6-(4-метоксифенил)-5-[2-(5-метил-2-фенил-1,3-оксазол-4-ил)-этокси]-2,3-дигидро-1H-инден-1-ил}-бутановую кислоту; и
2-(5-{2-[2-(2,3-дигидро-1-бензофуран-6-ил)-5-метил-1,3-оксазол-4-ил]-этокси}-2,3-дигидро-1H-инден-1-ил)-бутановую кислоту.
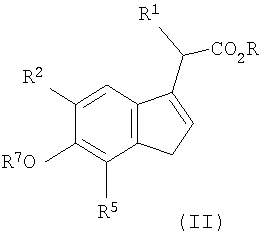
в котором R означает Н или C1-С6 алкил;
R1 означает Н, COOR, С3-C8 циклоалкил или C1-С6 алкил, С2-С6 алкенил или C1-С6 алкоксил, каждый из которых может быть незамещенным или содержать в качестве заместителей фтор или фенил, который может быть незамещенным или содержать в качестве заместителей R6;
R2 означает Н, галоген или C1-С6 алкил, который может быть незамещенным или содержать в качестве заместителей C1-С6 алкоксил, оксогруппу, фтор,
или R2 означает фенил, тиенил, пиридил, каждый из которых может быть незамещенным или содержать в качестве заместителей R6;
R5 означает Н, галоген или C1-С6 алкил, необязательно содержащий в качестве заместителя оксогруппу;
R6 означает галоген, CF3, C1-С6 алкил, необязательно содержащий в качестве заместителя оксогруппу или гидроксил или C1-С6 алкоксил, необязательно содержащий в качестве заместителя фтор;
R7 означает Н, C1-С6 алкил, необязательно содержащий в качестве заместителя фенил или оксогруппу, C1-С6 триалкилсилил, арилалкилсилил, COR8;
R8 означает C1-С6 алкил;
и их соли.

в котором R означает Н или C1-С6 алкил;
R1 означает Н, С3-C8 циклоалкил или
C1-С6 алкил, С2-С6 алкенил или C1-С6 алкоксил, каждый из которых может быть незамещенным или содержать в качестве заместителей фтор;
R2 означает Н, галоген или C1-С6 алкил, который может быть незамещенным или содержать в качестве заместителей C1-С6 алкоксил, оксогруппу, фтор,
или R2 означает фенил, тиенил, каждый из которых может быть незамещенным или содержать в качестве заместителей R6;
R5 означает Н, галоген или C1-С6 алкил, необязательно содержащий в качестве заместителя оксогруппу;
R6 означает галоген, CF3, C1-С6 алкил, необязательно содержащий в качестве заместителя оксогруппу или гидроксил или C1-С6 алкоксил, необязательно содержащий в качестве заместителя фтор;
R7 означает Н, C1-С6 алкил, необязательно содержащий в качестве заместителя фенил или оксогруппу, C1-С6 триалкилсилил, ариалкилсилил или COR8;
R8 означает C1-С6 алкил;
и их соли.
| SU 5842732 А, 30.06.1981 | |||
| Многовалковая машина для правки листового проката | 1958 |
|
SU116120A1 |
Авторы
Даты
2008-01-10—Публикация
2002-07-25—Подача