ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к обладающей высокой мощностью литиевой вторичной батарее с неводным электролитом, характеризующейся продолжительным сроком службы и превосходной безопасностью, как при комнатной температуре, так и при высокой температуре, даже после повторяющихся зарядки и разрядки сильным током.
УРОВЕНЬ ТЕХНИКИ
В последнее время строгие контроль и регулирование выбросов транспортных средств во многих странах, включая США и Европу, ускорили разработку электромобилей (ЭМ) и гибридных электромобилей (ГЭМ) с использованием двигателей внутреннего сгорания и аккумуляторных батарей в качестве источников питания, которые уже частично вошли в стадию коммерциализации.
В настоящее время имеются в продаже аккумуляторные батареи, которые могут быть использованы в электромобилях или гибридных электромобилях, которые представляют собой батареи высокой мощности и безопасность которых была подтверждена, например никель-металлогидридные (Ni-MH) вторичные батареи. Кроме того, в процессе разработки сейчас находятся также литиевые вторичные батареи, имеющие выходную мощность и плотность энергии, превосходящие эти характеристики у никель-металлогидридных вторичных батарей.
Однако от литиевых вторичных батарей, предназначенных для применения в электромобилях, требуются не только высокая плотность энергии и способность выдавать большие выходные мощности на протяжении короткого периода времени, но и продолжительный срок службы свыше 10 лет даже в тяжелых условиях эксплуатации, при которых циклы зарядки-разрядки сильным током повторяются на протяжении короткого срока, что требует свойств значительно более высокой безопасности и продолжительного срока службы по сравнению с традиционными малогабаритными литиевыми вторичными батареями.
В литий-ионных батареях, которые использовались до сих пор в качестве таких традиционных малогабаритных батарей, в качестве материала катода обычно используется сложный оксид лития-кобальта со слоистой структурой, а в качестве материала анода - материал на основе графита. Однако основной элемент, входящий в состав такого сложного оксида лития-кобальта, т.е. кобальт, является очень дорогостоящим и не подходящим для применения в электромобилях из-за проблем с безопасностью. Поэтому в качестве катодного материала литий-ионных батарей для электромобилей идеальным с точки зрения стоимости и безопасности является сложный оксид лития-марганца, имеющий шпинельную структуру, образованную марганцем. Однако сложный оксид лития-марганца при зарядке-разрядке сильным током и при высокой температуре претерпевает вымывание ионов марганца в электролит вследствие влияния этого электролита, что приводит в результате к ухудшению свойств и рабочих характеристик батареи. Таким образом, существует необходимость в разработке мер по предотвращению данных проблем. Кроме того, сложный оксид лития-марганца обладает таким недостатком, как низкая плотность заряда по сравнению с традиционным сложным оксидом лития-кобальта или сложным оксидом лития-никеля. Таким образом, существует предел по плотности заряда батареи, и для того, чтобы он нашел практическое применение в качестве источника питания в электромобилях, гибридных электромобилях и т.п., для преодоления этих недостатков должны быть совместно реализованы специальные конструкции батареи.
Для того чтобы частично преодолеть указанные выше относительные недостатки, были проведены многочисленные исследования и предприняты попытки получения электродов с использованием смешанного активного катодного материала. Например, в выложенных публикациях японских патентов №№ 2002-110253 и 2003-168430 раскрыты методики, согласно которым для улучшения отдаваемой мощности используется смесь оксида лития-марганца и/или оксида лития-кобальта со сложным оксидом (B) лития-никеля-марганца-кобальта. Эти методики, однако, имеют проблемы, связанные с плохим сроком службы при циклировании оксида лития-марганца и с ограниченным улучшением безопасности.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Поэтому цель настоящего изобретения состоит в том, чтобы решить указанные выше и другие технические проблемы, которые до сих пор не были решены.
Конкретнее, цель настоящего изобретения состоит в том, чтобы предложить активный катодный материал для вторичной батареи, содержащий смесь сложного оксида (A) лития-марганца-металла, имеющего шпинельную структуру и содержащего особый состав элементов-металлов, и сложного оксида (B) лития-никеля-марганца-кобальта, имеющего слоистую структуру и содержащего особый состав элементов-металлов, в результате чего этот активный катодный материал обладает превосходной безопасностью и продолжительным сроком службы, как при комнатной температуре, так и при высокой температуре, благодаря улучшенным свойствам оксида лития-марганца, даже после повторяющихся зарядки и разрядки сильным током.
Еще одна цель настоящего изобретения состоит в том, чтобы предложить литиевую вторичную батарею, содержащую указанный выше активный катодный материал. Такая литиевая вторичная батарея может быть предпочтительно применена в качестве батареи высокой мощности и большой емкости, в частности, для электромобилей (ЭМ) и гибридных электромобилей (ГЭМ).
В соответствии с одним аспектом настоящего изобретения, вышеуказанные и другие цели могут быть достигнуты посредством того, что предложен активный катодный материал для вторичной батареи, содержащий сложный оксид (A) лития-марганца-металла, имеющий шпинельную структуру и представленный следующей общей формулой 1, и сложный оксид (B) лития-никеля-марганца-кобальта, имеющий слоистую структуру и представленный следующей общей формулой 2:
Общая формула 1
Li1+xMn2-x-yMyO4,
где
0 < x < 0,2;
0 < y < 0,1; и
M представляет собой по меньшей мере один элемент, выбранный из группы, состоящей из Al, Mg, Ni, Co, Fe, Ti, V, Zr и Zn.
Общая Формула 2
Li1-aNibMncCo1-b-cO2,
где
-0,1 ≤ a ≤ 0,1;
0,3 < b < 0,5; и
0,3 < c < 0,5.
В соответствии с другим аспектом настоящего изобретения предложена литиевая вторичная батарея, включающая в себя катод, содержащий указанный выше активный катодный материал, анод, сепаратор и электролит.
Далее настоящее изобретение будет описано дополнительно.
Настоящее изобретение отличается использованием смеси из сложного оксида (A) лития-марганца-металла, в котором часть марганца в имеющем шпинельную структуру оксиде лития-марганца замещена другими элементами, и сложного оксида (B) лития-никеля-марганца-кобальта, имеющего слоистую структуру и особый состав элементов-металлов, в качестве активного катодного материала.
В частности, в сложном оксиде (B) лития-никеля-марганца-кобальта диапазоны содержаний входящих в вышеуказанный состав никеля (Ni), марганца (Mn) и кобальта (Co), как будет со всей очевидностью подтверждено в нижеследующих примерах и сравнительных примерах, являются существенными с точки зрения характеристик высокотемпературного циклирования и характеристик сохранения емкости и безопасности батареи.
В сложном оксиде (A) лития-марганца-металла, входящем в число активных катодных материалов в соответствии с настоящим изобретением, замещение Mn на другие металлы (M = Al, Mg, Ni, Co, Fe, Ti, V, Zr или Zn) дополнительно улучшает характеристики высокотемпературного циклирования по сравнению с незамещенным элементами-металлами оксидом лития-марганца. Это обусловлено тем, что замещение Mn3+ на другие металлы понижает концентрацию Mn3+, непосредственно связанного с растворением Mn при высокой температуре, вызывающего эффект Яна-Теллера, тем самым образуя структурно устойчивый (стабильный) оксид. Металл (M) предпочтительно выбран из группы, состоящей из Mg, Al, Co и Ni.
В сложном оксиде (A) лития-марганца-металла, когда x составляет больше 0, ионы лития замещают часть Mn3+, что приводит к снижению количества структурно неустойчивого элемента, т.е. Mn3+, способного вызывать эффект Яна-Теллера, а также ингибирует вымывание трехвалентного марганца в электролит. С другой стороны, в том случае, когда x составляет меньше 0, характеристики высокотемпературного циклирования батареи становятся плохими. Кроме того, в том случае, когда x составляет больше 0,2, концентрация ионов трехвалентного марганца в сложном оксиде (A) лития-марганца-металла, участвующих в обеспечении емкости активного материала, заметно снижается, что, в свою очередь, приводит в результате к пониженной плотности заряда активного материала.
В любом случае, даже несмотря на то, что возможно в некоторой степени улучшить характеристики высокотемпературного циклирования и характеристики сохранения емкости батареи путем регулирования соотношения элементов, входящих в состав сложного оксида (A) лития-марганца-металла, существует предел в отношении высокотемпературной устойчивости и плотности заряда батареи. Поэтому в настоящем изобретении в смеси со сложным оксидом (A) используется еще один активный материал, а именно сложный оксид (B) лития-никеля-марганца-кобальта, который является более устойчивым, и, таким образом, как ожидается, будет увеличивать срок службы.
Авторы настоящего изобретения установили, что кислотность (pH) увеличивается по мере того, как увеличивается массовая доля сложного оксида (B) лития-никеля-марганца-кобальта в таком смешанном активном катодном материале. Поэтому предполагается, что такое повышение pH способствует улучшению срока службы батареи за счет подавления вымывания ионов марганца в батарее вследствие влияния электролита, что представляло собой недостаток, проявляемый сложным оксидом (A) лития-марганца-металла. Принимая во внимание безопасность и срок службы батареи при высокой температуре, pH активного катодного материала предпочтительно находится в диапазоне от 8,9 до 10,4.
В частности, для того чтобы гарантировать приемлемую безопасность батареи, соотношение компонентов в смеси сложного оксида (A) лития-марганца-металла и сложного оксида (B) лития-никеля-марганца-кобальта в активном катодном материале по настоящему изобретению является предпочтительно таким, что содержание сложного оксида (A) лития-марганца-металла превышает 50% по массе. Этот факт может быть подтвержден следующими примерами и сравнительными примерами, которые будут проиллюстрированы далее. Более предпочтительное соотношение компонентов в смеси является таким, что массовая доля сложного оксида (A) лития-марганца-металла находится в диапазоне от 80 до 95% от общей массы смеси.
Способы получения сложных оксидов лития-металлов при варьировании состава элементов-металлов, таких как сложный оксид (A) лития-марганца-металла и сложный оксид (B) лития-никеля-марганца-кобальта, хорошо известны в данной области техники и поэтому здесь описываться не будут.
Кроме того, в соответствии с еще одним аспектом настоящего изобретения, предложена литиевая вторичная батарея, включающая в себя электродную сборку, состоящую из содержащего вышеуказанный активный катодный материал катода, анода и сепаратора, и неводный электролит.
Литиевые вторичные батареи в соответствии с настоящим изобретением могут быть в широком смысле подразделены, например, на батареи рулонного типа с гелевым электролитом и батареи пакетного типа в зависимости от вида электродной сборки. В дополнение к этому литиевые вторичные батареи могут быть в широком смысле подразделены на цилиндрические, призматические и «карманные» батареи в зависимости от их внешней формы.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Указанные выше и другие цели, признаки и прочие преимущества настоящего изобретения станут более понятными из нижеследующего подробного описания, приведенного в сочетании с прилагаемыми чертежами, на которых:
Фиг.1 схематично показывает электродную сборку пакетного типа, которая может быть использована в литиевой вторичной батарее в соответствии с настоящим изобретением;
Фиг.2 схематично показывает литиевую вторичную батарею, в которой электродная сборка пакетного типа согласно Фиг.1 содержится в корпусе «карманного» типа;
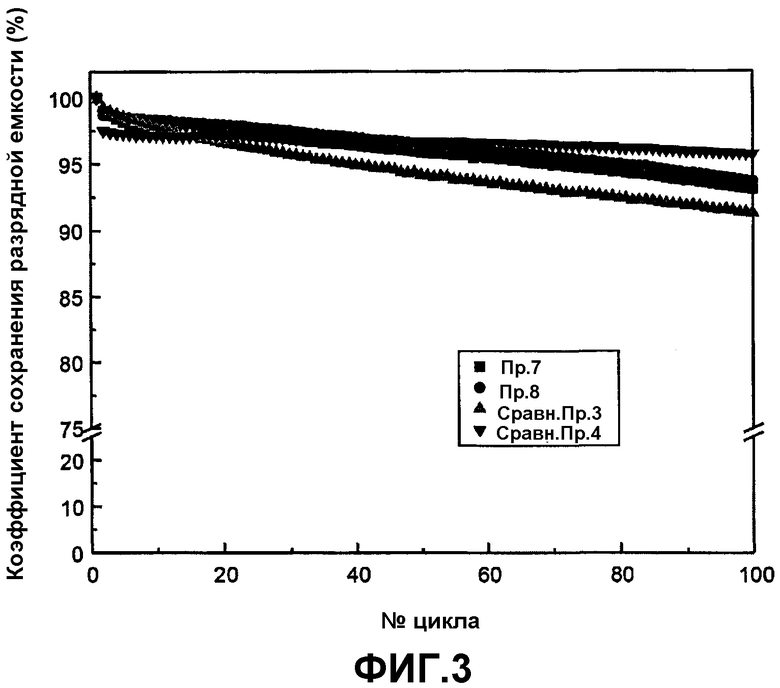
Фиг.3 представляет собой график, показывающий характеристики срока службы при циклировании при 50°C для батарей, полученных в Примерах 7 и 8 и Сравнительных Примерах 3 и 4 соответственно; и
Фиг.4 представляет собой график, показывающий характеристики срока службы при циклических зарядке-разрядке сильным током при комнатной температуре для батарей, полученных в Примерах 11 и 15 и Сравнительных Примерах 5 и 6 соответственно.
ПОДРОБНОЕ ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНЫХ ВАРИАНТОВ ВОПЛОЩЕНИЯ
Теперь настоящее изобретение будет описано более подробно со ссылкой на предпочтительные варианты воплощения и прилагаемые чертежи.
Фиг.1 схематично иллюстрирует примерную электродную сборку пакетного типа, которая может быть использована в литиевой вторичной батарее в соответствии с настоящим изобретением, а Фиг.2 схематично иллюстрирует примерную литиевую вторичную батарею, в которой такая электродная сборка пакетного типа содержится в корпусе «карманного» типа.
Обращаясь к Фиг.1 и 2, электродная сборка пакетного типа имеет конструкцию, при которой тонколистовые катод 1 и анод 2 расположены прилегающими друг к другу, но с расположенным между ними сепаратором 3. Что касается внешнего корпуса батареи, то могут использоваться ламинированные алюминием листы, применяемые в традиционных литиевых полимерных батареях. Настоящее изобретение может быть применено к батарее с внутренней конструкцией любого типа, независимо от типа укладывания в пакет (стопку) или типа наматывания.
Катод 1, например, изготавливают путем нанесения смеси из активного катодного материала в соответствии с настоящим изобретением, проводящего материала и связующего на катодный токосъемник с последующей сушкой. Если это желательно, в указанную выше смесь может быть дополнительно введен наполнитель.
Катодный токосъемник (коллектор катодного тока) обычно изготавливают имеющим толщину примерно от 3 до 500 мкм. Никаких особых ограничений в отношении катодных токосъемников нет, при условии, что они обладают высокой удельной проводимостью, при этом не испытывая в батарее никаких химических превращений. В качестве примеров катодных токосъемников можно упомянуть нержавеющую сталь, алюминий, никель, титан, спеченный углерод, а также алюминий или нержавеющую сталь, поверхность которых обработана (покрыта) углеродом, никелем, титаном или серебром. Токосъемник может быть изготовлен имеющим на своей поверхности микронеровности с тем, чтобы улучшить адгезионную способность к активному катодному материалу. В дополнение к этому, токосъемник может принимать различные формы, включая пленки, листы, фольгу, сетки, пористые структуры, пены и нетканые материалы (нетканое полотно).
Используемый в настоящем изобретении проводящий материал в типичном случае добавляют в количестве от 1 до 50% по массе из расчета на общую массу смеси, включающей в себя активный катодный материал. Никаких особых ограничений в отношении такого проводящего агента нет, при условии, что он имеет подходящую удельную проводимость, при этом не испытывая в батарее никаких химических превращений. В качестве примеров проводящих материалов можно упомянуть графит, такой как натуральный или искусственный графит; различные виды углеродной сажи, такие как простая углеродная сажа, ацетиленовая сажа, сажа Ketjen, канальная сажа, печная сажа, ламповая сажа и термическая сажа; проводящие волокна, такие как углеродные волокна и металлические волокна; фторид углерода; металлический порошок, такой как порошок алюминия или никеля; проводящие нитевидные кристаллы, такие как оксид цинка и титанат калия; проводящие оксиды металлов, такие как оксид титана; производные полифенилена и тому подобное.
Связующее представляет собой ингредиент, способствующий связыванию между активным материалом и проводящим материалом и сцеплению с токосъемниками. Используемое в настоящем изобретении связующее в типичном случае добавляют в количестве от 1 до 50% по массе из расчета на общую массу смеси, включающей в себя активный катодный материал. В качестве примеров такого связующего можно упомянуть поливинилиденфторид, поливиниловые спирты, карбоксиметилцеллюлозу (КМЦ), крахмал, гидроксипропилцеллюлозу, переработанную целлюлозу, поливинилпирролидон, тетрафторэтилен, полиэтилен, полипропилен, тройной полимер этилена, пропилена и диенового мономера (ЭПДМ), сульфированный ЭПДМ, бутадиен-стирольный каучук, фтор-каучук и различные сополимеры.
Наполнитель представляет собой ингредиент, который препятствует расширению катода и используется в необязательном порядке (по выбору). Никаких особых ограничений в отношении наполнителя нет, при условии, что он не испытывает никаких химических превращений в батарее, а также является волокнистым материалом. В качестве примеров такого наполнителя могут быть использованы олефиновые полимеры, такие как полиэтилен и полипропилен; и волокнистые материалы, такие как стекловолокно и углеродное волокно.
Анод 2 изготавливают путем нанесения анодного материала на анодный токосъемник с последующей сушкой. Если это необходимо, могут быть дополнительно введены другие компоненты, такие как проводящие материалы и связующие.
Анодный токосъемник (коллектор анодного тока) обычно изготавливают имеющим толщину от 3 до 500 мкм. Никаких особых ограничений в отношении анодных токосъемников нет, при условии, что они имеют подходящую удельную электропроводность, не испытывая при этом никаких химических превращений в батарее. В качестве примеров анодных токосъемников можно упомянуть медь, нержавеющую сталь, алюминий, никель, титан, спеченный углерод, а также медь или нержавеющую сталь, поверхность которых обработана (покрыта) углеродом, никелем, титаном или серебром, и сплавы алюминия-кадмия. Аналогично катодному токосъемнику, анодный токосъемник также может быть изготовлен с формированием микронеровностей на его поверхности с тем, чтобы улучшить адгезионную способность к активному анодному материалу. В дополнение к этому, анодный токосъемник может принимать различные формы, включая пленки, листы, фольгу, сетки, пористые структуры, пены и нетканые материалы (нетканое полотно).
В качестве примеров пригодных для применения в настоящем изобретении активных анодных материалов можно упомянуть углерод, такой как неграфитизированный углерод и углерод на графитовой основе; сложные оксиды металлов, такие как LixFe2O3 (0≤x≤1), LixWO2 (0≤x≤1) и SnxMe1-xMe'yOz (Me: Mn, Fe, Pb, Ge; Me': Al, B, P, Si, элементы I, II и III групп Периодической таблицы, атомы галогена; 0<x≤1; 1≤y≤3; 1≤z≤8); металлический литий; литиевые сплавы; сплавы на основе кремния; оловянные сплавы; оксиды металлов, такие как SnO, SnO2, PbO, PbO2, Pb2O3, Pb3O4, Sb2O3, Sb2O4, Sb2O5, GeO, GeO2, Bi2O3, Bi2O4 и Bi2O5; проводящие полимеры, такие как полиацетилен; и материалы на основе Li-Co-Ni.
Между катодом 1 и анодом 2 расположен сепаратор 3. В качестве сепаратора используют изолирующую тонкую пленку, имеющую высокую ионную проницаемость и механическую прочность. Сепаратор в типичном случае имеет диаметр пор от 0,01 до 10 мкм и толщину от 5 до 300 мкм. В качестве сепараторов, которые могут быть использованы в настоящем изобретении, можно упомянуть олефиновые полимеры, такие как химически стойкий и гидрофобный полипропилен; и листы или нетканые материалы, выполненные из стекловолокна или полиэтилена. Когда в качестве электролита используется твердый электролит, такой как полимер, этот твердый электролит может также служить в качестве и сепаратора, и электролита.
Неводный электролит, содержащий литиевую соль, состоит из неводного электролита и соли лития. В качестве неводного электролита могут быть использованы неводный раствор электролита, органический твердый электролит, неорганический твердый электролит и тому подобное.
В качестве неводного раствора электролита, например, можно упомянуть апротонные органические растворители, такие как н-метил-2-пирролидон (НМП), пропиленкарбонат, этиленкарбонат (ЭК), бутиленкарбонат, диметилкарбонат, диэтилкарбонат, гамма-бутиролактон, 1,2-диметоксиэтан, тетрагидрофуран, 2-метилтетрагидрофуран, диметилсульфоксид, 1,3-диоксолан, формамид, диметилформамид, диоксолан, ацетонитрил, нитрометан, метилформиат (метиловый эфир муравьиной кислоты), метилацетат (метиловый эфир уксусной кислоты), тройной сложный эфир фосфорной кислоты, триметоксиметан, производные диоксолана, сульфолан, метилсульфолан, l,3-диметил-2-имидазолидинон, производные пропиленкарбоната, производные тетрагидрофурана, простой эфир, метилпропионат и этилпропионат (метиловый и этиловый эфиры пропионовой кислоты) и тому подобное.
В качестве примеров используемого в настоящем изобретении органического твердого электролита можно упомянуть производные полиэтилена, производные полиэтиленоксида, производные полипропиленоксида, фосфатные полимеры, полилизин перемешивания, полиэфирсульфон, поливиниловый спирт, поли(винилиденфторид), полимеры, содержащие группы ионной диссоциации, и тому подобное.
В качестве примеров используемого в настоящем изобретении неорганического твердого электролита можно упомянуть нитриды, галогениды и сульфаты лития, такие как Li3N, LiI, Li5NI2, Li3N-LiI-LiOH, LiSiO4, LiSiO4-LiI-LiOH, Li2SiS3, Li4SiO4, Li4SiO4-LiI-LiOH, Li3PO4-Li2S-SiS2 и тому подобные.
Соль лития представляет собой материал, который легко растворим в неводном электролите и может включать в себя, например, LiCl, LiBr, LiI, LiClO4, LiBF4, LiB10Cl10, LiPF6, LiCF3SO3, LiCF3CO2, LiAsF6, LiSbF6, LiAlCl4, CH3SO3Li, CF3SO3Li, (CF3SO2)2NLi, хлороборат лития, соль низшей алифатической карбоновой кислоты и лития, тетрафенилборат лития, имид и тому подобное.
Дополнительно, с целью улучшения зарядно-разрядных характеристик и пламегашения, к неводному электролиту могут быть добавлены, например, пиридин, триэтилфосфит, триэтаноламин, циклический простой эфир, этилендиамин, n-glyme, триамид гексаметилфосфорной кислоты, производные нитробензола, сера, хинонимидные красители, н-замещенный оксазолидинон, н,н- замещенный имидазолидин, диалкиловый простой эфир этиленгликоля, соли аммония, пиррол, 2-метоксиэтанол, трихлорид алюминия и тому подобное. Если это необходимо, для того чтобы придать невоспламеняемость, неводный электролит может дополнительно включать в себя галогенсодержащие растворители, такие как тетрахлорид углерода и трифторид этилена. В дополнение к этому, неводный электролит может дополнительно включать в себя газообразный диоксид углерода с целью улучшения обратимости при высокой температуре.
ПРИМЕРЫ
Теперь настоящее изобретение будет описываться более подробно со ссылкой на нижеследующие примеры. Эти примеры приведены только с целью пояснения настоящего изобретения и не должны рассматриваться как ограничивающие объем и сущность настоящего изобретения.
Пример 1
Сложный оксид (A) лития-марганца-металла вида Li1,1Mn1,85Al0,05O4 и сложный оксид (B) лития-никеля-марганца-кобальта вида LiNi0,4Mn0,4Co0,2O2 смешали в массовом отношении 90:10. 1,25 г полученной в результате смеси добавили к 25 мл трижды дистиллированной воды, после чего подвергли обработке ультразвуком в течение 30 мин, с последующим измерением pH с помощью pH-метра. Полученные результаты приведены в таблице 1 ниже.
Примеры со 2 по 5
Эксперименты повторили с использованием такой же процедуры, как и в Примере 1, за исключением того, что варьировали отношение Li1,1Mn1,85Al0,05O4 к LiNi0,4Mn0,4Co0,2O2 в смеси, а затем измеряли pH полученного таким образом продукта. Полученные результаты приведены в таблице 1 ниже.
Сравнительный Пример 1
Эксперимент повторили с использованием такой же процедуры, как и в Примере 1, за исключением того, что отношение Li1,1Mn1,85Al0,05O4 к LiNi0,4Mn0,4Co0,2O2 в смеси (по массе) составляло 100:0, а затем измеряли pH полученного таким образом продукта. Полученные результаты приведены в таблице 1 ниже.
Сравнительный Пример 2
Эксперимент повторили с использованием такой же процедуры, как и в Примере 1, за исключением того, что отношение Li1,1Mn1,85Al0,05O4 к LiNi0,4Mn0,4Co0,2O2 в смеси (по массе) составляло 0:100, а затем измеряли pH полученного таким образом продукта. Полученные результаты приведены в таблице 1 ниже.
Пример 6
Таким же самым образом, как и в Примере 1, смешали Li1,1Mn1,85Al0,05O4 и LiNi0,4Mn0,4Co0,2O2 в массовом отношении 90:10 с получением активного катодного материала. Этот активный катодный материал, углеродную сажу и, в качестве связующего, поливинилиденфторид (ПВДФ) в массовом отношении 85:10:5 смешали в органическом растворителе, НМП, с получением суспензии. Полученную суспензию нанесли на обе стороны алюминиевой фольги с толщиной 20 мкм и высушили с получением катода. Собрали батарею пуговичного типа с использованием полученного таким образом катода, металлического лития в качестве анода, пористой полиэтиленовой пленки в качестве сепаратора и 1M раствора LiPF6 в ЭК/ЭМК в качестве электролита.
Для того чтобы оценить срок службы при высокой температуре полученной таким образом батареи, эту батарею подвергли 50-ти циклам зарядки-разрядки при плотности тока в 0,2 C и температуре в 50°C. Рассчитали коэффициент сохранения разрядной емкости батареи согласно нижеследующему уравнению 1. Полученные результаты приведены в таблице 2 ниже.
Уравнение 1
Коэффициент сохранения разрядной емкости (%) = (разрядная емкость после 100 циклов зарядки-разрядки / разрядная емкость после 1 цикла зарядки-разрядки) × 100
* Примечание: 100 циклов зарядки-разрядки задали, найдя оптимальные условия для относительного сравнения.
Примеры с 7 по 10
Батареи собирали с использованием такой же процедуры, как и в Примере 6, за исключением того, что отношение Li1,1Mn1,85Al0,05O4 к LiNi0,4Mn0,4Co0,2O2 в смеси (по массе) регулировали согласно тем значениям, которые перечислены в таблице 2 ниже, а затем оценили срок службы батарей при высокой температуре. Полученные результаты приведены соответственно в таблице 2 ниже и на Фиг.3.
Сравнительный Пример 3
Батарею собирали с использованием такой же процедуры, как и в Примере 6, за исключением того, что отношение Li1,1Mn1,85Al0,05O4 к LiNi0,4Mn0,4Co0,2O2 в смеси (по массе) составляло 100:0, а затем оценили срок службы батареи при высокой температуре. Полученные результаты приведены соответственно в таблице 2 ниже и на Фиг.3.
Сравнительный Пример 4
Батарею собирали с использованием такой же процедуры, как и в Примере 6, за исключением того, что отношение Li1,1Mn1,85Al0,05O4 к LiNi0,4Mn0,4Co0,2O2 в смеси (по массе) составляло 0:100, а затем оценили срок службы батареи при высокой температуре. Полученные результаты приведены соответственно в таблице 2 ниже и на Фиг.3.
Как можно видеть из Таблиц 1 и 2, при смешивании сложного оксида (A) лития-марганца-металла вида Li1+xMn2-x-yMyO4 и сложного оксида (B) лития-никеля-марганца-кобальта вида Li1-aNibMncCo1-b-cO2, величина pH активного катодного материала увеличивается по мере того, как увеличивается доля сложного оксида (B) в смеси. Полагают, что такое увеличение pH подавляет вымывание ионов марганца из сложного оксида (A) шпинельной структуры в электролит, что приводит к повышенному сроку службы батареи при высоких температурах. Кроме того, можно также увидеть, что благодаря смешиванию со сложным оксидом (B) лития-никеля-марганца-кобальта можно также решить проблемы, связанные с низкой плотностью заряда, неблагоприятным образом демонстрируемые сложным оксидом (A) лития-марганца-металла шпинельной структуры. Хотя активный катодный материал согласно Сравнительному Примеру 4 демонстрирует превосходное сохранение разрядной емкости, этот активный материал имеет проблемы с безопасностью, как будет показано в Сравнительном Примере 6.
Пример 11
Для получения активного катодного материала использовали сложный оксид (A) лития-марганца-металла вида Li1,1Mn1,85Mg0,05O4 и сложный оксид (B) лития-никеля-марганца-кобальта вида LiNi1/3Mn1/3Co1/3O2 в массовом отношении 90:10. Этот активный катодный материал, углеродную сажу и, в качестве связующего, ПВДФ в массовом отношении 85:10:5 смешали в органическом растворителе, НМП, с получением суспензии. Полученную суспензию нанесли на обе стороны алюминиевой фольги с толщиной в 20 мкм и высушили, с получением таким образом катода.
Порошок из сферических частиц искусственного графита, имевших высокую степень кристалличности и средний размер частиц в 12 мкм, и связующее ПВДФ смешали в массовом отношении 90:10, а затем примешали в НМП с получением суспензии. Полученную суспензию нанесли на медную фольгу с толщиной в 10 мкм и высушили, с последующей подпрессовкой прокаткой до толщины в 60 мкм, с получением таким образом анода.
Литиевую батарею пакетного типа, которая показана на Фиг.1, изготовили с использованием полученных таким образом катода и анода и 1M раствора LiPF6 в ЭК/ЭМК в качестве электролита.
Когда в качестве анода используется металлический литий, то трудно подтвердить наличие высокой выходной мощности, большей чем 5 C, вследствие низкой скорости диффузии металлического лития. Поэтому характеристики срока службы батареи при зарядке-разрядке сильным импульсным током испытывали с использованием углерода в качестве анода.
Для того чтобы оценить характеристики срока службы батареи при зарядке-разрядке сильным импульсным током, повторили большое число циклов зарядки-разрядки током в 50 A при комнатной температуре и глубине разрядки (DOD) от 40 до 60%. Коэффициент сохранения разрядной емкости при зарядке-разрядке батареи сильным током рассчитывали согласно нижеследующему уравнению 2. Полученные результаты приведены соответственно в таблице 3 ниже и на Фиг.4.
Уравнение 2
Коэффициент сохранения разрядной емкости при зарядке-разрядке сильным током (%) = (разрядная емкость при начальной плотности тока 1 C / разрядная емкость при плотности тока 1 C после цикла зарядки-разрядки током в 50 A) × 100
Кроме того, испытывали батарею на безопасность. Полученные результаты приведены в таблице 4 ниже. Испытание батареи на безопасность осуществляли путем избыточной зарядки батареи до состояния заряженности (SOC) при 200 или 20 вольтах током в 32 A и проверки наличия возгорания батареи.
Примеры с 12 по 15
Батареи собирали с использованием такой же процедуры, как и в Примере 11, за исключением того, что варьировали отношение Li1,1Mn1,85Mg0,05O4 к LiNi1/3Mn1/3Co1/3O2 в смеси (по массе). Оценивали характеристики срока службы батарей при зарядке-разрядке сильным импульсным током (скорость разрядки при большой нагрузке), а также осуществляли испытание батарей на безопасность. Полученные результаты приведены соответственно в нижеследующих Таблицах 3 и 4 и на Фиг.4.
Сравнительный Пример 5
Батарею собирали с использованием такой же процедуры, как и в Примере 11, за исключением того, что отношение Li1,1Mn1,85Mg0,05O4 к LiNi1/3Mn1/3Co1/3O2 в смеси (по массе) составляло 100:0. Оценивали характеристики срока службы батареи при зарядке-разрядке сильным импульсным током (скорость разрядки при большой нагрузке), а также осуществляли испытание батареи на безопасность. Полученные результаты приведены соответственно в нижеследующих Таблицах 3 и 4 и на Фиг.4.
Сравнительный Пример 6
Батарею собирали с использованием такой же процедуры, как и в Примере 11, за исключением того, что отношение Li1,1Mn1,85Mg0,05O4 к LiNi1/3Mn1/3Co1/3O2 в смеси (по массе) составляло 0:100. Оценивали характеристики срока службы батареи при зарядке-разрядке сильным импульсным током (скорость разрядки при большой нагрузке), а также осуществляли испытание батареи на безопасность. Полученные результаты приведены соответственно в нижеследующих Таблицах 3 и 4 и на Фиг.4.
к LiNi1/3Mn1/3Co1/3O2 в смешанном активном катодном материале
Как можно видеть из Таблицы 3, при смешивании сложного оксида (A) лития-марганца-металла и сложного оксида (B) лития-никеля-марганца-кобальта срок службы батареи при зарядке-разрядке сильным током повышается по мере того, как увеличивается доля сложного оксида (B) лития-никеля-марганца-кобальта в такой смеси. Это, как полагают, обусловлено тем, что, даже несмотря на то, что зарядка-разрядка литиевой вторичной батареи сильным током приводит к повышенной температуре этой батареи, смешанный электрод из сложного оксида (A) лития-марганца-металла шпинельной структуры и сложного оксида (B) лития-никеля-марганца-кобальта слоистой структуры имеет высокий pH и в основном устойчивую структуру при высокой температуре, тем самым обеспечивая результаты по повышению срока службы батареи, как это уже было показано в предыдущих примерах.
Из приведенных в Таблице 4 результатов можно увидеть, что при смешивании сложного оксида (A) лития-марганца-металла и сложного оксида (B) лития-никеля-марганца-кобальта безопасность батареи может быть гарантирована в том случае, когда массовая доля сложного оксида (A) превышает 50%. Этот результат, как полагают, обусловлен безопасностью сложного оксида (A) лития-марганца-металла шпинельной структуры. И хотя активный катодный материал согласно Сравнительному Примеру 5 продемонстрировал превосходную безопасность ввиду отсутствия возгорания в данных экспериментах, он имеет проблему, связанную с низким коэффициентом сохранения разрядной емкости после множества циклов зарядки-разрядки, что можно видеть в Таблице 3.
Пример 16
Батарею собирали с использованием такой же процедуры, как и в Примере 6, за исключением того, что вместо Li1,1Mn1,85Al0,05O4 в качестве сложного оксида (A) лития-марганца-металла использовали Li1,08Mn1,87Al0,05O4, а затем оценивали срок службы батареи при высокой температуре. Результаты приведены в Таблице 5 ниже.
Сравнительный Пример 7
Батарею собирали с использованием такой же процедуры, как и в Примере 16, за исключением того, что вместо Li1,08Mn1,87Al0,05O4 в качестве сложного оксида (A) лития-марганца-металла использовали Li1,08Mn1,92O4, а затем оценивали срок службы батареи при высокой температуре. Полученные результаты приведены в Таблице 5.
Как можно видеть из Таблицы 5, вследствие замещения Mn на другой металл M, сложный оксид (A) лития-марганца-металла вида Li1+xMn2-x-yMyO4 [при условии, что 0<x≤0,2, 0<y≤0,1, а M представляет собой по меньшей мере один элемент, выбранный из группы, состоящей из Al, Mg, Ni, Co, Fe, Ti, V, Zr и Zn] является более устойчивым при высоких температурах, чем оксид лития-марганца Li1+xMn2-xO4 шпинельной структуры (при условии, что 0<x<0,2) без замещения элементом-металлом. Это обусловлено, как полагают, тем, что сложный оксид (A) лития-марганца-металла, в котором Mn был замещен на другой металл M, дает в результате относительно сниженное вымывание ионов марганца при высоких температурах по сравнению с оксидом лития-марганца без замещения элементом-металлом.
Примеры 17 и 18
Катод получали с использованием такой же процедуры, как и в Примере 11, за исключением того, что в составе сложного оксида (B) лития-никеля-марганца-кобальта вида Li1-aNibMncCo1-b-cO2 доли никеля, кобальта и марганца регулировали таким образом, как описано в Таблице 6 ниже. Для того чтобы проверить безопасность активного катодного материала, проводили дифференциальную сканирующую калориметрию (ДСК). Температура начала и тепловой эффект пика приведены в Таблице 6 ниже.
Сравнительные Примеры с 8 по 10
Эксперименты повторили с использованием такой же процедуры, как и в Примере 11, за исключением того, что в составе сложного оксида (B) лития-никеля-марганца-кобальта вида Li1-aNibMncCo1-b-cO2 доли никеля, кобальта и марганца регулировали таким образом, как описано в Таблице 6 ниже. Полученные результаты приведены в Таблице 6 ниже.
Как можно видеть из Таблицы 6, по мере того, как доля марганца в сложном оксиде (B) лития-никеля-марганца-кобальта повышается, а доля кобальта соответственно понижается, температура начала пика растет, а тепловой эффект заметно уменьшается. В частности, такие изменения особенно заметны, когда содержание марганца составляет примерно 0,3. Этот факт означает, что безопасность катода улучшилась, поскольку марганец в данном материале является менее реакционноспособным при высокой температуре по сравнению с кобальтом. И хотя активный катодный материал согласно Сравнительному Примеру 10 демонстрирует результаты с высокой температурой начала пика и низким тепловым эффектом, такой активный материал имеет высокое содержание никеля, тем самым невыгодным образом вызывая вспучивание батареи.
Пример 19
Батарею собирали с использованием такой же процедуры, как и в Примере 11, за исключением того, что активный катодный материал получали с использованием сложного оксида (A) лития-марганца-металла вида Li1,1Mn1,85Mg0,05O4 и сложного оксида (B) лития-никеля-марганца-кобальта вида LiNi1/3Mn1/3Co1/3O2 при отношении этих компонентов в смеси 70:30, а затем осуществляли испытание батареи на безопасность. Полученные результаты приведены в Таблице 7 ниже.
Сравнительный Пример 11
Батарею собирали с использованием такой же процедуры, как и в Примере 11, за исключением того, что активный катодный материал получали с использованием сложного оксида (A) лития-марганца-металла вида Li1,1Mn1,85Mg0,05O4 и сложного оксида (B) лития-никеля-марганца-кобальта вида LiNi0,15Mn0,15Co0,7O2 при отношении этих компонентов в смеси 70:30, а затем осуществляли испытание батареи на безопасность. Полученные результаты приведены в Таблице 7 ниже.
Сравнительный Пример 12
Батарею собирали с использованием такой же процедуры, как и в Примере 11, за исключением того, что активный катодный материал получали с использованием сложного оксида (A) лития-марганца-металла вида Li1,1Mn1,85Mg0,05O4 и сложного оксида (B) лития-никеля-марганца-кобальта вида LiNi0,3Mn0,3Co0,4O2 при отношении этих компонентов в смеси 70:30, а затем осуществляли испытание батареи на безопасность. Полученные результаты приведены в Таблице 7 ниже.
Li1,1Mn1,85Mg0,05O4 к Li1-aNibMncCo1-b-cO2 в смеси
Как можно видеть из Таблицы 7, даже в том случае, когда массовое отношение сложного оксида (A) лития-марганца-металла шпинельной структуры к сложному оксиду (B) лития-никеля-марганца-кобальта слоистой структуры в смеси составляет 70:30, если доля Mn в составе сложного оксида (B) лития-никеля-марганца-кобальта Li1-aNibMncCo1-b-cO2 составляет менее 0,3 или доля Co в его составе составляет более 0,4, то невозможно гарантировать безопасность батареи. Поэтому, в частности, в случае смеси сложного оксида (A) лития-марганца-металла и сложного оксида (B) лития-никеля-марганца-кобальта, соотношение никеля, кобальта и марганца в составе сложного оксида (B) лития-никеля-марганца-кобальта является очень важным для безопасности батареи.
ПРОМЫШЛЕННАЯ ПРИМЕНИМОСТЬ
Как было описано выше, использование во вторичной батарее с неводным электролитом в соответствии с настоящим изобретением смеси из особого сложного оксида (A) лития-марганца-металла и особого сложного оксида (B) лития-никеля-марганца-кобальта в качестве активного катодного материала может гарантировать безопасность такой батареи и улучшить срок ее службы даже в условиях зарядки-разрядки сильным током за короткий период времени и в условиях высоких температур.
Хотя выше в иллюстративных целях были раскрыты предпочтительные варианты воплощения настоящего изобретения, специалистам в данной области будет понятно, что в них возможны различные модификации, дополнения и замены без отклонения от объема и сущности изобретения, которые определены в прилагаемой формуле изобретения.


Изобретение относится к обладающей высокой мощностью литиевой вторичной батарее с неводным электролитом. Техническим результатом является продолжительный срок службы батареи и превосходная безопасность, как при комнатной температуре, так и при высокой температуре даже после повторяющихся зарядки и разрядки сильным током. Согласно изобретению батарея в качестве активного катодного материала содержит смесь особого сложного оксида (А) лития-марганца-металла со шпинельной структурой и особого сложного оксида (В) лития-никеля-марганца-кобальта со слоистой структурой. 2 н. и 5 з.п. ф-лы, 4 ил., 7 табл.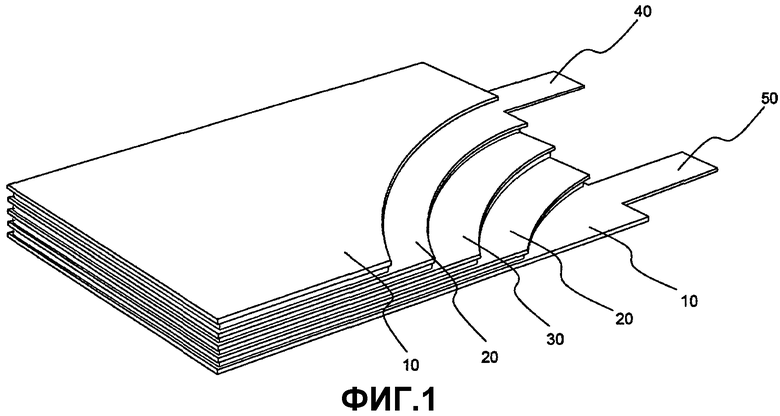
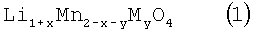
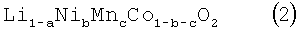 ,
,
где 0<х<0,2;
0<y<0,1;
М представляет собой по меньшей мере один элемент, выбранный из группы, состоящей из Al, Mg, Ni, Co, Fe, Ti, V, Zr и Zn;
-0,1≤а≤0,1;
0,3<b<0,5;и
0,3<c<0,5.
| US 2001031397 A1, 18.10.2001 | |||
| СПОСОБ ПОЛУЧЕНИЯ ОКСИДА ЛИТИЯ И МАРГАНЦА LIMnO СО СТРУКТУРОЙ ШПИНЕЛИ (ВАРИАНТЫ) И ВТОРИЧНАЯ ПЕРЕЗАРЯЖАЕМАЯ БАТАРЕЯ | 1997 |
|
RU2165390C2 |
| RU 2001107593 А, 10.03.2003 | |||
| US 6183911 B1, 06.02.2001. | |||
Авторы
Даты
2008-01-20—Публикация
2005-03-29—Подача