Изобретение относится к области химико-фармацевтической промышленности, в частности к производству комбинированных лекарственных форм в виде пленочных мембран для оказания кровоостанавливающего, ранозаживляющего, противовоспалительного действия в медицинской практике.
В фармацевтической технологии известен способ получения лекарственных форм в виде лекарственных пленочных мембран [3-5]. Однако изготовление их осуществляется с использованием в качестве основы-пленкообразователя желатина, агар-агара, метилцеллюлозы, Na-карбоксиметилцеллюлозы, коллагена, альгината натрия. Эти пленкообразователи не обладают широким спектром лечебного действия, что сокращает область их применения.
За прототип изобретения нами взят способ пористых пластин «альгипор», включающий использование альгината натрия, кальция глюконата, фурацилина [2] и предполагающий использование сложного оборудования.
Недостатком известного способа получения лекарственной мембраны является низкая эффективность лечебного воздействия и ограниченная область применения лекарственных мембран.
Целью создания изобретения является расширение области применения полученных лекарственных мембран и повышение эффективности их лечебного воздействия.
Поставленная цель достигается тем, что в процессе получения используют в качестве пленкообразователя хитозан и дополнительно вводят вспомогательные вещества диметилсульфоксид, аэросил, кислоту уксусную 98% для изготовления ее 2% раствора и воду очищенную, при следующем соотношении компонентов мас.%:
Сравнение предлагаемого способа с другими известными способами [1, 6-8] показала его соответствие критерию изобретения.
Заявленный способ реализуется следующим примером.
Пример 1.
а) изготовление раствора кислоты уксусной 2% из кислоты уксусной 98% ледяной (ГОСТ 61-75): в стерильную емкость на 50 мл отмеривают 79,28 мл воды очищенной и 1,62 мл кислоты уксусной 98%, перемешивают. Получают 80,9 мл 2% кислоты уксусной. Используют для приготовления 3% раствора хитозана.
б) изготовление 3% раствора хитозана: в стерильную емкость на 100 мл помещают 2,43 г хитозана (ТУ 9289-003-49857769-2003 - «Хитозан крабовый») и заливают 2% раствором кислоты уксусной комнатной температуры в количестве 80,9 мл. Выдерживают в асептических условиях 2-3 часа до растворения хитозана и образования прозрачного раствора. Полученный раствор фильтруют.
в) изготовление лекарственной мембраны:
В стерильную ступку отвешивают фурацилина 0,6 г (нижняя граница соотношения, указанного в формуле заявки) (ФС 42-2522-88), растворяют в 12,0 г (нижняя граница соотношения, указанного в формуле заявки) диметилсульфоксида (ДМСО) - (ВФС 42-1166-81). К полученному раствору фурацилина добавляют аэросил (ГОСТ 14922-77) в количестве 4,0 г (нижняя граница соотношения, указанного в формуле заявки) и перемешивают до получения однородного лимонно-желтого порошка. К нему добавляют частями приготовленный 3%-ый раствор хитозана, гомогенизируют, выдерживают 30 минут для удаления воздуха и разливают в стерильные стеклянные формы площадью 553 см2 при толщине слоя пленочной массы 5 мм.
Сушат в асептических условиях при комнатной температуре до остаточной влажности 2%.
После высушивания полученные пластины толщиной 1 мм дозируют на мембраны различных размеров: 1×2 см, 0,5×2 см, 2×3 см и др. размеры в зависимости от требуемой площади по назначению врача. Упаковывают в полиэтиленовую пленку (ГОСТ 10354-82 Н (пищевая)) или стеклянные флаконы (ТУ 9461-006-05766126-2002) с резиновой пробкой и алюминиевыми колпачками «под обкатку» и стерилизуют с помощью радиационной стерилизации (Со60) в течение 2 часов при мощности дозы 10 кГр/час.
Примеры других оптимальных соотношений даны в таблице 1 (составы 1-4). Технология изготовления лекарственных мембран осуществлялась аналогично примеру 1.
Оптимальные составы лекарственной мембраны
Изменение количеств (запредельные параметры) лекарственных и вспомогательных веществ по отношению к указанным в таблице не приводит к достижению положительного эффекта.
Для подтверждения заявляемых оптимальных составов оценку качества всех полученных в ходе выполнения эксперимента образцов лекарственных мембран применили сравнительный анализ органолептических свойств полученных мембран с помощью обобщенной функции желательности Харрингтона.
Метод обобщенной функции желательности [5] включает расчеты значений частных наиболее значимых показателей желательности отдельных свойств (d) и обобщенной функции желательности (D) этих показателей.
Значение D=0 соответствует абсолютно неприемлемому уровню данного свойства (очень плохое качество), a D=1 самому лучшему значению свойства (очень хорошее качество). Базовые отметки функции желательности представлены в таблице 2.
Базовые отметки шкалы желательности
Имея несколько откликов, преобразованных в шкалу d, можно рассчитать обобщенную функцию желательности как среднее геометрическое частных функций желательности отдельных свойств по формуле
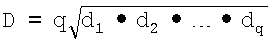
где q - количество частных функций желательности.
Оценивали следующие критерии мембран: цвет, однородность, эластичность, способность отставать от формы, которые служили откликами при расчете функции D. Ее значение рассчитывали по формуле
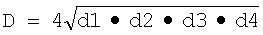
Желательность для отдельных свойств обозначена:
d1 - однородность; d2 - эластичность; d3 - способность отставать от формы; d4 - анмикробная активность.
Распределение желательности для отдельных свойств по составам мембран представлено в табл.3.
Распределение желательности для экспериментальных лекарственной мембраны
Как видно из данных таблицы 3, составы №№4, 5, 6, 7, 8 являются оптимальными по выбранным критериям оценки качества.
Образцы №1, 2, 3, 9, 10, 11 и 12, содержащие запредельные количества компонентов, не обладают оптимальными качествами. Запредельные количества в сторону увеличения (составы 9, 10, 11, 12) приводят к получению хрупких образцов, требующих добавления дополнительно пластификаторов и, в связи с этим, изменению состава. А запредельные составы в сторону уменьшения количеств исходных компонентов обладают низкой антимикробной активностью (составы 1-3).
Лекарственная форма, полученная заявляемым способом, оказывает выраженным пролонгированным очищающим и антимикробным действием, что подтверждается экспериментальными данными, представленными на фиг.1, 2, 3 и в таблицах 4-6.
Как известно, при создании терапевтических систем с любым лекарственным веществом необходима информация об особенностях диффузионного переноса в полимерных материалах. Одним из основных параметров системы, имеющей диффузионные возможности, является ее влагопоглощение.
Следовательно, процесс набухания мембраны будет влиять на процесс высвобождения содержащегося в ней фурацилина. Кроме этого, мембрана будет поглощать содержимое раны, способствуя ее очищению.
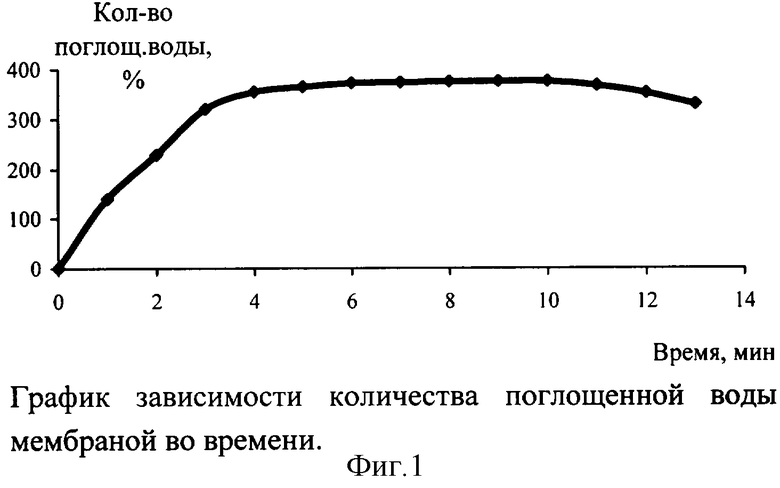
Результаты определения количества поглощенной воды мембраной массой 0,0695 представлены на фиг.1.
Кривая графика характеризует только процесс набухания. Уменьшение массы мембраны на 10-м часе эксперимента свидетельствует о начале ее растворения. Таким образом, разработанная мембрана длительно набухает, поглощая при этом воды в среднем на 375% больше массы исходной пленки, что свидетельствует о ее осмотической активности и очищающем действии.
Для изучения характера высвобождения фурацилина из разработанной лекарственной формы применяли известный метод равновесного диализа.
В эксперименте использовали диализные трубки с внутренним диаметром 25±0,1 мм и высотой 100 мм. На одном конце трубки фиксировали полупроницаемую мембрану, в качестве которой служил целлофан. Для удаления с его поверхности лакового покрытия целлофан предварительно вымачивали в воде, очищенной в течение 30 минут.
Из испытуемых образцов вырезали по 5 дисков диаметром 20±0,1 мм и помещали их внутрь трубки на целлофан, избегая попадания воздуха между ним и исследуемой мембраной. Трубки термостатировали при температуре 37±1°С вместе с химическими стаканами, в которые предварительно заливали 30 мл воды очищенной. Конец трубки с целлофаном опускали на поверхность воды. В течение 10 часов через определенные промежутки времени проводили забор проб в количестве 5 мл, при этом таким же объемом воды очищенной восполняли объем диализной жидкости. Концентрацию фурацилина определяли спектрофотометрическим методом. В основе метода лежит известная реакция взаимодействия фурацилина с раствором щелочи с образованием ацинитросоли желто-оранжевого цвета. Продукт реакции фурацилина и натрия гидроксида имеет максимум поглощения при длине волны 380 нм.
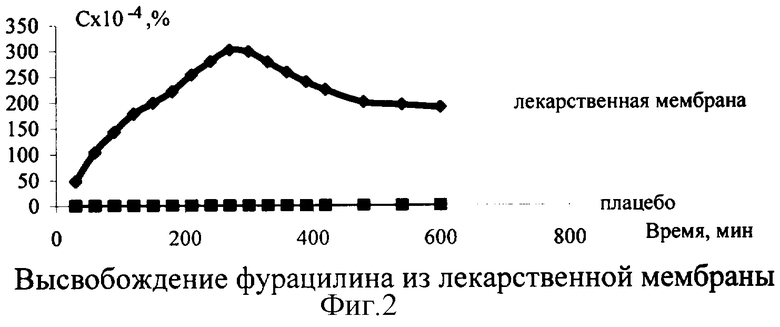
По полученным результатам строили графики зависимости концентрации фурацилина от времени. При этом раствором сравнения служила вода очищенная. Параллельно измеряли оптическую плотность диализной жидкости из лекарственной формы, не содержащей фурацилина (плацебо) (фиг.2).
Результаты, представленные на фиг.2, показывают, что на 1-м часе эксперимента в диализной жидкости создается бактерицидная концентрация фурацилина (1×10-6 г/мл), которая сохраняется на протяжении 10 часов наблюдения. Бактерицидную концентрацию определили предварительно по известной методике ГФ XI [4].
Для подтверждения антимикробной активности мембраны исследовали ее в опыте in vitro [4]. Полученные данные, представленные в таблице 4, свидетельствуют о высокой чувствительности микроорганизмов Е. coli и St. aureus к действию лекарственной формы.
Антимикробная активностьлекарственной мембра фурацилином
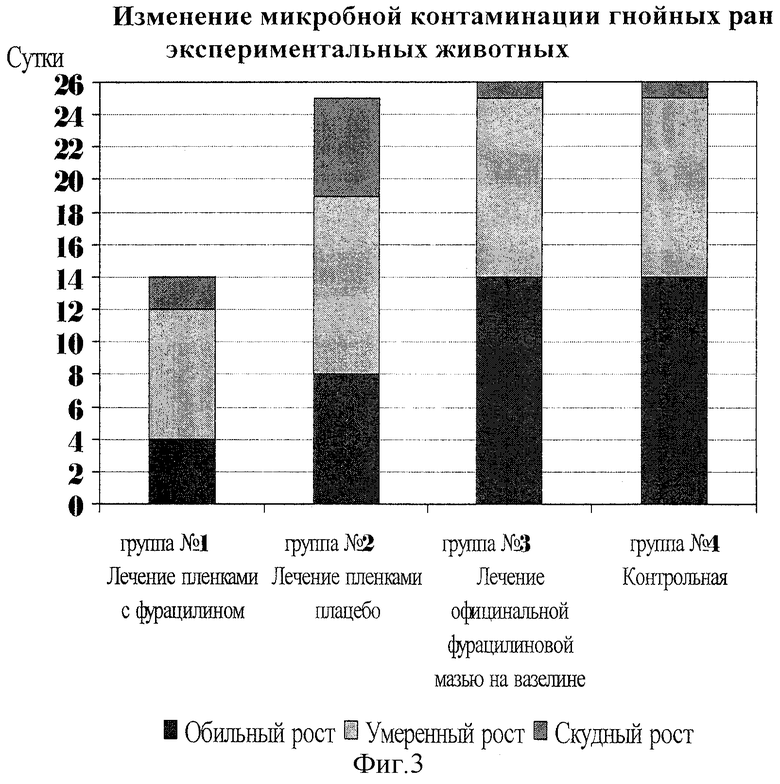
Для выявления корреляции опыта in vitro провели исследование антимикробного действия мембран на модели гнойной раны in vivo. Результаты свидетельствуют о выраженном антимикробном действии препарата (таблица 5) и о его способности оказывать эффективное заживляющее действие на гнойные раны (фиг.3, таблица 6).
Суммарный процент заживления ран при использовании лекарственных мембран с фурацилином (группа №1) составил к 25-м суткам 99,01%; мембраны плацебо (группа №2) - 90,43%; официнальной 0,2% мази фурацилина (группа №3) - 88,76%. В то время как в контрольной группе (группа №4) за аналогичный период заживление составило 78,68%. Результаты статистически достоверны (Р<0,05).
Бактериологическое исследование раневого содержимого у экспериментальных животных различных групп
Сроки заживления гнойных ран у экспериментальных животных разных групп
Таким образом, полученные экспериментальные данные создают основу для расширения ассортимента лекарственных средств антимикробного, осмотического, ранозаживляющего действия, используемых в хирургии, гинекологии, травматологии, дерматологии, оториноларингологии, офтальмологии, так как проведенный анализ лекарственных форм с фурацилином, зарегистрированных в Государственном реестре РФ [2] не позволили найти аналогичную лекарственную форму (табл.7).
ИСТОЧНИКИ ИНФОРМАЦИИ
1. Алексеева И.В. Разработка лекарственных форм для лечения ран //Фармация. - 2003. - №2. - С.43-45.
2. Государственный реестр лекарственных средств. - М., 2004 г. - Т.1. - 1404 с.
3. Государственная фармакопея Х изд. - М.: Медицина, 1968. - 1037 с.
4. Государственная фармакопея XI изд. - М.: Медицина, 1989.4.2 - С.187-225.
5. Грошовый Т.А. Математическое планирование эксперимента в фармацевтической технологии. / Т.А.Грошовый, Е.В.Маркова, В.А.Головкин. - Киев: Вища школа, 1992. - 185 с.
6. Патент РФ №2155071, выд. 27.08.2000 г.
7. Патент РФ №2179456, выд. 20.02.2002 г.
8. Справочник Видаль. - М.: АстраФармСервис, 2002 - 2005. - 1404 с.
Лекарственные формы с фурацилином, зарегистрированные в Государственном Реестре РФ
ФСП 42-0260-4472-03
| название | год | авторы | номер документа |
|---|---|---|---|
| СОСТАВ ПЛАСТИНЫ СОРБЦИОННОЙ | 2011 |
|
RU2474422C1 |
| КОМБИНИРОВАННОЕ АППЛИКАЦИОННОЕ ЛЕКАРСТВЕННОЕ ФИТОСРЕДСТВО | 2014 |
|
RU2561593C1 |
| СПОСОБ ЛЕЧЕНИЯ ПАРОДОНТИТА | 2005 |
|
RU2306925C2 |
| СПОСОБ ЛЕЧЕНИЯ ПОСЛЕРОДОВОГО ЭНДОМЕТРИТА | 2006 |
|
RU2309744C1 |
| Способ лечения гнойных ран | 1985 |
|
SU1421312A1 |
| СОРБЦИОННОЕ, АНТИМИКРОБНОЕ И ДЕЗОДОРИРУЮЩЕЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ НАРУЖНОГО ПРИМЕНЕНИЯ | 2011 |
|
RU2468795C1 |
| Фармацевтическая субстанция для лечения инфицированных ран различного генеза | 2018 |
|
RU2697869C1 |
| СТОМАТОЛОГИЧЕСКИЕ ФИТОПЛЕНКИ ДЛЯ ЛЕЧЕНИЯ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ ПАРОДОНТА И СЛИЗИСТОЙ ОБОЛОЧКИ ПОЛОСТИ РТА | 2016 |
|
RU2618392C1 |
| КОМПОЗИЦИЯ ДЛЯ ИЗОЛИРОВАНИЯ КИШЕЧНОГО АНАСТАМОЗА И ПРЕДОТВРАЩЕНИЯ ПОСЛЕОПЕРАЦИОННОГО СПАЕЧНОГО ПРОЦЕССА | 2022 |
|
RU2796007C1 |
| АНТИСЕПТИЧЕСКОЕ СРЕДСТВО | 2000 |
|
RU2163119C1 |
Изобретение относится к производству лекарственных форм в виде пленочных мембран для оказания кровоостанавливающего, ранозаживляющего, противовоспалительного действия в медицинской практике. Мембрана содержит в качестве лекарственного компонента фурацилин, в качестве пленкообразователя - хитозан, а также вспомогательные вещества - диметилсульфоксид, аэросил, кислоту уксусную 98% для изготовления ее 2% раствора и воду очищенную. Новая лекарственная мембрана обладает пролонгированным лечебным воздействием, что расширяет область ее применения. 3 ил., 7 табл.
Способ получения лекарственной мембраны, содержащей в качестве лекарственного компонента фурацилин, отличающийся тем, что в процессе получения использован в качестве пленкообразователя хитозан и дополнительно введены вспомогательные вещества диметилсульфоксид, аэросил, кислота уксусная 98%-ная для изготовления ее 2%-ного раствора и вода очищенная при следующем соотношении компонентов, мас.%:
| МАШКОВСКИЙ М.Д., Лекарственные средства, Москва, ООО «Новая Волна», 2001, с.302 | |||
| СПОСОБ ПОЛУЧЕНИЯ ЛЕКАРСТВЕННОЙ ФИТОПЛЕНКИ | 1999 |
|
RU2155071C1 |
| СПОСОБ ПОЛУЧЕНИЯ АППЛИКАЦИОННОГО СРЕДСТВА | 2001 |
|
RU2179456C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛЕКАРСТВЕННОЙ ФИТОПЛЕНКИ | 1999 |
|
RU2155071C1 |
Авторы
Даты
2008-01-27—Публикация
2005-07-20—Подача