Область техники, к которой относится изобретение
Настоящее изобретение относится к катализатору очистки для выхлопных газов, к способу его производства и к устройству на основе катализатора очистки для выхлопных газов, и в частности, относится к технологии производства катализатора очистки для выхлопных газов, в котором уровень оксидов азота (NOx), углеводородов (HC) и моноокиси углерода (CO), содержащихся в выхлопных газах, испускаемых двигателем внутреннего сгорания автомобиля или тому подобного устройства, во время работы при низкой температуре может одновременно и эффективно уменьшаться, так что выхлопные газы очищаются.
Уровень техники
При очистке выхлопных газов, содержащих, например, CO, HC, NO и NO2, благородные металлы (Pt, Rh, Pd и Ir) демонстрируют высокую производительность. По этой причине является предпочтительным использование указанных выше благородных металлов в катализаторе очистки для выхлопных газов. Эти благородные металлы, как правило, смешивают с Al2O3 или наносят на него с высоким отношением поверхность - масса вместе с добавками, такими как La, Ce и Nd. С другой стороны, смешанные оксиды (например, оксиды типа перовскита), приготавливаемые посредством объединения различных элементов, имеют исключительно широкий диапазон свойств. По этой причине для катализатора очистки для выхлопных газов является предпочтительным использование указанных выше смешанных оксидов. Кроме того, когда на смешанные оксиды наносится благородный металл, свойства благородного металла значительно изменяются. С этой точки зрения, предпочтительные рабочие характеристики очистки выхлопных газов могут быть получены в катализаторе очистки для выхлопных газов, в котором благородный металл наносят на смешанный оксид.
К настоящему времени разработаны различные катализаторы, рассмотренные выше, и предложена, например, технология, в которой скорость коалесценции благородного металла может быть снижена, когда носителем является перовскит, исходя из ухудшения свойств благородного металла с уменьшением количества активных центров, из-за коагуляции благородного металла (смотри формулу изобретения публикации нерассмотренной заявки на патент Японии №5-86259). Кроме того, предлагается другая технология, в которой восстановление PdO может быть уменьшено при использовании перовскита, в котором активный центр A является дефектным, исходя из восстановления PdO, который представляет собой активированные частицы в реакции восстановления NO, за счет чего PdO превращается в Pd, который является низкоактивной формой Pd, когда благородный металл представляет собой Pd (смотри формулу изобретения с реакциями, описанными в публикации нерассмотренной заявки на патент Японии №2003-175337). Обычно благородные металлы используются на носителе из Al2O3 или чего-либо подобного, либо по отдельности, либо в сочетании, но в жестких условиях, таких как в автомобиле, количество активных центров уменьшается из-за коагуляции, и активность значительно уменьшается. Для решения этой проблемы предлагается использовать благородные металлы вместе с другими элементами в форме смешанных оксидов. Что касается Pd, описываются, в частности, смешанные оксиды редкоземельных металлов и Pd (смотри формулу изобретения публикации нерассмотренной заявки на патент Японии №S61-209045, формулу изобретения публикации нерассмотренной заявки на патент Японии №HI-43347, формулу изобретения публикации нерассмотренной заявки на патент Японии №H4-27433, формулу изобретения публикации нерассмотренной заявки на патент Японии №H4-341343, формулу изобретения публикации нерассмотренной заявки на патент Японии №H7-88372 и формулу изобретения публикации нерассмотренной заявки на патент Японии №H10-277393).
Обычные катализаторы очистки для выхлопных газов демонстрируют достаточную производительность при восстановлении CO, HC и NOx (NO, NO2 и тому подобное), содержащихся в выхлопных газах, при движении транспортного средства, в особенности при работе при высоких температурах (не менее чем 400°С). Однако обычные катализаторы не могут демонстрировать достаточную производительность при восстановлении CO, HC и NOx для транспортного средства при его трогании с места или при работе на холостом ходу при низких температурах (ниже 400°C).
Как указано выше, причина того, что достаточная производительность очистки выхлопных газов не может быть получена при работе при низкой температуре, является следующей. В обычном катализаторе очистки для выхлопных газов благородный металл, например Pt, Rh или Pd, нанесен на Al2O3, имеющий высокое отношение поверхность - масса. Благодаря высокому отношению поверхность - масса у Al2O3 благородный металл преимущественно находится на носителе в высокодисперсном состоянии. Однако Al2O3 представляет собой стабильное соединение и не влияет со своей стороны на нанесенный благородный металл, в силу чего активность благородного металла не улучшается. Соответственно достаточная производительность во время работы при низкой температуре может не достигаться.
Кроме того, при движении транспортного средства предпочтительным является, чтобы Pd существовал в состоянии PdO, который является очень активным химически. Однако если даже Pd, нанесенный на Al2O3, изначально существует в состоянии PdO, Pd восстанавливается, переходя в металлическое состояние, при высоких температурах (не менее чем 900°C), и Pd коагулирует, количество активных центров уменьшается, при этом активность значительно уменьшается.
Описание изобретения
Настоящее изобретение осуществляется в свете указанных выше требований, и по этой причине целью его является создание катализатора очистки для выхлопных газов, у которого активность благородного металла улучшается и предотвращается уменьшение активности при высоких температурах, при этом может быть получена достаточная производительность, даже во время трогания с места транспортного средства или при его работе на холостом ходу при низких температурах (ниже 400°C), а также способ его получения и устройство на основе катализатора очистки для выхлопных газов.
Авторы настоящего изобретения интенсивно исследовали катализаторы очистки для выхлопных газов, у которых может проявляться достаточная производительность, даже при трогании с места транспортных средств или при его работе на холостом ходу при низких температурах (ниже 400°C). В результате обнаружено поддержание высокой активности при работе при низких температурах после воздействия высоких температур для катализатора очистки для выхлопных газов, полученного посредством нанесения оксида Pd на носитель из смешанного оксида типа перовскита, определяемого как LnAlO3 (Ln представляет собой любой редкоземельный элемент, включая La, Ce, Pr, Nd, Pm, Sm и тому подобное), полученный посредством спекания предшественника - соли сложного карбоксильного полимера.
Настоящее изобретение (первый аспект настоящего изобретения) было осуществлено в свете указанного выше знания. То есть катализатор очистки для выхлопных газов по настоящему изобретению представляет собой катализатор, в котором Pd наносится на оксид Al, и оксид представляет собой LnAlO3 (Ln - редкоземельный элемент).
Кроме того, авторы настоящего изобретения также обнаружили, что LaAlO3, среди соединений LnAlO3, является тригональным или ромбоэдрическим, а центр B в перовските представляет собой Al в LaAlO3, при этом дипольный момент LaAlO3 является большим, и локальный электрический заряд на PdO, связанном на LaAlO3, больше, чем у PdO, который существует независимо. По этой причине степень окисления Pd на поверхности нанесенного PdO представляет собой состояние Pd2+ на большой площади. Это состояние является предпочтительным состоянием для очистки выхлопных газов, при этом может быть получена высокая активность при низких температурах. В дополнение к этому авторы настоящего изобретения подтверждают, что данный катализатор может демонстрировать высокую активность при низких температурах даже после воздействия на катализатор рабочих условий примерно в 1000°C.
То есть в рассмотренном выше катализаторе очистки для выхлопных газов (первый аспект изобретения) является предпочтительным, чтобы оксид алюминия был тригональным или ромбоэдрическим (второй аспект настоящего изобретения).
Авторы попытались объединить оксид Pd со смешанным оксидом, содержащим Pd и, по меньшей мере, один редкоземельный элемент (например, Ln2PdO4), и нанести этот смешанный оксид на LnAlO3 (Ln - редкоземельный элемент), и обнаружили, что получается более высокая активность при низких температурах. Более конкретно, смешанный оксид Pd представляет собой соединение оксида Pd, которое является нестабильным при высокой температуре, и стабильного оксида редкоземельного элемента. По этой причине в смешанном оксиде Pd степень окисления Pd стабилизируется, и степень окисления Pd представляет собой Pd2+ на большой площади, что является предпочтительным для очистки выхлопных газов. В результате получается высокая активность при очистке выхлопных газов. В дополнение к этому, поскольку смешанный оксид Pd может сохраняться в состоянии оксида примерно до 1100°C, реализуется высокая термическая стойкость. Кроме того, смешанный оксид Pd представляет собой соединение редкоземельных элементов с невысокой степенью кристалличности и Pd, и получаемый смешанный оксид Pd представляет собой частицы с низкой степенью кристалличности, а следовательно, дисперсность Pd является высокой. Следовательно, увеличивается количество активных центров и получается высокая активность очистки выхлопных газов. В дополнение к этому катализатор по настоящему изобретению, имеющий смешанный оксид, нанесенный на LnAlO3, содержит редкоземельные элементы в обоих смешанных оксидах, и контактные поверхности двух смешанных оксидов частично образуют твердые растворы за счет редкоземельного элемента, и подвижность смешанного оксида Pd понижается, и подавляется взаимная коагуляция частиц смешанного оксида Pd, и получается высокая долговечность.
Настоящее изобретение (третий аспект настоящего изобретения) сделано в свете указанных выше знаний. То есть предпочтительно, третий аспект настоящего изобретения относится к катализатору очистки для выхлопных газов в первом или втором аспекте настоящего изобретения, в котором оксид Pd содержит, по меньшей мере, Ln2PdO4 (Ln редкоземельный элемент). В качестве смешанного оксида Pd наряду с Ln2PdO4 может содержаться также Ln2Pd2O5, Ln4PdO7 и тому подобное.
В способе получения LnAlO3 авторы пытались получить карбоксильный сложный полимер посредством выпаривания и отверждения водного раствора нитрата составляющих элементов, содержащего карбоновую кислоту, и обнаружили, что LnAlO3 получается в одной фазе, и, кроме того, что поверхность LnAlO3 легко взаимодействует с оксидом Pd, когда оксид Pd наносится на нее. В результате получается высокая активность при низкой температуре у катализатора очистки для выхлопных газов, имеющего оксид Pd, нанесенный на LnAlO3.
Настоящее изобретение (четвертый и пятый аспекты настоящего изобретения) выполнено в свете указанных выше знаний. То есть в указанных выше катализаторах очистки для выхлопных газов (первый и третий аспекты настоящего изобретения) является предпочтительным, чтобы, по меньшей мере, один вид соединения, выбранный из группы соединений (карбоновая кислота, имеющая гидроксильную группу или меркаптогруппу и имеющая количество атомов углерода от 2 до 20, дикарбоновая кислота, имеющая количество атомов углерода 2 или 3, и монокарбоновая кислота, имеющая количество атомов углерода от 1 до 20), добавлялся к водному раствору нитрата, содержащему компонент, при этом получается катализатор очистки для выхлопных газов (четвертый аспект настоящего изобретения). Кроме того, в катализаторах очистки для выхлопных газов (четвертый аспект настоящего изобретения) является предпочтительным, чтобы водный раствор нитрата выпаривался полностью с получением сложного полимера карбоновой кислоты и чтобы сложный полимер карбоновой кислоты нагревался, при этом получается катализатор очистки для выхлопных газов (пятый аспект настоящего изобретения).
В качестве карбоновой кислоты, имеющей гидроксильную группу или меркаптогруппу и имеющей количество атомов углерода от 2 до 20, упоминаются оксикарбоновая кислота и соединение, в котором атом кислорода в гидроксиле оксикарбоновой кислоты заменяется атомом серы. Количество атомов углерода этих карбоновых кислот составляет от 2 до 20 в свете растворимости в воде, предпочтительно равно от 2 до 12, более предпочтительно равно от 2 до 8 и наиболее предпочтительно от 2 до 6. Кроме того, количество атомов углерода в монокарбоновой кислоте равно 1-20, в свете растворимости в воде предпочтительно равно 1-12, более предпочтительно равно от 1 до 8 и наиболее предпочтительно 1-6.
Кроме того, в качестве конкретных примеров карбоновых кислот, имеющих гидроксильную группу или меркаптогруппу и имеющих количество атомов углерода от 2 до 20, перечисляются, например, гликолевая кислота, меркаптоянтарная кислота, тиогликолевая кислота, молочная кислота, β-гидроксипропионовая кислота, яблочная кислота, винная кислота, лимонная кислота, изолимонная кислота, аллолимонная кислота, глюконовая кислота, глиоксиловая кислота, глицериновая кислота, миндальная кислота, траловая кислота, бензиловая кислота и салициловая кислота. В качестве конкретных примеров монокарбоновых кислот перечисляются, например, муравьиная кислота, уксусная кислота, пропионовая кислота, масляная кислота, изомасляная кислота, валериановая кислота, изовалериановая кислота, гексановая кислота, гептановая кислота, 2-метилгексановая кислота, октановая кислота, 2-этилгексановая кислота, нонановая кислота, декановая кислота и лауриновая кислота. Среди указанных выше кислот предпочтительным является использование уксусной кислоты, щавелевой кислоты, малоновой кислоты, гликолевой кислоты, молочной кислоты, яблочной кислоты, винной кислоты, глиоксиловой кислоты, лимонной кислоты, глюконовой кислоты, а более предпочтительным является использование щавелевой кислоты, малоновой кислоты, гликолевой кислоты, молочной кислоты, яблочной кислоты, винной кислоты, глиоксиловой кислоты, лимонной кислоты или глюконовой кислоты.
Далее, способ получения катализатора очистки для выхлопных газов по настоящему изобретению (шестой аспект настоящего изобретения) представляет собой способ предпочтительного получения указанных выше катализаторов (первый-пятый аспекты настоящего изобретения). То есть шестой аспект настоящего изобретения представляет собой способ, в котором, когда катализатор очистки для выхлопных газов, в котором оксид Pd наносится на оксид алюминия, по меньшей мере, один вид соединения, выбранного из группы соединений (карбоновая кислота, имеющая гидроксильную группу или меркаптогруппу и имеющая количество атомов углерода от 2 до 20, дикарбоновая кислота, имеющая количество атомов углерода 2 или 3, и монокарбоновая кислота, имеющая количество атомов углерода от 1 до 20), добавляют к водному раствору нитрата, содержащему компонент, при этом получается катализатор очистки для выхлопных газов.
В указанном выше способе производства катализатора очистки для выхлопных газов (шестой аспект настоящего изобретения) является предпочтительным, чтобы водный раствор нитрата выпаривался полностью, с получением сложного полимера карбоновой кислоты и чтобы сложный полимер карбоновой кислоты нагревался (седьмой аспект настоящего изобретения), и является более предпочтительным, чтобы температура нагрева составляла не более чем 1000°C (восьмой аспект настоящего изобретения).
Указанный выше катализатор очистки для выхлопных газов и способ его производства представляют собой сущность настоящего изобретения, но авторы, кроме того, исследовали конкретные применения первого-восьмого аспектов настоящего изобретения и обнаружили, что катализатор очистки для выхлопных газов по настоящему изобретению является особенно пригодным для двигателя внутреннего сгорания автомобиля, и тем самым завершили девятый аспект настоящего изобретения.
Девятый аспект настоящего изобретения представляет собой катализатор очистки для выхлопных газов, предназначенный для очистки выхлопных газов от автомобиля, имеющий оксид Pd, нанесенный на оксид Al, в котором оксид Al представляет собой LnAlO3 (Ln - редкоземельный элемент).
Катализатор очистки для выхлопных газов по настоящему изобретению, в котором PdO нанесен на LnAlO3, имеет функцию, при которой восстановление PdO до металлического Pd может уменьшаться. Форма Ln (редкоземельного металла) изменяется в состояниях оксида в широких пределах. Например, когда катализатор, изготовленный посредством нанесения Pd на La2O3, экспонируются для условий высокой температуры, La2O3 мигрирует на зерна Pd из участка контакта между Pd и La2O3, при этом образуется форма заполнения La2O3 палладием Pd, что приводит к дополнительной миграции малых количеств La2O3 на поверхность Pd (Zhang et al., J. Phys. Chem., Vol.100, No.2, pp.744-755, 1996). Даже в настоящей системе (LnAlO3), Ln и Pd образуют сложное соединение, за счет чего может быть уменьшено восстановление PdO до металлического Pd. Благодаря этому эффекту катализатор очистки для выхлопных газов по настоящему изобретению может поддерживать состояние высокой активности при работе при низких температурах (ниже 400°C).
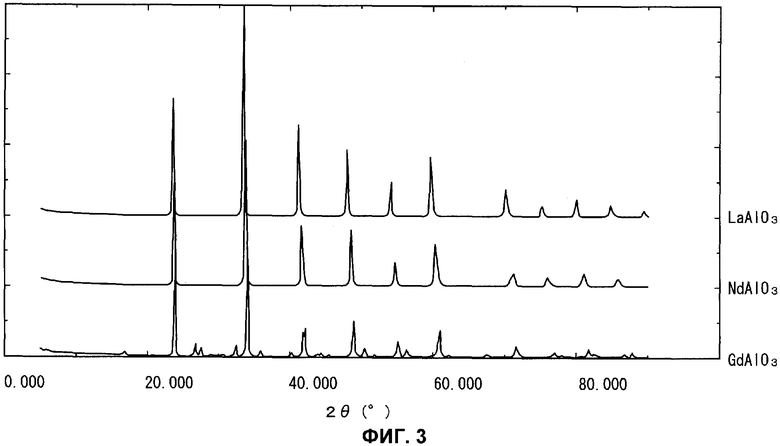
Кроме того, LnAlO3, например, LaAlO3, отличается тем, что кристаллическая система является тригональной или ромбоэдрической, и центр B перовскита представляет собой Al. Тригональной или ромбоэдрической является, как показано на фиг.1, кристаллическая система, в которой идеальная кубическая система элементарной ячейки изменяется в направлении c-оси, и угол между a-осью и b-осью равен 120°. То есть тригональная система представляет собой кристаллическую систему, в которой идеальная кубическая система структуры перовскита значительно деформируется. В кристаллической системе, электронное состояние составляющих атомов является исключительно нестабильным. В ромбоэдрической системе, как показано на фиг.2, тригональная система определяется тремя различными основными осями, а сама структура является такой же, как в тригональной системе. Фиг.3 представляет собой спектр РСА (дифрактограмму), в качестве данных, демонстрирующих разницу кристаллических систем LaAl3, на которые наносится Pd или оксид Pd. То есть, сравнивая структуры LaAlO3 и NdAlO3, и GdAlO3, которые представляют собой другие перовскиты, на которые наносятся Pd или оксид Pd в обычном катализаторе очистки для выхлопных газов, можно видеть из схемы, что кристаллические системы LaAlO3 и NdAlO3 являются тригональными или ромбоэдрическими, в то время как кристаллическая система GdAlO3 не является ни тригональной, ни ромбоэдрической, но является орторомбической.
С другой стороны, в LaAlO3, NdAlO3, центр B в перовските представляет собой Al, при этом связь между Al и O имеет высокую степень вероятности того, что она является ковалентной связью. Следовательно, некоторый дипольный момент генерируется в кристалле перовскита, который, в целом, имеет высокую степень вероятности оказаться ионной связью. Как описано выше, перовскит, то есть LaAlO3, NdAlO3, является тригональным или ромбоэдрическим, и центр B в смешанных оксидах типа перовскита представляет собой Al в оксидах, при этом дипольный момент оксидов больше чем у хорошо известного катализатора очистки для выхлопных газов, например, LaFeO3.
Благодаря дипольному моменту, локальный электрический заряд связи PdO на LaAlO3 или NdAlO3 является большим, чем там, где PdO существует независимо. По этой причине, степень окисления Pd на поверхности нанесенного слоя PdO представляет собой степень Pd2+на большой площади. Имеется две степени окисления Pd на поверхности PdO, которые представляют собой степень Pd2+ и степень Pd0 (металлическое состояние). То есть, в катализаторах очистки для выхлопных газов по настоящему изобретению, в которых PdO нанесен на LaAlO3 или NdAlO3, степень окисления Pd на поверхности PdO представляет собой степень Pd2+, при этом катализаторы по настоящему изобретению имеют высокую активность. Кроме того, катализаторы по настоящему изобретению могут демонстрировать высокую активность во время работы при низких температурах (ниже 400°C), даже после экспонирования катализатора для рабочих условий примерно 1000°C.
Кроме того, когда производится LaAlO3 или NdAlO3, водный раствор нитрата компонента, содержащего карбоновую кислоту, полностью выпаривают, с получением сложного полимера карбоновой кислоты, и полимер нагревают при относительно низкой температуре 800°C, при этом LaAlO3 или NdAlO3 генерируются как одна фаза.
С другой стороны, когда LaAlO3 или NdAlO3 производят другими способами, например, посредством твердофазной реакции, LaAlO3 или NdAlO3 не генерируются в виде одной фазы, даже если осуществляют нагрев при относительно высокой температуре 1700°C (смотри Rare Earth Science, Kagaku-Dojin Publishing Company, Inc, Ginya Adachi, p.564). То есть LaAlO3 или что-либо подобное в одной фазе может синтезироваться при указанной выше низкой температуре посредством использования карбоновой кислоты. Следовательно, может быть получено достаточное отношение поверхность - масса, и катализатор может использоваться в состоянии, в котором поверхность кристаллической решетки является активной. В катализаторе очистки для выхлопных газов, полученном посредством нанесения Pd на LnAlO3, с использованием способа по настоящему изобретению, может быть получено достаточное отношение поверхность - масса и сильное взаимодействие между LnAlO3 и Pd, при этом может быть реализована высокая активность при низких температурах.
В случае смешанного оксида Pd (например, Ln2PdO4), содержащего Pd и, по меньшей мере, один редкоземельный элемент, используемого как оксид Pd, в качестве составляющего элемента катализатора очистки для выхлопных газов по настоящему изобретению эффекты, реализуемые посредством этого смешанного оксида, объясняются ниже.
Смешанный оксид Pd представляет собой смешанное соединение нестабильного оксида Pd и очень стабильного оксида редкоземельного элемента. Например, в случае PdO поверхность PdO может иметь две степени окисления, Pd0 и Pd2+.
Однако в смешанном оксиде Pd в результате стабилизации степени окисления посредством редкоземельного элемента химическое состояние наружной поверхности соединения в основном представляет собой Pd2+. Если выбирать между Pd0 и Pd2+, то поскольку Pd2+имеет более высокую активность, в смешанном оксиде Pd получается высокая активность очистки выхлопных газов.
В то же время температура разложения PdO равна примерно 800°C, но при 1100°C смешанный оксид Pd по-прежнему присутствует в состоянии оксида. Следовательно, смешанный оксид Pd имеет высокую термическую стойкость. То есть Pd, у которого оксид является нестабильным при высокой температуре, объединяется с редкоземельным элементом или щелочноземельным элементом, который является стабильным в состоянии оксида, и связь Pd-O в объеме укрепляется. Смешанный оксид Pd представляет собой смешанное соединение редкоземельного элемента или щелочноземельного элемента с не слишком высокой степенью кристалличности и Pd. Следовательно, полученный смешанный оксид Pd имеет низкую степень кристалличности и высокую дисперсность Pd. В результате увеличивается количество активных центров и получается высокая производительность очистки выхлопных газов. В дополнение к этому, когда смешанный оксид редкоземельного элемента и Pd наносят на смешанный оксид, состоящий из LnAlO3, поскольку редкоземельные элементы содержатся в обоих смешанных оксидах, поверхности контакта двух смешанных оксидов частично образуют твердый раствор посредством редкоземельных элементов, и подвижность смешанного оксида Pd понижается и подавляется взаимная коагуляция частиц смешанного оксида Pd, и получается высокая долговечность.
Краткое описание чертежей
Фиг.1 представляет собой общий вид, показывающий пример кристаллической системы (тригональной) оксида Al, входящего в состав катализатора очистки для выхлопных газов по настоящему изобретению.
Фиг.2 представляет собой общий вид, показывающий пример кристаллической системы (ромбоэдрической) оксида Al, входящего в состав катализатора очистки для выхлопных газов по настоящему изобретению.
Фиг.3 представляет собой дифрактограмму XRD, показывающую разницу кристаллических систем различных оксидов Al, на которые наносятся оксиды Pd.
Наилучший способ осуществления изобретения
Далее настоящее изобретение будет конкретно объясняться посредством примеров.
<Пример получения 1>
Получение смешанных оксидов в качестве носителя
Заданные количества гексагидрата нитрата лантана и нонагидрата нитрата алюминия растворяют в воде, очищенной ионным обменом, при этом получается смешанный раствор. Далее растворяют заданное количество яблочной кислоты в воде, очищенной ионным обменом, при этом получают водный раствор яблочной кислоты. Эти два раствора смешивают, полученный смешанный раствор устанавливают на горячий столик с мешалкой и смешанный раствор нагревают до 250°C и перемешивают с помощью перемешивающего стержня, при этом осуществляется выпаривание воды в паровую фазу, осуществляется полное испарение, и высушенный образец измельчают в порошок с помощью ступки и пестика. Измельченный образец переносят в алюминиевый тигель, образец нагревают в муфельной печи до 350°C со скоростью 2,5°C/мин и осуществляют термическую обработку при 350°C в течение 3 часов. Благодаря термической обработке, получают промежуточное нагретое вещество, в котором удаляются малат и нитратный азот (нитратная соль и нитратный ион). После измельчения промежуточного нагретого вещества в порошок и перемешивания в течение 15 минут с помощью ступки и пестика полученную смесь опять помещают в алюминиевый тигель, образец нагревают в муфельной печи до 800°C со скоростью 5°C/мин и осуществляют термическую обработку при 800°C в течение 10 часов. Благодаря термической обработке получают смешанный оксид типа перовскита, композиция которого представляет собой LaAlO3.
Носитель для смешанного оксида Pd.
Смешанный водный раствор солей металлов получают посредством растворения заданных количеств дегидрата нитрата палладия и гексагидрата нитрата лантана в воде, очищенной ионным обменом. Водный раствор яблочный кислоты готовят посредством растворения заданного количества яблочной кислоты в воде, очищенной ионным обменом. Эти два водных раствора смешивают, и данную смесь и заданное количество порошка LaAlO3 помещают в круглодонную колбу с широким горлом и, эвакуируя колбу с помощью роторного испарителя, смесь выпаривают и отверждают на горячей бане при 60°C. Посредством нагрева в муфельной печи до 250°C со скоростью 2,5°C/мин температуру дополнительно повышают до 720°C со скоростью 5°C/мин и поддерживают равной 750°C в течение 3 часов. В результате получают порошкообразный катализатор Примера получения 1 из La2PdO4/LaAlO3, имеющий La2PdO4, пропитывающий LaAlO3 и нанесенный на него. Удельная площадь поверхности и степень дисперсности Pd для порошкообразного катализатора Примера получения 1 представлены в таблице 1.
Оценка активности
Далее оценивают начальные активности и активности после испытаний на долговечность для полученных порошкообразных катализаторов. Оценку осуществляют посредством протекания модельных выхлопных газов транспортного средства в катализаторы при условиях, в которых A/F (отношение воздух-горючее) практически равно 14,6, и SV (рабочий объем двигателя) равен 5000 час-1. Продолжительную работу осуществляют в течение 20 часов при температуре испытаний на долговечность 900°C посредством использования модельных выхлопных газов, в которых A/F (отношение воздух-горючее) практически равно 14,6. Эти результаты представлены в таблицах 2 и 3. То есть таблица 2 представляет температуры, при которых концентрации CO, HC и NO уменьшаются на 50% при исследовании катализаторов с повышением температуры перед испытаниями на долговечность. Кроме того, таблица 3 представляет температуру, при которой концентрации CO, HC, и NO уменьшаются на 50% при исследовании катализаторов с повышением температуры после испытаний на долговечность.
<Пример получения 2>
Таким же способом, как и в Примере получения 1, производят Nd2PdO4/LaAlO3 и осуществляют различные оценки для активности. Результаты представлены в таблицах 1-3.
<Пример получения 3>
Таким же способом, как и в Примере получения 1, производят Gd2PdO4/LaAlO3 и осуществляют различные оценки активности. Результат представлены в таблицах 1-3.
<Пример получения 4>
Таким же способом, как в Примере получения 1, производят La2PdO4/NdAlO3 и осуществляют различные оценки активности. Результат представлены в таблицах 1-3.
<Пример получения 5>
Таким же способом, как в и Примере получения 1, производят Pd/Al2O3 и осуществляют различные оценки активности. Результат представлены в таблице 1-таблице 3.
<Пример получения 6>
Заданные количества оксида лантана и оксида алюминия смешивают с помощью ступки и пестика, смешанный образец перемещают в алюминиевый тигель, образец нагревают в муфельной печи в течение 10 часов, при 1100°C, и получают LaAlO3 посредством твердофазной реакции. Используя его, наносят Tb2PdO4 таким же способом, как и в Примере получения 1, производят Tb2PdO4/LaAlO3, осуществляют различные оценки активности для этого катализатора. Результаты также представлены в таблицах 1-3.
<Пример получения 7>
Таким же способом, как и в Примере получения 1, производят La2PdO4/GdAlO3 и осуществляют различные оценки активности. Результаты представлены в таблицах 1-3.
В соответствии с таблицами 2 и 3 катализаторы очистки для выхлопных газов Примеров получения 1-3 демонстрируют превосходные температуры, при которых концентрация CO, HC и NO уменьшается на 50% при любом времени до и после испытаний на долговечность. Причина этого заключается в том, что катализаторы очистки для выхлопных газов Примеров получения 1-3 готовят посредством нанесения Pd на LaAlO3 (Ln - редкоземельный материал), и эти катализаторы имеют свойство подавления восстановления PdO до Pd при высоких температурах, при этом высокая активность может поддерживаться при работе при низких температурах после работы катализатора при высоких температурах. Также в катализаторах очистки для выхлопных газов в Примерах получения 1-4 кристаллическая система оксида Al является тригональной или ромбоэдрической, и центр B перовскита представляет собой Al, и следовательно, электрическая нестабильность является большей. Следовательно, оксид Pd рядом с LaAlO3 или NdAlO3 имеет больший локальный электрический заряд, чем независимый оксид Pd. Кроме того, в катализаторах очистки для выхлопных газов в Примерах получения 1-4, когда производится LaAlO3 или NdAlO3, посредством способа только лишь получения карбонового сложного полимера путем выпаривания и отверждения водного раствора нитрата составляющего элемента, содержащего карбоновую кислоту, LaAlO3 или NdAlO3 производится в одной фазе, и при нанесении оксида Pd состояние поверхности с большой вероятностью будет вызывать взаимодействие с оксидом Pd. В способе получения смешанного водного раствора используется яблочная кислота, но такие же эффекты получают посредством использования лимонной кислоты или щавелевой кислоты.
В противоположность этому у катализатора очистки для выхлопных газов в Примерах получения 5-7 достаточная производительность не может быть получена при низкой температуре работы по сравнению с катализатором очистки для выхлопных газов в Примерах получения 1-4, и причина является следующей. В Примере получения 5 Al2O3 представляет собой стабильное соединение, и он не взаимодействует с нанесенным благородным металлом Pd, и активность самого Pd не усиливается. В катализаторе очистки для выхлопных газов в Примере получения 6, хотя кристаллическая система оксида Al является тригональной или ромбоэдрической, LaAlO3 не может синтезироваться в одной фазе, поскольку карбоновая кислота не используется в способе получения катализатора. Следовательно, достаточная удельная площадь поверхности не получается, и поверхность кристаллической решетки не может использоваться в активном состоянии. У катализатора очистки для выхлопных газов в Примере получения 7 кристаллическая система оксида Al является орторомбической, и нахождение электронов среди атомов компонентов не является таким нестабильным, как в` тригональной или ромбоэдрической системе.
Катализатор очистки для выхлопных газов по настоящему изобретению может применяться в двигателе внутреннего сгорания автомобиля или тому подобного, где требуется очистка и восстановление, одновременно и эффективно, оксида азота (NOx), углеводородов (HC) и моноокиси углерода (CO), содержащихся в выхлопных газах.
| название | год | авторы | номер документа |
|---|---|---|---|
| КАТАЛИЗАТОР ОЧИСТКИ ВЫХЛОПНОГО ГАЗА, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ОБОРУДОВАНИЕ КАТАЛИЗАТОРА ОЧИСТКИ ВЫХЛОПНОГО ГАЗА | 2004 |
|
RU2316395C2 |
| КАТАЛИЗАТОР ДЛЯ ОЧИСТКИ ВЫХЛОПНОГО ГАЗА ДВИГАТЕЛЯ ВНУТРЕННЕГО СГОРАНИЯ И СПОСОБ ОЧИСТКИ ВЫХЛОПНОГО ГАЗА С ИСПОЛЬЗОВАНИЕМ УКАЗАННОГО КАТАЛИЗАТОРА | 2009 |
|
RU2457901C2 |
| КАТАЛИЗАТОР ДЛЯ ОЧИСТКИ ВЫХЛОПНОГО ГАЗА | 2018 |
|
RU2790008C2 |
| КАТАЛИЗАТОР ДЛЯ ОЧИСТКИ ВЫХЛОПНОГО ГАЗА | 2006 |
|
RU2372141C2 |
| ЖЕЛЕЗООКСИДНО-ЦИРКОНИЙОКСИДНЫЙ СМЕШАННЫЙ ОКСИД, СПОСОБ ЕГО ПОЛУЧЕНИЯ И КАТАЛИЗАТОР ОЧИСТКИ ВЫХЛОПНЫХ ГАЗОВ | 2013 |
|
RU2573022C1 |
| КАТАЛИЗАТОР ВЫХЛОПНЫХ ГАЗОВ И УСТРОЙСТВО ДЛЯ ОБРАБОТКИ ВЫХЛОПНЫХ ГАЗОВ, В КОТОРОМ ИСПОЛЬЗУЕТСЯ ЭТОТ КАТАЛИЗАТОР | 2007 |
|
RU2440187C2 |
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА ДЛЯ ОЧИСТКИ ВЫХЛОПНЫХ ГАЗОВ ДВИГАТЕЛЕЙ ВНУТРЕННЕГО СГОРАНИЯ | 2011 |
|
RU2465047C1 |
| КАТАЛИЗАТОРЫ ОЧИСТКИ ВЫХЛОПНОГО ГАЗА | 2014 |
|
RU2673344C2 |
| КАТАЛИЗАТОР ОЧИСТКИ ВЫХЛОПНОГО ГАЗА | 2016 |
|
RU2675373C9 |
| КАТАЛИЗАТОР ДЛЯ ОЧИСТКИ ВЫХЛОПНОГО ГАЗА И СПОСОБ ОЧИСТКИ ВЫХЛОПНОГО ГАЗА С ПРИМЕНЕНИЕМ УКАЗАННОГО КАТАЛИЗАТОРА | 2014 |
|
RU2621679C2 |

Изобретение относится к катализатору очистки для выхлопных газов, способу его производства и устройству на основе катализатора очистки для выхлопных газов. Описан катализатор очистки для выхлопных газов, содержащий оксид алюминия с нанесенным на него оксидом Pd, по меньшей мере, в виде Ln2PdO4, причем Ln представляет собой редкоземельный элемент, где оксид алюминия представляет собой LnAlO3, в котором Ln представляет собой редкоземельный элемент, и где кристаллическая система оксида алюминия является тригональной или ромбоэдрической. Описан также способ получения катализатора, включающий получение, по меньшей мере, одного вида соединения, выбранного из группы соединений, включающей карбоновую кислоту, имеющую гидроксильную группу или меркаптогруппу и имеющую количество атомов углерода от 2 до 20, дикарбоновую кислоту, имеющую количество атомов углерода 2 или 3, и монокарбоновую кислоту, имеющую количество атомов углерода от 1 до 20; добавление, по меньшей мере, одного соединения, выбранного из указанной группы соединений, к водному раствору нитрата, содержащему компоненты Al и редкоземельный металл; полное выпаривание водного раствора, содержащего карбоновую(-ые) кислоту(-ы), с получением сложного полимера карбоновой(-ых) кислоты(кислот); нагревание сложного полимера карбоновой(-ых) кислоты(кислот), так чтобы получить оксид Al; и нанесение оксида Pd на оксид Al. Описано устройство с катализатором очистки для выхлопных газов автомобиля, описанным выше. Технический эффект - эффективная очистка выхлопных газов при работе автомобиля на холостом ходу при низких температурах. 3 н.п., 2 з. ф-лы, 3 табл., 3 ил.
полного выпаривания водного раствора, содержащего карбоновую(-ые) кислоту(-ы), с получением сложного полимера карбоновой(-ых) кислоты(кислот);
нагревания сложного полимера карбоновой(-ых) кислоты (кислот), так чтобы получить оксид Al; и
нанесения оксида Pd на оксид Al.
получение, по меньшей мере, одного вида соединения, выбранного из группы соединений, включающей карбоновую кислоту, имеющую гидроксильную группу или меркаптогруппу и имеющую количество атомов углерода от 2 до 20, дикарбоновую кислоту, имеющую количество атомов углерода 2 или 3, и монокарбоновую кислоту, имеющую количество атомов углерода от 1 до 20;
добавление, по меньшей мере, одного соединения, выбранного из указанной группы соединений, к водному раствору нитрата, содержащему компоненты Al и редкоземельный металл;
полное выпаривание водного раствора, содержащего карбоновую(-ые) кислоту(-ы), с получением сложного полимера карбоновой(-ых) кислоты(кислот);
нагревание сложного полимера карбоновой(-ых) кислоты(кислот), так чтобы получить оксид Al; и
нанесение оксида Pd на оксид Al.
| Кипятильник для воды | 1921 |
|
SU5A1 |
| RU 2000109780 A, 27.03.2002 | |||
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА ОЧИСТКИ ОТРАБОТАВШИХ ГАЗОВ ДВИГАТЕЛЕЙ ВНУТРЕННЕГО СГОРАНИЯ | 2000 |
|
RU2190470C2 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Способ крашения тканей | 1922 |
|
SU62A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Способ запрессовки не выдержавших гидравлической пробы отливок | 1923 |
|
SU51A1 |
Авторы
Даты
2008-01-27—Публикация
2004-08-20—Подача