Область техники, к которой относится изобретение
Настоящее изобретение относится к катализатору очистки выхлопного газа, способу его получения и оборудованию катализатора очистки выхлопного газа и, особенно, относится к технологии получения катализатора очистки выхлопного газа, в котором оксиды азота (NOx), углеводород (НС) и монооксид углерода (СО), содержащиеся в выхлопном газе, исходящем из двигателя внутреннего сгорания (например, в транспортном средстве), могут быть одновременно эффективно снижены, таким образом, снижая нежелательные компоненты выхлопного газа.
Уровень техники
Для очистки выхлопного газа, содержащего, например, СО, НС и NO, демонстрируют высокую эффективность элементы благородных металлов (Pt, Rh, Pd и Ir). Поэтому предпочтительно применять вышеупомянутые элементы благородных металлов для катализатора очистки выхлопного газа. Указанные благородные металлы обычно наносят на Al2O3, который представляет собой носитель с высоким отношением поверхности к массе. С другой стороны, композитные оксиды (например, перовскитоподобный оксид), полученные объединением разных элементов, обладают исключительно варьируемыми свойствами. Поэтому для катализатора очистки выхлопного газа предпочтительно применять вышеупомянутые композитные оксиды. Кроме того, когда благородный металл наносят на композитные оксиды, свойства благородного металла значительно меняются. С данной точки зрения предпочтительное осуществление очистки выхлопного газа можно получить с катализатором очистки выхлопного газа, в котором благородный металл нанесен на композитный оксид.
Разработаны различные вышеупомянутые катализаторы и, например, предлагается технология, в которой скорость коалесценции благородного металла может быть уменьшена путем использования перовскитоподобного композитного оксида в качестве носителя, оценивая по ухудшению благородного металла уменьшение числа активных центров из-за коагуляции благородного металла (смотри формулу изобретения японской, нерассмотренной заявочной публикации №5-86259). Кроме того, предложена другая технология, в которой восстановление PdO может быть снижено использованием перовскитоподобного композитного оксида, в котором А центр является дефектным, оценивая уменьшение числа активных центров по восстановлению PdO, который представляет собой активные частицы в реакции восстановления NO, вследствие чего PdO переходит в Pd, который представляет собой малоактивный Pd, если благородный металл представляет собой Pd (смотри формулу изобретения японской, нерассмотренной публикации заявки №2003-175337).
Обычные катализаторы очистки выхлопного газа демонстрируют достаточную эффективность для снижения СО, НС и NOx, содержащихся в выхлопном газе, при работе транспортного средства, особенно во время работы при высокой температуре (не меньше, чем 400°С). Однако обычные катализаторы не могут демонстрировать достаточную эффективность для снижения СО, НС и NOx в транспортном средстве при его старте или на холостом ходу при низких температурах (не больше, чем 400°С).
Как отмечается выше, причина того, что достаточная эффективность очистки выхлопного газа не может быть получена при работе при низкой температуре, заключается в следующем. В обычном катализаторе очистки выхлопного газа благородный металл, например, Pt, Rh или Pd, наносят на Al2O3, имеющий высокое отношение поверхности к массе. Благодаря высокому отношению поверхности к массе Al2O3 благородный металл, предпочтительно, наносят в высокодисперсном состоянии. Однако Al2O3 представляет собой стабильное соединение и не оказывает влияния на нанесенный благородный металл, в соответствии с чем активность благородного металла не улучшается. Соответственно, достаточная эффективность во время работы при низкой температуре не может быть получена.
Кроме того, при работе транспортного средства для Pd предпочтительно существовать в виде PdO, который является сильно реакционноспособным. Однако, даже если Pd, нанесенный на Al2O3, изначально существует в виде PdO, Pd восстанавливается до металла при высоких температурах, в результате чего активность значительно снижается.
Описание изобретения
Данное изобретение было сделано в свете вышеуказанных требований, и, следовательно, его задачей является предложить катализатор очистки выхлопного газа, в котором активность благородного металла улучшена, и предотвращается уменьшение активности при высоких температурах, в результате чего может быть получена достаточная эффективность даже при старте транспортного средства или на холостом ходу при низких температурах (не больше, чем 400°С), и способ его получения, и оборудование катализатора очистки выхлопного газа.
Настоящие изобретатели интенсивно исследовали катализаторы очистки выхлопного газа, в которых может быть достигнута достаточная эффективность даже при старте транспортного средства или на холостом ходу при низких температурах (не больше, чем 400°С). В результате было установлено, что катализатор очистки выхлопного газа, приготовленный нанесением Pd на LnAlO3 (Ln: редкоземельный металл), имеет свойство подавлять восстановление PdO в Pd при высокой температуре, вследствие чего в вышеупомянутом катализаторе высокая активность может сохраняться во время работы при низких температурах после работы при высоких температурах.
Настоящее изобретение (первый аспект изобретения) было сделано в свете вышеприведенного знания. То есть катализатор очистки выхлопного газа по настоящему изобретению представляет собой катализатор, в котором Pd нанесен на оксид алюминия, и указанный оксид представляет собой LnAlO3 (Ln: редкоземельный металл).
Кроме того, настоящие изобретатели также выяснили, что LaAlO3 среди соединений LnAlO3 является тригональным или ромбоэдрическим, и В центр в перовскитоподобном композитном оксиде представляет собой Al в LaAlO3, вследствие чего дипольный момент LaAlO3 большой, и электрическая флуктуация PdO, связанного с LaAlO3, больше таковой для PdO, который существует независимо. Поэтому степень окисления Pd на поверхности PdO поддерживается в состоянии Pd2+ на большой площади. Данное состояние является предпочтительным состоянием для очистки выхлопного газа, вследствие чего может быть получена высокая активность при низких температурах. Кроме того, настоящие изобретатели подтвердили, что указанный катализатор может демонстрировать высокую активность при низких температурах даже после того, как катализатор подвергается воздействию температур около 1000°С.
Настоящее изобретение (второй аспект изобретения) было сделано в свете вышеприведенного знания. То есть в вышеуказанном катализаторе очистки выхлопного газа (первое изобретение) предпочтительно, чтобы оксид алюминия был тригональным или ромбоэдрическим.
Кроме того, настоящие изобретатели выяснили, что, когда получают LnAlO3, водный нитратный раствор компонента, содержащий водную карбоновую кислоту, можно выпаривать полностью, получая комплексный полимер карбоновой кислоты, вследствие чего LnAlO3 образуется в виде единственной фазы, и поверхность LnAlO3, несущая Pd, изменяется в конфигурацию, в которой взаимодействие с PdO более легкое.
Настоящее изобретение (третий и четвертый аспекты изобретения) было сделано в свете вышеприведенного знания. То есть в вышеуказанном катализаторе очистки выхлопного газа (первый и второй аспекты изобретения) предпочтительно, чтобы, по меньшей мере, один тип соединения, выбранного из группы карбоновая кислота, имеющая гидроксильную группу или меркаптогруппу и имеющая число атомов углерода от 2 до 20, дикарбоновая кислота, имеющая число атомов углерода 2 или 3, и монокарбоновая кислота, имеющая число углеродов от 1 до 20, был добавлен к водному раствору нитрата, включающему некоторый компонент, в результате чего получают катализатор очистки выхлопного газа (третий аспект изобретения). Кроме того, в катализаторе очистки выхлопного газа (третий аспект изобретения) предпочтительно, чтобы водный раствор нитрата был выпарен полностью, чтобы получить комплексный полимер карбоновой кислоты, и чтобы комплексный полимер карбоновой кислоты был нагрет, в результате чего получают катализатор очистки выхлопного газа (четвертый аспект изобретения).
В качестве карбоновой кислоты, имеющей гидроксильную группу или меркаптогруппу и имеющей число атомов углерода от 2 до 20, упоминаются оксикарбоновая кислота и соединение, в котором атом кислорода в гидроксильной группе оксикарбоновой кислоты замещен атомом серы. Число атомов углерода в указанных карбоновых кислотах составляет от 2 до 20, в свете растворимости в воде предпочтительно от 2 до 12, более предпочтительно от 2 до 8 и наиболее предпочтительно от 2 до 6. Кроме того, число атомов углерода монокарбоновой кислоты составляет от 1 до 20, в свете растворимости в воде предпочтительно от 1 до 12, более предпочтительно от 1 до 8 и наиболее предпочтительно от 1 до 6.
Более того, в качестве конкретных примеров карбоновых кислот, имеющих гидроксильную группу или меркаптогруппу и имеющих число атомов углерода от 2 до 20, приводятся, например, гликолевая кислота, меркаптоянтарная кислота, тиогликолевая кислота, молочная кислота, β-гидроксипропионовая кислота, яблочная кислота, винная кислота, лимонная кислота, изолимонная кислота, алло-лимонная кислота, глюконовая кислота, глиоксиловая кислота, глицериновая кислота, миндальная кислота, троповая кислота, бензильная кислота и салициловая кислота. В качестве конкретных примеров монокарбоновых кислот приводятся, например, муравьиная кислота, уксусная кислота, пропионовая кислота, масляная кислота, изомасляная кислота, валериановая кислота, изовалериановая кислота, гексановая кислота, гептановая кислота, 2-метилгексановая кислота, октановая кислота, 2-этилгексановая кислота, нонановая кислота, декановая кислота и лауриновая кислота. Из вышеуказанных кислот предпочтительно использовать уксусную кислоту, щавелевую кислоту, малоновую кислоту, гликолевую кислоту, молочную кислоту, яблочную кислоту, винную кислоту, глиоксиловую кислоту, лимонную кислоту, глюконовую кислоту и более предпочтительно использовать щавелевую кислоту, малоновую кислоту, гликолевую кислоту, молочную кислоту, яблочную кислоту, винную кислоту, глиоксиловую кислоту, лимонную кислоту, глюконовую кислоту.
Дополнительно, настоящие изобретатели особенно подробно исследовали катализатор очистки выхлопного газа, в котором редкоземельный металл находится в А центре перовскитоподобных сложных оксидов. LnAlO3 (Ln: редкоземельный металл) является тригональным или ромбоэдрическим. Поэтому электронное состояние очень нестабильно. Кроме того, в указанных оксидах Al находится в В центре перовскитоподобных композитных оксидов, вследствие чего существует дипольный момент благодаря сильной ковалентной связи между Al и О. Следовательно, дипольный момент LnAlO3 больше, чем дипольный момент обычного катализатора очистки выхлопного газа, например, LaFeO3. Благодаря свойствам LnAlO3 электрическая флуктуация PdO, связанного с LaAlO3, больше, чем таковая для PdO, который существует независимо, степень окисления Pd на поверхности нанесенного PdO представляет собой состояние Pd2+ на большой поверхности. В целом, Pd на поверхности PdO существует в двух состояниях Pd2+ и Pd0 (металлическое состояние). В указанных состояниях состояние Pd2+ имеет более высокую активность в качестве катализатора очистки выхлопного газа, чем состояние Pd0. То есть катализатор очистки выхлопного газа настоящего изобретения, в котором Pd нанесен на LnFeO3, имеет высокую активность, поскольку большая часть Pd на поверхности PdO существует в состоянии Pd2+. Кроме того, указанные катализаторы могут в равной степени сохранять состояние высокой активности даже после того, как катализаторы подвергались во время работы условиям 1000°С.
Настоящее изобретение (пятый аспект изобретения) было сделано в свете вышеприведенного знания. То есть в вышеуказанном катализаторе очистки выхлопного газа (аспекты изобретения от второго до четвертого) предпочтительно, чтобы Pd был нанесен на LnAlO3 (Ln: редкоземельный металл), и чтобы Pd существовал в состоянии Pd2+ на поверхности нанесенного Pd (пятый аспект изобретения).
Затем способ получения катализатора очистки выхлопного газа настоящего изобретения (шестой аспект изобретения) представляет собой способ предпочтительного получения вышеупомянутых катализаторов (аспекты изобретения от первого до пятого). То есть шестой аспект изобретения представляет собой способ, в котором, когда катализатор очистки выхлопного газа представляет собой Pd, нанесенный на оксид алюминия, по меньшей мере, один вид соединений, выбранный из группы соединений (карбоновая кислота, имеющая гидроксильную группу или меркаптогруппу и имеющая число атомов углерода от 2 до 20, дикарбоновая кислота, имеющая число атомов углерода 2 или 3, и монокарбоновая кислота, имеющая число атомов углерода от 1 до 20), добавляют к водному нитратному раствору, включающему некоторый компонент, в результате чего получают катализатор очистки выхлопного газа.
В вышеупомянутом способе получения катализатора очистки выхлопного газа (шестой аспект изобретения) предпочтительно, чтобы водный нитратный раствор выпаривали полностью, получая комплексный полимер карбоновой кислоты, и чтобы комплексный полимер карбоновой кислоты нагревали (седьмой аспект изобретения), и более предпочтительно, чтобы температура нагрева не превышала 1000°С (восьмой аспект изобретения).
Кроме того, приспособление для каталитической очистки выхлопного газа (девятый аспект изобретения), получаемое с использованием вышеупомянутого катализатора очистки выхлопного газа (аспекты изобретения от первого до пятого), является желательным для внутреннего сгорания, например, в транспортном средстве, особенно потому, что оксиды азота (NOx), углеводород (НС) и монооксид углерода (СО), содержащиеся в выхлопном газе, можно одновременно и эффективно снижать посредством использования данного оборудования.
Катализатор очистки выхлопного газа настоящего изобретения, в котором Pd нанесен на LnAlO3, имеет функцию, в которой восстановление PdO до металлического Pd может быть снижено. Форма Ln (редкоземельный металл) различным образом меняется в состояниях оксида. Например, когда катализатор, полученный нанесением Pd на La2O3, подвергают высокотемпературным условиям, La2O3 мигрирует на зерно Pd из области контакта между Pd и La2O3, вследствие чего образуется форма заполнения La2O3 палладием, приводя к дополнительной миграции незначительных количеств La2O3 на поверхность Pd (Zhang et al., J. Phys / Chem., Vol.100, No.2, pp.744-755, 1996). Даже в настоящей системе (LnAlO3) Ln и Pd образуют сложное соединение, вследствие чего может быть снижено восстановление PdO до металлического Pd. Благодаря данному эффекту катализатор очистки выхлопного газа по настоящему изобретению может сохранять высокоактивное состояние во время работы при низких температурах (не больше, чем 400°С).
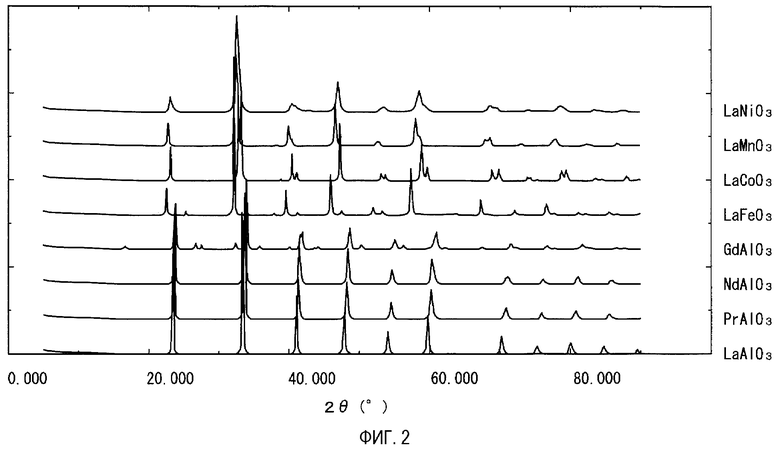
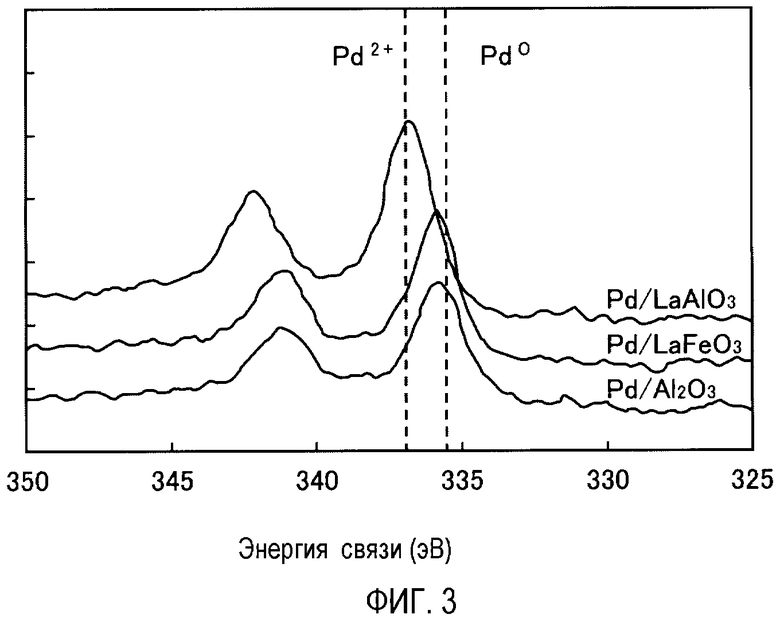
Кроме того, среди LnAlO3, например, LaAlO3 (включая в себя Pd/PrAlO3 или Pd/NdAlO3) характеризуется тем, что кристаллическая система является тригональной или ромбоэдрической. Тригональной или ромбоэдрической является, как показано на фиг.1, кристаллическая система, в которой идеальная кубическая система единичной решетки изменена в направлении оси с, и угол между осью а и осью b равен 120°С. То есть, тригональной или ромбоэдрической является кристаллическая система, в которой идеальная кубическая система структуры перовскита значительно искажена. В данной кристаллической системе состояние электронов составляющих атомов очень нестабильно. Фиг.2 представляет собой график, показывающий РДА спектр в качестве данных, подтверждающих различия кристаллических систем LaAlO3 с нанесенным Pd и др. То есть когда сравнивают Pd/LaAlO3, Pd/PrAlO3, Pd/NdAlO3 и другие перовскитоподобные композитные оксиды, несущие Pd, которые представляет собой обычные катализаторы очистки выхлопного газа (Pd/GdAlO3, Pd/LaCoO3, Pd/LaFeO3 и Pd/LaMnO3), разница в интенсивности основного пика и отклонение положения других пиков показаны на фиг.2. Соответственно, полагая, что LaAlO3, PrAlO3 или NdAlO3 являются тригональными или ромбоэдрическими, другие перовскитоподобные композитные оксиды (GdAlO3, LaCoO3, LaFeO3 или LaMnO3) не являются тригональными или ромбоэдрическими, а являются ромбическими. Кроме того, в обычном катализаторе очистки выхлопного газа LaNiO3 не имеет отличия в интенсивности основного пика и отклонении положения других пиков от LaAlO3, вследствие чего LaNiO3 является тригональным или ромбоэдрическим.
С другой стороны, в LaAlO3, PrAlO3 и NdAlO3 В центр в перовскитоподобном композитном оксиде представляет собой Al, вследствие чего связь между Al и О с высокой степенью вероятности является ковалентной связью. Поэтому создается некоторый дипольный момент в кристалле перовскитоподобного композитного оксида, который обычно имеет высокую степень вероятности ионной связи. Как описано выше, перовскитоподобные композитные оксиды, т.е. LaAlO3, PrAlO3 и NdAlO3, являются тригональными или ромбоэдрическими, и В центр в перовскит-подобных композитных оксидах представляет собой Al в оксидах, вследствие чего дипольный момент указанных оксидов больше, чем дипольный момент хорошо известного катализатора очистки выхлопного газа, например, LaFeO3.
Благодаря дипольному моменту электрическая флуктуация PdO, связанного с LaAlO3, PrAlO3 и NdAlO3, больше, чем таковая, когда PdO существует независимо. Поэтому степень окисления Pd на поверхности нанесенного PdO представляет собой состояние Pd2+ на большой поверхности. На поверхности PdO есть две степени окисления Pd, которые представляют собой состояние Pd2+ и состояние Pd0 (металлическое состояние). Состояние Pd2+ имело более высокую активность, чем состояние Pd0. То есть в катализаторе очистки выхлопного газа настоящего изобретения, в котором Pd нанесен на LaAlO3, PrAlO3 и NdAlO3, степень окисления Pd на поверхности PdO представляет собой состояние Pd2+, вследствие чего катализаторы настоящего изобретения имеют высокую активность. Кроме того, катализаторы настоящего изобретения могут демонстрировать высокую активность во время работы при низких температурах (не больше, чем 400°С) даже после воздействия на катализатор рабочих условий около 1000°С.
Более того, когда получают LaAlO3, PrAlO3 или NdAlO3, водный нитратный раствор компонента, содержащего карбоновую кислоту, выпаривают полностью, получая комплексный полимер карбоновой кислоты, и данный полимер нагревают при относительно низкой температуре 800°С, вследствие чего LaAlO3, PrAlO3 или NdAlO3 получаются в виде единственной фазы. С другой стороны, когда LaAlO3, PrAlO3 и NdAlO3 получают другими путями, например, твердофазной реакцией, LaAlO3, PrAlO3 или NdAlO3 не образуются в виде единственной фазы, даже если нагревание проводят при относительно высокой температуре 1700°С (смотри Rare Earth Science, Kagaku-Dojin Publishing Company, Inc., Ginya Adachi, p.564). То есть LaAlO3, PrAlO3 и NdAlO3 в виде единственной фазы можно синтезировать при вышеупомянутой низкой температуре с использованием карбоновой кислоты. Поэтому может быть получено достаточное отношение поверхности к массе, и катализатор можно использовать в состоянии, в котором поверхность кристаллической решетки является активной. В катализаторе очистки выхлопного газа, полученном нанесением Pd на LnAlO3, используя способ по настоящему изобретению, можно получить достаточное отношение поверхности к массе и сильное взаимодействие между LnAlO3 и Pd, в результате чего может быть реализована высокая активность при низких температурах.
Как указано выше, LnAlO3 (Ln: редкоземельный металл) является тригональным или ромбоэдрическим, вследствие чего состояние электронов составляющих атомов в LnAlO3 очень нестабильно, и связь между Al и О представляет собой сильную ковалентную связь, вследствие чего создается некоторый дипольный момент. Поэтому большая часть Pd, нанесенного на данные оксиды, существует в состоянии Pd2+. Чтобы доказать это, в Pd/LaAlO3, который является репрезентативным для настоящего изобретения, и в Pd/LaFeO3 и Pd/Al2O3, которые являются репрезентативными для обычной технологии, состояния Pd на поверхности PdO были изучены с помощью РФЭС (рентгеновская фотоэмиссионная спектроскопия). В общем, положение пика металлического компонента (Pd0) Pd составляет 335,5±0,3 эВ. С другой стороны, положение пика ионного компонента (Pd2+) Pd составляет 336,6±0,4 эВ. Основываясь на данном факте и результатах, показанных на фиг.3, в Pd/LaAlO3 есть пик в положении, которое эквивалентно Pd2+, и в Pd/LaFeO3 и Pd/Al2O3 есть пик в положении, которое эквивалентно Pd0. Соответственно, Pd на поверхности LaAlO3 находится, в основном, в состоянии Pd2+. Кроме того, состояния Pd на поверхности LaAlO3 подтверждены, как упомянуто выше, в результате чего состояния Pd на поверхности другого LnAlO3 (Ln: редкоземельный металл), например, PrAlO3 и NdAlO3 оценены аналогично.
Краткое описание чертежей
Фиг.1 представляет собой вид в перспективе, показывающий кристаллическую систему LaAlO3, составляющую катализатор очистки выхлопных газов по настоящему изобретению.
Фиг.2 представляет собой график, показывающий данные спектра рентгеновской дифракции (РДА), подтверждающие различия кристаллических систем LaAlO3, несущих Pd, и т.д.
Фиг.3 представляет собой график, показывающий окрестности 3d орбитали Pd, рассматриваемые относительно состояний Pd на поверхности PdO, с помощью РФЭС, в Pd/LaAlO3, который представляет собой пример настоящего изобретения, в Pd/LaFeO3 и в Pd/Al2O3, которые представляют собой пример общепринятой методики.
Лучший режим выполнения изобретения
Ниже данное изобретение будет конкретно объяснено примерами.
Практические примеры от 1 до 3
Получение композитных оксидов в качестве носителя
Заранее заданные количества гексагидрата нитрата лантана и нонагидрата нитрата алюминия растворяли в ионообменной воде, в результате чего получали смешанный раствор. Затем заранее определенное количество яблочной кислоты растворяли в ионообменной воде, в результате чего получали водный раствор яблочной кислоты. Данные два раствора смешивали, полученный смешанный раствор устанавливали на подогреваемую пластину с мешалкой, и смешанный раствор нагревали до 250°С и перемешивали с помощью мешалки, в результате чего происходило испарение воды, после полного испарения воды высушенный образец измельчали в ступке с пестиком. Измельченный образец переносили в алюминиевый тигель и нагревали до 350°С со скоростью подъема температуры 2,5°С/мин в муфельной печи, и выдерживали при 350°С в течение 3 часов. Благодаря термической обработке получали предварительно прогретое вещество, из которого был удален малат и нитратный азот (нитратная соль и нитратный ион). После измельчения предварительно прогретого вещества в порошок и перемешивания в ступке с пестиком в течение 15 минут полученную смесь снова помещали в алюминиевый тигель, и образец нагревали до 800°С со скоростью 5°С/мин в муфельной печи и прокаливали при 800°С в течение 10 часов. Благодаря термообработке получали перовскитоподобный композитный оксид, который имел композицию LaAlO3. Кроме того, аналогичным способом получали перовскитоподобные композитные оксиды с композициями PrAlO3 и NdAlO3.
Нанесение благородного металла
Затем определенное заранее количество дегидрата нитрата палладия растворяли в ионообменной воде, в результате чего получали водный раствор нитрата палладия. Нитрат палладия и определенное заранее количество LaAlO3, PrAlO3 или NdAlO3, находящихся в виде порошка, помещали в колбу, имеющую форму баклажана, и образец полностью высушивали на горячей водяной бане при 60°С при понижении давления в колбе с помощью роторного испарителя. После этого образец нагревали до 250°С со скоростью 2,5°С/мин в муфельной печи, затем продолжали нагревание до 750°С со скоростью 5°С/мин и выдерживали при 750°С в течение 3 часов. Благодаря данным обработкам получали порошки катализаторов Практических примеров от 1 до 3 с композициями Pd/LaAlO3, Pd/PrAlO3, и PdNdAlO3, в которых PdO был импрегнирован и нанесен на перовскитоподобные композитные оксиды. Отношение поверхность к массе для указанных катализаторов показано в таблице 1.
Оценка активности
Затем для полученных порошков катализаторов оценивали начальные активности и активности после продолжительного испытания. Оценку проводили для потоковой модели выхлопного газа транспортного средства на катализаторе при условиях, в которых В/Г (отношение воздух-горючее), в значительной степени, равно 14,6 и УО (ударный объем) составляет 5000 ч-1. Продолжительные испытания проводили в течение 20 часов при температуре продолжительного испытания, равной 900°С, с использованием модели выхлопного газа, в которой В/Г (отношение воздух-горючее) составляло, в значительной степени, 14,6. Полученные результаты показаны на фиг.2 и фиг.3. То есть на фиг.2 представлены температуры, при которых СО, НС и NO уменьшались на 50% при тестировании с увеличением температуры катализаторов перед продолжительным испытанием. Кроме того, на фиг.3 представлены температуры, при которых СО, НС и NO уменьшались на 50% при тестировании с увеличением температуры катализаторов после продолжительного испытания.
Сравнительный пример 1
Pd/Al2O3 получали способом, аналогичным способу в практическом примере 1, и проводили различные оценки активности.
Температуру продолжительного испытания устанавливали 900°С. Результат также показан в таблицах от 1 до 3.
Сравнительный пример 2
Pd/GdAlO3 получали способом, аналогичнымспособу в практическом примере 1. Кристаллическая система GdAlO3 является ромбической. Проводили различные оценки активности для данного катализатора. Температуру продолжительного испытания устанавливали 900°С. Результат также показан в таблицах от 1 до 3.
Сравнительный пример 3
Pd/LaNiO3 получали способом, аналогичнымспособу в практическом примере 1. LaNiO3 является тригональным или ромбоэдрическим. Проводили различные оценки активности для данного катализатора. Температуру продолжительного испытания устанавливали 800°С. Результат также показан в таблицах от 1 до 3.
Сравнительный пример 4
Pd/LaMnO3 получали способом, аналогичнымспособу в практическом примере 1. Кристаллическая система LaMnO3 является ромбической. Проводили различные оценки активности для данного катализатора. Температуру продолжительного испытания устанавливали 900°С. Результат также показан в таблицах от 1 до 3.
Сравнительный пример 5
Pd/LaCoO3 получали способом, аналогичнымспособу в практическом примере 1. Кристаллическая система LaCoO3 является ромбической. Проводили различные оценки активности для данного катализатора. Температуру продолжительного испытания устанавливали 800°С. Результат также показан в таблицах от 1 до 3.
Сравнительный пример 6
Pd/LaFeO3 получали способом, аналогичнымспособу в практическом примере 1. Кристаллическая система LaFeO3 является ромбической. Проводили различные оценки активности для данного катализатора. Температуру продолжительного испытания устанавливали 900°С. Результат также показан в таблицах от 1 до 3.
Сравнительный пример 7
Заданное количество оксида лантана и оксида алюминия смешивали в ступке пестиком, смешанный образец переносили в тигель, образец нагревали в течение 10 часов при 1100°С в муфельной печи, и LaAlO3 получали в результате твердофазной реакции. Благородный металл наносили способом, аналогичным способу в практическом примере 1, используя LaAlO3, в результате чего получали Pd/LaAlO3. Проводили различные оценки активности для данного катализатора. Температуру продолжительного испытания устанавливали 900°С. Результат также показан в таблицах от 1 до 3.
Согласно таблицам 2 и 3, катализаторы очистки выхлопного газа в практических примерах от 1 до 3 показали превосходные температуры, при которых CO, HC и NO уменьшались на 50% в любое время до или после продолжительного испытания. Причиной этого является то, что катализаторы очистки выхлопного газа получили нанесением Pd на LaAlO3, PrAlO3 или NdAlO3, и данные катализаторы имеют свойство подавлять восстановление PdO до Pd при высоких температурах, в результате чего высокая активность может сохраняться при испытаниях катализаторов при низких температурах после испытаний при высоких температурах. Кроме того, катализаторы очистки выхлопных газов в практических примерах от 1 до 3 являются тригональными или ромбоэдрическими, и В участок в перовскитоподобном композитном оксиде представляет собой Al в катализаторах практических примеров от 1 до 3, в результате чего дипольный момент катализатора является большим. Таким образом, электрические флуктуации PdO, связанного с LaAlO3, PrAlO3, или NdAlO3 являются большими, чем флуктуации PdO, который существует независимо. Кроме того, в катализаторах очистки выхлопного газа в практических примерах от 1 до 3 при получении LaAlO3, PrAlO3 или NdAlO3 водный раствор нитрата элемента, содержащий карбоновую кислоту, полностью упаривали с получением комплексного полимера карбоновой кислоты, в результате чего LaAlO3, PrAlO3 или NdAlO3 получали в качестве единственной фазы, и поверхность LaAlO3, PrAlO3 или NdAlO3, несущих Pd, имела форму, при которой взаимодействие с PdO осуществляется легко. Кроме того, при получении смешанного раствора можно использовать яблочную кислоту, как упомянуто выше, и если использовать лимонную или щавелевую кислоту, будет получен тот же эффект.
С другой стороны, катализаторы очистки выхлопного газа в сравнительных примерах от 1 до 7 не могут показать отличной температуры, при которой СО, НС и NO уменьшаются на 50% в любое время до или после продолжительного испытания. Причиной является следующее. В катализаторе сравнительного примера 1 Al2O3 представляет собой стабильное соединение, и Al2O3 не оказывает влияния на нанесенный благородный металл, вследствие чего активность Pd не улучшается. В катализаторе сравнительного примера 2 кристаллическая система является ромбической, вследствие чего электронное состояние в составляющих атомах не является более неустойчивым по сравнению с тригональной или ромбоэдрической системами. В катализаторе сравнительного примера 3, даже хотя кристаллическая система является тригональной или ромбоэдрической, Al не находится в B центре перовскитоподобного композитного оксида, вследствие чего трудно создать некоторый дипольный момент в кристалле перовскитоподобных композитных оксидов, который обычно имеет высокую степень вероятности существовать как ионная связь. В катализаторах сравнительных примеров от 4 до 6 кристаллическая система является ромбической, вследствие чего электронные состояния составляющих атомов не являются более неустойчивыми по сравнению с тригональной или ромбоэдрической системами. В катализаторе сравнительного примера 7 карбоновая кислота не использовалась при получении катализатора, вследствие чего LaAlO3 не генерировался как единственная фаза. Поэтому удовлетворительное отношение поверхность к массе не было получено, и поверхность кристаллической решетки не могла быть использована в активном состоянии.
Катализатор очистки выхлопного газа по настоящему изобретению может быть использован в двигателях внутреннего сгорания транспортных средств, в которых требуется в последнее время, чтобы оксид азота (NOx), углеводород (НС) и оксид углерода (СО) в выхлопном газе одновременно и эффективно очищались и снижались.
| название | год | авторы | номер документа |
|---|---|---|---|
| КАТАЛИЗАТОР ОЧИСТКИ ДЛЯ ВЫХЛОПНЫХ ГАЗОВ, СПОСОБ ЕГО ПРОИЗВОДСТВА И УСТРОЙСТВО НА ОСНОВЕ КАТАЛИЗАТОРА ОЧИСТКИ ДЛЯ ВЫХЛОПНЫХ ГАЗОВ | 2004 |
|
RU2315657C1 |
| КАТАЛИЗАТОР ДЛЯ ОЧИСТКИ ВЫХЛОПНОГО ГАЗА ДВИГАТЕЛЯ ВНУТРЕННЕГО СГОРАНИЯ И СПОСОБ ОЧИСТКИ ВЫХЛОПНОГО ГАЗА С ИСПОЛЬЗОВАНИЕМ УКАЗАННОГО КАТАЛИЗАТОРА | 2009 |
|
RU2457901C2 |
| КАТАЛИЗАТОР ДЛЯ ОЧИСТКИ ВЫХЛОПНОГО ГАЗА | 2006 |
|
RU2372141C2 |
| КАТАЛИЗАТОР ДЛЯ ОЧИСТКИ ВЫХЛОПНОГО ГАЗА | 2018 |
|
RU2790008C2 |
| ЖЕЛЕЗООКСИДНО-ЦИРКОНИЙОКСИДНЫЙ СМЕШАННЫЙ ОКСИД, СПОСОБ ЕГО ПОЛУЧЕНИЯ И КАТАЛИЗАТОР ОЧИСТКИ ВЫХЛОПНЫХ ГАЗОВ | 2013 |
|
RU2573022C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА ДЛЯ ОЧИСТКИ ВЫХЛОПНЫХ ГАЗОВ ДВИГАТЕЛЕЙ ВНУТРЕННЕГО СГОРАНИЯ | 2011 |
|
RU2465047C1 |
| КАТАЛИЗАТОР ВЫХЛОПНЫХ ГАЗОВ И УСТРОЙСТВО ДЛЯ ОБРАБОТКИ ВЫХЛОПНЫХ ГАЗОВ, В КОТОРОМ ИСПОЛЬЗУЕТСЯ ЭТОТ КАТАЛИЗАТОР | 2007 |
|
RU2440187C2 |
| КАТАЛИЗАТОР ОЧИСТКИ ВЫХЛОПНЫХ ГАЗОВ И СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ | 2006 |
|
RU2370308C1 |
| КАТАЛИЗАТОР ОЧИСТКИ ВЫХЛОПНОГО ГАЗА | 2016 |
|
RU2675373C9 |
| КАТАЛИЗАТОРЫ ОЧИСТКИ ВЫХЛОПНОГО ГАЗА | 2014 |
|
RU2673344C2 |
Настоящее изобретение относится к катализатору очистки выхлопного газа, способу его получения и оборудованию катализатора очистки выхлопного газа. Описан способ получения катализатора очистки выхлопного газа, включающий: приготовление, по меньшей мере, соединения одного вида, выбранного из группы соединений карбоновых кислот, имеющих гидроксильную группу или меркаптогруппу, и имеющих число атомов углерода от 2 до 20, дикарбоновых кислот, имеющих число атомов углерода 2 или 3, монокарбоновых кислот, имеющих число атомов углерода от 1 до 20; добавление, по меньшей мере, одного соединения, выбранного из группы, к водному раствору нитрата, включающему А1 и редкоземельный элемент; полное выпаривание водной карбоновой кислоты с получением комплекса полимера на основе карбоновой кислоты; нагревание комплексного полимера на основе карбоновой кислоты до не более чем 1000°С с образованием оксида алюминия; нанесение палладия на оксид алюминия. Описаны также оксид алюминия в качестве носителя Pd, в котором оксид алюминия представляет собой PrAlO3 или NdAlO3, катализатор очистки выхлопного газа, содержащий LnAlO3 (Ln: редкоземельный металл) в качестве носителя Pd, полученный описанным выше способом, и оборудование катализатора очистки выхлопного газа, содержащее указанный катализатор. Технический эффект - повышение активности катализатора, приводящее к повышению качества работы двигателя даже при низкой темературе при старте или холостом ходе. 4 н. и 2 з.п. ф-лы, 3 ил., 3 табл.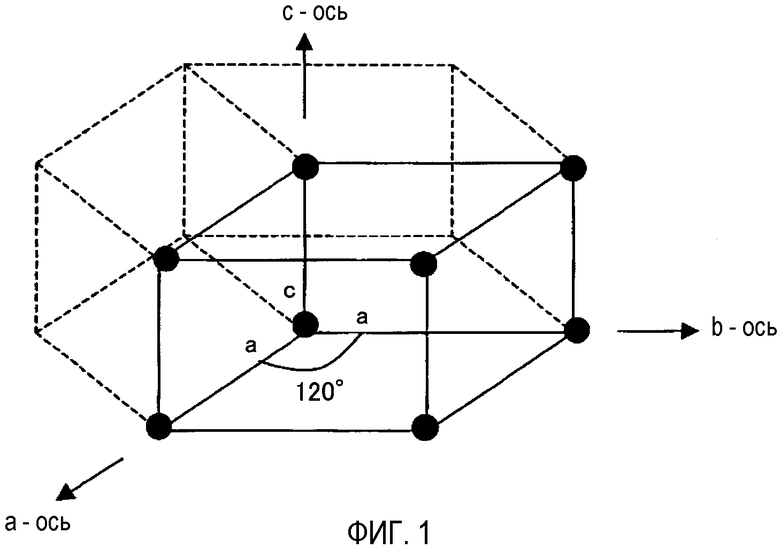
приготовление, по меньшей мере, соединения одного вида, выбранного из группы соединений карбоновых кислот, имеющих гидроксильную группу или меркаптогруппу и имеющих число атомов углерода от 2 до 20, дикарбоновых кислот, имеющих число атомов углерода 2 или 3, монокарбоновых кислот, имеющих число атомов углерода от 1 до 20;
добавление, по меньшей мере, одного соединения, выбранного из группы, к водному раствору нитрата, включающему Al и редкоземельный элемент;
полное выпаривание водной карбоновой кислоты с получением комплекса полимера на основе карбоновой кислоты;
нагревание комплексного полимера на основе карбоновой кислоты до не более чем 1000°С с образованием оксида алюминия;
нанесение палладия на оксид алюминия.
редкоземельный металл) в качестве носителя Pd, причем катализатор получают добавлением, по меньшей мере, одного вида соединения, выбранного из группы соединений карбоновых кислот, имеющих гидроксильную группу или меркаптогруппу и имеющих число атомов углерода от 2 до 20, дикарбоновых кислот, имеющих число атомов углерода 2 или 3, монокарбоновых кислот, имеющих число атомов углерода от 1 до 20, к водному раствору нитрата, содержащему Al и редкоземельный металл;
полное выпаривание водной карбоновой кислоты с получением комплекса полимера на основе карбоновой кислоты и
нагревание комплексного полимера на основе карбоновой кислоты с образованием оксида алюминия;
нанесение палладия на оксид алюминия.
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| RU 2000109780 A, 27.03.2002 | |||
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА ОЧИСТКИ ОТРАБОТАВШИХ ГАЗОВ ДВИГАТЕЛЕЙ ВНУТРЕННЕГО СГОРАНИЯ | 2000 |
|
RU2190470C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ КАТАЛИТИЧЕСКОГО БЛОКА ДЛЯ НЕЙТРАЛИЗАЦИИ ВРЕДНЫХ ГАЗОВЫХ ВЫБРОСОВ | 1994 |
|
RU2080179C1 |
| Способ приготовления сернистого красителя защитного цвета | 1915 |
|
SU63A1 |
| S.Subramanian et al | |||
| Composition of Pd-La/α-AlO catalysts | |||
| CATALYSIS LETTERS | |||
| Пуговица для прикрепления ее к материи без пришивки | 1921 |
|
SU1992A1 |
Авторы
Даты
2008-02-10—Публикация
2004-05-27—Подача