Изобретение относится к замещенным в циклах дифенилазетидинонам, их физиологически приемлемым солям, а также физиологически функциональным производным.
Уже описаны дифенилазетидиноны (как, например, эзетимиб), а также их применение для лечения гиперлипидемии, а также артериосклероза и гиперхолестеринемии [см. Drugs of the Future, 25 (7), 679-685 (2000), и патент США 5756470].
Задачей изобретения является получение других соединений, которые проявляют терапевтически применимое гиполипидемическое действие. Задача в особенности состоит в получении новых соединений, которые по сравнению с описанными в уровне техники соединениями являются очень незначительно резорбирующимися. Под выражением "очень незначительно резорбирующийся" понимают кишечную резорбцию меньше 10%, предпочтительно меньше или равную 5%.
Новые соединения должны обладать в особенности меньшей резорбцией, чем эзетимиб.
При более незначительной резорбции фармацевтические биологически активные вещества проявляют, как правило, отчетливо меньшие побочные действия.
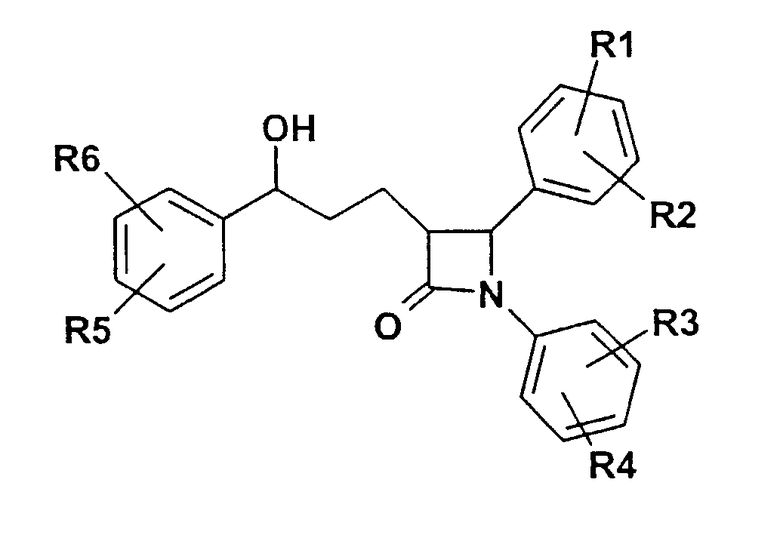
Изобретение относится поэтому к соединениям формулы (I):
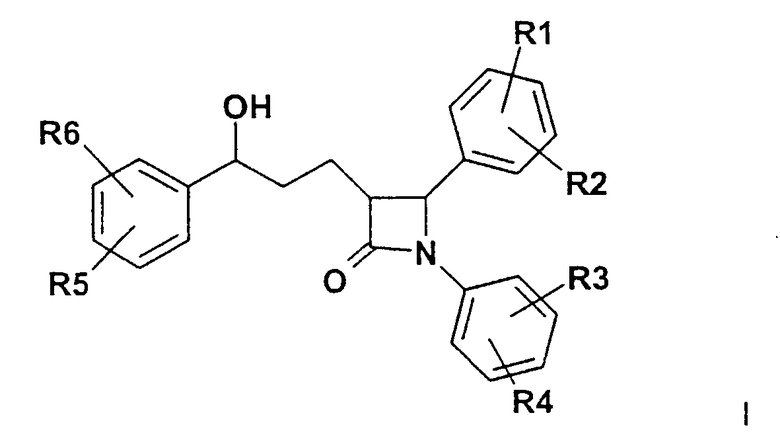
где R1, R2, R3, R4, R5, R6, независимо друг от друга, означают (С1-С30)-алкилен-(LAG)n, причем n=1-5 и причем один или несколько атомов углерода алкиленового остатка заменены замещенными вплоть до трехкратно с помощью R7 арильными или гетероарильными остатками или замещенными вплоть до четырехкратно с помощью R7 (С3-С10)-циклоалкильными или гетероциклоалкильными остатками
и один или несколько атомов углерода алкиленового остатка могут быть заменены на -S(O)n-, с n=0-2, -О-, -(С=О)-, -(C=S)-, -CH=CH-, -C≡C-, -N((C1-C6)-алкил)-, -N-(фенил)-, -N((C1-C6)-алкилфенил)-, -N(CO-(CH2)1-10-COOH)- или -NH-;
Н, F, Cl, Br, I, CF3, NO2, N3, CN, COOH, COO(C1-C6)-алкил, CONH2, CONH(C1-C6)-алкил, CON[(C1-C6)-алкил]2, (С1-С6)-алкил, (С2-С6)-алкенил, (С2-С6)-алкинил, О-(С1-С6)-алкил, причем в алкильных остатках один, несколько или все атомы водорода могут быть заменены атомами фтора;
SO2-NH2, SO2NH(C1-C6)-алкил, SO2N[(C1-C6)-алкил]2, S-(С1-С6)-алкил, S-(CH2)n-фенил, SO-(C1-C6)-алкил, SO-(CH2)n-фенил, SO2-(C1-C6)-алкил, SO2-(CH2)n-фенил, причем n может означать 0-6 и фенильный остаток может быть вплоть до двукратно замещен с помощью F, Cl, Br, OH, CF3, NO2, CN, OCF3, O-(C1-C6)-алкила, (С1-С6)-алкила, NH2;
NH2, NH-(C1-C6)-алкил, N((C1-C6)-алкил)2, NH-(C1-C7)-ацил, фенил, О-(СН2)n-фенил, причем n может означать 0-6 и причем фенильное кольцо может быть вплоть до трехкратно замещено с помощью F, Cl, Br, I, OH, CF3, NO2, CN, OCF3, O-(C1-C6)-алкила, (С1-С6)-алкила, NH2, NH(С1-С6)-алкила, N-((С1-С6)-алкил)2, SO2-CH3, COOH, COO-(C1-C6)-алкила, CONH2;
R7 означает F, Cl, Br, I, CF3, NO2, N3, CN, COOH, COO(C1-C6)-алкил, CONH2, CONH(C1-C6)-алкил, CON[(C1-C6)-алкил]2, (С1-С6)-алкил, (С2-С6)-алкенил, (С2-С6)-алкинил, О-(С1-С6)-алкил, причем в алкильных остатках один, несколько или все атомы водорода могут быть заменены атомами фтора;
PO3H2, SO3H, SO2-NH2, SO2NH(C1-C6)-алкил, SO2N[(C1-C6)-алкил]2, S-(С1-С6)-алкил, S-(CH2)n-фенил, SO-(C1-C6)-алкил, SO-(CH2)n-фенил, SO2-(C1-C6)-алкил, SO2-(CH2)n-фенил, причем n может означать 0-6 и фенильный остаток может быть вплоть до двукратно замещен с помощью F, Cl, Br, OH, CF3, NO2, CN, OCF3, O-(C1-C6)-алкила, (С1-С6)-алкила, NH2;
C(NH)(NH2), NH2, NH-(C1-C6)-алкил, N-((C1-C6)-алкил)2, NH-(C1-C7)-ацил, фенил, О-(СН2)n-фенил, причем n может означать 0-6 и причем фенильное кольцо может быть вплоть до трехкратно замещено с помощью F, Cl, Br, I, OH, CF3, NO2, CN, OCF3, O-(C1-C6)-алкила, (С1-С6)-алкила, NH2, NH(С1-С6)-алкила, N-((С1-С6)-алкил)2, SO2-CH3, COOH, COO-(C1-C6)-алкила, CONH2;
(LAG)n означает сахаридный остаток, дисахаридный остаток, трисахаридный остаток, тетрасахаридный остаток;
сахарную кислоту, аминосахар;
аминокислотный остаток, олигопептидный остаток, состоящий из 2-9 аминокислот;
ациклический, моно-, би- или трициклический триалкиламмониевый остаток, ациклический, моно-, би- или трициклический триалкиламмонийалкильный остаток, -O-(SO2)-OH, -(СН2)0-10-SO3H, -(CH2)0-10-P(O)(OH)2, -(CH2)0-10-O-P(O)(OH)2, -(CH2)0-10-COOH, -(СН2)0-10-С(=NH)(NH2), -(CH2)0-10-C(=NH)(NHOH), -NR8-C(=NR9)(NR10R11), причем n=1-5 и R8, R9, R10 и R11, независимо друг от друга, могут означать Н, (С1-С6)-алкил, фенил, (С1-С6)-алкилфенил, (С3-С8)-циклоалкил;
и причем всегда по меньшей мере один из остатков R1-R6 должен означать (С1-С30)-алкилен-(LAG)n, причем n=1-5 и один или несколько атомов углерода алкиленового остатка заменены замещенными вплоть до трехкратно с помощью R7 арильными или гетероарильными остатками или замещенными вплоть до четырехкратно с помощью R7 (С3-С10)-циклоалкильными или гетероциклоалкильными остатками и один или несколько атомов углерода алкиленового остатка могут быть заменены на -S(O)n, с n=0-2, -O-, -(C=O)-, -(C=S)-, -CH=CH-, -C≡C-, -N((C1-C6)-алкил)-, -N(фенил)-, -N((C1-C6)-алкилфенил)-, -N(СО-(СН2)1-10-СООН)- или -NH-;
а также к их физиологически приемлемым солям.
Предпочтительны соединения формулы (I), где по меньшей мере один из остатков R1-R6 означает (С1-С30)-алкилен-(LAG)n, причем n=1-5 и один или несколько атомов углерода алкиленового остатка заменены замещенными вплоть до трехкратно с помощью R7 арильными или гетероарильными остатками или замещенными вплоть до четырехкратно с помощью R7 (С3-С10)-циклоалкильными или гетероциклоалкильными остатками и один или несколько атомов углерода алкиленового остатка могут быть заменены на -S(O)n-, с n=0-2, -O-, -(C=O)-, -(C=S)-, -CH=CH-, -C≡C-, N((C1-C6)-алкил)-, -N(фенил)-, -N((C1-C6)-алкилфенил)-, -N(СО-(СН2)1-10-СООН)- или -NH-.
Особенно предпочтительны соединения формулы (I), где один из остатков R1 или R3 означает (С1-С30)-алкилен-(LAG), причем один или несколько атомов углерода алкиленового остатка заменены замещенными вплоть до трехкратно с помощью R7 арильными или гетероарильными остатками или замещенными вплоть до трехкратно с помощью R7 (С3-С10)-циклоалкильными или гетероциклоалкильными остатками и один или несколько атомов углерода алкиленового остатка могут быть заменены на -S(O)n-, с n=0-2, -O-, -(C=O)-, -N(CH3)-, -N(фенил)-, -N(СО-(СН2)1-10-СООН)- или -NH-.
В высшей степени предпочтительны соединения формулы (I), где по меньшей мере один из остатков R1 или R3 означает -(СН2)0-1-NH-(C=O)0-1-(C0-C25)-алкилен-(С=О)0-1-N(R13)0-1-(LAG) или -(СН2)0-1-(С=О)0-1-NH-(C0-C25)-алкилен-(C=O)0-1-N(R13)0-1-(LAG); где один или несколько атомов углерода алкиленового остатка заменены замещенными вплоть до трехкратно с помощью R7 арильными или гетероарильными остатками или замещенными вплоть до трехкратно с помощью R7 (С3-С10)-циклоалкильными или гетероциклоалкильными остатками и один или несколько атомов углерода алкиленового остатка могут быть заменены на атомы кислорода, NH, N(CH3) или SO2 и причем R13 может означать Н или СН3.
Далее, предпочтительны соединения формулы (I), где группа LAG означает моносахаридный остаток, ациклический, моно-, би- или трициклический триалкиламмонийалкильный остаток, сульфокислоту или карбоновую кислоту.
Под арильным остатком понимают фенильный, нафтильный, бифенильный, тетрагидронафтильный, альфа- или бета-тетралоновый, инданильный или индан-1-онильный остаток.
Под гетероарильным остатком понимают пиридильный, пиримидинильный, пиразинильный, пиридазинильный, пиридазин-3-он-ильный, пирролильный, имидазолильный, пиразолильный, 1,2,4-триазолильный, индолильный, бензимидазолильный, тиенильный, фурильный, тиазолильный, оксазолильный, изоксазолильный или изотиазолильный остаток.
Под гетероциклоалкильными остатками понимают (С3-С10)-циклоалкильные остатки, в которых по меньшей мере один и вплоть до трех атомов углерода, независимо друг от друга, заменены на NR8, O или S(O)n, причем n=0-2. Примерами являются азетидинильный, пирролидинильный, пиперидинильный, морфолинильный, 1,4-диоксанильный, тетрагидрофурильный, пиперазинильный или тиепанильный остаток.
Под ациклическим триалкиламмониевым остатком понимают следующую группу:
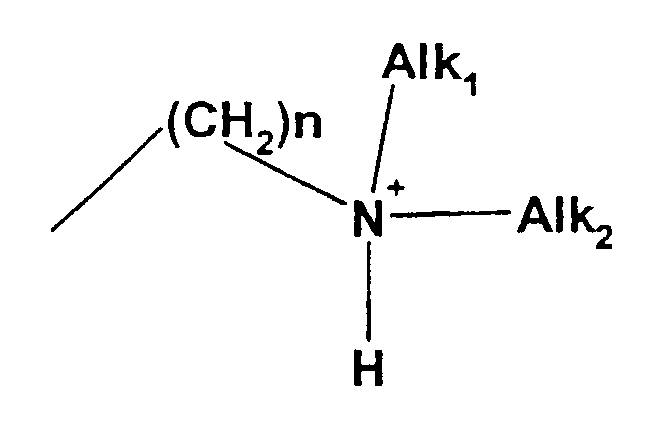
где n может означать 0-10 и Alk1 и Alk2, независимо друг от друга, означают, каждый, линейный или разветвленный алкильный остаток с 1-20 атомами углерода.
Под ациклическим триалкиламмонийалкильным остатком понимают следующую группу:
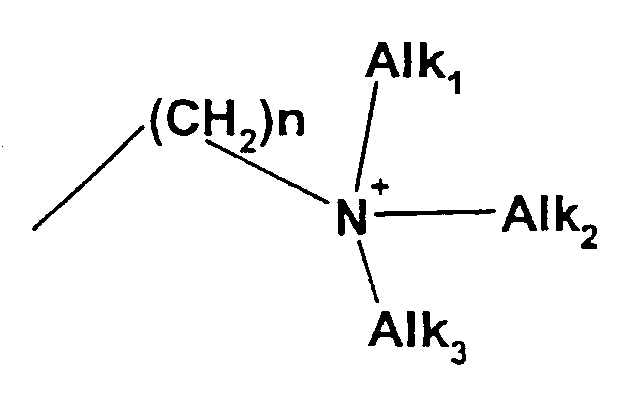
где n может означать 0-10 и Alk1, Alk2, Alk3, независимо друг от друга, означают, каждый, линейный или разветвленный алкильный остаток с 1-20 атомами углерода.
Под моно- или би- или трициклическим триалкиламмониевым остатком понимают, например, такие остатки, как:
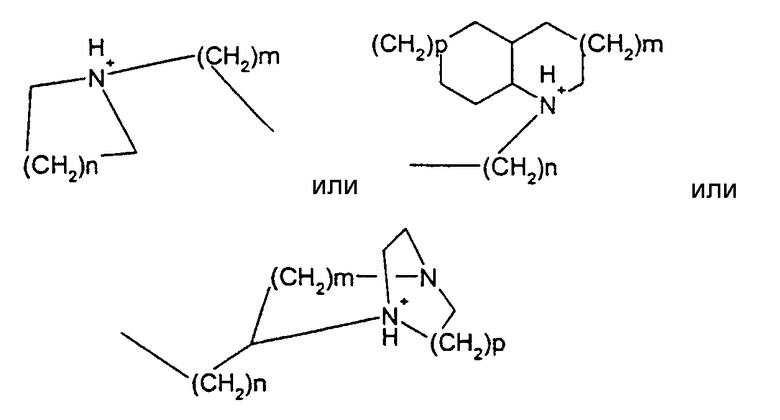
причем n, m и р, независимо друг от друга, могут означать 0-10 и одна или несколько групп -CH2-, независимо друг от друга, могут быть заменены на О, S(O)n, причем n может означать 0-2, NH, N-(C1-C10)-алкил, N-фенил или N-CH2-фенил.
Под моно- или бициклическим триалкиламмонийалкильным остатком понимают, например, такие остатки, как:
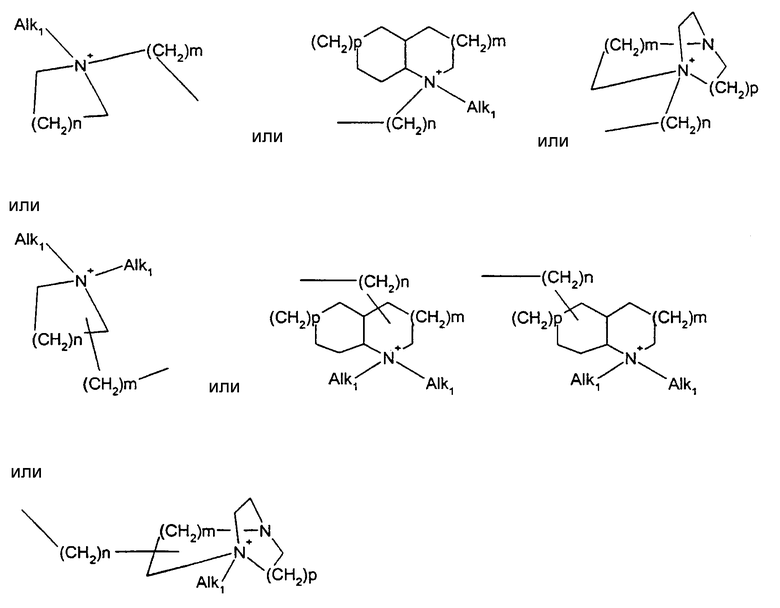
причем n, m и р, независимо друг от друга, могут означать 0-10 и одна или несколько групп -CH2-, независимо друг от друга, могут быть заменены на О, S(O)n, причем n может означать 0-2, NH, N-(C1-C10)-алкил, N-фенил или N-CH2-фенил, и Alk1 означает линейный или разветвленный алкильный остаток с 1-20 атомами углерода.
Фармацевтически приемлемые соли из-за их более высокой растворимости в воде по сравнению с исходными или базовыми соединениями особенно пригодны для применений в медицине. Эти соли должны иметь фармацевтически приемлемый анион или катион. Пригодными фармацевтически приемлемыми аддитивными солями кислот предлагаемых согласно изобретению соединений являются соли неорганических кислот таких, как соляная кислота, бромоводородная, фосфорная кислота, метафосфорная кислота, азотная кислота, сульфокислота и серная кислота, а также органических кислот таких, как, например, уксусная кислота, бензолсульфокислота, бензойная кислота, лимонная кислота, этансульфокислота, фумаровая кислота, глюконовая кислота, гликолевая кислота, изотионовая кислота, молочная кислота, лактобионовая кислота, малеиновая кислота, яблочная кислота, метансульфокислота, янтарная кислота, n-толуолсульфокислота, винная кислота и трифторуксусная кислота. Для медицинских целей особенно предпочтительно используют хлорид. Пригодными фармацевтически приемлемыми основными солями являются аммониевые соли, соли щелочных металлов (как натриевые и калиевые соли) и соли щелочно-земельных металлов (как магниевые и кальциевые соли).
Соли с фармацевтически неприемлемым анионом также относятся к данному изобретению как полезные промежуточные продукты для получения или очистки фармацевтически приемлемых солей и/или для использования в случае нетерапевтических, например, in vitro, применений.
Используемое в данном контексте понятие "физиологически функциональное производное" означает любое физиологически приемлемое производное предлагаемого согласно изобретению соединения, например, сложный эфир, которое при введении млекопитающему, как, например, человеку, способно (непосредственно или опосредованно) образовывать такое соединение или его активный метаболит.
Следующим объектом настоящего изобретения являются пролекарственные формы предлагаемых согласно изобретению соединений. Такие пролекарства in vivo могут метаболизироваться до предлагаемого согласно изобретению соединения. Эти пролекарства могут быть сами активными или неактивными.
Предлагаемые согласно изобретению соединения могут также находиться в различных полиморфных формах, например, в виде аморфной и кристаллической полиморфных формах. Все полиморфные формы предлагаемых согласно изобретению соединений относятся к данному изобретению и представляют объект изобретения.
В нижеследующем тексте все ссылки на "соединение (соединения) формулы (I)" относятся к соединению (соединениям) формулы (I), описанным выше, а также к их солям, сольватам и физиологически функциональным производным, описываемым в данном изобретении.
Соединения формулы (I) и их фармацевтически приемлемые соли и физиологически функциональные производные представляют собой идеальные лекарственные средства для лечения нарушений липидного обмена, в особенности гиперлипидемии. Соединения формулы (I) могут влиять на уровень холестерина в сыворотке и пригодны для предупреждения и лечения артериосклеротических явлений.
Соединение (соединения) формулы (I) можно вводить также в комбинации с другими биологически активными веществами.
Количество соединения формулы (I), которое необходимо для достижения желательного биологического эффекта, зависит от ряда факторов, например, от выбранного конкретного соединения, предусматриваемого применения, способа введения и клинического состояния пациента. В общем, суточная доза находится в пределах от 0,1 мг до 100 мг (обычно от 0,1 мг до 50 мг) в сутки на килограмм массы тела, например, 0,1-10 мг/кг/сутки. Таблетки или капсулы могут содержать, например, 0,01-100 мг, обычно 0,02-50 мг. В случае фармацевтически приемлемых солей вышеуказанные данные по массе относятся к массе образующегося из соли иона дифенилазетидинона. Для профилактики или лечения вышеуказанных состояний соединения формулы (I) можно применять индивидуально в виде соединения, однако, предпочтительно они находятся вместе с приемлемым носителем в форме фармацевтической композиции. Носитель, естественно, должен быть приемлемым, т.е. он должен быть совместимым с другими компонентами композиции и не быть вредным для здоровья пациента. Носитель может представлять собой твердое вещество или жидкость или то и другое и предпочтительно его используют вместе с соединением для получения лекарственного средства в виде разовой дозы, например, в виде таблетки, которая может содержать от 0,05% масс. до 95% масс. биологически активного вещества. Также могут иметься другие фармацевтически активные вещества, включая другие соединения формулы (I). Предлагаемые согласно изобретению фармацевтические композиции можно приготовлять одним из известных фармацевтических способов, которые по существу состоят в том, что компоненты смешиваются с фармакологически приемлемыми носителями и/или вспомогательными веществами.
Предлагаемые согласно изобретению фармацевтические композиции представляют собой композиции, пригодные для орального или перорального (например, подъязычного) введения, хотя самый пригодный способ введения в каждом отдельном случае зависит от рода и тяжести излечиваемого состояния и от рода используемого соединения формулы (I). Дражированные лекарственные формы и дражированные лекарственные формы пролонгированного действия также охватываются данным изобретением. Предпочтительны резистентные к кислоте и желудочному соку лекарственные формы. Пригодные резистентные к желудочному соку покрытия включают ацетатфталат целлюлозы, поливинилацетатфталат, гидроксипропилметилцеллюлозофталат и анионные полимеры метакриловой кислоты и метилового эфира метакриловой кислоты.
Пригодные фармацевтические соединения для орального введения могут находиться в виде отдельных единиц готовых лекарственных форм таких, как, например, капсулы, облатки, таблетки для сосания или таблетки, которые содержат определенное количество соединения формулы (I); в виде порошков или гранулятов; в виде раствора или суспензии в водной или неводной жидкости; или в виде эмульсии масло-в-воде или вода-в-масле. Эти композиции, как уже упоминалось, можно приготовлять любым пригодным фармацевтическим способом, который включает стадию, на которой биологически активное вещество вводят в контакт с носителем (который может состоять из одного или нескольких дополнительных компонентов). В общем, композиции получают путем равномерного и гомогенного смешения биологически активного вещества с жидким и/или твердым тонкодисперсным носителем, после чего продукт, если необходимо, формуют. Так, например, таблетки получают тем, что порошок или гранулят соединения прессуют или формуют, в случае необходимости, вместе с одним или несколькими дополнительными компонентами. Прессованные таблетки можно получать путем таблетирования в пригодной машине соединения в свободно текучей форме, как, например, порошок или гранулят, в случае необходимости, смешанного со связующим, придающим скользкость таблеткам веществом, инертным разбавителем и/или одним (несколькими) поверхностно-активным веществом и/или диспергатором. Формованные таблетки можно получать путем формования в пригодной машине порошкообразного, смоченного инертным жидким разбавителем соединения.
Фармацевтические композиции, которые пригодны для перорального (подъязычного) введения, включают таблетки для сосания, которые содержат соединение формулы (I) вместе с вкусовым веществом, обычно сахарозой и гуммиарабиком или трагантом, и пастилки, содержащие соединение в инертной основе такой, как желатина и глицерин или сахароза и гуммиарабик.
В качестве других биологически активных веществ для комбинированных препаратов пригодны все антидиабетические средства, которые указаны в Красном списке 2001, глава 12. Их можно комбинировать с предлагаемыми согласно изобретению соединениями формулы (I) в особенности для синергического повышения действия. Введение комбинации биологически активных веществ можно осуществлять либо путем раздельного введения биологически активных веществ пациенту, либо в форме комбинированных препаратов, в которых в фармацевтической композиции находятся несколько биологически активных веществ.
Антидиабетические средства включают инсулин и производные инсулина, как, например, Lantus′ или HMR 1964, производные GLP-1, как, например, такие, которые раскрыты в Международной заявке WO-98/088871 фирмы Novo Nordisk A/S, а также орально эффективные гипогликемические биологически активные вещества. Орально эффективные гипогликемические биологически активные вещества предпочтительно включают сульфонилмочевины, бигуадины, меглитиниды, оксадиазолидиндионы, тиазолидиндионы, ингибиторы глюкозидазы, антагонисты глюкагона, агонисты GLP-1, открыватели калиевых каналов, как, например, такие, которые раскрыты в Международных заявках WO-97/26265 и WO-99/03861 фирмы Novo Nordisk A/S, активаторы инсулина, ингибиторы ферментов печени, которые принимают участие в стимуляции глюконеогенеза и/или гликогенолиза, модуляторы поглощения глюкозы, изменяющие жировой обмен соединения такие, как антигиперлипидемические и антилипидемические биологически активные вещества, соединения, способствующие уменьшению потребления пищи, агонисты PPAR и PXR и биологически активные вещества, воздейстующие на АТФ-зависимый калиевый канал бета-клеток.
Согласно варианту осуществления изобретения, соединения формулы (I) вводят в комбинации с ингибитором HMGCoA-редуктазы таким, как симвастатин, флувастатин, правастатин, ловастатин, аторвастатин, церивастатин, росувастатин.
Согласно варианту осуществления изобретения, соединения формулы (I) вводят в комбинации с ингибитором резорбции холестерина таким, как, например, эзетимиб, тиквесид, памаквесид.
Согласно варианту осуществления изобретения, соединения формулы (I) вводят в комбинации с агонистом PPAR-гамма таким, как, например, росиглитазон, пиоглитазон, JTT-501, GI 262570.
Согласно варианту осуществления изобретения, соединения формулы (I) вводят в комбинации с агонистом PPAR-альфа таким, как, например, GW 9578, GW 7647.
Согласно варианту осуществления изобретения, соединения формулы (I) вводят в комбинации с агонистом смешанных PPAR-альфа/PPAR-гамма таким, как, например, GW 1536, AVE 8042, AVE 8134, AVE 0847.
Согласно варианту осуществления изобретения, соединения формулы (I) вводят в комбинации с фибратом таким, как, например, фенофибрат, клофибрат, безафибрат.
Согласно варианту осуществления изобретения, соединения формулы (I) вводят в комбинации с ингибитором МТР таким, как, например, Вау 13-9952, BMS-201038, R-103757.
Согласно варианту осуществления изобретения, соединения формулы (I) вводят в комбинации с ингибитором резорбции желчной кислоты таким, как, например, HMR 1453.
Согласно варианту осуществления изобретения, соединения формулы (I) вводят в комбинации с ингибитором СЕТР таким, как, например, Вау 194789.
Согласно варианту осуществления изобретения, соединения формулы (I) вводят в комбинации с полимерным адсорбером желчной кислоты таким, как, например, холестирамин, колесольвам.
Согласно варианту осуществления изобретения, соединения формулы (I) вводят в комбинации с активатором рецептора LDL таким, как, например, HMR 1171, HMR 1586.
Согласно варианту осуществления изобретения, соединения формулы (I) вводят в комбинации с ингибитором АСАТ таким, как, например, авасимиб.
Согласно варианту осуществления изобретения, соединения формулы (I) вводят в комбинации с антиоксидантом таким, как, например, ОРС-14117.
Согласно варианту осуществления изобретения, соединения формулы (I) вводят в комбинации с ингибитором липопротеинлипазы таким, как, например, NO-1886.
Согласно варианту осуществления изобретения, соединения формулы (I) вводят в комбинации с ингибитором АТФ-цитрат-лиазы таким, как, например, SB-204990.
Согласно варианту осуществления изобретения, соединения формулы (I) вводят в комбинации с ингибитором скваленсинтетазы таким, как, например, BMS-188494.
Согласно варианту осуществления изобретения, соединения формулы (I) вводят в комбинации с антагонистом липопротеина(а), как, например, CI-1027 или никотиновая кислота.
Согласно варианту осуществления изобретения, соединения формулы (I) вводят в комбинации с ингибитором липазы, как, например, орлистат.
Согласно варианту осуществления изобретения, соединения формулы (I) вводят в комбинации с инсулином.
Согласно варианту осуществления изобретения, соединения формулы (I) вводят в комбинации с сульфонилмочевиной, как, например, толбутамид, глибенкламид, глипицид или гликлацид.
Согласно варианту осуществления изобретения, соединения формулы (I) вводят в комбинации с бигуанидом, как, например, метформин.
Согласно варианту осуществления изобретения, соединения формулы (I) вводят в комбинации с меглитинидом, как, например, репаглинид.
Согласно варианту осуществления изобретения, соединения формулы (I) вводят в комбинации с тиазолидиндионом, как, например, троглитазон, циглитазон, пиоглитазон, росиглитазон или раскрытые в Международной заявке WO-97/41097 Dr. Reddy's Research Foundation соединения, в особенности 5-[[4-[(3,4-дигидро-3-метил-4-оксо-2-хиназолинил)метокси]фенил]метил]-2,4-тиазолидиндион.
Согласно варианту осуществления изобретения, соединения формулы (I) вводят в комбинации с ингибитором a-глюкозидазы, как, например, миглитол или акарбоза.
Согласно варианту осуществления изобретения, соединения формулы (I) вводят в комбинации с биологически активным веществом, воздействующим на АТФ-зависимый калиевый канал бета-клеток, как, например, толбутамид, глибенкламид, глипицид, глиацид или репаглинид.
Согласно варианту осуществления изобретения, соединения формулы (I) вводят в комбинации с более, чем одним из вышеуказанных соединений, например, в комбинации с сульфонилмочевиной и метформином, сульфонилмочевиной и акарбозой, репаглинидом и метформином, инсулином и сульфонилмочевиной, инсулином и метформином, инсулином и троглитазоном, инсулином и ловастатином, и т.д.
Согласно другому варианту осуществления изобретения, соединения формулы (I) вводят в комбинации с агонистами CART, агонистами NPY, агонистами МС-3 или МС-4, агонистами орексина, агонистами Н3, агонистами TNF, агонистами CRF, антагонистами CRF BP, агонистами урокортина, агонистами β3, антагонистами МСН (меланинконцентрирующий гормон), агонистами ССК, ингибиторами повторного поглощения серотонина, смешанными серотонин- и норадренергическими соединениями, агонистами 5НТ, агонистами бомбезина, антагонистами галанина, гормоном роста, высвобождающими гормон роста соединениями, агонистами TRH, 2- или 3-модуляторами разрыва протеиновой связи, агонистами лептина, агонистами DA (бромокриптин, допрексин), ингибторами липазы/амилазы, модуляторами PPAR, модуляторами RXR или агонистами TR-β.
Согласно варианту осуществления изобретения, другим биологически активным веществом является лептин.
Согласно варианту осуществления изобретения, другим биологически активным веществом является дексамфатамин или амфетамин.
Согласно варианту осуществления изобретения, другим биологически активным веществом является фенфлурамин или дексфенфлурамин.
Согласно еще одному варианту осуществления, другим биологически активным веществом является сибутрамин.
Согласно варианту осуществления, другим биологически активным веществом является орлистат.
Согласно варианту осуществления, другим биологически активным веществом является мазиндол или фентермин.
Согласно варианту осуществления, соединения формулы (I) вводят в комбинации с балластными веществами, предпочтительно с нерастворимыми балластными веществами, как, например, Caromax®. Комбинация с Caromax® может находиться в виде композиции или может быть введена путем раздельного введения соединений формулы (I) и Caromax®. Caromax® при этом также можно вводить в виде пищевых продуктов, как, например, в хлебобулочных изделиях или батончиках мюсли. Комбинация соединений формулы (I) с Caromax®, наряду с повышением активности, в особенности в отношении снижения LDL-холестерина, по сравнению с индивидуальными биологически активными веществами, также отличается своей улучшенной переносимостью.
Понятно, что каждая пригодная комбинация предлагаемых согласно изобретению соединений с одним или несколькими из вышеуказанных соединений и, на выбор, с одним или несколькими другими фармакологически активными веществами рассматривается как подпадающая под объем охраны настоящего изобретения.
Объектом изобретения, далее, являются как смеси стереоизомеров формулы (I), так и чистые стереоизомеры формулы (I), как смеси диастереомеров формулы (I), так и также чистые диастереомеры. Разделение смесей осуществляют хроматографическим способом.
Предпочтительны рацемические, а также энантиомерно чистые соединения формулы (I) следующей структуры:
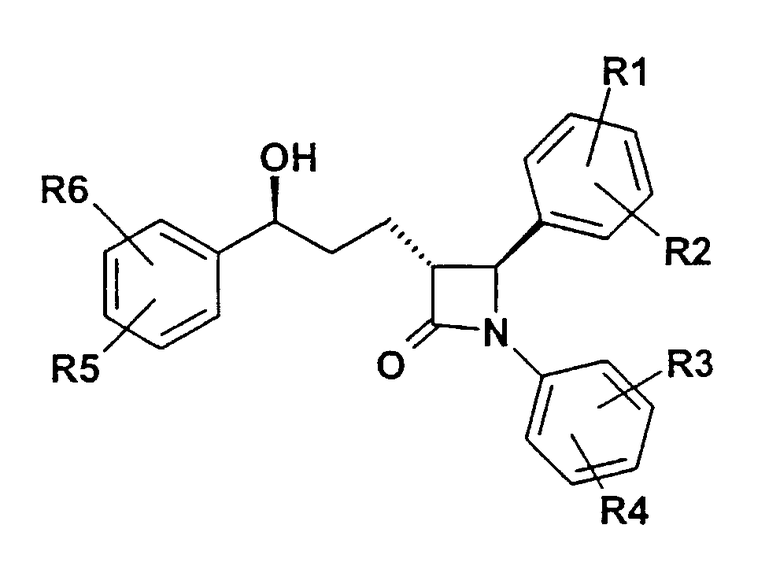
Под сахаридными остатками понимают соединения, которые образуются из альдоз и кетоз с 3-7 атомами углерода, которые могут принадлежать D- или L-ряду; к ним относятся также аминосахара, получаемые путем восстановления сахаров спирты или сахарные кислоты. Следует назвать, например, глюкозу, маннозу, фруктозу, галактозу, рибозу, эритрозу, глицеринальдегид, седогептулозу, глюкозамин, галактозамин, глюкуроновую кислоту, галактуроновую кислоту, глюконовую кислоту, галактоновую кислоту, манноновую кислоту, глюкамин, 3-амино-1,2-пропандиол, глюкаровую кислоту и галактаровую кислоту.
Под дисахарами подразумевают сахариды, которые состоят из двух сахаридных единиц. Ди-, три- или тетрасахариды образуются за счет ацеталеобразной связи двух или нескольких сахаров. Связи при этом могут образовываться в α- или β-форме. В качестве примера следует назвать лактозу, мальтозу и целлобиозу.
Если сахар является замещенным, то замещение происходит предпочтительно по атому водорода гидроксильной группы сахара.
Для гидроксильных групп сахара используются в основном следующие защитные группы: бензильная, ацетильная, бензоильная, пивалоильная, тритильная, трет-бутилдиметилсилильная, бензилиденовая, циклогексилиденовая или изопропилиденовая защитные группы.
Под понятием аминокислоты, соответственно, аминокислотные остатки подразумевают, например, стереоизомерные формы, то есть, D- или L-формы, следующих соединений: аланин, глицин, пролин, цистеин, гистидин, глутамин, аспарагиновая кислота, изолейцин, аргинин, глутаминовая кислота, лизин, серин, фенилаланин, лейцин, треонин, триптофан, метионин, валин, тирозин, аспарагин, 2-аминоадипиновая кислота, 2-аминоизомасляная кислота, 3-аминоадипиновая кислота, 3-аминоизомасляная кислота, бета-аланин, 2-аминопимелиновая кислота, 2-аминомасляная кислота, 2,4-диаминомасляная кислота, 4-аминомасляная кислота, десмозин, пиперидинкарбоновая кислота, 2,2-диаминопимелиновая кислота, 6-аминокапроновая кислота, 2,3-диаминопропионовая кислота, 2-аминогептановая кислота, N-этилглицин, 2-(2-тиенил)глицин, 3-(2-тиенил)аланин, пенициллин, саркозин, N-этиласпарагин, N-метилизолейцин, гидроксилизин, 6-N-метиллизин, алло-гидроксилизин, N-метилвалин, 3-гидроксипролин, норвалин, 4-гидроксипролин, норлейцин, изодесмозин, орнитин, алло-изолейцин, N-метилглицин.
Краткое написание названий аминокислот соответствует общепринятому способу написания (см. Schröder, Lübke, The Peptides, том I, Нью-Йорк, 1965, с.XXII-XXIII; Губен-Вейл, Методы органической химии, том XV/1 и 2, Штутгарт, 1974). Аминокислота pGlu означает пироглутамил, Nal означает 3-(2-нафтил)аланин, Azagly-NH2 означает соединение формулы NH2-NH-CONH2 и D-Asp означает D-форму аспарагиновой кислоты. Пептиды по своей химической природе представляют собой амиды кислот и при годролизе распадаются на аминокислоты.
Под олигопептидом понимают пептиды, которые состоят из 2-9 вышеуказанных аминокислот.
В качестве пригодных защитных групп (см., например, T.W. Greene "Protective Groups in Organic Synthesis") для аминокислот в первую очередь используют: Arg(Tos), Arg(Mts), Arg(Mtr), Arg(PMV), Asp(OBzl), Asp(OBut), Cys(4-MeBzl), Cys(Acm), Cys(SBut), Glu(Obzl), Glu(Obut), His(Tos), His(Fmoc), His(Dnp), His(Trt), Lys(Cl-Z), Lys(Boc), Met(O), Ser(Bzl), Ser(But), Thr(Bzl), Thr(But), Trp(Mts), Trp(CHO), Tyr(Br-Z), Tyr(Bzl) или Tyr(But).
В качестве аминозащитных групп предпочтительно используют отщепляющийся за счет каталитического гидрирования бензилоксикарбонильный (Z) остаток, отщепляющийся с помощью слабых кислот 2-(3,5-диметоксифенил)пропил(2)оксикарбонильный (Ddz) или тритильный (Trt) остаток, отщепляющийся с помощью кислот, как 3 М соляная кислота, трет-бутилкарбаматный (ВОС) остаток и отщепляющийся с помощью вторичных аминов 9-флуоренилметилоксикарбонильный (Fmoc) остаток.
Изобретение относится, далее, к способу получения производных дифенилазетидинона формулы (I):
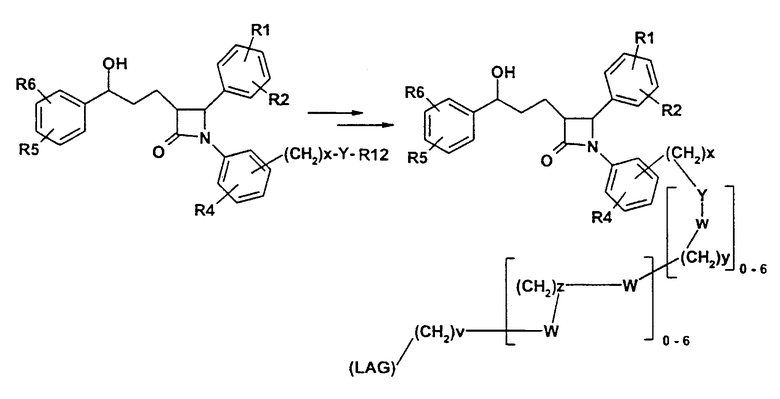
где Y может означать S, O, (C=O), (C=S), CH=CH, C≡C, N((C1-C6)-алкил), N(фенил), N((C1-C6)-алкилфенил), N(CO-(CH2)1-10-COOH) или NH;
R12 может означать Н или в случае, когда Y=(C=O) или (C=S), ОН;
W может означать, независимо от Y, вплоть до трехкратно замещенный арильный или гетероарильный остаток или вплоть до четырехкратно замещенный (С3-С10)-циклоалкильный или гетероциклоалкильный остаток или -S(O)n-, где n=0-2, -О-, -(C=O)-, -(C=S)-, -CH=CH-, -C≡C-, -N((C1-C6)-алкил)-, -N(фенил)-, -N((C1-C6)-алкилфенил)-, -N-(CO-(CH2)1-10-COOH)- или -NH- или связь;
v, х, у и z, независимо друг от друга, могут означать 0-10.
Связывание остатка -(СН2)х-Y-R12 в соединении формулы (II) альтернативно также может быть по одному из двух других фенильных циклов.
Способ получения соединений формулы (I), например, отличается тем, что амин формулы (II) вводят во взаимодействие с алкилирующим или ацилирующим реагентом, который предпочтительно в омега-положении содержит другую функциональную группу, возможно в защищенной форме. Ее используют (после удаления защитной группы) для присоединения (LAG), например, с образованием простой эфирной, аминной или амидной связей.
Нижеследующие примеры служат для более подробного пояснения изобретения без ограничения его объема охраны описанными в примерах продуктами и вариантами осуществления.
Пример I
2,3,4,5,6-Пентагидроксигексиламид 4-(4-{4-[3-[3-(4-фторфенил)-3-гидроксипропил]-2-(4-метоксифенил)-4-оксоазетидин-1-ил]-бензилкарбамоил}фенокси)бензойной кислоты (7)
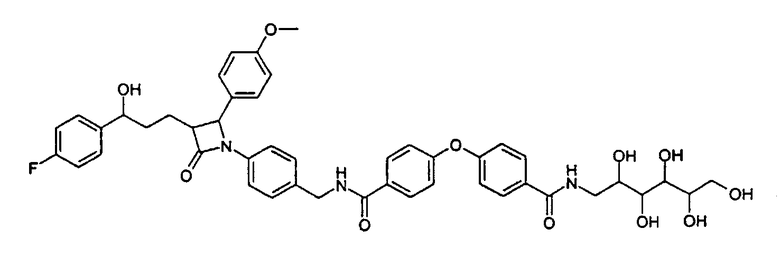
а) 3-[5-(трет-Бутилдиметилсиланилокси)-5-(4-фторфенил)пентаноил]-4-фенилоксазолидин-2-он (1)
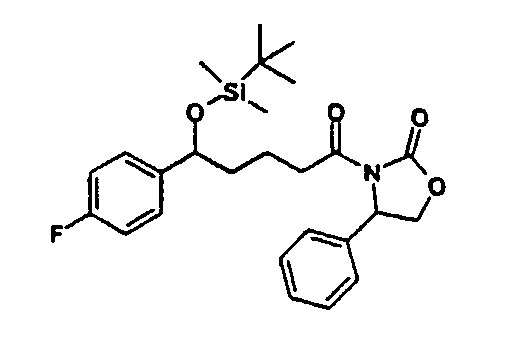
27 г 3-[5-(4-Фторфенил)-5-гидроксипентаноил]-4-фенилоксазолидин-2-она вместе с 13,6 г трет-бутилдиметилсилилхлорида и 10,2 г имидазола растворяют в 36 мл диметилформамида и перемешивают в течение 90 минут при температуре 60°С. После окончания реакции смесь растворяют в этилацетате и дважды встряхивают с водой. Органическую фазу сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Получают 3-[5-(трет-бутилдиметилсиланилокси)-5-(4-фторфенил)пентаноил]-4-фенилоксазолидин-2-он (1) с молекулярной массой 471,65 (С26Н34FNO4Si); МС (ESI) (масс-спектрометрия c ионизацией электронным распылением): 340,28 (МН+-HOSi(CH3)2C(CH3)3).
b) 4-[5-(трет-Бутилдиметилсиланилокси)-5-(4-фторфенил)-1-(4-метоксифенил)-2-(2-оксо-4-фенилоксазолидин-3-карбонил)пентиламино]бензонитрил (2)
16,2 г 3-[5-(трет-Бутилдиметилсиланилокси)-5-(4-фторфенил)пентаноил]-4-фенилоксазолидин-2-она (1) растворяют в 350 мл дихлорметана. Раствор смешивают с 19,8 мл основания Хенига и 10,14 г 4-[(4-метоксифенилимино)метил]бензонитрила и охлаждают до температуры -10°С. К охлажденному раствору добавляют 8,52 мл триметилсилилтрифлата и перемешивают в течение 30 минут при температуре -10°С. Раствор охлаждают теперь до температуры -30°С и добавляют 44 мл раствора тетрахлорида титана. Реакционную смесь перемешивают в течение 2 часов при температуре от -30°С до -40°С. Затем раствор оставляют нагреваться до комнатной температуры, реакционный раствор промывают последовательно с помощью 200 мл 2 н. серной кислоты, 300 мл 20%-ного раствора гидросульфита натрия и насыщенным раствором хлорида натрия. Органическую фазу сушат над сульфатом магния, концентрируют в вакууме и остаток очищают на силикагеле с помощью смеси н-гептана и этилацетата в соотношении 3:1. Получают 4-[5-(трет-бутилдиметилсиланилокси)-5-(4-фторфенил)-1-(4-метоксифенил)-2-(2-оксо-4-фенилоксазолидин-3-карбонил)пентиламино]-бензонитрил (2) с молекулярной массой 707,93 (С41Н46FN3O5Si); МС(ESI): 590,51 (MH+-C7H5N2).
с) 4-[3-[3-(трет-Бутилдиметилсиланилокси)-3-(4-фторфенил)-пропил]-2-(4-метоксифенил)-4-оксоазетидин-1-ил]бензонитрил (3)
13,2 г 4-[5-(трет-Бутилдиметилсиланилокси)-5-(4-фторфенил)-1-(4-метоксифенил)-2-(2-оксо-4-фенилоксазолидин-3-карбонил)пентиламино]бензонитрила (2) растворяют в 380 мл метил-трет-бутилового эфира, смешивают с 18,6 мл N,O-бис(триметилсилил)ацетамида и 1,86 мл 1 М раствора тетрабутиламмонийфторида в тетрагидрофуране и перемешивают в течение 2 часов при комнатной температуре. После окончания реакции добавляют 10 мл уксусной кислоты, реакционную смесь концентрируют в вакууме и остаток очищают на силикагеле с помощью смеси толуола и этилацетата в соотношении 50:1. Получают 4-[3-[3-(трет-бутилдиметилсиланилокси)-3-(4-фторфенил)пропил]-2-(4-метоксифенил)-4-оксоазетидин-1-ил]бензонитрил (3) с молекулярной массой 544,75 (С32Н37FN2O3Si); MC (ESI): 545,56 (M+H+).
d) 4-[3-[3-(4-Фторфенил)-3-гидроксипропил]-2-(4-метоксифенил)-4-оксоазетидин-1-ил]бензонитрил (4)
3,5 г 4-[3-[3-(трет-Бутилдиметилсиланилокси)-3-(4-фторфенил)пропил]-2-(4-метоксифенил)-4-оксоазетидин-1-ил]бензонитрила (3) растворяют в 65 мл тетрагидрофурана, смешивают с 0,74 мл уксусной кислоты и 8,03 мл 1 М раствора тетрабутиламмонийфторида в тетрагидрофуране и перемешивают в течение 2 часов при комнатной температуре. Затем добавляют дополнительно 4,82 мл раствора тетрабутиламмонийфторида и перемешивают следующие 3 часа при температуре кипения с обратным холодильником. Охлажденную реакционную смесь концентрируют в вакууме и остаток очищают хроматографически на силикагеле с помощью смеси н-гептана и этилацетата в соотношении 2:1. Получают 4-[3-[3-(4-фторфенил)-3-гидроксипропил]-2-(4-метоксифенил)-4-оксоазетидин-1-ил]бензонитрил (4) с молекулярной массой 430,48 (С26Н23FN2O3); MC (ESI): 431,24 (M + H+).
е) 1-(4-Аминометилфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-(4-метоксифенил)азетидин-2-он (5)
1,22 г 4-[3-[3-(4-Фторфенил)-3-гидроксипропил]-2-(4-метоксифенил)-4-оксоазетидин-1-ил]бензонитрила (4) растворяют в 90 мл этанола, смешивают с 10 мл концентрированного раствора аммиака и избытком никеля Ренея и перемешивают в течение 8 часов при температуре 60°С и давлении водорода 10 бар. Реакционную смесь охлаждают до комнатной температуры в течение ночи; на следующий день отделяют от катализатора, фильтрат концентрируют в вакууме и остаток очищают хроматографически на силикагеле с помощью смеси дихлорметана, метанола и раствора аммиака в соотношении 10:1:0,1. Получают 1-(4-аминометилфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-(4-метоксифенил)азетидин-2-он (5) с молекулярной массой 434,51 (С26Н27FN2O3); MC (ESI): 418,2 (MH+-NH3).
f) 2,3,4,5,6-Пентагидроксигексиламид 4,4'-оксибисбензойной кислоты (6)
0,52 г 4,4'-Оксибисбензойной кислоты и 0,36 г D-глюкамина при комнатной температуре суспендируют в 10 мл безводного диметилформамида, смешивают с 0,31 г N-гидроксибензотриазола (HOBt) и 0,39 г EDC и перемешивают при комнатной температуре в течение 12 часов. Реакционную смесь выпаривают досуха и высушивают в высоком вакууме. Остаток тщательно перемешивают с водой, образовавшуюся суспензию фильтруют, остаток перемешивают с метанолом и снова отфильтровывают. Фильтрат концентрируют в ротационном испарителе до половины объема и раствор охлаждают на бане со льдом. Выпавший осадок отфильтровывают под вакуумом, промывают небольшим количеством охлажденного льдом метанола и высушивают в вакууме. Получают 2,3,4,5,6-пентагидроксигексиламид 4,4'-оксибисбензойной кислоты (6) с молекулярной массой 421,40 (С20Н23NO9); МС (ESI): 422,28 (МН+).
g) 2,3,4,5,6-Пентагидроксигексиламид 4-(4-{4-[3-[3-(4-фторфенил)-3-гидроксипропил]-2-(4-метоксифенил)-4-оксоазетидин-1-ил]бензилкарбамоил}фенокси)бензойной кислоты (7)
87 мг Соединения, полученного согласно е), и 90 мг соединения, полученного согласно f), при комнатной температуре растворяют в 3 мл безводного диметилформамида, смешивают с 31 мг HOBt и 39 мг EDC и перемешивают в течение 12 часов при комнатной температуре. Реакционную смесь выпаривают досуха в высоком вакууме и остаток перемешивают с дихлорметаном, отфильтровывают под вакуумом, промывают дихлорметаном и высушивают в вакууме. Получают 2,3,4,5,6-пентагидроксигексиламид 4-(4-{4-[3-[3-(4-фторфенил)-3-гидроксипропил]-2-(4-метоксифенил)-4-оксоазетидин-1-ил]бензилкарбамоил}фенокси)бензойной кислоты (7) с молекулярной массой 837,90 (С46Н48FN3O11); МС (ESI): 838,39 (MH+).
Пример II
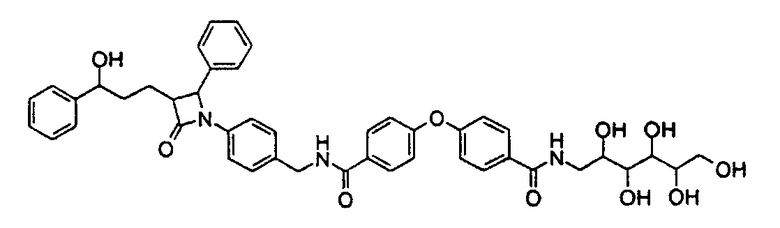
2,3,4,5,6-Пентагидроксигексиламид 4-(4-{4-[3-(3-гидрокси-3-фенилпропил)-2-оксо-4-фенилазетидин-1-ил]бензилкарбамоил}-фенокси)бензойной кислоты (9)
а) 1-(4-Аминометилфенил)-3-(3-гидрокси-3-фенилпропил)-4-фенилазетидин-2-он (8)
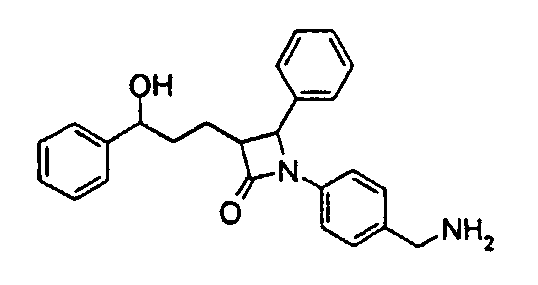
Это соединение получают как описано выше для получения 1-(4-аминометилфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-(4-метоксифенил)азетидин-2-она, с тем различием, что используют 3-[5-(трет-бутилдиметилсиланилокси)-5-фенилпентаноил]-4-фенилоксазолидин-2-он и 4-(бензилиденамино)бензонитрил. Получают 1-(4-аминометилфенил)-3-(3-гидрокси-3-фенилпропил)-4-фенилазетидин-2-он (8) с молекулярной массой 386,50 (С25Н26N2O2); MC (ESI): 370,2 (MH+- NH3).
b) 2,3,4,5,6-Пентагидроксигексиламид 4-(4-{4-[3-(3-гидрокси-3-фенилпропил)-2-оксо-4-фенилазетидин-1-ил]бензилкарбамоил}-фенокси)бензойной кислоты (9)
Бензиламин из IIa) вводят во взаимодействие с 2,3,4,5,6-пентагидроксигексиламидом 4,4'-оксибисбензойной кислоты из If), как описано в примере I. Получают 2,3,4,5,6-пентагидроксигексиламид 4-(4-{4-[3-(3-гидрокси-3-фенилпропил)-2-оксо-4-фенилазетидин-1-ил]бензилкарбамоил}фенокси)бензойной кислоты (9) с молекулярной массой 789,89 (С45Н47N3O10); MC (ESI): 790,26 (MH+).
Пример III
2,3,4,5,6-Пентагидроксигексиламид 4-(4-{4-[3-[3-(4-фторфенил)-3-гидроксипропил]-2-(4-метоксифенил)-4-оксоазетидин-1-ил]-бензилкарбамоил}бензил)бензойной кислоты (10)
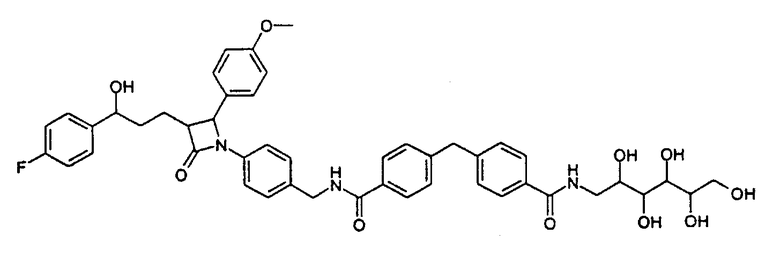
Соединение примера III получают аналогично методике примера I с тем различием, что используют 2,3,4,5,6-пентагидроксигексиламид дифенилметан-4,4'-дикарбоновой кислоты. Получают 2,3,4,5,6-пентагидроксигексиламид 4-(4-{4-[3-[3-(4-фторфенил)-3-гидроксипропил]-2-(4-метоксифенил)-4-оксоазетидин-1-ил]бензилкарбамоил}бензил)бензойной кислоты (10) с молекулярной массой 835,93 (С47Н50FN3O10); MC (ESI): 836,18 (MH+).
Пример IV
1-[4-(4-{1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил}феноксиметил)бензил]-4-аза-1-азонийбицикло[2,2,2]октанбромид (13)
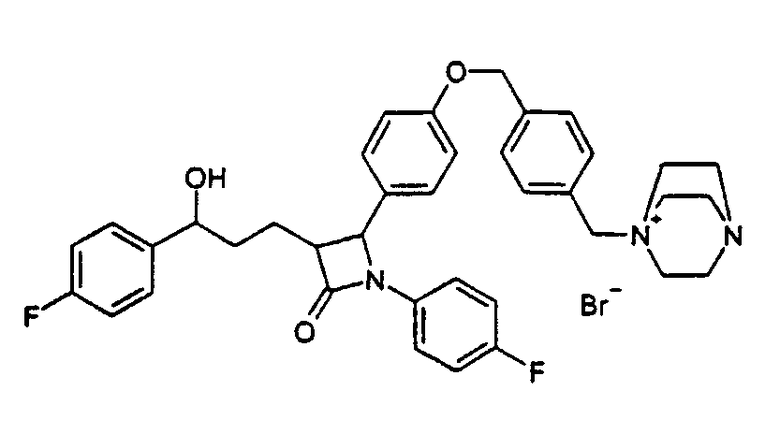
а) 4-[4-(4-Бромметилбензилокси)фенил]-1-(4-фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]азетидин-2-он (12)
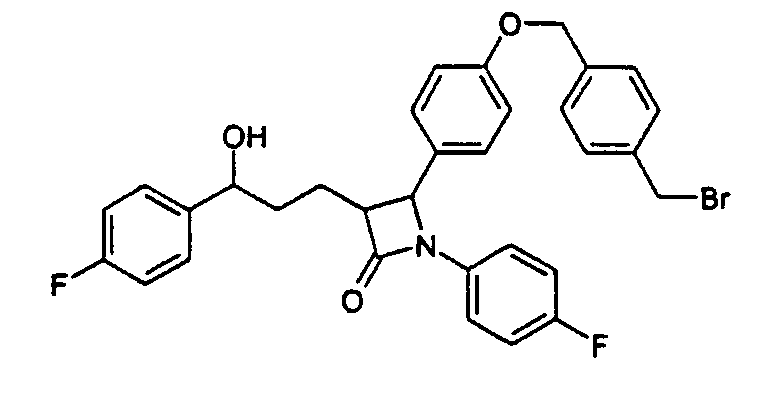
3,0 г 1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-(4-гидроксифенил)азетидин-2-она (11) вместе с 7,0 г 1,4-бисбромметилбензола и 5,0 г карбоната калия растворяют в 100 мл диметилформамида и перемешивают в течение 90 минут при комнатной температуре. После окончания реакции смесь растворяют в этилацетате и дважды встряхивают с водой. Органическую фазу сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Остаток очищают флэш-хроматографией (смесь н-гептана и этилацетата). Выход 3,2 г бесцветных кристаллов (12) с молекулярной массой 592,49 (С32Н28BrF2NO3); MC (ESI): 592,2 (MH+).
b) 1-[4-(4-{1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил}феноксиметил)бензил]-4-аза-1-азонийбицикло[2,2,2]октанбромид (13)
180 мг Соединения (12) вместе с 300 мг 1,4-диазабицикло[2,2,2]октана (DABCO) растворяют в 5 мл толуола и перемешивают в течение 90 минут при температуре 80°С. После окончания реакции смесь оставляют охлаждаться и бесцветное твердое вещество отфильтровывают под вакуумом. Получают 195 мг продукта (13) с молекулярной массой 704,66 (С38Н40BrF2N3O3); MC (ESI): 624,30 (MH+).
Пример V
1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-(4-{4-[(2,3,4,5,6-пентагидроксигексиламин)метил]бензилокси}фенил)-азетидин-2-он (14)
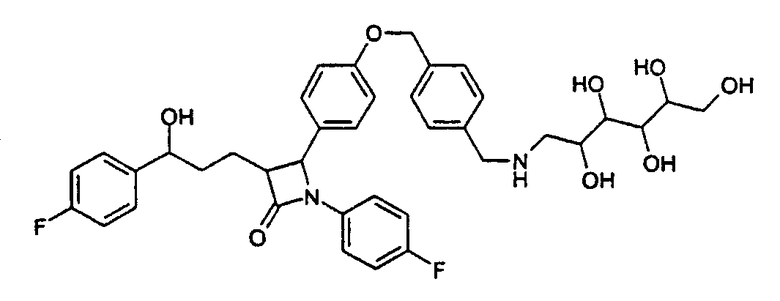
60 мг Соединения (12) вместе с 150 мг глюкамина растворяют в 5 мл диметилфорамида и перемешивают в течение 90 минут при температуре 80°С. После окончания реакции смесь растворяют в этилацетате и дважды встряхивают с водой. Органическую фазу сушат над сульфатом магния, фильтруют и концентрируют в вакууме. Остаток очищают флэш-хроматографией (смесь дихлорметана, метанола и концентрированного раствора аммиака в соотношении 30:10:3). Выход 33 мг бесцветного твердого вещества (14) с молекулярной массой 692,76 (С38Н42F2N2O8); MC (ESI): 693,5 (MH+).
Пример VI
1-[2-(4-{1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил}феноксиметил)бензил]-4-аза-1-азонийбицикло[2,2,2]октанбромид (16)
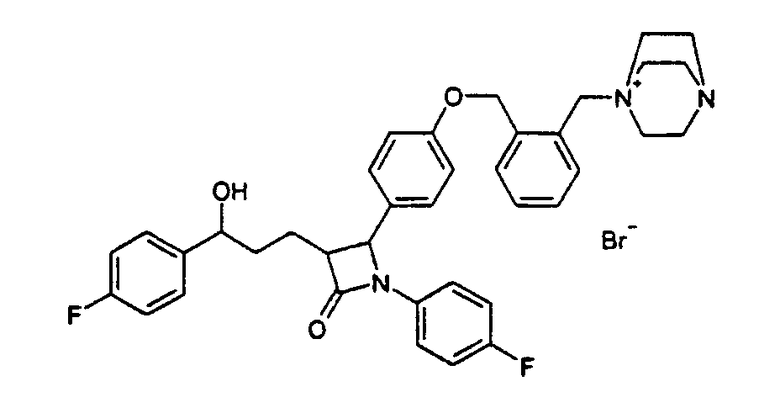
а) 4-[4-(2-Бромметилбензилокси)фенил]-1-(4-фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]азетидин-2-он (15)
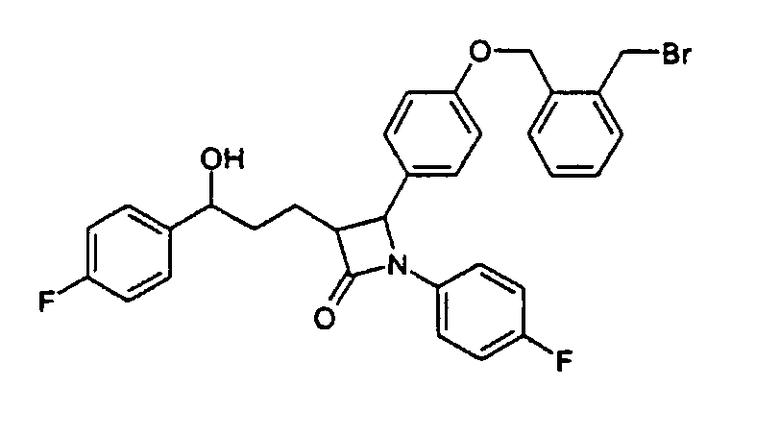
1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-(4-гидроксифенил)азетидин-2-он (11) вводят во взаимодействие с 1,2-бисбромметилбензолом и карбонатом калия аналогично методике примера IV и получают бесцветное твердое вещество (15) с молекулярной массой 592,49 (С32Н28BrF2NO3); MC (ESI): 592,2 (MH+).
b) 1-[2-(4-{1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил}феноксиметил)бензил]-4-аза-1-азонийбицикло[2,2,2]октанбромид (16)
Соединение (15) вместе с DABCO растворяют в толуоле и вводят во взаимодействие аналогично методике примера IV и получают продукт (16) в виде бесцветного твердого вещества с молекулярной массой 704,66 (С38Н40BrF2N3O3); MC (ESI): 624,30 (MH+).
Пример VII
1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-(4-{2-[(2,3,4,5,6-пентагидроксигексиламин)метил]бензилокси}фенил)-азетидин-2-он (17)
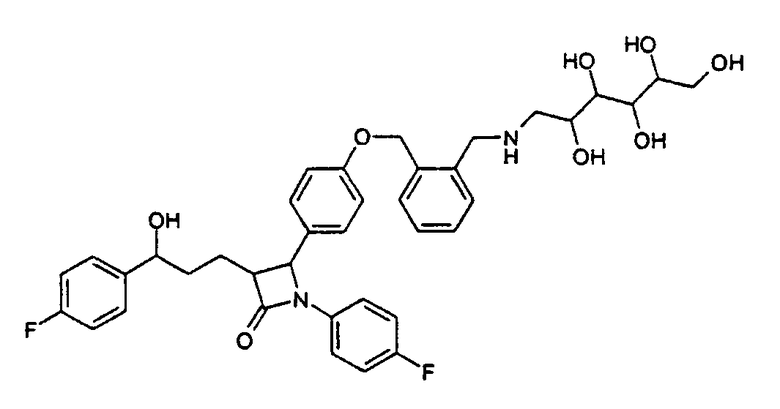
Соединение (15) вместе с глюкамином растворяют в диметилформамиде и вводят во взаимодействие аналогично методике примера V и получают продукт (17) в виде бесцветного твердого вещества с молекулярной массой 692,76 (С38Н42F2N2O8); MC (ESI): 693,5 (MH+).
Пример VIII
1-[3-(4-{1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил}феноксиметил)бензил]-4-аза-1-азонийбицикло[2,2,2]октанбромид (19)
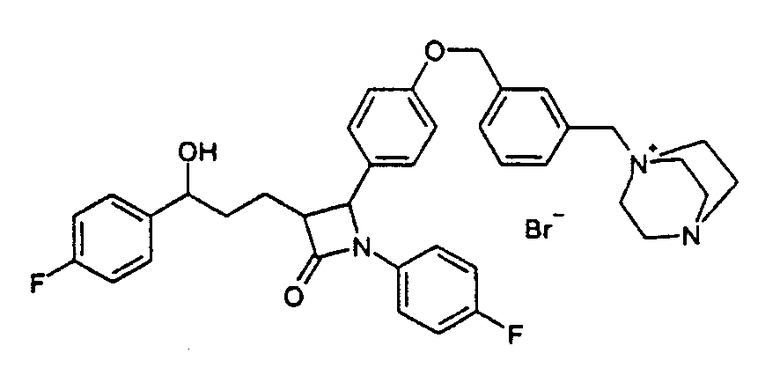
а) 4-[4-(3-Бромметилбензилокси)фенил]-1-(4-фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]азетидин-2-он (18)
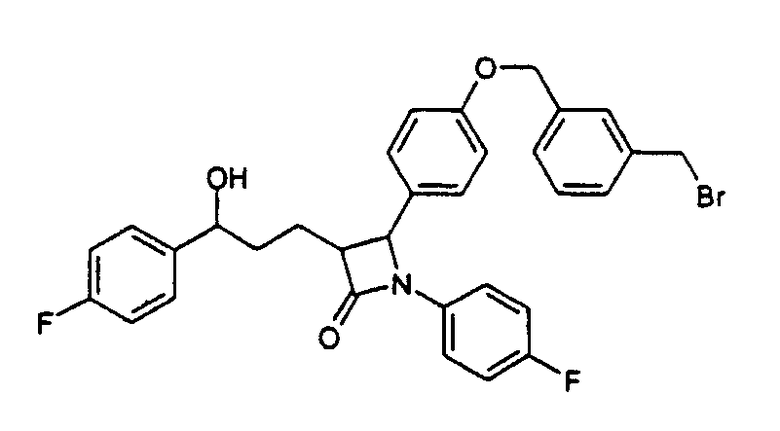
1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-(4-гидроксифенил)азетидин-2-он (11) вводят во взаимодействие с 1,3-бисбромметилбензолом и карбонатом калия аналогично методике примера IV и получают бесцветное твердое вещество (18) с молекулярной массой 592,49 (С32Н28BrF2NO3); MC (ESI): 592,2 (MH+).
b) 1-[3-(4-{1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил}феноксиметил)бензил]-4-аза-1-азонийбицикло[2,2,2]октанбромид (19)
Соединение (18) вместе с DABCO растворяют в толуоле и вводят во взаимодействие аналогично методике примера IV и получают продукт (19) в виде бесцветного твердого вещества с молекулярной массой 704,66 (С38Н40BrF2N3O3); MC (ESI): 624,30 (MH+).
Пример IX
1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-(4-{3-[(2,3,4,5,6-пентагидроксигексиламин)метил]бензилокси}фенил)-азетидин-2-он (20)
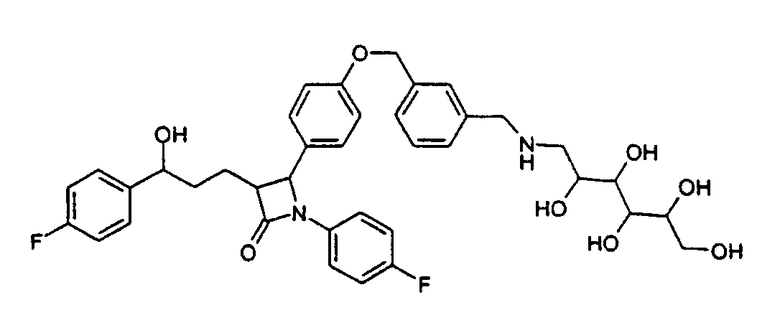
Соединение (18) вместе с глюкамином растворяют в диметилформамиде и вводят во взаимодействие аналогично методике примера V и получают продукт (20) в виде бесцветного твердого вещества с молекулярной массой 692,76 (С38Н42F2N2O8); MC (ESI): 693,5 (MH+).
Пример X
1-[4'-(4-{1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил}феноксиметил)бифенил-4-илметил]-4-аза-1-азонийбицикло[2,2,2]октанбромид (22)
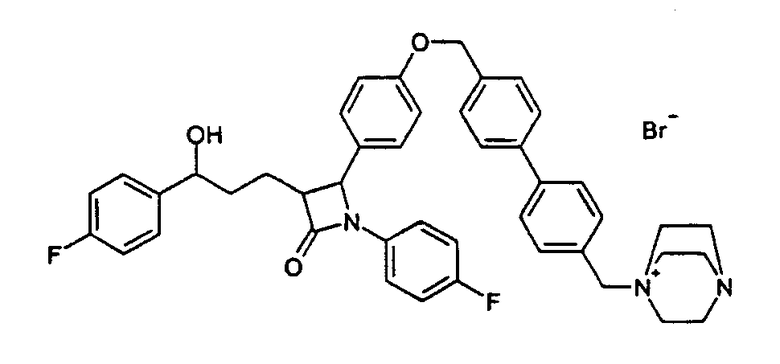
а) 4-[4-(4'-Бромметилбифенил-4-илметокси)фенил]-1-(4-фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]азетидин-2-он (21)
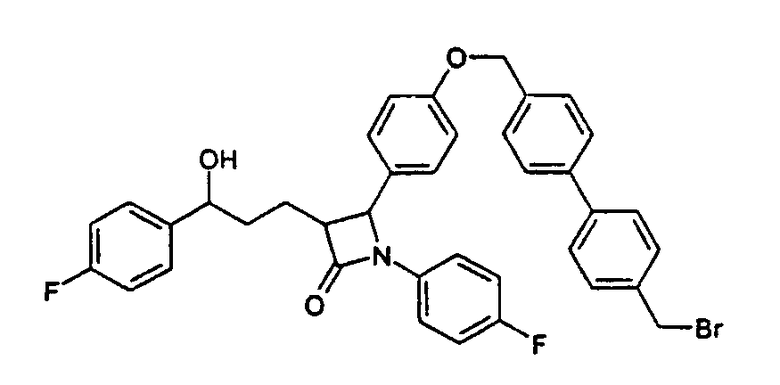
1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-(4-гидроксифенил)азетидин-2-он (11) вводят во взаимодействие с 4,4'-бисбромметилбифенилом и карбонатом калия аналогично методике примера IV и получают бесцветное твердое вещество (21) с молекулярной массой 668,54 (С38Н32BrF2NO3); MC (ESI): 668,1 (MH+).
b) 1-[4'-(4-{1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил}феноксиметил)бифенил-4-илметил]-4-аза-1-азонийбицикло[2,2,2]октанбромид (22)
Соединение (21) вместе с DABCO растворяют в толуоле и вводят во взаимодействие аналогично методике примера IV и получают продукт (22) в виде бесцветного твердого вещества с молекулярной массой 780,76 (С44Н44BrF2N3O3); MC (ESI): 700,3 (MH+).
Пример XI
1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-(4-{4'-[(2,3,4,5,6-пентагидроксигексиламин)метил]бифенил-4-илметокси}-фенил)азетидин-2-он (23)
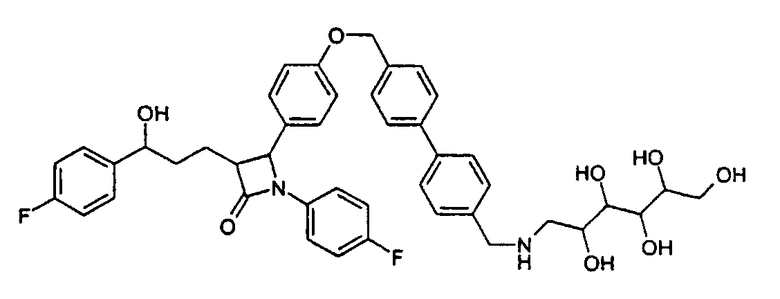
Соединение (21) вместе с глюкамином растворяют в диметилформамиде и вводят во взаимодействие аналогично методике примера V и получают продукт (23) в виде бесцветного твердого вещества с молекулярной массой 768,86 (С44Н46F2N2O8); MC (ESI): 769,3 (MH+).
Пример XII
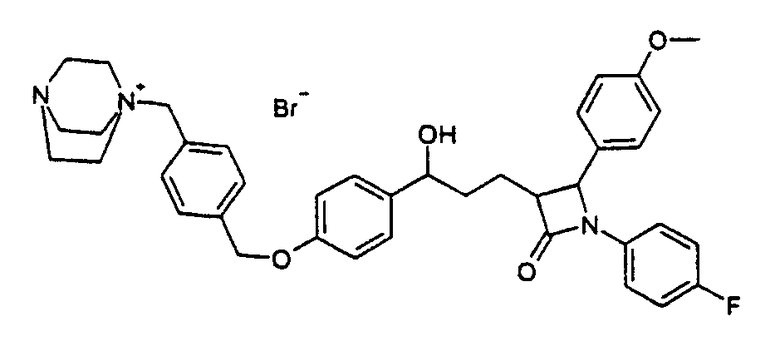
1-(4-{4-[3-[3-(4-Фторфенил)-3-гидроксипропил]-2-(4-метоксифенил)-4-оксоазетидин-1-ил]феноксиметил}бензил)-4-аза-1-азонийбицикло[2,2,2]октанбромид (26)
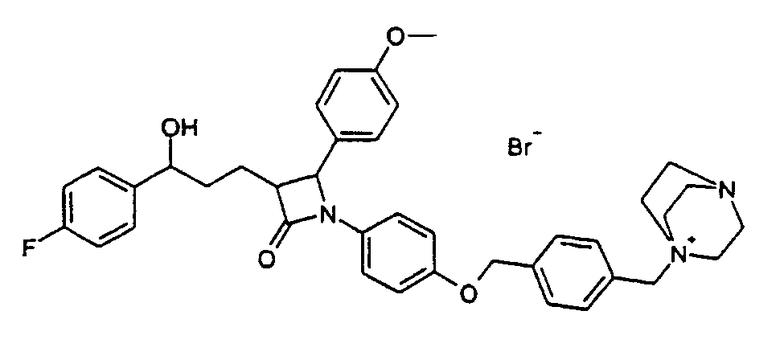
а) 3-[3-(4-Фторфенил)-3-гидроксипропил]-1-(4-гидроксифенил)-4-(4-метоксифенил)азетидин-2-он (24)
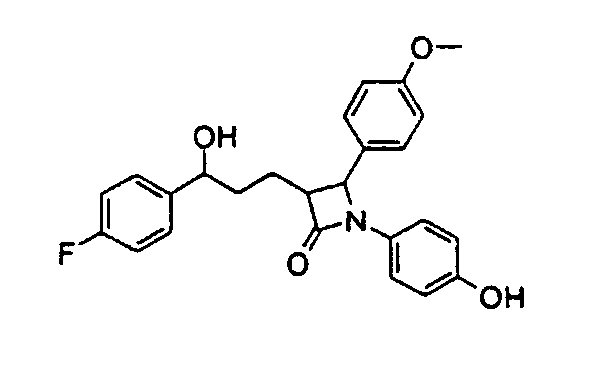
Это соединение получают как описано выше для получения 1-(4-аминометилфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-(4-метоксифенил)азетидин-2-она (стадии а, b, c и d), с тем различием, что используют 4-[(4-метоксибензилиден)амино]фенол. Получают 3-[3-(4-фторфенил)-3-гидроксипропил]-1-(4-гидроксифенил)-4-(4-метоксифенил)азетидин-2-он (24) с молекулярной массой 421,47 (С25Н24FNO4); MC (ESI): 422,2 (MH+).
b) 1-[4-(4-Бромметилбензилокси)фенил]-3-[3-(4-фторфенил)-3-гидроксипропил]-4-(4-метоксифенил)азетидин-2-он (25)
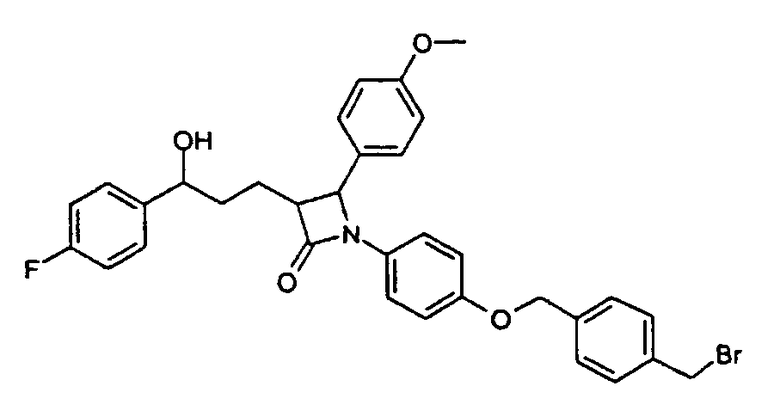
3-[3-(4-Фторфенил)-3-гидроксипропил]-1-(4-гидроксифенил)-4-(4-метоксифенил)азетидин-2-он вводят во взаимодействие с 1,4-бисбромметилбензолом и карбонатом калия аналогично методике примера IV и получают бесцветное твердое вещество (25) с молекулярной массой 604,52 (С33Н31BrFNO4); MC (ESI): 605,2 (MH+).
c) 1-(4-{4-[3-[3-(4-Фторфенил)-3-гидроксипропил]-2-(4-метоксифенил)-4-оксоазетидин-1-ил]феноксиметил}бензил)-4-аза-1-азонийбицикло[2,2,2]октанбромид (26)
Соединение (25) вместе с DABCO растворяют в толуоле и вводят во взаимодействие аналогично методике примера IV и получают продукт (26) в виде бесцветного твердого вещества с молекулярной массой 716,70 (С39Н43BrFN3O4); MC (ESI): 636,3 (MH+).
Пример XIII
3-[3-(4-Фторфенил)-3-гидроксипропил]-4-(4-метоксифенил)-1-(4-{4-[(2,3,4,5,6-пентагидроксигексиламин)метил]бензилокси}-фенил)азетидин-2-он (27)
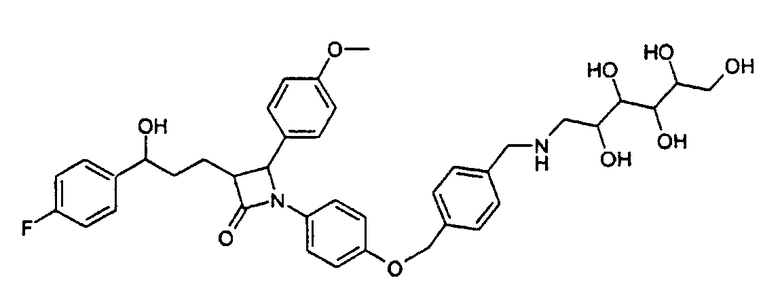
Соединение (25) вместе с глюкамином растворяют в диметилформамиде и вводят во взаимодействие аналогично методике примера V и получают продукт (27) в виде бесцветного твердого вещества с молекулярной массой 704,80 (С39Н45FN2O9); MC (ESI): 705,31 (MH+).
Пример XIV
1-[4-(4-{3-[1-(4-Фторфенил)-2-(4-метоксифенил)-4-оксоазетидин-3-ил]-1-гидроксипропил}феноксиметил)бензил]-4-аза-1-азонийбицикло[2,2,2]октанбромид (30)
а) 1-(4-Фторфенил)-3-[3-гидрокси-3-(4-гидроксифенил)пропил]-4-(4-метоксифенил)азетидин-2-он (28)
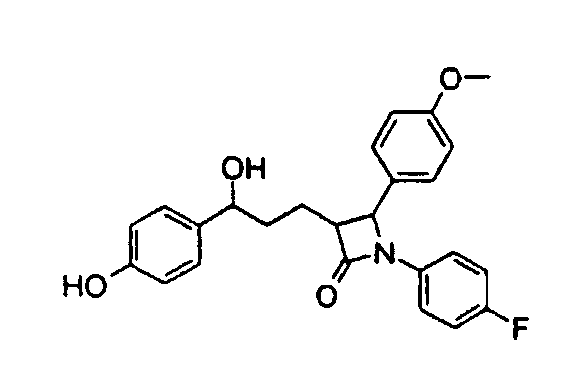
Это соединение получают, как описано выше в случае получения 1-(4-аминометилфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-(4-метоксифенил)азетидин-2-она, с тем различием, что используют 3-[5-(4-гидроксифенил)-5-гидроксипентаноил]-4-фенилоксазолидин-2-он и (4-фторфенил)-(4-метоксибензилиден)амин. Получают 1-(4-фторфенил)-3-[3-гидрокси-3-(4-гидроксифенил)пропил]-4-(4-метоксифенил)азетидин-2-он (28) с молекулярной массой 421,47 (С25Н24FNO4); MC (ESI): 422,2 (MH+).
b) 3-{3-[4-(4-Бромметилбензилокси)фенил]-3-гидроксипропил}-1-(4-фторфенил)-4-(4-метоксифенил)азетидин-2-он (29)
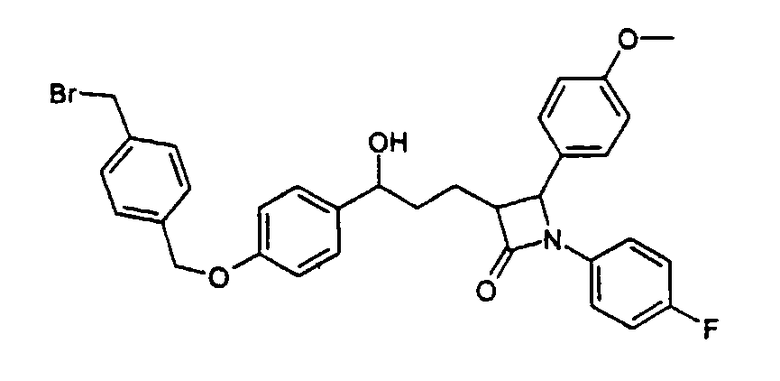
1-(4-Фторфенил)-3-[3-гидрокси-3-(4-гидроксифенил)пропил]-4-(4-метоксифенил)азетидин-2-он вводят во взаимодействие с 1,4-бисбромметилбензолом и карбонатом калия аналогично методике примера IV и получают бесцветное твердое вещество (29) с молекулярной массой 604,52 (С33Н31BrFNO4); MC (ESI): 605,2 (MH+).
c) 1-[4-(4-{3-[1-(4-Фторфенил)-2-(4-метоксифенил)-4-оксоазетидин-3-ил]-1-гидроксипропил}феноксиметил)бензил]-4-аза-1-азонийбицикло[2,2,2]октанбромид (30)
Соединение (29) вместе с DABCO растворяют в толуоле и вводят во взаимодействие аналогично методике примера IV и получают продукт (30) в виде бесцветного твердого вещества с молекулярной массой 716,70 (С39Н43BrFN3O4); MC (ESI): 636,3 (MH+).
Пример XV
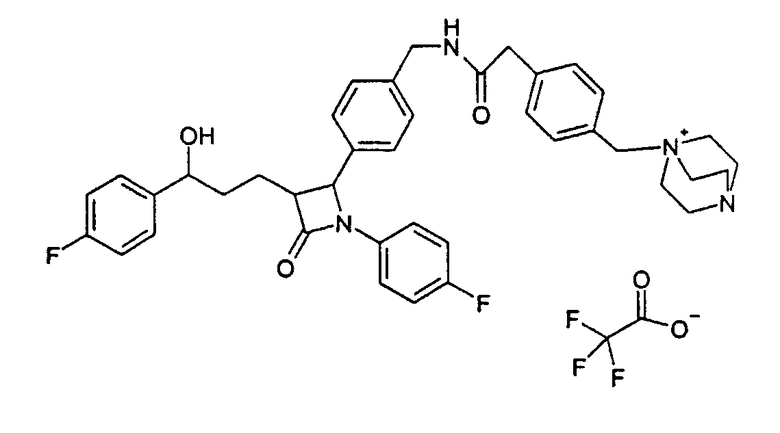
1-{4-[(4-{1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил}бензилкарбамоил)метил]бензил}-4-аза-1-азонийбицикло[2,2,2]октантрифторацетат (35)
а) 1-(4-Карбоксиметилбензил)-4-аза-1-азонийбицикло[2,2,2]октанбромид (31)
К раствору 1,5 г 1,4-диазабицикло[2,2,2]октана в 10 мл диметилсульфоксида при температуре 70°С добавляют 1,0 г (3-бромметилфенил)уксусной кислоты в 5 мл диметилсульфоксида. Спустя 1 час добавляют 100 мл воды и подвергают сушке вымораживанием. Остаток настаивают с ацетоном. Остаток содержит продукт с молекулярной массой 261,35 (катион: С15Н21N2O2 +); MC (ESI): 261,1 (M+).
b) 4-[5-(4-Фторфенил)-1-(4-фторфениламино)-5-гидрокси-2-(2-оксо-4-фенилоксазолидин-3-карбонил)пентил]бензонитрил (32)
2,5 г 3-[5-(4-Фторфенил)-5-гидроксипентаноил]-4-фенилоксазолидин-2-она растворяют в атмосфере аргона, в 30 мл дихлорметана, к полученному раствору добавляют 3,9 г 4-[(4-фторфениламино)метил]бензонитрила и охлаждают до температуры -10°С. К этой смеси добавляют 6,4 мл диизопропилэтиламина и в течение 30 минут 4,05 мл триметилсилилхлорида так, чтобы температура не превышала -5°С. При этой температуре дополнительно перемешивают в течение 1 часа и затем охлаждают до температуры -25°С. После этого медленно добавляют 0,8 мл тетрахлорида титана. Смесь темного цвета перемешивают в течение ночи при температуре от -25°С до -30°С, после чего разлагают с помощью 35 мл 7%-ного раствора винной кислоты и дополнительно перемешивают в течение 1 часа при комнатной температуре. Затем в эту смесь добавляют 15 мл 20%-ного раствора гидрокарбоната натрия и снова перемешивают в течение 1 часа. После разделения фаз органическую фазу промывают с помощью 30 мл воды, сушат над сульфатом магния и концентрируют до объема примерно 10 мл. После добавления 2 мл бистриметилсилилацетамида в течение 30 минут кипятят с обратным холодильником и после этого концентрируют в вакууме. Остаток с помощью смеси этилацетата и гептана доводят до кристаллизации. Отфильтровывают под вакуумом и высушивают в вакууме. Получают продукт с молекулярной массой 653,81 (С37Н37F2N3O4Si); MC (ионизация электронным распылением с образованием положительных ионов (ESI+)): 654,3 (М+Н+), 582,2 (М+Н+-Si(CH3)3).
с) {1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил}бензонитрил (33)
2 г 4-[5-(4-Фторфенил)-1-(4-фторфениламино)-5-гидрокси-2-(2-оксо-4-фенилоксазолидин-3-карбонил)пентил]бензонитрила растворяют в 20 мл метил-трет-бутилового эфира и вместе с 100 мг тетрабутиламмонийфторидтригидрата и 1,3 мл бистриметилсилилацетамида нагревают примерно 1 час при температуре 40°С. За протеканием реакции следят с помощью тонкослойной хроматограммы. По окончании взаимодействия сначала добавляют 0,2 мл ледяной уксусной кислоты, перемешивают в течение 30 минут и концентрируют. Остаток смешивают с 20 мл смеси из изопропанола и 2 н. серной кислоты в соотношении 10:1 и перемешивают в течение 1 часа. После добавления на кончике шпателя твердого гидрокарбоната натрия снова концентрируют в вакууме, обрабатывают этилацетатом, органическую фазу промывают водой, сушат и после удаления растворителя остаток очищают колоночной хроматографией (SiO2; CH2Cl2/метанол =100:1). Получают продукт с молекулярной массой 418,45 (С25Н20F2N2O2); MC (десорбционно-химическая ионизация с образованием положительных ионов (DCI+)): 419 (M + H+).
d) 4-(4-Аминометилфенил)-1-(4-фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]азетидин-2-он (34)
200 мг {1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил}бензонитрила растворяют в 20 мл этанола и вместе с 0,5 мл концентрированного раствора аммиака в присутствии никеля Ренея гидрируют в течение 30 часов при давлении водорода 75 бар и при температуре 25°С. Отфильтровывают под вакуумом от катализатора, концентрируют в вакууме и остаток очищают колоночной хроматографией (SiO2; смесь CH2Cl2, метанола и концентрированного раствора аммиака в соотношении 100:10:1). Получают продукт с молекулярной массой 422,5 (С25Н22F2N2O2); MC (DCI+): 423 (M+H+), 405 (M+H+- H2O).
e) 1-{4-[(4-{1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил}бензилкарбамоил)метил]бензил}-4-аза-1-азонийбицикло[2,2,2]октантрифторацетат (35)
К раствору из 84 мг 1-(4-карбоксиметилбензил)-4-аза-1-азонийбицикло[2,2,2]октанбромида, 64 мкл диизопропилкарбодиимида, 56 мг гидроксибензотриазола в 2 мл диметилформамида добавляют раствор из 70 мг 4-(4-аминометилфенил)-1-(4-фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]азетидин-2-она, 23 мкл триэтиламина в 0,5 мл диметилформамида и перемешивают в течение 12 часов при комнатной температуре. Реакционный раствор концентрируют и разделяют высокоэффективной жидкостной хроматографией (ВЭЖХ) (Knauer Eurosper-100-10-C18, вода (0,1% трифторуксусной кислоты)/ацетонитрил (0,1% трифторуксусной кислоты)=80:20 (10:90). Получают продукт с молекулярной массой 665,81 (катион: С40Н43F2N4O3); MC (ESI): 665,33 (M+).
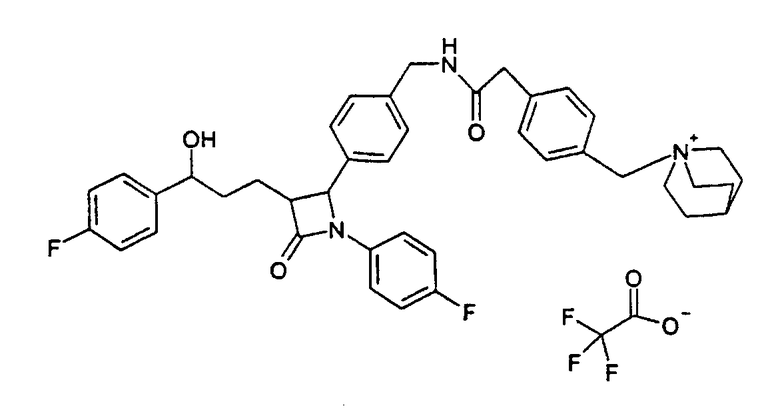
Пример XVI
1-{4-[(4-{1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил}бензилкарбамоил)метил]бензил}-1-азонийбицикло[2,2,2]октантрифторацетат (37)
а) 1-(4-Карбоксиметилбензил)-1-азонийбицикло[2,2,2]октанбромид (36)
Синтез осуществляют аналогично методике примера XVa), исходя из 1,67 г 1-азабицикло[2,2,2]октана. Получают продукт с молекулярной массой 260,36 (катион: С16Н22N1O2 +); MC (ESI): 260,1 (M+).
b) 1-{4-[(4-{1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил}бензилкарбамоил)метил]бензил}-1-азонийбицикло[2,2,2]октантрифторацетат (37)
Синтез осуществляют аналогично методике примера XVe), исходя из 70 мг 4-(4-аминометилфенил)-1-(4-фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]азетидин-2-она и 85 мг 1-(4-карбоксиметилбензил)-1-азонийбицикло[2,2,2]октанбромида. Получают продукт с молекулярной массой 664,82 (катион: С41Н44F2N3O3 +); MC (ESI): 664,33 (M+).
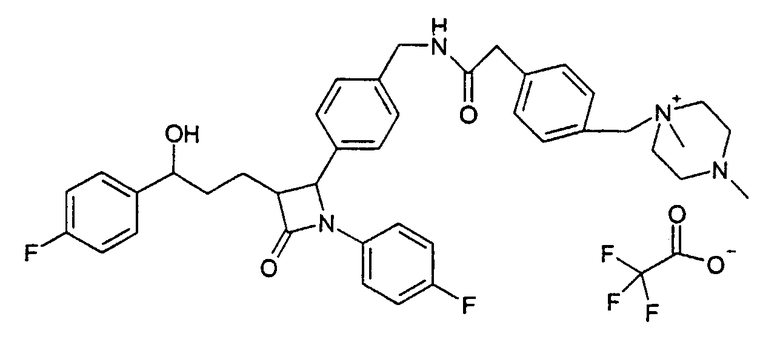
Пример XVII
1-{4-[(4-{1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил}бензилкарбамоил)метил]бензил}-1,4-диметилпиперазин-1-ийтрифторацетат (39)
а) 1-(4-Карбоксиметилбензил)-1,4-диметилпиперазин-1-ийбромид (38)
Синтез осуществляют аналогично методике примера XVa), исходя из 1,02 мл 1,4-диметилпиперазина. Получают продукт с молекулярной массой 263,36 (катион: С15Н23N2O2 +); MC (ESI): 263,1 (M+).
b) 1-{4-[(4-{1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил}бензилкарбамоил)метил]бензил}-1,4-диметилпиперазин-1-ийтрифторацетат (39)
Синтез осуществляют аналогично методике примера XVe), исходя из 70 мг 4-(4-аминометилфенил)-1-(4-фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]азетидин-2-она и 86 мг 1-(4-карбоксиметилбензил)-1,4-диметилпиперазин-1-ийбромида. Получают продукт с молекулярной массой 667,82 (катион: С40Н45F2N4O3 +); MC (ESI): 667,34 (M+).
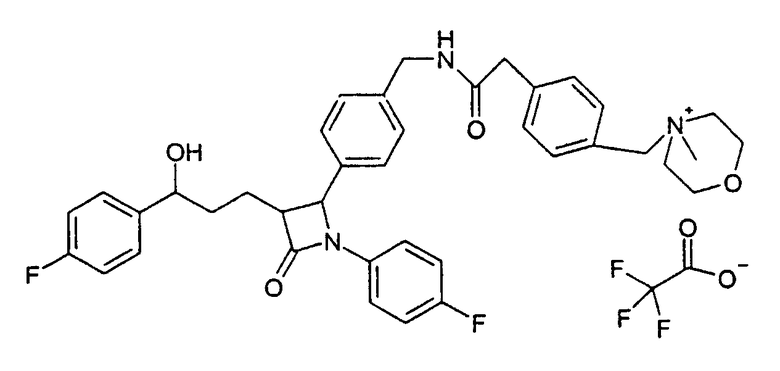
Пример XVIII
1-{4-[(4-{1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил}бензилкарбамоил)метил]бензил}-4-метилморфолин-4-ийтрифторацетат (41)
а) 4-(4-Карбоксиметилбензил)-4-метилморфолин-4-ийбромид (40)
Синтез осуществляют аналогично методике примера XVa), исходя из 1,65 мл N-метилморфолина. Получают продукт с молекулярной массой 250,32 (катион: С14Н20N1O3 +); MC (ESI): 250,1 (M+).
b) 4-{4-[(4-{1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил}бензилкарбамоил)метил]бензил}-4-метилморфолин-4-ийтрифторацетат (41)
Синтез осуществляют аналогично методике примера XVe), исходя из 70 мг 4-(4-аминометилфенил)-1-(4-фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]азетидин-2-она и 82 мг 4-(4-карбоксиметилбензил)-4-метилморфолин-4-ийбромида. Получают продукт с молекулярной массой 654,78 (катион: С39Н42F2N3O4 +); MC (ESI): 654,31 (M+).
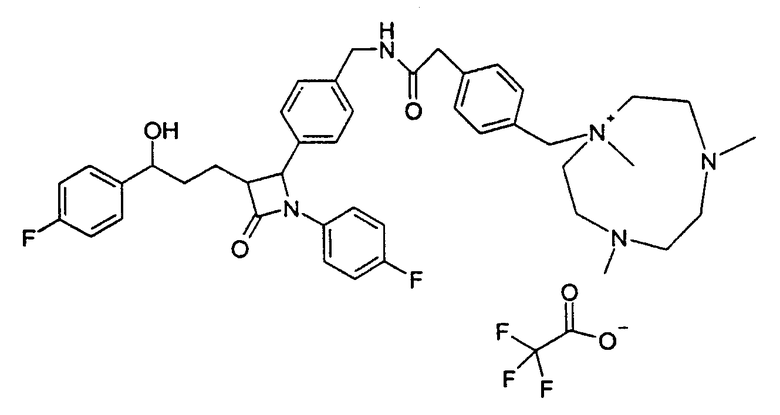
Пример XIX
1-{4-[(4-{1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил}бензилкарбамоил)метил]бензил}-1,4,7-триметил[1,4,7]триазонан-1-ийтрифторацетат (43)
а) 1,4,7-Триметил-1-[4-(2-оксопропил)бензил]-[1,4,7]триазонан-1-ийбромид (42)
Синтез осуществляют аналогично методике примера XVa), исходя из 500 мг 1,4,7-триметил-[1,4,7]триазонана. Получают продукт с молекулярной массой 321,47 (катион: С18Н31N3O2 +); MC (ESI): 321,2 (M+).
b) 1-{4-[(4-{1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил}бензилкарбамоил)метил]бензил}-1,4,7-триметил-[1,4,7]триазонан-1-ийтрифторацетат (43)
Синтез осуществляют аналогично методике примера XVe), исходя из 70 мг 4-(4-аминометилфенил)-1-(4-фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]азетидин-2-она и 200 мг 1,4,7-триметил-1-[4-(2-оксопропил)бензил]-[1,4,7]триазонан-1-ийбромида. Получают продукт с молекулярной массой 724,92 (катион: С40Н45F2N4O3 +); MC (ESI): 724,40 (M+).
Пример ХХ
1-[4-({4-[3-(3-Гидрокси-3-фенилпропил)-2-оксо-4-фенилазетидин-1-ил]бензилкарбамоил}метил)бензил]-4-аза-1-азонийбицикло[2,2,2]октантрифторацетат (44)
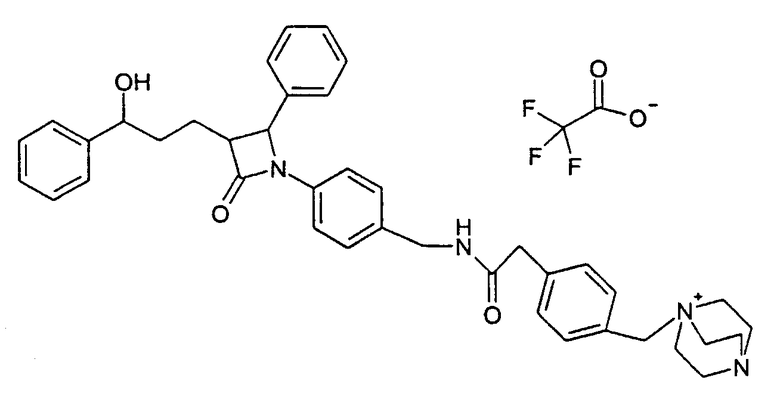
Синтез осуществляют аналогично методике примера XVe), исходя из 60 мг 1-(4-аминометилфенил)-3-(3-гидрокси-3-фенилпропил)-4-фенилазетидин-2-она (8) и 82 мг 1-(4-карбоксиметилбензил)-4-аза-1-азонийбицикло[2,2,2]октанбромида. Получают продукт с молекулярной массой 629,83 (катион: С40Н45F2N4O3 +); MC (ESI): 629,35 (M+).
Пример XXI
N-(4-{1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил}бензил)-2-{4-[(2,3,4,5,6-пентагидроксигексиламино)метил]фенил}ацетамид (46)
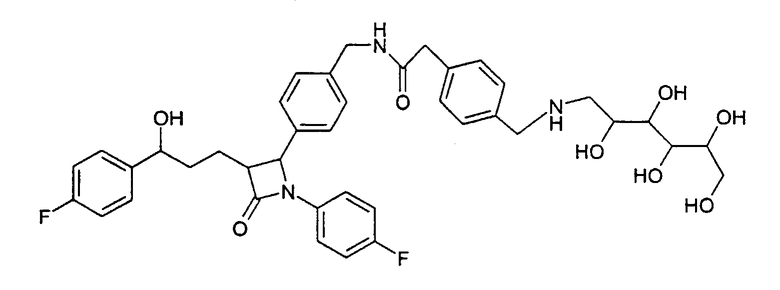
а) {4-[(2,3,4,5,6-Пентагидроксигексиламино)метил]фенил}уксусная кислота (45)
Синтез осуществляют аналогично методике примера XVa), исходя из 989 мг 6-аминогексан-1,2,3,4,5-пентаола. Получают продукт с молекулярной массой 329,35 (С15Н23N1O7); MC (ESI): 330,2 (M+Н+).
b) N-(4-{1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил}бензил)-2-{4-[(2,3,4,5,6-пентагидроксигексиламино)метил]фенил}ацетамид (46)
Синтез осуществляют аналогично методике примера XVe), исходя из 70 мг 4-(4-аминометилфенил)-1-(4-фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]азетидин-2-она и 110 мг {4-[(2,3,4,5,6-пентагидроксигексиламино)метил]фенил}уксусной кислоты. Получают продукт с молекулярной массой 733,82 (C40H45F2N3O8 +); MC (ESI): 734,32 (M+H+).
Пример XXII
N-(4-{1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил}бензил)-2-(4-{[метил-(2,3,4,5,6-пентагидроксигексил)амино]метил}фенил)ацетамид (48)
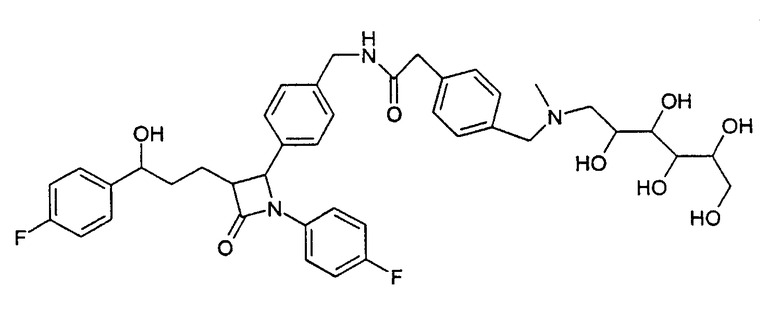
а) (4-{[Метил-(2,3,4,5,6-пентагидроксигексил)амино]метил}-фенил)уксусная кислота (47)
Синтез осуществляют аналогично методике примера XVa), исходя из 1,06 г 6-метиламиногексан-1,2,3,4,5-пентаола. Получают продукт с молекулярной массой 343,38 (С16Н25N1O7); MC (ESI): 344,2 (M+H+).
b) N-(4-{1-(4-Фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил}бензил)-2-(4-{[метил-(2,3,4,5,6-пентагидроксигексил)амино]метил}фенил)ацетамид (48)
Синтез осуществляют аналогично методике примера XVe), исходя из 70 мг 4-(4-аминометилфенил)-1-(4-фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]азетидин-2-она и 114 мг (4-{[метил-(2,3,4,5,6-пентагидроксигексил)амино]метил}фенил)уксусной кислоты. Получают продукт с молекулярной массой 747,84 (C41H47F2N3O8 +); MC (ESI): 748,35 (M+H+).
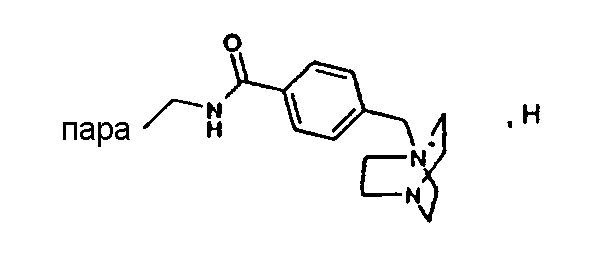
(М+)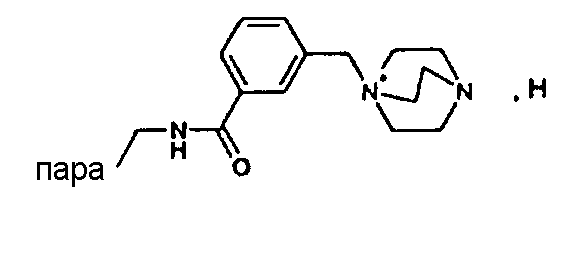
(М+)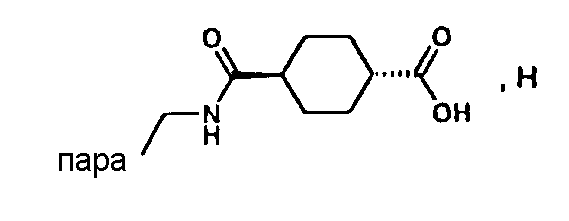
(МН+)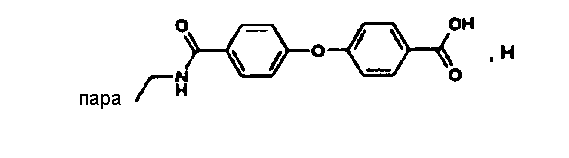
(МН+)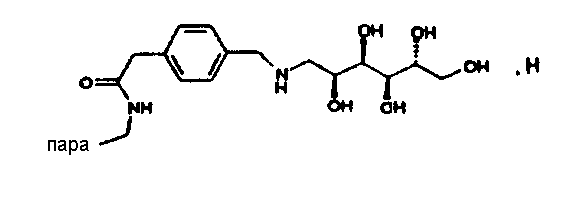
(МН+)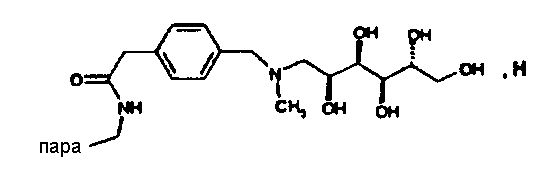
(МН+)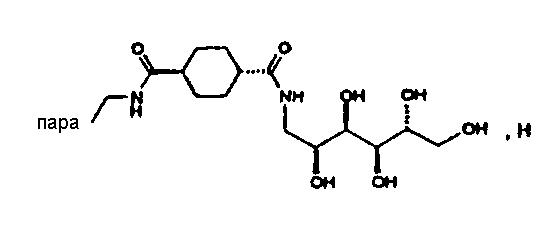
(МН+)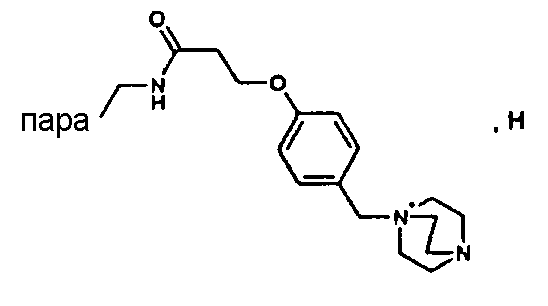
(М+)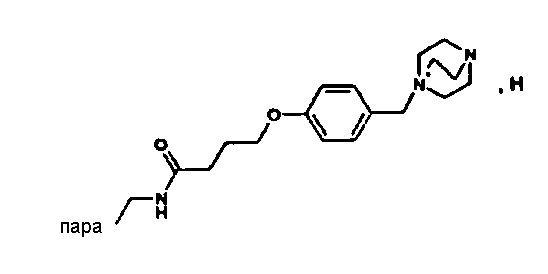
(М+)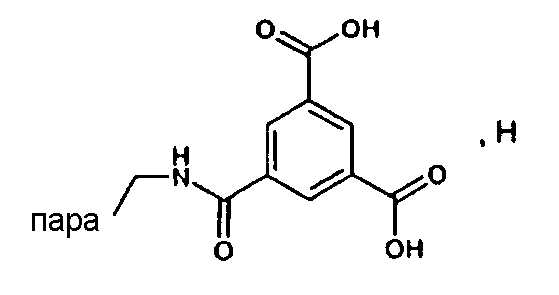
(МН+-H2O)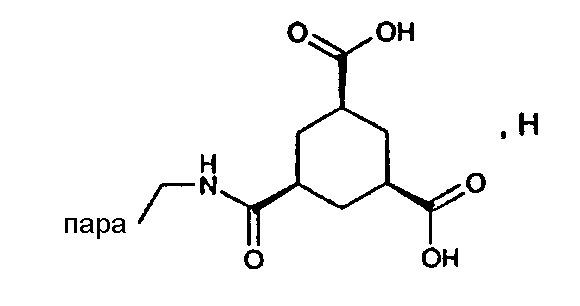
(МН+)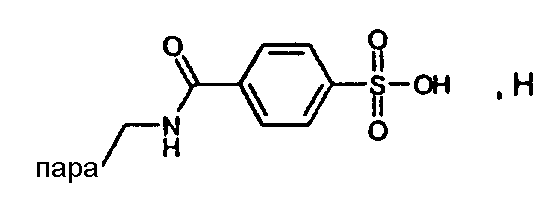
(МН+)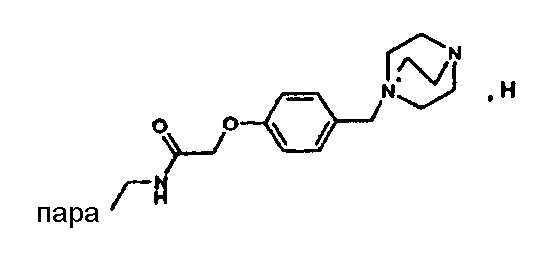
(М+)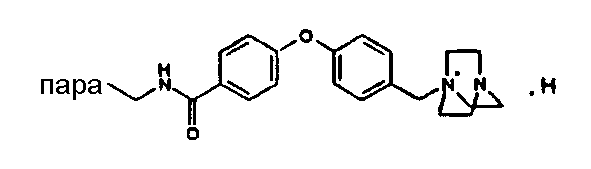
(М+)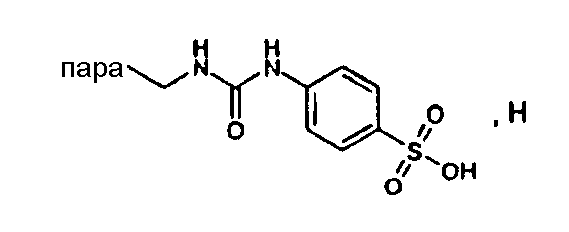
(МН+)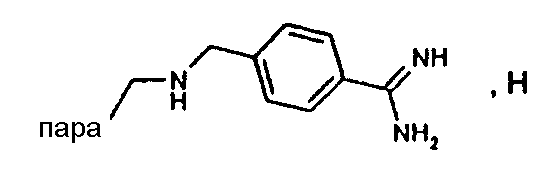
(МН+)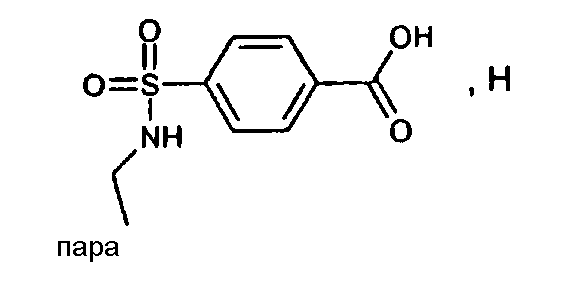
(МН+)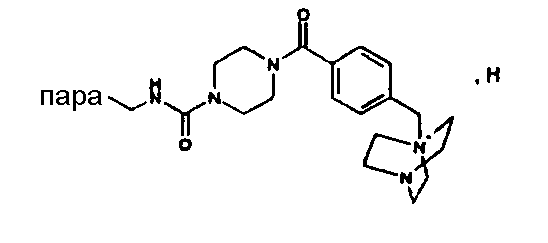
(М+)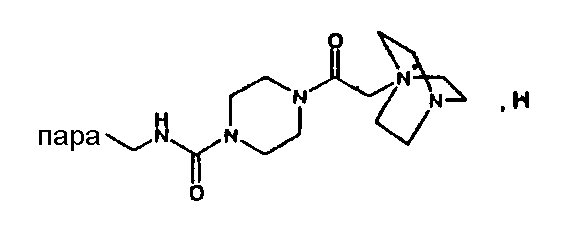
(М+)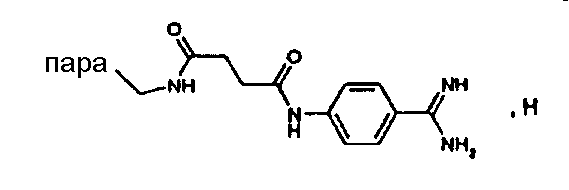
(МН+)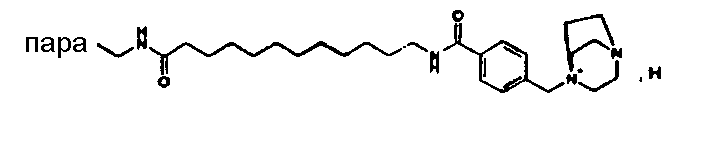
(М+)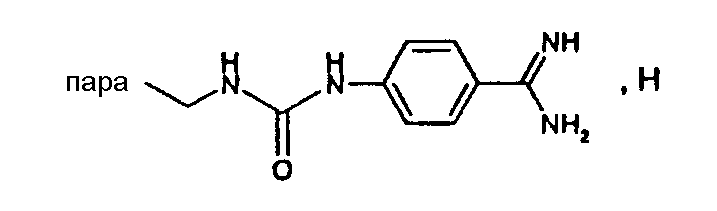
(МН+)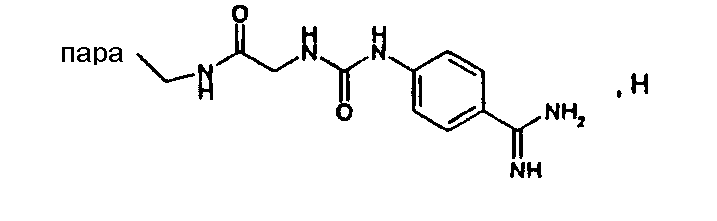
(МН+)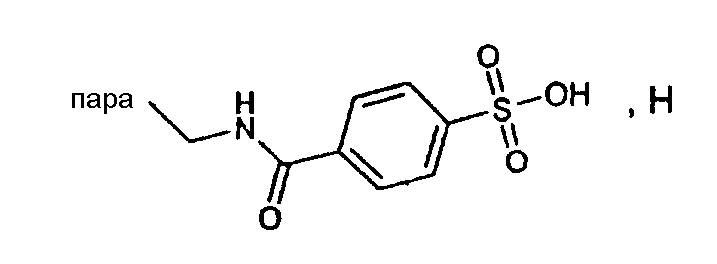
(М-Н+; измерено в отрицательной области)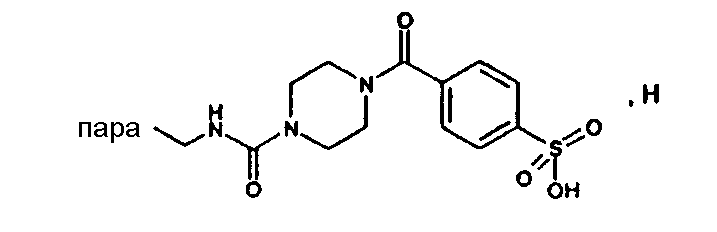
(МН+)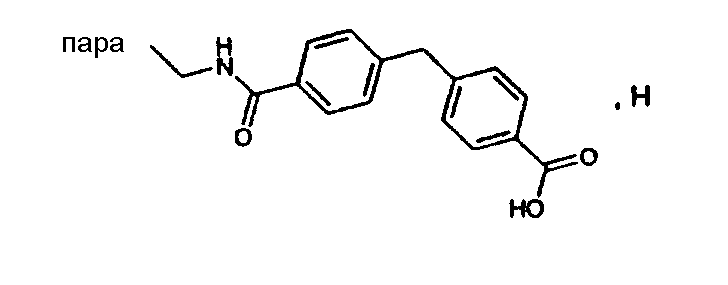
(МН+-H2O)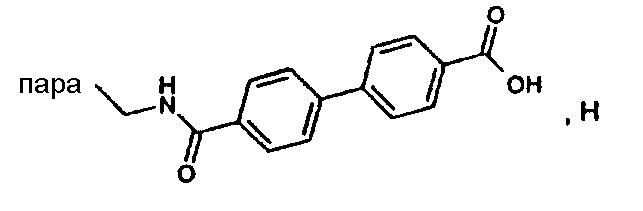
(МН+)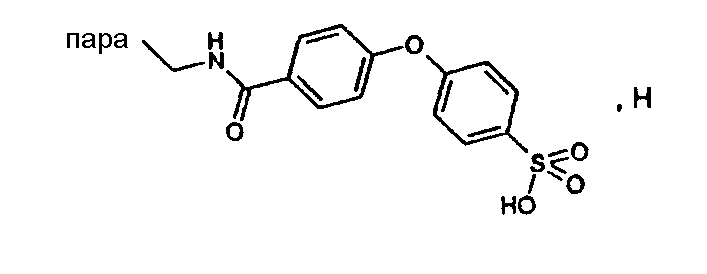
(МН+-H2O)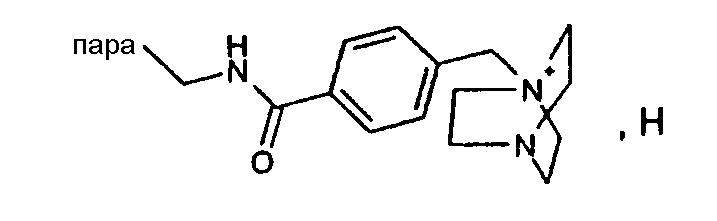
(М+)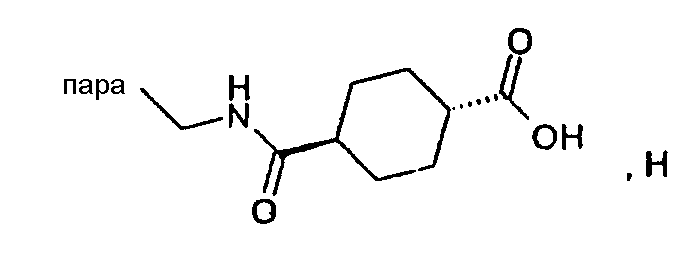
(МН+)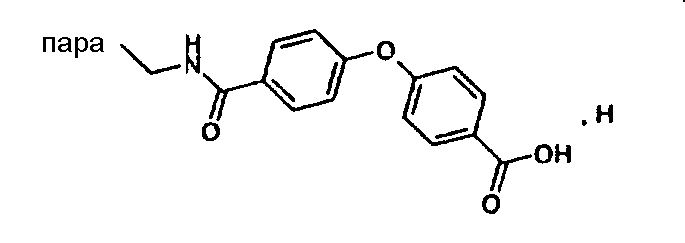
(МН+-H2O)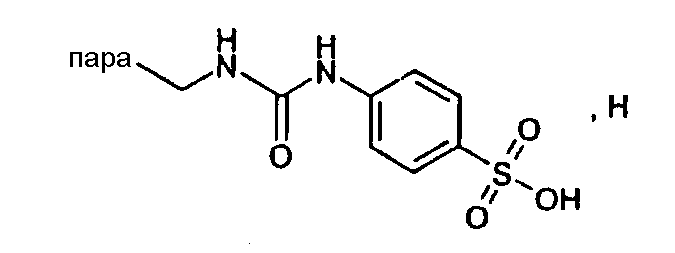
(М+-H2O)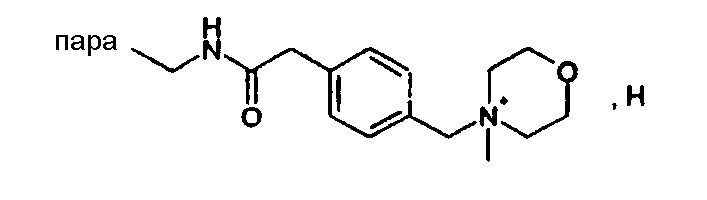
(М+)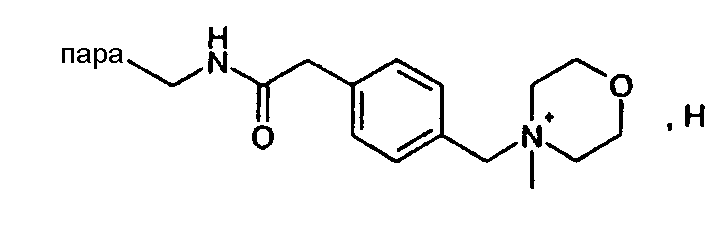
(М+)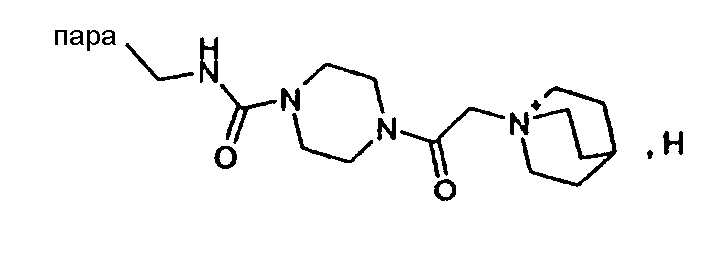
(М+)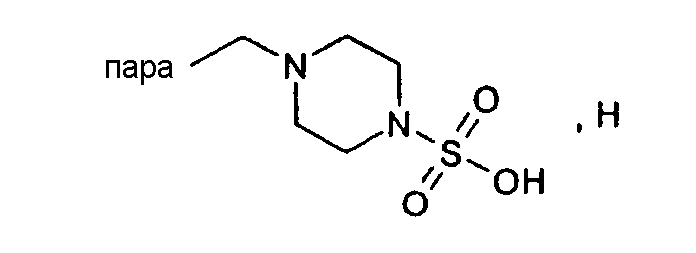
(МН+)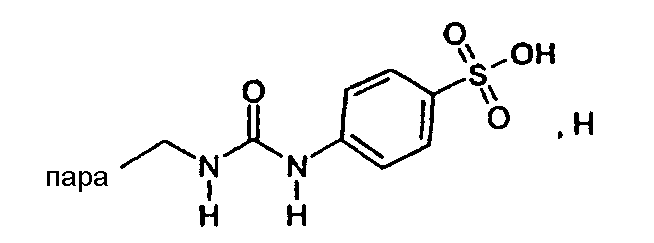
(МН+)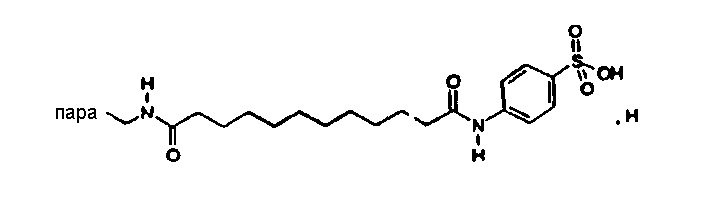
(М+-H2O)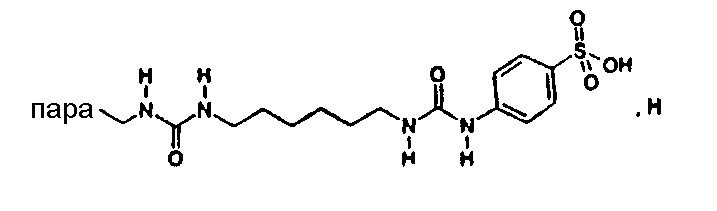
(М+-H2O)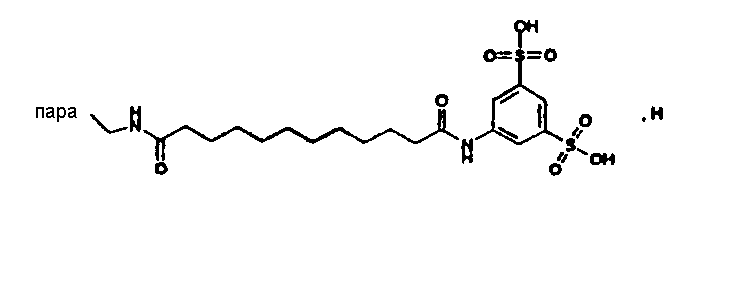
(МН+)
Предлагаемые согласно изобретению соединения формулы (I) тестировали на их активность с помощью нижеописанного метода:
Влияние на абсорбцию холестерина+выделение 3Н-таурохолевой кислоты на основании фекального выделения мыши, крысы или хомячка
Мышей (NMRI), крыс линии Wistar или золотистых сирийских хомячков (в группах с n=4-6) содержат на стандартной диете (альтромин; нанесение на губу) в респирационных камерах. Во второй половине дня перед введением радиоактивного индикатора (14С-холестерин) животных оставляют натощак и адаптируют к колосниковой решетке.
Дополнительно животных за 24 часа до перорального введения пробного завтрака (14С-холестерин в Intralipid®20, Pharmacia-Upjohn) подкожно метят с помощью 3Н-ТСА (таурохолевая кислота) (например, от 1 мКи/мышь до 5 мКи/крыса).
Тест на абсорбцию холестерина: 0,25 мл/мышь Intralipid®20 (Pharmacia-Upjohn) (потенциал действия с 0,25 мКи 14С-холестерина в 0,1 мг холестерина) вводят перорально с помощью желудочного зонда.
Тестируемые вещества вводят раздельно в 0,5% метилцеллюлоза (Sigma)/5% солутол (BASF, Людвигсхафен) или в пригодном эксципиенте.
Вводимый объем тестируемого вещества составляет 0,5 мл на мышь. Тестируемое вещество вводят непосредственно перед пробным завтраком (Intralipid с меченым 14С-холестерином) (тест на абсорбцию холестерина).
Фекалии собирают в течение 24 часов: удаление с фекалиями 14С-холестерина и 3Н-таурохолевой кислоты (ТСА) определяют спустя 24 часа.
Печени извлекают, гомогенизируют и аликвоты сжигают в Oximaten (модель 307, фирма Packard) для определения поглощенного/резорбированного количества 14С-холестерина.
Оценка
Образцы фекалиев:
Определяют общую массу, доливают водой до определенного объема, затем гомогенизируют, аликвоту высушивают и сжигают в Oximat (модель 307, фирма Packard, для сжигания радиоактивно меченых образцов): количество радиоактивных 3Н-Н2О и 14С-СО2 точно пересчитывают на выделившееся количество 3Н-таурохолевой кислоты, соответственно, 14С-холестерина (двоично-изотопный метод). Значения ED200 (доза, вызывающая 200%-ный эффект) интерполируют из кривой доза-действие как такие дозы, которые удваивают выделение ТСА или холестерина, по отношению к одновременно обработанной контрольной группе.
Образцы печени:
Поглощенное количество 14С-холестерина в печени относят к введенной дозе. Значения ED50 (доза, вызывающая 50%-ный эффект) интерполируют из кривой доза-действие как такую дозу, которая снижает наполовину (50%) поглощение 14С-холестерина печенью, по отношению к контрольной группе.
Следующие значения ED50 подтверждают активность предлагаемых согласно изобретению соединений формулы (I):
Из таблицы можно видеть, что соединения формулы (I) обладают очень хорошей активностью, снижающей уровень холестерина.
Резорбируемость:
Резорбируемость соединений формулы (I) испытывали на Сасо-клеточной модели (A.R.Hilgers и др., Caco-2 cell monolayers as a model for drug transport across the intestinal mucosa, Pharm. Res., 7, 902 (1990)).
Из данных измерения установлено, что предлагаемые согласно изобретению соединения формулы (I), по сравнению с описанными в уровне техники соединениями (сравнительная структура), обладают отчетливо более низкой резорбцией:
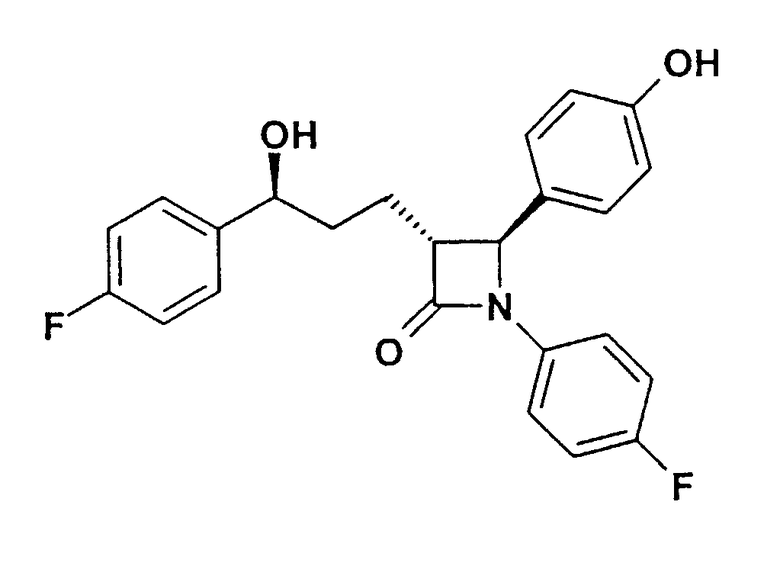
Сравнительная структура: эзетимиб
| название | год | авторы | номер документа |
|---|---|---|---|
| ЗАМЕЩЕННЫЕ КИСЛОТНЫМИ ГРУППАМИ ДИФЕНИЛАЗЕТИДИНОНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, СОДЕРЖАЩИЕ ЭТИ СОЕДИНЕНИЯ ЛЕКАРСТВЕННЫЕ СРЕДСТВА И ИХ ПРИМЕНЕНИЕ | 2003 |
|
RU2287522C2 |
| НОВЫЕ 1,2-ДИФЕНИЛАЗЕТИДИНОНЫ, ИХ ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ НАРУШЕНИЙ ЛИПИДНОГО ОБМЕНА, ЛЕКАРСТВЕННОЕ СРЕДСТВО И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2001 |
|
RU2286985C2 |
| КАТИОНОЗАМЕЩЕННЫЕ ДИФЕНИЛАЗЕТИДИНОНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ЛЕКАРСТВЕННЫЕ СРЕДСТВА, СОДЕРЖАЩИЕ ЭТИ СОЕДИНЕНИЯ, И ИХ ПРИМЕНЕНИЕ | 2003 |
|
RU2315753C2 |
| ПРОИЗВОДНЫЕ ДИФЕНИЛАЗЕТИДИНОНА, СОДЕРЖАЩИЕ ЭТИ СОЕДИНЕНИЯ ЛЕКАРСТВЕННЫЕ СРЕДСТВА И ИХ ПРИМЕНЕНИЕ | 2001 |
|
RU2275370C2 |
| ПРОИЗВОДНЫЕ ДИФЕНИЛАЗЕТИДИНОНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2001 |
|
RU2282628C2 |
| ПРОИЗВОДНЫЕ ГЛИЦИНА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ АНТАГОНИСТОВ МУСКАРИНОВЫХ РЕЦЕПТОРОВ | 2011 |
|
RU2585767C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 1,4-ДИФЕНИЛАЗЕТИДИНОНА | 2005 |
|
RU2380361C2 |
| АЛКАЛОИДНЫЙ ЭФИР И КАРБАМАТНЫЕ ПРОИЗВОДНЫЕ И ИХ МЕДИЦИНСКИЕ КОМПОЗИЦИИ | 2012 |
|
RU2611627C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ АРИЛСУЛЬФОНЫ, ПРИГОДНЫЕ ДЛЯ ЛЕЧЕНИЯ РАССТРОЙСТВ, КОТОРЫЕ ОТВЕЧАЮТ НА МОДУЛИРОВАНИЕ 5HT РЕЦЕПТОРОВ | 2007 |
|
RU2451012C2 |
| ПРОИЗВОДНЫЕ СЛОЖНОГО АМИНОЭФИРА АЛКАЛОИДА И ИХ ЛЕКАРСТВЕННЫЕ КОМПОЗИЦИИ | 2011 |
|
RU2567548C2 |
Описываются циклическизамещенные дифенилазетидиноны формулы (I), где R1, R2, R3, R4, R5, R6, независимо друг от друга, означают (C1-С30)-алкилен-(LAG)n, причем n=1-2, и причем один или два атома углерода алкиленового остатка заменены фенильными или пиперазинильными остатками или (С3-С10)-циклоалкильным остатком; и причем один или несколько атомов углерода алкиленового остатка могут быть заменены на -S(O)n-, где n=2, -О-, -(С=O)- или -NH-; H, F, Cl, Br, I, O-(С1-С6)-алкил; (LAG)n означает моно- или трициклический триалкиламмонийалкильный остаток, -(СН2)0-SO3Н, -(СН2)0-СООН, -(СН2)0-С(=NH)(NH2); а также их фармацевтически приемлемые соли. Соединения снижают уровень холестерина в сыворотке. Описывается также применение соединений для получения лекарственного средства для лечения нарушений липидного обмена. 2 н. и 5 з.п. ф-лы, 1 табл.
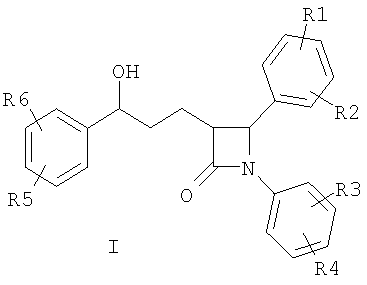
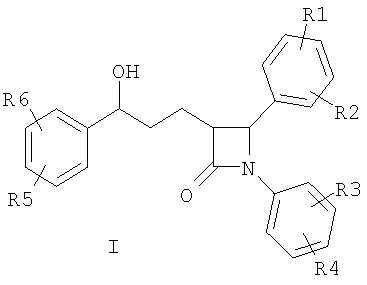
где R1, R2, R3, R4, R5, R6, независимо друг от друга, означают (C1-С30)-алкилен-(LAG)n, причем n=1-2, и причем один или два атома углерода алкиленового остатка заменены фенильными или пиперазинильными остатками или (С3-С10)-циклоалкильным остатком;
и причем один или несколько атомов углерода алкиленового остатка могут быть заменены на -S(O)n-, где n=2, -О-, -(С=O)- или -NH-;
Н, F, Cl, Br, I, O-(С1-С6)-алкил;
(LAG)n означает моно- или трициклический триалкиламмонийалкильный остаток формулы
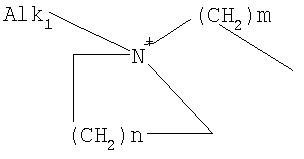
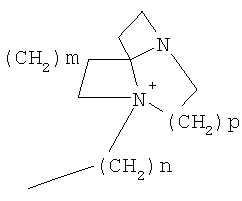
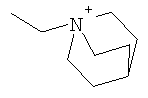
причем n, m и р, независимо друг от друга, могут означать 1-6, и одна или две группы -СН2-, независимо друг от друга, могут быть заменены на О или N-(С1-С10)-алкил, и Alk1 означает линейный или разветвленный алкильный остаток с 1-20 атомами углерода;
-(CH2)0-SO3Н, -(СН2)0-СООН, -(СН2)0-С(=NH)(NH2);
и причем всегда один из остатков R1-R6 должен означать (C1-С30)-алкилен-(LAG)n, причем n=1-2, и один или два атома углерода алкиленового остатка заменены фенильными или пиперазинильными остатками или (С3-С10)-циклоалкильным остатком и дополнительно могут быть заменены на -S(O)n-, где n=2, -О-, -(С=O)- или -NH-,
а также их фармацевтически приемлемые соли.
R2, R4, R5, R6, независимо друг от друга, означают Н, F, Cl, Br, I, O-(С1-С6)-алкил;
R1, R3, независимо друг от друга, означают (С1-С30)-алкилен-(LAG), причем один или несколько атомов углерода алкиленового остатка заменены фенильными или пиперазинильными остатками или (С3-С10)-циклоалкильным остатком и один или несколько атомов углерода алкиленового остатка могут быть заменены на -S(O)n-, где n=2, -О-, -(С=O)- или -NH-;
Н, F, Cl, Br, I, O-(С1-С6)-алкил;
(LAG) означает моно- или трициклический триалкиламмонийалкильный остаток формулы

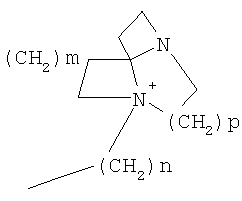

причем n, m и р, независимо друг от друга, могут означать 1-6, и одна или две группы -СН3-, независимо друг от друга, могут быть заменены на О или N-(С1-10)-алкил, и Alk1 означает линейный или разветвленный алкильный остаток с 1-20 атомами углерода;
-(CH2)0-SO3Н, -(CH2)0-СООН, -(CH2)0-C(=NH)(NH2);
и причем всегда один из остатков R1-R3 должен означать (C1-С30)-алкилен-(LAG), причем один или два атома углерода алкиленового остатка заменены фенильными или пиперазинильными остатками или (С3-С10)-циклоалкильным остатком и дополнительно могут быть заменены на -S(O)n-, где n=2, -О-, -(С=O)- или -NH-,
а также их фармацевтически приемлемые соли.
R2, R4, R5, R6, независимо друг от друга, означают Н, F, C1, Br, I, O-(С1-С6)-алкил;
R1, R3, независимо друг от друга, означают
-(СН2)-NH-(С=O)0-1-(С0-С25)-алкилен-(С=O)0-1-N(R13)0-1-(LAG), где один или два атома углерода алкиленового остатка заменены фенильными или пиперазинильными остатками или (С3-С10)-циклоалкильным остатком, и где один атом углерода алкиленового остатка может быть заменен атомом кислорода;
Н, F, Cl, Br, I, O-(С1-С6)-алкил;
(LAG)n означает моно- или трициклический триалкиламмонийалкильный остаток формулы
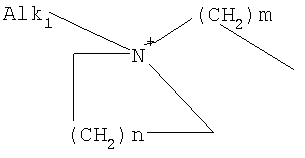

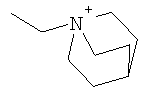
причем n, m и р, независимо друг от друга, могут означать 1-6, и одна или две группы -СН2-, независимо друг от друга, могут быть заменены на О или М-(С1-С10)-алкил, и Alk1 означает линейный или разветвленный алкильный остаток с 1-20 атомами углерода;
-(СН2)0-SO3Н, -(CH2)0-СООН, -(CH2)0-C(=NH)(NH2); n=2;
и причем всегда один из остатков R1-R3 должен означать
-(CH2)-NH-(C=0)0-1-(C0-C25)-алкилен-(C=0)0-1-N(R13)0-1-(LAG), где R13 означает водород, причем один или два атома углерода алкиленового остатка заменены фенильными или пиперазинильными остатками или (С3-С10)-циклоалкильным остатком и дополнительно могут быть заменены на -О-,
а также их фармацевтически приемлемые соли.
LAG означает моно- или трициклический триалкиламмонийалкильный остаток, определенный по пп.1-3, сульфокислоту или карбоновую кислоту,
а также их фармацевтически приемлемые соли.
| СПОСОБ ПОЛУЧЕНИЯ ТЕРМОСТОЙКИХ СОПОЛИМЕРОВ | 0 |
|
SU218432A1 |
| WO 9716455 A1, 05.05.1997 | |||
| WO 9619450 A1, 27.06.1996 | |||
| ПРОИЗВОДНЫЕ АЗЕТИДИНОНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ С ГИПОХОЛЕСТЕРИНЕМИЧЕСКОЙ АКТИВНОСТЬЮ И СПОСОБ СНИЖЕНИЯ УРОВНЯ ХОЛЕСТЕРИНА В СЫВОРОТКЕ | 1994 |
|
RU2138480C1 |
Авторы
Даты
2008-01-27—Публикация
2003-06-04—Подача