Изобретение относится к ядерной медицине и может быть использовано в лечебных учреждениях при диагностике и лечении рака щитовидной железы (РЩЖ), а также его метастазов, путем введения внутрь организма радиоактивных веществ (изотопов йода-131 и 123) с последующим измерением интенсивности их накопления.
Распространенность РЩЖ в Российской Федерации с 1995 по 2004 год увеличилась в 2 раза с 28,8 до 58,2 чел. на 100 тыс. населения. Тенденция к росту онкологической заболеваемости щитовидной железы сохраняется как следствие недостатка йода в пищевом рационе населения и загрязнения окружающей среды, в том числе и после Чернобыльской катастрофы. Рак щитовидной железы обладает выраженной способностью к метастазированию лимфогенным и гематогенным путями, поэтому 10-87% больных имеют регионарные и/или отдаленные метастазы, которые могут быть выявлены одновременно с установлением диагноза и через 25-30 лет после этого. Лечение метастазов РЩЖ основано на их способности захватывать радиоактивный йод-131. Этот химический элемент на 87% является источником β-излучения с максимальной энергией 0,6 МэВ и небольшим пробегом в биологических средах (0,5-1,5 мм). Он разрушает опухоль локально, не повреждая окружающие ткани. Захватывая радионуклид, клетки метастазов подвергаются облучению и последующей деструкции, которая зависит от величины поглощенной дозы и количества функционально активных клеток. Гамма-излучение йода-131 с энергией 364 кэВ позволяет зафиксировать распределение радионуклида в организме на гамма-камерах.
В настоящее время в большинстве клиник, где проводится радиойодтерапия, применяют комбинированное лечение, включающее удаление щитовидной железы (ЩЖ) с последующим введением лечебных активностей йода-131.
По данным Е.Е.Pochin (1971), И.М.Скоробогатова (1980), Е.С.Киселевой и соавторов (1987), способность метастазов захватывать 131-I в большинстве случаев выявляется через 4-12 недель после аблации щитовидной железы. Этот срок необходим для усиления дифференцировки клеток метастатических очагов под стимулирующим действием тиреотропина. Эффективный период полувыведения йода после удаления щитовидной железы варьирует от 3 до 12 дней, в среднем 4-6 дней.
В процессе лечения всем больным РЩЖ с регионарными и отдаленными метастазами вводятся лечебные активности радиоактивного йода-131 с последующим проведением сцинтиграфии всего тела. Курсы радиойодтерапии проводят через 3-6 месяцев в зависимости от результатов лечения (Пачес А.И., Пропп P.M., 1995). Данный ритм введения йода-131 основан на эксперементальных и клинических исследованиях, в ходе которых изучалась функция ЩЖ. При этом было отмечено, что в течение 25 дней после приема радиойода наблюдалось возбуждение функции ЩЖ с последующим ослаблением и повторным усилением йодконцентрирующей способности фолликул через 100 дней. Интервалы не менее 3 месяцев необходимы и для компенсации возможных лучевых повреждений в нормальных органах и тканях. Величина суммарной активности конкретному пациенту варьирует в зависимости от клинических, лабораторных и инструментальных данных обследования и обычно не превышает 37-74 ГБк.
Известен способ определения накопления йода-131 в метастазах РЩЖ по поглощаемости йода-131 в очагах. Способ осуществляется путем взятия биопсии метастатического очага с последующей ауторадиографией (Гельбштейн М.И., Обухов Н.В., 1963).
Недостатками способа является: а) невозможность определить концентрацию 131-I менее 2 микрокюри/г; б) наличие недоступных для биопсии метастазов; в) невозможность многократного проведения биопсии очагов.
Известен способ непосредственной радиометрии удаленных опухолевых узлов с последующим расчетом йода-131 на 1 г ткани (Seidlin S.M. et al, 1948).
Недостатком способа является возможность однократного проведения исследования.
Известен способ непосредственной регистрации счета над очагами поражения (наружняя радиометрия) in vivo с помощью радиодиагностической аппаратуры.
Недостатком способа является его трудоемкость при наличии множественных метастатических очагов и невозможность установить их точную локализацию.
Известен способ расчета радиоактивности, оставшейся в опухоли, после экскреции ее части с мочой и фекалиями (Rawson R., 1948).
Недостаток способа состоит в невозможности определения захвата йода в отдельных метастазах.
Все эти способы имеют недостатки, препятствующие широкому применению их в практике, и не подходят для длительного мониторинга больных с множественными метастазами различных локализаций.
При определении эффективности лечения отдаленных и регионарных метастазов РЩЖ применяют рентгенологические (Зедгенидзе Г.А., 1983) и ультразвуковые (А.Ф.Цыб, B.C.Паршин и соавт., 1997) способы на основе визуального определения изменения качественного состояния метастазов, их количества и размеров. При этих способах диагностируется лишь часть метастазов РЩЖ в кости, легкие и лимфатические узлы. Судить о динамике лечения рентгенонегативных и не определяемых при ультразвуковом исследовании микрометастазов не представляется возможным.
Известен сцинтиграфический способ выявления метастазов в кости и оценки эффективности их лечения при остеосцинтиграфии (Габуния Р.И. и соавтор., 1979). При этом эффект лечения определяют с помощью количественного критерия по изменению активности метаболических процессов в отдельных патологических очагах, их количества и размеров.
Недостаток способа заключается в том, что при небольших размерах метастазов в кости вне разрешающей способности применяемой радиодиагностической аппаратуры определить их наличие и оценить эффект лечения невозможно.
Известен радиоиммунологический способ определения эффекта лечения по изменению содержания тиреотропных гормонов в организме больных (Браверман Л.И., 2000). Сущность способа заключается в том, что при отсутствии прогрессирования метастатического процесса концентрация тиреоидных гормонов в плазме крови находится ниже нормы, а тиреоглобулина - в пределах нормы.
Недостаток способа заключается в том, что определить конкретные очаги поражения, где происходит прогрессирование, невозможно. Этот способ является дополнительным элементом в комплексной оценке эффективности лечения метастазов РЩЖ.
Известен способ сцинтиграфического контроля распределения йода-131 после введения лечебных активностей йода-131, предложенный Plannenstiel Р. и Hoffman G. в 1967 году, который заключается в том, что больным РЩЖ после удаления ЩЖ выполнялось исследование всего тела на первых гамма-камерах путем сцинтиграфии отдельных зон тела.
Недостатком этого способа является то, что информация о распределении йода-131 в организме больного носила неточный характер из-за отсутствия технической возможности получить целостное изображение всего тела.
Прототипом предлагаемого технического решения является способ сцинтиграфии всего тела с 131-I (Schlumberger M., Pacini F., 1999). Он заключается в том, что при поступлении в клинику больным РЩЖ проводят первичное инструментальное обследование и выполняют тиреоидэктомию. Через 2-3 недели после удаления ЩЖ с целью аблации остатков щитовидной железы и выявления метастазов с йоднакопительными свойствами per os вводят лечебные активности радиоактивного йода-131 с учетом веса, возраста и степени диссеминации метастатического процесса со средними разовыми активностями от 37 до 55,5 МБк на кг веса. Затем больного изолируют в экранированную палату до снижения мощности экспозиционной дозы излучения на расстоянии 1 м от тела до 0,08÷0,01 мкр/сек на 3-10 и более дней в зависимости от введенной активности и эффективного периода полувыведения йода. Во время нахождения в палате у пациентов на фоне физиологического накопления в проекции остатков ЩЖ, слюнных желез, ротоглотки, печени и желудочно-кишечного тракта происходит накопление йода-131 в регионарных и отдаленных метастазах. После прекращения "закрытого режима" проводят сцинтиграфию всего тела в режиме "все тело" с параллельным коллиматором для средних энергий (от 250 до 370 кэВ) и настройкой детектора гамма-камеры на фотопик 131-I (364 кэВ). В результате на сцинтиграмме получают распределение йода-131 в организме больного Информацию сохраняют в памяти компьютера и на других носителях. Затем больного отпускают на 3 месяца. При повторном поступлении пациента вновь обследуют и оценивают эффект лечения на основании данных рентгенографии легких и скелета, остеосцинтиграфии, ультразвукового исследования шеи, сцинтиграфии щитовидной железы, радиоиммунологических данных. При наличии метастазов или остатков ЩЖ ему повторно вводят радиоактивный йод-131 с активностью от 37 до 55,5 МБк на кг веса с последующей сцинтиграфией всего тела. Эффект лечения по данным сцинтиграфией всего тела с йодом-131 оценивается по изменению количества очагов патологической фиксации йода-131. Лечение радиоактивным йодом-131 проводят до полного исчезновения очагов патологической фиксации РФП. Противопоказанием для продолжения лечения радиоактивным йодом являются: тяжелое общее состояние больного с нарушением функции жизненно важных органов; появление осложнений в виде перманентной анемии, лейкопении или тромбоцитопении; прекращение захвата йода метастатическими очагами; регрессия опухоли при полном положительном эффекте лечения.
Основным недостатком способа является то, что отсутствуют количественные критерии положительной или отрицательной динамики лечения в метастазах, позволяющих судить о возрастании или убывании концентрации йода-131 в очагах поражения.
Выявленные недостатки прототипа обращают внимание на необходимость создать способ объективного наблюдения за изменением уровня накопления йода-131 в патологических очагах при сцинтиграфии всего тела с йодом.
Технический результат изобретения - повышение точности контроля эффективности лечения метастазов РЩЖ путем сравнительного анализа первичных и последующих значений количественного критерия - показателя относительного накопления (ПОН) йода, характеризующего накопление йода-131 или йода-123 в очагах поражения. Такую возможность обеспечивают путем двусторонней сцинтиграфии всего тела больного и измерения в точно локализованных очагах накопленной радиоактивности.
Сущность предлагаемого решения заключается в том, что в отличие от известного способа по прототипу для уточнения идентификации метастатических очагов (степени накопления йода-131 и локализации относительно изображения тела) после введения терапевтической активности йода-131 обязательно выполнение бидиректной сцинтиграфии всего тела (в передней (АР) и задней (РА) проекциях) с последующим определением показателя относительного накопления (ПОН) йода по соотношению:
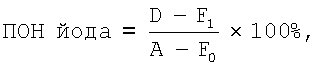
где D - число импульсов от патологического очага, F1 - число импульсов от фона тела в зоне патологического очага, А - общее число импульсов от всего тела, F0 - число импульсов от общего фона.
Для этого на сцинтиграмме всего тела выбирают прямоугольные "зоны интереса" на изображении: 1) всей сцинтиграммы (зона А); 2) фона вне тела (зона В); 3) бедра (зона С); 4) очагов патологической фиксации 131-I (зона Д), соответствующие их видимой площади. Тогда получают следующие соотношения:
F1=(С:N2)×N3,
где С - число импульсов от фона тела, N2 - число ячеек "зоны интереса" на бедре (зона С), N3 - число ячеек в области патологического очага (зона Д);
F0=(B:N1)×N0,
где В - число импульсов от фона вне тела, N1 - число ячеек от фона вне тела, N0 - общее количество ячеек от изображения всего тела (зона А).
Полученные первоначальные значения ПОН йода-131 в отдельных очагах сравнивают с последующими. После сравнительного анализа величин предыдущего и последующего ПОН йода с использованием разработанных критериев его значимого изменения определяют тактику дальнейшего лечения конкретного больного, которая заключается в снижении величины введенной активности йода-131 при высоком первоначальном ПОН йода при солитарных метастазах в кости или лимфатические узлы и множественном поражении легких при тенденции к значимому снижению ПОН йода и отсутствию прогрессирования при дополнительном инструментальном обследовании, изменении дозировки тиреоидных гормонов, продолжительности периодов между курсами радиойодтерапии и необходимости применения дистанционной лучевой терапии в лечебных и паллиативных дозах при значимом увеличении ПОН йода.
Перечень фигур
Фиг.1. Сцинтиграмма всего тела больной А. в положении АР (передней) после введения лечебной активности йода-131 с очагами патологической фиксации в проекции:
1 - ложа щитовидной железы (?)
2 - левой теменной кости
3 - грудной клетки слева
4 - передней брюшной стенки (?)
5 - проксимального конца диафиза левой бедренной кости
Фиг.2. Сцинтиграмма всего тела с йодом-131 больной А. в положении РА (задней) с очагами патологической фиксации РФП в проекции:
1 - ложа щитовидной железы (?)
2 - левой теменной кости
3 - грудной клетки слева
4 - передней брюшной стенки (?)
5 - проксимального конца диафиза левой бедренной кости
6 - 9-го грудного позвонка
7 - 12-го грудного позвонка
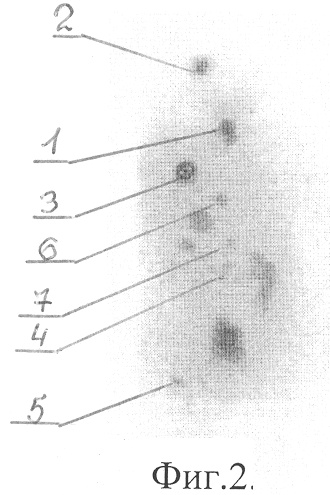
Фиг.3. Первичные сцинтиграммы всего тела с йодом-131 больного П. с физиологическим накоплением РФП в печени и очагами патологической фиксации в проекции:
1 - правой лопатки
2 - диафиза правой плечевой кости
3 - шейного отдела позвоночника
4 - грудного отдела позвоночника
5 - левого крестцово-подвздошного сочленения
6 - костей левой стопы
7 - левого голеностопного сустава
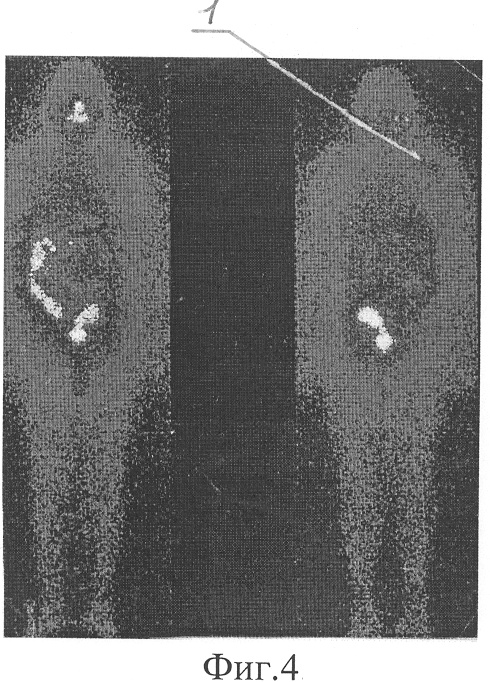
Фиг.4. Сцинтиграммы всего тела с йодом-131 больного П. через 6 месяцев с очагом патологической фиксации РФП в проекции:
1 - правой лопатки
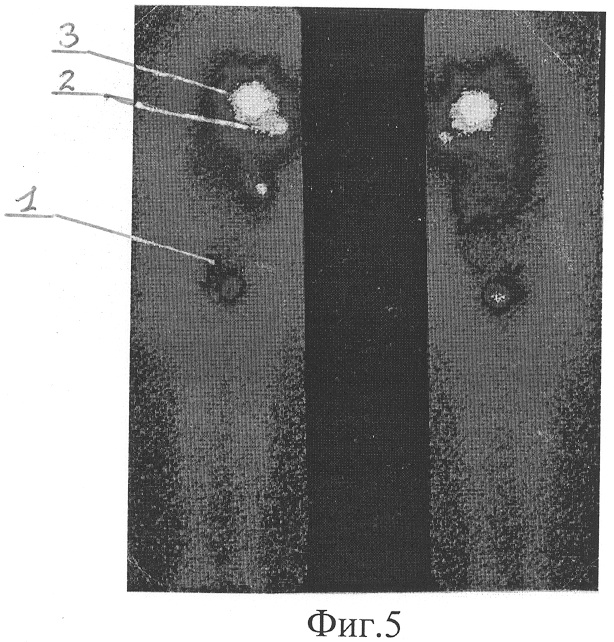
Фиг.5. Сцинтиграммы всего тела с йод ом-131 больного П. через 10 месяцев с очагами патологической фиксации РФП в проекции:
1 - левого крестцово-подвздошного сочленения
2 - диафиза правой плечевой кости
3 - правой лопатки
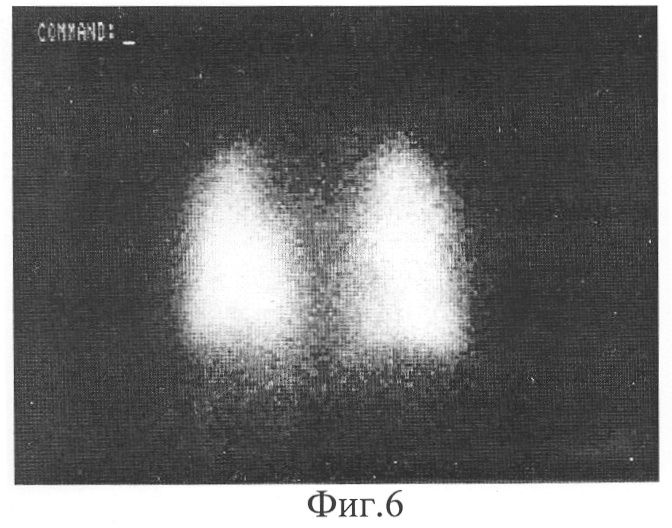
Фиг.6. Сцинтиграмма зоны легких больной Б. через 2 курса радиойодтерапии.
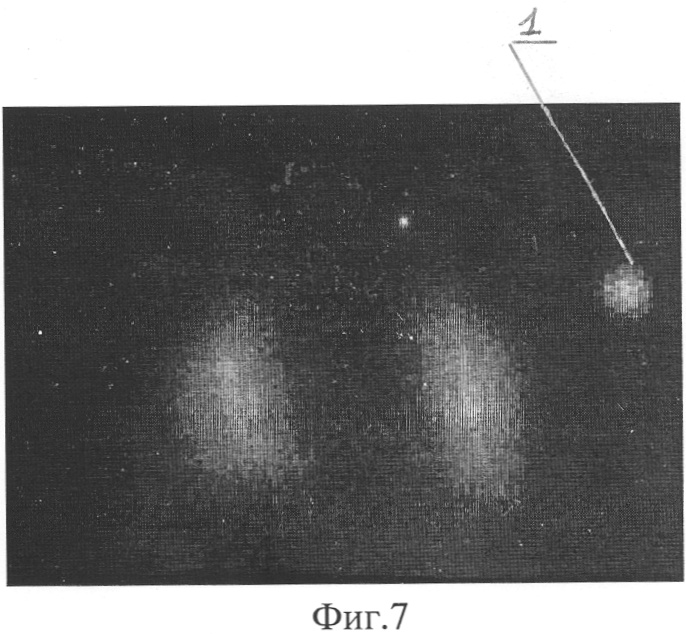
Фиг.7. Сцинтиграмма зоны легких больной Б. через 14 курсов радиойодтерапии с очагом в проекции:
1 - головки левой плечевой кости
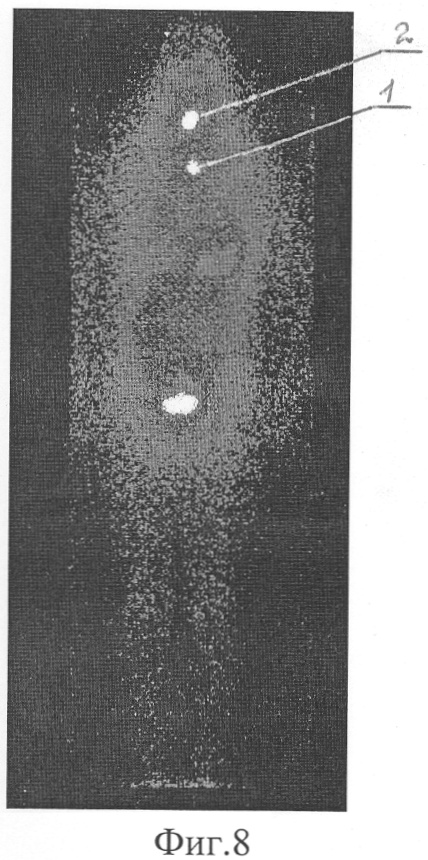
Фиг.8. Первичная сцинтиграмма всего тела с йодом-131 больного К. с очагами накопления РФП в проекции:
1 - верхнего средостения
2 - ложа щитовидной железы
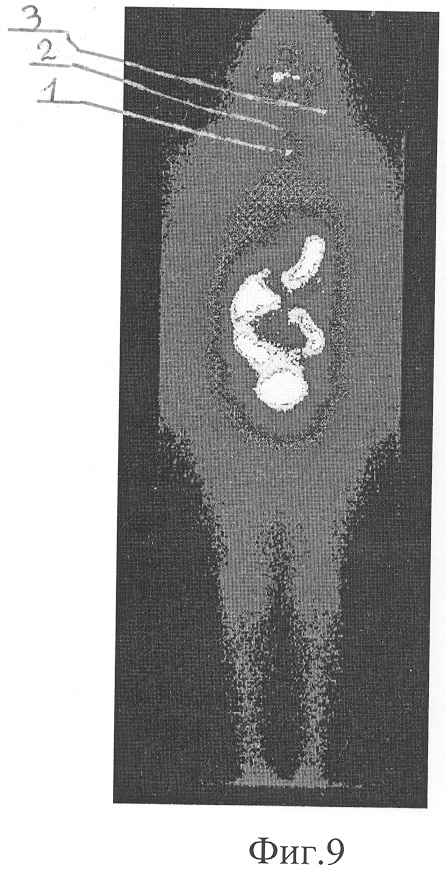
Фиг.9. Сцинтиграмма всего тела с йодом-131 больного К. с очагом в проекции:
1 - верхнего средостения
2 - яремной вырезки грудины
3 - подчелюстной области слева
Описание способа
Предлагаемое решение контроля эффективности радиойодтерапии заключается в том, что при поступлении больного РЩЖ проводят первичное клинико-инструментальное обследование с последующей тиреоидэктомией. Через 2-3 недели после удаления ЩЖ с целью аблации остатков щитовидной железы и выявления метастазов с йоднакопительными свойствами per os вводят лечебные активности радиоактивного йода-131 с учетом веса, возраста и степени диссеминации метастатического процесса со средними разовыми активностями от 37 до 55,5 МБк на кг веса. Затем больного изолируют в экранированную палату на 3 и более дней в зависимости от введенной активности и эффективного периода полувыведения йода до снижения мощности экспозиционной дозы излучения на расстоянии 1 м от тела до 0,08÷0,01 мкр/сек. Непосредственно перед исследованием больные проводят внешнюю дезактивацию, а также опорожнение мочевого пузыря и кишечника.
Затем выполняют сцинтиграфию всего тела на гамма-камере в режиме "все тело" обязательно в 2-х проекциях. Проведение сцинтиграфии всего тела больного в положении АР и РА (бидиректная сцинтиграфия) вызвано необходимостью идентификации очагов патологической фиксации йода-131, а именно установления их точного местоположения и степени накопления РФП. В качестве количественного критерия точности предложен показатель относительного накопления (ПОН) йода-131 в метастатических очагах.
Показатель относительного накопления (ПОН) йода определяют по соотношению:
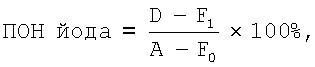
где D - число импульсов от патологического очага, F1 - число импульсов от фона тела в зоне патологического очага, А - общее число импульсов от всего тела, F0 - число импульсов от общего фона.
Величина ПОН прямо пропорциональна способности клеток метастатических очагов аккумулировать йод-131 и обратно пропорциональна накоплению его в других органах тела, но не отражает истинный процент накопленной активности. Уменьшение или увеличение ПОН в процессе лечения свидетельствует об изменении йодкумулятивной активности метастазов и позволяет судить об эффективности проводимой терапии.
На примере больной А. (фиг.1) показан порядок определения ПОН йода-131. Вначале больной А. выполнена сцинтиграфия всего тела в положении АР. На сцинтиграмме отмечены множественные очаги патологической фиксации йода-131, в том числе в проекции ложа щитовидной железы (1), грудной клетки слева (3) и передней брюшной стенки (4). Для уточнения локализации этих очагов и дифференциального диагноза по исключению поражения шейного и поясничного отделов позвоночника проведена сцинтиграфия всего тела в положении РА. На сцинтиграмме всего тела с йодом-131 в положении РА (фиг.2) помимо ранее обнаруженных очагов патологической фиксации РФП отмечают дополнительно два очага в проекции грудного отдела позвоночника (6 и 7).
На сцинтиграмме всего тела (фиг.1) выбирают прямоугольные "зоны интереса" на изображении: 1) сцинтиграммы всего тела (зона А); 2) фона вне тела (зона В); 3) бедра (зона С); 4) очагов патологической фиксации 131-I (зона Д), соответствующие их видимой площади. Тогда получают следующие соотношения:
F1=(C:N2)×N3,
где С - число импульсов от фона тела, N2 - число ячеек "зоны интереса"на бедре (зона С), N3 - число ячеек в области патологического очага (зона Д);
F0=(B:N1)×N0,
где В - число импульсов от фона вне тела, N1 - число ячеек от фона вне тела,
N0 - общее количество ячеек от изображения всего тела (зона А).
Очаг в проекции грудной клетки слева в положении АР имел ПОН йода = 1,5%, а в положении PA - 5%, то есть, он был идентифицирован как задний отрезок 6-7 ребра слева, который оказался рентгенонегативным микрометастазом. Очаг в проекции ложа щитовидной железы в положении АР имел ПОН йода = 9%, а в положении РА - 4%, то есть, являлся остатком ЩЖ. При ультразвуковом исследовании остатки ЩЖ не определялись. Очаг в проекции передней брюшной стенки в положении АР имел ПОН йода = 2%, а в положении PA = 0,7%, то есть действительно находился в области передней брюшной стенки.
При проведении сцинтиграфии всего тела с йодом-131 используют параллельный коллиматор для средних энергий. Перед исследованием аппаратуру настраивают на фотопик 131-I (364 кэВ) с шириной окна дискриминации 10-20% от фотопика. Отсечку фона задают 10-20% от общего счета. При необходимости делают дополнительные статические сцинтиграммы в прямых или боковых проекциях при наборе по счету от 100 до 500 тысяч импульсов на кадр. Используют матрицы 256×256 (для статики) и 512×512 (для "всего тела"). В режиме "все тело" общее число импульсов со всего тела колеблется от 500 тысяч до 4 миллионов. Информацию сохраняют в памяти компьютера и на других носителях. При компьютерной обработке сцинтиграмм всего тела определяют ПОН йода для каждого очага патологической фиксации.
В зависимости от результатов обследования и данных ПОН йода-131 больного отпускают по месту жительства на 3-6 месяцев. За 3-4 недели до очередного курса радиойодтерапии для эндогенной стимуляции синтеза тиреотропного гормона и увеличения степени захвата йода в функционально активных метастазах больные прекращают прием тиреоидных гормонов и исключают прием лекарств, содержащих йод, бром, литий, а также проводят диету, в продуктах которой не содержатся эти химические элементы. При этом развиваются клинические признаки гипотиреоза.
При очередном поступлении пациента вновь обследуют и оценивают эффект лечения на основании данных рентгенографии легких и скелета, остеосцинтиграфии, ультразвукового исследования шеи, сцинтиграфии щитовидной железы с Тс-99м-пертехнетатом, радиоиммунологических данных. При наличии метастазов или остатков ЩЖ ему повторно вводят радиоактивный йод-131 с активностью от 37 до 55,5 МБк на кг веса с последующей бидиректной сцинтиграфией всего тела. Супрессивную гормонотерапию возобновляют после прекращения "закрытого режима" или на 2-3 день после приема радиоактивного йода.
Эффект лечения оценивают по данным вторичного обследования и бидиректной сцинтиграфии всего тела с йодом-131 по изменению величины количественного показателя (ПОН йода) и числа очагов патологической фиксации РФП. Критерием завершенности лечения радиоактивным йодом-131 является полное исчезновение очагов патологической фиксации РФП или появление противопоказаний.
Для оценки первоначального накопления йода-131 относительно общего счета всего тела были определены диапазоны первоначальных значений ПОН йода в очагах в зависимости от вида метастазов (кости, легкие и лимфатические узлы) (таблица 1). Другая локализация метастазов встречалась крайне редко и не позволила сделать статистически достоверные выводы.
На основе распределения величин ПОН йода в разных группах метастазов объективно контролируют состояние больного в процессе радиойодтерапии и корректируют тактику лечения. Для этого разработаны градации значимого изменения относительного накопления йода в очагах в зависимости от вида метастазов и первоначальной величины ПОН йода (таблица 2).
Реализация способа
Пример 1. Пациентка П., 60 лет, история болезни №4256/88 с диагнозом: фолликулярный РЩЖ с метастазом в кости таза, pT1N0M1. При первичной сцинтиграфии всего тела после введения 3330 МБк йода-131 отмечалось накопление РФП в проекции: остатков щитовидной железы с ПОН йода = 2,5%; левого плечевого сустава, крыла правой подвздошной кости, левой половины черепа в области сосцевидного отростка с ПОН йода от 2 до 2,5%. Рентгенография легких, костей черепа, левого плечевого сустава - патологических изменений не выявила. При последующих 4 курсах радиойодтерапии с интервалом 3 месяца и разовых активностях по 3330 МБк йода-131 накопление йода отмечалось только в проекции метастаза крыла правой подвздошной кости с ПОН йода до 5%. Интервал между 4 и 5 курсом был увеличен до 6 месяцев, и ПОН йода возрос в 5 раз (до 13%), одновременно усилились боли в зоне метастаза. При рентгенографии и остеосцинтиграфии признаков прогрессирования не отмечалось. При следующем поступлении через 5 месяцев ПОН йода увеличился до 19%, и тогда же зарегистрирована отрицательная динамика со стороны очага деструкции (увеличение размеров до 8 см). С лечебной целью применен курс дистанционной лучевой терапии с СОД=46 Гр. После этого ПОН йода в метастазе снизился до значений менее 1%, а через 2 года после двух курсов радиойодтерапии наступило прекращение его накопительной активности.
Таким образом, увеличение интервала между курсами радиойодтерапии в первые 2 года лечения привело к прогрессированию метастатического процесса. Несмотря на одинаково высокие разовые активности йода-131, потребовалось дополнительное лучевое воздействие на метастаз.
Пример 2. Пациент П., 55 лет, история болезни №695/93 с диагнозом: папиллярный РЩЖ с метастазами в кости, pT4N0M1. При остеосцинтиграфии найдены множественные очаги патологической гиперфиксации РФП в проекции скелета. Все они были рентгенологически верифицированы. При первичной сцинтиграфии всего тела после введения 3700 МБк йода-131 (фиг.3) обнаружено физиологическое накопление РФП в печени и очаги патологической фиксации в проекции: правой лопатки (1), правой плечевой кости (2), шейного (3) и грудного (4) отделов позвоночника костей, костей левой стопы (6) и левого голеностопного сустава (7) с ПОН йода <1%, левого крестцово-подвздошного сочленения (5) с ПОН йода = 1,1%.
При повторном поступлении через 6 месяцев при сцинтиграфии всего тела после введения 2590 МБк йода-131 отмечалось исчезновение практически всех очагов патологического накопления РФП, за исключением слабого диффузного накопления в правой лопатке (ПОН йода = 0,2%) (фиг.4). При следующем поступлении через 6 месяцев после введения 3300 МБк на сцинтиграммах отмечалось восстановление йоднакопительной функции всех очагов, кроме очага в левом крестцово-подвздошном сочленении. Интенсивность включения йода-131 в остальных очагах значимо не отличалась от первоначального ПОН йода.
При проведении 4-го курса радиотерапии через 10 месяцев при сцинтиграфии всего тела после введения 3700 МБк йода-131 (фиг.5) вновь появилось накопление РФП в левом крестцово-подвздошном сочленении (1) (ПОН йода = 1,5%) и резко возросло - в очагах диафиза правой плечевой кости (2) и правой лопатки (3) (с расширением патологической зоны) (ПОН йода увеличился до 11,5 и 13,5%, соответственно). На рентгенограммах зафиксированы множественные йоднегативные метастазы в обоих легких и признаки прогрессирования метастатического процесса в правой лопатке с почти полным разрушение костной структуры. При очередном поступлении больного отмечено дальнейшее прогрессирование метастаза в правой лопатке, где по данным сцинтиграфии всего тела после введения 2960 МБк йода-131 накопление РФП увеличилось до ПОН йода = 23,5%. Одновременно рентгенологически зафиксировано прогрессирование йоднегативных метастазов в легких и метастаза в левом крестцово-подвздошном сочленении, где вновь наступило прекращение йоднакопительной активности. Лечение было прекращено вследствие тяжелого состояния больного.
Таким образом, увеличение интервала между первыми курсами радиойодтерапии не способствовало увеличению йоднакопительной функции метастазов, и, в конечном итоге, привело к развитию менее дифференцированных форм РЩЖ, не обладающих йодкумулятивными свойствами.
Пример 3. Больная Б., 23 лет, история болезни №3644/84 с диагнозом: фолликулярный РЩЖ с метастазами в лимфатические узлы шеи, легкие, T3N1aM1. Тиреоидэктомия с операцией Крайля (удаление лимфатических узлов) была выполнена по месту жительства. При первичной сцинтиграфии всего тела после введения 2220 МБк йода-131 выявлено высокое накопление РФП в проекции обоих легких с ПОН=63% и остатках щитовидной железы с ПОН=5%. При рентгенографии отмечались множественные метастазы в обоих легких. При ультразвуковом исследовании шеи остатки щитовидной железы и лимфатические узлы не определялись. При втором поступлении через 3 месяца накопление йода-131 в легких оставалось на прежнем уровне, а в проекции ложа щитовидной железы - исчезло (фиг.6). Последующие 4 курса радиойодтерапии проводились с интервалом 3 месяца с разовой активностью 2220-2590 МБк. На рентгенограммах неполная положительная динамика со стороны метастазов в легкие была зафиксирована через 4 курса. В это время при сцинтиграфии всего тела после введения 2590 МБк ПОН йода снизился до 42%, и впервые появился очаг в проекции головки левой плечевой кости. Следующее значимое снижение накопления йода в легких наблюдалось через 4 года лечения и 14 курсов радиойодтерапии, когда ПОН йода составил 23% (фиг.7). Одновременная рентгенография легких не выявила улучшения состояния метастазов, в то время как при бидиректной сцинтиграфии идентифицировано умеренное накопление йода-131 в проекции обоих легких и в проекции рентгенонегативного микрометастаза в головке левой плечевой кости (1).
Полный положительный эффект лечения на рентгенограммах был отмечен только через следующие 5 курсов радиойодтерапии, которые проводили с разовой активностью от 1850 до 2590 МБк. Накопление йода-131 в легких оставалось на прежнем уровне, т.е. ПОН йода соответствовал 20-25%. Далее уровень включения йода-131 снизился до ПОН=6%. Рентгенологически, несмотря на сохраняющуюся фиксацию РФП в легких, констатировали отсутствие метастатического поражения. Лечение было закончено после полного исчезновения аккумуляции йода-131 в легких и головке левой плечевой кости через 8,5 лет с момента начала радиойодтерапии.
Таким образом, показанием для прекращения радиойодтерапии являлись данные бидиректной сцинтиграфии всего тела с йодом-131. Высокий первоначальный уровень накопления йода-131 в легких указывает на наличие клеток высокодифференцированного РЩЖ. Первые 2 года лечение радиоактивным йодом проходило регулярно через 3-3,5 месяца. Данные бидиректной сцинтиграфии всего тела о положительной динамике лечения при значимом снижении накопления йода-131 в легких опережали рентгенографические данные и подтверждали выбор правильной тактики лечения.
Пример.4. Пациент К., 23 лет, история болезни №1454/93 с диагнозом: папиллярный РЩЖ с метастазами в лимфатические узлы шеи, средостение, T4N1бM1. Тиреоидэктомия с операцией Крайля (удаление лимфатических узлов с двух сторон) и удалением лимфатических узлов средостения была проведена по месту жительства. Для дальнейшего лечения больной был направлен в МРНЦ РАМН. При рентгенографии обнаружено увеличение претрахеальных лимфатических узлов в средостении. При ультразвуковом исследовании шеи ткань щитовидной железы и лимфатические узлы не определялись. При первичной бидиректной сцинтиграфии всего тела после введения 3300 МБк йода-131 на фоне физиологического распределения РФП в проекции желудочно-кишечного тракта и слюнных желез идентифицирована его умеренная фиксация в проекции верхнего средостения (1) с ПОН йода = 2% и ложа щитовидной железы (2) с ПОН йода = 4% (фиг.8). Следующий курс радиойодтерапии проведен через 6 месяцев. При сцинтиграфии всего тела после введения 2590 МБк йода-131 накопление РФП в остатках щитовидной железы исчезло, а в верхнем средостении (1) значимо снизилось до ПОН йода = 0,4% (фиг.9). После исчезновения конкурентного захвата йода-131 щитовидной железой на фоне физиологического накопления РФП в проекции желудочно-кишечного тракта и слюнных желез появились новые очаги патологической фиксации йода-131 в проекции яремной вырезки грудины (2) и подчелюстной области слева (3) с ПОН менее 1%, которые не были определены при ультразвуковом исследовании. Одновременно на рентгенограммах отмечался положительный, но неполный эффект лечения претрахеальных лимфатических узлов средостения. Учитывая положительный результат лечения, следующий курс радиойодтерапии проведен через 1 год. Накопление йода-131 в проекции верхнего средостения и других очагов оставалось на прежнем уровне (ПОН менее 1%), но на рентгенограммах признаков метастатического поражения средостения уже не определялось. Следующие 2 курса радиойодтерапии проводились с периодичностью раз в 1-1,5 года с разовой активностью 2590 МБк. Накопление йода-131 в проекции средостения исчезло, но в зоне яремной вырезки грудины и подчелюстной области слева оставалось на прежнем уровне. Последние 4 курса радиойодтерапии проводились с такой же периодичностью, но с диагностической разовой активностью 370 МБк до полного исчезновения очагов в проекции шеи.
Таким образом, значимое снижение ПОН йода в лимфатических узлах средостения соответствовало положительной динамике по данным рентгенологического исследования, но снижение ПОН йода до нуля произошло на 3 года позднее рентгенологического заключения о полном положительном эффекте лечения. Длительный промежуток между курсами радиойодтерапии у данного пациента был обусловлен отсутствием отдаленных метастазов в легкие и кости.
Положительный эффект применения ПОН йода
Наличие количественного критерия позволяет повысить точность и объективность контроля эффективности радиойодтерапии на разных этапах лечения больных РЩЖ, оценить динамику изменения уровня накопления йода-131 в метастатических очагах, используя количественный критерий и градации значимого изменения его величины, идентифицировать очаги по локализации и степени йодкуммулятивной активности, снизить продолжительность лечения и экономические затраты путем изменения интервалов между курсами и величины вводимой активности в соответствии с алгоритмом применения показателя относительного накопления йода-131.
Градации значимого изменения показателя относительного накопления йода в метастатических очагах в зависимости от вида метастазов и первоначальной величины ПОН йода основаны на величине критерия значимого изменения ПОН йода (К) (таблица 2) и получены в результате клинических наблюдений.
Критерий значимого изменения ПОН йода-131 (К)
Клинически значимым при высоких значениях ПОН йода в метастазах в кости оказались его колебания в 1,5 и более раз (таблица 2); при среднем - не менее чем в 2 раза; при низком ПОН йода - при увеличении не менее чем в 2,5 раза. Практические результаты свидетельствуют, что при первоначально низком ПОН йода его значимое увеличение проявляется в диапазоне свыше 10%, а уменьшение - в диапазоне менее 1%. При очень низком первоначальном ПОН йода его значимое увеличение находится в диапазоне более 3-5%. Изменения в пределах низких или очень низких значений оказались несущественными.
Критерий значимости (К) при первоначально высоких значениях ПОН йода в метастазах в легкие составил 1,5 и более; при средних и низких - 2 и более. Клинические наблюдения показали, что при низких значениях ПОН йода значимое увеличение проявляется в диапазоне свыше 20%. При этом величина ПОН приводилась к округленным значениям, кратным 5.
Критерий значимости (К) при высоких первоначальных значениях ПОН йода в метастазах в лимфатические узлы составил 1,5 и более; при средних - 2 и более. Практические результаты показывают, что при первоначально средних значениях ПОН значимое увеличение проявляется в диапазоне более 10%, а уменьшение - в диапазоне менее 1%. При низких значениях ПОН йода значимое увеличение находится в диапазоне свыше 5%.
При мониторинге больных с йодпозитивными метастазами полученные данные ПОН сравнивались с предыдущими, а также с заключениями клинического осмотра, рентгенографии, остеосцинтиграфии, ультразвуковыми и радиоиммунологическими данными.
Снижение величины ПОН йода в метастазах в кости в соответствии с приведенными критериями в 94% случаев совпадало с положительной динамикой со стороны костных метастазов по клиническим, рентгенологическим и радиоизотопным данным, а увеличение его величины в значимом большинстве случаев (71%) было связано с прогрессированием метастатического процесса.
Вычисление χ2 - Пирсона (58,14) (при n=1) показало наличие достоверного соответствия между состоянием метастазов в кости и изменением ПОН йода в сторону повышения или понижения.
Соответствие критерию значимости при метастазах в легкие отмечалось в 100% случаев, а при метастазах в лимфатические узлы - в 98% случаев.
Алгоритм применения ПОН йода-131 у больных РЩЖ с йодпозитивными метастазами
1. Курсы радиойодтерапии необходимо проводить с интервалом не более 3-3,5 месяцев до значимого снижения первоначальной величины ПОН йода-131 с высоких до средних, со средних до низких, с низких до очень низких и очень низких до нуля.
2. При вторичном снижении ПОН йода в соответствии с критерием значимости К интервалы между курсами радиойодтерапии рекомендуют увеличить до 6 месяцев.
3. При наличии солитарных метастазов в кости и лимфатические узлы, множественного поражения легких и первоначально высоких значениях ПОН йода-131 при значимом его снижении в соответствии с предложенным критерием значимости К разовая активность йода-131 может быть снижена до 70% от первоначальной величины.
4. При множественных метастазах в кости тактику лечения определяют, ориентируясь на наименьшие значения первоначального ПОН йода-131.
5. При клинически значимом повышении ПОН йода на любом этапе радиойодтерапии даже при отсутствии рентгенологических или иных признаков отрицательной динамики необходимо увеличить дозы супрессивной гормональной терапии и дополнительно использовать дистанционную лучевую терапию в паллиативных и лечебных дозах, причем, следующий курс радиойодтерапии надо проводить после внешнего облучения.
Использование алгоритма применения ПОН йода-131 у больных РЩЖ с йодпозитивными метастазами повышает эффективность радиойодтерапии, одновременно уменьшая общее время лечения радиоактивным йодом-131 и разовые активности, тем самым снижая экономические затраты на больного.
Список литературы
1. Габуния P.И, Кузьмин В.П., Фатеева М.Н. и соавт. Применение радиоактивных нуклидов в клинических исследованиях. - М.: Атомиздат, 1979. - 263 с.
2. Гельбштейн М.И., Обухов Н.В. Авторадиогистографическое изучение поглощения радиоактивного йода опухолями щитовидной железы // Мед. радиология. - 1963. - №9. - С.34-40.
3. Киселева Е.С., Скоробогатов И.М. и соавт. Комплексное лечение метастазов рака щитовидной железы в легкие в детском и юношеском возрасте // Мед. радиология. - 1987. - №3. - С.7-14.
4. Клиническая рентгенология / Под ред. Г.А.Зедгенидзе. - М.: Медицина, 1983.
5. Болезни щитовидной железы / Под ред. Л.И.Бравермана. - М.: Медицина, 2000. - 417 с.
6. Пачес А.И., Пропп P.M. Рак щитовидной железы. - М.: Медицина, 1995. - 370 с.
7. Скоробогатов Н.М. Вопросы экспериментальной и клинической онкологии. - М.: Медицина, 1980. - 195 с.
8. Цыб А.Ф., Паршин B.C. и соавт.Ультразвуковая диагностика заболеваний щитовидной железы. - М.: Медицина, 1997. - 329 с.
9. Pfannenstiel P., Hoffman G. Szintigraphische kontrolle der radiojodtherapie bei struma maligna/In: Radioisotope in der localisations diagnostic/Hoffmann G., Scheer K.E., eds. - Stuttgart, Schattauer, Verlag, 1967. - P.471-476.
10. Pochin E.E. Radioiodine therapy of thyroid cancer//Semin. Nucl. Med. - 1971. - V.1, №3-4. - Р.503-515.
11. Rawson R.W., Marinelli L.D., Scanse B.N., Trunnell J. et al. The effect of total thyroidectomy on function of metastatic thyroid cancer // J.Clin. Endocrinol. - 1948. - №8.- Р.826-841.
12. Schlumberger М., Pacini F. Thyroid tumors. - Paris, Nucleon, 1999. - 317 р.
13. Seidlin S.M., Oshry E.Y., Aloy A.A. Spontaneos and experimentally induced uptake of radioactive iodine in metastases from thyroid carcinoma: a preliminary report // J.Clin. Endocrinol. - 1948. - №8. - P.423-432.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ СОЧЕТАННОЙ РАДИОНУКЛИДНОЙ ТЕРАПИИ ДИФФЕРЕНЦИРОВАННОГО РАКА ЩИТОВИДНОЙ ЖЕЛЕЗЫ С МЕТАСТАТИЧЕСКИМ ПОРАЖЕНИЕМ ЛЕГКИХ И СКЕЛЕТА | 2023 |
|
RU2824276C2 |
| Способ диагностики хирургических заболеваний щитовидной железы с использованием динамической двухиндикаторной сцинтиграфии | 2019 |
|
RU2726601C1 |
| СПОСОБ ОЦЕНКИ РИСКА РЕЦИДИВА ДИФФЕРЕНЦИРОВАННОГО РАКА ЩИТОВИДНОЙ ЖЕЛЕЗЫ ПОСЛЕ ПРОВЕДЕНИЯ РАДИОЙОДТЕРАПИИ | 2020 |
|
RU2743275C1 |
| Способ оценки результатов остеосцинтиграфии у пациентов с метастатическим поражением костей скелета | 2022 |
|
RU2791402C1 |
| Способ диагностики рака щитовидной железы | 1991 |
|
SU1807409A1 |
| СПОСОБ ДИАГНОСТИКИ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ ОРГАНОВ МАЛОГО ТАЗА | 2004 |
|
RU2246259C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ИНТЕНСИВНОСТИ НАКОПЛЕНИЯ РАДИОФАРМАЦЕВТИЧЕСКОГО ЛЕКАРСТВЕННОГО ПРЕПАРАТА (РФЛП) В ОБЛАСТЯХ, СООТВЕТСТВУЮЩИХ СЛЕЗООТВОДЯЩИМ ПУТЯМ, ДЛЯ ПРОГНОЗИРОВАНИЯ РИСКА ВОЗНИКНОВЕНИЯ ВТОРИЧНОЙ ОБЛИТЕРАЦИИ СЛЕЗООТВОДЯЩИХ ПУТЕЙ У ПАЦИЕНТОВ ПОСЛЕ ПРОВЕДЕНИЯ РАДИОЙОДТЕРАПИИ | 2023 |
|
RU2834165C1 |
| СПОСОБ ОБРАБОТКИ СЦИНТИГРАФИЧЕСКИХ ИЗОБРАЖЕНИЙ ГОЛОВЫ И ШЕИ ДЛЯ ПРОГНОЗИРОВАНИЯ РИСКА ВОЗНИКНОВЕНИЯ ВТОРИЧНОЙ ОБЛИТЕРАЦИИ СЛЕЗООТВОДЯЩИХ ПУТЕЙ У ПАЦИЕНТОВ ПОСЛЕ ПРОВЕДЕНИЯ РАДИОЙОДТЕРАПИИ | 2022 |
|
RU2809914C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА ВОЗНИКНОВЕНИЯ ВТОРИЧНОЙ ОБЛИТЕРАЦИИ СЛЕЗООТВОДЯЩИХ ПУТЕЙ У ПАЦИЕНТОВ ПОСЛЕ ПРОВЕДЕНИЯ РАДИОЙОДТЕРАПИИ | 2023 |
|
RU2833127C1 |
| СПОСОБ ДООПЕРАЦИОННОГО ОПРЕДЕЛЕНИЯ ОБЪЕМА ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ВЫСОКОДИФФЕРЕНЦИРОВАННОГО РАКА ЩИТОВИДНОЙ ЖЕЛЕЗЫ | 2014 |
|
RU2548783C1 |

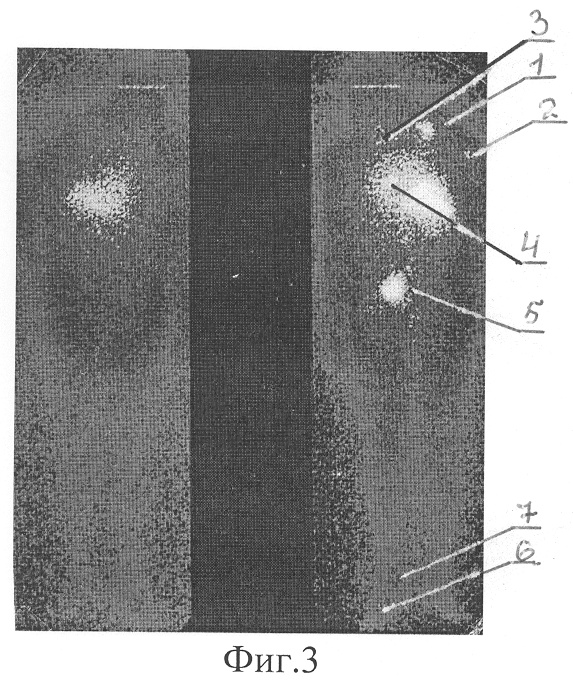
Изобретение относится к области медицины, в частности к радиологии и онкологии. Способ обеспечивает повышение точности контроля эффективности радиойодтерапии метастазов рака щитовидной железы. После дезактивации больным с остаточной лечебной активностью йода-131 выполняют бидиректную сцинтиграфию всего тела для идентификации регионарных и отдаленных метастазов и определяют первичный показатель относительного накопления (ПОН) йода-131 для каждого из метастатических очагов по соотношению:
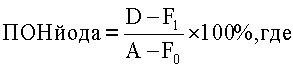
D - число импульсов от патологического очага, F1 - число импульсов от фона тела в зоне патологического очага, А - общее число импульсов от всего тела, F0 - число импульсов от общего фона. За 3-4 недели до очередного курса радиойодтерапии во время рекреационного периода больные проводят антитиреоидную диету и прекращают прием тиреоидных гормонов. При повторном поступлении им вводят лечебную активность йода-131 и выполняют бидиректную сцинтиграфию всего тела с определением показателя относительного накопления (ПОН) йода и критерия значимости (К) для каждого из метастатических очагов. По величине критерия значимости (К) производят коррекцию дальнейшего лечения. 6 з.п. ф-лы, 9 ил., 2 табл.
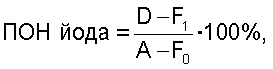
где D - число импульсов от патологического очага, F1 - число импульсов от фона тела в зоне патологического очага, А - общее число импульсов от всего тела, F0 -число импульсов от общего фона, затем при очередном поступлении больного при наличие метастазов или остатков щитовидной железы вновь вводят радиоактивный йод-131 с последующим проведением сцинтиграфии всего тела в передней и задней проекциях, а контроль за эффективностью лечения осуществляют по значимому изменению величины ПОН йода относительно первичного показателя при его высоких значениях в 1,5 и более раз, при средних и низких - в 2 и более раз.
| СПОСОБ ЛУЧЕВОЙ ДИАГНОСТИКИ МЕТАСТАЗОВ В СРЕДОСТЕНИИ | 1993 |
|
RU2109292C1 |
| ТРЕХОСНЫЙ АВТОМОБИЛЬ | 1927 |
|
SU9221A1 |
| WO 2004098652 А, 18.11.2004 | |||
| МЕДВЕДСКИЙ В.Е | |||
| и др | |||
| Радионуклидная диагностика в онкологии | |||
| Новости лучевой диагностики, 1999, №1, с.32-34 | |||
| LIN J.D | |||
| et al | |||
| The effects of radioactive iodine in thyroid remnant ablation and treatment of well differentiated thyroid carcinoma | |||
| Br J Radiol | |||
| Способ и аппарат для получения гидразобензола или его гомологов | 1922 |
|
SU1998A1 |
Авторы
Даты
2008-02-20—Публикация
2006-06-15—Подача