Изобретение относится к медицине, к хирургии, к онкологии и может быть использовано при дооперационном определении объема хирургического лечения высокодифференцированного рака щитовидной железы.
Прогноз для высокодифференцированного рака щитовидной железы (ВДРЩЖ) благоприятный, однако в 7-10% случаев имеет место персистенция заболевания и рецидивирование более чем через 5 лет после операции. Выделить эту группу пациентов на дооперационном этапе в настоящее время не представляется возможным, поэтому в хирургической тактике лечения остаются спорные вопросы. Одним из основных вопросов в лечении рака щитовидной железы является объем операции, т.к. это основной метод лечения. В частности, относительно необходимости выполнения профилактической центральной лимфодиссекции не существует консенсуса как в России, так и за рубежом. Следует отметить, что выполнение центральной лимфодиссекции увеличивает риск развития как транзиторного, так и стойкого гипопаратиреоза с 3% до 14.3%, увеличивается риск повреждения возвратного нерва. Также следует отметить, что по данным зарубежных авторов частота оккультных метастазов центральной клетчатки шеи колеблется от 9-20% (не определяемые на УЗИ до операции и не выявленные интраоперационно), что может стать причиной персистенции заболевания либо его рецидива. Таким образом, прогнозирование рецидива заболевания на дооперационном этапе позволит индивидуализировать тактику хирургического лечения.
В последние годы в ряде работ зарубежных авторов появились данные о наличии возможной связи между мутацией гена BRAF и менее благоприятным прогнозом течения ВДРЩЖ. Проведенное 15-летнее ретроспективное мультицентричное исследование показало, что наличие BRAF мутации достоверно коррелировало с более высоким риском рецидива, метастазирования и снижением способности к захвату радиойода. BRAF мутация является перспективным дооперационным маркером, который отражает распространенность заболевания.
В работе проф. Никифорова и соавт. (Gina M. Howell, Marina N. Nikiforova, Sally E. Carty, Michaele J. Armstrong, Steven P. Hodak, Michael T. Stang, Kelly L. McCoy, Yuri E. Nikiforov, Linwah Yip. BRAF V600E Mutation Independently Predicts Central Compartment Lymph Node Metastasis in Patients with Papillary Thyroid Cancer. Annals of Surgical Oncology January 2013, volume 20, Issue 1, pp 47-52) продемонстрирована возможность использовать BRAF мутацию в качестве маркера высокого риска развития локорегионарных рецидивов и предложено при выявлении BRAF положительной опухоли выполнять центральную лимфодиссекцию.
Однако известный способ не позволяет определить объем хирургического вмешательства при папиллярном раке щитовидной железы в случае BRAF отрицательной опухоли, хотя при таких опухолях известны рецидивы как местные, так и отдаленные. Кроме того, способ не позволяет корректировать хирургическую тактику у пациентов с диагнозом фолликулярного рака, так как BRAF мутация встречается только при папиллярном раке.
Технический результат, достигаемый изобретением, заключается в разработке достоверного маркера дооперационного определения объема хирургического лечения высокодифференцированных раков щитовидной железы - папиллярного и фолликулярного.
Заявленный технический результат достигается в способе дооперационного определения объема хирургического лечения высокодифференцированного рака щитовидной железы, включающем исследование материала тонкоигольной аспирационной биопсии опухоли, в котором определяют экспрессию натрий-йодного симпортера на мембране опухолевой клетки и при экспрессии менее 1% в объем операции дополнительно включают центральную лимфодиссекцию.
Целесообразно экспрессию натрий-йодного симпортера на мембране опухолевой клетки определять методом проточной флуороцитометрии.
При разработке способа авторы основывались на том, что восприимчивость ВДРЩЖ к лечению радиоактивным йодом I 131 зависит от количества специфического переносчика на поверхности опухолевой клетки - натрий-йодного симпортера (НИС). При его снижении или отсутствии эффективность радиойодтерапии (РИТ) снижается, что может привести к рецидиву заболевания.
В результате исследования уровня экспрессии НИС на гистологическом ретроспективном материале от 65 пациентов с ВДРЩЖ методом иммуногистохимии (ИГХ) авторами были выявлены особенности перераспределения НИС внутри опухолевой клетки. При оценке препаратов выявлено преимущественное накопление белка в цитоплазме или на ядерной мембране опухолевой клетки. Уровень экспрессии, выявленный в исследовании, не был снижен, однако нарушено встраивание НИС в клеточную мембрану, что, по всей вероятности, происходит вследствие посттрансляционных нарушений. Данное изменение ведет к значительному уменьшению функциональной активности белка ввиду невозможности выполнения транспорта йода внутрь клетки. Но необходимо отметить, что наряду с опухолевыми клетками, проявившими максимальное накопление белка во внутренних компартментах, имеются клетки с мембранной экспрессией НИС.
Таким образом, было установлено, что количественную оценку следует проводить именно по экспрессии НИС на мембране клетки.
Дополнительного был изучен характер экспрессии и распределения НИС при неопухолевых заболеваниях щитовидной железы (диффузный токсический зоб), в нормальной ткани щитовидной железы и при доброкачественных опухолях щитовидной железы. Уровень экспрессии НИС в нормальной ткани щитовидной железы составляет 30-60% всех клеток. При доброкачественных опухолях щитовидной железы - снижается до 20%. При изучении же уровня экспрессии НИС при папиллярном раке щитовидной железы он не превышает 10-15%.
Выполнено ретроспективное исследование уровня экспрессии НИС на мембране опухолевой клетки и определение мутации гена BRAF у 65 пациентов с папиллярным раком щитовидной железы, оперированных в период с 2002 по 2008 г. Пациенты были разделены на 3 группы: в первую вошли 20 пациентов с папиллярным раком щитовидной железы T1-2N0M0. Объем лечения этих пациентов ограничился только оперативным вмешательством и послеоперационной супрессивной терапией. Рецидив заболевания в срок наблюдения до 60 месяцев у пациентов группы диагностирован не был. Во вторую группу вошли 25 пациентов, которым было выполнено оперативное вмешательство, по результатам которого определены показания и выполнена РИТ. В дальнейшем проводилась супрессивная терапия. В этой группе рецидива заболевания в срок наблюдения до 60 месяцев не выявлено. Третью группу составили 20 пациентов, которые подверглись оперативному лечению, послеоперационной РИТ и супрессивной терапии, но в срок наблюдения до 60 месяцев у них был диагностирован рецидив заболевания. Критериями включения пациентов во вторую и третью группы также явились отсутствие патологического захвата радиофармпрепарата при сцинтиграфии I 131 после введения терапевтической дозы I 131 и не более 3% захвата от введенной дозы в ложе удаленной щитовидной железы.
В третьей группе у 17 пациентов рецидив носил локорегионарный характер, у 2 пациентов выявлены множественные метастазы в легкие, и у одной пациентки определялись повышенные уровни тиреоглобулина (ТГ) и антител к ТГ без отмены супрессивной терапии, однако топически верифицировать очаг не удалось.
Целью работы явился поиск корреляции между уровнем экспрессии НИС в первичной опухоли и риском рецидива ВДРЩЖ после выполнения РИТ. Снижение возможности захвата радиойода в метастатическом очаге считалось достоверным при возникновении рецидива заболевания после проведения РИТ по стандартной методике и отрицательной сцинтиграфии всего тела с I 131 после терапии. Помимо этого исследовалась корреляция между снижением уровня экспрессии НИС и наличием BRAF мутации.
Уровень экспрессии НИС оценивали иммуногистохимически с использованием моноклональных антител AbCam, BRAF мутацию выявляли коммерческими наборами Vienn Lab. Следует отметить, что уровень экспрессии НИС оценивали по количеству белка транспортера, встроенного в мембрану опухолевой клетки, т.к. именно он является биологически активным.
При изучении корреляции уровня экспрессии НИС в первичной опухоли и риском рецидива заболевания получены следующие данные: в первой группе пациентов уровень экспрессии НИС был максимальным и доходил до 16%, средний же уровень экспрессии составил 6.7%.
Во второй группе больных средний уровень экспрессии НИС первичной опухоли составил 2.8%.
Наибольший интерес представляет третья группа больных. При оценке уровня экспрессии НИС первичной опухоли выявлено значительное снижение уровня экспрессии НИС в первичной опухоли в среднем до 1% по данным ИГХ.
Таким образом, удалось доказать корреляцию между уровнем экспрессии натрий йодного симпортера и риском рецидива заболевания после радиойодтерапии.
Достоверной корреляции между наличием BRAF мутации и уровнем экспрессии НИС не получено, что возможно связано с другими генетическими механизмами, влияющими на экспрессию белка-транспортера.
Определение уровня экспрессии НИС на дооперационном этапе должно выполняться с помощью метода, позволяющего количественно определить наличие НИС на мембране опухолевой клетки. В связи с чем авторами была разработана, протестирована и запущена в работу методика определения НИС методом проточной флюороцитометрии (данный метод исследования экспрессии НИС применен впервые).
Таким образом, при снижении экспрессии НИС менее 1% в материале ТАБ опухоли щитовидной железы предлагается выполнять не только тиреоидэктомию, но и профилактическую центральную лимфодиссекцию, что позволит уменьшить риск рецидива заболевания и необходимость повторных операций.
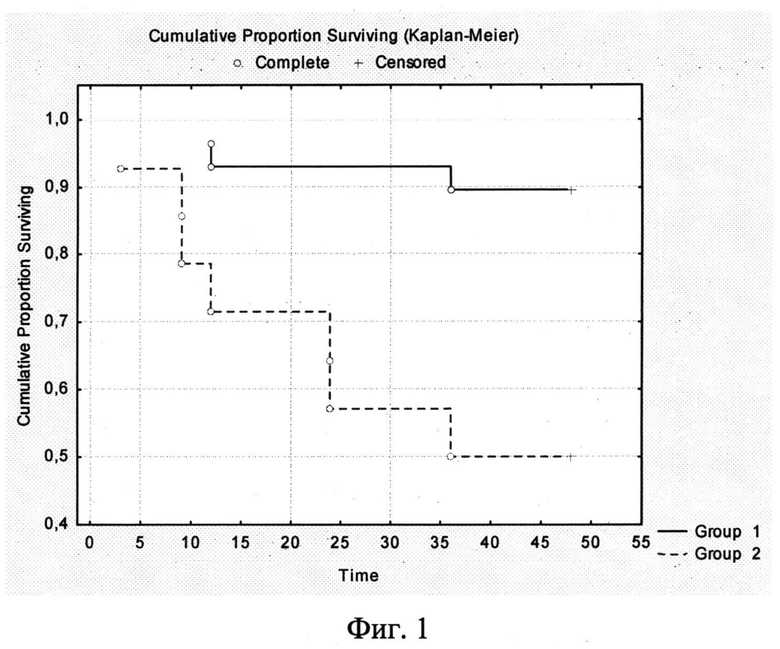
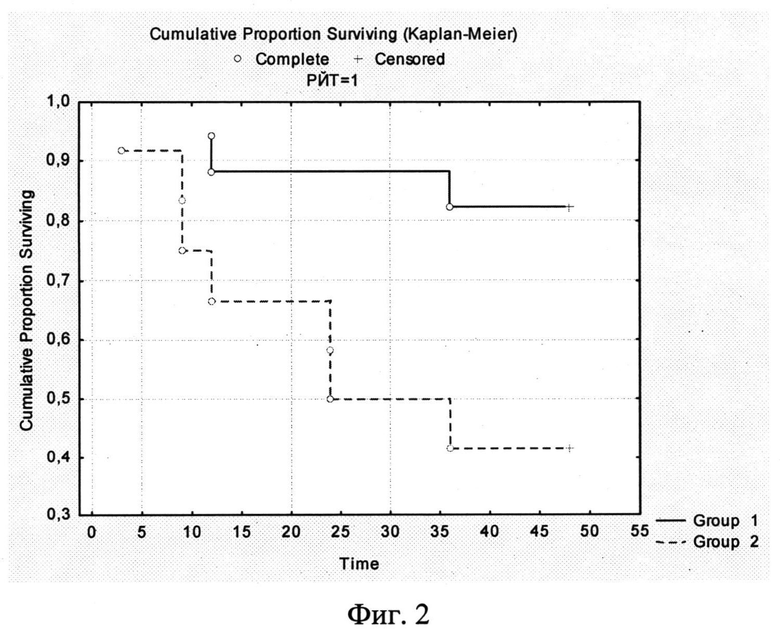
На фигурах представлены кривые безрецидивной выживаемости: на Фиг.1 - всех пациентов, в зависимости от уровня экспрессии натрий-йодного симпортера; на Фиг.2 - пациентов, получивших радиойодтерапию, в зависимости от уровня экспрессии натрий-йодного симпортера. На фигурах обозначено: Group 1 - группа пациентов, имеющих уровень экспрессии НИС≥1%; Group 2 - группа пациентов, имеющих уровень экспрессии НИС≤1%; Time - время до рецидива, измеренное в месяцах; Cumulative proportional surviving - кумулятивная выживаемость.
Способ осуществляют, например, следующим образом.
На дооперационном этапе пациенту выполняют тонкоигольную аспирационную биопсию (ТАБ) щитовидной железы и в материале ТАБ определяют экспрессию НИС методом проточной флуороцитометрии, который включает следующие этапы.
I. Подготовка проб.
1. Материал ТАБ обрабатывают неконъюгированными козьими поликлональными антителами к экстраклеточному (Р-14) домену белка НИС человека (Santa Cruz Biotechnology, Inc.).
2. Инкубация при температуре +4° 12 часов.
3. Отмывка: добавление в образцы 4 мл фосфатно-солевого буфера (Santa Cruz Biotechnology, Inc.); центрифугирование в режиме 1600 об/мин, 10 мин, при комнатной температуре; удаление надосадочной жидкости.
4. Обработка образцов антикозьими антителами осла конъюгированными FITC (Santa Cruz Biotechnology, Inc.).
5. Инкубация при температуре +4° 50 мин.
6. Отмывка: добавление в образцы 4 мл фосфатно-солевого буфера (Santa Cruz Biotechnology, Inc.); центрифугирование в режиме 1600 об/мин, 10 мин, при комнатной температуре; удаление надосадочной жидкости.
7. Обработка образцов мышиными моноклональными антителами конъюгированными РЕ к CD45 человека (10 test, Beckman Coulter).
8. Инкубация при комнатной температуре 15 мин.
II. Анализ проб.
Анализ проб проводят методом проточной флюороцитометрии на проточном цитометре EPICS XL-MCL (Beckman Coulter) с помощью программы System II.
Экспрессию НИС определяют в области CD45 негативных событий в созданной для исследования панели протоколов. Контроль экспрессии НИС осуществляют по протоколу без первичных антител.
При экспрессии НИС менее 1% в объем операции дополнительно включают центральную лимфодиссекцию.
Способ иллюстрируется следующими клиническими примерами.
1. Пациентка К., 40 лет, обратилась в клинику общей хирургии в связи с впервые выявленным узлом правой доли щитовидной железы. При УЗИ узел гипоэхогенный, в нижнем полюсе правой доли 1.3 см с нечетким неровным контуром и множеством кальцификатов. Выполнена тонкоигольная аспирационная биопсия узла правой доли. При цитологическом исследовании материала ТАБ выявлены клетки папиллярного рака. До операции выполнено определение в материале ТАБ наличия мутации гена BRAF и уровня экспрессии НИС на мембране опухолевой клетки. BRAF мутации не выявлено, уровень экспрессии НИС был значительно снижен -0.3%. До операции больная обследована. Выполнены клинико-лабораторный минимум, гормональное обследование, УЗИ щитовидной железы и регионарных лимфатических узлов, УЗИ органов брюшной полости, рентгенограмма органов грудной клетки. Данных за локорегионарное и отдаленное метастазирование не получено. 13.12.2010 г. выполнена операция. На операции: в нижнем полюсе правой доли выявлен каменистой плотности узел 1.3 см, без макроскопических признаков инвазии капсулы щитовидной железы. Выполнена тиреоидэктомия. Послеоперационное клиническое стадирование сТ1 Nx МО. При плановом гистологическом исследовании выявлены признаки инвазии капсулы щитовидной железы. Гистологическое стадирование заболевания рТ3 Nx МО. Поставлены показания к выполнению радиойодтерапии. 03.2011 г. больной выполнена РИТ (за пределами РФ), после чего назначена супрессивная гормональная терапия. При плановом осмотре в 09.2011 г. выявлены увеличенные до 2.5 см гипоэхогенные округлые среднерегулярные лимфатические узлы справа. Заподозрен рецидив заболевания. Выполнена ТАБ: метастаз папиллярного рака щитовидной железы. Поставлены показания к выполнению боковой и центральной шейной лимфодиссекции справа. 10.2011 г. больная повторно оперирована. При гистологическом исследовании материала в центральной и боковой клетчатке шеи справа выявлены метастатически пораженные лимфатические узлы. Больной вновь назначена РИТ и супрессивная гормональная терапия. В срок до 36 месяцев рецидива заболевания не зарегистрировано.
Проведенное на дооперационном этапе исследование НИС, показавшее значительное снижение уровня экспрессии НИС до 0.3%, указывало на агрессивное течение ВДРЩЖ при отсутствии BRAF мутации, развитие рецидива заболевания после РИТ и необходимость включения в объем операции центральной лимфодиссекции, что было подтверждено дальнейшим клиническим течением.
2. Больная Г.С., 70 лет, поступила в клинику в плановом порядке с диагнозом фолликулярная опухоль правой доли щитовидной железы. Из анамнеза известно, что при профилактическом осмотре выявлен узел в правой доле щитовидной железы. УЗИ - в правой доле гипоэхогенное образование 2,0×3,0 см с нечетким, ровным контуром с кальцификатами. TAB - фолликулярная опухоль. Выполнена экстирпация щитовидной железы. Центральная лимфодиссекция не выполнялась. При плановом гистологическом исследовании - фолликулярный рак. Через 6 месяцев после операции диагностированы метастазы в центральную и боковую клетчатку шеи справа. Выполнена центральная и боковая шейная лимфодиссекция справа. Проведен курс радиойодаблации. Через год выявлен рецидив заболевания - метастазы в боковую клетчатку слева. Выполнена боковая шейная лимфодиссекия слева, проведено 3 курса С. Через 7 лет после первой операции диагностирован повторный рецидив - метастазы фолликулярного низкодифференцированного рака в медиастинальные лимфоузлы, однако при выполнении сцинтиграфии с йодом очагов патологической фиксации не определялось. Выполнена видеоассистированная медиастинальная лимфодиссекия. При ретроспективном анализе биопсийного материала выявлена низкая экспрессия НИС (менее 1%). Мутация BRAF не исследовалась в связи с диагнозом фолликулярного рака, так как данная мутация встречается только при папиллярном раке. Таким образом, низкая экспрессия НИС позволяет прогнозировать нечувствительность к радиойодтерапии, что диктует расширение объема операции, а именно выполнение лимфодисекции.
На проспективном этапе исследования в период с 2009 г. по 2010 г. авторами было проведено лечение 43 пациентов с высокодифференцированным раком щитовидной железы. У всех пациентов до операции были исследованы уровень экспрессии НИС и наличие мутации BRAF V600E в материале ТАБ. Уровень экспрессии НИС оценивали количественно методом проточной флуороцитометрии, а также был выполнен молекулярно-генетический анализ материала ТАБ методом ПЦР-анализа с целью определения BRAF статуса опухоли (амплификации в режиме реального времени и амплификации в режиме учета электрофоретического сигнала). Средний возраст пациентов составил 47.4±13.9 лет; соотношение мужчин и женщин - 1:7 соответственно.
Всего в исследование вошло 39 пациентов с папиллярным раком щитовидной железы (ПРЩЖ) и 4 пациента с фолликулярным раком (ФРЩЖ).
Среди пациентов с ПРЩЖ 22 были BRAF положительные и 17 BRAF отрицательные. Уровень экспрессии БИС менее 1% был у 12 пациентов, у 27 - более 1%. Среди пациентов у 6 выявлен рецидив заболевания после проведения РИТ. BRAF положительных среди них было 4 человека, и у 2 пациентов опухоль была BRAF отрицательной. Следует отметить, что у всех 6 человек уровень экспрессии НИС не превышал 1%.
Среди пациентов с ФРЩЖ все пациенты были BRAF отрицательные, но уровень экспрессии НИС был снижен менее 1%, лишь у 1 пациента, у которого был выявлен рецидив заболевания в срок 36 месяцев. У оставшихся 3 человек уровень экспрессии НИС не превышал 1%.
При построении кривых дожития Каплан-Мейера (Фиг.1 и Фиг.2) достоверно видно, что период безрицидивного выживания пациентов с уровнем экспрессии НИС менее 1% достоверно ниже.
Анализ влияния уровня экспрессии НИС на безрецидивную выживаемость (Фиг.1) показал, что в группе больных с уровнем экспрессии НИС более 1% рецидив заболевания развился лишь в 10% случаев, тогда как в группе больных с уровнем экспрессии НИС менее 1% частота рецидивов достигла 50% (=0.00392). Следует отметить, что все пациенты с рецидивами заболевания прошли терапию радиоактивным йодом. Таким образом, получается, что в каждом втором случае при уровне экспрессии менее 1% в первичной опухоли в срок до 48 месяцев мы можем ожидать рецидива/прогрессирования заболевания после выполнения РИТ.
Интересными являются результаты анализа безрецидивной выживаемости в группе пациентов, получивших в послеоперационном периоде по показаниям радиойодтерапию (Фиг.2). При составлении кривых безрицидивной выживаемости в двух группах больных - с уровнем экспрессии НИС менее и более 1% - результаты аналогичны результатам у всех пациентов (Фиг.1). Т.е. у пациентов с уровнем экспрессии НИС первичной опухоли менее 1%, срок безрецидивной выживаемости после радиойодтерапии значительно ниже, в сравнении с пациентами, также получившими РИТ, но чей уровень экспрессии НИС был более 1%.
Таким образом, рецидив в группе больных после радиойодтерапии и уровнем экспрессии НИС менее 1% связан с нечувствительностью опухоли к радиоактивному йоду и неадекватным первичным объемом операции. При выполнении адекватного первичного объема операции данных рецидивов возможно было избежать.
Использование заявленного способа позволяет на основе дооперационного определения экспрессии натрий-йодного симпортера на мембране опухолевой клетки установить объем хирургического лечения высокодифференцированных раков щитовидной железы - папиллярного и фолликулярного.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ дооперационного определения объема хирургического лечения высокодифференцированного рака щитовидной железы | 2018 |
|
RU2709140C1 |
| Способ дифференциальной диагностики новообразований щитовидной железы | 2019 |
|
RU2705110C1 |
| Способ комплексной дооперационной дифференциальной диагностики доброкачественных и злокачественных узловых образований щитовидной железы | 2022 |
|
RU2805941C1 |
| Способ прогнозирования рецидива рака щитовидной железы после радикального хирургического вмешательства | 2024 |
|
RU2823255C1 |
| Способ дифференциальной диагностики узловых образований щитовидной железы человека | 2021 |
|
RU2757347C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЛЕЧЕБНОЙ ТАКТИКИ ПРИ ДИФФЕРЕНЦИРОВАННОМ РЩЖ В СОЧЕТАНИИ С АУТОИММУННЫМ ТИРЕОИДИТОМ С УЗЛООБРАЗОВАНИЕМ | 2013 |
|
RU2522388C1 |
| Способ выбора тактики лечения узловых образований щитовидной железы | 2023 |
|
RU2823767C1 |
| Способ определения риска развития папиллярного рака щитовидной железы | 2023 |
|
RU2807880C1 |
| Способ хирургического лечения рака щитовидной железы при тиреотоксикозе | 2020 |
|
RU2751971C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ НОВООБРАЗОВАНИЙ ЩИТОВИДНОЙ ЖЕЛЕЗЫ ЧЕЛОВЕКА | 2014 |
|
RU2569154C1 |
Изобретение относится к медицине, к хирургии, к онкологии и может быть использовано при дооперационном определении объема хирургического лечения высокодифференцированного рака щитовидной железы. Сущность способа: в материале опухоли, взятом тонкоигольной аспирационной биопсией, определяют экспрессию натрий-йодного симпортера на мембране опухолевой клетки и при экспрессии менее 1% в объем операции дополнительно включают центральную лимфодиссекцию. Экспрессию натрий-йодного симпортера на мембране опухолевой клетки определяю методом проточной флуороцитометрии. Способ позволяет на основе дооперационного определения экспрессии натрий-йодного симпортера на мембране опухолевой клетки достоверно установить объем хирургического лечения высокодифференцированных раков щитовидной железы - папиллярного и фолликулярного. 1 з.п. ф-лы, 2 ил., 2 пр.
1. Способ дооперационного определения объема хирургического лечения высокодифференцированного рака щитовидной железы, включающий исследование материала тонкоигольной аспирационной биопсии опухоли, отличающийся тем, что определяют экспрессию натрий-йодного симпортера на мембране опухолевой клетки и при ее значении менее 1% в объем операции дополнительно включают центральную лимфодиссекцию.
2. Способ по п. 1, отличающийся тем, что экспрессию натрий-йодного симпортера на мембране опухолевой клетки определяют методом проточной флуороцитометрии.
| БЕРШТЕЙН Л.М | |||
| Рак щитовидной железы: эпидемиология, эндокринология, факторы и механизмы канцерогенеза | |||
| Практическая онкология | |||
| Т | |||
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| UA 60699 U (ГОСУДАРСТВЕННОЕ УЧРЕЖДЕНИЕ "ИНСТИТУТ ЭНДОКРИНОЛОГИИ И ОБМЕНА ВЕЩЕСТВ ИМ | |||
| В | |||
| П | |||
| Видоизменение пишущей машины для тюркско-арабского шрифта | 1923 |
|
SU25A1 |
| MELLER J, BECKER W | |||
| The continuing importance of thyroid | |||
Авторы
Даты
2015-04-20—Публикация
2014-05-29—Подача