Настоящее изобретение относится к фармацевтическим композициям, более предпочтительно к пероральным фармацевтическим композициям, содержащим 4-(3'-хлор-4'-фторанилино)-7-метокси-6-(3-морфолинопропокси)хиназолин или его фармацевтически приемлемую соль (далее обозначается как "Средство").
Средство описано в международной заявке на патент WO 96/33980 (пример 1) и является эффективным ингибитором семейства ферментов тирозинкиназ рецептора эпидермального фактора роста (EGFR), таких как erbBl. Средство имеет структуру формулы I
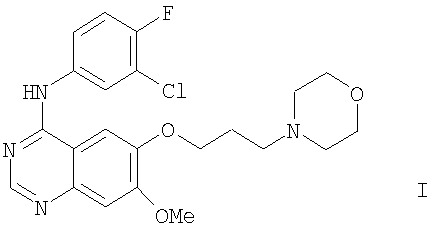
и в настоящее время известно как Иресса (зарегистрированный товарный знак), гефитиниб (принятое в США наименование), кодовый номер ZD1839 и регистрационный номер в Chemical Abstracts 184475-35-2.
Средство обладает антипролиферативным действием, таким как противораковое действие, и, следовательно, является полезным в способах лечения пролиферативных заболеваний, таких как злокачественное новообразование у человека или животного. Средство, как полагают, является полезным при лечении заболеваний или медицинских состояний, опосредованных только EGF (особенно erbB1) рецепторными тирозинкиназами или частично ими опосредованными, предпочтительно злокачественных новообразований, таких как рак легких (в частности не мелкоклеточный рак легких), молочной железы, предстательной железы, яичников, прямой кишки, желудочно-кишечного тракта, головного мозга, головы и шеи, мочевого пузыря, поджелудочной железы, пищевода, желудка, почек, кожи, женских половых органов и щитовидной железы и при лечении ряда лейкозов, злокачественных новообразований лимфоидной ткани и солидных опухолей, таких как рак и саркомы. В последнее время для средства проводятся исследования фазы III для лечения немелкоклеточного рака легких.
Средство является слабоосновным соединением и имеет 2 оснóвные группы с рКа' 5,3 и 7,2. Протонирование и депротонирование этих оснóвных групп оказывает существенное влияние на растворимость средства в водной среде. Следовательно, растворимость средства значительным образом зависит от значения рН. Например, свободноосновная форма средства растворяется при рН 1 (необходимо 10-30 мл водного растворителя для растворения 1 г средства), но практически не растворяется при значениях рН выше 7, и при значениях рН между 4 и 6 растворимость существенно снижается (необходимо ≥10000 мл водного растворителя для растворения 1 г средства при рН 6).
Соединения, растворимость которых зависит от рН, в особенности основные соединения, могут проявлять нежелательные фармакокинетические свойства, такие как сложности при их абсорбции, возможно наличие низкой или непостоянной биодоступности для пациентов и в пределах применяемых доз.
Фактором, который может оказывать влияние на абсорбцию лекарственного средства при пероральном введении, является изменение значения рН, которому подвергается лекарственное средство при его прохождение через ЖК тракт. Обычно лекарственное средство может всасываться во многих разных участках ЖК тракта после перорального введения, например, в слизистой оболочке щек, желудка, двенадцатиперстной кишки, тощей кишки, подвздошной кишки и ободочной кишки. Значение рН может отличаться в каждом участке всасывания, причем оно существенно различается на участке от желудка (рН 1-3,5) до тонкого кишечника (рН 4-8). Если растворимость лекарственного средства зависит от значения рН, то лекарственное средство может осаждаться из раствора при прохождении через ЖК тракт. Это может приводить к непостоянности степени и/или скорости всасывания в пределах применяемых доз и для разных пациентов, поскольку для всасывания лекарственное средство должно находиться в растворе.
Несмотря на то, что средство обладает хорошей растворимостью в кислой среде желудка, однако оно по существу не всасывается в этом участке. Полагают, что участок наивысшего характерного всасывания для средства находится в верхних отделах кишечника. Однако в этом участке желудочно-кишечного тракта значение рН относительно выше по сравнению с желудком и средство обладает меньшей растворимостью при повышенных значениях рН. В результате этого средство склонно к осаждению из раствора при переходе из кислой среды желудка в среду верхних отделов желудочно-кишечного тракта с повышенными значениями рН (такого, как верхний отдел кишечника), что приводит к уменьшению и/или непостоянному всасыванию средства. Кроме того, в связи с существенной чувствительностью средства к значениям рН, даже незначительные изменения местного значения рН могут оказывать значительное влияние на его фармакокинетический профиль. Значения рН желудочно-кишечного тракта также могут изменяться в результате того, например, находится ли пациент в сытом или в голодном состоянии и степени опорожнения желудка. Сочетание рН-чувствительности профиля растворимости средства совместно с различиями в значениях рН в желудочно-кишечном тракте может приводить к значительным различиям биодоступности средства для разных пациентов и/или его концентрации в плазме и возможно неоптимальной эффективности лечения для части пациентов. Таким образом, существует потребность в улучшении фармакокинетических свойств средства.
В патенте US 4344934 описана фармацевтическая композиция, содержащая смачиваемую смесь плохо растворимого в воде лекарственного среда и водорастворимого полимера, который предназначен для обеспечения улучшенной биодоступности.
В GB 2306885 описана композиция для местного введения, содержащая лекарственное средство с зависимой от рН растворимостью, где композиция становится перенасыщенной лекарственным средством при нанесении композиции на кожу в результате изменения значения рН. Композиции необязательно содержат средство против образования центров кристаллизации для ингибирования осаждения лекарственного средства из композиции.
Usui и др (Int. J.Pharmaceutics 154 (1997) 59-66) обнаружили, что определенные водорастворимые полимеры ингибируют осаждение конкретного соединения, RS-8359, из перенасыщенных водных метанольных растворов.
Loftsson и др. (Int. J. Pharmaceutics 127 (1996) 293-296) описали действие водорастворимых полимеров на растворимость лекарственных средств соединений ацетазоламида, гидрокортизона, празепама и сульфаметоксазола.
Нами неожиданно было обнаружено, что скорость, с какой средство осаждается из раствора, при повышении значения рН раствора от значения, подобному к значению рН в желудке, до обнаруженного в верхнем желудочно-кишечном тракте (таком как верхний отдел кишечника), существенно уменьшается, если средство приготовлено или вводится совместно с определенными эксципиентами. Это, как полагают, обеспечивает улучшенные фармакокинетические свойства, например, повышенную абсорбцию и/или биодоступность и может уменьшать различия в биодоступности средства для разных пациентов и/или его концентрации в плазме, так как средство остается в растворе более длительно в участке желудочно-кишечного тракта с наивысшими скоростями характерного всасывания для средства.
В соответствии с первым вариантом осуществления настоящего изобретения, обеспечивается фармацевтическая композиция, содержащая средство и простой водорастворимый эфир целлюлозы или сложный эфир простого водорастворимого эфира целлюлозы.
В соответствии с другим вариантом осуществления настоящего изобретения, обеспечивается фармацевтическая композиция, содержащая средство и простой водорастворимый эфир целлюлозы.
В соответствии с другим вариантом осуществления настоящего изобретения, обеспечивается фармацевтическая композиция, содержащая средство и сложный эфир простого водорастворимого эфира целлюлозы.
Под "простым эфиром целлюлозы" подразумевается простой эфир, образованный путем превращения одной или более гидроксильных групп, которые находятся на одном или более ангидроглюкозном повторяющемся звене полимера целлюлозы, обеспечивая одну или более эфирных связывающих групп на полимере целлюлозы. Например, подходящие эфирные связывающие группы, которые могут находится на ангидроглюкозных повторяющихся звеньях полимера целлюлозы, включают С1-С4-алкил, необязательно замещенный одним или более заместителем(ями), выбранными из гидрокси, карбокси, С1-С4-алкокси и гидроксиС1-С4-алкокси. Более предпочтительные эфирные связывающие группы включают, например, С1-С4-алкил, такой как метил или этил; гидроксиС1-С4-алкил, такой как 2-гидроксиэтил, 2-гидроксипропил или 3-гидроксипропил; С1-С4-алкоксиС1-С4-алкил, такой как 2-метоксиэтил, 3-метоксипропил, 2-метоксипропил или 2-этоксиэтил; гидроксиС1-С4-алкоксиС1-С4-алкил, такой как 2-(2-гидроксиэтокси)этил или 2-(2-гидроксипропокси)пропил; карбоксиС1-С4-алкил, такой как карбоксиметил; или группы формулы Н-[O-С1-С4-алкил-]m, где m=1-5, например 1, 2 или 3, такие как Н-[O-СН(СН3)CH2-]m или H-[O-CH2CH2-]m. Для избежания любой неопределенности, термин "эфир-связывающие группы" относится к одной или более вышеуказанных групп, связанных с полимером целлюлозы при помощи атома кислорода. Например, если эфирная связывающая группа представляет собой метил, то одна или более гидроксильных групп ангидроглюкозных повторяющихся звеньев превращены в метокси.
Простой водорастворимый эфир целлюлозы может нести одинаковые эфирные связывающие группы, например метильные группы, как в случае метилцеллюлозы. Альтернативно, простой водорастворимый эфир целлюлозы может нести много разных эфир-связывающих групп. Например, гидроксипропилметилцеллюлоза относится к целлюлозе, которая несет как метильную, так и гидроксипропильную (например, 2-гидроксипропильную) эфирные связывающие группы.
Под "водорастворимым простым эфиром целлюлозы" подразумевают простые эфиры целлюлозы, которые растворяются или диспергируются в воде, образуя коллоидный раствор или дисперсию при температуре ниже 30°С (например, от 10 до 20°С). Как правило, водорастворимые простые эфиры целлюлозы обладают растворимостью в воде по крайней мере 20 мг/мл, подходяще по крайней мере 30 мг/мл при температуре от 10 до 20°С (где растворимость определяется в незабуференной дистиллированной воде). Подходящими водорастворимыми простыми эфирами целлюлозы являются те, которые перечислены в "Справочнике фармацевтических наполнителей", 3-е издание Американского фармацевтического общества (Handbook of Pharmaceutical Excipients, 3rd Edition American Pharmaceutical Association), например метилцеллюлоза, гидроксиэтилцеллюлоза, гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза, гидроксибутилметилцеллюлоза, гидроксиэтилэтилцеллюлоза, водорастворимая соль карбоксиметилцеллюлозы (например, карбоксиметилцеллюлоза натрия) и водорастворимая соль карбоксиметилгидроксиэтилцеллюлозы (например, карбоксиметилгидроксиэтилцеллюлоза натрия). Более предпочтительно подходящий простой водорастворимый эфир целлюлозы выбран из, например, гидроксиэтилцеллюлозы, гидроксипропилцеллюлозы, гидроксипропилметилцеллюлозы и водорастворимой соли карбоксиметилцеллюлозы (например, карбоксиметилцеллюлозы натрия).
В одном варианте осуществления настоящего изобретения, простой водорастворимый эфир целлюлозы представляет собой гидроксипропилметилцеллюлозу (НРМС). Как было указано здесь выше, основная цепь целлюлозного полимера НРМС несет как метокси-, так и гидроксипропокси (предпочтительно 2-гидроксипропокси) группы. Могут применяться много классов НРМС, например, с динамической вязкостью <60 сП, такой как от 2 до 18, подходяще от 5 до 7 сП, где динамическую вязкость определяли в 2% мас./об. водном растворе НРМС при 20°С. Подходяще НРМС имеет степень замещения от 10 до 35% (подходяще от 25 до 35%) метоксильными группами и 3-30% (подходяще от 5 до 15%) гидроксипропокси группами. Если специально не указано иначе, термин "% степени замещения", который применяется в изобретении, относится к среднему значению % по весу метокси и гидроксипропокси групп, исходя из сухого веса водорастворимого простого эфира целлюлозы (например НРМС). Предпочтительные классы НРМС включают 2910, 1828, 2208 и 2906 (где первые две цифры относятся к среднему значению степени метокси замещения и вторые две цифры относятся к среднему значению степени гидроксипропокси замещения), как описано в "Справочнике фармацевтических наполнителей", 3-е издание, 2000, Американского фармацевтического общества, стр.252. Более предпочтительны вышеописанные виды НРМС с динамической вязкостью от 2 до 18 сП (например, от 5 до 7 сП). Наиболее предпочтительная НРМС представляет собой класс 2910 с динамической вязкостью от 5 до 7 сП, где динамическую вязкость определяли в 2% мас./об. водном растворе НРМС при 20°С.
Если специально не указано иначе, термин динамическая вязкость, который применяется в настоящем изобретении, относится к вязкости, измеренной при температуре, приведенной в кавычках, используя подходящее устройство, такое как вискозиметр Брукфилда, оборудованный #2 веретеном и при скорости вращения 60 об./мин.
В другом варианте осуществления настоящего изобретения простой водорастворимый эфир целлюлозы не представляет собой гидроксипропилметилцеллюлозу.
В дальнейшем варианте осуществления настоящего изобретения простой водорастворимый эфир целлюлозы выбран из гидроксиэтилцеллюлозы и гидроксипропилцеллюлозы. Если простой водорастворимый эфир целлюлозы представляет собой гидроксипропилцеллюлозу, степень замещения подходяще составляет более чем 16%, например от 20 до 40%. Подходяще гидроксипропилцеллюлоза имеет динамическую вязкость от 100 до 600 сП (например, от 150 до 450 сП), где вязкость определяли в 2% мас./об. водном растворе гидроксипропилцеллюлозы при 25°С. Альтернативно, гидроксипропилцеллюлоза может иметь степень замещения приблизительно от 5 до приблизительно 16% гидроксипропокси групп. Такие гидроксипропилцеллюлозы коммерчески доступны как "низкозамещенная" гидроксипропилцеллюлоза. Несмотря на то, что низкозамещенная гидроксипропилцеллюлоза часто описана как нерастворимая в воде, нами неожиданно было обнаружено, что низкозамещенная гидроксипропилцеллюлоза является достаточно гидрофильной для предотвращения осаждения средства из раствора, и для целей настоящего изобретения низкозамещенная гидроксипропилцеллюлоза принимается во внимание как простой водорастворимый эфир целлюлозы. Если простой эфир целлюлозы представляет собой гидроксиэтилцеллюлозу, подходящей является водорастворимая гидроксиэтилцеллюлоза с молекулярным весом, например, 150,000-350,000, таким как приблизительно 220,000-270,000. В целом, подходящими водорастворимыми гидроксиэтилцеллюлозами являются те, которые имеют динамическую вязкость от 50 до 250 сП, такую как 80-125 сП, где вязкость определяли в 2% мас./об. водном растворе гидроксиэтилцеллюлозы при 25°С. Подходяще гидроксиэтилцеллюлоза имеет степень замещения приблизительно от 0,8 до 2,5, такую как от 0,8 до 1,5, например, приблизительно 1, где степень замещения здесь относится к среднему числу гидроксиэтильных групп в ангидроглюкозном кольце целлюлозы.
В дальнейшем варианте осуществления простой водорастворимый эфир целлюлозы представляет собой метилцеллюлозу, в частности метилцеллюлозу с низкой вязкостью, например, с динамической вязкостью от 5 до 100 сП, такой как 10-25 сП (25 мас./об. раствора в воде при 20°С, измеренной при помощи, например, вискозиметра Ubbelohde в соответствии с ASTM D2363). Подходяще метилцеллюлоза имеет степень замещения от 1 до 2, например, от 1,64 до 1,92, такую как приблизительно 1,8, где степень замещения здесь относится к среднему числу метокси групп в ангидроглюкозном кольце целлюлозы. Подходяще метилцеллюлоза имеет молекулярный вес приблизительно 10,000-50,000, например 10,000-35,000. Подходящие метилцеллюлозы являются коммерчески доступными, например, под торговым наименованием Methocel™, такие как Methocel™ A и Methocel™ MC от Dow Inc.
В другом варианте осуществления настоящего изобретения простой водорастворимый эфир целлюлозы представляет собой водорастворимую соль щелочного метала карбоксиметилцеллюлозы, в частности карбоксиметилцеллюлозу натрия. Подходящей водорастворимой солью щелочного металла карбоксиметилцеллюлозы является соль со средним значением степени замещения приблизительно 0,7-1,2, например, от 0,8 до 0,95, где степень замещения здесь относится к среднему числу карбоксиметильных групп в ангидроглюкозном кольце целлюлозы. В целом, водорастворимая соль щелочного металла карбоксиметилцеллюлозы имеет низкую вязкость, подходяще динамическую вязкость приблизительно 10-2500 сП, например от 10 до 1500 сП, такую как от 10-15 сП или 900-1500 сП, где вязкость измеряли в 1% мас./об. водном растворе карбоксиметилцеллюлозы при 25°С.
Под "сложным эфиром простого водорастворимого эфира целлюлозы", который применяется в настоящем изобретении, подразумевают сложный эфир, образованный между одной или более гидроксильной(ыми) группой(ами), которые находятся в простом водорастворимом эфире целлюлозы, и одной или более подходящей(их) органической (их) кислотой(т) или их реакционоспособными производными, образуя таким образом сложноэфирные связывающие группы в простом водорастворимом эфире целлюлозы. Подходящими простыми водорастворимыми эфирами целлюлозы являются те, которые указаны выше. Подходящими органическими кислотами являются органические карбоновые кислоты, которые могут являться алифатическими или ароматическими карбоновыми кислотами. Подходящие алифатические карбоновые кислоты могут быть ациклическими (разветвленными или неразветвленными) или циклическими и могут быть насыщенными или ненасыщенными.
Предпочтительными ациклическими алифатическими карбоновыми кислотами являются те, которые содержат от 2 до 8 атомов углерода, такие, которые содержат от 2 до 5 атомов углерода. Примерами подходящим насыщенных ациклических алифатических карбоновых кислот являются уксусная кислота, пропионовая кислота, масляная кислота или валериановая кислота. Ациклическая алифатическая кислота может быть необязательно замещенной одной или более группами (например, 1, 2 или 3), которые могут быть одинаковыми или разными, выбранными из карбокси и гидрокси. Подходящие замещенные ациклические алифатические карбоновые кислоты включают, например, ациклические алифатические дикарбоновые кислоты, такие как малоновая, янтарная, глутаровая, фумаровая или малеиновая кислота; ациклические алифатические гидроксизамещенные карбоновые кислоты, например, гликолевая или молочная кислота; и ациклические алифатические гидроксизамещенные ди- или трикарбоновые кислоты, например тартроновая, яблочная, винная или лимонная кислота.
Подходящими ароматическими карбоновыми кислотами являются арильные карбоновые кислоты, содержащие вплоть до 14 атомов углерода. Подходящие арильные карбоновые кислоты содержат арильную группу, например фенильную или нафтильную группу, которая несет одну или более карбоксильных групп (например 1, 2 или 3 карбоксильных групп). Арильная группа необязательно замещена одной или более группами (например 1, 2 или 3), которые могут быть одинаковыми или разными, выбранными из гидрокси, C1-C4-алкокси (например метокси) и сульфонила. Подходящие примеры арильных карбоновых кислот включают фталевую, изофталевую, терефталевую или тримеллитовую кислоту (1,2,4-бензолтрикарбоновую кислоту).
Если органическая кислота несет более чем одну карбоновую кислотную группу, подходяще только одна карбоксильная группа кислоты образует сложноэфирную связь с простым водорастворимым эфиром целлюлозы. Например, в случае сукцината НРМС одна карбоксильная группа каждой сукцинатной группы образует сложноэфирную связь с целлюлозой, а другая карбоксильная группа присутствует в виде свободной кислоты. Если сложный эфир простого водорастворимого эфира целлюлозы содержит свободные кислотные группы, такие как карбоксильные группы, то сложный эфир может применятся в свободно-кислотной форме или в виде его фармацевтически приемлемой соли, например, натриевой соли.
Как очевидно, сложноэфирные связи в пределах простого водорастворимого эфира целлюлозы могут образовываться путем реакции целлюлозы или простого эфира целлюлозы с подходящей органической кислотой, как описано здесь выше, или с реакционноспособным производным органической кислоты. Подходящие реакционноспособные производные включают, например, ангидрид карбоновой кислоты, такой как фталевый ангидрид.
Сложный водорастворимый эфир целлюлозы может нести одинаковые сложноэфирные связывающие части, например, ацетатные группы, как в случае ацетата НРМС. Альтернативно, сложный эфир простого водорастворимого эфира целлюлозы может нести много разных сложноэфирных связывающих частей (например, 2 или больше частей, таких как, например, сукцинатная и фталатная группы). Например, ацетатсукцинат НРМС относится к смешанному сложному эфиру НРМС, который несет как сукцинатную, так и ацетатную группы, и ацетатсукцинаттримеллитат НРМС представляет собой смешанный эфир НРМС, который несет ацетатную, сукцинатную и тримеллитатную группы.
В предпочтительном варианте осуществления настоящего изобретения сложный эфир простого водорастворимого эфира целлюлозы представляет собой сложный эфир НРМС или гидроксипропилцеллюлозы (НРС), который несет одну или более сложноэфирных групп, выбранных из ацетата, сукцината, фталата, изофталата, терефталата и тримеллитата. Конкретными примерами сложных эфиров простых водорастворимых эфиров целлюлозы являются, но не ограничиваясь только ими, ацетат НРМС, сукцинат НМРС, ацетатсукцинат НРМС, фталат НРМС (коммерчески доступный как, например HP-55 и HP 55-S), тримеллитат НРМС, ацетатфталат НРМС, ацетаттримеллитат НРМС, ацетатфталат НРС, бутиратфталат НРС, ацетатфталат НРС, сукцинат и ацетаттримеллитатсукцинат НРС. Более предпочтительно сложный эфир простого водорастворимого эфира целлюлозы выбран из ацетатсукцината НРМС (коммерчески доступного как Aqoat от Shin-Etsu Chemical Co., например, Aqoat, AS-LG).
В другом варианте осуществления изобретения, простой водорастворимый эфир целлюлозы или сложный эфир простого водорастворимого эфира целлюлозы выбран из гидроксипропилцеллюлозы, НРМС, гидроксиэтилцеллюлозы, метилцеллюлозы, водорастворимой соли щелочного металла карбоксиметилцеллюлозы и сложного эфира НРМС или гидроксипропилцеллюлозы, который несет одну или более сложноэфирных группы, выбранных из ацетата, сукцината, фталата, изофталата, терефталата и тримеллитата. В этом варианте осуществления предпочтительно простые водорастворимые эфиры целлюлозы и/или сложные эфиры простых водорастворимых эфиров целлюлозы выбраны из гидроксипропилцеллюлозы, гидроксиэтилцеллюлозы, метилцеллюлозы, карбоксиметилцеллюлозы натрия и ацетатсукцината НРМС. Более предпочтительно, фармацевтическая композиция согласно настоящему изобретению содержит средство и простой водорастворимый эфир целлюлозы, выбранный из гидроксипропилцеллюлозы, гидроксиэтилцеллюлозы, метилцеллюлозы и карбоксиметилцеллюлозы натрия. Предпочтительно простой водорастворимый эфир целлюлозы представляет собой гидроксипропилцеллюлозу, более предпочтительно водорастворимая гидроксипропилцеллюлоза имеет степень замещения более чем 16%. Другой предпочтительный подходящий простой водорастворимый эфир целлюлозы в этом варианте осуществления представляет собой метилцеллюлозу. Подходящими классами вышеуказанных простых водорастворимых эфиров целлюлозы являются те, которые описаны выше.
Композиция в соответствии с настоящим изобретением может содержать один простой водорастворимый эфир целлюлозы или сложный эфир простого водорастворимого эфира целлюлозы или два или больше таких соединений.
Простой водорастворимый эфир целлюлозы или сложный эфир простого водорастворимого эфира целлюлозы представлен в композиции в количестве, достаточном для ингибирования скорости осаждения средства из кислого водного раствора, если значение рН указанного раствора повышается. В частности, простой водорастворимый эфир целлюлозы или сложный эфир простого водорастворимого эфира целлюлозы представлен в композиции в количестве, достаточном для ингибирования скорости осаждения средства из раствора в условиях in-vivo, так как средство переходит из кислой среды желудка в участки с повышенными значениями рН желудочно-кишечного тракта, где, как полагают, средство всасывается, такие как верхние отделы кишечника. Подходяще, весовое соотношение средства к простому водорастворимому эфиру целлюлозы, или сложному эфиру простого водорастворимого эфира целлюлозы составляет от 50:1 до 1:5, например, от 35:1 до 1:1, более предпочтительно от 40:1 до 2:1, еще более предпочтительно от 33:1 до 2:1, такое как от 33:1 до 10:1. В дальнейшем варианте осуществления весовое соотношение средства к простому эфиру целлюлозы или его сложному эфиру составляет вплоть до 32:1, например, от 32:1 до 1:1, более предпочтительно от 30:1 до 2:1, еще более предпочтительно от 25:1 до 3:1.
В другом варианте осуществления изобретения весовое соотношение средства к простому водорастворимому эфиру целлюлозы, или сложному эфиру простого водорастворимого эфира целлюлозы составляет от 40:1 до 2,5:1, предпочтительно от 30:1 до 3:1 и более предпочтительно от 5:1 до 3:1. Изобретатели обнаружили, что, в целом, повышение количества простого эфира целлюлозы или его сложного эфира, таким образом, что весовое соотношение средства к простому эфиру целлюлозы или его сложному эфиру составляет менее чем приблизительно 3:1 (например 1:1), не приводит к какому-либо дальнейшему существенному уменьшению скорости осаждения средства, выше тех значений, которые наблюдаются, когда весовое соотношение составляет приблизительно 3:1.
Подходяще композиция содержит, например, от 0,05 до 85%, предпочтительно от 0,5 до 50%, более предпочтительно от 1 до 30%, особенно предпочтительно от 0,5 до 20% и наиболее предпочтительно от 1 до 10% по весу, исходя из общего веса композиции простых водорастворимых эфиров целлюлозы и сложных эфиров простых водорастворимых эфиров целлюлозы.
Композиция может содержать от 0,01 мг до 1 г средства. Предпочтительно композиция содержит дневную дозу средства в количестве, достаточном для обеспечения желательного терапевтического благоприятного воздействия. Подходящими количествами средства являются, например, 10, 15, 25, 50, 75, 100, 125, 150, 200, 250, 300, 350, 400, 450, 500 или 550 мг, в зависимости от требуемой дозы и конкретной формы фармацевтической композиции. Согласно варианту осуществления, композиция содержит 100, 150, 250 или 500 мг средства, предпочтительно 250 мг средства.
Средство может применятся в виде свободного основания или в виде фармацевтически приемлемой соли, такой как фармацевтически приемлемая моно- или ди-кислото-аддитивная соль, например, с неорганической или органической кислотой, например, соляной кислотой. В одном варианте осуществления изобретения, средство находится в виде свободного основания, предпочтительно в кристаллической свободноосновной форме. Очевидно, что термин "свободноосновная форма" относится к тем случаям, когда средство не находится в виде соли.
Обычно средство находится в количестве в интервале от 1 до 99%, и подходяще от 1 до 70%, например, от 5 до 65% и более предпочтительно от 10 до 60% по весу композиции.
В другом варианте осуществления настоящего изобретения композиция дополнительно содержит смачивающее средство.
В другом варианте осуществления настоящего изобретения композиция содержит:
(a) средство;
(b) смачивающее средство; и
(c) простой водорастворимый эфир целлюлозы.
Нами было обнаружено, что сочетание смачивающего средства и простого водорастворимого эфира целлюлозы, или сложного эфира простого водорастворимого эфира целлюлозы, в композиции дополнительно уменьшает скорость осаждения средства из раствора при значениях рН, подобных к обнаруженным в участках желудочно-кишечного тракта, в которых, как полагают, средство всасывается, таких как верхние отделы кишечника.
Подходящими смачивающими средствами являются фармацевтически приемлемые поверхностно-активные материалы, например, фармацевтически приемлемые поверхностно-активные вещества, которые могут быть ионогенными или неионогенными.
Подходящие фармацевтические приемлемые неионогенные поверхностно-активные вещества включают, например, полиэтиленгликоли, сложные эфиры и простые эфиры полиоксиэтилена, например, полиэтоксилированное касторовое масло (например Cremophor EL), полиэтоксилированное гидрированное касторовое масло, полиэтоксилированные жирные кислоты, производные касторового масла, или полиэтоксилированные жирные кислоты, производные гидрированного касторового масла; этоксилированная стеариновая кислота, например Solutol HS15; и сополимеры этиленоксида-пропиленоксида, например, блоксополимеры этиленоксида-пропиленоксида, такие как Pluronic или Tetronic сурфактанты.
Подходящие фармацевтически приемлемые ионогенные поверхностно-активные вещества могут быть анионогенными, катионогенными или цвиттерионогенными. Подходящие анионогенные поверхностно-активные вещества включают:
(i) соли жирных кислот, такие как алкил- и арилсульфонаты, сульфаты или карбоксилаты, такие как С8-С22-алкилсульфат, сульфонат или карбоксилат щелочного металла, предпочтительно С8-С20-алкилсульфат, сульфонат или карбоксилат щелочного металла, например, додецилсульфат натрия (лаурилсульфат натрия), миристат калия, лаурат натрия или лаурилсульфонат натрия;
(ii) ди-алкилсульфосукцинаты, предпочтительно ди-С4-С12-алкилсульфосукцинаты, предпочтительно в виде соли щелочного металла или щелочноземельного металла, такой как соль натрия, калия или кальция, более предпочтительно натриевая соль. Предпочтительные примеры включают диоктилсульфосукцинат натрия, кальция или калия (например, Докузат натрия или Аэросол ОТ) или диамилсульфосукцинат натрия (Aerosol AY);
(iii) соли желчных кислот, такие как соли дезоксихолевой кислоты, таурохолевой кислоты, или гликохолевой кислоты, предпочтительно соли щелочных металлов желчных кислот, например, натриевая соль желчной кислоты, такая как таурохолат натрия, дезоксихолат натрия или гликохолат натрия; и
(iv) анионогенные диспергируемые в воде производные целлюлозы, такие как анионогенные диспергируемые в воде простые эфиры целлюлозы, например, карбоксиметилцеллюлоза и ее соли.
Подходящие катионогенные поверхностно-активные вещества включают, например, четвертичные аммониевые соединения, такие как:
(i) алкиламмониевые соединения (например С8-С22-алкиламмониевые, предпочтительно С8-С20-алкиламмониевые соединения, такие как галогениды), включая, например, хлорид лауриламмония;
(ii) алкилтриметиламмониевые соединения (например C8-C22-алкилтриметиламмониевые, предпочтительно С8-С20-алкилтриметиламмониевые соединения, такие как галогениды), например, бромид цетилтриметиламмония (Цетрамид), бромид триметилтетрадециламмония (Миристамид) или бромид лаурилтриметиламмония (Лаурамид);
(iii) галогениды бензалкония (такие как галогениды C8-C20-алкилбензилдиметиламмония, предпочтительно галогениды C8-C18-алкилбензилдиметиламмония и их смеси), например, хлорид бензалкония; и
(iv) соединения алкилпиридиния, такие как соединения C8-C20-алкилпиридиния, например, хлорид или бромид цетилпиридиния. Композиция может содержат одно смачивающее средство или два или больше смачивающих средств.
В варианте осуществления смачивающее средство представляет собой фармацевтически приемлемое катионогенное или анионогенное поверхностно-активное вещество, например четвертичное аммониевое соединение или C8-C22-алкилсульфат щелочного металла. Изобретатели обнаружили, что присутствие катионогенного или анионогенного фармацевтически приемлемого поверхностно-активного вещества (предпочтительно катионогенного поверхностно-активного вещества) обладает неожиданным синергетическим действием на уменьшение скорости осаждения средства по сравнению с применением простого водорастворимого эфира целлюлозы или его сложного эфира отдельно или поверхностно-активного вещества отдельно.
В дальнейшем варианте осуществления смачивающее средство представляет собой катионогенное поверхностно-активное вещество, предпочтительно четвертичное аммониевое соединение и более предпочтительно галогенид С8-С18-алкилбензилдиметиламмония, например хлорид бензалкония.
В другом варианте осуществления смачивающее средство выбрано из анионогенного и неоногенного поверхностно-активного вещества или их сочетания. Подходяще в этом варианте осуществления смачивающее средство представляет собой анионогенное поверхностно-активное вещество, предпочтительно С8-С20-алкилсульфат щелочного металла, более предпочтительно додецилсульфат щелочного металла. Еще более предпочтительно смачивающее средство в этом варианте осуществления представляет собой додецилсульфат натрия (лаурилсульфат натрия).
Смачивающее средство может находиться в композиции в соответствии с изобретением в концентрации ниже критической концентрации мицеллообразования (ККМ) смачивающего средства. Изобретатели обнаружили, что смачивающее средство ингибирует осаждение средства из раствора при значениях рН, подобным к тем значениям в желудочно-кишечном тракте, где всасывается средство (таком как верхние отделы кишечника). Это является неожиданным, поскольку смачивающее средство находится в концентрации ниже ККМ, необходимой для растворения средства путем образования мицелл.
ККМ для предпочтительного смачивающего средства в водной среде быстро может быть определено при помощи стандартных методик, например, при помощи планшетного способа Wilhelmy (см., например S.AHagan, A.G.A Coombes, M.C.Garnett, S.E.Dunn, M.C.Davies, L.Illum и S.S.Davis, Langmuir 1996, 12, 2153-2161).
Подходящее весовое соотношение средства к смачивающему средству составляет от 1:2 до 500:1, предпочтительно от 1:1 до 300:1, более предпочтительно от 100:1 до 250:1 и еще более предпочтительно от 150:1 до 200:1.
Подходяще композиция содержит от 0,01 до 10%, например от 0,05 до 5%, предпочтительно от 0,1 до 1% и более предпочтительно от 0,1 до 0,5% по весу смачивающего средства.
Подходящие простые водорастворимые эфиры целлюлозы и сложные эфиры простых водорастворимых эфиров целлюлозы и их количества для применения в композициях, описанных выше, содержащих смачивающее средство, определено выше относительно первого аспекта осуществления изобретения.
Учитывая изложенное выше, предпочтительная композиция в соответствии с этим вариантом осуществления изобретения содержит:
(a) от 1 до 99 (предпочтительно от 10 до 98) частей средства;
(b) от 0,01 до 10 (предпочтительно от 0,05 до 5) частей смачивающего средства (предпочтительно анионогенного поверхностно-активного вещества, например, додецилсульфата натрия); и
(c) от 0,1 до 90 (предпочтительно от 0,5 до 85) частей простого водорастворимого эфира целлюлозы (предпочтительно гидроксипропилметилцеллюлозы);
где все части представляют собой весовые части и сумма частей (а)+(b)+(с)=100.
Другая композиция в соответствии с настоящим изобретением содержит:
(a) от 60 до 99 (предпочтительно от 70 до 85) частей средства;
(b) от 0 до 10 (предпочтительно от 0,05 до 5) частей смачивающего средства (предпочтительно анионогенного поверхностно-активного вещества (например, выбранного из С8-С20-алкилсульфата щелочного металла, предпочтительно додецилсульфата натрия) или катионогенного поверхностно-активного вещества (например, четвертичного аммониевого соединения, такого как галогенид C8-C18-алкилбензилдиметиламмония, например хлорид бензалкония)); и
(c) от 0,1 до 40 (предпочтительно от 0,5 до 30) частей простого водорастворимого эфира целлюлозы, выбранного из гидроксипропилметилцеллюлозы, гидроксипропилцеллюлозы, гидроксиэтилцеллюлозы, метилцеллюлозы и карбоксиметилцеллюлозы натрия (предпочтительно выбранного из гидроксипропилцеллюлозы, гидроксиэтилцеллюлозы, метилцеллюлозы и карбоксиметилцеллюлозы натрия и наиболее предпочтительно водорастворимой гидроксипропилцеллюлозы);
где все части представляют собой весовые части и сумма частей (а)+(b)+(с)=100; и если простой водорастворимый эфир целлюлозы представляет собой НРМС, то весовое соотношение средства к НРМС составляет 32:1 или меньше (например от 32:1 до 1:1, такое как от 30:1 до 2:1).
Простой водорастворимый эфир целлюлозы и/или сложный эфир простого водорастворимого эфира целлюлозы, которые представлены в композиции в соответствии с изобретением, могут применятся в качестве, например, наполнителей, связующих, дезинтеграторов или пленочных покрытий, как, например, описано ниже.
Необязательно в фармацевтическую композицию в соответствии с настоящим изобретением могут включаться дополнительные эксципиенты. Дополнительные эксципиенты, которые могут входить в состав композиции, включают, например, один или более наполнителей (разбавителей), связующих, дезинтеграторов или смазывающих веществ.
В соответствии с дальнейшим вариантом осуществления изобретения, обеспечивается фармацевтическая композиция, содержащая средство, простой водорастворимый эфир целлюлозы и/или сложный эфир простого водорастворимого эфира целлюлозы, смачивающее средство и один или более наполнителей, связующих, дезинтеграторов или смазывающих веществ. В дальнейшем варианте осуществления изобретения обеспечивается твердая фармацевтическая композиция для перорального введения, содержащая средство, простой водорастворимый эфир целлюлозы и/или сложный эфир простого водорастворимого эфира целлюлозы, смачивающее средство, один или более наполнителей, одно или более связующих, один или более дезинтеграторов и одно или более смазывающих веществ.
Подходящие наполнители включают, например, лактозу (которая может находиться в безводной или гидратированной форме, например моногидрат лактозы), сахар, крахмалы (например кукурузный, пшеничный, маисовый, картофельный), модифицированные крахмалы (например, как гидролизированный крахмал или прежелатинированный крахмал, который может быть термически, механически или химически модифицирован), микрокристаллические крахмалы, маннит, сорбит, трегалоза, мальтоза, неорганические соли (например, карбонат кальция, карбонат магния, диосновный фосфат кальция (безводный/дигидратированный), триосновный фосфат кальция), целлюлоза, производные целлюлозы (например, микрокристаллическая целлюлоза), сульфат кальция, ксилит и лактит.
Подходящие связующие включают, например, поливинилпирролидон (например, повидон К25-32, предпочтительно К29-32, где "значение К" представляет собой интервал среднего значения молекулярного веса, полученного из уравнения Fikentscher, описанного в "Справочнике фармацевтических наполнителей", 3-е издание Американского фармацевтического общества, 2000, стр.433), лактозу (которая может находится в безводной или гидратированной форме, например, моногидрат лактозы), крахмалы, модифицированные крахмалы, сахара, аравийскую камедь, трагакантовую камедь, гуаровую камедь, пектин, восковые связующие, микрокристаллическую целлюлозу, метилцеллюлозу, карбоксиметилцеллюлозу и ее соли (например, карбоксиметилцеллюлозу натрия), гидроксипропилметилцеллюлозу, гидроксиэтилцеллюлозу, гидроксипропилцеллюлозу, коповидон, желатин и альгинаты (например, альгинат натрия).
Подходящие дезинтеграторы включают, например, кроскармеллозу натрия, кросповидон, поливинилпирролидон, натрийкрахмалгликолят, крахмалы, микрокристаллическую целлюлозу карбоксиметилцеллюлозу и ее соли (например карбоксиметилцеллюлозу натрия или кальция), гидроксипропилметилцеллюлозу, гидроксипропилцеллюлозу (предпочтительно низкозамещенную гидроксипропилцеллюлозу, то есть гидроксипропилцеллюлозу, которая содержит приблизительно 5-16% по весу гидроксипропокси групп) или альгиновую кислоту.
Подходящие смазывающие вещества включают, например, стеарат магния, стеариновую кислоту, пальмитиновую кислоту, стеарат кальция, тальк, карнубский воск, гидрированные растительные масла, минеральное масло, полиэтиленгликоли, лаурилсульфат натрия и стеарилфумарат натрия.
Дополнительные эксципиенты, которые могут быть добавлены, включают консерванты, стабилизаторы, антиоксиданты, улучшители текучести на основе диоксида кремния, антиадгезивы или средства, способствующие соскальзыванию таблеток с пресс-формы (глиданты).
Другие подходящие наполнители, связующие, дезинтеграторы, смазывающие вещества и дополнительные эксципиненты, которые могут применятся, описаны в "Справочнике фармацевтических наполнителей", 3-е издание (2000) Американского фармацевтического общества; "Теории и практике промышленной фармакологии" (The Theory и Practice of Industrial Pharmacy), 3-е издание, Lachman и др., 1986; "Фармацевтических лекарственных формах: Таблетки" (Pharmaceutical Dosage Forms: Tablets), том 1, 2-е издание, Lieberman, Hebert А., и др., 1989; "Современной технологии лекарственных форм" (Modern Pharmaceutics), Banker, Gilbert и Rhodes, Christopher Т, 3-е издание, 1995; и Remington's Pharmaceutical Sciences, 20-е издание, 2000.
Подходяще один или более наполнителей могут находится в количестве от 10 до 90% по весу, например от 30 до 50% по весу.
Подходяще одно или более связующих могут находится в количестве от 0,5 до 50% по весу, например от 0,5 до 10% по весу.
Подходяще один или более дезинтеграторов могут находится в количестве от 0,5 до 20%, например от 1 до 10% по весу.
Подходяще одно или более смазывающих веществ могут находится в количестве от 0,1 до 5% по весу, например от 0,5 до 3% по весу.
Также следует принять во внимание, что предпочтительный эксципиент может действовать и как связующее, и как наполнитель, или как связующее, наполнитель и дезинтегратор. Обычно объединенное количество наполнителя, связующего и дезинтегратора составляет, например, 40-80% по весу композиции.
В дальнейшем варианте осуществления композиция в соответствии с настоящим изобретением содержит:
(a) от 10 до 80 частей средства;
(b) от 0,05 до 5 частей смачивающего средства, выбранного из анионогенного поверхностно-активного вещества (предпочтительно додецилсульфата натрия);
(c) от 10 до 60 частей одного или более наполнителей, выбранных из лактозы (предпочтительно моногидрат лактозы), маннита и микрокристаллической целлюлозы;
(d) от 1 до 10 частей одного или более дезинтеграторов, выбранных из карбоксиметилцеллюлозы натрия, карбоксиметилцеллюлозы кальция, кроскармеллозы натрия, кросповидона и натрийкрахмалгликолята;
(e) от 1 до 20 частей связующего, выбранного из поливинилпирролидона (предпочтительно повидон (более предпочтительно К29-32) и гидроксипропилметилцеллюлозы (предпочтительно классы, 1828, 2208, 2906 и более предпочтительно 2910, имеющие динамическую вязкость от 2 до 18 сП, как описано выше); и
(f) 0 до 3 частей смазывающего вещества (такого как стеарат магния);
где все части представляют собой весовые части и сумма частей (a)+(b)+(c)+(d)+(e)+(f)=100, и где по крайней мере один из компонентов, выбранный из (d) или (е), содержит простой водорастворимый эфир целлюлозы, выбранный из гидроксипропилметилцеллюлозы и карбоксиметилцеллюлозы натрия.
В этом варианте осуществления является предпочтительным, когда компонент (е) композиции содержит гидроксипропилметилцеллюлозу.
Фармацевтическую композицию в соответствии с настоящим изобретением подходяще готовят в качестве физической смеси, содержащей средство и простой водорастворимый эфир целлюлозы или сложный эфир простого водорастворимого эфира целлюлозы. Альтернативно, средство и простой водорастворимый эфир целлюлозы или сложный эфир простого водорастворимого эфира целлюлозы может вводиться пациенту отдельно или одновременно. Если средство и простой водорастворимый эфир целлюлозы или сложный эфир простого водорастворимого эфира целлюлозы вводят отдельно, то компоненты композиции могут вводиться в любой последовательности, например средство, затем целлюлоза или наоборот. Если применяется раздельное введение, то интервал между введением двух компонентов композиции должен быть таким, чтобы сохранить ингибирующее действие на осаждение средства. Обычно введение в интервале менее чем 20 минут, например, менее чем 10 минут будет являться достаточным. В целом, однако, компоненты настоящей композиции вводятся в основном одновременно, подходяще в виде единичной лекарственной формы, содержащей все компоненты композиции, такой как таблетка или капсула.
В предпочтительном варианте осуществления фармацевтическая композиция по изобретению приготовлена в виде пероральной дозированной формы, например, в виде порошковой смеси или жидкой лекарственной формы, такой как раствор или суспензия в подходящей жидкой среде. В целом, однако, фармацевтическая композиция приготовлена в виде твердой дозированной формы, подходящей для перорального введения, предпочтительно твердой единичной дозированной формы, подходящей для ежедневного перорального введения. Примерами подходящих твердых дозированных форм являются таблетка, пилюля, гранула или капсула.
Если фармацевтическая композиция в соответствии с изобретением представлена в виде твердой дозированной формы, такой как таблетка, пилюля или гранулы, твердая композиция необязательно дополнительно содержит подходящее покрытие, например пленочной покрытие. Покрытие может применятся для обеспечения защиты, например, от доступа влажности или разложения под воздействием света, для окрашивания лекарственной формы, или для модификации или контроля высвобождения средства из лекарственной формы.
Подходящие покрытия, такие как пленочные покрытия, которые могут наносится на композицию в соответствии с изобретением, содержат пленкообразующее средство, например сахар или более предпочтительно пленкообразующий полимер. Подходящие сахарные покрытия хорошо известны и содержат, например, сахарозу или лактозу. Подходящее пленкообразующие средства включают, например, пленкообразующие полимеры, такие как простые эфиры целлюлозы, сложные эфиры и смешанные простые эфиры и сложные эфиры, включая сложные эфиры простых водорастворимых эфиров целлюлозы, например гидроксипропилметилцеллюлоза, гидроксипропилэтилцеллюлоза, гидроксипропилцеллюлоза, метилцеллюлоза, ацетатсукцинат гидроксипропилметилцеллюлозы или фталат гидроксипропилметилцеллюлозы; пленкообразующие акриловые полимеры, например сополимеры метакрилат-метилметакрилат; и пленкообразующие виниловые полимеры, например поливиниловые спирты или поливинилацетатфталат. Подходяще пленкообразующий полимер представляет собой водорастворимый пленкообразующий полимер, предпочтительно простой водорастворимый эфир целлюлозы, например гидроксипропилметилцеллюлозу (предпочтительно гидроксипропилметилцеллюлозу с динамической вязкостью от 2 до 18 сП (измеренной в 2% мас./об. растворе при 20°С), и выбран из, например классов 1828, 2208, 2906 и особенно 2910, как описано выше). Количество применяемого пленкообразующего средства зависит от желательных свойств пленочного покрытия. Как правило, пленкообразующее средство находится в количестве от 40 до 90% по весу пленочного покрытия, например от 50 до 80% пленочного покрытия. Пленкообразующее средство обычно находится в количестве от 0,5 до 5%, подходяще от 1 до 3% по весу лекарственного препарата в соответствии с изобретением.
Необязательно пленочное покрытие содержит дополнительные компоненты, такие как пластификатор, красители, вспомогательные диспергирующие средства и замутнители. Пластификаторы могут применяться для улучшения гибкости и прочности пленки и адгезионных свойств пленочного покрытия. Подходящие пластификаторы включают, например, глицерин, ацетилированные моноглицериды, нитратные сложные эфиры (например, триэтилцитрат), пропиленгликоли, полиэтиленгликоли (например, полиэтиленгликоли с молекулярным весом от 200 до 500, предпочтительно 300), триацетин (триацетат глицерина), триглицериды (например, касторовое масло), или фталатные сложные эфиры (например, диэтилфталат). Как правило, пластификатор, если он применяется, находится в количестве от 1 до 20%, например 5-15% по весу, исходя из веса пленочного покрытия.
Подходящие замутнители и красители хорошо известны и включают, например, диоксид титана, оксиды железа (III) (например, оксид железа).
Подходящие вспомогательные диспергирующие средства включают, например, тальк.
В варианте осуществления изобретения пленочное покрытие содержит
(i) от 50 до 100 (подходяще от 50 до 80) частей простого водорастворимого эфира целлюлозы (подходяще гидроксипропилметилцеллюлоза, предпочтительно гидроксипропилметилцеллюлоза с динамической вязкостью от 2 до 18 сП (измеренной в 2% мас./об. растворе при 20°С), например классы 2910, 1828, 2208 или 2906, как указано выше, с динамической вязкостью от 5 до 7 сП);
(ii) от 0 до 25 (предпочтительно от 5 до 20) частей пластификатора (подходяще полиэтиленгликоль, предпочтительно полиэтиленгликоль с молекулярным весом от 200 до 500); и
(iii) от 0 до 50 (предпочтительно от 0 до 30) частей в целом замутнителей (подходяще диоксид титана), красителей (подходяще диоксид железа) и вспомогательных диспергирующих средств;
где все части представляют собой весовые части и сумма частей (i)+(ii)+(iii)=100.
Покрытие может содержать, например, 0,5-10% по весу композиции, предпочтительно 1-6%, и предпочтительно 2-3%. Подходящие пленочные покрытия являются коммерчески доступными в виде концентратов, которые могут быть разведены водой, и необязательно простым эфиром целлюлозы, таким как НРМС и пластификатором, таким как полиэтиленгликоль, перед введением в композицию. Такие концентраты включают покрытия Opaspray™ от Colorcon, например Opaspray™Brown М-1-25092 и Opaspray Yellow M-l-22842.
В предпочтительном варианте осуществления изобретения фармацевтическая композиция содержит твердую фармацевтическую композицию (такую как таблетка, пилюля или гранула), содержащую:
(i) ядро, содержащее средство; и
(ii) покрытие, содержащее сложный эфир простого водорастворимого эфира целлюлозы или (предпочтительно) простой водорастворимый эфир целлюлозы.
В этом варианте осуществления подходящие простые водорастворимые эфиры целлюлозы являются такими, как описано выше, предпочтительно гидроксипропилметилцеллюлоза (предпочтительно классы 1828, 2208, 2906 и особенно 2910, имеющий динамическую вязкость от 2 до 18 сП). Подходящие сложные эфиры простых водорастворимых эфиров для применения в этом варианте осуществления являются такими, как описано выше относительно первого варианта осуществления настоящего изобретения. Подходяще покрытие наносят в виде пленочного покрытия, как описано в настоящем изобретении. Ядро, содержащее средство, может содержать любую из композиций, описанных здесь выше, содержащих простой водорастворимый эфир целлюлозы или сложный эфир простого водорастворимого эфира целлюлозы (и необязательно другие дополнительные эксципиенты, как описано здесь выше). Альтернативно, ядро может содержать средство без простого водорастворимого эфира целлюлозы или сложного эфира простого водорастворимого эфира целлюлозы. Таким образом, в этом варианте осуществления изобретения простой водорастворимый эфир целлюлозы, или сложный эфир простого водорастворимого эфира целлюлозы полностью может находиться в покрытии. Альтернативно, простой(ые) водорастворимый(ые) эфир(ы) целлюлозы или сложный эфир простого водорастворимого эфира целлюлозы могут находится как в ядре, так и в покрытии.
В дальнейшем варианте осуществления настоящего изобретения обеспечивается твердая фармацевтическая композиция (такая как таблетка, пилюля или гранула), содержащая (i) ядро, содержащее средство; и (ii) покрытие (предпочтительно пленочное покрытие), где простой водорастворимый эфир целлюлозы и/или сложный эфир простого водорастворимого эфира целлюлозы находятся по крайней мере в ядре или покрытии. В этом варианте осуществления простой водорастворимый эфир целлюлозы, или сложный эфир простого водорастворимого эфира целлюлозы может находиться полностью в покрытии, полностью в ядре или может находиться как в ядре, так и покрытии.
В другом предпочтительном варианте осуществления композиция в соответствии с настоящим изобретением представляет собой таблетку, пилюлю или гранулу, подходящую для перорального введения, содержащую ядро, покрытое пленочным покрытием, где ядро содержит:
от 45 до 55% средства (предпочтительно в виде свободного основания);
от 25 до 40% лактозы (предпочтительно моногидрата лактозы);
от 5 до 15% микрокристаллической целлюлозы;
от 2 до 6% дезинтегратора (предпочтительно кроскармеллозы натрия);
от 1 до 5% повидона (предпочтительно К29-32);
от 0,05 до 1% (предпочтительно 0,1 до 0,5%) додецилсульфата натрия; и
от 0,1 до 4% смазывающего вещества (предпочтительно стеарата магния);
и где пленочное покрытие содержит:
от 0,5 до 3% простого водорастворимого эфира целлюлозы (предпочтительно гидроксипропилметилцеллюлозы, более предпочтительно класс 2910, с динамической вязкостью от 5 до 7 сП);
от 0 до 0,5% (предпочтительно от 0,05 до 0,5%) пластификатора (предпочтительно полиэтиленгликоля, более предпочтительно полиэтиленгликоля с молекулярным весом 200 до 500, особенно 300);
от 0 до 0,5% (предпочтительно 0,1 до 0,4%) вспомогательного диспергирующего средства (подходяще талька);
от 0 до 0,5% (предпочтительно 0,1 до 0,4%) замутнителя (подходяще диоксида титана); и
от 0 до 0,5% (предпочтительно от 0,001 до 0,4%) красителя (предпочтительно оксида железа);
где все % представляют собой весовые значения исходя из общего веса композиции.
Фармацевтическая композиция по изобретению может быть приготовлена при помощи стандартных методик и промышленных способов, широко известных в данной области техники, например, путем сухой гомогенизации компонентов или, предпочтительно, методикой влажного гранулирования, затем прессованием с образованием таблетки или наполнением подходящих капсул. Подходящая методика влажного гранулирования предусматривает, например, гомогенизацию совместно средства, одного или более наполнителей, всего или части дезинтегратора и необязательно простого водорастворимого эфира целлюлозы и/или сложного эфира простого водорастворимого эфира целлюлозы, смачивающего средства и/или одного или более связующих, а также других дополнительных эксципиентов, если это является желательным, используя, например, гранулятор. Затем полученную порошковую смесь гранулируют с небольшим объемом очищенной воды, необязательно содержащей смачивающее средство и/или одно или более связующих (которое может представлять собой простой водорастворимый эфир целлюлозы). Гранулят пропускают через сито, разрушая большие агрегаты, высушивают и пропускают через мельницу. Затем к измельченному грануляту добавляют любые оставшиеся дезинтегратор и смачивающее средство и после гомогенизации полученную гомогенную смесь прессуют в таблетки. Альтернативно, измельченным гранулятом наполняют подходящую капсулу, получая лекарственный препарат в виде капсулы.
Подходящая методика сухой гомогенизации предусматривает, например, гомогенизацию вместе средства, простого водорастворимого эфира целлюлозы и/или сложного эфира простого водорастворимого эфира целлюлозы и необязательно смачивающего средства, одного или больше наполнителей, одного или больше связующих и одного или больше дезинтеграторов, а также других дополнительных эксципиентов, если это является желательным. Компоненты для гомогенизации перед гомогенизацией, или самогомогенизацией, можно пропускать через сито, например, сито 400-700 мкм. Смазывающее вещество, которое также можно просеивать, затем добавляют к смеси и продолжают гомогенизировать до получения гомогенной смеси. Затем смесь прессуют в таблетки. Альтернативно, смесью можно наполнять подходящие капсулы, получая лекарственный препарат в виде капсулы.
Следует принять во внимание, что модификации способов сухой гомогенизации и влажного гранулирования, включая также добавление компонентов и их просеивание и смешивание перед прессованием в таблетки, можно осуществлять в соответствии с принципами, хорошо известными в данной области техники.
Если композицию покрывают, например, пленочным покрытием, покрытие затем можно наносить при помощи обычных способов, например, при помощи покрытия составом для пленочного покрытия, предпочтительно, водоосновным пленочным покрывающим составом. Пленочно-покрывающий состав можно наносить на композицию в соответствии с настоящим изобретением путем, например, распыления покрытия или нанесения покрытия в псевдоожиженном слое. Приготовление пленочного покрытия, содержащего простой водорастворимый эфир целлюлозы и/или сложный эфир простого водорастворимого эфира целлюлозы, подходяще может применяться для обеспечения наличия в композиции в соответствии с настоящим изобретением простого водорастворимого эфира целлюлозы или сложного эфира простого водорастворимого эфира целлюлозы.
Если композицию готовят в виде состава для капсул, то сначала композицию готовят в виде порошка или гранул и затем (им)ими наполняют капсулы, обеспечивая получение состава в виде капсул, подходящие капсулы хорошо известны в данной области техники. Например, капсулы из твердого желатина, простого водорастворимого эфира целлюлозы (например, гидроксипропилметилцеллюлозы) и крахмала. Если капсула содержит простой водорастворимый эфир целлюлозы, то она может применятся для обеспечения наличия в композиции в соответствии с изобретением простого водорастворимого эфира целлюлозы.
Таким образом, дальнейшим аспектом настоящего изобретения является обеспечение способа приготовления фармацевтической композиции, который включает смешивание средства с простым водорастворимым эфиром целлюлозы и/или сложным эфиром простого водорастворимого эфира целлюлозы и необязательно с другими эксципиентами, где средство, простой водорастворимый эфир целлюлозы, сложный эфир простого водорастворимого эфира целлюлозы и необязательные наполнители являются такими, как описано выше относительно первого аспекта осуществления изобретения. Подходящие способы смешивания компонентов композиции являются такими, как описано выше.
Средство обладает антипролиферативным действием и, следовательно, композиции в соответствии с настоящим изобретением являются полезными для лечения состояний, таких как описанные в международной заявке на патент WO 96/33980. Например, композиция по изобретению является полезной для лечения многих распространенных злокачественных новообразований у людей, таких как злокачественные новообразования легкого (включая мелкоклеточный рак легкого и не мелкоклеточный рак легкого), молочной железы, предстательной железы, яичников, прямой кишки, желудочно-кишечного тракта, головного мозга (включая глиому и аденому гипофиза), головы и шеи, мочевого пузыря, поджелудочной железы, пищевода, желудка, почек, кожи (включая злокачественную меланому), женских половых органов (включая шейку матки, эндометрий, влагалище, наружные женские половые органы и матку) и рак щитовидной железы и для лечения ряда лейкозов, злокачественных новообразований лимфоидной ткани и солидных опухолей, таких как рак и саркомы. Также ожидают, что композиции по изобретению являются пригодными для лечения других заболеваний, связанных с избыточной клеточной пролиферацией, таких как доброкачественная гиперплазия кожи, например псориаз, и доброкачественная гипертрофия предстательной железы (ВРН).
Дальнейшим аспектом настоящего изобретения является обеспечение фармацевтической композиции в соответствии с изобретением, как описано выше, для применения в качестве лекарственного средства.
Средство, которое содержится в композициях по изобретению, обладает антипролиферативным действием, таким как противораковое действие, которое, как полагают, является следствием его ингибирующего действия по отношению к erbB1 рецепторной тирозинкиназе. Следовательно, композиция по изобретению, как полагают, является полезной для лечения заболеваний или медицинских состояний, опосредованных только erbB1 рецепторными тирозинкиназами или частично ими опосредованными, то есть композиция по изобретению может применяться для получения ингибирующего действия по отношению к erbB1 рецепторной тирозинкиназе у теплокровного животного, которое нуждается в таком лечении. Таким образом, композиция по изобретению обеспечивает способ лечения пролиферации злокачественных клеток, который характеризуется ингибированием erbB1 рецепторных тирозинкиназ, то есть композиция по изобретению может применяться для получения антипролиферативного действия, опосредованного ингибированием только erbB1 рецепторной тирозинкиназы или частично им опосредованным. Следовательно, активное вещество по изобретению, как полагают, является полезным для лечения псориаза и/или злокачественного новообразования путем обеспечения антипролиферативного действия, особенно для лечения злокачественных новообразований, чувствительных к erbB1 рецепторной тирозинкиназе, таких как злокачественные новообразования, описанные выше.
В варианте осуществления изобретения обеспечивается фармацевтическая композиция в соответствии с изобретением, как описано выше, для применения для получения антипролиферативного действия у теплокровного животного (предпочтительно у человека). В другом варианте осуществления обеспечивается фармацевтическая композиция в соответствии с изобретением, как описано выше, для применения для лечения злокачественного новообразования. В дальнейшем варианте осуществления обеспечивается фармацевтическая композиция в соответствии с изобретением для применения для предотвращения или лечения опухолей, которые чувствительны к ингибированию erbB1 рецепторной тирозинкиназы.
Дальнейший вариант осуществления настоящего изобретения обеспечивает применение композиции в соответствии с изобретением, как описано выше, для приготовления лекарственного средства для применения для получения антипролиферативного действия у теплокровного животного (предпочтительно у человека).
Дальнейший вариант осуществления настоящего изобретения обеспечивает применение композиции в соответствии с изобретением, как описано выше, для приготовления лекарственного средства для применения для лечения злокачественного новообразования.
Дальнейший вариант осуществления настоящего изобретения обеспечивает способ ингибирования скорости осаждения средства из раствора в желудочно-кишечном тракте пациента, который нуждается в этом средстве, который предусматривает пероральное введение указанному пациенту композиции в соответствии с первым вариантом осуществления настоящего изобретения, как описано выше.
Дальнейший вариант осуществления настоящего изобретения обеспечивает применение композиции в соответствии с первым вариантом осуществления изобретения, как описано выше, для приготовления лекарственного средства для ингибирования скорости осаждения средства из раствора в желудочно-кишечном тракте теплокровного млекопитающего (предпочтительно человека).
Дальнейший вариант осуществления настоящего изобретения обеспечивает применение простого водорастворимого эфира целлюлозы или сложного эфира или простого водорастворимого эфира для приготовления лекарственного средства, содержащего средство, для ингибирования скорости осаждения средства из раствора в желудочно-кишечном тракте теплокровного млекопитающего (предпочтительно человека).
Дальнейший вариант осуществления настоящего изобретения обеспечивает способ уменьшения непостоянности между пациентами в биодоступности средства и/или его концентрации в плазме у пациента, который нуждается в средстве, который предусматривает пероральное введение указанному пациенту фармацевтической композиции в соответствии с первым вариантом осуществления настоящего изобретения, как описано выше.
Дальнейший вариант осуществления настоящего изобретения обеспечивает применение фармацевтической композиции в соответствии с первым вариантом осуществления настоящего изобретения, как описано выше, для приготовления лекарственного средства для уменьшения непостоянности между пациентами в биодоступности средства и/или его концентрации в плазме крови.
Дальнейший вариант осуществления настоящего изобретения обеспечивает применение простого водорастворимого эфира целлюлозы или сложного эфира или простого водорастворимого эфира целлюлозы для приготовления лекарственного средства, содержащего средство, для уменьшения непостоянности между пациентами в биодоступности средства и/или его концентрации в плазме крови.
В вышеописанных вариантах осуществления изобретения средство может вводиться совместно с простым водорастворимым эфиром целлюлозы или сложным эфиром простого водорастворимого эфира целлюлозы, альтернативно средство и простой эфир целлюлозы или его сложный эфир могут вводиться раздельно в виде отдельных дозированных форм, содержащих соответственно средство и целлюлозу. Однако, как правило, средство и простой водорастворимый эфир целлюлозы или сложный эфир простого водорастворимого эфира целлюлозы вводятся вместе, например, в виде физической смеси, в подходящей пероральной дозированной форме, такой как таблетка, гранула или капсула.
В соответствии с дальнейшим вариантом осуществления изобретения, обеспечивается набор, содержащий единичную дозированную форму, содержащую средство, и единичную дозированную форму, содержащую простой водорастворимый эфир целлюлозы или сложный эфир простого водорастворимого эфира целлюлозы, необязательно с инструкциями по применению набора. Единичные дозированные формы в наборе могут вводиться пациенту совместно или последовательно, как описано выше.
Дальнейший вариант осуществления настоящего изобретения обеспечивает применение простого водорастворимого эфира целлюлозы или сложного эфира простого водорастворимого эфира целлюлозы для ингибирования осаждения средства из водного раствора. Более предпочтительно, применение в соответствии с этим вариантом осуществления настоящего изобретения уменьшает скорость осаждения средства из водного раствора, которое индицируется изменением значения рН раствора, предпочтительно повышения значения рН, по сравнению со скоростью осаждения средства из идентичного водного раствора при отсутствии простого водорастворимого эфира целлюлозы или сложного эфира простого водорастворимого эфира целлюлозы. Еще более предпочтительно применение в соответствии с этим вариантом осуществления изобретения ингибирует осаждение средства из водного раствора в условиях in-vivo, по мере того, как средство переходит из желудка пациента в участки желудочно-кишечного тракта с повышенными значениями рН, из которых происходит всасывание средства (основным местоположением которого, как полагают, является верхние отделы кишечника). Как указано в изобретении, простой водорастворимый эфир целлюлозы или сложный эфир простого водорастворимого эфира целлюлозы подходяще смешивают со средством, обеспечивая фармацевтическую композицию, как описано в изобретении. Следовательно, в варианте осуществления изобретения обеспечивается применение простого водорастворимого эфира целлюлозы или сложного эфира простого водорастворимого эфира целлюлозы в фармацевтической композиции, приспособленной к пероральному введению (подходяще твердой фармацевтической композиции, такой как таблетка или капсула), для ингибирования осаждения средства из водного раствора в условиях in-vivo после введения фармацевтической композиции пациенту.
Необходимая доза композиции по изобретению для лечения или профилактики конкретного пролиферативного заболевания обязательно изменяется, например, в зависимости от организма, который подвергается лечению, и тяжести заболевания, которое поддается лечению. Предпочтительно вводимая дневная доза средства находится в интервале, например, 0,5-15 мг на кг веса тела. Более предпочтительно, вводимая дневная доза композиции, содержащей средство, находится в интервале, например, 1-10 мг на кг веса тела. Предусмотренная стандартная доза композиции, содержащей средство, находится в интервале, например, 1-1000 мг, подходяще 100-750 мг, наиболее подходяще 200-600 мг, предпочтительно около 250 мг. Подходящие соотношения средства к простому водорастворимому эфиру целлюлозы или сложному эфиру простого водорастворимого эфира целлюлозы в таких стандартных дозированных формах являются такими, как описано выше.
Далее изобретение иллюстрируется примерами, которые его не ограничивают, в которых средство представляет собой свободноосновную форму формулы I.
В примерах используются следующие сокращения:
ВЭРХ: высокоэффективная жидкостная хроматография
ACN: ацетонитрил
НРМС: Гидроксипропилметилцеллюлоза
Краткое описание чертежей
На фигуре 1 показана скорость осаждения средства после растворения таблеток с пленочным покрытием, содержащих средство, в кислой среде и последующего сдвига значения рН до 6,5. Точки, обозначенные квадратами, относятся к значениям для таблеток с пленочным покрытием, описанным в примере 1, точки, обозначенные треугольниками, относятся к значениям для таблеток с пленочным покрытием, описанным в примере 2, и точки в виде ромбов относятся к значениям осаждения средства отдельно.
На фигуре 2 показана скорость осаждения средства из раствора после растворения и сдвига значения рН (i) композиции, содержащей смесь средства и метилцеллюлозы (пример 3 - точки, обозначенные ромбами) и (ii) композиции, содержащей смесь средства и гидроксипропилцеллюлозы (пример 5 - точки, обозначенные квадратами), по сравнению с осаждением средства отдельно.
На фигуре 3 показано действие повышения количества НРМС по отношению к средству в композиции на скорость осаждения средства после растворения и сдвига значения рН до 6,5. Точками в виде ромбов обозначены значения для композиции из примера 9 (75 мг НРМС), точками в виде квадратов обозначены значения для композиции из примера 7 (8,16 мг НРМС) и точками в виде треугольников обозначены значения для контрольного образца средства отдельно. В каждом случае на фигуре 3 использовали 250 мг средства.
На фигуре 4 показано дополнительное действие смачивающего средства совместно с простым водорастворимым эфиром целлюлозы на скорость осаждения средства после сдвига значения рН до 6,5. Точками в виде треугольников обозначены % средства в растворе после сдвига значения рН композиции, содержащей средство и НРМС (8,16 мг). Точками в виде ромбов обозначены значения для действия композиции, содержащей средство, НРМС (8,16 мг) и хлорид бензалкония (1,5 мг) на скорость осаждения средства после сдвига значения рН. Точками в виде квадратов обозначены значения для контрольного образца, содержащего средство отдельно. В каждом случае на фигуре 4 композиции содержали 250 мг средства.
Пример 1: Состав таблетки с покрытием
Ядро таблетки
Покрытие таблетки
Состав из примера готовили при помощи обычного влажного гранулирования, прессования и нанесения пленочного покрытия. Средство, моногидрат лактозы, микрокристаллическую целлюлозу и кроскармеллозу натрия смешивали вместе в высокосдвиговом грануляторе, получая гомогенную смесь. Затем к порошкам добавляли водный раствор повидона и лаурилсульфата натрия, перемешивая до получения подходящей влажной массы. Влажные гранулы пропускали через подходящее сито для удаления больших частичек, затем высушивали. Затем высушенные гранулы пропускали через дополнительное сито и гомогенизировали с предварительно измельченным стеаратом магния. Полученные гранулы спрессовывали в ядра таблеток, которые затем покрывали, используя обычную чашечную машину для нанесения покрытий. Пленочное покрытие наносили при помощи напыления водной суспензии гидроксипропилметилцеллюлозы, полиэтиленгликоля 300, талька, диоксида титана и желтого железооксидного пигмента на ядра таблеток.
Таблетки тестировали, используя способ осаждения путем сдвига значения рН, подробно описанный ниже.
Пример 2: Состав таблетки с покрытием
Ядро таблетки
Покрытие таблетки
Сноски: В примерах 1 и 2 использовали следующие эксципиенты:
[1] НРМС 606 класс 2910, динамическая вязкость 6 сП (измеренная при 2% мас./об. в воде при 20°С) от Shin Etsu.
[2] моногидрат лактозы - Pharmatose (от DMV International, Veghel, Голландия).
[3] Plasdone® повидон К29-К32 (International Speciality Products, Wayne, Нью Джерси, США).
[4] Avicel® микрокристаллическая целлюлоза (от FMC International, Филадельфия, Пенсильвания, США).
[5] Ac-Di.Sol® (FMC International, Филадельфия, Пенсильвания, США).
[6] Лаурилсульфат натрия, Albright и Wilson, Oldbury, Великобритания.
[7] Стеарат магния от Mallinckrodt, St Louis, Миссуори, США.
[8] Полиэтиленгликоль 300, Reagent Chemical Services Ltd (Runcorn Великобритания).
[9] Желтый железооксидный пигмент, диоксид титана, тальк и часть НРМС606 получали от Opaspray Yellow М-1-22842, от Colorcon Ltd, Dartford, Kent, Великобритания.
[10] Красный и желтый железооксидные пигменты, диоксид титана и часть 1 НРМС 606 получали от Opaspray Brown M-1-25092, Colorcon Ltd, Dartford, Kent, Великобритания.
Состав, описанный выше, готовили при помощи аналогичных к описанным в примере 1 способам влажного гранулирования, прессования и нанесения пленочного покрытия. Пленочное покрытие наносили, используя концентрат, содержащий красный железооксидный пигмент, желтый железооксидный пигмент и диоксид титана (OpasprayTM Brown M-1-25092, от Colorcon). Концентрат разводили в основании, которое содержит воду, полиэтиленгликоль 300 и НМРС, получая пленочное покрытие, которое затем наносили на ядра таблеток в чашечной машине для нанесения покрытий.
Таблетки тестировали, используя способ осаждения путем сдвига значения рН, подробно описанный ниже.
Способ растворения и сдвига рН
Составы, описанные в примерах выше, растворяли в среде, содержащей 500 мл 0,07 н. HCl (рН приблизительно 1,5) и хлорид натрия (0,2% мас./об.) в течение 1 часа при 37°С (скорость перемешивания 100 об./мин). Образец 5 мл вносили на 60 минут и среду заменяли. При помощи ВЭРХ анализа (описанного ниже) этого образца подтверждали, что 100% средства находилось в растворе.
Затем добавляли 10 мл 2,5 М КН2РО4 /16,72% (мас./об.) раствора NaOH для сдвига значения рН до 6,5. Затем отбирали 5 мл образцов при помощи пластмассового шприца через 2, 5, 15, 30, 45 и 60 минут после установки значения рН и среду заменяли после отбора каждого образца. Каждый образец центрифугировали (14,000 об./мин) при температуре окружающей среды в течении 15 минут и затем анализировали при помощи ВЭРХ, используя следующие условия:
Ссылка [11]: колонка от Hichrom, содержащая гранулы 3 мкм.
Сравнительный пример 1
Способ осаждения при сдвиге значения рН, описанный выше, повторяли, однако при этом использовали 250 мг средства отдельно.
Результаты
На фигуре 1 показаны профили осаждения при сдвиге значения рН для составов, описанных в примерах 1 и 2 и в сравнительном примере 1. Результаты свидетельствуют о том, что скорость осаждения средства после сдвига значения рН до 6,5 замедляется для композиций в соответствии с настоящим изобретением (примеры 1 и 2) по сравнению со средством отдельно, указывая на то, что перенасыщенность сохраняется более длительное время, если средство находится в композиции в соответствии с настоящим изобретением.
Тест осаждения при сдвиге рН моделирует действие изменения значения рН от низких до высоких значений, так как средство перемешается из кислой среды желудка в щелочную среду верхних отделов кишечника, где, как полагают, находится участок наивысшего характерного всасывания средства. На фигуре 1 четко видно, что композиции в соответствии с настоящим изобретением существенно уменьшают скорость осаждения средства из раствора после сдвига значения рН до 6,5. Это, как полагают, обеспечивает улучшение фармакокинетических свойств, например, повышает всасывание и/или биодоступность и может уменьшать непостоянность между пациентами в биодоступности средства и/или его концентрации в плазме.
Пример 3-13
Композиции, описанные ниже, готовили путем взвешивания требуемого количества средства и эксципиента(ов) в ступке. Затем компоненты перемешивали при помощи пестика до получения визуально гомогенной смеси.
Пример 3
Средство 250 мг
Метилцеллюлоза 8,16 мг
Пример 4
Средство 250 мг
Карбоксиметилцеллюлоза натрия 8,16 мг
Пример 5
Средство 250 мг
Гидроксипропилцеллюлоза 8,16 мг
Пример 6
Средство 250 мг
Гидроксиэтилцеллюлоза 8,16 мг
Пример 7
Средство 250 мг
Гидроксипропилметилцеллюлоза 8,16 мг
Пример 8
Средство 250 мг
Гидроксипропилметилцеллюлоза 100 мг
Пример 9
Средство 250 мг
Гидроксипропилметилцеллюлоза 75 мг
Пример 10
Средство 250 мг
Гидроксипропилметилцеллюлоза 25 мг
Пример 11
Средство 250 мг
Ацетатсукцинат гидроксипропилметилцеллюлозы 8,16 мг
Пример 12
Средство 250 мг
Фталат гидроксипропилметилцеллюлозы 8,16 мг
Пример 13
Средство 250 мг
Гидроксипропилметилцеллюлоза 8,16 мг
Лаурилсульфат натрия 1,5 мг
Пример 14
Композицию, содержащую:
Средство 250 мг;
Гидроксипропилметилцеллюлозу 8,16 мг; и
Хлорид бензалкония 1,5 мг
готовили in-situ в кислой среде исследования растворения при сдвиге значения рН (как описано выше относительно примеров 1 и 2) путем приготовления композиции, содержащей средство (250 мг) и гидроксипропилметилцеллюлозу (8,16 мг), используя способ, описанный в примере 7 выше. Затем эту композицию добавляли к кислой растворяющей среде в исследовании рН-зависимого растворения и, для удобства, добавляли хлорид бензалкония к растворяющей среде, содержащей средство, гидроксипропилметилцеллюлозу. Композицию, описанную выше, также можно получить путем добавления хлорида бензалкония непосредственно к смеси средства и гидроксипропилметилцеллюлозы. Это способ является более подходящим для получения больших партий композиции.
Сравнительные примеры 2-4
Следующие сравнительные композиции, содержащие средство, готовили в виде смесей, используя способ, аналогичный к описанному выше в примерах 3-13
Сравнительный пример 2
Средство 250 мг
Ацетатфталат целлюлозы 8,16 мг
Сравнительный пример 3
Средство 250 мг
Этилцеллюлоза 8,16 мг
Сравнительный пример 4
Средство 250 мг
Ацетат целлюлозы 8,16 мг
Контрольный образец
Контрольный образец, содержащий 250 мг средства отдельно, готовили для сравнения с композициями из вышеописанных примеров 3-13.
Все эксципиенты, которые использовались в примерах 3-14 и в сравнительных примерах 2-4, являются коммерчески доступными и имеют следующие характеристики:
Гидроксипропилметилцеллюлоза представляла собой Pharmacoat 606, от Shin-Etsu, вязкость 6 сП (2% мас./об. водный раствор при 20°С, как определялось при помощи способа согласно Фармакопеи США (USP) USP 24, NF 19, 2000, стр.843-844 и USP 24, NF 19, 2000 стр.2002-2003).
Хлорид бензалкония получали от Fluka.
Метилцеллюлоза представляла собой Methocel MC, вязкость 10-25 сП (2% мас./об. раствор в воде 20°С), от Fluka.
Гидроксипропилцеллюлоза от Aldrich, среднее значение ММ 370 000. Вязкость 150-400 сП (веретено Брукфилда #2, 60 об./мин, 2% мас./об. в воде, 25°С).
Карбоксиметилцеллюлоза натрия представляла собой Luxara 1316PA (от Arthur Branwell & Со Ltd). Степень замещения 0,8 - 0,95. Вязкость 900-1500 сП (1% мас./об. раствор).
Ацетатфталат целлюлозы от Aldrich, требуемая вязкость 45-90 сП при 25°С, фактическая вязкость образца 66,20 сП при 25°С.
Этилцеллюлоза от Fisher.
Ацетат целлюлозы от Fisher, вязкость 75-100 сП (6% мас./об. раствор в 95% ацетоне/воде при 25°С).
НРМС ацетатсукцинат представлял собой Aqoat AS-LG от Shin-Etsu.
Кинематическая вязкость 2,4-3,6 мм2/с (измеренная при помощи способа, описанного в "Фармацевтических наполнителях" (Япония) 1993).
НРМС фталат представлял собой НР55 от Shin-Etsu. Вязкость 4×10-5 мм2/с (10 мас.% в смеси равных весовых количеств метанола и метиленхлорида, измеренная в соответствии со способом USP/NF, описанным в USP 24, NF 19, 2000 стр.2002-2003).
Гидроксиэтилцеллюлоза от Aldrich. Требуемая вязкость 80-125 сП (2% мас./об. раствора в воде при 25°С. Фактическая вязкость 107 сП. ММ приблизительно 250 000.
Композиции согласно примерам 3-14 и сравнительным примерам 2-4 исследовали при помощи способа растворения при сдвиге значения рН, аналогичного к описанным в примерах 1 и 2, за исключением того, что:
(i) Каждую композицию взвешивали во флаконе и добавляли до 450 мл кислой растворяющей среды. Затем флакон промывали дополнительно 50 мл свежей кислой среды и после промывки добавляли к основной растворяющей среде для обеспечения полного переноса композиции (общий объем кислой среды =500 мл).
(ii) Для примеров 7 и 13, композицию из примеров растворяли в 50 мл кислой среды в мерной колбе и полученный раствор переносили в сосуд для растворения, содержащий 400 мл кислой растворяющей среды. Колбу дополнительно промывали 50 мл кислой среды для обеспечения полного переноса композиции в сосуд для растворения. Этот способ также применяли для измерения профиля растворения при сдвиге значения рН для контрольного образца, содержащего 250 мг средства отдельно.
(in) В примере 14, для удобства, добавляли хлорид бензалкония в сосуд для растворения, содержащий средство и НРМС в кислой растворяющей среде (см. описание примера 14).
(iv) Образцы растворяющей среды из примеров 3, 5, 9 и 14 и контрольный образец (средство отдельно) отбирали через 60 минут (кислая среда приблизительно рН 1,5 для определения количества средства в растворе перед сдвигом рН). Затем дальнейшие образцы отбирали через 60 минут после установления значения рН, как описано в примерах 1 и 2. Для оставшихся примеров и сравнительных примеров, отбирание образцов прекращали через 5 минут после установления значения рН от 1,5 до 6,5.
Результаты
Действие простых водорастворимых эфиров целлюлозы
В таблице 1 приведены результаты исследования растворения при сдвиге значения рН для примеров, описанных выше, которые содержат средство (250 мг) и 8,16 мг простого водорастворимого эфира целлюлозы или сложного эфира простого водорастворимого эфира целлюлозы. Также в таблице 1 представлены результаты для контрольного образца средства отдельно и данные сравнительных примеров 2-4. В третьей колонке таблицы указан % средства, которое остается растворенным в кислой растворяющей среде через 60 минут (те случаи, для которых указано значение >100%, являются следствием экспериментальной ошибки, связанной с ВЭРХ анализом). В колонках 4 и 5 указан % средства в растворе через 2 и 5 минут после сдвига значения рН до 6,5.
Из таблицы 1 явно следует, что примеры 3-7 в соответствии с настоящим изобретением ингибируют осаждение средства из раствора при сдвиге значения до рН 6,5 по сравнению с контрольным образцом, содержащим средство отдельно. В примере 3 (метилцеллюлоза+средство) 71,3% средства еще оставалось в растворе через 5 минут после сдвига рН до 6,5 по сравнению с только 6,9% для контрольного образца. Из таблицы 1 также следует, что композиции согласно сравнительным примерам 2-4, которые содержат водорастворимые производные целлюлозы, не обнаруживают существенного действия на ингибирование осаждения средства по сравнению с контрольным образцом средства отдельно.
На фигуре 2 показано заметное действие на уменьшение осаждения средства из примеров 3 и 5 по сравнению с контрольным образцом средства отдельно. Из фигуры 2 следует, что осаждение средства существенно уменьшается даже через 60 минут после сдвига рН до 6,5, при использовании относительно небольшого количества простого водорастворимого эфира целлюлозы по сравнению со средством отдельно. Через 60 минут после сдвига значения рН до 6,5, приблизительно 15% средства оставалось в растворе в примерах 3 и 5 (композиции, содержащие средство и метилцеллюлозу или гидроксипропилцеллюлозу), тогда как менее чем 5% средства находилось в растворе для контрольного образца средства отдельно.
В таблице 2 показано действие повышенного количества простого водорастворимого эфира целлюлозы, НРМС, в композициях, содержащих средство, на скорость осаждения средства из раствора после сдвига значения рН до 6,5.
В таблице 2 показано, что наблюдается заметное уменьшение скорости осаждения средства при повышенных уровнях НРМС в композиции. Особенно существенное уменьшение осаждения средства наблюдается для композиции из примера 9 (весовое соотношение средства к НРМС приблизительно 3,3:1).
На фигуре 3 сопоставлены профили растворения при сдвиге значения для примеров 7 и 9 с контрольным образцом, содержащим средство отдельно. Из фигуры 3 явно следует, что повышение уровня НРМС существенно ингибирует осаждение средства по сравнению с контрольным образцом, содержащим средство отдельно.
Действие сложных эфиров простых водорастворимых эфиров целлюлозы
В таблице 3 сопоставлены данные растворения при сдвиге значения рН средства отдельно (контроль) с соответствующими значениями для композиций, содержащих средство и сложный эфир простых водорастворимых эфиров целлюлозы из примеров 11 и 12 энтеросолюбильного полимера. В таблице 3 также приведены данные, полученные для сравнительных примеров 2 и 4, которые содержат сложные водорастворимые эфиры целлюлозы. В таблице 3 для каждой композиции содержание средства составляет 250 мг, а наполнителя - 8,16 мг.
Из таблицы 3 явно следует, что для композиций в соответствии с изобретением, содержащих сложный эфир простого водорастворимого эфира целлюлозы, существенно уменьшается скорость осаждения средства по сравнению со средством отдельно или композициями из сравнительных примеров.
Действие смачивающих средств
В таблице 4 сопоставлены данные растворения при сдвиге значения рН для композиций из примеров 13 и 14, которые содержат смачивающее средство и простой водорастворимый эфир целлюлозы, с такой же композицией без смачивающего средства (Пример 7). В таблице 4 также приведены данные для контрольного образца средства отдельно. В таблице 3 для каждой указанной композиции содержание средства составляет 250 мг, а содержание гидроксипропилметилцеллюлозы - 8,16 мг, и в примерах 13 и 14 смачивающее средство содержится в количестве 1,5 мг.
Из таблицы 4 следует, что включение смачивающего средства в композицию совместно с простым водорастворимым эфиром целлюлозы обладает заметным действием на уменьшение скорости осаждения средства после сдвига значения рН до 6,5. В частности, включение катионогенного поверхностно-активного вещества, такого как хлорид бензалкония, в композицию приводит к неожиданному уменьшению скорости осаждения средства.
На фигуре 4 также показано действие включения смачивающего средства в композиции в соответствии с настоящим изобретением. На фигуре 4 показано заметное уменьшение осаждения средства, если применяется композиция из примера 14, которая содержит НРМС и катионогенное поверхностно-активное вещество хлорид бензалкония по сравнению с применением НРМС отдельно или с контрольным образом, содержащим средство отдельно.
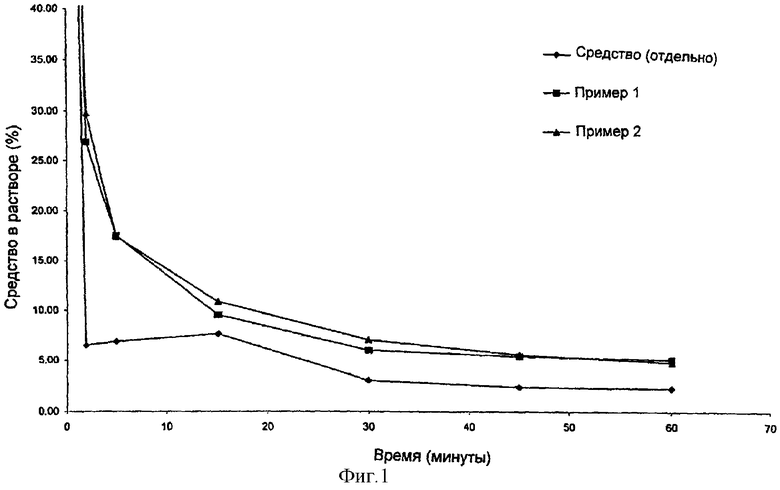
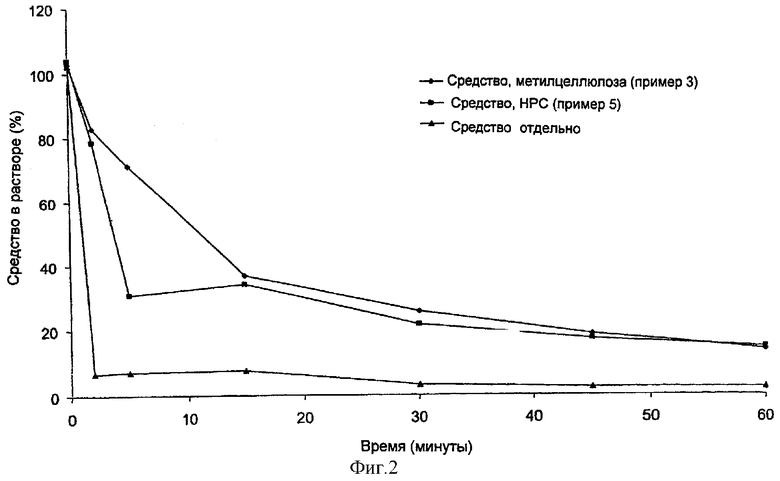
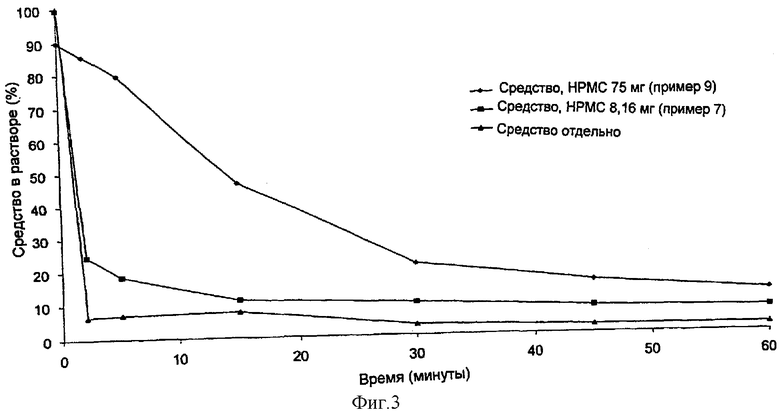

Фармацевтическая композиция содержит 4-(3'-хлор-4'-фторанилино)-7-метокси-6-(3-морфолинопропокси)хиназолин или его фармацевтически приемлемую соль (средство) и простой водорастворимый эфир целлюлозы или сложный эфир простого водорастворимого эфира целлюлозы. Композиция обладает антипролиферативным действием. Простой водорастворимый эфир целлюлозы или сложный эфир простого водорастворимого эфира целлюлозы, которые представлены в композиции, ингибируют скорость осаждения средства из раствора при переходе из кислой среды желудка в среду верхних отделов желудочно-кишечного тракта с повышенными значениями рН, что обеспечивает улучшенные фармакокинетические свойства. 7 н. и 16 з.п. ф-лы, 4 ил., 4 табл.
Приоритет по пунктам:
| WO 9633980 A, 31.10.1996 | |||
| US 4344934 A, 17.08.1982 | |||
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| СПОСОБ СОХРАНЕНИЯ СКОЛЬЗЯЩЕЙ ФУНКЦИИ ОТВОДЯЩИХ МЫШЦ БЕДРА ПРИ НИЗВЕДЕНИИ БОЛЬШОГО ВЕРТЕЛА | 2005 |
|
RU2306885C2 |
Авторы
Даты
2008-03-10—Публикация
2003-02-24—Подача