Область, к которой относится изобретение
Настоящее изобретение относится к электроду, включающему в себя алифатическое нитрильное соединение. Более конкретно, настоящее изобретение относится к электроду, поверхность которого покрыта алифатическим нитрильным соединением или который содержит активный электронный материал, содержащий алифатическое нитрильное соединение, а также к литиевой вторичной батарее, имеющей такой электрод.
Уровень техники
Обычно неводный электролит, содержащий соль лития, такую как LiPF6, и карбонатный растворитель, в ходе повторяющихся циклов заряда/разряда непрерывно реагирует с поверхностью активного катодного материала (в частности, LiCoO2), что приводит к непрерывному образованию резистивного слоя, который вызывает увеличение сопротивления и прерывает проводимость ионов Li+. Такой резистивный слой приводит к изоляции частиц активного материала друг от друга или от токосъемника (Al-ой фольги), таким образом снижая рабочие характеристики и срок службы батареи. Кроме того, такие проблемы в большей степени и преимущественно возникают при высокой температуре из-за ускорения побочных реакций между электролитом и поверхностью катода, когда батарея находится при высокой температуре (45°С или 60°С) в течение долгого времени, что приводит к существенному уменьшению срока службы батареи.
Между тем, вторичные батареи на основе неводного электролита характеризуются проблемами, касающимися безопасности при избыточной зарядке, по следующим причинам. Активные катодные материалы, такие как содержащие литий и/или ион лития оксиды металлов, способные к интеркалированию/деинтеркалированию ионов лития, превращаются в термически нестабильные вещества из-за высвобождения лития во время избыточной зарядки. Когда температура батареи достигает критической температуры, из таких нестабильных веществ высвобождается кислород, и этот свободный кислород может реагировать с растворителем электролита и т.д. посредством механизма сильноэкзотермичной реакции. Поэтому такая последовательность экзотермических реакций при нагревании приводит к термическому выходу из строя.
В целом, факторы, влияющие на безопасность батареи, включают в себя: (1) выделение тепла вследствие окисления электролитов; и (2) выделение тепла, происходящее в результате структурного разрушения катода вследствие избыточной зарядки. Когда имеет место избыточная зарядка, выделение тепла, происходящее из-за вышеуказанных факторов, независимо или одновременно вызывает увеличение внутренней температуры батареи, с последующим воспламенением или взрывом батареи. Таким образом, батареи демонстрируют проблему безопасности при избыточной зарядке.
В то же время, когда к батарее прикладываются внешние физические воздействия (например, воздействие высокой температуры, такой как температура в 150°С или выше, при нагревании), в то время, как батарея заряжена или избыточно заряжена, батарея перегревается вследствие выделения тепла, вызываемого реакцией легко воспламеняемого электролита с активным катодным материалом, и структура электрода (в частности, катода) разрушается с выделением кислорода, который ускоряет горение электролита. Поэтому разделитель, расположенный между катодом и анодом, плавится, и электрическая энергия вызывает термический выход из строя, приводящий к воспламенению и взрыву батареи.
Раскрытие изобретения
Авторы настоящего изобретения обнаружили, что алифатическое нитрильное соединение, которое образует сильную связь с переходным металлом или оксидом переходного металла в активном электродном материале, может улучшать безопасность батареи, когда эта батарея избыточно заряжается и/или подвергается физическим воздействиям, оказываемым извне батареи (например, воздействию высокой температуры при нагревании). В то же время, авторы также обнаружили проблему, заключающуюся в том, что, когда алифатическое динитрильное соединение используют в качестве добавки к электролиту, наблюдается увеличение вязкости электролита, так что не может беспрепятственно протекать диффузия ионов Li в экстремальных условиях (низкая температура от -20°С до -10°С), что приводит к снижению рабочих характеристик батареи при низкой температуре.
Поэтому настоящее изобретение было создано ввиду вышеуказанных проблем. Задача настоящего изобретения заключается в улучшении безопасности батареи без ухудшения рабочих характеристик батареи путем равномерного введения алифатического динитрильного соединения в электрод таким образом, что это алифатическое нитрильное соединение может вносить свой вклад только в образование комплекса с активным электродным материалом.
Согласно одному аспекту настоящего изобретения предлагается электрод, содержащий алифатическое нитрильное соединение, предпочтительно - соединение, представленное следующей формулой 1, поверхность которого покрыта этим алифатическим нитрильным соединением или который содержит активный электродный материал, содержащий это алифатическое нитрильное соединение. Согласно другому аспекту настоящего изобретения, предлагается литиевая вторичная батарея, имеющая вышеописанный электрод.
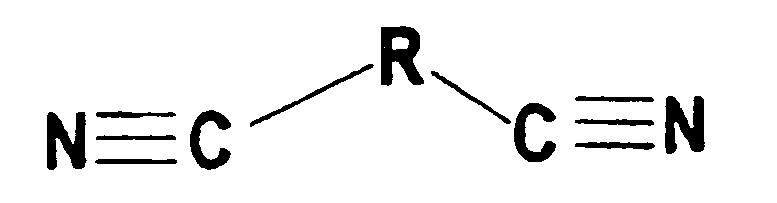
[Формула 1],
в которой R представляет собой алкан С2-С15.
Предпочтительно, алифатическое нитрильное соединение, предпочтительно - соединение, представленное формулой 1, равномерно нанесено на поверхность активного электродного материала в электроде.
Кроме того, является предпочтительным, чтобы электрод согласно настоящему изобретению включал в себя комплекс, образованный между поверхностью активного электродного материала и алифатическим нитрильным соединением.
Ниже настоящее изобретение будет объяснено более подробно.
Согласно настоящему изобретению электрод для литиевой вторичной батареи отличается тем, что он содержит алифатическое нитрильное соединение, предпочтительно - соединение, представленное приведенной выше формулой 1.
Алифатические нитрильные соединения могут образовывать сильную связь с переходным металлом или оксидом переходного металла, таким как кобальт, выступающим на поверхность активного электродного материала, посредством их функциональных цианогрупп, имеющих высокий дипольный момент. В частности, функциональные цианогруппы могут образовывать более сильный комплекс на поверхности активного электродного материала при температуре 45°С или выше (см. фиг.1).
Электрод, покрытый алифатическим нитрильным соединением, имеет поверхность с сильной защитой, которая защищает поверхность электрода от побочных реакций с электролитом. Поэтому, оказывается возможным осуществлять эффективное интеркалирование/деинтеркалирование ионов лития без изменения вязкости электролита и ионной проводимости и предотвращать образование резистивного слоя, способного снижать рабочие характеристики батареи, путем реакции электролита с электродом во время повторяющихся циклов зарядки/разрядки на поверхности электрода. В результате этого, можно сохранять рабочие характеристики батареи. Кроме того, согласно настоящему изобретению литиевая вторичная батарея, имеющая электрод с равномерно нанесенным алифатическим нитрильным соединением на поверхности активного электродного материала, а предпочтительно - содержащий алифатическое нитрильное соединение, образующее прочный комплекс с переходным металлом и/или оксидом переходного металла, присутствующим на поверхности активного электродного материала, может стабилизировать переходный металл и/или оксид переходного металла, предотвращая частичное выделение переходного металла из активного электродного материала во время повторяющихся циклов зарядки/разрядки. Кроме того, когда к батарее прилагаются внешние физические воздействия (в частности, когда батарея подвергается воздействию высокой температуры, такой как температура 150°С или выше), возможно эффективно подавлять экзотермическую реакцию, вызываемую взаимодействием электролита непосредственно с поверхностью электрода, и замедлять структурное разрушение активного электродного материала, тем самым предотвращая воспламенение и взрыв, возникающие из-за увеличения температуры внутри батареи. В особенности, так как алифатические нитрильные соединения могут защищать поверхность электрода сильнее при высокой температуре в 45°С или выше, чем комнатная температура, то можно обеспечивать термически устойчивые электроды.
Хотя соединение, выраженное приведенной выше формулой 1, приведено в качестве примера алифатического нитрильного соединения, которое может быть введено в электрод согласно настоящему изобретению, другое алифатическое нитрильное соединение, имеющее нитрильную группу только с одной стороны по сравнению с соединением, выраженным формулой 1, имеет большую возможность для обеспечения безопасности и/или рабочих характеристик батареи в такой степени, что является эквивалентным соединению, выраженному формулой 1, и, таким образом, оно также входит в объем настоящего изобретения.
Между тем, алканы, присутствующие в соединении, выраженном формулой 1, не имеют реакционной способности. Поэтому, когда соединение, выраженное формулой 1, вводят в электрод, вероятность необратимой реакции низка. В результате, добавление соединения, выраженного формулой 1, не вызывает ухудшения рабочих характеристик батареи.
Так как ароматическое нитрильное соединение разлагается на аноде во время первоначального цикла зарядки (во время формирования), увеличивая необратимую емкость и существенно ухудшая рабочие характеристики батареи, то предпочтительно не вводить ароматическое нитрильное соединение в электрод и не покрывать электрод ароматическим нитрильным соединением.
Частные примеры соединения, представленного формулой 1, включают в себя сукцинонитрил (R=C2H4), глутаронитрил (R=C3H6), адипонитрил (R=C4H8), пимелонитрил (R=C5H10), октандинитрил (R=C6H12), азелонитрил (R=C7H14), себацинонитрил (R=C8H16), 1,9-дицианононан (R=C9H18), додекандинитрил (R=C10H20) и т.п., но не ограничиваются ими.
В частности, сукцинонитрил образует самый прочный защитный слой среди соединений, представленных формулой 1. Чем длиннее алкан, тем слабее становится образуемый защитный слой. Поэтому, среди вышеуказанных соединений в качестве материала покрытия наиболее предпочтительно использовать сукцинонитрил.
Алифатическое нитрильное соединение присутствует в электроде предпочтительно в количестве 0,1 - 20 мас.% из расчета на массу электролита или 1 - 10 мас.% из расчета на массу активного материала, более предпочтительно - в количестве 10 мас.% или менее из расчета на массу электролита или 5 мас.% или менее из расчета на массу активного материала, а наиболее предпочтительно - в количестве 5 мас.% или менее из расчета на массу электролита или 2,5 мас.% или менее из расчета на массу активного материала.
Для того чтобы ввести алифатическое нитрильное соединение в электрод, можно нанести на электрод раствор покрытия, содержащий алифатическое нитрильное соединение. В противном случае, алифатическое нитрильное соединение можно добавлять в суспензию активного электродного материала при формировании электрода.
С той целью, чтобы нитрильное соединение участвовало только в образовании комплекса с оксидом переходного металла в активном электродном материале, раствор покрытия, содержащий алифатическое нитрильное соединение, наносят на электрод или алифатическое нитрильное соединение добавляют в суспензию, содержащую активный электродный материал, в адекватном количестве. Предпочтительно, электрод или суспензию, содержащие нитрильное соединение, обрабатывают при высокой температуре. Тогда поверхность электрода, то есть поверхность активного электродного материала, может быть равномерно защищена алифатическим нитрильным соединением. В добавление к вышеуказанной высокотемпературной обработке, применяемой к электроду или суспензии, батарею можно предпочтительно обрабатывать при высокой температуре после ее сборки.
Алифатическое нитрильное соединение диспергируют или растворяют в растворителе с получением раствора, этот раствор наносят на поверхность электрода, и затем растворитель высушивают, чтобы покрыть поверхность электрода, предпочтительно - поверхность активного электродного материала, алифатическим нитрильным соединением. Способ нанесения покрытия может включать в себя покрытие погружением, покрытие распылением или тому подобное.
Нет особых ограничений в выборе растворителя для использования в растворе покрытия, содержащем алифатическое нитрильное соединение, при условии, что этот растворитель имеет хорошую совместимость. Предпочтительно использовать в качестве растворителя для раствора покрытия неполярные растворители, такие как ТГФ (тетрагидрофуран), и полярные растворители, такие как НМП (H-метил-2-пирролидон), и карбонатные растворители, используемые в качестве растворителя для электролита. Хотя количество алифатического нитрильного соединения меняется с количеством, наносимым на электрод, алифатическое нитрильное соединение можно использовать в диапазоне от 1:9 до 9:1, выраженном в массовом отношении к растворителю.
Способ формирования электрода путем добавления алифатического нитрильного соединения к суспензии активного электродного материала включает в себя этапы: смешивания алифатического нитрильного соединения с активным электродным материалом и другими добавками, такими как связующее и проводящий агент, по мере необходимости, с получением суспензии активного электродного материала; нанесения суспензии активного электродного материала на токосъемник; и удаления используемого в этой суспензии растворителя путем сушки и т.п.
Чтобы нанести суспензию активного электродного материала, можно использовать нанесение экструзионной головкой, нанесение валиком, нанесение инструментом в форме запятой и их комбинации.
В то же время, так как соединение, представленное формулой 1, начинает немного улетучиваться при высокой температуре в 100°С или выше и затем по существу испаряется без остатка при температуре примерно 150°С, необходимо поддерживать адекватную температуру сушки, скорость сушки и вентиляционного потока с целью гладкого покрытия электрода соединением, представленным формулой 1, из суспензии, содержащей НМП в качестве растворителя.
Чтобы предохранить соединение, представленное формулой 1, от испарения и удалить остаточный НМП, температура сушки предпочтительно составляет в диапазоне от 90°С до 110°С. Скорость сушки предпочтительно составляет 3 м/мин или менее, более предпочтительно - 2 м/мин или менее, но может меняться с длиной сушильной печи и с температурой сушки суспензии. Вентиляционный поток предпочтительно составляет от 2000 до 3000 об/мин.
В частности, когда электрод, содержащий соединение, выраженное формулой 1, сушат при слишком низкой температуре с тем, чтобы сохранить данное соединение в электроде, содержание НМП и содержание воды в электроде увеличиваются, вызывая проблему, заключающуюся в том, что ухудшаются рабочие характеристики батареи. С другой стороны, когда электрод сушат при слишком высокой температуре, содержание НМП в электроде уменьшается, но соединение, выраженное формулой 1, существенно испаряется, и поэтому невозможно получить равномерно покрытый электрод. Поэтому важно, чтобы температура сушки, скорость сушки и вентиляционный поток поддерживались в указанных диапазонах.
В то же время предпочтительно, чтобы алифатические нитрильные соединения образовывали комплекс с поверхностью активного электродного материала. Предпочтительно, с целью образования комплекса электрод, содержащий активный электродный материал, поверхность которого покрыта алифатическим нитрильным соединением, дополнительно обрабатывают при высокой температуре. В частности, такую высокотемпературную обработку можно проводить в таком диапазоне температур, чтобы не влиять на активный электродный материал и связующее, обычно - при температуре 180°С или ниже. Иным образом, хотя высокотемпературная обработка меняется вместе с типом алифатического нитрильного соединения, ее можно проводить в таком диапазоне температур, чтобы предотвратить испарение алифатического нитрильного соединения, обычно - при температуре 120°С или ниже. Обычно высокотемпературную обработку проводят подходящим образом до или после сборки батареи при температуре между 30°С и 90°С, предпочтительно - между 60°С и 90°С. Длительное выдерживание при температуре между 30°С и 40°С может приводить к такому же эффекту.
В качестве активного катодного материала для применения в электродах могут быть использованы литийсодержащие оксиды переходных металлов. Активный катодный материал может представлять собой по меньшей мере один материал, выбранный из группы, состоящей из LiCoO2, LiNiO2, LiMn2O4, LiMnO2 и LiNi1-xCOxO2 (где 0<Х<1). Между тем, в качестве активного анодного материала для применения в электродах могут быть использованы углерод, металлический литий или сплав лития. Кроме того, в качестве активного анодного материала могут быть использованы другие оксиды металлов, способные к интеркалированию/деинтеркалированию лития и имеющие электрический потенциал относительно лития 2 В или менее (например, TiO2 и SnO2).
Помимо активных материалов, суспензия для электродов может дополнительно содержать связующее, проводящий агент, регулятор вязкости, дополнительное связующее и т.п.
Могут быть использованы любые обычные токосъемники (коллекторы), выполненные из проводящих материалов, без какого-либо ограничения. Более конкретно, широко используют токосъемники, выполненные из металлов, таких как железо, медь, алюминий и никель.
Литиевая вторичная батарея, в которой может быть применен содержащий алифатическое нитрильное соединение электрод согласно настоящему изобретению, может содержать:
(1) катод, способный к интеркалированию/деинтеркалированию ионов лития;
(2) анод, способный к интеркалированию/деинтеркалированию ионов лития;
(3) пористый разделитель (сепаратор); и
(4) а) соль лития; и
b) соединение - электролит.
Неводные электролиты для литиевой вторичной батареи обычно включают в себя легковоспламеняющиеся неводные органические растворители, включая циклические карбонаты и/или линейные карбонаты. Конкретные примеры циклических карбонатов, которые могут быть использованы в настоящем изобретении, включают в себя этиленкарбонат (ЭК), пропиленкарбонат (ПК), гамма-бутиролактон (ГБЛ) и т.п. Типичные примеры линейных карбонатов включают в себя диэтилкарбонат (ДЭК), диметилкарбонат (ДМК), этилметилкарбонат (ЭМК).
При использовании содержащего алифатическое нитрильное соединение электрода согласно настоящему изобретению возможно подавить термический выход из строя и улучшить безопасность батарей, не вызывая при этом ухудшения рабочих характеристик батареи, даже в том случае, если в качестве электролитов используются обычные легковоспламеняющиеся неводные органические растворители.
Неводные электролиты содержат соли лития, такие как LiClO4, LiCF3SO3, LiPF6, LiBF4, LiAsF6, LiN(CF3SO2)2 и т.п.
Литиевая вторичная батарея согласно настоящему изобретению может иметь цилиндрическую, призматическую или "карманную" форму.
Краткое описание чертежей
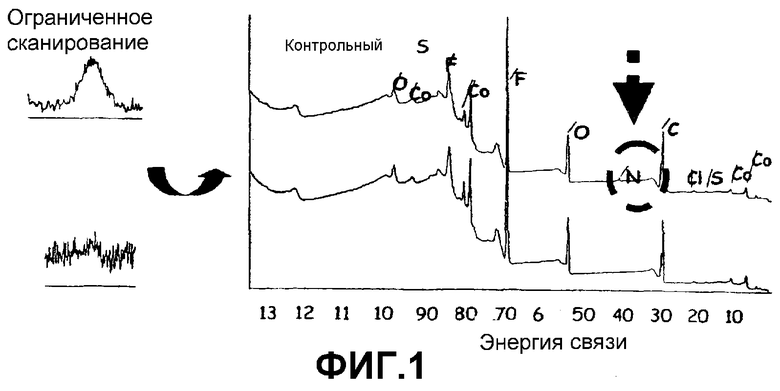
Фиг.1 представляет собой график, показывающий данные РФС (рентгеновской фотоэлектронной спектроскопии) для катодов в батареях, полученных в примере 1 и сравнительном примере 1.
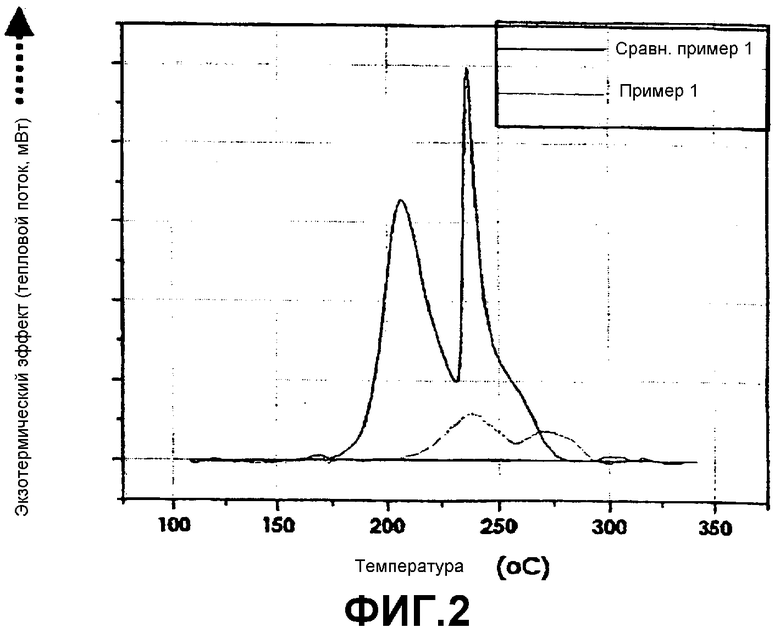
Фиг.2 представляет собой график, показывающий пики выделения тепла и результаты контроля выделения тепла для катодов в батареях, полученных в примере 1 и сравнительном примере 1.
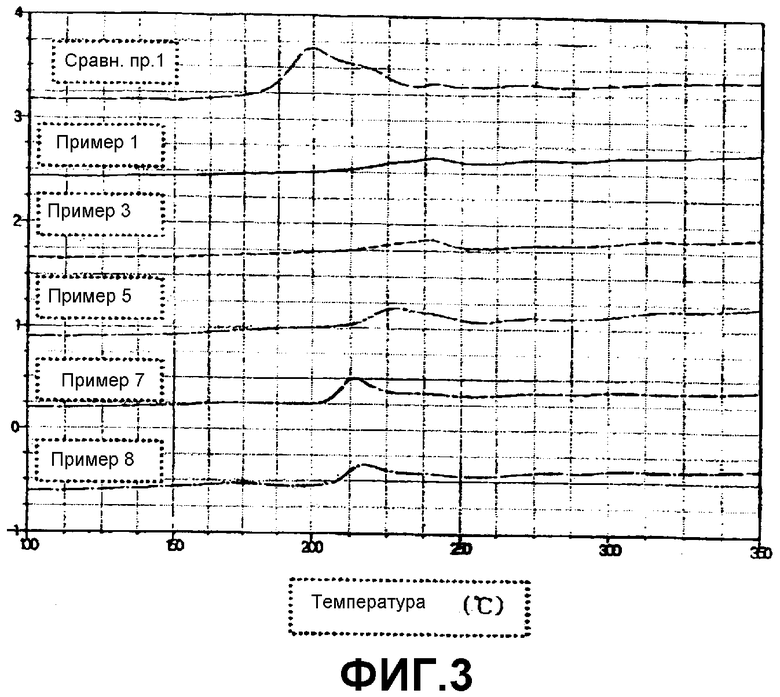
Фиг.3 представляет собой график, показывающий пики выделения тепла и результаты контроля выделения тепла для катодов в батареях, полученных в сравнительном примере 1 и примерах 1, 3, 5, 7 и 8.
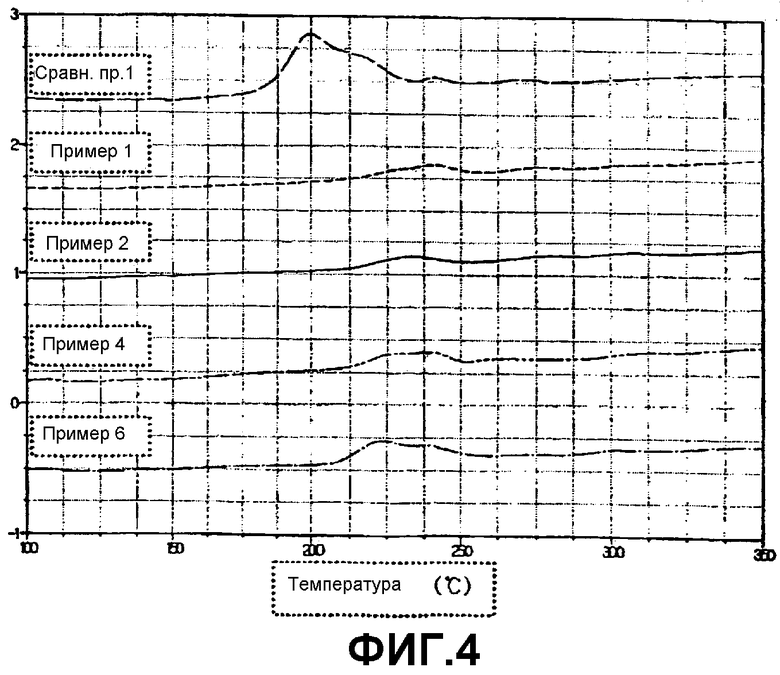
Фиг.4 представляет собой график, показывающий пики выделения тепла и результаты контроля выделения тепла для катодов в батареях, полученных в сравнительном примере 1 и примерах 1, 2, 4 и 6.
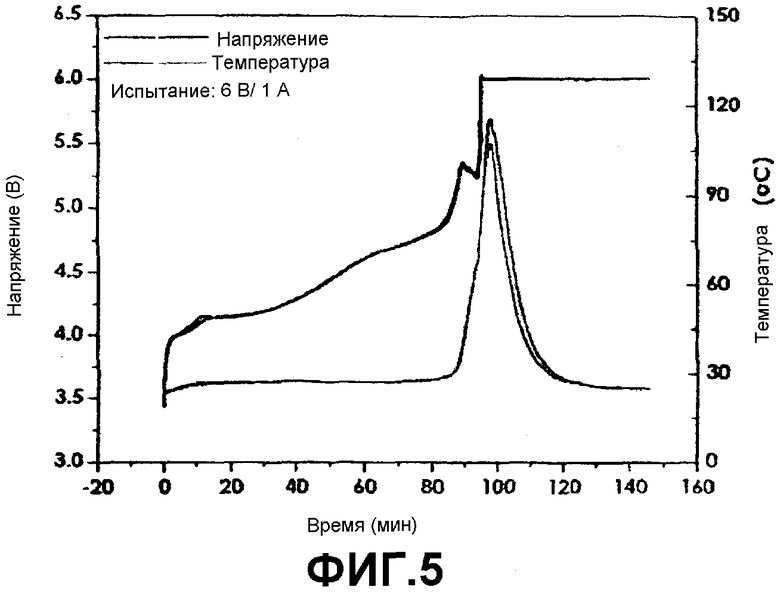
Фиг.5 представляет собой график, показывающий результаты испытания избыточной зарядкой для батареи, полученной в примере 1, в условиях 6 В/1 А (напряжение, температура).
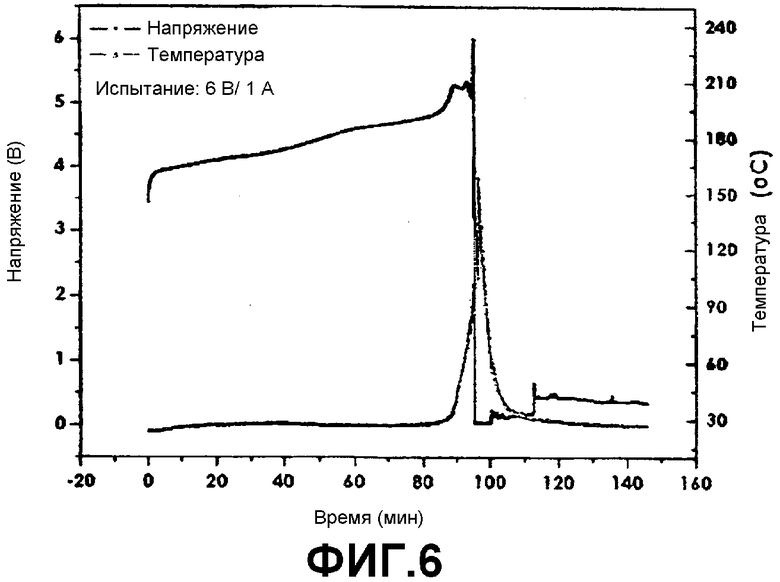
Фиг.6 представляет собой график, показывающий результаты испытания избыточной зарядкой для батареи, полученной в сравнительном примере 1, в условиях 6 В/1 А (напряжение, температура).
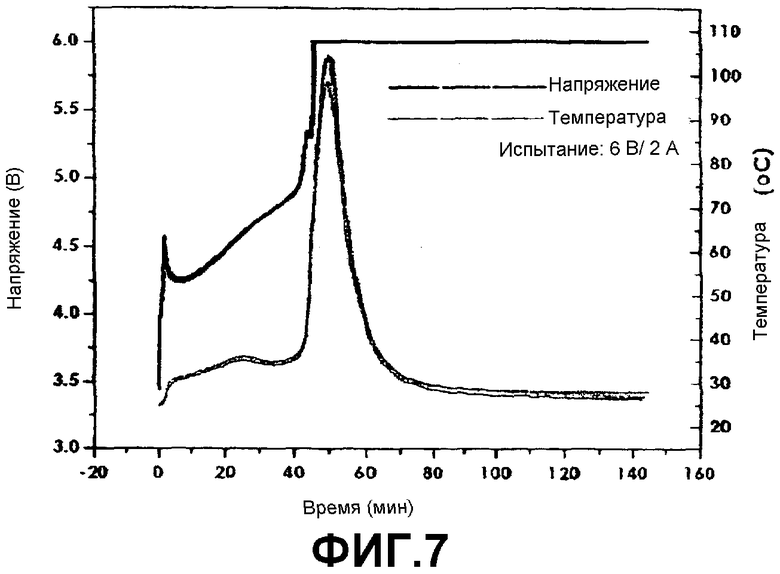
Фиг.7 представляет собой график, показывающий результаты испытания избыточной зарядкой для батареи, полученной в примере 1, в условиях 6 В/2 А (напряжение, температура).
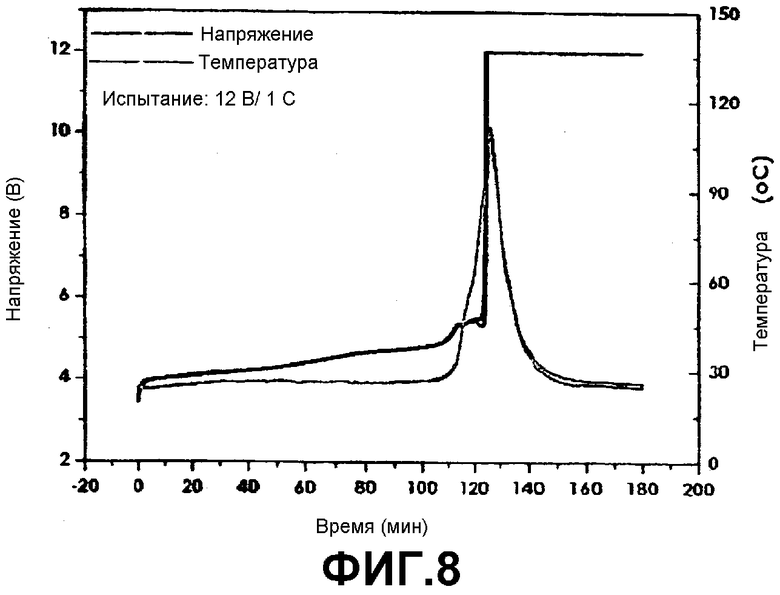
Фиг.8 представляет собой график, показывающий результаты испытания избыточной зарядкой для батареи, полученной в примере 1, в условиях 12 В/1 С (напряжение, температура).
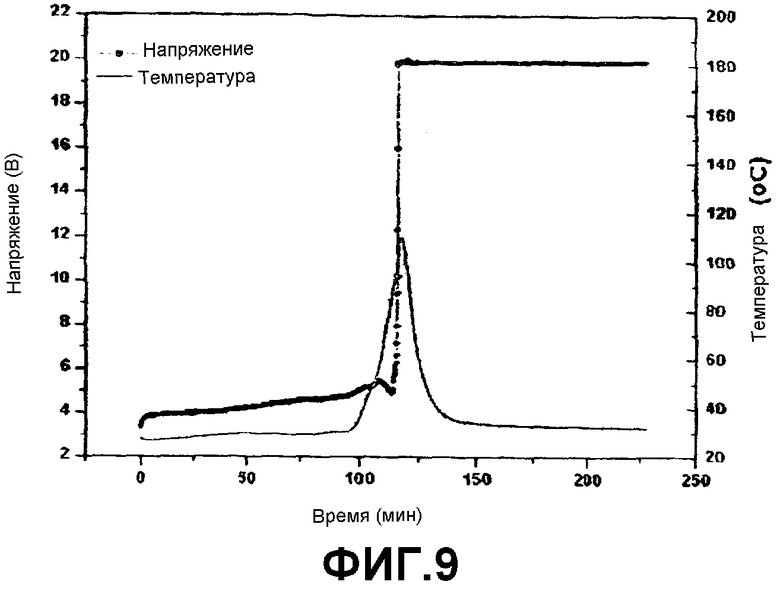
Фиг.9 представляет собой график, показывающий результаты испытания избыточной зарядкой для батареи, полученной в примере 1, в условиях 20 В/1 С (напряжение, температура).
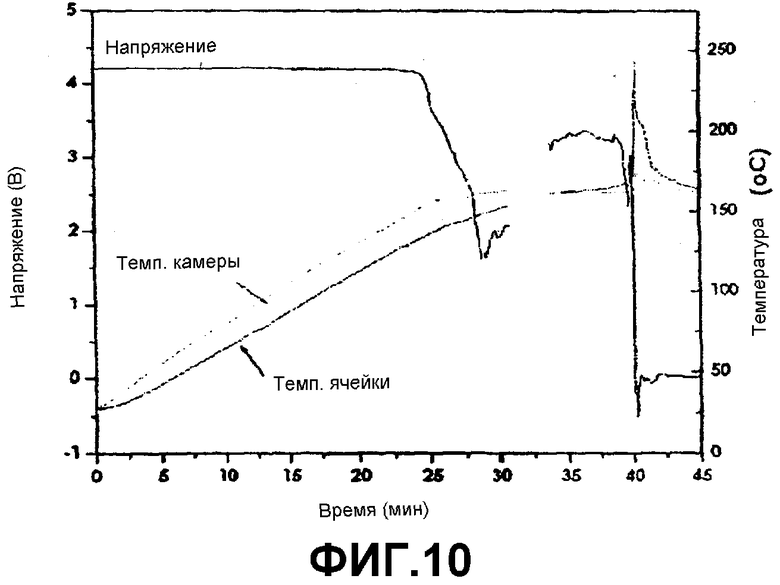
Фиг.10 представляет собой график, показывающий результаты испытания воздействием высокой температуры в 160°С для батареи, полученной в сравнительном примере 1 (напряжение, температура).
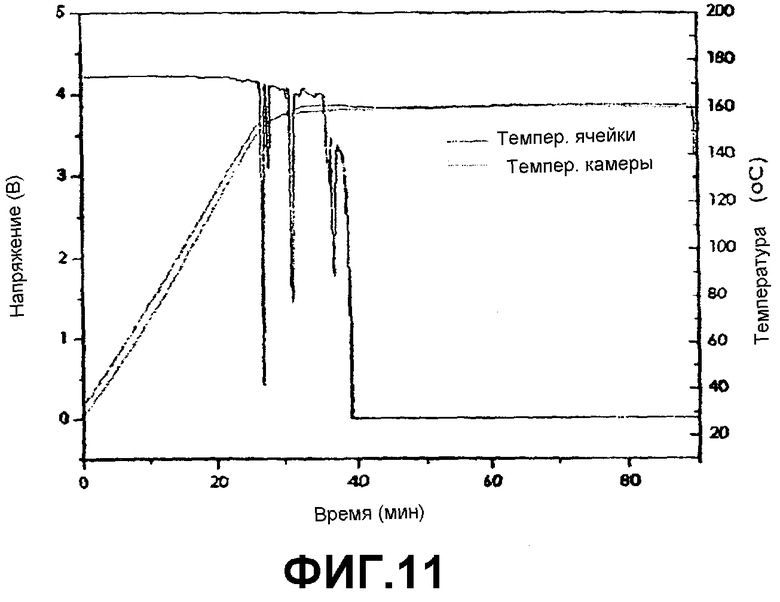
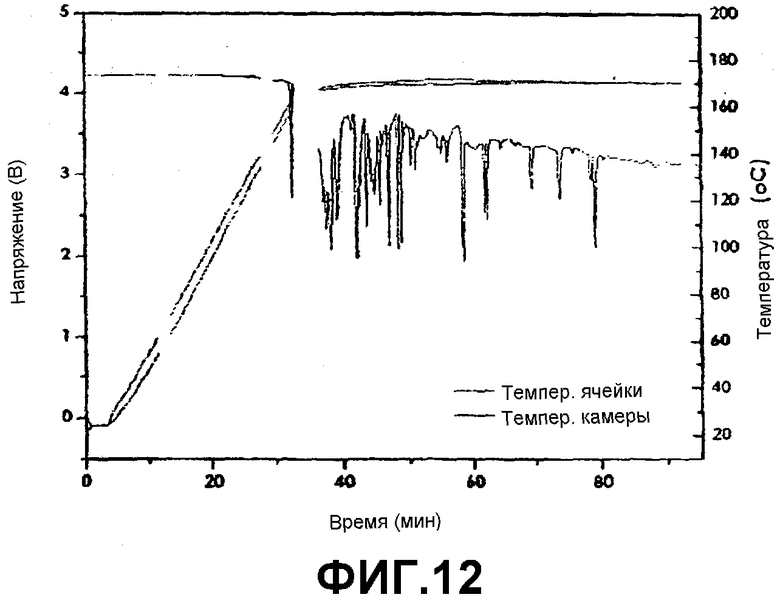
Фиг.11 и 12 представляют собой графики, показывающие результаты испытаний воздействием высокой температуры в 160°С и 170°С для батареи, полученной в примере 1 (напряжение, температура).
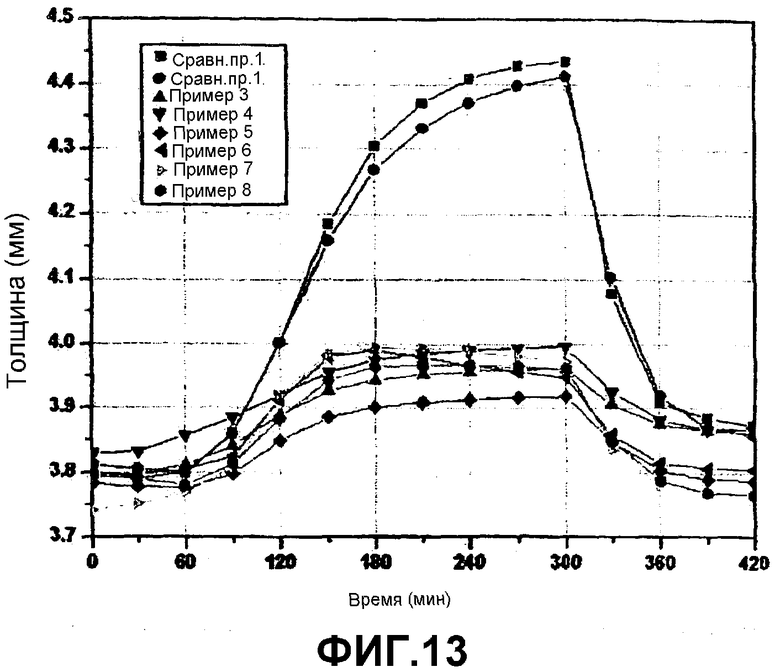
Фиг.13 представляет собой график, показывающий результаты, полученные при измерении изменения толщины батареи после того, как каждая батарея согласно примерам 3-8 и сравнительным примерам 1 и 2 была подвергнута воздействию высокой температуры 90°С в течение 4 часов.
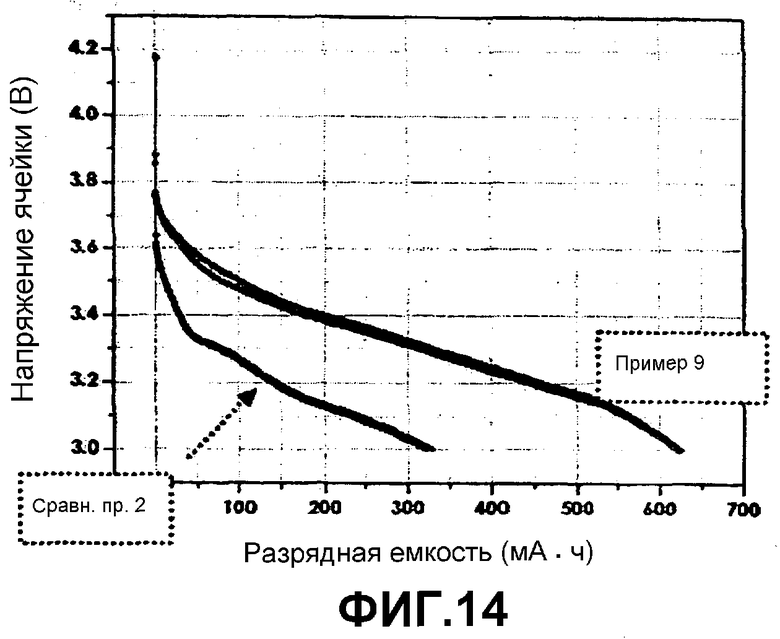
Фиг.14 представляет собой график, показывающий рабочие характеристики батарей при низкой температуре, для батареи согласно примеру 9 по сравнению с батареей согласно сравнительному примеру 2.
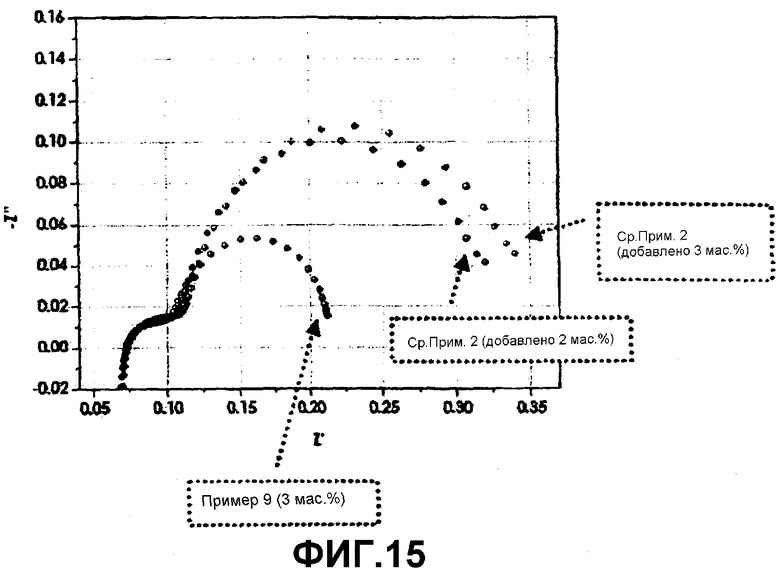
Фиг.15 представляет собой график, показывающий значения межфазного сопротивления каждой батареи согласно сравнительному примеру 2 и примеру 9 после хранения каждой батареи при высокой температуре.
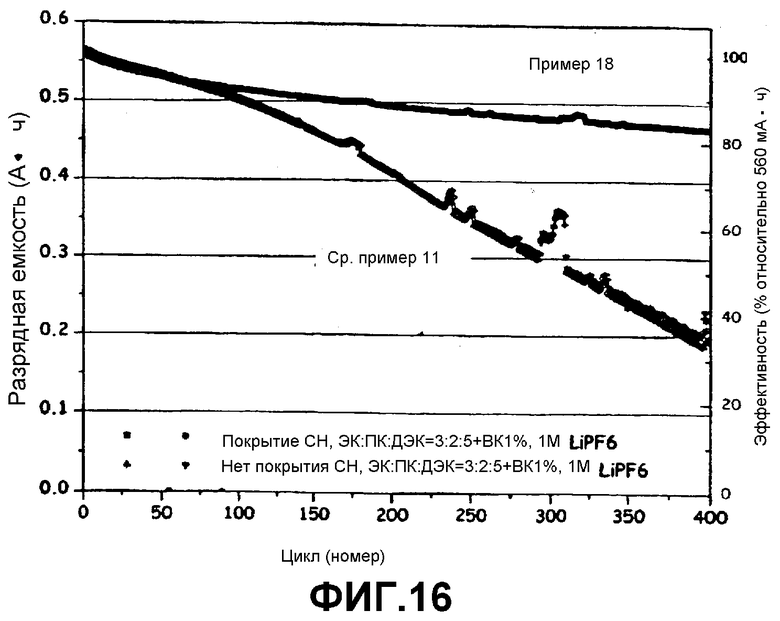
Фиг.16 представляет собой график, показывающий характеристики циклирования батарей согласно примеру 18 и сравнительному примеру 11 при 45°С.
Наилучшие варианты осуществления изобретения
Сейчас будут приведены в подробностях предпочтительные варианты осуществления настоящего изобретения. Следует понимать, что последующие примеры является лишь иллюстративными, и настоящее изобретение не ограничено ими.
[ПРИМЕРЫ]
Пример 1
Сукцинонитрил разбавляли ацетоном в качестве растворителя в массовом отношении 3:7, получая раствор, в который погружали катод. Затем катод обрабатывали при высокой температуре в 30°С в течение 2 дней для испарения растворителя, получая в результате катод, содержащий сукцинонитрил, образующий комплекс с поверхностью активного катода материала. Этим активным катодным материалом был LiCoO2. Искусственный графит использовали в качестве активного анодного материала. Использованным в данном примере электролитом был 1 М раствор LiPF6, полученный из ЭК:ПК:ДЭК=3:2:5. Литиевую полимерную батарею типа 383562 изготавливали, используя обычный способ, и батарею герметизировали алюминиевым слоистым корпусным материалом, получая батарею в герметичном корпусе. Затем батарею подвергали старению опять путем обработки при высокой температуре в 60°С в течение 12 часов или более, так чтобы весь непрореагировавший и/или оставшийся сукцинонитрил в электроде мог образовать комплекс.
Примеры 2-8
Пример 1 повторяли, получая литиевые полимерные батареи, за исключением того, что вместо сукцинонитрила (R=C2H4) использовали глутаронитрил (R=C3H6) (пример 2), адипонитрил (R=C4H8) (пример 3), пимелонитрил (R=C5H10) (пример 4), октандинитрил (R=C6H12) (пример 5), азелонитрил (R=C7H14) (пример 6), себацинонитрил (R=C8H16) (пример 7) и додекандинитрил (R=C10H20) (пример 8).
Сравнительный пример 1
Пример 1 повторяли, получая литиевую полимерную батарею, за исключением того, что катод не погружали в раствор, содержащий алифатическое нитрильное соединение.
Сравнительный пример 2
1 М раствор LiPF6, полученный из ЭК:ЭМК=1:2, использовали в качестве электролита, к которому добавляли 3 мас.% сукцинонитрила (R=C2H4). Искусственный графит и LiCoO2 использовали в качестве соответственно активного анодного материала и активного катодного материала, получая призматическую литиевую батарею типа 523450 согласно обычному способу. Затем эту батарею состаривали при высокой температуре в 60°С в течение 12 часов или более.
Пример 9
Катод погружали в раствор, содержащий сукцинонитрил (R=C2H4) в ацетоне в качестве растворителя, и затем обрабатывали при высокой температуре в 30°С в течение 2 дней с тем, чтобы испарить растворитель, получая таким образом катод, содержащий из расчета на массу электролита, 3-5 мас.% сукцинонитрила, образующего комплекс с поверхностью активного катодного материала. Активный катодный материал представлял собой LiCoO2. Электролит, используемый в данном примере, представлял собой 1 М раствор LiPF6, полученный из ЭК:ЭМК=1:2. Искусственный графит использовали в качестве активного анодного материала. Призматическую литиевую батарею типа 523450 изготовляли с использованием обычного способа. Затем батарею старили путем ее обработки при высокой температуре в 60°С в течение 12 часов или более, так чтобы весь непрореагировавший и/или оставшийся сукцинонитрил в электроде мог образовать комплекс.
Сравнительные примеры 3-10
Электролит, используемый в данных примерах, представлял собой 1 М раствор LiPF6, полученный из ЭК:ЭМК=1:2. К вышеуказанному электролиту добавляли:
сукцинонитрил (R=C2H4) (Сравнительный пример 3),
глутаронитрил (R=C3Н6) (Сравнительный пример 4),
адипонитрил (R=C4H8) (Сравнительный пример 5),
пимелинонитрил (R=С5Н10) (Сравнительный пример 6),
октанодинитрил (R=С6Н12) (Сравнительный пример 7),
азелаинонитрил (R=С7Н14) (Сравнительный пример 8),
себацинонитрил (R=С8Н16) (Сравнительный пример 9) и
додекадинитрил (R=С10Н20) (Сравнительный пример 10), каждый в количестве 3 мас.%. Искусственный графит и LiCoO2 использовали в качестве соответственно активного анодного материал и активного катодного материала. Литиевые полимерные батареи типа 383562 изготовляли с использованием обычного способа, и эти батареи герметизировали слоистым алюминиевым корпусным материалом, с получением батарей в герметичном корпусе. Затем батареи старили при высокой температуре в 60°С в течение 12 часов или более.
Примеры 10-17
Катоды погружали в растворы, каждым из которых содержал сукцинонитрил (R=C2H4) (Пример 10), глутаронитрил (R=С3Н6) (Пример 11), адипонитрил (R=С4Н8) (Пример 12), пимелонитрил (R=С5Н10) (Пример 13), октанодинитрил (R=С6Н12) (Пример 14), азелонитрил (R=С7Н14) (Пример 15), себацинонитрил (R=С8Н16) (Пример 16) и додекадинитрил (R=С10Н20) (Пример 17). Затем каждый катод подвергали высокотемпературной обработке при 30°С в течение 2 дней для испарения растворителя, получая таким образом катод, поверхность которого была покрыта 3-5 мас.% каждого алифатического нитрильного соединения (из расчета на массу электролита). Активный катодный материал представлял собой LiCoO2.
Электролит, используемый в данных примерах, представлял собой 1 М раствор LiPF6, полученный из ЭК:ЭМК=1:2. Искусственный графит использовали в качестве активного анодного материала. Литиевые полимерные батареи типа 383562 изготовляли с использованием обычного способа, и эти батареи гермитизировали слоистыми алюминиевыми корпусными материалами, с получением батарей в герметичном корпусе. Затем батареи старили при высокой температуре 60°С в течение 12 часов или более.
Пример 18
К катодной суспензии, содержащей LiCoO2 в качестве активного катодного материала, Super-p в качестве проводящего агента, гомополимер ПВДФ в качестве связующего и НМП в качестве растворителя, прибавили 5 мас.% сукцинонитрила из расчета на массу электролита (2,5 мас.% сукцинонитрила из расчета на массу активного катодного материала), а затем перемешали. Смешанную суспензию наносили на токосъемник и сушили в вакууме при примерно 100°С в течение 24 часов или более так, чтобы предотвратить испарение сукцинонитрила в наибольшей степени и удалить остаточный НМП. Далее скорость сушки (2 м/мин) и вентиляционный поток (2100 об/мин) уменьшали насколько возможно, чтобы суспензия могла быть нанесена равномерно на токосъемник. При такой процедуре получали катод, который содержит сукцинонитрил, образующий комплекс с поверхностью активного катодного материала, и однородно покрыт сукцинонитрилом.
Искусственный графит использовали в качестве активного анодного материала. 1 М раствор LiPF6, полученный из ЭК:ПК:ДЭК=3:2:5, использовали в качестве электролита, к которому добавляли 1 мас.% виниленкарбоната (ВК). Литиевую полимерную батарею типа 323456 изготовляли обычным способом, и эту батарею герметизировали слоистым алюминиевым корпусным материалом с получением батареи в герметичном корпусе. Затем батарею старили путем ее обработки снова при высокой температуре 60°С в течение 12 часов или более так, чтобы весь непрореагировавший и/или остаточный сукцинонитрил в электроде мог образовать комплекс.
Сравнительный пример 11
Пример 18 повторяли, получая литиевую полимерную батарею, за исключением того, что алифатическое нитрильное соединение к катодной суспензии не добавляли.
[Экспериментальные результаты]
1. Исследование образования лигандов на поверхности катода
Каждую батарею, полученную в Примере 1 и в Сравнительном Примере 1, полностью заряжали до 4,2 В, и каждый катод отделяли от каждой батареи для приготовления образца размером 1 см х 1 см. Кроме того, каждый образец очищали диметилкарбонатом (ДМК) для удаления примесей, остающихся на поверхности, и затем подвергали исследованию для проверки образования лигандов с использованием обычного аппарата для анализа поверхности на основе РФЭС (рентгеновской фотоэлектронной спектроскопии). Использованный входе данного исследования РФЭС - аппарат (ESCALAB 250) представляет собой аппарат, который показывает составляющие элементы, формирующие поверхность, за счет определения энергии специфической связи и кинетической энергии атомов и "считывания" атомной информации на глубину в несколько нанометров от поверхности. Образование комплекса содержащегося в электроде нитрильного соединения проверяли по пику, соответствующему образованию атомов азота. Как показано на фиг.1, атомы азота не обнаруживались на поверхности катода в случае батареи (Сравнительный пример 1), не использующей сукцинонитрила. С другой стороны, в случае батареи (Пример 1), использующей сукцинонитрил, атомы азота четко обнаруживались по наличию прочной связи, образованной между сукцинонитрилом и переходным металлом кобальтом или оксидом металл в активном катодом материале. Вышеуказанные результаты РФЭС показывают, что функциональные цианогруппы связывались с металлическим кобальтом или оксидом металла с образованием комплекса на поверхности.
Из этих результатов можно ожидать, что алифатическая нитрильная добавка может образовывать прочный комплекс с поверхностью активного катодного материала, ингибируя таким образом побочные реакции, возникающие в батарее во время повторяющихся циклов зарядки/разрядки.
2. Испытание по контролю выделения тепла
Каждую батарею, полученную в Примерах 1-8 и Сравнительном примере 1, заряжали до 4,2 В. Использовали обычный термогравиметрический анализатор - дифференциальный сканирующий калориметр (ТГ-ДСК), в котором две чашки высокого давления, устойчивые к давлению паров электролита, использовали в качестве чашек для измерений. В одну чашку вводили примерно 5-10 мг образца катода, отделенного от каждой из батарей согласно Примерам 1-8 и Сравнительному Примеру 1, в то время как вторую чашку оставляли пустой. Анализировали тепловое различие между двумя чашками при нагреве чашек со скоростью 5°С/мин до 350°С с тем, чтобы измерить те пики температуры, где происходит выделение тепла.
Как показано на фиг.2, батарея (Сравнительный пример 1), использующая электрод, не содержащий алифатического нитрильного соединения, показала пики выделения тепла при температурах примерно 200°С и 240°С. Пик при температуре примерно 200°С указывал на выделение тепла, вызванное реакцией между электролитом и катодом, в то время как пик при температуре примерно 240°С указывал на выделение тепла, вызванное объединенными факторами, включающими в себя реакцию между электролитом и катодом и структурное разрушение катода. В противоположность этому, как показано на фиг.2, 3 и 4, каждая батарея, использующая электрод, содержащий сукцинонитрил (R=С2Н4) (Пример 1), глутаронитрил (R=С3Н6) (Пример 2), адипонитрил (R=С4Н8) (Пример 3), пимелонитрил (R=С5Н10) (Пример 4), октандинитрил (R=С6Н12) (Пример 5), азелонитрил (R=С7Н14) (Пример 6), себацинонитрил (R=C8H16) (Пример 7) или додекандинитрил (R=С10Н20) (Пример 8), не демонстрировала вышеупомянутых двух температурных пиков. Это указывает на то, что в случае батарей согласно настоящему изобретению оказалось возможным ингибировать выделение тепла, вызванное реакциями между электролитом и катодом и структурным разрушением катода.
3. Испытание избыточной зарядкой
Каждую батарею, полученную в Примере 1 и в Сравнительном примере 1, испытывали в условиях избыточной зарядки (перезарядки) 6 В/1 А, 6 В/2 А, 12 В/1 С и 20 В/1 С способом ПТ/ПН (постоянный ток/постоянное напряжение). Результаты испытаний, включая изменение температуры, показаны на фиг.5-9. Как показано на фиг.5-9, батарея по Примеру 1 показывает улучшенную безопасность по сравнению с батареей по Сравнительному Примеру 1 (результаты испытаний батареи по Сравнительному Примеру 1 показаны на фиг.6 только для условий испытаний 6 В/1 А, а прочие не показаны).
В частности, как можно видеть из пиковой температуры на фиг.6 (Сравнительный пример 1), батарея воспламенилась и подверглась короткому замыканию при температуре измерения 200°С или выше из-за окисления присутствующего в батарее электролита и экзотермической реакции в результате структурного разрушения катода. С другой стороны, вторичная батарея, использующая электрод, содержащий сукцинонитрил (Пример 1), показывает пиковую температуру в примерно 100°С. Это указывает на то, что в батарее по Примеру 1 экзотермические реакции были ингибированы.
Вышеупомянутое испытание избыточной зарядкой повторяли много раз, и средние значения результатов этих испытаний показаны в следующей таблице 1.
нилась
нилась
нилась
нилась
4. Испытание в горячей камере
Каждую батарею, полученную в Примере 1 и в Сравнительном Примере 1, полностью заряжали. Заряженные батареи помещали в печь, способную к конвекции, и нагревали со скоростью 5°С/мин от комнатной температуры до 160°С и 170°С. Затем батареи выдерживали при таких высоких температурах в течение одного часа, чтобы проверить, воспламенятся они или нет.
Батарея по Сравнительному Примеру 1 воспламенилась при 160°С при нагреве со скоростью 5°С/мин (фиг.10), в то время как батарея по Примеру 1 не воспламенилась при тех же самых условиях (фиг.11 и 12).
5. Испытание рабочих характеристик батарей (1)
Каждую батарею, полученную в Примерах 1-8 и в Сравнительном Примере 1, выдерживали при высокой температуре 90°С в течение 4 часов и подвергали исследованию на вздутие, измеряя изменения в толщине батареи. Результаты исследования показаны на фиг.13. Хотя результаты, полученные для Примеров 1 и 2, на фиг.13 не показаны, батареи по Примеру 1 и 2 показали значительно уменьшенное изменение толщины по сравнению с батареей по Сравнительному Примеру 1. Как показано на фиг.13, батареи по Примерам 3-8 показали превосходную высокотемпературную устойчивость и по существу отсутствие изменений в толщине.
Изменения в толщине батареи могут обуславливаться безопасностью электролита, разложением при высокой температуре, реакцией между поверхностью катода и электролитом и т.д. Используемые в настоящем изобретении алканы, имеющие динитрильные функциональные группы, обеспечивают превосходное влияние на хранение при высоких температурах.
Поэтому, как показано на фиг.13, электроды, содержащие алифатические динитрильные соединения, обеспечивают превосходную термическую устойчивость.
6. Испытание рабочих характеристик батарей (2)
Батарею по Сравнительному Примеру 2 сравнивали с батареей по Примеру 9 с точки зрения низкотемпературных рабочих характеристик. Каждую батарею, полностью заряженную до 4,2 В, разряжали до 3 В при токе, равном 1 С (950 мА), в режиме постоянного тока (ПТ) при -10°С для того, чтобы измерить низкотемпературные рабочие характеристики. Результаты показаны на фиг.14.
Как показано на фиг.14, обе батареи показали значительное различие с точки зрения разрядной емкости при -10°С.
Как можно видеть на фиг.14, в случае батареи (Сравнительный пример 2), использующей алифатическое нитрильное соединение, добавленное к электролиту, имеется проблема в том, что эта добавка увеличивает вязкость электролита, уменьшая диффузию ионов Li, что приводит к ухудшению рабочих характеристик этой батареи. С другой стороны, в случае батареи (Пример 9), использующей катод, покрытый алифатическим нитрильным соединением, имеется преимущество в том, что безопасность батареи может быть улучшена при отсутствии ухудшения рабочих характеристик батареи за счет образования химически прочного комплекса между нитрильной функциональной группой и катодом даже в том случае, если содержание алифатического нитрильного соединения равно или больше, чем его количество, добавленное к электролиту.
Между тем, каждую батарею по Сравнительным Примерам 3-10 и Примерам 10-17, полностью заряженную до 4,2 В, разряжали до 3 В при токе, равном 1 С (750 мА), в режиме постоянного тока (ПТ) при -10°С для измерения низкотемпературных рабочих характеристик. Результаты показаны в следующей таблице 2.
(мА·ч)
(%)
Как можно видеть из таблицы 2, когда литиевые полимерные батареи типа 383562 по Сравнительным Примерам 3-10 и Примерам 10-17 испытывали на низкотемпературные рабочие характеристики батареи (Примеры 10-17), использующие катод, покрытый 3 мас.% или более алифатического нитрильного соединения, показывают превосходные рабочие характеристики по сравнению с батареями (Сравнительные Примеры 3-10), использующими 3 мас.%. алифатического нитрильного соединения в качестве добавки к электролиту, таким же образом, как и призматическими литиевыми батареями типа 523450 согласно Сравнительному Примеру 2 и Примеру 9.
Кроме того, в случае батарей по Примерам 10-17, большинство батарей показывает эффективность 83% или более независимо от типа алифатического нитрильного соединения. С другой стороны, батареи (Сравнительные Примеры 3-10), использующие алифатическое нитрильное соединение в качестве добавки к электролиту, показали различие в эффективности в интервале от 71% до 78% в зависимости от различия в физических свойствах добавки, вязкости и диффузии ионов Li.
7. Испытание рабочих характеристик батарей (3)
Каждую из батарей по Сравнительному Примеру 2 и Примеру 9 выдерживали при высокой температуре (90°С, 4 часа), а затем испытывали на межфазное сопротивление батареи (сопротивление переходного слоя на границе раздела).
Для измерения межфазного сопротивления батарею, полностью заряженную до 4,2 В, испытывали в условиях постоянного напряжения 0 В в режиме разомкнутой цепи, амплитуде переменного напряжения 5 мВ и частоте в интервале от 105 (Гц) до 10-1 (Гц). Кроме того, использовали представление по методу Найквиста, при котором Z' (реальную часть числа) и -Z'' (мнимую часть числа) откладывают соответственно на x-оси и y-оси. Результаты показаны на фиг.15.
Как видно на фиг.15, батарея по Сравнительному Примеру 2 показывает увеличение межфазного сопротивления по мере того, как возрастает содержание добавленного к электролиту алифатического нитрильного соединения. С другой стороны, батарея (Пример 9), использующая катод, покрытый 3 мас.% алифатического нитрильного соединения, полученный погружением катода в раствор покрытия, содержащий алифатическое нитрильное соединение, показывает очень низкое межфазное сопротивление.
Следовательно, возможно улучшение безопасности батареи без ухудшения ее рабочих характеристик, когда алифатическое нитрильное соединение не добавляют к электролиту, а вводят в электрод.
9. Испытание рабочих характеристик батарей (4)
Каждую батарею, полученную в Примере 18 (использующую катод, покрытый сукцинонитрилом) и в Сравнительном Примере 11 (использующую непокрытый катод), подвергли циклам зарядки/разрядки в горячей камере при 45°С при постоянном токе (1 С/1 С).
Как видно на фиг.16, имеется значительное различие между батареей (Пример 18), использующей катод, покрытый сукцинонитрилом, и батареей (Сравнительный Пример 11), использующей непокрытый катод, с точки зрения характеристик срока службы при высокой температуре. Сравнение батареи по Сравнительному Примеру 11 и батареи по Примеру 18 показывает меньшее уменьшение разрядной емкости во время повторяющихся циклов зарядки/разрядки, что обеспечивает улучшенные характеристики срока службы. С другой стороны, батарея по Сравнительному Примеру 11 показывает значительное уменьшение в разрядной емкости во время повторяющихся циклов зарядки/разрядки.
Промышленная применимость
Как можно видеть из вышеизложенного, батарея, использующая содержащий алифатическое нитрильное соединение электрод согласно настоящему изобретению, может ингибировать выделение тепла, вызванное реакцией электролита с катодом и структурным разрушением катода, и может уменьшать теплотворную способность, вызванную таким выделением тепла. Поэтому, возможно предохранить батарею от воспламенения вследствие образования внутреннего короткого замыкания цепи в результате чрезмерного выделения тепла при избыточной зарядке. Кроме того, возможно избежать ухудшения рабочих характеристик батареи, включая проблемы увеличения вязкости электролита и увеличения межфазного сопротивления, возникающие при добавлении алифатического нитрильного соединения к электролиту.
Кроме того, используемое в настоящем изобретении соединение, представленное формулой 1, не будет легко восстанавливаться во время цикла зарядки батареи и не будет легко разлагаться даже при высоком напряжении. Поэтому, возможно эффективно ингибировать структурное разрушение катода, а также улучшить безопасность и рабочие характеристики батареи благодаря электрохимической стабильности данного соединения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЭЛЕКТРОХИМИЧЕСКОЕ УСТРОЙСТВО, СОДЕРЖАЩЕЕ АЛИФАТИЧЕСКОЕ НИТРИЛЬНОЕ СОЕДИНЕНИЕ | 2005 |
|
RU2308792C1 |
| ДОБАВКИ К ЛИТИЕВОЙ ВТОРИЧНОЙ БАТАРЕЕ | 2005 |
|
RU2327260C1 |
| ФУНКЦИОНАЛЬНЫЕ ДОБАВКИ К ЭЛЕКТРОЛИТУ И ЭЛЕКТРОХИМИЧЕСКОЕ УСТРОЙСТВО, СОДЕРЖАЩЕЕ ТАКОЙ ЭЛЕКТРОЛИТ | 2006 |
|
RU2358361C1 |
| ЛИТИЕВЫЕ ВТОРИЧНЫЕ БАТАРЕИ С ПРЕДЕЛЬНЫМИ НАПРЯЖЕНИЯМИ ЗАРЯДКИ БОЛЕЕ 4,35 В | 2005 |
|
RU2325014C1 |
| ЛИТИЕВЫЙ ЭЛЕКТРОД И СОДЕРЖАЩАЯ ЕГО ЛИТИЕВАЯ АККУМУЛЯТОРНАЯ БАТАРЕЯ | 2014 |
|
RU2622108C1 |
| АКТИВНЫЙ ЭЛЕКТРОДНЫЙ МАТЕРИАЛ С ОКСИДНЫМИ СЛОЯМИ НА МНОГОЭЛЕМЕНТНОЙ ОСНОВЕ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2005 |
|
RU2333574C1 |
| ЭЛЕКТРОД С ПОВЫШЕННОЙ БЕЗОПАСНОСТЬЮ, ИЗГОТОВЛЕННЫЙ ВВЕДЕНИЕМ СШИВАЕМОГО ПОЛИМЕРА, И ЭЛЕКТРОХИМИЧЕСКОЕ УСТРОЙСТВО, СОДЕРЖАЩЕЕ ТАКОЙ ЭЛЕКТРОД | 2006 |
|
RU2358358C1 |
| ЛИТИЕВЫЙ ЭЛЕКТРОД И СОДЕРЖАЩАЯ ЕГО ЛИТИЕВАЯ АККУМУЛЯТОРНАЯ БАТАРЕЯ | 2014 |
|
RU2644006C2 |
| ЛИТИЕВЫЕ ВТОРИЧНЫЕ БАТАРЕИ С УЛУЧШЕННЫМИ БЕЗОПАСНОСТЬЮ И РАБОЧИМИ ХАРАКТЕРИСТИКАМИ | 2005 |
|
RU2321924C1 |
| ЛИТИЕВАЯ ИОННАЯ БАТАРЕЯ, ИМЕЮЩАЯ УЛУЧШЕННЫЕ СВОЙСТВА ХРАНЕНИЯ ПРИ ВЫСОКОЙ ТЕМПЕРАТУРЕ | 2004 |
|
RU2307430C1 |
Изобретение относится к литиевой вторичной батарее, а также к электроду, включающему в себя алифатическое нитрильное соединение. Алифатическое нитрильное соединение нанесено на поверхность электрода или введено в активные электродные материалы. Техническим результатом является улучшение безопасности батареи без ухудшения рабочих характеристик батареи. 2 н. и 8 з.п. ф-лы, 16 ил., 2 табл.
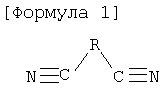
в которой R представляет собой алкан C2-C15.
| JP 62082648 А, 16.04.1987 | |||
| Катод для электрохимического восстановления | 1981 |
|
SU1006543A1 |
| US 5326658, 05.07.1994 | |||
| ПЕРЕЗАРЯЖАЕМЫЙ ПОЛОЖИТЕЛЬНЫЙ ЭЛЕКТРОД | 1995 |
|
RU2143768C1 |
Авторы
Даты
2008-04-27—Публикация
2005-02-16—Подача