Область техники, к которой относится изобретение
Настоящее изобретение относится к катоду (положительному электроду), содержащему комплекс (взаимодействие на границе раздела) между поверхностью активного катодного материала и алифатическим нитрильным соединением, а также к электрохимическому устройству, содержащему такой катод.
Уровень техники
Так как электронные устройства в последнее время становятся, в основном, беспроводными и портативными, в качестве источника питания на практике для работы таких электронных устройств применяется аккумуляторная батарея с неводным электролитом с высокой емкостью и высокой плотностью энергии. Однако существует проблема, связанная с такой перезаряжаемой аккумуляторной батареей с неводным электролитом, которая заключается в том, что ее емкость по разным указанным ниже причинам уменьшается с последовательной сменой циклов зарядки/разрядки и, в частности, когда батарея подвергается воздействию высокой температуры окружающей среды, ее емкость будет уменьшаться более заметно:
(1) переходный металл, содержащийся в смешанном оксиде, из которого состоит катод, растворяется в неводном электролите и осаждается на аноде, приводя к разрушению кристаллической структуры смешанного оксида катода или к увеличению сопротивления перехода на границе раздела;
(2) растворенный переходный металл катода продолжает нарастать, вызывая тем самым короткие микрозамыкания между катодом и анодом;
(3) переходный металл катода, осаждающийся на аноде, действует как катализатор, промотирующий разложение неводного электролита, вызывая тем самым газообразование в аккумуляторной батарее;
(4) с последовательной сменой циклов зарядки/разрядки слой SEI (промежуточной фазы твердого электролита) на аноде становится толще и препятствует миграции Li+; и
(5) увеличение (в объеме) и уплотнение активного анодного материала вызывает медленное разрушение слоя SEI.
Обычно проблема, связанная с перезаряжаемой аккумуляторной батареей с неводным электролитом, состоит в том, что эксплуатационные характеристики электрода и кпд (отношение емкости батареи при испытательном разряде к энергии, потребленной при заряде) заметно ухудшаются, особенно при высокой температуре, по следующим причинам: (1) сопротивление электрода увеличивается вследствие реакции между активным катодным материалом, таким как литийсодержащий оксид металла, способным к абсорбции и высвобождению лития и/или ионов лития, и раствором электролита, содержащим карбонатный растворитель и соль лития; и (2) вследствие непрерывных циклов зарядки/разрядки слой промежуточной фазы твердого электролита (SEI), образующийся на поверхности активного анодного материала и способный абсорбировать и высвобождать литий и/или ионы лития, медленно разрушается при высокой температуре, в то время как из карбонатного растворителя образуется недостаточный слой SEI, при этом ускоряются необратимые реакции, включая окисление (коррозию) Li.
Между тем, в перезаряжаемой аккумуляторной батарее с неводным электролитом причина проблемы безопасности аккумуляторной батареи при перезарядке заключается в следующем: активный катодный материал, такой как литийсодержащий оксид металла, способный к абсорбции и высвобождению лития и/или ионов лития, при высвобождении лития при перезарядке замещается на термически нестойкий материал. Когда температура аккумуляторной батареи достигает критической температуры, происходит разрушение кристаллической структуры активного катодного материала, который становится нестойким, с высвобождением кислорода. Высвобожденный кислород и раствор электролита и т.п. вызывают экзотермическую цепную реакцию, приводящую к тепловому пробою.
Обычно факторы, которые при перезарядке могут влиять на безопасность аккумуляторной батареи, могут включать в себя: (1) экзотермическое выделение тепла, вызванное окислением раствора электролита, и (2) экзотермическое выделение тепла, вызванное разрушением кристаллической структуры катода.
Теплота указанных экзотермических реакций, выделяющаяся во время процесса перезарядки в одной из них или в обеих, приводит к увеличению температуры внутри аккумуляторной батареи, которое ведет к воспламенению или взрыву аккумуляторной батареи, тем самым вызывая проблему безопасности аккумуляторной батареи при перезарядке.
Кроме того, явление воспламенения и взрыва перезаряжаемой литиевой аккумуляторной батареи, которое вызывается тепловым пробоем, происходит в следующих случаях: (1) в случае локальных коротких замыканий, вызванных внешними физическими воздействиями (например, воздействием высокой температуры при нагревании) в состоянии, когда перезаряжаемая литиевая аккумуляторная батарея заряжена или перезаряжена; (2) в случае, когда аккумуляторная батарея взрывается из-за экзотермического выделения тепла, вызванного реакцией между легковоспламеняющимся раствором электролита и активным катодным материалом при высокой температуре; и (3) в случае, когда воспламенение раствора электролита ускоряется кислородом, образующимся на электродах (в частности, на катоде).
Краткое описание чертежей
На фиг.1 приведены данные рентгеновской фотоэлектронной спектроскопии, указывающие на реакцию между поверхностью катода и сукцинонитрилом (SN), который является алифатическим нитрильным соединением и применяется в качестве добавки к электролиту.
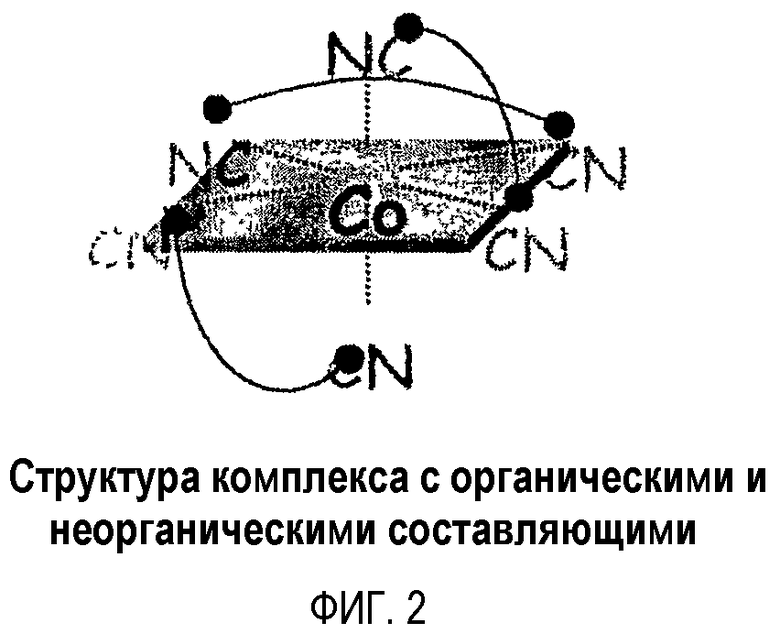
На фиг.2 представлена упрощенная схема структуры комплекса, образующегося при связывании цианогруппы алифатического нитрильного соединения с атомом кобальта катода.
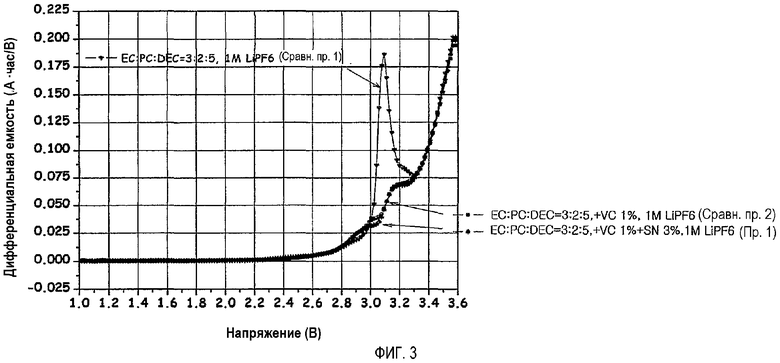
На фиг.3 показаны кривые зависимости дифференциальной емкости от напряжения (dQ/dV), полученные при исследовании необратимости и реакционной способности в отношении анода в зависимости от присутствия или отсутствия добавки VC в процессе зарядки на начальном этапе.
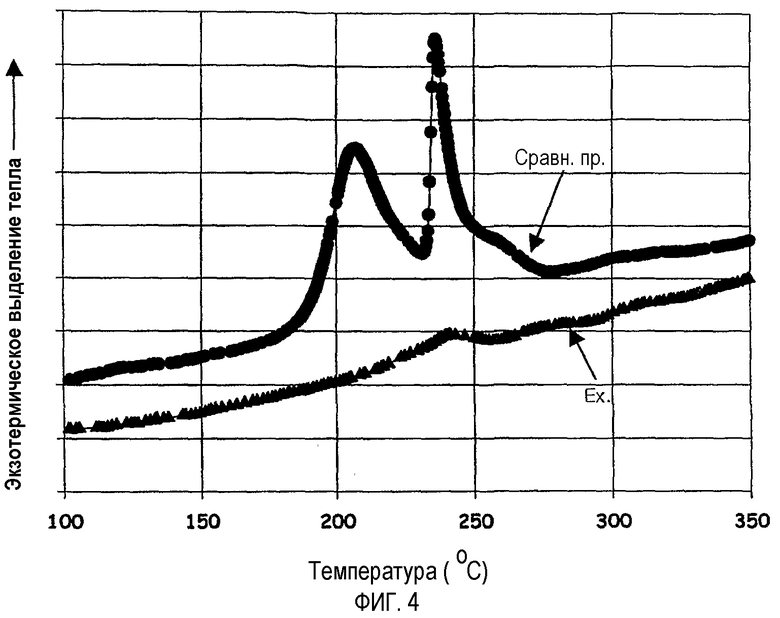
На фиг.4 графически показаны результаты анализа дифференциальной сканирующей калориметрии (ДСК), проведенной для исследования безопасности аккумуляторной батареи, содержащей алифатический динитрил (пример), и аккумуляторной батареи, содержащей неалифатический динитрил (сравнительный пример), при тепловых нагрузках.
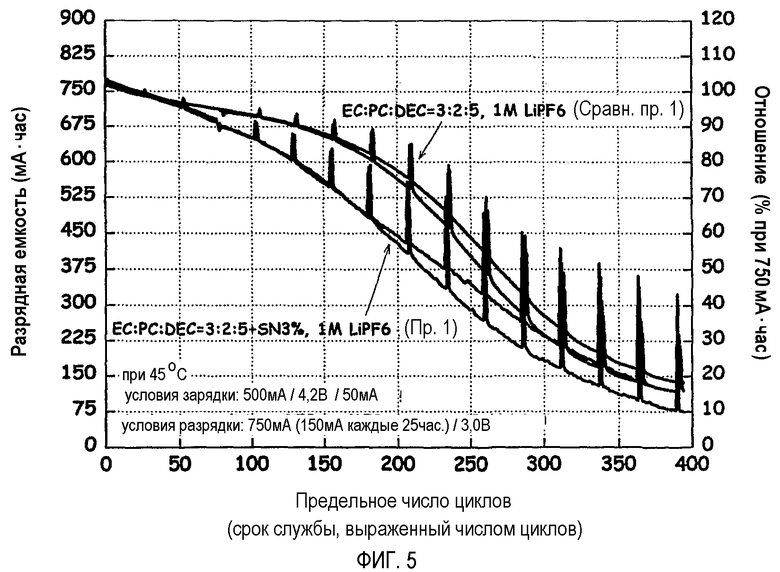
На фиг.5 графически показано сравнение при 45°C циклов аккумуляторной батареи с раствором электролита, содержащим карбонатный растворитель и 1M соль LiPF6, и аккумуляторной батареи с раствором электролита, содержащим сукцинонитрил (SN) в качестве добавки к карбонатному растворителю и 1M соль LiPF6.
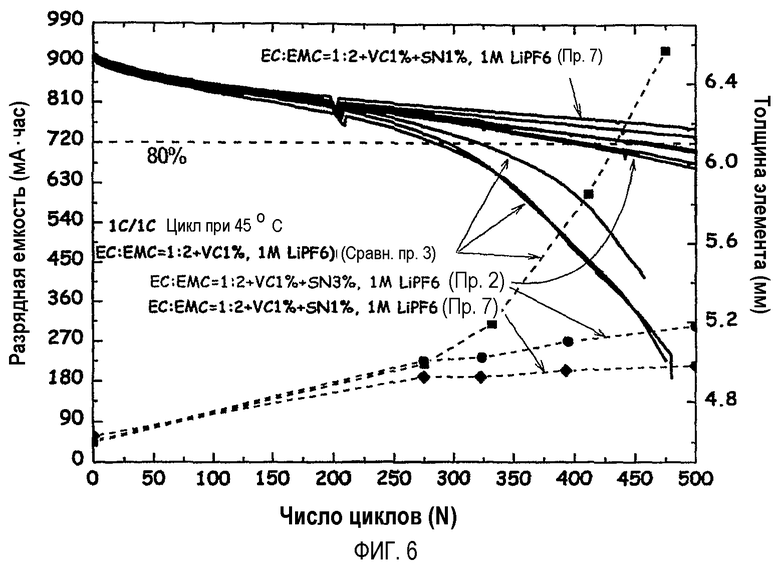
На фиг.6 графически показано сравнение при 45°C циклов аккумуляторной батареи, пассивированной с помощью добавок как VC, так и SN, и аккумуляторной батареи, пассивированной только с помощью добавки VC при отсутствии SN.
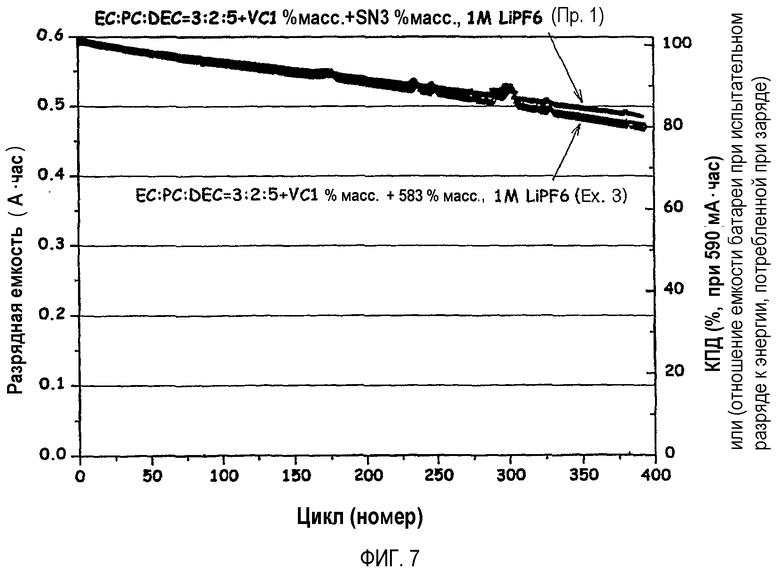
На фиг.7 графически показано сравнение при 45°C циклов аккумуляторной батареи, содержащей в качестве добавки к электролиту себацонитрил (нитрил себациновой кислоты), который является алифатическим нитрильным соединением (пример 4), и аккумуляторной батареи, содержащей в качестве добавки к электролиту SN.
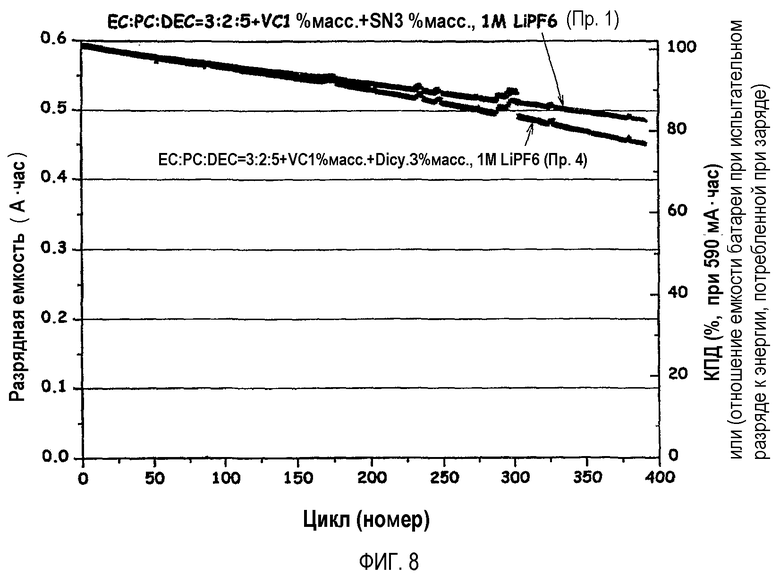
На фиг.8 графически показано сравнение при 45°C циклов аккумуляторной батареи, содержащей в качестве добавки к электролиту дицианопентан, который является алифатическим нитрильным соединением (пример 5), и аккумуляторной батареи, содержащей в качестве добавки к электролиту SN.
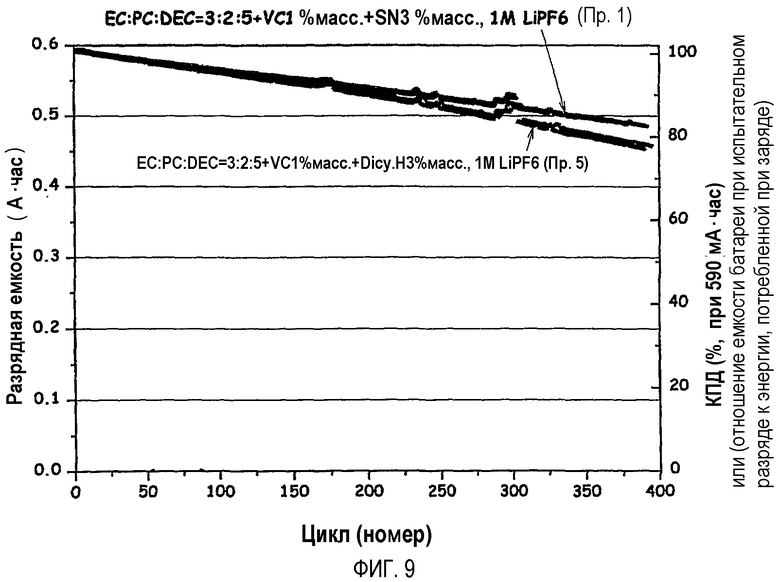
На фиг.9 графически показано сравнение при 45°C циклов аккумуляторной батареи, содержащей в качестве добавки к электролиту дицианогексан, который является алифатическим нитрильным соединением (пример 6), и аккумуляторной батареи, содержащей в качестве добавки к электролиту SN.
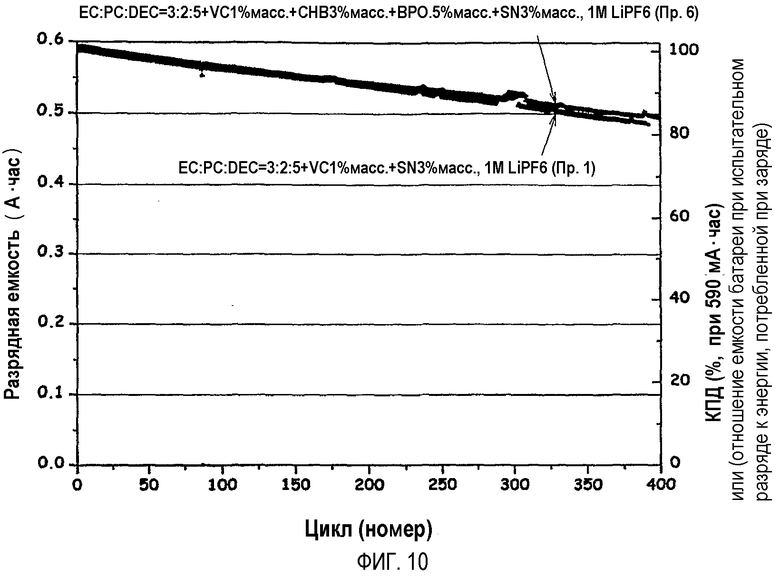
На фиг.10 графически показан цикл при 45°C аккумуляторной батареи, содержащей циклогексилбензол (CHB) и бифенил в качестве добавки, пассивирующей катод при перезарядке, вместе с SN (пример 6).
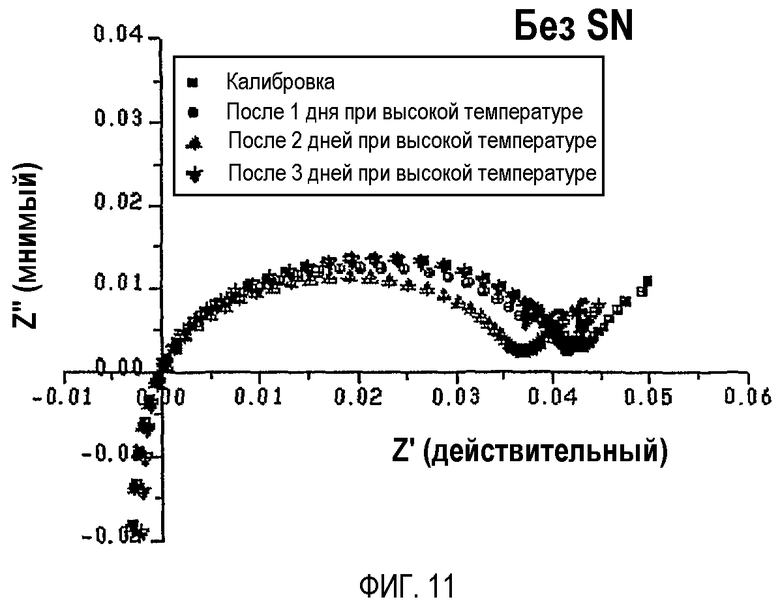
На фиг.11 графически показаны результаты EIS-испытания аккумуляторной батареи по сравнительному примеру 2, проведенного в заряженном состоянии после хранения аккумуляторной батареи в разряженном состоянии при 60°C в течение 1 дня, 2 дней и 3 дней.
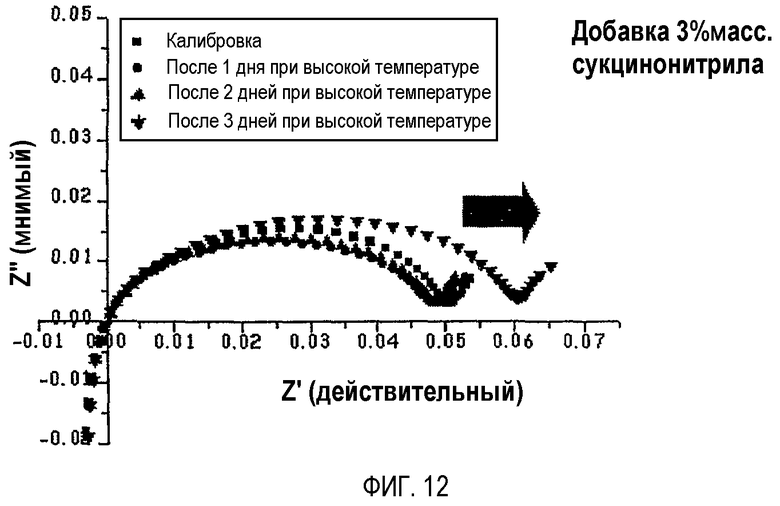
На фиг.12 графически показаны результаты EIS-испытания аккумуляторной батареи по примеру 1, проведенные в заряженном состоянии после хранения аккумуляторной батареи в разряженном состоянии при 60°C в течение 1 дня, 2 дней и 3 дней.
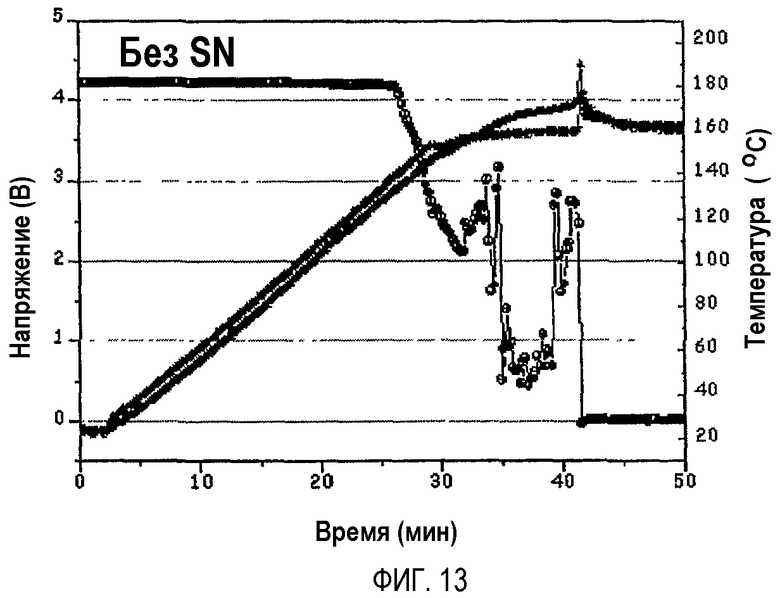
На фиг.13 графически показаны результаты испытания аккумуляторной батареи по сравнительному примеру 2 в термокамере, проведенного в полностью заряженном состоянии после хранения аккумуляторной батареи в разряженном состоянии при 60°C в течение 3 дней.
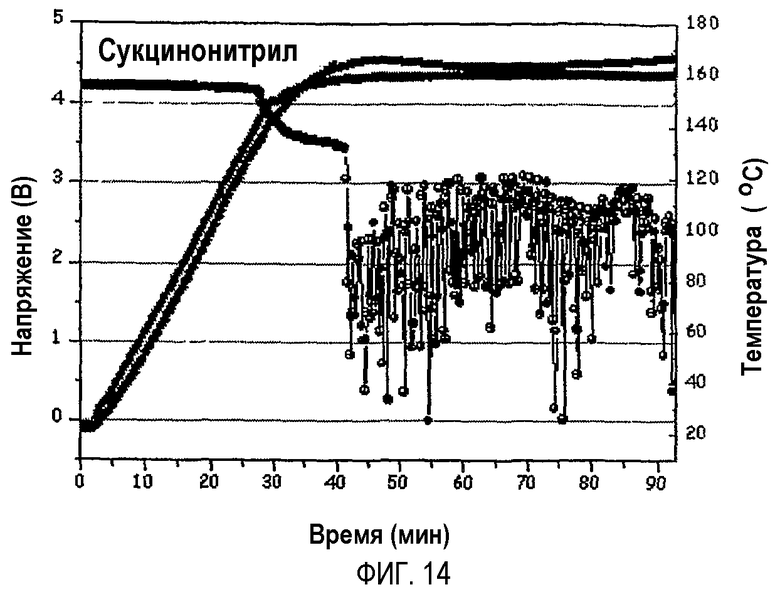
На фиг.14 графически показаны результаты испытания аккумуляторной батареи по примеру 1 в термокамере, проведенного в полностью заряженном состоянии после хранения аккумуляторной батареи в разряженном состоянии при 60°C в течение 3 дней.
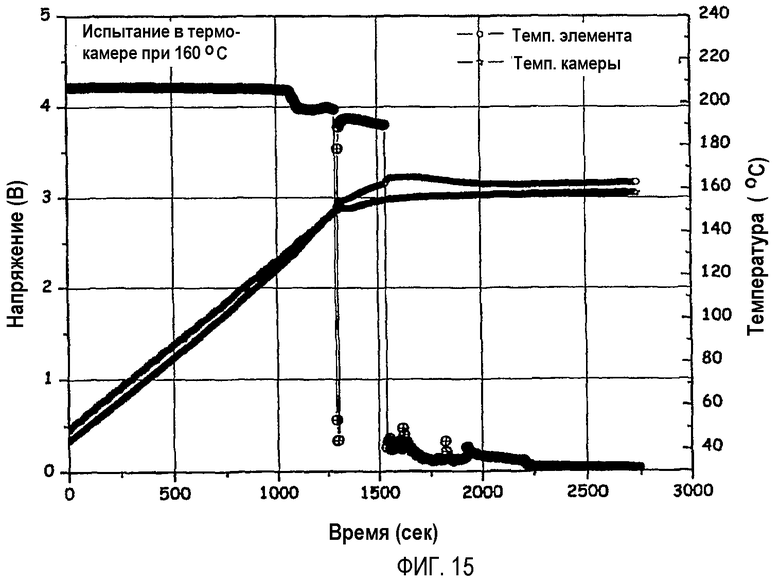
На фиг.15 графически показаны результаты испытания аккумуляторной батареи по примеру 1 или 8 в термокамере при 160°C.
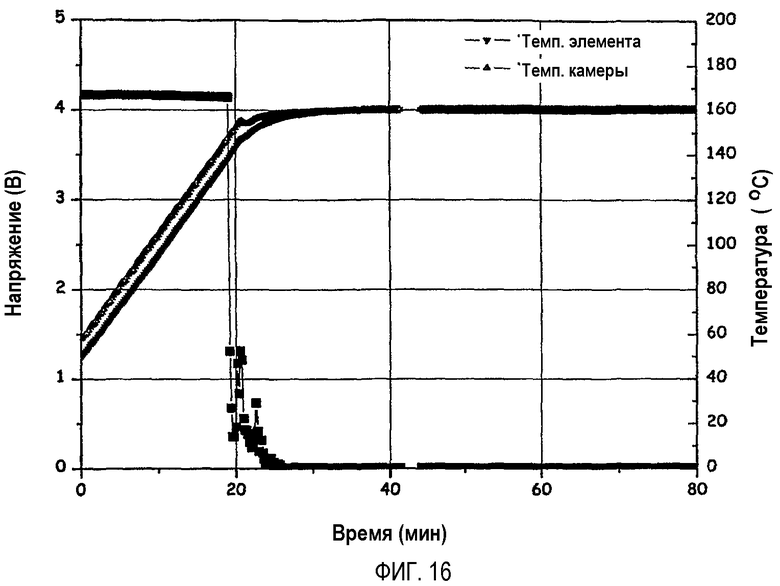
На фиг.16 графически показаны результаты испытания аккумуляторной батареи по примеру 2 или 9 в термокамере при 160°C.
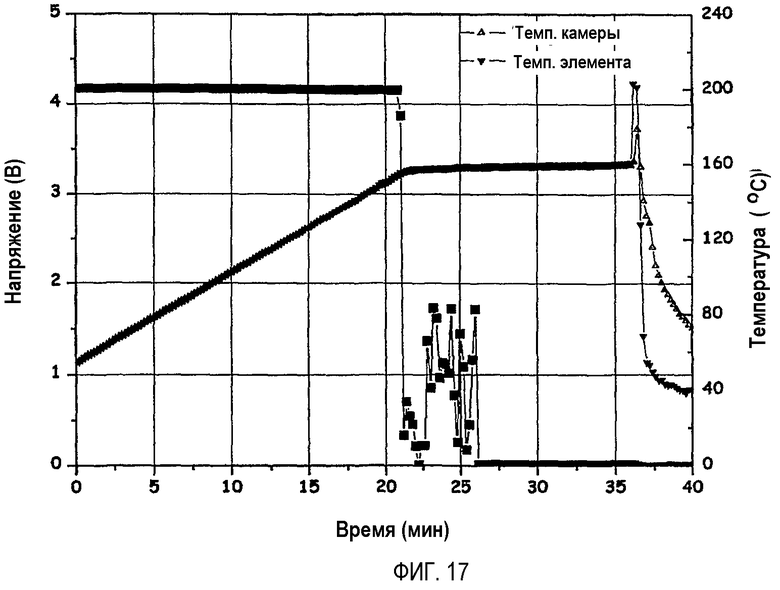
На фиг.17 графически показаны результаты испытания аккумуляторной батареи по сравнительному примеру 1 в термокамере при 160°C.
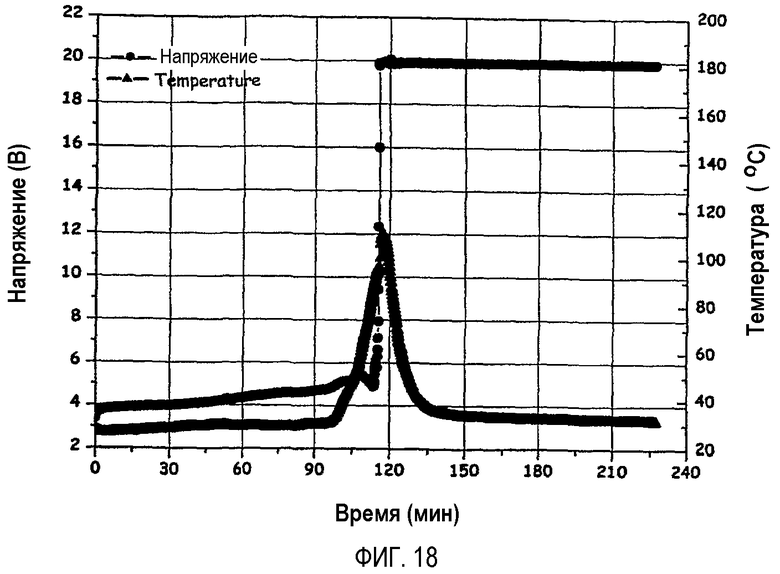
На фиг.18 графически показаны результаты испытания на перезаряд при 20В и 1С аккумуляторных батарей, изготовленных по примерам 8 и 9.
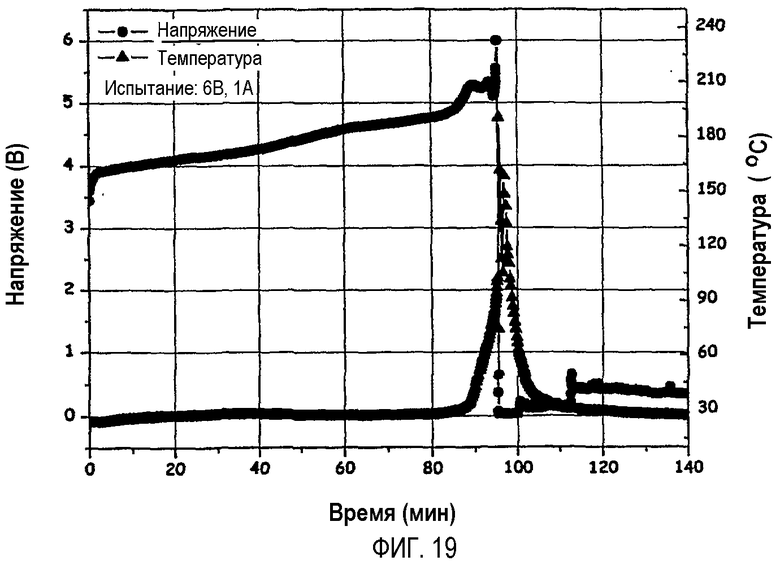
На фиг.19 графически показаны результаты испытания на перезаряд при 6В и 1A аккумуляторных батарей, изготовленных по сравнительным примерам 2 и 3.
Описание изобретения
Авторами настоящего изобретения установлено, что можно улучшить безопасность аккумуляторной батареи при перезарядке и/или физическом воздействии (например, при воздействии высокой температуры при нагревании) на внешнюю поверхность аккумуляторной батареи, если на катоде путем образования комплекса между поверхностью активного катодного материала и алифатическим нитрильным соединением, таким как сукцинонитрил, образовать защитный слой. Настоящее изобретение основано на таком открытии.
Кроме того, авторами настоящего изобретения установлено, что когда на аноде с помощью виниленкарбоната (VC), его производного или соединения простого эфира образуется пассивирующий слой, и одновременно на катоде образуется защитный слой путем образования комплекса между поверхностью активного катодного материала и алифатическим нитрильным соединением, можно улучшить высокотемпературные характеристики, определяющие срок службы аккумуляторной батареи, выраженный числом циклов, без ухудшения эксплуатационных характеристик аккумуляторной батареи, вследствие синергического эффекта, обусловленного стабильными защитными слоями на обоих электродах (аноде/катоде) во время циклов зарядки/разрядки; и также установлено, что такие защитные слои предотвращают разрушение кристаллической структуры обоих электродов и сдерживают побочную реакцию и увеличение сопротивления, обусловленное реакцией с раствором электролита, тем самым решаются различные проблемы, связанные с безопасностью (например, проблемы взрыва, воспламенения и т.д.), возникающие при воздействии на аккумуляторную батарею высокой температуры. Настоящее изобретение основано на таком открытии.
В одном из аспектов настоящее изобретение относится к катоду, на котором между поверхностью активного катодного материала и алифатическим нитрильным соединением образуется комплекс, а также к электрохимическому устройству, содержащему такой катод.
В другом аспекте настоящее изобретение относится к электрохимическому устройству, содержащему: (1) катод, на котором между поверхностью активного катодного материала и алифатическим нитрильным соединением образуется комплекс; (2) анод с пассивирующим слоем, образуемым соединением, выбранным из группы, состоящей из виниленкарбоната, его производного и соединения простого эфира; и (3) раствор электролита, содержащий соль лития и растворитель.
Ниже настоящее изобретение будет описано подробно.
В настоящем изобретении соединение, образующее комплекс на поверхности катода, представляет собой алифатическое нитрильное соединение. Примеры алифатического нитрильного соединения включают в себя соединения, представленные следующей формулой 1:
(Формула I)
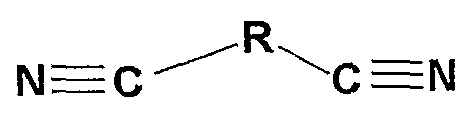
в которой R представляет собой алкановую группу, имеющую от 1 до 15 атомов углерода.
Полярные цианогруппы алифатического нитрильного соединения, обладающие высоким дипольным моментом, образуют связь с переходным металлом катода, таким как кобальт. В частности, при высокой температуре цианогруппы прочно связываются с поверхностью катода, образуя при этом комплексную структуру (или лиганд) (см. фиг.1, 2 и 12).
Данные рентгеновской фотоэлектронной спектроскопии на фиг.1 показывают, что комплекс образуется с помощью связи между атомом кобальта в оксиде металла и цианогруппой динитрильного соединения.
Образование защитного слоя на поверхности катода с помощью комплекса может не только предотвращать растворение некоторых ионов переходных металлов во время последовательной смены циклов зарядки/разрядки и их осаждение на аноде, но также ингибирует побочную реакцию и газообразование, вызванное реакцией между раствором электролита и катодом, чтобы дать возможность ионам лития хорошо абсорбироваться и высвобождаться даже при высокой температуре, предотвращая тем самым ухудшение характеристик, определяющих срок службы аккумуляторной батареи, выраженный числом циклов. В частности, алифатическое нитрильное соединение обладает тем преимуществом, что с его помощью можно обеспечивать термически стабильный электрод, так как оно более сильно защищает поверхность электрода при высокой температуре, чем при температуре окружающей среды.
Кроме того, с помощью комплекса, образуемого на поверхности катода алифатическим нитрильным соединением, можно сдерживать экзотермическое выделение тепла, вызванное реакцией между раствором электролита и катодом, и экзотермическое выделение тепла, вызванное разрушением кристаллической структуры катода, и уменьшать экзотермическое образование тепла. Тем самым можно предотвращать пожар или взрыв аккумуляторной батареи, происходящие вследствие ускорения воспламенения и образования теплового пробоя, которые вызываются кислородом, образующимся при разрушении кристаллической структуры катода при перезарядке, вследствие избыточного тепла, образующегося при внутренних коротких замыканиях или под действием высокой температуры.
Кроме того, добавки к электролиту, такие как циклогексилбензол (CHB), бифенил (BP) и анизол, которые применяются в перезаряжаемых литиевых аккумуляторных батареях, обычно используемых при 3В-4,2В, в качестве ингибиторов перезарядки, при перезарядке образуют на поверхности катода пассивирующий слой. Даже когда такие добавки применяются в сочетании с алифатическим нитрильным соединением, они независимо действуют на образование пассивирующего слоя без конкурентного взаимодействия с нитрильным соединением, так что можно сохранять эксплуатационные характеристики перезаряжаемых литиевых аккумуляторных батарей, обычно используемых при 3В-4,2В (см. фиг.10).
Между тем, поскольку алкановая группа соединения, представленного формулой 1, не обладает реакционной способностью, вероятность протекания необратимой реакции при использовании соединения формулы 1 является низкой, что приводит к уменьшению вероятности ухудшения эксплуатационных характеристик аккумуляторной батареи, вызванного использованием соединения формулы 1. В частности, среди соединений формулы 1 предпочтительным является сукцинонитрил.
Несмотря на то, что в настоящем изобретении в качестве алифатических нитрильных соединений в виде примера представлены соединения формулы 1, соединения, содержащие нитрильную группу только с одной стороны в алифатических нитрильных соединениях формулы 1, также включены в объем настоящего изобретения, поскольку они имеют высокую вероятность показывать эквивалентные соединениям формулы 1 безопасность и/или улучшение характеристик, определяющих срок службы аккумуляторной батареи, выраженный числом циклов.
Для упрощения способа изготовления аккумуляторной батареи предпочтительно, чтобы образование комплекса между поверхностью активного катодного материала и алифатическим нитрильным соединением происходило после введения алифатического нитрильного соединения в раствор электролита. Однако катод с комплексом, образованным на его поверхности, можно также получать отдельно и применять при сборке аккумуляторной батареи.
Комплекс между поверхностью активного катодного материала и алифатическим нитрильным соединением предпочтительно образуют путем погружения катода, содержащего активный катодный материал, нанесенный на коллектор, в раствор электролита, содержащий алифатическое нитрильное соединение, с последующей обработкой погруженного катода при высокой температуре. В таком случае высокотемпературную обработку обычно можно проводить либо при температуре менее 180°C, при которой активные электродные материалы и связующие вещества не оказывают воздействия друг на друга, либо при температуре менее 120°C, при которой алифатические нитрильные соединения не испаряются. Предпочтительно высокотемпературную обработку проводят при температуре 60-90°C, и в таком случае ее проводят в течение, по меньшей мере, 12 часов при 60°C и в течение, по меньшей мере, 12 часов при температуре более 80°C. Причина, по которой проводят высокотемпературную обработку, заключается в том, что цианогруппы алифатического нитрильного соединения образуют прочную комплексную структуру с металлическим кобальтом или оксидом металла, как показано на фиг.11 и 13.
Верхнее ограничение в отношении используемого количества алифатического нитрильного соединения устанавливают в зависимости от его растворимости в растворителе, используемом в неводном растворе электролита, однако использование слишком большого количества алифатического нитрильного соединения может вызвать чрезмерное увеличение вязкости раствора электролита и уменьшение ионной проводимости раствора электролита. Таким образом, алифатическое нитрильное соединение предпочтительно используют в количестве менее 20% по массе, и предпочтительно менее 5% по массе, в расчете на вес раствора электролита, принятый за 100% по массе. Нижнее ограничение в отношении используемого количества алифатического нитрильного соединения варьируется в зависимости от задачи улучшения безопасности аккумуляторной батареи согласно настоящему изобретению и предпочтительно составляет более 1% по массе.
В настоящем изобретении соединение, образующее пассивирующий слой на аноде, выбирают из группы, состоящей из винилкарбоната (VC), представленного следующей формулой 2, его производного и соединения простого эфира:
[Формула 2]
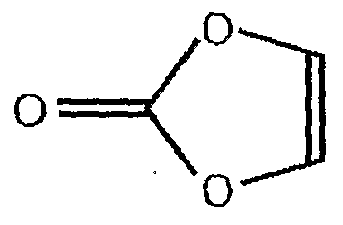
Производное соединения (VC) формулы 2 включает в себя производные, в которых неполярная боковая цепь, такая как алкильная группа, имеющая от 1 до 5 атомов углерода, связывается с кольцом формулы 2.
Примеры соединения простого эфира включают в себя простой бензилметиловый эфир, представленный следующей формулой 3, простой диметиловый эфир тетраэтиленгликоля, представленный следующей формулой 4, и т.п.:
[Формула 3]
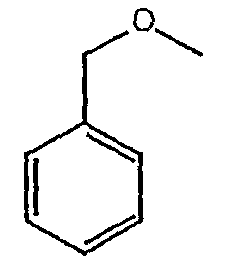
[Формула 4]
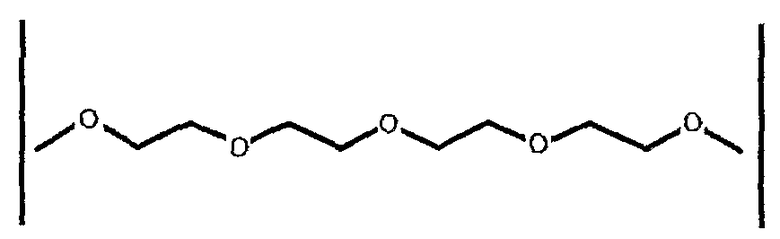
Соединение простого эфира образует пассивирующий слой на аноде подобно VC, так что появляется эффект, эквивалентный VC. Таким образом, соединение простого эфира дает синергический эффект с алифатическим нитрильным соединением (см. табл.1).
Ниже в таблице 1 приведены эксплуатационные характеристики аккумуляторной батареи при использовании добавок простого эфира наряду с добавками, пассивирующими анод.
Испытание полного элемента 323456-типа
1М LiPF6
Добавка (%)
0,5С/0,2С (мА·час)
0,5С/1,0С/1,5С
разрядка (%)
Пассивирующий слой, образуемый на поверхности анода карбонатным растворителем, является настолько недостаточным и неплотным, что это приводит к увеличению необратимых реакций во время циклов зарядки/разрядки, вызывая тем самым потерю Li и образование дендрита и приводя к значительному ухудшению эксплуатационных характеристик аккумуляторной батареи.
Соединение, пассивирующее анод, такое как виниленкарбонат (VC), его производное или соединение простого эфира, играют важную роль для улучшения характеристик, определяющих срок службы аккумуляторной батареи, выраженный числом циклов, не только путем образования массивного и плотного защитного слоя при первоначальной зарядке (обычно называемой «образование»), предотвращающего соинтеркалирование (внедрение) карбонатного растворителя в активный материал со слоистой структурой и реакцию разложения раствора электролита, что приводит к уменьшению необратимых реакций в аккумуляторной батарее, но также позволяет абсорбироваться и высвобождаться через образованный защитный слой только ионам Li+ (см. фиг.3). Однако можно видеть, что пассивирующий слой (слой SEI), образуемый таким соединением, также медленно разрушается при увеличении (в объеме) и уплотнении активного материала во время циклов зарядки/разрядки при высокой температуре, в то время как в области разрушения с помощью карбонатного растворителя образуется недостаточный слой SEI, при этом ускоряются необратимые реакции, включая окисление (коррозию) Li, и характеристики, определяющие срок службы аккумуляторной батареи, выраженный числом циклов, значительно ухудшаются с течением времени (см. фиг.6). В результате можно считать установленным, что характеристики, определяющие срок службы аккумуляторной батареи, выраженный числом циклов, нельзя улучшить только пассивированием только анода.
Между тем, когда с помощью алифатического нитрильного соединения защищается только катод, поверхность катода будет стабилизироваться путем взаимодействия между нитрильным соединением и катодом. Однако в таком случае существует проблема, состоящая в том, что недостаточный слой SEI, образуемый карбонатным растворителем, мешает равномерной миграции ионов Li+, при этом равновесие в аккумуляторной батарее нарушается и на поверхности анода осаждается металлический литий, что приводит к заметному ухудшению характеристик, определяющих срок службы аккумуляторной батареи, выраженный числом циклов, при температуре окружающей среды и при высокой температуре.
Таким образом, можно видеть, что высокотемпературные характеристики аккумуляторной батареи (эксплуатационные характеристики и отношение емкости батареи при испытательном разряде к энергии, потребленной при заряде), определяющие срок службы, выраженный числом циклов, нельзя поддерживать с помощью защиты только одного из электродов, катода или анода. Таким образом, в настоящем изобретении обеспечивается перезаряжаемая аккумуляторная батарея, в которой как катод, так и анод защищаются путем пассивирования для улучшения высокотемпературных характеристик, определяющих срок службы аккумуляторной батареи, выраженный числом циклов.
Несмотря на то, что для упрощения способа изготовления аккумуляторной батареи предпочтительно, чтобы добавки, обеспечивающие пассивирование каждого из обоих электродов, вводились в раствор электролита, пассивированные катод и анод также можно получать отдельно и применять при сборке аккумуляторной батареи.
Для того чтобы обеспечить синергический эффект между защитными слоями, защитный слой на аноде должен быть образован соединением, способным образовывать плотный (массивный) и прочный слой SEI, а катод должен быть защищен алифатическим нитрильным соединением, способным предотвращать растворение переходного металла и образовывать прочный комплекс с переходным металлом или оксидом металла.
Между тем, ароматическое динитрильное соединение разлагается при восстановлении быстрее, чем виниленкарбонат (VC), образуя при этом недостаточный слой SEI и тем самым препятствуя образованию массивного и плотного защитного слоя с помощью VC. Однако алифатическое нитрильное соединение не вызывает такой проблемы.
Когда в качестве добавки к электролиту используется соединение, пассивирующее анод, такое как виниленкарбонат (VC), его производное или соединение простого эфира, верхнее ограничение в отношении используемого количества такого соединения будет определяться независимо от вида растворителя, применяемого в неводном электролите. Однако использование чрезмерного количества такого соединения приводит при высокой температуре к образованию газа, тем самым вызывая проблему увеличения объема аккумуляторной батареи. Соответственно такое соединение предпочтительно используют в количестве менее 5% по массе из расчета на 100% по массе раствора электролита. Нижнее ограничение в отношении используемого количества такого соединения варьируется в зависимости от задачи улучшения высокотемпературных характеристик, определяющих срок службы аккумуляторной батареи, выраженный числом циклов, согласно настоящему изобретению и предпочтительно составляет более 1% по массе.
Обычно раствор неводного электролита содержит легковоспламеняющийся, неводный органический растворитель, такой как циклический карбонат, линейный карбонат или их сочетание. Примеры циклического карбоната включают в себя этиленкарбонат (EC), пропиленкарбонат (PC), гамма-бутиролактон (GBL) и т.п., а примеры линейного карбоната включают в себя диэтилкарбонат (DEC), диметилкарбонат (DMC), этилметилкарбонат (EMC) и т.п.
Раствор неводного электролита содержит соль лития. Примеры солей лития включают в себя, однако не ограничиваются перечисленным, LiClO4, LiCF3SO3, LiPF6, LiBF4, LiAsF6 и LiN(CF3SO2)2.
Типичным примером электрохимического устройства, которое можно изготовить согласно настоящему изобретению, является перезаряжаемая литиевая аккумуляторная батарея. Перезаряжаемая литиевая аккумуляторная батарея может содержать:
(1) катод, способный абсорбировать и высвобождать ионы лития;
(2) анод, способный абсорбировать и высвобождать ионы лития;
(3) пористое разделительное устройство; и
(4) раствор электролита, содержащий соль лития и растворитель для электролита.
Обычно литиевая перезаряжаемая аккумуляторная батарея в качестве активного катодного материала содержит литийсодержащий оксид переходного металла, и примером литийсодержащего оксида переходного металла является, по меньшей мере, одно соединение, выбранное из группы, состоящей из LiCoO2, LiNiO2, LiMn2О4, LiMnO2 и LiNi1-xCoxCO2, где 0<х<1. Также в качестве активного анодного материала применяют углерод, или металлический литий, или сплав. Кроме того, в качестве активного анодного материала можно применять оксид металла, такой как TiO2 или SnO2, который может абсорбировать и высвобождать ионы лития и иметь потенциал по литию менее 2В.
Внешние формы литиевой перезаряжаемой аккумуляторной батареи согласно настоящему изобретению могут включать в себя цилиндрическую форму с корпусом, призматическую форму и форму подушечки.
Способ осуществления изобретения
Далее настоящее изобретение будет описано более подробно с помощью следующих примеров. Однако следует понимать, что такие примеры даются только с иллюстративной целью и не должны рассматриваться как ограничивающие объем настоящего изобретения.
Пример 1
В качестве раствора электролита использовали 1M раствор LiPF6, имеющий состав EC:PC:DEC=3:2:5. К данному раствору электролита добавляли 1% по массе виниленкарбоната (VC) и 3% по массе сукцинонитрила (SN). Анод был изготовлен из искусственного графита, а катод был изготовлен из LiCoO2. Затем, используя полученный раствор электролита, анод и катод, традиционным способом изготавливали полимерную литиевую аккумуляторную батарею 323456-типа и запаковывали в упаковочный материал, ламинированный алюминием.
Пример 2
В качестве раствора электролита использовали 1M раствор LiPF6, имеющий состав EC:EMC=1:2. К данному раствору электролита добавляли 1% по массе VC и 3% по массе сукцинонитрила. Анод был изготовлен из искусственного графита, а катод был изготовлен из LiCoO2. Затем, используя полученный раствор электролита, анод и катод, традиционным способом изготавливали призматическую литиевую аккумуляторную батарею 423450-типа.
Примеры 3-5
Перезаряжаемые литиевые аккумуляторные батареи изготавливали по примеру 1 с той разницей, что в качестве добавки для анода к электролиту добавляли 1% по массе VC, а в качестве добавки для катода к электролиту вместо сукцинонитрила добавляли 3% по массе каждого из следующих соединений: себацонитрил (нитрил себациновой кислоты), дицианопентан и дицианогексан.
Пример 6
Перезаряжаемую полимерную литиевую аккумуляторную батарею изготавливали по примеру 1 с той разницей, что дополнительно использовали 3% по массе циклогексилбензола (CHB) и 1% по массе бифенила (BP).
Пример 7
Призматическую литиевую аккумуляторную батарею изготавливали по примеру 2 с той разницей, что добавляли 1% по массе VC, а сукцинонитрил использовали в количестве 1% по массе вместо 3% по массе.
Пример 8
Полимерную литиевую аккумуляторную батарею изготавливали по примеру 1 с той разницей, что добавляли 1% по массе VC, а сукцинонитрил использовали в количестве 5% по массе вместо 3% по массе.
Пример 9
Призматическую литиевую аккумуляторную батарею изготавливали по примеру 2 с той разницей, что добавляли 1% по массе VC, а сукцинонитрил использовали в количестве 3% по массе вместо 5% по массе.
Пример 10
Полимерную литиевую аккумуляторную батарею изготавливали по примеру 1 с той разницей, что добавляли 3% по массе сукцинонитрила, а VC к раствору электролита не добавляли.
Сравнительный пример 1
Полимерную литиевую аккумуляторную батарею изготавливали по примеру 1 с той разницей, что как VC, так и сукцинонитрил к раствору электролита не добавляли.
Сравнительный пример 2
Полимерную литиевую аккумуляторную батарею изготавливали по примеру 1 с той разницей, что добавляли 1% по массе VC, а сукцинонитрил к раствору электролита не добавляли.
Сравнительный пример 3
Призматическую литиевую аккумуляторную батарею изготавливали по примеру 2 с той разницей, что добавляли 1% по массе VC, а сукцинонитрил к раствору электролита не добавляли.
Результаты испытаний
1. Испытание по исследованию образования лиганда на поверхности катода
Каждую из аккумуляторных батарей, изготовленных по примеру 1 и по сравнительным примерам 1 и 2, полностью заряжали до 4,2В, затем из каждой выделяли катод размером приблизительно 1 см×1 см. Выделенный катод очищали диметилкарбонатом (DMC) для удаления загрязнений, остающихся на поверхности катода, и проводили испытание с помощью системы рентгеновской фотоэлектронной спектроскопии (XPS) для исследования образования лигандов на поверхности катода. Применяемая для анализа система XPS (ESCALAB 250) представляет собой систему для измерения энергии связи между атомами и кинетической энергии, дающей информацию об атомах на глубине нескольких нм от поверхности, тем самым можно проводить идентификацию составляющих компонентов поверхности. Образование лигандов изучали путем исследования полученных пиков атомов азота. Как показано на фиг.1, можно утверждать, что в аккумуляторных батареях, изготовленных при отсутствии сукцинонитрила (сравнительные примеры 1 и 2, нижний график на фиг.1), атомов азота на поверхности катода обнаружено не было, тогда как в аккумуляторной батарее, содержащей сукцинонитрил (пример 1, верхний график на фиг.1), сукцинонитрил образовывал прочную связь (в виде лиганда) с переходным металлическим кобальтом или оксидом металла, учитывая отчетливое детектирование атомов азота. На основании полученных результатов можно ожидать, что добавка алифатического нитрила будет образовывать прочный комплекс с поверхностью активного катодного материала, тем самым сдерживая различные побочные реакции в аккумуляторной батарее, связанные с последовательной сменой циклов зарядки/разрядки.
2. Испытание по исследованию образования на поверхности анода слоя SEI
Первоначальную зарядку (образование) аккумуляторных батарей, изготовленных по примеру 1 и сравнительным примерам 1 и 2, проводили при постоянном токе 0,2C в течение 50 минут. Чтобы исследовать, образуется ли слой SEI на аноде, изготовленном из искусственного графита, вследствие реакции разложения карбонатного растворителя, получали кривые зависимости дифференциальной емкости от напряжения (dQ/dV) во время процесса первоначальной зарядки, результаты приведены на фиг.3. Пики, показанные на графиках фиг.3, означают протекание необратимых реакций, вызванных реакцией разложения (т.е. реакций поглощения лития во время образования слоя SEI). Аккумуляторные батареи, изготовленные с применением раствора электролитов, содержащих VC (пример 1 и сравнительный пример 2), не показывали присутствия пиков, вызванных реакциями поглощения лития, позволяя предположить, что пассивирующий слой образуется из VC.
3. Испытания безопасности катода при высокой температуре и сдерживания экзотермического выделения тепла путем образования лиганда
Каждую из аккумуляторных батарей, изготовленных по примеру 1 и сравнительным примерам 1 и 2, полностью заряжали до 4,2В. Для измерения использовали дифференциальный сканирующий калориметр (ДСК) и две кюветы высокого давления, способные выдерживать давление пара раствора электролита. В одну кювету помещали 5-10 мг катода, выделенного из каждой аккумуляторной батареи, изготовленной по примеру 1 и сравнительным примерам 1 и 2 и заряженной до 4,2В, а другую кювету использовали в пустом виде. Для определения температуры, соответствующей экзотермическому пику, анализировали разницу между теплотами экзотермических реакций, измеренными для двух кювет, при нагревании до 400°C со скоростью 5°C/мин. Результаты представлены на фиг.4.
Как показано на фиг.4, для аккумуляторной батареи, изготовленной без сукцинонитрила (сравнительный пример 1 или 2), экзотермические пики наблюдались приблизительно при 200°C и 240°C. Пик при 200°C указывает на экзотермическое выделение тепла, вызванное реакцией между раствором электролита и катодом, а пик при 240°C указывает на экзотермическое выделение тепла, вызванное сложными факторами, включающими реакцию между раствором электролита и катодом и разрушение катода. С другой стороны, для аккумуляторной батареи, содержащей раствор неводного электролита с сукцинонитрилом (пример 1), вышеупомянутых двух температурных пиков не наблюдалось. Полученный результат позволяет предположить, что сукцинонитрил образует прочную связь с поверхностью катода, при этом сдерживается экзотермическое выделение тепла, вызванное реакцией между раствором электролита и катодом и разрушением катода.
Для аккумуляторных батарей, изготовленных по примерам 2-6, также получены графики температурной зависимости без экзотермических пиков, как для примера 1.
4. Испытания по исследованию высокотемпературных характеристик аккумуляторной батареи, определяющих срок службы, выраженный числом циклов
Аккумуляторные батареи, изготовленные по примерам 1-6 (аккумуляторные батареи, в которых как катод, так и анод пассивированы), и аккумуляторные батареи, изготовленные по сравнительным примерам 1-3 и по примеру 10 (аккумуляторные батареи, в которых либо катод, либо анод не подвергался пассивированию) подвергали циклам зарядки/разрядки при постоянном токе (1C/1C) в высокотемпературной камере при 45°C.
(1) На фиг.5 приведен выраженный числом циклов срок службы аккумуляторной батареи, изготовленной по сравнительному примеру 1 (не содержащей добавки), и аккумуляторной батареи, изготовленной по примеру 10 (содержащей только SN). Как можно видеть из фиг.5, для обеих аккумуляторных батарей наблюдалось заметное ухудшение высокотемпературных характеристик, определяющих срок службы аккумуляторной батареи, выраженный числом циклов. Ухудшение высокотемпературных характеристик, определяющих срок службы, выраженный числом циклов аккумуляторной батареи, в которой с помощью SN был защищен только катод, вызвано тем, что защитный слой, образованный на поверхности катода, действовал в аккумуляторной батарее как резистор, тем самым нарушая равновесие в аккумуляторной батарее.
(2) На фиг.6 показан срок службы, выраженный числом циклов, аккумуляторной батареи по сравнительному примеру 3 и по примерам 2 и 7. Как можно видеть из фиг.6, газообразование (побочная реакция) на катоде в аккумуляторных батареях, содержащих как VC, так и SN (примеры 2 и 7), ингибировалось по сравнению с аккумуляторной батареей, содержащей только VC (сравнительный пример 3), на что указывало уменьшение увеличения толщины аккумуляторной батареи и увеличение срока службы, выраженного числом циклов, при высокой температуре.
Как показано на фиг.6, сравнение примера 2 с примером 7 указывает на то, что когда SN используется в меньших количествах, влияние на срок службы аккумуляторной батареи, выраженный числом циклов, и на уменьшение толщины аккумуляторной батареи является более значительным. Поскольку защитный слой, образующийся между SN и поверхностью катода, действует в аккумуляторной батарее как резистор, SN предпочтительно используется в количестве менее 5% по массе.
Из фиг. 5 и 6 также видно, что высокотемпературные характеристики, определяющие срок службы аккумуляторных батарей, выраженный числом циклов, значительно отличаются для аккумуляторной батареи, в которой поверхности как анода, так и катода экранированы защитным слоем, сдерживающим побочные реакции, вызванные карбонатным растворителем электролита, и защитным слоем, сдерживающим газообразование, соответственно, и для аккумуляторной батареи, в которой пассивирован только один из электродов, анод или катод. При сравнении характеристик, определяющих срок службы аккумуляторной батареи, выраженный числом циклов, аккумуляторной батареи по сравнительному примеру 3 и аккумуляторной батареи по примеру 7, аккумуляторная батарея по сравнительному примеру 3 показывала заметное уменьшение разрядной емкости с последовательной сменой циклов зарядки/разрядки, тогда как аккумуляторная батарея по примеру 7 сохраняла ровные характеристики, определяющие срок службы аккумуляторной батареи, выраженный числом циклов.
(3) На фиг.7-9 показан 45°C цикл для каждой из аккумуляторных батарей, содержащих в качестве добавок к электролиту себацонитрил (пример 3), дицианопентан (пример 4) и дицианогексан (пример 5), соответственно, в сравнении с аккумуляторной батареей, содержащей SN. Аккумуляторные батареи по примерам 3-5 показывали превосходные характеристики в 45°C цикле, однако имело место уменьшение емкости по сравнению с аккумуляторной батареей, содержащей SN.
(4) На фиг.10 графически показан 45°C цикл аккумуляторной батареи, содержащей циклогексилбензол (CHB) и бифенил (BP), добавки, пассивирующие катод при перезарядке, в дополнение к SN (пример 6). Из результатов, приведенных на фиг.10, можно установить, что добавки, образующие пассивирующий слой на поверхности катода при перезарядке, такие как циклогексилбензол (CHB), бифенил (BP) и анизол, могут сохранять эксплуатационные характеристики перезаряжаемых литиевых аккумуляторных батарей, даже когда они применяются в растворе электролита в сочетании с алифатическим нитрильным соединением.
5. Испытание эксплуатационных характеристик аккумуляторной батареи
Каждую из аккумуляторных батарей, изготовленных по примеру 1 и сравнительному примеру 2, хранили в разряженном состоянии при 60°C в течение 1 дня, 2 дней и 3 дней и затем подвергали исследованию с помощью электрохимической импедансной спектроскопии (EIS), результаты которой представлены на фиг.12 (пример 1) и на фиг.11 (сравнительный пример 2). Как можно видеть из фиг.11 и 12, при хранении при высокой температуре SN образовывал прочный комплекс с поверхностью катода, а хранение в течение 3 дней при 60°C приводило к наибольшему увеличению в резистивной цепи, указывающему на самое высокое воздействие.
6. Испытание в термокамере
(1) Аккумуляторные батареи, изготовленные по примеру 1 и сравнительному примеру 2, хранили в разряженном состоянии при 60°C в течение 3 дней и затем полностью заряжали. Для испытания в термокамере полностью заряженные аккумуляторные батареи помещали в обычную термокамеру и нагревали от температуры окружающей среды до 160°C со скоростью 5°C/мин. Затем аккумуляторные батареи выдерживали при 160°C в течение 1 часа, чтобы проверить, воспламенятся ли аккумуляторные батареи или нет. Результаты приведены на фиг.13 (сравнительный пример 2) и на фиг.14 (пример 1).
Аккумуляторная батарея по сравнительному примеру 2 после достижения 160°C немедленно воспламенялась (см. фиг.13), тогда как аккумуляторная батарея по примеру 2 в тех же самых условиях не воспламенялась (см. фиг.14).
(2) Полностью заряжали аккумуляторные батареи, изготовленные по примерам 1, 2, 8 и 9 и сравнительному примеру 1. Для испытания в термокамере полностью заряженные аккумуляторные батареи помещали в обычную термокамеру и нагревали от температуры окружающей среды до 150°C или 160°C со скоростью 5°C/мин. Затем аккумуляторные батареи выдерживали при 150°C или 160°C в течение 1 часа, чтобы проверить, воспламенятся ли аккумуляторные батареи или нет.
Аккумуляторная батарея по сравнительному примеру 1 после достижения 160°C немедленно воспламенялась (см. фиг.17), тогда как аккумуляторные батареи по примерам 1 и 8 (фиг.15) и по примерам 2 и 9 (фиг.16) в тех же самых условиях не воспламенялись (см. фиг.14).
Результаты испытаний в термокамере суммированы ниже в табл.2.
выдержки
7. Испытание на перезаряд
(1) Для аккумуляторных батарей, изготовленных по примерам 8 и 9 и сравнительным примерам 2 и 3, испытания на перезаряд проводили в условиях 6В и 1A, 6В и 2A, 12В и 1C и 20В и 1C в режимах постоянного тока и постоянного напряжения, а полученная в результате динамика температуры показана на фиг.18 (в условиях 20В и 1C) и на фиг.19 (в условиях 6В и 1A). Как можно видеть на фиг.18 и 19, для аккумуляторных батарей по примерам 8 и 9 (фиг.18) наблюдалось улучшение безопасности при перезарядке по сравнению с аккумуляторными батареями по сравнительным примерам 2 и 3 (фиг.19). А именно на фиг.19 (сравнительные примеры 2 и 3) наблюдали температурный пик высотой более 200°C вследствие экзотермической реакции, вызванной окислением электролита в аккумуляторных батареях и разрушением кристаллической структуры катодов, в то же время аккумуляторные батареи воспламенялись и в них происходили короткие замыкания. С другой стороны, при сдерживании экзотермических реакций в аккумуляторных батареях для перезаряжаемых аккумуляторных батарей с раствором электролитов, содержащих добавку сукцинонитрила (примеры 8 и 9), температурный пик наблюдался высотой приблизительно в 100°С.
(2) Испытание на перезаряд повторяли несколько раз, и усредненные значения полученных результатов суммировали ниже в табл.3.
Промышленная применимость
Как описано выше, настоящее изобретение относится к электрохимическому устройству, содержащему катод с защитным слоем, образованным комплексом между поверхностью активного катодного материала и алифатическим нитрильным соединением. В таком электрохимическом устройстве можно сдерживать выделение тепла, вызванное реакцией между раствором электролита и катодом при нагревании, и выделение тепла, вызванное разрушением кристаллической структуры катода, и уменьшать экзотермическое выделение тепла, образующегося при указанных реакциях, тем самым предохраняя аккумуляторную батарею от воспламенения вследствие образования внутренних коротких замыканий, вызванных чрезмерным экзотермическим выделением тепла при перезарядке.
Электрохимическое устройство согласно изобретению также содержит анод с пассивирующим слоем, образованным на поверхности с помощью VC, его производных или соединений простого эфира, и катод с защитным слоем, образованным с помощью комплекса между поверхностью активного катодного материала и алифатическим нитрильным соединением. Благодаря такому электрохимическому устройству можно предотвращать ухудшение эксплуатационных характеристик аккумуляторной батареи (например, уменьшение емкости и изменение толщины, вызванное газообразованием) вследствие реакции между раствором электролита и катодом при высокотемпературном цикле (45°C) и побочных реакций, вызванных разрушением кристаллической структуры пассивирующего слоя на аноде. Благодаря такому электрохимическому устройству можно также предохранять аккумуляторную батарею от воспламенения и возгорания вследствие экзотермического выделения тепла, вызванного побочными реакциями, и одновременно вызывать синергический эффект для поддержания высокой емкости и высокого кпд (отношения емкости батареи при испытательном разряде к энергии, потребленной при заряде), тем самым улучшая характеристики аккумуляторной батареи, определяющие срок службы, выраженный числом циклов. Кроме того, такое электрохимическое устройство может быть в значительной степени безопасно при высокой температуре.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЭЛЕКТРОД ДЛЯ ЛИТИЕВОЙ ВТОРИЧНОЙ БАТАРЕИ | 2005 |
|
RU2323505C1 |
| ДОБАВКИ К ЛИТИЕВОЙ ВТОРИЧНОЙ БАТАРЕЕ | 2005 |
|
RU2327260C1 |
| ФУНКЦИОНАЛЬНЫЕ ДОБАВКИ К ЭЛЕКТРОЛИТУ И ЭЛЕКТРОХИМИЧЕСКОЕ УСТРОЙСТВО, СОДЕРЖАЩЕЕ ТАКОЙ ЭЛЕКТРОЛИТ | 2006 |
|
RU2358361C1 |
| ЛИТИЕВЫЙ ЭЛЕКТРОД И СОДЕРЖАЩАЯ ЕГО ЛИТИЕВАЯ АККУМУЛЯТОРНАЯ БАТАРЕЯ | 2014 |
|
RU2644006C2 |
| ЛИТИЕВЫЙ ЭЛЕКТРОД И СОДЕРЖАЩАЯ ЕГО ЛИТИЕВАЯ АККУМУЛЯТОРНАЯ БАТАРЕЯ | 2014 |
|
RU2622108C1 |
| ЭЛЕКТРОД С ПОВЫШЕННОЙ БЕЗОПАСНОСТЬЮ, ИЗГОТОВЛЕННЫЙ ВВЕДЕНИЕМ СШИВАЕМОГО ПОЛИМЕРА, И ЭЛЕКТРОХИМИЧЕСКОЕ УСТРОЙСТВО, СОДЕРЖАЩЕЕ ТАКОЙ ЭЛЕКТРОД | 2006 |
|
RU2358358C1 |
| ЛИТИЕВАЯ ИОННАЯ БАТАРЕЯ, ИМЕЮЩАЯ УЛУЧШЕННЫЕ СВОЙСТВА ХРАНЕНИЯ ПРИ ВЫСОКОЙ ТЕМПЕРАТУРЕ | 2004 |
|
RU2307430C1 |
| ЛИТИЕВАЯ ВТОРИЧНАЯ БАТАРЕЯ С ЭЛЕКТРОЛИТОМ, СОДЕРЖАЩИМ СОЕДИНЕНИЯ АММОНИЯ | 2006 |
|
RU2335044C1 |
| ПЕЧАТНЫЕ ЛИТИЕВЫЕ КОМПОЗИЦИИ ДЛЯ ФОРМИРОВАНИЯ ЭЛЕКТРОДОВ АККУМУЛЯТОРНЫХ БАТАРЕЙ | 2019 |
|
RU2799803C2 |
| УДЕРЖИВАТЕЛЬ ЭЛЕКТРОЛИТА ДЛЯ ЛИТИЕВОЙ АККУМУЛЯТОРНОЙ БАТАРЕИ И ЛИТИЕВАЯ АККУМУЛЯТОРНАЯ БАТАРЕЯ | 2012 |
|
RU2593596C2 |
Изобретение относится к катоду, имеющему комплекс между поверхностью активного катодного материала и алифатическим нитрильным соединением, а также к электрохимическому устройству, содержащему такой катод. Согласно изобретению, электрохимическое устройство содержит: катод, имеющий комплекс между поверхностью активного катодного материала и алифатическим нитрильным соединением; анод, имеющий пассивирующий слой, образованный соединением, выбранным из группы, состоящей из виниленкарбоната, его производного и соединения простого эфира; и раствор электролита, содержащий соль лития и растворитель. Техническим результатом является улучшение безопасности аккумуляторной батареи при переразрядке и/или физическом воздействии на внешнюю поверхность аккумуляторной батареи. 2 н. и 10 з.п. ф-лы, 19 ил., 3 табл.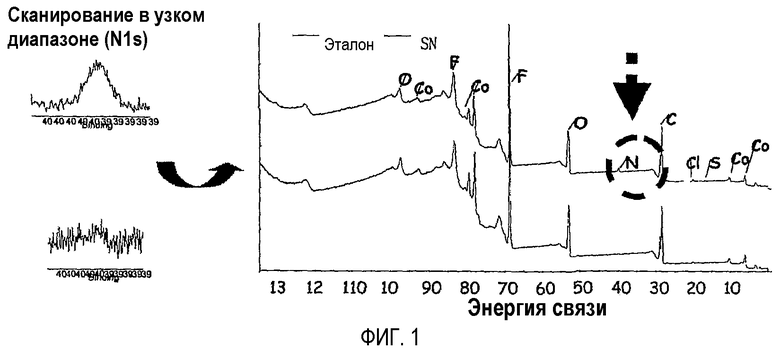
(Формула 1)
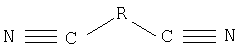
где R представляет собой алкановую группу, имеющую от 1 до 15 атомов углерода.
(Формула 2)
| JP 62082648 А, 16.04.1987 | |||
| Катод для электрохимического восстановления | 1981 |
|
SU1006543A1 |
| US 2004002002 А, 01.01.2004 | |||
| ПЕРЕЗАРЯЖАЕМЫЙ ПОЛОЖИТЕЛЬНЫЙ ЭЛЕКТРОД | 1995 |
|
RU2143768C1 |
Авторы
Даты
2007-10-20—Публикация
2005-01-14—Подача