Изобретение относится к медицинской и молекулярной генетике, а именно к генетическим конструкциям, продуцирующим siPHK, являющиеся ингибиторами репродукции вируса иммунодефицита человека (ВИЧ) 1 типа, и может быть использовано в медицине и научных исследованиях.
В настоящее время основным подходом лечения ВИЧ-инфекции является назначение пациентам противовирусной химиотерапии, включающей препараты, действующие на ключевые ферменты ВИЧ-1 - обратную транскриптазу, интегразу, протеазу. Наиболее эффективными из известных соединений являются 3'-азидо-3'-дезокситимидин (азидотимидин или AZT, зидовудин, «Ретровир», «Тимазид»), находящий применение в медицинской практике (Mitsuya, H.; Broder, S. Inhivition of the in vitro infectivity and cytiopathic effect of human T-lymphotropic virus type III/lymphoadenopathy-associated virus/HTLV-III(LAV) by 2',3'-dideoxynucleosides. Proc. Nat. Acad. Sci. USA, 1986, 83, 1911-1915), а также 2',3'-дидезоксицитидин (ddC, зальцитабин, «Гивид»), 2',3'-дидезоксиинозин (ddI, диданозин, «Видекс»), 3'-дезокси-2',3'-дидегидротимидин (d4T, ставудин, «Зерит») и 3'-тиоцитидин (ЗТС, ламивудин, «Эпивир»).
Однако, несмотря на большое количество разработанных анти-ВИЧ препаратов, существует проблема эффективности применяемой противовирусной терапии. Основная причина, объясняющая неэффективность лечения - адаптивный мутагенез вируса, приводящий к появлению вариантов ВИЧ-1, обладающих устойчивостью к противовирусным препаратам. Серьезными проблемами являются также токсичность и высокая стоимость применяемых лекарственных средств.
Известно применение рибозимов и антисмысловых РНК для терапии ВИЧ-инфекции [Dorman N. And Lever A.M. (2001) RNA-based gene therapy for HIV infection. HIV Med., 2, 114-122; Michienzi A., Conti L., Varano В., Prislei S., Gessani S., and Bozzoni I. (1998) Inhibition of human immunodeficiency virus type 1 replication by nuclear chimeric anti-HIVribozymes in a human Т lymphoblastoid cell line. Hum. Gene Ther., 9., 621-628; Veres G., Junker U., Baker J., Barske C., Kalfoglou C., Ilves H., Escaich S., Kaneshima H., and Bohnlein E. (1998) Comparative analisis of intracellularly expressed antisense RNAs as inhibitors of human immunodeficiency virus type 1 replication. J. Virol., 72, 1894-1901.], которые блокируют несколько генов ВИЧ, что снижает его активность.
Наиболее близким к заявленному техническому решению являются генетические конструкции, обеспечивающие экспрессию siPHK внутри ВИЧ-инфицированных клеток организма (Заявка на патент США № 20030059944, МПК С12N 15/867, опубл. 27.03.2003 г.).
Однако оценка действия интерферирующих РНК, продуцируемых в данных опубликованных генетических конструкциях, проводилась с использованием молекулярных клонов вируса иммунодефицита человека, что не позволяет прогнозировать их влияние на естественный пул вирусной популяции, заведомо обладающей генетическим разнообразием, что не допускает проведение более объективной оценки противовирусной эффективности таких генетических конструкций.
Техническим результатом предлагаемого изобретения является разработка более эффективных анти-ВИЧ препаратов на основе интерферирующих РНК (siPHK), продуцируемых в клетках с помощью введенных векторных экспрессирующих конструкций, содержащих палиндромы, предназначенные для образования "шпилек РНК" и отобранных с использованием вирусной модели - культуры клеток человека, инфицированных различными штаммами ВИЧ-1.
Поставленный технический результат достигается путем создания трех вариантов плазмидных конструкций, продуцирующих соответствующие участкам генов gag, pol и tat ВИЧ-1:
- генетическая конструкция на основе векторной плазмиды pEGFP-N1, продуцирующая siPHK-ингибиторы репродукции вируса иммунодефицита человека 1 типа, содержащая фрагмент генома ВИЧ-1: pr-hp-pEGFP-N1 с областью длиной 19 bp из консервативного района домена протеазы (1749...1767): 5' gaattccTGATTCAGATTGGTTGTACttttttGTACAACCAATCTGAATCAaccccggatcc 3'.
- генетическая конструкция на основе векторной плазмиды pEGFP-N1, продуцирующая siPHK-ингибиторы репродукции вируса иммунодефицита человека 1 типа, содержащая фрагмент генома ВИЧ-1 tat-hp-pEGFP-N1 с областью длиной 19 bp из консервативного района домена обратной транскриптазы (2116...2134):
5' gaattccTGCATATTTTTCAGTTCCCttttttGGGAACTGAAAAATATGCAtccccggatcc 3'.
- генетическая конструкция на основе векторной плазмиды pEGFP-N1, продуцирующая siPHK-ингибиторы репродукции вируса иммунодефицита человека 1 типа, содержащая фрагмент генома ВИЧ-1 RT-hp-pEGFP-N1 с областью длиной 19 bp из консервативного района tat-домена (5325...5343):
5' gaattccAGTAGGACTAATAGTAGCAttttttTGCTACTATTAGTCCTACTatccccggatcc 3',
где (во всех трех вариантах): строчными буквами показаны области, содержащие искусственные сайты рестрикции для рестриктаз EcoRI (на 5'-концах) и BamHI (на 3'-концах), а также петли, разделяющие области, способные образовать двуспиральный дуплекс с петлей, причем, области, соответствующие смысловой цепи РНК вируса, показаны в строке слева, а антисмысловой - справа.
Приведенные генетические конструкции обеспечивают целенаправленное воздействие на мРНК вируса иммунодефицита человека первого типа (ВИЧ-1) в клетках человека вирусспецифическими интерферирующими РНК (siPHK), продуцирующимися в клетках. Терапевтическим результатом такого воздействия является подавление репродукции ВИЧ-1 в клетках человека.
Для вируса иммунодефицита человека первого типа характерно быстрое возникновение и отбор мутантных вариантов, обладающих резистентностью к различным противовирусным препаратам. Для решения проблемы вирусной изменчивости разработано три генетических конструкции, стабильно экспрессирующие несколько siPHK. Затем для оценки эффективности действия используют вирусную модель - культуру клеток человека, инфицированную различными штаммами ВИЧ-1, в частности, штаммами, репродуцирующимися по типу острой и хронической инфекции. Такой подход позволяет проводить исследования, приближенные к реальным процессам развития ВИЧ-инфекции в организме. Применение лабораторных штаммов ВИЧ-1 (в отличие от молекулярных клонов вируса в прототипе) дает возможность оценивать влияние интерферирующих РНК на естественный пул вирусной популяции, заведомо обладающий генетическим разнообразием. Это также допускает проведение более объективной оценки противовирусной эффективности генетических конструкций.
На чертеже приведена физическая карта векторной плазмиды pEGFP-N1.
Пример 1. Описание генетических конструкций (три варианта) и способа их получения Плазмида pEGFP-N1 зарегистрирована GenBank Accession #U55762, номер по каталогу 6085-1, CLONOTECH Laboratories, Inc. (Prasher, D. С., et al. (1992) Primary structure of the Aequorea victoria green fluorescent protein. Gene 111: 229-233), имеет размер 4,7 т.п.о. и характеризующаяся тем, что содержит:
1. Ранний промотор цитомегаловируса человека (PCMV IE): 1-589
Энхансерный район: 59-465
ТАТА box: 554-560
Сайг начала транскрипции: 583
C->G мутацию, удаляющую сайт Sac I: 569
2. Сайты множественного клонирования (MSC). На последовательности отмечены участки узнавания для эндонуклеаз рестрикции, по которым проводилось встраивание ВИЧ-специфических фрагментов ДНК:

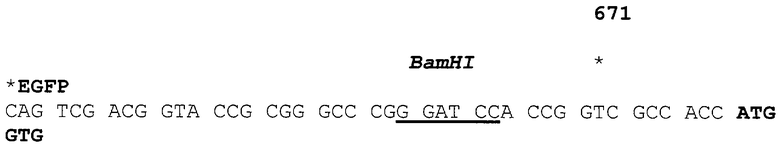
3. Ген EGFP (1-3), позволяющий осуществлять контроль введения векторных конструкций в клетки эукариот и проводить оптимизацию трансфекции (EGFP):
Участок последовательности Kozak (сайг инициации трансляции): 672-682
Старт кодон (ATG): 679-681; Стоп кодон: 1396-1398
Инсерция Val в позиции 2: 682-684
Мутации в гене GFPmutl (Phe-64 to Leu; Ser-65 to Thr): 871-876
His-231 to Leu mutation (A⊘T): 1373
4. Фрагмент SV40 сигнала полиаденилирования mRNA (SV40 poly A):
Сигнал полиаденилирования: 1552-1557 & 1581-1586
mRNA 3' конец: 1590 & 1602
5. Ориджин одноцепочечной ДНК фага f1 (f1 ori): 1649-2104
(пакуется некодирующая цепь EGFP)
6. Бактериальный промотор для экспрессии гена устойчивости к канамицину Kanr (Р):
- 35 район: 2166-2171; - 10 район: 2189-2194
Точка начала транскрипции: 2201
7. Ориджин репликации SV40 (SV40 ori): 2445-2580
8. Ранний промотор SV40 (PSV40e)
Энхансер (тандемный повтор 72-п.о.): 2278-2349 & 2350-2421
Повтор 21-п.о.: 2425-2445, 2446-2466, & 2468-2488
Элемент раннего промотора: 2501-2507
Основная точка начала транскрипции: 2497, 2535, 2541 & 2546
9. Ген устойчивости к канамицину/неомицину (Kanr/Neor):
Последовательность, кодирующая неомицинфосфотрансферазу:
Старт кодон (ATG): 2629-2631; стоп кодон: 3421-3423
G->A мутация, удаляющая сайт Pst 1: 2811
С->А (Arg to Ser) мутация, удаляющая сайт BssH II: 3157
10. Сигнал полиаденилирования тимидинкиназы (ТК) вируса простого герпеса (HSV ТК poly А): Сигнал полиаденилирования: 3659-3664 & 3672-3677
11. Ориджин репликации плазмиды pUC (pUC ori): 4008-4651
12. Праймеры для секвенирования
EGFP-N: 745-724
EGFP-C: 1332-1353
Векторная плазмида pEGFP-N1 кодирует ген GFP, позволяющий осуществлять контроль введения векторных конструкций в клетки эукариот по появлению в клетках флюоресцентного свечения и проводить оптимизацию трансфекини. Набор уникальных сайтов узнавания для эндонуклеаз рестрикции (MSC), расположенный между ранним промотором цитомегаловпруса человека (CMV) и HGFP кодирующей последовательностью позволяет проводить встраивание и получать экспрессию различных генов. Вектор содержит ориджин SV40, обеспечивающий репликацию в клетках млекопитающих. Кассета устойчивости к неомицину (neor), состоящая из раннего промотора SV40, гена устойчивости к канамицину/неомицину (Kanr/Neor) и сигнала полиаденилирования гена тимидинкиназы вируса простого герпеса позволяет стабильно трансфецировать клетки эукариот, используя селективное давление G418. Бактериальный промотор, расположенный рядом, обеспечивает устойчивость к канамицину клеток Е. Coli. pEGFP-N1 содержит также ориджин репликации pUC19, позволяющий проводить наработку векторной плазмиды на бактериальной культуре Е. coli и ориджин репликации фага 1 для получения одноцепочечных молекул ДНК.
Экспрессирующие "шпилечные" конструкции содержат фрагменты генома ВИЧ-1: pr-hp-pEGFP-N1, tat-hp-pEGFP-N1, RT-hp-pEGFP-N1. С помощью программы BLAST были выбраны наиболее консервативные области генома HIV-1, соответствующие функционально важным областям вируса - доменам протеазы, обратной транскриптазы и tat в последовательности AF316544 (HIV-1 подтип А). Мишенями конструкций, кодирующих siPHK, были данные области. Первая конструкция содержит область длиной 19 bp из консервативного района домена протеазы (1749...1767):
5' gaattccTGATTCAGATTGGTTGTACttttttGTACAACCAATCTGAATCAaccccggatcc 3'.
Вторая - область длиной 19 bp из консервативного района домена обратной транскриптазы (2116...2134):
5' gaattccTGCATATTTTTCAGTTCCCttttttGGGAACTGAAAAATATGCAtccccggatcc 3'.
Третья - область длиной 19 bp из консервативного района tat-домена (5325...5343):
5' gaattccAGTAGGACTAATAGTAGCAttttttTGCTACTATTAGTCCTACTatccccggatcc 3'. В вышеуказанных нуклеотидных текстах строчными буквами показаны области, содержащие искусственные сайты рестрикции для рестриктаз EcoRI (на 5'-концах) и BamHI (на 3'-концах), а также петли, разделяющие области, способные образовать двуспиральный дуплекс с петлей ("шпилька" дсРНК). Области, соответствующие смысловой цепи РНК вируса, показаны в строке слева, а антисмысловой - справа. Двуспиральные ДНК, соответствующие указанным текстам, были клонированы в EcoRI-BamHI-сайты вектора pEGFP-N1.
Пример 2. Подавление репродукции вируса иммунодефицита человека в культуре клеток МТ-4, трансфецированных различными вариантами плазмид, экспрессирующих вирусспецифичные короткие интерферирующие РНК.
Исследования проводят на перевиваемой линии лимфоидных клеток МТ-4. Клетки культивируют на среде RPMI-1640 с добавлением 10% фетальной сыворотки КРС, предварительно инактивированной прогреванием при 56°С в течение 30 минут, 300 мг/мл L-глютамина и 100 мкг/мл гентамицина.
Наработку и выделение ДНК плазмид проводят с помощью ацетата аммония согласно разработанной методике по подготовке ДНК для трансфекции клеток млекопитающих [Saporito-Irwin S.M., Geist R.T. and Gutmann D.H. (1997) Ammonium Acetate Protocol for the preparation of plasmid DNA Sutable for Mammalian Cell Transfections. BioTechniques 23(3), 424-427.]
Введение экспрессирующих плазмид в клетки осуществляют с помощью трансфекции. Трансфекцию проводят с использованием липофектамина (LipofectamineТМ 2000, Invitrogen). На третьи сутки культивирования клетки МТ-4 отмывают в минимальной среде (ДМЕМ без фенолового красного) и разводят до концентрации 0,5×106 кл/мл. 5 мкг плазмидной ДНК разводят в 50 мкл минимальной среды, выдерживают 5 мин при комнатной температуре и смешивают с 3 мкл липофектамина, разведенного в 50 мкл минимальной среды. Смесь инкубируют 20 мин при комнатной температуре. 100 мкл раствора ДНК/липофектамин добавляют к 500 мкл клеток МТ-4. Клетки культивируют в 24-луночном планшете. Клетки инкубируют 5 часов при 37°С в СО2-инкубаторе. Затем добавляют 500 мкл ростовой среды, содержащей 20% фетальную сыворотку КРС. Эффективность трансфекции составляет около 30%. Эффективность оценивают регистрацией появления зеленой флюоресценции с использованием флюоресцентного микроскопа "Olimpus". Клетки МТ-4, трансфецированные различными вариантами плазмид, инфицируют штаммом ВИЧ-1/ГКВ-4046 через 24 и 72 часа. Для заражения используют супернатант инфицированных штаммом ГКВ-4046 ВИЧ-1 клеток со множественностью заражения 2-5×10-1 и 2-5×10-2 инфекционных единиц на клетку. Планшет инкубируют при 37°С четверо суток в атмосфере 5% СО2. Ежедневно отбирают пробы для количественного определения вирусспецифического белка р24 методом прямого иммуноферментного анализа. Концентрацию и жизнеспособность клеток оценивают методом исключения трипанового синего.
Влияние введения в клетки экспрессирующих векторных конструкций на репродукцию ВИЧ-1 оценивают по накоплению вирусспецифического антигена р24 через 24, 48 и 72 часа. Результаты приведены в таблицах 1-4.
1 - клетки МТ-4;
2 - клетки МТ-4, трансфецированные плазмидой RT-hp-pEGFP-NI;
3 - клетки МТ-4, трансфецированные плазмидой tat-hp-pEGFP-NI;
4 - клетки МТ-4, трансфецированные плазмидой pr-hp-pEGEP-NI.
5 - клетки МТ-4, трансфецированные плазмидой RT-hp-pEGFP-NI (инфицирование клеток проводили через 72 часа).
При заражении клеток МТ-4 вирусом иммунодефицита человека первого типа показано ингибирование репродукции вируса в клетках, трансфецированных плазмидами, экспрессирующими вирусспецифические siPHK. Выраженный противовирусный эффект наблюдается при заражении клеток высокой концентрацией ВИЧ-1 (количество вирусных частиц эквивалентно 1081,5 нг р24), таблицы 1 и 3. Максимальное подавление вируса (60% и 91%) выявлено при заражении клеток через 72 часа после введения плазмиды.
Пример 3. Подавление репродукции ВИЧ в культуре клеток МТ-4 путем введения в клетки электропорацией векторных конструкций, экспрессирующих короткие интерферирующие РНК.
Клетки МТ-4 культивируют, как описано выше, 3 суток до концентрации 1,6 млн/мл, отмывают дважды средой RPMI, суспендируют в нужном объеме среды до концентрации 1×107 кл/мл. К 800 мкл суспензии клеток добавляют 40 мкг плазмидной ДНК, выдерживают 15 мин во льду и переносят в кювету для электропорации. Электропорацию проводят при 400 Вт, 960 мкФ (Gene PulserR Transfection Apparatus, Bio-Rad). Продолжительность импульса 31-36 мс. После электропорации клетки переносят в среду RPMI с добавлением 10% фетальной сыворотки КРС. Эффективность введения плазмидной ДНК 92-98% (оценивают регистрацией появления зеленой флюоресценции с использованием флюоресцентного микроскопа "Olimpus"). Клетки инфицируют через 3 суток после электропорации с различной множественностью заражения. Для заражения используют супернатант инфицированных штаммом ГКВ-4046 ВИЧ-1 клеток со множественностью заражения 2-5×10-1, 2-5×10-2 и 2-5×10-3 инфекционных единиц на клетку. Планшет инкубируют при 37°С четверо суток в атмосфере 5% СО2. На четвертые сутки отбирают пробы для количественного определения вирусспецифического белка р24 методом прямого иммуноферментного анализа. Концентрацию и жизнеспособность клеток оценивают методом исключения трипанового синего. Влияние введения в клетки экспрессирующих векторных конструкций на репродукцию ВИЧ-1 оценивают по накоплению вирусспецифического антигена р24. Результаты приведены в таблице 5.
2 - клетки МТ-4, трансфецированные плазмидой RT- hp-pEGFP-NI;
3 - клетки МТ-4, трансфецированные плазмидой tat-hp-pEGFP-NI;
4 - клетки МТ-4, трансфецированные плазмидой pr-hp-pEGEP-NI.
Показано, что в клетках, содержащих векторные конструкции, наблюдается значительное подавление репродукции ВИЧ-1 по сравнению с нетрансфецированными клетками (до 90%). При этом наблюдается зависимость величины ингибирования репродукции вируса от инфицирующей дозы ВИЧ-1.
Изобретение относится к медицинской и молекулярной генетике. Предложены три генетические конструкции на основе векторной плазмиды pEGFP-N1, продуцирующие siPHK-ингибиторы репродукции вируса иммунодефицита человека 1 типа. Изобретение может использоваться в разработке более эффективных анти-ВИЧ препаратов на основе интерферирующих РНК (siPHK), продуцируемых в клетках с помощью введенных векторных экспрессирующих конструкций. 3 н.п. ф-лы, 1 ил., 5 табл.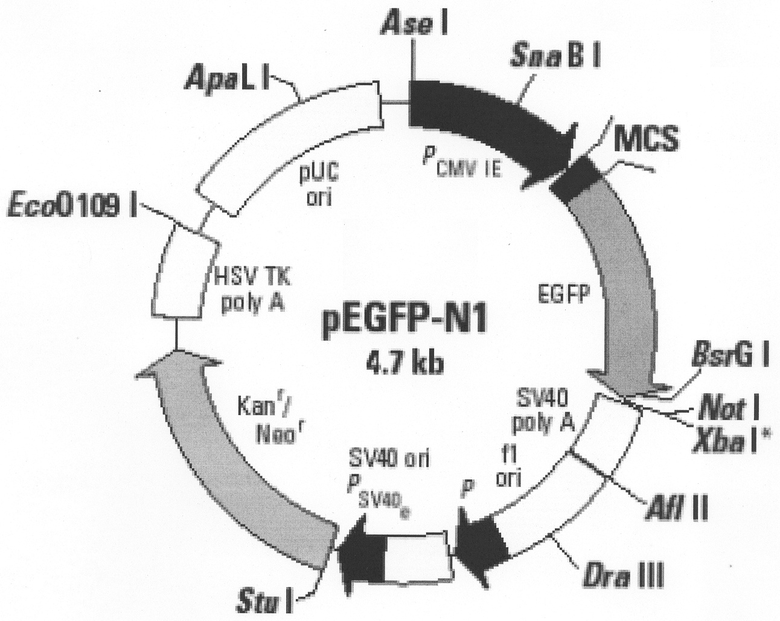
5'
gaattccTGATTCAGATTGGTTGTACttttttGTACAACCAATCTGAATCAaccc
cggatcc3',
где строчными буквами показаны области, содержащие искусственные
сайты рестрикции для рестриктаз EcoRI (на 5'-концах) и BamHI (на 3'-концах), а также петли, разделяющие области, способные образовать двуспиральный дуплекс с петлей, причем области, соответствующие смысловой цепи РНК вируса, показаны в строке слева, а антисмысловой - справа.
5'
gaattccTGCATATTTTTCAGTTCCCttttttGGGAACTGAAAAATATGCAtcccc
ggatcc3',
где строчными буквами показаны области, содержащие искусственные сайты рестрикции для рестриктаз EcoRI (на 5'-концах) и BamHI (на 3'- концах), а также петли, разделяющие области, способные образовать двуспиральный дуплекс с петлей, причем области, соответствующие смысловой цепи РНК вируса, показаны в строке слева, а антисмысловой - справа.
5'
gaattccAGTAGGACTAATAGTAGCAttttttTGCTACTATTAGTCCTACTatccc cggatcc 3',
где строчными буквами показаны области, содержащие искусственные сайты рестрикции для рестриктаз EcoRI (на 5'-концах) и BamHI (на 3'-концах), а также петли, разделяющие области, способные образовать двуспиральный дуплекс с петлей, причем области, соответствующие смысловой цепи РНК вируса, показаны в строке слева, а антисмысловой - справа.
| СПОСОБ ИЗМЕНЕНИЯ ГЕНЕТИЧЕСКИХ СВОЙСТВ ОРГАНИЗМА | 1999 |
|
RU2164944C1 |
| ХИМЕРНЫЙ ГЕН CR3 И КОДИРУЕМЫЙ ИМ ХИМЕРНЫЙ БЕЛОК CR3 (ВАРИАНТЫ), ИНДУЦИРУЮЩИЙ ИММУННЫЙ ОТВЕТ ПРОТИВ ВИЧ-1 | 2002 |
|
RU2302461C2 |
Авторы
Даты
2008-05-20—Публикация
2006-06-16—Подача