Настоящее изобретение относится к органической химии, а именно к способам получения алканоламинов, содержащих амино- и гидроксигруппы, связанные с ациклическими атомами углерода одного и того же углеродного скелета, а именно к способам получения алканоламинов общей формулы:
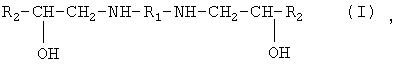
где 1. R1=-(СН2)2 -, R2=С6Н5-O-СН2-;
2. R1=-(СН2)6 -, R2=С6Н5-O-СН2-;
3. R1=-(СН2)2 -, R2=СН2=СН-СН2-O-СН2-;
4. R1=-(СН2)6 -, R2=СН2=СН-СН2-O-СН2-;
5. R1=-(СН2)2 -, R2=НО-СН2-;
6. R1=-(СН2)6 -, R2=НО-СН2-;
7. R1=-(СН2)6 -, R2=Cl-СН2-.
которые широко используются в качестве биологически активных препаратов, промежуточных соединений в органическом синтезе, а также в качестве отвердителей - модификаторов эпоксидных и уретановых композиций.
Известны способы получения этаноламинов взаимодействием окиси этилена и безводного аммиака в реакторе смешения при повышенных температуре и давлении, взаимодействие проводят при различных мольных соотношениях аммиак:окись этилена.
Полученную смесь продуктов взаимодействия направляют на стадию разделения. RU 2167147 7 С07С 215/08, С07С 213/04, 2001.05.20; RU 2162461 7 C07C 213/04, C07C 215/08, 2001.01.27.
Однако данные способы получения алканоламинов из окиси этилена и аммиака включает две основные стадии - синтез и выделение целевых продуктов. В результате проведения стадии синтеза образуется сложная смесь, состав которой зависит от способа синтеза. Это в свою очередь диктует условия проведения стадии разделения реакционной смеси. Причем при разделении получаются моно-, ди- и триэтаноламины, что ограничивает арсенал средств данного назначения.
Известен способ взаимодействия α-окисей (оксирансодержащих соединений) с ароматическими аминами, при этом в качестве α-окиси был взят фенилглицидиловый эфир, а в качестве амина - анилин [Х.А.Арутюнян, А.О.Тоноян, С.П.Давтян, Б.А.Розенберг, Н.С.Ениколопян // Докл. АН СССР. 1974, том 214, №4. С.832-834.]. Реакции проводили в о-дихлорбензоле и температуре 90°С. Также известен механизм взаимодействия α-окисей с алифатическими аминами [Пирожная Л.Н. Взаимодействие α-окисей с алифатическими аминами на примере фенилглицидилового эфира и н-бутиламина в 1,4-диоксане. // Высокомолек. соед. Сер. А. 1972. Т.14. С.112-116].
Известен способ получения новых производных этилендиамина, заключающийся во взаимодействии оксирансодержащего соединения (фенилглицидилового эфира) с алифатическими аминами (этилендиамином) в этиловом спирте путём кипячения в течение 2 часов [Пат. ПНР № 53677, кл. 12q, 1/01 (с07е), заявл. 04.04.65, опубл. 20.07.67].
Наиболее близким аналогом является способ получения 1,2-бис(у-хлор-(3-оксипропиламино)этана взаимодействием этилендиамина с эпихлоргидрином в водном этаноле при температуре 28-30°С при мольном соотношении оксирансодержащие соединения: алифатические амины как 2,3:1,0 и с выходом 50% (Андриянова Т.А., Минакова С.М. и др. "Синтез и противоопухолевая активность производных диаминов, содержащих у-хлор-р-оксипропильные группы", Химико-фармацевтический журнал, 16(12), стр.1460-1463, 1982).
Однако не известно получение указанным способом алканоламинов общей формулы: 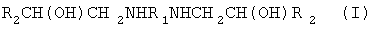 , где 1. R1= (CH2)2, R2=C6H5OCH2; 2. R1=(CH2)6, R2=С6Н5ОСН2; 3. R1=(CH2)2, R2=CH2=CHCH2OCH2; 4. R1=(CH2)6, R2=CH2=CHCH2OCH2; 5. R1=(CH2)2, R2=HOCH2; 6. R1=(CH2)6, R2=HOCH2; 7. R1=(CH2)6, R2=ClCH2 -.
, где 1. R1= (CH2)2, R2=C6H5OCH2; 2. R1=(CH2)6, R2=С6Н5ОСН2; 3. R1=(CH2)2, R2=CH2=CHCH2OCH2; 4. R1=(CH2)6, R2=CH2=CHCH2OCH2; 5. R1=(CH2)2, R2=HOCH2; 6. R1=(CH2)6, R2=HOCH2; 7. R1=(CH2)6, R2=ClCH2 -.
При создании изобретения ставилась задача получить алканоламины общей формулы: 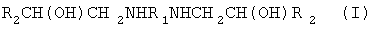 , где 1. R1=(CH2)2, R2=C6H5OCH2; 2. R1=(CH2)6, R2=С6Н5ОСН2; 3. R1=(CH2)2, R2=СН2=СНСН2ОСН2; 4. R1=(CH2)6, R2= CH2=CHCH2OCH2; 5. R1=(CH2)2, R2=HOCH2; 6. R1=(CH2)6, R2=HOCH2; 7. R1=(CH2)6, R2=ClCH2 -.
, где 1. R1=(CH2)2, R2=C6H5OCH2; 2. R1=(CH2)6, R2=С6Н5ОСН2; 3. R1=(CH2)2, R2=СН2=СНСН2ОСН2; 4. R1=(CH2)6, R2= CH2=CHCH2OCH2; 5. R1=(CH2)2, R2=HOCH2; 6. R1=(CH2)6, R2=HOCH2; 7. R1=(CH2)6, R2=ClCH2 -.
Техническим решением задачи является получение не описанных в литературе соединений, расширяющих арсенал средств данного назначения.
Это достигается тем, что способ получения алканоламинов общей формулы: 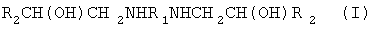 , где 1. R1=(CH2)2, R2=C6H5OCH2; 2. R1=(CH2)6, R2=С6Н5ОСН2; 3. R1=(CH2)2, R2=СН2=СНСН2ОСН2; 4. R1=(CH2)6, R2=CH2=CHCH2OCH2; 5. R1=(CH2)2, R2=HOCH2; 6. R1=(CH2)6, R2=HOCH2; 7. R1=(CH2)6, R2=ClCH2 -, включающий взаимодействие оксирансодержащих соединений с алифатическими аминами в среде ароматического растворителя при температуре 40-60°С.
, где 1. R1=(CH2)2, R2=C6H5OCH2; 2. R1=(CH2)6, R2=С6Н5ОСН2; 3. R1=(CH2)2, R2=СН2=СНСН2ОСН2; 4. R1=(CH2)6, R2=CH2=CHCH2OCH2; 5. R1=(CH2)2, R2=HOCH2; 6. R1=(CH2)6, R2=HOCH2; 7. R1=(CH2)6, R2=ClCH2 -, включающий взаимодействие оксирансодержащих соединений с алифатическими аминами в среде ароматического растворителя при температуре 40-60°С.
При этом способ в качестве оксирансодержащих соединений может содержать глицидиловые эфиры.
При этом способ в качестве оксирансодержащих соединений может содержать эпихлоргидрин.
Отличием заявленного способа от прототипа заключается в том, что взаимодействие проводят в ароматическом растворителе и при температуре 40-60°С.
Такие условия позволяют получить алканоламины взаимодействием двух молекул оксирансодержащего соединения с алифатическими аминами, проводить реакцию без побочных процессов с получением новых целевых продуктов. При этом получают алканоламины, неописанные в литературе, что расширяет арсенал средств данного назначения.
Для осуществления способа использовали следующие соединения:
Фенилглицидиловый эфир ТУ 6-09-08-715-75; аллилглицидиловый эфир ТУ 6-09-5136-83; эпихлоргидрин ГОСТ 12844-74; глицидол ТУ 6-09-3861-75; гексаметилендиамин ТУ 6-09-36-73; этилендиамин ТУ 6-09-147-75.
Сущность предлагаемого изобретения состоит в том, что способ получения алканоламинов включает взаимодействие оксирансодержащих соединений с алифатическими аминами в среде ароматического растворителя при температуре 40-60°С.
Пример 1. В колбу поместили 10,67 г (0,175 моль) этилендиамина и 10 мл толуола. Затем при постоянном перемешивании и нагревании до 40°С гомогенизировали смесь. В полученную смесь при интенсивном перемешивании добавили через капельную воронку по каплям 52,87 г (0,350 моль) фенилглицидилового эфира, поддерживая температуру 50°С. Через 15 мин после начала прибавления фенилглицидилового эфира начал выпадать осадок. После полного прибавления фенилглицидилового эфира реакционную смесь прогревали еще 3 часа при постоянной температуре и оставляли на 24 часа. Об окончании реакции судили методом ТСХ. Полученный осадок алканоламина отфильтровали и сушили при комнатной температуре. Выход, температура плавления (Тпл), фактор замедления (Rf), брутто-формула полученного соединения приведены в табл.3.
Пример 2. Способ осуществляли аналогично примеру 1. Условия, мольные соотношения и продолжительность способа приведены в табл.1. Выход, температура плавления (Тпл), фактор замедления (Rf), брутто-формула полученного соединения приведены в табл.3.
Пример 3. В колбу поместили 6,13 г (0,102 моль) этилендиамина и 15 мл бензола. Смесь при перемешивании гомогенизировали. В полученную смесь при интенсивном перемешивании добавили по каплям 29,30 г (0,257) аллилглицидилового эфира, поддерживая температуру 40°С. После полного прибавления аллилглицилилового эфира реакционную смесь прогревали еще 3 часа при температуре 50°С и оставляли на 24 часа. Об окончании реакции судили методом ТСХ. Полученный осадок отфильтровали и сушили при комнатной температуре. Выход, температура плавления (Тпл), факторы замедления (Rf), брутто-формула полученного соединения приведены в табл.3.
Пример 4. Способ осуществляли аналогично примеру 3. Условия, мольные соотношения и продолжительность способа приведены в табл.1. Выход, температура плавления (Тпл), факторы замедления (Rf), брутто-формула полученного соединения приведены в табл.3.
Пример 5. В колбу поместили 6,06 г (0,101 моль) этилендиамина и 15 мл толуола. Затем при перемешивании и нагревании до температуры 40°С гомогенизировали смесь. Далее в полученную смесь при интенсивном перемешивании добавили по каплям 16,87 г (0,228 моль) глицидола, поддерживая температуру 40°С. После полного прибавления реакционную смесь прогревали еще 4 часа при постоянной температуре до полного израсходования диамина и оставляли на 24 часа. Об окончании реакции судили методом ТСХ. Полученный осадок отфильтровывали и сушили при комнатной температуре. Выход, температура плавления (Тпл), фактор замедления (Rf), брутто-формула полученного соединения приведены в табл.3.
Пример 6. Способ осуществляли аналогично примеру 1. Условия, мольные соотношения и продолжительность способа приведены в табл.1. Выход, температура плавления (Тпл), фактор замедления (Rf), брутто-формула полученного соединения приведены в табл.3.
Пример 7. Способ осуществляли аналогично примеру 1. Условия, мольные соотношения и продолжительность способа приведены в табл.1. Выход, температура плавления (Тпл), фактор замедления (Rf), брутто-формула полученного соединения приведены в табл.3.
Индивидуальность полученных алканоламинов доказывали хроматографированием синтезированных соединений на силуфольной пластинке "Silufol UV-254", проявление осуществляли парами йода, факторы замедления приведены в табл.3.
Наличие полос поглощения характерных групп, таких как вторичные гидроксигруппы и аминогруппы доказывает структуру полученных алканоламинов. Также присутствие характерных групп в структуре доказывается сигналами 1Н ЯМР спектроскопией.
Данные ИК- и ЯМР 1Н спектров, подтверждающих строение полученных соединений представлены в таблице 2.
Выхода, температуры плавления (Тпл), факторы замедления (R×), брутто-формулы полученных соединений представлены в табл.3.
Таким образом, заявляемым способом были получены алканоламины, не описанные в литературе, с увеличенным выходом целевых продуктов, расширяющие арсенал средств данного назначения.
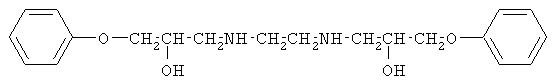
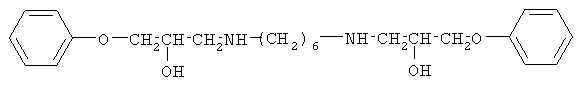
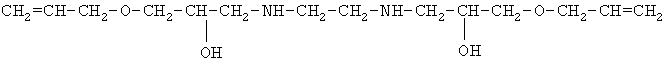
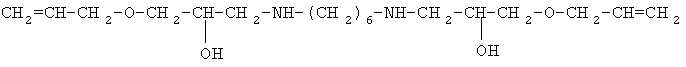
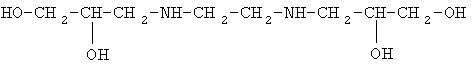
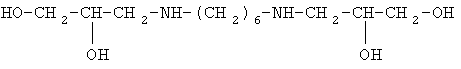
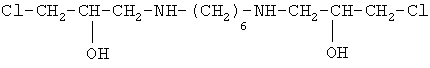
| название | год | авторы | номер документа |
|---|---|---|---|
| ЭПОКСИДНОЕ СВЯЗУЮЩЕЕ ДЛЯ КОМПОЗИЦИОННЫХ МАТЕРИАЛОВ | 2007 |
|
RU2327718C1 |
| СПОСОБ ПОЛУЧЕНИЯ АМИДОВ 5-АМИНО-1,2,4-ТРИАЗОЛ-3-ИЛКАРБОНОВЫХ КИСЛОТ | 2005 |
|
RU2292339C1 |
| СПОСОБ ЗАМЕДЛЕНИЯ ГОРЕНИЯ ПОЛИМЕРНОГО СУБСТРАТА И КОМПОЗИЦИЯ ИНГИБИТОРА ГОРЕНИЯ | 1998 |
|
RU2207352C2 |
| ЭМУЛЬГИРУЮЩИЙ СОСТАВ ДЛЯ ПРИГОТОВЛЕНИЯ ЭМУЛЬСИИ ВЗРЫВЧАТЫХ ВЕЩЕСТВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2001 |
|
RU2224587C2 |
| ПРОИЗВОДНЫЕ ИНДОЛА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1992 |
|
RU2074179C1 |
| ФУНКЦИОНАЛЬНЫЕ ФЛЮИДЫ ДЛЯ ДВИГАТЕЛЕЙ ВНУТРЕННЕГО СГОРАНИЯ | 2008 |
|
RU2485171C2 |
| ФЕНИЛСОДЕРЖАЩИЕ N-АЦИЛЬНЫЕ ПРОИЗВОДНЫЕ АМИНОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ПРОТИВОВОСПАЛИТЕЛЬНЫХ И АНАЛЬГЕТИЧЕСКИХ СРЕДСТВ | 2005 |
|
RU2309144C2 |
| ДИСПЕРСИЯ ПОЛИТЕТРАФТОРЭТИЛЕНА В ОРГАНИЧЕСКОМ РАСТВОРИТЕЛЕ И ДИСПЕРГАТОРЫ, ИСПОЛЬЗУЕМЫЕ ПРИ ЭТОМ | 1996 |
|
RU2164925C2 |
| ЗАМЕЩЁННЫЕ ИЗОКСАЗОЛЫ, ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ, ОБЛАДАЮЩИЕ ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ, И СПОСОБ ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2733945C2 |
| КОМПОЗИЦИЯ, СПОСОБ И ПРИМЕНЕНИЕ | 2011 |
|
RU2576039C2 |
Изобретение относится к способу получения новых алканоламинов общей формулы 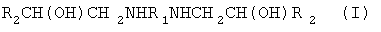 где 1. R1=(CH2)2, R2=С6Н5ОСН2; 2. R1=(СН2)6, R2=С6Н5ОСН2; 3. R1=(CH2)2, R2=CH2=CHCH2OCH2; 4. R1=(CH2)6, R2=СН2=СНСН2ОСН2; 5. R1=(CH2)2, R2=HOCH2; 6. R1=(СН2)6, R2=HOCH2; 7. R1=(СН2)6, R2=ClCH2, заключающийся во взаимодействии оксирансодержащих соединений с алифатическими аминами в среде ароматического растворителя при температуре 40-60°С. Соединения формулы (I) могут найти применение в качестве отвердителей-модификаторов эпоксидных и уретановых композиций, а также в качестве промежуточных соединений в органическом синтезе и основы для биологически активных препаратов. 2 з.п. ф-лы, 3 табл.
где 1. R1=(CH2)2, R2=С6Н5ОСН2; 2. R1=(СН2)6, R2=С6Н5ОСН2; 3. R1=(CH2)2, R2=CH2=CHCH2OCH2; 4. R1=(CH2)6, R2=СН2=СНСН2ОСН2; 5. R1=(CH2)2, R2=HOCH2; 6. R1=(СН2)6, R2=HOCH2; 7. R1=(СН2)6, R2=ClCH2, заключающийся во взаимодействии оксирансодержащих соединений с алифатическими аминами в среде ароматического растворителя при температуре 40-60°С. Соединения формулы (I) могут найти применение в качестве отвердителей-модификаторов эпоксидных и уретановых композиций, а также в качестве промежуточных соединений в органическом синтезе и основы для биологически активных препаратов. 2 з.п. ф-лы, 3 табл.
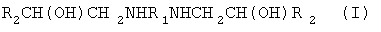 ,
,
где 1: R1=(CH2)2, R2=С6Н5ОСН2; 2: R1=(CH2)6, R2=С6Н5ОСН2; 3: R1=(CH2)2, R2=CH2=CHCH2OCH2; 4: R1=(CH2)6, R2=СН2=СНСН2ОСН2; 5 R1=(CH2)2, R2=HOCH2; 6: R1=(CH2)6, R2=HOCH2; 7: R1=(CH2)6, R2=ClCH2, заключающийся в взаимодействии оксирансодержащих соединений с алифатическими аминами в среде ароматического растворителя при температуре 40-60°С.
| Андриянова Т.А., Минакова С.М | |||
| и др | |||
| Синтез и противоопухолевая активность диаминовых производных, содержащих γ-хлор-β-гидроксипропильную группу | |||
| Химико-фармацевтический журнал, 16(12), с.1460-1463, 1982 | |||
| Biniecki S., Kabzinska Z | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Acta Poloniae Pharmaceutica, 40(3), p.285-288, 1983. | |||
Авторы
Даты
2008-06-27—Публикация
2006-12-20—Подача